Výroba a použití vodíku. Svět = 50 mil.tun H 2 /rok
|
|
|
- Marcela Bílková
- před 8 lety
- Počet zobrazení:
Transkript
1 Výroba a použití vodíku Svět = 50 mil.tun H 2 /rok
2 Obsah Výroba vodíku z rafinérských a petrochemických procesů On purpose výroba vodíku Nové směry ve výrobě vodíku Hlavní technologie na bázi vodíku Perspektivy vodíková ekonomika
3 Výroba vodíku distribuce postupů % Parní reforming Separace z rafinérských a 35 % petrochemických procesů (katalytický reforming, pyrolýza) 3 % POX 3 % Ostatní zdroje
4 Vodík možné výroby 1. Štěpení uhlovodíků vodní parou 2. Parciální oxidace uhlovodíkú 3. Konverze vodního plynu 4. Vodík z reformování benzinů 5. Koksárenský plyn - zdroj vodíku 6. Elektrolýza vody, kyselin, chloridu sodného 7. Rozklad vodní páry železem 8. Rozklad methanolu 9. Rozklad amoniaku 10. Rozklad vody 11. Moderní procesy pro výrobu vodíku
5 Hlavní směry použití vodíku Hydrogen reakce Rafinérské použití Methanol Amoniak Metalurgie polovodiče
6 Výroba vodíku z rafinérských a petrochemických procesů RAFINERIE Katalytický reforming SRR, CCR cca 1% hmot. Koksování a visbreaking Katalytické krakování PETROCHEMIE Pyrolýza cca 1 % hmot. Dehydrogenační procesy ČIŠTĚNÍ SEPARACE Procesy: kryogenní, difúzní, absorpční, adsorpční Nejdůležitější technologie: PSA, aminové vypírky
7 Vodík z pyrolýzy Metan do systému topného plynu Pyroplyn z odlučovače 5 výtlaku kompresoru Chlazení pyroplynu -37 C -72 C -96 C 3.08 MPa DA Demetanizer d 1 =2000 mm d 2 =3000 mm h=51700 mm DC 301 VT pára FA 301 FA 209A FA 209B -98 C FA C 40 Ch. voda C 3 chlad. 15 C 3.1 MPa -165 C C 3.13 MPa Metanizační reaktor d=2100 mm h=4700 mm výška náplně: 2400 mm Vodík Vodík do EA 406, 407 Zbytek demetanizeru do DA 401 Voda do DA 103 Propylenové chladivo +18 / +3 / -24 / -40 C Etylenové chladivo -55 / -75 / -100 C
8 Metanizace vodíku CO, CO 2, O 2 H 2 CH 4 + H 2 O EXO Teplota 300 C Katalyzátor Ni /Al 2 O 3
9 Vodík z katalytického reformování 1 % hmot. H 2
10 REFORMING - TERMODYNAMIKA
11 REFORMING - semiregenerativní
12 CCR reforming s kontinuální regenerací katalyzátoru
13 Syntézní plyn ze zemního plynu 1. Reakce
14 Výroba synplynu 1 - CH 4 + H 2 O CO + 3H CH 4 + CO 2 2CO + 2H CO + H 2 O CO 2 + H 2 neúplným spalováním CH4 + 0,5O2 CO + 2H2
15 Parní reformovámí vysoké teploty katalyzátory obsahující Ni katalyzátor je umístěný v trubkách parní reformér obsahuje dvě sekce - konvekční - radiační po odstranění síry se zemní plyn smísí s vodní parou a zahřeje se na teplotu 780 K před vstupem do trubek reforméru pomě páry/uhlík 2,5-4,5 mol H 2 O na mol C
16 Parní reformování Pokud se použijí pro parní reforming vyšší uhlovodíky, zařazuje se tzv. před-reformer Odstraňují se uhlíkové prekurzory Reaktor s katalytickým ložem Adiabatický, teplota cca 770K
17 Čištění synplynu synplyn z reforméru namá požadované složení a proto se musí upravovat složení se mění v závislosti na způsobu štěpení
18 Vypírání CO 2 a H 2 S Fyzikálně: RECTISOL (tlakové praní methanolem) Chemicky: alkanolaminy alkacidy (k. N-methylaminopropanová) potaš SULFINOL (sulfolan) konečný stupeň: je odstranění CO metanizací
19 Principy parní reforming vs. POX ENDO CH4 + H2O(g) = CO + 3H2 CH4 + 2H2O(g) = CO2 + 4H2 CO + H2O(g) = CO2 + H2 CO2 + H2 = CO + H2O parní reforming KONVERZE (EXO) CH4 + O2 = CO + 2H2 [EXO] CH4 + 2O2 = CO2 + 2H2O [EXO] CH4 + H2O = CO + 3H2 [ENDO] CH4 + CO2 = 2CO + 2H2 [ENDO] parciální oxidace
20 Výroba vodíku parní reforming Rafinace suroviny: CH 3 -SH + H 2 CH 4 + H 2 S T = 400 C Ni, Co-Mo /Al 2 O 3 Parní reforming: CH 4 + H 2 S (g) ZnO CH 4 + H 2 S (ads) Konverze: Methanizace: CH 4 + H 2 O CO + H 2 T = 800 C 15% Ni /α-al 2 O 3 CO + H 2 O CO 2 + H 2 1. Fe-Cr /Al 2 O 3 T = 350 C 2. Cu-Zn /Al 2 O 3 T = 200 C CO + H 2 CH 4 + H 2 O T = 300 C Ni /Al 2 O 3
21 ZP H trubek, 3,5 MPa technol.param. T = C P = 2,8-3,5 MPa S/O = 3-6 mol H 2 O 400 C Ni,Co- Mo/Al 2 O 3 CO + 3H 2 ZnO Ni/ Al 2 O C PARNÍ REFORMING CH 4 + H 2 O = CO + 3H 2 PARNÍ REFORMING 350 C Fe-Cr 200 C Cu-Zn CO + H 2 O = CO 2 + H 2 KONVERZE H 2 CO 2 + H 2 H 2 O DEA CO + H 2 = CH 4 + H 2 O METHANIZACE CO 2 + H 2 O AMINOVÁ VYPÍRKA 300 C Ni/Al 2 O 3 H 2
22 Výroba vodíku parní reforming Palivo Hydrodesulfurace Pec reformingu VT pára Spaliny Odplyn PSA - proces Vzduch Parní kotel Reaktor konverze CO Vodík - produkt Uhlovodíky Demin. voda
23 Výroba vodíku parní reforming Hydrogen production by steam reforming, gas purification by pressure swing adsorption (Design : German Linde) a) Desulfurization ; b) Feed preheater/superheater ; c) Reformer ; d) Waste-heat boiler ; e) CO shift reactor (HT shift) ; f) Cooling of raw gas ; g) Pressure swing adsorption ; h) Off-gas puffer for fuel ; i) Convection zone with steam production, steam superheating, and air preheating
24 PARNÍ REFORMING TEPLOTNÍ PROFIL V REAKTORU Tube wall temperature and heat flux in a reformer tube A) Outer tube wall temperature vs. heat flux profile divided into, e.g., eight reformer sections B) Hatched area: inclined to the right = heat requirements of the reaction; inclined to the
25 PSA
26 PSA pressure swing adsorption Six-bed PSA unit. Main flows for adsorption, repressurization, counterflow expansion (dump), counterflow purge, etc. for H 2 production by adsorber A. After termination of this adsorption step, next on-stream adsorber is B, etc. Adsorber A B C D E F Function Adsorptio n Repres- surizatio n Dum p Purg e Depres- surizatio n Start pressure, (MPa) Final pressure, (MPa) Depres- surizatio n
27
28
29 Výroba vodíku - POX C x H y + O 2 + H 2 O CO + H 2 + CO 2 (H 2 S, HCN) C x H y C + C m H n (endo) C + O 2 CO 2 (exo) C m H n + H 2 O CO + H 2 (endo) Teplota 1300 C Tlak 3.5 MPa Poměr uhlovodíky : O 2 : H 2 O = 1 : 1 : 0.6 Surový plyn, obj.% CO CO 46 H 2 49 CH H 2 S 0.7 COS 0.03
30 Litvínovský POX zplyňování zbytku z visbreakingu Resudual Oil Steam O 2 H 2 S water CO : H 2 Carbon Black 2 waste water water solution CO 2 H 2 CO 2 Wash Low Temp. CO Shift CO 2 Wash High Temp. CO Shift 2H 2 : CO 1 - Reactor, 2 TLE, 3 Carbon Black washing, 4 - Cyanide absorption, 5 H 2 S washing
31 Aminová vypírka odstranění kyselých plynů MEA monoethanolamin, DEA, MeDEA triethanolamin vhodný pro sorpci CO 2, methyldiethanolamin - vhodný pro sorpci H 2 S
32 Ropný zbytek (mazut, VBR) O 2 + H 2 O F : O 2 : H 2 O = 1 : 1 : 0,6 T= 1400 C P= 3,5 MPa C X H Y = C + C M H N C + O 2 = CO 2 C M H N + H 2 O = CO + H 2 EXO ENDO P O X H 2 O CO + 3H 2 CO 2 + CO + H 2 + C(SAZE) + H 2 S 350 C Fe-Cr 200 C Cu-Zn CO + H 2 O = CO 2 + H 2 KONVERZE 2.AV - CO 2 H2 + CO CO 2 + H 2 + CO H 2 O DEA CO + H 2 = CH 4 + H 2 O METHANIZACE CO 2 + H 2 O AMINOVÁ VYPÍRKA 300 C Ni/Al 2 O 3 H 2
33 Výroba vodíku - POX Oxidační reaktor Kotel na odpadní teplo Chlazení plynu Synplyn Mazut Voda Kyslík Kondenzát Napajecí voda Chladící voda Kyanovodíkova voda Saze
34 Zbytek z visbreakingu surovina POX Typické vlastnosti VFCR používaného jako surovina pro parciální oxidaci Rozmezí Penetrace 25 C [p.j.] Bod měknutí [ C] Hustota při 20 C [kg/m 3 ] Kinem. viskozita 150 C [cst] Dynam. viskozita 230 C [mpa.s] 17,2 20,2 Bod vzplanutí-ok [ C] Bod vzplanutí-zk [ C] Element. analýza C [%hm.] 85,3 87,7 H [%hm.] 8,3 10,2 S [%hm.] 2,5 3,5 Dusík [ppm] Obsah popela [ppm] MCRT [%hm.] Kovy V [ppm] Ni [ppm] Na [ppm] SimDist 5% [ C] % [ C] 590
35 Parametry reaktoru PROCESNÍ PODMÍNKY V REAKČNÍM OBJEMU _ REAKTORU vstup Postupová rychlost v reaktoru, při zanedbání plynné turbulence v důsledku probíhajících reakcí : Tlak 3,35 MPa Teplota 250,00 C množství pára + kyslík 803,86 m 3 /h surovina 10,20 m 3 /h výstup - reaktor tlak 3,35 MPa teplota 1300,00 C plyn ( Nm3/h) 5084,03 m 3 /h 1,66 m reaktor průměr 9,00 m výška 2,15 m 2 průřez - plocha 19,37 m 3 objem Postupová rychlost v reaktoru doba zdržení - reakční doba 0,66 m/s 13,72 s
36 Hořáky POX/ Litvínov Tři dvojice reaktorů Dvě čistící linky Výroba H2: Nm3/hod Výroba sazí Chezacarb
37 VÝROBA VODÍKU ELEKTROLÝZOU KATODA 2 H 2 O (l) + 2 e H 2 (g) + 2 OH (aq) ANODA 2 OH (aq) 1/2 O 2 (g) + H 2 O (l) + 2 e CELKOVÁ REAKCE H 2 O (l) H 2 (g) + 1/2 O 2 (g) Schematic of a water electrolysis cell a) Anode ; b) Diaphragm ; c) Cathode ; d) Oxygen outlet ; e) Anodic electrolyte cycle ; f) Anion ; g) Cation ; h) Cathodic electrolyte cycle ; i) Hydrogen outlet ; j) Cell wall DNES CENA VODÍKU Z ELEKTROLÝZY TROJNÁSOBNÁ!!!
38 Guvernér Arnold Schwarzenneger tankuje vodík do nádrže Toyoty a dole do Hummeru.
39 Varianty (novější) výroby vodíku
40 Autotermní reformování reformování ZP ve směsi s parou a kyslíkem v přítomnosti katalyzátoru: reformér: zóna spalování (2200K) zóna reformování ( K), s katalytickým lůžkem tlak bar molární poměr suroviny: H 2 O/CH 4 : 1-2 O 2 /CH 4 : 0,6
41 Autotermní technologie maximální efektivita výroby synplynu CH 4 + O 2 = CO + 2H 2 [EXO] CH 4 + 2O 2 = CO 2 + 2H 2 O [EXO] CH 4 + H 2 O = CO + 3H 2 [ENDO] CH 4 + CO 2 = 2CO + 2H 2 [ENDO]
42 Suché reformování CH 4 + CO 2 2 CO + 2H 2 Hr = 247,3 KJ / mol T 913 K Procesy : CALCOR a SPARG
43 Suché reformování Katalyzátory : La 2 NiO 4 zeolit (membránový katalyzátor) La NiO 3 La 0,8 Ca (anebo Sr ) 0,2 NiO 3 La Ni 1-x CO x O 3 ( x = 0,2 1 ) NiAl 2 O 4 La 2 NiO 4 + LaNiO 3 ( zmesné oxidy, t = C)
44 Sekundární reformer čpavkový synplyn vzduch 80 % konverze
45 Vstup dusíku
46 ZPLYŇOVÁNÍ UHLÍ - PRINCIP CmHn C + O 2 CxHy + H 2 O C + CxHy CO 2 EXO CO + H 2 ENDO
47 Zplyňování uhlí C H 0,8 O 0,1 O 2, H 2 O CO + H 2 + (CO 2 )
48 Hnědé uhlí dnes a zítra? Zplyňování v ČR Zplyňování hnědého uhlí 26 reaktorů Lurgi sesuvné lože zplyňovací médium kyslík, vodní pára tlaková varianta 2,7 MPa, 1000 C Vřesová Čištění vyrobeného plynu proces Rectisol Spalování plynu plynová turbina spalování plynu při 1100 C spaliny (540 C) vedeny do kotle na odpadní teplo
49 HLAVNÍ PETROCHEMIKÁLIE NA BÁZI VODÍKU METHANOL AMONIAK
50 Výroba amoniaku vodík : dusík = 3: 1 T= 490 až 520 C Tlak = 29 až 30 MPa Konverze = 17 % Železitý katalyzátor s promotory Exotermní reakce
51 Vstup dusíku
52 Sekundární reformer čpavkový synplyn vzduch 80 % konverze
53 Syntéza amoniaku - termodynamika
54 Čpavkový reaktor axiálně radiální tok
55
56 Methanol CO + 2H 2 CH 3 OH DELTA H = - 92 /mol Varianty výroby: 1. Vysokotlaký proces BASF: 34 MPa, 320 až 380 C, ZnO + Cr2O3 2. Nízkotlaké procesy ICI: 10 MPa, 240 až 260 C, CuO + ZnO 3. Nízkotlaké procesy Lurgi: 5 MPa, 250 až 260 C, CuO + ZnO (trubkový reaktor) 4. Středotlaké postupy
57 Použití methanolu APLIKACE PODÍL (%) Formaldehyd 40 MTBE 20 Dimethyltereftalát K.octová/acetáty 10 MTO?
58 Syntéza methanolu - termodynamika
59 Technologické varianty VÝROBCE KATALYZÁTOR TEPLOTA ( C) TLAK ( MPA) Topsoe CuO+ZnO+Cr2O Vulcan ZnO+Cr2O Pritchard CuO CCI CuO + ZnO/alumina BASF CuO + ZnO/alumina
60 Methanol synthesis a) Reactor ; b) Heat exchanger ; c) Cooler ; d) Separator ;e) Recycle compressor ; f ) Fresh gas compressor
61 Lurgi low-pressure methanol process
62 The ICI low-pressure methanol process a) Pure methanol column ; b) Light ends column ; c) Heat exchanger ; d) Cooler ; e) Separator ; f ) Reactor ; g) Compressor ; h) Compressor recycle stage
63 Pokroky ve výrobě methanolu 1. Zlepšování procesu 2. Použití CO 2 3. MegaMethanolTechnology 4. MTO 5. MTP
64 Výroba formaldehydu CH 3 OH CH 2 O + H 2 CH 3 OH+1/2 O 2 CH 2 O +H 2 O endo exo
65 Výroba k.octové karbonylací methanolu CH 3 OH + CO CH 3 COOH RADIKÁLOVÝ MECHANISMUS T= 200 C P= bar (kapalná fáze) HOMOGENNÍ KATALYZÁTOR Rh/HI REAKTOR: KONTINUÁLNÍ VSÁDKOVÝ MÍCHANÝ nebo PROBUBLÁVANÝ
66 K. octová z ethanolu fermentací
67 K. octová karbonylací methanolu
68
69 Výroba k. octové karbonylací methanolu
70 VÝROBA MOČOVINY Z AMONIAKU Krystalizace Granulace z taveniny
71 VODÍKOVÁ EKONOMIKA
72 VODÍK DNEŠKA 50 mil.tun za rok
73 Vodíková ekonomika
74 VODÍKOVÁ EKONOMIKA
75 VODÍK A ČISTÁ ENERGIE Z UHLÍ
76 Obsah energie v energetických materiálech (v nosičích energie): 1 kg palivového dřeva (biomasa) vydá 1 kg hnědého uhlí vydá 1 kg černého uhlí vydá 1 kg topného oleje 1 m zemního plynu <1 kwh 1 kwh 3 kwh 4 kwh 5 kwh 1 kg uranu 1 kg uranu kwh v reaktorech s pomalými neutrony kwh v rychlých množivých reaktorech Poznámka: Hnědé energetické uhlí v ČR postačí při současné těžbě na 35 let
77 Význam syntézního plynu Náhrada ropy?!
78 CHEMIE SYNTÉZNÍHO PLYNU
79 FTS Fischer-Tropschova syntéza
80 FISCHER-TROPSCH SYNTÉZA n CO + (2n+1) H 2 n CO + 2n H 2 n CO + 2n H 2 C n H 2n+2 + H 2 O C n H 2n + H 2 O H(-CH 2 -) n OH + (n-1)h 2 O Fe, Co - katalyzátory
81 FISCHER-TROPSCH SYNTÉZA REAKTOR MTFB RISER SLURRY Teplota C Tlak bar H2/CO mol/mol 1,7 2,5 0,6 Methan % hmot Benzin % hmot Diesel % hmot Wax % hmot
82 SASOL UHLÍ SYNGAS FT RAFINERIE SHELL MIDDLE DISTILLATES SYNTHESIS ZEMNÍ PLYN SYNGAS FT
83 GTP- Gas To Products
84 GTP.XTP univerzálnost syntézního plynu
85 FISCHER-TROPSCH SYNTÉZA n CO + (2n+1) H 2 n CO + 2n H 2 n CO + 2n H 2 C n H 2n+2 + H 2 O C n H 2n + H 2 O H(-CH 2 -) n OH + (n-1)h 2 O Fe, Co - katalyzátory
86 FISCHER-TROPSCH SYNTÉZA REAKTOR MTFB RISER SLURRY Teplota C Tlak bar H2/CO mol/mol 1,7 2,5 0,6 Methan % hmot Benzin % hmot Diesel % hmot Wax % hmot
87 FTS vliv katalyzátoru a podmínek
88 Výtěžek hlavních produktů při pyrolýze vyšších n-alkanů Produkt Výtěžek (% hm.) Ethylen 44,7 Propylen 18,9 Butadien 8,2 BTX 5,0 Ostatní 23,0 Oleje 0,2
89 Jednotky GTL
90 SYNTÉZNÍ PLYN PŘES METHANOL NA CHEMIKÁLIE
91 Synplyn + methanol = vítězný tým
92 Pokroky ve výrobě methanolu 1. Zlepšování procesu 2. Použití CO 2 3. MegaMethanolTechnology 4. MTO 5. MTP
93 MTP methanol na propylen
94 Rafinerie na bázi methanolu ETHYLEN, PROPYLEN
95 BIOMASA - ALTERNATIVNÍ SUROVINA PRO CHEMICKÝ PRŮMYSL
96 GLOBÁLNÍ ENERGETICKÝ POTENCIÁL BIOMASY 5 1 Celková spotřeba energie a ropných produktů Potencionální energie z ročního přírůstku biomasy bioamasy
97 BIOMASA PŘEVÁŽNĚ SACHARIDY A ROSTLINNÉ OLEJE roční produkce 100 biliónů tun obnovitelných zdrojů
98 ZPLYŇOVÁNÍ BIOMASY BIOPLYN FERMENTAČNÍ PROCESY BEŽNĚ ZAVÁDĚNO NÍZKÁ PRODUKČNÍ EFEKTIVITA ZPLYŇOVÁNÍ NA SYNTÉZNÍ PLYN JEN POKUSNÉ PROVOZY ALOTERMÍ PROCESY AUTOTERMNÍ PROCESY PYROLÝZA A NÁSLEDNÁ PARCIÁLNÍ OXIDACE ZPLYŇOVÁNÍ NA METHAN SNG (Substitute Natural Gas)
99 Zplyňování uhlí + BIOMASY ve fluidním loži BIOMASA
100 ZPLYŇOVÁNÍ BIOMASY - PYROLÝZA PYROLÝZA NA OLEJ A KOKS SYNPLYN
101 ZPLYŇOVÁNÍ BIOMASY
102 GTL REÁLNÉ APLIKACE GAS TO LIQUID
103 FT syntéza moderní (promotované) Co katalyzátory trubkové reaktory s pevně uloženým kytalyzátorem
104 FT Syntéza
105 GTL produkty, výtěžky a použití Ethylen Propylen Benzen
106 SMDS Bintulu (Malaisie) ASU...separace vzduchu na dusík a kyslík SGP... zplyňování - výroba syntézního plynu HPC... hydrokrakování 575 kt/rok
107 GTL v Qataru start: 2009 kapacita: 5,5 mil. t/rok
108 surovina pro GTL Relativní ekonomika GTL investiční náklady Methan (ZP) 1 Uhlí 2 Biomasa 3
109 Vodík Vodík je ve vesmíru nejrozšířenějším prvkem, na Zemi se vyskytuje převážně ve sloučeninách. Plynný elementární vodík, H 2, se vzhledem k nízké měrné hmotnosti udržuje ve vysokých vrstvách stratosféry (neobyčejně zředěný) ale při povrchu planety jej prakticky nenajdeme. Zato v přebytku najdeme jeho základní anorganickou sloučeninu, vodu H 2 O. Vázaný vodík obíhá v přírodním koloběhu řadou sloučenin organického původu, je součástí živé hmoty a z ní vzniklých produktů jako jsou fosilní paliva (zemní plyn, ropa, uhlí). Přes živou hmotu se dostaly do oběhu i další hydridy jako třeba amoniak, NH 3, a sulfan, H 2 S. Další sloučeniny vodíku jsou produkty průmyslové činnosti. V chemii zaujímá vodík důležitou úlohu, k němu se např. vztahují standardní potenciály elektrodových reakcí, koncentrace vodíkových iontů slouží jako měřítko kyselosti - ph. Vodík tvoří ionty H + (proton), i H - (hydridový ion), takže jej můžeme srovnávat jak s s-prvky (kovy) tak i s p-prvky (nekovy). Velkovýroba vodíku Vodík jako vedlejší produkt vzniká i při pyrolýze uhlovodíků (vysokoteplotním štěpení). Hlavním produktem zde jsou nenasycené uhlovodíky pro průmysl polymerů, zejména ethylen, ale i propylen, butadien aj. Odpadající vodík se většinou spotřebuje v návazných petrochemických výrobách. Hlavním výrobním postupem pro vodík je štěpení (parní reforming) zemního plynu nebo jiných uhlovodíků, kterou se v současné době vyrábí přes 80% vodíku. Poněkud méně náročné, avšak také méně účinné je získání vodíku z methanu nebo jiných ropných frakcí a zbytků částečným spalováním -POX. Výroba vodíku elektrolýzou vody by nebyla příliš hospodárná, určité množství vodíku však je vedlejším produktem jiných elektrochemických výrob. Vodík z amalgamové elektrolýzy soli je kontaminován stopami rtuťové páry, v ostatních případech je elektrolytický vodík dosti čistý. Štěpení zemního plynu (parní reforming) K redukci vody je možno použít i uhlovodíků, při čemž podíl vodíku ve výsledné směsi je vyšší, protože uhlovodíky ropy samy přinášejí do reakce až 15% hm. vodíku, a největší podíl 25% hm. je v zemním plynu. Jde o endotermní reakci CH 4 + H 2 O 3H 2 + CO Standardní hodnoty (při 298 K) této reakce jsou ΔH= 206 kj/mol, ΔG= 143 kj/mol a reakce běží obráceným směrem. (Toho se využívá při Fischer-Tropschově syntéze uhlovodíků.) Avšak nad 620 C je již ΔG záporné; např při 1000 C je ΔH= 227 kj/mol, ΔG= -96 kj/mol a lze tak získávat vodík. Provozně se pracuje při teplotě C za použití katalyzátoru NiO. Aby nedošlo k otravě tohoto katalyzátoru sulfanem, odchytávají se poslední stopy sulfanu (pod 1 ppm) ze zemního plynu prosáváním vrstvou ZnO. Cena vodíku závisí na ceně zemního plynu, ale i na dodané tepelné energii. (S použitím oxidů La, Ce, Cr by se snad mohlo pracovat při teplotě jen 450 C.)
110 Pec se svislými, 10 m vysokými trubkami, naplněnými katalyzátorem, kterými proudí reakční směs CH 4 + H 2 O. Trubky jsou uloženy v peci a hořáky jsou namířeny přímo na ně. Jednotka vybudovaná v BC-MCHZ v roce 2005 má již kratší trubky, uložené jako svazek v peci s jediným, dobře regulovaným hořákem. produktem je až 99,999%ní H 2. Cena zemního plynu na světových trzích v roce 2003 byla asi 0.60 Kč/kWh. Dobré využití tepla hotového produktu při výrobě páry a předehřevu reakční směsi je základním požadavkem. Vodík se asi z 25% využívá k syntéze jednoduchých organických látek. Pro tento účel můžeme využít obou produktů dané reakce a podle účelu syntézy jen upravit poměr H 2 : CO v syntézním plynu. Většina vodíku je ale potřebná k výrobě amoniaku, NH 3, při které přítomnost uhlíkatých látek vadí, takže provedeme dále nejprve tzv. konverzi na železitém katalyzátoru při 500 o C CO + H 2 O H 2 + CO 2 ΔH= -41 kj/mol Z této směsi se dá vyprat CO 2 do bazického roztoku, např. K 2 CO 3 nebo do organické báze ethanolaminu. Pro syntézu NH 3 oxidy uhlíku vadí i va stopách odstraní se methanací na Ni při 300 o C; odtud odchází 98%H 2 (zbytek je N 2 a CH 4 ). Příměsi plynů je možno od vodíku odloučit velmi dokonale metodou PSA na molekulových sítech. Malé vodíkové molekuly se na zeolitových výplních prakticky nezachycují. Tato metoda se používá také v BC-MCHZ Ostrava a Částečná oxidace zemního plynu Vodík lze z uhlovodíků získat také oxidací neboť vedle klasického úplného spalování CH 4 + 2O 2 H 2 O +CO 2 ΔH= -802 kj/mol je možno dosáhnout i exotermické částečné oxidace CH 4 + O 2 H 2 + H 2 O +CO ΔH= -321 kj/mol nebo dokonce CH 4 + ½ O 2 2H 2 + CO ΔH= -36 kj/mol. Obdobně lze získat vodík i oxidací levných vyšších uhlovodíků z mazutu. Pro ty organické syntézy, ve kterých vadí přítomnost dusíku, musíme na spalování vzít čistý kyslík. Obráceně, s použitím vzduchu můžeme získat v produktu částečného spalování směs vodíku a dusíku, kterou po odstranění oxidů uhlíku můžeme použít na přípravu syntézního plynu pro výrobu amoniaku aniž bychom museli dusík speciálně vyrábět.
111 Výroba vodíku v malém Rozklad methanolu a amoniaku Methanol a amoniak jsou látky, které ve velkém vyrábíme reakcí vodíku. Obě tyto látky se poměrně snadno skladují a dopravují. Vhodným katalyzázorem a podmínkami je možno směr vratné syntézní reakce obrátit a dostaneme se tak zpět k vodíku reakcemi CH 3 OH + H 2 O 3H 2 + CO o C, katalyzátor Cu 2NH 3 3H 2 + N 2 2 MPa, katalyzátor Ni Reakce jsou poměrně jednoduché a CO 2 nebo N 2 a zbytky výchozích látek nemusejí v některých výrobách vadit, takže pak odpadá problém dalšího čištění vodíku. Pochopitelně takto vyrobený vodík je několikrát dražší než vodík, získávaný přímo ze zemního plynu. Elektrolýza vody Elektrolýzou se voda rozkládá na plynný kyslík a plynný vodík. Protože samotná voda má malou elektrickou vodivost (destilovaná deionizovaná voda je prakticky nevodič), zvyšuje se její vodivost pomocným elektrolytem, např. H 2 SO 4 nebo KOH. Pro výrobu vodíku se nejčastěji volí jako elektrolyt KOH a pracuje se za tlaku 3 MPa. Spotřeba energie je 4-4,5 kwh/nm 3 tj kwh/kg. Příprava vodíku v laboratoři V minulosti se používal rozklad kyseliny zinkem v Kippově přístroji, např. 2 HCl + Zn ZnCl 2 + H 2. Touto reakcí se připravoval vodík pro plnění vzduchoplaveckých balonů (vynalezeny roku 1783). V malém množství přítomné páry kyseliny poškozovaly hedvábný materiál obalu. Kolik kyseliny a zinku je zapotřebí k naplnění balonu, který unese sebe a dvoučlennou posádku (celkem 300 kg)? Jaký je průměr balonu? Laboratoře i menší provozovny dnes odebírají plyn v tlakových lahvích o tlaku 20 MPa. Kolik kg vodíku je v tlakové lahvi o objemu 40 dm3 při tlaku 20 MPa? Větší pracoviště dopravují vodík ve svazcích válcových nádob na automobilních podvozcích. Iodový cyklus rozkladu vody V poslední době se studuje cyklus rozkladu vody na vodík a kyslík reakcemi 2 CaO + 2 I 2 2 CaI 2 + O 2 (100 C), CaI 2 + H 2 O CaO + 2 HI (500 C), 2 HI H 2 + I 2 ( C). Tento proces by mohl být energeticky výrazně výhodnější než parní reforming. Průmyslově se prozatím neprovozuje. Deuterium Voda v přírodě obsahuje asi 0,015 % D 2 O. Je zajímavé, že při elektrolýze uvolňovaný plyn obsahuje menší podíl D 2 zatímco elektrolyt se mírně obohacuje o těžkou vodu, D 2 O. Mnohonásobné opakování elektrolýzy je jeden z významných postupů přípravy D 2 O, používaného např. jako moderátor v jaderných reaktorech. Deuterovaná rozpouštědla v analytické laboratoři slouží k tomu aby se nepřekrylo NMR chování vodíku ve vlastním vzorku. Vodík jako zdroj čisté energie Velmi módní jsou úvahy o využití vodíku jako čistého zdroje energie jak pro spalovací motory, tak pro palivové články. Palivové články, přeměňující chemickou energii reakce kyslíku s vodíkem přímo na energii elektrickou, již existují a probíhá intenzivní výzkum
112 možnosti zlepšit jejich účinnost a spolehlivost a snížit objem a cenu. Problematické zůstává i skladování vodíku a bezpečnosti práce s ním. Akumulace chemické energie vodíku do snáze transportovatelných látek jako CH 3 OH nebo NH 3 se zdá být alternativou. Intenzivně se pracuje na vratných reakcích kapalných organických látek, které by byly schopny katalyticky uvolňovat vodík při běžných teplotách. Uvažuje se o skladování v nestechiometrických hydridech Ti, Fe, Mg, Ni. Hydridy lehkých kovů představují další možnost; např. práškovitý Li 4 BN 3 H 10 má vyšší koncentraci vratně zachyceného vodíku než vodík kapalný. I když se podaří všechny technické obtíže využití vodíku zvládnout, přenese se problém k výrobě velmi čistého vodíku. Ta je energeticky vysoce náročná, takže v celkové bilanci fosilní paliva neušetříme a produkci skleníkových plynů jen přeneseme na jiné místo. V současnosti se při výrobě 1 kg vodíku vyprodukuje asi 10 kg CO 2. Technické úvahy se zaměřují na přímý rozklad nad 2000 o C H 2 O(g) H 2 + 1/2 O 2 ΔH 298 = 242 kj/mol ΔG 298 = 228 kj/mol který však není zatím technicky využitelný (problém materiálu reaktoru a jeho ohřevu). Dokud nebude úspěšněji vyřešeno využití nukleární energie, nemá vodík jako prostředek přenosu energie k malým spotřebičům velkou nadějnost. Nicméně, vývoj spotřebičů s vysokou energetickou účinností a řešení problémů infrastruktury distribuce a skladování vodíku musí být na pořadu výzkumu již dnes. Bezpečnost práce s vodíkem Ve směsi se vzduchem je vodík výbušný v širokých mezích 4-74%. Známý je zvukový efekt štěknutí při zapálení směsi v otevřené zkumavce; pokud je směs v nádobě s úzkým hrdlem nebo je otvor zkumavky zčásti ucpán, hrozí exploze, doprovázená roztržením nádoby. Malé molekuly vodíku snadno difundují v různých materiálech a pronikají i malými kapilárními otvory. Vodík má již při normální teplotě záporný Joule-Thomsonův koeficient, takže se při expanzi samovolně ohřívá. Rozpustnost vodíku v kovech je velká, například v paladiu a platině se rozpustí několik hmotnostních procent vodíku ve formě "kovového" atomu H. Proto jsou tyto kovy významnými katalyzátory reakcí, v nichž vystupuje vodík. Vodík, přítomný v kovech může mít i nežádoucí účinky, např. dochází k vodíkovému křehnutí oceli. Tlakové lahve s vodíkem jsou opatřeny speciálním levotočivým závitem. (Obecně má každá třída technických plynů na tlakových nádobách jiné závitové koncovky, aby nemohlo nepozorností dojít k jejich chybnému napojení do technických aparatur s katastrofálními následky.) Manipulace s vodíkem je vymezena mezinárodními, národními i podnikovými normami a může ji provádět pouze zaškolená osoba.
Technické plyny. kapalný vzduch kyslík dusík vzácné plyny vodík (syntézní plyny)
 Technické plyny kapalný vzduch kyslík dusík vzácné plyny vodík (syntézní plyny) Kapalný vzduch složení vzduchu Před zkapalněním odstranění nežádoucích složek, např. vodní pára, CO 2, prach Zkapalňování
Technické plyny kapalný vzduch kyslík dusík vzácné plyny vodík (syntézní plyny) Kapalný vzduch složení vzduchu Před zkapalněním odstranění nežádoucích složek, např. vodní pára, CO 2, prach Zkapalňování
Zplyňování biomasy. Sesuvný generátor. Autotermní zplyňování Autotermní a alotermní zplyňování
 Zplyňování = termochemická přeměna uhlíkatého materiálu v pevném či kapalném skupenství na výhřevný energetický plyn pomocí zplyňovacích médií a tepla. Produktem je plyn obsahující výhřevné složky (H 2,
Zplyňování = termochemická přeměna uhlíkatého materiálu v pevném či kapalném skupenství na výhřevný energetický plyn pomocí zplyňovacích médií a tepla. Produktem je plyn obsahující výhřevné složky (H 2,
Amoniak. 1913 průmyslová výroba syntetického amoniaku
 Amoniak 1913 průmyslová výroba syntetického amoniaku využití 20 % výroba dusíkatých hnojiv 80 % nejrůznější odvětví průmyslu (plasty, vlákna, výbušiny, hydrazin, aminy, amidy, nitrily a další organické
Amoniak 1913 průmyslová výroba syntetického amoniaku využití 20 % výroba dusíkatých hnojiv 80 % nejrůznější odvětví průmyslu (plasty, vlákna, výbušiny, hydrazin, aminy, amidy, nitrily a další organické
TERMICKÉ PROCESY PŘI VYUŽITÍ ALTERNATIVNÍCH SUROVIN. Most, 13.6.2013 Autor: Doc. Ing. J.LEDERER, CSc.
 TERMICKÉ PROCESY PŘI VYUŽITÍ ALTERNATIVNÍCH SUROVIN Most, 13.6.2013 Autor: Doc. Ing. J.LEDERER, CSc. OBSAH PRINCIPY POUŽÍVANÝCH TERMOCHEMICKÝCH PROCESŮ VELKOKAPACITNÍ REALIZACE TERMOCHEMICKÝCH PROCESŮ
TERMICKÉ PROCESY PŘI VYUŽITÍ ALTERNATIVNÍCH SUROVIN Most, 13.6.2013 Autor: Doc. Ing. J.LEDERER, CSc. OBSAH PRINCIPY POUŽÍVANÝCH TERMOCHEMICKÝCH PROCESŮ VELKOKAPACITNÍ REALIZACE TERMOCHEMICKÝCH PROCESŮ
OMEZOVÁNÍ NEGATIVNÍCH ENVIRONMENTÁLNÍCH DOPADŮ PŘI VÝROBĚ PALIV A PETROCHEMIKÁLIÍ. Seminář, Bratislava, 6.6.2013 Autor: J.LEDERER
 OMEZOVÁNÍ NEGATIVNÍCH ENVIRONMENTÁLNÍCH DOPADŮ PŘI VÝROBĚ PALIV A PETROCHEMIKÁLIÍ Seminář, Bratislava, 6.6.2013 Autor: J.LEDERER OBSAH - CESTY K REDUKCI NOVOTVORBY CO 2 NEOBNOVITELNÉ SUROVINY OMEZENÍ UHLÍKOVÝCH
OMEZOVÁNÍ NEGATIVNÍCH ENVIRONMENTÁLNÍCH DOPADŮ PŘI VÝROBĚ PALIV A PETROCHEMIKÁLIÍ Seminář, Bratislava, 6.6.2013 Autor: J.LEDERER OBSAH - CESTY K REDUKCI NOVOTVORBY CO 2 NEOBNOVITELNÉ SUROVINY OMEZENÍ UHLÍKOVÝCH
NEKONVENČNÍ ZPŮSOBY VÝROBY TEPELNÉ A ELEKTRICKÉ ENERGIE. Ing. Stanislav HONUS
 NEKONVENČNÍ ZPŮSOBY VÝROBY TEPELNÉ A ELEKTRICKÉ ENERGIE Ing. Stanislav HONUS ORGANICKÝ MATERIÁL Spalování Chemické přeměny Chem. přeměny ve vodním prostředí Pyrolýza Zplyňování Chemické Biologické Teplo
NEKONVENČNÍ ZPŮSOBY VÝROBY TEPELNÉ A ELEKTRICKÉ ENERGIE Ing. Stanislav HONUS ORGANICKÝ MATERIÁL Spalování Chemické přeměny Chem. přeměny ve vodním prostředí Pyrolýza Zplyňování Chemické Biologické Teplo
Ing.Hugo Kittel, CSc., MBA, ČeR a.s. Kralupy n.vlt. Presentace vypracovaná pro ČAPPO Praha 2.10.2002
 Ing.Hugo Kittel, CSc., MBA, ČeR a.s. Kralupy n.vlt Presentace vypracovaná pro ČAPPO Praha 2.10.2002 GTL (Gas-to-Liquid) představuje obecný pojem používaný pro technologie konverze plynu na kapalné produkty
Ing.Hugo Kittel, CSc., MBA, ČeR a.s. Kralupy n.vlt Presentace vypracovaná pro ČAPPO Praha 2.10.2002 GTL (Gas-to-Liquid) představuje obecný pojem používaný pro technologie konverze plynu na kapalné produkty
OMEZOVÁNÍ NEGATIVNÍCH ENVIRONMENTÁLNÍCH DOPADŮ PŘI VÝROBĚ PALIV A PETROCHEMIKÁLIÍ. Most, Autor: Doc. Ing. J.LEDERER, CSc.
 OMEZOVÁNÍ NEGATIVNÍCH ENVIRONMENTÁLNÍCH DOPADŮ PŘI VÝROBĚ PALIV A PETROCHEMIKÁLIÍ Most, 29.11.2012 Autor: Doc. Ing. J.LEDERER, CSc. OBSAH - CESTY K REDUKCI NOVOTVORBY CO 2 NEOBNOVITELNÉ SUROVINY OMEZENÍ
OMEZOVÁNÍ NEGATIVNÍCH ENVIRONMENTÁLNÍCH DOPADŮ PŘI VÝROBĚ PALIV A PETROCHEMIKÁLIÍ Most, 29.11.2012 Autor: Doc. Ing. J.LEDERER, CSc. OBSAH - CESTY K REDUKCI NOVOTVORBY CO 2 NEOBNOVITELNÉ SUROVINY OMEZENÍ
zpracování těžkých frakcí na motorová paliva (mazut i vakuový zbytek)
 Ropa štěpné procesy zpracování těžkých frakcí na motorová paliva (mazut i vakuový zbytek) typy štěpných procesů: - termické krakování - katalytické krakování - hydrogenační krakování (hydrokrakování) podmínky
Ropa štěpné procesy zpracování těžkých frakcí na motorová paliva (mazut i vakuový zbytek) typy štěpných procesů: - termické krakování - katalytické krakování - hydrogenační krakování (hydrokrakování) podmínky
Ropa Kondenzované uhlovodíky
 Nejdůležitější surovina pro výrobu organických sloučenin Nejvýznamnější surovina světové ekonomiky Výroba energie Chemické zpracování - 15 % Cena a zásoby ropy (70-100 let) Ropné krize Nutnost hledání
Nejdůležitější surovina pro výrobu organických sloučenin Nejvýznamnější surovina světové ekonomiky Výroba energie Chemické zpracování - 15 % Cena a zásoby ropy (70-100 let) Ropné krize Nutnost hledání
Zpracování ropy doc. Ing. Josef Blažek, CSc. 4. přednáška
 ODBORNÉ VZDĚLÁVÁNÍ ÚŘEDNÍKŮ PRO VÝKON STÁTNÍ SPRÁVY OCHRANY OVZDUŠÍ V ČESKÉ REPUBLICE Zpracování ropy doc. Ing. Josef Blažek, CSc. 4. přednáška Rafinace pohonných hmot, zpracování sulfanu, výroba vodíku
ODBORNÉ VZDĚLÁVÁNÍ ÚŘEDNÍKŮ PRO VÝKON STÁTNÍ SPRÁVY OCHRANY OVZDUŠÍ V ČESKÉ REPUBLICE Zpracování ropy doc. Ing. Josef Blažek, CSc. 4. přednáška Rafinace pohonných hmot, zpracování sulfanu, výroba vodíku
Kolik energie by se uvolnilo, kdyby spalování ethanolu probíhalo při teplotě o 20 vyšší? Je tato energie menší nebo větší než při teplotě 37 C?
 TERMOCHEMIE Reakční entalpie při izotermním průběhu reakce, rozsah reakce 1 Kolik tepla se uvolní (nebo spotřebuje) při výrobě 2,2 kg acetaldehydu C 2 H 5 OH(g) = CH 3 CHO(g) + H 2 (g) (a) při teplotě
TERMOCHEMIE Reakční entalpie při izotermním průběhu reakce, rozsah reakce 1 Kolik tepla se uvolní (nebo spotřebuje) při výrobě 2,2 kg acetaldehydu C 2 H 5 OH(g) = CH 3 CHO(g) + H 2 (g) (a) při teplotě
Vodík jako alternativní ekologické palivo. palivové články a vodíkové hospodářství
 Vodík jako alternativní ekologické palivo palivové články a vodíkové hospodářství Charakteristika vodíku vodík je nejrozšířenějším prvkem ve vesmíru na Zemi je třetím nejrozšířenějším prvkem po kyslíku
Vodík jako alternativní ekologické palivo palivové články a vodíkové hospodářství Charakteristika vodíku vodík je nejrozšířenějším prvkem ve vesmíru na Zemi je třetím nejrozšířenějším prvkem po kyslíku
Průmysl dusíku. amoniak - kyselina dusičná - dusičnan amonný - močovina - chloramin - hydrazin. NaClO NaOH CO(NH 2 ) 2.
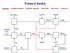 Průmysl dusíku amoniak - kyselina dusičná - dusičnan amonný - močovina - chloramin - hydrazin CO(NH 2 ) 2 NaClO NaOH NH 2 Cl N 2 H 4 methan CO 2 (uhlí, ropa) H 2 NH 3 NO 2 HNO 3 O 2 vzduch voda vzduch
Průmysl dusíku amoniak - kyselina dusičná - dusičnan amonný - močovina - chloramin - hydrazin CO(NH 2 ) 2 NaClO NaOH NH 2 Cl N 2 H 4 methan CO 2 (uhlí, ropa) H 2 NH 3 NO 2 HNO 3 O 2 vzduch voda vzduch
Paliva. nejběžnějším zdrojem tepla musí splňovat tyto podmínky: co nejmenší náklady na těžbu a výrobu snadno uskutečnitelné spalování
 Paliva Paliva nejběžnějším zdrojem tepla musí splňovat tyto podmínky: co nejmenší náklady na těžbu a výrobu snadno uskutečnitelné spalování Dělení paliv podle skupenství pevná uhlí, dřevo kapalná benzín,
Paliva Paliva nejběžnějším zdrojem tepla musí splňovat tyto podmínky: co nejmenší náklady na těžbu a výrobu snadno uskutečnitelné spalování Dělení paliv podle skupenství pevná uhlí, dřevo kapalná benzín,
Energetické využití odpadu. 200 let První brněnské strojírny
 200 let První brněnské strojírny Řešení využití odpadů v nové produktové linii PBS Spalování odpadů Technologie spalování vytříděného odpadu, kontaminované dřevní hmoty Depolymerizace a možnosti využití
200 let První brněnské strojírny Řešení využití odpadů v nové produktové linii PBS Spalování odpadů Technologie spalování vytříděného odpadu, kontaminované dřevní hmoty Depolymerizace a možnosti využití
1. Termochemie - příklady 1. ročník
 1. Termochemie - příklady 1. ročník 1.1. Urči reakční teplo reakce: C (g) + 1/2 O 2 (g) -> CO (g), ΔH 1 =?, známe-li C (g) + O 2 (g) -> CO 2 (g) ΔH 2 = -393,7 kj/mol CO (g) + 1/2 O 2 -> CO 2 (g) ΔH 3 =
1. Termochemie - příklady 1. ročník 1.1. Urči reakční teplo reakce: C (g) + 1/2 O 2 (g) -> CO (g), ΔH 1 =?, známe-li C (g) + O 2 (g) -> CO 2 (g) ΔH 2 = -393,7 kj/mol CO (g) + 1/2 O 2 -> CO 2 (g) ΔH 3 =
ČESKÉ RAFINÉRSKÉ, a.s.
 Bilance vodíku v ČESKÉ RAFINÉRSKÉ, a.s. APROCHEM 2010 Kouty nad Desnou 19 21.4.2010 Ing.Hugo Kittel, CSc., MBA www.ceskarafinerska.cz 1 Obsah Úvod do problému Zdroje vodíku pro rafinérie Využití vodíku
Bilance vodíku v ČESKÉ RAFINÉRSKÉ, a.s. APROCHEM 2010 Kouty nad Desnou 19 21.4.2010 Ing.Hugo Kittel, CSc., MBA www.ceskarafinerska.cz 1 Obsah Úvod do problému Zdroje vodíku pro rafinérie Využití vodíku
Úlohy: 1) Vypočítejte tepelné zabarvení dané reakce z následujících dat: C 2 H 4(g) + H 2(g) C 2 H 6(g)
 Úlohy: 1) Vypočítejte tepelné zabarvení dané reakce z následujících dat: C 2 H 4(g) + H 2(g) C 2 H 6(g) C 2 H 4(g) + 3O 2(g ) 2CO 2(g) +2H 2 O (l) H 0 298,15 = -1410,9kJ.mol -1 2C 2 H 6(g) + 7O 2(g) 4CO
Úlohy: 1) Vypočítejte tepelné zabarvení dané reakce z následujících dat: C 2 H 4(g) + H 2(g) C 2 H 6(g) C 2 H 4(g) + 3O 2(g ) 2CO 2(g) +2H 2 O (l) H 0 298,15 = -1410,9kJ.mol -1 2C 2 H 6(g) + 7O 2(g) 4CO
Zpracování ropy doc. Ing. Josef Blažek, CSc. 3. přednáška
 ODBORNÉ VZDĚLÁVÁNÍ ÚŘEDNÍKŮ PRO VÝKON STÁTNÍ SPRÁVY OCHRANY OVZDUŠÍ V ČESKÉ REPUBLICE Zpracování ropy doc. Ing. Josef Blažek, CSc. 3. přednáška Termické a katalytické krakování a hydrokrakování těžkých
ODBORNÉ VZDĚLÁVÁNÍ ÚŘEDNÍKŮ PRO VÝKON STÁTNÍ SPRÁVY OCHRANY OVZDUŠÍ V ČESKÉ REPUBLICE Zpracování ropy doc. Ing. Josef Blažek, CSc. 3. přednáška Termické a katalytické krakování a hydrokrakování těžkých
www.zlinskedumy.cz Inovace výuky prostřednictvím šablon pro SŠ
 Název projektu Číslo projektu Název školy Autor Název šablony Název DUMu Inovace výuky prostřednictvím šablon pro SŠ CZ.1.07/1.5.00/34.0748 Gymnázium Jana Pivečky a Střední odborná škola Slavičín Mgr.
Název projektu Číslo projektu Název školy Autor Název šablony Název DUMu Inovace výuky prostřednictvím šablon pro SŠ CZ.1.07/1.5.00/34.0748 Gymnázium Jana Pivečky a Střední odborná škola Slavičín Mgr.
Perspektivní metody. PROČ sušení pevných paliv? Většina dodané energie se ztrácí. Klasická metoda sušení horkými spalinami
 Perspektivní metody sušení pevných paliv Klasická metoda sušení horkými spalinami Uzavřený mlecí okruh PROČ sušení pevných paliv? zvýšení výhřevnosti snazší vzněcování spalování při vyšší teplotě menší
Perspektivní metody sušení pevných paliv Klasická metoda sušení horkými spalinami Uzavřený mlecí okruh PROČ sušení pevných paliv? zvýšení výhřevnosti snazší vzněcování spalování při vyšší teplotě menší
Zplyňování a zkapalňování uhlí Doc. Ing. Karel Ciahotný, CSc.
 ODBORNÉ VZDĚLÁVÁNÍ ÚŘEDNÍKŮ PRO VÝKON STÁTNÍ SPRÁVY OCHRANY OVZDUŠÍ V ČESKÉ REPUBLICE Zplyňování a zkapalňování uhlí Doc. Ing. Karel Ciahotný, CSc. Zplyňování uhlí technologický proces přeměny pevných
ODBORNÉ VZDĚLÁVÁNÍ ÚŘEDNÍKŮ PRO VÝKON STÁTNÍ SPRÁVY OCHRANY OVZDUŠÍ V ČESKÉ REPUBLICE Zplyňování a zkapalňování uhlí Doc. Ing. Karel Ciahotný, CSc. Zplyňování uhlí technologický proces přeměny pevných
11. Zemní plyn jako energetická a chemická surovina. Ing. Tomáš Hlinčík, Ph.D.
 11. Zemní plyn jako energetická a chemická surovina Ing. Tomáš Hlinčík, Ph.D. Zpracování zemního plynu Nepřímá přeměna methanu syntézní plyn (chemikálie, paliva) - výroba vodíku pro syntézu amoniaku -
11. Zemní plyn jako energetická a chemická surovina Ing. Tomáš Hlinčík, Ph.D. Zpracování zemního plynu Nepřímá přeměna methanu syntézní plyn (chemikálie, paliva) - výroba vodíku pro syntézu amoniaku -
Chemické procesy v ochraně životního prostředí
 Chemické procesy v ochraně životního prostředí 1. Vliv výroby energie na životní prostředí 2. Zpracování výfukových plynů ze spalovacích motorů 3. Zachycování oxidů síry ve spalinách 4. Výroba paliv pro
Chemické procesy v ochraně životního prostředí 1. Vliv výroby energie na životní prostředí 2. Zpracování výfukových plynů ze spalovacích motorů 3. Zachycování oxidů síry ve spalinách 4. Výroba paliv pro
Inovace bakalářského studijního oboru Aplikovaná chemie CZ.1.07/2.2.00/ Výpočty z chemických vzorců
 Výpočty z chemických vzorců 1. Hmotnost kyslíku je 80 g. Vypočítejte : a) počet atomů kyslíku ( 3,011 10 atomů) b) počet molů kyslíku (2,5 mol) c) počet molekul kyslíku (1,505 10 24 molekul) d) objem (dm
Výpočty z chemických vzorců 1. Hmotnost kyslíku je 80 g. Vypočítejte : a) počet atomů kyslíku ( 3,011 10 atomů) b) počet molů kyslíku (2,5 mol) c) počet molekul kyslíku (1,505 10 24 molekul) d) objem (dm
Kyslík a vodík. Bezbarvý plyn, bez chuti a zápachu, asi 14krát lehčí než vzduch. Běžně tvoří molekuly H2. hydridy (např.
 1 Kyslík a vodík Kyslík Vlastnosti Bezbarvý reaktivní plyn, bez zápachu, nejčastěji tvoří molekuly O2. Kapalný kyslík je modrý. S jinými prvky tvoří sloučeniny oxidy (např. CO, CO2, SO2...) Výskyt Nejrozšířenější
1 Kyslík a vodík Kyslík Vlastnosti Bezbarvý reaktivní plyn, bez zápachu, nejčastěji tvoří molekuly O2. Kapalný kyslík je modrý. S jinými prvky tvoří sloučeniny oxidy (např. CO, CO2, SO2...) Výskyt Nejrozšířenější
Registrační číslo projektu: CZ.1.07/1.4.00/21.2939. Název projektu: Investice do vzdělání - příslib do budoucnosti
 Registrační číslo projektu: CZ.1.07/1.4.00/21.2939 Název projektu: Investice do vzdělání - příslib do budoucnosti Číslo přílohy: VY_číslo šablony_inovace_číslo přílohy Autor Datum vytvoření vzdělávacího
Registrační číslo projektu: CZ.1.07/1.4.00/21.2939 Název projektu: Investice do vzdělání - příslib do budoucnosti Číslo přílohy: VY_číslo šablony_inovace_číslo přílohy Autor Datum vytvoření vzdělávacího
Model dokonalého spalování pevných a kapalných paliv Teoretické základy spalování. Teoretické základy spalování
 Spalování je fyzikálně chemický pochod, při kterém probíhá organizovaná příprava hořlavé směsi paliva s okysličovadlem a jejich slučování (hoření) za intenzivního uvolňování tepla, což způsobuje prudké
Spalování je fyzikálně chemický pochod, při kterém probíhá organizovaná příprava hořlavé směsi paliva s okysličovadlem a jejich slučování (hoření) za intenzivního uvolňování tepla, což způsobuje prudké
Omezování plynných emisí. Ochrana ovzduší ZS 2012/2013
 Omezování plynných emisí Ochrana ovzduší ZS 2012/2013 1 Úvod Různé fyzikální a chemické principy + biotechnologie Principy: absorpce adsorpce oxidace a redukce katalytická oxidace a redukce kondenzační
Omezování plynných emisí Ochrana ovzduší ZS 2012/2013 1 Úvod Různé fyzikální a chemické principy + biotechnologie Principy: absorpce adsorpce oxidace a redukce katalytická oxidace a redukce kondenzační
Zpracování ropy doc. Ing. Josef Blažek, CSc. 9. přednáška
 ODBORNÉ VZDĚLÁVÁNÍ ÚŘEDNÍKŮ PRO VÝKON STÁTNÍ SPRÁVY OCHRANY OVZDUŠÍ V ČESKÉ REPUBLICE Zpracování ropy doc. Ing. Josef Blažek, CSc. 9. přednáška Emise ze zpracování ropy, BREF, komplexita rafinérií Emise
ODBORNÉ VZDĚLÁVÁNÍ ÚŘEDNÍKŮ PRO VÝKON STÁTNÍ SPRÁVY OCHRANY OVZDUŠÍ V ČESKÉ REPUBLICE Zpracování ropy doc. Ing. Josef Blažek, CSc. 9. přednáška Emise ze zpracování ropy, BREF, komplexita rafinérií Emise
CÍL. 20 % motorových paliv nahradit alternativními palivy
 BIOPALIVA BIOFUELS Situace kolem ropy 1 barel ropy = 159 litrů Denní těžba ropy na světě : asi 75 milionů barelů Roční těžba ropy na světě : asi 27 miliard barelů Ropa pokrývá asi 40 % primární spotřeby
BIOPALIVA BIOFUELS Situace kolem ropy 1 barel ropy = 159 litrů Denní těžba ropy na světě : asi 75 milionů barelů Roční těžba ropy na světě : asi 27 miliard barelů Ropa pokrývá asi 40 % primární spotřeby
Test vlastnosti látek a periodická tabulka
 DUM Základy přírodních věd DUM III/2-T3-2-08 Téma: Test vlastnosti látek a periodická tabulka Střední škola Rok: 2012 2013 Varianta: A Zpracoval: Mgr. Pavel Hrubý Mgr. Josef Kormaník TEST Test vlastnosti
DUM Základy přírodních věd DUM III/2-T3-2-08 Téma: Test vlastnosti látek a periodická tabulka Střední škola Rok: 2012 2013 Varianta: A Zpracoval: Mgr. Pavel Hrubý Mgr. Josef Kormaník TEST Test vlastnosti
Separace plynů a par. Karel Friess. Ústav fyzikální chemie, VŠCHT Praha. Seminář 10. 5. 2012 Praha
 Separace plynů a par Karel Friess Ústav fyzikální chemie, VŠCHT Praha Seminář 10. 5. 2012 Praha Membránové separace SEPARAČNÍ MEMBRÁNA pasivní nebo aktivní bariéra průchodu částic mezi dvěma fázemi Pro
Separace plynů a par Karel Friess Ústav fyzikální chemie, VŠCHT Praha Seminář 10. 5. 2012 Praha Membránové separace SEPARAČNÍ MEMBRÁNA pasivní nebo aktivní bariéra průchodu částic mezi dvěma fázemi Pro
H H C C C C C C H CH 3 H C C H H H H H H
 Alkany a cykloalkany sexta Martin Dojiva uhlovodíky obsahující pouze jednoduché vazby obecný vzorec alkanů: C n 2n+2 cykloalkanů: C n 2n homologický přírůstek C 2 Dělení alkanů přímé větvené u větvených
Alkany a cykloalkany sexta Martin Dojiva uhlovodíky obsahující pouze jednoduché vazby obecný vzorec alkanů: C n 2n+2 cykloalkanů: C n 2n homologický přírůstek C 2 Dělení alkanů přímé větvené u větvených
ANODA KATODA elektrolyt:
 Ukázky z pracovních listů 1) Naznač pomocí šipek, které částice putují k anodě a které ke katodě. Co je elektrolytem? ANODA KATODA elektrolyt: Zn 2+ Cl - Zn 2+ Zn 2+ Cl - Cl - Cl - Cl - Cl - Zn 2+ Cl -
Ukázky z pracovních listů 1) Naznač pomocí šipek, které částice putují k anodě a které ke katodě. Co je elektrolytem? ANODA KATODA elektrolyt: Zn 2+ Cl - Zn 2+ Zn 2+ Cl - Cl - Cl - Cl - Cl - Zn 2+ Cl -
CHEMICKÉ VÝPOČTY I. ČÁST LÁTKOVÉ MNOŽSTVÍ. HMOTNOSTI ATOMŮ A MOLEKUL.
 CHEMICKÉ VÝPOČTY I. ČÁST LÁTKOVÉ MNOŽSTVÍ. HMOTNOSTI ATOMŮ A MOLEKUL. Látkové množství Značka: n Jednotka: mol Definice: Jeden mol je množina, která má stejný počet prvků, jako je atomů ve 12 g nuklidu
CHEMICKÉ VÝPOČTY I. ČÁST LÁTKOVÉ MNOŽSTVÍ. HMOTNOSTI ATOMŮ A MOLEKUL. Látkové množství Značka: n Jednotka: mol Definice: Jeden mol je množina, která má stejný počet prvků, jako je atomů ve 12 g nuklidu
ÚPRAVA VODY V ENERGETICE. Ing. Jiří Tomčala
 ÚPRAVA VODY V ENERGETICE Ing. Jiří Tomčala Úvod Voda je v elektrárnách po palivu nejdůležitější surovinou Její množství v provozních systémech elektráren je mnohonásobně větší než množství spotřebovaného
ÚPRAVA VODY V ENERGETICE Ing. Jiří Tomčala Úvod Voda je v elektrárnách po palivu nejdůležitější surovinou Její množství v provozních systémech elektráren je mnohonásobně větší než množství spotřebovaného
Zplyňování. Ing. Martin Lisý, PhD. Energetický ústav VUT v Brně Fakulta strojního inženýrství
 Zplyňování Ing. Martin Lisý, PhD. Energetický ústav VUT v Brně Fakulta strojního inženýrství Projekt je spolufinancován Evropským sociálním fondem a Statním rozpočtem ČR Technologie zpracování biomasy
Zplyňování Ing. Martin Lisý, PhD. Energetický ústav VUT v Brně Fakulta strojního inženýrství Projekt je spolufinancován Evropským sociálním fondem a Statním rozpočtem ČR Technologie zpracování biomasy
rní zdroj energie pro elektromobily Petr Vysoký
 Vodík k jako primárn rní zdroj energie pro elektromobily Petr Vysoký Dopravní fakulta ČVUT Vodík palivo budoucnosti Sloučen ením m vodíku s kyslíkem kem dojde k uvolnění energie, odpadem je voda Vodík
Vodík k jako primárn rní zdroj energie pro elektromobily Petr Vysoký Dopravní fakulta ČVUT Vodík palivo budoucnosti Sloučen ením m vodíku s kyslíkem kem dojde k uvolnění energie, odpadem je voda Vodík
Elektrárny část II. Tepelné elektrárny. Ing. M. Bešta
 Tepelné elektrárny 1) Kondenzační elektrárny uhelné K výrobě elektrické energie se využívá tepelné energie uvolněné z uhlí spalováním. Teplo uvolněné spalováním se využívá k výrobě přehřáté (ostré) páry.
Tepelné elektrárny 1) Kondenzační elektrárny uhelné K výrobě elektrické energie se využívá tepelné energie uvolněné z uhlí spalováním. Teplo uvolněné spalováním se využívá k výrobě přehřáté (ostré) páry.
Učební osnovy Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Chemický kroužek ročník 6.-9.
 Učební osnovy Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Chemický kroužek ročník 6.-9. Školní rok 0/03, 03/04 Kapitola Téma (Učivo) Znalosti a dovednosti (výstup) Počet hodin pro kapitolu Úvod
Učební osnovy Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Chemický kroužek ročník 6.-9. Školní rok 0/03, 03/04 Kapitola Téma (Učivo) Znalosti a dovednosti (výstup) Počet hodin pro kapitolu Úvod
VÝUKOVÝ MODUL MEMBRÁNOVÝCH PROCESŮ TÉMATA PŘEDNÁŠEK
 VÝUKOVÝ MODUL MEMBRÁNOVÝCH PROCESŮ TÉMATA PŘEDNÁŠEK TRANSPORT LÁTEK MEMBRÁNAMI Transport látek porézními membránami - Plouživý tok nestlačitelných tekutin vrstvou částic - Plouživý tok stlačitelných tekutin
VÝUKOVÝ MODUL MEMBRÁNOVÝCH PROCESŮ TÉMATA PŘEDNÁŠEK TRANSPORT LÁTEK MEMBRÁNAMI Transport látek porézními membránami - Plouživý tok nestlačitelných tekutin vrstvou částic - Plouživý tok stlačitelných tekutin
Vliv chemické aktivace na sorpční charakteristiky uhlíkatých materiálů
 VYSOKÁ ŠKOLA BÁŇSKÁ TECHNICKÁ UNIVERZITA OSTRAVA HORNICKO GEOLOGICKÁ FAKULTA Institut čistých technologií těžby a užití energetických surovin Vliv chemické aktivace na sorpční charakteristiky uhlíkatých
VYSOKÁ ŠKOLA BÁŇSKÁ TECHNICKÁ UNIVERZITA OSTRAVA HORNICKO GEOLOGICKÁ FAKULTA Institut čistých technologií těžby a užití energetických surovin Vliv chemické aktivace na sorpční charakteristiky uhlíkatých
Kombinovaná výroba elektrické energie, tepla a biosorbentu z biomasy. Michael Pohořelý & Siarhei Skoblia. Zplyňování
 ÚSTAV CHEMICKÝCH PROCESŮ AV ČR VYSOKÁ ŠKOLA CHEMICKO-TECHNOLOGICKÁ V PRAZE Kombinovaná výroba elektrické energie, tepla a biosorbentu z biomasy Michael Pohořelý & Siarhei Skoblia Zplyňování H 2 + CO +
ÚSTAV CHEMICKÝCH PROCESŮ AV ČR VYSOKÁ ŠKOLA CHEMICKO-TECHNOLOGICKÁ V PRAZE Kombinovaná výroba elektrické energie, tepla a biosorbentu z biomasy Michael Pohořelý & Siarhei Skoblia Zplyňování H 2 + CO +
Složení soustav (roztoky, koncentrace látkového množství)
 VZOROVÉ PŘÍKLADY Z CHEMIE A DOPORUČENÁ LITERATURA pro přípravu k přijímací zkoušce studijnímu oboru Nanotechnologie na VŠB TU Ostrava Doporučená literatura z chemie: Prakticky jakákoliv celostátní učebnice
VZOROVÉ PŘÍKLADY Z CHEMIE A DOPORUČENÁ LITERATURA pro přípravu k přijímací zkoušce studijnímu oboru Nanotechnologie na VŠB TU Ostrava Doporučená literatura z chemie: Prakticky jakákoliv celostátní učebnice
Kyselina dusičná. jedna z nejdůležitějších chemikálií
 Kyselina dusičná jedna z nejdůležitějších chemikálií Výroba: minulost - surovinou pro průmyslovou výrobu dusičnan sodný (ledek sodný, guano) současnost - katalytické spalování amoniaku (první výrobní jednotka
Kyselina dusičná jedna z nejdůležitějších chemikálií Výroba: minulost - surovinou pro průmyslovou výrobu dusičnan sodný (ledek sodný, guano) současnost - katalytické spalování amoniaku (první výrobní jednotka
Zadání příkladů řešených na výpočetních cvičeních z Fyzikální chemie I, obor CHTP. Termodynamika. Příklad 10
 Zadání příkladů řešených na výpočetních cvičeních z Fyzikální chemie I, obor CHTP Termodynamika Příklad 1 Stláčením ideálního plynu na 2/3 původního objemu vzrostl při stálé teplotě jeho tlak na 15 kpa.
Zadání příkladů řešených na výpočetních cvičeních z Fyzikální chemie I, obor CHTP Termodynamika Příklad 1 Stláčením ideálního plynu na 2/3 původního objemu vzrostl při stálé teplotě jeho tlak na 15 kpa.
EU peníze středním školám digitální učební materiál
 EU peníze středním školám digitální učební materiál Číslo projektu: Číslo a název šablony klíčové aktivity: Tematická oblast, název DUMu: Autor: CZ.1.07/1.5.00/34.0515 III/2 Inovace a zkvalitnění výuky
EU peníze středním školám digitální učební materiál Číslo projektu: Číslo a název šablony klíčové aktivity: Tematická oblast, název DUMu: Autor: CZ.1.07/1.5.00/34.0515 III/2 Inovace a zkvalitnění výuky
Základní škola, Ostrava Poruba, Bulharská 1532, příspěvková organizace
 Chemie - 8. ročník pozorování, pokus a bezpečnost práce Určí společné a rozdílné vlastnosti látek vlastnosti látek hustota, rozpustnost, tepelná a elektrická vodivost, vliv atmosféry na vlastnosti a stav
Chemie - 8. ročník pozorování, pokus a bezpečnost práce Určí společné a rozdílné vlastnosti látek vlastnosti látek hustota, rozpustnost, tepelná a elektrická vodivost, vliv atmosféry na vlastnosti a stav
ANODA KATODA elektrolyt:
 Ukázky z pracovnívh listů 1) Naznač pomocí šipek, které částice putují k anodě a které ke katodě. Co je elektrolytem? ANODA KATODA elektrolyt: Zn 2+ Cl - Zn 2+ Zn 2+ Cl - Cl - Cl - Cl - Cl - Zn 2+ Cl -
Ukázky z pracovnívh listů 1) Naznač pomocí šipek, které částice putují k anodě a které ke katodě. Co je elektrolytem? ANODA KATODA elektrolyt: Zn 2+ Cl - Zn 2+ Zn 2+ Cl - Cl - Cl - Cl - Cl - Zn 2+ Cl -
ZŠ ÚnO, Bratří Čapků 1332
 Animovaná chemie Top-Hit Analytická chemie Analýza anorganických látek Důkaz aniontů Důkaz kationtů Důkaz kyslíku Důkaz vody Gravimetrická analýza Hmotnostní spektroskopie Chemická analýza Nukleární magnetická
Animovaná chemie Top-Hit Analytická chemie Analýza anorganických látek Důkaz aniontů Důkaz kationtů Důkaz kyslíku Důkaz vody Gravimetrická analýza Hmotnostní spektroskopie Chemická analýza Nukleární magnetická
STEJNOSMĚRNÝ PROUD Galvanické články TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY.
 STEJNOSMĚRNÝ PROUD Galvanické články TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY. Galvanické články Většina kovů ponořených do vody nebo elektrolytu
STEJNOSMĚRNÝ PROUD Galvanické články TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY. Galvanické články Většina kovů ponořených do vody nebo elektrolytu
Přehled technologii pro energetické využití biomasy
 Přehled technologii pro energetické využití biomasy Tadeáš Ochodek Seminář BIOMASA JAKO ZDROJ ENERGIE 6. - 7.6. 2006, Hotel Montér, Ostravice Z principiálního hlediska lze rozlišit několik způsobů získávání
Přehled technologii pro energetické využití biomasy Tadeáš Ochodek Seminář BIOMASA JAKO ZDROJ ENERGIE 6. - 7.6. 2006, Hotel Montér, Ostravice Z principiálního hlediska lze rozlišit několik způsobů získávání
ODSTRAŇOVÁNÍ KYSELÝCH SLOŽEK Z PLYNŮ ZE ZPLYŇOVÁNÍ BIOMASY
 ODSTRAŇOVÁNÍ KYSELÝCH SLOŽEK Z PLYNŮ ZE ZPLYŇOVÁNÍ BIOMASY Petr Pekárek, Pavel Machač, Václav Koza, Božena Kremanová, Kateřina Bradáčová, Josef Kuba, Pedro Delgado Moniz Článek se zabývá čištěním generátorového
ODSTRAŇOVÁNÍ KYSELÝCH SLOŽEK Z PLYNŮ ZE ZPLYŇOVÁNÍ BIOMASY Petr Pekárek, Pavel Machač, Václav Koza, Božena Kremanová, Kateřina Bradáčová, Josef Kuba, Pedro Delgado Moniz Článek se zabývá čištěním generátorového
ELEKTROLÝZA. Autor: Mgr. Stanislava Bubíková. Datum (období) tvorby: 13. 3. 2012. Ročník: osmý
 Autor: Mgr. Stanislava Bubíková ELEKTROLÝZA Datum (období) tvorby: 13. 3. 2012 Ročník: osmý Vzdělávací oblast: Člověk a příroda / Chemie / Chemické reakce 1 Anotace: Žáci se seznámí s elektrolýzou. V rámci
Autor: Mgr. Stanislava Bubíková ELEKTROLÝZA Datum (období) tvorby: 13. 3. 2012 Ročník: osmý Vzdělávací oblast: Člověk a příroda / Chemie / Chemické reakce 1 Anotace: Žáci se seznámí s elektrolýzou. V rámci
Chemické veličiny, vztahy mezi nimi a chemické výpočty
 SBÍRKA ŘEŠENÝCH PŘÍKLADŮ PRO PROJEKT PŘÍRODNÍ VĚDY AKTIVNĚ A INTERAKTIVNĚ CZ.1.07/1.1.24/01.0040 Chemické veličiny, vztahy mezi nimi a chemické výpočty Mgr. Jana Žůrková, 2013, 20 stran Obsah 1. Veličiny
SBÍRKA ŘEŠENÝCH PŘÍKLADŮ PRO PROJEKT PŘÍRODNÍ VĚDY AKTIVNĚ A INTERAKTIVNĚ CZ.1.07/1.1.24/01.0040 Chemické veličiny, vztahy mezi nimi a chemické výpočty Mgr. Jana Žůrková, 2013, 20 stran Obsah 1. Veličiny
ZŠ ÚnO, Bratří Čapků 1332
 Úvodní obrazovka Menu (vlevo nahoře) Návrat na hlavní stránku Obsah Výsledky Poznámky Záložky edunet Konec Chemie 1 (pro 12-16 let) LangMaster Obsah (střední část) výběr tématu - dvojklikem v seznamu témat
Úvodní obrazovka Menu (vlevo nahoře) Návrat na hlavní stránku Obsah Výsledky Poznámky Záložky edunet Konec Chemie 1 (pro 12-16 let) LangMaster Obsah (střední část) výběr tématu - dvojklikem v seznamu témat
Základní škola, Ostrava Poruba, Bulharská 1532, příspěvková organizace
 Chemie - 8. ročník pozorování, pokus a bezpečnost práce Určí společné a rozdílné vlastnosti látek vlastnosti látek hustota, rozpustnost, tepelná a elektrická vodivost, vliv atmosféry na vlastnosti a stav
Chemie - 8. ročník pozorování, pokus a bezpečnost práce Určí společné a rozdílné vlastnosti látek vlastnosti látek hustota, rozpustnost, tepelná a elektrická vodivost, vliv atmosféry na vlastnosti a stav
SHRNUTÍ A ZÁKLADNÍ POJMY chemie 8.ročník ZŠ
 SHRNUTÍ A ZÁKLADNÍ POJMY chemie 8.ročník ZŠ 1. ČÍM SE ZABÝVÁ CHEMIE VLASTNOSTI LÁTEK, POKUSY - chemie přírodní věda, která studuje vlastnosti a přeměny látek pomocí pozorování, měření a pokusu - látka
SHRNUTÍ A ZÁKLADNÍ POJMY chemie 8.ročník ZŠ 1. ČÍM SE ZABÝVÁ CHEMIE VLASTNOSTI LÁTEK, POKUSY - chemie přírodní věda, která studuje vlastnosti a přeměny látek pomocí pozorování, měření a pokusu - látka
CHEMICKÉ TECHNOLOGIE PRO PROCESNÍ INŽENÝRSTVÍ N VÝROBA MTBE
 CHEMICKÉ TECHNOLOGIE PRO PROCESNÍ INŽENÝRSTVÍ N409059 VÝROBA MTBE Fyzikální a chemické vlastnosti Suroviny Reakce Technologie Dvoustupňová výroba Jednostupňová výroba Charakteristiky technologií Zdroje
CHEMICKÉ TECHNOLOGIE PRO PROCESNÍ INŽENÝRSTVÍ N409059 VÝROBA MTBE Fyzikální a chemické vlastnosti Suroviny Reakce Technologie Dvoustupňová výroba Jednostupňová výroba Charakteristiky technologií Zdroje
Přírodní zdroje uhlovodíků. a jejich zpracování
 Přírodní zdroje uhlovodíků a jejich zpracování 1 Rozdělení: Přírodní zdroje org. látek fosilní - zemní plyn, ropa, uhlí (vznikají geochemickými procesy miliony let) recentní (současné) - dřevo, rostlinné
Přírodní zdroje uhlovodíků a jejich zpracování 1 Rozdělení: Přírodní zdroje org. látek fosilní - zemní plyn, ropa, uhlí (vznikají geochemickými procesy miliony let) recentní (současné) - dřevo, rostlinné
VÝROBA VODÍKU reforming benzinových frakcí parní reforming zemního plynu parciální oxidace ropných zbytků zplyňováním biomasy elektrolýza
 VODÍK - představuje jeden z hlavních chemických prvků v celém vesmíru jak ve hvězdách, tak i mezigalaktickém prostoru; - tvoří přibližně 75 % jeho hmoty a dokonce 90 % všech atomů; - z chemického hlediska
VODÍK - představuje jeden z hlavních chemických prvků v celém vesmíru jak ve hvězdách, tak i mezigalaktickém prostoru; - tvoří přibližně 75 % jeho hmoty a dokonce 90 % všech atomů; - z chemického hlediska
Termochemie. Katedra materiálového inženýrství a chemie A Ing. Martin Keppert Ph.D.
 Termochemie Ing. Martin Keppert Ph.D. Katedra materiálového inženýrství a chemie keppert@fsv.cvut.cz A 329 http://tpm.fsv.cvut.cz/ Termochemie: tepelné jevy při chemických reakcích Chemická reakce: CH
Termochemie Ing. Martin Keppert Ph.D. Katedra materiálového inženýrství a chemie keppert@fsv.cvut.cz A 329 http://tpm.fsv.cvut.cz/ Termochemie: tepelné jevy při chemických reakcích Chemická reakce: CH
Energetické využití obnovitelných a alternativních zdrojů z hlediska celkových emisí
 Energetické využití obnovitelných a alternativních zdrojů z hlediska celkových emisí Doc. Ing. Jaromír Lederer, CSc. VUANCH, a.s., Unipetrol/UniCRE Obsah Co jsou obnovitelné a alternativní zdroje Principy
Energetické využití obnovitelných a alternativních zdrojů z hlediska celkových emisí Doc. Ing. Jaromír Lederer, CSc. VUANCH, a.s., Unipetrol/UniCRE Obsah Co jsou obnovitelné a alternativní zdroje Principy
Omezování plynných emisí. Ochrana ovzduší ZS 2010/2011
 Omezování plynných emisí Ochrana ovzduší ZS 2010/2011 1 Úvod Různé fyzikální a chemické principy + biotechnologie Principy: absorpce adsorpce oxidace a redukce katalytická oxidace a redukce kondenzační
Omezování plynných emisí Ochrana ovzduší ZS 2010/2011 1 Úvod Různé fyzikální a chemické principy + biotechnologie Principy: absorpce adsorpce oxidace a redukce katalytická oxidace a redukce kondenzační
SHRNUTÍ A ZÁKLADNÍ POJMY UČEBNICE ZÁKLADY CHEMIE 1
 SHRNUTÍ A ZÁKLADNÍ POJMY UČEBNICE ZÁKLADY CHEMIE 1 1. ČÍM SE ZABÝVÁ CHEMIE VLASTNOSTI LÁTEK, POKUSY - chemie přírodní věda, která studuje vlastnosti a přeměny látek pomocí pozorování, měření a pokusu -
SHRNUTÍ A ZÁKLADNÍ POJMY UČEBNICE ZÁKLADY CHEMIE 1 1. ČÍM SE ZABÝVÁ CHEMIE VLASTNOSTI LÁTEK, POKUSY - chemie přírodní věda, která studuje vlastnosti a přeměny látek pomocí pozorování, měření a pokusu -
TECHNOLOGIE KE SNIŽOVÁNÍ EMISÍ (SEKUNDÁRNÍ OPATŘENÍ K OMEZOVÁNÍ EMISÍ)
 TECHNOLOGIE KE SNIŽOVÁNÍ EMISÍ (SEKUNDÁRNÍ OPATŘENÍ K OMEZOVÁNÍ EMISÍ) 5. část TĚKAVÉ ORGANICKÉ SLOUČENINY A PACHOVÉ LÁTKY Zpracoval: Tým autorů EVECO Brno, s.r.o. TĚKAVÉ ORGANICKÉ SLOUČENINY Těkavé organické
TECHNOLOGIE KE SNIŽOVÁNÍ EMISÍ (SEKUNDÁRNÍ OPATŘENÍ K OMEZOVÁNÍ EMISÍ) 5. část TĚKAVÉ ORGANICKÉ SLOUČENINY A PACHOVÉ LÁTKY Zpracoval: Tým autorů EVECO Brno, s.r.o. TĚKAVÉ ORGANICKÉ SLOUČENINY Těkavé organické
Kombinovaná výroba elektrické energie a tepla pomocí vysokoteplotních palivových článků s tuhým elektrolytem
 VYSOKÁ ŠKOLA CHEMICKO-TECHNOLOGICKÁ V PRAZE Ústav chemických procesů Akademie věd ČR Kombinovaná výroba elektrické energie a tepla pomocí vysokoteplotních palivových článků s tuhým elektrolytem Michael
VYSOKÁ ŠKOLA CHEMICKO-TECHNOLOGICKÁ V PRAZE Ústav chemických procesů Akademie věd ČR Kombinovaná výroba elektrické energie a tepla pomocí vysokoteplotních palivových článků s tuhým elektrolytem Michael
Termochemie se zabývá tepelným zabarvením chemických reakcí Vychází z 1. termodynamického zákona. U změna vnitřní energie Q teplo W práce
 Termochemie Termochemie se zabývá tepelným zabarvením chemických reakcí Vychází z 1. termodynamického zákona U = Q + W U změna vnitřní energie Q teplo W práce Teplo a práce dodané soustavě zvyšují její
Termochemie Termochemie se zabývá tepelným zabarvením chemických reakcí Vychází z 1. termodynamického zákona U = Q + W U změna vnitřní energie Q teplo W práce Teplo a práce dodané soustavě zvyšují její
H - -I (hydridy kovů) vlastnosti: plyn - nekov 14x lehčí než vzduch bez barvy, chuti, zápachu se vzduchem tvoří výbušnou směs redukční činidlo
 Otázka: Vodík, kyslík Předmět: Chemie Přidal(a): Prang Vodík 1. Charakteristika 1 1 H 1s 1 ; 1 proton, jeden elektron nejlehčí prvek výskyt: volný horní vrstva atmosféry, vesmír - elementární vázaný- anorganické,
Otázka: Vodík, kyslík Předmět: Chemie Přidal(a): Prang Vodík 1. Charakteristika 1 1 H 1s 1 ; 1 proton, jeden elektron nejlehčí prvek výskyt: volný horní vrstva atmosféry, vesmír - elementární vázaný- anorganické,
VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ FAKULTA STROJNÍHO INŽENÝRSTVÍ - ENERGETICKÝ ÚSTAV ODBOR TERMOMECHANIKY A TECHNIKY
 VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ FAKULTA STROJNÍHO INŽENÝRSTVÍ - ENERGETICKÝ ÚSTAV ODBOR TERMOMECHANIKY A TECHNIKY PROSTŘEDÍ doc. Ing. Josef ŠTETINA, Ph.D. Předmět 3. ročníku BS http://ottp.fme.vutbr.cz/sat/
VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ FAKULTA STROJNÍHO INŽENÝRSTVÍ - ENERGETICKÝ ÚSTAV ODBOR TERMOMECHANIKY A TECHNIKY PROSTŘEDÍ doc. Ing. Josef ŠTETINA, Ph.D. Předmět 3. ročníku BS http://ottp.fme.vutbr.cz/sat/
VÝUKOVÝ MODUL MEMBRÁNOVÝCH PROCESŮ SYLABY PŘEDNÁŠEK TRANSPORT LÁTEK MEMBRÁNAMI MEMBRÁNOVÉ MATERIÁLY
 VÝUKOVÝ MODUL MEMBRÁNOVÝCH PROCESŮ SYLABY PŘEDNÁŠEK TRANSPORT LÁTEK MEMBRÁNAMI zodpovědni: P. Mikulášek, H. Jiránková, M. Šípek, K. Friess, K. Bouzek Transport látek porézními membránami (P. Mikulášek)
VÝUKOVÝ MODUL MEMBRÁNOVÝCH PROCESŮ SYLABY PŘEDNÁŠEK TRANSPORT LÁTEK MEMBRÁNAMI zodpovědni: P. Mikulášek, H. Jiránková, M. Šípek, K. Friess, K. Bouzek Transport látek porézními membránami (P. Mikulášek)
Odstraňování Absorption minoritních nečistot z bioplynu
 www.vscht.cz Ústav plynárenství, koksochemie a ochrany ovzduší Laboruntersuchungen der Karel Ciahotný Gastrocknung e-mail:karel.ciahotny@vscht.cz mit Hilfe von Adsorption und Odstraňování Absorption minoritních
www.vscht.cz Ústav plynárenství, koksochemie a ochrany ovzduší Laboruntersuchungen der Karel Ciahotný Gastrocknung e-mail:karel.ciahotny@vscht.cz mit Hilfe von Adsorption und Odstraňování Absorption minoritních
E ŘEŠENÍ KONTROLNÍHO TESTU ŠKOLNÍHO KOLA
 Ústřední komise Chemické olympiády 48. ročník 2011/2012 ŠKOLNÍ KOLO kategorie A a E ŘEŠENÍ KONTROLNÍ TESTU ŠKOLNÍ KOLA KONTROLNÍ TEST ŠKOLNÍ KOLA (60 BODŮ) ANORGANICKÁ CEMIE 16 BODŮ Úloha 1 8 bodů Napište
Ústřední komise Chemické olympiády 48. ročník 2011/2012 ŠKOLNÍ KOLO kategorie A a E ŘEŠENÍ KONTROLNÍ TESTU ŠKOLNÍ KOLA KONTROLNÍ TEST ŠKOLNÍ KOLA (60 BODŮ) ANORGANICKÁ CEMIE 16 BODŮ Úloha 1 8 bodů Napište
CCS technologie typu pre-combustion v podmínkách České Republiky
 CCS technologie typu pre-combustion v podmínkách České Republiky VITVAROVÁ M., NOVOTNÝ V., DLOUHÝ T., HRDLIČKA F. (ČVUT v Praze, Fakulta strojní) JAKOBSEN J., BERSTAD D., HAGEN B., ROUSSANALY S., ANANTHARAMAN
CCS technologie typu pre-combustion v podmínkách České Republiky VITVAROVÁ M., NOVOTNÝ V., DLOUHÝ T., HRDLIČKA F. (ČVUT v Praze, Fakulta strojní) JAKOBSEN J., BERSTAD D., HAGEN B., ROUSSANALY S., ANANTHARAMAN
chartakterizuje přírodní vědy,charakterizuje chemii, orientuje se v možných využití chemie v běžníém životě
 Kapitola Téma (Učivo) Znalosti a dovednosti (výstup). Úvod do chemie Charakteristika chemie a její význam Charakteristika přírodních věd charakteristika chemie Chemie kolem nás chartakterizuje přírodní
Kapitola Téma (Učivo) Znalosti a dovednosti (výstup). Úvod do chemie Charakteristika chemie a její význam Charakteristika přírodních věd charakteristika chemie Chemie kolem nás chartakterizuje přírodní
Kyselina fosforečná Suroviny: Výroba: termický způsob extrakční způsob
 Kyselina fosforečná bezbarvá krystalická sloučenina snadno rozpustná ve vodě komerčně dodávané koncentrace 75% H 3 PO 4 s 54,3% P 2 O 5 80% H 3 PO 4 s 58.0% P 2 O 5 85% H 3 PO 4 s 61.6% P 2 O 5 po kyselině
Kyselina fosforečná bezbarvá krystalická sloučenina snadno rozpustná ve vodě komerčně dodávané koncentrace 75% H 3 PO 4 s 54,3% P 2 O 5 80% H 3 PO 4 s 58.0% P 2 O 5 85% H 3 PO 4 s 61.6% P 2 O 5 po kyselině
Chemie - 3. ročník. přesahy, vazby, mezipředmětové vztahy průřezová témata. očekávané výstupy RVP. témata / učivo. očekávané výstupy ŠVP.
 očekávané výstupy RVP témata / učivo Chemie - 3. ročník Žák: očekávané výstupy ŠVP přesahy, vazby, mezipředmětové vztahy průřezová témata 1.1., 1.2., 1.3., 1.4., 2.1. 1. Látky přírodní nebo syntetické
očekávané výstupy RVP témata / učivo Chemie - 3. ročník Žák: očekávané výstupy ŠVP přesahy, vazby, mezipředmětové vztahy průřezová témata 1.1., 1.2., 1.3., 1.4., 2.1. 1. Látky přírodní nebo syntetické
Název odpadu. 010307 N Jiné odpady z fyzikálního a chemického zpracování rudných nerostů obsahující nebezpečné látky x
 5. Stabilizace CELIO a.s. Název odpadu 010304 N Hlušina ze zpracování sulfidické rudy obsahující kyseliny nebo kyselinotvorné látky x 010305 N Jiná hlušina obsahující nebezpečné látky x 010307 N Jiné odpady
5. Stabilizace CELIO a.s. Název odpadu 010304 N Hlušina ze zpracování sulfidické rudy obsahující kyseliny nebo kyselinotvorné látky x 010305 N Jiná hlušina obsahující nebezpečné látky x 010307 N Jiné odpady
Gymnázium a Střední odborná škola, Rokycany, Mládežníků 1115
 Gymnázium a Střední odborná škola, Rokycany, Mládežníků 1115 Číslo projektu: Číslo šablony: CZ.1.07/1.5.00/34.0410 III/2 Inovace a zkvalitnění výuky prostřednictvím ICT. Název materiálu: Fosilní zdroje
Gymnázium a Střední odborná škola, Rokycany, Mládežníků 1115 Číslo projektu: Číslo šablony: CZ.1.07/1.5.00/34.0410 III/2 Inovace a zkvalitnění výuky prostřednictvím ICT. Název materiálu: Fosilní zdroje
Třídění látek. Chemie 1.KŠPA
 Třídění látek Chemie 1.KŠPA Systém (soustava) Vymezím si kus prostoru, látky v něm obsažené nazýváme systém soustava okolí svět Stěny soustavy Soustava může být: Izolovaná = stěny nedovolí výměnu částic
Třídění látek Chemie 1.KŠPA Systém (soustava) Vymezím si kus prostoru, látky v něm obsažené nazýváme systém soustava okolí svět Stěny soustavy Soustava může být: Izolovaná = stěny nedovolí výměnu částic
Denitrifikace. Ochrana ovzduší ZS 2012/2013
 Denitrifikace Ochrana ovzduší ZS 2012/2013 1 Úvod Pojem oxidy dusíku NO NO 2 Další formy NO x Vznik NO x 2 Vlastnosti NO Oxid dusnatý Vlastnosti M mol,no = 30,01 kg/kmol V mol,no,n = 22,41 m 3 /kmol ρ
Denitrifikace Ochrana ovzduší ZS 2012/2013 1 Úvod Pojem oxidy dusíku NO NO 2 Další formy NO x Vznik NO x 2 Vlastnosti NO Oxid dusnatý Vlastnosti M mol,no = 30,01 kg/kmol V mol,no,n = 22,41 m 3 /kmol ρ
2. KINETICKÁ ANALÝZA HOMOGENNÍCH REAKCÍ
 2. KINETICKÁ ANALÝZA HOMOGENNÍCH REAKCÍ Úloha 2-1 Řád reakce a rychlostní konstanta integrální metodou stupeň přeměny... 2 Úloha 2-2 Řád reakce a rychlostní konstanta integrální metodou... 2 Úloha 2-3
2. KINETICKÁ ANALÝZA HOMOGENNÍCH REAKCÍ Úloha 2-1 Řád reakce a rychlostní konstanta integrální metodou stupeň přeměny... 2 Úloha 2-2 Řád reakce a rychlostní konstanta integrální metodou... 2 Úloha 2-3
Bilan a ce c zák á l k ad a ní pojm j y m aplikace zákonů o zachování čehokoli 10.10.2008 3
 Výpočtový seminář z Procesního inženýrství podzim 2008 Bilance Materiálové a látkové 10.10.2008 1 Tématické okruhy bilance - základní pojmy bilanční schéma způsoby vyjadřování koncentrací a přepočtové
Výpočtový seminář z Procesního inženýrství podzim 2008 Bilance Materiálové a látkové 10.10.2008 1 Tématické okruhy bilance - základní pojmy bilanční schéma způsoby vyjadřování koncentrací a přepočtové
Technologie přímého aditivního odsíření pro fluidní kotle malých a středních výkonů
 Technologie přímého aditivního odsíření pro fluidní kotle malých a středních výkonů Ing. Matěj Obšil, Uchytil, s.r.o. doc. Ing. Jan Hrdlička, Ph.D., ČVUT v Praze, Ústav energetiky MOTIVACE Ø emisní limit
Technologie přímého aditivního odsíření pro fluidní kotle malých a středních výkonů Ing. Matěj Obšil, Uchytil, s.r.o. doc. Ing. Jan Hrdlička, Ph.D., ČVUT v Praze, Ústav energetiky MOTIVACE Ø emisní limit
Amoniak průmyslová výroba syntetického amoniaku
 Amoniak 1913 průmyslová výroba syntetického amoniaku využití 20 % výroba dusíkatých hnojiv 80 % nejrůznější odvětví průmyslu (plasty, vlákna, výbušiny, hydrazin, aminy, amidy, nitrily a další organické
Amoniak 1913 průmyslová výroba syntetického amoniaku využití 20 % výroba dusíkatých hnojiv 80 % nejrůznější odvětví průmyslu (plasty, vlákna, výbušiny, hydrazin, aminy, amidy, nitrily a další organické
Přírodní zdroje uhlovodíků
 Tento výukový materiál vznikl za přispění Evropské unie, státního rozpočtu ČR a Středočeského kraje Říjen 2010 Mgr. Alena Jirčáková Zemní plyn - vznik: Výskyt často spolu s ropou (naftový zemní plyn) nebo
Tento výukový materiál vznikl za přispění Evropské unie, státního rozpočtu ČR a Středočeského kraje Říjen 2010 Mgr. Alena Jirčáková Zemní plyn - vznik: Výskyt často spolu s ropou (naftový zemní plyn) nebo
"...s určitými riziky ve vztahu k životnímu prostředí jsou spojeny všechny systémy a druhy lidské činnosti, ať už si toho jsme vědomi, či nikoli...
 Vlivy a účinky na ŽP "...s určitými riziky ve vztahu k životnímu prostředí jsou spojeny všechny systémy a druhy lidské činnosti, ať už si toho jsme vědomi, či nikoli..." ŽP (příroda)... nikdy není zakonzervovaná
Vlivy a účinky na ŽP "...s určitými riziky ve vztahu k životnímu prostředí jsou spojeny všechny systémy a druhy lidské činnosti, ať už si toho jsme vědomi, či nikoli..." ŽP (příroda)... nikdy není zakonzervovaná
UHLOVODÍKOVÉ TECHNOLOGIE PERSPEKTIVY A VÝZVY
 UHLOVODÍKOVÉ TECHNOLOGIE PERSPEKTIVY A VÝZVY Doc. Ing. Jaromír Lederer, CSc. VUANCH/UniCRE O ČEM BUDEME DISKUTOVAT? CO POTŘEBUJEME DNES? KRYTÍ NAŠICH POTŘEB - DOSTATEK ROPY ZÁKLADNÍ CHEMIKÁLIE A PALIVA
UHLOVODÍKOVÉ TECHNOLOGIE PERSPEKTIVY A VÝZVY Doc. Ing. Jaromír Lederer, CSc. VUANCH/UniCRE O ČEM BUDEME DISKUTOVAT? CO POTŘEBUJEME DNES? KRYTÍ NAŠICH POTŘEB - DOSTATEK ROPY ZÁKLADNÍ CHEMIKÁLIE A PALIVA
Energie z odpadních vod. Karel Plotěný
 Energie z odpadních vod Karel Plotěný Propojení vody a energie Voda pro Energii Produkce paliv (methan, ethanol, vodík, ) Těžba a rafinace Vodní elektrárny Chladící okruhy Čištění odpadních vod Ohřev vody
Energie z odpadních vod Karel Plotěný Propojení vody a energie Voda pro Energii Produkce paliv (methan, ethanol, vodík, ) Těžba a rafinace Vodní elektrárny Chladící okruhy Čištění odpadních vod Ohřev vody
Energetika se zabývá získáváním, přeměnou a distribucí všech forem energie. Energii nevytváříme, pouze transformujeme z jedné formy na druhou.
 VŠB TU Ostrava Energetika se zabývá získáváním, přeměnou a distribucí všech forem energie. Energii nevytváříme, pouze transformujeme z jedné formy na druhou. VŠB TU Ostrava 2 VŠB TU Ostrava 3 Dle zdroje:
VŠB TU Ostrava Energetika se zabývá získáváním, přeměnou a distribucí všech forem energie. Energii nevytváříme, pouze transformujeme z jedné formy na druhou. VŠB TU Ostrava 2 VŠB TU Ostrava 3 Dle zdroje:
ZŠ ÚnO, Bratří Čapků 1332
 Úvodní obrazovka Menu (vlevo nahoře) Návrat na hlavní stránku Obsah Výsledky Poznámky Záložky edunet Konec Chemie 2 (pro 12-16 let) LangMaster Obsah (střední část) výběr tématu - dvojklikem v seznamu témat
Úvodní obrazovka Menu (vlevo nahoře) Návrat na hlavní stránku Obsah Výsledky Poznámky Záložky edunet Konec Chemie 2 (pro 12-16 let) LangMaster Obsah (střední část) výběr tématu - dvojklikem v seznamu témat
Vzdělávací oblast: Člověk a příroda. Vyučovací předmět: Chemie. Třída: tercie. Očekávané výstupy. Poznámky. Přesahy. Žák: Průřezová témata
 Vzdělávací oblast: Člověk a příroda Vyučovací předmět: Chemie Třída: tercie Očekávané výstupy Uvede příklady chemického děje a čím se zabývá chemie Rozliší tělesa a látky Rozpozná na příkladech fyzikální
Vzdělávací oblast: Člověk a příroda Vyučovací předmět: Chemie Třída: tercie Očekávané výstupy Uvede příklady chemického děje a čím se zabývá chemie Rozliší tělesa a látky Rozpozná na příkladech fyzikální
Technologie zplyňování biomasy
 Technologie zplyňování biomasy Obsah prezentace Profil společnosti Proces zplyňování Zplyňovací technologie Generátorový plyn Rozdělení technologií Typy zplyňovacích jednotek Čištění plynu Systém GB Gasifired
Technologie zplyňování biomasy Obsah prezentace Profil společnosti Proces zplyňování Zplyňovací technologie Generátorový plyn Rozdělení technologií Typy zplyňovacích jednotek Čištění plynu Systém GB Gasifired
Negativní vliv energetického využití biomasy Ing. Marek Baláš, Ph.D.
 Negativní vliv energetického využití biomasy Ing. Marek Baláš, Ph.D. Osnova 2 Legislativa Biomasa druhy složení Emise vznik, množství, vlastnosti, dopad na ŽP a zdraví, opatření CO SO 2 NO x Chlor TZL
Negativní vliv energetického využití biomasy Ing. Marek Baláš, Ph.D. Osnova 2 Legislativa Biomasa druhy složení Emise vznik, množství, vlastnosti, dopad na ŽP a zdraví, opatření CO SO 2 NO x Chlor TZL
ZÁKLADNÍ CHEMICKÉ VÝPOČTY
 ZÁKLADNÍ CHEMICKÉ VÝPOČTY Látkové množství - vyjadřování množství: jablka pivo chleba uhlí - (téměř každá míra má svojí jednotku) v chemii existuje univerzální veličina pro vyjádření množství látky LÁTKOVÉ
ZÁKLADNÍ CHEMICKÉ VÝPOČTY Látkové množství - vyjadřování množství: jablka pivo chleba uhlí - (téměř každá míra má svojí jednotku) v chemii existuje univerzální veličina pro vyjádření množství látky LÁTKOVÉ
