Návod k Použití Soupravy SURVEYOR Scan KRAS Kit Exons 3 & 4 CE IVD pro Systémy DHPLC
|
|
|
- Jana Kopecká
- před 6 lety
- Počet zobrazení:
Transkript
1 1 Výrobce Návod k Použití Soupravy SURVEYOR Scan KRAS Kit Exons 3 & 4 CE IVD pro Systémy DHPLC Tento návod k použití si důkladně přečtěte před použitím tohoto produktu. Uschovejte si tento návod k použití, abyste se k němu mohli v případě potřeby vrátit.
2 Tato stránka je úmyslně ponechána prázdná.
3 Obsah 1 Výrobce Souprava SURVEYOR Scan KRAS Kit Exons 3 & 4 CE IVD Použití Indikace pro použití Principy testu pro detekci mutací SURVEYOR Scan KRAS Geny KRAS a NRAS Analýza vzorků pacientů s použitím souprav SURVEYOR Scan Nukleáza SURVEYOR Nuclease Původ kontrol v soupravě Součásti Počet vzorků, které lze testovat pomocí jedné soupravy Sekvenování DNA Další požadované vybavení a reagencie Příprava reagencií Skladování a doba použitelnosti Upozornění a preventivní opatření Získání primárního vzorku, manipulace a uchovávání Postup testu Detekce somatických mutací s použitím souprav SURVEYOR Scan - přehled Pokyny pro jednotlivé kroky POČÁTEČNÍ nastavení/kalibrace systému DHPLC Před analýzou vzorků KRAS Templát Pracovní schéma Amplifikační protokol Program termocykleru pro amplifikační protokol Kontrola kvality produktů PCR Digesce nukleázou SURVEYOR Nuclease Kontrolní postupy Kontrola kvality soupravy SURVEYOR Scan KRAS Kit Exons 3 & 4 CE IVD Použití kontrolních plasmidových DNA Interpretace výsledků Analýza exonů KRAS Exons 3 & 4 pomocí nukleázy SURVEYOR Nuclease Kontrola výsledků SURVEYOR Scan Příklady výsledků Co je třeba dodržovat Detekční hladina mutací získaných soupravou SURVEYOR Scan Potvrzení sekvence Omezení testu Příloha A A.1 Návrh uspořádání destičky pro soupravy SURVEYOR Scan A.2 Označení na kontrolní DNA A.3 Požadavky pro denaturaci v systému HPLC (DHPLC) A.4 Uspořádání laboratoře pro testy PCR A.5 Odkazy na literaturu Příloha B Pokyny pro řešení problémů Podrobnosti pro objednávku Kontaktní údaje Překlad Prohlášení Licence, obchodní známky a autorská práva... 35
4 1 Výrobce 1 Výrobce Výrobce Zástupce pro EU M P Transgenomic, Inc Emmet Street, Omaha, NE 68164, USA Tel: Transgenomic Limited 40 Watt Road, Hillington Park, Glasgow G52 4RY, UK Tel: Souprava SURVEYOR Scan KRAS Kit Exons 3 & 4 CE IVD 2.1 Použití Pouze pro profesionální použití. Souprava od společnosti Transgenomic SURVEYOR Scan KRAS Kit Exons 3 & 4 CE IVD tvoří diagnostický test in vitro zjišťující somatické mutace v části Exons 3 a 4 genu KRAS. Tyto mutace jsou indikovány píky, které jsou výsledkem štěpení enzymem SURVEYOR Nuclease a zahrnují mutace známé svým potenciálním klinickým významem. Tato souprava je určena pro použití v klinické diagnostické laboratoři příslušně školenými pracovníky provádějícími testování DNA extrahované z tkání zalitých v parafínu a fixovaných formalinem. Tato souprava (katalogové číslo ) je dodávána jako jedna krabice obsahující níže uvedené komponenty. Tento návod k použití je k dispozici ke stažení na Indikace pro použití Kliničtí pracovníci mohou používat soupravu SURVEYOR Scan KRAS Kit Exons 3 & 4 CE IVD se systémem DHPLC jako vodítko k rozhodnutí, zda nádor kolorektálního karcinomu pacienta nebude vykazovat odezvu vůči léčivům na bázi anti-egfr (receptor pro epidermální růstový faktor), jako je panitumumab. Souprava SURVEYOR Scan KRAS kit Exons 3 & 4 CE IVD se používá pro analýzu vzorků identifikovaných po analýze pomocí soupravy SURVEYOR Scan KRAS Kit Exon 2 CE IVD jako KRAS Exon 2 Wild-Type. Tato souprava se rovněž používá v souvislosti se soupravou SURVEYOR Scan NRAS Kit Exons 2, 3 & 4 CE IVD. Souprava SURVEYOR Scan KRAS Kit Exons 3 & 4 CE IVD se nesmí používat pro diagnózu kolorektálního nebo jiného karcinomu. Souprava SURVEYOR Scan KRAS Kit Exons 3 & 4 CE IVD tvoří test zjišťující přítomnost potenciálních somatických mutací v části Exons 3 a 4 genu KRAS, avšak neověřuje sekvenci mutace. Pro potvrzení přesné zjištěné mutace je třeba použít další analytickou metodu, jako je sekvenování DNA. Ačkoli výsledky analýzy získané touto soupravou ukážou mutační stav pacienta, je třeba zvážit i další faktory, včetně mutací v úsecích KRAS Exon 2 a NRAS Exons 2, 3 a 4. Výsledky získané soupravou SURVEYOR Scan KRAS Kit Exons 3 & 4 CE IVD nesmí být jedinou cestou k učinění rozhodnutí o léčbě pacienta s kolorektálním karcinomem. Je důležité mít na mysli, že použití systému DHPLC k identifikaci vzorků pozitivních na mutaci genu KRAS lze brát pouze jako vodítko a všechny mutace musí být potvrzeny další analýzou, jako je např. sekvenování DNA. Návod k použití soupravy SURVEYOR Scan KRAS kit Exons 3 & 4 CE IVD pro systém DHPLC strana 3
5 3 Principy testu pro detekci mutací SURVEYOR Scan KRAS 3 Principy testu pro detekci mutací SURVEYOR Scan KRAS 3.1 Geny KRAS a NRAS Léčivé přípravky cílící na receptor pro epidermální růstový faktor (EGFR) prokázaly svoji účinnost vůči kolorektálnímu karcinomu. Výzkum ukázal, že přibližně 40 % kolorektálních nádorů obsahuje somatické mutace genu KRAS a klinické studie ukázaly, že mutace v úseku KRAS exon 2 (kodony 12 a 13) předpovídají nedostatečnou odezvu vůči léčbě cílené na EGFR. Poslední výzkumné studie ukázaly, že populaci pacientů lze dále specifikovat jako pacienty, jejichž metastazovaný nádor kolorektálního karcinomu obsahuje další mutaci v úseku KRAS exons 3 a 4 a úsek NRAS exons 2, 3 a 4 rovněž vykazoval tendenci k nedostatečné odezvě vůči léčbě cílené na EGFR 1-7. Tato souprava je určena k použití v diagnostické analýze somatických mutací v úseku KRAS Exons 3 a 4. Souprava SURVEYOR Scan KRAS Kit Exons 3 & 4 CE IVD je testem pro detekci sekvencí a malých změn v důsledku inzerce/delece v úseku Exons 3 a 4 genu KRAS. Mutace v kodonech 59, 61, 117 a 146 genu KRAS souvisejí s nedostatečnou účinností přípravku panitumumab. Pro mutace v kodonech 61, 117 a 146 jsou v této soupravě dodány kontroly Positive Controls. V této soupravě je použita chráněná technologie společnosti Transgenomic s názvem SURVEYOR Nuclease, která spolu se systémem DHPLC poskytuje jednoduchou a citlivou detekci potenciálních mutací. Tato technologie může zjistit 2-5% směs mutantů na pozadí nezmutované DNA. Validační studie ukázaly extrémně vysokou konkordanci se sekvenováním kvalitně charakterizovaných vzorků kolorektálního karcinomu. Použití soupravy SURVEYOR Scan KRAS Kit Exons 3 & 4 CE IVD sníží pro uživatele nároky na sekvenování a umožní zjištění sekvence, když software pro automatické sekvenování nezjistí přítomnost mutace nízké hladiny. Vzhledem vysoké citlivosti tohoto testu ve srovnání se Sanger metodou sekvenování se doporučuje uspořádat laboratoř tak, aby se zabránilo příčné kontaminaci vzorků a kontrol. Ukázku optimálního uspořádání laboratoře naleznete v Příloze A.4 Uspořádání laboratoře pro testy PCR. 3.2 Analýza vzorků pacientů s použitím souprav SURVEYOR Scan Soupravu SURVEYOR Scan KRAS Kit Exons 3 & 4 CE IVD lze použít pouze v rámci jednoho z níže uvedených pracovních schémat. Pracovní schéma A Vzorek pacienta Vzorek pacienta Pracovní schéma B Provést test v KRAS Exons 2, 3 a 4 a NRAS Exons 2, 3 a 4 Zaznamenat výsledky Provést test v KRAS Exon 2 Výsledek mutace KRAS v kodonu 12 nebo 13 Výsledek KRAS kodon 12 nebo 13 Wild-type Zaznamenat výsledky Provést test v KRAS Exons 3 a 4 a NRAS Exons 2, 3 a 4 Zaznamenat výsledky Obrázek 1 Schémata pro detekci mutací soupravou SURVEYOR Scan při screeningu genů KRAS a NRAS Návod k použití soupravy SURVEYOR Scan KRAS kit Exons 3 & 4 CE IVD pro systém DHPLC strana 4
6 3 Principy testu pro detekci mutací SURVEYOR Scan KRAS Návrh uspořádání 96jamkových destiček pro analýzu všech úseků KRAS a NRAS Exons 2-4 naleznete v Příloze A.1 Uspořádání destiček v soupravách SURVEYOR Scan. 3.3 Nukleáza SURVEYOR Nuclease Nukleáza SURVEYOR Nuclease od společnosti Transgenomic je mismatch - specifická (specifická pro chybné párování) endonukleáza z rostlinné DNA, která skenuje známé i neznámé mutace a polymorfismy v heteroduplexní DNA 8.Tento enzym štěpí s vysokou specificitou DNA v místech substituce báze chybným párováním a v místech jiných odchylek. Tato DNA endonukleáza štěpí oba řetězce heteroduplexu DNA na straně 3 chybně párovaného místa. Rozpoznává se chybné párování vzniklé inzercí/delecí a substitucí bází, avšak účinnost štěpení se mění podle sekvence chybného párování. Obrázek 2. Obrázek 1. Mechanismus účinku nukleázy SURVEYOR Nuclease. Endonukleáza rozpoznává chybné párování a provádí štěpení na straně 3 každé báze v chybném párování. Tím je štěpena dvoušroubovice DNA s přesahující jednou bází na konci 3. Nukleáza SURVEYOR Nuclease byla použita v širokém rozsahu situací pro přesnou detekci mutací a genetického polymorfismu.nukleáza SURVEYOR Nuclease byl například použita k ověření přítomnosti známých mutací v řadě genů spojených s karcinomem ledvin, plic, hlavy a krku, s leukémií, endometriálním karcinomem a s předpovědí výsledku radioterapie 9,10,11. Účelem soupravy SURVEYOR Scan KRAS Kit Exons 3 & 4 CE IVD je štěpit chybná párování v úseku KRAS Exons 3 a 4 před následnou analýzou systémem DHPLC. Poznámka:Je-li vzorek 100% mutantní DNA, nebudou se tvořit žádné heteroduplexy a vzorek se bude jevit jako Wild-Type. Avšak bioptické vzorky nádorů budou obsahovat vzhledem k heterogenitě nádorů buňky Wild-Type a kontaminující normální tkáň; 5% typ Wild-Type je pomocí této soupravy detekovatelný na křivkách identických s 5% mutantní DNA. Poznámka: Pro tento test lze používat pouze polymerázu DNA Polymerase dodávanou v soupravě. Poznámka: Dodržujte konkrétní pokyny v příručce pro systém DHPLC. V zájmu úspěšného používání této soupravy důrazně doporučujeme, abyste si tuto příručku důkladně přečetli a pozorně postupovali podle pokynů a návodů v ní obsažených. Uživatelé pracující s touto soupravou poprvé by měli provést kontrolní experimenty uvedené v části Použití kontrolních plasmidových DNA. Máte-li další dotazy nebo potřebujete-li asistenci, zatelefonujte na číslo (888) (pouze pro severní Ameriku), +1 (402) nebo +44 (0) (Evropa) a požádejte o KRAS support (podporu pro KRAS). Další možností je poslat nám na: 4 Původ kontrol v soupravě SURVEYORscan@Transgenomic.com Kontroly dodávané s touto soupravou jsou plasmidové klony sekvencí v KRAS Exons 3 a 4. Všechny klony byly sekvenovány, aby byla ověřena věrnost jejich sekvence ve srovnání s referenční NCBI Reference Sequence: NG_ Kontroly mají genetickou známku. Viz Příloha A.2 Označení na kontrolní DNA; tyto varianty sekvence KRAS Wild-Type v úseku, kde se mutace nepředpokládají, lze použít k řešení problémů Návod k použití soupravy SURVEYOR Scan KRAS kit Exons 3 & 4 CE IVD pro systém DHPLC strana 5
7 4 Původ kontrol v soupravě s kontaminací vzorků pomocí kontrol Positive Controls. Ukázku takové kontaminace ukazuje křivka SURVEYOR Scan v Příloze B - Pokyny pro řešení problémů, 8. Kontrola KRAS Control Wild-Type byla vytvořena syntézou a klonováním sekvence KRAS Exons 2, 3 a 4 s použitím výše uvedené sekvence NCBI. Kontrola KRAS Positive Control Exon 3 byla vytvořena syntézou sekvence KRAS Exon 3 s použitím výše referenční sekvence obsahující mutaci Q61H. Sekvenováním DNA bylo potvrzeno, že jediná změna v sekvenci je v kodonu 61, a to změna CAA>CAC (mutace Q61H). Tento klon je poté zkombinován s DNA KRAS Control Wild-Type za vytvoření heterozygotní směsi. Kontrola KRAS Positive Control Exon 4A byla vytvořena syntézou úseku KRAS Exon 4 s použitím výše uvedené reference, avšak obsahující mutaci K117N. Sekvenováním DNA bylo potvrzeno, že jediná změna v sekvenci je v kodonu 117, a to změna AAA>AAT (mutace K117N). Tento klon je poté zkombinován s DNA KRAS Control Wild-Type za vytvoření heterozygotní směsi. Kontrola KRAS Positive Control Exon 4B byla vytvořena syntézou úseku KRAS Exon 4 s použitím výše uvedené reference, avšak obsahující mutaci A146T. Sekvenováním DNA bylo potvrzeno, že jediná změna v sekvenci je v kodonu 146, a to změna GCA>ACA (mutace A146T). Tento klon je poté zkombinován s KRAS Control Wild-Type Exon DNA za vytvoření heterozygotní směsi. 5 Součásti Souprava SURVEYOR Scan KRAS Kit Exons 3 & 4 CE IVD obsahuje (1) krabici se složkami pro digesci SURVEYOR s10 reagenčními zkumavkami bez prázdných otvorů a (2) složky pro PCR a kontroly s nosičem zkumavek obsahujícím 13 reagenčních zkumavek a 7 prázdných otvorů. Katalogové číslo Komponenta Krabice se složkami pro digesci SURVEYOR Barva víčka zkumavky Objem pro 100 reakcí SURVEYOR Nuclease W růžová 2 x 105 µl SURVEYOR Enhancer W2 černá 105 µl SURVEYOR Enhancer Cofactor růžová 105 µl M MgCl 2 Solution hnědá 105 µl SURVEYOR Stop Solution červená 250 µl F Universal Sequencing Primer 1 (10 µm) oranžová 2 x 125 µl R Universal Sequencing Primer 2 (10 µm) oranžová 2 x 125 µl Krabice se složkami pro PCR a s kontrolami DNA Polymerase červená 100 µl DNA Polymerase 10X PCR Buffer čirá 1 ml dntps (10 mm) čirá 500 µl F KRAS Primer Exon 3 Forward (10 µm) modrá 90 µl R KRAS Primer Exon 3 Forward (10 µm) modrá 90 µl F KRAS Primer Exon 2 Forward (10 µm) modrá 90 µl R KRAS Primer Exon 2 Forward (10 µm) modrá 90 µl F KRAS Primer Exon 2 Forward (10 µm) modrá 90 µl R KRAS Primer Exon 2 Forward (10 µm) modrá 90 µl KRAS Control Wild-Type žlutá 120 µl KRAS Positive Control Exon 3 zelená 40 µl KRAS Positive Control Exon 4A zelená 40 µl KRAS Positive Control Exon 4B zelená 40 µl Návod k použití Lze stáhnout z webu* Návod k použití soupravy SURVEYOR Scan KRAS kit Exons 3 & 4 CE IVD pro systém DHPLC strana 6
8 5 Součásti 5.1 Počet vzorků, které lze testovat pomocí jedné soupravy Souprava SURVEYOR Scan KRAS Kit Exons 3 & 4 CE IVD je určena pro testování 100 reakcí. Celkový počet vzorků, které lze testovat pomocí soupravy, závisí na průměrné velikosti testované dávky vzorků, neboť v každé destičce s reakčními směsmi musí být zahrnuta jedna sestava kontrolních reakcí (kontroly Wild-Type Controls, Positive Controls a kontroly bez templátu). Níže uvedená tabulka ukazuje počet vzorků, které lze analyzovat soupravou KRAS v závislosti na průměrné velikosti dávky vzorků. To zahrnuje (a) 9 kontrol (3x Wild-Type, 3x Positive Controls, 3x kontroly bez templátu) požadovaných pro každý běh a (b) limit 100 reakcí na jednu soupravu. Poznámka: Analyzuje-li se více destiček, musí být na každé destičce zahrnuta sestava 9 výše uvedených kontrol. Proto dvě destičky budou vyžadovat celkem 18 kontrolních reakcí, 3 destičky budou vyžadovat 27 kontrolních reakcí, atd. Zvýší-li se velikost dávky vzorků, zvýší se tím i počet vzorků, které lze testovat pomocí jedné soupravy a tím se sníží průměrné náklady na reagencie vztažené na jeden vzorek. Níže uvedená tabulka slouží jako vodítko pro počet vzorků, které lze testovat pomocí jedné soupravy. Velikost dávky vzorků Počet kontrolních reakcí + Počet amplikonů vzorků Počet reakcí vyžadovaný na jeden běh Celkový počet běhů dávek vzorků na soupravu Celkový počet vzorků testovaný na soupravu Sekvenování DNA Pro sekvenování DNA všech testovaných vzorků jsou k dispozici primery Universal Sequencing Primers (PN F a R). Pro sekvenování je třeba používat amplikony PCR vytvořené před digescí nukleázou SURVEYOR Nuclease. Návod k použití soupravy SURVEYOR Scan KRAS kit Exons 3 & 4 CE IVD pro systém DHPLC strana 7
9 6 Další požadované vybavení a reagencie 6 Další požadované vybavení a reagencie Další komponenty a vybavení požadované pro použití soupravy SURVEYOR Scan KRAS Kit Exons 3 & 4 CE IVD pro DHPLC zahrnují následující: Systém DHPLC, kolona, pufry, velikostní standard DNA - viz Příloha A.3.1 Specifikace systému DHPLC pro aplikace SURVEYOR Scan,kde naleznete popis vhodného systému DHPLC pro použití s touto soupravou Voda jakosti pro molekulární biologii 0,2 ml zkumavky pro PCR, pásy nebo 96jamková destička Mikropipety Pipetové špičky Ledová lázeň Míchadlo vortex Mikrocentrifuga Termocykler Agarózové gely a zařízení pro elektroforézu v agarózovém gelu 10% chlornan nebo podobný čisticí přípravek 7 Příprava reagencií Všechny reagencie dodávané v soupravě jsou připravené k použití. Některé komponenty je nutné před použitím rozmrazit, zamíchat na vortexu nebo odstředit v mikrocentrifuze; příslušné podrobnosti naleznete v níže uvedeném postupu testování. Sloučením reagencií se získají výchozí směsi a reakční směsi; úplné podrobnosti jsou uvedené v níže popsaném postupu testování. 8 Skladování a doba použitelnosti Souprava se skladuje až do použití při teplotě mezi 18 ºC a -25 C v mrazáku s konstantní teplotou. Poznamenejte si datum použitelnosti u každé dodané soupravy. Po vypršení data použitelnosti soupravu nepoužívejte. Směs s nukleázou SURVEYOR Nuclease připravená v kroku 7 Digesce nukleázou SURVEYOR Nuclease se musí použít okamžitě, neboť nukleáza SURVEYOR Nuclease W se v přítomnosti ostatních složek reakční směsi nukleázy SURVEYOR Nuclease během času deaktivuje. 9 Upozornění a preventivní opatření Žádná z reagencií v této soupravě není v dodaném množství nebezpečná pro lidské zdraví. Dokument společnosti Transgenomic pod číslem MSD lze stáhnout z Souprava neobsahuje žádné látky lidského nebo živočišného původu, které by mohly způsobit infekci. Tuto soupravu mohou používat pouze osoby, které jsou vyškolené v příslušných laboratorních metodách. Při práci s komponentami této soupravy vždy používejte laboratorní plášť, jednorázové rukavice a ochranu očí. Po použití soupravy zlikvidujte komponenty, jako je např. nemocniční odpad, v souladu s místními pravidly a předpisy. Alikvotní množství reagencií odpipetovaná ze zkumavek v soupravě jsou určená pouze pro jedno použití. Komponenty soupravy zůstávají stabilní i po 25 cyklech zmrazení-rozmrazení. Po překročení tohoto počtu cyklů zmrazení-rozmrazení soupravu nepoužívejte. Návod k použití soupravy SURVEYOR Scan KRAS kit Exons 3 & 4 CE IVD pro systém DHPLC strana 8
10 10 Získání primárního vzorku, manipulace a uchovávání 10 Získání primárního vzorku, manipulace a uchovávání Souprava SURVEYOR Scan KRAS Kit Exons 3 & 4 CE IVD je validována pro použití s DNA extrahovanou ze vzorků nádorů kolorektálního karcinomu zalitých v parafínu a fixovaných formalinem (FFPE). V zájmu optimální extrakce DNA je třeba tkáň hodin před zalitím v parafinu fixovat ve formalinu. Biopsie z nádorů jsou heterogenní směsi nádorových a nenádorových buněk. Nádor samotný je navíc heterogenní směsí národových buněk s mutacemi a nádorových buněk bez mutací. Vzhledem k tomu, že tyto somatické mutace nemusí být rozptýleny v nádoru rovnoměrně, mohou být výsledné analýzy mutací z různých částí stejného nádoru různé. Aby se zvýšila pravděpodobnost detekce mutace, je třeba izolovat DNA z nádorové části tkáně oddělením pouze nádorové části ze sklíčka pomocí nově sterilizovaného skalpelu pro každé nové sklíčko. V zájmu úspěšného použití této soupravy musí extrahovaná DNA splňovat kritéria v části Templát. POZNÁMKA:Extrahované vzorky DNA neurčené k okamžité analýze je třeba uchovávat zmražené při teplotě od -20 ºC do -80 ºC. 11 Postup testu 11.1 Detekce somatických mutací s použitím souprav SURVEYOR Scan - přehled Detekce mutace a potvrzení nukleázou SURVEYOR Nuclease zahrnuje tři kroky: Krok 1 - Připravte amplikony PCR z mutantní (testované) a normální (referenční) DNA, v návaznosti na konečný amplifikační cyklus PCR rozpusťte veškeré dvoušroubovice a poté pomalu ochlazujte, čímž dojde k optimalizované tvorbě heteroduplexů a homoduplexů (heteroduplexy se tvoří, když jeden řetězec se sekvencí Wild-Type se spáruje s jedním řetězcem mutantní sekvence). Návod k použití soupravy SURVEYOR Scan KRAS kit Exons 3 & 4 CE IVD pro systém DHPLC strana 9
11 11 Postup testu Krok 2 - Aplikujte na směs spárovaných heteroduplexů/homoduplexů nukleázu SURVEYOR Nuclease. SURVEYOR Nuclease rozštěpí oba dva řetězce heteroduplexní DNA za vzniku fragmentů DNA. DNA Control Wild-Type, vystavená obdobnému postupu, slouží jako kontrola na pozadí. Krok 3 - Proveďte analýzu fragmentů DNA v systému DHPLC. Tvorba nových produktů štěpení je v důsledku jednoho nebo více chybných párování indikována přítomností dodatečných chromatických píků. Migrační časy produktů štěpení indikují velikost fragmentů a tím i umístění chybného nebo více chybných párování. 12 Pokyny pro jednotlivé kroky 12.1 POČÁTEČNÍ nastavení/kalibrace systému DHPLC Při přípravě destičky SURVEYOR Nuclease pro analýzu v DHPLC se obraťte na Přílohu A.3 Požadavky pro denaturaci v systému HPLC (DHPLC) Před analýzou vzorků KRAS Před analýzou vzorků v systému DHPLC se musí provést běh s velikostním standardem DNA, aby se ověřila správná funkce systému. Před analýzou musí laboratorní pracovník používající přístroj zkontrolovat kvalitu rozlišení velikostního standardu DNA Templát 1. U izolované templátové FFPE DNA proveďte pomocí běžných laboratorních postupů kvalitativní a kvantitativní vyhodnocení extrahované DNA, aby bylo jisté, že je k dispozici dostatečné množství templátu pro PCR. 2. Poměr absorbance 260/280 musí být >1, Pro optimální nastavení PCR musí být pracovní koncentrace templátu přibližně 12,5 ng/µl. Je-li třeba, zřeďte templátovou DNA ve vodě o jakosti pro molekulární biologii. Návod k použití soupravy SURVEYOR Scan KRAS kit Exons 3 & 4 CE IVD pro systém DHPLC strana 10
12 12 Pokyny pro jednotlivé kroky 12.4 Pracovní schéma Souprava umožňuje analýzu 100 reakcí. Lze analyzovat i menší dávky vzorků, avšak s každou dávkou vzorků musí být zahrnuty kontroly ze soupravy i kontrola bez templátu. Souprava obsahuje dostatečný materiál pro kontrolu 100 reakcí všech kombinací používaných velikostí dávek vzorků. Zpracování vzorků musí být všeobecně prováděno od zahájení až do konce podle popisu v tomto návodu k použití. Musí-li být před dokončením celého postupu zpracování vzorku zastaveno, je nutné DNA uložit do -20 C, jak je ukázáno. Avšak zmrazené vzorky nemají být vystavovány opakovanému zmrazování a rozmrazování a zmrazená DNA amplifikovaná pomocí PCR ani produkty digesce nukleázou SURVEYOR Nuclease nemají být skladovány při teplotě od -18 do -25 C po delší dobu (>1 týden). Analýza vzorků se provádí podle níže znázorněného pracovního schématu: Oddělení tkáně 1 Izolace DNA a PCR 2 Gelová elektroforéza 3 Vyhodnocení robustní/slabá PCR 5 Neúspěšný SURVEYOR Scan SURVEYOR Scan Pozitivní 4 SURVEYOR Nuclease a analýza v DHPLC SURVEYOR Scan Negativní 7 6 Potvrzení sekvence NVD (varianta nedetekována) 8 Kvalita sekvence neúspěšná Kvalita sekvence prošla 9 Mutace v kodonech A59, Q61, K117 nebo A146 NVD Obrázek 3 Pracovní schéma analýzy pomocí soupravy SURVEYOR Scan KRAS Návod k použití soupravy SURVEYOR Scan KRAS kit Exons 3 & 4 CE IVD pro systém DHPLC strana 11
13 12 Pokyny pro jednotlivé kroky Poznámky k obrázku 3 1. DNA izolujte z FFPE (tkáň zalitá v parafínu a fixovaná formalinem) podle standardních laboratorních postupů. 2. Proveďte PCR a ověřte kvalitu DNA gelovou elektroforézou., 3. Vyhodnoťte a proveďte záznam, zda je proužek PCR Robustní ( 20 ng) nebo Slabý (<20 ng). Dojde-li k vytvoření více proužků PCR, připravte čerstvou genomickou DNA z FFPE. 4. U vzorků vyhodnocených po amplifikaci pomocí PCR buď jako Robustní PCR nebo Slabá PCR proveďte krok s nukleázou SURVEYOR Nuclease a analýzu v systému DHPLC. Se slabou PCR může být množství DNA k získání smysluplných výsledků systémem DHPLC nedostatečné, avšak může být dostatečné pro sekvenování. 5. Viz Příloha B Pokyny k řešení problémů, kde naleznete příklady neúspěšných výsledků ze SURVEYOR Scan. Všechny vzorky s neúspěšným výsledkem ze SURVEYOR Scan musí být znovu zpracovány jedním z následujících způsobů: a. opakování PCR, zbývá-li dostatečné množství genomické DNA b. nová extrakce DNA z FFPE; to by měla být až sekundární volba, neboť obvykle není žádoucí řezat další blok FFPE. c. použije-li se další řez nebo blok, musí být celý test znovu opakován, neboť vzhledem k heterogenní povaze nádoru může dojít k odchylkám při digesci. 6. Nejsou-li žádné viditelné píky v důsledku štěpení, zaznamenejte si negativní výsledek ze SURVEYOR Scan, tj. NVD = varianta nedetekována. 7. Ukazuje-li vzorek produkty štěpení enzymem SURVEYOR Nuclease (neshodující se s příslušnou kontrolou Wild-Type Control), je třeba je předat k ověření sekvenováním. 8. Je-li ověřovací analýza sekvence nevyhovující, poté zvolte jeden z následujících kroků: a. opakujte PCR, zbývá-li dostatečné množství genomické DNA b. proveďte novou extrakci DNA z FFPE; to by měla být až sekundární volba, neboť obvykle není žádoucí oddělovat další řezy z bloku FFPE. 9. Je-li ověřovací analýza sekvence vyhovující, potom výsledky znamenají jedno z následujícího: a. Sekvence Wild-Type, tzn. varianta nedetekována (NVD); nebo b. Varianta detekována. Ukazuje-li ověření sekvence jakoukoli změnu báze s výsledkem změny aminokyseliny: i. kodon 59 ii. kodon 61 iii. kodon 117; nebo iv. kodon 146 vyhodnoťte jako pozitivní mutaci v KRAS. Poznámka: je možné získat pozitivní výsledek ze SURVEYOR Scan, který bude sekvenováním zároveň potvrzen jako varianta nedetekována. Hladina detekce (LOD) pro SURVEYOR Nuclease v systému DHPLC je pro některé mutace 2% mutantů v 98% typu Wild-Type, zatímco hodnota LOD sekvenování je přibližně 10-25% mutantů v 90-75% typu Wild-Type. Pozn: Je-li vzorek 100% mutantní DNA, nebudou se tvořit žádné heteroduplexy a vzorek se bude jevit jako Wild-Type.Avšak vzorky z biopsie nádoru budou obsahovat buňky typu Wild-Type v důsledku heterogenity nádoru nebo kontaminace normální tkání; 5% typ Wild-Type lze touto soupravou detekovat křivkami identickými s 5% mutantní DNA. Poznámka: pozitivní výsledky se SURVEYOR Scan mohou být způsobeny jinými změnami bází, než jsou ty, které jsou považovány za KRAS aktivující. Tyto mutace jsou sice vzácné, avšak je nutné potvrzení další metodou, jako je např. sekvenování DNA, aby se určilo, zda pozitivní výsledek ze SURVEYOR Scan je či není KRAS aktivující mutací. Návod k použití soupravy SURVEYOR Scan KRAS kit Exons 3 & 4 CE IVD pro systém DHPLC strana 12
14 12 Pokyny pro jednotlivé kroky Pozn: proces fixace ve formalinu, požívaný při přípravě FFPE, může vést k deaminaci cytosinů. Během této deaminace se cytosin převádí na uracil. Polymeráza bude detekovat tento uracil jako thymin a začlení do kopírovaných řetězců adenin. To může být považováno za mutaci, při které se normální G nahrazuje za A s výsledkem mutace G/C na A/T, což je uměle vytvořená mutace, nikoli skutečná somatická mutace. Jedná se o vzácné případy, avšak dojde-li k brzkému kopírování při cyklování PCR, mohou být považovány za mutace. Při duplikované analýze se neopakují. Příkladem potenciální mutace vyvolané deaminací cytosinu, která by byla zvažována při rozhodování o léčbě pacienta, je KRAS A146T. - Kodon 146: GCA>ACA (A146T) Proto se doporučuje ověřit takové mutace duplikovanou analýzou stejné genomické DNA nebo podrobením všech vzorků duplikované analýze od začátku analýzy Amplifikační protokol 1. K dispozici je předmíchaný roztok dntp od Transgenomic (PN ) s celkovou pracovní koncentrací deoxynukleotidů 10 mm (2,5 mm na každý ze čtyř deoxynukleotidů). 2. KRAS Exon 3, Exon 4A a primery pro PCR Exon 4B Forward a Reverse (PN F/R, F/R a F/R) jsou dodány o koncentraci 10 µm. 3. Vyjměte 10 µm primery, 10mM dntp a pufr DNA Polymerase 10X PCR Buffer (kat. č ) z mrazáku a nechte rozmrazit na ledu. 4. Po rozmrazení důkladně promíchejte všechny složky soupravy na vortexu (~10 sekund), krátce odstřeďte (~10 sekund), aby na víčkách zkumavek nezůstala žádná kapalina, a umístěte do ledu. 5. Na ledu připravte výchozí směsi. 6. Podle následující tabulky jako vodítka připravte výchozí směs pro každou z reakcí KRAS Exon 3, KRAS Exon 4A a KRAS Exon 4B: Počet reakcí: 10 Výpočet objemu: Objem vody (µl) 330** DNA Polymerase 10X PCR Buffer (µl) 50 dntp (µl) 40 KRAS Primer Exon 3, 4A nebo 4B Forward (µl) 25 KRAS Primer Exon 3, 4A nebo 4B Reverse (µl) 25 DNA Polymerase (µl) 10 Celkový objem výchozí směsi 48,0 **Poznámka:Je třeba dosáhnout minimálního množství 25 ng DNA na 50 µl reakční směsi.je-li koncentrace extrahované DNA nižší než 12,5 ng/µl, zvyšte úměrně objem extrahované DNA, abyste zajistili množství 25 ng na reakční směs. Rovněž snižte odpovídajícím způsobem objem vody ve výchozích směsích, abyste získali 50 µl na reakční směs. Ve všech vzorcích připravených s použitím těchto výchozích směsí bude muset být extrahovaná DNA naředěna na přibližně stejnou nejnižší hladinu koncentrace.nedoporučuje se používat extrahovanou DNA o koncentraci <5 ng/µl. 7. Pro každou hlavní směs vypočítejte požadované objemy s použitím výše uvedené tabulky a dbejte na následující: (a) Pro hlavní směs 1, KRAS Exon 3, budou zapotřebí tři další reakce pro kontroly KRAS Control Wild-Type, KRAS Positive Control Exon 3 a kontrolu bez templátu KRAS Exon 3 (NTC1). (b) Pro hlavní směs 2, KRAS Exon 4A budou zapotřebí tři další reakce pro kontroly KRAS Control Wild-Type, KRAS Positive Control Exon 4A a kontrolu bez templátu KRAS Exon 4A (NTC2). Návod k použití soupravy SURVEYOR Scan KRAS kit Exons 3 & 4 CE IVD pro systém DHPLC strana 13
15 12 Pokyny pro jednotlivé kroky (c) Pro hlavní směs 3, KRAS Exon 4B budou zapotřebí tři další reakce pro kontroly KRAS Control Wild-Type, KRAS Positive Control Exon 4B a kontrolu bez templátu KRAS Exon 4B (NTC3). Poznámka: vezměte na vědomí, že bude zapotřebí mírně větší objem výchozí směsi, aby se tak kompenzovaly ztráty během pipetování. 8. Označte 0,2 ml zkumavky pro PCR nebo jamky na 96 jamkové destičce údajem příslušného vzorku. 9. Označte 2,0 ml centrifugační zkumavky pro přípravu hlavní směsi. 10. Přidejte do 2,0 ml centrifugačních zkumavek s označením Výchozí směs požadovaný objem vody o jakosti pro molekulární biologii. 11. Přidejte do zkumavek s výchozí směsí požadované množství pufru DNA Polymerase 10X PCR Buffer. 12. Přidejte do zkumavek s výchozí směsí požadovaný objem 10mM nukleotidů dntp. 13. Přidejte do příslušných zkumavek s výchozí směsí požadovaný objem primerů KRAS Forward. 14. Přidejte do příslušných zkumavek s výchozí směsí požadovaný objem primerů KRAS Reverse. 15. Vyjměte enzym DNA Polymerase (PN ) z mrazáku. 16. Odstřeďte enzym DNA Polymerase přibližně 10 sek. 17. Zamíchejte enzym DNA Polymerase na vortexu přibližně 10 sek. 18. Přidejte požadovaný objem polymerázy DNA Polymerase do zkumavek s výchozí směsí. 19. Zavřete zkumavky s výchozí směsí víčkem. 20. Před použitím zkumavky s výchozí směsí zamíchejte na vortexu přibližně 30 sek. a poté krátce odstřeďte přibližně 10 sek. 21. Až do použití uložte do ledu. 22. Odpipetujte 48,0 µl (viz poznámka v kroku 6 výše) výchozí směsi do příslušných jamek; používáte-li jednokanálovou pipetu, vyměňujte špičky pipety mezi jednotlivými jamkami. Používáte-li opakovací pipetu, nesmí mezi jamkami docházet k úniku nebo rozstřiku. Uložte destičku na led. 23. Do příslušných jamek přidejte 2,0 µl (viz poznámka výše v kroku 6) templátové DNA ze všech vzorků nebo vodu (kontrola bez templátu, NTC). Pro každý vzorek použijte novou pipetovou špičku; snažte se zabránit kontaminaci mezi vzorky v důsledku rozstřikování. Zakryjte jamky pásem s 8 kryty (používáte-li 96jamkovou destičku) nebo uzavřete 0,2ml zkumavky pro PCR. Zkontrolujte, že kryty jsou bezpečně utěsněny. 24. Až poté postupně otevřete kontroly s templátovou DNA ze soupravy (PN , , , ). Nakonec odpipetujte 2,0 µl z každé kontroly templátu, aby se zminimalizovala možnost kontaminace vzorků DNA. Znovu zakryjte každou jamku pásem s 8 kryty (používáte-li 96-jamkovou desku) nebo uzavřete 0,2 ml zkumavky pro PCR. Zkontrolujte, že kryty jsou bezpečně utěsněny. POZNÁMKA: Dobrou praxí je umístit kontroly bez templátu (NTC) do jamek, které nesousedí s kontrolou Positive Control ani se vzorky. POZNÁMKA:Návrh uspořádání 96jamkových destiček pro analýzu všech úseků KRAS a NRAS Exons 2-4 naleznete v Příloze A.1 Uspořádání destiček v soupravách SURVEYOR Scan. 25. Zamíchejte na vortexu 10 sek. (při přibližně poloviční rychlosti). 26. Odstřeďte 1-2 minuty, aby se všechny roztoky shromáždily na dně jamek a zkumavek. Přesvědčte se, že roztoky jsou na dně každé jamky a zkumavky. Pokud tomu tak není, odstřeďte znovu. Návod k použití soupravy SURVEYOR Scan KRAS kit Exons 3 & 4 CE IVD pro systém DHPLC strana 14
16 12 Pokyny pro jednotlivé kroky 12.6 Program termocykleru pro amplifikační protokol 1. Pro amplifikaci PCR a tvorbu heteroduplexů použijte následující protokol pro termocykler: 15 cyklů 30 cyklů Počáteční denaturace 95 C 5 minut Touchdown amplifikace 95 C 30 sekund 62 C, -0,5 ºC/cyklus 30 sekund 72 C 25 sekund Amplifikace 95 C 30 sekund 55 C 30 sekund 72 C 25 sekund Konečné prodloužení 1 cyklus 72 C 2 minuty Tvorba heteroduplexů 95 ºC 2 minuty 12 C Ponechat 12.7 Kontrola kvality produktů PCR 1. Před digescí nukleázou SURVEYOR Nuclease se doporučuje zkontrolovat kvalitu a množství amplikonů gelovou elektroforézou (nebo jí ekvivalentním způsobem). 2. Proveďte analýzu alikvotního podílu produktu PCR s různým množstvím hmotnostního žebříčku 100-bp DNA. 3. S použitím žebříčku proveďte odhad koncentrace amplifikované DNA. 4. Měl by být zřetelný pouze jediný proužek >20 ng/µl odpovídající hlavnímu produktu PCR. 5. Je-li přítomno více proužků, zkontrolujte, že byla dostačující kvalita vstupní templátové DNA (viz Příloha B Pokyny k řešení problémů). 6. Není-li přítomen žádný produkt, zkontrolujte, že byla dostačující kvalita vstupní templátové DNA (viz Příloha B Pokyny k řešení problémů). Splňuje-li kvalita požadované specifikace, zvyšte objem templátu na 4,0 µl/50 µl reakci (snižte množství vody na reakci na 31,0 µl). 7. V kontrolním vzorku bez templátu by neměly být viditelné žádné produkty PCR. Jsou-li v této kontrole produkty DNA zřetelné, je pravděpodobná kontaminace; viz Příloha B Pokyny k řešení problémů. 8. Vyhodnoťte, zda PCR je robustní nebo slabá. a. Robustní PCR se projevuje jedním proužkem > 20 ng/µl. b. Slabá PCR se projevuje jedním proužkem < 20 ng/µl. c. Pro obě vyhodnocení, robustní i slabou PCR, přejděte k digesci nukleázou SURVEYOR Nuclease. RADA: v této fázi mohou být produkty PCR skladovány při teplotě < -20 ºC až 1 týden Digesce nukleázou SURVEYOR Nuclease 1. Je-li PCR vzorku o dostatečné kvalitě a množství, proveďte digestivní reakci s nukleázou SURVEYOR Nuclease podle níže uvedeného popisu. 2. Rozmrazte na ledu zkumavky obsahující roztok 0.15 M MgCl 2 Solution a SURVEYOR Enhancer Cofactor. 3. Do nové 0,2 ml zkumavky pro PCR nebo do jamky v 96jamkové destičce přidejte 10,0 µl z každého vzorku amplifikovaného pomocí PCR. Návod k použití soupravy SURVEYOR Scan KRAS kit Exons 3 & 4 CE IVD pro systém DHPLC strana 15
17 12 Pokyny pro jednotlivé kroky 4. Připravte čerstvou směs z následujícího: 0.15 M MgCl 2 Solution, SURVEYOR Enhancer Cofactor, SURVEYOR Enhancer W2 a SURVEYOR Nuclease W (směs SURVEYOR Nuclease). Použijte následující tabulku jako vodítko pro přípravu výchozí směsi pro digesci nukleázou SURVEYOR Nuclease. Níže uvedený příklad představuje objem výchozí směsi pro 10 vzorků. Vezměte na vědomí, že bude zapotřebí mírně větší objem výchozí směsi než je tento výpočet, aby se tak kompenzovaly ztráty během pipetování. Počet digestivních reakcí s nukleázou SURVEYOR Nuclease: Výpočet objemu: 0.15 M MgCl 2 Solution (µl) 10,0 SURVEYOR Enhancer Cofactor (µl) 10,0 SURVEYOR Enhancer W2 (µl) 10,0 SURVEYOR Nuclease W (µl) 20,0 Celkový objem výchozí směsi: 50,0 Přidejte 5 µl výchozí směsi SURVEYOR Nuclease ke každému vzorku amplifikovanému pomocí PCR (µl) 10,0 Celkový objem digestivní reakce s nukleázou SURVEYOR Nuclease: 15,0 a. Před použitím každou reagencii odstřeďte. b. Před pipetováním každou reagencii mírně promíchejte na vortexu; po každém promíchání krátce odstřeďte asi 10 sekund. c. Pro každou digesci přidejte do 0,2 ml (nebo větší) mikrocentrifugační zkumavky pro PCR následující komponenty. 1,0 µl 0.15 M MgCl 2 Solution (PN ) 1,0 µl SURVEYOR Enhancer Cofactor (PN ) 1,0 µl SURVEYOR Enhancer W2 (PN ) 2,0 µl SURVEYOR Nuclease W (PN ) Nebo přidejte 5 µl výchozí směsi připravené podle výše uvedené tabulky. 5. Mírně zamíchejte výchozí směs pro digesci se SURVEYOR Nuclease na vortexu po dobu 10 sek. při nízké rychlosti. 6. Odstřeďte výchozí směs pro digesci se SURVEYOR Nuclease po dobu 10 sek. při nízké rychlosti. 7. Uložte výchozí směs pro digesci se SURVEYOR Nuclease do ledu, dokud ji nepoužijete. Poznámka: Výchozí směs pro digesci nukleázou SURVEYOR Nuclease připravená v kroku 7 musí být použita okamžitě, neboť u enzymu SURVEYOR Nuclease W dochází za přítomnosti ostatních složek této reakční směsi SURVEYOR Nuclease k jeho deaktivaci. 8. Odpipetujte 5,0 µl alikvotní podíly výchozí směsi pro digesci se SURVEYOR Nuclease do každé zkumavky nebo jamky obsahující 10,0 µl alikvotní podíl amplifikovaného produktu PCR (viz krok 3 výše). 9. Po dokončení pipetování odstřeďte 0,2 ml zkumavky PCR nebo 96jamkovou destičku po dobu 10 sek. 10. Mírně zamíchejte 0,2 ml zkumavky PCR nebo 96jamkovou destičku po dobu 10 sek. 11. Odstřeďte po dobu 10 sekund při nízké rychlosti (tento krok je velmi důležitý, je-li digesce prováděna v přístroji bez zahřívaného krytu). 12. Inkubujte při teplotě 42 C po dobu 30 min. 13. Do každé zkumavky nebo jamky přidejte 1,0 µl roztoku SURVEYOR Stop Solution (PN ) a mírně zamíchejte na vortexu (celkový reakční objem s nukleázou SURVEYOR Nuclease je 16,0 µl). 10 Návod k použití soupravy SURVEYOR Scan KRAS kit Exons 3 & 4 CE IVD pro systém DHPLC strana 16
18 12 Pokyny pro jednotlivé kroky RADA: Produkty digesce SURVEYOR lze uchovávat po dobu až jednoho týdne při teplotě -20 ºC. 14. Umístěte digestované vzorky do systému DHPLC. Poznámka: Navrhované nastavení gradientu v systému DHPLC pro analýzu produktů digesce enzymem SURVEYOR Nuclease naleznete na 13 Kontrolní postupy 13.1 Kontrola kvality soupravy SURVEYOR Scan KRAS Kit Exons 3 & 4 CE IVD Souprava obsahuje kontrolní plasmidovou DNA pro provádění kontroly kvality během specifických kroků testu. V Amplifikačním protokolu se pomocí těchto kontrol ověřuje, zda jsou výchozí směsi správně připraveny a zda amplifikace probíhá správně. Doporučuje se používat i kontroly bez templátu (s vodou místo templátové DNA), aby se tak mohla zjistit možná kontaminace složek souprav jakýmkoli cizorodým templátem DNA. Během kroku digesce nukleázou SURVEYOR Nuclease umožňují amplikony z kontrolní plasmidové DNA účinnou kontrolu, zda podmínky při štěpící reakci (příprava výchozí směsi pro digesci enzymem SURVEYOR Nuclease a podmínky inkubace) byly uspokojivé. Ve fázi analýzy poskytují chromatogramy digestovaných kontrolních amplikonů nukleázou SURVEYOR Nuclease v systému DHPLC vodítko, zda se píky odpovídající této mutaci v úseku Exons 3 a 4 budou eluovat i při nízké hladině (viz Obrázky 4-6). Píky produktů štěpení odpovídající jiným mutacím v úseku KRAS Exons 3 a 4 se mohou eluovat v mírně odlišných pozicích. Pokud amplikony PCR neodpovídají výsledkům uvedeným v části Kontrola kvality produktů PCR, obraťte se na Přílohu B -Pokyny pro řešení problémů nebo kontaktujte technickou podporu společnosti Transgenomic, než přejdete k dalším krokům analýzy vzorků Použití kontrolních plasmidových DNA Součástí soupravy jsou čtyři kontrolní DNA: KRAS Control Wild-Type; PN KRAS Positive Control Exon 3; PN KRAS Positive Control Exon 4A; PN KRAS Positive Control Exon 4B; PN Tyto kontrolní DNA jsou plasmidy s inzerty. Každá kontrola Positive Control obsahuje dva plasmidy: směs KRAS Control Wild-Type a mutační klon odlišující se od typu Wild-Type v jediném páru bází. Kontroly se dodávají v samostatných lahvičkách o koncentraci 10 5 kopií/µl. KRAS Exons 3 a 4 a primery Forward a Reverse PCR pro amplifikaci pomocí PCR se dodávají v soupravě samostatně. Při používání těchto kontrol dodržujte pokyny uvedené v částech Amplifikační protokol, Digesce nukleázou SURVEYOR Nuclease a Analýza KRAS Exons 3 a 4 pomocí nukleázy SURVEYOR Nuclease. PŘI PRVNÍM POUŽITÍ SOUPRAVY DŮRAZNĚ DOPORUČUJEME PROVÉST PŘED TESTOVÁNÍM GENOMICKÝCH VZORKŮ NEJPRVE EXPERIMENTY SE SAMOTNÝMI KONTROLAMI Návod k použití soupravy SURVEYOR Scan KRAS kit Exons 3 & 4 CE IVD pro systém DHPLC strana 17
19 14 Interpretace výsledků 14 Interpretace výsledků 14.1 Analýza exonů KRAS Exons 3 & 4 pomocí nukleázy SURVEYOR Nuclease Pro účely porovnání a kontroly VŽDY proveďte digesci enzymem SURVEYOR Nuclease u každé kontroly (typu Wild-Type a Positive Controls) a u kontroly bez templátu, u DNA vzorků a analyzujte je na stejné destičce pro vzorky v systému DHPLC. Během kroku digesce nukleázou SURVEYOR Nuclease umožňují amplikony z těchto kontrolních plasmidových DNA účinnou kontrolu, zda podmínky při štěpící reakci (příprava směsi SURVEYOR Nuclease a podmínky inkubace) byly uspokojivé. Ve fázi analýzy umožňují křivky digestovaných kontrolních amplikonů nukleázou SURVEYOR Nuclease v systému DHPLC vodítko, kde dojde k eluci fragmentů DNA vzniklých štěpením v místech specifických mutací v důsledku chybného párování, a to i při jejich nízké koncentraci (viz Obrázky 4-6). Pokud ani amplikony PCR ani fragmenty štěpení nukleázou SURVEYOR Nuclease odvozené z kontrolní DNA neodpovídají uvedeným výsledkům, obraťte se na Přílohu B - Pokyny pro řešení problémů nebo kontaktujte technickou podporu Transgenomic, než přejdete k dalším krokům analýzy vzorků. Níže uvedené ukázky jsou pouze pro účely ilustrace a NEJSOU určeny pro stanovení identity jakékoli konkrétní mutace. Potvrzení identity mutace je nutné, aby se jednoznačně stanovila přítomnost specifické záměny bází v Exons 3 a 4 genu KRAS. Enzym SURVEYOR Nuclease štěpí ve všech místech chybného párování vzniklých v důsledku tvorby heteroduplexů mezi typem Wild-Type a mutovanou DNA, nikoli pouze v mutacích v úseku Exons 3 a 4.Enzym SURVEYOR Nuclease umožňuje potvrzení přítomnosti chybného párování. Identita změny bází specifická pro danou mutaci se požaduje ke stanovení KRAS aktivujícího stavu a musí být ověřena jiným způsobem, např. sekvenováním Kontrola výsledků SURVEYOR Scan Prohlédněte chromatogramy a porovnejte náležející kontrolám Wild-Type a Positive Controls s chromatogramem vzorku. Určete, zda chromatogram vzorku je svým charakterem podobný nebo odlišný od kontroly Wild-Type. Je-li odlišný, potom vzorek je Pozitivní SURVEYOR Scan a bude předán k analýze DNA sekvenováním. Příklady ukazují Obrázky 4-6 a příklady takových vzorků ukazuje Příloha B Pokyny pro řešení problémů, 7 a 8. Každý vzorek s charakterem SURVEYOR Nuclease odlišným od Wild-Type by měl být předán k ověření sekvence, i když není identický s kontrolou Positive Control. Viz příklad takového vzorku v Příloze B Pokyny pro řešení problémů, 7. Je-li třeba, zvětšete zkoumanou oblast a překryjte chromatogram vzorku chromatogramem kontroly Wild-Type Control pro daný amplikon. Pozorujte rozdíly mezi kontrolou Wild-Type Control a analyzovaným vzorkem. Důležité! Po důkladném prozkoumání každého vzorku vyhodnocující ověří, zda sousedící vzorky v analytické destičce mají identické pozitivní výsledky SURVEYOR Scan. Vyskytují-li se identické pozitivní výsledky, mohou být důsledkem příčné kontaminace mezi vzorky nebo kontrolami a analýza se musí zopakovat. Návod k použití soupravy SURVEYOR Scan KRAS kit Exons 3 & 4 CE IVD pro systém DHPLC strana 18
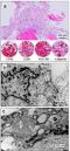
20 14 Interpretace výsledků 14.3 Příklady výsledků Ukázky výsledků získaných soupravou SURVEYOR Scan KRAS Kit Exons 3 & 4 CE IVD pro systém DHPLC jsou ukázány na Obrázcích 4-6 níže. Tyto ukázky byly získány systémem WAVE 4500 Systems s použitím UV a fluorescenčních detektorů a s přesným dodržením pokynů v části Pokyny pro jednotlivé kroky. Pokyny pro navrhované nastavení gradientu v systému DHPLC pro analýzu produktů digesce enzymem SURVEYOR Nuclease naleznete na Obrázek 4A Průtok systémem DHPLC KRAS Control Wild-Type KRAS Positive Control Exon 3 Uncleaved Vzorek 1, KRAS Exon bp Vzorek 2, KRAS Exon 3 amplicon Vzorek 3, KRAS Exon 3 Velikostní standard DNA Q61H tvoří fragmenty 65 a 135-bp Neštěpený amplikon 200-bp Promytí systému DHPLC Obrázek 4B Q61H tvoří fragmenty 65 a 135-bp KRAS Control Wild-Type KRAS Positive Control Exon 3 Uncleaved Vzorek 1, KRAS Exon bp Vzorek 2, KRAS Exon 3 amplicon Vzorek 3, KRAS Exon 3 Velikostní standard DNA Neštěpený amplikon 200-bp Obrázky 4A a 4B: Analýza v systému WAVE DHPLC s UV (Obrázek 4A) a fluorescenční (Obrázek 4B) detekcí produktů digesce enzymem SURVEYOR Nuclease kontroly KRAS Positive Control Exon 3 a kontroly KRAS Control Wild-Type a CRC DNA izolované z řezů FFPE. Při vizuálním prohlížení chromatogramů je třeba porovnávat vzorky po digesci s kontrolou Wild-Type Control (hnědá čára). Kontrola KRAS Positive Control Exon 3 (zelená čára) je směsí typu Wild-Type a mutantních plasmidů Q61H dávající digesční píky 65 a 135 bp; tato kontrola ukazuje, že krok digesce enzymem SURVEYOR Nuclease proběhl správně a ukazuje oblast chromatogramu, kterou je třeba vizuálně prozkoumat a určit, zda by měl být vzorek předán k analýze sekvence DNA. Z porovnání charakteru digesce u vzorků 1-3 s elektroferogramem typu Wild-Type bez digesce je zřejmé, že vzorek 2 (černá čára) obsahuje pravděpodobnou mutaci a měl by být sekvenován, aby se potvrdila přítomnost či absence mutace v příslušném kodonu. Vzorky 1 a 3 (modrá a červená čára) mají podobné chromatogramy jako kontrola Wild-Type Control a není třeba jej předávat k sekvenční analýze DNA. Konečným výsledkem je výsledek Návod k použití soupravy SURVEYOR Scan KRAS kit Exons 3 & 4 CE IVD pro systém DHPLC strana 19
21 14 Interpretace výsledků sekvenování, neboť se mohou vyskytovat i jiné nerelevantní mutace poskytující fragmenty o stejné velikosti. Obrázek 5A Průtok systémem DHPLC DHPLC KRAS Control Wild-Type Wash-off KRAS Positive Control Exon 4A Uncleaved Vzorek 1, KRAS Exon 4A 200-bp Vzorek 2, KRAS Exon 4A amplicon Velikostní standard DNA K117N tvoří fragmenty 80 a 88-bp Nerozštěpený amplikon 168-bp Obrázek 5B K117N tvoří fragmenty 80 a 88-bp DHPLC KRAS Control Wild-Type Wash-off KRAS Positive Control Exon 4A Uncleaved Vzorek 1, KRAS Exon 4A 200-bp Vzorek 2, KRAS Exon 4A amplicon Velikostní standard DNA Nerozštěpený amplikon 168-bp Obrázky 5A a 5B: Analýza v systému WAVE DHPLC s UV (Obrázek 5A) a fluorescenční (Obrázek 5B) detekcí produktů digesce enzymem SURVEYOR Nuclease kontroly KRAS Positive Control Exon 4A a kontroly KRAS Control Wild-Type a CRC DNA izolované z řezů FFPE. Při vizuálním prohlížení chromatogramů je třeba porovnávat vzorky po digesci s kontrolou Wild-Type Control (zelená čára). Kontrola KRAS Positive Control Exon 4A (modrá čára) je směsí typu Wild-Type a mutantních plasmidů K117N dávající digesční píky 80 a 88 bp; tato kontrola ukazuje, že krok digesce enzymem SURVEYOR Nuclease proběhl správně a ukazuje oblast chromatogramu, kterou je třeba vizuálně prozkoumat a určit, zda by měl být vzorek předán k analýze sekvence DNA. Z porovnání charakteru digesce u vzorků 1 a 2 s elektroferogramem typu Wild-Type bez digesce je zřejmé, že vzorek 1 (červená čára) obsahuje pravděpodobnou mutaci a měl by být sekvenován, aby se potvrdila přítomnost či absence mutace v příslušném kodonu. Vzorek 2 (černá čára) má podobný chromatogram jako kontrola Wild-Type Control a není třeba jej předávat k sekvenční analýze DNA. Konečným výsledkem je výsledek sekvenování, neboť se mohou vyskytovat i jiné nerelevantní mutace poskytující fragmenty o stejné velikosti. Návod k použití soupravy SURVEYOR Scan KRAS kit Exons 3 & 4 CE IVD pro systém DHPLC strana 20
22 14 Interpretace výsledků Obrázek 6A Průtok systémem DHPLC Neštěpený amplikon 194-bp DHPLC KRAS Wash-off Control Wild-Type KRAS Positive Control Exon 4B Uncleaved Vzorek 1, KRAS Exon 4B 200-bp Vzorek 2, KRAS Exon 4B amplicon Vzorek 3, KRAS Exon 4B Velikostní standard DNA A146T tvoří fragmenty 78 a 116-bp Promytí systému DHPLC Obrázek 6B A146T tvoří fragmenty 78 a 116-bp DHPLC KRAS Wash-off Control Wild-Type KRAS Postive Control Exon 4B Uncleaved Vzorek 1, KRAS Exon 4B 200-bp Vzorek 2, KRAS Exon 4B amplicon Vzorek 3, KRAS Exon 4B Velikostní standard DNA Neštěpený amplikon 194-bp Obrázky 6A a 6B: Analýza v systému WAVE DHPLC s UV (Obrázek 6A) a fluorescenční (Obrázek 6B) detekcí produktů digesce enzymem SURVEYOR Nuclease kontroly KRAS Positive Control Exon 4B a kontroly KRAS Control Wild-Type a CRC DNA izolované z řezů FFPE. Při vizuálním prohlížení chromatogramů je třeba porovnávat vzorky po digesci s kontrolou Wild-Type Control (hnědá čára). Kontrola KRAS Positive Control Exon 4B (tmavozelená čára) je směsí typu Wild-Type a mutantních plasmidů A146T dávající digesční píky 78 a 116 bp; tato kontrola ukazuje, že krok digesce enzymem SURVEYOR Nuclease proběhl správně a ukazuje oblast chromatogramu, kterou je třeba vizuálně prozkoumat a určit, zda by měl být vzorek předán k analýze sekvence DNA. Z porovnání charakteru digesce u vzorků 1-3 s elektroferogramem typu Wild-Type bez digesce je zřejmé, že vzorek 3 (červená čára) obsahuje pravděpodobnou mutaci a měl by být sekvenován, aby se potvrdila přítomnost či absence mutace v příslušném kodonu. Vzorky 2 a 3 (černá a světlezelená čára) mají podobné chromatogramy jako kontrola Wild-Type Control a není třeba jej předávat k sekvenční analýze DNA. Konečným výsledkem je výsledek sekvenování, neboť se mohou vyskytovat i jiné nerelevantní mutace poskytující fragmenty o stejné velikosti. Návod k použití soupravy SURVEYOR Scan KRAS kit Exons 3 & 4 CE IVD pro systém DHPLC strana 21
23 15 Co je třeba dodržovat 15 Co je třeba dodržovat 15.1 Detekční hladina mutací získaných soupravou SURVEYOR Scan Validace souprav SURVEYOR Scan pro platformu DHPLC pomocí plasmidových klonů všech indikovaných mutací ukázala, že píky pro SURVEYOR Nuclease lze detekovat ve směsi 2-5% mutantu na pozadí Wild-Type. Automatické zjišťování sekvenováním přímého a zpětného řetězce často selhává v detekci mutací o koncentraci ve směsi s DNA typu Wild-Type nižší než 10%. Společně s výsledky získanými nukleázou SURVEYOR Nuclease lze důvěryhodněji interpretovat elektroferogramy sekvenování obsahující 5-10% mutantů. Ukáže-li analýza vzorku pro SURVEYOR Scan pozitivní výsledek, avšak sekvenování DNA neukáže žádnou detekovatelnou mutaci v KRAS nebo NRAS, doporučujeme takový výsledek vyhodnotit a zaznamenat jako Žádná varianta nezjištěna. Viz více podrobností v části Pracovní schéma Potvrzení sekvence U všech pozitivních výsledků ze SURVEYOR Scan přejděte k ověření sekvence, aby se určila identita sekvence mutací v KRAS Exon 3 a 4. Nepostupujte ověřování sekvence s negativními výsledky ze SURVEYOR Scan. Takový vzorek lze vyhodnotit jako Wild-Type nebo varianta nezjištěna. Primery Universal Sequencing Primers dodávané v soupravě jsou určeny k použití při ověřování sekvence. Přímý primer je PN F (Universal Sequencing Primer 1) a zpětný primer je PN R (Universal Sequencing Primer 2) Omezení testu Kontaminující látky přenesené ze vzorků zalitých v parafínu a fixovaných formalinem mohou narušovat amplifikaci metodou PCR a digesci nukleázou SURVEYOR Nuclease. Postupy kontroly kvality uvedenými v části Kontrola kvality produktů PCR se zajistí, že extrahovaná DNA bude vhodná pro použití s touto soupravou. Tato souprava byla validována pro analýzu vzorků získaných z nádoru kolorektálního karcinomu zalitých v parafínu a fixovaných formalinem. Není validována pro diagnostické použití s jinými druhy karcinomů ani pro čerstvé nebo zmrazené vzorky získané biopsií. Řešení problémů s nestandardními výsledky a podrobnosti k faktorům, které ovlivňují tento test, naleznete v části Příloha B - Pokyny pro řešení problémů v následujícím textu. Během práce se soupravou je nutné věnovat pozornost zabránění přenosu a křížové kontaminaci. Extrémní citlivost metody testování vyžaduje v následujících bodech preventivní opatření: Manipulaci se vzorky je nutné provádět tak, aby mezi vzorky nemohlo dojít ke křížové kontaminaci Pracujte na pracovišti pro PCR nebo na jiném vhodném místě, které lze před přípravou amplifikačních reakcí PCR vystavit UV záření. K otevření vzorků po amplifikaci pomocí PCR určených ke kontrole kvality gelovou elektroforézou použijte oddělené pracoviště pro PCR. Příprava k digesci enzymem SURVEYOR Nuclease má být provedena v oddělené místnosti nebo na jiném pracovišti pro PCR, než kde byla provedena původní PCR. Návod k použití soupravy SURVEYOR Scan KRAS kit Exons 3 & 4 CE IVD pro systém DHPLC strana 22
24 15 Co je třeba dodržovat Během všech kroků testu se s plasmidovými kontrolami v soupravě musí manipulovat odděleně od testovaných vzorků. o o o Všechny roztoky a jamky pro kontrolu bez templátu a pro DNA vzorků musí být před otevřením zkumavek s kontrolní plasmidovou DNA uzavřeny. MANIPULACI S KONTROLAMI PROVÁDĚJTE JAKO POSLEDNÍ. Kontrolní plasmidovou DNA přidávejte do příslušných zkumavek pouze AŽ PO uzavření všech jamek s kontrolou bez templátu a se vzorky. Po uzavření zkumavek s kontrolní DNA otřete VŠECHNY zkumavky a víčka před přenesením na jiné pracoviště přípravkem destruujícím DNA (např. 10% chlornanem). Pipetování vzorků do 96jamkových destiček nesmí umožnit kontaminaci sousedících jamek vzorkem, ke které by mohlo dojít vystříknutím během míchání nebo opomenutím vyměnit špičku pipety. Návod k použití soupravy SURVEYOR Scan KRAS kit Exons 3 & 4 CE IVD pro systém DHPLC strana 23
25 Příloha A Příloha A A.1 Návrh uspořádání destičky pro soupravy SURVEYOR Scan Níže znázorněný návrh uspořádání destičky je určen pro analýzu SURVEYOR Scan všech sedmi exonů KRAS a NRAS Exons současně v deseti vzorcích. Legenda: Ex = Exon; WT = Wild-Type; Mut = mutace; NTC = kontrola bez templátu. A.2 Označení na kontrolní DNA Sekvence s označením jsou ukázány níže. Legenda: Úseky s nejčastější mutací jsou zvýrazněny růžově. Sekvenci ve velkém písmu tvoří kódující báze; malým písmem jsou nekódující báze. Kontroly obsahují genetické označení zvýrazněné žlutě; tuto odchylku od sekvence NRAS Wild-Type v úseku, kde se mutace neočekávají, lze využít k řešení problémů s kontaminací vzorků s použitím kontrol Positive Controls. Ukázku takové kontaminace ukazuje křivka SURVEYOR Scan v Příloze B - Pokyny pro řešení problémů, 8. Označení v exonu KRAS Exon 3 Velikost amplikonu: 200 bp. Při přípravě kontrolního plasmidu KRAS Exon 3 je genetické označení ACC změněno na TGG. Kodony 59 a 61 jsou zvýrazněny níže. GAATGGTGTCTCTTGGATATTCTCGACACAGCAGGTCAAGAG Označení v exonu KRAS Exon 4A Velikost amplikonu: 168 bp. Při přípravě kontrolního plasmidu KRAS Exon 4A je genetické označení AGA změněno na TCT. Kodon 117 je zvýrazněn níže. AATAAATGTGATTTGCCTTCTAGAACAGTTCTCAC Označení v exonu KRAS Exon 4B Velikost amplikonu: 194 bp. Při přípravě kontrolního plasmidu KRAS Exon 4B je genetické označení agt změněno na tca. Kodon 146 je zvýrazněn níže. TCAGCAAAGACAAGACAGgtatcaaac A.3 Požadavky pro denaturaci v systému HPLC (DHPLC) A.3.1 Specifikace systému DHPLC pro aplikace v rámci SURVEYOR Scan Následující specifikace představují minimální požadavky pro specifikace systému DHPLC k provádění testů s použitím soupravy SURVEYOR Scan KRAS a NRAS. Systém dávkování gradientového rozpouštědla do HPLC Funkce binárního gradientu; vysoký tlak nebo nízký tlak Návod k použití soupravy SURVEYOR Scan KRAS kit Exons 3 & 4 CE IVD pro systém DHPLC strana 24
26 Příloha A Ovládání rychlosti průtoku, minimální rozsah: 0,7 1,6 ml/min Přesnost rychlosti průtoku: ± 2% (H 2 O při 20 ºC) Odplyňovač rozpouštědla Automatický vzorkovač Ovládání teploty k chlazení destiček, nastavitelné: 4 až 14 ºC Objem vstřiku: 5 50 µl Separační kolona Určena k separaci fragmentů dsdna různých velikostí, fragmenty od 50 bp do 250 bp Inkubátor s velmi přesným nastavením teploty Teplotní rozsah: 40 až 70 ºC Přesnost teploty: ± 0.2 ºC Reprodukovatelnost teploty: ± 0.2 ºC Linearita v celém rozsahu teplot: ± 2.0 ºC Alternativa detekce 1 UV/VIS detektor Rozsah vlnových délek: nm UV zdroj: Deuteriová lampa Alternativa detekce 2 Fluorescenční detektor Rozsah vlnových délek: buzení: nm; emise: nm Fluorescenční zdroj: 150 W xenonová lampa Pumpa pro fluorescenční barvivo Fixní rychlost průtoku 0,1 ml/min 20%/+50% Nízkopulzní průtok A.3.2 Obsluha systému Při nastavení a obsluze systému DHPLC dodržujte doporučení výrobce pro analýzu fragmentů dsdna o velikosti od 50 bp to 250 bp s dosaženým rozlišením velikosti 10 bp nebo vyšším. Takový je rozsah velikostí fragmentů po digesci enzymem SURVEYOR Nuclease s použitím této soupravy. Pokyny pro navrhované nastavení gradientu v systému DHPLC pro analýzu produktů digesce enzymem SURVEYOR Nuclease naleznete na A.3.3 Údržba kolon v systému DHPLC Při údržbě kolon v DHPLC dodržujte doporučení výrobce. Poznámka: analýza reakcí se SURVEYOR Nuclease vyžaduje dodržování častějších a přísnějších protokolů ve srovnání s analýzou standardních vzorků PCR. Další podrobnosti naleznete v pokynech pro systém DHPLC Návod k použití soupravy SURVEYOR Scan KRAS kit Exons 3 & 4 CE IVD pro systém DHPLC strana 25
27 Příloha A A.4 Uspořádání laboratoře pro testy PCR V zájmu získání spolehlivých a nekontaminovaných výsledků PCR dodržujte při přípravě laboratoře pro PCR správnou laboratorní praxi. Při přípravě laboratorního uspořádání dbejte na prostorové oddělení činností během přípravy pro PCR od činností po amplifikaci. Je důležité oddělit (i) izolaci DNA; (ii) amplifikaci PCR; a (iii) činnosti následující po PCR, které zahrnují otevírání zkumavek obsahujících amplifikované vzorky při přípravě analýzy v gelu a při přípravě ostatních testů, jako je analýza produktů digesce enzymem SURVEYOR Nuclease a sekvenování DNA. Je rovněž důležité mít laboratorní potřeby a zařízení určené pro jednotlivé prostory a používat je pouze v těchto prostorech. Utírání ploch 10% (obj/obj) chlornanem, připravovaným jednou týdně, pomůže eliminovat fragmenty DNA 500 bp, jako jsou templáty pro PCR. Dále může být vhodné ošetřit plastové potřeby a roztoky expozicí krátkovlnnému UV záření s použitím UV síťovadla po dobu 7-10 minut. Poznámka: enzymy a DNA určená k amplifikaci nesmí být vystavovány UV záření. K minimalizaci kontaminace velmi pomůže nošení náležitého ochranného oděvu, častá výměna rukavic a utírání rukavic na rukou 10% (obj/obj) roztokem chlornanu před vstupem na pracoviště. Mělo by být dodrženo uspořádání alespoň o dvou místnostech znázorněné na schématu níže, které je určeno specificky pro PCR a pro analýzu s použitím enzymu SURVEYOR Nuclease. Návod k použití soupravy SURVEYOR Scan KRAS kit Exons 3 & 4 CE IVD pro systém DHPLC strana 26
28 Příloha A A.5 Odkazy na literaturu 1. Amgen News Release (2013) New analyses identify predictive biomarkers for Vectibix (panitumumab) in patients with metastatic colorectal cancer Peeters M et al (2013) Massively parallel tumor multigene sequencing to evaluate response to panitumumab in a randomized phase III study of metastatic colorectal cancer. Clin Cancer Res De Roock W et al (2010) Association of KRAS p.g13d mutation with outcome in patients with chemotherapy-refractory metastatic colorectal cancer treated with cetuximab. JAMA Peeters M et al (2013) Mutant KRAS codon 12 and 13 alleles in patients with metastatic colorectal cancer: assessment as prognostic and predictive biomarkers of response to panitumumab. J Clin Oncol Andre T et al (2013) Panitumumab combined with irinotecan for patients with KRAS wildtype metastatic colorectal cancer refractory to standard chemotherapy: a GERCOR efficacy, tolerance, and translational molecular study. Ann Oncol Loupakis F et al (2009) KRAS codon 61, 146 and BRAF mutations predict resistance to cetuximab plus irinotecan in KRAS codon 12 and 13 wild-type metastatic colorectal cancer. Br J Cancer De Roock W et al (2010) Effects of KRAS, BRAF, NRAS, and PIK3CA mutations on the efficacy of cetuximab plus chemotherapy in chemotherapy-refractory metastatic colorectal cancer: a retrospective consortium analysis. Lancet Oncol Qiu P et al (2004) Mutation detection using Surveyor nuclease. Biotechniques Kuang Y et al (2009) Noninvasive detection of EGFR T790M in gefitinib or erlotinib resistant non-small cell lung cancer.clin. Cancer Res Mitani N et al (2007) Surveyor nuclease-based detection of p53 gene mutations in haematological malignancy.ann. Clin. Biochem Engelman JA et al (2006) Allelic dilution obscures detection of a biologically significant resistance mutation in EGFR-amplified lung cancer.j. Clin. Invest Viz též odkazy na o nukleáze SURVEYOR Nuclease a jejím použití. Návod k použití soupravy SURVEYOR Scan KRAS kit Exons 3 & 4 CE IVD pro systém DHPLC strana 27
29 Příloha B Příloha B Pokyny pro řešení problémů Efektivní použití souprav SURVEYOR Scan pro systém DHPLC závisí na úspěšném provedení celé řady kroků. Jedním z nejdůležitějších kroků je amplifikace metodou PCR, která musí vést k tvorbě specifické DNA o jednotné velikosti a v dostatečném množství, aby byla po hybridizaci a štěpení detekovatelná. To závisí na kvalitě původního vzorku. Provádění testu s DNA, která nesplňuje kritéria kvality a množství, se nedoporučuje. Poznámka: Používáte-li enzym SURVEYOR Nuclease poprvé, prostudujte si Pokyny pro jednotlivé kroky a proveďte experimenty v části Použití kontrolních plasmidových DNA.Před kontaktováním technické podpory společnosti Transgenomic mějte výsledky získané pomocí kontrolní plasmidové DNA připravené u sebe. Tyto pokyny pro řešení problémů obsahují seznam problémů, se kterými se můžete setkat při používání souprav SURVEYOR Scan pro DHPLC a také návrhy jejich řešení. Podrobné informace k obsluze a údržbě přístroje naleznete v příručce pro systém DHPLC. Příručka obsahuje konkrétní pokyny pro kontrolu a udržování funkčnosti kolony a podrobnosti k řešení problémů. Problém 1 nízký výtěžek PCR nebo analýza na agarózovém gelu neukazuje žádný produkt PCR NÍZKÝ VÝTĚŽEK PCR Správný výtěžek PCR Nízký výtěžek PCR MOŽNÁ PŘÍČINA Špatná kvalita templátové DNA Velké množství RNA ve vzorku zvyšující odhadovanou koncentraci DNA Termocykler není zkalibrován Není dostatek templátu ŘEŠENÍ Opakujte purifikaci DNA; ověřte používanou purifikační metodu. Je-li DNA extrahovaná z FFPE příliš fragmentovaná, mohou být zapotřebí další bloky FFPE. Opakujte ošetření vzorku DNA RNázou a purifikaci DNA. Zkalibrujte termocykler. Zvyšte množství templátu. Proužek RNA Poznámka: Je třeba používat DNA vysoké kvality z FFPE. Podle měření absorbance při 260 nm musí mít DNA koncentraci 25 ng/µl, absorbanční poměr při 260/280 nm >1,8 a čistotu >90% DNA (tj. neobsahovat kontaminaci trna a rrna na základě pozorování agarózového gelu). Vzorky s DNA uchovávejte při teplotě od -20 C do -80 C. Analýza templátu DNA extrahované z tkání zalitých v parafínu vyžaduje některá preventivní opatření. Extrahovanou DNA lze ošetřit uracil DNA glykosylázou a tím zabránit amplifikaci fragmentů DNA obsahujících deaminovaná C residua. Často dochází k tomu, že vysoký podíl materiálu extrahovaného z tkání zalitých v parafinu a adsorbujícího při A 260 není během PCR správně amplifikován. Použití většího množství počáteční DNA často napomůže tvorbě správného produktu amplifikace. Další možností je vybrat nádorovou tkáň z FFPE s vyšším podílem nádorových buněk. Lze též použít mikrořez, avšak to je velmi časově náročný postup a nedoporučuje se pro běžnou laboratorní analýzu. Návod k použití soupravy SURVEYOR Scan KRAS kit Exons 3 & 4 CE IVD pro systém DHPLC strana 28
30 Příloha B Problém 2 analýza na agarózovém gelu ukazuje více produktů PCR VÍCE PRODUKTŮ PCR MOŽNÁ PŘÍČINA ŘEŠENÍ Správný výtěžek PCR Více proužků PCR Příliš nízká teplota párování Zkontrolujte kalibraci termocykleru. Poznámka: PCR musí poskytnout dostatečně vysoký výtěžek (> 20 ng/µl) JEDINÉHO amplifikovaného druhu správné velikosti. Pro PCR se musí používat enzym DNA Polymerase a pufr DNA Polymerase 10X PCR Buffer, které jsou součástí soupravy. Amplikony z kontrol musí být digestovány enzymem SURVEYOR Nuclease a analyzovány odděleně, aby se zamezilo jejich rušivému pozadí při vizuálním srovnávání profilů na elektroferogramech (viz Příklady výsledků, Obrázky 4-6). Před digescí zkontrolujte všechny produkty amplifikované DNA gelovou elektroforézou (nebo analýzou v systému DHPLC), abyste si ověřili přítomnost jednoho druhu o předpokládané velikosti. Problém 3 Po působení nukleázy SURVEYOR Nuclease na heteroduplexy a analýze nejsou pozorovány žádné produkty štěpení ŽÁDNÉ PRODUKTY ŠTĚPENÍ Pozice chybějících heteroduplexů Pík nerozštěpeného homoduplexu MOŽNÁ PŘÍČINA Příliš malý podíl chybně párovaných bází Neefektivní tvorba heteroduplexů Neaktivní nukleáza SURVEYOR Nuclease ŘEŠENÍ Ověřte test pomocí kontrol. Dodržujte správný postup při PCR a hybridizaci. Pro digesci nukleázou SURVEYOR Nuclease používejte čerstvě hybridizovanou DNA. Proveďte novou amplifikaci PCR s použitím (1) templátové DNA stejného množství; (2) zvýšeného množství počáteční DNA; nebo (3) izolujte čerstvou DNA ze stejného nebo jiného řezu FFPE. Pro ověření funkčnosti enzymu proveďte Positive Control. Používejte pouze čerstvě připravené výchozí směsi enzymu SURVEYOR Nuclease. Návod k použití soupravy SURVEYOR Scan KRAS kit Exons 3 & 4 CE IVD pro systém DHPLC strana 29
31 Příloha B Poznámka: SURVEYOR Nuclease převážně štěpí v místech s chybným párováním v heteroduplexech. Podíl heteroduplexu vůči homoduplexu v hybridizovaném vzorku určuje velikost signálu digesce nukleázou SURVEYOR Nuclease. Je-li ve vzorku genomické DNA přítomna mutace genu KRAS ve velmi nízké koncentraci, signál může být příliš nízký na to, aby vytvořil pozitivní výsledek. Důležité je zajistit zahrnutí kroku hybridizace do programu termocykleru (viz Amplifikační protokol), aby byla maximalizována účinnost tvorby heteroduplexu. Heteroduplexy se během standardních reakcí PCR tvoří velmi neefektivně. Poznámka: poměr signálu vůči šumu je všeobecně dosti vysoký pro detekci mutací přítomných v nízkém procentu celkového templátu DNA; je možné detekovat 1% až 2% mutantní DNA. Obrázky 4-6 ukazují produkty štěpení vzniklé s použitím homoduplexní a heteroduplexní kontrolní DNA KRAS Positive Control (obsažené v soupravě) a vzorků FFPE v systému WAVE DHPLC 4500 System. Lze zřetelně pozorovat produkty štěpení jako dva nové píky eluující o předpokládaných velikostech, které lze odhadnout v porovnání s velikostním markerem DNA. Pozor: komerčně dostupné pufry pro PCR mají výrazně rozdílný obsah a jejich složení často není dodavatelem definováno. Některé pufry NEJSOU kompatibilní s nukleázou SURVEYOR Nuclease vzhledem k ph nebo přítomnosti přísad, povrchově aktivních činidel a jiných přidaných složek.nepoužívejte žádnou jinou polymerázu ani 10X polymerázový pufr než ty, které jsou dodávané v soupravě. Problém 4 Silné pozadí po působení nukleázy SURVEYOR Nuclease SILNÉ POZADÍ MOŽNÁ PŘÍČINA ŘEŠENÍ Neoptimální hybridizace Proveďte následující: 1. Zkontrolujte, zda koncentrace DNA je v rozsahu >25 ng/µl. 2. Zopakujte vytvoření heteroduplexu a dbejte na dodržování doporučeného postupu; viz bod Příliš nízké množství DNA Ověřte výtěžek a kvalitu templátové DNA Průtok systémem DHPLC Vzorek s rušivou základní linií Promytí systému DHPLC Nespecifické produkty PCR SURVEYOR Enhancer W2 a/nebo SURVEYOR Enhancer Cofactor ztratili svojí aktivitu Ověřte výtěžek a kvalitu templátové DNA. Zkontrolujte datum vypršení použitelnosti soupravy. Poznámka: Nukleáza SURVEYOR Nuclease někdy štěpí dvouřetězcovou DNA v náhodně párovaných místech pouze v jednom řetězci. To způsobuje vznik pozadí po digesci. Tato činnost je potlačována zesilovačem SURVEYOR Enhancer W2 a jeho kofaktorem Cofactor, aniž by došlo k negativnímu ovlivnění reakce štěpení v místě chybného párování. SURVEYOR Enhancer W2 a SURVEYOR Enhancer Cofactor jsou obsaženy v soupravě a tyto je třeba vždy používat. Dochází-li k tomuto štěpení pouze na jednom řetězci, vytváří se tak v systému DHPLC menší píky. Porovnání kontrolní digesce homoduplexů s digescí vzorků umožní tyto píky identifikovat. Návod k použití soupravy SURVEYOR Scan KRAS kit Exons 3 & 4 CE IVD pro systém DHPLC strana 30
32 Příloha B Problém 5 Píky po digesci nukleázou SURVEYOR Nuclease u negativních kontrol PÍKY DIGESCE U NEGATIVNÍCH KONTROL MOŽNÁ PŘÍČINA ŘEŠENÍ Píky kontroly Wild-Type po digesci se slabým signálem Kontaminace obsahu soupravy amplikony genu KRAS nebo plasmidovými kontrolami. Zlikvidujte všechny komponenty soupravy a použijte novou soupravu. Průtok systémem DHPLC Pík nerozštěpeného homoduplexu Promytí systému DHPLC Obraťte se technickou podporu společnosti Transgenomic a poraďte se o možných příčinách a zdrojích kontaminace. Problém 6 Neúspěšné výsledky s nukleázou SURVEYOR Nuclease DIGESCE POZITIVNÍCH KONTROL NUKLEÁZOU SURVEYOR NUCLEASE SE NEZDAŘILA MOŽNÁ PŘÍČINA ŘEŠENÍ Nejasné píky po digesci Pík nerozštěpeného homoduplexu SURVEYOR Nuclease nebyla přidána Digesce nukleázou SURVEYOR Nuclease proběhla při nesprávné teplotě Proveďte digesci nového vzorku Proveďte digesci nového vzorku Návod k použití soupravy SURVEYOR Scan KRAS kit Exons 3 & 4 CE IVD pro systém DHPLC strana 31
33 Příloha B Problém 7 Neočekávané píky na křivce digesce nukleázou SURVEYOR Nuclease DIGESCE POZITIVNÍCH KONTROL NUKLEÁZOU SURVEYOR NUCLEASE SE NEZDAŘILA MOŽNÁ PŘÍČINA ŘEŠENÍ Pík nerozštěpeného homoduplexu Mutace v neobvyklém místě Ověřte mutaci sekvenováním vzorku Neočekávaný pík po digesci Průtok systémem DHPLC Očekávané píky po digesci Promytí systému DHPLC Návod k použití soupravy SURVEYOR Scan KRAS kit Exons 3 & 4 CE IVD pro systém DHPLC strana 32
34 Příloha B Problém 8 Kontaminace vzorků kontrolami Positive Controls Charakter digesce odpovídá přítomnosti označeného úseku smíšených Positive Control a heteroduplexů Wild- Type Vzorek 1 Vzorek 2 Vzorek 3 Oblast s kodony 12 a 13 Oblast s kontrolním označením Vzorek 1 NVD v kodonech 12 a 13 Označení detekováno MOŽNÁ PŘÍČINA Nesprávný způsob pipetování ŘEŠENÍ Při pipetování vzorků je třeba věnovat pozornost zabránění příčné kontaminaci. Zkontrolujte, zda úseky sekvence s kontrolním označením nejsou kontaminovány kontrolou Positive Control Vzorek 2 c.34g>t p.g12c, 30% Označení nedetekováno Vzorek 3 NVD v kodonech 12 a 13 Označení nedetekováno Návod k použití soupravy SURVEYOR Scan KRAS kit Exons 3 & 4 CE IVD pro systém DHPLC strana 33
Návod k použití soupravy SURVEYOR Scan NRAS Kit Exons 2, 3 & 4 CE IVD pro systémy DHPLC
 1 Výrobce Návod k použití soupravy SURVEYOR Scan NRAS Kit Exons 2, 3 & 4 CE IVD pro systémy DHPLC Tento návod k použití si důkladně přečtěte před použitím tohoto produktu. Uschovejte si tento návod k použití,
1 Výrobce Návod k použití soupravy SURVEYOR Scan NRAS Kit Exons 2, 3 & 4 CE IVD pro systémy DHPLC Tento návod k použití si důkladně přečtěte před použitím tohoto produktu. Uschovejte si tento návod k použití,
Návod k použití CRC RAScan Combination Kit
 Návod k použití CRC RAScan Combination Kit Souprava SURVEYOR Scan KRAS a NRAS Exons 2, 3 & 4 CE IVD se systémy Tento návod k použití si důkladně přečtěte před použitím tohoto produktu. Uschovejte si tento
Návod k použití CRC RAScan Combination Kit Souprava SURVEYOR Scan KRAS a NRAS Exons 2, 3 & 4 CE IVD se systémy Tento návod k použití si důkladně přečtěte před použitím tohoto produktu. Uschovejte si tento
Návod k Použití Soupravy SURVEYOR Scan KRAS Kit Exon 2 CE IVD pro Systémy DHPLC
 1 Výrobce Návod k Použití Soupravy SURVEYOR Scan KRAS Kit Exon 2 CE IVD pro Systémy DHPLC Tento návod k použití si důkladně přečtěte před použitím tohoto produktu. Uschovejte si tento návod k použití,
1 Výrobce Návod k Použití Soupravy SURVEYOR Scan KRAS Kit Exon 2 CE IVD pro Systémy DHPLC Tento návod k použití si důkladně přečtěte před použitím tohoto produktu. Uschovejte si tento návod k použití,
EGFR XL StripAssay. Kat. číslo 5-630. 20 testů 2-8 C
 EGFR XL StripAssay Kat. číslo 5-630 20 testů 2-8 C Popis stripu Pracovní postup 1. Izolace DNA Pro izolaci DNA použijte vhodný izolační kit. Doporučené kity jsou následující: Pro izolaci čerstvých nebo
EGFR XL StripAssay Kat. číslo 5-630 20 testů 2-8 C Popis stripu Pracovní postup 1. Izolace DNA Pro izolaci DNA použijte vhodný izolační kit. Doporučené kity jsou následující: Pro izolaci čerstvých nebo
NRAS StripAssay. Kat. číslo 5-610. 20 testů 2-8 C
 NRAS StripAssay Kat. číslo 5-610 20 testů 2-8 C Popis stripu: Pracovní postup 1. Izolace DNA Pro izolaci DNA musí být použita vhodná metoda vzhledem k typu tkáně vzorku. Pro doporučení vhodné metody kontaktujte
NRAS StripAssay Kat. číslo 5-610 20 testů 2-8 C Popis stripu: Pracovní postup 1. Izolace DNA Pro izolaci DNA musí být použita vhodná metoda vzhledem k typu tkáně vzorku. Pro doporučení vhodné metody kontaktujte
Braf V600E StripAssay
 Braf V600E StripAssay Kat. číslo 5-570 20 testů 2-8 C Popis stripu: Pracovní postup 1. Izolace DNA Pro izolaci čerstvých nebo mražených biopsií použijte soupravy Qiagen QIAmp DNA Mini nebo Micro. Pro izolaci
Braf V600E StripAssay Kat. číslo 5-570 20 testů 2-8 C Popis stripu: Pracovní postup 1. Izolace DNA Pro izolaci čerstvých nebo mražených biopsií použijte soupravy Qiagen QIAmp DNA Mini nebo Micro. Pro izolaci
α-globin StripAssay Kat. číslo 4-160 10 testů 2-8 C
 α-globin StripAssay Kat. číslo 4-160 10 testů 2-8 C Popis stripů: Pracovní postup Izolace DNA Doporučujeme použít následující kit pro izolaci DNA z plné krve nebo jiných typů vzorků: Spin Micro DNA Extraction
α-globin StripAssay Kat. číslo 4-160 10 testů 2-8 C Popis stripů: Pracovní postup Izolace DNA Doporučujeme použít následující kit pro izolaci DNA z plné krve nebo jiných typů vzorků: Spin Micro DNA Extraction
cdna synthesis kit First-Strand cdna Synthesis System Verze 1.2
 cdna synthesis kit First-Strand cdna Synthesis System Verze 1.2 Obsah soupravy a její skladování Tato souprava pro reverzní transkripci obsahuje reagencie potřebné k provedení reverzní transkripce (RT)
cdna synthesis kit First-Strand cdna Synthesis System Verze 1.2 Obsah soupravy a její skladování Tato souprava pro reverzní transkripci obsahuje reagencie potřebné k provedení reverzní transkripce (RT)
Braf 600/601 StripAssay
 Braf 600/601 StripAssay Kat. číslo 5-560 20 testů 2-8 C Popis stripu: Pracovní postup Kit umožňuje detekci 9 mutací v genu BRAF (kodón 600 a 601) Další informace najdete v OMIM Online Mendelian Inheritance
Braf 600/601 StripAssay Kat. číslo 5-560 20 testů 2-8 C Popis stripu: Pracovní postup Kit umožňuje detekci 9 mutací v genu BRAF (kodón 600 a 601) Další informace najdete v OMIM Online Mendelian Inheritance
Kras XL StripAssay. Kat. číslo 5-680. 20 testů 2-8 C
 Kras XL StripAssay Kat. číslo 5-680 20 testů 2-8 C Popis stripu: Pracovní postup 1. Izolace DNA Musí být použity vhodné metody extrakce DNA, v závislosti na typu vzorku, který má být vyšetřován. Doporučení
Kras XL StripAssay Kat. číslo 5-680 20 testů 2-8 C Popis stripu: Pracovní postup 1. Izolace DNA Musí být použity vhodné metody extrakce DNA, v závislosti na typu vzorku, který má být vyšetřován. Doporučení
Uživatelská příručka
 PGM Barcoding Set 1-8 Navrženo pro PGM ION-TORRENT KÓD PRODUKTU: 2001 (1-8) BALEN9: 32 testů Uživatelská příručka Rev02.2015 Str. 1 Rejstřík 1. POUŽITÍ VÝROBKU 3 2. OBSAH KITU 4 3. SKLADOVÁNÍ 4 4. STABILITA
PGM Barcoding Set 1-8 Navrženo pro PGM ION-TORRENT KÓD PRODUKTU: 2001 (1-8) BALEN9: 32 testů Uživatelská příručka Rev02.2015 Str. 1 Rejstřík 1. POUŽITÍ VÝROBKU 3 2. OBSAH KITU 4 3. SKLADOVÁNÍ 4 4. STABILITA
DIAGNOSTICKÝ KIT PRO DETEKCI MINIMÁLNÍ REZIDUÁLNÍ CHOROBY U KOLOREKTÁLNÍHO KARCINOMU
 Úvod IntellMed, s.r.o., Václavské náměstí 820/41, 110 00 Praha 1 DIAGNOSTICKÝ KIT PRO DETEKCI MINIMÁLNÍ REZIDUÁLNÍ CHOROBY U KOLOREKTÁLNÍHO KARCINOMU Jednou z nejvhodnějších metod pro detekci minimální
Úvod IntellMed, s.r.o., Václavské náměstí 820/41, 110 00 Praha 1 DIAGNOSTICKÝ KIT PRO DETEKCI MINIMÁLNÍ REZIDUÁLNÍ CHOROBY U KOLOREKTÁLNÍHO KARCINOMU Jednou z nejvhodnějších metod pro detekci minimální
MagPurix Forensic DNA Extraction Kit
 MagPurix Forensic DNA Extraction Kit Kat. č. ZP02010 Doba zpracování: 40-50 minut pro MagPurix 12S 40-60 minut pro MagPurix 24 Použití Souprava MagPurix Forensic DNA Extraction Kit je určena pro izolátor
MagPurix Forensic DNA Extraction Kit Kat. č. ZP02010 Doba zpracování: 40-50 minut pro MagPurix 12S 40-60 minut pro MagPurix 24 Použití Souprava MagPurix Forensic DNA Extraction Kit je určena pro izolátor
DIAGNOSTICKÝ KIT PRO DETEKCI MINIMÁLNÍ REZIDUÁLNÍ CHOROBY U KARCINOMU PANKREATU
 Úvod IntellMed, s.r.o., Václavské náměstí 820/41, 110 00 Praha 1 DIAGNOSTICKÝ KIT PRO DETEKCI MINIMÁLNÍ REZIDUÁLNÍ CHOROBY U KARCINOMU PANKREATU Jednou z nejvhodnějších metod pro detekci minimální reziduální
Úvod IntellMed, s.r.o., Václavské náměstí 820/41, 110 00 Praha 1 DIAGNOSTICKÝ KIT PRO DETEKCI MINIMÁLNÍ REZIDUÁLNÍ CHOROBY U KARCINOMU PANKREATU Jednou z nejvhodnějších metod pro detekci minimální reziduální
CVD-T StripAssay. Kat. číslo 4-360. 20 testů 2-8 C
 CVD-T StripAssay Kat. číslo 4-360 20 testů 2-8 C Popis stripu Pracovní postup Izolace DNA Použijte čerstvou nebo zmraženou krev s EDTA nebo citrátem, jako antikoagulans, vyhněte se krvi s obsahem heparinu.
CVD-T StripAssay Kat. číslo 4-360 20 testů 2-8 C Popis stripu Pracovní postup Izolace DNA Použijte čerstvou nebo zmraženou krev s EDTA nebo citrátem, jako antikoagulans, vyhněte se krvi s obsahem heparinu.
NÁVOD K POUŽITÍ PRO HER2 DNA QUANTIFICATION KIT
 IČ: 80 DIČ: CZ80 sales@intellmed.eu NÁVOD K POUŽITÍ PRO HER DNA QUANTIFICATION KIT IČ: 80 DIČ: CZ80 sales@intellmed.eu OBSAH Návod k použití pro HER DNA QUANTIFICATION KIT.... Úvod.... Označení.... Rozsah
IČ: 80 DIČ: CZ80 sales@intellmed.eu NÁVOD K POUŽITÍ PRO HER DNA QUANTIFICATION KIT IČ: 80 DIČ: CZ80 sales@intellmed.eu OBSAH Návod k použití pro HER DNA QUANTIFICATION KIT.... Úvod.... Označení.... Rozsah
DIAGNOSTICKÝ KIT PRO DETEKCI MINIMÁLNÍ REZIUDÁLNÍ CHOROBY MRD EGFR
 Úvod IntellMed, s.r.o., Václavské náměstí 820/41, 110 00 Praha 1 DIAGNOSTICKÝ KIT PRO DETEKCI MINIMÁLNÍ REZIUDÁLNÍ CHOROBY MRD EGFR Jednou z nejvhodnějších metod pro detekci minimální reziduální choroby
Úvod IntellMed, s.r.o., Václavské náměstí 820/41, 110 00 Praha 1 DIAGNOSTICKÝ KIT PRO DETEKCI MINIMÁLNÍ REZIUDÁLNÍ CHOROBY MRD EGFR Jednou z nejvhodnějších metod pro detekci minimální reziduální choroby
MagPurix Viral/Pathogen Nucleic Acids Extraction Kit B
 MagPurix Viral/Pathogen Nucleic Acids Extraction Kit B Kat. č. ZP02012 Doba zpracování: 45-60 minut pro MagPurix 12S 45-65 minut pro MagPurix 24 Použití Souprava MagPurix Viral/Pathogen Nucleic Acids Extraction
MagPurix Viral/Pathogen Nucleic Acids Extraction Kit B Kat. č. ZP02012 Doba zpracování: 45-60 minut pro MagPurix 12S 45-65 minut pro MagPurix 24 Použití Souprava MagPurix Viral/Pathogen Nucleic Acids Extraction
Jednotné pracovní postupy zkoušení krmiv
 Národní referenční laboratoř Strana KVANTITATIVNÍ STANOVENÍ GENETICKÝCH MODIFIKACÍ METODOU qpcr POMOCÍ ROTOR-GENE PROBE PCR KITU Účel a rozsah Postup slouží ke kvantitativnímu stanovení genetických modifikací
Národní referenční laboratoř Strana KVANTITATIVNÍ STANOVENÍ GENETICKÝCH MODIFIKACÍ METODOU qpcr POMOCÍ ROTOR-GENE PROBE PCR KITU Účel a rozsah Postup slouží ke kvantitativnímu stanovení genetických modifikací
Určeno pro obecné laboratorní užití. Není určeno pro použití v diagnostických postupech. POUZE PRO POUŽITÍ IN VITRO.
 Určeno pro obecné laboratorní užití. Není určeno pro použití v diagnostických postupech. POUZE PRO POUŽITÍ IN VITRO. PCR Nucleotide Mix Předem připravený roztok ultračistých PCR deoxynukleotidů (datp,
Určeno pro obecné laboratorní užití. Není určeno pro použití v diagnostických postupech. POUZE PRO POUŽITÍ IN VITRO. PCR Nucleotide Mix Předem připravený roztok ultračistých PCR deoxynukleotidů (datp,
MagPurix Viral Nucleic Acid Extraction Kit
 MagPurix Viral Nucleic Acid Extraction Kit Kat. č. ZP02003 Doba zpracování: 40-55 minut pro MagPurix 12S 40-60 minut pro MagPurix 24 Použití Souprava MagPurix Viral Nucleic Acid Extraction Kit je určena
MagPurix Viral Nucleic Acid Extraction Kit Kat. č. ZP02003 Doba zpracování: 40-55 minut pro MagPurix 12S 40-60 minut pro MagPurix 24 Použití Souprava MagPurix Viral Nucleic Acid Extraction Kit je určena
MagPurix Blood DNA Extraction Kit 200
 MagPurix Blood DNA Extraction Kit 200 Kat. č. ZP02001-48 Doba zpracování: 50-60 minut pro MagPurix 12S 50-70 minut pro MagPurix 24 Použití Souprava MagPurix Blood DNA Extraction Kit 200 je určena pro izolátor
MagPurix Blood DNA Extraction Kit 200 Kat. č. ZP02001-48 Doba zpracování: 50-60 minut pro MagPurix 12S 50-70 minut pro MagPurix 24 Použití Souprava MagPurix Blood DNA Extraction Kit 200 je určena pro izolátor
HR1 BRCA 1/2 NGS IVD KIT
 HR1 BRCA 1/2 NGS IVD KIT Navrženo pro PGM ION-TORRENT KÓD PRODUKTU: PRG-HR1-01 VELIKOST BALENÍ: 16 TEST Uživatelská příručka Rev03.2015 Str. 1 Obsah 1. ÚVOD 3 2. ÚČEL POUŽITÍ 3 3. OBSAH KITU 4 4. SKLADOVÁNÍ
HR1 BRCA 1/2 NGS IVD KIT Navrženo pro PGM ION-TORRENT KÓD PRODUKTU: PRG-HR1-01 VELIKOST BALENÍ: 16 TEST Uživatelská příručka Rev03.2015 Str. 1 Obsah 1. ÚVOD 3 2. ÚČEL POUŽITÍ 3 3. OBSAH KITU 4 4. SKLADOVÁNÍ
Návod k použití Informace o produktech jsou dostupné na internetových stránkách: www.demeditec.com
 Návod k použití Informace o produktech jsou dostupné na internetových stránkách: www.demeditec.com TPA IRMA Radioimunoanalýza pro kvantitativní stanovení cytokeratinu 8 a 18 v séru Prosím používejte pouze
Návod k použití Informace o produktech jsou dostupné na internetových stránkách: www.demeditec.com TPA IRMA Radioimunoanalýza pro kvantitativní stanovení cytokeratinu 8 a 18 v séru Prosím používejte pouze
Yi TPMT. Diagnostická souprava. Návod k použití. Haasova 27 Brno Česká republika. tel.:
 Yi TPMT Diagnostická souprava Návod k použití Výrobce: YBUX s.r.o. Haasova 27 Brno 616 00 Česká republika IČ 63487951 tel.: +420 541 423 710 e-mail: ybux@ybux.eu Název: Yi TPMT Popis: Diagnostická souprava
Yi TPMT Diagnostická souprava Návod k použití Výrobce: YBUX s.r.o. Haasova 27 Brno 616 00 Česká republika IČ 63487951 tel.: +420 541 423 710 e-mail: ybux@ybux.eu Název: Yi TPMT Popis: Diagnostická souprava
Konečná zpráva hodnocení různých způsobů přípravy vzorků pro AMPLICOR HPV test firmy Roche
 Konečná zpráva hodnocení různých způsobů přípravy vzorků pro AMPLICOR HPV test firmy Roche Charakteristika testu: Set AMPLICOR HPV vyráběný firmou Roche je určený pro detekci vysoko-rizikových typů lidských
Konečná zpráva hodnocení různých způsobů přípravy vzorků pro AMPLICOR HPV test firmy Roche Charakteristika testu: Set AMPLICOR HPV vyráběný firmou Roche je určený pro detekci vysoko-rizikových typů lidských
C V C. Návod k použití pro Biofortuna SSPGo TM HLA No Template Control Kit BF-40-02. Revize 2. Červenec 2014
 DOT130v1 Instructions for Use Biofortuna SSPGo TM HLA No Template Control Kit BF-40-02 Strana 1 / 7 Návod k použití pro Biofortuna SSPGo TM HLA No Template Control Kit BF-40-02 Revize 2 Červenec 2014 DOT130v1
DOT130v1 Instructions for Use Biofortuna SSPGo TM HLA No Template Control Kit BF-40-02 Strana 1 / 7 Návod k použití pro Biofortuna SSPGo TM HLA No Template Control Kit BF-40-02 Revize 2 Červenec 2014 DOT130v1
CHORUS COPROCOLLECT. Výrobce: DIESSE Diagnostica Senese Via delle Rose Monteriggioni (Siena) Itálie
 CHORUS COPROCOLLECT 86602 Výrobce: DIESSE Diagnostica Senese Via delle Rose 10 53035 Monteriggioni (Siena) Itálie OBSAH 1 Úvod... 3 2 Princip testu... 3 3 Složení soupravy... 3 4 Další potřebné vybavení
CHORUS COPROCOLLECT 86602 Výrobce: DIESSE Diagnostica Senese Via delle Rose 10 53035 Monteriggioni (Siena) Itálie OBSAH 1 Úvod... 3 2 Princip testu... 3 3 Složení soupravy... 3 4 Další potřebné vybavení
Sure-MeDIP I. with magnetic beads and MNase. www.krd.cz
 Sure-MeDIP I with magnetic beads and MNase www.krd.cz 1 Obsah soupravy a skladování MeDIP souprava obsahuje reagencie na provedení 25 reakcí. Souprava je rozdělen do dvou částí, jedna je distribuována
Sure-MeDIP I with magnetic beads and MNase www.krd.cz 1 Obsah soupravy a skladování MeDIP souprava obsahuje reagencie na provedení 25 reakcí. Souprava je rozdělen do dvou částí, jedna je distribuována
Jednotné pracovní postupy zkoušení krmiv STANOVENÍ OBSAHU DEKOCHINÁTU METODOU HPLC
 Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU DEKOCHINÁTU METODOU HPLC 1 Rozsah a účel Tato metoda specifikuje podmínky pro stanovení dekochinátu metodou vysokoúčinné kapalinové chromatografie
Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU DEKOCHINÁTU METODOU HPLC 1 Rozsah a účel Tato metoda specifikuje podmínky pro stanovení dekochinátu metodou vysokoúčinné kapalinové chromatografie
List protokolu QIAsymphony SP
 Únor 2017 List protokolu QIAsymphony SP circdna_2000_dsp_v1 a circdna_4000_dsp_v1 Tento dokument je Listem protokolu QIAsymphony circdna_2000_dsp_v1 a circdna_4000_dsp_v1, verze 1, R1 Sample to Insight
Únor 2017 List protokolu QIAsymphony SP circdna_2000_dsp_v1 a circdna_4000_dsp_v1 Tento dokument je Listem protokolu QIAsymphony circdna_2000_dsp_v1 a circdna_4000_dsp_v1, verze 1, R1 Sample to Insight
ÚLOHA C Klonování PCR produktu do plasmidu
 Jméno a učo: Datum: ÚLOHA C Klonování PCR produktu do plasmidu TEORETICKÝ ÚVOD Při klonování PCR produktů do plasmidů se využívá vlastnosti Taq polymerasy, a jiných non-proofreading polymeras, přidávat
Jméno a učo: Datum: ÚLOHA C Klonování PCR produktu do plasmidu TEORETICKÝ ÚVOD Při klonování PCR produktů do plasmidů se využívá vlastnosti Taq polymerasy, a jiných non-proofreading polymeras, přidávat
Polymorfismus délky restrikčních fragmentů (RFLP)
 ÚSTAV LÉKAŘSKÉ BIOCHEMIE A LABORATORNÍ DIAGNOSTIKY 1. LF UK Polymorfismus délky restrikčních fragmentů (RFLP) Praktické cvičení z lékařské biochemie Všeobecné lékařství Martin Vejražka 2017/18 Obsah POLYMORFISMUS
ÚSTAV LÉKAŘSKÉ BIOCHEMIE A LABORATORNÍ DIAGNOSTIKY 1. LF UK Polymorfismus délky restrikčních fragmentů (RFLP) Praktické cvičení z lékařské biochemie Všeobecné lékařství Martin Vejražka 2017/18 Obsah POLYMORFISMUS
List protokolu QIAsymphony SP
 List protokolu QIAsymphony SP Srpen 2015 Tissue_LC_200_V7_DSP a Tissue_HC_200_V7_DSP (uživatelem validovaný pro použití s minisadou QIAsymphony DSP DNA) Tento dokument Tissue_LC_200_V7_DSP a Tissue_HC_200_V7_DSP
List protokolu QIAsymphony SP Srpen 2015 Tissue_LC_200_V7_DSP a Tissue_HC_200_V7_DSP (uživatelem validovaný pro použití s minisadou QIAsymphony DSP DNA) Tento dokument Tissue_LC_200_V7_DSP a Tissue_HC_200_V7_DSP
Sure-MeDIP II. with agarose beads and Mse I. www.krd.cz
 Sure-MeDIP II with agarose beads and Mse I www.krd.cz 1 Obsah soupravy a skladování MeDIP souprava obsahuje reagencie na provedení 25 reakcí. Souprava je rozdělen do dvou částí, jedna je distribuována
Sure-MeDIP II with agarose beads and Mse I www.krd.cz 1 Obsah soupravy a skladování MeDIP souprava obsahuje reagencie na provedení 25 reakcí. Souprava je rozdělen do dvou částí, jedna je distribuována
Chromoprobe Multiprobe - T System
 Návod k použití REF: PMP 009/PMP 008/ PMP 007 Chromoprobe Multiprobe - T System Pouze pro profesionální použití Fluorescenční In Situ Hybridizace (FISH) je technika, která umožňuje detekci DNA sekvencí
Návod k použití REF: PMP 009/PMP 008/ PMP 007 Chromoprobe Multiprobe - T System Pouze pro profesionální použití Fluorescenční In Situ Hybridizace (FISH) je technika, která umožňuje detekci DNA sekvencí
MOLEKULÁRNÍ BIOLOGIE. 2. Polymerázová řetězová reakce (PCR)
 MOLEKULÁRNÍ BIOLOGIE 2. Polymerázová řetězová reakce (PCR) Náplň praktik 1. Izolace DNA z buněk bukální sliznice - izolační kit MACHEREY-NAGEL 2. PCR polymerázová řetězová reakce (templát gdna) 3. Restrikční
MOLEKULÁRNÍ BIOLOGIE 2. Polymerázová řetězová reakce (PCR) Náplň praktik 1. Izolace DNA z buněk bukální sliznice - izolační kit MACHEREY-NAGEL 2. PCR polymerázová řetězová reakce (templát gdna) 3. Restrikční
Column DNA Lego Kit UNIVERZÁLNÍ SOUPRAVY PRO RYCHLOU IZOLACI ČISTÉ DNA (Katalogové číslo D201 + D202)
 Column DNA Lego Kit UNIVERZÁLNÍ SOUPRAVY PRO RYCHLOU IZOLACI ČISTÉ DNA (Katalogové číslo D201 + D202) Popis Column DNA Lego Kit je základ moderní stavebnicové (Lego) soupravy pro izolaci čisté DNA různého
Column DNA Lego Kit UNIVERZÁLNÍ SOUPRAVY PRO RYCHLOU IZOLACI ČISTÉ DNA (Katalogové číslo D201 + D202) Popis Column DNA Lego Kit je základ moderní stavebnicové (Lego) soupravy pro izolaci čisté DNA různého
List protokolu QIAsymphony SP
 List protokolu QIAsymphony SP PC_AXpH_HC2_V1_DSP protokol Použití Pro diagnostické použití in vitro. Tento protokol byl vytvořen k použití s cervikálními vzorky uloženými v roztoku PreservCyt s využití
List protokolu QIAsymphony SP PC_AXpH_HC2_V1_DSP protokol Použití Pro diagnostické použití in vitro. Tento protokol byl vytvořen k použití s cervikálními vzorky uloženými v roztoku PreservCyt s využití
HbA1c. Axis - Shield. Společnost je zapsána v obchodním rejstříku Městského soudu v Praze, odd. C vložka 1299
 Lékařská technika a speciální zdravotní materiál Společnost je zapsána v obchodním rejstříku Městského soudu v Praze, odd. C vložka 1299 Obchodní 110, 251 70 Praha Čestlice Tel. +420 296 328 300 Fax. +420
Lékařská technika a speciální zdravotní materiál Společnost je zapsána v obchodním rejstříku Městského soudu v Praze, odd. C vložka 1299 Obchodní 110, 251 70 Praha Čestlice Tel. +420 296 328 300 Fax. +420
BlueWell Intrinsic Factor IgG ELISA Cat.. IF01-96
 BlueWell Intrinsic Factor IgG ELISA Cat.. IF01-96 96 D-tek s.a. rue René Descartes 19 BE-7000 Mons BELGIUM Tel. +32 65 84 18 88 Fax. +32 65 84 26 63 Email: info@d-tek.be Domovská stránka www.d-tek.be R.C.
BlueWell Intrinsic Factor IgG ELISA Cat.. IF01-96 96 D-tek s.a. rue René Descartes 19 BE-7000 Mons BELGIUM Tel. +32 65 84 18 88 Fax. +32 65 84 26 63 Email: info@d-tek.be Domovská stránka www.d-tek.be R.C.
DNA TECHNIKY IDENTIFIKACE ŽIVOČIŠNÝCH DRUHŮ V KRMIVU A POTRAVINÁCH. Michaela Nesvadbová
 DNA TECHNIKY IDENTIFIKACE ŽIVOČIŠNÝCH DRUHŮ V KRMIVU A POTRAVINÁCH Michaela Nesvadbová Význam identifikace živočišných druhů v krmivu a potravinách povinností každého výrobce je řádně a pravdivě označit
DNA TECHNIKY IDENTIFIKACE ŽIVOČIŠNÝCH DRUHŮ V KRMIVU A POTRAVINÁCH Michaela Nesvadbová Význam identifikace živočišných druhů v krmivu a potravinách povinností každého výrobce je řádně a pravdivě označit
CA15-3 IRMA Souprava CA15-3 IRMA umožňuje přímé in-vitro kvantitativní stanovení s tumorem asociovaného antigenu CA15-3 v lidském séru
 Informace o výrobku Informace o ostatních produktech jsou dostupné na www.demeditec.com Návod k použití CA15-3 IRMA Souprava CA15-3 IRMA umožňuje přímé in-vitro kvantitativní stanovení s tumorem asociovaného
Informace o výrobku Informace o ostatních produktech jsou dostupné na www.demeditec.com Návod k použití CA15-3 IRMA Souprava CA15-3 IRMA umožňuje přímé in-vitro kvantitativní stanovení s tumorem asociovaného
Cvičení ke kurzu Obecná ekotoxikologie. Úloha A - Stanovení ekotoxicity v testu klíčení rostlin
 Cvičení ke kurzu Obecná ekotoxikologie Nutné potřeby, které studenti přinesou s sebou do cvičení: - Tento návod - Poznámkový sešit, psací potřeby - Nůžky - Pravítko (s milimetrovým rozlišením) - Přezůvky
Cvičení ke kurzu Obecná ekotoxikologie Nutné potřeby, které studenti přinesou s sebou do cvičení: - Tento návod - Poznámkový sešit, psací potřeby - Nůžky - Pravítko (s milimetrovým rozlišením) - Přezůvky
HR1 BRCA 1/2 NGS IVD KIT
 HR1 BRCA 1/2 NGS IVD KIT Navrženo pro PGM ION-TORRENT KÓD PRODUKTU: PRG-HR1-01 VELIKOST BALENÍ: 16 TEST Uživatelská příručka Rev05.2015 Str. 1 Obsah 1. ÚVOD 3 2. ÚČEL POUŽITÍ 3 3. OBSAH KITU 4 4. SKLADOVÁNÍ
HR1 BRCA 1/2 NGS IVD KIT Navrženo pro PGM ION-TORRENT KÓD PRODUKTU: PRG-HR1-01 VELIKOST BALENÍ: 16 TEST Uživatelská příručka Rev05.2015 Str. 1 Obsah 1. ÚVOD 3 2. ÚČEL POUŽITÍ 3 3. OBSAH KITU 4 4. SKLADOVÁNÍ
Systém pro kvantitativní multiplex amplifikaci DNA PLEXAMP KIT. PXT5 Detekce genomové přestavby genu BRCA2 NÁVOD K POUŽITÍ
 Systém pro kvantitativní multiplex amplifikaci DNA PLEXAMP KIT PXT5 Detekce genomové přestavby genu BRCA2 NÁVOD K POUŽITÍ REFERENCE: PXT5-01.01.25: 25 testů PXT5-01.01.50: 50 testů PXT5-01.01.100: 100
Systém pro kvantitativní multiplex amplifikaci DNA PLEXAMP KIT PXT5 Detekce genomové přestavby genu BRCA2 NÁVOD K POUŽITÍ REFERENCE: PXT5-01.01.25: 25 testů PXT5-01.01.50: 50 testů PXT5-01.01.100: 100
Polymorfismus délky restrikčních fragmentů
 Polymorfismus délky restrikčních fragmentů Princip: Chemikálie: PCR produkt z předchozího praktického cvičení Endonukleáza KpnI 10 U μl -1 Pufr pro KpnI 10 koncentrovaný (Tris-HCl 100 mmol l -1 ph 7,5,
Polymorfismus délky restrikčních fragmentů Princip: Chemikálie: PCR produkt z předchozího praktického cvičení Endonukleáza KpnI 10 U μl -1 Pufr pro KpnI 10 koncentrovaný (Tris-HCl 100 mmol l -1 ph 7,5,
cobas KRAS Mutation Test KRAS
 cobas KRAS Mutation Test PRO ÚČELY DIAGNOSTIKY IN VITRO. cobas DNA Sample Preparation Kit DNA SP 24 Tests P/N: 05985536190 cobas KRAS Mutation Test KRAS 24 Tests P/N: 05852170190 POZNÁMKA: Díky koupi tohoto
cobas KRAS Mutation Test PRO ÚČELY DIAGNOSTIKY IN VITRO. cobas DNA Sample Preparation Kit DNA SP 24 Tests P/N: 05985536190 cobas KRAS Mutation Test KRAS 24 Tests P/N: 05852170190 POZNÁMKA: Díky koupi tohoto
POLYMERÁZOVÁ ŘETĚZOVÁ REAKCE (PCR)
 POLYMERÁZOVÁ ŘETĚZOVÁ REAKCE (PCR) Polymerázová řetězová reakce (PCR, z anglického Polymerase Chain Reaction) je metoda rychlého zmnožení (amplifikace) vybraného úseku DNA. Množený (amplifikovaný) úsek
POLYMERÁZOVÁ ŘETĚZOVÁ REAKCE (PCR) Polymerázová řetězová reakce (PCR, z anglického Polymerase Chain Reaction) je metoda rychlého zmnožení (amplifikace) vybraného úseku DNA. Množený (amplifikovaný) úsek
Validace sérologických testů výrobcem. Vidia spol. s r.o. Ing. František Konečný IV/2012
 Validace sérologických testů výrobcem Vidia spol. s r.o. Ing. František Konečný IV/2012 Legislativa Zákon č. 123/2000 Sb. o zdravotnických prostředcích ve znění pozdějších předpisů Nařízení vlády č. 453/2004
Validace sérologických testů výrobcem Vidia spol. s r.o. Ing. František Konečný IV/2012 Legislativa Zákon č. 123/2000 Sb. o zdravotnických prostředcích ve znění pozdějších předpisů Nařízení vlády č. 453/2004
DETEKCE A IDENTIFIKACE FYTOPATOGENNÍCH BAKTERIÍ METODOU PCR-RFLP
 DETEKCE A IDENTIFIKACE FYTOPATOGENNÍCH BAKTERIÍ METODOU PCR-RFLP Polymerázová řetězová reakce (PCR) je in vitro metoda pro enzymatickou syntézu definované sekvence DNA. Reakce využívá dvou oligonukleotidových
DETEKCE A IDENTIFIKACE FYTOPATOGENNÍCH BAKTERIÍ METODOU PCR-RFLP Polymerázová řetězová reakce (PCR) je in vitro metoda pro enzymatickou syntézu definované sekvence DNA. Reakce využívá dvou oligonukleotidových
NÁVOD K POUŽITÍ PRO KIT BRAF P.VAL600GLU
 NÁVOD K POUŽITÍ PRO KIT BRAF P.VAL600GLU IntellMed, s.r.o. Šlechtitelů 21 78371 Olomouc IČ: 27780317 DIČ: CZ27780317-18 C 1 2 OBSAH IntellMed, s.r.o., Šlechtitelů 21, 78371 Olomouc Návod k použití pro
NÁVOD K POUŽITÍ PRO KIT BRAF P.VAL600GLU IntellMed, s.r.o. Šlechtitelů 21 78371 Olomouc IČ: 27780317 DIČ: CZ27780317-18 C 1 2 OBSAH IntellMed, s.r.o., Šlechtitelů 21, 78371 Olomouc Návod k použití pro
Objednací číslo Určení Ig-třída Substrát Formát EI 2192-9601 M Chlamydia pneumoniae IgM Ag-potažené mikrotitrační jamky
 Protilátky proti Chlamydia pneumoniae (IgM) Návod na použití ELISA testu Objednací číslo Určení Ig-třída Substrát Formát EI 2192-9601 M Chlamydia pneumoniae IgM Ag-potažené mikrotitrační jamky 96 x 01
Protilátky proti Chlamydia pneumoniae (IgM) Návod na použití ELISA testu Objednací číslo Určení Ig-třída Substrát Formát EI 2192-9601 M Chlamydia pneumoniae IgM Ag-potažené mikrotitrační jamky 96 x 01
PSA ELISA test pro kvantitativní stanovení celkového prostatického specifického antigenu (PSA) v lidském séru
 PSA ELISA test pro kvantitativní stanovení celkového prostatického specifického antigenu (PSA) v lidském séru Obj. číslo: 52030 96 testů kompletní souprava Účel použití Prostatický specifický antigen (PSA)
PSA ELISA test pro kvantitativní stanovení celkového prostatického specifického antigenu (PSA) v lidském séru Obj. číslo: 52030 96 testů kompletní souprava Účel použití Prostatický specifický antigen (PSA)
CRP. Axis - Shield. SINGLE TESTS CRP kvantitativní stanovení pomocí přístroje NycoCard Reader II
 Lékařská technika a speciální zdravotní materiál Společnost je zapsána v obchodním rejstříku Městského soudu v Praze, odd. C vložka 1299 Obchodní 110, 251 70 Praha Čestlice Tel. +420 296 328 300 Fax. +420
Lékařská technika a speciální zdravotní materiál Společnost je zapsána v obchodním rejstříku Městského soudu v Praze, odd. C vložka 1299 Obchodní 110, 251 70 Praha Čestlice Tel. +420 296 328 300 Fax. +420
TESTOVÁNÍ GMO Praktikum fyziologie rostlin
 Teoretický úvod: TESTOVÁNÍ GMO Praktikum fyziologie rostlin 1 Teoretický úvod: TESTOVÁNÍ GMO Obecně na úvod Určitě jste už slyšeli pojem geneticky modifikovaný organismus (GMO). Úprava vlastností přirozeně
Teoretický úvod: TESTOVÁNÍ GMO Praktikum fyziologie rostlin 1 Teoretický úvod: TESTOVÁNÍ GMO Obecně na úvod Určitě jste už slyšeli pojem geneticky modifikovaný organismus (GMO). Úprava vlastností přirozeně
Rapid-VIDITEST. Rota-Adeno Card. (Jednokrokový kazetový test pro in vitro diagnostiku rotavirů a adenovirů) Návod k použití soupravy
 Rapid-VIDITEST Rota-Adeno Card (Jednokrokový kazetový test pro in vitro diagnostiku rotavirů a adenovirů) Návod k použití soupravy Výrobce: VIDIA spol. s r.o., Nad Safinou II č. 365, Vestec, 252 42 Jesenice
Rapid-VIDITEST Rota-Adeno Card (Jednokrokový kazetový test pro in vitro diagnostiku rotavirů a adenovirů) Návod k použití soupravy Výrobce: VIDIA spol. s r.o., Nad Safinou II č. 365, Vestec, 252 42 Jesenice
CYCLER CHECK. Test pro validaci teplotní uniformity cyklérů. Připraveno k použití, prealiquotováno. REF 7104 (10 testů) REF (4 testy)
 CZ Návod k použití CYCLER CHECK Test pro validaci teplotní uniformity cyklérů Připraveno k použití, prealiquotováno REF 7104 (10 testů) REF 71044 (4 testy) Obsah 1. Popis výrobku... 2 2. Materiál... 3
CZ Návod k použití CYCLER CHECK Test pro validaci teplotní uniformity cyklérů Připraveno k použití, prealiquotováno REF 7104 (10 testů) REF 71044 (4 testy) Obsah 1. Popis výrobku... 2 2. Materiál... 3
Jednotné pracovní postupy zkoušení krmiv STANOVENÍ OBSAHU MELAMINU A KYSELINY KYANUROVÉ METODOU LC-MS
 Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU MELAMINU A KYSELINY KYANUROVÉ METODOU LC-MS 1 Rozsah a účel Postup je určen pro stanovení obsahu melaminu a kyseliny kyanurové v krmivech. 2 Princip
Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU MELAMINU A KYSELINY KYANUROVÉ METODOU LC-MS 1 Rozsah a účel Postup je určen pro stanovení obsahu melaminu a kyseliny kyanurové v krmivech. 2 Princip
CEA ELISA test pro kvantitativní stanovení karcinoembryonického antigenu (CEA) v lidském séru
 CEA ELISA test pro kvantitativní stanovení karcinoembryonického antigenu (CEA) v lidském séru Obj. číslo: 52020 96 testů kompletní souprava Účel použití Karcinoembryonický antigen (CEA) je glykoprotein
CEA ELISA test pro kvantitativní stanovení karcinoembryonického antigenu (CEA) v lidském séru Obj. číslo: 52020 96 testů kompletní souprava Účel použití Karcinoembryonický antigen (CEA) je glykoprotein
 Pyroquant 1. LAL 1.1. PYROTELL : Gelová metoda (Metoda A a B, EP) Jednotlivé testy, lahvičky 12 x 75 mm (10 lahviček v balení) Citlivost 20003A PYROTELL : 0.2 ml LAL / lahv. 0.03 EU / ml 20006A PYROTELL
Pyroquant 1. LAL 1.1. PYROTELL : Gelová metoda (Metoda A a B, EP) Jednotlivé testy, lahvičky 12 x 75 mm (10 lahviček v balení) Citlivost 20003A PYROTELL : 0.2 ml LAL / lahv. 0.03 EU / ml 20006A PYROTELL
Tkáňový homogenizátor MagNA Lyser od společnosti Roche
 Izolace RNA Pracovní postup Homogenizace: Pozn. Postup homogenizace platí pouze pro izolaci RNA z nativní tkáně, v případě izolace z buněčné suspenze je tento krok vynechán a začíná se přídavkem homogenizačního
Izolace RNA Pracovní postup Homogenizace: Pozn. Postup homogenizace platí pouze pro izolaci RNA z nativní tkáně, v případě izolace z buněčné suspenze je tento krok vynechán a začíná se přídavkem homogenizačního
TheraScreen : souprava k detekci mutací K-RAS Pro detekci 7 typů mutací genu K-RAS
 TheraScreen : souprava k detekci mutací K-RAS Pro detekci 7 typů mutací genu K-RAS K použití se systémem Roche LightCycler 480 Real-Time PCR (Přístroj II) (katalogové číslo: 05015278001) a se systémem
TheraScreen : souprava k detekci mutací K-RAS Pro detekci 7 typů mutací genu K-RAS K použití se systémem Roche LightCycler 480 Real-Time PCR (Přístroj II) (katalogové číslo: 05015278001) a se systémem
Protilátky proti Helicobacter pylori (IgG) Návod na použití ELISA testu
 Protilátky proti Helicobacter pylori (IgG) Návod na použití ELISA testu Objednací číslo Určení Ig-třída Substrát Formát EI 2080-9601 G Helicobacter pylori IgG Ag-potažené mikrotitrační jamky 96 x 01 (96)
Protilátky proti Helicobacter pylori (IgG) Návod na použití ELISA testu Objednací číslo Určení Ig-třída Substrát Formát EI 2080-9601 G Helicobacter pylori IgG Ag-potažené mikrotitrační jamky 96 x 01 (96)
Optimalizace metody PCR pro její využití na vzorky KONTAMINOVANÝCH PITNÝCH VOD
 Optimalizace metody PCR pro její využití na vzorky KONTAMINOVANÝCH PITNÝCH VOD Dana Vejmelková, Milan Šída, Kateřina Jarošová, Jana Říhová Ambrožová VODÁRENSKÁ BIOLOGIE, 1. 2. 2017 ÚVOD Sledované parametry,
Optimalizace metody PCR pro její využití na vzorky KONTAMINOVANÝCH PITNÝCH VOD Dana Vejmelková, Milan Šída, Kateřina Jarošová, Jana Říhová Ambrožová VODÁRENSKÁ BIOLOGIE, 1. 2. 2017 ÚVOD Sledované parametry,
2) Připravte si 3 sady po šesti zkumavkách. Do všech zkumavek pipetujte 0.2 ml roztoku BAPNA o různé koncentraci podle tabulky.
 CVIČENÍ Z ENZYMOLOGIE 1) Stanovení Michaelisovy konstanty trypsinu pomocí chromogenního substrátu. Aktivita trypsinu se určí změřením rychlosti hydrolýzy chromogenního substrátu BAPNA (Nα-benzoyl-L-arginin-p-nitroanilid)
CVIČENÍ Z ENZYMOLOGIE 1) Stanovení Michaelisovy konstanty trypsinu pomocí chromogenního substrátu. Aktivita trypsinu se určí změřením rychlosti hydrolýzy chromogenního substrátu BAPNA (Nα-benzoyl-L-arginin-p-nitroanilid)
IMMUVIEW L. PNEUMOPHILA AND L. LONGBEACHE URINARY ANTIGEN TEST
 Dodává: GALI spol. s r.o., Ke Stadionu 179, Semily 513 01 tel. 481 689 050 fax. 481 689 051 info@gali.cz www.gali.cz IMMUVIEW L. PNEUMOPHILA AND L. LONGBEACHE URINARY ANTIGEN TEST 1 IMMUVIEW L. PNEUMOPHILA
Dodává: GALI spol. s r.o., Ke Stadionu 179, Semily 513 01 tel. 481 689 050 fax. 481 689 051 info@gali.cz www.gali.cz IMMUVIEW L. PNEUMOPHILA AND L. LONGBEACHE URINARY ANTIGEN TEST 1 IMMUVIEW L. PNEUMOPHILA
ProFlow Rotavirus-Adenovirus Combi
 KATALOGOVÉ ČÍSLO: PL.3010 (20 testů) ProFlow Rotavirus-Adenovirus Combi ZAMÝŠLENÉ POUŽITÍ ProFlow Rotavirus-Adenovirus je jednoduchý, rychlý imunologický test pro kvalitativní detekci antigenů Rotaviru
KATALOGOVÉ ČÍSLO: PL.3010 (20 testů) ProFlow Rotavirus-Adenovirus Combi ZAMÝŠLENÉ POUŽITÍ ProFlow Rotavirus-Adenovirus je jednoduchý, rychlý imunologický test pro kvalitativní detekci antigenů Rotaviru
IZOLACE DNA (KIT DNeasy Plant Mini)
 17.1 Izolace DNA (kit DNeasy Plant Mini) Strana 1 IZOLACE DNA (KIT DNeasy Plant Mini) 1 Účel a rozsah Postup slouží k získání deoxyribonukleové kyseliny (DNA) ze vzorku pomocí komerčního kitu DNeasy Plant
17.1 Izolace DNA (kit DNeasy Plant Mini) Strana 1 IZOLACE DNA (KIT DNeasy Plant Mini) 1 Účel a rozsah Postup slouží k získání deoxyribonukleové kyseliny (DNA) ze vzorku pomocí komerčního kitu DNeasy Plant
Rapid-VIDITEST RSV. (Jednokrokový kazetový test pro in vitro diagnostiku Respiračního syncytiálního viru z nosních výtěrů, výplachů a aspirátů)
 Rapid-VIDITEST RSV (Jednokrokový kazetový test pro in vitro diagnostiku Respiračního syncytiálního viru z nosních výtěrů, výplachů a aspirátů) Návod k použití soupravy Výrobce: VIDIA spol. s r.o., Nad
Rapid-VIDITEST RSV (Jednokrokový kazetový test pro in vitro diagnostiku Respiračního syncytiálního viru z nosních výtěrů, výplachů a aspirátů) Návod k použití soupravy Výrobce: VIDIA spol. s r.o., Nad
QMS Kvalita v mikrobiologii 14. vydání Datum vydání: červen 2018
 Příjem a uchování Při příjmu vzorků zaznamenejte datum dodání a skladujte vzorek při chladničkové teplotě 2-8 C až do provedení analýzy. Vzorky by měly být analyzovány dle termínů uvedených na webové stránce
Příjem a uchování Při příjmu vzorků zaznamenejte datum dodání a skladujte vzorek při chladničkové teplotě 2-8 C až do provedení analýzy. Vzorky by měly být analyzovány dle termínů uvedených na webové stránce
Polymerázová řetězová reakce. Základní technika molekulární diagnostiky.
 Polymerázová řetězová reakce Základní technika molekulární diagnostiky. Kdo za to může? Kary Mullis 1983 Nobelova cena 1993 Princip PCR Polymerázová řetězová reakce (polymerase chain reaction PCR) umožňuje
Polymerázová řetězová reakce Základní technika molekulární diagnostiky. Kdo za to může? Kary Mullis 1983 Nobelova cena 1993 Princip PCR Polymerázová řetězová reakce (polymerase chain reaction PCR) umožňuje
TECHNICKÁ SPECIFIKACE Vybavení genetické laboratoře pro projekt EXTEMIT-K část B
 TECHNICKÁ SPECIFIKACE Vybavení genetické laboratoře pro projekt EXTEMIT-K část B OBSAH Sestava pro vertikální elektroforézu... 2 Jednotka pro elektroforézu... 3 Termocykler... 4 Elektrický zdroj pro elektroforézu...
TECHNICKÁ SPECIFIKACE Vybavení genetické laboratoře pro projekt EXTEMIT-K část B OBSAH Sestava pro vertikální elektroforézu... 2 Jednotka pro elektroforézu... 3 Termocykler... 4 Elektrický zdroj pro elektroforézu...
MagPurix Bacterial DNA Extraction Kit
 MagPurix Bacterial DNA Extraction Kit Kat. č. ZP02006 Doba zpracování: 55-65 minut pro MagPurix 12S 55-75 minut pro MagPurix 24 Použití Souprava MagPurix Bacterial DNA Extraction Kit je určena pro izolátor
MagPurix Bacterial DNA Extraction Kit Kat. č. ZP02006 Doba zpracování: 55-65 minut pro MagPurix 12S 55-75 minut pro MagPurix 24 Použití Souprava MagPurix Bacterial DNA Extraction Kit je určena pro izolátor
Souprava je určená výhradně pro výzkumné účely, nikoliv pro diagnostické postupy.
 We take care of our customers Výrobky CARE jsou určené pro zásobování našich zákazníků na celém světě vysoce kvalitními spotřebními materiály, příslušenstvím a speciálními soupravami. Řada výrobků CARE
We take care of our customers Výrobky CARE jsou určené pro zásobování našich zákazníků na celém světě vysoce kvalitními spotřebními materiály, příslušenstvím a speciálními soupravami. Řada výrobků CARE
Polymerázová řetězová reakce
 Polymerázová řetězová reakce doc. RNDr. Milan Bartoš, Ph.D. bartosm@vfu.cz Přírodovědecká fakulta MU, 2013 Obsah přednášky 1) Co je to PCR, princip, jednotlivé kroky 2) Technické provedení PCR 3) Fyzikální
Polymerázová řetězová reakce doc. RNDr. Milan Bartoš, Ph.D. bartosm@vfu.cz Přírodovědecká fakulta MU, 2013 Obsah přednášky 1) Co je to PCR, princip, jednotlivé kroky 2) Technické provedení PCR 3) Fyzikální
Diagnostika infekce Chlamydia trachomatis pomocí molekulárně genetické metody real time PCR nejen u pacientek z gynekologických zařízení
 Diagnostika infekce Chlamydia trachomatis pomocí molekulárně genetické metody real time PCR nejen u pacientek z gynekologických zařízení Mgr. Klára Vilimovská Dědečková, Ph.D. Synlab genetics s.r.o. Molekulární
Diagnostika infekce Chlamydia trachomatis pomocí molekulárně genetické metody real time PCR nejen u pacientek z gynekologických zařízení Mgr. Klára Vilimovská Dědečková, Ph.D. Synlab genetics s.r.o. Molekulární
Rapid-VIDITEST FOB. (Jednokrokový blisterový test pro detekci hemoglobinu ve stolici) Návod k použití soupravy
 Rapid-VIDITEST FOB (Jednokrokový blisterový test pro detekci hemoglobinu ve stolici) Návod k použití soupravy Výrobce: VIDIA spol. s r.o., Nad Safinou II 365, Vestec, 252 42 Jesenice u Prahy, Tel: 261
Rapid-VIDITEST FOB (Jednokrokový blisterový test pro detekci hemoglobinu ve stolici) Návod k použití soupravy Výrobce: VIDIA spol. s r.o., Nad Safinou II 365, Vestec, 252 42 Jesenice u Prahy, Tel: 261
cobas 4800 BRAF V600 Mutation Test BRAF
 cobas 4800 BRAF V600 Mutation Test PRO ÚČELY DIAGNOSTIKY IN VITRO. cobas DNA Sample Preparation Kit DNA SP 24 Tests P/N: 05985536190 cobas 4800 BRAF V600 Mutation Test BRAF 24 Tests P/N: 05985595190 POZNÁMKA:
cobas 4800 BRAF V600 Mutation Test PRO ÚČELY DIAGNOSTIKY IN VITRO. cobas DNA Sample Preparation Kit DNA SP 24 Tests P/N: 05985536190 cobas 4800 BRAF V600 Mutation Test BRAF 24 Tests P/N: 05985595190 POZNÁMKA:
Filozofie validace. Je validace potřebná? Mezinárodní doporučení pro provádění validací ve forenzně genetických laboratořích
 INVESTICE DO ROZVOJE VZDĚLÁVÁNÍ Vzdělávání v oblasti forenzní genetiky reg. č. CZ.1.07/2.3.00/09.0080 Mezinárodní doporučení pro provádění validací ve forenzně genetických laboratořích INVESTICE DO ROZVOJE
INVESTICE DO ROZVOJE VZDĚLÁVÁNÍ Vzdělávání v oblasti forenzní genetiky reg. č. CZ.1.07/2.3.00/09.0080 Mezinárodní doporučení pro provádění validací ve forenzně genetických laboratořích INVESTICE DO ROZVOJE
NOVÁ VERZE. Systém pro kvantitativní multiplex amplifikaci DNA PLEXAMP KIT. PXT3 Detekce genomové přestavby genů MSH2 a MSH6 NÁVOD K POUŽITÍ
 NOVÁ VERZE Systém pro kvantitativní multiplex amplifikaci DNA PLEXAMP KIT PXT3 Detekce genomové přestavby genů MSH2 a MSH6 NÁVOD K POUŽITÍ REFERENCE: PXT3-02.01.25: 25 testů PXT3-02.01.50: 50 testů PXT3-02.01.100:
NOVÁ VERZE Systém pro kvantitativní multiplex amplifikaci DNA PLEXAMP KIT PXT3 Detekce genomové přestavby genů MSH2 a MSH6 NÁVOD K POUŽITÍ REFERENCE: PXT3-02.01.25: 25 testů PXT3-02.01.50: 50 testů PXT3-02.01.100:
Objednací číslo Určení Třída IgG Substrát Formát EI G Parainfluenza viry typu 1. Ag-potažené mikrotitrační jamky
 Protilátky proti virům parainfluenzy 1 (IgG) Návod na použití ELISA testu Objednací číslo Určení Třída IgG Substrát Formát EI 2721-9601 G Parainfluenza viry typu 1 IgG Ag-potažené mikrotitrační jamky 96
Protilátky proti virům parainfluenzy 1 (IgG) Návod na použití ELISA testu Objednací číslo Určení Třída IgG Substrát Formát EI 2721-9601 G Parainfluenza viry typu 1 IgG Ag-potažené mikrotitrační jamky 96
Verifikace sérologických testů v imunologických laboratořích ISO 15189 5.5 Postupy vyšetření
 Verifikace sérologických testů v imunologických laboratořích ISO 15189 5.5 Postupy vyšetření Andrea Vinciková Centrum imunologie a mikrobiologie Zdravotní ústav se sídlem v Ústí nad Labem Validace Ověřování,
Verifikace sérologických testů v imunologických laboratořích ISO 15189 5.5 Postupy vyšetření Andrea Vinciková Centrum imunologie a mikrobiologie Zdravotní ústav se sídlem v Ústí nad Labem Validace Ověřování,
Dodává: GALI spol. s r.o., Ke Stadionu 179, Semily tel fax
 Dodává: GALI spol. s r.o., Ke Stadionu 179, Semily 513 01 tel. 481 689 050 fax. 481 689 051 info@gali.cz www.gali.cz IMMUVIEW S. PNEUMONIAE AND L. PNEUMOPHILA URINARY ANTIGEN TEST Kombinovaný průtokový
Dodává: GALI spol. s r.o., Ke Stadionu 179, Semily 513 01 tel. 481 689 050 fax. 481 689 051 info@gali.cz www.gali.cz IMMUVIEW S. PNEUMONIAE AND L. PNEUMOPHILA URINARY ANTIGEN TEST Kombinovaný průtokový
METODY MOLEKULÁRNÍ PATOLOGIE. Mgr. Jana Slováčková, Ph.D. Ústav patologie FN Brno
 METODY MOLEKULÁRNÍ PATOLOGIE Mgr. Jana Slováčková, Ph.D. Ústav patologie FN Brno Molekulární patologie Využívá molekulární a genetický přístup k určení diagnózy a klasifikaci onemocnění Rutinně využívá
METODY MOLEKULÁRNÍ PATOLOGIE Mgr. Jana Slováčková, Ph.D. Ústav patologie FN Brno Molekulární patologie Využívá molekulární a genetický přístup k určení diagnózy a klasifikaci onemocnění Rutinně využívá
Rychlý test ze slin pro odhad hladiny alkoholu v krvi
 Rychlý test ze slin pro odhad hladiny alkoholu v krvi Charakteristika testu: DRY-veControl test je rychlá vysoce citlivá metoda pro semikvantitativní detekci alkoholu ve slinách, sloužící i pro odhad koncentrace
Rychlý test ze slin pro odhad hladiny alkoholu v krvi Charakteristika testu: DRY-veControl test je rychlá vysoce citlivá metoda pro semikvantitativní detekci alkoholu ve slinách, sloužící i pro odhad koncentrace
Rapid-VIDITEST Adenovirus Resp.
 Rapid-VIDITEST Adenovirus Resp. (Jednokrokový kazetový test pro in vitro diagnostiku Adenoviru z nosních výtěrů, výplachů a aspirátů) Návod k použití soupravy Výrobce: VIDIA spol. s r.o., Nad Safinou II
Rapid-VIDITEST Adenovirus Resp. (Jednokrokový kazetový test pro in vitro diagnostiku Adenoviru z nosních výtěrů, výplachů a aspirátů) Návod k použití soupravy Výrobce: VIDIA spol. s r.o., Nad Safinou II
SD Rapid test TnI/Myo Duo
 SD Rapid test TnI/Myo Duo Návod k použití soupravy Výrobce: STANDARD DIAGNOSTICS, INC. 156-68 Hagal-dong, Giheung-gu, Yongin-si, Kyonggido, Korea. Tel: +82 31 899 2800, fax: +82 31 899 2840, www.standardia.com
SD Rapid test TnI/Myo Duo Návod k použití soupravy Výrobce: STANDARD DIAGNOSTICS, INC. 156-68 Hagal-dong, Giheung-gu, Yongin-si, Kyonggido, Korea. Tel: +82 31 899 2800, fax: +82 31 899 2840, www.standardia.com
QUIDEL. Objednací kód: A003
 QUIDEL C1-Inhibitor Objednací kód: A003 Quidel BioVendor - Laboratorní medicína a.s. MCKellar Court 10165, 92121-4201 San Diego,CA, USA Karásek 1767/1, 621 00 Brno Tel: +1-858-552-1100 Fax: ++1-858-552-7995
QUIDEL C1-Inhibitor Objednací kód: A003 Quidel BioVendor - Laboratorní medicína a.s. MCKellar Court 10165, 92121-4201 San Diego,CA, USA Karásek 1767/1, 621 00 Brno Tel: +1-858-552-1100 Fax: ++1-858-552-7995
Rapid-VIDITEST Strep A. Jednokrokový kazetový test pro detekci antigenu Steptokoka A ve výtěru z krku. Návod k použití soupravy
 Rapid-VIDITEST Strep A Jednokrokový kazetový test pro detekci antigenu Steptokoka A ve výtěru z krku Návod k použití soupravy Výrobce: VIDIA spol. s r.o., Nad Safinou II 365, Vestec, 252 42 Jesenice u
Rapid-VIDITEST Strep A Jednokrokový kazetový test pro detekci antigenu Steptokoka A ve výtěru z krku Návod k použití soupravy Výrobce: VIDIA spol. s r.o., Nad Safinou II 365, Vestec, 252 42 Jesenice u
CHORUS CARDIOLIPIN-G
 CHORUS CARDIOLIPIN-G 86046 (36 testů) Výrobce: DIESSE Diagnostica Senese Via delle Rose 10 53035 Monteriggioni (Siena) Itálie OBSAH 1 Úvod... 3 2 Princip testu... 3 3 Složení soupravy... 3 4 Další potřebné
CHORUS CARDIOLIPIN-G 86046 (36 testů) Výrobce: DIESSE Diagnostica Senese Via delle Rose 10 53035 Monteriggioni (Siena) Itálie OBSAH 1 Úvod... 3 2 Princip testu... 3 3 Složení soupravy... 3 4 Další potřebné
Devyser AZF. Návod k použití
 Devyser AZF Kat.č. 8-A019 Pro in vitro diagnostiku Návod k použití Devyser AZF, Návod k použití, 7-A012-CZ, May-2012 Strana 1 z 20 Devyser AZF, Návod k použití, 7-A012-CZ, May-2012 Strana 2 z 20 Obsah
Devyser AZF Kat.č. 8-A019 Pro in vitro diagnostiku Návod k použití Devyser AZF, Návod k použití, 7-A012-CZ, May-2012 Strana 1 z 20 Devyser AZF, Návod k použití, 7-A012-CZ, May-2012 Strana 2 z 20 Obsah
Testovací kity Protrans HLA SBT 1 1.0 Strategie Protrans sekvenování 3 2.0 PROTRANS HLA Sekvenační systém 4 2.0 PROTRANS Sekvenačníí kity (S4, S3,
 Návod k použití Obsah Strana Testovací kity Protrans HLA SBT 1 1.0 Strategie Protrans sekvenování 3 2.0 PROTRANS HLA Sekvenační systém 4 2.0 PROTRANS Sekvenačníí kity (S4, S3, Domino Stones, S2, S1) 4
Návod k použití Obsah Strana Testovací kity Protrans HLA SBT 1 1.0 Strategie Protrans sekvenování 3 2.0 PROTRANS HLA Sekvenační systém 4 2.0 PROTRANS Sekvenačníí kity (S4, S3, Domino Stones, S2, S1) 4
IMUNOENZYMATICKÉ SOUPRAVY K DIAGNOSTICE CYTOMEGALOVIROVÉ INFEKCE
 INFEKČNÍ SÉROLOGIE Virologie IMUNOENZYMATICKÉ SOUPRAVY K DIAGNOSTICE CYTOMEGALOVIROVÉ INFEKCE Cytomegalovirus ELISA soupravy jsou určeny ke stanovení specifických protilátek třídy IgA, IgG a IgM v lidském
INFEKČNÍ SÉROLOGIE Virologie IMUNOENZYMATICKÉ SOUPRAVY K DIAGNOSTICE CYTOMEGALOVIROVÉ INFEKCE Cytomegalovirus ELISA soupravy jsou určeny ke stanovení specifických protilátek třídy IgA, IgG a IgM v lidském
Implementace laboratorní medicíny do systému vzdělávání na Univerzitě Palackého v Olomouci. reg. č.: CZ.1.07/2.2.00/
 Implementace laboratorní medicíny do systému vzdělávání na Univerzitě Palackého v Olomouci reg. č.: CZ.1.07/2.2.00/28.0088 Hybridizační metody v diagnostice Mgr. Gabriela Kořínková, Ph.D. Laboratoř molekulární
Implementace laboratorní medicíny do systému vzdělávání na Univerzitě Palackého v Olomouci reg. č.: CZ.1.07/2.2.00/28.0088 Hybridizační metody v diagnostice Mgr. Gabriela Kořínková, Ph.D. Laboratoř molekulární
PŘÍPRAVA REAGENCIÍ A STABILITA:
 REF 816A 10 lahviček z nichž každá obsahuje 0,5ml LAtrol Abnormální kontroly REF 816N 10 lahviček z nichž každá obsahuje 1,0ml LAtrol Normální kontroly UŽITÍ: LAtrol Abnormální kontrolní plazma (REF 816A)
REF 816A 10 lahviček z nichž každá obsahuje 0,5ml LAtrol Abnormální kontroly REF 816N 10 lahviček z nichž každá obsahuje 1,0ml LAtrol Normální kontroly UŽITÍ: LAtrol Abnormální kontrolní plazma (REF 816A)
Inovace studia molekulární a buněčné biologie reg. č. CZ.1.07/2.2.00/07.0354
 Inovace studia molekulární a buněčné biologie reg. č. CZ.1.07/2.2.00/07.0354 Genomika (KBB/GENOM) SNPs Odvozování a genotyping Ing. Hana Šimková, CSc. Cíl přednášky - seznámení s problematikou hledání
Inovace studia molekulární a buněčné biologie reg. č. CZ.1.07/2.2.00/07.0354 Genomika (KBB/GENOM) SNPs Odvozování a genotyping Ing. Hana Šimková, CSc. Cíl přednášky - seznámení s problematikou hledání
MOLEKULÁRNÍ BIOLOGIE I PŘÍPRAVA TKÁNĚ K IZOLACI DNA
 Cvičení 9,10,11: MOLEKULÁRNÍ BIOLOGIE Jméno: Skupina: Cíl: Seznámení se se základními metodami, využívanými k analýze DNA 1. izolace DNA 2. amplifikace DNA pomocí PCR a elektroforéza 3. vizualizace DNA
Cvičení 9,10,11: MOLEKULÁRNÍ BIOLOGIE Jméno: Skupina: Cíl: Seznámení se se základními metodami, využívanými k analýze DNA 1. izolace DNA 2. amplifikace DNA pomocí PCR a elektroforéza 3. vizualizace DNA
Rapid-VIDITEST Influenza A+B
 Rapid-VIDITEST Influenza A+B (Jednokrokový blisterový test pro in vitro diagnostiku viru Influenzy typu A a B z nosních výtěrů, výplachů a aspirátů) Návod k použití soupravy Výrobce: VIDIA spol. s r.o.,
Rapid-VIDITEST Influenza A+B (Jednokrokový blisterový test pro in vitro diagnostiku viru Influenzy typu A a B z nosních výtěrů, výplachů a aspirátů) Návod k použití soupravy Výrobce: VIDIA spol. s r.o.,
713000 Bezpečnostní list dle směrnice (ES) č. 453/2010 Datum vydání: 14 Květen 2015 Datum zpracování 14 Květen 2015 Verze: 1.0
 Datum vydání: 14 Květen 2015 Datum zpracování 14 Květen 2015 Verze: 1.0 ODDÍL 1: Identifikace látky/směsi a společnosti/podniku 1.1. Identifikátor výrobku Forma výrobku : Směsi Název přípravku : - RAScan
Datum vydání: 14 Květen 2015 Datum zpracování 14 Květen 2015 Verze: 1.0 ODDÍL 1: Identifikace látky/směsi a společnosti/podniku 1.1. Identifikátor výrobku Forma výrobku : Směsi Název přípravku : - RAScan
