FÁZOVÉ PŘECHODY. Fyzikální děj, při kterém se mění skupenství látky, se nazývá změna skupenství.
|
|
|
- Lenka Marková
- před 9 lety
- Počet zobrazení:
Transkript
1 SSPU OPAVA, Fyzika 3, školní rok FÁZOVÉ PŘECHODY Skupenství je stav tělesa z terodynaického hlediska. Skupenství rozeznáváe: 1. Pevné potenciální energie olekul je značně větší než jejich kinetická energie, proto se olekuly pohybují jen v blízkosti jednoho bodu, neohou se vzájeně vyěňovat. ají olekuly uspořádány v krystalické řížce pevná struktura, v níž se pravidelně opakuje geoetrické uspořádání atoů. zachovávají tvar a obje pevné skupenství vody je led 2. Kapalné potenciální energie olekul je trochu větší než jejich kinetická energie, proto se olekuly ohou pohybovat a vzájeně se po sobě sýkat, ale neohou se odpoutat neají stálý tvar, ale zachovávají stálý obje kapalné skupenství vody je voda kapalina 3. Plynné potenciální energie už je enší než kinetická energie, proto se olekuly pohybují volně prostore, dokud nenarazí na jinou olekulu neají stálý tvar ani obje plynné skupenství vody jsou vodní páry Fyzikální děj, při které se ění skupenství látky, se nazývá zěna skupenství. Tání Když zahříváe těleso z pevné látky, při dosažení teploty tání t t se přestane zvyšovat teplota a pevná látka se začne přeěňovat na kapalinu stejné teploty. Když pevná látka taje, přijíá teplo a zvětšuje se kinetická energie olekul. Částice zvětšují vzdálenosti od bodů, kole kterých kitají. Při dostatečné rychlosti olekul se narušuje vazba ezi částicei, krystalická řížka se bourá. Běhe tání látka přijíá teplo, které se nazývá skupenské teplo tání L t. Skupenské teplo tání vztažené na jeden kilogra je ěrné skupenské teplo tání l t L t l t = Měrné skupenské teplo tání je teplo (energie), která se usí dodat jednou kilograu pevné látky, aby se rozpustila v kapalinu téže teploty. [l t ] = J kg 1 Měrná skupenská tepla tání různých látek jsou v tabulkách na str. 152 Tuhnutí Když ochlazujee kapalinu, ění se při teplotě tuhnutí v pevnou látku téže teploty. Teplota tuhnutí je rovna teplotě tání. Při tuhnutí nevzniká pevné skupenství okažitě. Při dosažení teploty tuhnutí se začnou v kapalině vytvářet krystalizační jádra. K ni se připojují a pravidelně uspořádávají další částice látky. V tavenině tak vzniká při krystalizaci soustava volně se pohybujících krystalků nepravidelného tvaru. V okažiku, kdy všechna látka ztuhne, se krystalky vzájeně dotýkají a vytvářejí zrna. Z několika krystalizačních jader vznikne polykrystalická látka. Když je krystalické jádro jen jedno, připojují se postupně všechny částice látky a vznikne onokrystal. Vzniku onokrystalu se dosahuje tí, že do tuhnoucí taveniny se hned od
2 SSPU OPAVA, Fyzika 3, školní rok začátku ponoří alý onokrystal, aby jej částice obalovaly. Monokrystaly ají široké využití, protože z onokrystalů křeíku se vyrábějí polovodičové součástky od diod a tranzistorů do rádií až po procesory počítačů. Při tuhnutí kapalina předá okolí skupenské teplo tuhnutí, vztažené na jeden kilogra ěrné skupenské teplo tuhnutí, která jsou stejná jako skupenské teplo tání a ěrné skupenské teplo tání. Látky při tání nebo tuhnutí ění svůj obje. Většinou je obje pevné látky enší než obje kapaliny, protože olekuly uspořádané v krystalické řížce zabírají enší obje než neuspořádané. Takové látky tuhnou ode dna. Ale některé látky tvoří výjiku. Nejběžnější z nich je voda. Led á větší obje než voda, proto se drží u hladiny a pak uožňuje izolaci vody pod ní, takže nezarzne celý rybník a vodní organisy přečkají ziu. Led ale také způsobuje narušování skal, praskání zdí, potrubí apod. Když zvýšíe tlak na pevnou látku, zenší se teplota tání. To lze dokázat tí, že necháe drát projít ledový kvádre. Drát zatížíe závažíi, která pověsíe na oba jeho konce. Tí vyvoláe velký tlak. Led pod dráte roztaje, voda vniká nad drát, kde opět tuhne, protože už ta není takový tlak. Drát pronikne lede, aniž by ho rozdělil. Bruslení uožňuje tenká vrstva vody, která je na ledu pod bruslí. Ta však není způsobena jen zvýšený tlake, ale také tření. Subliace a desubliace Subliace je přeěna pevné látky přío ve skupenství plynné a desubliace je přeěna látky ve skupenství plynné na skupenství pevné. Za norálního tlaku kole 1000 hpa subliují např. jod, suchý led (pevný CO 2 ), ale i led nebo sníh. Subliují také pevné látky, které voní nebo páchnou (naftalen). Při subliaci se pevné látce usí dodat skupenské teplo subliace L s, vztažené na jeden kilogra ěrné skupenské teplo subliace l s. Desubliace je přeěna látky ze skupenství plynného na skupenství pevné. Příklade je například vznik krystalků jodu z jodových par. Vypařování, var a kapalnění Vypařování je přeěna kapaliny v páru. Vypařování probíhá na volné povrchu kapaliny za každé teploty. Rychlost, kterou se kapalina vypařuje, závisí na látce (líh se vypařuje rychleji než voda), na teplotě kapaliny (voda se vypaří rychleji v létě než pozdě na podzi, kdy je teplota kole nuly), na ploše volného povrchu (rychleji se vypaří litr vody, když ho rozlijee po zei než když ho necháe ve sklenici) a na nožství par nad volný povrche kapaliny (z tohoto důvodu se nevypaří všechna kapalina v uzavřené nádobě; po dosažení určitého nožství par se už látka dál nevypařuje vypařování lze zvýšit odsávání, foukání, větre). Při vypařování získávají olekuly na povrchu kapaliny kinetickou energii, která je větší než potenciální, takže překonají síly, které je poutají k ostatní olekulá a uniknou do volného prostoru na kapalinou a vytvoří páru. Pára patří do plynného skupenství látky, ale á jiné vlastnosti než plyn. Když je volný povrch kapaliny ve styku se vzduche, uniknou částice a rozptýlí se ve vzduchu. Některé olekuly se opět vracejí do kapaliny, proto se z uzavřené nádoby nevypaří všechna kapalina. Když kapalinu zahříváe, při dosažení určité teploty se pára začne tvořit po celé objeu kapaliny, a bubliny stoupají k volnéu povrchu. Tento děj se nazývá var. Teplota t v, při které kapalina začne vřít, je teplota varu. Teplota varu je závislá na vnější tlaku. S rostoucí tlake zvětšuje ( Papinův hrnec je ta vyšší tlak, proto voda vře až při asi 110 C; naopak při snížené tlaku vře voda při nohe nižší teplotě výroba sirupů, krystalového cukru)
3 SSPU OPAVA, Fyzika 3, školní rok Teplo, které usíe kapalině dodat, aby se přeěnila na páru stejné teploty a tlaku, se nazývá skupenské teplo varu L v, vztažené na jeden kilogra ěrné skupenské teplo varu l v ( tab. 152) L l = v v Při vypařování se usí olekulá, které se uvolňují z kapaliny, dodat kinetická energie skupenské teplo vypařování, ale při to látce nedodáváe žádné teplo zvnějšku. Při vypařování se snižuje teplota kapaliny toho se využívá pro konstrukci chladniček. Obrácený děj k vypařování a varu je kapalnění (kondenzace). Při toto ději se pára v důsledku zenšování svého objeu nebo snížení teploty přeění na kapalinu. Při kapalnění se uvolní skupenské teplo kondenzační, vztaženo na kilogra ěrné skupenské teplo kondenzační. Je stejně velké jako skupenské teplo varu a ěrné skupenské teplo varu. Sytá pára Když je kapalina v uzavřené nádobě, začne se vypařovat. Na začátku tohoto děje se vypaří víc olekul, než se do kapaliny vrátí, ale když se stav ustálí, bude z kapaliny unikat a do kapaliny se vracet stejné nožství olekul. Soustava kapaliny a par je v rovnovážné stavu. Sytá pára je pára, která je v rovnovážné stavu se svou kapalinou. U sytých par se vždy nachází kapalina. Dokud se všechna kapalina nevypaří, neůže být pára dál ohřívána. Tlak syté páry nezávisí při stálé teplotě na objeu páry. Tlak syté páry nad kapalinou s rostoucí teplotou roste. Fázový diagra To, v jaké skupenství se látka nachází, závisí na jeho stavu. Terodynaický stav popisují stavové veličiny tlak p a teplota T. Proto se skupenství zakresluje do diagrau, kde na ose x je teplota a na ose y tlak pt diagra, fázový diagra. Fázový diagra je rozdělen třei křivkai na tři plochy. Každá plocha znázorňuje jednotlivá skupenství pevné (I), kapalné (II), plynné (III). Na rozhraní ezi jednotlivýi plochai jsou křivky: Mezi I a II křivka tání k t při teplotě a tlaku, který jí odpovídá, je pevné a kapalné skupenství pohroadě. Tato křivka je závislostí teploty tání na vnější tlaku. Mezi II a III křivka sytých par k p při této teplotě a tlaku se vyskytují syté páry. Je závislost tlaku syté páry na teplotě. Mezi I a III subliační křivka k s každý bod této křivky znázorňuje stav látky, při které existuje vedle sebe v rovnovážné stavu pevná látka a její sytá pára.
4 SSPU OPAVA, Fyzika 3, školní rok Fázový diagra á dva význané body: Trojný bod T (A) protínají se v ně všechny tři křivky. Při této teplotě a tlaku se vyskytuje látka ve všech třech skupenstvích pohroadě vyskytují se pevná látka, kapalina i sytá pára pohroadě význaný teplotní bod trojný bod vody s absolutní nulou určuje teplotní stupnici T = 273,16 K = 0,01 C při tlaku asi 0,61 kpa. Kritický bod K končí jí křivka sytých par. Význaná je kritická teplota T K. Při vyšších teplotách se už nevyskytuje kapalina. Mezi kapalinou a plyne zizí rozhraní a látka se stane stejnorodou. Plocha I znázorňuje pevnou látku, plocha II kapalinu a plocha III přehřátou páru. Přehřátá pára se už nevyskytuje spolu s kapalinou. Má nižší tlak a hustotu než sytá pára téže teploty. Vzniknout ze syté páry ůže zvětšení objeu bez přítonosti kapaliny nebo zahřívání také bez přítonosti kapaliny. Plyn se vyskytuje při teplotách vyšších než je kritická teplota. Při nižších teplotách se vyskytuje jen sytá nebo přehřátá pára, které ají podstatně jiné vlastnosti než ideální plyn. Vodní pára v atosféře Ve spodní vrstvě atosféry se vyskytuje vodní pára, která se odpařuje z ploch oří, řek, jezer a z vody obsažené v půdě a organisech. Množství vodní páry v atosféře se ění podle atosférických podínek závisí na denní době, roční době, na ístě pozorování. Míru vodní páry ve vzduchu popisuje vlhkost vzduchu absolutní nožství vodní páry ve vzduchu Φ = V absolutní vlhkost vzduchu Φ je hotnost vodní páry obsažené ve vzduchu o objeu V. [Φ] = kg 3 Vodní pára ve vzduchu je obvykle pára přehřátá. Když se s poklese teploty stane sytou, dosáhne nejvyšší ožné vlhkosti vzduchu Φ při dané teplotě. Při další ochlazování začne pára kapalnět lha, srážky. relativní tvoření vodních srážek a vypařování vody nezávisí absolutní vlhkostí, ale na poěru k vlhkosti sytých par Φ ϕ = 100 % Φ p ϕ = 100 % ps p je tlak vodní páry, p s je tlak syté vodní páry za téže teploty při rel. vlhkosti 100 % se páry sráží a tvoří lhu. 0 % á suchý vzduch nejvhodnější vlhkost je % ěří se vlhkoěre vlasový odaštěný lidský vlas ění svou délku podle vlhkosti vzduchu Rosný bod t r je teplota, na kterou by bylo třeba ochladit vzduch, aby se vodní pára stala sytou vodní párou. Při další snížení teploty pára zkapalní vznik rosy, lhy, při teplotách pod 0 C jinovatky, sněhu.
5 SSPU OPAVA, Fyzika 3, školní rok JEVY NA ROZHRANÍ KAPLIN A VZDUCHU Kapaliny ají stálý obje, ale už ne tvar. Kapaliny tvoří přechod ezi úplně uspořádanýi pevnýi látkai a neuspořádanýi plyny. Uspořádání kapalin je krátkodosahové, podobné aorfní látká. Molekuly kapalin se po krátký časový úsek pohybují v kitech kole jedné rovnovážné polohy, ale ají takovou kinetickou energii, že z této rovnovážné polohy uniknou a zaujou jinou polohu. Zahřátí kapaliny se projeví zvýšení kinetické energie olekul a tí kratší intervale, ve které setrvávají kole jedné rovnovážné polohy. My to rozeznáe zvýšení tekutosti (např. ed za pokojové teploty teče ze lžičky veli poalu, při ohřátí asi jako sirup). Molekuly kapaliny na sebe vzájeně působí přitažlivýi silai. Tyto síly ají vliv na vlastnosti kapaliny. Volný povrch kapaliny se chová jako pružná blána (kapky na okně, kapka u kohoutku je to, jako by se nafukoval balónek). Je to způsobeno vzájený silový působení olekul. Kole každé olekuly je silové pole. V poloěru r je velikost tohoto silového působení ještě patrná. Když je celé kulové silové pole dané olekuly uvnitř kapaliny, je výslednice přitažlivých sil, kterýi ostatní olekuly v kapalině působí na danou olekulu, nulová. Ovše jiná situace nastane, když je vzdálenost olekuly od volné povrchu kapaliny enší než r. Molekuly plynu, které působí na danou olekulu už nevyvolají takovou přitažlivou sílu jako olekuly kapaliny, proto výslednice sil působí dovnitř kapaliny. Vrstva olekul, které ají vzdálenost od volného povrchu kapaliny vzdálenost enší než r, se nazývá povrchová vrstva kapaliny. Na každou olekulu ležící v povrchové vrstvě kapaliny působí sousední olekuly výslednou přitažlivou silou, která á sěr dovnitř kapaliny. Volný povrch je kolý na sěr této síly. Při posunutí olekuly z vnitřku kapaliny do povrchové vrstvy je nutno vykonat práci k překonání této síly. Molekuly povrchové vrstvy ají větší energii než ostatní olekuly. Celá povrchová vrstva á povrchovou energii jedna ze složek vnitřní energie kapaliny. Kapalina á snahu ít co nejenší energii, proto se snaží ít i nejenší energii povrchovou. Proto se snaží ít při dané objeu co nejenší povrch. Pokud bycho porovnali povrch těles o stejné objeu, zjistili bycho, že nejenší povrch vzhlede k objeu á koule. Proto se i kapalina snaží vytvořit kulovitý tvar. Takový tvar by ěla, kdyby na ni nepůsobily vůbec žádné síly. Na Zei ale působí tíha, proto kapaliny zaujíají kapkovitý tvar. Když chcee zvětšit velikost povrchu kapaliny o S, usíe dodat přírůstek povrchové energie E, kterou usíe dodat olekulá, které se staly olekulai povrchové vrstvy kapaliny. Veličina, která charakterizuje závislost povrchové energie kapaliny na její povrchu je povrchové napětí σ E σ = S [σ] = J 2 = N 1 Povrchové napětí závisí na kapalině, na látce nad volný povrche, na teplotě kapaliny. Když vytvoříe blánu z ýdlového roztoku v drátěné ráečku, jehož jedna strana je pohyblivá, posune blána saovolně pohyblivou stranu o x. Při to na stranu působí oba povrchy (horní i dolní) silou F. Vykoná se práce W = 2 F x a zároveň se plocha blány zenší o plochu S = 2 l x (opět se zenší horní i dolní povrchová vrstva), kde l je délka pohyblivé strany
6 SSPU OPAVA, Fyzika 3, školní rok E 2 F x σ = = S 2 l x = F l Jevy na rozhraní pevného tělesa a kapaliny Nalijee-li kapalinu do nádoby, u hladiny na sebe budou vzájeně působit olekuly stěny nádoby, olekuly plynu nad hladinou a olekuly kapaliny. Nádoba působí silou F 1, kapalina silou F 2 a plyn silou F 3, která je vzhlede k druhý dvěa silá zanedbatelná. Výslednice sil určuje sklon hladiny, která je kolá na povrchovou sílu. Mohou nastat dva případy: Síla sěřuje do nádoby kapalina sáčí stěnu nádoby, tzn. u stěny se vytvoří eniskus, alý zdvih hladiny např. voda. Kapalina vytváří dutý povrch. Síla sěřuje do kapaliny kapalina nesáčí stěnu nádoby např. rtuť, kapalina vytváří vypuklý povrch. Hladina svírá se stěnou nádoby stykový úhel ϑ. Pro 0 < ϑ < π/2 rad kapalina sáčí, pro π/2 < ϑ < π rad nesáčí. Voda á ϑ = 8, rtuť 128. Je-li ϑ = 0 rad, kapalina dokonale sáčí stěny, pro π/2 je povrch kapaliny nezakřivený, pro π kapalina dokonale nesáčí. Ponoříe-li trubici s veli alý vnitřní průěre (kapiláru r < 1 ) svisle do kapaliny, vytvoří se v ní u kapalin sáčejících dutý kulový vrchlík nad hladinou kapaliny kapilární elevace; u kapalin nesáčejících se vytvoří vypuklý kulový vrchlík níže než je hladina okolní kapaliny kapilární deprese. Při kapilární elevaci vystoupá kapalina do takové výšky, ve které bude povrchová a tíhová síla kapaliny v rovnováze. F = F G σ l = g σ 2 π r = V ρ g σ 2 π r = π r h ρ g 2 σ = r h ρ g 2 r h ρ g σ = 2 2 σ h = r ρ g l je obvod hladiny v kapiláře, V je obje kapaliny v kapiláře. Z těchto vzorců lze určit povrchové napětí kapaliny nebo určit, jak vysoko by kapalina vystoupala. Kapilární jevy ají velký praktický význa. Na kapilární elevaci je založena výživa rostlin voda s živinai vzlíná kene. Kapilární elevací vzlíná petrolej knote, ale také vlhnou stěny podáčených doů.
FYZIKA 2. ROČNÍK. Změny skupenství látek. Tání a tuhnutí. Pevná látka. soustava velkého počtu částic. Plyn
 Zěny skuenství látek Pevná látka Kaalina Plyn soustava velkého očtu částic Má-li soustava v rovnovážné stavu ve všech částech stejné fyzikální a cheické vlastnosti (stejnou hustotu, stejnou strukturu a
Zěny skuenství látek Pevná látka Kaalina Plyn soustava velkého očtu částic Má-li soustava v rovnovážné stavu ve všech částech stejné fyzikální a cheické vlastnosti (stejnou hustotu, stejnou strukturu a
Změna skupenství, Tání a tuhnutí, Sublimace a desublimace Vypařování a kapalnění Sytá pára, Fázový diagram, Vodní pára
 Zěny skupenství átek Zěna skupenství, Tání a tuhnutí, Subiace a desubiace Vypařování a kapanění Sytá pára, Fázový diagra, Vodní pára Zěna skupenství = fyzikání děj, při které se ění skupenství átky Skupenství
Zěny skupenství átek Zěna skupenství, Tání a tuhnutí, Subiace a desubiace Vypařování a kapanění Sytá pára, Fázový diagra, Vodní pára Zěna skupenství = fyzikání děj, při které se ění skupenství átky Skupenství
Termika. Nauka o teple se zabývá měřením teploty, tepla a tepelnými ději.
 Termika Nauka o teple se zabývá měřením teploty, tepla a tepelnými ději. 1. Vnitřní energie Brownův pohyb a difúze látek prokazují, že částice látek jsou v neustálém neuspořádaném pohybu. Proto mají kinetickou
Termika Nauka o teple se zabývá měřením teploty, tepla a tepelnými ději. 1. Vnitřní energie Brownův pohyb a difúze látek prokazují, že částice látek jsou v neustálém neuspořádaném pohybu. Proto mají kinetickou
Vlastnosti kapalin. Povrchová vrstva kapaliny
 Struktura a vlastnosti kapalin Vlastnosti kapalin, Povrchová vrstva kapaliny Jevy na rozhraní pevného tělesa a kapaliny Kapilární jevy, Teplotní objemová roztažnost Vlastnosti kapalin Kapalina - tvoří
Struktura a vlastnosti kapalin Vlastnosti kapalin, Povrchová vrstva kapaliny Jevy na rozhraní pevného tělesa a kapaliny Kapilární jevy, Teplotní objemová roztažnost Vlastnosti kapalin Kapalina - tvoří
ZMĚNY SKUPENSTVÍ LÁTEK
 ZMĚNY SKUPENSTVÍ LÁTEK TÁNÍ A TUHNUTÍ - OSNOVA Kapilární jevy příklad Skupenské přeměny látek Tání a tuhnutí Teorie s video experimentem Příklad KAPILÁRNÍ JEVY - OPAKOVÁNÍ KAPILÁRNÍ JEVY - PŘÍKLAD Jak
ZMĚNY SKUPENSTVÍ LÁTEK TÁNÍ A TUHNUTÍ - OSNOVA Kapilární jevy příklad Skupenské přeměny látek Tání a tuhnutí Teorie s video experimentem Příklad KAPILÁRNÍ JEVY - OPAKOVÁNÍ KAPILÁRNÍ JEVY - PŘÍKLAD Jak
KAPALINY. Mgr. Jan Ptáčník - GJVJ - Fyzika - Termika - 2. ročník
 KAPALINY Mgr. Jan Ptáčník - GJVJ - Fyzika - Termika - 2. ročník Kapaliny Krátkodosahové uspořádání molekul. Molekuly kmitají okolo rovnovážných poloh. Při zvýšení teploty se zmenšuje doba setrvání v rovnovážné
KAPALINY Mgr. Jan Ptáčník - GJVJ - Fyzika - Termika - 2. ročník Kapaliny Krátkodosahové uspořádání molekul. Molekuly kmitají okolo rovnovážných poloh. Při zvýšení teploty se zmenšuje doba setrvání v rovnovážné
LOGO. Struktura a vlastnosti kapalin
 Struktura a vlastnosti kapalin Povrchová vrstva kapaliny V přírodě velmi často pozorujeme, že se povrch kapaliny, např. vody, chová jako pružná blána, která unese např. hmyz Vysvětlení: Molekuly kapaliny
Struktura a vlastnosti kapalin Povrchová vrstva kapaliny V přírodě velmi často pozorujeme, že se povrch kapaliny, např. vody, chová jako pružná blána, která unese např. hmyz Vysvětlení: Molekuly kapaliny
STRUKTURA A VLASTNOSTI KAPALIN
 STRUKTURA A VLASTNOSTI KAPALIN Struktura kapalin je něco mezi plynem a pevnou látkou Částice kmitají ale mohou se také přemísťovat Zvýšením teploty se a tím se zvýší tekutost kapaliny Malé vzdálenosti
STRUKTURA A VLASTNOSTI KAPALIN Struktura kapalin je něco mezi plynem a pevnou látkou Částice kmitají ale mohou se také přemísťovat Zvýšením teploty se a tím se zvýší tekutost kapaliny Malé vzdálenosti
Transportní jevy v plynech Reálné plyny Fázové přechody Kapaliny
 Transportní jevy v plynech Reálné plyny Fázové přechody Kapaliny Hustota toku Zatím jsme studovali pouze soustavy, které byly v rovnovážném stavu není-li soustava v silovém poli, je hustota částic stejná
Transportní jevy v plynech Reálné plyny Fázové přechody Kapaliny Hustota toku Zatím jsme studovali pouze soustavy, které byly v rovnovážném stavu není-li soustava v silovém poli, je hustota částic stejná
SKUPENSKÉ PŘEMĚNY POJMY K ZOPAKOVÁNÍ. Testové úlohy varianta A
 Škola: Autor: DUM: Vzdělávací obor: Tematický okruh: Téma: Masarykovo gymnázium Vsetín Mgr. Jitka Novosadová MGV_F_SS_3S3_D11_Z_OPAK_T_Skupenske_premeny_T Člověk a příroda Fyzika Skupenské přeměny Opakování
Škola: Autor: DUM: Vzdělávací obor: Tematický okruh: Téma: Masarykovo gymnázium Vsetín Mgr. Jitka Novosadová MGV_F_SS_3S3_D11_Z_OPAK_T_Skupenske_premeny_T Člověk a příroda Fyzika Skupenské přeměny Opakování
STRUKTURA KAPALIN STRUKTURA KAPALIN
 Předmět: Ročník: Vytvořil: Datum: FYZIKA PRVNÍ MGR. JÜTTNEROVÁ 18. 5. 2013 Název zpracovaného celku: STRUKTURA KAPALIN STRUKTURA KAPALIN Struktura kapalin, povrchová vrstva kapaliny: Každá molekula kapaliny
Předmět: Ročník: Vytvořil: Datum: FYZIKA PRVNÍ MGR. JÜTTNEROVÁ 18. 5. 2013 Název zpracovaného celku: STRUKTURA KAPALIN STRUKTURA KAPALIN Struktura kapalin, povrchová vrstva kapaliny: Každá molekula kapaliny
LOGO. Změny skupenství
 Změny skupenství Látka existuje ve třech skupenstvích Pevném Kapalném Plynném Látka může přecházet z jednoho skupenství do druhého. Existují tedy tyto změny skupenství: Změny skupenství plyn sublimace
Změny skupenství Látka existuje ve třech skupenstvích Pevném Kapalném Plynném Látka může přecházet z jednoho skupenství do druhého. Existují tedy tyto změny skupenství: Změny skupenství plyn sublimace
Digitální učební materiál
 Evidenční číslo materiálu: 516 Digitální učební materiál Autor: Mgr. Pavel Kleibl Datum: 22. 1. 2013 Ročník: 8. Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Fyzika Tematický okruh: Energie Téma:
Evidenční číslo materiálu: 516 Digitální učební materiál Autor: Mgr. Pavel Kleibl Datum: 22. 1. 2013 Ročník: 8. Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Fyzika Tematický okruh: Energie Téma:
Struktura a vlastnosti kapalin
 Struktura a vlastnosti kapalin (test version, not revised) Petr Pošta pposta@karlin.mff.cuni.cz 24. listopadu 2010 Obsah Povrchová vrstva Jevy na rozhraní Kapilární tlak Kapilární jevy Objemová roztažnost
Struktura a vlastnosti kapalin (test version, not revised) Petr Pošta pposta@karlin.mff.cuni.cz 24. listopadu 2010 Obsah Povrchová vrstva Jevy na rozhraní Kapilární tlak Kapilární jevy Objemová roztažnost
Popis fyzikálního chování látek
 Popis fyzikálního chování látek pro vysvětlení noha fyzikálních jevů již nevystačíe s pouhý echanický popise Terodynaika oblast fyziky, která kroě echaniky zkouá vlastnosti akroskopických systéů, zejéna
Popis fyzikálního chování látek pro vysvětlení noha fyzikálních jevů již nevystačíe s pouhý echanický popise Terodynaika oblast fyziky, která kroě echaniky zkouá vlastnosti akroskopických systéů, zejéna
2 Jevy na rozhraní Kapilární tlak Kapilární jevy Objemová roztažnost kapalin 7
 Obsah Obsah 1 Povrchová vrstva 1 2 Jevy na rozhraní 3 2.1 Kapilární tlak........................... 4 2.2 Kapilární jevy........................... 5 3 Objemová roztažnost kapalin 7 1 Povrchová vrstva
Obsah Obsah 1 Povrchová vrstva 1 2 Jevy na rozhraní 3 2.1 Kapilární tlak........................... 4 2.2 Kapilární jevy........................... 5 3 Objemová roztažnost kapalin 7 1 Povrchová vrstva
SKUPENSTVÍ LÁTEK Prima - Fyzika
 SKUPENSTVÍ LÁTEK Prima - Fyzika Skupenství látek Pevné skupenství Skupenství látek Skupenství látek Pevné skupenství Kapalné skupenství Skupenství látek Pevné skupenství Kapalné skupenství Plynné skupenství
SKUPENSTVÍ LÁTEK Prima - Fyzika Skupenství látek Pevné skupenství Skupenství látek Skupenství látek Pevné skupenství Kapalné skupenství Skupenství látek Pevné skupenství Kapalné skupenství Plynné skupenství
(test version, not revised) 24. listopadu 2010
 Změny skupenství (test version, not revised) Petr Pošta pposta@karlin.mff.cuni.cz 24. listopadu 2010 Obsah Tání Tuhnutí Sublimace a desublimace Vypařování a var. Kondenzace Sytá pára Fázový diagram Vodní
Změny skupenství (test version, not revised) Petr Pošta pposta@karlin.mff.cuni.cz 24. listopadu 2010 Obsah Tání Tuhnutí Sublimace a desublimace Vypařování a var. Kondenzace Sytá pára Fázový diagram Vodní
FYZIKA 2. ROČNÍK. ρ = 8,0 kg m, M m 29 10 3 kg mol 1 p =? Příklady
 Příklady 1. Jaký je tlak vzduchu v pneuatice nákladního autoobilu při teplotě C a hustotě 8, kg 3? Molární hotnost vzduchu M 9 1 3 kg ol 1. t C T 93 K -3 ρ 8, kg, M 9 1 3 kg ol 1 p? p R T R T ρ M V M 8,31
Příklady 1. Jaký je tlak vzduchu v pneuatice nákladního autoobilu při teplotě C a hustotě 8, kg 3? Molární hotnost vzduchu M 9 1 3 kg ol 1. t C T 93 K -3 ρ 8, kg, M 9 1 3 kg ol 1 p? p R T R T ρ M V M 8,31
F - Změny skupenství látek
 F - Změny skupenství látek Určeno jako učební text pro studenty dálkového studia a jako shrnující text pro studenty denního studia. VARIACE 1 Tento dokument byl kompletně vytvořen, sestaven a vytištěn
F - Změny skupenství látek Určeno jako učební text pro studenty dálkového studia a jako shrnující text pro studenty denního studia. VARIACE 1 Tento dokument byl kompletně vytvořen, sestaven a vytištěn
2.6.6 Sytá pára. Předpoklady: 2604
 .6.6 Sytá ára Předolady: 604 Oaování: aaliny se vyařují za aždé teloty. Nejrychlejší částice uniají z aaliny a stává se z nich ára. Do isy nalijee vodu voda se ostuně vyařuje naonec zůstane isa rázdná,
.6.6 Sytá ára Předolady: 604 Oaování: aaliny se vyařují za aždé teloty. Nejrychlejší částice uniají z aaliny a stává se z nich ára. Do isy nalijee vodu voda se ostuně vyařuje naonec zůstane isa rázdná,
23_ 2 24_ 2 25_ 2 26_ 4 27_ 5 28_ 5 29_ 5 30_ 7 31_
 Obsah 23_ Změny skupenství... 2 24_ Tání... 2 25_ Skupenské teplo tání... 2 26_ Anomálie vody... 4 27_ Vypařování... 5 28_ Var... 5 29_ Kapalnění... 5 30_ Jak určíš skupenství látky?... 7 31_ Tepelné motory:...
Obsah 23_ Změny skupenství... 2 24_ Tání... 2 25_ Skupenské teplo tání... 2 26_ Anomálie vody... 4 27_ Vypařování... 5 28_ Var... 5 29_ Kapalnění... 5 30_ Jak určíš skupenství látky?... 7 31_ Tepelné motory:...
KAPALINY. Mgr. Jan Ptáčník - GJVJ - Fyzika - Sekunda
 KAPALINY Mgr. Jan Ptáčník - GJVJ - Fyzika - Sekunda Vlastnosti molekul kapalin V neustálém pohybu Ve stejných vzdálenostech, nejsou ale vázány Působí na sebe silami: odpudivé x přitažlivé Vlastnosti kapalin
KAPALINY Mgr. Jan Ptáčník - GJVJ - Fyzika - Sekunda Vlastnosti molekul kapalin V neustálém pohybu Ve stejných vzdálenostech, nejsou ale vázány Působí na sebe silami: odpudivé x přitažlivé Vlastnosti kapalin
GrafoTherm popis systému antikondenzační mikroporézní systém do interiéru ochranný, sanační
 GrafoTherm popis systému antikondenzační mikroporézní systém do interiéru ochranný, sanační Kondenzace 1.1. Vznik kondenzátu Kondenzát na střešní konstrukci ze strany interiéru Vzduch obsahuje vlhkost
GrafoTherm popis systému antikondenzační mikroporézní systém do interiéru ochranný, sanační Kondenzace 1.1. Vznik kondenzátu Kondenzát na střešní konstrukci ze strany interiéru Vzduch obsahuje vlhkost
Mol. fyz. a termodynamika
 Molekulová fyzika pracuje na základě kinetické teorie látek a statistiky Termodynamika zkoumání tepelných jevů a strojů nezajímají nás jednotlivé částice Molekulová fyzika základem jsou: Látka kteréhokoli
Molekulová fyzika pracuje na základě kinetické teorie látek a statistiky Termodynamika zkoumání tepelných jevů a strojů nezajímají nás jednotlivé částice Molekulová fyzika základem jsou: Látka kteréhokoli
1. Molekulová stavba kapalin
 1 Molekulová stavba kapalin 11 Vznik kapaliny kondenzací Plyn Vyjdeme z plynu Plyn je soustava molekul pohybujících se neuspořádaně všemi směry Pohybová energie molekul převládá nad energii polohovou Každá
1 Molekulová stavba kapalin 11 Vznik kapaliny kondenzací Plyn Vyjdeme z plynu Plyn je soustava molekul pohybujících se neuspořádaně všemi směry Pohybová energie molekul převládá nad energii polohovou Každá
DUM č. 12 v sadě. 10. Fy-1 Učební materiály do fyziky pro 2. ročník gymnázia
 projekt GML Brno Docens DUM č. 12 v sadě 10. Fy-1 Učební materiály do fyziky pro 2. ročník gymnázia Autor: Vojtěch Beneš Datum: 03.05.2014 Ročník: 1. ročník Anotace DUMu: Kapaliny, změny skupenství Materiály
projekt GML Brno Docens DUM č. 12 v sadě 10. Fy-1 Učební materiály do fyziky pro 2. ročník gymnázia Autor: Vojtěch Beneš Datum: 03.05.2014 Ročník: 1. ročník Anotace DUMu: Kapaliny, změny skupenství Materiály
Základem molekulové fyziky je kinetická teorie látek. Vychází ze tří pouček:
 Molekulová fyzika zkoumá vlastnosti látek na základě jejich vnitřní struktury, pohybu a vzájemného působení částic, ze kterých se látky skládají. Termodynamika se zabývá zákony přeměny různých forem energie
Molekulová fyzika zkoumá vlastnosti látek na základě jejich vnitřní struktury, pohybu a vzájemného působení částic, ze kterých se látky skládají. Termodynamika se zabývá zákony přeměny různých forem energie
Řešení: Fázový diagram vody
 Řešení: 1) Menší hustota ledu v souladu s Archimédovým zákonem zapříčiňuje plování jedu ve vodě. Vodní nádrže a toky tudíž zamrzají shora (od hladiny). Kdyby hustota ledu byla větší než hustota vody, docházelo
Řešení: 1) Menší hustota ledu v souladu s Archimédovým zákonem zapříčiňuje plování jedu ve vodě. Vodní nádrže a toky tudíž zamrzají shora (od hladiny). Kdyby hustota ledu byla větší než hustota vody, docházelo
Zavádění inovativních metod a výukových materiálů do přírodovědných předmětů na Gymnáziu v Krnově
 Zavádění inovativních metod a výukových materiálů do přírodovědných předmětů na Gymnáziu v Krnově 06_6_ Změny skupenství látek Ing. Jakub Ulmann 6 Změny skupenství látek 6.1 Tání 6.2 Tuhnutí 6.3 Změna
Zavádění inovativních metod a výukových materiálů do přírodovědných předmětů na Gymnáziu v Krnově 06_6_ Změny skupenství látek Ing. Jakub Ulmann 6 Změny skupenství látek 6.1 Tání 6.2 Tuhnutí 6.3 Změna
Vnitřní energie pevné látky < Vnitřní energie kapaliny < Vnitřní energie plynu (nejmenší energie)
 Změny skupenství Při změně tělesa z pevné látky na kapalinu nebo z kapaliny na plyn se jeho vnitřní energie zvyšuje musíme dodávat teplo (zahřívat). Při změně tělesa z plynu na kapalinu, nebo z kapaliny
Změny skupenství Při změně tělesa z pevné látky na kapalinu nebo z kapaliny na plyn se jeho vnitřní energie zvyšuje musíme dodávat teplo (zahřívat). Při změně tělesa z plynu na kapalinu, nebo z kapaliny
Přehled otázek z fyziky pro 2.ročník
 Přehled otázek z fyziky pro 2.ročník 1. Z jakých základních poznatků vychází teorie látek + důkazy. a) Látka kteréhokoli skupenství se skládá z částic molekul, atomů, iontů. b) Částice se v látce pohybují,
Přehled otázek z fyziky pro 2.ročník 1. Z jakých základních poznatků vychází teorie látek + důkazy. a) Látka kteréhokoli skupenství se skládá z částic molekul, atomů, iontů. b) Částice se v látce pohybují,
3.3 Částicová stavba látky
 3.3 Částicová stavba látky Malé (nejmenší) částice látky očekávali nejprve filozofové (atomisté) a nazvali je atomy (z řeckého atomos = nedělitelný) starověké Řecko a Řím. Mnohem později chemici zjistili,
3.3 Částicová stavba látky Malé (nejmenší) částice látky očekávali nejprve filozofové (atomisté) a nazvali je atomy (z řeckého atomos = nedělitelný) starověké Řecko a Řím. Mnohem později chemici zjistili,
1) Skupenství fáze, forma, stav. 2) 3 druhy skupenství (1 látky): pevné (led) kapalné (voda) plynné (vodní pára)
 SKUPENSTVÍ 1) Skupenství fáze, forma, stav 2) 3 druhy skupenství (1 látky): pevné (led) kapalné (voda) plynné (vodní pára) 3) Pevné látky nemění tvar, objem částice blízko sebe, pohybují se kolem urč.
SKUPENSTVÍ 1) Skupenství fáze, forma, stav 2) 3 druhy skupenství (1 látky): pevné (led) kapalné (voda) plynné (vodní pára) 3) Pevné látky nemění tvar, objem částice blízko sebe, pohybují se kolem urč.
VÝUKOVÝ MATERIÁL Ing. Yvona Bečičková Tematická oblast. Termika Číslo a název materiálu VY_32_INOVACE_0301_0220 Anotace
 VÝUKOVÝ MATERIÁL Identifikační údaje školy Vyšší odborná škola a Střední škola, Varnsdorf, příspěvková organizace Bratislavská 2166, 407 47 Varnsdorf, IČO: 18383874 www.vosassvdf.cz, tel. +420412372632
VÝUKOVÝ MATERIÁL Identifikační údaje školy Vyšší odborná škola a Střední škola, Varnsdorf, příspěvková organizace Bratislavská 2166, 407 47 Varnsdorf, IČO: 18383874 www.vosassvdf.cz, tel. +420412372632
F8 - Změny skupenství Číslo variace: 1
 F8 - Změny skupenství Číslo variace: 1 1. K vypařování kapaliny dochází: při každé teplotě v celém jejím objemu pouze při teplotě 100 C v celém objemu kapaliny pouze při normální teplotě a normálním tlaku
F8 - Změny skupenství Číslo variace: 1 1. K vypařování kapaliny dochází: při každé teplotě v celém jejím objemu pouze při teplotě 100 C v celém objemu kapaliny pouze při normální teplotě a normálním tlaku
TEPELNÉ JEVY. Mgr. Jan Ptáčník - GJVJ - Fyzika - Tercie
 TEPELNÉ JEVY Mgr. Jan Ptáčník - GJVJ - Fyzika - Tercie Vnitřní energie tělesa Každé těleso se skládá z látek. Látky se skládají z částic. neustálý neuspořádaný pohyb kinetická energie vzájemné působení
TEPELNÉ JEVY Mgr. Jan Ptáčník - GJVJ - Fyzika - Tercie Vnitřní energie tělesa Každé těleso se skládá z látek. Látky se skládají z částic. neustálý neuspořádaný pohyb kinetická energie vzájemné působení
Fyzikální učebna vybavená audiovizuální technikou, interaktivní tabule, fyzikální pomůcky
 Předmět: Náplň: Třída: Počet hodin: Pomůcky: Fyzika (FYZ) Molekulová fyzika, termika 2. ročník, sexta 2 hodiny týdně Fyzikální učebna vybavená audiovizuální technikou, interaktivní tabule, fyzikální pomůcky
Předmět: Náplň: Třída: Počet hodin: Pomůcky: Fyzika (FYZ) Molekulová fyzika, termika 2. ročník, sexta 2 hodiny týdně Fyzikální učebna vybavená audiovizuální technikou, interaktivní tabule, fyzikální pomůcky
Termodynamika. T [K ]=t [ 0 C] 273,15 T [ K ]= t [ 0 C] termodynamická teplota: Stavy hmoty. jednotka: 1 K (kelvin) = 1/273,16 část termodynamické
![Termodynamika. T [K ]=t [ 0 C] 273,15 T [ K ]= t [ 0 C] termodynamická teplota: Stavy hmoty. jednotka: 1 K (kelvin) = 1/273,16 část termodynamické Termodynamika. T [K ]=t [ 0 C] 273,15 T [ K ]= t [ 0 C] termodynamická teplota: Stavy hmoty. jednotka: 1 K (kelvin) = 1/273,16 část termodynamické](/thumbs/24/2778201.jpg) Termodynamika termodynamická teplota: Stavy hmoty jednotka: 1 K (kelvin) = 1/273,16 část termodynamické teploty trojného bodu vody (273,16 K = 0,01 o C). 0 o C = 273,15 K T [K ]=t [ 0 C] 273,15 T [ K ]=
Termodynamika termodynamická teplota: Stavy hmoty jednotka: 1 K (kelvin) = 1/273,16 část termodynamické teploty trojného bodu vody (273,16 K = 0,01 o C). 0 o C = 273,15 K T [K ]=t [ 0 C] 273,15 T [ K ]=
MOLEKULOVÁ FYZIKA A TERMODYNAMIKA
 MOLEKULOVÁ FYZIKA A TERMODYNAMIKA 2 metody zkoumání látek na základě vnějších projevů: I. KINETICKÁ TEORIE LÁTEK -studium vlastností látek na základě vnitřní struktury, pohybu a vzájemného působení jednotlivých
MOLEKULOVÁ FYZIKA A TERMODYNAMIKA 2 metody zkoumání látek na základě vnějších projevů: I. KINETICKÁ TEORIE LÁTEK -studium vlastností látek na základě vnitřní struktury, pohybu a vzájemného působení jednotlivých
LOGO. Molekulová fyzika
 Molekulová fyzika Molekulová fyzika Molekulová fyzika vysvětluje fyzikální jevy na základě znalosti jejich částicové struktury. Jejím základem je kinetická teorie látek (KTL). KTL obsahuje tři tvrzení:
Molekulová fyzika Molekulová fyzika Molekulová fyzika vysvětluje fyzikální jevy na základě znalosti jejich částicové struktury. Jejím základem je kinetická teorie látek (KTL). KTL obsahuje tři tvrzení:
ABSOLVENTSKÁ PRÁCE ZÁKLADNÍ ŠKOLA, ŠKOLNÍ 24, BYSTRÉ 9. ROČNÍK. Změny skupenství. Filip Skalský, David Řehůřek
 ABSOLVENTSKÁ PRÁCE ZÁKLADNÍ ŠKOLA, ŠKOLNÍ 24, 569 92 BYSTRÉ 9. ROČNÍK Změny skupenství Filip Skalský, David Řehůřek ŠKOLNÍ ROK 2011/2012 Prohlašujeme, že jsme absolventskou práci vypracovali samostatně
ABSOLVENTSKÁ PRÁCE ZÁKLADNÍ ŠKOLA, ŠKOLNÍ 24, 569 92 BYSTRÉ 9. ROČNÍK Změny skupenství Filip Skalský, David Řehůřek ŠKOLNÍ ROK 2011/2012 Prohlašujeme, že jsme absolventskou práci vypracovali samostatně
Zavádění inovativních metod a výukových materiálů do přírodovědných předmětů na Gymnáziu v Krnově. 06_5_ Struktura a vlastnosti kapalin
 Zavádění inovativních metod a výukových materiálů do přírodovědných předmětů na Gymnáziu v Krnově 06_5_ Struktura a vlastnosti kapalin Ing. Jakub Ulmann 5 Struktura a vlastnosti kapalin 5.1 Povrchové napětí
Zavádění inovativních metod a výukových materiálů do přírodovědných předmětů na Gymnáziu v Krnově 06_5_ Struktura a vlastnosti kapalin Ing. Jakub Ulmann 5 Struktura a vlastnosti kapalin 5.1 Povrchové napětí
Název DUM: Změny skupenství v příkladech
 Základní škola národního umělce Petra Bezruče, Frýdek-Místek, tř. T. G. Masaryka 454 Zpracováno v rámci OP VK - EU peníze školám Jednička ve vzdělávání CZ.1.07/1.4.00/21.2759 Název DUM: Změny skupenství
Základní škola národního umělce Petra Bezruče, Frýdek-Místek, tř. T. G. Masaryka 454 Zpracováno v rámci OP VK - EU peníze školám Jednička ve vzdělávání CZ.1.07/1.4.00/21.2759 Název DUM: Změny skupenství
VÝUKOVÝ MATERIÁL. 0301 Ing. Yvona Bečičková Tematická oblast. Termika Číslo a název materiálu VY_32_INOVACE_0301_0215 Anotace
 VÝUKOVÝ MATERIÁL Identifikační údaje školy Vyšší odborná škola a Střední škola, Varnsdorf, příspěvková organizace Bratislavská 2166, 407 47 Varnsdorf, IČO: 18383874 www.vosassvdf.cz, tel. +420412372632
VÝUKOVÝ MATERIÁL Identifikační údaje školy Vyšší odborná škola a Střední škola, Varnsdorf, příspěvková organizace Bratislavská 2166, 407 47 Varnsdorf, IČO: 18383874 www.vosassvdf.cz, tel. +420412372632
4. Kolmou tlakovou sílu působící v kapalině na libovolně orientovanou plochu S vyjádříme jako
 1. Pojem tekutiny je A) synonymem pojmu kapaliny B) pojmem označujícím souhrnně kapaliny a plyny C) synonymem pojmu plyny D) označením kapalin se zanedbatelnou viskozitou 2. Příčinou rozdílné tekutosti
1. Pojem tekutiny je A) synonymem pojmu kapaliny B) pojmem označujícím souhrnně kapaliny a plyny C) synonymem pojmu plyny D) označením kapalin se zanedbatelnou viskozitou 2. Příčinou rozdílné tekutosti
Molekulová fyzika a termika
 Molekulová fyzika a termika Fyzika 1. ročník Vzdělávání pro konkurenceschopnost Inovace výuky oboru Informační technologie MěSOŠ Klobouky u Brna Mgr. Petr Kučera 1 Obsah témat v kapitole Molekulová fyzika
Molekulová fyzika a termika Fyzika 1. ročník Vzdělávání pro konkurenceschopnost Inovace výuky oboru Informační technologie MěSOŠ Klobouky u Brna Mgr. Petr Kučera 1 Obsah témat v kapitole Molekulová fyzika
STRUKTURA PEVNÝCH LÁTEK A KAPALIN
 STRUKTURA PEVNÝCH LÁTEK A KAPALIN 19. ZMĚNY SKUPENSTVÍ, FÁZOVÝ DIAGRAM Autor: Ing. Eva Jančová DESS SOŠ a SOU spol. s r. o. SKUPENSTVÍ - Skupenství neboli stav je konkrétní forma látky, charakterizovaná
STRUKTURA PEVNÝCH LÁTEK A KAPALIN 19. ZMĚNY SKUPENSTVÍ, FÁZOVÝ DIAGRAM Autor: Ing. Eva Jančová DESS SOŠ a SOU spol. s r. o. SKUPENSTVÍ - Skupenství neboli stav je konkrétní forma látky, charakterizovaná
5. Stavy hmoty Kapaliny a kapalné krystaly
 a kapalné krystaly Vlastnosti kapalin kapalných krystalů jako rozpouštědla Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti kapaliny nestálé atraktivní interakce (kohezní síly) mezi molekulami,
a kapalné krystaly Vlastnosti kapalin kapalných krystalů jako rozpouštědla Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti kapaliny nestálé atraktivní interakce (kohezní síly) mezi molekulami,
Hydromechanické procesy Hydrostatika
 Hydromechanické procesy Hydrostatika M. Jahoda Hydrostatika 2 Hydrostatika se zabývá chováním tekutin, které se vzhledem k ohraničujícímu prostoru nepohybují - objem tekutiny bude v klidu, pokud výslednice
Hydromechanické procesy Hydrostatika M. Jahoda Hydrostatika 2 Hydrostatika se zabývá chováním tekutin, které se vzhledem k ohraničujícímu prostoru nepohybují - objem tekutiny bude v klidu, pokud výslednice
Fyzika - Sexta, 2. ročník
 - Sexta, 2. ročník Fyzika Výchovné a vzdělávací strategie Kompetence komunikativní Kompetence k řešení problémů Kompetence sociální a personální Kompetence občanská Kompetence k podnikavosti Kompetence
- Sexta, 2. ročník Fyzika Výchovné a vzdělávací strategie Kompetence komunikativní Kompetence k řešení problémů Kompetence sociální a personální Kompetence občanská Kompetence k podnikavosti Kompetence
SBÍRKA ŘEŠENÝCH FYZIKÁLNÍCH ÚLOH
 SBÍRKA ŘEŠENÝCH FYZIKÁLNÍCH ÚLOH MECHANIKA MOLEKULOVÁ FYZIKA A TERMIKA ELEKTŘINA A MAGNETISMUS KMITÁNÍ A VLNĚNÍ OPTIKA FYZIKA MIKROSVĚTA TERMODYNAMICKÁ TEPLOTNÍ STUPNICE, TEPLOTA 1) Převeďte hodnoty v
SBÍRKA ŘEŠENÝCH FYZIKÁLNÍCH ÚLOH MECHANIKA MOLEKULOVÁ FYZIKA A TERMIKA ELEKTŘINA A MAGNETISMUS KMITÁNÍ A VLNĚNÍ OPTIKA FYZIKA MIKROSVĚTA TERMODYNAMICKÁ TEPLOTNÍ STUPNICE, TEPLOTA 1) Převeďte hodnoty v
UČIVO. Termodynamická teplota. První termodynamický zákon Přenos vnitřní energie
 PŘEDMĚT: FYZIKA ROČNÍK: SEXTA VÝSTUP UČIVO MEZIPŘEDM. VZTAHY, PRŮŘEZOVÁ TÉMATA, PROJEKTY, KURZY POZNÁMKY Zná 3 základní poznatky kinetické teorie látek a vysvětlí jejich praktický význam Vysvětlí pojmy
PŘEDMĚT: FYZIKA ROČNÍK: SEXTA VÝSTUP UČIVO MEZIPŘEDM. VZTAHY, PRŮŘEZOVÁ TÉMATA, PROJEKTY, KURZY POZNÁMKY Zná 3 základní poznatky kinetické teorie látek a vysvětlí jejich praktický význam Vysvětlí pojmy
Fyzika, maturitní okruhy (profilová část), školní rok 2014/2015 Gymnázium INTEGRA BRNO
 1. Jednotky a veličiny soustava SI odvozené jednotky násobky a díly jednotek skalární a vektorové fyzikální veličiny rozměrová analýza 2. Kinematika hmotného bodu základní pojmy kinematiky hmotného bodu
1. Jednotky a veličiny soustava SI odvozené jednotky násobky a díly jednotek skalární a vektorové fyzikální veličiny rozměrová analýza 2. Kinematika hmotného bodu základní pojmy kinematiky hmotného bodu
CELKOVÉ OPAKOVÁNÍ UČIVA + ZÁPIS DO ŠKOLNÍHO SEŠITU část 03 VNITŘNÍ ENERGIE, TEPLO.
 CELKOVÉ OPAKOVÁNÍ UČIVA + ZÁPIS DO ŠKOLNÍHO SEŠITU část 03 VNITŘNÍ ENERGIE, TEPLO. 01) Složení látek opakování učiva 6. ročníku: Všechny látky jsou složeny z částic nepatrných rozměrů (tj. atomy, molekuly,
CELKOVÉ OPAKOVÁNÍ UČIVA + ZÁPIS DO ŠKOLNÍHO SEŠITU část 03 VNITŘNÍ ENERGIE, TEPLO. 01) Složení látek opakování učiva 6. ročníku: Všechny látky jsou složeny z částic nepatrných rozměrů (tj. atomy, molekuly,
Názvosloví Kvalita Výroba Kondenzace Teplosměnná plocha
 Názvosloví Kvalita Výroba Kondenzace Teplosměnná plocha Názvosloví páry Pro správné pochopení funkce parních systémů musíme znát základní pojmy spojené s párou. Entalpie Celková energie, příslušná danému
Názvosloví Kvalita Výroba Kondenzace Teplosměnná plocha Názvosloví páry Pro správné pochopení funkce parních systémů musíme znát základní pojmy spojené s párou. Entalpie Celková energie, příslušná danému
Půdní voda. *vyplňuje póry v půdách. *nevytváří souvislou hladinu. *je důležitá pro růst rostlin.
 PODPOVRCHOVÁ VODA Půdní voda *vyplňuje póry v půdách. *nevytváří souvislou hladinu. *je důležitá pro růst rostlin. Podzemní voda hromadí se na horninách, které jsou málo propustné pro vodu vytváří souvislou
PODPOVRCHOVÁ VODA Půdní voda *vyplňuje póry v půdách. *nevytváří souvislou hladinu. *je důležitá pro růst rostlin. Podzemní voda hromadí se na horninách, které jsou málo propustné pro vodu vytváří souvislou
Molekulová fyzika a termika. Přehled základních pojmů
 Molekulová fyzika a termika Přehled základních pojmů Kinetická teorie látek Vychází ze tří experimentálně ověřených poznatků: 1) Látky se skládají z částic - molekul, atomů nebo iontů, mezi nimiž jsou
Molekulová fyzika a termika Přehled základních pojmů Kinetická teorie látek Vychází ze tří experimentálně ověřených poznatků: 1) Látky se skládají z částic - molekul, atomů nebo iontů, mezi nimiž jsou
34_Mechanické vlastnosti kapalin... 2 Pascalův zákon _Tlak - příklady _Hydraulické stroje _PL: Hydraulické stroje - řešení...
 34_Mechanické vlastnosti kapalin... 2 Pascalův zákon... 2 35_Tlak - příklady... 2 36_Hydraulické stroje... 3 37_PL: Hydraulické stroje - řešení... 4 38_Účinky gravitační síly Země na kapalinu... 6 Hydrostatická
34_Mechanické vlastnosti kapalin... 2 Pascalův zákon... 2 35_Tlak - příklady... 2 36_Hydraulické stroje... 3 37_PL: Hydraulické stroje - řešení... 4 38_Účinky gravitační síly Země na kapalinu... 6 Hydrostatická
Látkové množství n poznámky 6.A GVN
 Látkové množství n poznámky 6.A GVN 10. září 2007 charakterizuje látky z hlediska počtu částic (molekul, atomů, iontů), které tato látka obsahuje je-li v tělese z homogenní látky N částic, pak látkové
Látkové množství n poznámky 6.A GVN 10. září 2007 charakterizuje látky z hlediska počtu částic (molekul, atomů, iontů), které tato látka obsahuje je-li v tělese z homogenní látky N částic, pak látkové
1. Mechanika - úvod. [ X ] - měřící jednotka. { X } - označuje kvantitu (množství)
![1. Mechanika - úvod. [ X ] - měřící jednotka. { X } - označuje kvantitu (množství) 1. Mechanika - úvod. [ X ] - měřící jednotka. { X } - označuje kvantitu (množství)](/thumbs/24/3153976.jpg) . Mechanika - úvod. Základní pojy V echanice se zabýváe základníi vlastnosti a pohybe hotných těles. Chcee-li přeístit těleso (echanický pohyb), potřebujee k tou znát tyto tři veličiny: hota, prostor,
. Mechanika - úvod. Základní pojy V echanice se zabýváe základníi vlastnosti a pohybe hotných těles. Chcee-li přeístit těleso (echanický pohyb), potřebujee k tou znát tyto tři veličiny: hota, prostor,
mechanická práce W Studentovo minimum GNB Mechanická práce a energie skalární veličina a) síla rovnoběžná s vektorem posunutí F s
 1 Mechanická práce mechanická práce W jednotka: [W] = J (joule) skalární veličina a) síla rovnoběžná s vektorem posunutí F s s dráha, kterou těleso urazilo 1 J = N m = kg m s -2 m = kg m 2 s -2 vyjádření
1 Mechanická práce mechanická práce W jednotka: [W] = J (joule) skalární veličina a) síla rovnoběžná s vektorem posunutí F s s dráha, kterou těleso urazilo 1 J = N m = kg m s -2 m = kg m 2 s -2 vyjádření
7. MECHANIKA TEKUTIN - statika
 7. - statika 7.1. Základní vlastnosti tekutin Obecným pojem tekutiny jsou myšleny. a. Mají společné vlastnosti tekutost, částice jsou od sebe snadno oddělitelné, nemají vlastní stálý tvar apod. Reálné
7. - statika 7.1. Základní vlastnosti tekutin Obecným pojem tekutiny jsou myšleny. a. Mají společné vlastnosti tekutost, částice jsou od sebe snadno oddělitelné, nemají vlastní stálý tvar apod. Reálné
Kalorimetrická rovnice, skupenské přeměny
 Základní škola Nový Bor, náměstí Míru 128, okres Česká Lípa, příspěvková organizace e mail: info@zsnamesti.cz; www.zsnamesti.cz; telefon: 487 722 010; fax: 487 722 378 Registrační číslo: CZ.1.07/1.4.00/21.3267
Základní škola Nový Bor, náměstí Míru 128, okres Česká Lípa, příspěvková organizace e mail: info@zsnamesti.cz; www.zsnamesti.cz; telefon: 487 722 010; fax: 487 722 378 Registrační číslo: CZ.1.07/1.4.00/21.3267
MECHANIKA KAPALIN A PLYNŮ. Mgr. Jan Ptáčník - GJVJ - Fyzika - Mechanika - 1. ročník
 MECHANIKA KAPALIN A PLYNŮ Mgr. Jan Ptáčník - GJVJ - Fyzika - Mechanika - 1. ročník Mechanika kapalin a plynů Hydrostatika - studuje podmínky rovnováhy kapalin. Aerostatika - studuje podmínky rovnováhy
MECHANIKA KAPALIN A PLYNŮ Mgr. Jan Ptáčník - GJVJ - Fyzika - Mechanika - 1. ročník Mechanika kapalin a plynů Hydrostatika - studuje podmínky rovnováhy kapalin. Aerostatika - studuje podmínky rovnováhy
Molekulová fyzika a termika:
 Molekulová fyzika a termika: 1. Měření teploty: 2. Délková roztažnost a Objemová roztažnost látek 3. Bimetal 4. Anomálie vody 5. Částicová stavba látek, vlastnosti látek 6. Atomová hmotnostní konstanta
Molekulová fyzika a termika: 1. Měření teploty: 2. Délková roztažnost a Objemová roztažnost látek 3. Bimetal 4. Anomálie vody 5. Částicová stavba látek, vlastnosti látek 6. Atomová hmotnostní konstanta
III/2 Inovace a zkvalitnění výuky prostřednictvím ICT. Pracovní list č.3 k prezentaci Křivky chladnutí a ohřevu kovů
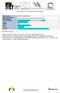 Číslo projektu CZ.1.07/1.5.00/34.0514 Číslo a název šablony klíčové aktivity III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Tematická oblast Strojírenská technologie, vy_32_inovace_ma_22_06 Autor
Číslo projektu CZ.1.07/1.5.00/34.0514 Číslo a název šablony klíčové aktivity III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Tematická oblast Strojírenská technologie, vy_32_inovace_ma_22_06 Autor
Základní poznatky. Teplota Vnitřní energie soustavy Teplo
 Molekulová fyzika a termika Základní poznatky Základní poznatky Teplota Vnitřní energie soustavy Teplo Termika = část fyziky zabývající se studiem vlastností látek a jejich změn souvisejících s teplotou
Molekulová fyzika a termika Základní poznatky Základní poznatky Teplota Vnitřní energie soustavy Teplo Termika = část fyziky zabývající se studiem vlastností látek a jejich změn souvisejících s teplotou
Kapaliny Molekulové vdw síly, vodíkové můstky
 Kapaliny Molekulové vdw síly, vodíkové můstky Metalické roztavené kovy, ionty + elektrony, elektrostatické síly Iontové roztavené soli, FLINAK (LiF + NaF + KF), volně pohyblivé anionty a kationty, iontová
Kapaliny Molekulové vdw síly, vodíkové můstky Metalické roztavené kovy, ionty + elektrony, elektrostatické síly Iontové roztavené soli, FLINAK (LiF + NaF + KF), volně pohyblivé anionty a kationty, iontová
Chemie - cvičení 2 - příklady
 Cheie - cvičení 2 - příklady Stavové chování 2/1 Zásobník o objeu 50 obsahuje plynný propan C H 8 při teplotě 20 o C a přetlaku 0,5 MPa. Baroetrický tlak je 770 torr. Kolik kg propanu je v zásobníku? Jaká
Cheie - cvičení 2 - příklady Stavové chování 2/1 Zásobník o objeu 50 obsahuje plynný propan C H 8 při teplotě 20 o C a přetlaku 0,5 MPa. Baroetrický tlak je 770 torr. Kolik kg propanu je v zásobníku? Jaká
molekuly zanedbatelné velikosti síla mezi molekulami zanedbatelná molekuly se chovají jako dokonale pružné koule
 . PLYNY IDEÁLNÍ PLYN: olekuly zanedbatelné velikosti síla ezi olekulai zanedbatelná olekuly se chovají jako dokonale pružné koule Pro ideální plyn platí stavová rovnice. Pozn.: blízkosti zkapalnění (velké
. PLYNY IDEÁLNÍ PLYN: olekuly zanedbatelné velikosti síla ezi olekulai zanedbatelná olekuly se chovají jako dokonale pružné koule Pro ideální plyn platí stavová rovnice. Pozn.: blízkosti zkapalnění (velké
2.2. Termika Teplota a teplo
 .. Terika Terika se zabývá zkouání tepelných vlastností látek. Podle současných poznatků vědy je každá látka kteréhokoli skupenství složena z částic, a to olekul, atoů nebo iontů. Prostor, který látka
.. Terika Terika se zabývá zkouání tepelných vlastností látek. Podle současných poznatků vědy je každá látka kteréhokoli skupenství složena z částic, a to olekul, atoů nebo iontů. Prostor, který látka
Mezi krystalické látky nepatří: a) asfalt b) křemík c) pryskyřice d) polvinylchlorid
 Mezi krystalické látky nepatří: a) asfalt b) křemík c) pryskyřice d) polvinylchlorid Mezi krystalické látky patří: a) grafit b) diamant c) jantar d) modrá skalice Mezi krystalické látky patří: a) rubín
Mezi krystalické látky nepatří: a) asfalt b) křemík c) pryskyřice d) polvinylchlorid Mezi krystalické látky patří: a) grafit b) diamant c) jantar d) modrá skalice Mezi krystalické látky patří: a) rubín
Nauka o materiálu. Přednáška č.2 Poruchy krystalické mřížky
 Nauka o materiálu Přednáška č.2 Poruchy krystalické mřížky Opakování z minula Materiál Degradační procesy Vnitřní stavba atomy, vazby Krystalické, amorfní, semikrystalické Vlastnosti materiálů chemické,
Nauka o materiálu Přednáška č.2 Poruchy krystalické mřížky Opakování z minula Materiál Degradační procesy Vnitřní stavba atomy, vazby Krystalické, amorfní, semikrystalické Vlastnosti materiálů chemické,
Pracovní list číslo 01
 Pracovní list číslo 01 Měření délky Jak se nazývá základní jednotka délky? Jaká délková měřidla používáme k měření rozměrů a) knihy b) okenní tabule c) třídy.. d) obvodu svého pasu.. Jaké díly a násobky
Pracovní list číslo 01 Měření délky Jak se nazývá základní jednotka délky? Jaká délková měřidla používáme k měření rozměrů a) knihy b) okenní tabule c) třídy.. d) obvodu svého pasu.. Jaké díly a násobky
13 otázek za 1 bod = 13 bodů Jméno a příjmení:
 13 otázek za 1 bod = 13 bodů Jméno a příjmení: 4 otázky za 2 body = 8 bodů Datum: 1 příklad za 3 body = 3 body Body: 1 příklad za 6 bodů = 6 bodů Celkem: 30 bodů příklady: 1) Sportovní vůz je schopný zrychlit
13 otázek za 1 bod = 13 bodů Jméno a příjmení: 4 otázky za 2 body = 8 bodů Datum: 1 příklad za 3 body = 3 body Body: 1 příklad za 6 bodů = 6 bodů Celkem: 30 bodů příklady: 1) Sportovní vůz je schopný zrychlit
Fyzikální vzdělávání. 1. ročník. Učební obor: Kuchař číšník Kadeřník. Implementace ICT do výuky č. CZ.1.07/1.1.02/02.0012 GG OP VK
 Fyzikální vzdělávání 1. ročník Učební obor: Kuchař číšník Kadeřník 1 2 Termika 2.1Teplota, teplotní roztažnost látek 2.2 Teplo a práce, přeměny vnitřní energie tělesa 2.3 Tepelné motory 2.4 Struktura pevných
Fyzikální vzdělávání 1. ročník Učební obor: Kuchař číšník Kadeřník 1 2 Termika 2.1Teplota, teplotní roztažnost látek 2.2 Teplo a práce, přeměny vnitřní energie tělesa 2.3 Tepelné motory 2.4 Struktura pevných
Fyzika je přírodní věda, která zkoumá a popisuje zákonitosti přírodních jevů.
 Fyzika je přírodní věda, která zkoumá a popisuje zákonitosti přírodních jevů. Násobky jednotek název značka hodnota kilo k 1000 mega M 1000000 giga G 1000000000 tera T 1000000000000 Tělesa a látky Tělesa
Fyzika je přírodní věda, která zkoumá a popisuje zákonitosti přírodních jevů. Násobky jednotek název značka hodnota kilo k 1000 mega M 1000000 giga G 1000000000 tera T 1000000000000 Tělesa a látky Tělesa
Termodynamika 2. UJOP Hostivař 2014
 Termodynamika 2 UJOP Hostivař 2014 Skupenské teplo tání/tuhnutí je (celkové) teplo, které přijme pevná látka při přechodu na kapalinu během tání nebo naopak Značka Veličina Lt J Nedochází při něm ke změně
Termodynamika 2 UJOP Hostivař 2014 Skupenské teplo tání/tuhnutí je (celkové) teplo, které přijme pevná látka při přechodu na kapalinu během tání nebo naopak Značka Veličina Lt J Nedochází při něm ke změně
JEVY NA ROZHRANÍ PEVNÉHO TĚLESA A KAPALINY
 Škola: Autor: DUM: Vzdělávací obor: Tematický okruh: Téma: Masarykovo gymnázium Vsetín Mgr. Dagmar Horká MGV_F_SS_1S3_D17_Z_MOLFYZ_Jevy_na_rozhrani_pevneho_tel esa_a_kapaliny_pl Člověk a příroda Fyzika
Škola: Autor: DUM: Vzdělávací obor: Tematický okruh: Téma: Masarykovo gymnázium Vsetín Mgr. Dagmar Horká MGV_F_SS_1S3_D17_Z_MOLFYZ_Jevy_na_rozhrani_pevneho_tel esa_a_kapaliny_pl Člověk a příroda Fyzika
Maturitní témata fyzika
 Maturitní témata fyzika 1. Kinematika pohybů hmotného bodu - mechanický pohyb a jeho sledování, trajektorie, dráha - rychlost hmotného bodu - rovnoměrný pohyb - zrychlení hmotného bodu - rovnoměrně zrychlený
Maturitní témata fyzika 1. Kinematika pohybů hmotného bodu - mechanický pohyb a jeho sledování, trajektorie, dráha - rychlost hmotného bodu - rovnoměrný pohyb - zrychlení hmotného bodu - rovnoměrně zrychlený
VY_32_INOVACE_246. Základní škola Luhačovice, příspěvková organizace Ing. Dagmar Zapletalová. Člověk a příroda Fyzika Opakování učiva fyziky
 VY_32_INOVACE_246 Škola Základní škola Luhačovice, příspěvková organizace Ing. Dagmar Zapletalová Datum: 1.9.2012 Ročník: 9. Člověk a příroda Fyzika Opakování učiva fyziky Téma: Souhrnné opakování učiva
VY_32_INOVACE_246 Škola Základní škola Luhačovice, příspěvková organizace Ing. Dagmar Zapletalová Datum: 1.9.2012 Ročník: 9. Člověk a příroda Fyzika Opakování učiva fyziky Téma: Souhrnné opakování učiva
Výpočty za použití zákonů pro ideální plyn
 ýočty za oužití zákonů ro ideální lyn Látka v lynné stavu je tvořena volnýi atoy(onoatoickýi olekulai), ionty nebo olekulai. Ideální lyn- olekuly na sebe neůsobí žádnýi silai, jejich obje je ve srovnání
ýočty za oužití zákonů ro ideální lyn Látka v lynné stavu je tvořena volnýi atoy(onoatoickýi olekulai), ionty nebo olekulai. Ideální lyn- olekuly na sebe neůsobí žádnýi silai, jejich obje je ve srovnání
Elektrický proud v elektrolytech
 Elektrolytický vodič Elektrický proud v elektrolytech Vezěe nádobu s destilovanou vodou (ta nevede el. proud) a vlože do ní dvě elektrody, které připojíe do zdroje stejnosěrného napětí. Do vody nasypee
Elektrolytický vodič Elektrický proud v elektrolytech Vezěe nádobu s destilovanou vodou (ta nevede el. proud) a vlože do ní dvě elektrody, které připojíe do zdroje stejnosěrného napětí. Do vody nasypee
Termodynamika 1. UJOP Hostivař 2014
 Termodynamika 1 UJOP Hostivař 2014 Termodynamika Zabývá se tepelnými ději obecně. Existují 3 termodynamické zákony: 1. Celkové množství energie (všech druhů) izolované soustavy zůstává zachováno. 2. Teplo
Termodynamika 1 UJOP Hostivař 2014 Termodynamika Zabývá se tepelnými ději obecně. Existují 3 termodynamické zákony: 1. Celkové množství energie (všech druhů) izolované soustavy zůstává zachováno. 2. Teplo
Skupenské stavy látek. Mezimolekulární síly
 Skupenské stavy látek Mezimolekulární síly 1 Interakce iont-dipól Např. hydratační (solvatační) interakce mezi Na + (iont) a molekulou vody (dipól). Jde o nejsilnější mezimolekulární (nevazebnou) interakci.
Skupenské stavy látek Mezimolekulární síly 1 Interakce iont-dipól Např. hydratační (solvatační) interakce mezi Na + (iont) a molekulou vody (dipól). Jde o nejsilnější mezimolekulární (nevazebnou) interakci.
ČÍSLO PROJEKTU: OPVK 1.4
 NÁZEV ŠKOLY: Základní škola Javorník, okres Jeseník REDIZO: 600 150 585 NÁZEV: VY_32_INOVACE_185_Skupenství AUTOR: Ing. Gavlas Miroslav ROČNÍK, DATUM: 8., 16.11.2011 VZDĚL. OBOR, TÉMA: Fyzika, ČÍSLO PROJEKTU:
NÁZEV ŠKOLY: Základní škola Javorník, okres Jeseník REDIZO: 600 150 585 NÁZEV: VY_32_INOVACE_185_Skupenství AUTOR: Ing. Gavlas Miroslav ROČNÍK, DATUM: 8., 16.11.2011 VZDĚL. OBOR, TÉMA: Fyzika, ČÍSLO PROJEKTU:
TERMODYNAMIKA Ideální plyn TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY.
 TERMODYNAMIKA Ideální plyn TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY. Ideální plyn je zjednodušená představa skutečného plynu. Je dokonale stlačitelný
TERMODYNAMIKA Ideální plyn TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY. Ideální plyn je zjednodušená představa skutečného plynu. Je dokonale stlačitelný
Mechanika kontinua. Mechanika elastických těles Mechanika kapalin
 Mechanika kontinua Mechanika elastických těles Mechanika kapalin Mechanika kontinua Mechanika elastických těles Mechanika kapalin a plynů Kinematika tekutin Hydrostatika Hydrodynamika Kontinuum Pro vyšetřování
Mechanika kontinua Mechanika elastických těles Mechanika kapalin Mechanika kontinua Mechanika elastických těles Mechanika kapalin a plynů Kinematika tekutin Hydrostatika Hydrodynamika Kontinuum Pro vyšetřování
Připravil: Roman Pavlačka, Markéta Sekaninová Hydrostatika
 Připravil: Roman Pavlačka, Markéta Sekaninová Hydrostatika OPVK CZ.1.07/2.2.00/28.0220, "Inovace studijních programů zahradnických oborů s důrazem na jazykové a odborné dovednosti a konkurenceschopnost
Připravil: Roman Pavlačka, Markéta Sekaninová Hydrostatika OPVK CZ.1.07/2.2.00/28.0220, "Inovace studijních programů zahradnických oborů s důrazem na jazykové a odborné dovednosti a konkurenceschopnost
Řešení úloh 1. kola 58. ročníku fyzikální olympiády. Kategorie C Autoři úloh: J. Thomas (1, 2, 5, 6, 7), J. Jírů (3), L.
 Řešení úloh 1. kola 58. ročníku fyzikální olympiády. Kategorie C Autoři úloh: J. Thomas (1, 2, 5, 6, 7), J. Jírů (3), L. Ledvina (4) 1.a) Na dosažení rychlosti v 0 potřebuje každý automobil dobu t v 0
Řešení úloh 1. kola 58. ročníku fyzikální olympiády. Kategorie C Autoři úloh: J. Thomas (1, 2, 5, 6, 7), J. Jírů (3), L. Ledvina (4) 1.a) Na dosažení rychlosti v 0 potřebuje každý automobil dobu t v 0
MOLEKULOVÁ FYZIKA KAPALIN
 MOLEKULOVÁ FYZIKA KAPALIN Struktura kapalin Povrchová vrstva kapaliny Povrchová energie, povrchová síla, povrchové napětí Kapilární tlak Kapilarita Prof. RNDr. Emanuel Svoboda, CSc. STRUKTURA KAPALIN Tvoří
MOLEKULOVÁ FYZIKA KAPALIN Struktura kapalin Povrchová vrstva kapaliny Povrchová energie, povrchová síla, povrchové napětí Kapilární tlak Kapilarita Prof. RNDr. Emanuel Svoboda, CSc. STRUKTURA KAPALIN Tvoří
Mechanika tekutin. Hydrostatika Hydrodynamika
 Mechanika tekutin Hydrostatika Hydrodynamika Hydrostatika Kapalinu považujeme za kontinuum, můžeme využít předchozí úvahy Studujeme kapalinu, která je v klidu hydrostatika Objem kapaliny bude v klidu,
Mechanika tekutin Hydrostatika Hydrodynamika Hydrostatika Kapalinu považujeme za kontinuum, můžeme využít předchozí úvahy Studujeme kapalinu, která je v klidu hydrostatika Objem kapaliny bude v klidu,
ZÁKLADNÍ ŠKOLA KOLÍN II., KMOCHOVA 943 škola s rozšířenou výukou matematiky a přírodovědných předmětů
 ZÁKLADNÍ ŠKOLA KOLÍN II., KMOCHOVA 943 škola s rozšířenou výukou matematiky a přírodovědných předmětů Autor Číslo materiálu Mgr. Vladimír Hradecký 8_F_1_13 Datum vytvoření 2. 11. 2011 Druh učebního materiálu
ZÁKLADNÍ ŠKOLA KOLÍN II., KMOCHOVA 943 škola s rozšířenou výukou matematiky a přírodovědných předmětů Autor Číslo materiálu Mgr. Vladimír Hradecký 8_F_1_13 Datum vytvoření 2. 11. 2011 Druh učebního materiálu
ÚVODNÍ POJMY, VNITŘNÍ ENERGIE, PRÁCE A TEPLO POJMY K ZOPAKOVÁNÍ. Testové úlohy varianta A
 Škola: Autor: DUM: Vzdělávací obor: Tematický okruh: Téma: Masarykovo gymnázium Vsetín Mgr. Jitka Novosadová MGV_F_SS_3S3_D08_Z_OPAK_T_Uvodni_pojmy_vnitrni_energie _prace_teplo_t Člověk a příroda Fyzika
Škola: Autor: DUM: Vzdělávací obor: Tematický okruh: Téma: Masarykovo gymnázium Vsetín Mgr. Jitka Novosadová MGV_F_SS_3S3_D08_Z_OPAK_T_Uvodni_pojmy_vnitrni_energie _prace_teplo_t Člověk a příroda Fyzika
V izolované soustavě nedochází k výměně tepla s okolím. Dokonalá izolovaná soustava neexistuje, nejvíce se jí blíží kalorimetr nebo termoska.
 Teplo a vnitřní energie pracovní list Vnitřní energie Všechny tělesa se skládají z částic, které vykonávají neustálý a neuspořádaný pohyb a které na sebe navzájem silově působí. Částice uvnitř všech těles
Teplo a vnitřní energie pracovní list Vnitřní energie Všechny tělesa se skládají z částic, které vykonávají neustálý a neuspořádaný pohyb a které na sebe navzájem silově působí. Částice uvnitř všech těles
POZNÁMKA: V USA se používá ještě Fahrenheitova teplotní stupnice. Převodní vztahy jsou vzhledem k volbě základních bodů složitější: 9 5
 TEPLO, TEPLOTA Tepelný stav látek je charakterizován veličinou termodynamická teplota T Jednotkou je kelvin T K Mezi Celsiovou a Kelvinovou teplotní stupnicí existuje převodní vztah T 73,5C t POZNÁMKA:
TEPLO, TEPLOTA Tepelný stav látek je charakterizován veličinou termodynamická teplota T Jednotkou je kelvin T K Mezi Celsiovou a Kelvinovou teplotní stupnicí existuje převodní vztah T 73,5C t POZNÁMKA:
13. Skupenské změny látek
 13. Skuenské změny látek Skuenství je konkrétní forma látky, charakterizovaná ředevším usořádáním částic v látce a rojevující se tyickými fyzikálními a chemickými vlastnostmi. Pro označení skuenství se
13. Skuenské změny látek Skuenství je konkrétní forma látky, charakterizovaná ředevším usořádáním částic v látce a rojevující se tyickými fyzikálními a chemickými vlastnostmi. Pro označení skuenství se
VNITŘNÍ ENERGIE. Mgr. Jan Ptáčník - GJVJ - Fyzika - 2. ročník - Termika
 VNITŘNÍ ENERGIE Mgr. Jan Ptáčník - GJVJ - Fyzika - 2. ročník - Termika Zákon zachování energie Ze zákona zachování mechanické energie platí: Ek + Ep = konst. Ale: Vnitřní energie tělesa Každé těleso má
VNITŘNÍ ENERGIE Mgr. Jan Ptáčník - GJVJ - Fyzika - 2. ročník - Termika Zákon zachování energie Ze zákona zachování mechanické energie platí: Ek + Ep = konst. Ale: Vnitřní energie tělesa Každé těleso má
Změna skupenství Zhotoveno ve školním roce: 2011/2012 Jméno zhotovitele: Ing. Iva Procházková
 Název a adresa školy: Střední škola průmyslová a uměleká Opava příspěvková organizae Praskova 399/8 Opava 7460 Název operačního programu: OP Vzdělávání pro konkureneshopnost oblast podpory.5 Registrační
Název a adresa školy: Střední škola průmyslová a uměleká Opava příspěvková organizae Praskova 399/8 Opava 7460 Název operačního programu: OP Vzdělávání pro konkureneshopnost oblast podpory.5 Registrační
