(test version, not revised) 24. listopadu 2010
|
|
|
- Jakub Šimek
- před 6 lety
- Počet zobrazení:
Transkript
1 Změny skupenství (test version, not revised) Petr Pošta 24. listopadu 2010
2 Obsah Tání Tuhnutí Sublimace a desublimace Vypařování a var. Kondenzace Sytá pára Fázový diagram Vodní pára v atmosféře
3 Změna skupenství = Fázový přechod Fyzikální děj, při kterém se mění skupenství látky, nazýváme změna skupenství látek nebo také fázovým přechodem. Některé látky existují ve všech třech skupenstvích plynné kapalné pevné.
4 Změny skupenství Látka může přecházet z pevného skupenství do kapalného skupenství (tání) z kapalného skupenství do pevného skupenství (tuhnutí) z pevného skupenství do plynného skupenství (sublimace) z plynného skupenství do pevného skupenství (desublimace) z kapalného skupenství do plynného skupenství (vypařování, var) z plynného skupenství do kapalného skupenství (kondenzace)
5 Tání
6 Tání přechod z pevného do kapalného skupenství probíhá při teplotě tání, která závisí na látce a vnějších podmínkách (zejména tlaku). Při normálním tlaku mluvíme o tzv. normální teplotě tání, kterou najdeme v tabulkách. (led 0 C, olovo 327,4 C, kysĺık 218, 4 C) Proces tání u krystalické pevné látky probíhá takto: dodáním tepla (energie) látku nejprve zahřejeme na teplotu tání. Poté dodáním dalšího tepla látka roztaje. Toto teplo (energii) je potřeba dodat na roztrhání vazeb mezi molekulami. U amorfní pevné látky se teplota látky zvyšuje i během procesu tání, kdy látka postupně více a více měkne, až se přemění v kapalinu.
7 Tání graf závislosti teploty krystalické a amorfní látky na dodaném teple
8 (měrné) skupenské teplo tání Teplo, které je potřeba dodat (krystalické) látce zahřáté na teplotu tání, aby se přeměnila v kapalinu, se nazývá skupenské teplo tání a značí se L t. Má jednotku J (joule). Teplo, které je potřeba dodat 1 kg (krystalické) látky zahřáté na teplotu tání, aby se přeměnila v kapalinu, se nazývá měrné skupenské teplo tání a značí se l t. Má jednotku J. kg 1 Platí l t = L t m, kde m je hmotnost látky. Měrné skupenské teplo lze najít v tabulkách, např. led 334 kj. kg 1, olovo 23 kj. kg 1, hliník 397 kj. kg 1, železo 279 kj. kg 1. Pokud porovnáme teplo potřebné na zahřátí látky na teplotu tání a teplo potřebné na roztání látky, pak je to druhé obvykle značně větší!
9 Tání z hlediska molekulové fyziky látka přijímá teplo = zvyšuje se vnitřní kinetická energie částic = zvyšuje se jejich rychlost, a tím i rozkmit, potažmo vzdálenost mezi částicemi při dosažení teploty tání už je rozkmit tak velký, že se začínají narušovat vazby mezi částicemi v místě, kde došlo ke zrušení vazeb, se mohou částice volně pohybovat a pevná látka se tak stává kapalinou
10 Tuhnutí
11 Tuhnutí přechod z kapalného do pevného skupenství probíhá při teplotě tuhnutí, která je stejná jako teplota tání. Proces tuhnutí u krystalické látky probíhá takto: odebráním tepla (energie) látku nejprve ochladíme na teplotu tání (tuhnutí). Poté odebíráním další energie látka postupně tuhne. Toto teplo vzniká postupným vytvářením vazeb mezi molekulami. Nejprve vznikají krystalizační jádra, tzv. zárodky malé pevné částečky uvnitř kapaliny. Obvykle jich vzniká více kolem pevných částeček přítomných v kapalině, např. zrníček prachu. Ve chvíli, kdy látka ztuhne, se všechny krystalky spojí a vznikne polykrystal. Ke vzniku monokrystalu je tak zapotřebí velmi čistá kapalina, ve které vznikne pouze jeden zárodek. U amorfní látky se teplota kapaliny snižuje i během procesu tuhnutí, kdy látka postupně více a více tuhne, až se přemění v amorfní pevnou látku.
12 Přechlazená kapalina U velmi čisté kapaliny se může stát, že zárodečný krystal nevznikne a kapalina se ochladí na nižší teplotu, než je teplota tání/tuhnutí. Takové kapalině se říká přechlazená kapalina. (Lze pozorovat i u vody, typické je to pro thiosíran sodný nebo octan sodný, čehož se využívá u tzv. termováčků.) V případě, že do přechlazené kapaliny vhodíme malý krystalek nebo nečistotu, látka obvykle rychle (zčásti) ztuhne a přitom se zahřeje na teplotu tání.
13 (měrné) skupenské teplo tuhnutí Teplo, které je potřeba odebrat kapalině ochlazené na teplotu tání, aby se přeměnila v (krystalickou) pevnou látku, se nazývá skupenské teplo tuhnutí a značí se L t. Má jednotku J (joule). Je stejné jako skupenské teplo tání. Teplo, které je potřeba odebrat 1 kg kapaliny ochlazené na teplotu tání, aby se přeměnila v (krystalickou) pevnou látku, se nazývá měrné skupenské teplo tuhnutí a značí se l t. Má jednotku J. kg 1. Platí l t = L t m, kde m je hmotnost látky. Taktéž je stejné jako měrné skupenské teplo tání.
14 Tuhnutí z hlediska molekulové fyziky látka odevzdává teplo = snižuje se vnitřní kinetická energie částic = snižuje se jejich rychlost při dosažení teploty tání/tuhnutí už je rychlost částic tak malá, že při náhodném vzniku vazby mezi částicemi nemají tyto částice dostatek energie (resp. dost rychlosti) na to, aby došlo k opětnému zrušení této vazby (resp. k úniku ze vzájemného silového působení) v místě, kde dojde ke vzniku vazeb, se částice už nemohou dále volně pohybovat a začíná vznikat krystalová mřížka
15 Změny objemu (hustoty) při tání/tuhnutí Příklady: led má zhruba o 9% větší objem než voda stejné hmotnosti naopak tekuté olovo má o cca 3,5% větší objem než pevné olovo Většina látek při tání svůj objem zvětšuje, ale z tohoto pravidla je řada výjimek (led/voda, bismut, germanium, některé slitiny). Růst objemu při tání je způsobený zvýšením střední vzdálenosti jednotlivých částic, což nastává u všech látek. Výjimečné látky, jejichž objem se zvětšuje při tuhnutí, mají tu vlastnost, že jejich krystalová mřížka obvykle obsahuje četné mezery.
16 Sublimace a desublimace
17 Sublimace přechod z pevného do plynného skupenství sublimuje např. jod, kafr, pevný CO 2 (suchý led), led, sníh nebo všechny páchnoucí pevné látky probíhá při všech teplotách, s rostoucí teplotou se proces urychluje
18 (měrné) skupenské teplo sublimace Teplo, které je potřeba dodat pevné látce, aby se přeměnila přímo v plyn procesem sublimace, se nazývá skupenské teplo sublimace a značí se L s. Má jednotku J (joule). Teplo, které je potřeba dodat 1 kg pevné látky, aby se přeměnila přímo v plyn, se nazývá měrné skupenské teplo sublimace a značí se l s. Má jednotku J. kg 1 Platí l s = L s m, kde m je hmotnost látky. Měrné skupenské teplo lze najít v tabulkách, např. pro led při teplotě 0 C je 2,8 MJ. kg 1 (tedy asi 10x větší než při přeměně na kapalinu).
19 Sublimace z hlediska molekulové fyziky molekuly v pevné látce se pohybují, obvykle kmitají kolem rovnovážných poloh čas od času se (vlivem náhodných srážek) podaří nějaké molekule z rovnovážné polohy uniknout pokud je tato molekula v povrchové vrstvě, pak může uniknout přímo do vzduchu; tyto uniklé molekuly tvoří vznikající plyn úniky z rovnovážné polohy jsou tím častější, čím rychlejší jsou částice v látce, tj. čím vyšší je teplota látky
20 Desublimace přechod z plynného do pevného skupenství probíhá při všech teplotách vždycky doprovází sublimaci: zatímco při sublimaci unikají částice pevné látky do vzduchu, při procesu sublimace se uniklé částice vrací nazpět do pevné látky Příkladem desublimace může být tvorba jinovatky (z vodní páry za mrazu) nebo drobných jodových krystalků z jodových par.
21 Desublimace z hlediska molekulové fyziky uniklé molekuly tvořící plyn se mohou volně pohybovat v prostoru čas od času nějaká z těchto molekul narazí na povrch pevné látky pokud není příliš rychlá nebo se náhodou trefí do uvolněného místa, pak se mezi ní a jejími sousedy vytvoří vazba a molekula tak zůstane v pevné látce Pokud necháme sublimaci volně běžet v uzavřené nádobě, pak se po nějakém čase vyrovná počet unikajících molekul z pevné látky a naopak proces navracejících se molekul z plynu.
22 Vypařování a var. Kondenzace
23 Vypařování přechod z kapalného do plynného skupenství probíhá při všech teplotách urychluje se s rostoucí teplotou, větším povrchem kapaliny a snížením koncentrace par nad kapalinou (odsáváním, větrem) Proces vypařování u kapalin probíhá podobně jako sublimace u pevných látek: částice z povrchové vrstvy mohou (vlivem náhodných srážek) uniknout ze sféry působení molekul kapaliny a vytvoří plyn (páru).
24 (měrné) skupenské teplo vypařování Teplo, které je potřeba dodat kapalině, aby se přeměnila v plyn procesem vypařování, se nazývá skupenské teplo vypařování a značí se L v. Má jednotku J (joule). Teplo, které je potřeba dodat 1 kg kapaliny, aby se přeměnila v plyn, se nazývá měrné skupenské teplo vypařování a značí se l v. Má jednotku J. kg 1. Platí l v = L V m, kde m je hmotnost látky. Měrné skupenské teplo vypařování lze najít v tabulkách. S rostoucí teplotou klesá. Např. pro vodu při teplotě 0 C je 2,51 MJ. kg 1, při teplotě kolem 100 C asi 2,26 MJ. kg 1.
25 Vypařování z hlediska molekulové fyziky Analogické vysvětlení jako u sublimace. molekuly v kapalině se pohybují, kmitají kolem rovnovážných poloh nebo přechází z jedné rovnovážné polohy do jiné, tj. čas od času se (vlivem náhodných srážek) podaří nějaké molekule z rovnovážné polohy uniknout (a to podstatně častěji než u pevných látek) pokud je tato molekula v povrchové vrstvě, pak může uniknout přímo do vzduchu; tyto uniklé molekuly tvoří vznikající plyn (páru) úniky z rovnovážné polohy jsou tím častější, čím rychlejší jsou částice v látce, tj. čím vyšší je teplota látky
26 Var (poprvé) Při dosažení určité teploty pozorujeme, že látka se dalším dodávání tepla nezahřívá. Namísto toho uvnitř začnou vznikat bubliny páry (a to tím rychleji, čím více tepla dodáváme). Tento jev nazýváme var. var nastává při určité teplotě, tzv. teplotě varu, která závisí na látce a na vnějších podmínkách (zejména tlaku). V případě normálního tlaku mluvíme o normální teplotě varu. Např. pro vodu je normální teplota varu 99,98 C, při dvojnásobném tlaku 200 kpa je to asi 120 C (Papinův hrnec), při tlaku 20 kpa je to asi 60 C.
27 (měrné) skupenské teplo varu Je to teplo, které se rovná (měrnému) skupenskému teplu vypařování při teplotě varu. Pro vodu již zmíněných 2,26 MJ. kg 1, pro ethylalkohol 0,84 MJ. kg 1. Vysoká teplota varu vody je důvodem, proč je voda dobrým hasicím prostředkem (na její přeměnu na páru je potřeba velké množství energie, kterou odebere hořící látce).
28 Kondenzace (kapalnění) přechod z plynného do kapalného skupenství probíhá při všech teplotách urychluje se se zvšením koncentrace par nad kapalinou Podobný procesu desublimace u pevných látek. Příkladem může být orosení skel za nízkých teplot.
29 Kondenzace z hlediska molekulové fyziky Molekuly tvořící plyn se mohou volně pohybovat v prostoru. Čas od času nějaká z těchto molekul narazí na povrch kapaliny, popřípadě na jinou molekulu plynu. Pokud není příliš rychlá, pak se mezi ní a jejími sousedy vytvoří vazba. Molekula tak bud zůstane v kapalině nebo shluklé molekuly začnou vytvářet kapku. Pokud necháme proces vypařování volně běžet v uzavřené nádobě, pak se po nějakém čase vyrovná počet unikajících molekul z kapaliny a naopak proces navracejících se molekul z plynu. V takovém případě mluvíme o vzniku syté páry.
30 Sytá pára
31 Vznik syté páry Pokud necháme proces vypařování volně běžet v uzavřené nádobě, pak se po nějakém čase vyrovná počet unikajících molekul z kapaliny a naopak proces navracejících se molekul z plynu. Kapalina a pára se dostanou do rovnovážného stavu. Pára, která je v rovnovážném stavu se svou kapalinou, se nazývá sytá pára.
32 Tlak syté páry (objem páry) Z experimentů vyplývá následující poznatek: tlak syté páry nezávisí při stálé teplotě na objemu páry. Jinak řečeno: pokud zvětšíme objem nádoby a tak poklesne tlak par, část kapaliny se opět vypaří, dokud tlak nestoupne na původní hodnotu. (Pro sytou páru tedy neplatí Boyle-Mariottův zákon, protože nejde o izotermický děj, při kterém by se neměnil počet částic plynu.) Někdy se můžete dočíst v učebnicích fyziky, že z tohoto důvodu neplatí pro sytou páru ani stavová rovnice pro ideální plyn (pv = NkT ). Její použití skutečně není vhodné, výsledné chyby jsou příliš velké, skutečný důvod ale leží někde úplně jinde.
33 Tlak syté páry (teplota páry) Z experimentů dále vyplývá: tlak syté páry při rostoucí teplotě roste. Křivka syté páry Závislost tlaku syté páry na teplotě se nazývá křivka syté páry. Pro různé látky je různá, pro látky typu vody viz obrázek.
34 Křivka syté páry trojný bod Tato křivka má počáteční a koncový bod. Počátečnímu bodu přísluší nejmenší hodnota teploty T A a tlaku p A, při kterých existuje kapalina a sytá pára v rovnovážném stavu (příslušná teplota je teplotou tuhnutí kapaliny při tlaku p A ). Při této teplotě a tlaku tedy může být v rovnováze s kapalinou a párou také pevné skupenství látky. Někdy tedy tento bod A nazýváme trojným bodem (podle toho, že v rovnováze se nachází všechna tři skupenství).
35 Křivka syté páry kritický bod Tato křivka má počáteční a koncový bod. Koncovému bodu přísluší největší hodnota teploty T K a tlaku p K, při kterých existuje kapalina a sytá pára v rovnovážném stavu a přitom tato dvě skupenství lze od sebe rozeznat. S rostoucím tlakem se totiž zvyšuje hustota páry a s rostoucí teplotou snižuje hustota kapaliny, přitom tyto změny jdou ruku v ruce. V kritickém bodě je hustota kapaliny i páry stejná a látka se stává homogenní. Koncový bod nazýváme kritickým bodem, příslušnou teplotu a tlak kritickou teplotou a kritickým tlakem, hustotu kritickou hustotou. Např. pro vodu to jsou 647,3 K (374,15 C), 22,13 MPa a 315 kg. m 3.
36 Křivka syté páry teplota varu Z křivky syté páry lze také odečíst teplotu varu. Připomeňme, že při varu vznikají uvnitř kapaliny bubliny v celém jejím objemu, které poté stoupají vzhůru. Vnitřek bublin tvoří pára, která musí vzdorovat tlaku vnějšího prostředí (především atmosféry). K varu tedy dochází tehdy, kdy tlak sytých par uvnitř bubliny je přibližně roven tlaku vnějšího prostředí, tj. atmosférickému tlaku. Na svislé ose tedy najdeme hodnotu odpovídající tlaku vzduchu, k němu příslušný bod na křivce a k tomuto bodu příslušnou teplotu, která je přibližně rovna teplotě varu za tohoto tlaku.
37 Fázový diagram
38 Fázový diagram Na svislé ose tlak, na vodorovné teplota. Sestává se ze tří křivek křivka syté páry k p (už známe) křivka tání k t (a tuhnutí) sublimační křivka k s (též křivka sublimace a desublimace)
39 Fázový diagram Body jednotlivých křivek označují hodnoty tlaku a teploty, kdy jsou v rovnováze obě skupenství: v případě křivky tání pevné a kapalné, v případě křivky syté páry kapalné a plynné a v případě sublimační křivky pevná látka a její sytá pára. Rovnovážný stav pevné látky a její syté páry je obdobný rovnovážnému stavu kapaliny a páry, tj. z páry do pevné látky (desublimace) přechází stejné množství částic jako z pevné látky do páry (sublimace).
40 Fázový diagram křivka tání Křivka tání začíná v bodě A (již zmíněném trojném bodě). Nejsou známy experimenty, které by svědčily o tom, že tato křivka má někde konec (podobně jako křivka sytých par).
41 Fázový diagram sublimační křivka Křivka směřuje od počátku do bodu A (již zmíněného trojného bodu). V případě velmi nízkých teplot se ale vlastnosti látek velmi výrazně mění, proto ji obvykle nekresĺıme už od počátku.
42 Fázový diagram trojný bod V trojném bodě (bod A) mohou v rovnováze vedle sebe existovat kapalina, plyn i pevná látka. Tento stav nastává při jediné kombinaci tlaku a teploty.
43 Fázový diagram tři oblasti Tři křivky děĺı diagram do tří oblastí. Oblast I je oblast, ve které může látka v rovnováze existovat pouze v pevném skupenství. Oblast II je oblast, ve které může látka v rovnováze existovat pouze v kapalném skupenství. Konečně oblast III je oblast, ve které může látka v rovnováze existovat pouze v plynném skupenství. Přitom tento plyn má nižší tlak, než sytá pára téže teploty. Někdy mluvíme o tzv. přehřáté páře. Přechod z jedné oblasti do druhé odpovídá změně skupenství látky.
44 Fázový diagram přehřátá pára Přehřátá pára může vzniknout ze syté páry dvěma základními způsoby: zvětšením objemu syté páry bez přítomnosti kapaliny při konstantní teplotě zahříváním syté páry bez přítomnosti kapaliny při konstantním tlaku Přehřátá pára je pára, která má nižší tlak a hustotu než sytá pára téže teploty.
45 Fázový diagram čtvrtá oblast Někdy rozlišujeme také čtvrtou oblast ve fázovém diagramu, která odpovídá vyšší než kritické teplotě. Při takové teplotě je látka vždy homogenní. Zkapalnění látky tak lze provést více způsoby. Při podkritické teplotě jde o viditelný přechod, proces kondenzace. Při ději, kdy plyn nejprve ohřejeme na nadkritickou teplotu, poté stlačíme na nadkritický tlak, následně zchladíme a tlak snížíme, je tento přechod plynulý a látka je neustále homogenní. Znázornění ve fázovém diagramu!
46 Vodní pára v atmosféře
47 Absolutní vlhkost značka: Φ jednotka: kg m 3 Absolutní vlhkost je skalární fyzikální veličina, která je vlastně hustotou vodních par ve vzduchu. Definujeme ji jako podíl Φ = m V, kde m je hmotnost vodních par ve vzduchu o objemu V. Měří se vlhkoměrem bud pomocí lidského vlasu (mění délku) nebo pomocí hygroskopických látek, které dokáží všechnu vodu ze vzduchu vstřebat (čímž se zvýší jejich hmotnost právě o tuto vstřebanou vodu).
48 Přehřátá a sytá vodní pára Vodní pára ve vzduchu bývá obvykle přehřátá. Při rostoucím množství vodních par nebo při snížení teploty se může stát sytou parou. Tím absolutní vlhkost dosáhne své maximální hodnoty Φ m. (Další příbytek vodní páry už není možný, tato přebytečná vodní pára totiž kondenzuje.) Hodnoty maximální absolutní vlhkosti pro různé teploty jsou tabelovány.
49 Relativní vlhkost značka: ϕ jednotka: 1 (bezrozm.) Je to podíl absolutní vlhkosti a její maximální hodnoty při dané teplotě: Vztah lze psát také ve tvaru ϕ = Φ Φ m 100%. ϕ = p p m 100% kde p je skutečný tlak vodních par a p m tlak sytých vodních par při dané teplotě. suchý vzduch relativní vlhkost 0% vzduch nasycený vodní parou rel. vlh. 100% nejvhodnější pro člověka: 50%-70%
50 Teplota rosného bodu (rosný bod) Je to teplota, na kterou by bylo potřeba ochladit vzduch (při daném tlaku), aby se vodní pára stala sytou. Tedy teplota, pod kterou začne vodní pára ze vzduchu kondenzovat (a orosí např. skla nebo jiné předměty v místnosti). Z páry vzniká na chladných předmětech rosa, nad povrchem země mlha, ve vyšších polohách mraky. Při teplotách nižších než 0 C vzniká jinovatka nebo sníh. (Mlhu a mraky tedy tvoří přímo rozptýlené kapičky vody, popř. ledu, nikoliv vodní pára!)
LOGO. Změny skupenství
 Změny skupenství Látka existuje ve třech skupenstvích Pevném Kapalném Plynném Látka může přecházet z jednoho skupenství do druhého. Existují tedy tyto změny skupenství: Změny skupenství plyn sublimace
Změny skupenství Látka existuje ve třech skupenstvích Pevném Kapalném Plynném Látka může přecházet z jednoho skupenství do druhého. Existují tedy tyto změny skupenství: Změny skupenství plyn sublimace
ZMĚNY SKUPENSTVÍ LÁTEK
 ZMĚNY SKUPENSTVÍ LÁTEK TÁNÍ A TUHNUTÍ - OSNOVA Kapilární jevy příklad Skupenské přeměny látek Tání a tuhnutí Teorie s video experimentem Příklad KAPILÁRNÍ JEVY - OPAKOVÁNÍ KAPILÁRNÍ JEVY - PŘÍKLAD Jak
ZMĚNY SKUPENSTVÍ LÁTEK TÁNÍ A TUHNUTÍ - OSNOVA Kapilární jevy příklad Skupenské přeměny látek Tání a tuhnutí Teorie s video experimentem Příklad KAPILÁRNÍ JEVY - OPAKOVÁNÍ KAPILÁRNÍ JEVY - PŘÍKLAD Jak
SKUPENSKÉ PŘEMĚNY POJMY K ZOPAKOVÁNÍ. Testové úlohy varianta A
 Škola: Autor: DUM: Vzdělávací obor: Tematický okruh: Téma: Masarykovo gymnázium Vsetín Mgr. Jitka Novosadová MGV_F_SS_3S3_D11_Z_OPAK_T_Skupenske_premeny_T Člověk a příroda Fyzika Skupenské přeměny Opakování
Škola: Autor: DUM: Vzdělávací obor: Tematický okruh: Téma: Masarykovo gymnázium Vsetín Mgr. Jitka Novosadová MGV_F_SS_3S3_D11_Z_OPAK_T_Skupenske_premeny_T Člověk a příroda Fyzika Skupenské přeměny Opakování
Digitální učební materiál
 Evidenční číslo materiálu: 516 Digitální učební materiál Autor: Mgr. Pavel Kleibl Datum: 22. 1. 2013 Ročník: 8. Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Fyzika Tematický okruh: Energie Téma:
Evidenční číslo materiálu: 516 Digitální učební materiál Autor: Mgr. Pavel Kleibl Datum: 22. 1. 2013 Ročník: 8. Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Fyzika Tematický okruh: Energie Téma:
F - Změny skupenství látek
 F - Změny skupenství látek Určeno jako učební text pro studenty dálkového studia a jako shrnující text pro studenty denního studia. VARIACE 1 Tento dokument byl kompletně vytvořen, sestaven a vytištěn
F - Změny skupenství látek Určeno jako učební text pro studenty dálkového studia a jako shrnující text pro studenty denního studia. VARIACE 1 Tento dokument byl kompletně vytvořen, sestaven a vytištěn
Vnitřní energie pevné látky < Vnitřní energie kapaliny < Vnitřní energie plynu (nejmenší energie)
 Změny skupenství Při změně tělesa z pevné látky na kapalinu nebo z kapaliny na plyn se jeho vnitřní energie zvyšuje musíme dodávat teplo (zahřívat). Při změně tělesa z plynu na kapalinu, nebo z kapaliny
Změny skupenství Při změně tělesa z pevné látky na kapalinu nebo z kapaliny na plyn se jeho vnitřní energie zvyšuje musíme dodávat teplo (zahřívat). Při změně tělesa z plynu na kapalinu, nebo z kapaliny
F8 - Změny skupenství Číslo variace: 1
 F8 - Změny skupenství Číslo variace: 1 1. K vypařování kapaliny dochází: při každé teplotě v celém jejím objemu pouze při teplotě 100 C v celém objemu kapaliny pouze při normální teplotě a normálním tlaku
F8 - Změny skupenství Číslo variace: 1 1. K vypařování kapaliny dochází: při každé teplotě v celém jejím objemu pouze při teplotě 100 C v celém objemu kapaliny pouze při normální teplotě a normálním tlaku
Zavádění inovativních metod a výukových materiálů do přírodovědných předmětů na Gymnáziu v Krnově
 Zavádění inovativních metod a výukových materiálů do přírodovědných předmětů na Gymnáziu v Krnově 06_6_ Změny skupenství látek Ing. Jakub Ulmann 6 Změny skupenství látek 6.1 Tání 6.2 Tuhnutí 6.3 Změna
Zavádění inovativních metod a výukových materiálů do přírodovědných předmětů na Gymnáziu v Krnově 06_6_ Změny skupenství látek Ing. Jakub Ulmann 6 Změny skupenství látek 6.1 Tání 6.2 Tuhnutí 6.3 Změna
Název DUM: Změny skupenství v příkladech
 Základní škola národního umělce Petra Bezruče, Frýdek-Místek, tř. T. G. Masaryka 454 Zpracováno v rámci OP VK - EU peníze školám Jednička ve vzdělávání CZ.1.07/1.4.00/21.2759 Název DUM: Změny skupenství
Základní škola národního umělce Petra Bezruče, Frýdek-Místek, tř. T. G. Masaryka 454 Zpracováno v rámci OP VK - EU peníze školám Jednička ve vzdělávání CZ.1.07/1.4.00/21.2759 Název DUM: Změny skupenství
TEPELNÉ JEVY. Mgr. Jan Ptáčník - GJVJ - Fyzika - Tercie
 TEPELNÉ JEVY Mgr. Jan Ptáčník - GJVJ - Fyzika - Tercie Vnitřní energie tělesa Každé těleso se skládá z látek. Látky se skládají z částic. neustálý neuspořádaný pohyb kinetická energie vzájemné působení
TEPELNÉ JEVY Mgr. Jan Ptáčník - GJVJ - Fyzika - Tercie Vnitřní energie tělesa Každé těleso se skládá z látek. Látky se skládají z částic. neustálý neuspořádaný pohyb kinetická energie vzájemné působení
1) Skupenství fáze, forma, stav. 2) 3 druhy skupenství (1 látky): pevné (led) kapalné (voda) plynné (vodní pára)
 SKUPENSTVÍ 1) Skupenství fáze, forma, stav 2) 3 druhy skupenství (1 látky): pevné (led) kapalné (voda) plynné (vodní pára) 3) Pevné látky nemění tvar, objem částice blízko sebe, pohybují se kolem urč.
SKUPENSTVÍ 1) Skupenství fáze, forma, stav 2) 3 druhy skupenství (1 látky): pevné (led) kapalné (voda) plynné (vodní pára) 3) Pevné látky nemění tvar, objem částice blízko sebe, pohybují se kolem urč.
SKUPENSTVÍ LÁTEK Prima - Fyzika
 SKUPENSTVÍ LÁTEK Prima - Fyzika Skupenství látek Pevné skupenství Skupenství látek Skupenství látek Pevné skupenství Kapalné skupenství Skupenství látek Pevné skupenství Kapalné skupenství Plynné skupenství
SKUPENSTVÍ LÁTEK Prima - Fyzika Skupenství látek Pevné skupenství Skupenství látek Skupenství látek Pevné skupenství Kapalné skupenství Skupenství látek Pevné skupenství Kapalné skupenství Plynné skupenství
Kalorimetrická rovnice, skupenské přeměny
 Základní škola Nový Bor, náměstí Míru 128, okres Česká Lípa, příspěvková organizace e mail: info@zsnamesti.cz; www.zsnamesti.cz; telefon: 487 722 010; fax: 487 722 378 Registrační číslo: CZ.1.07/1.4.00/21.3267
Základní škola Nový Bor, náměstí Míru 128, okres Česká Lípa, příspěvková organizace e mail: info@zsnamesti.cz; www.zsnamesti.cz; telefon: 487 722 010; fax: 487 722 378 Registrační číslo: CZ.1.07/1.4.00/21.3267
STRUKTURA KAPALIN STRUKTURA KAPALIN
 Předmět: Ročník: Vytvořil: Datum: FYZIKA PRVNÍ MGR. JÜTTNEROVÁ 18. 5. 2013 Název zpracovaného celku: STRUKTURA KAPALIN STRUKTURA KAPALIN Struktura kapalin, povrchová vrstva kapaliny: Každá molekula kapaliny
Předmět: Ročník: Vytvořil: Datum: FYZIKA PRVNÍ MGR. JÜTTNEROVÁ 18. 5. 2013 Název zpracovaného celku: STRUKTURA KAPALIN STRUKTURA KAPALIN Struktura kapalin, povrchová vrstva kapaliny: Každá molekula kapaliny
23_ 2 24_ 2 25_ 2 26_ 4 27_ 5 28_ 5 29_ 5 30_ 7 31_
 Obsah 23_ Změny skupenství... 2 24_ Tání... 2 25_ Skupenské teplo tání... 2 26_ Anomálie vody... 4 27_ Vypařování... 5 28_ Var... 5 29_ Kapalnění... 5 30_ Jak určíš skupenství látky?... 7 31_ Tepelné motory:...
Obsah 23_ Změny skupenství... 2 24_ Tání... 2 25_ Skupenské teplo tání... 2 26_ Anomálie vody... 4 27_ Vypařování... 5 28_ Var... 5 29_ Kapalnění... 5 30_ Jak určíš skupenství látky?... 7 31_ Tepelné motory:...
Řešení: Fázový diagram vody
 Řešení: 1) Menší hustota ledu v souladu s Archimédovým zákonem zapříčiňuje plování jedu ve vodě. Vodní nádrže a toky tudíž zamrzají shora (od hladiny). Kdyby hustota ledu byla větší než hustota vody, docházelo
Řešení: 1) Menší hustota ledu v souladu s Archimédovým zákonem zapříčiňuje plování jedu ve vodě. Vodní nádrže a toky tudíž zamrzají shora (od hladiny). Kdyby hustota ledu byla větší než hustota vody, docházelo
DUM č. 12 v sadě. 10. Fy-1 Učební materiály do fyziky pro 2. ročník gymnázia
 projekt GML Brno Docens DUM č. 12 v sadě 10. Fy-1 Učební materiály do fyziky pro 2. ročník gymnázia Autor: Vojtěch Beneš Datum: 03.05.2014 Ročník: 1. ročník Anotace DUMu: Kapaliny, změny skupenství Materiály
projekt GML Brno Docens DUM č. 12 v sadě 10. Fy-1 Učební materiály do fyziky pro 2. ročník gymnázia Autor: Vojtěch Beneš Datum: 03.05.2014 Ročník: 1. ročník Anotace DUMu: Kapaliny, změny skupenství Materiály
Molekulová fyzika a termika
 Molekulová fyzika a termika Fyzika 1. ročník Vzdělávání pro konkurenceschopnost Inovace výuky oboru Informační technologie MěSOŠ Klobouky u Brna Mgr. Petr Kučera 1 Obsah témat v kapitole Molekulová fyzika
Molekulová fyzika a termika Fyzika 1. ročník Vzdělávání pro konkurenceschopnost Inovace výuky oboru Informační technologie MěSOŠ Klobouky u Brna Mgr. Petr Kučera 1 Obsah témat v kapitole Molekulová fyzika
Mol. fyz. a termodynamika
 Molekulová fyzika pracuje na základě kinetické teorie látek a statistiky Termodynamika zkoumání tepelných jevů a strojů nezajímají nás jednotlivé částice Molekulová fyzika základem jsou: Látka kteréhokoli
Molekulová fyzika pracuje na základě kinetické teorie látek a statistiky Termodynamika zkoumání tepelných jevů a strojů nezajímají nás jednotlivé částice Molekulová fyzika základem jsou: Látka kteréhokoli
VÝUKOVÝ MATERIÁL. 0301 Ing. Yvona Bečičková Tematická oblast. Termika Číslo a název materiálu VY_32_INOVACE_0301_0215 Anotace
 VÝUKOVÝ MATERIÁL Identifikační údaje školy Vyšší odborná škola a Střední škola, Varnsdorf, příspěvková organizace Bratislavská 2166, 407 47 Varnsdorf, IČO: 18383874 www.vosassvdf.cz, tel. +420412372632
VÝUKOVÝ MATERIÁL Identifikační údaje školy Vyšší odborná škola a Střední škola, Varnsdorf, příspěvková organizace Bratislavská 2166, 407 47 Varnsdorf, IČO: 18383874 www.vosassvdf.cz, tel. +420412372632
FYZIKA 2. ROČNÍK. Změny skupenství látek. Tání a tuhnutí. Pevná látka. soustava velkého počtu částic. Plyn
 Zěny skuenství látek Pevná látka Kaalina Plyn soustava velkého očtu částic Má-li soustava v rovnovážné stavu ve všech částech stejné fyzikální a cheické vlastnosti (stejnou hustotu, stejnou strukturu a
Zěny skuenství látek Pevná látka Kaalina Plyn soustava velkého očtu částic Má-li soustava v rovnovážné stavu ve všech částech stejné fyzikální a cheické vlastnosti (stejnou hustotu, stejnou strukturu a
ABSOLVENTSKÁ PRÁCE ZÁKLADNÍ ŠKOLA, ŠKOLNÍ 24, BYSTRÉ 9. ROČNÍK. Změny skupenství. Filip Skalský, David Řehůřek
 ABSOLVENTSKÁ PRÁCE ZÁKLADNÍ ŠKOLA, ŠKOLNÍ 24, 569 92 BYSTRÉ 9. ROČNÍK Změny skupenství Filip Skalský, David Řehůřek ŠKOLNÍ ROK 2011/2012 Prohlašujeme, že jsme absolventskou práci vypracovali samostatně
ABSOLVENTSKÁ PRÁCE ZÁKLADNÍ ŠKOLA, ŠKOLNÍ 24, 569 92 BYSTRÉ 9. ROČNÍK Změny skupenství Filip Skalský, David Řehůřek ŠKOLNÍ ROK 2011/2012 Prohlašujeme, že jsme absolventskou práci vypracovali samostatně
Měření měrného skupenského tepla tání ledu
 KATEDRA EXPERIMENTÁLNÍ FYZIKY PŘÍRODOVĚDECKÁ FAKULTA UNIVERZITY PALACKÉHO V OLOMOUCI FYZIKÁLNÍ PRAKTIKUM Z MOLEKULOVÉ FYZIKY A TERMODYNAMIKY Měření měrného skupenského tepla tání ledu Úvod Tání, měrné
KATEDRA EXPERIMENTÁLNÍ FYZIKY PŘÍRODOVĚDECKÁ FAKULTA UNIVERZITY PALACKÉHO V OLOMOUCI FYZIKÁLNÍ PRAKTIKUM Z MOLEKULOVÉ FYZIKY A TERMODYNAMIKY Měření měrného skupenského tepla tání ledu Úvod Tání, měrné
Transportní jevy v plynech Reálné plyny Fázové přechody Kapaliny
 Transportní jevy v plynech Reálné plyny Fázové přechody Kapaliny Hustota toku Zatím jsme studovali pouze soustavy, které byly v rovnovážném stavu není-li soustava v silovém poli, je hustota částic stejná
Transportní jevy v plynech Reálné plyny Fázové přechody Kapaliny Hustota toku Zatím jsme studovali pouze soustavy, které byly v rovnovážném stavu není-li soustava v silovém poli, je hustota částic stejná
Změna skupenství, Tání a tuhnutí, Sublimace a desublimace Vypařování a kapalnění Sytá pára, Fázový diagram, Vodní pára
 Zěny skupenství átek Zěna skupenství, Tání a tuhnutí, Subiace a desubiace Vypařování a kapanění Sytá pára, Fázový diagra, Vodní pára Zěna skupenství = fyzikání děj, při které se ění skupenství átky Skupenství
Zěny skupenství átek Zěna skupenství, Tání a tuhnutí, Subiace a desubiace Vypařování a kapanění Sytá pára, Fázový diagra, Vodní pára Zěna skupenství = fyzikání děj, při které se ění skupenství átky Skupenství
STRUKTURA PEVNÝCH LÁTEK A KAPALIN
 STRUKTURA PEVNÝCH LÁTEK A KAPALIN 19. ZMĚNY SKUPENSTVÍ, FÁZOVÝ DIAGRAM Autor: Ing. Eva Jančová DESS SOŠ a SOU spol. s r. o. SKUPENSTVÍ - Skupenství neboli stav je konkrétní forma látky, charakterizovaná
STRUKTURA PEVNÝCH LÁTEK A KAPALIN 19. ZMĚNY SKUPENSTVÍ, FÁZOVÝ DIAGRAM Autor: Ing. Eva Jančová DESS SOŠ a SOU spol. s r. o. SKUPENSTVÍ - Skupenství neboli stav je konkrétní forma látky, charakterizovaná
3.2 Látka a její skupenství
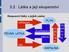 3.2 Látka a její skupenství Skupenství látky a jejich změny sublimace PEVNÁ LÁTKA tání desublimace tuhnutí PLYN vy pa řo vá ní KAPALINA zka pal ňo vá ní Látka a změna vnitřní energie Změna vnitřní energie
3.2 Látka a její skupenství Skupenství látky a jejich změny sublimace PEVNÁ LÁTKA tání desublimace tuhnutí PLYN vy pa řo vá ní KAPALINA zka pal ňo vá ní Látka a změna vnitřní energie Změna vnitřní energie
13. Skupenské změny látek
 13. Skuenské změny látek Skuenství je konkrétní forma látky, charakterizovaná ředevším usořádáním částic v látce a rojevující se tyickými fyzikálními a chemickými vlastnostmi. Pro označení skuenství se
13. Skuenské změny látek Skuenství je konkrétní forma látky, charakterizovaná ředevším usořádáním částic v látce a rojevující se tyickými fyzikálními a chemickými vlastnostmi. Pro označení skuenství se
III/2 Inovace a zkvalitnění výuky prostřednictvím ICT. Pracovní list č.3 k prezentaci Křivky chladnutí a ohřevu kovů
 Číslo projektu CZ.1.07/1.5.00/34.0514 Číslo a název šablony klíčové aktivity III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Tematická oblast Strojírenská technologie, vy_32_inovace_ma_22_06 Autor
Číslo projektu CZ.1.07/1.5.00/34.0514 Číslo a název šablony klíčové aktivity III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Tematická oblast Strojírenská technologie, vy_32_inovace_ma_22_06 Autor
POZNÁMKA: V USA se používá ještě Fahrenheitova teplotní stupnice. Převodní vztahy jsou vzhledem k volbě základních bodů složitější: 9 5
 TEPLO, TEPLOTA Tepelný stav látek je charakterizován veličinou termodynamická teplota T Jednotkou je kelvin T K Mezi Celsiovou a Kelvinovou teplotní stupnicí existuje převodní vztah T 73,5C t POZNÁMKA:
TEPLO, TEPLOTA Tepelný stav látek je charakterizován veličinou termodynamická teplota T Jednotkou je kelvin T K Mezi Celsiovou a Kelvinovou teplotní stupnicí existuje převodní vztah T 73,5C t POZNÁMKA:
Ideální plyn. Stavová rovnice Děje v ideálním plynu Práce plynu, Kruhový děj, Tepelné motory
 Struktura a vlastnosti plynů Ideální plyn Vlastnosti ideálního plynu: Ideální plyn Stavová rovnice Děje v ideálním plynu Práce plynu, Kruhový děj, epelné motory rozměry molekul jsou ve srovnání se střední
Struktura a vlastnosti plynů Ideální plyn Vlastnosti ideálního plynu: Ideální plyn Stavová rovnice Děje v ideálním plynu Práce plynu, Kruhový děj, epelné motory rozměry molekul jsou ve srovnání se střední
5.7 Vlhkost vzduchu 5.7.5 Absolutní vlhkost 5.7.6 Poměrná vlhkost 5.7.7 Rosný bod 5.7.8 Složení vzduchu 5.7.9 Měření vlhkosti vzduchu
 Fázové přechody 5.6.5 Fáze Fázové rozhraní 5.6.6 Gibbsovo pravidlo fází 5.6.7 Fázový přechod Fázový přechod prvního druhu Fázový přechod druhého druhu 5.6.7.1 Clausiova-Clapeyronova rovnice 5.6.8 Skupenství
Fázové přechody 5.6.5 Fáze Fázové rozhraní 5.6.6 Gibbsovo pravidlo fází 5.6.7 Fázový přechod Fázový přechod prvního druhu Fázový přechod druhého druhu 5.6.7.1 Clausiova-Clapeyronova rovnice 5.6.8 Skupenství
Fyzikální učebna vybavená audiovizuální technikou, interaktivní tabule, fyzikální pomůcky
 Předmět: Náplň: Třída: Počet hodin: Pomůcky: Fyzika (FYZ) Molekulová fyzika, termika 2. ročník, sexta 2 hodiny týdně Fyzikální učebna vybavená audiovizuální technikou, interaktivní tabule, fyzikální pomůcky
Předmět: Náplň: Třída: Počet hodin: Pomůcky: Fyzika (FYZ) Molekulová fyzika, termika 2. ročník, sexta 2 hodiny týdně Fyzikální učebna vybavená audiovizuální technikou, interaktivní tabule, fyzikální pomůcky
Energie. Název sady DUM. Člověk a příroda. Vzdělávací oblast. Fyzika. Autor, datum vytvoření Mgr. Zbyněk Šostý, 2012. interaktivní tabule
 Název DUM: Skupenství látek Název sady DUM Číslo DUM Vzdělávací oblast Vzdělávací obor Energie VY_32_INOVACE_14_S1 12 Člověk a příroda Fyzika Ročník 8. Autor, datum vytvoření Mgr. Zbyněk Šostý, 2012 Doporučená
Název DUM: Skupenství látek Název sady DUM Číslo DUM Vzdělávací oblast Vzdělávací obor Energie VY_32_INOVACE_14_S1 12 Člověk a příroda Fyzika Ročník 8. Autor, datum vytvoření Mgr. Zbyněk Šostý, 2012 Doporučená
Tepelná vodivost. střední rychlost. T 1 > T 2 z. teplo přenesené za čas dt: T 1 T 2. tepelný tok střední volná dráha. součinitel tepelné vodivosti
 Tepelná vodivost teplo přenesené za čas dt: T 1 > T z T 1 S tepelný tok střední volná dráha T součinitel tepelné vodivosti střední rychlost Tepelná vodivost součinitel tepelné vodivosti při T = 300 K součinitel
Tepelná vodivost teplo přenesené za čas dt: T 1 > T z T 1 S tepelný tok střední volná dráha T součinitel tepelné vodivosti střední rychlost Tepelná vodivost součinitel tepelné vodivosti při T = 300 K součinitel
Půdní voda. *vyplňuje póry v půdách. *nevytváří souvislou hladinu. *je důležitá pro růst rostlin.
 PODPOVRCHOVÁ VODA Půdní voda *vyplňuje póry v půdách. *nevytváří souvislou hladinu. *je důležitá pro růst rostlin. Podzemní voda hromadí se na horninách, které jsou málo propustné pro vodu vytváří souvislou
PODPOVRCHOVÁ VODA Půdní voda *vyplňuje póry v půdách. *nevytváří souvislou hladinu. *je důležitá pro růst rostlin. Podzemní voda hromadí se na horninách, které jsou málo propustné pro vodu vytváří souvislou
Termika. Nauka o teple se zabývá měřením teploty, tepla a tepelnými ději.
 Termika Nauka o teple se zabývá měřením teploty, tepla a tepelnými ději. 1. Vnitřní energie Brownův pohyb a difúze látek prokazují, že částice látek jsou v neustálém neuspořádaném pohybu. Proto mají kinetickou
Termika Nauka o teple se zabývá měřením teploty, tepla a tepelnými ději. 1. Vnitřní energie Brownův pohyb a difúze látek prokazují, že částice látek jsou v neustálém neuspořádaném pohybu. Proto mají kinetickou
Termodynamika 2. UJOP Hostivař 2014
 Termodynamika 2 UJOP Hostivař 2014 Skupenské teplo tání/tuhnutí je (celkové) teplo, které přijme pevná látka při přechodu na kapalinu během tání nebo naopak Značka Veličina Lt J Nedochází při něm ke změně
Termodynamika 2 UJOP Hostivař 2014 Skupenské teplo tání/tuhnutí je (celkové) teplo, které přijme pevná látka při přechodu na kapalinu během tání nebo naopak Značka Veličina Lt J Nedochází při něm ke změně
CELKOVÉ OPAKOVÁNÍ UČIVA + ZÁPIS DO ŠKOLNÍHO SEŠITU část 03 VNITŘNÍ ENERGIE, TEPLO.
 CELKOVÉ OPAKOVÁNÍ UČIVA + ZÁPIS DO ŠKOLNÍHO SEŠITU část 03 VNITŘNÍ ENERGIE, TEPLO. 01) Složení látek opakování učiva 6. ročníku: Všechny látky jsou složeny z částic nepatrných rozměrů (tj. atomy, molekuly,
CELKOVÉ OPAKOVÁNÍ UČIVA + ZÁPIS DO ŠKOLNÍHO SEŠITU část 03 VNITŘNÍ ENERGIE, TEPLO. 01) Složení látek opakování učiva 6. ročníku: Všechny látky jsou složeny z částic nepatrných rozměrů (tj. atomy, molekuly,
Základem molekulové fyziky je kinetická teorie látek. Vychází ze tří pouček:
 Molekulová fyzika zkoumá vlastnosti látek na základě jejich vnitřní struktury, pohybu a vzájemného působení částic, ze kterých se látky skládají. Termodynamika se zabývá zákony přeměny různých forem energie
Molekulová fyzika zkoumá vlastnosti látek na základě jejich vnitřní struktury, pohybu a vzájemného působení částic, ze kterých se látky skládají. Termodynamika se zabývá zákony přeměny různých forem energie
Kapaliny Molekulové vdw síly, vodíkové můstky
 Kapaliny Molekulové vdw síly, vodíkové můstky Metalické roztavené kovy, ionty + elektrony, elektrostatické síly Iontové roztavené soli, FLINAK (LiF + NaF + KF), volně pohyblivé anionty a kationty, iontová
Kapaliny Molekulové vdw síly, vodíkové můstky Metalické roztavené kovy, ionty + elektrony, elektrostatické síly Iontové roztavené soli, FLINAK (LiF + NaF + KF), volně pohyblivé anionty a kationty, iontová
UČIVO. Termodynamická teplota. První termodynamický zákon Přenos vnitřní energie
 PŘEDMĚT: FYZIKA ROČNÍK: SEXTA VÝSTUP UČIVO MEZIPŘEDM. VZTAHY, PRŮŘEZOVÁ TÉMATA, PROJEKTY, KURZY POZNÁMKY Zná 3 základní poznatky kinetické teorie látek a vysvětlí jejich praktický význam Vysvětlí pojmy
PŘEDMĚT: FYZIKA ROČNÍK: SEXTA VÝSTUP UČIVO MEZIPŘEDM. VZTAHY, PRŮŘEZOVÁ TÉMATA, PROJEKTY, KURZY POZNÁMKY Zná 3 základní poznatky kinetické teorie látek a vysvětlí jejich praktický význam Vysvětlí pojmy
Fyzika - Sexta, 2. ročník
 - Sexta, 2. ročník Fyzika Výchovné a vzdělávací strategie Kompetence komunikativní Kompetence k řešení problémů Kompetence sociální a personální Kompetence občanská Kompetence k podnikavosti Kompetence
- Sexta, 2. ročník Fyzika Výchovné a vzdělávací strategie Kompetence komunikativní Kompetence k řešení problémů Kompetence sociální a personální Kompetence občanská Kompetence k podnikavosti Kompetence
IV. Fázové rovnováhy. 4. Fázové rovnováhy Ústav procesní a zpracovatelské techniky FS ČVUT v Praze
 IV. Fázové rovnováhy 1 4. Fázové rovnováhy 4.1 Základní pojmy 4.2 Fázové rovnováhy jednosložkové soustavy 4.3 Fázové rovnováhy dvousložkových soustav 4.3.1 Soustava tuhá složka tuhá složka 4.3.2 Soustava
IV. Fázové rovnováhy 1 4. Fázové rovnováhy 4.1 Základní pojmy 4.2 Fázové rovnováhy jednosložkové soustavy 4.3 Fázové rovnováhy dvousložkových soustav 4.3.1 Soustava tuhá složka tuhá složka 4.3.2 Soustava
PROCESY V TECHNICE BUDOV 8
 UNIVERZITA TOMÁŠE BATI VE ZLÍNĚ FAKULTA APLIKOVANÉ INFORMATIKY PROCESY V TECHNICE BUDOV 8 Dagmar Janáčová, Hana Charvátová Zlín 2013 Tento studijní materiál vznikl za finanční podpory Evropského sociálního
UNIVERZITA TOMÁŠE BATI VE ZLÍNĚ FAKULTA APLIKOVANÉ INFORMATIKY PROCESY V TECHNICE BUDOV 8 Dagmar Janáčová, Hana Charvátová Zlín 2013 Tento studijní materiál vznikl za finanční podpory Evropského sociálního
4IS09F8 změna skupenství.notebook. Registrační číslo projektu: CZ.1.07/1.4.00/21.3075. Šablona: III/2. Sada: VY_32_INOVACE_4IS Pořadové číslo: 09
 Registrační číslo projektu: CZ.1.07/1.4.00/21.3075 Šablona: III/2 Sada: VY_32_INOVACE_4IS Pořadové číslo: 09 Ověření ve výuce Třída: 8.A Datum: 20.2.2013 1 Změna skupenství Předmět: Fyzika Ročník: 8. ročník
Registrační číslo projektu: CZ.1.07/1.4.00/21.3075 Šablona: III/2 Sada: VY_32_INOVACE_4IS Pořadové číslo: 09 Ověření ve výuce Třída: 8.A Datum: 20.2.2013 1 Změna skupenství Předmět: Fyzika Ročník: 8. ročník
EU peníze středním školám digitální učební materiál
 EU peníze středním školám digitální učební materiál Číslo projektu: Číslo a název šablony klíčové aktivity: Tematická oblast, název DUMu: Autor: CZ.1.07/1.5.00/34.0515 III/2 Inovace a zkvalitnění výuky
EU peníze středním školám digitální učební materiál Číslo projektu: Číslo a název šablony klíčové aktivity: Tematická oblast, název DUMu: Autor: CZ.1.07/1.5.00/34.0515 III/2 Inovace a zkvalitnění výuky
Ch - Rozlišování látek
 Ch - Rozlišování látek Autor: Mgr. Jaromír JUŘEK Kopírování a jakékoliv další využití výukového materiálu je povoleno pouze s uvedením odkazu na www.jarjurek.cz. VARIACE 1 Tento dokument byl kompletně
Ch - Rozlišování látek Autor: Mgr. Jaromír JUŘEK Kopírování a jakékoliv další využití výukového materiálu je povoleno pouze s uvedením odkazu na www.jarjurek.cz. VARIACE 1 Tento dokument byl kompletně
III. STRUKTURA A VLASTNOSTI PLYNŮ
 III. STRUKTURA A VLASTNOSTI PLYNŮ 3.1 Ideální plyn a) ideální plyn model, předpoklady: 1. rozměry molekul malé (ve srovnání se střední vzdáleností molekul). molekuly na sebe navzálem silově nepůsobí (mimo
III. STRUKTURA A VLASTNOSTI PLYNŮ 3.1 Ideální plyn a) ideální plyn model, předpoklady: 1. rozměry molekul malé (ve srovnání se střední vzdáleností molekul). molekuly na sebe navzálem silově nepůsobí (mimo
2.6.7 Fázový diagram. Předpoklady: Popiš děje zakreslené v diagramu křivky syté páry. Za jakých podmínek mohou proběhnout?
 2.6.7 Fázový diagram Předoklady: 2606 Př. 1: Poiš děje zakreslené v diagramu křivky syté áry. Za jakých odmínek mohou roběhnout? 4 2 1 3 1) Sytá ára je za stálého tlaku zahřívána. Zvětšuje svůj objem a
2.6.7 Fázový diagram Předoklady: 2606 Př. 1: Poiš děje zakreslené v diagramu křivky syté áry. Za jakých odmínek mohou roběhnout? 4 2 1 3 1) Sytá ára je za stálého tlaku zahřívána. Zvětšuje svůj objem a
Skupenské stavy látek. Mezimolekulární síly
 Skupenské stavy látek Mezimolekulární síly 1 Interakce iont-dipól Např. hydratační (solvatační) interakce mezi Na + (iont) a molekulou vody (dipól). Jde o nejsilnější mezimolekulární (nevazebnou) interakci.
Skupenské stavy látek Mezimolekulární síly 1 Interakce iont-dipól Např. hydratační (solvatační) interakce mezi Na + (iont) a molekulou vody (dipól). Jde o nejsilnější mezimolekulární (nevazebnou) interakci.
ZÁKLADNÍ ŠKOLA KOLÍN II., KMOCHOVA 943 škola s rozšířenou výukou matematiky a přírodovědných předmětů
 ZÁKLADNÍ ŠKOLA KOLÍN II., KMOCHOVA 943 škola s rozšířenou výukou matematiky a přírodovědných předmětů Autor Číslo materiálu Mgr. Vladimír Hradecký 8_F_1_13 Datum vytvoření 2. 11. 2011 Druh učebního materiálu
ZÁKLADNÍ ŠKOLA KOLÍN II., KMOCHOVA 943 škola s rozšířenou výukou matematiky a přírodovědných předmětů Autor Číslo materiálu Mgr. Vladimír Hradecký 8_F_1_13 Datum vytvoření 2. 11. 2011 Druh učebního materiálu
MOLEKULOVÁ FYZIKA A TERMODYNAMIKA
 MOLEKULOVÁ FYZIKA A TERMODYNAMIKA 2 metody zkoumání látek na základě vnějších projevů: I. KINETICKÁ TEORIE LÁTEK -studium vlastností látek na základě vnitřní struktury, pohybu a vzájemného působení jednotlivých
MOLEKULOVÁ FYZIKA A TERMODYNAMIKA 2 metody zkoumání látek na základě vnějších projevů: I. KINETICKÁ TEORIE LÁTEK -studium vlastností látek na základě vnitřní struktury, pohybu a vzájemného působení jednotlivých
Vnitřní energie, teplo a práce
 Přednáška 3 Vnitřní energie, teplo a práce 3.1 Vnitřní energie Pro popis stavu termodynamických soustav je výhodné zavést stavovou funkci, tzv. vnitřní energii soustavy U, která vyjadřuje charakter pohybu
Přednáška 3 Vnitřní energie, teplo a práce 3.1 Vnitřní energie Pro popis stavu termodynamických soustav je výhodné zavést stavovou funkci, tzv. vnitřní energii soustavy U, která vyjadřuje charakter pohybu
Chemická kinetika. Reakce 1. řádu rychlost přímo úměrná koncentraci složky
 Chemická kinetika Chemická kinetika Reakce 0. řádu reakční rychlost nezávisí na čase a probíhá konstantní rychlostí v = k (rychlost se rovná rychlostní konstantě) velmi pomalé reakce (prakticky se nemění
Chemická kinetika Chemická kinetika Reakce 0. řádu reakční rychlost nezávisí na čase a probíhá konstantní rychlostí v = k (rychlost se rovná rychlostní konstantě) velmi pomalé reakce (prakticky se nemění
Příklady k zápočtu molekulová fyzika a termodynamika
 Příklady k zápočtu molekulová fyzika a termodynamika 1. Do vody o teplotě t 1 70 C a hmotnosti m 1 1 kg vhodíme kostku ledu o teplotě t 2 10 C a hmotnosti m 2 2 kg. Do soustavy vzápětí přilijeme další
Příklady k zápočtu molekulová fyzika a termodynamika 1. Do vody o teplotě t 1 70 C a hmotnosti m 1 1 kg vhodíme kostku ledu o teplotě t 2 10 C a hmotnosti m 2 2 kg. Do soustavy vzápětí přilijeme další
VÝUKOVÝ MATERIÁL Ing. Yvona Bečičková Tematická oblast. Termika Číslo a název materiálu VY_32_INOVACE_0301_0220 Anotace
 VÝUKOVÝ MATERIÁL Identifikační údaje školy Vyšší odborná škola a Střední škola, Varnsdorf, příspěvková organizace Bratislavská 2166, 407 47 Varnsdorf, IČO: 18383874 www.vosassvdf.cz, tel. +420412372632
VÝUKOVÝ MATERIÁL Identifikační údaje školy Vyšší odborná škola a Střední škola, Varnsdorf, příspěvková organizace Bratislavská 2166, 407 47 Varnsdorf, IČO: 18383874 www.vosassvdf.cz, tel. +420412372632
Molekulová fyzika a termika:
 Molekulová fyzika a termika: 1. Měření teploty: 2. Délková roztažnost a Objemová roztažnost látek 3. Bimetal 4. Anomálie vody 5. Částicová stavba látek, vlastnosti látek 6. Atomová hmotnostní konstanta
Molekulová fyzika a termika: 1. Měření teploty: 2. Délková roztažnost a Objemová roztažnost látek 3. Bimetal 4. Anomálie vody 5. Částicová stavba látek, vlastnosti látek 6. Atomová hmotnostní konstanta
Termomechanika 8. přednáška Doc. Dr. RNDr. Miroslav Holeček
 Termomechanika 8. přednáška Doc. Dr. RNDr. Miroslav Holeček Upozornění: Tato prezentace slouží výhradně pro výukové účely Fakulty strojní Západočeské univerzity v Plzni. Byla sestavena autorem s využitím
Termomechanika 8. přednáška Doc. Dr. RNDr. Miroslav Holeček Upozornění: Tato prezentace slouží výhradně pro výukové účely Fakulty strojní Západočeské univerzity v Plzni. Byla sestavena autorem s využitím
Nauka o materiálu. Přednáška č.10 Difuze v tuhých látkách, fáze a fázové přeměny
 Nauka o materiálu Přednáška č.10 Difuze v tuhých látkách, fáze a fázové přeměny Difuze v tuhých látkách Difuzí nazýváme přesun atomů nebo iontů na vzdálenost větší než je meziatomová vzdálenost. Hnací
Nauka o materiálu Přednáška č.10 Difuze v tuhých látkách, fáze a fázové přeměny Difuze v tuhých látkách Difuzí nazýváme přesun atomů nebo iontů na vzdálenost větší než je meziatomová vzdálenost. Hnací
Vnitřní energie. Teplo. Tepelná výměna.
 Vnitřní energie. Teplo. Tepelná výměna. A) Výklad: Vnitřní energie vnitřní energie označuje součet celkové kinetické energie částic (tj. rotační + vibrační + translační energie) a celkové polohové energie
Vnitřní energie. Teplo. Tepelná výměna. A) Výklad: Vnitřní energie vnitřní energie označuje součet celkové kinetické energie částic (tj. rotační + vibrační + translační energie) a celkové polohové energie
Kapaliny Molekulové vdw síly, vodíkové můstky
 Kapaliny Molekulové vdw síly, vodíkové můstky Metalické roztavené kovy, ionty + elektrony, elektrostatické síly Iontové roztavené soli, FLINAK (LiF + NaF + KF), volně pohyblivé anionty a kationty, iontová
Kapaliny Molekulové vdw síly, vodíkové můstky Metalické roztavené kovy, ionty + elektrony, elektrostatické síly Iontové roztavené soli, FLINAK (LiF + NaF + KF), volně pohyblivé anionty a kationty, iontová
Termodynamika. T [K ]=t [ 0 C] 273,15 T [ K ]= t [ 0 C] termodynamická teplota: Stavy hmoty. jednotka: 1 K (kelvin) = 1/273,16 část termodynamické
![Termodynamika. T [K ]=t [ 0 C] 273,15 T [ K ]= t [ 0 C] termodynamická teplota: Stavy hmoty. jednotka: 1 K (kelvin) = 1/273,16 část termodynamické Termodynamika. T [K ]=t [ 0 C] 273,15 T [ K ]= t [ 0 C] termodynamická teplota: Stavy hmoty. jednotka: 1 K (kelvin) = 1/273,16 část termodynamické](/thumbs/24/2778201.jpg) Termodynamika termodynamická teplota: Stavy hmoty jednotka: 1 K (kelvin) = 1/273,16 část termodynamické teploty trojného bodu vody (273,16 K = 0,01 o C). 0 o C = 273,15 K T [K ]=t [ 0 C] 273,15 T [ K ]=
Termodynamika termodynamická teplota: Stavy hmoty jednotka: 1 K (kelvin) = 1/273,16 část termodynamické teploty trojného bodu vody (273,16 K = 0,01 o C). 0 o C = 273,15 K T [K ]=t [ 0 C] 273,15 T [ K ]=
Přehled otázek z fyziky pro 2.ročník
 Přehled otázek z fyziky pro 2.ročník 1. Z jakých základních poznatků vychází teorie látek + důkazy. a) Látka kteréhokoli skupenství se skládá z částic molekul, atomů, iontů. b) Částice se v látce pohybují,
Přehled otázek z fyziky pro 2.ročník 1. Z jakých základních poznatků vychází teorie látek + důkazy. a) Látka kteréhokoli skupenství se skládá z částic molekul, atomů, iontů. b) Částice se v látce pohybují,
Kapaliny Molekulové vdw síly, vodíkové můstky
 Kapaliny Molekulové vdw síly, vodíkové můstky Metalické roztavené kovy, ionty + elektrony, elektrostatické síly Iontové roztavené soli, FLINAK (LiF + NaF + KF), volně pohyblivé anionty a kationty, iontová
Kapaliny Molekulové vdw síly, vodíkové můstky Metalické roztavené kovy, ionty + elektrony, elektrostatické síly Iontové roztavené soli, FLINAK (LiF + NaF + KF), volně pohyblivé anionty a kationty, iontová
Krása fázových diagramů jak je sestrojit a číst Silvie Mašková
 Krása fázových diagramů jak je sestrojit a číst Silvie Mašková Katedra fyziky kondenzovaných látek Matematicko-fyzikální fakulta Univerzita Karlova Praha Pár základích pojmů na začátek Co jsou fázové diagramy?
Krása fázových diagramů jak je sestrojit a číst Silvie Mašková Katedra fyziky kondenzovaných látek Matematicko-fyzikální fakulta Univerzita Karlova Praha Pár základích pojmů na začátek Co jsou fázové diagramy?
Vlastnosti kapalin. Povrchová vrstva kapaliny
 Struktura a vlastnosti kapalin Vlastnosti kapalin, Povrchová vrstva kapaliny Jevy na rozhraní pevného tělesa a kapaliny Kapilární jevy, Teplotní objemová roztažnost Vlastnosti kapalin Kapalina - tvoří
Struktura a vlastnosti kapalin Vlastnosti kapalin, Povrchová vrstva kapaliny Jevy na rozhraní pevného tělesa a kapaliny Kapilární jevy, Teplotní objemová roztažnost Vlastnosti kapalin Kapalina - tvoří
Fyzika, maturitní okruhy (profilová část), školní rok 2014/2015 Gymnázium INTEGRA BRNO
 1. Jednotky a veličiny soustava SI odvozené jednotky násobky a díly jednotek skalární a vektorové fyzikální veličiny rozměrová analýza 2. Kinematika hmotného bodu základní pojmy kinematiky hmotného bodu
1. Jednotky a veličiny soustava SI odvozené jednotky násobky a díly jednotek skalární a vektorové fyzikální veličiny rozměrová analýza 2. Kinematika hmotného bodu základní pojmy kinematiky hmotného bodu
d T FP = fázový přechod (tání, tuhnutí, vypařování, kapalnění, sublimace)
 Fázové rovnováhy jednoložkový ytém Gibbův fázový zákon k f C Popi záviloti tlaku naycených par na teploě Clapeyronova rovnice: d p F P m n e b o F P d l np F P m F P z FP fázový přechod (tání, tuhnutí,
Fázové rovnováhy jednoložkový ytém Gibbův fázový zákon k f C Popi záviloti tlaku naycených par na teploě Clapeyronova rovnice: d p F P m n e b o F P d l np F P m F P z FP fázový přechod (tání, tuhnutí,
VNITŘNÍ ENERGIE. Mgr. Jan Ptáčník - GJVJ - Fyzika - 2. ročník - Termika
 VNITŘNÍ ENERGIE Mgr. Jan Ptáčník - GJVJ - Fyzika - 2. ročník - Termika Zákon zachování energie Ze zákona zachování mechanické energie platí: Ek + Ep = konst. Ale: Vnitřní energie tělesa Každé těleso má
VNITŘNÍ ENERGIE Mgr. Jan Ptáčník - GJVJ - Fyzika - 2. ročník - Termika Zákon zachování energie Ze zákona zachování mechanické energie platí: Ek + Ep = konst. Ale: Vnitřní energie tělesa Každé těleso má
Názvosloví Kvalita Výroba Kondenzace Teplosměnná plocha
 Názvosloví Kvalita Výroba Kondenzace Teplosměnná plocha Názvosloví páry Pro správné pochopení funkce parních systémů musíme znát základní pojmy spojené s párou. Entalpie Celková energie, příslušná danému
Názvosloví Kvalita Výroba Kondenzace Teplosměnná plocha Názvosloví páry Pro správné pochopení funkce parních systémů musíme znát základní pojmy spojené s párou. Entalpie Celková energie, příslušná danému
13 otázek za 1 bod = 13 bodů Jméno a příjmení:
 13 otázek za 1 bod = 13 bodů Jméno a příjmení: 4 otázky za 2 body = 8 bodů Datum: 1 příklad za 3 body = 3 body Body: 1 příklad za 6 bodů = 6 bodů Celkem: 30 bodů příklady: 1) Sportovní vůz je schopný zrychlit
13 otázek za 1 bod = 13 bodů Jméno a příjmení: 4 otázky za 2 body = 8 bodů Datum: 1 příklad za 3 body = 3 body Body: 1 příklad za 6 bodů = 6 bodů Celkem: 30 bodů příklady: 1) Sportovní vůz je schopný zrychlit
Fyzikální vzdělávání. 1. ročník. Učební obor: Kuchař číšník Kadeřník. Implementace ICT do výuky č. CZ.1.07/1.1.02/02.0012 GG OP VK
 Fyzikální vzdělávání 1. ročník Učební obor: Kuchař číšník Kadeřník 1 2 Termika 2.1Teplota, teplotní roztažnost látek 2.2 Teplo a práce, přeměny vnitřní energie tělesa 2.3 Tepelné motory 2.4 Struktura pevných
Fyzikální vzdělávání 1. ročník Učební obor: Kuchař číšník Kadeřník 1 2 Termika 2.1Teplota, teplotní roztažnost látek 2.2 Teplo a práce, přeměny vnitřní energie tělesa 2.3 Tepelné motory 2.4 Struktura pevných
Termodynamika 1. UJOP Hostivař 2014
 Termodynamika 1 UJOP Hostivař 2014 Termodynamika Zabývá se tepelnými ději obecně. Existují 3 termodynamické zákony: 1. Celkové množství energie (všech druhů) izolované soustavy zůstává zachováno. 2. Teplo
Termodynamika 1 UJOP Hostivař 2014 Termodynamika Zabývá se tepelnými ději obecně. Existují 3 termodynamické zákony: 1. Celkové množství energie (všech druhů) izolované soustavy zůstává zachováno. 2. Teplo
Test vlastnosti látek a periodická tabulka
 DUM Základy přírodních věd DUM III/2-T3-2-08 Téma: Test vlastnosti látek a periodická tabulka Střední škola Rok: 2012 2013 Varianta: A Zpracoval: Mgr. Pavel Hrubý Mgr. Josef Kormaník TEST Test vlastnosti
DUM Základy přírodních věd DUM III/2-T3-2-08 Téma: Test vlastnosti látek a periodická tabulka Střední škola Rok: 2012 2013 Varianta: A Zpracoval: Mgr. Pavel Hrubý Mgr. Josef Kormaník TEST Test vlastnosti
Struktura a vlastnosti kapalin
 Struktura a vlastnosti kapalin (test version, not revised) Petr Pošta pposta@karlin.mff.cuni.cz 24. listopadu 2010 Obsah Povrchová vrstva Jevy na rozhraní Kapilární tlak Kapilární jevy Objemová roztažnost
Struktura a vlastnosti kapalin (test version, not revised) Petr Pošta pposta@karlin.mff.cuni.cz 24. listopadu 2010 Obsah Povrchová vrstva Jevy na rozhraní Kapilární tlak Kapilární jevy Objemová roztažnost
3.5 Tepelné děje s ideálním plynem stálé hmotnosti, izotermický děj
 3.5 Tepelné děje s ideálním plynem stálé hmotnosti, izotermický děj a) tepelný děj přechod plynu ze stavu 1 do stavu tepelnou výměnou nebo konáním práce dále uvaž., že hmotnost plynu m = konst. a navíc
3.5 Tepelné děje s ideálním plynem stálé hmotnosti, izotermický děj a) tepelný děj přechod plynu ze stavu 1 do stavu tepelnou výměnou nebo konáním práce dále uvaž., že hmotnost plynu m = konst. a navíc
Zmena skupenstva látok
 1. Keď má sústava v rovnovážnom stave vo vrtkých častiach rovnaké fyzikálne a chemické vlastnosti, napr. rovnakú hustotu, štruktúru, rovnaké chemické zloženie, nazýva sa fáza. Prechod látky z jednej fázy
1. Keď má sústava v rovnovážnom stave vo vrtkých častiach rovnaké fyzikálne a chemické vlastnosti, napr. rovnakú hustotu, štruktúru, rovnaké chemické zloženie, nazýva sa fáza. Prechod látky z jednej fázy
Fázové změny. Manuál k programu
 Fázové změny Manuál k programu Jiří Mazurek 2009 OBSAH Úvod... 3 1 O programu... 3 2 Kapitoly programu... 4 2.1 Jak pracovat s programem... 4 2.2 Úvodní kapitola... 5 2.3 Tání... 7 2.4 Tuhnutí... 11 2.5
Fázové změny Manuál k programu Jiří Mazurek 2009 OBSAH Úvod... 3 1 O programu... 3 2 Kapitoly programu... 4 2.1 Jak pracovat s programem... 4 2.2 Úvodní kapitola... 5 2.3 Tání... 7 2.4 Tuhnutí... 11 2.5
Práce, výkon, energie
 Práce, výkon, energie (test version, not revised) Petr Pošta pposta@karlin.mff.cuni.cz 23. října 2009 Obsah Mechanická práce Výkon, příkon, účinnost Mechanická energie Kinetická energie Potenciální energie
Práce, výkon, energie (test version, not revised) Petr Pošta pposta@karlin.mff.cuni.cz 23. října 2009 Obsah Mechanická práce Výkon, příkon, účinnost Mechanická energie Kinetická energie Potenciální energie
ČÍSLO PROJEKTU: OPVK 1.4
 NÁZEV ŠKOLY: Základní škola Javorník, okres Jeseník REDIZO: 600 150 585 NÁZEV: VY_32_INOVACE_185_Skupenství AUTOR: Ing. Gavlas Miroslav ROČNÍK, DATUM: 8., 16.11.2011 VZDĚL. OBOR, TÉMA: Fyzika, ČÍSLO PROJEKTU:
NÁZEV ŠKOLY: Základní škola Javorník, okres Jeseník REDIZO: 600 150 585 NÁZEV: VY_32_INOVACE_185_Skupenství AUTOR: Ing. Gavlas Miroslav ROČNÍK, DATUM: 8., 16.11.2011 VZDĚL. OBOR, TÉMA: Fyzika, ČÍSLO PROJEKTU:
Fázové heterogenní rovnováhy Fáze = homogenní část soustavy, oddělná fyzickým rozhraním, na rozhraní se vlastnosti mění skokem
 Fázové heterogenní rovnováhy Fáze = homogenní část soustavy, oddělná fyzickým rozhraním, na rozhraní se vlastnosti mění skokem Rovnováha Tepelná - T všude stejná Mechanická - p všude stejný Chemická -
Fázové heterogenní rovnováhy Fáze = homogenní část soustavy, oddělná fyzickým rozhraním, na rozhraní se vlastnosti mění skokem Rovnováha Tepelná - T všude stejná Mechanická - p všude stejný Chemická -
Kinetická teorie ideálního plynu
 Přednáška 10 Kinetická teorie ideálního plynu 10.1 Postuláty kinetické teorie Narozdíl od termodynamiky kinetická teorie odvozuje makroskopické vlastnosti látek (např. tlak, teplotu, vnitřní energii) na
Přednáška 10 Kinetická teorie ideálního plynu 10.1 Postuláty kinetické teorie Narozdíl od termodynamiky kinetická teorie odvozuje makroskopické vlastnosti látek (např. tlak, teplotu, vnitřní energii) na
2.6.4 Kapalnění, sublimace, desublimace
 264 Kapalnění, sublimace, desublimace Předpoklady: 2603 Kapalnění (kondenzace) Snižování eploy páry pára se mění v kapalinu Kde dochází ke kondenzaci? na povrchu kapaliny, na povrchu pevné láky (orosení
264 Kapalnění, sublimace, desublimace Předpoklady: 2603 Kapalnění (kondenzace) Snižování eploy páry pára se mění v kapalinu Kde dochází ke kondenzaci? na povrchu kapaliny, na povrchu pevné láky (orosení
Změna skupenství Zhotoveno ve školním roce: 2011/2012 Jméno zhotovitele: Ing. Iva Procházková
 Název a adresa školy: Střední škola průmyslová a uměleká Opava příspěvková organizae Praskova 399/8 Opava 7460 Název operačního programu: OP Vzdělávání pro konkureneshopnost oblast podpory.5 Registrační
Název a adresa školy: Střední škola průmyslová a uměleká Opava příspěvková organizae Praskova 399/8 Opava 7460 Název operačního programu: OP Vzdělávání pro konkureneshopnost oblast podpory.5 Registrační
EU PENÍZE ŠKOLÁM Operační program Vzdělávání pro konkurenceschopnost
 ZÁKLADNÍ ŠKOLA OLOMOUC příspěvková organizace MOZARTOVA 48, 779 00 OLOMOUC tel.: 585 427 142, 775 116 442; fax: 585 422 713 e-mail: kundrum@centrum.cz; www.zs-mozartova.cz Projekt: ŠKOLA RADOSTI, ŠKOLA
ZÁKLADNÍ ŠKOLA OLOMOUC příspěvková organizace MOZARTOVA 48, 779 00 OLOMOUC tel.: 585 427 142, 775 116 442; fax: 585 422 713 e-mail: kundrum@centrum.cz; www.zs-mozartova.cz Projekt: ŠKOLA RADOSTI, ŠKOLA
Vnitřní energie, práce, teplo.
 Vnitřní energie, práce, teplo. Vnitřní energie tělesa Částice uvnitř látek mají kinetickou a potenciální energii. Je to energie uvnitř tělesa, proto ji nazýváme vnitřní energie. Značíme ji písmenkem U
Vnitřní energie, práce, teplo. Vnitřní energie tělesa Částice uvnitř látek mají kinetickou a potenciální energii. Je to energie uvnitř tělesa, proto ji nazýváme vnitřní energie. Značíme ji písmenkem U
LOGO. Molekulová fyzika
 Molekulová fyzika Molekulová fyzika Molekulová fyzika vysvětluje fyzikální jevy na základě znalosti jejich částicové struktury. Jejím základem je kinetická teorie látek (KTL). KTL obsahuje tři tvrzení:
Molekulová fyzika Molekulová fyzika Molekulová fyzika vysvětluje fyzikální jevy na základě znalosti jejich částicové struktury. Jejím základem je kinetická teorie látek (KTL). KTL obsahuje tři tvrzení:
1. Molekulová stavba kapalin
 1 Molekulová stavba kapalin 11 Vznik kapaliny kondenzací Plyn Vyjdeme z plynu Plyn je soustava molekul pohybujících se neuspořádaně všemi směry Pohybová energie molekul převládá nad energii polohovou Každá
1 Molekulová stavba kapalin 11 Vznik kapaliny kondenzací Plyn Vyjdeme z plynu Plyn je soustava molekul pohybujících se neuspořádaně všemi směry Pohybová energie molekul převládá nad energii polohovou Každá
Měření teplotní roztažnosti
 KATEDRA EXPERIMENTÁLNÍ FYZIKY PŘÍRODOVĚDECKÁ FAKULTA UNIVERZITY PALACKÉHO V OLOMOUCI FYZIKÁLNÍ PRAKTIKUM Z MOLEKULOVÉ FYZIKY A TERMODYNAMIKY Měření teplotní roztažnosti Úvod Zvyšování termodynamické teploty
KATEDRA EXPERIMENTÁLNÍ FYZIKY PŘÍRODOVĚDECKÁ FAKULTA UNIVERZITY PALACKÉHO V OLOMOUCI FYZIKÁLNÍ PRAKTIKUM Z MOLEKULOVÉ FYZIKY A TERMODYNAMIKY Měření teplotní roztažnosti Úvod Zvyšování termodynamické teploty
Základní poznatky. Teplota Vnitřní energie soustavy Teplo
 Molekulová fyzika a termika Základní poznatky Základní poznatky Teplota Vnitřní energie soustavy Teplo Termika = část fyziky zabývající se studiem vlastností látek a jejich změn souvisejících s teplotou
Molekulová fyzika a termika Základní poznatky Základní poznatky Teplota Vnitřní energie soustavy Teplo Termika = část fyziky zabývající se studiem vlastností látek a jejich změn souvisejících s teplotou
KAPALINY. Mgr. Jan Ptáčník - GJVJ - Fyzika - Termika - 2. ročník
 KAPALINY Mgr. Jan Ptáčník - GJVJ - Fyzika - Termika - 2. ročník Kapaliny Krátkodosahové uspořádání molekul. Molekuly kmitají okolo rovnovážných poloh. Při zvýšení teploty se zmenšuje doba setrvání v rovnovážné
KAPALINY Mgr. Jan Ptáčník - GJVJ - Fyzika - Termika - 2. ročník Kapaliny Krátkodosahové uspořádání molekul. Molekuly kmitají okolo rovnovážných poloh. Při zvýšení teploty se zmenšuje doba setrvání v rovnovážné
6. Jaký je výkon vařiče, který ohřeje 1 l vody o 40 C během 5 minut? Měrná tepelná kapacita vody je W)
 TEPLO 1. Na udržení stále teploty v místnosti se za hodinu spotřebuje 4,2 10 6 J tepla. olik vody proteče radiátorem ústředního topení za hodinu, jestliže má voda při vstupu do radiátoru teplotu 80 ºC
TEPLO 1. Na udržení stále teploty v místnosti se za hodinu spotřebuje 4,2 10 6 J tepla. olik vody proteče radiátorem ústředního topení za hodinu, jestliže má voda při vstupu do radiátoru teplotu 80 ºC
IDEÁLNÍ PLYN. Stavová rovnice
 IDEÁLNÍ PLYN Stavová rovnice Ideální plyn ) rozměry molekul jsou zanedbatelné vzhledem k jejich vzdálenostem 2) molekuly plynu na sebe působí jen při vzájemných srážkách 3) všechny srážky jsou dokonale
IDEÁLNÍ PLYN Stavová rovnice Ideální plyn ) rozměry molekul jsou zanedbatelné vzhledem k jejich vzdálenostem 2) molekuly plynu na sebe působí jen při vzájemných srážkách 3) všechny srážky jsou dokonale
Fyzikální chemie. Magda Škvorová KFCH CN463 magda.skvorova@ujep.cz, tel. 3302. 14. února 2013
 Fyzikální chemie Magda Škvorová KFCH CN463 magda.skvorova@ujep.cz, tel. 3302 14. února 2013 Co je fyzikální chemie? Co je fyzikální chemie? makroskopický přístup: (klasická) termodynamika nerovnovážná
Fyzikální chemie Magda Škvorová KFCH CN463 magda.skvorova@ujep.cz, tel. 3302 14. února 2013 Co je fyzikální chemie? Co je fyzikální chemie? makroskopický přístup: (klasická) termodynamika nerovnovážná
Pomůcky, které poskytuje sbírka fyziky, a audiovizuální technika v učebně fyziky, interaktivní tabule a i-učebnice
 Předmět: Náplň: Třída: Počet hodin: Pomůcky: Fyzika (FYZ) Práce a energie, tepelné jevy, elektrický proud, zvukové jevy Tercie 1+1 hodina týdně Pomůcky, které poskytuje sbírka fyziky, a audiovizuální technika
Předmět: Náplň: Třída: Počet hodin: Pomůcky: Fyzika (FYZ) Práce a energie, tepelné jevy, elektrický proud, zvukové jevy Tercie 1+1 hodina týdně Pomůcky, které poskytuje sbírka fyziky, a audiovizuální technika
Chemie. Mgr. Petra Drápelová Mgr. Jaroslava Vrbková. Gymnázium, SOŠ a VOŠ Ledeč nad Sázavou
 Chemie Mgr. Petra Drápelová Mgr. Jaroslava Vrbková Gymnázium, SOŠ a VOŠ Ledeč nad Sázavou Složení látek VY_32_INOVACE_03_3_02_CH Gymnázium, SOŠ a VOŠ Ledeč nad Sázavou SLOŽENÍ LÁTEK Fyzikálním kritériem
Chemie Mgr. Petra Drápelová Mgr. Jaroslava Vrbková Gymnázium, SOŠ a VOŠ Ledeč nad Sázavou Složení látek VY_32_INOVACE_03_3_02_CH Gymnázium, SOŠ a VOŠ Ledeč nad Sázavou SLOŽENÍ LÁTEK Fyzikálním kritériem
Vnitřní energie, práce a teplo
 Vnitřní energie, práce a teplo Zákon zachování mechanické energie V izolované soustavě těles je v každém okamžiku úhrnná mechanická energie stálá. Mění se navzájem jen potenciální energie E p a kinetická
Vnitřní energie, práce a teplo Zákon zachování mechanické energie V izolované soustavě těles je v každém okamžiku úhrnná mechanická energie stálá. Mění se navzájem jen potenciální energie E p a kinetická
9. Struktura a vlastnosti plynů
 9. Struktura a vlastnosti plynů Osnova: 1. Základní pojmy 2. Střední kvadratická rychlost 3. Střední kinetická energie molekuly plynu 4. Stavová rovnice ideálního plynu 5. Jednoduché děje v plynech a)
9. Struktura a vlastnosti plynů Osnova: 1. Základní pojmy 2. Střední kvadratická rychlost 3. Střední kinetická energie molekuly plynu 4. Stavová rovnice ideálního plynu 5. Jednoduché děje v plynech a)
