LABORATORNÍ ÚLOHY Z POLYMERNÍ CHEMIE PRO STŘEDOŠKOLSKÉ STUDENTY
|
|
|
- Milada Ludmila Jandová
- před 9 lety
- Počet zobrazení:
Transkript
1 LABORATORNÍ ÚLOHY Z POLYMERNÍ CHEMIE PRO STŘEDOŠKOLSKÉ STUDENTY 1. RADIKÁLOVÁ POLYMERACE STYRENU V BLOKU 2. EMULZNÍ POLYMERACE STYRENU 3. STANOVENÍ HODNOTY ZMÝDELNĚNÍ POLYVINYLACETÁTU 4. CHEMICKÁ RECYKLACE PLEXISKLA 5. ANIONTOVÁ POLYMERACE KYANOAKRYLÁTŮ 6. STANOVENÍ ZMĚKČOVADLA V PVC 7. VYTVRZOVÁNÍ EPOXIDOVÉ PRYSKYŘICE LABORATORNÍ ÚLOHY Z POLYMERNÍ CHEMIE PRO STŘEDOŠKOLSKÉ STUDENTY, jejichž autory jsou Jan Merna, Zdeněk Hošťálek, Robert Mundil a Pavla Doubravová podléhají licenci Creative Commons Attribution- NonCommercial-NoDerivs 3.0 Unported License
2 RADIKÁLOVÁ POLYMERACE STYRENU V BLOKU Úvod: Technicky nejjednodušší metodou pro přípravu polymerů je tzv. bloková polymerace neboli polymerace v monomerní fázi. Polymerační násada je tvořena pouze monomerem a iniciátorem. Získaný polymer je proto velice čistý. Nevýhodou blokové polymerace je však značný nárůst viskozity reakční směsi a s tím spojené problémy s odvodem tepla. V úloze proto polymeraci povedeme pouze do nízké konverze monomeru na polymer. Cílem úlohy je provedení blokové polymerace styrenu pomocí radikálového mechanismu. Iniciační radikály poskytne tepelným rozkladem labilní azosloučenina azo-bis-isobutyronitril: teplo 2 N 2 ABIN iniciující radikály Radikály reagují s molekulami styrenu a radikál se vždy přesouvá na konec rostoucího řetězce (propagace), zbytek molekuly iniciátoru zůstane zabudovaný v molekule polymeru: n+1 Ukončení (terminace) reakce může proběhnout několika způsoby, jedním z nich je rekombinace vysoce reaktivních radikálů na koncích dvou rostoucích řetězců: q=m+n+2 Pomůcky a chemikálie: Zkumavka ml s gumovou zátkou, kádinka 250 ml, vodní lázeň, magnetická míchačka, špachtle, stříkačka 5 ml Azo-bis-isobutyronitril (ABIN), styren (stabilizovaný), ethanol technický (denaturovaný), toluen Bezpečnost Styren je toxická látka. Při práci s ním pracujte čistě, v případě ukápnutí styren ihned setřete buničinou a nechte odvětrat v digestoři. Po celou dobu pobytu v laboratoři používejte ochranné brýle. Pracovní postup: 1. Do zkumavky navážíme přibližně přesně 15 mg iniciátoru ABIN.
3 2. Podle naváženého množství ABIN přidáme takové množství styrenu, aby výsledná koncentrace iniciátoru byla 0,4 hm. %. (Máme-li možnost, probubláme po dobu 5 min reakční násadu dusíkem.) 3. Zkumavku uzavřeme gumovou zátkou (vzduch polymeraci zastavuje) a vložíme do lázně vyhřáté na C a ponecháme polymerovat 30 min. 4. Pro ukončení polymerace zkumavku ochladíme pod tekoucí vodou. 5. Polymer vysrážíme (nejlépe v digestoři) vlitím obsahu zkumavky do kádinky se 100 ml míchaného denaturovaného ethanolu. Po vysrážení mícháme směs ještě dalších 10 min, aby nezreagovaný monomer vydifundoval z polystyrenových částeček. 6. Polymer odfiltrujeme na hladkém filtru nebo Büchnerově nálevce, filtrační koláč promyjeme ethanolem. 7. Necháme polymer volně vysušit přes noc (do příštích laboratoří) na vzduchu. 8. Zkumavku od polymerační násady vypláchneme toluenem a ethanolem. 9. Polymer zvážíme a vypočteme konverzi monomeru na polymer.
4 EMULZNÍ POLYMERACE STYRENU Úvod: Emulzní polymerace patří k nejrozšířenějším polymeračním technikám využívaným průmyslově. Polymerační násada je tvořena monomerem, iniciátorem rozpustným v disperzním prostředí a nerozpustným v monomeru, emulgátorem, disperzním prostředím nemísitelným s monomerem (nejčastěji voda). Získaný polymer je znečištěn emulgátorem a nehodí se tak pro elektrotechnické aplikace (zvýšená vodivost) a aplikace, kde je důležitá čirost materiálů. Emulgátor je látka amfifilní povahy, př. takové látky je mýdlo.: nepolární řetězec (interakce s nepolárním monomerem) polární skupina (interakce s vodnou fází) V této úloze si vyzkoušíme emulzní polymeraci styrenu probíhající radikálovým mechanismem ve vodném prostředí. Pro tvorbu micel využijeme běžného detergentu (jar, mýdlo). Jako iniciátor bude využit vodorozpustný peroxodisíran amonný (NH4) 2S2O8, který obdobně jako ABIN zahříváním generuje iniciující radikály: 2 peroxoradikál Tyto radikály reagují s molekulami styrenu za tvorby krátkých oligomerů, které pronikají do micely s nepolárním styrenem. Po vniknutí oligomeru nesoucího radikál začne v micele polymerace. Při vniknutí dalšího radikálů dojde k terminaci rekombinací. Jelikož má micela obsahující monomer rozměry v řádu desítek až stovek nanometrů, je dokonale odváděno polymerační teplo. Produktem polymerace je latex, který je možno využít např. jako součást nátěrových hmot (pojivo). Pomůcky a chemikálie: kulatá baňka 100 ml s plastovou zátkou, injekční stříkačka 2 ml, vodní lázeň (ideálně mg. Míchaná) pro baňku 100 ml, 4x zkumavka se zátkou mýdlo/jar, destilovaná voda, styren, peroxodisíran amonný, síran amonný (nebo sodný), toluen, ethanol, technický benzín, aceton Bezpečnost Styren je toxická látka. Při práci s ním pracujte čistě, v případě ukápnutí styren ihned setřete buničinou a nechte odvětrat v digestoři. Po celou dobu pobytu v laboratoři používejte ochranné brýle.
5 Pracovní postup: 1. Ve 100 ml baňce rozpustíme ~0,7 g mýdla (nebo jiného detergentu) ve 20 ml destilované vody. 2. Stříkačkou přidáme 1 ml styrenu a intenzivním mícháním (třepáním zazátkované baňky) vytvoříme emulzi. 3. K emulzi přidáme 0,1 g (NH4)2S2O8, opět protřepeme. 4. Polymerační násadu zahříváme (ideálně za míchání mg. míchadlem) na C ve vodní lázni. Za těchto podmínek probíhá polymerační reakce, která styren přeměňuje na polystyren. S časem reakce slábne zápach styrenu, který se spotřebovává polymerací. 5. Po 60 min přidáme do horkého roztoku asi 2 g (NH4)2SO4, který iontovým šokem způsobí koagulaci latexu. 6. Po asi 15 min podtlakovou filtrací přes Büchnerovu nálevku vyizolujeme připravený polystyren, promyjeme ethanolem, necháme sušit přes noc a stanovíme konverzi styrenu na polymer 7. Rozpustnost polystyrenu (připraveného předchozí skupinou) vyzkoušíme v následujících rozpouštědlech: toluen, ethanol, aceton, technický benzín. Rozpustnost zkoušíme na malém množství suchého polystyrenu (~10 mg) v 1 ml rozpouštědla v zazátkovaných zkumavkách. Rozpouštění urychlujeme třepáním a přihříváním zkumavky v horké lázni. 8. Na základě provedených rozpustnostních testů rozpustíme zbytek PS ve vhodném rozpouštědle (10 ml) a za míchání vysrážíme do vhodného srážedla (100 ml).
6 STANOVENÍ HODNOTY ZMÝDELNĚNÍ POLYVINYLACETÁTU Úvod: Polyvinylalkohol (PVAL) je jedním z mála vodorozpustných syntetických polymerů. Jelikož monomerní vinylalkohol je nestabilní látka (ihned přesmykuje na ethanal), nelze PVAL připravit jeho polymerací. PVAL se tak připravuje nepřímo hydrolýzou acetátových skupin polyvinylacetátu, který lze připravit snadno radikálovou polymerací vinylacetátu: radikálová polymerace hydrolýza vinylacetát polyvinylacetát zbytková acetátová skupina polyvinylalkohol Podle stupně hydrolýzy acetátových jednotek se mění rozpustnost vznikajícího PVAL, při malém stupni zmýdelnění je polymer (převážně stále polyvinylacetát) rozpustný v alkoholech, při vyšším rozsahu hydrolýzy začíná být PVAL rozpustný ve vodě (horké, a později i studené) a nerozpustný v alkoholech. Stupeň hydrolýzy polyvinylacetátu se běžně vyjadřuje číslem zmýdelnění (DIN 53401), tj. hmotností KOH v mg nutných pro zmýdelnění (hydrolýzu) zbytkových acetátových skupin. Podobným způsobem se stanovuje číslo zmýdelnění např. v tucích, triacylglycerolech, kde lze dle jeho hodnoty stanovit délku mastných kyselin v daném tuku. Pomůcky a chemikálie: Polyvinylalkohol (zbytkový obsah acetátových skupin okolo 10%, např. Mowiol 26-88), Erlenmayerova baňka 250 ml 2ks, zpětný chladič 2 ks, vodní lázeň, odměrný válec 50 ml, byreta ml 0,5 mol/l roztok KOH, 0,5 mol/l vodný roztok kyseliny chlorovodíkové, fenolftalein (indikátor), destilovaná voda Bezpečnost Po celou dobu pobytu v laboratoři používejte ochranné brýle. Kyselina chlorovodíková a hydroxid draselný jsou i ve zředěném stavu žíravinami, při potřísnění se ihned opláchněte postiženou část vodou. Pracovní postup:
7 1. Navažte 1 g polyvinylalkoholu (PVAL) do vytárované Erlenmayerovy baňky s mg. míchadlem, přidejte 20 ml destilované vody a 25ml 0,5 M roztoku KOH, baňku zahřívejte za míchání při C po dobu 20 min 2. Přidejte do baňky varný kamínek, nasaďte na baňku chladič 3. Připravte stejnou baňku s chladičem se všemi chemikáliemi kromě PVAL jako slepý test 4. Obě baňky zahřívejte ve vroucí vodní lázni po dobu 30 min 5. Zchlaďte obě baňky na laboratorní teplotu 6. Do obou baněk přidejte fenolftalein a titrujte pomocí 0,5 M HCl 7. Zapište si spotřebu HCl ve slepém testu 8. Rozdíl mezi spotřebou HCl ve slepém testu a testu vzorku dává množství mililitrů 0,5M KOH nutného pro zmýdelnění 1g PVAL. 9. Spočtěte hodnotu (číslo) zmýdelnění PVAL pomocí vzorců: Hodnota zmýdelnění = mg KOH spotřebované na 1g PVAL Hmotnost KOH = c(koh) x M(KOH) x objem KOH roztoku v litrech objem KOH roztoku = V(HCl, slepý test) - V(HCl, test vzorku) ml
8 CHEMICKÁ RECYKLACE PLEXISKLA Úvod: Fyzikální recyklace, kdy je polymer po separaci znovu přetaven a získá se tak znovu polymerní materiál, vede vždy k částečné degradaci polymeru v důsledku převodu do taveniny (tepelného namáhání a degradace). Důsledkem je vznik méně kvalitního materiálu vhodného pouze pro méně náročné aplikace. Alternativou k fyzikální recyklaci je u vybraných polymerů recyklace chemická. Její výhodou je příprava čistého monomeru, jehož polymerací se získá opět panenský polymer, který nebyl vystaven degradaci při použití a může být opět využit v původní aplikaci. Nevýhodou je vznik vedlejších produktů, které jsou problematickým odpadem. K chemické recyklaci se tak hodí pouze postupy, které vedou ke vzniku monomerů ve vysokém výtěžku nad 90%. Chemická recyklace může být založena: a) na katalytickém rozkladu některých polymerů (např. katalyzované hydrolýzy polyamidů a polyesterů, zejm. PET) nebo b) na tepelné depolymeraci polymerů, zejména těch, které obsahují kvarterní uhlíkové atomy, -methylstyren) nebo polymethylmethakrylát (PMMA, Plexisklo), které vytvářejí štepěním stabilní terciární radikály. Principem tepelné depolymerace je zahřátí polymeru nad tzv. stropní teplotu, kdy z termodynamických důvodů převažuje depolymerační (depropagační) reakce nad polymerační reakcí (propagací): T> T(stropní) depolymerace M(M) n M* polymer T< T(stropní) polymerace M(M) n-m M* polymer se sníženou molární hmotností m M monomer V této úloze si vyzkoušíme tepelnou depolymeraci PMMA, která vede k opětovnému získání monomeru methyl methakrylátu (MMA). Prvním krokem depolymerace je náhodné štěpení řetězců, které vede ke vzniku polymerních radikálů, které v druhém kroku podléhají depolymeraci za vniku monomeru: PMMA polymerní radikály depolymerace (nad 300 C) polymerní radikál polymerace (T<300 C + radikálový iniciátor) -1 monomer methyl methakrylát T v =101 C
9 Čistota takto získaného MMA je vzhledem k jeho přečištění při destilaci z depolymerujícího PMMA dostatečná i pro opětovnou polymeraci. Tu provedeme pomocí radikálového iniciátoru dibenzoylperoxidu. Pomůcky a chemikálie: Depolymerace: Zkumavka ~20 ml s pryžovou zátkou, destilační nástavec, jímací zkumavka ~10 ml, gumička, horkovzdušná pistole, polymethylmethakrylát (PMMA)-např. deska. Polymerace: 2x zkumavka 5 ml s pryžovou zátkou, dibenzoylperoxid, připravený MMA monomer, špachtle, vodní lázeň C, ethanol Bezpečnost Methylmethakrylát je málo toxická látka. Při depolymeraci však mohou tepelným rozkladem polymeru vznikat i další toxické látky. Práci proto provádějte v dobře větrané digestoři. Po celou dobu pobytu v laboratoři používejte ochranné brýle. Pracovní postup: 9. Plexisklo nadrtíme na malé kousky (nebo odvrtáme hobliny) a do zkumavky vložíme přesně zvážené množství PMMA drtě (asi 1-2 g). 10. Zkumavku uzavřeme destilačním nástavcem z gumové zátky a trubičky. Na druhou stranu trubičky umístíme předem zváženou jímací zkumavku a připevníme ji k nástavci gumičkou. 11. Destilační nástavec omotáme kouskem hadříku nebo buničiny namočené ve studené vodě pro lepší chlazení. 12. Zkumavku s PMMA drtí upneme do laboratorního stojanu a začneme ohřívat horkovzdušnou pistolí nařízenou na plný výkon. Pozor na hořlavé kapaliny v okolí. Pistoli nasměrujeme zespodu zkumavky (co nejblíže dnu zkumavky), tak aby proudící horký vzduch ohříval stěny celé zkumavky a usnadnila se tak destilace MMA. 13. Při dosažení depolymerační teploty ( C) začne rozklad PMMA, vznikající monomer se ihned odpařuje (Tv=101 C) a kondenzuje na stěnách zkumavky a dále v destilačním nástavci, odkud stéká do jímací zkumavky. Po ukončení vývoje MMA (konec destilace, hnědnutí zbytku PMMA termickým rozkladem) ukončíme zahřívání. 14. Zvážíme zkumavku s najímaným produktem a vypočteme výtěžek depolymerace. Opatrně můžeme čichem identifikovat typický zápach methylmethakrylátu. 15. Nadestilovaný methylmethakrylát rozdělíme na polovinu odlitím do další zkumavky. 16. K odlitému MMA přidáme střičkou ethanol (3-4 ml), měl by vzniknout čirý roztok. Tímto ověříme nepřítomnost polymeru v námi získaném monomeru. 17. K druhému dílu nadestilovaného MMA přidáme malé množství dibenzoylperoxidu (na špičku špachtle, ~0,5 hm.%)
10 18. Zkumavku zahřejeme ve vodní lázni s vodou asi na C po dobu 30 min. 19. Do zkumavky vstříkneme ethanol (3-4 ml), který vysráží znovuvytvořený PMMA ve formě suspenze. Tím ověříme, že připravený monomer je schopný opětovné polymerace. Z PMMA jsme taky vytvořili pyrolýzou monomer, který jsme opět převedli v polymer PMMA-provedli jsme chemickou recyklaci PMMA.
11 ANIONTOVÁ POLYMERACE KYANOAKRYLÁTŮ Úvod: Vedle radikálových a katalytických polymerací se i průmyslově využívají iontové polymerace. Aktivující částicí jsou anionty nebo kationty. U vinylických monomerů obsahující dvojnou vazbu je pro iontovou polymeraci nutná aktivace dvojné vazby monomeru, nejčastěji polarizací pomocí substituentů. Aniontové polymeraci podléhají vinylické monomery substituované elektronakceptornímí (schopnými přitahovat elektrony) substituenty, tj. např. CN, -COOR, -NO2 skupina. Tato skupina odsává z dojné vazby elektrony a polarizuje dvojnou vazbu: + R= -COOR, -CN, -NO 2 apod. Jako iniciátory je pro tyto polymerace možno využít báze (nukleofily), jejichž atak na dvojnou vazbu (na uhlíkový atom s parciálním kladným nábojem) monomeru vede k vytvoření aniontu (iniciace), který dále reaguje s dalšími molekulami monomeru za tvorby polymerního řetězce (propagace): iniciace propagace + n B - báze aniontové růstové centrum (nukleofil) Terminace se většinou uskuteční protickým vodíkem např. z alkoholu, vody, kyseliny. Podle síly aktivující elektronakceptorní skupiny je potřeba zvolit iniciátor-bázi. Velmi slabě aktivující skupina, např. fenylová skupina v molekule styrenu, vyžaduje použití velmi silné báze (např. alkalické kovy a jejich hydridy). Naopak vysoce aktivované monomery je možno převést na polymer působením i tak slabých bází jako je voda, resp. v ní přítomnými OH- anionty. Takovým monomerem je např. ethylkyanokrylát, jehož molekula obsahuje dvě silně aktivující skupiny, tj. esterovou COOEt skupinu a nitrilovou CN skupinu: Schopnost takto snadné polymerace je prakticky využívána v tzv. sekundových lepidlech, kdy běžná vzdušná vlhkost nebo vlhkost na povrchu lepeného materiálu je dostatečným iniciátorem velmi rychlé aniontové polymerace. V této úloze si vyzkoušíme různá provedení této polymerace. Pomůcky a chemikálie: kádinka 50 ml 6 ks, 4x zkumavka 5 ml, kádinka 600 ml, mg. míchačka, mg. míchadlo 6x20 mm 4 ks, špachtle sekundové lepidlo (ethylkyanoakrylát, uchovávat v lednici), ethanol technický (denaturovaný), toluen, diethylether, voda, cyklohexan (nebo technický benzín), aceton (střička), kyselina octová (99%) Bezpečnost
12 Při práci se sekundovým lepidlem dejte pozor na potřísnění prstů, na kterých dochází k rychlému vytvrzení lepidla (takto je využíváno i v chirurgii místo šití tkání pomocí niti). Po celou dobu pobytu v laboratoři používejte ochranné brýle. Pracovní postup: A. Srážecí nebo roztoková polymerace 1. Do každé z 50 ml kádinek vložím mg. míchadlo. Do kádinek poté nadávkujeme a) 20 ml vody, b) 20ml 10% roztoku kyseliny octové ve vodě, c) 20 ml ethanolu, d) 20 ml cyklohexanu, e) 20 ml diethyletheru, f) 20 ml 10% roztoku kyseliny octové v diethyletheru a g) 20 ml toluenu. 2. Opatrně otevřeme tubu se sekundovým lepidlem (skladovaným v lednici) a do kádinek postupně míchaných na mg. míchačce (jemně aby se tvořil malý vír) za pozorného sledování přikapeme z výšky asi 5-10 cm několik kapek lepidla. Všímáme si rychlosti reakce a tvaru a lepkavosti případně vznikajících polymerních částic a pozorování zapisujeme do tabulky: Rozpouštědlo voda 10% CH3COOH ve vodě ethanol cyklohexan diethylether 10% CH3COOH v diethyletheru toluen Rychlá polymerace (ANO/NE) Polymer se sráží (ANO/NE)+ Tvar částic (kulovitý/nepravidelný) Lepkavost částic (ANO/NE) B. Mezifázová aniontová polymerace 1. Do 50 ml kádinky nalijeme 20 ml vody a 20 ml cyklohexanu. 2. Do horní cyklohexanové fáze pak rychle přikapeme asi 0.5 g sekundového lepidla (tubu zvážíme před a po nadávkování). Na rozhraní kapalin se ihned vytváří film polymeru, který můžeme z rozhraní odebírat pomocí špachtle. Polymerace a tvorba polymeru je ukončena v okamžiku spotřebování veškerého monomeru. Polymer lehce promyjeme diethyletherem a osušíme buničinou. C. Test rozpustnosti 1. Rozpustnost malého množství polymeru získaného v předchozích experimentech (~2 mg) otestujeme v a) acetonu, b) ethanolu a c) toluenu vložením do zkumavky a občasným protřepáváním po dobu 15 min. 2. V rozpouštědle nejlépe rozpouštějícím polykyanoakrylát pak vymyjeme všechny kádinky a zkumavky znečištěné polymerem. Otázky: 1. Co způsobilo polymeraci kyanokrylátu v cyklohexanu a diethyletheru? 2. Polymeroval kyanokrylát v toluenu? 3. Který z materiálů lze lepit kyanoakrylátovým lepidlem rychleji: a) sklo (bazický povrch) b) dřevo (kyselý povrch)
13 Úvod: STANOVENÍ ZMĚKČOVADLA V PVC Polyvinylchlorid se používá buď jako tvrdý plast (např. na výrobu okenních a dveřních rámů) nebo jako měkčený materiál (pro výrobu hadic a podlahových krytin). Princip změkčení, pomocí tzv. změkčovadel, je snížení teploty skelného přechodu (Tg) interakcí mezi polymerními řetězci a molekulami změkčovadla. Jako změkčovadla se nejčastěji používají málo těkavé estery organických kyselin, např. dioktylftalát (DOP), přesněji (2-ethylhexyl)ftalát: Obsah změkčovadel je poměrně vysoký, běžně desítky procent. Pokles obsahu změkčovadel s časem v důsledku jejich vypocování (migrace) vede k nárůstu Tg a křehnutí PVC výrobku. Tento proces může v konečné fázi vést až k popraskání výrobku. V této úloze si vyzkoušíme, jak zpětně stanovit množství změkčovadla v měkčeném PVC. Pomůcky a chemikálie: kulatá baňka 250 ml, topné hnízdo ml, Soxhletův nástavec 100 ml ( zpětný chladič k Soxhletovu nástavci ( skleněná patrona s fritou( ), Erlenmayerova baňka 250 ml, alobal 5x5 cm, Büchnerova nálevka, varné kamínky PVC měkčené (gumová hadička, lino apod.), ethanol denaturovaný, aceton, tetrahydrofuran (THF, č. stabilizovaný) Bezpečnost S rozpouštědly pracujte vždy v digestoři. THF používejte vždy stabilizovaný a čerstvý- při delším skladování THF tvoří nebezpečné peroxidy! Po celou dobu pobytu v laboratoři používejte ochranné brýle. Pracovní postup: A. Extrakce pomocí Soxhletova nástavce 1. Do předem zvážené patrony Soxhletova nástavce navažte přesně asi 1 g měkčeného PVC. 2. Sestavte aparaturu dle obrázku, a shora do nástavce vlijte takové množství acetonu, které bude dostatečné pro naplnění celé patrony, a k tomu přidejte dalších 100 ml. Nezapomeňte vložit do baňky varný kamínek. 3. Zapojte vodu chladiče. 4. Ponechte zkontrolovat aparaturu vedoucím práce 5. Zapněte topné hnízdo a nastavte ho opatrně tak, aby rozpouštědlo intenzivně vřelo a kondenzovalo na chladiči. 6. Ponechte PVC extrahovat po dobu 1 h od počátku varu. 7. Patronu s extrahovaným PVC vysušte v sušárně při 80 C po dobu 30 min. 8. Patronu zvažte a z rozdílů hmotnosti PVC před a po extrakci změkčovadla vypočtěte hmotnostní zlomek změkčovadla v původním vzorku PVC.
14 Schéma aparatury: 1. Varná baňka s rozpouštědlem, 2. Tělo extraktoru 3. Zpětný chladič 4. Patrona pro vložení extrahovaného vzorku, 5. Propojka pro páry rozpouštědla 6. Přepad 7. Topné hnízdo B. Extrakce přesrážením roztoku PVC 1. Do 250 ml Erlenmayerovy baňky navažte přesně asi 1 g měkčeného PVC, přidejte 40 ml THF a baňku uzavřete kouskem alobalu. 2. Baňku za míchání (nebo třepání) zahřívejte v horké vodě (asi 50 C) pro urychlení rozpouštění PVC. 3. Po úplném rozpuštění vzorku přidejte 100 ml ethanolu pro vysrážení PVC. 4. Filtrací pomocí Büchnerovy nálevky oddělte PVC od extraktu. 5. Vysušte PVC v sušárně při 80 C po dobu asi 30 min. 6. Po ochlazení PVC zvažte a z rozdílů hmotností před a po extrakci změkčovadla vypočtěte hmotnostní zlomek změkčovadla v původním vzorku. Závěr Po vyhodnocení hmotnostního úbytku u obou metod (extrakce a srážení) je porovnejte mezi sebou. Zkuste odhadnout, proč se výsledná hodnota u obou postupů liší a která z hodnot je správnější?
15 VYTVRZOVÁNÍ EPOXIDOVÉ PRYSKYŘICE Úvod: Epoxidové pryskyřice mají výbornou adhezi k jiným materiálů a po vytvrzení se stávají nerozpustnými a netavitelnými. Tato vlastnosti je předurčují k využití ve formě lepidel a tmelů. Nejběžněji se tyto pryskyřice připravují reakcí Bisfenolu A a epichlorhydrinem. (viz. pracovní list ZÁKLADNÍ SYNTETICKÉ REAKTOPLASTY II.) Vytvrzení pryskyřice je dosaženo prosíťováním pomocí vícefunkčních činidel, často aminů: pryskyřice síťovadlo prosíťovaná pryskyřice V této práci budeme sledovat časový průběh síťování epoxidové pryskyřice (lepidla). Pomůcky a chemikálie: Dvousložkové epoxidové lepidlo (30 min, např. párátka, hliníkové mističky ( plastové stříkačky 10 ml (na jedno použití) opatřené 10 cm PE hadičkami ( mm/), hliníková folie, olej, stopky, termočlánek, ( skleněná tyčinka nebo špachtle Bezpečnost Při práci dodržujte bezpečnostními pokyny výrobce pryskyřice. Se získanými produkty naložte dle pokynu vyučujícího. Po celou dobu přítomnosti v laboratoři používejte ochranné brýle. Pracovní postup:
16 1. Teploměr potřete lehce silikonovým olejem a zabalte do kousku alobalu (aby šel vyjmout z pryskyřice po ztuhnutí). Nepoužívejte teploměr k míchání reakční směsi. 2. Do mističky nadávkujte pomocí stříkaček s PE hadičkami asi 15 ml epoxidové pryskyřice (6 8 ml každé komponenty). Dbejte na to, abyste každou složku lepidla navažovali čistou stříkačkou, aby nedošlo ke vzájemné kontaminaci výchozích složek. 3. Obě komponenty důkladně zamíchejte špachtlí, přičemž se snažte zabránit vzniku vzduchových bublinek v pryskyřici. Začněte měřit čas. 4. Odeberte trochu vzorku do druhé mističky, tak aby vznikla jen tenká vrstva lepidla. 5. Do stojanu upevněte teploměr, zapište pokojovou teplotu, teploměr vnořte do mističky s většinou pryskyřice a zapište počáteční teplotu. Očistěte špachtli. 6. V intervalu 2-3 min odečítejte teplotu na teploměru a sledujte viskozitu pryskyřice v obou miskách pomocí párátka (jak snadno lze vnořit do pryskyřice, kolik pryskyřice na něm ulpí, lepivost), Údaje zapisujte do následující tabulky: Čas (min) Teplota ( C) Viskozita Otázky: 7. Po dosažení teplotního maxima sledujte průběh reakce ještě asi min, pak vyjměte teploměr. Vyneste teplotní data do grafu. 1. Jak si odpovídají teplotní záznam a průběh viskozity (párátkový vpichovací test)? 2. Vytvrdilo se 30 minutové lepidlo zcela během 30 min? 3. Liší se průběh síťování v závislosti na množství vytvrzované pryskyřice? 4. Proč jsou obě složky lepidla baleny zvlášť?
KARBOXYLOVÉ KYSELINY
 LABORATORNÍ PRÁCE Č. 28 KARBOXYLOVÉ KYSELINY PRINCIP Karboxylové kyseliny jsou látky, které ve své molekule obsahují jednu nebo více karboxylových skupin. Odvozují se od nich dva typy derivátů, substituční
LABORATORNÍ PRÁCE Č. 28 KARBOXYLOVÉ KYSELINY PRINCIP Karboxylové kyseliny jsou látky, které ve své molekule obsahují jednu nebo více karboxylových skupin. Odvozují se od nich dva typy derivátů, substituční
Dilatometrické sledování kinetiky radikálové polymerizace 1
 Dilatometrické sledování kinetiky radikálové polymerizace 1 1. Úvod Radikálovou polymerizací se průmyslově vyrábí asi 50 % syntetických polymerů. Detailní znalost vlivu reakčních parametrů na rychlost
Dilatometrické sledování kinetiky radikálové polymerizace 1 1. Úvod Radikálovou polymerizací se průmyslově vyrábí asi 50 % syntetických polymerů. Detailní znalost vlivu reakčních parametrů na rychlost
Ústřední komise Chemické olympiády. 55. ročník 2018/2019 ŠKOLNÍ KOLO. Kategorie C ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ)
 Ústřední komise Chemické olympiády 55. ročník 2018/2019 ŠKOLNÍ KOLO Kategorie C ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ) PRAKTICKÁ ČÁST 40 BODŮ Autor RNDr. Jan Břížďala Gymnázium Třebíč RNDr. Jan Havlík, Ph.D.
Ústřední komise Chemické olympiády 55. ročník 2018/2019 ŠKOLNÍ KOLO Kategorie C ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ) PRAKTICKÁ ČÁST 40 BODŮ Autor RNDr. Jan Břížďala Gymnázium Třebíč RNDr. Jan Havlík, Ph.D.
UHLOVODÍKY A HALOGENDERIVÁTY
 LABORATORNÍ PRÁCE Č. 25 UHLOVODÍKY A HALOGENDERIVÁTY PRINCIP Uhlovodíky jsou nejjednodušší organické sloučeniny, jejichž molekuly jsou tvořeny pouze uhlíkem a vodíkem. Uhlovodíky klasifikujeme z několika
LABORATORNÍ PRÁCE Č. 25 UHLOVODÍKY A HALOGENDERIVÁTY PRINCIP Uhlovodíky jsou nejjednodušší organické sloučeniny, jejichž molekuly jsou tvořeny pouze uhlíkem a vodíkem. Uhlovodíky klasifikujeme z několika
RUŠENÁ KRYSTALIZACE A SUBLIMACE
 LABORATORNÍ PRÁCE Č. 5 RUŠENÁ KRYSTALIZACE A SUBLIMACE KRYSTALIZACE PRINCIP Krystalizace je důležitý postup při získávání čistých tuhých látek z jejich roztoků. Tuhá látka se rozpustí ve vhodném rozpouštědle.
LABORATORNÍ PRÁCE Č. 5 RUŠENÁ KRYSTALIZACE A SUBLIMACE KRYSTALIZACE PRINCIP Krystalizace je důležitý postup při získávání čistých tuhých látek z jejich roztoků. Tuhá látka se rozpustí ve vhodném rozpouštědle.
I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í LABORATORNÍ PRÁCE Č. 14 SRÁŽECÍ REAKCE
 LABORATORNÍ PRÁCE Č. 14 SRÁŽECÍ REAKCE PRINCIP Srážecí reakce je reakce, při níž se alespoň jeden z produktů vylučuje z reakční směsi ve formě tuhé fáze (sraženiny). A + (aq) + B - (aq) AB (s) (Reakce
LABORATORNÍ PRÁCE Č. 14 SRÁŽECÍ REAKCE PRINCIP Srážecí reakce je reakce, při níž se alespoň jeden z produktů vylučuje z reakční směsi ve formě tuhé fáze (sraženiny). A + (aq) + B - (aq) AB (s) (Reakce
I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í
 I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY Laboratorní práce č. 10 Bílkoviny Pro potřeby projektu
I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY Laboratorní práce č. 10 Bílkoviny Pro potřeby projektu
LABORATORNÍ STANOVENÍ SÍRANŮ VE VODNÉM ROZTOKU
 LABORATORNÍ STANOVENÍ SÍRANŮ VE VODNÉM ROZTOKU Cílem práce je stanovit koncentraci síranů v neznámém vzorku postupem A, B a C a porovnat jednotlivé metody mezi sebou. Protokol musí osahovat veškeré výpočty
LABORATORNÍ STANOVENÍ SÍRANŮ VE VODNÉM ROZTOKU Cílem práce je stanovit koncentraci síranů v neznámém vzorku postupem A, B a C a porovnat jednotlivé metody mezi sebou. Protokol musí osahovat veškeré výpočty
Laboratorní cvičení z kinetiky chemických reakcí
 Laboratorní cvičení z kinetiky chemických reakcí LABORATORNÍ CVIČENÍ 1. Téma: Ovlivňování průběhu reakce změnou koncentrace látek. podmínek průběhu reakce. Jednou z nich je změna koncentrace výchozích
Laboratorní cvičení z kinetiky chemických reakcí LABORATORNÍ CVIČENÍ 1. Téma: Ovlivňování průběhu reakce změnou koncentrace látek. podmínek průběhu reakce. Jednou z nich je změna koncentrace výchozích
LABORATORNÍ PRÁCE č.2
 LABORATORNÍ PRÁCE č.2 Téma: Dělení směsí II Úkol č.1: Destilace směsi manganistan draselný voda Teorie: Jedná se o jeden z nejdůležitějších způsobů oddělování složek kapalných směsí a jejich čištění. Složky
LABORATORNÍ PRÁCE č.2 Téma: Dělení směsí II Úkol č.1: Destilace směsi manganistan draselný voda Teorie: Jedná se o jeden z nejdůležitějších způsobů oddělování složek kapalných směsí a jejich čištění. Složky
I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í
 I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY Laboratorní práce č. 9 Lipidy Pro potřeby projektu
I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY Laboratorní práce č. 9 Lipidy Pro potřeby projektu
Ústřední komise Chemické olympiády. 53. ročník 2016/2017. KRAJSKÉ KOLO kategorie C. ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ) časová náročnost: 120 minut
 Ústřední komise Chemické olympiády 53. ročník 2016/2017 KRAJSKÉ KOLO kategorie C ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ) časová náročnost: 120 minut Zadání praktické části krajského kola ChO kat. C 2016/2017
Ústřední komise Chemické olympiády 53. ročník 2016/2017 KRAJSKÉ KOLO kategorie C ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ) časová náročnost: 120 minut Zadání praktické části krajského kola ChO kat. C 2016/2017
I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í LABORATORNÍ PRÁCE Č. 6 PRÁCE S PLYNY
 LABORATORNÍ PRÁCE Č. 6 PRÁCE S PLYNY Mezi nejrozšířenější práce s plyny v laboratoři patří příprava a důkazy oxidu uhličitého CO 2, kyslíku O 2, vodíku H 2, oxidu siřičitého SO 2 a amoniaku NH 3. Reakcí
LABORATORNÍ PRÁCE Č. 6 PRÁCE S PLYNY Mezi nejrozšířenější práce s plyny v laboratoři patří příprava a důkazy oxidu uhličitého CO 2, kyslíku O 2, vodíku H 2, oxidu siřičitého SO 2 a amoniaku NH 3. Reakcí
CHEMIE Pracovní list č.3 žákovská verze Téma: Acidobazická titrace Mgr. Lenka Horutová Student a konkurenceschopnost
 www.projektsako.cz CHEMIE Pracovní list č.3 žákovská verze Téma: Acidobazická titrace Lektor: Projekt: Reg. číslo: Mgr. Lenka Horutová Student a konkurenceschopnost CZ.1.07/1.1.07/03.0075 Teorie: Základem
www.projektsako.cz CHEMIE Pracovní list č.3 žákovská verze Téma: Acidobazická titrace Lektor: Projekt: Reg. číslo: Mgr. Lenka Horutová Student a konkurenceschopnost CZ.1.07/1.1.07/03.0075 Teorie: Základem
Ministerstvo školství, mládeže a tělovýchovy Ústřední komise Chemické olympiády. 46. ročník 2009/2010. KRAJSKÉ KOLO kategorie D
 Ministerstvo školství, mládeže a tělovýchovy Ústřední komise Chemické olympiády 46. ročník 2009/2010 KRAJSKÉ KOLO kategorie D ŘEŠENÍ SOUTĚŽNÍCH ÚLOH TEORETICKÁ ČÁST (60 bodů) Úloha 1 Vlastnosti prvků 26
Ministerstvo školství, mládeže a tělovýchovy Ústřední komise Chemické olympiády 46. ročník 2009/2010 KRAJSKÉ KOLO kategorie D ŘEŠENÍ SOUTĚŽNÍCH ÚLOH TEORETICKÁ ČÁST (60 bodů) Úloha 1 Vlastnosti prvků 26
Jazykové gymnázium Pavla Tigrida, Ostrava-Poruba Název projektu: Podpora rozvoje praktické výchovy ve fyzice a chemii
 Datum: Jazykové gymnázium Pavla Tigrida, Ostrava-Poruba Název projektu: Podpora rozvoje praktické výchovy ve fyzice a chemii Tlak vzduchu: Teplota vzduchu: Laboratorní cvičení č. Oddělování složek směsí
Datum: Jazykové gymnázium Pavla Tigrida, Ostrava-Poruba Název projektu: Podpora rozvoje praktické výchovy ve fyzice a chemii Tlak vzduchu: Teplota vzduchu: Laboratorní cvičení č. Oddělování složek směsí
Sešit pro laboratorní práci z chemie
 Sešit pro laboratorní práci z chemie téma: Příprava roztoků a měření ph autor: ing. Alena Dvořáková vytvořeno při realizaci projektu: Inovace školního vzdělávacího programu biologie a chemie registrační
Sešit pro laboratorní práci z chemie téma: Příprava roztoků a měření ph autor: ing. Alena Dvořáková vytvořeno při realizaci projektu: Inovace školního vzdělávacího programu biologie a chemie registrační
Ústřední komise Chemické olympiády. 56. ročník 2019/2020 ŠKOLNÍ KOLO. Kategorie A. Praktická část Zadání 40 bodů
 Ústřední komise Chemické olympiády 56. ročník 2019/2020 ŠKOLNÍ KOLO Kategorie A Praktická část Zadání 40 bodů PRAKTICKÁ ČÁST 40 BODŮ Autor Doc. Ing. Petr Exnar, CSc. Technická univerzita v Liberci Recenze
Ústřední komise Chemické olympiády 56. ročník 2019/2020 ŠKOLNÍ KOLO Kategorie A Praktická část Zadání 40 bodů PRAKTICKÁ ČÁST 40 BODŮ Autor Doc. Ing. Petr Exnar, CSc. Technická univerzita v Liberci Recenze
Téma : Uhlovodíky Areny Toluen a naftalen Název : Vlastnosti toluenu a naftalenu
 Téma : Uhlovodíky Areny Toluen a naftalen Název : Vlastnosti toluenu a naftalenu Typ pokusu : demonstrační Princip : Areny starším názvem aromatické uhlovodíky, vzaly tento svůj název podle své typické
Téma : Uhlovodíky Areny Toluen a naftalen Název : Vlastnosti toluenu a naftalenu Typ pokusu : demonstrační Princip : Areny starším názvem aromatické uhlovodíky, vzaly tento svůj název podle své typické
NOVÉ NÁMĚTY PRO DEMONSTRAČNÍ POKUSY. Ondřej Maca, Tereza Kudrnová
 NOVÉ NÁMĚTY PRO DEMONSTRAČNÍ POKUSY Ondřej Maca, Tereza Kudrnová HUSTÝ DÝM 1) pro koho: 1. ročník čtyřletého gymnázia 2) zařazení do učiva: vlastnosti látek; halogeny; pentely 3) pomůcky: zkumavka se zátkou,
NOVÉ NÁMĚTY PRO DEMONSTRAČNÍ POKUSY Ondřej Maca, Tereza Kudrnová HUSTÝ DÝM 1) pro koho: 1. ročník čtyřletého gymnázia 2) zařazení do učiva: vlastnosti látek; halogeny; pentely 3) pomůcky: zkumavka se zátkou,
Obrázek 3: Zápis srážecí reakce
 VG STUDENT CHEMIE T É M A: SRÁŽENÍ, IZOLACE SRAŽENIN Vypracoval/a: Spolupracoval/a: Třída: Datum: ANOTACE: V této laboratorní práci se žáci seznámí s pojmem sraženina a srážení, provedou srážení jodidu
VG STUDENT CHEMIE T É M A: SRÁŽENÍ, IZOLACE SRAŽENIN Vypracoval/a: Spolupracoval/a: Třída: Datum: ANOTACE: V této laboratorní práci se žáci seznámí s pojmem sraženina a srážení, provedou srážení jodidu
ORGANICKÁ CHEMIE Laboratorní práce č. 3
 Téma: Hydroxyderiváty uhlovodíků ORGANICKÁ CHEMIE Laboratorní práce č. 3 Úkol 1: Dokažte přítomnost ethanolu ve víně. Ethanol bezbarvá kapalina, která je základní součástí alkoholických nápojů. Ethanol
Téma: Hydroxyderiváty uhlovodíků ORGANICKÁ CHEMIE Laboratorní práce č. 3 Úkol 1: Dokažte přítomnost ethanolu ve víně. Ethanol bezbarvá kapalina, která je základní součástí alkoholických nápojů. Ethanol
ORGANICKÁ CHEMIE Laboratorní práce č. 4 Téma: Karbonylové sloučeniny, karboxylové kyseliny
 ORGANICKÁ CHEMIE Laboratorní práce č. 4 Téma: Karbonylové sloučeniny, karboxylové kyseliny Úkol 1: Připravte acetaldehyd. Karbonylová skupina aldehydů podléhá velmi snadno oxidaci až na skupinu karboxylovou.
ORGANICKÁ CHEMIE Laboratorní práce č. 4 Téma: Karbonylové sloučeniny, karboxylové kyseliny Úkol 1: Připravte acetaldehyd. Karbonylová skupina aldehydů podléhá velmi snadno oxidaci až na skupinu karboxylovou.
Oborový workshop pro ZŠ CHEMIE
 PRAKTICKÁ VÝUKA PŘÍRODOVĚDNÝCH PŘEDMĚTŮ NA ZŠ A SŠ CZ.1.07/1.1.30/02.0024 Tento projekt je spolufinancován Evropským sociálním fondem a státním rozpočtem České republiky. Oborový workshop pro ZŠ CHEMIE
PRAKTICKÁ VÝUKA PŘÍRODOVĚDNÝCH PŘEDMĚTŮ NA ZŠ A SŠ CZ.1.07/1.1.30/02.0024 Tento projekt je spolufinancován Evropským sociálním fondem a státním rozpočtem České republiky. Oborový workshop pro ZŠ CHEMIE
JODOMETRICKÉ STANOVENÍ ROZPUŠTĚNÉHO KYSLÍKU
 JODOMETRICKÉ STANOVENÍ ROZPUŠTĚNÉHO KYSLÍKU (dle Winklera v Alsterbergově modifikaci) Cílem je stanovení rozpuštěného kyslíku v pitné vodě z vodovodního řádu. Protokol musí osahovat veškeré potřebné hodnoty
JODOMETRICKÉ STANOVENÍ ROZPUŠTĚNÉHO KYSLÍKU (dle Winklera v Alsterbergově modifikaci) Cílem je stanovení rozpuštěného kyslíku v pitné vodě z vodovodního řádu. Protokol musí osahovat veškeré potřebné hodnoty
Ústřední komise Chemické olympiády. 55. ročník 2018/2019 KRAJSKÉ KOLO. Kategorie A ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ) Časová náročnost 120 minut
 Ústřední komise Chemické olympiády 55. ročník 2018/2019 KRAJSKÉ KOLO Kategorie A ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ) Časová náročnost 120 minut Úloha 1 Příprava Mohrovy soli 15 bodů Mezi podvojné soli patří
Ústřední komise Chemické olympiády 55. ročník 2018/2019 KRAJSKÉ KOLO Kategorie A ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ) Časová náročnost 120 minut Úloha 1 Příprava Mohrovy soli 15 bodů Mezi podvojné soli patří
Sešit pro laboratorní práci z chemie
 Sešit pro laboratorní práci z chemie téma: Příprava oxidu měďnatého autor: ing. Alena Dvořáková vytvořeno při realizaci projektu: Inovace školního vzdělávacího programu biologie a chemie registrační číslo
Sešit pro laboratorní práci z chemie téma: Příprava oxidu měďnatého autor: ing. Alena Dvořáková vytvořeno při realizaci projektu: Inovace školního vzdělávacího programu biologie a chemie registrační číslo
ORGANICKÁ CHEMIE Laboratorní práce č. 9
 Téma: Bílkoviny, enzymy ORGANICKÁ CHEMIE Laboratorní práce č. 9 Úkol 1: Dokažte, že mléko obsahuje bílkovinu kasein. Kasein je hlavní bílkovinou obsaženou v savčím mléce. Výroba řady mléčných výrobků je
Téma: Bílkoviny, enzymy ORGANICKÁ CHEMIE Laboratorní práce č. 9 Úkol 1: Dokažte, že mléko obsahuje bílkovinu kasein. Kasein je hlavní bílkovinou obsaženou v savčím mléce. Výroba řady mléčných výrobků je
13/sv. 8 (85/503/EHS) Tato směrnice je určena členským státům.
 62 31985L0503 L 308/12 ÚŘEDNÍ VĚSTNÍK EVROPSKÝCH SPOLEČENSTVÍ 20.11.1985 PRVNÍ SMĚRNICE KOMISE ze dne 25. října 1985 o metodách pro analýzu potravinářských kaseinů a kaseinátů (85/503/EHS) KOMISE EVROPSKÝCH
62 31985L0503 L 308/12 ÚŘEDNÍ VĚSTNÍK EVROPSKÝCH SPOLEČENSTVÍ 20.11.1985 PRVNÍ SMĚRNICE KOMISE ze dne 25. října 1985 o metodách pro analýzu potravinářských kaseinů a kaseinátů (85/503/EHS) KOMISE EVROPSKÝCH
Všeobecné lékařství 2014/15
 ÚSTAV LÉKAŘSKÉ BIOCHEMIE A LABORATORNÍ DIAGNOSTIKY 1. LF UK Úvod do práce v laboratoři Měření objemů, filtrace, centrifugace, rozpustnost, dělení směsí Praktické cvičení z lékařské biochemie Všeobecné
ÚSTAV LÉKAŘSKÉ BIOCHEMIE A LABORATORNÍ DIAGNOSTIKY 1. LF UK Úvod do práce v laboratoři Měření objemů, filtrace, centrifugace, rozpustnost, dělení směsí Praktické cvičení z lékařské biochemie Všeobecné
HYDROXYDERIVÁTY - ALKOHOLY
 LABORATORNÍ PRÁCE Č. 26 HYDROXYDERIVÁTY - ALKOHOLY PRINCIP Hydroxyderiváty jsou kyslíkaté deriváty uhlovodíků, které vznikají náhradou jednoho nebo více atomů vodíku v molekule uhlovodíku hydroxylovou
LABORATORNÍ PRÁCE Č. 26 HYDROXYDERIVÁTY - ALKOHOLY PRINCIP Hydroxyderiváty jsou kyslíkaté deriváty uhlovodíků, které vznikají náhradou jednoho nebo více atomů vodíku v molekule uhlovodíku hydroxylovou
látka Obr. k úkolům 1 a 2 Obr. k úkolu 3
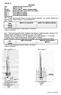 cvičení: A Téma: Základní vlastnosti organických látek Cíl: Teplota varu a tání Pomůcky: žákovská souprava, teploměr, skleněná trubička, Chemikálie: ethanol CH 3 CH 2 OH, aceton CH 3 COCH 3, naftalen Úkol
cvičení: A Téma: Základní vlastnosti organických látek Cíl: Teplota varu a tání Pomůcky: žákovská souprava, teploměr, skleněná trubička, Chemikálie: ethanol CH 3 CH 2 OH, aceton CH 3 COCH 3, naftalen Úkol
Návod k laboratornímu cvičení. Fenoly
 Návod k laboratornímu cvičení Fenoly Úkol č. 1: Příprava fenolátu sodného Pomůcky: váhy, kádinka, zkumavky Chemikálie: 10% roztok hydroxidu sodného NaOH (C), 5%roztok kyseliny chlorovodíkové HCl (C, X
Návod k laboratornímu cvičení Fenoly Úkol č. 1: Příprava fenolátu sodného Pomůcky: váhy, kádinka, zkumavky Chemikálie: 10% roztok hydroxidu sodného NaOH (C), 5%roztok kyseliny chlorovodíkové HCl (C, X
LABORATOŘ ANALÝZY POTRAVIN A PŘÍRODNÍCH PRODUKTŮ
 LABORATOŘ ANALÝZY POTRAVIN A PŘÍRODNÍCH PRODUKTŮ Stanovení tuku a hodnocení kvality tuků a olejů (Soxhletova metoda pro extrakci tuku a titrační stanovení čísla kyselosti) Garant úlohy: doc. Ing. Zuzana
LABORATOŘ ANALÝZY POTRAVIN A PŘÍRODNÍCH PRODUKTŮ Stanovení tuku a hodnocení kvality tuků a olejů (Soxhletova metoda pro extrakci tuku a titrační stanovení čísla kyselosti) Garant úlohy: doc. Ing. Zuzana
RCOOR + H 2 O. Inovace bakalářského studijního oboru Aplikovaná chemie CZ.1.07/2.2.00/ Esterifikace
 Esterifikace Estery jsou funkční deriváty karboxylových kyselin. Připravují se reakcí karboxylových kyselin s alkoholy nebo s fenoly. RCOOH+ HOR RCOOR + H 2 O K přípravě esterů je vhodné použít vyšší alifatické
Esterifikace Estery jsou funkční deriváty karboxylových kyselin. Připravují se reakcí karboxylových kyselin s alkoholy nebo s fenoly. RCOOH+ HOR RCOOR + H 2 O K přípravě esterů je vhodné použít vyšší alifatické
Ústřední komise Chemické olympiády. 55. ročník 2018/2019 NÁRODNÍ KOLO. Kategorie E. Zadání praktické části Úloha 1 (20 bodů)
 Ústřední komise Chemické olympiády 55. ročník 2018/2019 NÁRODNÍ KOLO Kategorie E Zadání praktické části Úloha 1 (20 bodů) PRAKTICKÁ ČÁST 20 BODŮ Úloha 1 Stanovení Ni 2+ a Ca 2+ ve směsi konduktometricky
Ústřední komise Chemické olympiády 55. ročník 2018/2019 NÁRODNÍ KOLO Kategorie E Zadání praktické části Úloha 1 (20 bodů) PRAKTICKÁ ČÁST 20 BODŮ Úloha 1 Stanovení Ni 2+ a Ca 2+ ve směsi konduktometricky
DĚLÍCÍ METODY. Autor: Mgr. Stanislava Bubíková. Datum (období) tvorby: 28. 5. 2012. Ročník: osmý. Vzdělávací oblast: Člověk a příroda / Chemie / Směsi
 Autor: Mgr. Stanislava Bubíková DĚLÍCÍ METODY Datum (období) tvorby: 28. 5. 2012 Ročník: osmý Vzdělávací oblast: Člověk a příroda / Chemie / Směsi 1 Anotace: Žáci se seznámí s nejčastěji používanými separačními
Autor: Mgr. Stanislava Bubíková DĚLÍCÍ METODY Datum (období) tvorby: 28. 5. 2012 Ročník: osmý Vzdělávací oblast: Člověk a příroda / Chemie / Směsi 1 Anotace: Žáci se seznámí s nejčastěji používanými separačními
Ústřední komise Chemické olympiády. 55. ročník 2018/2019 ŠKOLNÍ KOLO. Kategorie B ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ)
 Ústřední komise Chemické olympiády 55. ročník 2018/2019 ŠKOLNÍ KOLO Kategorie B ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ) PRAKTICKÁ ČÁST 40 BODŮ Autor Bc. Lukáš Tomaník VŠCHT Praha RNDr. Petr Holzhauser, Ph.D.
Ústřední komise Chemické olympiády 55. ročník 2018/2019 ŠKOLNÍ KOLO Kategorie B ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ) PRAKTICKÁ ČÁST 40 BODŮ Autor Bc. Lukáš Tomaník VŠCHT Praha RNDr. Petr Holzhauser, Ph.D.
Neutralizační (acidobazické) titrace
 Neutralizační (acidobazické) titrace Neutralizační titrace jsou založeny na reakci mezi kyselinou a zásadou. V podstatě se vždy jedná o reakci iontů H + s ionty OH - podle schematu: H + + OH - H O V průběhu
Neutralizační (acidobazické) titrace Neutralizační titrace jsou založeny na reakci mezi kyselinou a zásadou. V podstatě se vždy jedná o reakci iontů H + s ionty OH - podle schematu: H + + OH - H O V průběhu
NEUTRALIZAČNÍ ODMĚRNÁ ANALÝZA (TITRACE)
 NEUTRALIZAČNÍ ODMĚRNÁ ANALÝZA (TITRACE) Cíle a princip: Stanovit TITR (přesnou koncentraci) odměrného roztoku kyseliny nebo zásady pomocí známé přesné koncentrace již stanoveného odměrného roztoku. Podstatou
NEUTRALIZAČNÍ ODMĚRNÁ ANALÝZA (TITRACE) Cíle a princip: Stanovit TITR (přesnou koncentraci) odměrného roztoku kyseliny nebo zásady pomocí známé přesné koncentrace již stanoveného odměrného roztoku. Podstatou
STANOVENÍ CHLORIDŮ. Odměrné argentometrické stanovení chloridů podle Mohra
 STANOVENÍ CHLORIDŮ Odměrné argentometrické stanovení chloridů podle Mohra Cíl práce Stanovte titr odměrného standardního roztoku dusičnanu stříbrného titrací 5 ml standardního srovnávacího roztoku chloridu
STANOVENÍ CHLORIDŮ Odměrné argentometrické stanovení chloridů podle Mohra Cíl práce Stanovte titr odměrného standardního roztoku dusičnanu stříbrného titrací 5 ml standardního srovnávacího roztoku chloridu
Ústřední komise Chemické olympiády. 55. ročník 2018/2019 ŠKOLNÍ KOLO. Kategorie B ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ)
 Ústřední komise Chemické olympiády 55. ročník 2018/2019 ŠKOLNÍ KOLO Kategorie B ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ) PRAKTICKÁ ČÁST 40 BODŮ Autor Bc. Lukáš Tomaník VŠCHT Praha RNDr. Petr Holzhauser, Ph.D.
Ústřední komise Chemické olympiády 55. ročník 2018/2019 ŠKOLNÍ KOLO Kategorie B ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ) PRAKTICKÁ ČÁST 40 BODŮ Autor Bc. Lukáš Tomaník VŠCHT Praha RNDr. Petr Holzhauser, Ph.D.
Chemický kroužek pro žáky ZŠ. Téma č.1:
 Téma č.1: ZAČÍNÁME Teoretický úvod: 1. Základy bezpečnosti a ochrany zdraví při práci v laboratoři Chemická laboratoř je místo, kde se pracuje s mnoha látkami, které nám mohou být za určitých okolností
Téma č.1: ZAČÍNÁME Teoretický úvod: 1. Základy bezpečnosti a ochrany zdraví při práci v laboratoři Chemická laboratoř je místo, kde se pracuje s mnoha látkami, které nám mohou být za určitých okolností
Stanovení izoelektrického bodu kaseinu
 Stanovení izoelektrického bodu kaseinu Shlukování koloidních částic do větších celků makroskopických rozměrů nazýváme koagulací. Ke koagulaci koloidních roztoků bílkovin dochází porušením solvatačního
Stanovení izoelektrického bodu kaseinu Shlukování koloidních částic do větších celků makroskopických rozměrů nazýváme koagulací. Ke koagulaci koloidních roztoků bílkovin dochází porušením solvatačního
Jazykové gymnázium Pavla Tigrida, Ostrava-Poruba Název projektu: Podpora rozvoje praktické výchovy ve fyzice a chemii
 Datum: Jazykové gymnázium Pavla Tigrida, Ostrava-Poruba Název projektu: Podpora rozvoje praktické výchovy ve fyzice a chemii Laboratorní cvičení č. Tlak vzduchu: Teplota vzduchu: Bílkoviny(proteiny) Vlhkost
Datum: Jazykové gymnázium Pavla Tigrida, Ostrava-Poruba Název projektu: Podpora rozvoje praktické výchovy ve fyzice a chemii Laboratorní cvičení č. Tlak vzduchu: Teplota vzduchu: Bílkoviny(proteiny) Vlhkost
Sešit pro laboratorní práci z chemie
 Sešit pro laboratorní práci z chemie téma: Oddělování složek směsí autor: MVDr. Alexandra Gajová vytvořeno při realizaci projektu: Inovace školního vzdělávacího programu biologie a chemie registrační číslo
Sešit pro laboratorní práci z chemie téma: Oddělování složek směsí autor: MVDr. Alexandra Gajová vytvořeno při realizaci projektu: Inovace školního vzdělávacího programu biologie a chemie registrační číslo
Výukový materiál zpracován v rámci projektu. EU peníze školám. Registrační číslo projektu: CZ.1.07/1.5.00/34.0996
 Výukový materiál zpracován v rámci projektu EU peníze školám Registrační číslo projektu: CZ.1.07/1.5.00/34.0996 Šablona: III/2 č. materiálu: VY_INOVACE_CHE_417 Jméno autora: Třída/ročník: Mgr. Alena Krejčíková
Výukový materiál zpracován v rámci projektu EU peníze školám Registrační číslo projektu: CZ.1.07/1.5.00/34.0996 Šablona: III/2 č. materiálu: VY_INOVACE_CHE_417 Jméno autora: Třída/ročník: Mgr. Alena Krejčíková
P + D PRVKY Laboratorní práce
 Téma: Reakce sloučenin zinku P + D PRVKY Laboratorní práce Pozn: Výsledky úkolu 1 zapisujte až po 14 dnech. Úkol 4 provádějte pouze pod dohledem učitele. Úkol 1: Připravte 5 gramů bílé skalice. Bílá skalice
Téma: Reakce sloučenin zinku P + D PRVKY Laboratorní práce Pozn: Výsledky úkolu 1 zapisujte až po 14 dnech. Úkol 4 provádějte pouze pod dohledem učitele. Úkol 1: Připravte 5 gramů bílé skalice. Bílá skalice
Návody na laboratorní cvičení z makromolekulární chemie
 Návody na laboratorní cvičení z makromolekulární chemie Interní grant Masarykovy university č.:.. Podklady pro studenty Číslo zprávy 2 Příjemce zprávy... Autoři RNDr. Richard Ševčík, Ph.D. Mgr. Gabriela
Návody na laboratorní cvičení z makromolekulární chemie Interní grant Masarykovy university č.:.. Podklady pro studenty Číslo zprávy 2 Příjemce zprávy... Autoři RNDr. Richard Ševčík, Ph.D. Mgr. Gabriela
Chemie. Mgr. Petra Drápelová Mgr. Jaroslava Vrbková. Gymnázium, SOŠ a VOŠ Ledeč nad Sázavou
 Chemie Mgr. Petra Drápelová Mgr. Jaroslava Vrbková Gymnázium, SOŠ a VOŠ Ledeč nad Sázavou Směsi VY_32_INOVACE_03_3_01_CH Gymnázium, SOŠ a VOŠ Ledeč nad Sázavou SMĚSI Směsi jsou složitější látky, které
Chemie Mgr. Petra Drápelová Mgr. Jaroslava Vrbková Gymnázium, SOŠ a VOŠ Ledeč nad Sázavou Směsi VY_32_INOVACE_03_3_01_CH Gymnázium, SOŠ a VOŠ Ledeč nad Sázavou SMĚSI Směsi jsou složitější látky, které
Neutralizace, měření senzorem ph Vernier Laboratorní práce
 Neutralizace, měření senzorem ph Vernier Laboratorní práce VY_52_INOVACE_209 Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Chemie Ročník: 8.,9. Neutralizace, měření senzorem ph Vernier Laboratorní
Neutralizace, měření senzorem ph Vernier Laboratorní práce VY_52_INOVACE_209 Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Chemie Ročník: 8.,9. Neutralizace, měření senzorem ph Vernier Laboratorní
Ústřední komise Chemické olympiády. 54. ročník 2017/2018. ŠKOLNÍ KOLO kategorie A ZADÁNÍ PRAKTICKÉ ČÁSTI: 40 BODŮ
 Ústřední komise Chemické olympiády 54. ročník 2017/2018 ŠKOLNÍ KOLO kategorie A ZADÁNÍ PRAKTICKÉ ČÁSTI: 40 BODŮ Zadání praktické části školního kola ChO kat. A 2017/2018. Autoři Recenze Ing. Ondřej Šimůnek
Ústřední komise Chemické olympiády 54. ročník 2017/2018 ŠKOLNÍ KOLO kategorie A ZADÁNÍ PRAKTICKÉ ČÁSTI: 40 BODŮ Zadání praktické části školního kola ChO kat. A 2017/2018. Autoři Recenze Ing. Ondřej Šimůnek
T É M A: SRÁŽENÍ, GRAVIMETRIE. Spolupracoval/a: ANOTACE: TEORIE: VÁŽKOVÁ ANALÝZA (GRAVIMETRIE)
 SEMINÁŘ STUDENT CHEMIE T É M A: Vypracoval/a: Spolupracoval/a: SRÁŽENÍ, GRAVIMETRIE Třída: Datum: ANOTACE: V této laboratorní práci se žáci seznámí s využití metody srážení v kvantitativní analýze tzv.
SEMINÁŘ STUDENT CHEMIE T É M A: Vypracoval/a: Spolupracoval/a: SRÁŽENÍ, GRAVIMETRIE Třída: Datum: ANOTACE: V této laboratorní práci se žáci seznámí s využití metody srážení v kvantitativní analýze tzv.
Ústřední komise Chemické olympiády. 50. ročník 2013/2014. OKRESNÍ KOLO kategorie D ŘEŠENÍ SOUTĚŽNÍCH ÚLOH
 Ústřední komise Chemické olympiády 50. ročník 2013/2014 OKRESNÍ KOLO kategorie D ŘEŠENÍ SOUTĚŽNÍCH ÚLOH TEORETICKÁ ČÁST (70 BODŮ) Informace pro hodnotitele Ve výpočtových úlohách jsou uvedeny dílčí výpočty
Ústřední komise Chemické olympiády 50. ročník 2013/2014 OKRESNÍ KOLO kategorie D ŘEŠENÍ SOUTĚŽNÍCH ÚLOH TEORETICKÁ ČÁST (70 BODŮ) Informace pro hodnotitele Ve výpočtových úlohách jsou uvedeny dílčí výpočty
Návod k laboratornímu cvičení. Bílkoviny
 Úkol č. 1: Důkazy bílkovin ve vaječném bílku a) natvrdo uvařené vejce s kyselinou dusičnou Pomůcky: Petriho miska, pipeta, nůž. Návod k laboratornímu cvičení Bílkoviny Chemikálie: koncentrovaná kyselina
Úkol č. 1: Důkazy bílkovin ve vaječném bílku a) natvrdo uvařené vejce s kyselinou dusičnou Pomůcky: Petriho miska, pipeta, nůž. Návod k laboratornímu cvičení Bílkoviny Chemikálie: koncentrovaná kyselina
SHRNUTÍ A ZÁKLADNÍ POJMY chemie 8.ročník ZŠ
 SHRNUTÍ A ZÁKLADNÍ POJMY chemie 8.ročník ZŠ 1. ČÍM SE ZABÝVÁ CHEMIE VLASTNOSTI LÁTEK, POKUSY - chemie přírodní věda, která studuje vlastnosti a přeměny látek pomocí pozorování, měření a pokusu - látka
SHRNUTÍ A ZÁKLADNÍ POJMY chemie 8.ročník ZŠ 1. ČÍM SE ZABÝVÁ CHEMIE VLASTNOSTI LÁTEK, POKUSY - chemie přírodní věda, která studuje vlastnosti a přeměny látek pomocí pozorování, měření a pokusu - látka
OKRUH 7 Karboxylové kyseliny
 OKRUH 7 Karboxylové kyseliny Pro karboxylové kyseliny je charakteristická přítomnost jedné nebo více karboxylových skupin Monokarboxylové kyseliny Příprava kyseliny mravenčí z chloroformu a její důkaz
OKRUH 7 Karboxylové kyseliny Pro karboxylové kyseliny je charakteristická přítomnost jedné nebo více karboxylových skupin Monokarboxylové kyseliny Příprava kyseliny mravenčí z chloroformu a její důkaz
Jednotné pracovní postupy zkoušení krmiv STANOVENÍ OBSAHU VITAMÍNU D METODOU LC/MS
 Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU VITAMÍNU D METODOU LC/MS 1 Účel a rozsah Tento postup specifikuje podmínky pro stanovení vitamínu D3 v krmivech metodou LC/MS. 2 Princip Zkušební
Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU VITAMÍNU D METODOU LC/MS 1 Účel a rozsah Tento postup specifikuje podmínky pro stanovení vitamínu D3 v krmivech metodou LC/MS. 2 Princip Zkušební
Ústřední komise Chemické olympiády. 55. ročník 2018/2019 KRAJSKÉ KOLO. Kategorie E ZADÁNÍ PRAKTICKÉ ČÁSTI (50 BODŮ)
 Ústřední komise Chemické olympiády 55. ročník 2018/2019 KRAJSKÉ KOLO Kategorie E ZADÁNÍ PRAKTICKÉ ČÁSTI (50 BODŮ) Úloha 1 Stanovení Bi 3+ a Zn 2+ ve směsi 50 bodů Chelatometricky lze stanovit ionty samostatně,
Ústřední komise Chemické olympiády 55. ročník 2018/2019 KRAJSKÉ KOLO Kategorie E ZADÁNÍ PRAKTICKÉ ČÁSTI (50 BODŮ) Úloha 1 Stanovení Bi 3+ a Zn 2+ ve směsi 50 bodů Chelatometricky lze stanovit ionty samostatně,
Inovace bakalářského studijního oboru Aplikovaná chemie CZ.1.07/2.2.00/ Výpočty z chemických vzorců
 Výpočty z chemických vzorců 1. Hmotnost kyslíku je 80 g. Vypočítejte : a) počet atomů kyslíku ( 3,011 10 atomů) b) počet molů kyslíku (2,5 mol) c) počet molekul kyslíku (1,505 10 24 molekul) d) objem (dm
Výpočty z chemických vzorců 1. Hmotnost kyslíku je 80 g. Vypočítejte : a) počet atomů kyslíku ( 3,011 10 atomů) b) počet molů kyslíku (2,5 mol) c) počet molekul kyslíku (1,505 10 24 molekul) d) objem (dm
Úloha č. 9 Stanovení hydroxidu a uhličitanu vedle sebe dle Winklera
 Úloha č. 9 Stanovení hydroxidu a uhličitanu vedle sebe dle Winklera Princip Jde o klasickou metodu kvantitativní chemické analýzy. Uhličitan vedle hydroxidu se stanoví ve dvou alikvotních podílech zásobního
Úloha č. 9 Stanovení hydroxidu a uhličitanu vedle sebe dle Winklera Princip Jde o klasickou metodu kvantitativní chemické analýzy. Uhličitan vedle hydroxidu se stanoví ve dvou alikvotních podílech zásobního
Laboratorní pomůcky, chemické nádobí
 Laboratorní pomůcky, chemické nádobí Laboratorní sklo: měkké (tyčinky, spojovací trubice, kapiláry) tvrdé označení SIMAX (většina varného a odměrného skla) Zahřívání skla: Tenkostěnné nádoby (kádinky,
Laboratorní pomůcky, chemické nádobí Laboratorní sklo: měkké (tyčinky, spojovací trubice, kapiláry) tvrdé označení SIMAX (většina varného a odměrného skla) Zahřívání skla: Tenkostěnné nádoby (kádinky,
Vodík, kyslík a jejich sloučeniny
 I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY Laboratorní práce č. 8 Vodík, kyslík a jejich sloučeniny
I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY Laboratorní práce č. 8 Vodík, kyslík a jejich sloučeniny
Kopolymerace polymerace dvou a více monomerů
 Kopolymerace polymerace dvou a více monomerů ( 1 monomer homopolymer; 2 monomery kopolymer; 3 monomery ternární kopolymer [ př ABS]) mezní případy kopolymerace: n A n B A A n B B n A B n Struktury vznikajících
Kopolymerace polymerace dvou a více monomerů ( 1 monomer homopolymer; 2 monomery kopolymer; 3 monomery ternární kopolymer [ př ABS]) mezní případy kopolymerace: n A n B A A n B B n A B n Struktury vznikajících
LP č. 6 - BÍLKOVINY. Autor: Mgr. Stanislava Bubíková. Datum (období) tvorby: 28. 2. 2013. Ročník: devátý
 LP č. 6 - BÍLKOVINY Autor: Mgr. Stanislava Bubíková Datum (období) tvorby: 28. 2. 2013 Ročník: devátý Vzdělávací oblast: Člověk a příroda / Chemie / Organické sloučeniny 1 Anotace: Žáci prakticky ověří
LP č. 6 - BÍLKOVINY Autor: Mgr. Stanislava Bubíková Datum (období) tvorby: 28. 2. 2013 Ročník: devátý Vzdělávací oblast: Člověk a příroda / Chemie / Organické sloučeniny 1 Anotace: Žáci prakticky ověří
Jazykové gymnázium Pavla Tigrida, Ostrava-Poruba Název projektu: Podpora rozvoje praktické výchovy ve fyzice a chemii
 Datum: Jazykové gymnázium Pavla Tigrida, Ostrava-Poruba Název projektu: Podpora rozvoje praktické výchovy ve fyzice a chemii Laboratorní cvičení č. Tlak vzduchu: Teplota vzduchu: Vodík a kyslík Vlhkost
Datum: Jazykové gymnázium Pavla Tigrida, Ostrava-Poruba Název projektu: Podpora rozvoje praktické výchovy ve fyzice a chemii Laboratorní cvičení č. Tlak vzduchu: Teplota vzduchu: Vodík a kyslík Vlhkost
Směsi, roztoky. Disperzní soustavy, roztoky, koncentrace
 Směsi, roztoky Disperzní soustavy, roztoky, koncentrace 1 Směsi Směs je soustava, která obsahuje dvě nebo více chemických látek. Mezi složkami směsi nedochází k chemickým reakcím. Fyzikální vlastnosti
Směsi, roztoky Disperzní soustavy, roztoky, koncentrace 1 Směsi Směs je soustava, která obsahuje dvě nebo více chemických látek. Mezi složkami směsi nedochází k chemickým reakcím. Fyzikální vlastnosti
Směsi a čisté látky, metody dělení
 Směsi a čisté látky, metody dělení LÁTKY Chemicky čisté látky Sloučeniny Chemické prvky Homogenní Roztoky pevné kapalné plynné Směsi Heterogenní Suspenze Emulze Pěna Aerosol Chemicky čisté látky: prvky
Směsi a čisté látky, metody dělení LÁTKY Chemicky čisté látky Sloučeniny Chemické prvky Homogenní Roztoky pevné kapalné plynné Směsi Heterogenní Suspenze Emulze Pěna Aerosol Chemicky čisté látky: prvky
Inhibitory koroze kovů
 Inhibitory koroze kovů Úvod Korozní rychlost kovových materiálů lze ovlivnit úpravou prostředí, ve kterém korozní děj probíhá. Mezi tyto úpravy patří i použití inhibitorů koroze kovů. Inhibitor je látka,
Inhibitory koroze kovů Úvod Korozní rychlost kovových materiálů lze ovlivnit úpravou prostředí, ve kterém korozní děj probíhá. Mezi tyto úpravy patří i použití inhibitorů koroze kovů. Inhibitor je látka,
Ministerstvo školství, mládeže a tělovýchovy Ústřední komise Chemické olympiády. 46. ročník 2009/2010. OKRESNÍ KOLO kategorie D
 Ministerstvo školství, mládeže a tělovýchovy Ústřední komise Chemické olympiády 46. ročník 2009/2010 OKRESNÍ KOLO kategorie D ŘEŠENÍ SOUTĚŽNÍCH ÚLOH TEORETICKÁ ČÁST (55 bodů) Úloha 1 Závislost rozpustnosti
Ministerstvo školství, mládeže a tělovýchovy Ústřední komise Chemické olympiády 46. ročník 2009/2010 OKRESNÍ KOLO kategorie D ŘEŠENÍ SOUTĚŽNÍCH ÚLOH TEORETICKÁ ČÁST (55 bodů) Úloha 1 Závislost rozpustnosti
Návod k laboratornímu cvičení. Alkoholy
 Úkol č. 1: Ověřování fyzikálních vlastností alkoholů Návod k laboratornímu cvičení Alkoholy Pomůcky: 3 velké zkumavky - A,B,C, hodinové sklíčko, kapátko nebo skleněná tyčinka Chemikálie: etanol (F), etan-1,2-
Úkol č. 1: Ověřování fyzikálních vlastností alkoholů Návod k laboratornímu cvičení Alkoholy Pomůcky: 3 velké zkumavky - A,B,C, hodinové sklíčko, kapátko nebo skleněná tyčinka Chemikálie: etanol (F), etan-1,2-
ORGANICKÁ CHEMIE Laboratorní práce č. 2
 Téma: Uhlovodíky ORGANICKÁ CHEMIE Laboratorní práce č. 2 Pozn: Organické látky, jako jsou petrolej, hexan nebo naftalen, nepatří do umyvadla, ale do speciální nádoby na organický odpad!! Úkol 1: Zkoumejte
Téma: Uhlovodíky ORGANICKÁ CHEMIE Laboratorní práce č. 2 Pozn: Organické látky, jako jsou petrolej, hexan nebo naftalen, nepatří do umyvadla, ale do speciální nádoby na organický odpad!! Úkol 1: Zkoumejte
Jednotné pracovní postupy zkoušení krmiv STANOVENÍ OBSAHU VÁPNÍKU MANGANOMETRICKY
 Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU VÁPNÍKU MANGANOMETRICKY 1 Rozsah a účel Tato metoda specifikuje podmínky pro stanovení celkového obsahu vápníku v krmivech, krmných směsích a premixech.
Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU VÁPNÍKU MANGANOMETRICKY 1 Rozsah a účel Tato metoda specifikuje podmínky pro stanovení celkového obsahu vápníku v krmivech, krmných směsích a premixech.
Netkané textilie. Materiály 2
 Materiály 2 1 Pojiva pro výrobu netkaných textilií Pojivo je jednou ze dvou základních složek pojených textilií. Forma pojiva a jeho vlastnosti předurčují technologii a podmínky procesu pojení způsob rozmístění
Materiály 2 1 Pojiva pro výrobu netkaných textilií Pojivo je jednou ze dvou základních složek pojených textilií. Forma pojiva a jeho vlastnosti předurčují technologii a podmínky procesu pojení způsob rozmístění
METODY ČIŠTĚNÍ ORGANICKÝCH LÁTEK
 METODY ČIŠTĚNÍ ORGANICKÝCH LÁTEK Chemické sloučeniny se připravují z jiných chemických sloučenin. Tento děj se nazývá chemická reakce, kdy z výchozích látek (reaktantů) vznikají nové látky (produkty).
METODY ČIŠTĚNÍ ORGANICKÝCH LÁTEK Chemické sloučeniny se připravují z jiných chemických sloučenin. Tento děj se nazývá chemická reakce, kdy z výchozích látek (reaktantů) vznikají nové látky (produkty).
 LEKCE 5 Krystalizace separace složek homogenních směsí - krystalizace druhy krystalizace: volná krystalizace rušená krystalizace frakční krystalizace krystalizace změnou složení rozpouštědla vykrývání
LEKCE 5 Krystalizace separace složek homogenních směsí - krystalizace druhy krystalizace: volná krystalizace rušená krystalizace frakční krystalizace krystalizace změnou složení rozpouštědla vykrývání
téma: Halogeny-úvod autor: Ing. František Krejčí, CSc. cíl praktika: žáci si osvojí znalosti z chemie halogenů doba trvání: 2 h
 téma: Halogeny-úvod cíl praktika: žáci si osvojí znalosti z chemie halogenů pomůcky: psací potřeby popis aktivit: Žáci si osvojí problematiku halogenů, popíší jejich elektronovou konfiguraci a z ní vyvodí
téma: Halogeny-úvod cíl praktika: žáci si osvojí znalosti z chemie halogenů pomůcky: psací potřeby popis aktivit: Žáci si osvojí problematiku halogenů, popíší jejich elektronovou konfiguraci a z ní vyvodí
PLASTY A SYNTETICKÁ VLÁKNA
 PLASTY A SYNTETICKÁ VLÁKNA Autor: Mgr. Stanislava Bubíková Datum (období) tvorby: 15. 1. 2013 Ročník: devátý Vzdělávací oblast: Člověk a příroda / Chemie / Chemie a společnost 1 Anotace: Žáci se seznámí
PLASTY A SYNTETICKÁ VLÁKNA Autor: Mgr. Stanislava Bubíková Datum (období) tvorby: 15. 1. 2013 Ročník: devátý Vzdělávací oblast: Člověk a příroda / Chemie / Chemie a společnost 1 Anotace: Žáci se seznámí
Stanovení kritické micelární koncentrace
 Stanovení kritické micelární koncentrace TEORIE KONDUKTOMETRIE Měrná elektrická vodivost neboli konduktivita je fyzikální veličinou, která popisuje schopnost látek vést elektrický proud. Látky snadno vedoucí
Stanovení kritické micelární koncentrace TEORIE KONDUKTOMETRIE Měrná elektrická vodivost neboli konduktivita je fyzikální veličinou, která popisuje schopnost látek vést elektrický proud. Látky snadno vedoucí
Sada lexsolar Palivový článek Obj. číslo:
 Sada lexsolar Palivový článek Obj. číslo: 1142006 Strana 1 ze 32 Schéma uložení pomůcek sady lexsolar-biofuel Large 1 L2-06-079 Hustoměr 5 L2-06-076 Kvasný uzávěr 2 3xL2-06-085 Pasteurova pipeta 6 L2-06-084
Sada lexsolar Palivový článek Obj. číslo: 1142006 Strana 1 ze 32 Schéma uložení pomůcek sady lexsolar-biofuel Large 1 L2-06-079 Hustoměr 5 L2-06-076 Kvasný uzávěr 2 3xL2-06-085 Pasteurova pipeta 6 L2-06-084
MAKROMOLEKULÁRNÍ LÁTKY
 MAKROMOLEKULÁRNÍ LÁTKY 1. Základní pojmy - makromolekulární látky = molekulové systémy složené z velkého počtu atomů, které jsou vázány chemickou vazbou do dlouhých řetězců - řetězce jsou tvořeny stavebními
MAKROMOLEKULÁRNÍ LÁTKY 1. Základní pojmy - makromolekulární látky = molekulové systémy složené z velkého počtu atomů, které jsou vázány chemickou vazbou do dlouhých řetězců - řetězce jsou tvořeny stavebními
Makromolekulární látky
 Makromolekulární látky Učební texty k výuce chemie školní rok 2016/2017 Makromolekuly látky složené z velkého počtu atomů vázaných chemickými vazbami do dlouhých řetězců látky s velkou relativní molekulovou
Makromolekulární látky Učební texty k výuce chemie školní rok 2016/2017 Makromolekuly látky složené z velkého počtu atomů vázaných chemickými vazbami do dlouhých řetězců látky s velkou relativní molekulovou
Název: Deriváty uhlovodíků II S N 1, S N 2
 Název: Deriváty uhlovodíků II S N 1, S N 2 Autor: Mgr. Štěpán Mička Název školy: Gymnázium Jana Nerudy, škola hl. města Prahy Předmět, mezipředmětové vztahy: chemie, fyzika Ročník: 4. Tématický celek:
Název: Deriváty uhlovodíků II S N 1, S N 2 Autor: Mgr. Štěpán Mička Název školy: Gymnázium Jana Nerudy, škola hl. města Prahy Předmět, mezipředmětové vztahy: chemie, fyzika Ročník: 4. Tématický celek:
LEPIDLA POUŽÍVANÁ V MUZEJNÍ PRAXI A PRO KONZERVOVÁNÍ A RESTAUROVÁNÍ
 LEPIDLA POUŽÍVANÁ V MUZEJNÍ PRAXI A PRO KONZERVOVÁNÍ A RESTAUROVÁNÍ Lepení se jako účinná technika spojování materiálů, pouţívá jiţ více neţ 6000 let. Zpočátku se pouţívaly pouze přírodní látky, zejména
LEPIDLA POUŽÍVANÁ V MUZEJNÍ PRAXI A PRO KONZERVOVÁNÍ A RESTAUROVÁNÍ Lepení se jako účinná technika spojování materiálů, pouţívá jiţ více neţ 6000 let. Zpočátku se pouţívaly pouze přírodní látky, zejména
Hydroxidy a indikátory demonstrační
 název typ: zařazení: Pomůcky: Chemikálie: Postup: pozorování rovnice, vysvětlení Hydroxidy a indikátory demonstrační Hydroxidy. Indikátory. 3 zkumavky, kapátko NaOH(C), fenolftalein, lakmus, ph papírek
název typ: zařazení: Pomůcky: Chemikálie: Postup: pozorování rovnice, vysvětlení Hydroxidy a indikátory demonstrační Hydroxidy. Indikátory. 3 zkumavky, kapátko NaOH(C), fenolftalein, lakmus, ph papírek
Inovace bakalářského studijního oboru Aplikovaná chemie CZ.1.07/2.2.00/15.0247
 Papírová a tenkovrstvá chromatografie Jednou z nejrozšířenějších analytických metod je bezesporu chromatografie, umožňující účinnou separaci látek nutnou pro spolehlivou identifikaci a kvantifikaci složek
Papírová a tenkovrstvá chromatografie Jednou z nejrozšířenějších analytických metod je bezesporu chromatografie, umožňující účinnou separaci látek nutnou pro spolehlivou identifikaci a kvantifikaci složek
215.1.12 STANOVENÍ PARAMETRŮ TĚŽKÝCH TOPNÝCH OLEJŮ
 215.1.12 STANOVENÍ PARAMETRŮ TĚŽKÝCH TOPNÝCH OLEJŮ ÚVOD V minulosti patřily topné oleje mezi nejmasovější ropné výrobky tvořící téměř 50 % ze zpracované ropy. S rozvojem plynofikace se však jejich význam
215.1.12 STANOVENÍ PARAMETRŮ TĚŽKÝCH TOPNÝCH OLEJŮ ÚVOD V minulosti patřily topné oleje mezi nejmasovější ropné výrobky tvořící téměř 50 % ze zpracované ropy. S rozvojem plynofikace se však jejich význam
Polymery lze rozdělit podle několika kritérií. Podle původu rozlišujeme polymery přírodní a syntetické. Přírodní polymery jsou:
 MAKROMOLEKULÁRNÍ LÁTKY (POLYMERY) Makromolekuly jsou molekulové systémy složené z velkého počtu atomů vázaných chemickými vazbami do dlouhých řetězců. Tyto řetězce tvoří pravidelně se opakující části,
MAKROMOLEKULÁRNÍ LÁTKY (POLYMERY) Makromolekuly jsou molekulové systémy složené z velkého počtu atomů vázaných chemickými vazbami do dlouhých řetězců. Tyto řetězce tvoří pravidelně se opakující části,
Název: Deriváty uhlovodíků karbonylové sloučeniny
 Název: Deriváty uhlovodíků karbonylové sloučeniny Autor: Mgr. Štěpán Mička Název školy: Gymnázium Jana Nerudy, škola hl. města Prahy Předmět, mezipředmětové vztahy: chemie, fyzika Ročník: 4. Tématický
Název: Deriváty uhlovodíků karbonylové sloučeniny Autor: Mgr. Štěpán Mička Název školy: Gymnázium Jana Nerudy, škola hl. města Prahy Předmět, mezipředmětové vztahy: chemie, fyzika Ročník: 4. Tématický
Návod k laboratornímu cvičení. Cukry(sacharidy)
 Návod k laboratornímu cvičení Cukry(sacharidy) Úkol č. 1: Odlišení glukosy a fruktosy Pomůcky: zkumavky, lžička na chemikálie, kádinka, stojan, držák, kruh, síťka, plynový kahan, zápalky Chemikálie: fruktosa,
Návod k laboratornímu cvičení Cukry(sacharidy) Úkol č. 1: Odlišení glukosy a fruktosy Pomůcky: zkumavky, lžička na chemikálie, kádinka, stojan, držák, kruh, síťka, plynový kahan, zápalky Chemikálie: fruktosa,
215.1.9 - REKTIFIKACE DVOUSLOŽKOVÉ SMĚSI, VÝPOČET ÚČINNOSTI
 215.1.9 - REKTIFIKACE DVOUSLOŽKOVÉ SMĚSI, VÝPOČET ÚČINNOSTI ÚVOD Rektifikace je nejčastěji používaným procesem pro separaci organických látek. Je široce využívána jak v chemické laboratoři, tak i v průmyslu.
215.1.9 - REKTIFIKACE DVOUSLOŽKOVÉ SMĚSI, VÝPOČET ÚČINNOSTI ÚVOD Rektifikace je nejčastěji používaným procesem pro separaci organických látek. Je široce využívána jak v chemické laboratoři, tak i v průmyslu.
EU peníze středním školám digitální učební materiál
 EU peníze středním školám digitální učební materiál Číslo projektu: Číslo a název šablony klíčové aktivity: Tematická oblast, název DUMu: Autor: CZ.1.07/1.5.00/34.0515 III/2 Inovace a zkvalitnění výuky
EU peníze středním školám digitální učební materiál Číslo projektu: Číslo a název šablony klíčové aktivity: Tematická oblast, název DUMu: Autor: CZ.1.07/1.5.00/34.0515 III/2 Inovace a zkvalitnění výuky
Návod k laboratornímu cvičení. Alkaloidy a steroidy
 Návod k laboratornímu cvičení Úkol č. 1: Sublimace kofeinu Alkaloidy a steroidy Pomůcky: 2 hodinová sklíčka, elektrický vařič, siťka, stojan s kruhem, filtrační papír Chemikálie: suché čajové lístky (černý,
Návod k laboratornímu cvičení Úkol č. 1: Sublimace kofeinu Alkaloidy a steroidy Pomůcky: 2 hodinová sklíčka, elektrický vařič, siťka, stojan s kruhem, filtrační papír Chemikálie: suché čajové lístky (černý,
Vzdělávací oblast: Člověk a příroda Vzdělávací obor (předmět): Chemie - ročník: PRIMA
 Směsi Látky a jejich vlastnosti Předmět a význam chemie Vzdělávací oblast: Člověk a příroda Vzdělávací obor (předmět): Chemie - ročník: PRIMA Téma Učivo Výstupy Kódy Dle RVP Školní (ročníkové) PT K Předmět
Směsi Látky a jejich vlastnosti Předmět a význam chemie Vzdělávací oblast: Člověk a příroda Vzdělávací obor (předmět): Chemie - ročník: PRIMA Téma Učivo Výstupy Kódy Dle RVP Školní (ročníkové) PT K Předmět
LABORATOŘ ANALÝZY POTRAVIN A PŘÍRODNÍCH PRODUKTŮ
 LABORATOŘ ANALÝZY POTRAVIN A PŘÍRODNÍCH PRODUKTŮ Stanovení monosacharidů a oligosacharidů (metoda titrace po inverzi) Garant úlohy: Ing. Lucie Drábová, Ph.D. OBSAH Základní požadované znalosti pro vstupní
LABORATOŘ ANALÝZY POTRAVIN A PŘÍRODNÍCH PRODUKTŮ Stanovení monosacharidů a oligosacharidů (metoda titrace po inverzi) Garant úlohy: Ing. Lucie Drábová, Ph.D. OBSAH Základní požadované znalosti pro vstupní
Ústřední komise Chemické olympiády. 42. ročník. KRAJSKÉ KOLO Kategorie D. SOUTĚŽNÍ ÚLOHY TEORETICKÉ ČÁSTI Časová náročnost: 60 minut
 Ústřední komise Chemické olympiády 42. ročník 2005 2006 KRAJSKÉ KOLO Kategorie D SOUTĚŽNÍ ÚLOHY TEORETICKÉ ČÁSTI Časová náročnost: 60 minut Institut dětí a mládeže Ministerstva školství, mládeže a tělovýchovy
Ústřední komise Chemické olympiády 42. ročník 2005 2006 KRAJSKÉ KOLO Kategorie D SOUTĚŽNÍ ÚLOHY TEORETICKÉ ČÁSTI Časová náročnost: 60 minut Institut dětí a mládeže Ministerstva školství, mládeže a tělovýchovy
Sešit pro laboratorní práci z chemie
 Sešit pro laboratorní práci z chemie téma: Důkaz C, H, N a halogenů v organických sloučeninách autor: ing. Alena Dvořáková vytvořeno při realizaci projektu: Inovace školního vzdělávacího programu biologie
Sešit pro laboratorní práci z chemie téma: Důkaz C, H, N a halogenů v organických sloučeninách autor: ing. Alena Dvořáková vytvořeno při realizaci projektu: Inovace školního vzdělávacího programu biologie
Pracovní postupy k experimentům s využitím PC
 Inovace profesní přípravy budoucích učitelů chemie CZ..07/2.2.00/5.0324 Prof. PhDr. Martin Bílek, Ph.D. Pracovní postupy k experimentům s využitím PC (teplotní čidlo Vernier propojeno s PC) Stanovení tepelné
Inovace profesní přípravy budoucích učitelů chemie CZ..07/2.2.00/5.0324 Prof. PhDr. Martin Bílek, Ph.D. Pracovní postupy k experimentům s využitím PC (teplotní čidlo Vernier propojeno s PC) Stanovení tepelné
H H C C C C C C H CH 3 H C C H H H H H H
 Alkany a cykloalkany sexta Martin Dojiva uhlovodíky obsahující pouze jednoduché vazby obecný vzorec alkanů: C n 2n+2 cykloalkanů: C n 2n homologický přírůstek C 2 Dělení alkanů přímé větvené u větvených
Alkany a cykloalkany sexta Martin Dojiva uhlovodíky obsahující pouze jednoduché vazby obecný vzorec alkanů: C n 2n+2 cykloalkanů: C n 2n homologický přírůstek C 2 Dělení alkanů přímé větvené u větvených
