Název: Konstrukce hasicího přístroje
|
|
|
- Ondřej Havlíček
- před 9 lety
- Počet zobrazení:
Transkript
1 Název: Konstrukce hasicího přístroje Téma: Organické plyny Úroveň: střední škola Tematický celek: Látky a jejich přeměny, makrosvět přírody Výukové materiály Předmět (obor): chemie Doporučený věk žáků: let Doba trvání: 2 vyučovací hodiny Specifický cíl: aplikace teoretických znalostí a logického myšlení při sestrojování funkčního hasicího přístroje Seznam potřebného materiálu: Demonstrační experiment 1: Chemikálie: práškový zinek, dusičnan amonný, chlorid amonný, voda Pomůcky: třecí miska s tloučkem, velká nehořlavá podložka, pipeta, ocelová miska, váhy Demonstrační experiment 2: Chemikálie: manganistan draselný, koncentrovaná kyselina sírová Pomůcky: pinzeta, lžička, čtverečky buničiny, tyčinka, hodinové sklo, kádinka, kapátko (pipeta) Demonstrační experiment 3: Chemikálie: hydrogenuhličitan sodný, kyselina octová Pomůcky: zkumavka, lžička, pipeta Badatelská činnost konstrukce hasicího přístroje: Chemikálie: kyselina octová (kuchyňský ocet), hydrogenuhličitan sodný (kypřící prášek), jar, voda Pomůcky: PET lahve (1,5l; 0,5l), zkumavky, lepicí pásky, brčka, hadice (čím více materiálu, tím lépe) Seznam praktických (badatelských) aktivit: Konstrukce hasicího přístroje Zjištění takového poměru výchozích látek, aby přístroj byl co nejúčinnější
2 Anotace: Jako motivace pro laboratorní práci byly zvoleny dva demonstrační experimenty zapalování vodou a zapalování oxidem manganistým, které ukazují netradiční způsoby zapalování ohně. V rámci samotných laboratorních prací je řešen problém opačný jak oheň uhasit. Žáci mají za úkol sestrojit a ozkoušet svůj vlastní hasicí přístroj, založený na principu jednoduché chemické reakce. Tuto reakci uvidí ve třetím demonstračním pokusu. Mají navrhnout způsob, jakým zajistí nejúčinnější poměr výchozích látek reakce. Harmonogram výuky: náplň práce Čas potřebné vybavení a pomůcky činnost učitele činnosti žáků Úvod do tématu motivace Demonstrační experimenty 1 a 2 5 min. diskuze 10 min. provedení experimentu Třecí miska s tloučkem, velká nehořlavá podložka, pipeta, ocelová miska, váhy; zinek, NH 4 NO 3, NH 4 Cl Provádí demonstrační experiment. Řídí diskuzi s žáky. Diskutují s učitelem, pozorují demonstrační experiment. Předlaboratorní příprava Práce s textem a pracovním listem. Demonstrační experiment 3 20 min. Kartičky s charakteristikami hasicích přístrojů; pracovní listy pro žáky; NaHCO 3, CH 3 COOH Kontroluje přiřazování charakteristik hasicích přístrojů; demonstruje a vysvětluje reakci. Přiřazují charakteristiky k jednotlivým typům hasicích přístrojů, pozorují demonstrační reakci. Praktická (badatelská) činnost Konstrukce hasicího přístroje 40 min. PET láhve, brčka, hadice, lepicí páska, vrták, malé zkumavky Kontroluje práci žáků, v případě potřeby pomáhá, odpovídá na otázky. Konstruují hasicí přístroj a vylepšují ho. Vyhodnocení výsledků Prezentace hasicího přístroje 15 min. Pracovní listy Hodnotí prezentaci, doplňuje, pokládá otázky. Prezentují své výsledky. Prezentace výsledků Závěrečná diskuze: Co se žákům podařilo. Co je překvapilo. 5 min. Pracovní listy Klade žákům kontrolní otázky a vyhodnocuje správnost odpovědí. Formulují závěry laboratorní práce. Domácí úkol pro žáky: Není.
3 Přípravy pro učitele Úvod do tématu motivace Učitel položí žákům otázku: Jakým způsobem se dá rozdělat oheň? Žáci budou postupně říkat svoje nápady (zapalovač, sirky, třít dřevo o dřevo, lupa atd.). Pak se učitel zeptá, zda je možné zapalovat vzduchem? Žáci pravděpodobně odpovědí, že ne. Učitel může jako zajímavost přednést následující příběh. Slavný německý vědec a vynálezce Carl von Linde během svých cest po Malajsii zpozoroval fascinující metodu zapalování ohně. Tamní domorodci používali k rozdělávání ohně primitivní zapalovač pracující na principu stlačení vzduchu. Domorodec si vzal dutou bambusovou tyčku, která byla na jednom konci zaslepena, a druhou dřevěnou tyčku, která přesně zapadala do dutiny první tyčky. Na konec dřevěné tyčky připevnil suchou trávu. Poté rychlým pohybem zasunul dřevěnou tyčku s trávou do duté bambusové tyčky. Jeho počínáním došlo k rychlému stlačení vzduchu v bambusu, což způsobilo zapálení suché trávy na konci dřevěné tyčky. Vysvětlení tohoto principu není vůbec složité. Vzduch uvnitř bambusu je složen především z molekul plynného dusíku a kyslíku. Tyto molekuly mají samozřejmě určitou energii, která se projevuje jejich pohybem a vzájemnými srážkami molekul mezi sebou i se stěnami bambusové tyčky. Čím víc srážek mezi molekulami, tím vyšší je teplota. Prudkým stlačením vzduchu prudce vzroste teplota až na takovou míru, že se suchá tráva samovznítí. Když se Linde vrátil ze svých cest zpět domů do Německa, přivezl si s sebou svůj nový objev a ukázal jej jednomu ze svých studentů, kteří pracovali v jeho laboratoři v Mnichově. Tím studentem nebyl nikdo jiný než později velmi slavný Rudolf Diesel, který převzal tento velice jednoduchý princip a vyvinul z něj tzv. Dieselův motor. Ten využívá stlačení vzduchu k tomu, aby se vznítila palivová směs, která do motoru přichází. Tento motor má nejvyšší tepelnou účinnost ze všech spalovacích motorů. K zapálení nepotřebuje elektrické svíčky, a proto má vyšší spolehlivost. Použité palivo tedy nafta méně poškozuje písty i válce motoru, který má proto i vyšší životnost. Nyní se učitel zeptá, zda je možné zapalovat vodou? Žáci pravděpodobně opět odpovědí, že ne, a učitel předvede demonstrační experiment Zapalování vodou (viz návody pro učitele). Tento experiment je lepší ponechat ryze jako demonstrační a motivační, protože jeho mechanismus přesahuje středoškolskou látku. Po předvedení experimentu učitel žákům sdělí, že dnes se zabývali rozděláváním ohně, ale v laboratorním cvičení budou řešit hašení ohně. Druhý experiment, který může posloužit jako demonstrační v motivačním úvodu hodiny, je Zapalování oxidem manganistým (popsán níže).
4 Demonstrační experiment 1: Zapalování vodou Chemikálie: práškový zinek, dusičnan amonný, chlorid amonný, voda Pomůcky: třecí miska s tloučkem, velká nehořlavá podložka, pipeta, ocelová miska, váhy Postup: 4 g práškového zinku opatrně smícháme se 4 g rozetřeného dusičnanu amonného a 1 g chloridu amonného. Do směsi je dobré přidat smotek vaty podporující hoření. Směs v misce přemístíme na nehořlavou podložku. Kapkou vody iniciujeme reakci. Vysvětlení: Jedná se o vodou katalyzovanou reakci, při které se rozkládá dusičnan amonný, uvolňuje se teplo a práškový zinek shoří. Chloridový anion Cl - z NH 4 Cl působí v následující reakci jako katalyzátor rozkladu NH 4 NO 3. NH 4 NO 3 (s) N 2 O (g) + 2H 2 O (aq). Voda v reakci zapříčiní rozklad dalšího NH 4 NO 3, což má za následek autokatalytický efekt. Produkty první reakce umožňují oxidaci zinku. Souhrnná reakce potom je: Zn (s) + NH 4 NO 3 (s) N 2 (g) + ZnO (s) + 2 H 2 O (g). Poznámky: 1. Všechny chemikálie musí být suché, jinak hrozí spontánní reakce. Reakce poměrně prská, proto by měla být nehořlavá podložka dostatečně velká. 2. Většího efektu lze dosáhnout použitím ledové kostky jako iniciátoru reakce. Demonstrační experiment 2: Zapalování oxidem manganistým Chemikálie: manganistan draselný, koncentrovaná kyselina sírová Pomůcky: pinzeta, lžička, čtverečky buničiny nebo kousek vaty, tyčinka, hodinové sklo, kádinka, kapátko (pipeta) Postup: Na hodinové sklíčko umístíme asi polovinu lžičky manganistanu draselného, který následně přelijeme malým množstvím koncentrované kyseliny sírové. Reakční směs by měla získat tmavě zelenou barvu. Poté za pomocí pinzety ke směsi přiblížíme čtvereček buničiny nebo malý kousek vaty, který se samovolně vznítí. Je lepší použít opravdu malé množství vaty nebo buničiny, třída se jinak zaplní všudypřítomnými sazemi. Vysvětlení: Reakcí koncentrované kyseliny sírové a manganistanu draselného vzniká oxid manganistý, (tmavě zelená kapalina; t. t. 5,9 C), podle reakce: 2 KMnO H 2 SO 4 Mn 2 O 7 + H 2 O + 2 KHSO 4. Meziproduktem je kyselina manganistá, která ale okamžitě podléhá dehydrataci. Oxid manganistý je silné oxidační činidlo, snadno podléhá rozkladu na oxid manganičitý a kyslík. Jako vedlejší produkt vzniká ozón. Tyto produkty jsou schopny zapálit organické látky (buničinu, vatu atd.). Poznámky: 1. Reakce je intenzivní a prská, proto je nutné ji provádět na nehořlavé podložce v digestoři a zajistit dostatečný odstup žáků od demonstračního experimentu. 2. Likvidace odpadu: Sklíčko se zbylým oxidem manganistým a odpadními produkty dát do většího množství vody (oxid manganistý se přemění zpátky na manganistan, zbylá kyselina se naředí) a poté lze směs vylít do výlevky.
5 Předlaboratorní příprava Učitel rozdá žákům kartičky s charakteristikami různých hasicích náplní. (Tabulka, kterou musí učitel před hodinou rozstříhat, je součástí pracovních listů pro žáky.) Úkolem žáků je přiřazovat správné charakteristiky, náplně, výhody a nevýhody k jednotlivým typům hasicích přístrojů. Žáci získají správným přiřazením tabulku charakteristik jednotlivých hasicích přístrojů, kterou si po společném zkontrolování mohou nalepit na papír a přidat k pracovnímu listu. Po sestavení tabulky předvede učitel třetí demonstrační experiment. Žáci pak na základě pozorování napíší do pracovních listů rovnici reakce a uvedou poměr, v jakém výchozí látky reagují. Demonstrační experiment 3: Reakce hydrogenuhličitanu sodného s kyselinou octovou Chemikálie: hydrogenuhličitan sodný, kyselina octová nebo kuchyňský ocet Pomůcky: zkumavka, lžička, pipeta, případně jar Provedení záleží na učiteli. Do zkumavky lze umístit lžičku hydrogenuhličitanu sodného a poté z pipety přikápnout kyselinu octovou, nebo kuchyňský ocet. V jiném uspořádání je možné nejdříve hydrogenuhličitan rozpustit ve vodě v Erlenmayerově baňce, popř. jako nápovědu pro žáky přidat jar pro tvorbu bublin a až poté přikápnout kyselinu octovou. Praktická badatelská činnost (laboratorní práce) Žáci budou mít za úkol ve svých pracovních skupinách na základě pozorované reakce sestrojit hasicí přístroj. Po sestrojení hasicího přístroje a určení nejvhodnějších výchozích poměrů látek bude mít pracovní skupina za úkol svůj přístroj krátce prezentovat před ostatními. Chemikálie: kyselina octová (z bezpečnostních důvodů nepoužíváme ledovou kyselinu, ale zředíme ji vodou v poměru 1:1), kuchyňský ocet, hydrogenuhličitan sodný (kypřící prášek), jar Pomůcky: PET lahve (1,5l; 0,5l), zkumavky, lepicí pásky, brčka, hadice (čím více materiálu, tím lépe, aby si žáci měli z čeho vybrat a nesestavovali hasicí přístroj jako skládačku) Autorské řešení PL: 1. NaHCO 3 + CH 3 COOH CH 3 COO - Na + + H 2 O + CO 2 2. Výchozí látky reagují v poměru 1 : 1. Jedná se o molární poměr. 3. Jedna z možností, jak postupovat: Do víčka opatrně nůžkami vyvrtáme otvor a zasuneme hadici. Do 1,5 l PET lahve umístíme 8 g hydrogenuhličitanu sodného rozpuštěného ve 300 ml vody, pro lepší pěnění přikápneme trochu jaru, poté opatrně zasuneme na drátku přivázanou zkumavku naplněnou zředěnou kyselinou octovou (cca 5 cm výšky zkumavky) tak, aby se oba roztoky nedostaly do kontaktu. Víčko s hadicí zašroubujeme, čímž je hasicí přístroj připraven. Prudkým trhnutím s hasicím přístrojem převrhneme uvnitř umístěnou zkumavku s kyselinou octovou, rychle promícháme a spustíme tak reakci. Začne vznikat mohutná pěna, kterou hadicí směřujeme do výlevky. 4. Hydrogenuhličitan sodný reaguje s kyselinou octovou v poměru 1 : 1. Na 1 mol kyseliny potřebuji tedy 1 mol hydrogenuhličitanu. Např. 10 g kyseliny zreaguje stechiometricky s 14 g hydrogenuhličitanu sodného. (10 g kyseliny představuje 0,1665 molů. Toto množství je podle vztahu n=m/m 14 g hydrogenuhličitanu.) 5. Při reakci kyseliny octové s hydrogenuhličitanem sodným se uvolňuje oxid uhličitý, který probublává roztokem a tvoří pěnu (pro lepší pěnění je přidán jar). Ta slouží jako hasicí látka.
6 Obr. 1: Zkonstruovaný hasicí přístroj Obr. 2: Materiál potřebný pro konstrukci hasicího přístroje. Chemikálie: jar, ledová kyselina octová, hydrogenuhličitan sodný, voda, dále z pomůcek: zkumavka s přivázaným drátkem pro manipulaci a PET láhev s víčkem, do kterého je utěsněna hadice
7 Závěrečné poznámky Jiné varianty a další možné úpravy či doporučení: V rámci motivačního teoretického úvodu lze zařadit následující témata: podmínky hoření, rozdíl mezi hořením a požárem, druhy hořlavin v domácnosti a zásady chování při vypuknutí požáru. Různé hořlaviny a zásady chování při požáru žáky zpravidla velmi zaujmou. Třetí demonstrační experiment lze uspořádat jako sopku (reakce roztoku sody, jaru a octa v Erlenmayerově baňce). Takový pokus demonstruje pěkně průběh reakce v hasicím přístroji a je dobrý pro interpretaci reakce. Reflexe po hodině: Při sestrojování hasicího přístroje by měl učitel pouze poskytnout žákům materiál a chemikálie a dále jejich práci neřídit. Na základě pozorované reakce a vlastní kreativity by měli být žáci schopni hasicí přístroj sestrojit samostatně. Pokud budou žáci používat na výrobu hasicího přístroje 0,5l PET láhve, je lepší použít pro odvod pěny brčko. Pozor: Čím je použitá kyselina octová koncentrovanější, tím je reakce bouřlivější. Toho lze vhodně využít při třetím demonstračním pokusu. Tato laboratorní práce předpokládá znalost výpočtů z chemické rovnice. Pokud se žáci ještě výpočty z rovnic neučili, je možné jim vhodný poměr výchozích látek napovědět. Nebo mohou žáci zvolit nejúčinnější poměr postupným zkoušením různých množství kyseliny a hydrogenuhličitanu. Navazující a rozšiřující aktivity: Úlohu je možné rozšířit např. různými závody mezi hasicími přístroji (který má nejsilnější proud, který se spustí jako první, atd.). Možno doplnit dalšími výpočty, např.: Kolik litrů oxidu uhličitého použitou reakcí vznikne?
Laboratorní cvičení z kinetiky chemických reakcí
 Laboratorní cvičení z kinetiky chemických reakcí LABORATORNÍ CVIČENÍ 1. Téma: Ovlivňování průběhu reakce změnou koncentrace látek. podmínek průběhu reakce. Jednou z nich je změna koncentrace výchozích
Laboratorní cvičení z kinetiky chemických reakcí LABORATORNÍ CVIČENÍ 1. Téma: Ovlivňování průběhu reakce změnou koncentrace látek. podmínek průběhu reakce. Jednou z nich je změna koncentrace výchozích
Název: Exotermní reakce
 Název: Exotermní reakce Autor: Mgr. Jiří Vozka, Ph.D. Název školy: Gymnázium Jana Nerudy, škola hl. města Prahy Předmět, mezipředmětové vztahy: chemie, fyzika Ročník: 3. Tématický celek: Kovy či redoxní
Název: Exotermní reakce Autor: Mgr. Jiří Vozka, Ph.D. Název školy: Gymnázium Jana Nerudy, škola hl. města Prahy Předmět, mezipředmětové vztahy: chemie, fyzika Ročník: 3. Tématický celek: Kovy či redoxní
Název: Exotermický a endotermický děj
 Název: Exotermický a endotermický děj Téma: Exotermický a endotermický děj Úroveň: 2. stupeň ZŠ Tematický celek: Tradiční a nové způsoby využití energie Výukové materiály Předmět (obor): chemie Doporučený
Název: Exotermický a endotermický děj Téma: Exotermický a endotermický děj Úroveň: 2. stupeň ZŠ Tematický celek: Tradiční a nové způsoby využití energie Výukové materiály Předmět (obor): chemie Doporučený
Název: Fyzikální a chemický děj Výukové materiály
 Název: Fyzikální a chemický děj Výukové materiály Téma: Fyzikální a chemický děj Úroveň: 2. stupeň ZŠ Tematický celek: Materiály a jejich přeměny Předmět (obor): chemie Doporučený věk žáků: 13 14 let Doba
Název: Fyzikální a chemický děj Výukové materiály Téma: Fyzikální a chemický děj Úroveň: 2. stupeň ZŠ Tematický celek: Materiály a jejich přeměny Předmět (obor): chemie Doporučený věk žáků: 13 14 let Doba
Spektrofotometrické stanovení fosforečnanů ve vodách
 Spektrofotometrické stanovení fosforečnanů ve vodách Úkol: Spektrofotometricky stanovte obsah fosforečnanů ve vodě Chemikálie: 0,07165 g dihydrogenfosforečnan draselný KH 2 PO 4 75 ml kyselina sírová H
Spektrofotometrické stanovení fosforečnanů ve vodách Úkol: Spektrofotometricky stanovte obsah fosforečnanů ve vodě Chemikálie: 0,07165 g dihydrogenfosforečnan draselný KH 2 PO 4 75 ml kyselina sírová H
Název: Barvy chromu. Autor: Mgr. Jiří Vozka, Ph.D. Název školy: Gymnázium Jana Nerudy, škola hl. města Prahy
 Název: Barvy chromu Autor: Mgr. Jiří Vozka, Ph.D. Název školy: Gymnázium Jana Nerudy, škola hl. města Prahy Předmět, mezipředmětové vztahy: chemie, biologie Ročník: 3. Tématický celek: Systematická anorganická
Název: Barvy chromu Autor: Mgr. Jiří Vozka, Ph.D. Název školy: Gymnázium Jana Nerudy, škola hl. města Prahy Předmět, mezipředmětové vztahy: chemie, biologie Ročník: 3. Tématický celek: Systematická anorganická
Název školy: Gymnázium Jana Nerudy, škola hl. města Prahy
 Název: xidy dusíku Autor: Mgr. Štěpán Mička Název školy: Gymnázium Jana Nerudy, škola hl. města Prahy Předmět, mezipředmětové vztahy: chemie, fyzika, Ročník: 3. Tématický celek: Systematická anorganická
Název: xidy dusíku Autor: Mgr. Štěpán Mička Název školy: Gymnázium Jana Nerudy, škola hl. města Prahy Předmět, mezipředmětové vztahy: chemie, fyzika, Ročník: 3. Tématický celek: Systematická anorganická
POPIS VÝUKOVÉ AKTIVITY (METODICKÝ LIST):
 POPIS VÝUKOVÉ AKTIVITY (METODICKÝ LIST): Název výukové aktivity: Faraónův had dvěma způsoby Vyučovací předmět: Technický kroužek. Anotace: Úkolem žáků je vytvořit efektní pokusy založené na chemických
POPIS VÝUKOVÉ AKTIVITY (METODICKÝ LIST): Název výukové aktivity: Faraónův had dvěma způsoby Vyučovací předmět: Technický kroužek. Anotace: Úkolem žáků je vytvořit efektní pokusy založené na chemických
Název: Archimédův zákon pro plyny
 Název: Archimédův zákon pro plyny Téma: Mechanika kapalin a plynů Úroveň: střední škola Tematický celek: Látky a jejich přeměny, makrosvět přírody Výukové materiály Předmět (obor): fyzika Doporučený věk
Název: Archimédův zákon pro plyny Téma: Mechanika kapalin a plynů Úroveň: střední škola Tematický celek: Látky a jejich přeměny, makrosvět přírody Výukové materiály Předmět (obor): fyzika Doporučený věk
Název: Halogeny I. Autor: Mgr. Štěpán Mička. Název školy: Gymnázium Jana Nerudy, škola hl. města Prahy
 Název: Halogeny I Autor: Mgr. Štěpán Mička Název školy: Gymnázium Jana Nerudy, škola hl. města Prahy Předmět, mezipředmětové vztahy: chemie, fyzika, biologie Ročník: 3. Tématický celek: Systematická anorganická
Název: Halogeny I Autor: Mgr. Štěpán Mička Název školy: Gymnázium Jana Nerudy, škola hl. města Prahy Předmět, mezipředmětové vztahy: chemie, fyzika, biologie Ročník: 3. Tématický celek: Systematická anorganická
CHEMICKÉ REAKCE A HMOTNOSTI A OBJEMY REAGUJÍCÍCH LÁTEK
 CHEMICKÉ REAKCE A HMOTNOSTI A OBJEMY REAGUJÍCÍCH LÁTEK Význam stechiometrických koeficientů 2 H 2 (g) + O 2 (g) 2 H 2 O(l) Počet reagujících částic 2 molekuly vodíku reagují s 1 molekulou kyslíku za vzniku
CHEMICKÉ REAKCE A HMOTNOSTI A OBJEMY REAGUJÍCÍCH LÁTEK Význam stechiometrických koeficientů 2 H 2 (g) + O 2 (g) 2 H 2 O(l) Počet reagujících částic 2 molekuly vodíku reagují s 1 molekulou kyslíku za vzniku
REAKCE V ORGANICKÉ CHEMII A BIOCHEMII
 REAKCE V ORGANICKÉ CHEMII A BIOCHEMII PaedDr. Ivana Töpferová Střední průmyslová škola, Mladá Boleslav, Havlíčkova 456 CZ.1.07/1.5.00/34.0861 MODERNIZACE VÝUKY Anotace: laboratorní práce z organické chemie
REAKCE V ORGANICKÉ CHEMII A BIOCHEMII PaedDr. Ivana Töpferová Střední průmyslová škola, Mladá Boleslav, Havlíčkova 456 CZ.1.07/1.5.00/34.0861 MODERNIZACE VÝUKY Anotace: laboratorní práce z organické chemie
Název: Krystalizace. Výukové materiály. Téma: Krystalizace. Úroveň: 2. stupeň ZŠ. Tematický celek: Vidět a poznat neviditelné. Předmět (obor): chemie
 Název: Krystalizace Výukové materiály Téma: Krystalizace Úroveň: 2. stupeň ZŠ Tematický celek: Vidět a poznat neviditelné Předmět (obor): chemie Doporučený věk žáků: 13 14 let Doba trvání: 2 vyučovací
Název: Krystalizace Výukové materiály Téma: Krystalizace Úroveň: 2. stupeň ZŠ Tematický celek: Vidět a poznat neviditelné Předmět (obor): chemie Doporučený věk žáků: 13 14 let Doba trvání: 2 vyučovací
VI. VÝPOČET Z CHEMICKÉ ROVNICE
 VI. VÝPOČET Z CHEMICKÉ ROVNICE ZÁKLADNÍ POJMY : Chemická rovnice (např. hoření zemního plynu): CH 4 + 2 O 2 CO 2 + 2 H 2 O CH 4, O 2 jsou reaktanty; CO 2, H 2 O jsou produkty; čísla 2 jsou stechiometrické
VI. VÝPOČET Z CHEMICKÉ ROVNICE ZÁKLADNÍ POJMY : Chemická rovnice (např. hoření zemního plynu): CH 4 + 2 O 2 CO 2 + 2 H 2 O CH 4, O 2 jsou reaktanty; CO 2, H 2 O jsou produkty; čísla 2 jsou stechiometrické
Název: Nenewtonovská kapalina
 Název: Nenewtonovská kapalina Autor: Mgr. Jiří Vozka, Ph.D. Název školy: Gymnázium Jana Nerudy, škola hl. města Prahy Předmět, mezipředmětové vztahy: chemie, biologie, fyzika Ročník: 5. Tématický celek:
Název: Nenewtonovská kapalina Autor: Mgr. Jiří Vozka, Ph.D. Název školy: Gymnázium Jana Nerudy, škola hl. města Prahy Předmět, mezipředmětové vztahy: chemie, biologie, fyzika Ročník: 5. Tématický celek:
Termochemie. Úkol: A. Určete změnu teploty při rozpouštění hydroxidu sodného B. Určete reakční teplo reakce zinku s roztokem měďnaté soli
 1. Termochemie Úkol: Určete změnu teploty při rozpouštění hydroxidu sodného B. Určete reakční teplo reakce zinku s roztokem měďnaté soli Pomůcky : a) kádinky, teploměr, odměrný válec, váženka, váhy, kalorimetr,
1. Termochemie Úkol: Určete změnu teploty při rozpouštění hydroxidu sodného B. Určete reakční teplo reakce zinku s roztokem měďnaté soli Pomůcky : a) kádinky, teploměr, odměrný válec, váženka, váhy, kalorimetr,
Jazykové gymnázium Pavla Tigrida, Ostrava-Poruba Název projektu: Podpora rozvoje praktické výchovy ve fyzice a chemii
 Datum: Jazykové gymnázium Pavla Tigrida, Ostrava-Poruba Název projektu: Podpora rozvoje praktické výchovy ve fyzice a chemii Laboratorní cvičení č. Tlak vzduchu: Teplota vzduchu: Vodík a kyslík Vlhkost
Datum: Jazykové gymnázium Pavla Tigrida, Ostrava-Poruba Název projektu: Podpora rozvoje praktické výchovy ve fyzice a chemii Laboratorní cvičení č. Tlak vzduchu: Teplota vzduchu: Vodík a kyslík Vlhkost
Kyslík a vodík. Bezbarvý plyn, bez chuti a zápachu, asi 14krát lehčí než vzduch. Běžně tvoří molekuly H2. hydridy (např.
 1 Kyslík a vodík Kyslík Vlastnosti Bezbarvý reaktivní plyn, bez zápachu, nejčastěji tvoří molekuly O2. Kapalný kyslík je modrý. S jinými prvky tvoří sloučeniny oxidy (např. CO, CO2, SO2...) Výskyt Nejrozšířenější
1 Kyslík a vodík Kyslík Vlastnosti Bezbarvý reaktivní plyn, bez zápachu, nejčastěji tvoří molekuly O2. Kapalný kyslík je modrý. S jinými prvky tvoří sloučeniny oxidy (např. CO, CO2, SO2...) Výskyt Nejrozšířenější
Návod k laboratornímu cvičení. Efektní pokusy
 Návod k laboratornímu cvičení Efektní pokusy Úkol č. 1: Chemikova zahrádka Pomůcky: skleněná vana, lžička na chemikálie. Chemikálie: vodní sklo, síran zinečnatý ZnSO 4 (X i ), síran železnatý FeSO 4, chlorid
Návod k laboratornímu cvičení Efektní pokusy Úkol č. 1: Chemikova zahrádka Pomůcky: skleněná vana, lžička na chemikálie. Chemikálie: vodní sklo, síran zinečnatý ZnSO 4 (X i ), síran železnatý FeSO 4, chlorid
Ch - Chemické reakce a jejich zápis
 Ch - Chemické reakce a jejich zápis Autor: Mgr. Jaromír Juřek Kopírování a jakékoliv další využití výukového materiálu je povoleno pouze s uvedením odkazu na www.jarjurek.cz. VARIACE Tento dokument byl
Ch - Chemické reakce a jejich zápis Autor: Mgr. Jaromír Juřek Kopírování a jakékoliv další využití výukového materiálu je povoleno pouze s uvedením odkazu na www.jarjurek.cz. VARIACE Tento dokument byl
Obecná a anorganická chemie. Zásady a jejich neutralizace, amoniak
 Šablona č. I, sada č. 2 Vzdělávací oblast Vzdělávací obor Tematický okruh Člověk a příroda Chemie Obecná a anorganická chemie Téma Zásady a jejich neutralizace, amoniak Ročník 9. Anotace Aktivita slouží
Šablona č. I, sada č. 2 Vzdělávací oblast Vzdělávací obor Tematický okruh Člověk a příroda Chemie Obecná a anorganická chemie Téma Zásady a jejich neutralizace, amoniak Ročník 9. Anotace Aktivita slouží
Návod k laboratornímu cvičení. Alkoholy
 Úkol č. 1: Ověřování fyzikálních vlastností alkoholů Návod k laboratornímu cvičení Alkoholy Pomůcky: 3 velké zkumavky - A,B,C, hodinové sklíčko, kapátko nebo skleněná tyčinka Chemikálie: etanol (F), etan-1,2-
Úkol č. 1: Ověřování fyzikálních vlastností alkoholů Návod k laboratornímu cvičení Alkoholy Pomůcky: 3 velké zkumavky - A,B,C, hodinové sklíčko, kapátko nebo skleněná tyčinka Chemikálie: etanol (F), etan-1,2-
KDE VZÍT PLYNY? Václav Piskač, Brno 2014
 KDE VZÍT PLYNY? Václav Piskač, Brno 2014 Tento článek se zabývá možnostmi, jak pro školní experimenty s plyny získat něco jiného než vzduch. V dalším budu předpokládat, že nemáte kamarády ve výzkumném
KDE VZÍT PLYNY? Václav Piskač, Brno 2014 Tento článek se zabývá možnostmi, jak pro školní experimenty s plyny získat něco jiného než vzduch. V dalším budu předpokládat, že nemáte kamarády ve výzkumném
téma: Úvodní praktikum - Práce v laboratoři autor: Ing. Dagmar Kučerová
 téma: Úvodní praktikum - Práce v laboratoři cíl praktika: Žáci budou seznámeni s laboratorním řádem a poučeni o bezpečnosti práce. pomůcky: laboratorní řád popis aktivit: Žáci se seznámí se všemi body
téma: Úvodní praktikum - Práce v laboratoři cíl praktika: Žáci budou seznámeni s laboratorním řádem a poučeni o bezpečnosti práce. pomůcky: laboratorní řád popis aktivit: Žáci se seznámí se všemi body
I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í LABORATORNÍ PRÁCE Č. 6 PRÁCE S PLYNY
 LABORATORNÍ PRÁCE Č. 6 PRÁCE S PLYNY Mezi nejrozšířenější práce s plyny v laboratoři patří příprava a důkazy oxidu uhličitého CO 2, kyslíku O 2, vodíku H 2, oxidu siřičitého SO 2 a amoniaku NH 3. Reakcí
LABORATORNÍ PRÁCE Č. 6 PRÁCE S PLYNY Mezi nejrozšířenější práce s plyny v laboratoři patří příprava a důkazy oxidu uhličitého CO 2, kyslíku O 2, vodíku H 2, oxidu siřičitého SO 2 a amoniaku NH 3. Reakcí
Reakce kyselin a zásad
 seminář 6. 1. 2011 Chemie Reakce kyselin a zásad Známe několik teorií, které charakterizují definují kyseliny a zásady. Nejstarší je Arrheniova teorie, která je platná pro vodné prostředí, podle které
seminář 6. 1. 2011 Chemie Reakce kyselin a zásad Známe několik teorií, které charakterizují definují kyseliny a zásady. Nejstarší je Arrheniova teorie, která je platná pro vodné prostředí, podle které
Název: Exotermický a endotermický děj
 Název: Exotermický a endotermický děj 1) Kypřící prášek, skořápka či zinek s octem? Pomůcky: ocet, zinek, kypřící prášek, led, sůl, hydroxid sodný, skořápka, chlorid vápenatý, chlorid sodný, 4 větší zkumavky,
Název: Exotermický a endotermický děj 1) Kypřící prášek, skořápka či zinek s octem? Pomůcky: ocet, zinek, kypřící prášek, led, sůl, hydroxid sodný, skořápka, chlorid vápenatý, chlorid sodný, 4 větší zkumavky,
2.12 Vyvíjení CO 2 bublinky kolem nás. Projekt Trojlístek
 2. Vlastnosti látek a chemické reakce 2.12 Vyvíjení CO 2 bublinky kolem nás. Projekt úroveň 1 2 3 1. Předmět výuky Metodika je určena pro vzdělávací obsah vzdělávacího předmětu Chemie. Chemie 2. Cílová
2. Vlastnosti látek a chemické reakce 2.12 Vyvíjení CO 2 bublinky kolem nás. Projekt úroveň 1 2 3 1. Předmět výuky Metodika je určena pro vzdělávací obsah vzdělávacího předmětu Chemie. Chemie 2. Cílová
téma: Halogeny-úvod autor: Ing. František Krejčí, CSc. cíl praktika: žáci si osvojí znalosti z chemie halogenů doba trvání: 2 h
 téma: Halogeny-úvod cíl praktika: žáci si osvojí znalosti z chemie halogenů pomůcky: psací potřeby popis aktivit: Žáci si osvojí problematiku halogenů, popíší jejich elektronovou konfiguraci a z ní vyvodí
téma: Halogeny-úvod cíl praktika: žáci si osvojí znalosti z chemie halogenů pomůcky: psací potřeby popis aktivit: Žáci si osvojí problematiku halogenů, popíší jejich elektronovou konfiguraci a z ní vyvodí
Pomůcky a materiál: plastelína, talíř, lžička, lžíce, sklenice, voda, Jar, zelené potravinářské barvivo, jedlá soda, ocet
 LÁVA Typ učiva: např. Anorganická chemie Časová náročnost: 15 minut Forma: např. ukázka/skupinová práce/práce ve dvojici Pomůcky a materiál: plastelína, talíř, lžička, lžíce, sklenice, voda, Jar, zelené
LÁVA Typ učiva: např. Anorganická chemie Časová náročnost: 15 minut Forma: např. ukázka/skupinová práce/práce ve dvojici Pomůcky a materiál: plastelína, talíř, lžička, lžíce, sklenice, voda, Jar, zelené
ORGANICKÁ CHEMIE Laboratorní práce č. 4 Téma: Karbonylové sloučeniny, karboxylové kyseliny
 ORGANICKÁ CHEMIE Laboratorní práce č. 4 Téma: Karbonylové sloučeniny, karboxylové kyseliny Úkol 1: Připravte acetaldehyd. Karbonylová skupina aldehydů podléhá velmi snadno oxidaci až na skupinu karboxylovou.
ORGANICKÁ CHEMIE Laboratorní práce č. 4 Téma: Karbonylové sloučeniny, karboxylové kyseliny Úkol 1: Připravte acetaldehyd. Karbonylová skupina aldehydů podléhá velmi snadno oxidaci až na skupinu karboxylovou.
Název: Chemická kinetika - enzymy
 Název: Chemická kinetika - enzymy Autor: Mgr. Štěpán Mička Název školy: Gymnázium Jana Nerudy, škola hl. města Prahy Předmět, mezipředmětové vztahy: chemie, fyzika, biologie Ročník: 5. Tématický celek:
Název: Chemická kinetika - enzymy Autor: Mgr. Štěpán Mička Název školy: Gymnázium Jana Nerudy, škola hl. města Prahy Předmět, mezipředmětové vztahy: chemie, fyzika, biologie Ročník: 5. Tématický celek:
Návod k laboratornímu cvičení. Fenoly
 Návod k laboratornímu cvičení Fenoly Úkol č. 1: Příprava fenolátu sodného Pomůcky: váhy, kádinka, zkumavky Chemikálie: 10% roztok hydroxidu sodného NaOH (C), 5%roztok kyseliny chlorovodíkové HCl (C, X
Návod k laboratornímu cvičení Fenoly Úkol č. 1: Příprava fenolátu sodného Pomůcky: váhy, kádinka, zkumavky Chemikálie: 10% roztok hydroxidu sodného NaOH (C), 5%roztok kyseliny chlorovodíkové HCl (C, X
Inovace bakalářského studijního oboru Aplikovaná chemie CZ.1.07/2.2.00/ Výpočty z chemických vzorců
 Výpočty z chemických vzorců 1. Hmotnost kyslíku je 80 g. Vypočítejte : a) počet atomů kyslíku ( 3,011 10 atomů) b) počet molů kyslíku (2,5 mol) c) počet molekul kyslíku (1,505 10 24 molekul) d) objem (dm
Výpočty z chemických vzorců 1. Hmotnost kyslíku je 80 g. Vypočítejte : a) počet atomů kyslíku ( 3,011 10 atomů) b) počet molů kyslíku (2,5 mol) c) počet molekul kyslíku (1,505 10 24 molekul) d) objem (dm
LP č. 5 - SACHARIDY. Autor: Mgr. Stanislava Bubíková. Datum (období) tvorby: 28. 2. 2013. Ročník: devátý
 LP č. 5 - SACHARIDY Autor: Mgr. Stanislava Bubíková Datum (období) tvorby: 28. 2. 2013 Ročník: devátý Vzdělávací oblast: Člověk a příroda / Chemie / Organické sloučeniny 1 Anotace: Žáci si prakticky vyzkouší
LP č. 5 - SACHARIDY Autor: Mgr. Stanislava Bubíková Datum (období) tvorby: 28. 2. 2013 Ročník: devátý Vzdělávací oblast: Člověk a příroda / Chemie / Organické sloučeniny 1 Anotace: Žáci si prakticky vyzkouší
2.03 Endotermní/exotermní děje. Projekt Trojlístek
 2. Vlastnosti látek a chemické reakce 2.03 Endotermní/exotermní děje. Projekt úroveň 1 2 3 1. Předmět výuky Metodika je určena pro vzdělávací obsah vzdělávacího předmětu Chemie. Chemie 2. Cílová skupina
2. Vlastnosti látek a chemické reakce 2.03 Endotermní/exotermní děje. Projekt úroveň 1 2 3 1. Předmět výuky Metodika je určena pro vzdělávací obsah vzdělávacího předmětu Chemie. Chemie 2. Cílová skupina
Funkce chemického pokusu ve výuce chemie
 Funkce chemického pokusu ve výuce Funkce vyplývají ze struktury pokusu a charakteristiky výuky a vzhledem k cílům výuky Informativní Formativní Metodologická Vyberte si každý jednu chemickou reakci (z
Funkce chemického pokusu ve výuce Funkce vyplývají ze struktury pokusu a charakteristiky výuky a vzhledem k cílům výuky Informativní Formativní Metodologická Vyberte si každý jednu chemickou reakci (z
CHEMIE. Pracovní list č. 4 - žákovská verze Téma: Tepelné zabarvení chemických reakcí. Mgr. Kateřina Dlouhá. Student a konkurenceschopnost
 www.projektsako.cz CHEMIE Pracovní list č. 4 - žákovská verze Téma: Tepelné zabarvení chemických reakcí Lektor: Projekt: Reg. číslo: Mgr. Kateřina Dlouhá Student a konkurenceschopnost CZ.1.07/1.1.07/03.0075
www.projektsako.cz CHEMIE Pracovní list č. 4 - žákovská verze Téma: Tepelné zabarvení chemických reakcí Lektor: Projekt: Reg. číslo: Mgr. Kateřina Dlouhá Student a konkurenceschopnost CZ.1.07/1.1.07/03.0075
HYDROXYDERIVÁTY - ALKOHOLY
 LABORATORNÍ PRÁCE Č. 26 HYDROXYDERIVÁTY - ALKOHOLY PRINCIP Hydroxyderiváty jsou kyslíkaté deriváty uhlovodíků, které vznikají náhradou jednoho nebo více atomů vodíku v molekule uhlovodíku hydroxylovou
LABORATORNÍ PRÁCE Č. 26 HYDROXYDERIVÁTY - ALKOHOLY PRINCIP Hydroxyderiváty jsou kyslíkaté deriváty uhlovodíků, které vznikají náhradou jednoho nebo více atomů vodíku v molekule uhlovodíku hydroxylovou
KARBOXYLOVÉ KYSELINY
 LABORATORNÍ PRÁCE Č. 28 KARBOXYLOVÉ KYSELINY PRINCIP Karboxylové kyseliny jsou látky, které ve své molekule obsahují jednu nebo více karboxylových skupin. Odvozují se od nich dva typy derivátů, substituční
LABORATORNÍ PRÁCE Č. 28 KARBOXYLOVÉ KYSELINY PRINCIP Karboxylové kyseliny jsou látky, které ve své molekule obsahují jednu nebo více karboxylových skupin. Odvozují se od nich dva typy derivátů, substituční
Důkaz uhličitanu ve vodním kameni
 Důkaz uhličitanu ve vodním kameni Časový harmonogram a) doba na přípravu - 10 minut b) doba na provedení - 10 minut Metodický list pro učitele Pomůcky a) chemikálie - ocet b) potřeby - varná konvice zanesená
Důkaz uhličitanu ve vodním kameni Časový harmonogram a) doba na přípravu - 10 minut b) doba na provedení - 10 minut Metodický list pro učitele Pomůcky a) chemikálie - ocet b) potřeby - varná konvice zanesená
NEUTRALIZAČNÍ ODMĚRNÁ ANALÝZA (TITRACE)
 NEUTRALIZAČNÍ ODMĚRNÁ ANALÝZA (TITRACE) Cíle a princip: Stanovit TITR (přesnou koncentraci) odměrného roztoku kyseliny nebo zásady pomocí známé přesné koncentrace již stanoveného odměrného roztoku. Podstatou
NEUTRALIZAČNÍ ODMĚRNÁ ANALÝZA (TITRACE) Cíle a princip: Stanovit TITR (přesnou koncentraci) odměrného roztoku kyseliny nebo zásady pomocí známé přesné koncentrace již stanoveného odměrného roztoku. Podstatou
chemie Chemické směsi Akademie věd ČR hledá mladé vědce
 chemie Chemické směsi Akademie věd ČR hledá mladé vědce Úvodní list Předmět: Chemie Cílová skupina: 1. ročník SŠ Délka trvání: 90 min. (laboratorní cvičení) Název hodiny: Směsi Výukový celek: Soustavy
chemie Chemické směsi Akademie věd ČR hledá mladé vědce Úvodní list Předmět: Chemie Cílová skupina: 1. ročník SŠ Délka trvání: 90 min. (laboratorní cvičení) Název hodiny: Směsi Výukový celek: Soustavy
Název: Elektromagnetismus 2. část (Vzájemné působení magnetu a vodiče s proudem)
 Výukové materiály Název: Elektromagnetismus 2. část (Vzájemné působení magnetu a vodiče s proudem) Téma: Vzájemné působení magnetu a vodiče s proudem, využití tohoto jevu v praxi Úroveň: 2. stupeň ZŠ,
Výukové materiály Název: Elektromagnetismus 2. část (Vzájemné působení magnetu a vodiče s proudem) Téma: Vzájemné působení magnetu a vodiče s proudem, využití tohoto jevu v praxi Úroveň: 2. stupeň ZŠ,
2. Chemický turnaj. kategorie starší žáci Teoretická část. Řešení úloh
 2. Chemický turnaj kategorie starší žáci 31. 5. 2013 Teoretická část Řešení úloh Téma: Oxidy celkem 29 bodů 1. Příprava oxidů Rovnice:...S + O 2 SO 2... Název oxidu:...siřičitý... rovnice 2 b. Rovnice:
2. Chemický turnaj kategorie starší žáci 31. 5. 2013 Teoretická část Řešení úloh Téma: Oxidy celkem 29 bodů 1. Příprava oxidů Rovnice:...S + O 2 SO 2... Název oxidu:...siřičitý... rovnice 2 b. Rovnice:
Předmět: CHEMIE Ročník: 8. ŠVP Základní škola Brno, Hroznová 1. Výstupy předmětu
 Chemie ukázka chemického skla Chemie přírodní věda, poznat chemické sklo a pomůcky, zásady bezpečné práce práce s dostupnými a běžně používanými látkami (směsmi). Na základě piktogramů žák posoudí nebezpečnost
Chemie ukázka chemického skla Chemie přírodní věda, poznat chemické sklo a pomůcky, zásady bezpečné práce práce s dostupnými a běžně používanými látkami (směsmi). Na základě piktogramů žák posoudí nebezpečnost
Inovace výuky - Přírodovědný seminář. Pokusy s vejci. Přs / 31, 32. vejce, skořápka, papírová blána, žloutek, bílek, uhličitan vápenatý
 Inovace výuky - Přírodovědný seminář Pokusy s vejci Přs / 31, 32 Vzdělávací oblast: Vzdělávací obor: Tematický okruh: Cílová skupina: Klíčová slova: Očekávaný výstup: Člověk a příroda Přírodopis Praktické
Inovace výuky - Přírodovědný seminář Pokusy s vejci Přs / 31, 32 Vzdělávací oblast: Vzdělávací obor: Tematický okruh: Cílová skupina: Klíčová slova: Očekávaný výstup: Člověk a příroda Přírodopis Praktické
Název: Tajná písma. Výukové materiály. Téma: Organické a anorganické látky a indikátory. Úroveň: 2. stupeň ZŠ
 Název: Tajná písma Výukové materiály Téma: Organické a anorganické látky a indikátory Úroveň: 2. stupeň ZŠ Tematický celek: Vidět a poznat neviditelné Předmět (obor): chemie Doporučený věk žáků: 13 14
Název: Tajná písma Výukové materiály Téma: Organické a anorganické látky a indikátory Úroveň: 2. stupeň ZŠ Tematický celek: Vidět a poznat neviditelné Předmět (obor): chemie Doporučený věk žáků: 13 14
Ústřední komise Chemické olympiády. 42. ročník. KRAJSKÉ KOLO Kategorie D. SOUTĚŽNÍ ÚLOHY TEORETICKÉ ČÁSTI Časová náročnost: 60 minut
 Ústřední komise Chemické olympiády 42. ročník 2005 2006 KRAJSKÉ KOLO Kategorie D SOUTĚŽNÍ ÚLOHY TEORETICKÉ ČÁSTI Časová náročnost: 60 minut Institut dětí a mládeže Ministerstva školství, mládeže a tělovýchovy
Ústřední komise Chemické olympiády 42. ročník 2005 2006 KRAJSKÉ KOLO Kategorie D SOUTĚŽNÍ ÚLOHY TEORETICKÉ ČÁSTI Časová náročnost: 60 minut Institut dětí a mládeže Ministerstva školství, mládeže a tělovýchovy
Název: Acidobazické indikátory
 Název: Acidobazické indikátory Autor: Mgr. Jiří Vozka, Ph.D. Název školy: Gymnázium Jana Nerudy, škola hl. města Prahy Předmět, mezipředmětové vztahy: chemie, biologie, fyzika Ročník: 3. (1. ročník vyššího
Název: Acidobazické indikátory Autor: Mgr. Jiří Vozka, Ph.D. Název školy: Gymnázium Jana Nerudy, škola hl. města Prahy Předmět, mezipředmětové vztahy: chemie, biologie, fyzika Ročník: 3. (1. ročník vyššího
Název: Směsi. Výukové materiály. Téma: Směsi. Úroveň: 2. stupeň ZŠ. Tematický celek: Materiály a jejich přeměny. Předmět (obor): chemie
 Název: Směsi Výukové materiály Téma: Směsi Úroveň: 2. stupeň ZŠ Tematický celek: Materiály a jejich přeměny Předmět (obor): chemie Doporučený věk žáků: 13 14 let Doba trvání: 2 vyučovací hodiny (laboratorní
Název: Směsi Výukové materiály Téma: Směsi Úroveň: 2. stupeň ZŠ Tematický celek: Materiály a jejich přeměny Předmět (obor): chemie Doporučený věk žáků: 13 14 let Doba trvání: 2 vyučovací hodiny (laboratorní
Trojské trumfy. pražským školám BARVY U ŽIVOČICHŮ A ROSTLIN. projekt CZ.2.17/3.1.00/32718 EVROPSKÝ SOCIÁLNÍ FOND
 EVROPSKÝ SOCIÁLNÍ FOND PRAHA & EU INVESTUJEME DO VAŠÍ BUDOUCNOSTI Pracovní Didaktický list balíček č. 7 č. 9 Trojské trumfy pražským školám projekt CZ.2.17/3.1.00/32718 BARVY U ŽIVOČICHŮ A ROSTLIN A B?
EVROPSKÝ SOCIÁLNÍ FOND PRAHA & EU INVESTUJEME DO VAŠÍ BUDOUCNOSTI Pracovní Didaktický list balíček č. 7 č. 9 Trojské trumfy pražským školám projekt CZ.2.17/3.1.00/32718 BARVY U ŽIVOČICHŮ A ROSTLIN A B?
P + D PRVKY Laboratorní práce
 Téma: Reakce sloučenin zinku P + D PRVKY Laboratorní práce Pozn: Výsledky úkolu 1 zapisujte až po 14 dnech. Úkol 4 provádějte pouze pod dohledem učitele. Úkol 1: Připravte 5 gramů bílé skalice. Bílá skalice
Téma: Reakce sloučenin zinku P + D PRVKY Laboratorní práce Pozn: Výsledky úkolu 1 zapisujte až po 14 dnech. Úkol 4 provádějte pouze pod dohledem učitele. Úkol 1: Připravte 5 gramů bílé skalice. Bílá skalice
11 13 let, popř. i starší
 Název: Mosty Výukové materiály Téma: Pevnost, stabilita, síly Úroveň: 2. stupeň ZŠ Tematický celek: Materiály a jejich přeměny Předmět (obor): Doporučený věk žáků: Doba trvání: Specifický cíl: fyzika 11
Název: Mosty Výukové materiály Téma: Pevnost, stabilita, síly Úroveň: 2. stupeň ZŠ Tematický celek: Materiály a jejich přeměny Předmět (obor): Doporučený věk žáků: Doba trvání: Specifický cíl: fyzika 11
Laboratorní pomůcky, chemické nádobí
 Laboratorní pomůcky, chemické nádobí Laboratorní sklo: měkké (tyčinky, spojovací trubice, kapiláry) tvrdé označení SIMAX (většina varného a odměrného skla) Zahřívání skla: Tenkostěnné nádoby (kádinky,
Laboratorní pomůcky, chemické nádobí Laboratorní sklo: měkké (tyčinky, spojovací trubice, kapiláry) tvrdé označení SIMAX (většina varného a odměrného skla) Zahřívání skla: Tenkostěnné nádoby (kádinky,
Ročník VIII. Chemie. Období Učivo téma Metody a formy práce- kurzívou. Kompetence Očekávané výstupy. Průřezová témata. Mezipřed.
 Úvod IX. -ukázka chem.skla přírodní věda, poznat chemické sklo a pomůcky, zásady bezpečné práce-práce s dostupnými a běžně používanými látkami, hodnocení jejich rizikovosti, posoudí bezpečnost vybraných
Úvod IX. -ukázka chem.skla přírodní věda, poznat chemické sklo a pomůcky, zásady bezpečné práce-práce s dostupnými a běžně používanými látkami, hodnocení jejich rizikovosti, posoudí bezpečnost vybraných
Oborový workshop pro ZŠ CHEMIE
 PRAKTICKÁ VÝUKA PŘÍRODOVĚDNÝCH PŘEDMĚTŮ NA ZŠ A SŠ CZ.1.07/1.1.30/02.0024 Tento projekt je spolufinancován Evropským sociálním fondem a státním rozpočtem České republiky. Oborový workshop pro ZŠ CHEMIE
PRAKTICKÁ VÝUKA PŘÍRODOVĚDNÝCH PŘEDMĚTŮ NA ZŠ A SŠ CZ.1.07/1.1.30/02.0024 Tento projekt je spolufinancován Evropským sociálním fondem a státním rozpočtem České republiky. Oborový workshop pro ZŠ CHEMIE
Vodík, kyslík a jejich sloučeniny
 I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY Laboratorní práce č. 8 Vodík, kyslík a jejich sloučeniny
I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY Laboratorní práce č. 8 Vodík, kyslík a jejich sloučeniny
Název: Projevy živé hmoty
 Název: Projevy živé hmoty Výukové materiály Téma: Obecné vlastnosti živé hmoty Úroveň: střední škola Tematický celek: Obecné zákonitosti přírodovědných disciplín a principy poznání ve vědě Předmět (obor):
Název: Projevy živé hmoty Výukové materiály Téma: Obecné vlastnosti živé hmoty Úroveň: střední škola Tematický celek: Obecné zákonitosti přírodovědných disciplín a principy poznání ve vědě Předmět (obor):
Vlastnosti kyseliny sírové
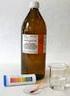 Vlastnosti kyseliny sírové Metodický list pro učitele Časový harmonogram a) doba na přípravu - 10 minut b) doba na provedení - 10 minut Pomůcky a) chemikálie - kyselina sírová - voda - kostka cukru b)
Vlastnosti kyseliny sírové Metodický list pro učitele Časový harmonogram a) doba na přípravu - 10 minut b) doba na provedení - 10 minut Pomůcky a) chemikálie - kyselina sírová - voda - kostka cukru b)
Téma: Elektrický proud, elektrické napětí, bezpečné zacházení s elektrickými spotřebiči
 Název: Zkrat Výukové materiály Téma: Elektrický proud, elektrické napětí, bezpečné zacházení s elektrickými spotřebiči Úroveň: 2. stupeň ZŠ Tematický celek: Riziko a bezpečí, aneb co se stane, když se
Název: Zkrat Výukové materiály Téma: Elektrický proud, elektrické napětí, bezpečné zacházení s elektrickými spotřebiči Úroveň: 2. stupeň ZŠ Tematický celek: Riziko a bezpečí, aneb co se stane, když se
Ministerstvo školství, mládeže a tělovýchovy Ústřední komise Chemické olympiády. 46. ročník 2009/2010. KRAJSKÉ KOLO kategorie D
 Ministerstvo školství, mládeže a tělovýchovy Ústřední komise Chemické olympiády 46. ročník 2009/2010 KRAJSKÉ KOLO kategorie D ŘEŠENÍ SOUTĚŽNÍCH ÚLOH TEORETICKÁ ČÁST (60 bodů) Úloha 1 Vlastnosti prvků 26
Ministerstvo školství, mládeže a tělovýchovy Ústřední komise Chemické olympiády 46. ročník 2009/2010 KRAJSKÉ KOLO kategorie D ŘEŠENÍ SOUTĚŽNÍCH ÚLOH TEORETICKÁ ČÁST (60 bodů) Úloha 1 Vlastnosti prvků 26
Zařazení do výuky Experiment je vhodné zařadit v rámci učiva chemie v 8. třídě (kyseliny, zásady, ph roztoků).
 Název: Dýchání do vody Úvod Někdy je celkem jednoduché si v chemické laboratoři nebo dokonce i doma připravit kyselinu. Pokud máte kádinku, popř. skleničku, a brčko, tak neváhejte a můžete to zkusit hned!
Název: Dýchání do vody Úvod Někdy je celkem jednoduché si v chemické laboratoři nebo dokonce i doma připravit kyselinu. Pokud máte kádinku, popř. skleničku, a brčko, tak neváhejte a můžete to zkusit hned!
Název: Nejznámější chemikálie světa
 Název: Nejznámější chemikálie světa Téma: Destilace Úroveň: střední škola Tematický celek: Praktické aplikace přírodovědných a technických poznatků Výukové materiály Předmět (obor): chemie Doporučený věk
Název: Nejznámější chemikálie světa Téma: Destilace Úroveň: střední škola Tematický celek: Praktické aplikace přírodovědných a technických poznatků Výukové materiály Předmět (obor): chemie Doporučený věk
Název: Halogeny II - halogenidy
 Název: Halogeny II - halogenidy Autor: Mgr. Jiří Vozka, Ph.D. Název školy: Gymnázium Jana Nerudy, škola hl. města Prahy Předmět, mezipředmětové vztahy: chemie, biologie, fyzika Ročník: 3. Tématický celek:
Název: Halogeny II - halogenidy Autor: Mgr. Jiří Vozka, Ph.D. Název školy: Gymnázium Jana Nerudy, škola hl. města Prahy Předmět, mezipředmětové vztahy: chemie, biologie, fyzika Ročník: 3. Tématický celek:
1. Chemický turnaj. kategorie mladší žáci 30.11. 2012. Zadání úloh
 1. Chemický turnaj kategorie mladší žáci 30.11. 2012 Zadání úloh Vytvořeno v rámci projektu OPVK CZ.1.07/1.1.26/01.0034,,Zkvalitňování výuky chemie a biologie na GJO spolufinancovaného Evropským sociálním
1. Chemický turnaj kategorie mladší žáci 30.11. 2012 Zadání úloh Vytvořeno v rámci projektu OPVK CZ.1.07/1.1.26/01.0034,,Zkvalitňování výuky chemie a biologie na GJO spolufinancovaného Evropským sociálním
7) Uveď příklad chemické reakce, při níž se sloučí dva prvky za vzniku sloučeniny. (3) hoření vodíku s kyslíkem a vzniká voda
 Chemické reakce a děje Chemické reakce 1) Jak se chemické reakce odlišují od fyzikálních dějů? (2) změna vlastností látek, změna vazeb mezi atomy 2) Co označujeme v chemických reakcích jako reaktanty a
Chemické reakce a děje Chemické reakce 1) Jak se chemické reakce odlišují od fyzikálních dějů? (2) změna vlastností látek, změna vazeb mezi atomy 2) Co označujeme v chemických reakcích jako reaktanty a
Složení soustav (roztoky, koncentrace látkového množství)
 VZOROVÉ PŘÍKLADY Z CHEMIE A DOPORUČENÁ LITERATURA pro přípravu k přijímací zkoušce studijnímu oboru Nanotechnologie na VŠB TU Ostrava Doporučená literatura z chemie: Prakticky jakákoliv celostátní učebnice
VZOROVÉ PŘÍKLADY Z CHEMIE A DOPORUČENÁ LITERATURA pro přípravu k přijímací zkoušce studijnímu oboru Nanotechnologie na VŠB TU Ostrava Doporučená literatura z chemie: Prakticky jakákoliv celostátní učebnice
Tepelné změny chladicí směsi (laboratorní práce)
 Zvyšování kvality výuky v přírodních a technických oblastech CZ.1.07/1.1.28/02.0055 Tepelné změny chladicí směsi (laboratorní práce) Označení: EU-Inovace-BFCh-Ch-09 Předmět: Biologická, fyzikální a chemická
Zvyšování kvality výuky v přírodních a technických oblastech CZ.1.07/1.1.28/02.0055 Tepelné změny chladicí směsi (laboratorní práce) Označení: EU-Inovace-BFCh-Ch-09 Předmět: Biologická, fyzikální a chemická
Neutralizace kyseliny zásadou
 Neutralizace kyseliny zásadou Metodický list pro učitele Časový harmonogram a) doba na přípravu - 10 minut b) doba na provedení - 15 minut Pomůcky a) chemikálie - kyselina chlorovodíková - hydroxid sodný
Neutralizace kyseliny zásadou Metodický list pro učitele Časový harmonogram a) doba na přípravu - 10 minut b) doba na provedení - 15 minut Pomůcky a) chemikálie - kyselina chlorovodíková - hydroxid sodný
DUM č. 2 v sadě. 24. Ch-2 Anorganická chemie
 projekt GML Brno Docens DUM č. 2 v sadě 24. Ch-2 Anorganická chemie Autor: Aleš Mareček Datum: 26.09.2014 Ročník: 2A Anotace DUMu: Materiál je určen pro druhý ročník čtyřletého a šestý ročník víceletého
projekt GML Brno Docens DUM č. 2 v sadě 24. Ch-2 Anorganická chemie Autor: Aleš Mareček Datum: 26.09.2014 Ročník: 2A Anotace DUMu: Materiál je určen pro druhý ročník čtyřletého a šestý ročník víceletého
STŘEDNÍ ODBORNÁ ŠKOLA a STŘEDNÍ ODBORNÉ UČILIŠTĚ, Česká Lípa, 28. října 2707, příspěvková organizace. Digitální učební materiály
 Název školy Číslo projektu Název projektu Klíčová aktivita Označení materiálu: Typ materiálu: Předmět, ročník, obor: Tematická oblast: Téma: Jméno a příjmení autora: STŘEDNÍ ODBORNÁ ŠKOLA a STŘEDNÍ ODBORNÉ
Název školy Číslo projektu Název projektu Klíčová aktivita Označení materiálu: Typ materiálu: Předmět, ročník, obor: Tematická oblast: Téma: Jméno a příjmení autora: STŘEDNÍ ODBORNÁ ŠKOLA a STŘEDNÍ ODBORNÉ
ZÁKLADNÍ CHEMICKÉ VÝPOČTY
 ZÁKLADNÍ CHEMICKÉ VÝPOČTY Látkové množství - vyjadřování množství: jablka pivo chleba uhlí - (téměř každá míra má svojí jednotku) v chemii existuje univerzální veličina pro vyjádření množství látky LÁTKOVÉ
ZÁKLADNÍ CHEMICKÉ VÝPOČTY Látkové množství - vyjadřování množství: jablka pivo chleba uhlí - (téměř každá míra má svojí jednotku) v chemii existuje univerzální veličina pro vyjádření množství látky LÁTKOVÉ
CHEMIE výpočty. 5 z chemických ROVNIC. 1 vyučovací hodina chemie 9. ročník Mgr. Renata Zemková ZŠ a MŠ L. Kuby 48, České Budějovice
 CHEMIE výpočty 5 z chemických ROVNIC 1 vyučovací hodina chemie 9. ročník Mgr. Renata Zemková ZŠ a MŠ L. Kuby 48, České Budějovice 1 definice pojmu a vysvětlení vzorové příklady test poznámky pro učitele
CHEMIE výpočty 5 z chemických ROVNIC 1 vyučovací hodina chemie 9. ročník Mgr. Renata Zemková ZŠ a MŠ L. Kuby 48, České Budějovice 1 definice pojmu a vysvětlení vzorové příklady test poznámky pro učitele
TEORETICKÁ ČÁST (70 BODŮ)
 TEORETICKÁ ČÁST (70 BODŮ) Úloha 1 Válka mezi živly 7 bodů 1. Doplňte text: Sloučeniny obsahující kation draslíku (draselný) zbarvují plamen fialově. Dusičnan tohoto kationtu má vzorec KNO 3 a chemický
TEORETICKÁ ČÁST (70 BODŮ) Úloha 1 Válka mezi živly 7 bodů 1. Doplňte text: Sloučeniny obsahující kation draslíku (draselný) zbarvují plamen fialově. Dusičnan tohoto kationtu má vzorec KNO 3 a chemický
ODDĚLOVÁNÍ SLOŽEK SMĚSÍ, PŘÍPRAVA ROZTOKU URČITÉHO SLOŽENÍ
 ODDĚLOVÁNÍ SLOŽEK SMĚSÍ, PŘÍPRAVA ROZTOKU URČITÉHO SLOŽENÍ PaedDr. Ivana Töpferová Střední průmyslová škola, Mladá Boleslav, Havlíčkova 456 CZ.1.07/1.5.00/34.0861 MODERNIZACE VÝUKY Anotace: laboratorní
ODDĚLOVÁNÍ SLOŽEK SMĚSÍ, PŘÍPRAVA ROZTOKU URČITÉHO SLOŽENÍ PaedDr. Ivana Töpferová Střední průmyslová škola, Mladá Boleslav, Havlíčkova 456 CZ.1.07/1.5.00/34.0861 MODERNIZACE VÝUKY Anotace: laboratorní
I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í
 I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY Laboratorní práce č. 10 Bílkoviny Pro potřeby projektu
I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY Laboratorní práce č. 10 Bílkoviny Pro potřeby projektu
ilit Laboratorní technika s aplikací Chemist
 Téma aktivity: Předmět: laboratorní cvičení Doporučený věk studentů: 15 16 let Vazba na ŠVP: laboratorní technika Cíle: student popíše některé druhy laboratorního skla a nářadí student sestaví jednoduché
Téma aktivity: Předmět: laboratorní cvičení Doporučený věk studentů: 15 16 let Vazba na ŠVP: laboratorní technika Cíle: student popíše některé druhy laboratorního skla a nářadí student sestaví jednoduché
CHEMICKÉ VÝPOČTY I. ČÁST LÁTKOVÉ MNOŽSTVÍ. HMOTNOSTI ATOMŮ A MOLEKUL.
 CHEMICKÉ VÝPOČTY I. ČÁST LÁTKOVÉ MNOŽSTVÍ. HMOTNOSTI ATOMŮ A MOLEKUL. Látkové množství Značka: n Jednotka: mol Definice: Jeden mol je množina, která má stejný počet prvků, jako je atomů ve 12 g nuklidu
CHEMICKÉ VÝPOČTY I. ČÁST LÁTKOVÉ MNOŽSTVÍ. HMOTNOSTI ATOMŮ A MOLEKUL. Látkové množství Značka: n Jednotka: mol Definice: Jeden mol je množina, která má stejný počet prvků, jako je atomů ve 12 g nuklidu
Ústřední komise Chemické olympiády. 55. ročník 2018/2019 ŠKOLNÍ KOLO. Kategorie B ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ)
 Ústřední komise Chemické olympiády 55. ročník 2018/2019 ŠKOLNÍ KOLO Kategorie B ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ) PRAKTICKÁ ČÁST 40 BODŮ Autor Bc. Lukáš Tomaník VŠCHT Praha RNDr. Petr Holzhauser, Ph.D.
Ústřední komise Chemické olympiády 55. ročník 2018/2019 ŠKOLNÍ KOLO Kategorie B ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ) PRAKTICKÁ ČÁST 40 BODŮ Autor Bc. Lukáš Tomaník VŠCHT Praha RNDr. Petr Holzhauser, Ph.D.
Vitamin C důkaz, vlastnosti
 Předmět: Doporučený ročník: 4. - 5. ročník Zařazení do ŠVP: biochemie, přírodní látky, vitaminy Doba trvání pokusu: 45 minut Seznam pomůcek: zkumavky, kádinky, pipety (automatické), míchací tyčinky, odměrné
Předmět: Doporučený ročník: 4. - 5. ročník Zařazení do ŠVP: biochemie, přírodní látky, vitaminy Doba trvání pokusu: 45 minut Seznam pomůcek: zkumavky, kádinky, pipety (automatické), míchací tyčinky, odměrné
N A = 6,023 10 23 mol -1
 Pro vyjadřování množství látky se v chemii zavádí veličina látkové množství. Značí se n, jednotkou je 1 mol. Látkové množství je jednou ze základních veličin soustavy SI. Jeden mol je takové množství látky,
Pro vyjadřování množství látky se v chemii zavádí veličina látkové množství. Značí se n, jednotkou je 1 mol. Látkové množství je jednou ze základních veličin soustavy SI. Jeden mol je takové množství látky,
100 přírodovědných pokusů. Laboratorní pomůcky. Mgr. Tomáš Kudrna
 100 přírodovědných pokusů Mgr. Tomáš Kudrna Baňka kuželová dle Erlenmeyera Vlastnosti: skleněná baňka, odolná chemikáliím a vysokým teplotám Použití: k přípravě a uchovávání chemických látek, jako součást
100 přírodovědných pokusů Mgr. Tomáš Kudrna Baňka kuželová dle Erlenmeyera Vlastnosti: skleněná baňka, odolná chemikáliím a vysokým teplotám Použití: k přípravě a uchovávání chemických látek, jako součást
Oddíl E učební osnovy XII.2.A LABORATORNÍ TECHNIKA - CH
 Oddíl E učební osnovy XII.2.A LABORATORNÍ TECHNIKA - CH Charakteristika předmětu: LABORATORNÍ TECHNIKA - CH v nižším stupni osmiletého studia Obsah předmětu Laboratorní technika - Ch je součástí vzdělávací
Oddíl E učební osnovy XII.2.A LABORATORNÍ TECHNIKA - CH Charakteristika předmětu: LABORATORNÍ TECHNIKA - CH v nižším stupni osmiletého studia Obsah předmětu Laboratorní technika - Ch je součástí vzdělávací
2.01 Aerobní/anaerobní reakce aneb kvasinky v akci. Projekt Trojlístek
 2. Vlastnosti látek a chemické reakce 2.01 Aerobní/anaerobní reakce aneb kvasinky v akci. Projekt úroveň 1 2 3 1. Předmět výuky Metodika je určena pro vzdělávací obsah vzdělávacího předmětu Chemie. Chemie
2. Vlastnosti látek a chemické reakce 2.01 Aerobní/anaerobní reakce aneb kvasinky v akci. Projekt úroveň 1 2 3 1. Předmět výuky Metodika je určena pro vzdělávací obsah vzdělávacího předmětu Chemie. Chemie
UHLOVODÍKY A HALOGENDERIVÁTY
 LABORATORNÍ PRÁCE Č. 25 UHLOVODÍKY A HALOGENDERIVÁTY PRINCIP Uhlovodíky jsou nejjednodušší organické sloučeniny, jejichž molekuly jsou tvořeny pouze uhlíkem a vodíkem. Uhlovodíky klasifikujeme z několika
LABORATORNÍ PRÁCE Č. 25 UHLOVODÍKY A HALOGENDERIVÁTY PRINCIP Uhlovodíky jsou nejjednodušší organické sloučeniny, jejichž molekuly jsou tvořeny pouze uhlíkem a vodíkem. Uhlovodíky klasifikujeme z několika
Ročník: 1. Mgr. Jan Zmátlík Zpracováno dne: 11.10.2012
 Označení materiálu: VY_32_INOVACE_ZMAJA_VYTAPENI_11 Název materiálu: Paliva, spalování paliv Tematická oblast: Vytápění 1. ročník Instalatér Anotace: Prezentace uvádí a popisuje význam, druhy a použití
Označení materiálu: VY_32_INOVACE_ZMAJA_VYTAPENI_11 Název materiálu: Paliva, spalování paliv Tematická oblast: Vytápění 1. ročník Instalatér Anotace: Prezentace uvádí a popisuje význam, druhy a použití
Příprava vápenné vody
 Příprava vápenné vody Metodický list pro učitele Časový harmonogram a) doba na přípravu - 10 minut b) doba na provedení - 10 minut Pomůcky a) chemikálie - oxid vápenatý - voda b) potřeby - kádinka 2 ks
Příprava vápenné vody Metodický list pro učitele Časový harmonogram a) doba na přípravu - 10 minut b) doba na provedení - 10 minut Pomůcky a) chemikálie - oxid vápenatý - voda b) potřeby - kádinka 2 ks
5.06 Teichmanovy krystaly (důkaz krve). Projekt Trojlístek
 5. Forenzní chemie (chemie v kriminalistice) 5.06 Teichmanovy krystaly (důkaz krve). Projekt úroveň 1 2 3 1. Předmět výuky Metodika je určena pro vzdělávací obsah vzdělávacího předmětu Chemie. Chemie 2.
5. Forenzní chemie (chemie v kriminalistice) 5.06 Teichmanovy krystaly (důkaz krve). Projekt úroveň 1 2 3 1. Předmět výuky Metodika je určena pro vzdělávací obsah vzdělávacího předmětu Chemie. Chemie 2.
zadání příkladů 10. výsledky příkladů 7. 3,543 litru kyslíku
 zadání Jaký bude objem vodíku při tlaku 105 kpa a teplotě 15 stupňů Celsia, který vznikne reakcí 8 gramů zinku s nadbytkem kyseliny trihydrogenfosforečné? Jaký bude objem vodíku při tlaku 97 kpa a teplotě
zadání Jaký bude objem vodíku při tlaku 105 kpa a teplotě 15 stupňů Celsia, který vznikne reakcí 8 gramů zinku s nadbytkem kyseliny trihydrogenfosforečné? Jaký bude objem vodíku při tlaku 97 kpa a teplotě
Název: Deriváty uhlovodíků karbonylové sloučeniny
 Název: Deriváty uhlovodíků karbonylové sloučeniny Autor: Mgr. Štěpán Mička Název školy: Gymnázium Jana Nerudy, škola hl. města Prahy Předmět, mezipředmětové vztahy: chemie, fyzika Ročník: 4. Tématický
Název: Deriváty uhlovodíků karbonylové sloučeniny Autor: Mgr. Štěpán Mička Název školy: Gymnázium Jana Nerudy, škola hl. města Prahy Předmět, mezipředmětové vztahy: chemie, fyzika Ročník: 4. Tématický
Rozklad uhličitanu vápenatého kyselinou
 Časový harmonogram Rozklad uhličitanu vápenatého kyselinou a) doba na přípravu - 10 minut b) doba na provedení - 10 minut Pomůcky a) chemikálie - kyselina chlorovodíková b) potřeby - kádinka - vápenec
Časový harmonogram Rozklad uhličitanu vápenatého kyselinou a) doba na přípravu - 10 minut b) doba na provedení - 10 minut Pomůcky a) chemikálie - kyselina chlorovodíková b) potřeby - kádinka - vápenec
I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í
 I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY Laboratorní práce č. 8 Sacharidy Pro potřeby projektu
I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY Laboratorní práce č. 8 Sacharidy Pro potřeby projektu
NOVÉ NÁMĚTY PRO DEMONSTRAČNÍ POKUSY. Ondřej Maca, Tereza Kudrnová
 NOVÉ NÁMĚTY PRO DEMONSTRAČNÍ POKUSY Ondřej Maca, Tereza Kudrnová HUSTÝ DÝM 1) pro koho: 1. ročník čtyřletého gymnázia 2) zařazení do učiva: vlastnosti látek; halogeny; pentely 3) pomůcky: zkumavka se zátkou,
NOVÉ NÁMĚTY PRO DEMONSTRAČNÍ POKUSY Ondřej Maca, Tereza Kudrnová HUSTÝ DÝM 1) pro koho: 1. ročník čtyřletého gymnázia 2) zařazení do učiva: vlastnosti látek; halogeny; pentely 3) pomůcky: zkumavka se zátkou,
Návod k laboratornímu cvičení. Bílkoviny
 Úkol č. 1: Důkazy bílkovin ve vaječném bílku a) natvrdo uvařené vejce s kyselinou dusičnou Pomůcky: Petriho miska, pipeta, nůž. Návod k laboratornímu cvičení Bílkoviny Chemikálie: koncentrovaná kyselina
Úkol č. 1: Důkazy bílkovin ve vaječném bílku a) natvrdo uvařené vejce s kyselinou dusičnou Pomůcky: Petriho miska, pipeta, nůž. Návod k laboratornímu cvičení Bílkoviny Chemikálie: koncentrovaná kyselina
Ústřední komise Chemické olympiády. 55. ročník 2018/2019 ŠKOLNÍ KOLO. Kategorie B ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ)
 Ústřední komise Chemické olympiády 55. ročník 2018/2019 ŠKOLNÍ KOLO Kategorie B ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ) PRAKTICKÁ ČÁST 40 BODŮ Autor Bc. Lukáš Tomaník VŠCHT Praha RNDr. Petr Holzhauser, Ph.D.
Ústřední komise Chemické olympiády 55. ročník 2018/2019 ŠKOLNÍ KOLO Kategorie B ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ) PRAKTICKÁ ČÁST 40 BODŮ Autor Bc. Lukáš Tomaník VŠCHT Praha RNDr. Petr Holzhauser, Ph.D.
Návod k laboratornímu cvičení. Kovy a elektrochemická(beketovova) řada napětí kovů
 Návod k laboratornímu cvičení Kovy a elektrochemická(beketovova) řada napětí kovů Úkol č. 1: Barvení plamene Pomůcky: kahan, zápalky, tuha upevněná ve verzatilce nebo platinový drátek Chemikálie: nasycené
Návod k laboratornímu cvičení Kovy a elektrochemická(beketovova) řada napětí kovů Úkol č. 1: Barvení plamene Pomůcky: kahan, zápalky, tuha upevněná ve verzatilce nebo platinový drátek Chemikálie: nasycené
Experiment C-8 KYSELÝ DÉŠŤ
 Experiment C-8 KYSELÝ DÉŠŤ CÍL EXPERIMENTU Praktické ověření vzniku kyselého deště. Ověření souvislosti mezi změnou kyselosti roztoku a změnou ph. Příprava oxidu uhličitého. MODULY A SENZORY PC + program
Experiment C-8 KYSELÝ DÉŠŤ CÍL EXPERIMENTU Praktické ověření vzniku kyselého deště. Ověření souvislosti mezi změnou kyselosti roztoku a změnou ph. Příprava oxidu uhličitého. MODULY A SENZORY PC + program
Podstata krápníkových jevů. Ch 8/07
 Inovace výuky Chemie Podstata krápníkových jevů Ch 8/07 Vzdělávací oblast: Vzdělávací obor: Tematický okruh: Cílová skupina: Klíčová slova: Očekávaný výstup: Člověk a příroda Chemie Anorganické sloučeniny
Inovace výuky Chemie Podstata krápníkových jevů Ch 8/07 Vzdělávací oblast: Vzdělávací obor: Tematický okruh: Cílová skupina: Klíčová slova: Očekávaný výstup: Člověk a příroda Chemie Anorganické sloučeniny
BENZIN A MOTOROVÁ NAFTA
 BENZIN A MOTOROVÁ NAFTA BENZIN je směs kapalných uhlovodíků s pěti až jedenácti atomy uhlíku v řetězci (C 5 - C 11 ). Jeho složení je proměnlivé podle druhu a zpracování ropy, ze které pochází. 60-65%
BENZIN A MOTOROVÁ NAFTA BENZIN je směs kapalných uhlovodíků s pěti až jedenácti atomy uhlíku v řetězci (C 5 - C 11 ). Jeho složení je proměnlivé podle druhu a zpracování ropy, ze které pochází. 60-65%
