LÉČBA NEMOCNÝCH SE SYSTÉMOVÝM LUPUS ERYTHEMATODES
|
|
|
- Jozef Novotný
- před 8 lety
- Počet zobrazení:
Transkript
1 LÉČBA NEMOCNÝCH SE SYSTÉMOVÝM LUPUS ERYTHEMATODES MUDr. Pavel Horák, CSc. III. interní klinika FN a LF UP Olomouc Prognóza nemocných se systémovým lupus erythematodes (SLE) se v posledních dekádách výrazně zlepšila. Přispěla k tomu zejména včasná diagnostika choroby a orgánového postižení, zejména lupus nefritidy a systematická terapie glukokortikoidy a imunosupresními přípravky, zejména cyklofosfamidem. Na druhou stranu existuje mnoho léčebně refrakterních nemocných a široká paleta vedlejších účinků stávajících léků, které spolu podmiňují potřebu vývoje a klinického zkoušení dalších léčiv a nefarmakologických postupů, ještě účinnějších a zejména bezpečnějších než současně aplikované režimy. Článek se soustředí zejména na současné názory na léčbu nemocných se SLE, okrajově shrnuje experimentální terapii odrážející pokrok na poli biotechnologií, která se brzy může stát součástí rutinních postupů. Klíčová slova: systémový lupus erythematodes, farmakoterapie, experimentální léčba, nefarmakologická léčba. MANAGEMENT OF PATIENTS WITH SYSTEMIC LUPUS ERYTHEMATOSUS Prognosis of patients with systematic lupus erythematodes has been improving significantly during last decades. The early diagnosis of this condition and of possible organ damage mainly to kidneys (lupus nephrititis) has contributed tremendously to it, as well as systematic glucocorticoid and immunosuppressive therapy (e. g. cyclophosphamid). On the other hand, there are still some patients refractory to existing treatment, furthermore wide range of side effects of current drugs have been described. That calls for the further development and clinical testing of new drugs and non pharmacologic approaches, more efficient and mainly safe than current applying regimes. The paper concentrates on current trends in management of patients with SLE, experimental therapy is mentioned as well, reflecting progress in the area of biotechnology, which can ultimately become a standard treatment modality. Key words: systematic lupus erythematodes, pharmacotherapy, experimental therapy, non pharmacologic management. Systémový lupus erythematodes (SLE) je chronické zánětlivé autoimunní onemocnění, jehož průběh je charakterizován akutními relapsy (flary) a remisemi aktivity choroby. Jedná se o onemocnění potenciálně ohrožující život. Nemocný může trpět pestrou paletou symptomů a má různou prognózu, která závisí na závažnosti orgánového postižení. Vzhledem k nejistému průběhu onemocnění je ve většině případů nutná dlouhodobá účinná léčba a sledování nemocného založené na dobré komunikaci mezi lékařem a pacientem, případně jeho rodinou. Léčba SLE je zaměřena jednak na zvládnutí aktivity nemoci, v chronickém stadiu choroby pak na udržení remise onemocnění a zabránění vzniku závažného orgánového postižení. Vyžaduje správnou interpretaci řady klinických symptomů i laboratorních nálezů a systematickou prevenci a terapii relapsů onemocnění, interkurentních infekcí, jakož i efektivní tlumení vedlejších účinků terapie a chronického zánětlivého onemocnění. Prognóza nemocných se SLE se v průběhu posledních desetiletí signifikantně zlepšila (9, 15). Včasná diagnostika založená na větším povědomí o nemoci a dostupnost patřičných imunologických vyšetření (antinukleární protilátky, anti-dsdna protilátky, ENA protilátky atd.) umožňují účinné použití dostupné terapie. Hlavní roli ve zlepšení prognózy nemocných sehrálo však zejména zavedení pulzní terapie cyklofosfamidem pro nemocné s lupus nefritidou a dalšími závažnými orgánovými manifestacemi choroby a všeobecně dobrá dostupnost hemodialyzačních technik, jelikož v minulosti to bylo především nevratné selhání ledvinných funkcí a z něho vyplývající důsledky, které ovlivňovaly nejpodstatněji mortalitu nemocných. Přes nesporné úspěchy je onemocnění spojeno stále se zvýšenou mortalitou během pěti let od stanovené diagnózy. Střední věková expektance postižených je signifikantně kratší než ve zdravé populaci, na čemž se podílí zejména progresivní terapeuticky rezistentní varianty SLE a výskyt závažných komorbidit u některých nemocných. Škála léčebných prostředků používaná u SLE je neobyčejně široká, sahající od nesteroidních antirevmatik přes antimalarika, kortikosteroidy k cytotoxickým látkám, imunoglobulinům, imunoablativní terapii, nověji pak k biologické léčbě, na jejímž úsvitu se nacházíme. Pro některé klinické situace existují propracovaná léčebná schémata (lupus nefritida), jedná se však o onemocnění s heterogenním klinickým obrazem, který si vyžaduje často velmi individuální přístup k terapii. Předložené sdělení se věnuje jednotlivým lékům a jejich výběru z hlediska orgánového postižení a aktivity choroby. Všeobecná doporučení Dieta a nutrice Jelikož existují pouze omezená data o vlivu dietních modifikací u SLE (jedna studie referovala o vztahu zvýšeného příjmu masa s aktivnější a progresivní chorobou, je zvažován pozitivní vliv rybího tuku), doporučuje se konzervativní přístup založený na dobře vyvážené stravě obsahující dostatek uhlovodanů, proteinů a tuků. Dieta by měla být modifikovaná dle průběhu a aktivity choroby. Nemocní s vysokou zánětlivou aktivitou a horečkou vyžadují větší kalorický přísun. Na druhou stranu glukokortikoidy samy o sobě zvyšují apetenci, což má za důsledek nežádoucí přibývání na hmotnosti. Pocit hladu může být někdy úspěšně tlumen dostatečným přívodem tekutin, anacid, H2 blokátory. U nefrotického syndromu se vyskytuje výrazná hypercholesterolémie a hyperlipidémie, tito nemocní by měli být instruováni k dietě se sníženým množstvím tuků. Lze 394
2 doporučit multivitaminy v situaci, kdy je potřeba uplatnit dietní restrikce. Většina pacientů se SLE má nižší sérové hladiny 25 hydroxyvitaminu D, snad jako důsledek vyhýbání se slunci při fotosenzitivitě, proto by nemocní užívající dlouhodobě glukokortikoidy a ženy v menopauze měli dostávat 400 IU vitaminu D a mg kalcia denně jako prevenci ztrát kostní hmoty (9, 15). Cvičení se doporučuje jako prevence rychlé ztráty svalové hmoty. K odstranění často přítomné chronické únavy přispějí malé dávky glukokortikoidů či antimalarika (15). Imunizace V minulosti se považovala imunizace za rizikovou a byla zvažována možnost exacerbace SLE v souvislosti s ní. Ukázalo se však, že například vakcinace proti chřipce je bezpečná a efektivní u stabilizovaných nemocných. Naopak nedoporučuje se používat živé vakcíny u imunokompromitovaných jedinců s aktivní chorobou. Nebyla zatím stanovena účinnost a bezpečnost vakcinace proti hepatitidě B (15). Další medikace Existují kazuistická data, která svědčí pro možnost vlivu sulfonamidů na exacerbaci lupusu. Naopak léky, které mohou vyvolávat tzv. léky indukovaný lupus (prokainamid, hydralazin), nezpůsobují vzplanutí idiopatického SLE, poněvadž tyto dvě jednotky jsou patogeneticky rozdílné. U SLE je často nutná terapie častých komorbidit, jako jsou hypertenze, hypercholesterolémie, infekce, osteoporóza a vedlejší účinky terapie kortikoidy či dalšími medikamenty (4). Těhotenství a antikoncepce Jelikož aktivní choroba s přítomností orgánového postižení přispívá k vysokému riziku potratovosti a následnému zhoršení průběhu SLE a léčba imunosupresivy je spojena s vyšším rizikem embryotoxicity a teratogenicity, doporučuje se ženám neotěhotnět, pokud choroba není v remisi alespoň šest měsíců. Kontraceptiva, která obsahují vysokou dávku estrogenů, mohou přispívat k exacerbaci choroby. Tato komplikace se ale prakticky neobjevuje u moderních přípravků obsahujících nízkou dávku estrogenu či progesteron. Hormonální antikoncepce je kontraindikovaná u nemocných s antifosfolipidovým syndromem či anamnézou tromboembolické choroby. Hormonálním kontraceptivům bychom se měli vyhnout rovněž u nemocných s migrenózními bolestmi hlavy (lupus headache) či s těžším Raynaudovým syndromem (15). Těhotné ženy s aktivním lupusem mohou být léčeny kortikoidy. V těhotenství mohou být rovněž s opatrností použity nesteroidní antirevmatika (NSAID) a antimalarika. Cyklofosfamid a methotrexát jsou v graviditě kontraindikovány, azathioprin a cyklosporin A mohou být v případě nezbytnosti použity. Samostatnou problematiku představuje riziko spontánních potratů u žen s přítomností antifosfolipidového syndromu. Medikamentózní léčba Nesteroidní antirevmatika (NSA) Jsou často předepisována u SLE k symptomatickému potlačení projevů choroby, jako je únava, teploty, obtíže ze strany skeletomuskulárního systému a mírné serositidy. Dosud neexistuje přesvědčivý důkaz, že by některé z NSA bylo u lupusu všeobecně vhodnější. Nežádoucí účinky NSA jsou dobře známy, v popředí zájmu stojí gastrotoxicita, rizikovější při kombinaci s glukokortikoidy. Velmi riziková je také kombinace s warfarinem. Poškození ledvin či neurologické postižení jako vzácnější vedlejší účinky NSA mohou být lehce zaměněny s postižením těchto orgánů při samotném lupusu (8). Glukokortikoidy Glukokortikoidy jsou stále nejúčinnějším prostředkem v léčbě SLE, jejich podání vede k rychlému, byť pouze dočasnému ústupu všech či většiny projevů SLE. Mohou být podávány různým způsobem místně u kožních manifestací, aplikací přímo do hlubokých kožních lézí u diskoidní kožní formy, injekčně při entezopatiích či synovitidách, v nízkých či ve vysokých dávkách perorálně i parenterálně (velmi často také pulzně ) při akutních, těžkých orgánových projevech choroby (4, 5, 19). U choroby s nízkou aktivitou procesu vystačíme s úvodním dávkováním prednisonu (či metylprednisolonu) menším než 0,5 mg/kg/den, při vysoké aktivitě choroby pak s dávkami do 1 mg/kg/den. Vysoké dávky steroidů (až 1 g metylprednisolonu) lze podávat intravenózně ve 3-5 pulzech obden. Podávání vysokých dávek kortikosteroidů by mělo být časově omezeno na 6 8 týdnů. Po dosažení ústupu aktivity choroby je třeba dávku postupně redukovat na nejnižší možnou úroveň. Je třeba mít na zřeteli, že nežádoucí účinky léčby kortikosteroidy jsou jednou z nejčastějších příčin morbidity nemocných se SLE (8). Nežádoucí účinky steroidů jsou časté, velká pozornost je v současné době věnována glukokortikoidy indukované osteoporóze. Je třeba mít na zřeteli také přítomnost útlumu činnost nadledvin u nemocných v dlouhodobé terapii steroidy (nutnost podání hydrokortizonu v rámci předoperační přípravy nemocných, potřeba zvýšení dávky při infekcích). Další úskalí terapie představují vývoj iatrogenního hyperkortizolizmu, myopatie, avaskulární nekrózy hlavice kosti stehenní, glaukomu, vředové choroby žaludku a duodena, pankreatitidy, neuropsychiatrických komplikací, poruchy glukózové tolerance či steroidního diabetu. U pulzní terapie pak hrozí bezprostředně vznik arytmie, srdečního selhání a hypertenzní krize zejména u disponovaných jedinců (9). Přes všechna úskalí, která s sebou přináší léčba kortikosteroidy, je jejich použití u SLE zpravidla nezbytné a někdy život zachraňující. Antimalarika Jedná se o léky původně určené pro terapii a prevenci malárie, které se postupem času staly významnými pro
3 středky v terapii revmatoidní artritidy a SLE. Jsou nezastupitelná při terapii kožních forem lupusu, ale také u muskuloskeletárního postižení a u mírnějších serozitid. Aktivně stabilizují lysozomální membrány, potlačují chemotaxi a migraci polymorfonukleárů a zasahují i do některých funkcí T a B lymfocytů. V monoterapii mají význam u mírnějších forem SLE, u středně závažných pak téměř vždy v kombinaci s glukokortikoidy. Nejsou vhodné u lupusu s postižením centrálního nervového systému, protože samy o sobě mohou způsobovat bolesti hlavy, labilitu, ataxie či křeče (6). Na trhu jsou k dispozici dva preparáty z této skupiny, chlorochin v tabletách po 250 mg (Delagil ) a hydroxychlorochin v tabletách s obsahem 200 mg účinné látky (Plaquenil ). Dávkování je velmi jednoduché, na počátku léčby se podávají dvě tablety po dobu 6 8 týdnů, pak se dávka snižuje na jednu tabletu denně (4, 5). Mezi nežádoucí účinky antimalarik patří gastrointestinální potíže v podobě nevolnosti, vzácně útlum krvetvorby či rozvoj hemolytické anémie při nedostatečnosti glukóza-6 fosfátdehydrogenázy či při závažnějších poruchách jater. Závažným problémem podávání antimalarik je poškození zraku. Existuje možnost ukládání léku do rohovky projevující se rozmazaným viděním a kruhy kolem světelných bodů. Keratopatie je však v naprosté většině případů po vysazení léku plně reverzibilní. Obávanější komplikací je retinopatie, která je způsobena vazbou antimalarik na melanin pigmentové vrstvy a na poškození tyčinek a čípků sítnice. Dle dnešních poznatků představuje vysoká denní dávka větší riziko poškození zraku než dávka kumulativní. Pozdní formy postižení sítnice vedou k makulární degeneraci, atrofii očního nervu a nenávratné ztrátě zraku. Mezi základní vyšetření před podáním antimalarik proto patří vždy vyšetření zrakové ostrosti, vyšetření štěrbinovou lampou a zhodnocení očního pozadí. Kontroly jsou nutné v intervalech šesti měsíců (5). Azathioprin Je purinový analog ovlivňující biosyntézu purinů, má výrazný imunosupresní a protizánětlivý účinek. Je indikován u aktivních forem lupusu s orgánovým postižením mimo lupus nefritidy. Je méně účinný než cyklofosfamid, je ale bezesporu bezpečnější. Lze jej také podávat jako udržovací léčbu remise dosažené cyklofosfamidem či jako prostředek umožňující snížit stávající dávku kortikoidů. Podává se v dávkách 1 3 mg/kg/den, udržovací dávka se pohybuje mezi 1 2 mg/kg/den. Na trhu je k dispozici v tabletách po 25 a 50 mg. Experimentálně se v současnosti zkouší i pulzní intravenózní podání vysokých dávek azathioprinu v terapii lupus nefritidy. Mezi hlavní nežádoucí účinky patří útlum krvetvorby, zažívací potíže, hepatopatie s elevací jaterních enzymů, větší dispozice k oportunním infekcím (herpes zoster). Při dlouhodobém podávání se předpokládá možnost vyšší incidence malignit zejména hemopoetického a lymforetikulárního systému, podle některých novějších prací není tento trend u SLE jednoznačně nepotvrzen (Lisabon 2003). Je třeba dávat pozor na známou, ale někdy opomíjenou interakci s allopurinolem, který zvyšuje toxicitu azathioprinu a navozuje provleklý útlum kostní dřeně s pancytopenií (5, 11). Cyklofosfamid (CFA) Alkylační agens cyklofosfamid účinkuje na úrovni nukleových kyselin prakticky během všech fází buněčného cyklu, zejména však v S fázi. Má účinek cytotoxický, imunosupresivní a protizánětlivý. Představuje v současnosti standardní terapii aktivního SLE s přítomností lupus nefritidy zejména III. a IV. histologického typu (fokální a difuzní proliferativní glomerulonefritida), vaskulitidy, rezistentní trombocytopunie či postižení CNS (1, 3, 13, 14). Cyklofosfamid se metabolizuje v játrech na aktivní alkylační metabolity. Lze jej podávat jak perorálně, tak intravenózně. Vylučuje se zejména ledvinami, takže při poruše funkce ledvin je třeba jeho dávku redukovat. Perorálně se cyklofosfamid podává kontinuálně v dávce 1-3 mg/kg/den. Jako velmi účinné a poměrně bezpečné se ukázaly intravenózní pulzy CFA v dávce 5 10 mg/kg (0,3 1 g/m 2 ). Pulzy se obvykle opakují v intervalu 3 4 týdnů po dobu prvních šesti měsíců, pak se interval infuzí prodlužuje na tři měsíce po dobu dvou let. Pro intravenózní podání CFA existuje řada dalších schémat, která je nutno často přizpůsobit individualitě nemocného s ohledem na výsledky monitorace aktivity choroby a bezpečnosti podávání látky. Četné klinické studie prokázaly, že CFA zpomaluje progresi jizvícího procesu v ledvinných glomerulech a snižuje riziko rozvoje konečného stadia ledvinného selhání (13, 17). Nežádoucí účinky CFA jsou častější než u azathioprinu, jedná se především o útlum krvetvorby, gastrointestinální potíže, většinou reverzibilní alopecii, poškození gonád, zvýšené riziko infekce, urotoxicitu (hemoragická cystitida, fibróza močového měchýře, karcinom močového měchýře), vznik sekundárních malignit. Zvláště opatrně musí být CFA podáván u nemocných s leukopenií, je pravidlem, že počet leukocytů by neměl klesnout pod /l či počet neutrofilů pod /l. Pravidelné sledování hodnot krevního obrazu je zcela nezbytné. Jako prevence poškození močového měchýře je nutno zajistit dostatečný příjem tekutin a lze podávat 2-merkaptoetansulfonát (MESNA), který na sebe váže akrolein (metabolit CFA, který vyvolává akutní cystitidu). Je rovněž prokázáno, že CFA působí teratogenně, před zahájením léčby a během ní je nutno vyloučit případnou graviditu. Jako prevence předčasného ovariálního selhání se někdy doporučuje podávání hormonálních kontraceptiv s nízkým obsahem estrogenů (viz výše) či u bezdětných mladších žen zajištění odběru a uložení vajíček. U mužů může vést podávání CFA k ireverzibilním změnám spermiogramu (azoospermie), před zahájením podávání u mladších mužů se doporučuje provést odběr a zmrazení spermatu (4). Methotrexat Postavení methotrexatu, antagonisty kyseliny listové, v terapii SLE, není tak výlučné jako je tomu v léčbě rev
4 matoidní artritidy, i když jsou jeho indikace i na tomto poli stále častější. Představuje alternativu podání antimalarik u dominantního postižení kůže, synovie, serózních blan a u forem doprovázených pyretickou reakcí. Je podáván v dávce 7,5 15 (20) mg jedenkrát týdně, perorálně či parenterálně (1, 4). Cyklosporin A (CyA) Lék, který byl primárně používaný v transplantologii, našel své uplatnění také v léčbě orgánových manifestací aktivního SLE. Brzdí aktivaci T pomahačských lymfocytů prostřednictvím snížené produkce IL-2. Je to látka s vysokým imunosupresním účinkem. Nejvýraznější úspěch zaznamenává CyA v léčbě nefrotických syndromů u různých typů lupus nefritidy (zejména V. typu). Jeho použití u lupus nefritidy III. a IV. typu není ve světě všeobecně přijímáno, v některých zemích (Česká republika, Itálie) je však v této indikaci používán relativně často. Komparativní kontrolované a randomizované studie oproti cyklofosfamidu zatím chybí (4). Byl rovněž účinný u některých nemocných refrakterních na běžnou imunosupresní léčbu či jako alternativa podání cyklofosfamidu při jeho špatné toleranci zejména ze strany hemopoetického systému. Lze jej použít také v terapii trombocytopenie a leukopenie či rezistentních serozitid. Cyklosporin A se podává v dávce 3-5 mg/kg/den. Rovněž podávání CyA s sebou nese řadu nežádoucích účinků, na prvním místě je třeba jmenovat vznik hypertenze. Mimo hypertenze se v rámci terapie CyA mohou objevit projevy nefro-, neuro- a hepatotoxicity. Při podávání je třeba pravidelně sledovat hodnoty krevního tlaku, krevního obrazu, urey, kreatininu, urikémii a dle dostupnosti také jeho sérové hladiny (18). Warfarin a heparin Antikoagulační léčba je v rámci SLE indikována v terapii projevů antifosfolipidového syndromu jako prevence tromboembolické choroby. U těhotných žen s antifosfolipidovým syndromem je po celou dobu gravidity indikovaná terapie heparinem eventuálně jeho nízkomolekulárními analogy. Lidské imunoglobuliny Intravenózní podávání imunoglobulinů je indikováno u SLE výjimečně. Hlavní klinickou indikací, a to ve vybraných případech, je refrakterní trombopenie. Experimentálně byly použity také v léčbě lupus nefritidy a vaskulitidy. Zpravidla se podávají v dávce mg/kg/den po dobu pěti dnů s možností opakování za 3 4 týdny dle klinické odpovědi a dle závažnosti stavu nemocného. Kontraindikací podání imunoglobulinů je IgA deficience, kdy jejich podání vyvolá vysokou horečku, třesavky, bolesti břicha, na hrudi či ve svalech (2). Dapson Jedná se o oslabený androgen, který se používá někdy v terapii trombocytopenie a léčbě diskoidní formy SLE (1). Experimentální léčba Mykofenolát mofetil byl zkoušen u 42 pacientů s proliferativní lupus nefritidou a porovnáván s cyklofosfamidem. Obě ramena dosáhla podobného účinku na sledované parametry lupus nefritidy, přičemž skupina léčená mykofenolátem měla menší incidenci nežádoucích účinků (amenorea, infekce, leukopenie). Nicméně relaps choroby se objevil častěji v ramenu léčeném mykofenolátem (46 % vs 17 %). Velká multicentrická studie porovnávající oba léky probíhá v současnosti (7, 16). Leflunomid byl zkoušen spíše kazuisticky u nemocných s dominující artritidou, kteří byli rezistentní k podávání antimalarik či methotrexatu. Teprve budoucí studie mohou odpovědět na otázku po jeho skutečném místě v terapii SLE a případném efektu na další orgánové manifestace choroby (7, 16). Tacrolimus (FK 506) lokálně aplikovaný zlepšoval kožní chorobu u několika nemocných rezistentních na cyklofosfamid a cyklosporin. Je plánovaná studie fáze II zkoumající efekt lokálně aplikovaného takrolimu u kožního lupusu (16). Dehydroepiandrosteron vedl ke snížení aktivity SLE v některých klinických studiích a je v rámci léčby SLE sledován více než deset let. Zatím však chybí jednoznačné závěry a samozřejmě také doporučení pro jeho použití (20). Podobně jako u revmatoidní artritidy, rovněž v rámci SLE se v posledních letech objevila řada klinických studií s biologickými přípravky například blokátory kostimulačních molekul (CTLA4Ig a CD40L), monoklonální protilátky anti C5b, anti CD20 (Rituxibam), anticytokinové přípravky (anti BLyS, anti IL-10, anti TNF alfa) či vakcinace peptidy indukujících toleranci T a B buněk (LJP 394) (7, 12, 16). Zhodnocení jejich významu přinesou zřejmě příští roky. Do sféry experimentální léčby patří bezesporu rovněž imunoablativní chemoterapie cyklofosfamidem s následnou záchrannou transplantací autologních kmenových buněk, která má rekonstituovat imunitní systém. Může se jednat o perspektivní léčbu agresivních a rychle progredujících forem SLE (16). Nefarmakologická léčba Plazmaferéza je u SLE stále diskutovanou metodou. Je schopna odstranit cirkulující imunokomplexy a protilátky z oběhu, které jsou pokládány za prostředníky tkáňového poškození. Jeví se užitečná ve vybraných situacích (refrakterní lupus nefritida) ve spojení s bezprostředně po plasmaferéze podanými pulzy cyklofosfamidu (10). Postupné celotělové ozáření lymfatické tkáně bylo zkoušeno jen u malých skupin SLE nemocných s nekonkluzívními závěry (4). Chirurgická splenektomie je efektivní léčbou závažných, na terapii nereagujících cytopénií. Bezprostředně po výkonu existuje zvýšené riziko infekcí. Extrakorporální fotochemoterapie při této metodě, která patří mezi experimentální, jsou krevní elementy vystaveny extrakorporálně účinku metoxypsoralenu a UV záře
5 ní. Tento postup ovlivňuje zejména T buňky (CD8) a vede k poklesu klinické aktivity choroby (1). Imunoadsorpce patří rovněž mezi extrakorporální metody. Je používaná u refrakterního SLE k odstranění cirkulujících imunokomplexů a protilátek. Pozitivně ovlivňuje aktivitu choroby. Jedná se rovněž o experimentální metodu (16). Závěr Je nesporné, že prognóza nemocných se systémovým lupusem se mění ruku v ruce s pokroky v jeho léčbě. Literatura 1. Baart de la Faille H. Lupus therapy. Clin Invest 1994; 72: Boletis JN, Ionnidis JP, Boki KA, et al. Intravenous immunoglobulin compared with cyclophosphamide for proliferative lupus nephritis. Lancet 1999; 354: Boumpas D, Barez S, Klippel J, et al. Intermittent Cyclophosphamide for the treatment of autoimmune thrompocytopenia in systemic lupus erythematosus. Ann Int Med 1990; 112: Dostál C, Rovenský J, Lukáč J, et al. Systémový lupus erythematodes. In: Pavelka K, Rovenský J, et al. Klinická revmatologie. Galén Praha 2003: Dostál C, Vencovský J. Léčení SLE. In: Dostál C, Vencovský J, et al. Systémový lupus erythematodes. Medprint Cheb 1997: Esdaile J, et al. The efficacy of antimalarials in systemic lupus erytheamtosus. Lupus 1993; 2: (Suppl 1): S3 S8. 7. Gescuk BD, Davis JC. Novel therapeutic afents for systemic lupus erythematosus. Curr Opin Rheumatol 2002; 14: Horák P, Faltýnek L, Ščudla V. Terapie systémového lupus erythematodes. Zpravodaj klinické farmakologie a farmacie 1996; 10: Klippe JH, Dieppe PA. Rheumatology, Mosby-Year Book Eurolimited. 1994; 8: Lewis EJ, Hunsicker LG, Lan SP, et al. A controlled trial of plasmapheresis therapy during severe lupus nephritis. N England J Med 1992; 326: V období před zavedením kortikoidů se pětileté přežívání od stanovení diagnózy pohybovalo kolem 50 %. Po zavedení glukokortikoidní léčby se pětiletelé přežívání zvýšilo na 75 %. Použití imunosupresní terapie zvyšuje dále pětileté přežívání na 90 % (9). Je jisté, že účinnost zabránění orgánovému selhání se bude i nadále zlepšovat. Pokroky v imunologii, molekulární biologii a biotechnologiích poskytly nové nadějné látky s potenciálním účinkem na aktivitu a prognózu SLE. Je úkolem dalších let, aby nové léčebné postupy jednoznačně prokázaly svoji efektivitu a bezpečnost v dobře naplánovaných klinických studiích. 11. Nossent HC, Koldingsnes W. Long-term efficacy of azathioprine treatment for proliferative lupus nephritis. Rheumatology 2000; 39: Perrota S, Locatelli F, La Manna A, et al. Anti CD20 monoclonal antibody (Rituximab) for life- threatening autoimmune haemolytic anaemia in a patient with systemic lupus erythematosus. B.J. Haematol; 116: Rose BD, Appel GA. Treatment of resistant lupus nephritis. UpToDate 2003; 11: Sesso R, Monteiro M, Sato E, et al. A controlled trial of pulse cyclophosphamide versus pulse methylprednisolone in severe lupus nephritis. Lupus 1994; 3: Shur PH. Overview of the therapy and prognosis of systemic lupus erythematosus in adults. UpToDate 2003; 11: Smolen JS. Therapy of systemic lupus erythematosus: a look into the future. Arhtritis Res. 2002; 4 (Suppl 3): S25 S Steinberg AD. The therapy of lupus nephritis. Kidney Int. 1986; 30: Tam LS, Li EK, Leung CB, et al. Long-term treatment of lupus nephritis with cyclosporin A. QJM 1998; 91: Trnavský K. Příručka farmakoterapie revmatických chorob. Grada Avicenum Praha 1994: Vollenhoven R, Engleman E, McGuire J. An open study of dehydroepiandrosterone in systemic lupus erythematosus. Arthr Rheum 1994; 37:
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 2 k rozhodnutí o změně registrace sp. zn. sukls25846/2010 a sukls25848/2010 a příloha ke sp. zn. sukls156917/2010 a sukls157010/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 NÁZEV PŘÍPRAVKU Pentasa Sachet
Příloha č. 2 k rozhodnutí o změně registrace sp. zn. sukls25846/2010 a sukls25848/2010 a příloha ke sp. zn. sukls156917/2010 a sukls157010/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 NÁZEV PŘÍPRAVKU Pentasa Sachet
sp.zn. sukls226144/2009 a sp.zn.:sukls109033/2012, sukls173847/2012
 sp.zn. sukls226144/2009 a sp.zn.:sukls109033/2012, sukls173847/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PLAQUENIL 200 mg Potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Hydroxychloroquini
sp.zn. sukls226144/2009 a sp.zn.:sukls109033/2012, sukls173847/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PLAQUENIL 200 mg Potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Hydroxychloroquini
Systémový lupus erythematosus
 www.printo.it/pediatric-rheumatology/cz/intro Systémový lupus erythematosus Verze č 2016 1. CO JE SYSTÉMOVÝ LUPUS ERYTHEMATOSUS 1.1 Co je to? Systémový lupus erythematosus (SLE) je chronické autoimunní
www.printo.it/pediatric-rheumatology/cz/intro Systémový lupus erythematosus Verze č 2016 1. CO JE SYSTÉMOVÝ LUPUS ERYTHEMATOSUS 1.1 Co je to? Systémový lupus erythematosus (SLE) je chronické autoimunní
Příloha č. 1 k opravě rozhodnutí o změně registrace sp.zn. sukls164200/2010
 Příloha č. 1 k opravě rozhodnutí o změně registrace sp.zn. sukls164200/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU (SPC) 1. NÁZEV PŘÍPRAVKU BELODERM Mast 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Betamethasoni dipropionas
Příloha č. 1 k opravě rozhodnutí o změně registrace sp.zn. sukls164200/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU (SPC) 1. NÁZEV PŘÍPRAVKU BELODERM Mast 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Betamethasoni dipropionas
Sp.zn.sukls113275/2013, sukls113277/2013, sukls113278/2013, sukls113279/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Sp.zn.sukls113275/2013, sukls113277/2013, sukls113278/2013, sukls113279/2013 1. NÁZEV PŘÍPRAVKU SOUHRN ÚDAJŮ O PŘÍPRAVKU Vitamin D 3 Radaydrug 800 IU potahované tablety Vitamin D 3 Radaydrug 1 000 IU potahované
Sp.zn.sukls113275/2013, sukls113277/2013, sukls113278/2013, sukls113279/2013 1. NÁZEV PŘÍPRAVKU SOUHRN ÚDAJŮ O PŘÍPRAVKU Vitamin D 3 Radaydrug 800 IU potahované tablety Vitamin D 3 Radaydrug 1 000 IU potahované
Příloha č. 2 k rozhodnutí o změně registrace sp.zn.sukls157416/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 2 k rozhodnutí o změně registrace sp.zn.sukls157416/2011 1. NÁZEV PŘÍPRAVKU Aspirin 100 tablety SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 tableta obsahuje léčivou látku:
Příloha č. 2 k rozhodnutí o změně registrace sp.zn.sukls157416/2011 1. NÁZEV PŘÍPRAVKU Aspirin 100 tablety SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 tableta obsahuje léčivou látku:
PROGRAM Pracovní verze aktualizace k 30.11.2012 s výhradou dalších změn a úprav
 PROGRAM Pracovní verze aktualizace k 30.11.2012 s výhradou dalších změn a úprav Sekce lékařů 8. ledna 18.00 22.00 Stavba doprovodné výstavy I (Foyer recepce, foyer kongresového sálu) 9. ledna 07.30 11.00
PROGRAM Pracovní verze aktualizace k 30.11.2012 s výhradou dalších změn a úprav Sekce lékařů 8. ledna 18.00 22.00 Stavba doprovodné výstavy I (Foyer recepce, foyer kongresového sálu) 9. ledna 07.30 11.00
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 3 k rozhodnutí o prodloužení registrace sp.zn. sukls6972/2006 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PARALEN 500 SUP čípky 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden čípek obsahuje Paracetamolum
Příloha č. 3 k rozhodnutí o prodloužení registrace sp.zn. sukls6972/2006 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PARALEN 500 SUP čípky 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden čípek obsahuje Paracetamolum
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 1. Název přípravku SOUHRN ÚDAJŮ O PŘÍPRAVKU Vitamin AD SLOVAKOFARMA 2. Kvalitativní a kvantitavní složení retinoli acetas (vitamin A) 25 000 m. j., ergocalciferolum (vitamin D 2 ) 5 000 m. j. v 1 měkké
1. Název přípravku SOUHRN ÚDAJŮ O PŘÍPRAVKU Vitamin AD SLOVAKOFARMA 2. Kvalitativní a kvantitavní složení retinoli acetas (vitamin A) 25 000 m. j., ergocalciferolum (vitamin D 2 ) 5 000 m. j. v 1 měkké
Co je to imunoterapie?
 Co je to imunoterapie? Imunitní systém má důležitou úlohu v ochraně člověka před nádorovým onemocněním. Jestliže přesto dojde k rozvoji nádorového onemocnění, může vhodně povzbuzený imunitní systém pacienta
Co je to imunoterapie? Imunitní systém má důležitou úlohu v ochraně člověka před nádorovým onemocněním. Jestliže přesto dojde k rozvoji nádorového onemocnění, může vhodně povzbuzený imunitní systém pacienta
Příloha č. 2 ke sdělení sp.zn.sukls59753/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU NUROFEN 400 MG
 Příloha č. 2 ke sdělení sp.zn.sukls59753/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU NUROFEN 400 MG 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivá látka: Ibuprofenum 400 mg v jedné obalené tabletě
Příloha č. 2 ke sdělení sp.zn.sukls59753/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU NUROFEN 400 MG 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivá látka: Ibuprofenum 400 mg v jedné obalené tabletě
U pacientů, jejichž tělesná hmotnost je vyšší než 100 kg, se dávky přesahující 800 mg/infuzi nedoporučují.
 EDUKAČNÍ MATERIÁLY RoActemra (tocilizumab) Kapesní dávkovací karta pro revmatoidní artritidu Přípravek RoActemra v kombinaci s metotrexátem (MTX) je indikován k léčbě středně těžké až těžké aktivní revmatoidní
EDUKAČNÍ MATERIÁLY RoActemra (tocilizumab) Kapesní dávkovací karta pro revmatoidní artritidu Přípravek RoActemra v kombinaci s metotrexátem (MTX) je indikován k léčbě středně těžké až těžké aktivní revmatoidní
Příloha č. 3 k rozhodnutí o prodloužení registrace sp. zn.:sukls167009/2008 a příloha k sp.zn. sukls80895/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 3 k rozhodnutí o prodloužení registrace sp. zn.:sukls167009/2008 a příloha k sp.zn. sukls80895/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU LODRONAT 520 potahované tablety 2. KVALITATIVNÍ
Příloha č. 3 k rozhodnutí o prodloužení registrace sp. zn.:sukls167009/2008 a příloha k sp.zn. sukls80895/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU LODRONAT 520 potahované tablety 2. KVALITATIVNÍ
www.printo.it/pediatric-rheumatology/cz/intro
 www.printo.it/pediatric-rheumatology/cz/intro Candle Verze č 2016 1. CO JE CANDLE 1.1 Co je to? Chronická atypická neutrofilní dermatóza s lipodystrofií a zvýšenou teplotou (CANDLE) patří mezi vzácná dědičná
www.printo.it/pediatric-rheumatology/cz/intro Candle Verze č 2016 1. CO JE CANDLE 1.1 Co je to? Chronická atypická neutrofilní dermatóza s lipodystrofií a zvýšenou teplotou (CANDLE) patří mezi vzácná dědičná
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. PROPAFENON AL 150 PROPAFENON AL 300 potahované tablety propafenoni hydrochloridum
 Příloha č.1 ke sdělení sp.zn.sukls8522/2012 a sukls8523/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE PROPAFENON AL 150 PROPAFENON AL 300 potahované tablety propafenoni hydrochloridum Přečtěte si pozorně
Příloha č.1 ke sdělení sp.zn.sukls8522/2012 a sukls8523/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE PROPAFENON AL 150 PROPAFENON AL 300 potahované tablety propafenoni hydrochloridum Přečtěte si pozorně
Jedna obalená tableta obsahuje acidum acetylsalicylicum 500 mg.
 Sp.zn.sukls259906/2011 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU Aspirin 500 mg obalené tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna obalená tableta obsahuje acidum acetylsalicylicum 500 mg.
Sp.zn.sukls259906/2011 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU Aspirin 500 mg obalené tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna obalená tableta obsahuje acidum acetylsalicylicum 500 mg.
Příloha č. 1 k opravě rozhodnutí o změně registrace sp.zn. sukls165529/2010
 Příloha č. 1 k opravě rozhodnutí o změně registrace sp.zn. sukls165529/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU FLUTAMID SANDOZ 250 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Flutamidum
Příloha č. 1 k opravě rozhodnutí o změně registrace sp.zn. sukls165529/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU FLUTAMID SANDOZ 250 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Flutamidum
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 3 k rozhodnutí o změně registrace sp. zn. sukls159867/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Rismyl 35 mg potahované tablety natrii risedronas 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Příloha č. 3 k rozhodnutí o změně registrace sp. zn. sukls159867/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Rismyl 35 mg potahované tablety natrii risedronas 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
PARALEN 500 tablety. Doporučené dávkování paracetamolu; VĚK HMOTNOST Jednotlivá dávka Max. denní dávka 21-25 kg
 Příloha č. 2 k opravě sdělení sp.zn. sukls226519/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PARALEN 500 tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje paracetamolum 500 mg.
Příloha č. 2 k opravě sdělení sp.zn. sukls226519/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PARALEN 500 tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje paracetamolum 500 mg.
Tvrdá tobolka se světle modrým víčkem a světle modrým tělem.
 Příloha č. 3 k rozhodnutí o registraci sp.zn. sukls127013/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Orlistat Polpharma 60 mg, tvrdé tobolky 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tvrdá tobolka
Příloha č. 3 k rozhodnutí o registraci sp.zn. sukls127013/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Orlistat Polpharma 60 mg, tvrdé tobolky 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tvrdá tobolka
Souhrn údajů o přípravku
 1. Název přípravku Brufen sirup 2. Kvalitativní a kvantitativní složení Ibuprofenum 100 mg v 5 ml sirupu Obsahuje methylparaben, propylparaben, sacharosu, sorbitol, oranžovou žluť. Úplný seznam pomocných
1. Název přípravku Brufen sirup 2. Kvalitativní a kvantitativní složení Ibuprofenum 100 mg v 5 ml sirupu Obsahuje methylparaben, propylparaben, sacharosu, sorbitol, oranžovou žluť. Úplný seznam pomocných
Sp.zn.sukls88807/2015
 Sp.zn.sukls88807/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU NORMAGLYC 500 mg, potahované tablety NORMAGLYC 850 mg, potahované tablety NORMAGLYC 1000 mg, potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ
Sp.zn.sukls88807/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU NORMAGLYC 500 mg, potahované tablety NORMAGLYC 850 mg, potahované tablety NORMAGLYC 1000 mg, potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ
sp.zn.sukls188553/2014
 sp.zn.sukls188553/2014 1. NÁZEV PŘÍPRAVKU SOUHRN ÚDAJŮ O PŘÍPRAVKU tablety s prodlouženým uvolňováním. 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta s prodlouženým uvolňováním obsahuje pentoxifyllinum
sp.zn.sukls188553/2014 1. NÁZEV PŘÍPRAVKU SOUHRN ÚDAJŮ O PŘÍPRAVKU tablety s prodlouženým uvolňováním. 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta s prodlouženým uvolňováním obsahuje pentoxifyllinum
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 sp.zn. sukls197050/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU RANISAN 75 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna potahovaná tableta obsahuje ranitidini hydrochloridum
sp.zn. sukls197050/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU RANISAN 75 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna potahovaná tableta obsahuje ranitidini hydrochloridum
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU CYSAXAL 100 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje cyproteroni acetas 100 mg. Pomocné látky: monohydrát laktosy 167,0
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU CYSAXAL 100 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje cyproteroni acetas 100 mg. Pomocné látky: monohydrát laktosy 167,0
Toxické myopatie. Edvard Ehler
 Toxické myopatie Edvard Ehler Toxické myopatie Medikamenty, rekreační drogy Průmyslové látky Biologické toxiny Různý patomechanismus Reverzibilita (zčásti) Iatrogenní Prevence Actin-myosin: kontrakce svalu
Toxické myopatie Edvard Ehler Toxické myopatie Medikamenty, rekreační drogy Průmyslové látky Biologické toxiny Různý patomechanismus Reverzibilita (zčásti) Iatrogenní Prevence Actin-myosin: kontrakce svalu
Souhrn údajů o přípravku
 sp.zn. sukls219612/2015 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU BONEFOS koncentrát pro infuzní roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 ml koncentrátu obsahuje: dinatrii clodronas tetrahydricus
sp.zn. sukls219612/2015 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU BONEFOS koncentrát pro infuzní roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 ml koncentrátu obsahuje: dinatrii clodronas tetrahydricus
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 sp.zn. sukls146011/2014 a sukls35098/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Varilrix Prášek a rozpouštědlo pro injekční roztok. Vakcína proti planým neštovicím 2. KVALITATIVNÍ A KVANTITATIVNÍ
sp.zn. sukls146011/2014 a sukls35098/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Varilrix Prášek a rozpouštědlo pro injekční roztok. Vakcína proti planým neštovicím 2. KVALITATIVNÍ A KVANTITATIVNÍ
Injekční roztok. Tmavě hnědý, neprůhledný roztok s ph 5,0 7,0 a s přibližnou osmolaritou 400 mosm/l.
 sp.zn. sukls57833/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakákoli
sp.zn. sukls57833/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakákoli
Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn. sukls82168/2008 SOUHRN ÚDAJŮ O PŘÍPRAVKU. 1. NÁZEV PŘÍPRAVKU NeuroMax forte
 Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn. sukls82168/2008 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU NeuroMax forte 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Thiamini hydrochloridum ( vitamin
Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn. sukls82168/2008 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU NeuroMax forte 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Thiamini hydrochloridum ( vitamin
CO POTŘEBUJETE VĚDĚT O NÁDORECH
 CO POTŘEBUJETE VĚDĚT O NÁDORECH varlat OBSAH Co jsou varlata................................... 2 Co jsou nádory................................... 3 Jaké jsou rizikové faktory vzniku nádoru varlete......
CO POTŘEBUJETE VĚDĚT O NÁDORECH varlat OBSAH Co jsou varlata................................... 2 Co jsou nádory................................... 3 Jaké jsou rizikové faktory vzniku nádoru varlete......
Henoch-Schönleinova purpura
 www.printo.it/pediatric-rheumatology/cz/intro Henoch-Schönleinova purpura Verze č 2016 1. CO JE HENOCH-SCHÖNLEINOVA PURPURA 1.1 Co je to? Henoch-Schönleinova purpura je onemocnění, při kterém dochází k
www.printo.it/pediatric-rheumatology/cz/intro Henoch-Schönleinova purpura Verze č 2016 1. CO JE HENOCH-SCHÖNLEINOVA PURPURA 1.1 Co je to? Henoch-Schönleinova purpura je onemocnění, při kterém dochází k
Příloha č.3 k rozhodnutí o registraci sp.zn. sukls48796/2009
 Příloha č.3 k rozhodnutí o registraci sp.zn. sukls48796/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU GLUCOPHAGE XR 750 mg tablety s prodlouženým uvolňováním 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Příloha č.3 k rozhodnutí o registraci sp.zn. sukls48796/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU GLUCOPHAGE XR 750 mg tablety s prodlouženým uvolňováním 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. INTRATECT 50 g/l infuzní roztok Immunoglobulinum humanum normale ad usum intravenosum (IVIg)
 Příloha č. 1 k rozhodnutí o registraci sp.zn. sukls228408/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE INTRATECT 50 g/l infuzní roztok Immunoglobulinum humanum normale ad usum intravenosum (IVIg)
Příloha č. 1 k rozhodnutí o registraci sp.zn. sukls228408/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE INTRATECT 50 g/l infuzní roztok Immunoglobulinum humanum normale ad usum intravenosum (IVIg)
Příloha č. 2 k rozhodnutí o změně registrace sp. zn. sukls20675/2011 a příloha ke sp. zn. sukls155771/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 2 k rozhodnutí o změně registrace sp. zn. sukls20675/2011 a příloha ke sp. zn. sukls155771/2011 1. NÁZEV PŘÍPRAVKU LODRONAT 520 potahované tablety SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A
Příloha č. 2 k rozhodnutí o změně registrace sp. zn. sukls20675/2011 a příloha ke sp. zn. sukls155771/2011 1. NÁZEV PŘÍPRAVKU LODRONAT 520 potahované tablety SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A
Pomocná látka se známým účinkem: 1 tvrdá tobolka obsahuje 37,68 mg sacharózy.
 sp.zn. sukls93386/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU SUPRELIP 200 mg, tvrdé tobolky 2. KVALITATIVNÍ I KVANTITATIVNÍ SLOŽENÍ Fenofibratum 200 mg v l tvrdé tobolce. Pomocná látka se známým
sp.zn. sukls93386/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU SUPRELIP 200 mg, tvrdé tobolky 2. KVALITATIVNÍ I KVANTITATIVNÍ SLOŽENÍ Fenofibratum 200 mg v l tvrdé tobolce. Pomocná látka se známým
příčiny porucha činnosti střev bez určité organické 11.6.2014 motilita (pohyb střev) dyskinezie (porucha hybnosti střev)
 OŠETŘOVATELSTVÍ ONEMOCNĚNÍ TENKÉHO STŘEVA Mgr. Hana Ottová Projekt POMOC PRO TEBE CZ.1.07/1.5.00/34.0339 Označení Název DUM Anotace Autor Jazyk Klíčová slova Cílová skupina Stupeň vzdělávání Studijní obor
OŠETŘOVATELSTVÍ ONEMOCNĚNÍ TENKÉHO STŘEVA Mgr. Hana Ottová Projekt POMOC PRO TEBE CZ.1.07/1.5.00/34.0339 Označení Název DUM Anotace Autor Jazyk Klíčová slova Cílová skupina Stupeň vzdělávání Studijní obor
Phenylephrini hydrochloridum Acidum ascorbicum. Pomocné látky se známým účinkem: sacharóza 3725 mg/sáček, sodík 116 mg/sáček.
 sp. zn. sukls189078/2015 SOUHRN ÚDAJU O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU COLDREX MaxGrip Citron prášek pro perorální roztok v sáčku 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden sáček obsahuje: Paracetamolum
sp. zn. sukls189078/2015 SOUHRN ÚDAJU O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU COLDREX MaxGrip Citron prášek pro perorální roztok v sáčku 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden sáček obsahuje: Paracetamolum
Biologický materiál je tvořen vzorky tělních tekutin, tělesných sekretů, exkretů a tkání.
 Otázka: Druhy biologického materiálu Předmět: Biologie Přidal(a): moni.ka Druhy biologického materiálu Biologický materiál je tvořen vzorky tělních tekutin, tělesných sekretů, exkretů a tkání. Tělní tekutiny
Otázka: Druhy biologického materiálu Předmět: Biologie Přidal(a): moni.ka Druhy biologického materiálu Biologický materiál je tvořen vzorky tělních tekutin, tělesných sekretů, exkretů a tkání. Tělní tekutiny
Potransfuzní reakce. Rozdělení potransfuzních reakcí a komplikací
 Potransfuzní reakce Potransfuzní reakcí rozumíme nežádoucí účinek podaného transfuzního přípravku. Od roku 2005 (dle platné legislativy) rozlišujeme: závažná nežádoucí příhoda ( vzniká v souvislosti s
Potransfuzní reakce Potransfuzní reakcí rozumíme nežádoucí účinek podaného transfuzního přípravku. Od roku 2005 (dle platné legislativy) rozlišujeme: závažná nežádoucí příhoda ( vzniká v souvislosti s
Juvenilní dermatomyozitida
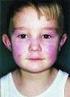 www.printo.it/pediatric-rheumatology/cz/intro Juvenilní dermatomyozitida Verze č 2016 1. CO JE JUVENILNÍ DERMATOMYOZITIDA 1.1 Co je to? Juvenilní dermatomyozitida (JDM) je vzácné onemocnění, které postihuje
www.printo.it/pediatric-rheumatology/cz/intro Juvenilní dermatomyozitida Verze č 2016 1. CO JE JUVENILNÍ DERMATOMYOZITIDA 1.1 Co je to? Juvenilní dermatomyozitida (JDM) je vzácné onemocnění, které postihuje
MALÝ. PRAKTICKÝ. ÚČINNÝ.
 MALÝ. PRAKTICKÝ. ÚČINNÝ. 1) NOVÝ 50 mg/ml Nový 50 mg/ml methotrexát v předplněných injekčních stříkačkách Metoject je vysoce účinný 1) Metoject je účinnější než perorální mtx ve stejné dávce 1) 90 % ACR
MALÝ. PRAKTICKÝ. ÚČINNÝ. 1) NOVÝ 50 mg/ml Nový 50 mg/ml methotrexát v předplněných injekčních stříkačkách Metoject je vysoce účinný 1) Metoject je účinnější než perorální mtx ve stejné dávce 1) 90 % ACR
Příloha č. 2 k rozhodnutí o změně registrace sp.zn. sukls118033/2010
 Příloha č. 2 k rozhodnutí o změně registrace sp.zn. sukls118033/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Cardioxane prášek pro přípravu infuzního roztoku. 2. KVALITATIVNÍ A KVANTITATIVNÍ
Příloha č. 2 k rozhodnutí o změně registrace sp.zn. sukls118033/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Cardioxane prášek pro přípravu infuzního roztoku. 2. KVALITATIVNÍ A KVANTITATIVNÍ
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. SALAZOPYRIN EN enterosolventní tablety sulfasalazinum
 sp.zn. sukls272322/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE SALAZOPYRIN EN enterosolventní tablety sulfasalazinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
sp.zn. sukls272322/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE SALAZOPYRIN EN enterosolventní tablety sulfasalazinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 2 k rozhodnutí o změně registrace sp. zn. sukls170515/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Risedronat Mylan 35 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna
Příloha č. 2 k rozhodnutí o změně registrace sp. zn. sukls170515/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Risedronat Mylan 35 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna
Příbalová informace: informace pro pacienta. Milurit 100 Milurit 300 tablety allopurinolum
 sp. zn. sukls107451/2015 a sukls107472/2015 Příbalová informace: informace pro pacienta Milurit 100 Milurit 300 tablety allopurinolum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
sp. zn. sukls107451/2015 a sukls107472/2015 Příbalová informace: informace pro pacienta Milurit 100 Milurit 300 tablety allopurinolum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
Souhrn údajů o přípravku
 Příloha č. 3 ke sdělení sp.zn. sukls93024/2010 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU Isoprinosine tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivá látka: inosinum pranobexum 500 mg v 1 tabletě
Příloha č. 3 ke sdělení sp.zn. sukls93024/2010 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU Isoprinosine tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivá látka: inosinum pranobexum 500 mg v 1 tabletě
Příloha č. 3 k rozhodnutí o převodu registrace sp. zn. sukls198549/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 3 k rozhodnutí o převodu registrace sp. zn. sukls198549/2010 1. NÁZEV PŘÍPRAVKU LANBICA 50 mg Potahované tablety SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 potahovaná
Příloha č. 3 k rozhodnutí o převodu registrace sp. zn. sukls198549/2010 1. NÁZEV PŘÍPRAVKU LANBICA 50 mg Potahované tablety SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 potahovaná
Deficit mevalonátkinázy (MKD) (nebo hyper IgD syndrom)
 www.printo.it/pediatric-rheumatology/cz/intro Deficit mevalonátkinázy (MKD) (nebo hyper IgD syndrom) Verze č 2016 1. CO JE MKD? 1.1 Co je to? Deficit mevalonákinázy patří mezi dědičná onemocnění. Jedná
www.printo.it/pediatric-rheumatology/cz/intro Deficit mevalonátkinázy (MKD) (nebo hyper IgD syndrom) Verze č 2016 1. CO JE MKD? 1.1 Co je to? Deficit mevalonákinázy patří mezi dědičná onemocnění. Jedná
CÍL 8: SNÍŽENÍ VÝSKYTU NEINFEKČNÍCH NEMOCÍ
 CÍL 8: SNÍŽENÍ VÝSKYTU NEINFEKČNÍCH NEMOCÍ DO ROKU 2020 BY SE MĚLA SNÍŽIT NEMOCNOST, ČETNOST ZDRAVOTNÍCH NÁSLEDKŮ A PŘEDČASNÁ ÚMRTNOST V DŮSLEDKU HLAVNÍCH CHRONICKÝCH NEMOCÍ NA NEJNIŽŠÍ MOŽNOU ÚROVEŇ Nejčastějšími
CÍL 8: SNÍŽENÍ VÝSKYTU NEINFEKČNÍCH NEMOCÍ DO ROKU 2020 BY SE MĚLA SNÍŽIT NEMOCNOST, ČETNOST ZDRAVOTNÍCH NÁSLEDKŮ A PŘEDČASNÁ ÚMRTNOST V DŮSLEDKU HLAVNÍCH CHRONICKÝCH NEMOCÍ NA NEJNIŽŠÍ MOŽNOU ÚROVEŇ Nejčastějšími
Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat.
 sp.zn. sukls88228/2014 Příbalová informace: Informace pro uživatele BONEFOS koncentrát pro infuzní roztok (Dinatrii clodronas) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
sp.zn. sukls88228/2014 Příbalová informace: Informace pro uživatele BONEFOS koncentrát pro infuzní roztok (Dinatrii clodronas) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn.: sukls55068/2009
 Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn.: sukls55068/2009 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE AGOFOLLIN Injekční roztok (Estradioli dipropionas) Přečtěte si pozorně celou příbalovou
Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn.: sukls55068/2009 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE AGOFOLLIN Injekční roztok (Estradioli dipropionas) Přečtěte si pozorně celou příbalovou
OBSAH. Nové poznatky o mikroalbuminurii jako biologickém markeru renálních a kardiovaskulárních onemocnění...37
 OBSAH Ročník 1 Ročník 1, č. 1-2007 Měření glomerulární filtrace v klinické praxi...2 Cévní přístup a srdeční onemocnění existuje mezi nimi nějaký vztah?...7 Antihypertenzní léčba obézních hypertoniků...12
OBSAH Ročník 1 Ročník 1, č. 1-2007 Měření glomerulární filtrace v klinické praxi...2 Cévní přístup a srdeční onemocnění existuje mezi nimi nějaký vztah?...7 Antihypertenzní léčba obézních hypertoniků...12
Livial tablety tibolonum
 Livial tablety tibolonum Příbalová informace - RP Informace pro použití, čtěte pozorně! Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat. Ponechte si příbalovou
Livial tablety tibolonum Příbalová informace - RP Informace pro použití, čtěte pozorně! Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat. Ponechte si příbalovou
V roce 1981 byly v USA poprvé popsány příznaky nového onemocnění, které později dostalo jméno AIDS /Acquired Immune Deficiency Syndrome/ neboli
 Lenka Klimešová V roce 1981 byly v USA poprvé popsány příznaky nového onemocnění, které později dostalo jméno AIDS /Acquired Immune Deficiency Syndrome/ neboli Syndrom získaného imunodeficitu. V roce 1983
Lenka Klimešová V roce 1981 byly v USA poprvé popsány příznaky nového onemocnění, které později dostalo jméno AIDS /Acquired Immune Deficiency Syndrome/ neboli Syndrom získaného imunodeficitu. V roce 1983
Juvenilní spondylartritida/artritida s entezitidou (SPA/ERA)
 www.printo.it/pediatric-rheumatology/cz/intro Juvenilní spondylartritida/artritida s entezitidou (SPA/ERA) Verze č 2016 1. CO JE JUVENILNÍ SPONDYLARTRITIDA/ARTRITIDA S ENTEZITIDOU (SpA-ERA) 1.1 Co je to?
www.printo.it/pediatric-rheumatology/cz/intro Juvenilní spondylartritida/artritida s entezitidou (SPA/ERA) Verze č 2016 1. CO JE JUVENILNÍ SPONDYLARTRITIDA/ARTRITIDA S ENTEZITIDOU (SpA-ERA) 1.1 Co je to?
Diagnostika a příznaky mnohočetného myelomu. J.Minařík, V.Ščudla
 Diagnostika a příznaky mnohočetného myelomu J.Minařík, V.Ščudla Mnohočetný myelom Nekontrolované zmnožení nádorově změněných plasmatických buněk v kostní dřeni Mnohočetný = obvykle více oblastí kostní
Diagnostika a příznaky mnohočetného myelomu J.Minařík, V.Ščudla Mnohočetný myelom Nekontrolované zmnožení nádorově změněných plasmatických buněk v kostní dřeni Mnohočetný = obvykle více oblastí kostní
II. Interní klinika, odd. gastroenterologie, FNKV, 3.LF UK Hnaníček J., Mandys V., Kment M., Zádorová Z.
 II. Interní klinika, odd. gastroenterologie, FNKV, 3.LF UK Hnaníček J., Mandys V., Kment M., Zádorová Z. Copaxon - spouštěcí faktor ulcerózní kolitidy? hypotéza: může copaxon indukovat ulcerózní kolitidu?
II. Interní klinika, odd. gastroenterologie, FNKV, 3.LF UK Hnaníček J., Mandys V., Kment M., Zádorová Z. Copaxon - spouštěcí faktor ulcerózní kolitidy? hypotéza: může copaxon indukovat ulcerózní kolitidu?
Vyšetření imunoglobulinů
 Vyšetření imunoglobulinů Celkové mn. Ig elektroforéza bílkovin jako procentuální zastoupení gamafrakce, vyšetřením ke zjištění možného paraproteinu. velmi hrubé vyšetření, odhalení pouze výrazných změn
Vyšetření imunoglobulinů Celkové mn. Ig elektroforéza bílkovin jako procentuální zastoupení gamafrakce, vyšetřením ke zjištění možného paraproteinu. velmi hrubé vyšetření, odhalení pouze výrazných změn
Souhrn údajů o přípravku
 sp.zn. sukls22891/2008 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU Salofalk 500, čípky 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivá látka: jeden čípek obsahuje mesalazinum 500 mg Úplný seznam pomocných
sp.zn. sukls22891/2008 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU Salofalk 500, čípky 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivá látka: jeden čípek obsahuje mesalazinum 500 mg Úplný seznam pomocných
KURZ ZÁPADNÍ FYTOTERAPIE
 KURZ ZÁPADNÍ FYTOTERAPIE Západní fytoterapie jako samostatný obor, či jako jeden z profesních oborů klinické naturopatie se velmi specificky aplikuje při léčbě a prevenci široké škály zdravotních problémů.
KURZ ZÁPADNÍ FYTOTERAPIE Západní fytoterapie jako samostatný obor, či jako jeden z profesních oborů klinické naturopatie se velmi specificky aplikuje při léčbě a prevenci široké škály zdravotních problémů.
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 3 k rozhodnutí o registraci sp.zn. sukls42544-6/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Pexogies 0,088 mg tablety Pexogies 0,18 mg tablety Pexogies 0,7 mg tablety 2. KVALITATIVNÍ A
Příloha č. 3 k rozhodnutí o registraci sp.zn. sukls42544-6/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Pexogies 0,088 mg tablety Pexogies 0,18 mg tablety Pexogies 0,7 mg tablety 2. KVALITATIVNÍ A
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 3 k rozhodnutí o prodloužení registrace sp.zn. sukls2006/2007 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PANADOL Rapide potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna potahovaná
Příloha č. 3 k rozhodnutí o prodloužení registrace sp.zn. sukls2006/2007 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PANADOL Rapide potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna potahovaná
sp. zn. sukls178963/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU FAMOSAN 10 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
 sp. zn. sukls178963/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU FAMOSAN 10 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna potahovaná tableta obsahuje famotidinum 10 mg. Pomocné
sp. zn. sukls178963/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU FAMOSAN 10 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna potahovaná tableta obsahuje famotidinum 10 mg. Pomocné
Seminář 6: Diagnostika
 DIAGNOSTIKA AUTOIMUNITNÍCH CHOROB Seminář 6: Diagnostika autoimunitních chorob I Anamnéza plemenná predispozice, stáří (spíše zvířata středního věku), akutnost x chronicita, teplota a jiné léky (antibiotika
DIAGNOSTIKA AUTOIMUNITNÍCH CHOROB Seminář 6: Diagnostika autoimunitních chorob I Anamnéza plemenná predispozice, stáří (spíše zvířata středního věku), akutnost x chronicita, teplota a jiné léky (antibiotika
SOUHRN ÚDAJŮ O PŘÍPRAVKU. 1. NÁZEV PŘÍPRAVKU Ramonna 1500 mikrogramů, tableta
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Ramonna 1500 mikrogramů, tableta 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje levonorgestrelum1500 mikrogramů. Pomocné látky se známým účinkem:
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Ramonna 1500 mikrogramů, tableta 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje levonorgestrelum1500 mikrogramů. Pomocné látky se známým účinkem:
SOUHRN ÚDAJŮ O PŘÍPRAVKU. Injekční suspenze, adsorbovaná vakcína proti tetanu, bez konzervačních prosředků
 Tento dokument je odbornou informací k léčivému přípravku, který je předmětem specifického léčebného programu. Odborná informace byla předložena žadatelem o specifický léčebný program. Nejedná se o dokument
Tento dokument je odbornou informací k léčivému přípravku, který je předmětem specifického léčebného programu. Odborná informace byla předložena žadatelem o specifický léčebný program. Nejedná se o dokument
Vlastnosti Medroxyprogesteron acetát (17-alfa-hydroxy-6-alfa-methylprogesteron acetát) je derivátem progesteronu a patří tak do skupiny gestagenů.
 PŘÍBALOVÁ INFORMACE Informace pro použití, čtěte pozorně! DEPO-PROVERA (medroxyprogesteroni acetas) injekční suspenze Složení Jeden ml obsahuje: Léčivá látka: Medroxyprogesteroni acetas 150 mg Pomocné
PŘÍBALOVÁ INFORMACE Informace pro použití, čtěte pozorně! DEPO-PROVERA (medroxyprogesteroni acetas) injekční suspenze Složení Jeden ml obsahuje: Léčivá látka: Medroxyprogesteroni acetas 150 mg Pomocné
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 sp.zn.sukls143731/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU BISEPTOL 120 BISEPTOL 480 Tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ BISEPTOL 120 Trimethoprimum 20 mg, sulfamethoxazolum 100 mg
sp.zn.sukls143731/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU BISEPTOL 120 BISEPTOL 480 Tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ BISEPTOL 120 Trimethoprimum 20 mg, sulfamethoxazolum 100 mg
Souhrn údajů o přípravku
 Příloha č. 3 k rozhodnutí o převodu registrace sp.zn.sukls90018/2010 1. NÁZEV PŘÍPRAVKU Imuran Souhrn údajů o přípravku 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Azathioprinum, 50 mg lyofilizované substance
Příloha č. 3 k rozhodnutí o převodu registrace sp.zn.sukls90018/2010 1. NÁZEV PŘÍPRAVKU Imuran Souhrn údajů o přípravku 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Azathioprinum, 50 mg lyofilizované substance
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 3 k rozhodnutí o prodloužení registrace sp.zn. sukls104507/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Alendronat-ratiopharm 70 mg tablety 2. KVALITATIVNÍ I KVANTITATIVNÍ SLOŽENÍ Jedna
Příloha č. 3 k rozhodnutí o prodloužení registrace sp.zn. sukls104507/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Alendronat-ratiopharm 70 mg tablety 2. KVALITATIVNÍ I KVANTITATIVNÍ SLOŽENÍ Jedna
Symtomatická cholecystolitiáza současný pohled na chenodisoluci
 Symtomatická cholecystolitiáza současný pohled na chenodisoluci Papík Z.,Vítek J.,Bureš J. II.interní klinika Fakultní nemocnice Hradec Králové Cholelitiáza patří mezi nejčastěji se vyskytující choroby
Symtomatická cholecystolitiáza současný pohled na chenodisoluci Papík Z.,Vítek J.,Bureš J. II.interní klinika Fakultní nemocnice Hradec Králové Cholelitiáza patří mezi nejčastěji se vyskytující choroby
Příloha č. 2 k rozhodnutí o změně registrace sp. zn. sukls10679/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 2 k rozhodnutí o změně registrace sp. zn. sukls10679/2012 1. NÁZEV PŘÍPRAVKU THYMOGLOBULINE 5 mg/ml, prášek pro infuzní roztok SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Příloha č. 2 k rozhodnutí o změně registrace sp. zn. sukls10679/2012 1. NÁZEV PŘÍPRAVKU THYMOGLOBULINE 5 mg/ml, prášek pro infuzní roztok SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Příloha II. Vědecké závěry
 Příloha II Vědecké závěry 11 Vědecké závěry Po zvážení revidovaného konečného doporučení Farmakovigilančního výboru pro posuzování rizik léčiv (PRAC) ze dne 10. července 2014 týkajícího se léčivých přípravků
Příloha II Vědecké závěry 11 Vědecké závěry Po zvážení revidovaného konečného doporučení Farmakovigilančního výboru pro posuzování rizik léčiv (PRAC) ze dne 10. července 2014 týkajícího se léčivých přípravků
Adalimumabum je rekombinantní lidská monoklonální protilátka produkovaná ovariálními buňkami čínských křečků.
 1. NÁZEV PŘÍPRAVKU Humira 40 mg injekční roztok v předplněném peru 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna předplněné pero na jedno použití o objemu 0,8 ml obsahuje adalimumabum 40 mg. Adalimumabum
1. NÁZEV PŘÍPRAVKU Humira 40 mg injekční roztok v předplněném peru 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna předplněné pero na jedno použití o objemu 0,8 ml obsahuje adalimumabum 40 mg. Adalimumabum
Příloha č. 1 k rozhodnutí o změně registrace sp.zn.sukls90890/2011 PŘÍBALOVÁ INFORMACE - INFORMACE PRO UŽIVATELE
 Příloha č. 1 k rozhodnutí o změně registrace sp.zn.sukls90890/2011 PŘÍBALOVÁ INFORMACE - INFORMACE PRO UŽIVATELE DICLOREUM, injekční roztok (diclofenacum natricum) Přečtěte si pozorně celou příbalovou
Příloha č. 1 k rozhodnutí o změně registrace sp.zn.sukls90890/2011 PŘÍBALOVÁ INFORMACE - INFORMACE PRO UŽIVATELE DICLOREUM, injekční roztok (diclofenacum natricum) Přečtěte si pozorně celou příbalovou
Rekombinantní lidský keratinocyty stimulující faktor - palifermin ( Kepivance, Amgen )
 Rekombinantní lidský keratinocyty stimulující faktor - palifermin ( Kepivance, Amgen ) Návrh Co - trialu CMG 2006 Palifermin -prevence orální mukositidy MUDr. Evžen Gregora OKH FNKV Praha PALIFERMIN (
Rekombinantní lidský keratinocyty stimulující faktor - palifermin ( Kepivance, Amgen ) Návrh Co - trialu CMG 2006 Palifermin -prevence orální mukositidy MUDr. Evžen Gregora OKH FNKV Praha PALIFERMIN (
SOUHRN ÚDAJŮ O PŘÍPRAVKU. Jeden gram gelu obsahuje calcipotriolum 50 mikrogramů (jako monohydrát) a betamethasonum 0,5 mg (jako dipropionát).
 Sp.zn.sukls13650/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Xamiol 50 mikrogramů/g + 0,5 mg/g gel 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden gram gelu obsahuje calcipotriolum 50 mikrogramů (jako
Sp.zn.sukls13650/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Xamiol 50 mikrogramů/g + 0,5 mg/g gel 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden gram gelu obsahuje calcipotriolum 50 mikrogramů (jako
Příloha č.1 k rozhodnutí o změně registrace sp.zn.sukls147275/2010. PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE LUCRIN DEPOT 3,75 mg,
 Příloha č.1 k rozhodnutí o změně registrace sp.zn.sukls147275/2010 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE LUCRIN DEPOT 3,75 mg, prášek pro přípravu injekční suspenze s rozpouštědlem (Leuprorelini
Příloha č.1 k rozhodnutí o změně registrace sp.zn.sukls147275/2010 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE LUCRIN DEPOT 3,75 mg, prášek pro přípravu injekční suspenze s rozpouštědlem (Leuprorelini
Příbalová informace: informace pro pacienty. Chloramphenicol VUAB 1 g. prášek pro injekční roztok chloramphenicolum
 sp.zn.sukls75310/2015 Příbalová informace: informace pro pacienty Chloramphenicol VUAB 1 g prášek pro injekční roztok chloramphenicolum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete
sp.zn.sukls75310/2015 Příbalová informace: informace pro pacienty Chloramphenicol VUAB 1 g prášek pro injekční roztok chloramphenicolum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete
Příloha č. 3 k rozhodnutí o prodloužení registrace sp.zn. sukls122181/2011 a příloha k sp. zn. sukls91704/2011
 Příloha č. 3 k rozhodnutí o prodloužení registrace sp.zn. sukls122181/2011 a příloha k sp. zn. sukls91704/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU SANDOMIGRAN 0,5 mg obalené tablety 2. KVALITATIVNÍ
Příloha č. 3 k rozhodnutí o prodloužení registrace sp.zn. sukls122181/2011 a příloha k sp. zn. sukls91704/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU SANDOMIGRAN 0,5 mg obalené tablety 2. KVALITATIVNÍ
Klinický význam protilátek proti C1q složce komplementu. Eliška Potluková 3. Interní klinika VFN a 1. LF UK
 Klinický význam protilátek proti C1q složce komplementu Eliška Potluková 3. Interní klinika VFN a 1. LF UK 1. Úvod 1. C1q, C1q a apoptóza, C1q u SLE 2. Anti-C1q, patogenita anti-c1q 3. Stanovení anti-c1q
Klinický význam protilátek proti C1q složce komplementu Eliška Potluková 3. Interní klinika VFN a 1. LF UK 1. Úvod 1. C1q, C1q a apoptóza, C1q u SLE 2. Anti-C1q, patogenita anti-c1q 3. Stanovení anti-c1q
Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn. sukls48002/2008
 Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn. sukls48002/2008 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 NÁZEV PŘÍPRAVKU Lipoplus 20% infuzní emulze 2 KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1000 ml emulze obsahuje:
Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn. sukls48002/2008 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 NÁZEV PŘÍPRAVKU Lipoplus 20% infuzní emulze 2 KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1000 ml emulze obsahuje:
SEMINÁŘ: KLINICKÁ A LABORATORNÍ DIAGNOSTIKA IMUNODEFICIENCÍ
 OSNOVA SEMINÁŘ: KLINICKÁ A LABORATORNÍ DIAGNOSTIKA IMUNODEFICIENCÍ Stavy spojené se sekundárními imunodeficiencemi Anamnestické a klinické indikace sekundárních imunodeficiencí Praktická interpretace výsledků
OSNOVA SEMINÁŘ: KLINICKÁ A LABORATORNÍ DIAGNOSTIKA IMUNODEFICIENCÍ Stavy spojené se sekundárními imunodeficiencemi Anamnestické a klinické indikace sekundárních imunodeficiencí Praktická interpretace výsledků
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Aerius 5 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje desloratadinum v množství 5 mg. Úplný seznam pomocných
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Aerius 5 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje desloratadinum v množství 5 mg. Úplný seznam pomocných
3.3 KARCINOM SLINIVKY BŘIŠNÍ
 3.3 KARCINOM SLINIVKY BŘIŠNÍ Epidemiologie Zhoubné nádory pankreatu se vyskytují převážně ve vyšším věku po 60. roce života, převážně u mužů. Zhoubné nádory pankreatu Incidence a mortalita v České republice
3.3 KARCINOM SLINIVKY BŘIŠNÍ Epidemiologie Zhoubné nádory pankreatu se vyskytují převážně ve vyšším věku po 60. roce života, převážně u mužů. Zhoubné nádory pankreatu Incidence a mortalita v České republice
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 1 ke sdělení sp.zn.sukls38824/2012 1. NÁZEV PŘÍPRAVKU ANASTAR 1 MG Potahované tablety SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna potahovaná tableta obsahuje anastrozolum
Příloha č. 1 ke sdělení sp.zn.sukls38824/2012 1. NÁZEV PŘÍPRAVKU ANASTAR 1 MG Potahované tablety SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna potahovaná tableta obsahuje anastrozolum
Souhrn údajů o přípravku
 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU Proviron - 25 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivá látka: mesterolonum 25 mg v 1 tabletě Pomocné látky: monohydrát laktózy, methylparaben, propylparaben
Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU Proviron - 25 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivá látka: mesterolonum 25 mg v 1 tabletě Pomocné látky: monohydrát laktózy, methylparaben, propylparaben
Vítám vás na přednášce
 Vítám vás na přednášce Téma dnešní přednášky ANTIDEKUBITNÍ PODLOŽKY JAKO PROSTŘEDKY VE ZDRAVOTNICTVÍ Dekubit proleženina, je to poškození kůže a podkožních tkání, které je způsobeno tlakem na hmatné kostní
Vítám vás na přednášce Téma dnešní přednášky ANTIDEKUBITNÍ PODLOŽKY JAKO PROSTŘEDKY VE ZDRAVOTNICTVÍ Dekubit proleženina, je to poškození kůže a podkožních tkání, které je způsobeno tlakem na hmatné kostní
SOUHRN ÚDAJŮ O PŘÍPRAVKU. BELOGENT mast 0,5 mg/g + 1 mg/g
 sp.zn. sukls145537/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU BELOGENT mast 0,5 mg/g + 1 mg/g 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden gram masti obsahuje betamethasoni dipropionas 0,64 mg (odpovídá
sp.zn. sukls145537/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU BELOGENT mast 0,5 mg/g + 1 mg/g 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden gram masti obsahuje betamethasoni dipropionas 0,64 mg (odpovídá
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU SPC (cs) Leflunomide medac 10 mg, Leflunomide medac 20 mg 1 1. NÁZEV PŘÍPRAVKU Leflunomide medac 10 mg potahované tablety Leflunomide medac 20 mg potahované tablety 2.
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU SPC (cs) Leflunomide medac 10 mg, Leflunomide medac 20 mg 1 1. NÁZEV PŘÍPRAVKU Leflunomide medac 10 mg potahované tablety Leflunomide medac 20 mg potahované tablety 2.
Souhrn údajů o přípravku
 sp.zn. sukls207942/2012 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU Salofalk 4 g, rektální suspenze 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivá látka: mesalazinum (acidum 5-aminosalicylicum) 4,0 g v
sp.zn. sukls207942/2012 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU Salofalk 4 g, rektální suspenze 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivá látka: mesalazinum (acidum 5-aminosalicylicum) 4,0 g v
Doporučení ČRS pro léčbu nemocných se SLE
 Doporučení ČRS pro léčbu nemocných se SLE Horák P, Tegzová D, Závada Z, Olejárová M, Skácelová M, Smržová A, Žurek M Souhrn Článek představuje doporučení České revmatologické společnosti pro léčbu systémového
Doporučení ČRS pro léčbu nemocných se SLE Horák P, Tegzová D, Závada Z, Olejárová M, Skácelová M, Smržová A, Žurek M Souhrn Článek představuje doporučení České revmatologické společnosti pro léčbu systémového
SOUHRN ÚDAJŮ O PŘÍPRAVKU. Alclometasoni dipropionas 0,5 mg (odpovídá 0,392 mg alklometasonu) v 1 g masti.
 sp.zn. sukls104332/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU AFLODERM mast 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Alclometasoni dipropionas 0,5 mg (odpovídá 0,392 mg alklometasonu) v 1 g masti.
sp.zn. sukls104332/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU AFLODERM mast 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Alclometasoni dipropionas 0,5 mg (odpovídá 0,392 mg alklometasonu) v 1 g masti.
Norifaz 35 mg potahované tablety
 Příloha č. 3 k rozhodnutí o registraci sp. zn. sukls18991/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Norifaz 35 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna potahovaná tableta
Příloha č. 3 k rozhodnutí o registraci sp. zn. sukls18991/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Norifaz 35 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna potahovaná tableta
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 sp.zn.: sukls221245/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU INDOCOLLYRE 0,1% oční kapky Oční kapky, roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivá látka: Jeden ml obsahuje indometacinum
sp.zn.: sukls221245/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU INDOCOLLYRE 0,1% oční kapky Oční kapky, roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivá látka: Jeden ml obsahuje indometacinum
Phenylephrini hydrochloridum Acidum ascorbicum ethylcelluloso obductum (odpovídá acidum ascorbicum 58,5 mg)
 sp. zn. sukls189077/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU COLDREX HORKÝ NÁPOJ CITRON S MEDEM prášek pro perorální roztok v sáčku 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden sáček obsahuje:
sp. zn. sukls189077/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU COLDREX HORKÝ NÁPOJ CITRON S MEDEM prášek pro perorální roztok v sáčku 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden sáček obsahuje:
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU VPRIV 200 U prášek pro přípravu infuzního roztoku 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna injekční lahvička obsahuje 200 jednotek* (U) velaglucerasum
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU VPRIV 200 U prášek pro přípravu infuzního roztoku 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna injekční lahvička obsahuje 200 jednotek* (U) velaglucerasum
Systémový lupus erythematodes prototyp autoimunitní choroby, diagnostika a léčba
 Přehledové články 177 Systémový lupus erythematodes prototyp autoimunitní choroby, diagnostika a léčba doc. MUDr. Pavel Horák, CSc., MUDr. Martina Skácelová, MUDr. Andrea Smržová, doc. MUDr. Josef Zadražil,
Přehledové články 177 Systémový lupus erythematodes prototyp autoimunitní choroby, diagnostika a léčba doc. MUDr. Pavel Horák, CSc., MUDr. Martina Skácelová, MUDr. Andrea Smržová, doc. MUDr. Josef Zadražil,
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Topotecan Eagle 3 mg/1 ml koncentrát pro přípravu infuzního roztoku 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 ml koncentrátu pro přípravu infuzního
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Topotecan Eagle 3 mg/1 ml koncentrát pro přípravu infuzního roztoku 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 ml koncentrátu pro přípravu infuzního
