pracovní list studenta Komplexní sloučeniny Stanovení koncentrace železnaté soli Aleš Mareček
|
|
|
- Marian Ovčačík
- před 8 lety
- Počet zobrazení:
Transkript
1 Výstup RVP: Klíčová slova: Komplexní sloučeniny Aleš Mareček žák se seznámí s moderní měřicí technikou a propojí poznatky z oblasti fyziky s metodami chemické analýzy, dále si rozšíří vědomosti z oblasti komplexních sloučenin; při přesné práci s byretou se rovněž rozvíjí jeho psychomotorické schopnosti absorbance, kalibrační křivka Sexta Laboratorní práce Doba na přípravu: 15 min Doba na provedení: 90 min Obtížnost: střední Úkol Pomůcky Na základě fotometrického stanovení určete koncentraci železnaté soli a výsledek ověřte manganometrickou tirací. 1. Na základě měření absorbance připravených roztoků vytvořte kalibrační křivku pro stanovení obsahu železnatých iontů. 2. Za využití kalibrační křivky stanovte koncentraci železnatých iontů ve vzorku. 3. Koncentraci vzorku ověřte i manganometricky. Chemikálie: heptahydrát síranu železnatého, manganistan draselný, kyselina sírová Sklo: 2 odměrné baňky 100 cm 3, 4 odměrné baňky 25 cm 3, byreta, pipeta o objemu 10 cm 3, titrační baňka Přístroje: spektrometr SpectroVis Plus, počítač s programem Logger Pro Teoretický úvod Princip fotometrie Některé látky částečně pohlcují záření, které jimi prochází. Množství dopadajícího záření charakterizuje veličina označovaná jako intenzita. Intenzitu záření dopadajícího na vzorek označíme jako I 0 a intenzitu záření, které vzorkem prošlo, jako I. Poměr intenzit prošlého a dopadajícího záření označíme jako propustnost neboli transmitanci T. I T = I 0 Transmitance se v některých případech uvádí v procentech. Pro toto vyjádření je třeba hodnotu T získanou jako podíl intenzit dopadajícího a prošlého záření vynásobit stem. Záporně vzatý dekadický logaritmus propustnosti (transmitance) se označuje jako absorbance A. A = logt Obě veličiny jsou funkcí vlnové délky a jsou bezrozměrné. Transmitance nabývá hodnot od 0 (naprosto nepropustný vzorek) do 1 (zcela propustný vzorek). Absorbance nabývá hodnot od 0 (vzorek neabsorbuje) do (absorbuje všechny vlnové délky). Graf závislosti absorbance a transmitance na vlnové délce se nazývá spektrum. Na osu x je vynesena vlnová délka dopadajícího záření a na osu y hodnota transmitance nebo absorbance. Měření kalibrační křivky 1. Podle návodu (viz níže) připravte koncentrace pro měření kalibrační křivky. 2. měřte spektrum jednoho vzorku. Po ukončení sběru dat stiskněte tlačítko Konfigurovat spektrometr. 3. Zobrazí se spektrum měřené látky. V nabídce na levé straně okna zatrhněte Abs vs Koncentrace. 129
2 Fotometr vypíše několik vlnových délek, při nichž je absorpce nejvýraznější. Označena je vlnová délka s maximální absorbancí, při které bude fotometr měřit automaticky. Zatržením jiného políčka na levé straně nabídky vlnových délek však můžete zvolit i jinou vlnovou délku. Pozn.: Je dobré si před laboratorní prací proměřit spektra několika různě koncentrovaných roztoků zkoumané látky a nechat si přístrojem nabídnout vlnovou délku měření. Často se mohou automaticky nabízené vlnové délky pro různé koncentrace lišit. V tomto případě proměřte vzorky pro kalibrační křivku na všech navržených vlnových délkách. Pro další měření použijte vlnovou délku, na které kalibrační křivka nejlépe spojuje naměřené hodnoty absorbance. V některých případech bude nejlépe vyhovovat vlnová délka, kterou jste naměřili při vysoké koncentraci roztoku. Po volbě vhodné vlnové délky stiskněte tlačítko OK. 4. Následuje dotaz na uložení dat před započetím režimu sběru dat. Zvolte Ne. 5. Kliknutím na Sběr dat zahajte měření. 130
3 6. Jakmile přístroj změří absorbanci v první kyvetě, stiskněte tlačítko Zachovat a do okna, které se objeví, zapište hodnotu koncentrace měřeného roztoku. Po stisknutí OK můžete vložit další vzorek a 6. krok opakovat. 7. Po proměření posledního vzorku stiskněte tlačítko Zastavit. Získanými body proložte přímku (tlačítko Proložit přímku) a kalibrační křivka je hotova. Stanovení koncentrace neznámých vzorků 1. Po vložení kyvety se zkoumaným vzorkem stiskněte opět tlačítko Sběr dat. Objeví se nabídka, z níž zvolíte Přidat na konec. 2. Poté, co se v grafu objeví bod, který přísluší měřenému vzorku, zadejte v menu Analýza povel Interpolace (pozor! spodním tlačítkem jsou tam dvě). Program zobrazí okno s údajem o koncentraci. 3. Po stisknutí tlačítka OK panel zmizí a až po zastavení měření se v grafu objeví zjištěný údaj o koncentraci. 131
4 Vypracování 4. Pro měření koncentračních závislostí, u kterých očekáváte kvantitativní výsledek (stanovení koncentrace), je třeba volit koncentrační rozpětí, pro které nebude (alespoň ne o velkou hodnotu) absorbance přesahovat hodnotu 1. Železnaté ionty se v roztoku vyskytují ve formě kationů hexaaquaželeznatých [Fe(H 2 O) 6 ] 2+ a absorbují záření z oblasti viditelného světla. Této skutečnosti využijete při stanovení jejich koncentrace. Pro měření kalibrační křivky připravte 100 cm 3 0,1 M roztoku železnatých iontů. Použijte heptahydrát síranu železnatého. Navažte 2,779 g této látky a kvantitativně spláchněte do odměrné baňky o objemu 100 cm 3. Roztok okyselte kyselinou sírovou a doplňte po rysku vodou. Připravený roztok nalijte do byrety a do čtyř baněk o objemu 25 cm 3 odměřte postupně 20; 15; 10 a 5 cm 3 roztoku. Před měřením kalibrační křivky pořiďte spektra všech připravených roztoků a zjistěte, jaké vlnové délky vám pro měření kalibrační křivky v jednotlivých případech spektrometr navrhuje (nezapomeňte proměřit i neředěný roztok). Pokud se vlnové délky, které spektrometr nabídne pro různé koncentrace, budou lišit, využijte nejprve tu, která bude přístrojem navržena pro koncentrace připravené pro kalibrační křivku. V případě, že bude naměřená křivka vykazovat velké chyby, změřte kalibrační křivku při dalších fotometrem navržených vlnových délkách. Po naměření kalibrační křivky připravte ze zbývajícího zásobního roztoku vzorky pro kontrolu kalibrační křivky. Připravujte vždy koncentrace, které se nacházejí mezi body kalibrační křivky. Zapište si údaj o objemu použitého zásobního roztoku a koncentraci vypočtenou pro ředění. Tu porovnejte s koncentrací, kterou přístroj odečte z kalibrační křivky. Ze získaných hodnot (teoretické a prakticky naměřené) vypočítejte procentickou odchylku teorie a praxe. Nyní proměřte vzorek připravený učitelem. Koncentraci vzorku zadaného učitelem zjistěte i manganometrickou titrací. Pro stanovení pipetujte vždy 10 cm 3 vzorku. Ke stanovovanému roztoku do titrační baňky přidejte 5 cm 3 20% roztoku kyseliny sírové a titrujte 0,02 M roztokem manganistanu draselného do trvale fialového zbarvení. Reakce probíhá podle rovnice: 10 FeSO KMnO H 2 SO 4 5 Fe 2 (SO 4 ) MnSO 4 + K 2 SO H 2 O 1 cm 3 0,02 M KMnO 4 odpovídá 27, g Uvedený údaj ověřte výpočtem, který uvedete do protokolu. Výsledky obou stanovení porovnejte. 132
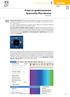
5 informace pro učitele Komplexní sloučeniny Aleš Mareček Sexta Laboratorní úkol je z oblasti analytické chemie. Žáci v průběhu práce porovnají fotometrické stanovení koncentrace železnatých iontů se stanovením manganometrickým. Pro zvládnutí celé úlohy v čase dvou vyučovacích hodin je třeba, aby žáci pracovali ve dvojicích a dobře si práci zorganizovali. Je nutné, aby žáci měli návod pro tuto laboratorní práci již před jejím vypracováním a mohli si vypracování promyslet, případně konzultovat nejasnosti. Před vlastním provedením je třeba žáky upozornit, že je ve vymezeném čase proveditelná, ale velmi záleží na tom, jak si dvojice rozdělí práci. Před vypracováním této úlohy je vhodné zařadit úlohy Barevnost chemických látek a Stanovení koncentrace kationu přechodného prvku, které ji logicky předcházejí. Pro přípravu vzorků, které budou žáci stanovovat, je vhodné použít 1 M roztok heptahydrátu síranu železnatého. Jako vzorek pro žáky odměřit z byrety do odměrných baněk o objemu 100 cm 3 3 až 7 cm 3 roztoku. Žáci provedou naředění a vzorek stanoví fotometricky i titračně. Roztok 0,02 M manganistanu draselného je dobré žákům poskytnout. Chyba fotometrického stanovení se pohybuje od 1 do 5 %. Kalibrační křivka železnaté soli Absorbance at 907,1 nm 0,10 0,05 Proložení přímky pro: Poslední měření I Absorbance at 907,1 nm Abs-907,1 = mx+b m (směrnice): 1,694 b (průsečík s Y): 0, Correlation: 0,9992 RMSE: 0,0028 0,00 0,0 0,2 0,4 0,6 0,8 (0,010931, 0,13409) Koncentrace (mol/l) 133
pracovní list studenta Komplexní sloučeniny Stanovení koncentrace kationtů přechodných kovů
 Výstup RVP: Klíčová slova: pracovní list studenta Komplexní sloučeniny Stanovení koncentrace kationtů přechodných kovů Aleš Mareček žák se seznámí s moderními metodami kvantitativní analýzy (práce propojuje
Výstup RVP: Klíčová slova: pracovní list studenta Komplexní sloučeniny Stanovení koncentrace kationtů přechodných kovů Aleš Mareček žák se seznámí s moderními metodami kvantitativní analýzy (práce propojuje
Práce se spektrometrem SpectroVis Plus Vernier
 informace pro učitele Práce se spektrometrem SpectroVis Plus Vernier Aleš Mareček Kvinta úloha Měřené veličiny Přístroj SpectroVis Plus umožní studovat viditelnou část spektra a část blízké infračervené
informace pro učitele Práce se spektrometrem SpectroVis Plus Vernier Aleš Mareček Kvinta úloha Měřené veličiny Přístroj SpectroVis Plus umožní studovat viditelnou část spektra a část blízké infračervené
pracovní list studenta Analytická chemie Barevnost chemických látek Aleš Mareček
 Výstup RVP: Klíčová slova: Analytická chemie Aleš Mareček žák se na základě vlastního pozorování seznámí s příčinami barevnosti chemických sloučenin; v průběhu práce získá základní informace o moderních
Výstup RVP: Klíčová slova: Analytická chemie Aleš Mareček žák se na základě vlastního pozorování seznámí s příčinami barevnosti chemických sloučenin; v průběhu práce získá základní informace o moderních
Ústřední komise Chemické olympiády. 55. ročník 2018/2019 NÁRODNÍ KOLO. Kategorie E. Zadání praktické části Úloha 2 (30 bodů)
 Ústřední komise Chemické olympiády 55. ročník 2018/2019 NÁRODNÍ KOLO Kategorie E Zadání praktické části Úloha 2 (30 bodů) PRAKTICKÁ ČÁST 30 BODŮ Úloha 2 Stanovení Cu 2+ spektrofotometricky 30 bodů Cu 2+
Ústřední komise Chemické olympiády 55. ročník 2018/2019 NÁRODNÍ KOLO Kategorie E Zadání praktické části Úloha 2 (30 bodů) PRAKTICKÁ ČÁST 30 BODŮ Úloha 2 Stanovení Cu 2+ spektrofotometricky 30 bodů Cu 2+
Název: Redoxní titrace - manganometrie
 Název: Redoxní titrace - manganometrie Autor: RNDr. Markéta Bludská Název školy: Gymnázium Jana Nerudy, škola hl. města Prahy Předmět, mezipředmětové vztahy: chemie a její aplikace, matematika Ročník:
Název: Redoxní titrace - manganometrie Autor: RNDr. Markéta Bludská Název školy: Gymnázium Jana Nerudy, škola hl. města Prahy Předmět, mezipředmětové vztahy: chemie a její aplikace, matematika Ročník:
fenanthrolinem Příprava
 1 ÚLOHA 9: Spektrofotometrické fenanthrolinem studium komplexu Fe(II) s 1,10- Příprava 2. 3. 4. 5. 6. Zopakujte si základní pojmy z optiky - elektromagnetické záření a jeho šíření absorbujícím prostředím,
1 ÚLOHA 9: Spektrofotometrické fenanthrolinem studium komplexu Fe(II) s 1,10- Příprava 2. 3. 4. 5. 6. Zopakujte si základní pojmy z optiky - elektromagnetické záření a jeho šíření absorbujícím prostředím,
Automatická potenciometrická titrace Klinická a toxikologická analýza Chemie životního prostředí Geologické obory
 Automatická potenciometrická titrace Klinická a toxikologická analýza Chemie životního prostředí Geologické obory Titrace je spolehlivý a celkem nenáročný postup, jak zjistit koncentraci analytu, její
Automatická potenciometrická titrace Klinická a toxikologická analýza Chemie životního prostředí Geologické obory Titrace je spolehlivý a celkem nenáročný postup, jak zjistit koncentraci analytu, její
Oborový workshop pro SŠ CHEMIE
 PRAKTICKÁ VÝUKA PŘÍRODOVĚDNÝCH PŘEDMĚTŮ NA ZŠ A SŠ CZ.1.07/1.1.30/02.0024 Tento projekt je spolufinancován Evropským sociálním fondem a státním rozpočtem České republiky. Oborový workshop pro SŠ CHEMIE
PRAKTICKÁ VÝUKA PŘÍRODOVĚDNÝCH PŘEDMĚTŮ NA ZŠ A SŠ CZ.1.07/1.1.30/02.0024 Tento projekt je spolufinancován Evropským sociálním fondem a státním rozpočtem České republiky. Oborový workshop pro SŠ CHEMIE
Měření koncentrace roztoku absorpčním spektrofotometrem
 Měření koncentrace roztoku absorpčním spektrofotometrem Teoretický úvod Absorpční spektrofotometrie je metoda stanovení koncentrace disperzního podílu analytické disperze, založená na měření absorpce světla.
Měření koncentrace roztoku absorpčním spektrofotometrem Teoretický úvod Absorpční spektrofotometrie je metoda stanovení koncentrace disperzního podílu analytické disperze, založená na měření absorpce světla.
Voda a život Wasser und Leben
 Počítání fólií měřením úbytku světla Cíl: Cílem této úlohy je připravit u žáků půdu pro pochopení důležité fyzikálně-chemické metody: stanovení koncentrace měřením absorbance s využitím Lambertova-Beerova
Počítání fólií měřením úbytku světla Cíl: Cílem této úlohy je připravit u žáků půdu pro pochopení důležité fyzikálně-chemické metody: stanovení koncentrace měřením absorbance s využitím Lambertova-Beerova
Luxmetr LS-BTA, lampička, izolepa, 32 kusů průhledné fólie (nejlépe obaly od CD).
 Počítání fólií měřením úbytku světla Cíl: Cílem této úlohy je připravit u žáků půdu pro pochopení důležité fyzikálně-chemické metody: stanovení koncentrace měřením absorbance s využitím Lambertova-Beerova
Počítání fólií měřením úbytku světla Cíl: Cílem této úlohy je připravit u žáků půdu pro pochopení důležité fyzikálně-chemické metody: stanovení koncentrace měřením absorbance s využitím Lambertova-Beerova
Optimalizace podmínek měření a práce s AAS
 S (KT & Geochemie) Optimalizace podmínek měření a práce s S Teoretický základ úlohy: 1: OPTIMLIZCE PRCOVNÍCH PODMÍNEK Jedním z prvních úkolů při práci s atomovým absorpčním spektrometrem (S) je vždy nalezení
S (KT & Geochemie) Optimalizace podmínek měření a práce s S Teoretický základ úlohy: 1: OPTIMLIZCE PRCOVNÍCH PODMÍNEK Jedním z prvních úkolů při práci s atomovým absorpčním spektrometrem (S) je vždy nalezení
1. Příloha 1 Návod úlohy pro Pokročilé praktikum z biochemie I
 1. Příloha 1 Návod úlohy pro Pokročilé praktikum z biochemie I Vazba bromfenolové modři na sérový albumin Princip úlohy Albumin má unikátní vlastnost vázat menší molekuly mnoha typů. Díky struktuře, tvořené
1. Příloha 1 Návod úlohy pro Pokročilé praktikum z biochemie I Vazba bromfenolové modři na sérový albumin Princip úlohy Albumin má unikátní vlastnost vázat menší molekuly mnoha typů. Díky struktuře, tvořené
SPEKTROSKOPICKÉ VLASTNOSTI LÁTEK (ZÁKLADY SPEKTROSKOPIE)
 SPEKTROSKOPICKÉ VLASTNOSTI LÁTEK (ZÁKLADY SPEKTROSKOPIE) Elektromagnetické vlnění SVĚTLO Charakterizace záření Vlnová délka - (λ) : jednotky: m (obvykle nm) λ Souvisí s povahou fotonu Charakterizace záření
SPEKTROSKOPICKÉ VLASTNOSTI LÁTEK (ZÁKLADY SPEKTROSKOPIE) Elektromagnetické vlnění SVĚTLO Charakterizace záření Vlnová délka - (λ) : jednotky: m (obvykle nm) λ Souvisí s povahou fotonu Charakterizace záření
ULTRAFIALOVÁ A VIDITELNÁ SPEKTROMETRIE
 Pracovní úkol 1. Vytvořte kalibrační řadu roztoků pro stanovení orthofosforečnanů (viz část 1), stanovte vhodnou vlnovou délku pro kalibraci a proveďte kalibraci přístroje pro toto stanovení. 2. Na základě
Pracovní úkol 1. Vytvořte kalibrační řadu roztoků pro stanovení orthofosforečnanů (viz část 1), stanovte vhodnou vlnovou délku pro kalibraci a proveďte kalibraci přístroje pro toto stanovení. 2. Na základě
Spektrofotometrické stanovení fosforečnanů ve vodách
 Spektrofotometrické stanovení fosforečnanů ve vodách Úkol: Spektrofotometricky stanovte obsah fosforečnanů ve vodě Chemikálie: 0,07165 g dihydrogenfosforečnan draselný KH 2 PO 4 75 ml kyselina sírová H
Spektrofotometrické stanovení fosforečnanů ve vodách Úkol: Spektrofotometricky stanovte obsah fosforečnanů ve vodě Chemikálie: 0,07165 g dihydrogenfosforečnan draselný KH 2 PO 4 75 ml kyselina sírová H
Určení koncentrace proteinu fluorescenční metodou v mikrotitračních destičkách
 Určení koncentrace proteinu fluorescenční metodou v mikrotitračních destičkách Teorie Stanovení celkových proteinů Celkové množství proteinů lze stanovit pomocí několika metod; například: Hartree-Lowryho
Určení koncentrace proteinu fluorescenční metodou v mikrotitračních destičkách Teorie Stanovení celkových proteinů Celkové množství proteinů lze stanovit pomocí několika metod; například: Hartree-Lowryho
NEUTRALIZAČNÍ ODMĚRNÁ ANALÝZA (TITRACE)
 NEUTRALIZAČNÍ ODMĚRNÁ ANALÝZA (TITRACE) Cíle a princip: Stanovit TITR (přesnou koncentraci) odměrného roztoku kyseliny nebo zásady pomocí známé přesné koncentrace již stanoveného odměrného roztoku. Podstatou
NEUTRALIZAČNÍ ODMĚRNÁ ANALÝZA (TITRACE) Cíle a princip: Stanovit TITR (přesnou koncentraci) odměrného roztoku kyseliny nebo zásady pomocí známé přesné koncentrace již stanoveného odměrného roztoku. Podstatou
Adsorpce barviva na aktivním uhlí
 Adsorpce barviva na aktivním uhlí TEORIE ABSORBANCE Prochází-li světelný tok monochromatických paprsků o intenzitě I 0 určitým prostředím dojde k pohlcení jisté části záření a intenzita záření se sníží
Adsorpce barviva na aktivním uhlí TEORIE ABSORBANCE Prochází-li světelný tok monochromatických paprsků o intenzitě I 0 určitým prostředím dojde k pohlcení jisté části záření a intenzita záření se sníží
Základy fotometrie, využití v klinické biochemii
 Základy fotometrie, využití v klinické biochemii Základní vztahy ve fotometrii transmitance (propustnost): T = I / I 0 absorbance: A = log (I 0 / I) = log (1 / T) = log T Lambertův-Beerův zákon A l = e
Základy fotometrie, využití v klinické biochemii Základní vztahy ve fotometrii transmitance (propustnost): T = I / I 0 absorbance: A = log (I 0 / I) = log (1 / T) = log T Lambertův-Beerův zákon A l = e
Ústřední komise Chemické olympiády. 55. ročník 2018/2019 KRAJSKÉ KOLO. Kategorie E ZADÁNÍ PRAKTICKÉ ČÁSTI (50 BODŮ)
 Ústřední komise Chemické olympiády 55. ročník 2018/2019 KRAJSKÉ KOLO Kategorie E ZADÁNÍ PRAKTICKÉ ČÁSTI (50 BODŮ) Úloha 1 Stanovení Bi 3+ a Zn 2+ ve směsi 50 bodů Chelatometricky lze stanovit ionty samostatně,
Ústřední komise Chemické olympiády 55. ročník 2018/2019 KRAJSKÉ KOLO Kategorie E ZADÁNÍ PRAKTICKÉ ČÁSTI (50 BODŮ) Úloha 1 Stanovení Bi 3+ a Zn 2+ ve směsi 50 bodů Chelatometricky lze stanovit ionty samostatně,
pracovní list studenta
 Výstup RVP: Klíčová slova: pracovní list studenta Analytická geometrie lineárních útvarů Mirek Kubera žák řeší analyticky polohové a metrické úlohy o lineárních útvarech v rovině a prostoru souřadnice,
Výstup RVP: Klíčová slova: pracovní list studenta Analytická geometrie lineárních útvarů Mirek Kubera žák řeší analyticky polohové a metrické úlohy o lineárních útvarech v rovině a prostoru souřadnice,
Derivační spektrofotometrie a rozklad absorpčního spektra
 Derivační spektrofotometrie a rozklad absorpčního spektra Teorie: Derivační spektrofotometrie, využívající derivace absorpční křivky, je obecně používanou metodou pro zvýraznění detailů průběhu záznamu,
Derivační spektrofotometrie a rozklad absorpčního spektra Teorie: Derivační spektrofotometrie, využívající derivace absorpční křivky, je obecně používanou metodou pro zvýraznění detailů průběhu záznamu,
Ústřední komise Chemické olympiády. 55. ročník 2018/2019 ŠKOLNÍ KOLO. Kategorie B ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ)
 Ústřední komise Chemické olympiády 55. ročník 2018/2019 ŠKOLNÍ KOLO Kategorie B ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ) PRAKTICKÁ ČÁST 40 BODŮ Autor Bc. Lukáš Tomaník VŠCHT Praha RNDr. Petr Holzhauser, Ph.D.
Ústřední komise Chemické olympiády 55. ročník 2018/2019 ŠKOLNÍ KOLO Kategorie B ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ) PRAKTICKÁ ČÁST 40 BODŮ Autor Bc. Lukáš Tomaník VŠCHT Praha RNDr. Petr Holzhauser, Ph.D.
Stanovení celkové kyselosti nápojů potenciometrickou titrací
 Stanovení celkové kyselosti nápojů potenciometrickou titrací Princip metody U acidobazických titrací se využívají dva druhy indikace bodu ekvivalence - vizuální a instrumentální. K vizuální indikaci bodu
Stanovení celkové kyselosti nápojů potenciometrickou titrací Princip metody U acidobazických titrací se využívají dva druhy indikace bodu ekvivalence - vizuální a instrumentální. K vizuální indikaci bodu
chemie Stanovení isosbestického bodu bromkresolové zeleně (BKZ) Cíle Podrobnější rozbor cílů Zařazení do výuky Časová náročnost Návaznost experimentů
 Stanovení isosbestického bodu bromkresolové zeleně (BKZ) pracovní návod s metodickým komentářem pro učitele připravil M. Škavrada chemie 20 úloha číslo Cíle Cílem této laboratorní úlohy je stanovení isosbestického
Stanovení isosbestického bodu bromkresolové zeleně (BKZ) pracovní návod s metodickým komentářem pro učitele připravil M. Škavrada chemie 20 úloha číslo Cíle Cílem této laboratorní úlohy je stanovení isosbestického
Ústřední komise Chemické olympiády. 55. ročník 2018/2019 KRAJSKÉ KOLO. Kategorie A ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ) Časová náročnost 120 minut
 Ústřední komise Chemické olympiády 55. ročník 2018/2019 KRAJSKÉ KOLO Kategorie A ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ) Časová náročnost 120 minut Úloha 1 Příprava Mohrovy soli 15 bodů Mezi podvojné soli patří
Ústřední komise Chemické olympiády 55. ročník 2018/2019 KRAJSKÉ KOLO Kategorie A ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ) Časová náročnost 120 minut Úloha 1 Příprava Mohrovy soli 15 bodů Mezi podvojné soli patří
Název: Standardizace roztoku manganistanu
 Název: Standardizace roztoku manganistanu Autor: RNDr. Markéta Bludská Název školy: Gymnázium Jana Nerudy, škola hl. města Prahy Předmět, mezipředmětové vztahy: chemie a její aplikace, matematika Ročník:
Název: Standardizace roztoku manganistanu Autor: RNDr. Markéta Bludská Název školy: Gymnázium Jana Nerudy, škola hl. města Prahy Předmět, mezipředmětové vztahy: chemie a její aplikace, matematika Ročník:
Ústřední komise Chemické olympiády. 50. ročník 2013/2014. OKRESNÍ KOLO kategorie D ŘEŠENÍ SOUTĚŽNÍCH ÚLOH
 Ústřední komise Chemické olympiády 50. ročník 2013/2014 OKRESNÍ KOLO kategorie D ŘEŠENÍ SOUTĚŽNÍCH ÚLOH TEORETICKÁ ČÁST (70 BODŮ) Informace pro hodnotitele Ve výpočtových úlohách jsou uvedeny dílčí výpočty
Ústřední komise Chemické olympiády 50. ročník 2013/2014 OKRESNÍ KOLO kategorie D ŘEŠENÍ SOUTĚŽNÍCH ÚLOH TEORETICKÁ ČÁST (70 BODŮ) Informace pro hodnotitele Ve výpočtových úlohách jsou uvedeny dílčí výpočty
pracovní list studenta
 Výstup RVP: Klíčová slova: pracovní list studenta Funkce kvadratická funkce Mirek Kubera žák načrtne grafy požadovaných funkcí, formuluje a zdůvodňuje vlastnosti studovaných funkcí, modeluje závislosti
Výstup RVP: Klíčová slova: pracovní list studenta Funkce kvadratická funkce Mirek Kubera žák načrtne grafy požadovaných funkcí, formuluje a zdůvodňuje vlastnosti studovaných funkcí, modeluje závislosti
SPEKTROFOTOMETRICKÉ STABOVENÍ SO 4 VE VODÁCH
 Pracovní úkol 1. Vytvořte 2 kalibrační řady pro stanovení šestimocného SO 4 a to v rozsahu koncentrací 5-40 mg/l (po 5 mg/l). 2. Na základě absorpční křivky SO 4 určete vhodnou vlnovou délku (λ) s maximální
Pracovní úkol 1. Vytvořte 2 kalibrační řady pro stanovení šestimocného SO 4 a to v rozsahu koncentrací 5-40 mg/l (po 5 mg/l). 2. Na základě absorpční křivky SO 4 určete vhodnou vlnovou délku (λ) s maximální
Ústřední komise Chemické olympiády. 55. ročník 2018/2019 NÁRODNÍ KOLO. Kategorie E. Zadání praktické části Úloha 1 (20 bodů)
 Ústřední komise Chemické olympiády 55. ročník 2018/2019 NÁRODNÍ KOLO Kategorie E Zadání praktické části Úloha 1 (20 bodů) PRAKTICKÁ ČÁST 20 BODŮ Úloha 1 Stanovení Ni 2+ a Ca 2+ ve směsi konduktometricky
Ústřední komise Chemické olympiády 55. ročník 2018/2019 NÁRODNÍ KOLO Kategorie E Zadání praktické části Úloha 1 (20 bodů) PRAKTICKÁ ČÁST 20 BODŮ Úloha 1 Stanovení Ni 2+ a Ca 2+ ve směsi konduktometricky
Ústřední komise Chemické olympiády. 55. ročník 2018/2019 ŠKOLNÍ KOLO. Kategorie B ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ)
 Ústřední komise Chemické olympiády 55. ročník 2018/2019 ŠKOLNÍ KOLO Kategorie B ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ) PRAKTICKÁ ČÁST 40 BODŮ Autor Bc. Lukáš Tomaník VŠCHT Praha RNDr. Petr Holzhauser, Ph.D.
Ústřední komise Chemické olympiády 55. ročník 2018/2019 ŠKOLNÍ KOLO Kategorie B ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ) PRAKTICKÁ ČÁST 40 BODŮ Autor Bc. Lukáš Tomaník VŠCHT Praha RNDr. Petr Holzhauser, Ph.D.
Úvod. Náplň práce. Úkoly
 Název práce: Zkouška disoluce pevných lékových forem Vedoucí práce: Doc. Ing. Petr Zámostný, Ph.D. Jméno zástupce: Ing. Jan Patera Umístění práce: S25b Úvod Uvolňování léčiva z tuhých perorálních lékových
Název práce: Zkouška disoluce pevných lékových forem Vedoucí práce: Doc. Ing. Petr Zámostný, Ph.D. Jméno zástupce: Ing. Jan Patera Umístění práce: S25b Úvod Uvolňování léčiva z tuhých perorálních lékových
Spektroskopie v UV-VIS oblasti. UV-VIS spektroskopie. Roztok KMnO 4. pracuje nejčastěji v oblasti 200-800 nm
 Spektroskopie v UV-VIS oblasti UV-VIS spektroskopie pracuje nejčastěji v oblasti 2-8 nm lze měřit i < 2 nm či > 8 nm UV VIS IR Ultra Violet VISible Infra Red Roztok KMnO 4 roztok KMnO 4 je červenofialový
Spektroskopie v UV-VIS oblasti UV-VIS spektroskopie pracuje nejčastěji v oblasti 2-8 nm lze měřit i < 2 nm či > 8 nm UV VIS IR Ultra Violet VISible Infra Red Roztok KMnO 4 roztok KMnO 4 je červenofialový
Pufry, pufrační kapacita. Oxidoredukce, elektrodové děje.
 ÚSTAV LÉKAŘSKÉ BIOCHEMIE A LABORATORNÍ DIAGNOSTIKY 1. LF UK Pufry, pufrační kapacita. Oxidoredukce, elektrodové děje. Praktické cvičení z lékařské biochemie Všeobecné lékařství Martin Vejražka, Tomáš Navrátil
ÚSTAV LÉKAŘSKÉ BIOCHEMIE A LABORATORNÍ DIAGNOSTIKY 1. LF UK Pufry, pufrační kapacita. Oxidoredukce, elektrodové děje. Praktické cvičení z lékařské biochemie Všeobecné lékařství Martin Vejražka, Tomáš Navrátil
CHEMIE Pracovní list č.3 žákovská verze Téma: Acidobazická titrace Mgr. Lenka Horutová Student a konkurenceschopnost
 www.projektsako.cz CHEMIE Pracovní list č.3 žákovská verze Téma: Acidobazická titrace Lektor: Projekt: Reg. číslo: Mgr. Lenka Horutová Student a konkurenceschopnost CZ.1.07/1.1.07/03.0075 Teorie: Základem
www.projektsako.cz CHEMIE Pracovní list č.3 žákovská verze Téma: Acidobazická titrace Lektor: Projekt: Reg. číslo: Mgr. Lenka Horutová Student a konkurenceschopnost CZ.1.07/1.1.07/03.0075 Teorie: Základem
chemie Stanovení částečné přechodné tvrdosti vody Cíle Podrobnější rozbor cílů Zařazení do výuky Časová náročnost Zadání úlohy Návaznost experimentů
 Stanovení částečné přechodné tvrdosti vody pracovní návod s metodickým komentářem pro učitele připravil M. Škavrada chemie 13 úloha číslo Cíle Cílem tohoto laboratorního cvičení je stanovení částečné přechodné
Stanovení částečné přechodné tvrdosti vody pracovní návod s metodickým komentářem pro učitele připravil M. Škavrada chemie 13 úloha číslo Cíle Cílem tohoto laboratorního cvičení je stanovení částečné přechodné
Pracovní návod 1/7 www.expoz.cz
 Pracovní návod 1/7 www.expoz.cz Chemie úloha č. 14 Kolik železa spolykáme Autor: Tomáš Feltl Cíle Seznámení se s teoretickým a praktickým základem spektrofotometrických metod na příkladu stanovení koncentrace
Pracovní návod 1/7 www.expoz.cz Chemie úloha č. 14 Kolik železa spolykáme Autor: Tomáš Feltl Cíle Seznámení se s teoretickým a praktickým základem spektrofotometrických metod na příkladu stanovení koncentrace
CHSK. Pro hodnocení kvality vod obvykle postačí základní sumární ukazatele. Pro organické látky se jedná zejména o ukazatele:
 CHSK Ve vodách mohou být obsažené různé organické látky v širokém rozmezí koncentrací od stopových množství až po majoritní složky podle druhu vod. Vzhledem k této různorodosti se organické látky ve vodách
CHSK Ve vodách mohou být obsažené různé organické látky v širokém rozmezí koncentrací od stopových množství až po majoritní složky podle druhu vod. Vzhledem k této různorodosti se organické látky ve vodách
Pracovní list - Laboratorní práce č. 7 Jméno: Třída: Skupina:
 Projekt Efektivní Učení Reformou oblastí gymnaziálního vzdělávání je spolufinancován Evropským sociálním fondem a státním rozpočtem České republiky. Pracovní list - Laboratorní práce č. 7 Jméno: Třída:
Projekt Efektivní Učení Reformou oblastí gymnaziálního vzdělávání je spolufinancován Evropským sociálním fondem a státním rozpočtem České republiky. Pracovní list - Laboratorní práce č. 7 Jméno: Třída:
Sešit pro laboratorní práci z chemie
 Sešit pro laboratorní práci z chemie téma: Standardizace. Alkalimetrie. autor: ing. Alena Dvořáková vytvořeno při realizaci projektu: Inovace školního vzdělávacího programu biologie a chemie registrační
Sešit pro laboratorní práci z chemie téma: Standardizace. Alkalimetrie. autor: ing. Alena Dvořáková vytvořeno při realizaci projektu: Inovace školního vzdělávacího programu biologie a chemie registrační
pracovní list studenta
 Výstup RVP: Klíčová slova: pracovní list studenta Funkce Petra Směšná žák chápe funkci jako vyjádření závislosti veličin, umí vyjádřit funkční vztah tabulkou, rovnicí i grafem, dovede vyjádřit reálné situace
Výstup RVP: Klíčová slova: pracovní list studenta Funkce Petra Směšná žák chápe funkci jako vyjádření závislosti veličin, umí vyjádřit funkční vztah tabulkou, rovnicí i grafem, dovede vyjádřit reálné situace
PRÁCE S ROZTOKY A JEJICH KONCENTRACE
 LABORATORNÍ PRÁCE Č. 3 PRÁCE S ROZTOKY A JEJICH KONCENTRACE PRINCIP Roztoky jsou hoogenní soustavy sestávající se ze dvou nebo více složek. V cheii se kapalné roztoky skládají z rozpouštědla (nejčastěji
LABORATORNÍ PRÁCE Č. 3 PRÁCE S ROZTOKY A JEJICH KONCENTRACE PRINCIP Roztoky jsou hoogenní soustavy sestávající se ze dvou nebo více složek. V cheii se kapalné roztoky skládají z rozpouštědla (nejčastěji
STŘEDNÍ ODBORNÁ ŠKOLA a STŘEDNÍ ODBORNÉ UČILIŠTĚ, Česká Lípa, 28. října 2707, příspěvková organizace
 Název školy: Číslo a název projektu: Číslo a název šablony klíčové aktivity: Označení materiálu: Typ materiálu: STŘEDNÍ ODBORNÁ ŠKOLA a STŘEDNÍ ODBORNÉ UČILIŠTĚ, Česká Lípa, 28. října 2707, příspěvková
Název školy: Číslo a název projektu: Číslo a název šablony klíčové aktivity: Označení materiálu: Typ materiálu: STŘEDNÍ ODBORNÁ ŠKOLA a STŘEDNÍ ODBORNÉ UČILIŠTĚ, Česká Lípa, 28. října 2707, příspěvková
Ústřední komise Chemické olympiády. 56. ročník 2019/2020 ŠKOLNÍ KOLO. Kategorie A. Praktická část Zadání 40 bodů
 Ústřední komise Chemické olympiády 56. ročník 2019/2020 ŠKOLNÍ KOLO Kategorie A Praktická část Zadání 40 bodů PRAKTICKÁ ČÁST 40 BODŮ Autor Doc. Ing. Petr Exnar, CSc. Technická univerzita v Liberci Recenze
Ústřední komise Chemické olympiády 56. ročník 2019/2020 ŠKOLNÍ KOLO Kategorie A Praktická část Zadání 40 bodů PRAKTICKÁ ČÁST 40 BODŮ Autor Doc. Ing. Petr Exnar, CSc. Technická univerzita v Liberci Recenze
Moravské gymnázium Brno s.r.o. RNDr. Miroslav Štefan. Chemie anorganická analytická chemie kvantitativní. Datum tvorby
 Číslo projektu CZ.1.07/1.5.00/34.0743 Název školy Autor Tematická oblast Ročník Moravské gymnázium Brno s.r.o. RNDr. Miroslav Štefan Chemie anorganická analytická chemie kvantitativní 2. ročník Datum tvorby
Číslo projektu CZ.1.07/1.5.00/34.0743 Název školy Autor Tematická oblast Ročník Moravské gymnázium Brno s.r.o. RNDr. Miroslav Štefan Chemie anorganická analytická chemie kvantitativní 2. ročník Datum tvorby
Úloha č. 9 Stanovení hydroxidu a uhličitanu vedle sebe dle Winklera
 Úloha č. 9 Stanovení hydroxidu a uhličitanu vedle sebe dle Winklera Princip Jde o klasickou metodu kvantitativní chemické analýzy. Uhličitan vedle hydroxidu se stanoví ve dvou alikvotních podílech zásobního
Úloha č. 9 Stanovení hydroxidu a uhličitanu vedle sebe dle Winklera Princip Jde o klasickou metodu kvantitativní chemické analýzy. Uhličitan vedle hydroxidu se stanoví ve dvou alikvotních podílech zásobního
REDOX TITRACE ANEB STANOVENÍ PEROXIDU VODÍKU
 REDOX TITRACE ANEB STANOVENÍ PEROXIDU VODÍKU Jak zkontrolovat, zda vás váš dodavatel nešidí? Karel Černý je majitelem lékárny. Kromě jiného prodává také peroxid vodíku jako desinfekci. Prodávaný roztok
REDOX TITRACE ANEB STANOVENÍ PEROXIDU VODÍKU Jak zkontrolovat, zda vás váš dodavatel nešidí? Karel Černý je majitelem lékárny. Kromě jiného prodává také peroxid vodíku jako desinfekci. Prodávaný roztok
Kurz 1 Úvod k biochemickému praktiku
 Kurz 1 Úvod k biochemickému praktiku Pavla Balínová http://vyuka.lf3.cuni.cz/ Důležité informace Kroužkový asistent: RNDr. Pavla Balínová e-mailová adresa: pavla.balinova@lf3.cuni.cz místnost: 410 studijní
Kurz 1 Úvod k biochemickému praktiku Pavla Balínová http://vyuka.lf3.cuni.cz/ Důležité informace Kroužkový asistent: RNDr. Pavla Balínová e-mailová adresa: pavla.balinova@lf3.cuni.cz místnost: 410 studijní
pracovní list studenta
 Výstup RVP: Klíčová slova: pracovní list studenta Goniometrické funkce Mirek Kubera žák načrtne grafy elementárních funkcí a určí jejich vlastnosti, při konstrukci grafů aplikuje znalosti o zobrazeních,
Výstup RVP: Klíčová slova: pracovní list studenta Goniometrické funkce Mirek Kubera žák načrtne grafy elementárních funkcí a určí jejich vlastnosti, při konstrukci grafů aplikuje znalosti o zobrazeních,
Laboratorní cvičení z lékařské chemie II
 Laboratorní cvičení z lékařské chemie II 1. ročník, všeobecné lékařství Ústav lékařské chemie a biochemie Lékařská fakulta v Plzni, Univerzita Karlova Jméno: Potvrzení o účasti na praktikách Studijní skupina:
Laboratorní cvičení z lékařské chemie II 1. ročník, všeobecné lékařství Ústav lékařské chemie a biochemie Lékařská fakulta v Plzni, Univerzita Karlova Jméno: Potvrzení o účasti na praktikách Studijní skupina:
Stanovení kritické micelární koncentrace
 Stanovení kritické micelární koncentrace TEORIE KONDUKTOMETRIE Měrná elektrická vodivost neboli konduktivita je fyzikální veličinou, která popisuje schopnost látek vést elektrický proud. Látky snadno vedoucí
Stanovení kritické micelární koncentrace TEORIE KONDUKTOMETRIE Měrná elektrická vodivost neboli konduktivita je fyzikální veličinou, která popisuje schopnost látek vést elektrický proud. Látky snadno vedoucí
JODOMETRICKÉ STANOVENÍ ROZPUŠTĚNÉHO KYSLÍKU
 JODOMETRICKÉ STANOVENÍ ROZPUŠTĚNÉHO KYSLÍKU (dle Winklera v Alsterbergově modifikaci) Cílem je stanovení rozpuštěného kyslíku v pitné vodě z vodovodního řádu. Protokol musí osahovat veškeré potřebné hodnoty
JODOMETRICKÉ STANOVENÍ ROZPUŠTĚNÉHO KYSLÍKU (dle Winklera v Alsterbergově modifikaci) Cílem je stanovení rozpuštěného kyslíku v pitné vodě z vodovodního řádu. Protokol musí osahovat veškeré potřebné hodnoty
FLUORIMETRICKÉ STANOVENÍ FLUORESCEINU
 FLUORIMETRICKÉ STANOVENÍ FLUORESCEINU návod vznikl jako součást bakalářské práce Martiny Vidrmanové Fluorimetrie s využitím spektrofotometru SpectroVis Plus firmy Vernier (http://is.muni.cz/th/268973/prif_b/bakalarska_prace.pdf)
FLUORIMETRICKÉ STANOVENÍ FLUORESCEINU návod vznikl jako součást bakalářské práce Martiny Vidrmanové Fluorimetrie s využitím spektrofotometru SpectroVis Plus firmy Vernier (http://is.muni.cz/th/268973/prif_b/bakalarska_prace.pdf)
Název: Pozorování a měření emisních spekter různých zdrojů
 Název: Pozorování a měření emisních spekter různých zdrojů Autor: Doc. RNDr. Milan Rojko, CSc. Název školy: Gymnázium Jana Nerudy, škola hl. města Prahy Předmět, mezipředmětové vztahy: fyzika, chemie Ročník:
Název: Pozorování a měření emisních spekter různých zdrojů Autor: Doc. RNDr. Milan Rojko, CSc. Název školy: Gymnázium Jana Nerudy, škola hl. města Prahy Předmět, mezipředmětové vztahy: fyzika, chemie Ročník:
Název: Vitamíny. Autor: Mgr. Jiří Vozka, Ph.D. Název školy: Gymnázium Jana Nerudy, škola hl. města Prahy
 Název: Vitamíny Autor: Mgr. Jiří Vozka, Ph.D. Název školy: Gymnázium Jana Nerudy, škola hl. města Prahy Předmět, mezipředmětové vztahy: chemie, biologie, matematika Ročník: 5. Tématický celek: Biochemie
Název: Vitamíny Autor: Mgr. Jiří Vozka, Ph.D. Název školy: Gymnázium Jana Nerudy, škola hl. města Prahy Předmět, mezipředmětové vztahy: chemie, biologie, matematika Ročník: 5. Tématický celek: Biochemie
ÚSTAV ORGANICKÉ TECHNOLOGIE
 LABORATOŘ OBORU I ÚSTAV ORGANICKÉ TECHNOLOGIE (111) F Imobilizace na alumosilikátové materiály Vedoucí práce: Ing. Eliška Leitmannová, Ph.D. Umístění práce: laboratoř F07, F08 1 Úvod Imobilizace aktivních
LABORATOŘ OBORU I ÚSTAV ORGANICKÉ TECHNOLOGIE (111) F Imobilizace na alumosilikátové materiály Vedoucí práce: Ing. Eliška Leitmannová, Ph.D. Umístění práce: laboratoř F07, F08 1 Úvod Imobilizace aktivních
Půdy vlastnosti II. (laboratorní práce)
 Zvyšování kvality výuky v přírodních a technických oblastech CZ.1.07/1.1.28/02.0055 Půdy vlastnosti II. (laboratorní práce) Označení: EU-Inovace-Př-9-39 Předmět: přírodopis Cílová skupina: 9. třída Autor:
Zvyšování kvality výuky v přírodních a technických oblastech CZ.1.07/1.1.28/02.0055 Půdy vlastnosti II. (laboratorní práce) Označení: EU-Inovace-Př-9-39 Předmět: přírodopis Cílová skupina: 9. třída Autor:
Molekulová spektroskopie 1. Chemická vazba, UV/VIS
 Molekulová spektroskopie 1 Chemická vazba, UV/VIS 1 Chemická vazba Silová interakce mezi dvěma atomy. Chemické vazby jsou soudržné síly působící mezi jednotlivými atomy nebo ionty v molekulách. Chemická
Molekulová spektroskopie 1 Chemická vazba, UV/VIS 1 Chemická vazba Silová interakce mezi dvěma atomy. Chemické vazby jsou soudržné síly působící mezi jednotlivými atomy nebo ionty v molekulách. Chemická
Úloha 3: Mřížkový spektrometr
 Petra Suková, 2.ročník, F-14 1 Úloha 3: Mřížkový spektrometr 1 Zadání 1. Seřiďte spektrometr pro kolmý dopad světla(rovina optické mřížky je kolmá k ose kolimátoru) pomocí bočního osvětlení nitkového kříže.
Petra Suková, 2.ročník, F-14 1 Úloha 3: Mřížkový spektrometr 1 Zadání 1. Seřiďte spektrometr pro kolmý dopad světla(rovina optické mřížky je kolmá k ose kolimátoru) pomocí bočního osvětlení nitkového kříže.
OBCHOD S KOVOVÝM ŠROTEM (ČÁST 2)
 OBCHOD S KOVOVÝM ŠROTEM (ČÁST 2) Měď je rozšířený kov používaný například do počítačů, jako elektrické kabely, okapy, instalatérské prvky a všemožný spojovací materiál. Po mědi je tedy velká poptávka a
OBCHOD S KOVOVÝM ŠROTEM (ČÁST 2) Měď je rozšířený kov používaný například do počítačů, jako elektrické kabely, okapy, instalatérské prvky a všemožný spojovací materiál. Po mědi je tedy velká poptávka a
Jednotné pracovní postupy zkoušení krmiv STANOVENÍ OBSAHU SELENU METODOU ICP-OES
 Strana 1 STANOVENÍ OBSAHU SELENU METODOU ICP-OES 1 Rozsah a účel Postup specifikuje podmínky pro stanovení celkového obsahu selenu v minerálních krmivech a premixech metodou optické emisní spektrometrie
Strana 1 STANOVENÍ OBSAHU SELENU METODOU ICP-OES 1 Rozsah a účel Postup specifikuje podmínky pro stanovení celkového obsahu selenu v minerálních krmivech a premixech metodou optické emisní spektrometrie
Ústřední komise Chemické olympiády. 55. ročník 2018/2019 ŠKOLNÍ KOLO. Kategorie C ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ)
 Ústřední komise Chemické olympiády 55. ročník 2018/2019 ŠKOLNÍ KOLO Kategorie C ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ) PRAKTICKÁ ČÁST 40 BODŮ Autor RNDr. Jan Břížďala Gymnázium Třebíč RNDr. Jan Havlík, Ph.D.
Ústřední komise Chemické olympiády 55. ročník 2018/2019 ŠKOLNÍ KOLO Kategorie C ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ) PRAKTICKÁ ČÁST 40 BODŮ Autor RNDr. Jan Břížďala Gymnázium Třebíč RNDr. Jan Havlík, Ph.D.
KARBOXYLOVÉ KYSELINY
 LABORATORNÍ PRÁCE Č. 28 KARBOXYLOVÉ KYSELINY PRINCIP Karboxylové kyseliny jsou látky, které ve své molekule obsahují jednu nebo více karboxylových skupin. Odvozují se od nich dva typy derivátů, substituční
LABORATORNÍ PRÁCE Č. 28 KARBOXYLOVÉ KYSELINY PRINCIP Karboxylové kyseliny jsou látky, které ve své molekule obsahují jednu nebo více karboxylových skupin. Odvozují se od nich dva typy derivátů, substituční
pracovní list studenta Kombinatorika, pravděpodobnost, základy statistiky Jak jsou vysocí? Mirek Kubera
 Výstup RVP: Klíčová slova: pracovní list studenta Kombinatorika, pravděpodobnost, základy statistiky Mirek Kubera žák diskutuje a kriticky zhodnotí statistické informace a daná statistická sdělení, volí
Výstup RVP: Klíčová slova: pracovní list studenta Kombinatorika, pravděpodobnost, základy statistiky Mirek Kubera žák diskutuje a kriticky zhodnotí statistické informace a daná statistická sdělení, volí
pracovní list studenta Elektrický proud v kovech Voltampérová charakteristika spotřebiče Eva Bochníčková
 pracovní list studenta Elektrický proud v kovech Eva Bochníčková Výstup RVP: Klíčová slova: žák měří vybrané veličiny vhodnými metodami, zpracuje získaná data formou grafu; porovná získanou závislost s
pracovní list studenta Elektrický proud v kovech Eva Bochníčková Výstup RVP: Klíčová slova: žák měří vybrané veličiny vhodnými metodami, zpracuje získaná data formou grafu; porovná získanou závislost s
INFRAČERVENÁ SPEKTROMETRIE A BIOSLOŽKY PALIV
 VYSOKÁ ŠKOLA CHEMICKO-TECHNOLOGICKÁ V PRAZE Fakulta technologie ochrany prostředí Ústav technologie ropy a alternativních paliv INFRAČERVENÁ SPEKTROMETRIE A BIOSLOŽKY PALIV Laboratorní cvičení ÚVOD V několika
VYSOKÁ ŠKOLA CHEMICKO-TECHNOLOGICKÁ V PRAZE Fakulta technologie ochrany prostředí Ústav technologie ropy a alternativních paliv INFRAČERVENÁ SPEKTROMETRIE A BIOSLOŽKY PALIV Laboratorní cvičení ÚVOD V několika
Vyjadřuje poměr hmotnosti rozpuštěné látky k hmotnosti celého roztoku.
 Koncentrace roztoků Hmotnostní zlomek w Vyjadřuje poměr hmotnosti rozpuštěné látky k hmotnosti celého roztoku. w= m A m s m s...hmotnost celého roztoku, m A... hmotnost rozpuštěné látky Hmotnost roztoku
Koncentrace roztoků Hmotnostní zlomek w Vyjadřuje poměr hmotnosti rozpuštěné látky k hmotnosti celého roztoku. w= m A m s m s...hmotnost celého roztoku, m A... hmotnost rozpuštěné látky Hmotnost roztoku
Měření odrazu a absorpce světla (experiment)
 Zvyšování kvality výuky v přírodních a technických oblastech CZ.1.07/1.1.28/02.0055 Označení: EU-Inovace-F-9-08 Předmět: Fyzika Cílová skupina: 9. třída Autor: Mgr. Monika Rambousková Časová dotace: 1
Zvyšování kvality výuky v přírodních a technických oblastech CZ.1.07/1.1.28/02.0055 Označení: EU-Inovace-F-9-08 Předmět: Fyzika Cílová skupina: 9. třída Autor: Mgr. Monika Rambousková Časová dotace: 1
pracovní list studenta
 ýstup RP: Klíčová slova: pracovní list studenta Funkce nepřímá úměrnost Mirek Kubera žák načrtne grafy požadovaných funkcí, formuluje a zdůvodňuje vlastnosti studovaných funkcí, modeluje závislosti reálných
ýstup RP: Klíčová slova: pracovní list studenta Funkce nepřímá úměrnost Mirek Kubera žák načrtne grafy požadovaných funkcí, formuluje a zdůvodňuje vlastnosti studovaných funkcí, modeluje závislosti reálných
UNIVERZITA PARDUBICE
 UNIVERZITA PARDUBICE Fakulta chemicko technologická Katedra analytické chemie Licenční studium chemometrie na téma Využití tabulkového procesoru jako laboratorního deníku Vedoucí licenčního studia Prof.
UNIVERZITA PARDUBICE Fakulta chemicko technologická Katedra analytické chemie Licenční studium chemometrie na téma Využití tabulkového procesoru jako laboratorního deníku Vedoucí licenčního studia Prof.
STANOVENÍ CHLORIDŮ. Odměrné argentometrické stanovení chloridů podle Mohra
 STANOVENÍ CHLORIDŮ Odměrné argentometrické stanovení chloridů podle Mohra Cíl práce Stanovte titr odměrného standardního roztoku dusičnanu stříbrného titrací 5 ml standardního srovnávacího roztoku chloridu
STANOVENÍ CHLORIDŮ Odměrné argentometrické stanovení chloridů podle Mohra Cíl práce Stanovte titr odměrného standardního roztoku dusičnanu stříbrného titrací 5 ml standardního srovnávacího roztoku chloridu
LABORATORNÍ STANOVENÍ SÍRANŮ VE VODNÉM ROZTOKU
 LABORATORNÍ STANOVENÍ SÍRANŮ VE VODNÉM ROZTOKU Cílem práce je stanovit koncentraci síranů v neznámém vzorku postupem A, B a C a porovnat jednotlivé metody mezi sebou. Protokol musí osahovat veškeré výpočty
LABORATORNÍ STANOVENÍ SÍRANŮ VE VODNÉM ROZTOKU Cílem práce je stanovit koncentraci síranů v neznámém vzorku postupem A, B a C a porovnat jednotlivé metody mezi sebou. Protokol musí osahovat veškeré výpočty
Název: Halogeny II - halogenidy
 Název: Halogeny II - halogenidy Autor: Mgr. Jiří Vozka, Ph.D. Název školy: Gymnázium Jana Nerudy, škola hl. města Prahy Předmět, mezipředmětové vztahy: chemie, biologie, fyzika Ročník: 3. Tématický celek:
Název: Halogeny II - halogenidy Autor: Mgr. Jiří Vozka, Ph.D. Název školy: Gymnázium Jana Nerudy, škola hl. města Prahy Předmět, mezipředmětové vztahy: chemie, biologie, fyzika Ročník: 3. Tématický celek:
Pufry, pufrační kapacita. Oxidoredukce, elektrodové děje.
 ÚSTAV LÉKAŘSKÉ BIOCHEMIE A LABORATORNÍ DIAGNOSTIKY 1. LF UK Pufry, pufrační kapacita. Oxidoredukce, elektrodové děje. Praktické cvičení z lékařské biochemie Všeobecné lékařství Martin Vejražka 2018/19
ÚSTAV LÉKAŘSKÉ BIOCHEMIE A LABORATORNÍ DIAGNOSTIKY 1. LF UK Pufry, pufrační kapacita. Oxidoredukce, elektrodové děje. Praktické cvičení z lékařské biochemie Všeobecné lékařství Martin Vejražka 2018/19
Měření účinnosti rychlovarné konvice
 Zvyšování kvality výuky v přírodních a technických oblastech CZ.1.07/1.1.28/02.0055 Měření účinnosti rychlovarné konvice Označení: EU-Inovace-F-8-13 Předmět: fyzika Cílová skupina: 8. třída Autor: Mgr.
Zvyšování kvality výuky v přírodních a technických oblastech CZ.1.07/1.1.28/02.0055 Měření účinnosti rychlovarné konvice Označení: EU-Inovace-F-8-13 Předmět: fyzika Cílová skupina: 8. třída Autor: Mgr.
Název: Titrace Savo. Autor: RNDr. Markéta Bludská. Název školy: Gymnázium Jana Nerudy, škola hl. města Prahy
 Název: Titrace Savo Autor: RNDr. Markéta Bludská Název školy: Gymnázium Jana Nerudy, škola hl. města Prahy Předmět, mezipředmětové vztahy: chemie a její aplikace, matematika Ročník: 3., ChS (1. ročník
Název: Titrace Savo Autor: RNDr. Markéta Bludská Název školy: Gymnázium Jana Nerudy, škola hl. města Prahy Předmět, mezipředmětové vztahy: chemie a její aplikace, matematika Ročník: 3., ChS (1. ročník
SPEKTROFOTOMETRIE VE VIDITELNÉ OBLASTI SPEKTRA
 SPEKTROFOTOMETRIE VE VIDITELNÉ OBLASTI SPEKTRA Alla Sinica Obecné základy Molekuly mají schopnost pohlcovat elektromagnetické záření pouze určitých vlnových délek. Je to dáno tím, že mohou existovat v
SPEKTROFOTOMETRIE VE VIDITELNÉ OBLASTI SPEKTRA Alla Sinica Obecné základy Molekuly mají schopnost pohlcovat elektromagnetické záření pouze určitých vlnových délek. Je to dáno tím, že mohou existovat v
215.1.19 ČÍSLO KYSELOSTI
 215.1.19 ČÍSLO KYSELOSTI ÚVOD Stanovení čísla kyselosti patří k základním normovaným metodám hodnocení ropných produktů. Tento návod je vytvořen podle norem IP 177/96 a ASTM D66489. Tyto normy specifikují
215.1.19 ČÍSLO KYSELOSTI ÚVOD Stanovení čísla kyselosti patří k základním normovaným metodám hodnocení ropných produktů. Tento návod je vytvořen podle norem IP 177/96 a ASTM D66489. Tyto normy specifikují
Ústřední komise Chemické olympiády. 55. ročník 2018/2019 ŠKOLNÍ KOLO. Kategorie A ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ)
 Ústřední komise Chemické olympiády 55. ročník 2018/2019 ŠKOLNÍ KOLO Kategorie A ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ) PRAKTICKÁ ČÁST 40 BODŮ Autor Mgr. Filip Smrčka Masarykova univerzita, Brno prof. RNDr. Přemysl
Ústřední komise Chemické olympiády 55. ročník 2018/2019 ŠKOLNÍ KOLO Kategorie A ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ) PRAKTICKÁ ČÁST 40 BODŮ Autor Mgr. Filip Smrčka Masarykova univerzita, Brno prof. RNDr. Přemysl
ODDĚLOVÁNÍ SLOŽEK SMĚSÍ, PŘÍPRAVA ROZTOKU URČITÉHO SLOŽENÍ
 ODDĚLOVÁNÍ SLOŽEK SMĚSÍ, PŘÍPRAVA ROZTOKU URČITÉHO SLOŽENÍ PaedDr. Ivana Töpferová Střední průmyslová škola, Mladá Boleslav, Havlíčkova 456 CZ.1.07/1.5.00/34.0861 MODERNIZACE VÝUKY Anotace: laboratorní
ODDĚLOVÁNÍ SLOŽEK SMĚSÍ, PŘÍPRAVA ROZTOKU URČITÉHO SLOŽENÍ PaedDr. Ivana Töpferová Střední průmyslová škola, Mladá Boleslav, Havlíčkova 456 CZ.1.07/1.5.00/34.0861 MODERNIZACE VÝUKY Anotace: laboratorní
Gymnázium a Střední odborná škola, Rokycany, Mládežníků 1115
 Gymnázium a Střední odborná škola, Rokycany, Mládežníků 1115 Číslo projektu: CZ.1.07/1.5.00/34.0410 Číslo šablony: 19 Název materiálu: Ročník: Identifikace materiálu: Jméno autora: Předmět: Tématický celek:
Gymnázium a Střední odborná škola, Rokycany, Mládežníků 1115 Číslo projektu: CZ.1.07/1.5.00/34.0410 Číslo šablony: 19 Název materiálu: Ročník: Identifikace materiálu: Jméno autora: Předmět: Tématický celek:
Ústřední komise Chemické olympiády. 55. ročník 2018/2019 TEST ŠKOLNÍHO KOLA. Kategorie E ZADÁNÍ (60 BODŮ) časová náročnost: 120 minut
 Ústřední komise Chemické olympiády 55. ročník 2018/2019 TEST ŠKOLNÍHO KOLA Kategorie E ZADÁNÍ (60 BODŮ) časová náročnost: 120 minut ANORGANICKÁ CHEMIE 16 BODŮ Body celkem Úloha 1 Vlastnosti sloučenin manganu
Ústřední komise Chemické olympiády 55. ročník 2018/2019 TEST ŠKOLNÍHO KOLA Kategorie E ZADÁNÍ (60 BODŮ) časová náročnost: 120 minut ANORGANICKÁ CHEMIE 16 BODŮ Body celkem Úloha 1 Vlastnosti sloučenin manganu
Univerzita Pardubice 8. licenční studium chemometrie
 Univerzita Pardubice 8. licenční studium chemometrie Statistické zpracování dat při managementu jakosti Semestrální práce Výpočet nejistoty analytického stanovení Ing. Jan Balcárek, Ph.D. vedoucí Centrálních
Univerzita Pardubice 8. licenční studium chemometrie Statistické zpracování dat při managementu jakosti Semestrální práce Výpočet nejistoty analytického stanovení Ing. Jan Balcárek, Ph.D. vedoucí Centrálních
VY_52_INOVACE_2NOV43. Autor: Mgr. Jakub Novák. Datum: 4. 10. 2012 Ročník: 7., 8.
 VY_52_INOVACE_2NOV43 Autor: Mgr. Jakub Novák Datum: 4. 10. 2012 Ročník: 7., 8. Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Fyzika Tematický okruh: Látky a tělesa, Mechanické vlastnosti tekutin
VY_52_INOVACE_2NOV43 Autor: Mgr. Jakub Novák Datum: 4. 10. 2012 Ročník: 7., 8. Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Fyzika Tematický okruh: Látky a tělesa, Mechanické vlastnosti tekutin
ODMĚRNÁ ANALÝZA - TITRACE
 LABORATORNÍ PRÁCE Č. 35 ODMĚRNÁ ANALÝZA - TITRACE PRINCIP Odměrnou analýzou (titrací) se stanovuje obsah určité složky ve vzorku. Podstatou odměrného stanovení je chemická reakce mezi odměrným roztokem
LABORATORNÍ PRÁCE Č. 35 ODMĚRNÁ ANALÝZA - TITRACE PRINCIP Odměrnou analýzou (titrací) se stanovuje obsah určité složky ve vzorku. Podstatou odměrného stanovení je chemická reakce mezi odměrným roztokem
PŘÍRUČKA SPRÁVNÉHO ZPRACOVÁNÍ VÝSLEDKŮ A TVORBY PROTOKOLŮ
 PŘÍRUČKA SPRÁVNÉHO ZPRACOVÁNÍ VÝSLEDKŮ A TVORBY PROTOKOLŮ TATO PŘÍRUČKA VZNIKLA V RÁMCI PROJEKTU FONDU ROZVOJE VYSOKÝCH ŠKOL FRVŠ G6 1442/2013 PŘEDMLUVA Milí studenti, vyhodnocení výsledků a vytvoření
PŘÍRUČKA SPRÁVNÉHO ZPRACOVÁNÍ VÝSLEDKŮ A TVORBY PROTOKOLŮ TATO PŘÍRUČKA VZNIKLA V RÁMCI PROJEKTU FONDU ROZVOJE VYSOKÝCH ŠKOL FRVŠ G6 1442/2013 PŘEDMLUVA Milí studenti, vyhodnocení výsledků a vytvoření
nano.tul.cz Inovace a rozvoj studia nanomateriálů na TUL
 Inovace a rozvoj studia nanomateriálů na TUL nano.tul.cz Tyto materiály byly vytvořeny v rámci projektu ESF OP VK: Inovace a rozvoj studia nanomateriálů na Technické univerzitě v Liberci Experimentální
Inovace a rozvoj studia nanomateriálů na TUL nano.tul.cz Tyto materiály byly vytvořeny v rámci projektu ESF OP VK: Inovace a rozvoj studia nanomateriálů na Technické univerzitě v Liberci Experimentální
LABORATOŘ OBORU Výroba léčiv
 LABORATOŘ OBORU Výroba léčiv Ústav organické technologie (111) Testování pevných lékových forem: Zkouška disoluce Vedoucí práce: Ing. Diem Trang Tran Doc. Ing. Petr Zámostný, PhD. Umístění práce: S25b
LABORATOŘ OBORU Výroba léčiv Ústav organické technologie (111) Testování pevných lékových forem: Zkouška disoluce Vedoucí práce: Ing. Diem Trang Tran Doc. Ing. Petr Zámostný, PhD. Umístění práce: S25b
Pracovní postupy k experimentům s využitím PC
 Inovace profesní přípravy budoucích učitelů chemie CZ..07/2.2.00/5.0324 Prof. PhDr. Martin Bílek, Ph.D. Pracovní postupy k experimentům s využitím PC (teplotní čidlo Vernier propojeno s PC) Stanovení tepelné
Inovace profesní přípravy budoucích učitelů chemie CZ..07/2.2.00/5.0324 Prof. PhDr. Martin Bílek, Ph.D. Pracovní postupy k experimentům s využitím PC (teplotní čidlo Vernier propojeno s PC) Stanovení tepelné
The acquisition of science competencies using ICT real time experiments COMBLAB. Krásný skleník. K čemu je dobrá spektroskopie?
 Krásný skleník K čemu je dobrá spektroskopie? V časopise Zahrádkář se v dopisech čtenářů objevil tento problém: Pan Sklenička se rozhodl postavit na zahradě nový skleník. Bylo to na popud jeho manželky,
Krásný skleník K čemu je dobrá spektroskopie? V časopise Zahrádkář se v dopisech čtenářů objevil tento problém: Pan Sklenička se rozhodl postavit na zahradě nový skleník. Bylo to na popud jeho manželky,
Stanovení koncentrace složky v roztoku vodivostním měřením
 Laboratorní úloha B/2 Stanovení koncentrace složky v roztoku vodivostním měřením Úkol: A. Stanovte vodivostním měřením koncentraci HCl v dodaném vzorku roztoku. Zjistěte vodivostním měřením body konduktometrické
Laboratorní úloha B/2 Stanovení koncentrace složky v roztoku vodivostním měřením Úkol: A. Stanovte vodivostním měřením koncentraci HCl v dodaném vzorku roztoku. Zjistěte vodivostním měřením body konduktometrické
STANOVENÍ AZOBARVIV VE SMĚSI METODOU RP-HPLC SE SPEKTROFOTOMETRICKOU DETEKCÍ
 STANOVENÍ AZOBARVIV VE SMĚSI METODOU RP-HPLC SE SPEKTROFOTOMETRICKOU DETEKCÍ 1 Úkol Separovat a metodou kalibrační křivky stanovit azobarviva (methyloranž - MO, dimethylová žluť - DMŽ) ve směsi metodou
STANOVENÍ AZOBARVIV VE SMĚSI METODOU RP-HPLC SE SPEKTROFOTOMETRICKOU DETEKCÍ 1 Úkol Separovat a metodou kalibrační křivky stanovit azobarviva (methyloranž - MO, dimethylová žluť - DMŽ) ve směsi metodou
Studium komplexace -cyklodextrinu s diclofenacem s využitím NMR spektroskopie
 Jména: Datum: Studium komplexace -cyklodextrinu s diclofenacem s využitím NMR spektroskopie Cílem laboratorního cvičení je prozkoumat interakce léčiva diclofenac s -cyklodextrinem v D 2 O při tvorbě komplexu
Jména: Datum: Studium komplexace -cyklodextrinu s diclofenacem s využitím NMR spektroskopie Cílem laboratorního cvičení je prozkoumat interakce léčiva diclofenac s -cyklodextrinem v D 2 O při tvorbě komplexu
Jazykové gymnázium Pavla Tigrida, Ostrava-Poruba Název projektu: Podpora rozvoje praktické výchovy ve fyzice a chemii
 Datum: Jazykové gymnázium Pavla Tigrida, Ostrava-Poruba Název projektu: Podpora rozvoje praktické výchovy ve fyzice a chemii Laboratorní cvičení č. Tlak vzduchu: Teplota vzduchu: Vitamíny Vlhkost vzduchu
Datum: Jazykové gymnázium Pavla Tigrida, Ostrava-Poruba Název projektu: Podpora rozvoje praktické výchovy ve fyzice a chemii Laboratorní cvičení č. Tlak vzduchu: Teplota vzduchu: Vitamíny Vlhkost vzduchu
Měření osvětlení svíčky, klasické a úsporné žárovky v závislosti na vzdálenosti od zdroje (experiment)
 Zvyšování kvality výuky v přírodních a technických oblastech CZ.1.07/1.1.28/02.0055 Měření osvětlení svíčky, klasické a úsporné žárovky v závislosti na vzdálenosti od zdroje (experiment) Označení: EU-Inovace-F-9-05
Zvyšování kvality výuky v přírodních a technických oblastech CZ.1.07/1.1.28/02.0055 Měření osvětlení svíčky, klasické a úsporné žárovky v závislosti na vzdálenosti od zdroje (experiment) Označení: EU-Inovace-F-9-05
Úvod k biochemickému. mu praktiku. Vladimíra Kvasnicová
 Úvod k biochemickému mu praktiku Vladimíra Kvasnicová organizace praktik pravidla bezpečné práce v laboratoři laboratorní vybavení práce s automatickou pipetou návody: viz. aplikace Výuka automatická pipeta
Úvod k biochemickému mu praktiku Vladimíra Kvasnicová organizace praktik pravidla bezpečné práce v laboratoři laboratorní vybavení práce s automatickou pipetou návody: viz. aplikace Výuka automatická pipeta
Praktikum III - Optika
 Oddělení fyzikálních praktik při Kabinetu výuky obecné fyziky MFF UK Praktikum III - Optika Úloha č. 17 Název: Měření absorpce světla Pracoval: Matyáš Řehák stud.sk.: 13 dne: 17. 4. 008 Odevzdal dne:...
Oddělení fyzikálních praktik při Kabinetu výuky obecné fyziky MFF UK Praktikum III - Optika Úloha č. 17 Název: Měření absorpce světla Pracoval: Matyáš Řehák stud.sk.: 13 dne: 17. 4. 008 Odevzdal dne:...
Měření optických vlastností materiálů
 E Měření optických vlastností materiálů Úkoly : 1. Určete spektrální propustnost vybraných materiálů různých typů stavebních skel a optických filtrů pomocí spektrofotometru 2. Určete spektrální odrazivost
E Měření optických vlastností materiálů Úkoly : 1. Určete spektrální propustnost vybraných materiálů různých typů stavebních skel a optických filtrů pomocí spektrofotometru 2. Určete spektrální odrazivost
