NEUPOGEN 48 MU/0,5 ml injekční roztok v předplněné injekční stříkačce /koncentrát pro přípravu infuzního roztoku v předplněné injekční stříkačce.
|
|
|
- Bohumila Vacková
- před 9 lety
- Počet zobrazení:
Transkript
1 Příloha č. 2 k rozhodnutí o změně registrace sp.zn. sukls117183/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU NEUPOGEN 48 MU/0,5 ml injekční roztok v předplněné injekční stříkačce /koncentrát pro přípravu infuzního roztoku v předplněné injekční stříkačce. 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna předplněná injekční stříkačka obsahuje filgrastimum 48 miliónů jednotek (480 mikrogramů ( g)) v 0,5 ml roztoku (0,96 mg/ml). Filgrastim (rekombinantní methionyl humánní růstový faktor stimulující kolonie granulocytů) byl vyroben pomocí r-dna technologie na E. coli (K12). Pomocné látky: Jeden ml roztoku obsahuje 0,0015 až 0,0023 mmol nebo 0,035 až 0,052 mg sodíku a 50 mg sorbitolu (E420). Úplný seznam pomocných látek viz bod LÉKOVÁ FORMA Injekční roztok v předplněné injekční stříkačce. Koncentrát pro přípravu infuzního roztoku v předplněné injekční stříkačce. Čirý, bezbarvý roztok. 4. KLINICKÉ ÚDAJE 4.1 Terapeutické indikace NEUPOGEN je určen ke zkrácení doby trvání neutropenie a snížení výskytu febrilní neutropenie u pacientů léčených zavedenou cytotoxickou chemoterapií pro maligní nádorové onemocnění (s výjimkou chronické myeloidní leukemie a myelodysplastických syndromů) a ke zkrácení období neutropenie u pacientů léčených myeloablativní terapií následovanou transplantací kostní dřeně, kteří jsou považováni za zvýšeně ohrožené prolongovanou těžkou neutropenií. Bezpečnost a účinnost NEUPOGENU jsou obdobné jak u dospělých, tak i u dětí, léčených cytotoxickou chemoterapií. 1/24
2 NEUPOGEN je určen k mobilizaci periferních kmenových (progenitorových) buněk (peripheral blood progenitor cells -PBPC). Dlouhodobé podávání NEUPOGENU ke zvýšení počtu neutrofilů a snížení četnosti výskytu a délky trvání infekčních komplikací je indikováno u pacientů, dětí nebo dospělých, s těžkou vrozenou (kongenitální), cyklickou nebo idiopatickou neutropenií, kteří mají ANC (absolutní počet neutrofilů) 0,5 x 10 9 /l a těžké nebo opakované infekce v anamnéze. NEUPOGEN je určen k léčbě přetrvávající neutropenie (ANC nižší nebo roven 1,0 x10 9 /l) u pacientů s pokročilou formou HIV infekce, aby se omezilo riziko bakteriálních infekcí tam, kde jsou další možnosti léčby neutropenie nevhodné. 4.2 Dávkování a způsob podání Zavedená cytotoxická chemoterapie Doporučené dávkování NEUPOGENU JE 0,5 MU (5 g)/kg/den. První dávka NEUPOGENU by neměla být podána dříve než 24 hodin po cytotoxické chemoterapii. NEUPOGEN může být podáván denně podkožní injekcí nebo rozředěný v 5% roztoku glukózy a aplikovaný intravenózní infuzí po dobu 30 minut (viz níže, bod 6.6 Návod k použití přípravku a zacházení s ním, ve které jsou uvedeny pokyny pro ředění). Subkutánní způsob podání je ve většině případů upřednostňován. Výsledky klinického hodnocení, které posuzovalo efekt jediné dávky, ukázaly, že intravenózní podání může zkrátit dobu účinku přípravku. Klinický význam těchto zjištění pro podávání vícečetných dávek není jasný. Výběr způsobu podání přípravku by měl záviset na individuálních klinických okolnostech. V randomizovaných klinických hodnoceních byl přípravek podáván subkutánně v dávce 230 g/m 2 /den (4,0 až 8,4 g/kg/den). Denní podávání NEUPOGENU by mělo pokračovat až do doby, než byla překonána nejnižší očekávaná hranice množství (nadir) neutrofilů a než se jejich počet vrátil zpět do normálního rozmezí. Předpokládá se, že po zavedené chemoterapii solidních nádorů, lymfomů a lymfoidních leukemií, bude léčba podle těchto kritérií trvat až 14 dní. Léčba po indukční a konsolidační terapii akutní myeloidní leukemie může být podstatně delší, (až 38 dní) v závislosti na druhu, dávce a časovém rozvrhu použité cytotoxické terapie. U pacientů, kteří jsou léčeni cytotoxickou chemoterapií, bývá typicky pozorován přechodný vzestup počtu neutrofilů 1 až 2 dny po zahájení léčby NEUPOGENEM. K dosažení trvalé odpovědi na léčbu však nesmí být podávání NEUPOGENU ukončeno před tím, než je překonána očekávaná nejnižší hranice množství neutrofilů (nadir) a než se počet neutrofilů vrátí do 2/24
3 normálního rozmezí. Předčasné ukončení léčby NEUPOGENEM před očekávaným nejnižším poklesem počtu (nadirem) neutrofilů se nedoporučuje. Pacienti léčení myeloablativní terapií a následnou transplantací kostní dřeně Doporučená zahajovací dávka přípravku NEUPOGEN je 1,0 MU (10 g)/kg/den ve formě infuze podávané intravenózně 30 minut nebo 24 hodin, případně 1,0 MU (10 g)/kg/den ve formě kontinuální subkutánní infuze po dobu 24 hodin. NEUPOGEN se ředí do 20 ml 5% roztoku glukózy (viz bod 6.6 Návod k použití přípravku a zacházení s ním, ve které jsou uvedeny pokyny pro ředění). První dávka NEUPOGENU by neměla být podána dříve než za 24 hodin po cytotoxické chemoterapii a měla by se podat do 24 hodin po transfúzi kostní dřeně. Jakmile byla překročena nejnižší hranice počtu (nadir) neutrofilů, denní dávka NEUPOGENU by měla být titrována podle neutrofilní odpovědi, jak je uvedeno v následující tabulce: Počet neutrofilů Úprava dávky NEUPOGENU > 1,0 x 10 9 /l 3 po sobě následující dny Snížit na 0,5 MU/kg/den Poté, jestliže ANC zůstane > 1,0 x 10 9 /l po dobu dalších 3 po sobě následujících dní Ukončit léčbu NEUPOGENEM Jestliže ANC poklesne pod < 1,0 x 10 9 /l v průběhu léčby, dávkování NEUPOGENU by se mělo zvyšovat podle výše uvedeného postupu ANC = absolutní počet neutrofilů Mobilizace periferních kmenových (progenitorových) buněk (peripheral blood progenitor cells - PBPC) u pacientů léčených myelosupresivní nebo myeloablativní terapií s následnou autologní transplantací periferních kmenových (progenitorových) buněk Doporučená dávka NEUPOGENU pro mobilizaci PBPC v monoterapii je 1,0 MU (10 g)/kg/den ve formě podkožní kontinuální infuze podávané 24 hodin nebo jednorázové podkožní injekce podávané denně 5 a 7 po sobě následujících dní. Pro podání infuzí se NEUPOGEN ředí do 20 ml 5% roztoku glukózy (viz bod 6.6 Návod k použití přípravku a zacházení s ním, ve které jsou uvedeny pokyny pro ředění). Časový rozvrh leukaferézy: jedna nebo dvě leukaferézy provedené 5. a 6. den obvykle postačují. Za určitých okolností mohou být nezbytné ještě další leukaferézy. Dávkování NEUPOGENU je třeba dodržovat až do poslední leukaferézy. Doporučená dávka NEUPOGENU k mobilizaci PBPC po myelosupresivní chemoterapii je 0,5 MU (5 g)/kg/den podávaná denně ve formě podkožních injekcí od prvního dne ukončení chemoterapie až do překročení očekávaného nejnižšího poklesu (nadiru) neutrofilů a návratu 3/24
4 počtu neutrofilů do normálního rozmezí. Leukaferéza by měla být provedena v době, kdy se ANC pohybuje v rozmezí od < 0.5 x 10 9 /l do > 5.0 x 10 9 /l. Pacientům, kteří nebyli léčeni extenzívní chemoterapií, stačí často jediná leukaferéza. V ostatních případech jsou doporučovány další leukaferézy. Mobilizace periferních kmenových (progenitorových) buněk (peripheral blood progenitor cells - PBPC) u normálních dárců před alogenní transplantací periferních kmenových (progenitorových) buněk Zdravým dárcům by měl být NEUPOGEN podáván kvůli mobilizaci PBPC podkožní injekcí obvykle v dávce 10 g/kg/den po dobu 4 až 5 po sobě následujících dní. Leukaferéza by měla být zahájena 5. den a může pokračovat do 6. dne, aby bylo možné odebrat 4 x 10 6 buněk CD34 + /kg tělesné hmotnosti příjemce. Pacienti s těžkou chronickou neutropenií Vrozená (kongenitální) neutropenie: doporučená zahajovací dávka je 1,2 MU (12 g)/kg/den podkožní injekcí v jedné dávce nebo rozděleně do více dávek. Idiopatická nebo cyklická neutropenie: doporučená zahajovací dávka je 0,5 MU (5 g)/kg/den podkožní injekcí v jedné dávce nebo rozděleně do více dávek. Úprava dávky: NEUPOGEN se podává denně podkožní injekcí až do té doby, než je dosažen a udržen počet neutrofilů vyšší než 1,5 x 10 9 /l. Po dosažení odpovědi by měla být nastavena minimální účinná dávka, která by tento počet udržovala. Dlouhodobé podávání přípravku je zapotřebí k udržení přiměřeného počtu neutrofilů. Po jednom až dvou týdnech léčby lze zahajovací dávku zdvojnásobit nebo snížit na polovinu v závislosti na odpovědi pacienta. V dalším období může být dávka individuálně nastavena každé 1-2 týdny, aby byl průměrný počet neutrofilů v rozmezí 1,5 x 10 9 /l a 10 x 10 9 /l. Při léčbě pacientů s těžkými infekcemi lze uvažovat i o rychlejším zvyšování dávky. 97% pacientů, u kterých byla zaznamenána odpověď v klinických hodnoceních, vykazovalo kompletní odpověď při dávkách 24 g/kg/den. Bezpečnost dlouhodobé léčby NEUPOGENEM v dávce 24 g/kg/den u pacientů s těžkou chronickou neutropenií nebyla stanovena. Další údaje Léčba NEUPOGENEM by měla probíhat pouze ve spolupráci s hematologií a s onkologickým pracovištěm (které má zkušenostmi s podáváním G-CSF), a pouze na těch pracovištích, kde mají k dispozici nezbytné diagnostické možnosti. Mobilizace a aferéza by se měla provádět ve spolupráci s onkologicko-hematologickými pracovištěm, které má dostatečnou zkušenost s touto léčbou a které je schopno správně monitorovat krvetvorné kmenové (progenitorové) buňky. 4/24
5 Klinických hodnocení uskutečněných s NEUPOGENEM se sice zúčastnil menší počet pacientů v pokročilém věku, ale pro tuto skupinu pacientů nebylo provedeno žádné zvláštní klinické hodnocení a nelze proto stanovit specifické doporučené dávkování. Farmakokinetický a farmakodynamický profil NEUPOGENU u pacientů s těžkým postižením funkce ledvin nebo jater byl v klinických hodnoceních podobný jako u normálních pacientů. V těchto případech není zapotřebí upravovat dávku přípravku. Použití u dětí se těžkou chronickou neutropenií (severe chronic neutropenia - SCN) a nádorovým onemocněním Šedesát pět procent pacientů hodnocených v programu SCN (SCN trial program) bylo mladších 18 let. Účinnost léčby pro tuto věkovou skupinu, která do které patřila většina pacientů s vrozenou (kongenitální) neutropenií, byla zřejmá. Nebyly zjištěny žádné rozdíly v profilech bezpečnosti u dětských pacientů, kteří byli léčeni pro těžkou chronickou neutropenii. Údaje získané z klinických hodnocení dětských pacientů ukazují, že bezpečnost a účinnost NEUPOGENU jsou obdobné jak u dětí, tak i dospělých léčených cytotoxickou chemoterapií,. Doporučené dávkování u dětí je stejné jako u dospělých léčených myelosupresivní cytotoxickou chemoterapií. Pacienti s HIV infekcí Dosažení reverze (obratu) neutropenie Doporučená zahajovací dávka NEUPOGENU je 0,1 MU (1 g)/kg/den, podávaná každý den subkutánní injekcí a titrovaná postupně do maximální dávky 0,4 MU (4 g)/kg/den, dokud není dosažen a udržen normální počet neutrofilů (ANC > 2.0 x10 9 /l). V klinických hodnoceních odpovídalo na tuto dávku více než 90% pacientů, kteří dosáhli reverze neutropenie v mediánu 2 dní. U malého počtu pacientů (< 10%), bylo nezbytné podávat až 1,0 MU (10 g)/kg/den k dosažení reverze (obratu) neutropenie. Udržení normálního počtu neutrofilů Po dosažení reverze by měla být nastavena minimální účinná dávka přípravku nezbytná k udržení normálního počtu neutrofilů. Dávka 30 MU (300 g)/den podkožní injekcí je doporučována k zahájení úpravy dávkování. Může být zapotřebí dávku dále upravit podle pacientova ANC tak, aby byl počet neutrofilů > 2.0 x 10 9 /l. Dávky 30 MU (300 g)/den podávané při klinických 5/24
6 hodnoceních 1 až 7 dní v týdnu byly nezbytné k udržení ANC > 2.0 x 10 9 /l, při mediánu frekvence 3 dávky za týden. Pro udržení ANC > 2.0 x 10 9 /l může být zapotřebí dlouhodobé podávání přípravku. 4.3 Kontraindikace NEUPOGEN nesmí být podáván pacientům se známou přecitlivělostí na filgrastim nebo na kteroukoli pomocnou látku. 4.4 Zvláštní upozornění a zvláštní opatření pro použití NEUPOGEN nesmí být používán ke zvýšení dávky cytotoxické chemoterapie nad rámec ustanovených režimů dávkování. NEUPOGEN nesmí být podáván pacientům s těžkou kongenitální neutropenií, u kterých se vyvinula leukemie nebo jsou příznaky vznikající leukemie. Růst maligních buněk Faktor stimulující kolonie granulocytů (G-CSF) může podporovat růst myeloidních buněk in vitro a podobné účinky lze pozorovat i u některých nemyeloidních buněk in vitro. Bezpečnost a účinnost podávání NEUPOGENU pacientům s myelodysplastickým syndromem nebo chronickou myelogenní leukemií nebyla dosud stanovena. NEUPOGEN není k léčbě těchto onemocnění indikován. Zvláštní pozornost je třeba věnovat rozlišení diagnózy blastické transformace chronické myeloidní leukemie od akutní myeloidní leukemie. Vzhledem k omezeným údajům o bezpečnosti a účinnosti přípravku u pacientů se sekundární AML je třeba v těchto případech podávat NEUPOGEN se zvýšenou opatrností. Bezpečnost a účinnost podávání NEUPOGENU pacientům s de novo AML ve věku < 55 let s dobrým cytogenetickým nálezem (t(8;21), t(15;17), a inv(16)) nebyla dosud stanovena. Další zvláštní upozornění U pacientů s osteoporózou, kteří jsou léčeni kontinuálním podáváním NEUPOGENU po dobu delší než 6 měsíců, může být nezbytné monitorovat kostní denzitu. Byly popsány nežádoucí účinky související s postižením plic, a to hlavně intersticiální pneumonie po podání G-CSF. Pacienti s plicními infiltráty nebo pneumonií v anamnéze mohou být více rizikoví. Příznaky onemocnění dýchacího ústrojí, jako jsou kašel, horečka a dušnost, 6/24
7 spolu s rentgenologickým nálezem plicních infiltrátů a zhoršením respiračních funkcí mohou být prvními známkami syndromu akutního respiračního selhání (ARDS - Acute Respiratory Distress Syndrome). Podávání NEUPOGENU se musí v tomto případě ukončit a musí být zahájena příslušná léčba. Kryt jehly přeplněné injekční stříkačky obsahuje přírodní pryž (derivát latexu), která může způsobit alergické reakce. Zvláštní upozornění u pacientů s nádorovým onemocněním Leukocytóza U méně než 5% pacientů, kteří byli léčení NEUPOGENEM v dávce vyšší než 0,3 MU/kg/den (3 g/kg/den), byl pozorován počet bílých krvinek 100 x 10 9 /l nebo vyšší. Nebyly zaznamenány žádné nežádoucí účinky, které by přímo souvisely s tímto stupněm leukocytózy. Nicméně, vhledem k možnému riziku, které souvisí s těžkou leukocytózou, měl by být počet bílých krvinek během léčby NEUPOGENEM pravidelně kontrolován. Jestliže počet leukocytů přesáhne 50 x 10 9 /l poté, co byla překročena očekávaná nejnižší hranice počtu leukocytů (nadir), léčba NEUPOGENEM musí být ihned ukončena. Je-li NEUPOGEN podáván kvůli mobilizaci PBPC, měla být léčba tímto přípravkem ukončena nebo dávka snížena, pokud počet leukocytů přesáhne 70 x 10 9 /l. Rizika spojená se zvýšenými dávkami cytostatik Zvláštní opatrnosti je třeba při léčbě pacientů vysokými dávkami cytostatik, neboť u těchto pacientů nebylo prokázáno zlepšení výsledků léčby nádorového onemocnění. Zvýšené dávky cytostatik mohou vést ke zvýšené toxicitě s následným postižením srdce, plic, kůže a neurologickými příznaky (viz předepsané informace o použití přípravků specifické chemoterapie). Léčbou NEUPOGENEM samotným nelze zabránit vzniku trombocytopenie a anémie, které se objevují jako následek myelosupresivní chemoterapie. Vzhledem k přepokládanému podávání vyšších dávek cytostatik (např. plné dávky podle předepsaného dávkovacího schématu) může být pacient silněji ohrožen trombocytopenií a anémií. Doporučuje se kontrolovat pravidelně počet krevních destiček a hematokrit. Zvláštní pozornost je třeba věnovat podávání jednotlivých dávek nebo kombinované chemoterapii přípravky, o kterých je známo, že mohou způsobovat těžkou trombocytopenii. 7/24
8 Podávání NEUPOGENU k mobilizaci PBPC se projevilo zmírněním poklesu počtu krevních destiček a zkrácení doby trvání trombocytopenie po myelosupresivní nebo myeloablativní chemoterapii. Další zvláštní upozornění Účinky NEUPOGENU u pacientů s podstatně sníženým počtem myeloidních kmenových progenitorových buněk nebyly dosud hodnoceny. NEUPOGEN působí v první řadě na prekurzory neutrofilů se snahou zvýšit počet neutrofilů. Odpověď u pacientů se sníženým počtem prekurzorů neutrofilů může být proto oslabená (podobně jako u pacientů, kteří jsou léčeni extenzívní radioterapií nebo chemoterapií, nebo u těch, kteří trpí nádorovou infiltrací kostní dřeně). Byla zaznamenána hlášení o nemoci vyvolané reakcí štěpu proti hostiteli ( graft versus host disease -GvHD) a fatálních příhod u pacientů dostávajících G-CSF (faktor stimulující kolonie granulocytů = granulocyte colony-stimulating factor) po alogenní transplantaci kostní dřeně (viz bod 5.1). Zvýšení hematopoetické aktivity kostní dřeně jako odpověď na léčbu růstovým faktorem bylo spojeno s přechodnými abnormálními nálezy při zobrazovacích vyšetřeních kostí.to je třeba zvážit při interpretaci výsledků těchto vyšetření. Zvláštní upozornění u pacientů s mobilizací periferních kmenových (progenitorových) buněk Mobilizace Neexistuje žádné prospektivně randomizované srovnání dvou doporučovaných způsobů mobilizace (NEUPOGEN v monoterapii (samotný) nebo v kombinaci s myelosupresivní chemoterapií) ve stejné populaci pacientů. Stupeň variability mezi jednotlivými pacienty a mezi laboratorními analýzami buněk CD34 + způsobuje, že přímé srovnání mezi různými hodnoceními je obtížné. Doporučit optimální způsob mobilizace je proto komplikované. Výběr vhodné mobilizační metody musí vycházet z celkového cíle léčby každého jednotlivého pacienta. Předchozí léčba cytotoxickými přípravky U pacientů, kteří nejprve podstoupili velmi agresivní myelosupresivní terapii, nemusí být mobilizace PBPC dostatečná k dosažení doporučeného minimálního výtěžku progenitorových buněk ( 2.0 x 10 6 CD34 + buněk/kg) nebo k urychlení obnovy krevních destiček na stejné úrovni. Některé cytotoxické látky působí toxicky právě na krvetvorné progenitorové buňky a mohou nepříznivě ovlivnit jejich mobilizaci. Látky jako melfalan, karmustin (BCNU) a karboplatina, jsou-li podávány delší dobu před mobilizací progenitorových buněk, mohou snížit výtěžek 8/24
9 mobilizace. Podávání melfalanu, karboplatiny nebo BCNU současně s NEUPOGENEM působí pozitivně na mobilizaci progenitorových buněk. Pokud se uvažuje o transfúzi periferních kmenových (progenitorových) buněk, je vhodné naplánovat jejich mobilizaci do počáteční fáze léčby. Před podáváním vysokých dávek cytostatik je třeba se u těchto pacientů zaměřit především na počet progenitorových buněk. Je-li jejich výtěžek nedostatečný (podle výše uvedených kriterií), měly by být zváženy jiné způsoby léčby, které podporu progenitorových buněk nevyžadují. Zhodnocení výtěžku progenitorových buněk Při hodnocení počtu získaných progenitorových buněk u pacientů léčených NEUPOGENEM je třeba věnovat zvýšenou pozornost způsobu jejich kvantifikace. Výsledky průtokové cytometrie buněk CD34 + se liší v závislosti na použité metodice a doporučení založená na počtech stanovených v jiných laboratořích by měla být interpretována velmi opatrně. Statistická analýza poměru mezi počtem reinfundovaných buněk CD34 + a rychlostí obnovy krevních destiček po vysokých dávkách cytostatik naznačuje komplexní, ale kontinuální vztah. Hodnota doporučeného minimálního výtěžku 2.0 x 10 6 buněk CD34 + /kg je založena na publikovaných zkušenostech s odpovídající hematologickou obnovou. Uvedené hodnoty zřejmě korelují s rychlejším zotavením, hodnoty pod touto hranicí jsou spojeny s pomalejším zotavením. Zvláštní upozornění u zdravých dárců, kteří podstupují mobilizaci periferních kmenových (progenitorových) buněk. Mobilizace PBPC nepřináší zdravým dárcům žádný přímý klinický užitek a měla by být vyhrazena pouze pro alogenní transplantaci kmenových buněk. Mobilizaci PBPC lze provádět pouze u dárců, kteří splňují obvyklá klinická a laboratorní kriteria pro dárcovství kmenových buněk se zvláštním zřetelem na hodnoty hematologických vyšetření a možná infekční onemocnění. Bezpečnost a účinnost NEUPOGENU u zdravých dárců ve věku < 16 let nebo > 60 let nebyla stanovena. Přechodná trombocytopenie (počet krevních destiček < 100 x 10 9 /l) po podání filgrastimu a leukaferéze byla pozorována u 35 % hodnocených subjektů. Pouze ve dvou případech byl zaznamenán počet destiček < 50 x 10 9 /l, který byl přisuzován provedené leukaferéze. 9/24
10 Pokud je nezbytné provést více než jednu leukaferézu, je třeba věnovat zvláštní pozornost dárcům, kteří mají před leukaferézou počet krevních destiček < 100 x 10 9 /l; obecně by se leukaferéza neměla provádět při počtu destiček < 75 x 10 9 /l. Leukaferéza by se dále neměla provádět u dárců užívajících antikoagulancia nebo u těch, kteří mají poruchu srážení krve. Podávání NEUPOGENU by mělo být přerušeno nebo dávka snížena v případě, že počet leukocytů překročí 70 x10 9 /l. Dárci, kterým byl podáván G-CSFs kvůli mobilizaci PBPC by měli být sledováni do doby, než se jejich hematologické hodnoty vrátí k normě. Byly popsány přechodné cytogenetické abnormality u zdravých dárců po podání G-CSF. Význam těchto změn je dosud neznámý. V současné době pokračuje sledování dlouhodobé bezpečnosti přípravku u dárců. U zdravých dárců nelze zcela vyloučit riziko vzniku maligního myeloidního klonu. Doporučuje se proto, aby centra provádějící aferézu nejméně 10 let systematicky sledovala dárce kmenových buněk z hlediska dlouhodobé monitorace bezpečnosti přípravku. Po podání G-CSF se běžně objevovaly asymptomatické případy splenomegalie, velmi vzácné byly případy ruptury sleziny u zdravých dárců (a pacientů). Některé případy ruptury sleziny skončily fatálně. Je třeba proto pečlivě kontrolovat velikost sleziny (např. klinickým vyšetřením, ultrazvukem) a na možnost ruptury sleziny pomýšlet u dárců a/nebo pacientů, kteří si stěžují na bolesti v levém podžebří nebo v levém rameni. U zdravých dárců byly v postmarketingových klinických hodnoceních velmi vzácně popsány plicní nežádoucí účinky (hemoptýza, plicní krvácení, plicní infiltráty, dyspnoe a hypoxie). Při podezření nebo výskytu plicních nežádoucích účinků je třeba zvážit přerušení léčby Neupogenem a poskytnout odpovídající zdravotní péči. Zvláštní upozornění u příjemců alogenních periferních kmenových (progenitorových) buněk mobilizovaných NEUPOGENEM. Z údajů, které jsou v současnosti dostupné, vyplývá, že imunologické interakce mezi alogenním PBPC štěpem a příjemcem mohou být spojeny se zvýšeným rizikem akutní nebo chronické nemoci vyvolané reakcí štěpu proti hostiteli (Graft versus Host Disease - GvHD) ve srovnání s transplantací kostní dřeně. 10/24
11 Zvláštní upozornění u pacientů s těžkou chronickou neutropenií (SCN) Krevní obraz Je nezbytné pečlivě sledovat počet krevních destiček, a to zejména v průběhu prvních několika týdnů léčby NEUPOGENEM. Je třeba zvážit možnost snížení dávky nebo přechodného vysazení NEUPOGENU u pacientů s trombocytopenií. t.j. při počtu krevních destiček trvale pod /mm 3. Může docházet i k dalším změnám počtu krvinek včetně anémie a přechodného zvýšení počtu myeloidních progenitorových buněk. Tyto změny vyžadují pečlivé sledování krevního obrazu. Transformace do leukemie nebo myelodysplastického syndromu V případě těžké chronické neutropenie je třeba věnovat zvýšenou pozornost jejímu odlišení od jiných poruch krvetvorby, jako je aplastická anémie, myelodysplasie a myeloidní leukemie. Před zahájením léčby by měl být vyšetřen kompletní diferenciální krevní obraz, počet krevních destiček a morfologie kostní dřeně s určením karyotypu. V průběhu klinických hodnocení byl u pacientů s těžkou formou chronické neutropenie léčených NEUPOGENEM zaznamenán malý počet případů (přibližně 3%) myelodysplastického syndromu nebo leukemie. Tento výskyt byl zjištěn pouze u pacientů s kongenitální neutropenií. Myelodysplastický syndrom (MDS) a leukemie jsou přirozenými komplikacemi tohoto onemocnění a jejich spojitost s podáváním NEUPOGENU je nejistá. Ve skupině čítající přibližně 12% pacientů, kteří měli na počátku léčby normální cytogenetický nález, byly následně objeveny při pravidelných vyšetřeních abnormality včetně monosomie 7. chromozomu. V současné době není zcela jasné, zda dlouhodobá léčba pacientů trpících těžkou formou chronické neutropenie predisponuje tyto pacienty ke vzniku cytogenetických abnormalit, MDS nebo leukemické transformace. U těchto pacientů se doporučuje pravidelné (každých 12 měsíců) morfologické a cytogenetické vyšetření kostní dřeně. Další zvláštní upozornění Měly by být vyloučeny další příčiny přechodné neutropenie, jako jsou například virové infekce. Splenomegalie je přímým následkem léčby NEUPOGENEM. U třiceti jednoho procenta (31%) pacientů, kteří se zúčastnili klinických hodnocení, byla nalezena pohmatem zjistitelná splenomegalie. Zvětšení objemu sleziny, určené radiograficky, se objevovalo časně po zahájení léčby NEUPOGENEM, a mělo tendenci dále stagnovat. Snížení dávky vedlo ke zpomalení růstu sleziny nebo se zvětšování zastavilo. U 3% pacientů bylo nutné slezinu chirurgicky odstranit. 11/24
12 Velikost sleziny by měla být pravidelně kontrolována. Ke zhodnocení abnormálního zvětšení sleziny by mělo stačit palpační vyšetření břicha (pohmatem). U nízkého počtu pacientů se vyskytovala hematurie/proteinurie. Ke sledování těchto příznaků je nezbytný pravidelný rozbor moči. Bezpečnost a účinnost podávání přípravku novorozencům a pacientům s autoimunní neutropenií nebyla stanovena. Zvláštní upozornění u pacientů s HIV infekcí Krevní obraz Absolutní počet neutrofilů (absolute neutrophil count - ANC) by měl být pečlivě sledován, a to zejména během prvních týdnů po zahájení léčby NEUPOGENEM. Někteří pacienti mohou na zahajovací dávku NEUPOGENU reagovat velmi rychle a značným zvýšením počtu neutrofilů. První 2 až 3 dny léčby NEUPOGENEM se doporučuje kontrolovat ANC denně. V průběhu další léčby se doporučuje kontrolovat ANC nejméně dvakrát týdně během prvních dvou týdnů léčby a poté jednou za týden nebo jednou za dva týdny po dobu udržovací terapie. Při intermitentním podávání 30 MU (300 g) NEUPOGENU za den může docházet k výraznému kolísání počtu neutrofilů. K určení nejnižší hranice (nadiru) absolutního počtu neutrofilů se doporučuje odebírat krevní vzorky ke stanovení ANC bezprostředně před plánovaným podáním NEUPOGENU. Riziko spojené se zvýšenými dávkami myelosupresivních léčiv Léčbou samotným NEUPOGENEM nelze předejít vzniku trombocytopenie a anémie vyvolané myelosupresivní léčbou. Důsledkem případného podávání vysokých dávek nebo velkého počtu těchto přípravků zároveň s léčbou NEUPOGENEM může být pro pacienta zvýšené riziko trombocytopenie a anémie. Doporučuje se pravidelně kontrolovat krevní obraz (viz výše). Infekce a maligní onemocnění vyvolávající myelosupresi (útlum kostní dřeně) Neutropenie může vzniknout následkem infekce oportunními mikroorganizmy, infiltrujícími kostní dřeň, jakými je například Mycobacterium avium, nebo na podkladě maligních onemocnění, jako je lymfom. U pacientů, kterým byla zjištěna infekční infiltrace kostní dřeně nebo malignita, je třeba kromě podávání NEUPOGENU kvůli neutropenii i zvážit příslušnou léčbu základního onemocnění. Účinky NEUPOGENU na neutropenii vyvolanou infekční infiltrací kostní dřeně nebo maligním onemocněním nebyly dostatečně zhodnoceny. 12/24
13 Zvláštní upozornění u pacientů se srpkovitou anémií U pacientů se srpkovitou anemií byly ve spojení s podáváním NEUPOGENU popsány vazookluzivní krize, v některých případech s fatálním koncem. Při úvaze o použití NEUPOGENU u pacientů se srpkovitou anemií by měl proto lékař postupovat velice opatrně a podrobně zvážit vzájemný poměr možných rizik a přínosů léčby. Všichni pacienti Neupogen obsahuje sorbitol (E420). Pacienti se vzácnými vrozenými problémy s intolerancí fruktózy by neměli být léčeni tímto přípravkem. Neupogen obsahuje méně než 1 mmol (23 mg) sodíku na 0,6 mg/ml, čili je v podstatě bez sodíku. Pro lepší dohledatelnost faktorů stimulujících kolonie granulocytů (G-CSF) se má vzáznamu pacienta zřetelně zaznamenávat obchodní název podaného přípravku. 4.5 Interakce s jinými léčivými přípravky a jiné formy interakce Bezpečnost a účinnost NEUPOGENU podávaného ve stejný den s myelosupresivní cytotoxickou chemoterapií nebyla definitivně stanovena. Vzhledem k citlivosti rychle se dělících myeloidních buněk na myelosupresivní cytotoxickou chemoterapii, není podání NEUPOGENU doporučováno v časovém období od 24 hodin před chemoterapií až 24 hodin po chemoterapii. Předběžné výsledky získané od malého počtu pacientů léčených NEUPOGENEM současně s 5- fluorouracilem ukazují na možnost zhoršení neutropenie. Případné interakce s jinými hematopoetickýni růstovými faktory a cytokiny nebyly dosud v rámci klinických hodnocení studovány. Vzhledem k tomu, že lithium podporuje uvolňování neutrofilů, může dojít při jeho podávání k zesílení účinku NEUPOGENU. Přestože tato interakce nebyla formálně hodnocena, není k dispozici důkaz o její škodlivosti. 4.6 Těhotenství a kojení Bezpečnost podávání NEUPOGENU těhotným ženám nebyla stanovena. Existují literární údaje popisující transplacentární průnik filgrastimu u těhotných žen. Studie na krysách a králících nepodaly důkaz o teratogenitě NEUPOGENU. U králíků byla zaznamenána vyšší incidence potratů, ale nebyly pozorovány žádné malformace. Možné riziko léčby NEUPOGENEM u těhotných žen musí být zváženo v poměru k předpokládanému léčebnému prospěchu. Není známo, zda NEUPOGEN přechází do mateřského mléka. Kojícím ženám se nedoporučuje NEUPOGEN podávat. 13/24
14 4.7 Účinky na schopnost řídit a obsluhovat stroje Žádná klinická hodnocení o vlivu NEUPOGENU na schopnost řídit nebo obsluhovat stroje nebyla prováděna. 4.8 Nežádoucí účinky Zkušenosti z klinických studií Všechny nežádoucí účinky jsou uvedeny ve skupinách podle orgánových systémů dle MedDRA (SOC).V každé skupině četnosti výskytu jsou nežádoucí účinky popsány v pořadí podle klesající závažnosti. Posouzení nežádoucích účinků je založeno na následujících skupinách dle četnosti: Velmi časté: 1/10 Časté: 1/100, <1/10 Méně časté: 1/1,000, <1/100 Vzácné: 1/10,000, <1/1,000 Velmi vzácné: <1/10,000 Není známo: z dostupných údajů nelze určit Pacienti s nádorovým onemocněním Nejčastějším nežádoucím účinkem, který byl pozorován v souvislosti s podáváním doporučených dávek NEUPOGENU při klinických hodnoceních, byly bolesti pohybového systému mírné až střední intenzity, které se vyskytovaly u 10 % pacientů. U 3 % pacientů byly tyto bolesti silné. Bolesti pohybového systému lze obvykle potlačit běžnými analgetiky. K méně častým nežádoucím účinkům patřily poruchy močení, především lehká až středně závažná dysurie. V randomizovaných, placebem kontrolovaných klinických hodnoceních nezvyšoval NEUPOGEN incidenci nežádoucích účinků spojených s cytotoxickou chemoterapií. Nežádoucí účinky uváděné se stejnou frekvencí u pacientů léčených kombinací NEUPOGEN/chemoterapie a placebo/chemoterapie byly : nevolnost a zvracení, alopecie, průjem, únava, nechutenství, záněty sliznic, bolesti hlavy, kašel, vyrážka, bolesti na hrudi, astenie, faryngolaryngeální bolest, zácpa a bolest. Reverzibilní a na dávce závislé mírné až střední zvýšení laktátdehydrogenázy, alkalické fosfatázy, kyseliny močové a -glutamyl transferázy bylo zaznamenáno při léčbě doporučenými dávkami NEUPOGENU přibližně u 50%, 35%, 25%, respektive 10% pacientů. Ojediněle byly uváděny přechodné poklesy krevního tlaku nevyžadující klinickou léčbu. Byly popsány případy GvHD a úmrtí pacientů, kteří byli léčeni G-CSF po alogenní transplantaci kostní dřeně (viz. bod 5.1). 14/24
15 Cévní onemocnění včetně venookluzívní choroby a poruch bilance tekutin byly uváděny ojediněle u pacientů léčených vysokými dávkami cytostatik a následnou autologní transplantací kostní dřeně. Příčinná souvislost s podáváním NEUPOGENU nebyla stanovena. Třídy orgánových systémů Frekvence Nežádoucí účinek Poruchy metabolismu a výživy Velmi časté Časté Zvýšení alkalické fosfatázy krvi Zvýšení laktátdehydrogenázy v krvi Zvýšení kyseliny močové v krvi Anorexie Poruchy nervového systému Časté Bolest hlavy Cévní poruchy Vzácné Angiopatie Respirační, hrudní a mediastinální poruchy Gastrointestinální poruchy Časté Velmi vzácné Velmi časté Časté Kašel Faryngolaryngeální bolest Plicní infiltrace Nausea Zvracení Zácpa Průjem Poruchy jater a žlučových cest Velmi časté Zvýšení gamaglutamyltransferázy Poruchy kůže a podkožní tkáně Časté Alopecie Vyrážka Poruchy svalové a kosterní soustavy a pojivové tkáně Časté Bolesti kostí a svalů Poruchy ledvin a močových cest Velmi vzácné Abnormality moči Celkové poruchy a reakce v místě aplikace Časté Méně časté Únava Astenie Záněty sliznic Bolest na hrudi Bolest Nežádoucí účinky u zdravých dárců s mobilizací periferních kmenových (progenitorových) buněk Nejčastěji uváděným nežádoucím účinkem byly přechodné bolesti pohybového systému mírné až střední intenzity. Leukocytóza (počet bílých krvinek /WBC/ > 50 x 10 9 /l) byla zaznamenána u 15/24
16 41% dárců a přechodná trombocytopenie (počet krevních destiček < 100 x 10 9 /l) po podání filgrastimu a leukaferéze se vyskytovala u 35% dárců. Přechodné, lehké zvýšení alkalické fosfatázy, laktátdehydrogenázy, aspartátaminotransferázy a kyseliny močové bylo popsáno u zdravých dárců, kterým byl podáván filgrastim; tyto nálezy neměly klinickou odezvu. Exacerbace příznaků artritidy byla pozorována velmi vzácně. Bolesti hlavy, které jsou přičítány podávání filgrastimu, byly popsány v klinických hodnoceních dárců PBPC. U zdravých dárců byl často zaznamenán výskyt splenomegalie, obvykle však bezpříznakové. Velmi vzácně byly popsány případy ruptury sleziny u zdravých dárců a pacientů po podávání faktoru stimulujícího kolonie granulocytů (G-CSF = granulocyte colony-stimulating factor) (viz bod 4.4). Třídy orgánových systémů Frekvence Nežádoucí účinek Poruchy krve a lymfatického systému Poruchy metabolismu a výživy Velmi časté Méně časté Časté Méně časté Leukocytóza Trombocytopenie Poruchy sleziny Zvýšení alkalické fosfatázy v krvi Zvýšení laktátdehydrogenázy v krvi Zvýšení aspartátaminotransferázy Hyperurikémie Poruchy nervového systému Velmi časté Bolest hlavy Poruchy svalové a kosterní soustavy a pojivové tkáně Velmi časté Méně časté Bolest pohybového systému Exacerbace revmatoidní artritidy Nežádoucí účinky u pacientů s těžkou formou chronické neutropenie (SCN) Frekvence nežádoucích účinků, které byly popsány v souvislosti s léčbou NEUPOGENEM U pacientů s SCN, se postupem času snižovala. Nejčastějšími nežádoucími účinky, přisuzovanými NEUPOGENU, byly bolesti kostí a obecně bolesti pohybového systému. 16/24
17 K dalším pozorovaným nežádoucím účinkům patřila splenomegalie, v menšině případů progresivní, a trombocytopenie. Bolesti hlavy a průjmy byly zaznamenány krátce po zahájení léčby NEUPOGENEM u méně než 10% pacientů. Popsána byla také anémie a případy epistaxe. Přechodné zvýšení sérové hladiny kyseliny močové, laktátdehydrogenázy a alkalické fosfatázy nebylo doprovázeno klinickými příznaky. Bylo zaznamenáno také přechodné mírné snížení glykémie. Nežádoucí účinky pravděpodobně související s léčbou NEUPOGENEM, které se vyskytují u < 2% pacientů s SCN byly: reakce v místě vpichu injekce, bolest hlavy, hepatomegalie, bolesti kloubů, alopecie, osteoporóza a kožní vyrážka. Při dlouhodobé léčbě byla u 2 % pacientů s SCN zjištěna kožní vaskulitida. Velmi zřídka došlo k výskytu proteinurie/hematurie. Třídy orgánových systémů Frekvence Nežádoucí účinek Poruchy krve a lymfatického systému Poruchy metabolismu a výživy Velmi časté Časté Méně časté Velmi časté Anemie Splenomegalie Trombocytopenie Poruchy sleziny Zvýšení alkalické fosfatázy v krvi Zvýšení laktátdehydrogenázy v krvi Snížení glukózy v krvi Hyperurikémie Poruchy nervového systému Časté Bolest hlavy Respirační, hrudní a mediastinální poruchy Velmi časté Epistaxe Gastrointestinální poruchy Časté Průjem Poruchy jater a žlučových cest Poruchy kůže a podkožní tkáně Poruchy svalové a kosterní soustavy a pojivové tkáně Poruchy ledvin a močových cest Celkové poruchy a reakce v místě aplikace Časté Časté Velmi časté Časté Méně časté Časté Hepatomegalie Alopecie Kožní vaskulitida Vyrážka Bolesti pohybového systému Osteoporóza Hematurie Proteinurie Bolest v místě vpichu 17/24
18 Nežádoucí účinky u pacientů s infekcí HIV Jedinými nežádoucími účinky, které byl pozorovány v souvislosti s podáváním doporučených dávek NEUPOGENU při klinických hodnoceních, byly bolesti pohybového systému, především bolesti kostí mírné až střední intenzity a bolesti svalů. Incidence těchto případů byla podobná jako u pacientů s nádorovým onemocněním. Splenomegalie související s léčbou NEUPOGENEM se vyskytovalo u < 3% pacientů. Ve všech případech se jednalo o mírné až střední zvětšení, diagnostikované fyzikálním vyšetřením. Klinický průběh byl vždy benigní; u žádného pacienta nebyl zjištěn hypersplenizmus a žádný pacient nemusel podstoupit splenektomii. Vzhledem k tomu, že splenomegalie bývá u pacientů infikovaných HIV časté a objevuje se v různém stupni u pacientů s AIDS, je souvislost s léčbou NEUPOGENEM nejasná. Třídy orgánových systémů Frekvence Nežádoucí účinek Poruchy krve a lymfatického systému Poruchy svalové a kosterní soustavy a pojivové tkáně Časté Velmi časté Poruchy sleziny Bolesti pohybového systému Zkušenosti po uvedení na trh Pacienti s nádorovým onemocněním U pacientů léčených NEUPOGENEM byly velmi vzácně zaznamenány případy výskytu kožní vaskulitidy. Mechanizmus vzniku této vaskulitidy u pacientů, kterým je podáván NEUPOGEN, není znám. Ojediněle byl hlášen výskyt Sweetova syndromu (akutní febrilní dermatóza). V individuálních případech byla zaznamenána exacerbace revmatoidní artritidy. Vzácně byl uváděn výskyt nežádoucích účinků souvisejících s postižením plic typu intersticiální pneumonie, plicního otoku a plicních infiltrátů s následným rozvojem respiračního selhání nebo syndromem akutní dechové tísně (ARDS), které může být fatální (viz bod 4.4.). U pacientů, kterým byl podáván filgrastim, byl v úvodu léčby či v jejím průběhu popsán v postmarketingovém období výskyt alergických reakcí různých typů včetně anafylaxe, vyrážky, 18/24
19 kopřivky, angioedému, dyspnoe a hypotenze. Celkově byla hlášení častější po i.v. podání. V některých případech se tyto reakce znovu vyskytly při opětném zahájení léčby, naznačujíc tak příčinnou souvislost. NEUPOGEN by neměl být vůbec podáván pacientům s anamnézou prodělaných závažných alergických reakcí. U pacientů se srpkovitou anemií byly hlášeny izolované případy vazo-okluzivní krize (viz bod 4.4.). U pacientů s rakovinou léčených filgrastimem byla popsána pseudodna. Zdraví dárci U zdravých dárců byla v postmarketingovém období popsána anafylaxe. Plicní nežádoucí účinky (hemoptýza, plicní krvácení, plicní infiltráty, dyspnoe a hypoxie) byly hlášeny u zdravých dárců v postmarketingovém období (viz bod 4.4). 4.9 Předávkování Účinky NEUPOGENU v případě předávkování nebyly stanoveny. Ukončení léčby NEUPOGENEM vede obvykle k poklesu cirkulujících neutrofilů o 50% během 1 až 2 dnů, jejich návrat do normy trvá 1 až 7 dnů. 5. FARMAKOLOGICKÉ VLASTNOSTI 5.1 Farmakodynamické vlastnosti Farmakoterapeutická skupina: cytokiny, ATC kód: L03AA02 Lidský G-CSF je glykoprotein, který reguluje tvorbu a uvolňování funkčních neutrofilů z kostní dřeně. NEUPOGEN obsahující rekombinantní methionyl humánní G-CSF (filgrastim) způsobuje během 24 hodin významné zvýšení počtu neutrofilů v periferní krvi spolu s lehkým zvýšením monocytů. U některých pacientů s těžkou formou chronické neutropenie může filgrastim také vyvolávat mírné zvýšení počtu cirkulujících eosinofilů a bazofilů vzhledem k jejich počátečním hodnotám; někteří tito pacienti mohou mít eosinofilii nebo bazofilii již před zahájením léčby. Zvýšení počtu neutrofilů je v rozsahu doporučovaného dávkování závislé na dávce. Neutrofily tvořené vlidském těle po podání filgrastimu mají normální nebo zesílenou funkci, jak bylo prokázáno testy chemotaktických a fagocytárních funkcí. Ukončení léčby filgrastimem vede obvykle k poklesu cirkulujících neutrofilů o 50% během 1 až 2 dní, jejich návrat do normy trvá 1 až 7dní. 19/24
20 Podávání filgrastimu pacientů léčených cytotoxickou chemoterapií vede k signifikantnímu poklesu incidence, závažnosti a doby trvání neutropenie a febrilní neutropenie. Léčba filgrastimem významně zkracuje dobu trvání febrilní neutropenie, užívání antibiotik a hospitalizace po chemoterapii pro akutní myelogenní leukemii nebo po myeloablativní léčbě s následnou transplantací kostní dřeně. Incidence horečky a prokázaných infekcí snížena nebyla. Doba horečky nebyla zkrácena u pacientů podstupujících myeloablativní léčbu následovanou transplantací kostní dřeně. Užívání filgrastimu, ať už samotného nebo po chemoterapii, mobilizuje hematopoetické kmenové (progenitorové) buňky do periferní krve. Tyto autologní periferní progenitorové buňky (peripheral blood progenitor cells- PBPC) mohou být odebrány a podávány zpět infuzí po léčbě vysokými dávkami cytotoxických přípravků, buď namísto transplantace kostní dřeně nebo jako její doplněk. Podání PBPC urychluje obnovu krvetvorby, zkracuje tím dobu, po kterou trvá riziko krvácivých komplikací a snižuje spotřebu transfúzí krevních destiček. U příjemců alogenních periferních progenitorových buněk mobilizovaných NEUPOGENEM došlo podstatně rychleji k obnově hematologických parametrů, což vedlo k významnému zkrácení doby neléčené obnovy počtu krevních destiček v porovnání s alogenní transplantací kostní dřeně. Jedno retrospektivní evropské hodnocení hodnotící používání G-CSF po alogenní transplantaci kostní dřeně u pacientů s akutními leukemiemi naznačuje zvýšené riziko GvHD, mortality související s léčbou (TRM) a mortality, pokud byl G-CSF podáván. V jiném retrospektivním mezinárodním hodnocení u pacientů s akutní a chronickou myeloidní leukemií nebyl žádný vliv na riziko GvHD, TRM a mortalitu pozorován. Metaanalýzou hodnocení alogenních transplantací, včetně výsledků 9 prospektivních randomizovaných hodnocení, 8 retrospektivních hodnocení a 1 hodnocení případů a kontrol, nebyl zjištěný žádný vliv na riziko akutní GvHD, chronickou GvHD nebo časnou TRM. Relativní Riziko (95% CI) GvHD a TRM po léčbě s G-CSF po transplantaci kostní dřeně Trvání studie Akutní stupeň II-IV chronická Publikace N GvHD GvHD TRM Meta-Analýza (2003) a (0.87, 1.33) 1.02 (0.82, 1.26) 0.70 (0.38, 1.31) Evropské retrospektivní hodnocení (2004) b (1.08, 1.64) 1.29 (1.02, 1.61) 1.73 (1.30, 2.32) 20/24
21 Mezinárodní retrospektivní hodnocení (2006) b (0.86, 1.42) 1.10 (0.86, 1.39) 1.26 (0.95, 1.67) a Analýza zahrnuje hodnocení týkající se transplantace kostní dřeně v tomto období; v některých hodnoceních se používal GM-CSF b Analýza zahrnuje pacienty po transplantaci kostní dřeně v tomto období Podávání filgrastimu zdravým dárcům k mobilizaci periferních kmenových (progenitorových) buněk před alogenní transplantací periferních kmenových (progenitorových) buněk Dávka 10 g/kg/den podávaná subkutánně zdravým dárcům po dobu 4 až 5 po sobě následujících dní umožňuje získat 4 x 10 6 CD34 + buněk/kg tělesné váhy u většiny dárců po dvou leukaferézách. Podávání filgrastimu pacientům (dětem nebo dospělým) s těžkou formou chronické neutropenie (těžká vrozená, cyklická a idiopatická neutropenie) vede k přetrvávajícímu zvýšení absolutního počtu neutrofilů v periferní krvi a sníženému počtu infekčních komplikací a souvisejících stavů. Podávání filgrastimu pacientům infikovaným HIV vede k udržení normálního počtu neutrofilů, což umožňuje podávání antivirových a/nebo dalších myelosupresívních léčiv podle plánovaného schématu dávkování. Nejsou důkazy o tom, že by u pacientů infikovaných HIV docházelo ke zvýšené replikaci HIV. Tak jako jiné hematopoetické růstové faktory, G-CSF vykazuje in vitro stimulační vlastnosti na lidských endoteliálních buňkách. 5.2 Farmakokinetické vlastnosti Clearance filgrastimu probíhá podle farmakokinetiky prvního řádku (first-order pharmacokinetics) po subkutánním i intravenózním podání. Poločas sérové eliminace filgrastimu je přibližně 3,5 hodiny při rychlostí clearance přibližně 0,6 ml/min/kg. Kontinuální podávání NEUPOGENU v infuzi po dobu až 28 dní pacientům v rekonvalescenci po autologní transplantaci kostní dřeně nevedlo k akumulaci filgrastimu, přičemž poločas eliminace byl srovnatelný po celou dobu podávání. Mezi dávkou a sérovou koncentrací filgrastimu existuje pozitivní lineární korelace, ať je podán intravenózně nebo subkutánně. Po subkutánním podání doporučených dávek přetrvávaly sérové koncentrace nad 10 ng/ml po dobu 8 až 16 hodin. Distribuční objem v krvi je přibližně 150 ml/kg. 21/24
22 5.3 Předklinické údaje vztahující se k bezpečnosti Nejsou žádné další předklinické údaje důležité pro preskripci, které by doplňovaly údaje již uvedené v ostatních kapitolách Souhrnu údajů o přípravku. 6. FARMACEUTICKÉ ÚDAJE 6.1 Seznam pomocných látek Trihydrát octanu sodného* Sorbitol (E420) Polysorbát 80 Voda na injekci * Trihydrát octanu sodného byl vyroben titrací ledové kyseliny octové s hydroxidem sodným 6.2 Inkompatibility NEUPOGEN se nesmí ředit solnými roztoky. Rozpuštěný filgrastim může se může adsorbovat na skle a plastech. Tento léčivý přípravek nesmí být mísen s jinými léčivými přípravky s výjimkou těch, které jsou uvedeny v bodě 6.6 (Návod k použití přípravku, zacházení s ním a k jeho likvidaci). 6.3 Doba použitelnosti 30 měsíců. Chemická a fyzikální stabilita naředěného roztoku před použitím byla prokázána po dobu 24 hodin při teplotě 2 až 8ºC. Z mikrobiologického hlediska má být přípravek použit ihned po naředění. Jestliže není použit ihned, doba použitelnosti naředěného přípravku a podmínky jeho uchovávání před použitím podléhají odpovědnosti uživatele a neměly by obvykle překračovat 24 hodin při 2 až 8 C, pokud ředění neproběhlo za kontrolovaných a validovaných aseptických podmínek. 6.4 Zvláštní opatření pro uchovávání Uchovávejte při teplotě 2 C - 8 C. Naředěný roztok NEUPOGENU je třeba uchovávat při teplotě 2 C až 8 C Náhodné vystavení přípravku teplotám pod bodem mrazu nemá nepříznivý vliv na stabilitu NEUPOGENU. 22/24
23 6.5 Druh obalu a velikost balení Jedno balení obsahuje jednu nebo pět předplněných stříkaček s 0,5 ml NEUPOGENU ve formě injekčního roztoku. Předplněné injekční stříkačky jsou vyrobeny ze skla typu I a mají trvale připojenu injekční jehlu z nerezavějící oceli. Kryt jehly předplněné injekční stříkačky obsahuje suchou přírodní gumu (derivát latexu). Viz bod 4.4. Na trhu nemusí být všechny velikosti balení. 6.6 Návod k použití přípravku, zacházení s ním a jeho likvidaci Pokud je třeba, NEUPOGEN může být ředěn 5% roztokem glukózy. V žádném případě se nedoporučuje ředění na výslednou koncentraci nižší než 0,2 MU (2 g)/ml. Roztok přípravku před podáním prohlédněte. Použít lze jen čiré roztoky bez volných částic. Při léčbě filgrastimem naředěným do koncentrace nižší než 1.5 MU (15 g)/ml je třeba do roztoku přidat lidský albumin (HSA) až do výsledné koncentrace 2 mg/ml. Například: v připravené injekci o obsahu 20 ml s celkovou dávkou filgrastimu nižší než 30 MU (300 g) by mělo být přidáno 0,2 ml 20% lidského albuminu (human albumin solution Ph. Eur). NEUPOGEN neobsahuje žádné konzervační látky. Vzhledem k možnému riziku mikrobiální kontaminace jsou injekční lahvičky NEUPOGENU určeny pouze k jednorázovému použití. NEUPOGEN, pokud je naředěný 5% roztokem glukózy, je kompatibilní se sklem a řadou plastických materiálů včetně PVC, polyolefinu (kopolymer polypropylrnu a polyethylenu) a polypropylenu. Všechen nepoužitý přípravek nebo odpad musí být zlikvidován v souladu s místními požadavky. 7. DRŽITEL ROZHODNUTÍ O REGISTRACI Amgen Europe B.V. Minervum ZK Breda Nizozemsko 8. REGISTRAČNÍ ČÍSLO 87/267/05-C 23/24
24 9. DATUM PRVNÍ REGISTRACE/PRODLOUŽENÍ REGISTRACE / DATUM REVIZE TEXTU /24
Jeden ml injekčního nebo infuzního roztoku obsahuje 60 miliónů mezinárodních jednotek [MIU] (600 g) filgrastimum.
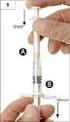
![Jeden ml injekčního nebo infuzního roztoku obsahuje 60 miliónů mezinárodních jednotek [MIU] (600 g) filgrastimum. Jeden ml injekčního nebo infuzního roztoku obsahuje 60 miliónů mezinárodních jednotek [MIU] (600 g) filgrastimum.](/thumbs/39/18709091.jpg) 1. NÁZEV PŘÍPRAVKU Biograstim 48 MIU/0,8 ml injekční nebo infúzní roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden ml injekčního nebo infuzního roztoku obsahuje 60 miliónů mezinárodních jednotek [MIU]
1. NÁZEV PŘÍPRAVKU Biograstim 48 MIU/0,8 ml injekční nebo infúzní roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden ml injekčního nebo infuzního roztoku obsahuje 60 miliónů mezinárodních jednotek [MIU]
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Tevagrastim 30 MIU/0,5 ml injekční nebo infúzní roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden ml injekčního nebo infuzního roztoku obsahuje
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Tevagrastim 30 MIU/0,5 ml injekční nebo infúzní roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden ml injekčního nebo infuzního roztoku obsahuje
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakákoli podezření
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakákoli podezření
Sp.zn.sukls55906/2014 A sp.zn.sukls123263/2013, sukls16683/2014, sukls126174/2014, sukls 95474/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Sp.zn.sukls55906/2014 A sp.zn.sukls123263/2013, sukls16683/2014, sukls126174/2014, sukls 95474/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Neupogen 48 MU/0,5 ml (0,96 mg/ml) Injekční roztok v předplněné
Sp.zn.sukls55906/2014 A sp.zn.sukls123263/2013, sukls16683/2014, sukls126174/2014, sukls 95474/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Neupogen 48 MU/0,5 ml (0,96 mg/ml) Injekční roztok v předplněné
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Neupogen 30 MU/0,5 ml (0,6 mg/ml) Neupogen 48 MU/0,5 ml (0,96 mg/ml) Injekční roztok v předplněné injekční stříkačce Neupogen 0,3mg/ ml Injekční roztok Filgrastimum
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Neupogen 30 MU/0,5 ml (0,6 mg/ml) Neupogen 48 MU/0,5 ml (0,96 mg/ml) Injekční roztok v předplněné injekční stříkačce Neupogen 0,3mg/ ml Injekční roztok Filgrastimum
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Neupogen 0,3mg/ ml Injekční roztok / koncentrát pro infuzní roztok Neupogen 30 MU/0,5 ml Neupogen 48 MU/0,5 ml injekční roztok v předplněné injekční stříkačce/
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Neupogen 0,3mg/ ml Injekční roztok / koncentrát pro infuzní roztok Neupogen 30 MU/0,5 ml Neupogen 48 MU/0,5 ml injekční roztok v předplněné injekční stříkačce/
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Neupogen 0,3mg/ ml Injekční roztok Neupogen 30 MU/0,5 ml (0,6 mg/ml) Neupogen 48 MU/0,5 ml (0,96 mg/ml) Injekční roztok v injekční lahvičce/předplněné injekční
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Neupogen 0,3mg/ ml Injekční roztok Neupogen 30 MU/0,5 ml (0,6 mg/ml) Neupogen 48 MU/0,5 ml (0,96 mg/ml) Injekční roztok v injekční lahvičce/předplněné injekční
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Sp.zn.sukls48783/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Neupogen 48 MU/0,5 ml (0,96 mg/ml) Injekční roztok v předplněné injekční stříkačce Filgrastimum 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Sp.zn.sukls48783/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Neupogen 48 MU/0,5 ml (0,96 mg/ml) Injekční roztok v předplněné injekční stříkačce Filgrastimum 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Sp.zn.sukls48783/2015 1. NÁZEV PŘÍPRAVKU Neupogen 0,3mg/ ml Injekční roztok Filgrastimum SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna injekční lahvička obsahuje filgrastimum 30
Sp.zn.sukls48783/2015 1. NÁZEV PŘÍPRAVKU Neupogen 0,3mg/ ml Injekční roztok Filgrastimum SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna injekční lahvička obsahuje filgrastimum 30
Pomocné látky s uznaným účinkem: sorbitol E420, octan sodný (viz bod 4.4).
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Neulasta 6 mg injekční roztok. 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna předplněná injekční stříkačka obsahuje 6 mg pegfilgrastimum* v 0,6 ml injekčního
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Neulasta 6 mg injekční roztok. 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna předplněná injekční stříkačka obsahuje 6 mg pegfilgrastimum* v 0,6 ml injekčního
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakákoli podezření
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakákoli podezření
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Tevagrastim 30 MIU/0,5 ml injekční nebo infúzní roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden ml injekčního nebo infuzního roztoku obsahuje
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Tevagrastim 30 MIU/0,5 ml injekční nebo infúzní roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden ml injekčního nebo infuzního roztoku obsahuje
SOUHRN ÚDAJŮ O PŘÍPRAVKU. Jedna předplněná injekční stříkačka obsahuje filgrastimum 12 miliónů jednotek (MU) (120 mikrogramů) v 0,2 ml (0,6 mg/ml).
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Nivestim 12 MU/0,2 ml injekční/infuzní roztok Nivestim 30 MU/0,5 ml injekční/infuzní roztok Nivestim 48 MU/0,5 ml injekční/infuzní roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Nivestim 12 MU/0,2 ml injekční/infuzní roztok Nivestim 30 MU/0,5 ml injekční/infuzní roztok Nivestim 48 MU/0,5 ml injekční/infuzní roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. NEUPOGEN 0,3 mg/ml (0,3 mg/ml) Injekční roztok / koncentrát pro přípravu infuzního roztoku.
 Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls117178/2010 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE NEUPOGEN 0,3 mg/ml (0,3 mg/ml) Injekční roztok / koncentrát pro přípravu infuzního roztoku
Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls117178/2010 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE NEUPOGEN 0,3 mg/ml (0,3 mg/ml) Injekční roztok / koncentrát pro přípravu infuzního roztoku
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Nivestim 12 MU/0,2 ml injekční/infuzní roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden ml injekčního nebo infuzního roztoku obsahuje filgrastimum*
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Nivestim 12 MU/0,2 ml injekční/infuzní roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden ml injekčního nebo infuzního roztoku obsahuje filgrastimum*
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Nivestim 12 MU/0,2 ml injekční/infuzní roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden ml injekčního nebo infuzního roztoku obsahuje filgrastimum*
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Nivestim 12 MU/0,2 ml injekční/infuzní roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden ml injekčního nebo infuzního roztoku obsahuje filgrastimum*
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Zarzio 30 MU/0,5 ml, injekční nebo infuzní roztok v předplněné injekční stříkačce Zarzio 48 MU/0,5 ml, injekční nebo infuzní roztok v předplněné
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Zarzio 30 MU/0,5 ml, injekční nebo infuzní roztok v předplněné injekční stříkačce Zarzio 48 MU/0,5 ml, injekční nebo infuzní roztok v předplněné
SOUHRN ÚDAJŮ O PŘÍPRAVKU. PNEUMO 23, injekční roztok v předplněné injekční stříkačce Vakcína proti pneumokokům polysacharidová
 sp.zn.sukls44523/2015 1. NÁZEV PŘÍPRAVKU SOUHRN ÚDAJŮ O PŘÍPRAVKU PNEUMO 23, injekční roztok v předplněné injekční stříkačce Vakcína proti pneumokokům polysacharidová 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
sp.zn.sukls44523/2015 1. NÁZEV PŘÍPRAVKU SOUHRN ÚDAJŮ O PŘÍPRAVKU PNEUMO 23, injekční roztok v předplněné injekční stříkačce Vakcína proti pneumokokům polysacharidová 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Příbalová informace: informace pro uživatele. Neupogen 0,3 mg/ml injekční roztok filgrastimum
 Sp.zn.sukls55906/2014 A sp.zn.sukls123263/2013, sukls16683/2014 Příbalová informace: informace pro uživatele Neupogen 0,3 mg/ml injekční roztok filgrastimum Přečtěte si pozorně celou příbalovou informaci
Sp.zn.sukls55906/2014 A sp.zn.sukls123263/2013, sukls16683/2014 Příbalová informace: informace pro uživatele Neupogen 0,3 mg/ml injekční roztok filgrastimum Přečtěte si pozorně celou příbalovou informaci
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn. sukls17735/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU GUAJACURAN 5% injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Guaifenesinum
Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn. sukls17735/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU GUAJACURAN 5% injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Guaifenesinum
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Nivestim 12 MU/0,2 ml injekční/infuzní roztok Nivestim 30 MU/0,5 ml injekční/infuzní roztok Nivestim 48 MU/0,5 ml injekční/infuzní roztok 2. KVALITATIVNÍ
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Nivestim 12 MU/0,2 ml injekční/infuzní roztok Nivestim 30 MU/0,5 ml injekční/infuzní roztok Nivestim 48 MU/0,5 ml injekční/infuzní roztok 2. KVALITATIVNÍ
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Zarzio 30 MU/0,5 ml, injekční nebo infuzní roztok v předplněné injekční stříkačce 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden ml roztoku obsahuje
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Zarzio 30 MU/0,5 ml, injekční nebo infuzní roztok v předplněné injekční stříkačce 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden ml roztoku obsahuje
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Ristempa 6 mg injekční roztok. 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna předplněná injekční stříkačka obsahuje 6 mg pegfilgrastimum* v 0,6 ml
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Ristempa 6 mg injekční roztok. 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna předplněná injekční stříkačka obsahuje 6 mg pegfilgrastimum* v 0,6 ml
VNL. Onemocnění bílé krevní řady
 VNL Onemocnění bílé krevní řady Změny leukocytů V počtu leukocytů Ve vzájemném zastoupení morfologických typů leukocytů Ve funkci leukocytů Reaktivní změny leukocytů Leukocytóza: při bakteriální infekci
VNL Onemocnění bílé krevní řady Změny leukocytů V počtu leukocytů Ve vzájemném zastoupení morfologických typů leukocytů Ve funkci leukocytů Reaktivní změny leukocytů Leukocytóza: při bakteriální infekci
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Accofil 30 MU/0,5 ml, injekční/infuzní roztok v předplněné injekční stříkačce 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden ml roztoku obsahuje 60
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Accofil 30 MU/0,5 ml, injekční/infuzní roztok v předplněné injekční stříkačce 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden ml roztoku obsahuje 60
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakákoli podezření
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakákoli podezření
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakákoli podezření
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakákoli podezření
Souhrn údajů o přípravku
 Příloha č. 2 k rozhodnutí o změně registrace sp.zn.: sukls19325/2006 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU TYPHERIX 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka vakcíny (0,5 ml) obsahuje 25
Příloha č. 2 k rozhodnutí o změně registrace sp.zn.: sukls19325/2006 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU TYPHERIX 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka vakcíny (0,5 ml) obsahuje 25
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Neulasta 6 mg injekční roztok. 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna předplněná injekční stříkačka obsahuje 6 mg pegfilgrastimum* v 0,6 ml
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Neulasta 6 mg injekční roztok. 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna předplněná injekční stříkačka obsahuje 6 mg pegfilgrastimum* v 0,6 ml
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Grastofil 30 MU/0,5 ml, injekční/infuzní roztok v předplněné injekční stříkačce 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden ml roztoku obsahuje
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Grastofil 30 MU/0,5 ml, injekční/infuzní roztok v předplněné injekční stříkačce 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden ml roztoku obsahuje
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Tevagrastim 30 MIU/0,5 ml injekční/infuzní roztok Tevagrastim 48 MIU/0,8 ml injekční/infuzní roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Tevagrastim 30 MIU/0,5 ml injekční/infuzní roztok Tevagrastim 48 MIU/0,8 ml injekční/infuzní roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden
Pomocné látky s uznaným účinkem: sorbitol E420, octan sodný (viz bod 4.4).
 1. NÁZEV PŘÍPRAVKU Neulasta 6 mg injekční roztok. 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna předplněná injekční stříkačka obsahuje 6 mg pegfilgrastimum* v 0,6 ml injekčního roztoku. Koncentrace je
1. NÁZEV PŘÍPRAVKU Neulasta 6 mg injekční roztok. 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna předplněná injekční stříkačka obsahuje 6 mg pegfilgrastimum* v 0,6 ml injekčního roztoku. Koncentrace je
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU Borgal 200/40 mg/ml injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 ml obsahuje: Léčivé látky: Sulfadoxinum 200 mg Trimethoprimum
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU Borgal 200/40 mg/ml injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 ml obsahuje: Léčivé látky: Sulfadoxinum 200 mg Trimethoprimum
Příbalová informace: informace pro uživatele. Neupogen 0,3 mg/ml injekční roztok /koncentrát pro infuzní roztok v injekční lahvičce.
 Příbalová informace: informace pro uživatele Neupogen 0,3 mg/ml injekční roztok /koncentrát pro infuzní roztok v injekční lahvičce. Neupogen 30 MU/0,5 ml (0,6 mg/ml) Neupogen 48 MU/0,5 ml (0,96 mg/ml)
Příbalová informace: informace pro uživatele Neupogen 0,3 mg/ml injekční roztok /koncentrát pro infuzní roztok v injekční lahvičce. Neupogen 30 MU/0,5 ml (0,6 mg/ml) Neupogen 48 MU/0,5 ml (0,96 mg/ml)
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č.3 ke sdělení sp.zn.sukls44100/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Fucithalmic oční kapky, suspenze 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Acidum fusidicum hemihydricum 10 mg v 1
Příloha č.3 ke sdělení sp.zn.sukls44100/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Fucithalmic oční kapky, suspenze 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Acidum fusidicum hemihydricum 10 mg v 1
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Filgrastim HEXAL 30 MU/0,5 ml injekční/infuzní roztok v předplněné injekční stříkačce Filgrastim HEXAL 48 MU/0,5 ml injekční/infuzní roztok v předplněné
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Filgrastim HEXAL 30 MU/0,5 ml injekční/infuzní roztok v předplněné injekční stříkačce Filgrastim HEXAL 48 MU/0,5 ml injekční/infuzní roztok v předplněné
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Zarzio 30 MU/0,5 ml injekční/infuzní roztok v předplněné injekční stříkačce Zarzio 48 MU/0,5 ml injekční/infuzní roztok v předplněné injekční stříkačce
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Zarzio 30 MU/0,5 ml injekční/infuzní roztok v předplněné injekční stříkačce Zarzio 48 MU/0,5 ml injekční/infuzní roztok v předplněné injekční stříkačce
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 3 k rozhodnutí o registraci sp.zn. sukls187009/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU ARTAXIN 625 mg, tvrdé tobolky 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tobolka obsahuje glucosaminum
Příloha č. 3 k rozhodnutí o registraci sp.zn. sukls187009/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU ARTAXIN 625 mg, tvrdé tobolky 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tobolka obsahuje glucosaminum
Souhrn údajů o přípravku
 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU Luivac 2. KVALITATIVNÍ I KVANTITATIVNÍ SLOŽENÍ Léčivá látka: 1 tableta obsahuje 3 mg Lysatum bacteriale mixtum ex min. 1x10 9 bakterií z každého následujícího
Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU Luivac 2. KVALITATIVNÍ I KVANTITATIVNÍ SLOŽENÍ Léčivá látka: 1 tableta obsahuje 3 mg Lysatum bacteriale mixtum ex min. 1x10 9 bakterií z každého následujícího
Dospělí: Jeden čípek ráno, večer a po každém vyprázdnění střev. Zavést do rekta zaobleným koncem.
 sp.zn. sukls186765/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PREPARATION H čípky 23 mg / 69 mg 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivé látky: Faecis extractum fluidum 1,00 % hmot., t.j. 23
sp.zn. sukls186765/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PREPARATION H čípky 23 mg / 69 mg 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivé látky: Faecis extractum fluidum 1,00 % hmot., t.j. 23
Souhrn údajů o přípravku. Typhoidi capsulae Vi polysaccharidum purificatum (stirpe Ty 2)
 sp. zn. sukls133524/2015 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU Typherix, injekční roztok v předplněné injekční stříkačce Polysacharidová vakcína proti tyfu 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
sp. zn. sukls133524/2015 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU Typherix, injekční roztok v předplněné injekční stříkačce Polysacharidová vakcína proti tyfu 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Příbalová informace: informace pro uživatele
 Příbalová informace: informace pro uživatele Neupogen 30 MU/0,5 ml (0,6 mg/ml) Neupogen 48 MU/0,5 ml (0,96 mg/ml) injekční roztok v předplněné injekční stříkačce Neupogen 0,3 mg/ml injekční roztok filgrastimum
Příbalová informace: informace pro uživatele Neupogen 30 MU/0,5 ml (0,6 mg/ml) Neupogen 48 MU/0,5 ml (0,96 mg/ml) injekční roztok v předplněné injekční stříkačce Neupogen 0,3 mg/ml injekční roztok filgrastimum
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 sp.zn. sukls221052/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Fucithalmic oční kapky, suspenze 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Acidum fusidicum hemihydricum 10 mg v 1 g očních kapek Pomocná
sp.zn. sukls221052/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Fucithalmic oční kapky, suspenze 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Acidum fusidicum hemihydricum 10 mg v 1 g očních kapek Pomocná
Příloha č. 3 k rozhodnutí o převodu registrace sp.zn. sukls62363/2011 a sukls62355/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 3 k rozhodnutí o převodu registrace sp.zn. sukls62363/2011 a sukls62355/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Procto-Glyvenol 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Čípky:Tribenosidum
Příloha č. 3 k rozhodnutí o převodu registrace sp.zn. sukls62363/2011 a sukls62355/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Procto-Glyvenol 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Čípky:Tribenosidum
Příloha č. 3 k rozhodnutí o převodu registrace sp.zn. sukls8465/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 3 k rozhodnutí o převodu registrace sp.zn. sukls8465/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. Název přípravku E-Z-HD 2. Kvalitativní a kvantitativní složení Léčivá látka: Barii sulfas (síran barnatý)
Příloha č. 3 k rozhodnutí o převodu registrace sp.zn. sukls8465/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. Název přípravku E-Z-HD 2. Kvalitativní a kvantitativní složení Léčivá látka: Barii sulfas (síran barnatý)
SOUHRN ÚDAJŮ O PŘÍPRAVKU. 100 ml roztoku obsahuje Hederae helicis folii extractum siccum (4 8 : 1), extrahováno ethanolem 30 % (m/m).
 Sp.zn.sukls15900/2016 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Mucoplant břečťanový sirup proti kašli sirup 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 100 ml roztoku obsahuje Hederae helicis folii extractum
Sp.zn.sukls15900/2016 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Mucoplant břečťanový sirup proti kašli sirup 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 100 ml roztoku obsahuje Hederae helicis folii extractum
Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn.: sukls20204/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn.: sukls20204/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU TYPHIM Vi, injekční roztok v předplněné injekční stříkačce Polysacharidová vakcína
Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn.: sukls20204/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU TYPHIM Vi, injekční roztok v předplněné injekční stříkačce Polysacharidová vakcína
Popis přípravku : Prášek: bílý lyofilizát. Rozpouštědlo: čirá bezbarvá tekutina
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU MENINGOCOCCAL POLYSACCHARIDE A+C VACCINE Prášek pro přípravu injekční suspenze s rozpouštědlem 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka (0,5 ml) rozpuštěné
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU MENINGOCOCCAL POLYSACCHARIDE A+C VACCINE Prášek pro přípravu injekční suspenze s rozpouštědlem 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka (0,5 ml) rozpuštěné
SOUHRN ÚDAJŮ O PŘÍPRAVKU. 400 mg + 40 mg. čípky PROCTO-GLYVENOL. 50 mg/g + 20 mg/g. rektální krém
 sp.zn. sukls74884/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PROCTO-GLYVENOL 400 mg + 40 mg čípky PROCTO-GLYVENOL 50 mg/g + 20 mg/g rektální krém 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Čípky: Jeden
sp.zn. sukls74884/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PROCTO-GLYVENOL 400 mg + 40 mg čípky PROCTO-GLYVENOL 50 mg/g + 20 mg/g rektální krém 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Čípky: Jeden
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 2 k rozhodnutí o změně registrace sp. zn. sukls79120/2012 1. NÁZEV PŘÍPRAVKU NIZORAL krém SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Ketoconazolum 20,0 mg v 1 g krému Pomocné
Příloha č. 2 k rozhodnutí o změně registrace sp. zn. sukls79120/2012 1. NÁZEV PŘÍPRAVKU NIZORAL krém SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Ketoconazolum 20,0 mg v 1 g krému Pomocné
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Voda na injekci Viaflo 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Každé balení obsahuje 100% w/v aqua pro iniectione. 3. LÉKOVÁ FORMA Rozpouštědlo pro parenterální
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Voda na injekci Viaflo 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Každé balení obsahuje 100% w/v aqua pro iniectione. 3. LÉKOVÁ FORMA Rozpouštědlo pro parenterální
Odběr krvetvorných buněk z periferní krve: příprava, průběh a komplikace
 Odběr krvetvorných buněk z periferní krve: příprava, průběh a komplikace Helena Švábová, Andrea Žmijáková Interní hematologická a onkologická klinika FN Brno Separační středisko je součástí Interní hematologické
Odběr krvetvorných buněk z periferní krve: příprava, průběh a komplikace Helena Švábová, Andrea Žmijáková Interní hematologická a onkologická klinika FN Brno Separační středisko je součástí Interní hematologické
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Pelmeg 6 mg injekční roztok v předplněné injekční stříkačce. 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna předplněná injekční stříkačka obsahuje pegfilgrastimum*
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Pelmeg 6 mg injekční roztok v předplněné injekční stříkačce. 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna předplněná injekční stříkačka obsahuje pegfilgrastimum*
Příloha č. 2 k rozhodnutí o změně registrace sp.zn. sukls118033/2010
 Příloha č. 2 k rozhodnutí o změně registrace sp.zn. sukls118033/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Cardioxane prášek pro přípravu infuzního roztoku. 2. KVALITATIVNÍ A KVANTITATIVNÍ
Příloha č. 2 k rozhodnutí o změně registrace sp.zn. sukls118033/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Cardioxane prášek pro přípravu infuzního roztoku. 2. KVALITATIVNÍ A KVANTITATIVNÍ
Fludeoxythymidine ( 18 F) 1 8 GBq k datu a hodině kalibrace voda na injekci, chlorid sodný 9 mg/ml
 Příbalová informace Informace pro použití, čtěte pozorně! Název přípravku 3 -[ 18 F]FLT, INJ Kvalitativní i kvantitativní složení 1 lahvička obsahuje: Léčivá látka: Pomocné látky: Léková forma Injekční
Příbalová informace Informace pro použití, čtěte pozorně! Název přípravku 3 -[ 18 F]FLT, INJ Kvalitativní i kvantitativní složení 1 lahvička obsahuje: Léčivá látka: Pomocné látky: Léková forma Injekční
Přecitlivělost na léčivé látky nebo na kteroukoliv z pomocných látek uvedených v bodě 6.1.
 sp.zn.: sukls50035/2010, sukls106419/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PREPARATION H rektální mast 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivé látky: Faecis extractum fluidum 1,00 g Selachiorum
sp.zn.: sukls50035/2010, sukls106419/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PREPARATION H rektální mast 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivé látky: Faecis extractum fluidum 1,00 g Selachiorum
sp.zn.: sukls7967/2011
 sp.zn.: sukls7967/2011 Souhrn údajů o přípravku. 1. NÁZEV PŘÍPRAVKU sáčky 2. SLOŽENÍ KVALITATIVNÍ A KVANTITATIVNÍ Jedna tobolka obsahuje léčivou látku: Lysatum bacteriale OM 85 cryodesicatum, odpovídá
sp.zn.: sukls7967/2011 Souhrn údajů o přípravku. 1. NÁZEV PŘÍPRAVKU sáčky 2. SLOŽENÍ KVALITATIVNÍ A KVANTITATIVNÍ Jedna tobolka obsahuje léčivou látku: Lysatum bacteriale OM 85 cryodesicatum, odpovídá
Příloha č. 1 k rozhodnutí o změně registrace sp.zn.: sukls135179/2011
 Příloha č. 1 k rozhodnutí o změně registrace sp.zn.: sukls135179/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU NIZORAL krém 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Ketoconazolum 20,0 mg v 1 g krému
Příloha č. 1 k rozhodnutí o změně registrace sp.zn.: sukls135179/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU NIZORAL krém 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Ketoconazolum 20,0 mg v 1 g krému
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn.:sukls59594/25009, a příloha k sp.zn.: sukls230271/2012 1. NÁZEV PŘÍPRAVKU SOUHRN ÚDAJŮ O PŘÍPRAVKU MENINGOCOCCAL POLYSACCHARIDE A+C VACCINE Prášek
Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn.:sukls59594/25009, a příloha k sp.zn.: sukls230271/2012 1. NÁZEV PŘÍPRAVKU SOUHRN ÚDAJŮ O PŘÍPRAVKU MENINGOCOCCAL POLYSACCHARIDE A+C VACCINE Prášek
Příloha č. 2 k rozhodnutí o změně registrace sp.zn.sukls124916/2011. Souhrn údajů o přípravku
 Příloha č. 2 k rozhodnutí o změně registrace sp.zn.sukls124916/2011 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU Typherix 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka vakcíny (0,5 ml) obsahuje 25
Příloha č. 2 k rozhodnutí o změně registrace sp.zn.sukls124916/2011 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU Typherix 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka vakcíny (0,5 ml) obsahuje 25
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU. Přípavek již není registrován
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Neupopeg 6 mg injekční roztok. 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna předplněná injekční stříkačka obsahuje 6 mg pegfilgrastimum* v 0,6 ml
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Neupopeg 6 mg injekční roztok. 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna předplněná injekční stříkačka obsahuje 6 mg pegfilgrastimum* v 0,6 ml
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 3 k rozhodnutí o registraci sp. zn. sukls115710/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU GLYPRESSIN 1 mg injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna ampule s 8,5 ml
Příloha č. 3 k rozhodnutí o registraci sp. zn. sukls115710/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU GLYPRESSIN 1 mg injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna ampule s 8,5 ml
Příloha I. Vědecké závěry a zdůvodnění změny v registraci
 Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy/aktualizovaných zpráv o bezpečnosti (PSUR)
Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy/aktualizovaných zpráv o bezpečnosti (PSUR)
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 2 k rozhodnutí o změně registrace sp. zn. sukls25846/2010 a sukls25848/2010 a příloha ke sp. zn. sukls156917/2010 a sukls157010/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 NÁZEV PŘÍPRAVKU Pentasa Sachet
Příloha č. 2 k rozhodnutí o změně registrace sp. zn. sukls25846/2010 a sukls25848/2010 a příloha ke sp. zn. sukls156917/2010 a sukls157010/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 NÁZEV PŘÍPRAVKU Pentasa Sachet
3. LÉKOVÁ FORMA Injekční suspenze vpředplněné injekční stříkačce; bezbarvá průhledná tekutina, v jednodávkových inj. stříkačkách (sklo, typu I).
 Příloha č.2 k rozhodnutí o změně registrace sp. zn. sukls97832/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Influvac Injekční suspenze (vakcína proti chřipce, povrchový antigen, inaktivovaná) Sezóna
Příloha č.2 k rozhodnutí o změně registrace sp. zn. sukls97832/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Influvac Injekční suspenze (vakcína proti chřipce, povrchový antigen, inaktivovaná) Sezóna
Injekční roztok. Tmavě hnědý, neprůhledný roztok s ph 5,0 7,0 a s přibližnou osmolaritou 400 mosm/l.
 sp.zn. sukls57833/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakákoli
sp.zn. sukls57833/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakákoli
Souhrn údajů o přípravku
 Sp.zn. sukls120620/2013 1. NÁZEV PŘÍPRAVKU Souhrn údajů o přípravku Influvac Injekční suspenze (vakcína proti chřipce, povrchový antigen, inaktivovaná) Sezóna 2013/2014 2. KVALITATIVNÍ A KVANTITATIVNÍ
Sp.zn. sukls120620/2013 1. NÁZEV PŘÍPRAVKU Souhrn údajů o přípravku Influvac Injekční suspenze (vakcína proti chřipce, povrchový antigen, inaktivovaná) Sezóna 2013/2014 2. KVALITATIVNÍ A KVANTITATIVNÍ
Gynekologie: Metroragie, primární menoragie nebo menoragie související s nitroděložním tělískem bez prokazatelné organické příčiny.
 Sp.zn.sukls81671/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Cyclonamine 500 mg Tvrdé tobolky 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tobolka obsahuje etamsylatum 500 mg. Léčivý přípravek obsahuje
Sp.zn.sukls81671/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Cyclonamine 500 mg Tvrdé tobolky 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tobolka obsahuje etamsylatum 500 mg. Léčivý přípravek obsahuje
Příloha I. Vědecké závěry a zdůvodnění změny v registraci
 Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy (PSUR) pro bendamustin-hydrochlorid byly
Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy (PSUR) pro bendamustin-hydrochlorid byly
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Neulasta 6 mg injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna předplněná injekční stříkačka obsahuje pegfilgrastimum* 6 mg v 0,6 ml
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Neulasta 6 mg injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna předplněná injekční stříkačka obsahuje pegfilgrastimum* 6 mg v 0,6 ml
Souhrn údajů o přípravku
 sp. zn. sukls208148/2014 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU Influvac Injekční suspenze (vakcína proti chřipce, povrchový antigen, inaktivovaná) 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Povrchové
sp. zn. sukls208148/2014 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU Influvac Injekční suspenze (vakcína proti chřipce, povrchový antigen, inaktivovaná) 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Povrchové
2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 g masti obsahuje calcitriolum 0,003 mg (3 mikrogramy). Úplný seznam pomocných látek viz bod 6.1.
 Sp. zn. sukls155368/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Silkis mast 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 g masti obsahuje calcitriolum 0,003 mg (3 mikrogramy). Úplný seznam pomocných
Sp. zn. sukls155368/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Silkis mast 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 g masti obsahuje calcitriolum 0,003 mg (3 mikrogramy). Úplný seznam pomocných
PŘÍLOHA III ÚPRAVY SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE. Tyto změny k SPC a příbalové informace jsou platné v den Rozhodnutí Komise
 PŘÍLOHA III ÚPRAVY SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE Tyto změny k SPC a příbalové informace jsou platné v den Rozhodnutí Komise Po Rozhodnutí Komise aktualizuje národní kompetentní autorita
PŘÍLOHA III ÚPRAVY SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE Tyto změny k SPC a příbalové informace jsou platné v den Rozhodnutí Komise Po Rozhodnutí Komise aktualizuje národní kompetentní autorita
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Glucosum monohydricum
 sp.zn.sukls126426/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Glukóza 5 Braun infuzní roztok Glucosum monohydricum Přečtěte si pozorně celou příbalovou informaci dříve, než Vám tento přípravek bude
sp.zn.sukls126426/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Glukóza 5 Braun infuzní roztok Glucosum monohydricum Přečtěte si pozorně celou příbalovou informaci dříve, než Vám tento přípravek bude
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 1. NÁZEV PŘÍPRAVKU TETAVAX Injekční suspenze Vakcína proti tetanu (adsorbovaná) SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivá látka: 1 dávka (0,5 ml) obsahuje Tetani anatoxinum
1. NÁZEV PŘÍPRAVKU TETAVAX Injekční suspenze Vakcína proti tetanu (adsorbovaná) SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivá látka: 1 dávka (0,5 ml) obsahuje Tetani anatoxinum
Urychlení úpravy krvetvorby poškozené cytostatickou terapií (5-fluorouracil a cisplatina) p.o. aplikací IMUNORu
 Urychlení úpravy krvetvorby poškozené cytostatickou terapií (5-fluorouracil a cisplatina) p.o. aplikací IMUNORu Úvod Myelosuprese (poškození krvetvorby) patří mezi nejčastější vedlejší účinky chemoterapie.
Urychlení úpravy krvetvorby poškozené cytostatickou terapií (5-fluorouracil a cisplatina) p.o. aplikací IMUNORu Úvod Myelosuprese (poškození krvetvorby) patří mezi nejčastější vedlejší účinky chemoterapie.
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha k sp. zn. sukls224939/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Molaxole prášek pro přípravu perorálního roztoku 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden sáček obsahuje následující
Příloha k sp. zn. sukls224939/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Molaxole prášek pro přípravu perorálního roztoku 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden sáček obsahuje následující
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Neulasta 6 mg injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna předplněná injekční stříkačka obsahuje pegfilgrastimum* 6 mg v 0,6 ml
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Neulasta 6 mg injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna předplněná injekční stříkačka obsahuje pegfilgrastimum* 6 mg v 0,6 ml
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU. Metacam 5 mg/ml injekční roztok pro skot a prasata
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU Metacam 5 mg/ml injekční roztok pro skot a prasata 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden ml obsahuje: Léčivá látka: Meloxicamum
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU Metacam 5 mg/ml injekční roztok pro skot a prasata 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden ml obsahuje: Léčivá látka: Meloxicamum
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU Feligen CRP Lyofilizát pro přípravu injekční suspenze s rozpouštědlem 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Lyofilizovaná složka Léčivé
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU Feligen CRP Lyofilizát pro přípravu injekční suspenze s rozpouštědlem 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Lyofilizovaná složka Léčivé
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 1. NÁZEV PŘÍPRAVKU SOUHRN ÚDAJŮ O PŘÍPRAVKU IMOVAX POLIO, injekční suspenze v předplněné injekční stříkačce Vakcína proti poliomyelitidě (inaktivovaná) 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 dávka (0,5
1. NÁZEV PŘÍPRAVKU SOUHRN ÚDAJŮ O PŘÍPRAVKU IMOVAX POLIO, injekční suspenze v předplněné injekční stříkačce Vakcína proti poliomyelitidě (inaktivovaná) 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 dávka (0,5
s energií 172 kev (91 %) a 246 kev (94 %). Vnitřní konverzí vzniká záření rentgenové s energií 23 kev a 26 kev.
 sp.zn. sukls101319/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Indium (In111) Chloride 370 MBq/ml, radionuklidový prekurzor, roztok 2. KVALITATIVNÍ I KVANTITATIVNÍ SLOŽENÍ Obsah lahvičky k datu a
sp.zn. sukls101319/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Indium (In111) Chloride 370 MBq/ml, radionuklidový prekurzor, roztok 2. KVALITATIVNÍ I KVANTITATIVNÍ SLOŽENÍ Obsah lahvičky k datu a
Praxbind doporučení pro podávání (SPC)
 Praxbind doporučení pro podávání (SPC) Idarucizumab je indikován pro použití v případech, kde je zapotřebí rychlá antagonizace antagonizačních účinků dabigatranu Idarucizumab je specifický přípravek pro
Praxbind doporučení pro podávání (SPC) Idarucizumab je indikován pro použití v případech, kde je zapotřebí rychlá antagonizace antagonizačních účinků dabigatranu Idarucizumab je specifický přípravek pro
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 sp.zn. sukls71941/2012 a sukls103573/2013, sukls103568/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Fucidin Mast 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivá látka: Natrii fusidas 20,0 mg v 1 g masti.
sp.zn. sukls71941/2012 a sukls103573/2013, sukls103568/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Fucidin Mast 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivá látka: Natrii fusidas 20,0 mg v 1 g masti.
BIOVISC ORTHO M. Sterilní viskoelastický roztok kyseliny hyaluronové k intraartikulární injekci.
 Česky BIOVISC ORTHO M Sterilní viskoelastický roztok kyseliny hyaluronové k intraartikulární injekci. NÁVOD K POUŽITÍ SLOŽENÍ Jeden ml obsahuje: Kyselina hyaluronová Mannitol 20 mg 5 mg Fosfátem pufrovaný
Česky BIOVISC ORTHO M Sterilní viskoelastický roztok kyseliny hyaluronové k intraartikulární injekci. NÁVOD K POUŽITÍ SLOŽENÍ Jeden ml obsahuje: Kyselina hyaluronová Mannitol 20 mg 5 mg Fosfátem pufrovaný
v kombinaci s dexamethasonem u dospělých, jejichž onemocnění bylo alespoň jednou v minulosti léčeno.
 EMA/113870/2017 EMEA/H/C/000717 Souhrn zprávy EPAR určený pro veřejnost lenalidomidum Tento dokument je souhrnem Evropské veřejné zprávy o hodnocení (European Public Assessment Report, EPAR) pro přípravek.
EMA/113870/2017 EMEA/H/C/000717 Souhrn zprávy EPAR určený pro veřejnost lenalidomidum Tento dokument je souhrnem Evropské veřejné zprávy o hodnocení (European Public Assessment Report, EPAR) pro přípravek.
AJATIN PROFARMA tinktura s mechanickým rozprašovačem kožní roztok
 www.lekarna-madona.cz zpět na stránku produktu zpět na obdobná léčiva SOUHRN ÚDAJŮ O PŘÍPRAVKU 1.NÁZEV PŘÍPRAVKU: AJATIN PROFARMA tinktura s mechanickým rozprašovačem kožní roztok 2.KVALITATIVNÍ A KVANTITATIVNÍ
www.lekarna-madona.cz zpět na stránku produktu zpět na obdobná léčiva SOUHRN ÚDAJŮ O PŘÍPRAVKU 1.NÁZEV PŘÍPRAVKU: AJATIN PROFARMA tinktura s mechanickým rozprašovačem kožní roztok 2.KVALITATIVNÍ A KVANTITATIVNÍ
NeuroBloc. botulinový toxin typu B injekční roztok, U/ml
 NeuroBloc botulinový toxin typu B injekční roztok, 5 000 U/ml Důležité bezpečnostní informace určené lékařům Účelem této příručky je poskytnout lékařům, kteří jsou oprávněni předepisovat a aplikovat přípravek
NeuroBloc botulinový toxin typu B injekční roztok, 5 000 U/ml Důležité bezpečnostní informace určené lékařům Účelem této příručky je poskytnout lékařům, kteří jsou oprávněni předepisovat a aplikovat přípravek
Pomocné látky se známým účinkem: prostý sirup 67%, usušená tekutá glukosa.
 sp.zn. sukls24303/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Strepsils Pomeranč s vitaminem C pastilky 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna pastilka obsahuje amylmetacresolum 0,6 mg, alcohol
sp.zn. sukls24303/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Strepsils Pomeranč s vitaminem C pastilky 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna pastilka obsahuje amylmetacresolum 0,6 mg, alcohol
Nové léčebné možnosti v léčbě mnohočetného myelomu GROUP. Roman Hájek 3.9.2005. Lednice
 Nové léčebné možnosti v léčbě mnohočetného myelomu CZECH CMG M Y E L O M A GROUP ČESKÁ MYELOMOVÁ SKUPINA ČESKÁ MYELOMOVÁ SKUPINA CZECH CMG M Y E L O M A NADAČNÍ FOND GROUP Roman Hájek 3.9.2005 Lednice
Nové léčebné možnosti v léčbě mnohočetného myelomu CZECH CMG M Y E L O M A GROUP ČESKÁ MYELOMOVÁ SKUPINA ČESKÁ MYELOMOVÁ SKUPINA CZECH CMG M Y E L O M A NADAČNÍ FOND GROUP Roman Hájek 3.9.2005 Lednice
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Sp.zn. sukls277451/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Azelastin COMOD 0,5 mg/ml oční kapky, roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Azelastini hydrochloridum 0,05 % (0,50 mg/ml) Jedna
Sp.zn. sukls277451/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Azelastin COMOD 0,5 mg/ml oční kapky, roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Azelastini hydrochloridum 0,05 % (0,50 mg/ml) Jedna
1 dávka - 0,5 ml obsahuje: Typhoidi capsulae Vi polysaccharidum purificatum (stirpe Ty2)..25 mikrogramů
 sp.zn. sukls120097/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU TYPHIM Vi, injekční roztok v předplněné injekční stříkačce Polysacharidová vakcína proti břišnímu tyfu 2. KVALITATIVNÍ A KVANTITATIVNÍ
sp.zn. sukls120097/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU TYPHIM Vi, injekční roztok v předplněné injekční stříkačce Polysacharidová vakcína proti břišnímu tyfu 2. KVALITATIVNÍ A KVANTITATIVNÍ
Infuzní roztok. Roztok je čirý, bezbarvý až slabě narůžověle-oranžový. Vnímání zabarvení se může lišit. Teoretická osmolarita: 305 mosm/l ph: 4,5 5,5
 Sp.zn.sukls176520/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Paracetamol B. Braun 10 mg/ml infuzní roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden ml infuzního roztoku obsahuje paracetamolum
Sp.zn.sukls176520/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Paracetamol B. Braun 10 mg/ml infuzní roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden ml infuzního roztoku obsahuje paracetamolum
Příloha II. Vědecké závěry a zdůvodnění změny v registraci
 Příloha II Vědecké závěry a zdůvodnění změny v registraci 6 Vědecké závěry Celkové shrnutí vědeckého hodnocení přípravku Cymevene i.v. a souvisejících názvů (viz příloha I) Evropská komise jménem všech
Příloha II Vědecké závěry a zdůvodnění změny v registraci 6 Vědecké závěry Celkové shrnutí vědeckého hodnocení přípravku Cymevene i.v. a souvisejících názvů (viz příloha I) Evropská komise jménem všech
Příloha III. Úpravy odpovídajících bodů souhrnu údajů o přípravku a příbalové informace
 Příloha III Úpravy odpovídajících bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Úpravy v souhrnu údajů o přípravku a příbalové informaci mohou být dále aktualizovány příslušnými vnitrostátními
Příloha III Úpravy odpovídajících bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Úpravy v souhrnu údajů o přípravku a příbalové informaci mohou být dále aktualizovány příslušnými vnitrostátními
Ibandronic Acid Accord 2 mg koncentrát pro infuzní roztok Ibandronic Acid Accord 6 mg koncentrát pro infuzní roztok acidum ibandronicum
 Ibandronic Acid Accord 2 mg koncentrát pro infuzní roztok acidum ibandronicum Máte- Pokud se kterýkoli z než V 1. Ibandronic Acid Accord a k 2. Ibandronic Acid Accord používat 3. Ibandronic Acid Accord
Ibandronic Acid Accord 2 mg koncentrát pro infuzní roztok acidum ibandronicum Máte- Pokud se kterýkoli z než V 1. Ibandronic Acid Accord a k 2. Ibandronic Acid Accord používat 3. Ibandronic Acid Accord
Příloha č. 2 k rozhodnutí o změně registrace sp.zn. sukls30063/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU. Chondrostad 1500 mg
 Příloha č. 2 k rozhodnutí o změně registrace sp.zn. sukls30063/2010 1. NÁZEV PŘÍPRAVKU SOUHRN ÚDAJŮ O PŘÍPRAVKU Chondrostad 1500 mg 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden sáček obsahuje 1884,0 mg
Příloha č. 2 k rozhodnutí o změně registrace sp.zn. sukls30063/2010 1. NÁZEV PŘÍPRAVKU SOUHRN ÚDAJŮ O PŘÍPRAVKU Chondrostad 1500 mg 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden sáček obsahuje 1884,0 mg
sp.zn.: sukls132182/2010 a sp.zn.: sukls82396/2014
 sp.zn.: sukls132182/2010 a sp.zn.: sukls82396/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU MYTELASE tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Ambenonii chloridum 10 mg v 1 tabletě. Pomocné látky
sp.zn.: sukls132182/2010 a sp.zn.: sukls82396/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU MYTELASE tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Ambenonii chloridum 10 mg v 1 tabletě. Pomocné látky
Příloha č. 2 k rozhodnutí o registraci sp.zn. sukls178251/2009
 Příloha č. 2 k rozhodnutí o registraci sp.zn. sukls178251/2009 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Topotecan Mylan 1 mg/ml koncentrát pro přípravu infuzního roztoku topotecanum Přečtěte si pozorně
Příloha č. 2 k rozhodnutí o registraci sp.zn. sukls178251/2009 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Topotecan Mylan 1 mg/ml koncentrát pro přípravu infuzního roztoku topotecanum Přečtěte si pozorně
záření gama s energií 172 kev (91 %) a 246 kev (94 %). Vnitřní konverzí vzniká záření rentgenové s energií 23 kev a 26 kev.
 sp.zn. sukls50264/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Indium (In111) Chloride 370 MBq/ml, radionuklidový prekurzor, roztok 2. KVALITATIVNÍ I KVANTITATIVNÍ SLOŽENÍ Obsah lahvičky k datu a hodině
sp.zn. sukls50264/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Indium (In111) Chloride 370 MBq/ml, radionuklidový prekurzor, roztok 2. KVALITATIVNÍ I KVANTITATIVNÍ SLOŽENÍ Obsah lahvičky k datu a hodině
