VETERINÁRNÍ A FARMACEUTICKÁ UNIVERZITA FAKULTA FARMACEUTICKÁ ÚSTAV CHEMICKÝCH LÉČIV. Závěrečná zpráva. řešení projektu IVA číslo 2014FaF/3150/064
|
|
|
- Oldřich Blažek
- před 8 lety
- Počet zobrazení:
Transkript
1 VETERINÁRNÍ A FARMACEUTICKÁ UNIVERZITA FAKULTA FARMACEUTICKÁ ÚSTAV CHEMICKÝCH LÉČIV Závěrečná zpráva řešení projektu IVA číslo 2014FaF/3150/064 Zavedení fotochemických úloh do cvičení z organické chemie Řešitel: Jan tevřel Spoluřešitelé: Michal Fedor Pavel Bobáľ Brno
2 1. Fotochemické úlohy 2.1. Úlohy zaměřené na luminiscenční reakce Příprava DNP a pozorování chemiluminiscence Část 1. Příprava DNP N N 2 2 N 2 H Me 2 + Cl Cl NEt 3 2 N N 2 2 N PRACVNÍ PSTUP: Ve 25ml zábrusové baňce s magnetickým míchadlem rozpustíme 3,55 mmol 2,4-dinitrofenolu (MW 184,11) v 10 ml suchého toluenu. Baňku uzavřeme gumovým septem a injekční stříkačkou přidáme 3,55 mmol suchého triethylaminu (MW 101,19; d 0,73) a směs vložíme do ledové vody. Až se obsah baňky vychladí, injekční stříkačkou přilijeme 1,78 mmol oxalyl chloridu (MW 126,93; d 1,48). Po 5 min baňku vytáhneme z ledové lázně a reakci necháme jěště 60 min míchat a postupně ohřát na laboratorní teplotu. Po skončení požadované doby se obsah baňky vlije na fritu a odsaje. dpojíme vakuum a ke zbytku na fritě přidáme 10 ml methanolu a ještě jednou odsajeme, abychom se zbavili triethylammonium-chloridu, filtrační koláč necháme vysušit procházejícím vzduchem a produkt zvážíme a vhodným způsobem charakterizujeme. Část 2. Pozorování chemiluminiscence PRACVNÍ PSTUP: Z předchozí reakce získaný bis(2,4-dinitrofenyl)-oxalát společně s 300 mg octanu sodného a 3 mg 9,10-bis(fenylethynyl)anthracenu protřepeme v lahvičce se šroubovacím uzávěrem s 10 ml diethyl-ftalátu. Pro iniciaci luminiscenční reakce nakonec přidáme 29,37 mmol 30% H 2 2 (MW 34,02; d 1,11) a ve tmavé místnosti směs intenzivně protřepeme. Luminiscence vydrží několik hodin. 2
3 Příprava fluoresceinu a pozorování fluorescence Část 1. Příprava fluoresceinu + H 2 H H 2 S 4 H CH PRACVNÍ PSTUP: lejovou lázeň předehřejeme na C (je nesmírně důležité udržet teplotu v tomto rozsahu, jinak dojde k degradaci produktu). Do větší zkumavky (asi mm) vsypeme 2,72 mmol resorcinolu (MW 110,10) a 1,35 mmol jemně rozetřeného ftalanhydridu (MW 148,10). Do této směsi pomalu přikapeme 6 kapek 2M roztoku H 2 S 4 (98% H 2 S 4 ; MW 98,08; d 1,84) (ne více), promícháme skleněnou tyčinkou a umístíme do lázně, kde směs necháme 30 min zahřívat. Po této době zkumavku odstavíme a necháme 5 min zchladnout. Do zkumavky přidáme 10 ml acetonu a magnetické míchadélko a nad magnetickou míchačkou ponecháme 5 10 min míchat, až se vytvoří žlutý roztok fluoresceinu. Pokud uvedené množství acetonu nebude stačit, lze přidat dalších 5 ml atd. až do celkového množství max. 25 ml. Aceton odpaříme buď za varu v 50ml kádince nebo na rotační odparce a zůstane nám oranžový zbytek. Ten opětovně rozpustíme v 30 ml diethyletheru s 1,5 ml vody (bez vody se fluorescein nerozpustí). Znovu vložíme míchadlo a necháme několik minut rozpouštět, následně roztok přeneseme do dělící nálevky, přidáme 15 ml vody a 10 ml nasyceného roztoku NaCl, etherickou vrstvu vysušíme bezvodým Na 2 S 4, po 5 min sušidlo zfiltrujeme a filtrát odpaříme. Získáme oranžový produkt, který zvážíme a vhodným způsobem charakterizujeme. Část 2. Pozorování fluorescence PRACVNÍ PSTUP: V baňce rozpustíme 5 mg produktu v 50 ml 0,1M NaH (MW 40,00) a umístíme ji na filtrační papír na laboratorní stůl u okna, pozorujeme barvu roztoku tak, že ho pozorujeme v úhlu 180 a 90 vzhledem k oknu a nakonec ve tmavé místnosti, kdy na roztok svítíme dlouhovlnným ultrafialovým zářením, výsledky pozorování si zapíšeme a vysvětlíme je do protokolu. 3
4 2.2. Úlohy zaměřené na fotochromismus Příprava 2-(2,4-dinitrobenzyl)pyridinu a pozorování fotochromismu Část 1. Příprava 2-(2,4-dinitrobenzyl)pyridinu 70% HN 3 N 2 N 18M H 2 S 4 N N 2 PRACVNÍ PSTUP: Do 50ml Erlenmeyerovy baňky s míchadlem předložíme 220 mmol 98% H 2 S 4 (MW 98,08; d 1,84) a baňku ochladíme v ledové lázni na teplotu 0 C. Za stálého míchání postupně přidáme 16 mmol 2-benzylpyridinu (MW 169,22; d 1,05). Směs intenzivně mícháme a po kapkách přiléváme 36 mmol 65% HN 3 (MW 63,01; d 1,35) po dobu alespoň 5 min. Po první kapce HN 3 směs zhnědne, ale barva se po dalších kapkách částečně vytratí. Po skončení přikapávání reakční směs zahřejeme 20 min na vroucí vodní lázni. bsah baňky vlijeme do 200 g drceného ledu v 1000ml kádince nebo Erlenmeyerově baňce a vzniklý roztok zalkalizujeme pomalým přidáním 500 mmol NaH (MW 40,00) ve 250 ml vody (nejprve rozpustíme hydroxid jen ve 25 ml vody, čímž se roztok intenzivně zahřeje a poté jej zředíme 225 ml vody). Ke konci alkalizace směsi se produkt sráží ve formě mléčné suspenze. Přidáme cca 200 ml diethyletheru a reakční směs intenzivně mícháme a necháme min extrahovat. Vrstvy oddělíme v 1000ml dělící nálevce (separace není čistá a někdy vznikne emulze na rozhraní fází, kterou lze rozrazit přidáním nasyceného vodného roztoku NaCl nebo pevného NaCl). Etherický extrakt promyjeme nasyceným roztokem NaCl, vysušíme bezvodým Na 2 S 4, sušidlo po 5 min zfiltrujeme a filtrát zahustíme ve vakuu. Již v průběhu odpařování často dochází ke krystalizaci. Směs ochladíme v ledové lázni a krystaly vakuově zfiltrujeme a promyjeme malým množstvím ledového ethanolu. Produkt rekrystalizujeme asi z 10 ml ethanolu na gram, do kterého přidáme několik kapek vody na indukci krystalizace. Po vysušení produkt zvážíme a vhodným způsobem charakterizujeme. 4
5 Část 2. Pozorování fotochromismu N 2 hv N 2 H N tma H N žluté až světle hnědé zbarvení tmavě modré zbarvení PRACVNÍ PSTUP: Po skladování zhruba 24 h ve tmě jsou krystaly 2-(2,4-dinitrobenzyl)pyridinu bezbarvé, po expozici slunečnímu světlu nebo např. UV lampě se do několika minut vyvine tmavě modré zbarvení, proces je zcela reverzibilní. Výsledky pozorování si zapíšeme do protokolu. 5
6 2.3. Úlohy z radikálových fotohalogenací Radikálová fotochlorace benzenu Část 1. Příprava plynného chloru 16 HCl + 2 KMn 4 5 Cl MnCl KCl + 8 H 2 PRACVNÍ PSTUP: Pracujeme v digestoři!!! Do dvouhrdlé baňky navážíme potřebné množství KMn 4 (asi jedna lžička) a na jedno hrdlo baňky nasadíme přikapávací nálevku se zředěnou kyselinou chlorovodíkovou (asi 1 : 1), na druhé hrdlo připojíme nástavec s hadičkou vedoucí do 1. promývačky s H 2 a 2. promývačky s koncentrovanou H 2 S 4. Z přikapávací nálevky pomalu a po kapkách dávkujeme zředěnou kyselinu chlorovodíkovou tak, aby se kontinuálně vyvíjel plynný chlor. Část 2. Příprava HCH PRACVNÍ PSTUP: hv Cl 2 Cl Cl Cl Cl Cl Cl Pracujeme v digestoři!!! Do dvouhrdlé 50ml baňky vlijeme asi 100 mmol benzenu (MW 78,11; d 0,88), na hlavní hrdlo baňky nasadíme zpětný chladič zakončený absorbérem kyselých plynů a na zábrus postranního hrdla umístíme zátku s trubičkou sahající pod hladinu benzenu, kterou napojíme na vyvíječ chloru. Do baňky s benzenem zavádíme plynný chlor a její obsah ozařujeme světlem lampy nebo zářivky. V průběhu reakce pozorujeme nejprve žlutozelené zbarvení směsi, které se pomalu odbarvuje a dochází ke vzniku produktu ve formě bílého prášku. Krystalický produkt zvážíme a vhodným způsobem charakterizujeme. 6
7 2.4. Úlohy z fotochemie alkenů a příbuzných sloučenin Fotocyklodimerizace trans-skořicové kyseliny v pevné fázi Část 1. Fotocyklodimerizace trans-skořicové kyseliny 2 CH hv HC CH + CH CH truxillové kyseliny truxinové kyseliny PRACVNÍ PSTUP: 10 mmol trans-skořicové kyseliny (MW 148,16) umístíme do širší zkumavky a na vroucí vodní lázni ji za varu rozpustíme ve 2 ml THF. Po rozpuštění kyseliny horkým roztokem ve zkumavce opatrně kroužíme a otáčíme, abychom ho rozprostřeli co nejlépe a homogenně po stěnách zkumavky a vytvořili tenký film skořicové kyseliny. Pokud film není dostatečně stejnorodý, vzorek opětovně rozpustíme a postup opakujeme. Jakmile se THF ze zkumavky dostatečně odpaří, tak otevřenou zkumavku opatrně otočíme dnem vzhůru tak, abychom neztratili ani jediný krystal vzorku a necháme ji alespoň 30 min stát k odpaření zbytků rozpouštědla. Poté zkumavku popíšeme, zazátkujeme, zátku zaparafinujeme a zkumavku necháme stát na okenním parapetu, římse nebo na střeše budovy zhruba po dobu 2 týdnů. Po skončení reakční doby (ověříme pomocí TLC) produkt zvážíme a stanovíme jeho TLC čistotu a teplotu tání. Část 2. Esterifikace produktu HC H 2 S 4 H 3 CC CH CH 3 H CCH 3 PRACVNÍ PSTUP: CH H 2 S 4 CCH 3 CH CH 3 H CCH 3 Do 25ml baňky přesypeme produkt předchozí reakce, přidáme 10 ml methanolu a 2 3 kapky koncentrované H 2 S 4 a varný kamínek. Na vroucí vodní lázni směs 60 min jemně refluxujeme, poté ochladíme, převedeme do dělící nálevky, kam přidáme 25 ml 7
8 vody, 25 ml diethyletheru a nálevku intenzivně protřepeme. Vodnou vrstvu oddělíme, organickou promyjeme nasyceným roztokem NaHC 3 a nasyceným roztokem NaCl. rganickou vrstvu vypustíme do Erlenmeyerovy baňky, kde ji vysušíme bezvodým MgS 4, po 5 min sušidlo zfiltrujeme a filtrát odpaříme. Diester rekrystalizujeme z minimálního množství methanolu nebo hexanu, vysušíme a stanovíme jeho TLC čistotu a bod tání. Část 3. Epimerizace a příprava anhydridu HC Ac 2 Ac HC 2 NaAc CH CH cis trans CH H CH Ac 2 Ac 2 NaAc CH H CH cis trans PRACVNÍ PSTUP: Do 10ml baňky nebo zkumavky přeneseme produkt fotochemické reakce a přidáme 3,66 mmol bezvodého octanu sodného (MW 82,03), 21,16 mmol acetanhydridu (MW 102,09; d 1,08) a varný kamínek. Reakční směs necháme jemně refluxovat v topném hnízdě nebo v pískové lázni po dobu 10 min a následně do horké reakční směsi po kapkách přidáme 1 ml destilované vody na hydrolýzu přebytku acetanhydridu (pozor, exotermická reakce!!!). Jakmile vývin tepla ustane, přilijeme dalších 5 ml destilované vody a směs přeneseme do dělící nálevky. Zbytky v baňce nebo zkumavce vypláchneme 20 ml destilované vody a 10 ml dichlormethanu a obě fáze přidáme k obsahu dělící nálevky. Dělící nálevku uzavřeme, důkladně protřepeme a oddělíme vodnou fázi. rganickou vrstvu promyjeme nasyceným roztokem NaHC 3, nasyceným roztokem NaCl a vysušíme bezvodým MgS 4. Sušidlo po 5 min odfiltrujeme a k filtrátu přidáme varný kamínek a varem jej v digestoři zahustíme na objem asi 2 ml. K horkému roztoku přidáme 2 4 ml 96% ethanolu, čímž by se měla indukovat tvorba krystalů. Krystalky anhydridu po ochlazení roztoku sesbíráme vakuovou filtrací. Zahuštěním matečného louhu lze získat druhou várku krystalů produktu. Anhydrid necháme vysušit na vzduchu a stanovíme jeho TLC čistotu a bod tání. 8
9 Část 4. Identifikace isomeru na základě zjištěných dat PRACVNÍ PSTUP: Závěry vytvořené na základě teplot tání porovnáme s následující tabulkou a výsledky v podobě zjištěného isomeru sdělíme vyučujícímu. ISMER t. t. kyseliny t. t. anhydridu t. t. diesteru 1 ( C) 286 epimerizuje ( C) ( C) epimerizuje není známý epimerizuje epimerizuje není známý epimerizuje 77 9
10 Fotochemická isomerizace trans-azobenzenu N N hv 1 hv 2 / Δ N N PRACVNÍ PSTUP: Pracujeme v digestoři, oči a kůži chráníme před zdrojem UV záření!!! Do 50ml baňky s magnetickým míchadlem a zpětným chladičem navážíme 2,7 mmol trans-azobenzenu (MW 182,22) a přilijeme 25 ml petroletheru. bsah baňky ozařujeme světlem střednětlaké rtuťové výbojky ze vzdálenosti cm po dobu 30 min. Po uplynutí této doby by měl být roztok intenzivně červeně zbarven. Směs přefiltrujeme přes krátkou chromatografickou kolonu z aluminy (asi mm) a vzorek eluujeme přibližně ml petroletheru. Eluát je tvořený nezreagovaným trans-azobenzenem. Cis-azobenzen zůstal adsorbovaný na koloně v ostře ohraničené zóně o délce asi 4 cm začínající zhruba 1 cm pod vrcholem kolony. Cis-azobenzen z kolony eluujeme 1% roztokem methanolu v petroletheru (obvykle stačí použít ml). Eluát obsahující cis-azobenzen promyjeme vodou (na odstranění methanolu), vysušíme bezvodým Na 2 S 4 a po zfiltrování sušidla filtrát odpaříme ve vakuu při teplotě do 20 C. Krystalický produkt lze opatrně rekrystalizovat ze studeného petroletheru. U cis- a trans-azobenzenu stanovíme TLC čistotu a porovnáme jejich teploty tání. 10
11 2.5. Úlohy z fotochemie karbonylových sloučenin Fotochemická a termická redukce 4,4 -dimethylbenzofenonu Část 1. Fotochemická redukce 3 * + H AcH H + H PRACVNÍ PSTUP: K přípravě je ideální vybrat slunný týden. V zábrusové zkumavce rozpustíme za třepání 13,72 mmol 4,4 -dimethylbenzofenonu (MW 210,27) v 10 ml isopropanolu a k roztoku přidáme 1 kapku octové kyseliny (je-li to nezbytné, můžeme směs mírně zahřát na rozpuštění 4,4 -dimethylbenzofenonu). Zkumavku pod proudem dusíku velmi těsně zazátkujeme (zátku obalíme parafinem) a umístíme na parapet k oknu, kde ji necháme celý týden vystavenu slunečnímu záření. Již po 4 6 h pozorujeme tvorbu bezbarvých krystalků 4,4 -dimethylbenzopinakolu, která je dokončena zhruba po 4 5 dnech. Po této době krystaly benzopinakolu zfiltrujeme, vysušíme a charakterizujeme teplotou tání a IČ spektrem. Část 2. Termická redukce NaBH 4 EtH H 2 H PRACVNÍ PSTUP: Ve 250ml Erlenmeyerově baňce rozpustíme 5,49 mmol 4,4 -dimethylbenzofenonu (MW 210,27) v 8 ml ethanolu a 2 ml vody. Přisypeme 6,61 mmol NaBH 4 (MW 37,83) a krouživým pohybem směs promícháváme. Po cca min přilijeme 100 ml ledové destilované vody a reakční směs extrahujeme 2 50 ml diethyletheru. Etherické extrakty spojíme a promyjeme 50 ml 2M HCl a 50 ml vody. rganickou vrstvu vysušíme bezvodým MgS 4, po 5 min sušidlo zfiltrujeme a filtrát odpaříme ve vakuu. U produktu změříme IČ spektrum, TLC čistotu a bod tání. 11
12 Část 3. Porovnání výsledků obou metod PRACVNÍ PSTUP: Na základě naměřených teplot tání a IČ spekter porovnáme výsledky obou redukčních metod a pokusíme se odhadnout rozdíly v identitě produktu fotochemické a termické redukce. 12
13 2. Termické pericyklické reakce 2.1. Dielsovy Alderovy reakce Příprava ferrocenu Část 1. Příprava cyklopentadienu > 160 C 2 25 C PRACVNÍ PSTUP: lejovou nebo pískovou lázeň vyhřejeme na 250 C. Do 5ml baňky vlijeme 2,5 ml minerálního oleje, připojíme malou límcovou kolonku s chladičem a aparaturu vsadíme do lázně. Po vytemperování začneme přikapávat dicyklopentadien (MW 132,20; d 0,98) rychlostí 1 kapky za 5 10 s, dokud nezískáme přibližně 3 4 ml destilátu. Část 2. Příprava ferrocenu PRACVNÍ PSTUP: V mezičase druhý z dvojice rozdrtí 14,26 mmol KH (MW 56,11) ve třecí misce co nejrychleji je to možné a rychle KH přesype do malé baňky s magnetickým míchadlem, která byla předem vyfouknutá dusíkem, a následně ihned baňku uzavře gumovým septem propíchnutým balónkem dusíku. Pomocí injekční stříkačky s jehlou přidá 3 ml glymu (1,2-dimethoxyethanu). Po nadestilování cyklopentadienu (MW 66,10; d 0,79) odebereme 2,39 mmol destilátu opět pomocí injekční stříkačky s jehlou, přidáme jej k roztoku KH v glymu a necháme reakční médium intenzivně míchat, přičemž pozorujeme změnu zbarvení směsi do hněda. 1. KH, FeCl 2.4H 2, DMS 2 Fe 2. HCl Mezitím si v malé uzavřené baňce připravíme roztok 7,4 mmol FeCl 2.4H 2 (MW 198,81) v 1,2 ml DMS, který pomocí stříkačky po dobu 10 min přikapáváme do baňky s cyklopentadienidem draselným a poté směs ještě 30 min mícháme při laboratorní teplotě. Reakční směs přelijeme do Erlenmeyerovy baňky, do níž přidáme 13
14 předem připravenou směs 4 g drceného ledu a 3,5 ml 6M HCl (MW 36,46; d 1,19), kterou zneutralizujeme přebytečný KH. ranžové krystalky zfiltrujeme, promyjeme 1 ml vody a necháme usušit na vzduchu. Čistý ferrocen získáme sublimací při teplotě asi 100 C. Produkt zvážíme a vhodným způsobem charakterizujeme. 14
15 Příprava trypticen-2,5-diolu Část 1. Adice benzochinonu na anthracen + Δ xylen PRACVNÍ PSTUP: V 10ml baňce se vzdušným chladičem 2 h refluxujeme 6,06 mmol anthracenu (MW 178,23) a 6,75 mmol 1,4-benzochinonu (MW 108,09), po ochlazení produkt sesbíráme vakuovou filtrací, filtrační koláč promyjeme ledovým xylenem, vysušíme, zvážíme a vhodným způsobem charakterizujeme. Část 2. Isomerizace endionu H H HBr AcH PRACVNÍ PSTUP: V 50ml baňce se vzdušným chladičem uvedeme k varu suspenzi 4,92 mmol primárního aduktu z předchozí reakce ve 20 ml kyseliny octové a pomalu k ní přidáme 1 2 kapky 48% HBr (MW 80,91; d 1,49). Směs následně ještě 20 min povaříme, poté necháme ochladit na laboratorní teplotu, produkt odsajeme, promyjeme ledovou vodou a necháme vysušit na vzduchu. Bílé krystaly trypticen- 2,5-diolu vhodným způsobem charakterizujeme. 15
Úloha č. 1 Příprava nifedipinu
 Úloha č. 1 Příprava nifedipinu Do kulaté baňky o objemu 50 ml předložíme 4 mmol 2-nitrobenzaldehydu, 9 mmol methylacetacetátu, 1,2 ml 25% NH 4 OH a 1 ml methanolu. Na baňku nasadíme zpětný chladič a umístíme
Úloha č. 1 Příprava nifedipinu Do kulaté baňky o objemu 50 ml předložíme 4 mmol 2-nitrobenzaldehydu, 9 mmol methylacetacetátu, 1,2 ml 25% NH 4 OH a 1 ml methanolu. Na baňku nasadíme zpětný chladič a umístíme
C3070 Organická chemie - laboratorní cvičení molekulární biologie
 Seznam úloh předmětu: C3070 Organická chemie - laboratorní cvičení molekulární biologie 3) Nitrace fenolu 5) Ethylenacetal ethylesteru 3-oxobutanové kyseliny 10) Kyselina benzoová 11) Kyselina anthranilová
Seznam úloh předmětu: C3070 Organická chemie - laboratorní cvičení molekulární biologie 3) Nitrace fenolu 5) Ethylenacetal ethylesteru 3-oxobutanové kyseliny 10) Kyselina benzoová 11) Kyselina anthranilová
I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í
 I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY Laboratorní práce č. 10 Bílkoviny Pro potřeby projektu
I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY Laboratorní práce č. 10 Bílkoviny Pro potřeby projektu
LABORATORNÍ PRÁCE č.2
 LABORATORNÍ PRÁCE č.2 Téma: Dělení směsí II Úkol č.1: Destilace směsi manganistan draselný voda Teorie: Jedná se o jeden z nejdůležitějších způsobů oddělování složek kapalných směsí a jejich čištění. Složky
LABORATORNÍ PRÁCE č.2 Téma: Dělení směsí II Úkol č.1: Destilace směsi manganistan draselný voda Teorie: Jedná se o jeden z nejdůležitějších způsobů oddělování složek kapalných směsí a jejich čištění. Složky
RUŠENÁ KRYSTALIZACE A SUBLIMACE
 LABORATORNÍ PRÁCE Č. 5 RUŠENÁ KRYSTALIZACE A SUBLIMACE KRYSTALIZACE PRINCIP Krystalizace je důležitý postup při získávání čistých tuhých látek z jejich roztoků. Tuhá látka se rozpustí ve vhodném rozpouštědle.
LABORATORNÍ PRÁCE Č. 5 RUŠENÁ KRYSTALIZACE A SUBLIMACE KRYSTALIZACE PRINCIP Krystalizace je důležitý postup při získávání čistých tuhých látek z jejich roztoků. Tuhá látka se rozpustí ve vhodném rozpouštědle.
UHLOVODÍKY A HALOGENDERIVÁTY
 LABORATORNÍ PRÁCE Č. 25 UHLOVODÍKY A HALOGENDERIVÁTY PRINCIP Uhlovodíky jsou nejjednodušší organické sloučeniny, jejichž molekuly jsou tvořeny pouze uhlíkem a vodíkem. Uhlovodíky klasifikujeme z několika
LABORATORNÍ PRÁCE Č. 25 UHLOVODÍKY A HALOGENDERIVÁTY PRINCIP Uhlovodíky jsou nejjednodušší organické sloučeniny, jejichž molekuly jsou tvořeny pouze uhlíkem a vodíkem. Uhlovodíky klasifikujeme z několika
I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í
 I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY Laboratorní práce č. 9 Lipidy Pro potřeby projektu
I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY Laboratorní práce č. 9 Lipidy Pro potřeby projektu
KARBOXYLOVÉ KYSELINY
 LABORATORNÍ PRÁCE Č. 28 KARBOXYLOVÉ KYSELINY PRINCIP Karboxylové kyseliny jsou látky, které ve své molekule obsahují jednu nebo více karboxylových skupin. Odvozují se od nich dva typy derivátů, substituční
LABORATORNÍ PRÁCE Č. 28 KARBOXYLOVÉ KYSELINY PRINCIP Karboxylové kyseliny jsou látky, které ve své molekule obsahují jednu nebo více karboxylových skupin. Odvozují se od nich dva typy derivátů, substituční
Schlenkovské techniky II
 Schlenkovské techniky II Cílem této úlohy je další procvičování činností s vakuovou linkou a další využití schlenkovských technik. Bude se jednat o práci s organickými rozpouštědly, extrakci a destilaci
Schlenkovské techniky II Cílem této úlohy je další procvičování činností s vakuovou linkou a další využití schlenkovských technik. Bude se jednat o práci s organickými rozpouštědly, extrakci a destilaci
OKRUH 7 Karboxylové kyseliny
 OKRUH 7 Karboxylové kyseliny Pro karboxylové kyseliny je charakteristická přítomnost jedné nebo více karboxylových skupin Monokarboxylové kyseliny Příprava kyseliny mravenčí z chloroformu a její důkaz
OKRUH 7 Karboxylové kyseliny Pro karboxylové kyseliny je charakteristická přítomnost jedné nebo více karboxylových skupin Monokarboxylové kyseliny Příprava kyseliny mravenčí z chloroformu a její důkaz
VÝROBA UHLIČITANU SODNÉHO TEXT PRO UČITELE
 VÝROBA UHLIČITANU SODNÉHO TEXT PRO UČITELE Mgr. Jana Prášilová prof. RNDr. Jiří Kameníček, CSc. Olomouc, 2013 Obsah 1. Téma v učebnicích používaných na gymnáziích 2. Teoretické poznatky k problematice
VÝROBA UHLIČITANU SODNÉHO TEXT PRO UČITELE Mgr. Jana Prášilová prof. RNDr. Jiří Kameníček, CSc. Olomouc, 2013 Obsah 1. Téma v učebnicích používaných na gymnáziích 2. Teoretické poznatky k problematice
Standardní operační postup
 Standardní operační postup CHOL_1 Stanovení cholesterolu v potravinách metodou HPLC V Brně dne 20. 3. 2011 Vypracoval: RNDr. Ivana Borkovcová, Ph.D. 1. Princip Po alkalické hydrolýze (saponifikaci, zmýdelnění)
Standardní operační postup CHOL_1 Stanovení cholesterolu v potravinách metodou HPLC V Brně dne 20. 3. 2011 Vypracoval: RNDr. Ivana Borkovcová, Ph.D. 1. Princip Po alkalické hydrolýze (saponifikaci, zmýdelnění)
RCOOR + H 2 O. Inovace bakalářského studijního oboru Aplikovaná chemie CZ.1.07/2.2.00/ Esterifikace
 Esterifikace Estery jsou funkční deriváty karboxylových kyselin. Připravují se reakcí karboxylových kyselin s alkoholy nebo s fenoly. RCOOH+ HOR RCOOR + H 2 O K přípravě esterů je vhodné použít vyšší alifatické
Esterifikace Estery jsou funkční deriváty karboxylových kyselin. Připravují se reakcí karboxylových kyselin s alkoholy nebo s fenoly. RCOOH+ HOR RCOOR + H 2 O K přípravě esterů je vhodné použít vyšší alifatické
Návod k laboratornímu cvičení. Fenoly
 Návod k laboratornímu cvičení Fenoly Úkol č. 1: Příprava fenolátu sodného Pomůcky: váhy, kádinka, zkumavky Chemikálie: 10% roztok hydroxidu sodného NaOH (C), 5%roztok kyseliny chlorovodíkové HCl (C, X
Návod k laboratornímu cvičení Fenoly Úkol č. 1: Příprava fenolátu sodného Pomůcky: váhy, kádinka, zkumavky Chemikálie: 10% roztok hydroxidu sodného NaOH (C), 5%roztok kyseliny chlorovodíkové HCl (C, X
látka Obr. k úkolům 1 a 2 Obr. k úkolu 3
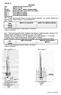 cvičení: A Téma: Základní vlastnosti organických látek Cíl: Teplota varu a tání Pomůcky: žákovská souprava, teploměr, skleněná trubička, Chemikálie: ethanol CH 3 CH 2 OH, aceton CH 3 COCH 3, naftalen Úkol
cvičení: A Téma: Základní vlastnosti organických látek Cíl: Teplota varu a tání Pomůcky: žákovská souprava, teploměr, skleněná trubička, Chemikálie: ethanol CH 3 CH 2 OH, aceton CH 3 COCH 3, naftalen Úkol
Laboratorní cvičení z kinetiky chemických reakcí
 Laboratorní cvičení z kinetiky chemických reakcí LABORATORNÍ CVIČENÍ 1. Téma: Ovlivňování průběhu reakce změnou koncentrace látek. podmínek průběhu reakce. Jednou z nich je změna koncentrace výchozích
Laboratorní cvičení z kinetiky chemických reakcí LABORATORNÍ CVIČENÍ 1. Téma: Ovlivňování průběhu reakce změnou koncentrace látek. podmínek průběhu reakce. Jednou z nich je změna koncentrace výchozích
Jazykové gymnázium Pavla Tigrida, Ostrava-Poruba Název projektu: Podpora rozvoje praktické výchovy ve fyzice a chemii
 Datum: Jazykové gymnázium Pavla Tigrida, Ostrava-Poruba Název projektu: Podpora rozvoje praktické výchovy ve fyzice a chemii Tlak vzduchu: Teplota vzduchu: Laboratorní cvičení č. Oddělování složek směsí
Datum: Jazykové gymnázium Pavla Tigrida, Ostrava-Poruba Název projektu: Podpora rozvoje praktické výchovy ve fyzice a chemii Tlak vzduchu: Teplota vzduchu: Laboratorní cvičení č. Oddělování složek směsí
I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í LABORATORNÍ PRÁCE Č. 6 PRÁCE S PLYNY
 LABORATORNÍ PRÁCE Č. 6 PRÁCE S PLYNY Mezi nejrozšířenější práce s plyny v laboratoři patří příprava a důkazy oxidu uhličitého CO 2, kyslíku O 2, vodíku H 2, oxidu siřičitého SO 2 a amoniaku NH 3. Reakcí
LABORATORNÍ PRÁCE Č. 6 PRÁCE S PLYNY Mezi nejrozšířenější práce s plyny v laboratoři patří příprava a důkazy oxidu uhličitého CO 2, kyslíku O 2, vodíku H 2, oxidu siřičitého SO 2 a amoniaku NH 3. Reakcí
I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í
 I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY Laboratorní práce č. 8 Sacharidy Pro potřeby projektu
I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY Laboratorní práce č. 8 Sacharidy Pro potřeby projektu
Vodík, kyslík a jejich sloučeniny
 I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY Laboratorní práce č. 8 Vodík, kyslík a jejich sloučeniny
I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY Laboratorní práce č. 8 Vodík, kyslík a jejich sloučeniny
Návod k laboratornímu cvičení. Efektní pokusy
 Návod k laboratornímu cvičení Efektní pokusy Úkol č. 1: Chemikova zahrádka Pomůcky: skleněná vana, lžička na chemikálie. Chemikálie: vodní sklo, síran zinečnatý ZnSO 4 (X i ), síran železnatý FeSO 4, chlorid
Návod k laboratornímu cvičení Efektní pokusy Úkol č. 1: Chemikova zahrádka Pomůcky: skleněná vana, lžička na chemikálie. Chemikálie: vodní sklo, síran zinečnatý ZnSO 4 (X i ), síran železnatý FeSO 4, chlorid
Název: Acidobazické indikátory
 Název: Acidobazické indikátory Autor: Mgr. Jiří Vozka, Ph.D. Název školy: Gymnázium Jana Nerudy, škola hl. města Prahy Předmět, mezipředmětové vztahy: chemie, biologie, fyzika Ročník: 3. (1. ročník vyššího
Název: Acidobazické indikátory Autor: Mgr. Jiří Vozka, Ph.D. Název školy: Gymnázium Jana Nerudy, škola hl. města Prahy Předmět, mezipředmětové vztahy: chemie, biologie, fyzika Ročník: 3. (1. ročník vyššího
Cíl úlohy: Najít vhodné rozpouštědlo pro překrystalování zkoušené látky a samotná krystalizace.
 Úloha A Krystalizace ejdůležitější metodou čištění tuhých látek je krystalizace. Zakládá se na rozdílné rozpustnosti zkoumané látky a její příměsí v určitém rozpouštědle za různých teplot. Při krystalizaci
Úloha A Krystalizace ejdůležitější metodou čištění tuhých látek je krystalizace. Zakládá se na rozdílné rozpustnosti zkoumané látky a její příměsí v určitém rozpouštědle za různých teplot. Při krystalizaci
Teoretický protokol ze cvičení 6. 12. 2010 Josef Bušta, skupina: 1, obor: fytotechnika
 Úloha: Karboxylové kyseliny, č. 3 Úkoly: Příprava kys. mravenčí z chloroformu Rozklad kys. mravenčí Esterifikace Rozklad kys. šťavelové Příprava kys. benzoové oxidací toluenu Reakce kys. benzoové a salicylové
Úloha: Karboxylové kyseliny, č. 3 Úkoly: Příprava kys. mravenčí z chloroformu Rozklad kys. mravenčí Esterifikace Rozklad kys. šťavelové Příprava kys. benzoové oxidací toluenu Reakce kys. benzoové a salicylové
Téma : Uhlovodíky Areny Toluen a naftalen Název : Vlastnosti toluenu a naftalenu
 Téma : Uhlovodíky Areny Toluen a naftalen Název : Vlastnosti toluenu a naftalenu Typ pokusu : demonstrační Princip : Areny starším názvem aromatické uhlovodíky, vzaly tento svůj název podle své typické
Téma : Uhlovodíky Areny Toluen a naftalen Název : Vlastnosti toluenu a naftalenu Typ pokusu : demonstrační Princip : Areny starším názvem aromatické uhlovodíky, vzaly tento svůj název podle své typické
NOVÉ NÁMĚTY PRO DEMONSTRAČNÍ POKUSY. Ondřej Maca, Tereza Kudrnová
 NOVÉ NÁMĚTY PRO DEMONSTRAČNÍ POKUSY Ondřej Maca, Tereza Kudrnová HUSTÝ DÝM 1) pro koho: 1. ročník čtyřletého gymnázia 2) zařazení do učiva: vlastnosti látek; halogeny; pentely 3) pomůcky: zkumavka se zátkou,
NOVÉ NÁMĚTY PRO DEMONSTRAČNÍ POKUSY Ondřej Maca, Tereza Kudrnová HUSTÝ DÝM 1) pro koho: 1. ročník čtyřletého gymnázia 2) zařazení do učiva: vlastnosti látek; halogeny; pentely 3) pomůcky: zkumavka se zátkou,
Hydroxidy a indikátory demonstrační
 název typ: zařazení: Pomůcky: Chemikálie: Postup: pozorování rovnice, vysvětlení Hydroxidy a indikátory demonstrační Hydroxidy. Indikátory. 3 zkumavky, kapátko NaOH(C), fenolftalein, lakmus, ph papírek
název typ: zařazení: Pomůcky: Chemikálie: Postup: pozorování rovnice, vysvětlení Hydroxidy a indikátory demonstrační Hydroxidy. Indikátory. 3 zkumavky, kapátko NaOH(C), fenolftalein, lakmus, ph papírek
Sešit pro laboratorní práci z chemie
 Sešit pro laboratorní práci z chemie téma: Příprava oxidu měďnatého autor: ing. Alena Dvořáková vytvořeno při realizaci projektu: Inovace školního vzdělávacího programu biologie a chemie registrační číslo
Sešit pro laboratorní práci z chemie téma: Příprava oxidu měďnatého autor: ing. Alena Dvořáková vytvořeno při realizaci projektu: Inovace školního vzdělávacího programu biologie a chemie registrační číslo
různorodé suspenze (pevná látka v kapalné) emulze (nemísitelné kapaliny) pěna (plynná l. v kapalné l.) mlha (kapalná l. v plynné l.
 Obsah: 6_Směsi... 2 7_Roztoky, složení roztoku... 3 8_PL_Složení roztoku - příklady... 4 9_Rozpustnost látky... 8 10_ PL_Rozpustnost ve vodě... 9 11_ Dělení směsí... 11 1 6_ Směsi - jsou látky složené
Obsah: 6_Směsi... 2 7_Roztoky, složení roztoku... 3 8_PL_Složení roztoku - příklady... 4 9_Rozpustnost látky... 8 10_ PL_Rozpustnost ve vodě... 9 11_ Dělení směsí... 11 1 6_ Směsi - jsou látky složené
Návod k laboratornímu cvičení. Alkoholy
 Úkol č. 1: Ověřování fyzikálních vlastností alkoholů Návod k laboratornímu cvičení Alkoholy Pomůcky: 3 velké zkumavky - A,B,C, hodinové sklíčko, kapátko nebo skleněná tyčinka Chemikálie: etanol (F), etan-1,2-
Úkol č. 1: Ověřování fyzikálních vlastností alkoholů Návod k laboratornímu cvičení Alkoholy Pomůcky: 3 velké zkumavky - A,B,C, hodinové sklíčko, kapátko nebo skleněná tyčinka Chemikálie: etanol (F), etan-1,2-
Jednotné pracovní postupy zkoušení krmiv STANOVENÍ OBSAHU VITAMÍNU D METODOU LC/MS
 Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU VITAMÍNU D METODOU LC/MS 1 Účel a rozsah Tento postup specifikuje podmínky pro stanovení vitamínu D3 v krmivech metodou LC/MS. 2 Princip Zkušební
Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU VITAMÍNU D METODOU LC/MS 1 Účel a rozsah Tento postup specifikuje podmínky pro stanovení vitamínu D3 v krmivech metodou LC/MS. 2 Princip Zkušební
Termochemie. Úkol: A. Určete změnu teploty při rozpouštění hydroxidu sodného B. Určete reakční teplo reakce zinku s roztokem měďnaté soli
 1. Termochemie Úkol: Určete změnu teploty při rozpouštění hydroxidu sodného B. Určete reakční teplo reakce zinku s roztokem měďnaté soli Pomůcky : a) kádinky, teploměr, odměrný válec, váženka, váhy, kalorimetr,
1. Termochemie Úkol: Určete změnu teploty při rozpouštění hydroxidu sodného B. Určete reakční teplo reakce zinku s roztokem měďnaté soli Pomůcky : a) kádinky, teploměr, odměrný válec, váženka, váhy, kalorimetr,
Vybraná vyšetření u pacientů s diabetes mellitus
 ÚSTAV LÉKAŘSKÉ BIOCHEMIE A LABORATORNÍ DIAGNOSTIKY 1. LF UK Vybraná vyšetření u pacientů s diabetes mellitus Praktické cvičení z lékařské biochemie Všeobecné lékařství Martin Vejražka 2018/19 Obsah 1.
ÚSTAV LÉKAŘSKÉ BIOCHEMIE A LABORATORNÍ DIAGNOSTIKY 1. LF UK Vybraná vyšetření u pacientů s diabetes mellitus Praktické cvičení z lékařské biochemie Všeobecné lékařství Martin Vejražka 2018/19 Obsah 1.
Sešit pro laboratorní práci z chemie
 Sešit pro laboratorní práci z chemie téma: Příprava roztoků a měření ph autor: ing. Alena Dvořáková vytvořeno při realizaci projektu: Inovace školního vzdělávacího programu biologie a chemie registrační
Sešit pro laboratorní práci z chemie téma: Příprava roztoků a měření ph autor: ing. Alena Dvořáková vytvořeno při realizaci projektu: Inovace školního vzdělávacího programu biologie a chemie registrační
Oxidace benzaldehydu vzdušným kyslíkem a roztokem
 Úloha: Karbonylové sloučeniny a sacharidy, č. 2 Úkoly: Oxidace benzaldehydu Důkaz aldehydu Schiffovým činidlem Redukční vlastnosti karbonylových sloučenin a sacharidů (Reakce s Tollensovým a Fehlingovým
Úloha: Karbonylové sloučeniny a sacharidy, č. 2 Úkoly: Oxidace benzaldehydu Důkaz aldehydu Schiffovým činidlem Redukční vlastnosti karbonylových sloučenin a sacharidů (Reakce s Tollensovým a Fehlingovým
Směsi a čisté látky, metody dělení
 Směsi a čisté látky, metody dělení LÁTKY Chemicky čisté látky Sloučeniny Chemické prvky Homogenní Roztoky pevné kapalné plynné Směsi Heterogenní Suspenze Emulze Pěna Aerosol Chemicky čisté látky: prvky
Směsi a čisté látky, metody dělení LÁTKY Chemicky čisté látky Sloučeniny Chemické prvky Homogenní Roztoky pevné kapalné plynné Směsi Heterogenní Suspenze Emulze Pěna Aerosol Chemicky čisté látky: prvky
LABORATORNÍ STANOVENÍ SÍRANŮ VE VODNÉM ROZTOKU
 LABORATORNÍ STANOVENÍ SÍRANŮ VE VODNÉM ROZTOKU Cílem práce je stanovit koncentraci síranů v neznámém vzorku postupem A, B a C a porovnat jednotlivé metody mezi sebou. Protokol musí osahovat veškeré výpočty
LABORATORNÍ STANOVENÍ SÍRANŮ VE VODNÉM ROZTOKU Cílem práce je stanovit koncentraci síranů v neznámém vzorku postupem A, B a C a porovnat jednotlivé metody mezi sebou. Protokol musí osahovat veškeré výpočty
I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í LABORATORNÍ PRÁCE Č. 14 SRÁŽECÍ REAKCE
 LABORATORNÍ PRÁCE Č. 14 SRÁŽECÍ REAKCE PRINCIP Srážecí reakce je reakce, při níž se alespoň jeden z produktů vylučuje z reakční směsi ve formě tuhé fáze (sraženiny). A + (aq) + B - (aq) AB (s) (Reakce
LABORATORNÍ PRÁCE Č. 14 SRÁŽECÍ REAKCE PRINCIP Srážecí reakce je reakce, při níž se alespoň jeden z produktů vylučuje z reakční směsi ve formě tuhé fáze (sraženiny). A + (aq) + B - (aq) AB (s) (Reakce
Oborový workshop pro ZŠ CHEMIE
 PRAKTICKÁ VÝUKA PŘÍRODOVĚDNÝCH PŘEDMĚTŮ NA ZŠ A SŠ CZ.1.07/1.1.30/02.0024 Tento projekt je spolufinancován Evropským sociálním fondem a státním rozpočtem České republiky. Oborový workshop pro ZŠ CHEMIE
PRAKTICKÁ VÝUKA PŘÍRODOVĚDNÝCH PŘEDMĚTŮ NA ZŠ A SŠ CZ.1.07/1.1.30/02.0024 Tento projekt je spolufinancován Evropským sociálním fondem a státním rozpočtem České republiky. Oborový workshop pro ZŠ CHEMIE
KVALITATIVNÍ ELEMENTÁRNÍ ANALÝZA ORGANICKÝCH LÁTEK
 LABORATORNÍ PRÁCE Č. 24 KVALITATIVNÍ ELEMENTÁRNÍ ANALÝZA ORGANICKÝCH LÁTEK PRINCIP Organická kvalitativní elementární analýza zkoumá chemické složení organických látek, zabývá se identifikací jednotlivých
LABORATORNÍ PRÁCE Č. 24 KVALITATIVNÍ ELEMENTÁRNÍ ANALÝZA ORGANICKÝCH LÁTEK PRINCIP Organická kvalitativní elementární analýza zkoumá chemické složení organických látek, zabývá se identifikací jednotlivých
1. AMFOTERNÍ VLASTNOSTI HLINÍKU
 27. 1. 2016 TÉMA: Komplexní sloučeniny Ernest Török ÚKOL: Důkaz komplexních sloučenin 2M/14M 1. AMFOTERNÍ VLASTNOSTI HLINÍKU 2x zkumavka, odměrný válec (malý), lžička o HCl (20%) o NaOH (10%), hliníkové
27. 1. 2016 TÉMA: Komplexní sloučeniny Ernest Török ÚKOL: Důkaz komplexních sloučenin 2M/14M 1. AMFOTERNÍ VLASTNOSTI HLINÍKU 2x zkumavka, odměrný válec (malý), lžička o HCl (20%) o NaOH (10%), hliníkové
Návod k laboratornímu cvičení. Cukry(sacharidy)
 Návod k laboratornímu cvičení Cukry(sacharidy) Úkol č. 1: Odlišení glukosy a fruktosy Pomůcky: zkumavky, lžička na chemikálie, kádinka, stojan, držák, kruh, síťka, plynový kahan, zápalky Chemikálie: fruktosa,
Návod k laboratornímu cvičení Cukry(sacharidy) Úkol č. 1: Odlišení glukosy a fruktosy Pomůcky: zkumavky, lžička na chemikálie, kádinka, stojan, držák, kruh, síťka, plynový kahan, zápalky Chemikálie: fruktosa,
Pokusy z organické chemie
 Pokusy z organické chemie Iveta Turková, Jiří Šibor 1. HALOGENACE ALKANŮ A CYKLOALKANŮ Pomůcky: 3 zkumavky se zátkami, indikátorový papírek, stojánek na zkumavky Chemikálie: hexan, cyklohexan, benzin,
Pokusy z organické chemie Iveta Turková, Jiří Šibor 1. HALOGENACE ALKANŮ A CYKLOALKANŮ Pomůcky: 3 zkumavky se zátkami, indikátorový papírek, stojánek na zkumavky Chemikálie: hexan, cyklohexan, benzin,
VÝŽIVA LIDSTVA Mléko a zdraví
 GYMNÁZIUM JANA OPLETALA LITOVEL Odborná práce přírodovědného kroužku VÝŽIVA LIDSTVA Mléko a zdraví Vypracovali: Martina Hubáčková, Petra Vašíčková, Pavla Kubíčková, Michaela Pavlovská, Jitka Tichá, Petra
GYMNÁZIUM JANA OPLETALA LITOVEL Odborná práce přírodovědného kroužku VÝŽIVA LIDSTVA Mléko a zdraví Vypracovali: Martina Hubáčková, Petra Vašíčková, Pavla Kubíčková, Michaela Pavlovská, Jitka Tichá, Petra
Vzdělávání středoškolských pedagogů a studentů středních škol jako nástroj ke zvyšování kvality výuky přírodovědných předmětů CZ.1.07/1.1.00/14.
 Praktické cvičení z chemie 1) Stanovení lipofilních listových barviv pomocí adsorpční chromatografie. 2) Stanovení proteinů v roztoku. 3) Homogenizace rostlinného materiálu pomocí tekutého dusíku a stanovení
Praktické cvičení z chemie 1) Stanovení lipofilních listových barviv pomocí adsorpční chromatografie. 2) Stanovení proteinů v roztoku. 3) Homogenizace rostlinného materiálu pomocí tekutého dusíku a stanovení
Návody na praktika z Cytologie verze 2015
 Návody na praktika z Cytologie verze 2015 Témata cvičení: 1. Úvodní cvičení, výpočty a příprava roztoků 2. Prvkové složení rostlinné buňky 3. Bílkoviny 4. Sacharidy 5. Lipidy, cholesterol, důkaz mýdla
Návody na praktika z Cytologie verze 2015 Témata cvičení: 1. Úvodní cvičení, výpočty a příprava roztoků 2. Prvkové složení rostlinné buňky 3. Bílkoviny 4. Sacharidy 5. Lipidy, cholesterol, důkaz mýdla
Stanovení vit. A a vit. E metodou HPLC v krmivech a premixech dopl ňkových látek
 STANOVENÍ VITAMINU A (RETINOLU) A VITAMINU E (a-tocopherolu) METODOU HPLC V KRMIVECH A PREMIXECH DOPLŇKOVÝCH LÁTEK. 1. Definice Účinnou formou vitaminu A obecného vzorce C 16 H 23 - R je retinol a neoretinol
STANOVENÍ VITAMINU A (RETINOLU) A VITAMINU E (a-tocopherolu) METODOU HPLC V KRMIVECH A PREMIXECH DOPLŇKOVÝCH LÁTEK. 1. Definice Účinnou formou vitaminu A obecného vzorce C 16 H 23 - R je retinol a neoretinol
Stanovení složení mastných kyselin
 LABORATOŘ ANALÝZY POTRAVIN A PŘÍRODNÍCH PRODUKTŮ Stanovení složení mastných kyselin (metoda: plynová chromatografie s plamenovým ionizačním detektorem) Garant úlohy: Ing. Jana Kohoutková, Ph.D. 1 Obsah
LABORATOŘ ANALÝZY POTRAVIN A PŘÍRODNÍCH PRODUKTŮ Stanovení složení mastných kyselin (metoda: plynová chromatografie s plamenovým ionizačním detektorem) Garant úlohy: Ing. Jana Kohoutková, Ph.D. 1 Obsah
VY_52_INOVACE_O6 _ Krystalizace
 Základní škola a mateřská škola J. A. Komenského v Novém Strašecí Komenského nám. 209, 271 01 Nové Strašecí tel. 311 240 401, 311 240 400, email: zsnovstra@email.cz AUTOR: Hana Růžičková NÁZEV: VY_52_INOVACE_O6
Základní škola a mateřská škola J. A. Komenského v Novém Strašecí Komenského nám. 209, 271 01 Nové Strašecí tel. 311 240 401, 311 240 400, email: zsnovstra@email.cz AUTOR: Hana Růžičková NÁZEV: VY_52_INOVACE_O6
Laboratorní cvičení organická chemie
 Laboratorní cvičení organická chemie Seznam úloh: 1a Ethylbromid 1b terc-butylchlorid 2 Kyselina 3-fenylpropanová 3 Nitrace fenolu 4 Azobenzen 5 Ethylenacetal ethylesteru 3-oxobutanové kyseliny 6a Ethylenacetal
Laboratorní cvičení organická chemie Seznam úloh: 1a Ethylbromid 1b terc-butylchlorid 2 Kyselina 3-fenylpropanová 3 Nitrace fenolu 4 Azobenzen 5 Ethylenacetal ethylesteru 3-oxobutanové kyseliny 6a Ethylenacetal
Všeobecné lékařství 2014/15
 ÚSTAV LÉKAŘSKÉ BIOCHEMIE A LABORATORNÍ DIAGNOSTIKY 1. LF UK Úvod do práce v laboratoři Měření objemů, filtrace, centrifugace, rozpustnost, dělení směsí Praktické cvičení z lékařské biochemie Všeobecné
ÚSTAV LÉKAŘSKÉ BIOCHEMIE A LABORATORNÍ DIAGNOSTIKY 1. LF UK Úvod do práce v laboratoři Měření objemů, filtrace, centrifugace, rozpustnost, dělení směsí Praktické cvičení z lékařské biochemie Všeobecné
167 ml Folinova činidla doplníme do 500 ml destilovanou vodou. Toto činidlo je nestabilní, je nutné připravit vždy čerstvé a uložit při 4 C.
 ROZTOKY 1. Činidlo A 12,5 g (NH 4 ) 6 MO 7 O 4. 4H 2 O rozpustíme ve 125 ml bidestilované vody; 0,5 g K(SbO)C 4 H 4 O 6. 0,5 H 2 O rozpustíme ve 20 ml bidestilované vody; Oba tyto roztoky důkladně promícháme
ROZTOKY 1. Činidlo A 12,5 g (NH 4 ) 6 MO 7 O 4. 4H 2 O rozpustíme ve 125 ml bidestilované vody; 0,5 g K(SbO)C 4 H 4 O 6. 0,5 H 2 O rozpustíme ve 20 ml bidestilované vody; Oba tyto roztoky důkladně promícháme
Návod k laboratornímu cvičení. Oddělování složek směsí I
 Návod k laboratornímu cvičení Oddělování složek směsí I Úkol č. 1: Usazování Pomůcky: dělící nálevka, držák, svorka, stojan, kádinka Chemikálie: voda, potravinářské barvivo, olej 1. Dělící nálevku upevníme
Návod k laboratornímu cvičení Oddělování složek směsí I Úkol č. 1: Usazování Pomůcky: dělící nálevka, držák, svorka, stojan, kádinka Chemikálie: voda, potravinářské barvivo, olej 1. Dělící nálevku upevníme
UHLIČITAN NIKELNATÝ BAZICKÝ (SRÁŽENÍ)
 UHLIČITAN NIKELNATÝ BAZICKÝ (SRÁŽENÍ) NaHCO 3 + 3 NiSO 4 + 3 H 2 O NiCO 3. 2 Ni(OH) 2. 4 H 2 O + 3 Na 2 SO 4 + 5 CO 2 Na 2 CO 3 + 3 NiSO 4 + 6 H 2 O NiCO 3. 2 Ni(OH) 2. 4 H 2 O + 3 Na 2 SO 4 + 2 CO 2 (NH
UHLIČITAN NIKELNATÝ BAZICKÝ (SRÁŽENÍ) NaHCO 3 + 3 NiSO 4 + 3 H 2 O NiCO 3. 2 Ni(OH) 2. 4 H 2 O + 3 Na 2 SO 4 + 5 CO 2 Na 2 CO 3 + 3 NiSO 4 + 6 H 2 O NiCO 3. 2 Ni(OH) 2. 4 H 2 O + 3 Na 2 SO 4 + 2 CO 2 (NH
UHLIČITAN NIKELNATÝ (SRÁŽENÍ)
 UHLIČITAN NIKELNATÝ (SRÁŽENÍ) NaHCO 3 + NiSO 4 NiCO 3 + NaHSO 4 Připravte 5g uhličitanu nikelnatého. Připravíme si 10% roztok hydrogenuhličitanu sodného a zahřejeme ho téměř k varu. Za stálého míchání
UHLIČITAN NIKELNATÝ (SRÁŽENÍ) NaHCO 3 + NiSO 4 NiCO 3 + NaHSO 4 Připravte 5g uhličitanu nikelnatého. Připravíme si 10% roztok hydrogenuhličitanu sodného a zahřejeme ho téměř k varu. Za stálého míchání
Ústřední komise Chemické olympiády. 55. ročník 2018/2019 ŠKOLNÍ KOLO. Kategorie C ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ)
 Ústřední komise Chemické olympiády 55. ročník 2018/2019 ŠKOLNÍ KOLO Kategorie C ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ) PRAKTICKÁ ČÁST 40 BODŮ Autor RNDr. Jan Břížďala Gymnázium Třebíč RNDr. Jan Havlík, Ph.D.
Ústřední komise Chemické olympiády 55. ročník 2018/2019 ŠKOLNÍ KOLO Kategorie C ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ) PRAKTICKÁ ČÁST 40 BODŮ Autor RNDr. Jan Břížďala Gymnázium Třebíč RNDr. Jan Havlík, Ph.D.
DĚLÍCÍ METODY. Autor: Mgr. Stanislava Bubíková. Datum (období) tvorby: 28. 5. 2012. Ročník: osmý. Vzdělávací oblast: Člověk a příroda / Chemie / Směsi
 Autor: Mgr. Stanislava Bubíková DĚLÍCÍ METODY Datum (období) tvorby: 28. 5. 2012 Ročník: osmý Vzdělávací oblast: Člověk a příroda / Chemie / Směsi 1 Anotace: Žáci se seznámí s nejčastěji používanými separačními
Autor: Mgr. Stanislava Bubíková DĚLÍCÍ METODY Datum (období) tvorby: 28. 5. 2012 Ročník: osmý Vzdělávací oblast: Člověk a příroda / Chemie / Směsi 1 Anotace: Žáci se seznámí s nejčastěji používanými separačními
ORGANICKÁ CHEMIE Laboratorní práce č. 3
 Téma: Hydroxyderiváty uhlovodíků ORGANICKÁ CHEMIE Laboratorní práce č. 3 Úkol 1: Dokažte přítomnost ethanolu ve víně. Ethanol bezbarvá kapalina, která je základní součástí alkoholických nápojů. Ethanol
Téma: Hydroxyderiváty uhlovodíků ORGANICKÁ CHEMIE Laboratorní práce č. 3 Úkol 1: Dokažte přítomnost ethanolu ve víně. Ethanol bezbarvá kapalina, která je základní součástí alkoholických nápojů. Ethanol
ORGANICKÁ CHEMIE Laboratorní práce č. 4 Téma: Karbonylové sloučeniny, karboxylové kyseliny
 ORGANICKÁ CHEMIE Laboratorní práce č. 4 Téma: Karbonylové sloučeniny, karboxylové kyseliny Úkol 1: Připravte acetaldehyd. Karbonylová skupina aldehydů podléhá velmi snadno oxidaci až na skupinu karboxylovou.
ORGANICKÁ CHEMIE Laboratorní práce č. 4 Téma: Karbonylové sloučeniny, karboxylové kyseliny Úkol 1: Připravte acetaldehyd. Karbonylová skupina aldehydů podléhá velmi snadno oxidaci až na skupinu karboxylovou.
Bakteriální bioluminiscenční test. Stanovení účinnosti čištění odpadních vod pomocí bakteriálního bioluminiscenčního testu
 Bakteriální bioluminiscenční test Stanovení účinnosti čištění odpadních vod pomocí bakteriálního bioluminiscenčního testu BBTT Cíl: Stanovit účinek odpadních vod na bakterie Vibrio fischeri. Principem
Bakteriální bioluminiscenční test Stanovení účinnosti čištění odpadních vod pomocí bakteriálního bioluminiscenčního testu BBTT Cíl: Stanovit účinek odpadních vod na bakterie Vibrio fischeri. Principem
2. Laboratorní den Příprava jodičnanu draselného oxidačně-redukční reakce v roztoku. 15 % přebytek KMnO 4. jméno: datum:
 2. Laboratorní den 2.2.4. Příprava jodičnanu draselného oxidačně-redukční reakce v roztoku Str. 91 správné provedení oxidačně-redukční reakce v roztoku krystalizace produktu z připraveného roztoku soli
2. Laboratorní den 2.2.4. Příprava jodičnanu draselného oxidačně-redukční reakce v roztoku Str. 91 správné provedení oxidačně-redukční reakce v roztoku krystalizace produktu z připraveného roztoku soli
Reakce kyselin a zásad
 seminář 6. 1. 2011 Chemie Reakce kyselin a zásad Známe několik teorií, které charakterizují definují kyseliny a zásady. Nejstarší je Arrheniova teorie, která je platná pro vodné prostředí, podle které
seminář 6. 1. 2011 Chemie Reakce kyselin a zásad Známe několik teorií, které charakterizují definují kyseliny a zásady. Nejstarší je Arrheniova teorie, která je platná pro vodné prostředí, podle které
Jednotné pracovní postupy zkoušení krmiv STANOVENÍ OBSAHU MYKOTOXINŮ METODOU LC-MS - FUMONISIN B 1 A B 2
 Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU MYKOTOXINŮ METODOU LC-MS - FUMONISIN B 1 A B 2 1 Rozsah a účel Metoda je vhodná pro stanovení fumonisinů B 1 a B 2 v krmivech. 2 Princip Fumonisiny
Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU MYKOTOXINŮ METODOU LC-MS - FUMONISIN B 1 A B 2 1 Rozsah a účel Metoda je vhodná pro stanovení fumonisinů B 1 a B 2 v krmivech. 2 Princip Fumonisiny
 LEKCE 5 Krystalizace separace složek homogenních směsí - krystalizace druhy krystalizace: volná krystalizace rušená krystalizace frakční krystalizace krystalizace změnou složení rozpouštědla vykrývání
LEKCE 5 Krystalizace separace složek homogenních směsí - krystalizace druhy krystalizace: volná krystalizace rušená krystalizace frakční krystalizace krystalizace změnou složení rozpouštědla vykrývání
ÚSTAV ORGANICKÉ TECHNOLOGIE
 LABORATOŘ OBORU I ÚSTAV ORGANICKÉ TECHNOLOGIE (111) F Imobilizace na alumosilikátové materiály Vedoucí práce: Ing. Eliška Leitmannová, Ph.D. Umístění práce: laboratoř F07, F08 1 Úvod Imobilizace aktivních
LABORATOŘ OBORU I ÚSTAV ORGANICKÉ TECHNOLOGIE (111) F Imobilizace na alumosilikátové materiály Vedoucí práce: Ing. Eliška Leitmannová, Ph.D. Umístění práce: laboratoř F07, F08 1 Úvod Imobilizace aktivních
EU peníze středním školám digitální učební materiál
 EU peníze středním školám digitální učební materiál Číslo projektu: Číslo a název šablony klíčové aktivity: Tematická oblast, název DUMu: Autor: CZ.1.07/1.5.00/34.0515 III/2 Inovace a zkvalitnění výuky
EU peníze středním školám digitální učební materiál Číslo projektu: Číslo a název šablony klíčové aktivity: Tematická oblast, název DUMu: Autor: CZ.1.07/1.5.00/34.0515 III/2 Inovace a zkvalitnění výuky
Michaela Novotná. Mikrobiologický ústav AV ČR Laboratoř Biotransformací Praha
 Michaela ovotná 2006 Mikrobiologický ústav AV ČR Laboratoř Biotransformací Praha ZAVEDEÍ DVOJÉ VAZBY DO MOLEKULY DIYDROLYSERGOLU ÚVOD ámelové alkaloidy patří mezi farmakologicky významné přírodní látky.
Michaela ovotná 2006 Mikrobiologický ústav AV ČR Laboratoř Biotransformací Praha ZAVEDEÍ DVOJÉ VAZBY DO MOLEKULY DIYDROLYSERGOLU ÚVOD ámelové alkaloidy patří mezi farmakologicky významné přírodní látky.
Jednotné pracovní postupy zkoušení krmiv STANOVENÍ OBSAHU MYKOTOXINŮ METODOU HPLC - OCHRATOXIN A
 Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU MYKOTOXINŮ METODOU HPLC - OCHRATOXIN A 1 Rozsah a účel Metoda specifikuje podmínky pro stanovení ochratoxinu A v krmivech. 1 Ochratoxin A patří mezi
Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU MYKOTOXINŮ METODOU HPLC - OCHRATOXIN A 1 Rozsah a účel Metoda specifikuje podmínky pro stanovení ochratoxinu A v krmivech. 1 Ochratoxin A patří mezi
Jednotné pracovní postupy zkoušení krmiv STANOVENÍ OBSAHU VITAMÍNU A A VITAMÍNU E METODOU HPLC S UV DETEKCÍ
 Národní referenční laboratoř Strana 1 STANOENÍ OBSAHU ITAMÍNU A A ITAMÍNU E METODOU HPLC S U DETEKCÍ 1 Rozsah a účel Metoda je vhodná pro stanovení vitamínu A a vitamínu E v kompletních krmivech i premixech
Národní referenční laboratoř Strana 1 STANOENÍ OBSAHU ITAMÍNU A A ITAMÍNU E METODOU HPLC S U DETEKCÍ 1 Rozsah a účel Metoda je vhodná pro stanovení vitamínu A a vitamínu E v kompletních krmivech i premixech
Jednotné pracovní postupy zkoušení krmiv STANOVENÍ OBSAHU VÁPNÍKU MANGANOMETRICKY
 Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU VÁPNÍKU MANGANOMETRICKY 1 Rozsah a účel Tato metoda specifikuje podmínky pro stanovení celkového obsahu vápníku v krmivech, krmných směsích a premixech.
Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU VÁPNÍKU MANGANOMETRICKY 1 Rozsah a účel Tato metoda specifikuje podmínky pro stanovení celkového obsahu vápníku v krmivech, krmných směsích a premixech.
P + D PRVKY Laboratorní práce
 Téma: Reakce sloučenin zinku P + D PRVKY Laboratorní práce Pozn: Výsledky úkolu 1 zapisujte až po 14 dnech. Úkol 4 provádějte pouze pod dohledem učitele. Úkol 1: Připravte 5 gramů bílé skalice. Bílá skalice
Téma: Reakce sloučenin zinku P + D PRVKY Laboratorní práce Pozn: Výsledky úkolu 1 zapisujte až po 14 dnech. Úkol 4 provádějte pouze pod dohledem učitele. Úkol 1: Připravte 5 gramů bílé skalice. Bílá skalice
Návod k laboratornímu cvičení. Bílkoviny
 Úkol č. 1: Důkazy bílkovin ve vaječném bílku a) natvrdo uvařené vejce s kyselinou dusičnou Pomůcky: Petriho miska, pipeta, nůž. Návod k laboratornímu cvičení Bílkoviny Chemikálie: koncentrovaná kyselina
Úkol č. 1: Důkazy bílkovin ve vaječném bílku a) natvrdo uvařené vejce s kyselinou dusičnou Pomůcky: Petriho miska, pipeta, nůž. Návod k laboratornímu cvičení Bílkoviny Chemikálie: koncentrovaná kyselina
2.07 Krystalizace. Projekt Trojlístek
 2. Vlastnosti látek a chemické reakce 2.07 Krystalizace. Projekt úroveň 1 2 3 1. Předmět výuky Metodika je určena pro vzdělávací obsah vzdělávacího předmětu Chemie. Chemie 2. Cílová skupina Metodika je
2. Vlastnosti látek a chemické reakce 2.07 Krystalizace. Projekt úroveň 1 2 3 1. Předmět výuky Metodika je určena pro vzdělávací obsah vzdělávacího předmětu Chemie. Chemie 2. Cílová skupina Metodika je
Vybrané úlohy z toxikologie
 ÚSTAV LÉKAŘSKÉ BIOCHEMIE A LABORATORNÍ DIAGNOSTIKY 1. LF UK Vybrané úlohy z toxikologie Praktické cvičení z lékařské biochemie Všeobecné lékařství Martin Vejražka 2018/19 Obsah 1. TENKOVRSTEVNÁ CHROMATOGRAFIE
ÚSTAV LÉKAŘSKÉ BIOCHEMIE A LABORATORNÍ DIAGNOSTIKY 1. LF UK Vybrané úlohy z toxikologie Praktické cvičení z lékařské biochemie Všeobecné lékařství Martin Vejražka 2018/19 Obsah 1. TENKOVRSTEVNÁ CHROMATOGRAFIE
METODY ČIŠTĚNÍ ORGANICKÝCH LÁTEK
 METODY ČIŠTĚNÍ ORGANICKÝCH LÁTEK Chemické sloučeniny se připravují z jiných chemických sloučenin. Tento děj se nazývá chemická reakce, kdy z výchozích látek (reaktantů) vznikají nové látky (produkty).
METODY ČIŠTĚNÍ ORGANICKÝCH LÁTEK Chemické sloučeniny se připravují z jiných chemických sloučenin. Tento děj se nazývá chemická reakce, kdy z výchozích látek (reaktantů) vznikají nové látky (produkty).
Spektrofotometrické stanovení fosforečnanů ve vodách
 Spektrofotometrické stanovení fosforečnanů ve vodách Úkol: Spektrofotometricky stanovte obsah fosforečnanů ve vodě Chemikálie: 0,07165 g dihydrogenfosforečnan draselný KH 2 PO 4 75 ml kyselina sírová H
Spektrofotometrické stanovení fosforečnanů ve vodách Úkol: Spektrofotometricky stanovte obsah fosforečnanů ve vodě Chemikálie: 0,07165 g dihydrogenfosforečnan draselný KH 2 PO 4 75 ml kyselina sírová H
Praktické ukázky analytických metod ve vinařství
 Praktické ukázky analytických metod ve vinařství Ing. Mojmír Baroň Stanovení v moštu Stanovení ph a veškerých titrovatelných kyselin Stanovení ph Princip: Hodnota ph je záporný dekadický logaritmus aktivity
Praktické ukázky analytických metod ve vinařství Ing. Mojmír Baroň Stanovení v moštu Stanovení ph a veškerých titrovatelných kyselin Stanovení ph Princip: Hodnota ph je záporný dekadický logaritmus aktivity
Jazykové gymnázium Pavla Tigrida, Ostrava-Poruba Název projektu: Podpora rozvoje praktické výchovy ve fyzice a chemii
 Datum: Jazykové gymnázium Pavla Tigrida, Ostrava-Poruba Název projektu: Podpora rozvoje praktické výchovy ve fyzice a chemii Laboratorní cvičení č. Tlak vzduchu: Teplota vzduchu: Vitamíny Vlhkost vzduchu
Datum: Jazykové gymnázium Pavla Tigrida, Ostrava-Poruba Název projektu: Podpora rozvoje praktické výchovy ve fyzice a chemii Laboratorní cvičení č. Tlak vzduchu: Teplota vzduchu: Vitamíny Vlhkost vzduchu
Jednotné pracovní postupy zkoušení krmiv STANOVENÍ OBSAHU AMINOKYSELIN
 Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU AMINOKYSELIN 1 Rozsah a účel Tato metoda specifikuje podmínky pro stanovení aminokyselin kyseliny asparagové, threoninu, serinu, kyseliny glutamové,
Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU AMINOKYSELIN 1 Rozsah a účel Tato metoda specifikuje podmínky pro stanovení aminokyselin kyseliny asparagové, threoninu, serinu, kyseliny glutamové,
Návod k laboratornímu cvičení. Alkaloidy a steroidy
 Návod k laboratornímu cvičení Úkol č. 1: Sublimace kofeinu Alkaloidy a steroidy Pomůcky: 2 hodinová sklíčka, elektrický vařič, siťka, stojan s kruhem, filtrační papír Chemikálie: suché čajové lístky (černý,
Návod k laboratornímu cvičení Úkol č. 1: Sublimace kofeinu Alkaloidy a steroidy Pomůcky: 2 hodinová sklíčka, elektrický vařič, siťka, stojan s kruhem, filtrační papír Chemikálie: suché čajové lístky (černý,
LP č. 6 - BÍLKOVINY. Autor: Mgr. Stanislava Bubíková. Datum (období) tvorby: 28. 2. 2013. Ročník: devátý
 LP č. 6 - BÍLKOVINY Autor: Mgr. Stanislava Bubíková Datum (období) tvorby: 28. 2. 2013 Ročník: devátý Vzdělávací oblast: Člověk a příroda / Chemie / Organické sloučeniny 1 Anotace: Žáci prakticky ověří
LP č. 6 - BÍLKOVINY Autor: Mgr. Stanislava Bubíková Datum (období) tvorby: 28. 2. 2013 Ročník: devátý Vzdělávací oblast: Člověk a příroda / Chemie / Organické sloučeniny 1 Anotace: Žáci prakticky ověří
Jazykové gymnázium Pavla Tigrida, Ostrava-Poruba Název projektu: Podpora rozvoje praktické výchovy ve fyzice a chemii
 Datum: Jazykové gymnázium Pavla Tigrida, Ostrava-Poruba Název projektu: Podpora rozvoje praktické výchovy ve fyzice a chemii Laboratorní cvičení č. Tlak vzduchu: Teplota vzduchu: Vodík a kyslík Vlhkost
Datum: Jazykové gymnázium Pavla Tigrida, Ostrava-Poruba Název projektu: Podpora rozvoje praktické výchovy ve fyzice a chemii Laboratorní cvičení č. Tlak vzduchu: Teplota vzduchu: Vodík a kyslík Vlhkost
Ústřední komise Chemické olympiády. 42. ročník. KRAJSKÉ KOLO Kategorie D. SOUTĚŽNÍ ÚLOHY TEORETICKÉ ČÁSTI Časová náročnost: 60 minut
 Ústřední komise Chemické olympiády 42. ročník 2005 2006 KRAJSKÉ KOLO Kategorie D SOUTĚŽNÍ ÚLOHY TEORETICKÉ ČÁSTI Časová náročnost: 60 minut Institut dětí a mládeže Ministerstva školství, mládeže a tělovýchovy
Ústřední komise Chemické olympiády 42. ročník 2005 2006 KRAJSKÉ KOLO Kategorie D SOUTĚŽNÍ ÚLOHY TEORETICKÉ ČÁSTI Časová náročnost: 60 minut Institut dětí a mládeže Ministerstva školství, mládeže a tělovýchovy
Odborná práce přírodovědného kroužku Gymnázia Jana Opletala Litovel, Opletalova 189. Sacharidy
 Odborná práce přírodovědného kroužku Gymnázia Jana Opletala Litovel, Opletalova 189 Sacharidy Vypracovali: Jana Andrýsková, Aneta Čulíková, Jan Dvořáček, David Hrachovina, Petra Hrachovinová, Eva Podivínská,
Odborná práce přírodovědného kroužku Gymnázia Jana Opletala Litovel, Opletalova 189 Sacharidy Vypracovali: Jana Andrýsková, Aneta Čulíková, Jan Dvořáček, David Hrachovina, Petra Hrachovinová, Eva Podivínská,
Roztok je homogenní (stejnorodá) směs dvou a více látek. Částice, které tvoří roztok, jsou dokonale rozptýleny a vzájemně nereagují.
 ROZTOKY Roztok je homogenní (stejnorodá) směs dvou a více látek. Částice, které tvoří roztok, jsou dokonale rozptýleny a vzájemně nereagují. Roztoky podle skupenství dělíme na: a) plynné (čistý vzduch)
ROZTOKY Roztok je homogenní (stejnorodá) směs dvou a více látek. Částice, které tvoří roztok, jsou dokonale rozptýleny a vzájemně nereagují. Roztoky podle skupenství dělíme na: a) plynné (čistý vzduch)
Ministerstvo školství, mládeže a tělovýchovy Ústřední komise Chemické olympiády. 46. ročník 2009/2010. KRAJSKÉ KOLO kategorie D
 Ministerstvo školství, mládeže a tělovýchovy Ústřední komise Chemické olympiády 46. ročník 2009/2010 KRAJSKÉ KOLO kategorie D ŘEŠENÍ SOUTĚŽNÍCH ÚLOH TEORETICKÁ ČÁST (60 bodů) Úloha 1 Vlastnosti prvků 26
Ministerstvo školství, mládeže a tělovýchovy Ústřední komise Chemické olympiády 46. ročník 2009/2010 KRAJSKÉ KOLO kategorie D ŘEŠENÍ SOUTĚŽNÍCH ÚLOH TEORETICKÁ ČÁST (60 bodů) Úloha 1 Vlastnosti prvků 26
Chemie. Mgr. Petra Drápelová Mgr. Jaroslava Vrbková. Gymnázium, SOŠ a VOŠ Ledeč nad Sázavou
 Chemie Mgr. Petra Drápelová Mgr. Jaroslava Vrbková Gymnázium, SOŠ a VOŠ Ledeč nad Sázavou Směsi VY_32_INOVACE_03_3_01_CH Gymnázium, SOŠ a VOŠ Ledeč nad Sázavou SMĚSI Směsi jsou složitější látky, které
Chemie Mgr. Petra Drápelová Mgr. Jaroslava Vrbková Gymnázium, SOŠ a VOŠ Ledeč nad Sázavou Směsi VY_32_INOVACE_03_3_01_CH Gymnázium, SOŠ a VOŠ Ledeč nad Sázavou SMĚSI Směsi jsou složitější látky, které
téma: Halogeny-úvod autor: Ing. František Krejčí, CSc. cíl praktika: žáci si osvojí znalosti z chemie halogenů doba trvání: 2 h
 téma: Halogeny-úvod cíl praktika: žáci si osvojí znalosti z chemie halogenů pomůcky: psací potřeby popis aktivit: Žáci si osvojí problematiku halogenů, popíší jejich elektronovou konfiguraci a z ní vyvodí
téma: Halogeny-úvod cíl praktika: žáci si osvojí znalosti z chemie halogenů pomůcky: psací potřeby popis aktivit: Žáci si osvojí problematiku halogenů, popíší jejich elektronovou konfiguraci a z ní vyvodí
ÚLOHA č.5 STANOVENÍ SÍRY METODA PODLE SCHÖNIGERA
 1 ÚLOHA č.5 STANOVENÍ SÍRY METODA PODLE SCHÖNIGERA 5.1. PRINCIP METODY Společným rysem metod pro stanovení síry je mineralizace organické sloučeniny a převedení organicky vázané síry na jednotnou formu
1 ÚLOHA č.5 STANOVENÍ SÍRY METODA PODLE SCHÖNIGERA 5.1. PRINCIP METODY Společným rysem metod pro stanovení síry je mineralizace organické sloučeniny a převedení organicky vázané síry na jednotnou formu
Jednotné pracovní postupy zkoušení krmiv
 Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU -KAROTENU METODOU HPLC 1 Účel a rozsah Postup specifikuje podmínky pro stanovení celkového -karotenu v krmivech a premixech metodou vysokoúčinné kapalinové
Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU -KAROTENU METODOU HPLC 1 Účel a rozsah Postup specifikuje podmínky pro stanovení celkového -karotenu v krmivech a premixech metodou vysokoúčinné kapalinové
Jazykové gymnázium Pavla Tigrida, Ostrava-Poruba Název projektu: Podpora rozvoje praktické výchovy ve fyzice a chemii
 Datum: Jazykové gymnázium Pavla Tigrida, Ostrava-Poruba Název projektu: Podpora rozvoje praktické výchovy ve fyzice a chemii Laboratorní cvičení č. Tlak vzduchu: Teplota vzduchu: Bílkoviny(proteiny) Vlhkost
Datum: Jazykové gymnázium Pavla Tigrida, Ostrava-Poruba Název projektu: Podpora rozvoje praktické výchovy ve fyzice a chemii Laboratorní cvičení č. Tlak vzduchu: Teplota vzduchu: Bílkoviny(proteiny) Vlhkost
13/sv. 8 (85/503/EHS) Tato směrnice je určena členským státům.
 62 31985L0503 L 308/12 ÚŘEDNÍ VĚSTNÍK EVROPSKÝCH SPOLEČENSTVÍ 20.11.1985 PRVNÍ SMĚRNICE KOMISE ze dne 25. října 1985 o metodách pro analýzu potravinářských kaseinů a kaseinátů (85/503/EHS) KOMISE EVROPSKÝCH
62 31985L0503 L 308/12 ÚŘEDNÍ VĚSTNÍK EVROPSKÝCH SPOLEČENSTVÍ 20.11.1985 PRVNÍ SMĚRNICE KOMISE ze dne 25. října 1985 o metodách pro analýzu potravinářských kaseinů a kaseinátů (85/503/EHS) KOMISE EVROPSKÝCH
Neutralizace kyseliny zásadou
 Neutralizace kyseliny zásadou Metodický list pro učitele Časový harmonogram a) doba na přípravu - 10 minut b) doba na provedení - 15 minut Pomůcky a) chemikálie - kyselina chlorovodíková - hydroxid sodný
Neutralizace kyseliny zásadou Metodický list pro učitele Časový harmonogram a) doba na přípravu - 10 minut b) doba na provedení - 15 minut Pomůcky a) chemikálie - kyselina chlorovodíková - hydroxid sodný
FYZIKÁLNÍ A CHEMICKÝ ROZBOR PITNÉ VODY
 LABORATORNÍ PRÁCE Č. 13 FYZIKÁLNÍ A CHEMICKÝ ROZBOR PITNÉ VODY PRINCIP V přírodě se vyskytující voda není nikdy čistá, obsahuje vždy určité množství rozpuštěných látek, plynů a nerozpuštěných pevných látek.
LABORATORNÍ PRÁCE Č. 13 FYZIKÁLNÍ A CHEMICKÝ ROZBOR PITNÉ VODY PRINCIP V přírodě se vyskytující voda není nikdy čistá, obsahuje vždy určité množství rozpuštěných látek, plynů a nerozpuštěných pevných látek.
Sešit pro laboratorní práci z chemie
 Sešit pro laboratorní práci z chemie téma: Oddělování složek směsí autor: MVDr. Alexandra Gajová vytvořeno při realizaci projektu: Inovace školního vzdělávacího programu biologie a chemie registrační číslo
Sešit pro laboratorní práci z chemie téma: Oddělování složek směsí autor: MVDr. Alexandra Gajová vytvořeno při realizaci projektu: Inovace školního vzdělávacího programu biologie a chemie registrační číslo
Reakce organických látek
 Pavel Lauko 5.2.2002 DI I. roč. 3.sk. Reakce organických látek 1. Příprava methanu dekarboxylací octanu sodného Roztoky a materiál: octan sodný, natronové vápno, manganistan draselný, cyklohexan. Postup:
Pavel Lauko 5.2.2002 DI I. roč. 3.sk. Reakce organických látek 1. Příprava methanu dekarboxylací octanu sodného Roztoky a materiál: octan sodný, natronové vápno, manganistan draselný, cyklohexan. Postup:
Obrázek 3: Zápis srážecí reakce
 VG STUDENT CHEMIE T É M A: SRÁŽENÍ, IZOLACE SRAŽENIN Vypracoval/a: Spolupracoval/a: Třída: Datum: ANOTACE: V této laboratorní práci se žáci seznámí s pojmem sraženina a srážení, provedou srážení jodidu
VG STUDENT CHEMIE T É M A: SRÁŽENÍ, IZOLACE SRAŽENIN Vypracoval/a: Spolupracoval/a: Třída: Datum: ANOTACE: V této laboratorní práci se žáci seznámí s pojmem sraženina a srážení, provedou srážení jodidu
ODMĚRNÁ ANALÝZA - TITRACE
 LABORATORNÍ PRÁCE Č. 35 ODMĚRNÁ ANALÝZA - TITRACE PRINCIP Odměrnou analýzou (titrací) se stanovuje obsah určité složky ve vzorku. Podstatou odměrného stanovení je chemická reakce mezi odměrným roztokem
LABORATORNÍ PRÁCE Č. 35 ODMĚRNÁ ANALÝZA - TITRACE PRINCIP Odměrnou analýzou (titrací) se stanovuje obsah určité složky ve vzorku. Podstatou odměrného stanovení je chemická reakce mezi odměrným roztokem
CHEMICKÉ VÝPOČTY I. ČÁST LÁTKOVÉ MNOŽSTVÍ. HMOTNOSTI ATOMŮ A MOLEKUL.
 CHEMICKÉ VÝPOČTY I. ČÁST LÁTKOVÉ MNOŽSTVÍ. HMOTNOSTI ATOMŮ A MOLEKUL. Látkové množství Značka: n Jednotka: mol Definice: Jeden mol je množina, která má stejný počet prvků, jako je atomů ve 12 g nuklidu
CHEMICKÉ VÝPOČTY I. ČÁST LÁTKOVÉ MNOŽSTVÍ. HMOTNOSTI ATOMŮ A MOLEKUL. Látkové množství Značka: n Jednotka: mol Definice: Jeden mol je množina, která má stejný počet prvků, jako je atomů ve 12 g nuklidu
Výukový materiál zpracován v rámci projektu. EU peníze školám. Registrační číslo projektu: CZ.1.07/1.5.00/34.0996
 Výukový materiál zpracován v rámci projektu EU peníze školám Registrační číslo projektu: CZ.1.07/1.5.00/34.0996 Šablona: III/2 č. materiálu: VY_INOVACE_CHE_417 Jméno autora: Třída/ročník: Mgr. Alena Krejčíková
Výukový materiál zpracován v rámci projektu EU peníze školám Registrační číslo projektu: CZ.1.07/1.5.00/34.0996 Šablona: III/2 č. materiálu: VY_INOVACE_CHE_417 Jméno autora: Třída/ročník: Mgr. Alena Krejčíková
