Chem. Listy 104, (2010) H 3 C NH 2. AcOH
|
|
|
- Jiří Viktor Havel
- před 9 lety
- Počet zobrazení:
Transkript
1 SLEDVÁNÍ ZPŮSBU VAZBY MDELVÝCH LÁTEK NA NANČÁSTICE STŘÍBRA CH 3 H 3 C NH 2 N CH 3 MENH2 H 3 C ET3EN N PYR PAVEL ŽVÁTRA*, PAVEL ŘEZANKA, KAMIL ZÁRUBA a VLADIMÍR KRÁL Ústav analytické chemie, Vysoká škola chemickotechnologická v Praze, Technická 5, Praha 6 pavel.zvatora@vscht.cz Došlo , přepracováno , přijato H 3 C C4SH H 3 C H AcH SH H 3 C H C12SH SH H Klíčová slova: nanočástice stříbra, interakce s povrchem, SERS, koloidní roztok, H 3MPA SH BZA S S LIPA Úvod Přímá imobilizace analyticky užitečných receptorů na povrchu nanočástic často není možná, protože neobsahují vhodné funkční skupiny. Proto je nutná předřazená povrchová modifikace multifunkčními molekulami (spacery 1,2 ). Jedna funkční skupina je využita pro vazbu na povrch nanočástice, zatímco další, prostorově volná, umožní imobilizaci požadovaného receptoru. Z těchto důvodů je vhodné věnovat se studiu modifikace nanočástic stříbra látkami s různými funkčními skupinami tak, aby při následné modifikaci bylo zřejmé, za jakých podmínek se daná funkční skupina váže nebo s povrchem neinteraguje. Asi nejznámější je vazba thiolových derivátů 3, na povrch nanočástic stříbra se ale váží i aminy a dusíkaté heterocykly 4 a s povrchem interagují i karboxylové deriváty 5. Některé z těchto látek (citrát sodný) lze pak použít při přípravě a stabilizaci koloidních roztoků nanočástic ušlechtilých kovů 6,7. Tvar a velikost nanočástic, tedy i vlastnosti povrchu, souvisí se zvolenou metodou přípravy. Tyto faktory mají zásadní vliv na fyzikální a chemické vlastnosti nanočástic. Vhodnou metodou sledování jejich povrchové modifikace je spektroskopie povrchem zesíleného Ramanova rozptylu (SERS). Jde o techniku, při které dochází k interakci excitujícího laserového záření s povrchovými elektrony některých kovů, mezi něž patří stříbro, zlato a měď. Při vhodné morfologii kovu a vhodné vlnové délce excitujícího záření dochází k řádovému zesílení Ramanova rozptylu 8. Intenzita měřeného signálu závisí na vzdálenosti molekuly od povrchu nanočástice a s rostoucí vzdáleností výrazně klesá. br. 1. Struktury modelových látek použitých v této práci. (MENH2) methylamin; (ET3EN) triethylamin; (PYR) pyridin; (C4SH) butanthiol; (C10SH) dodekanthiol; (AcH) octová kyselina; (BZA) benzoová kyselina; (LIPA) lipoová kyselina; (3MPA) 3-merkaptopropanová kyselina V této práci byl sledován vliv koncentrace modelových látek (obr. 1) a vliv ph na způsob jejich vazby na povrch nanočástic stříbra stabilizovaných citrátem. Modelové látky byly vybrány tak, aby jejich struktury a vazebné schopnosti pokryly co možná nejširší oblast molekul, které by bylo možné použít pro zprostředkování imobilizace analyticky užitečných receptorů. Experimentální část Chemikálie a zařízení Všechny použité chemikálie byly čistoty p.a. Pro přípravu nanočástic byla použita voda od firmy Merck (LiChrosolv, R = 1 M ). Absorpční spektra byla měřena na přístroji Varian Cary 400 SCAN. Měření bylo prováděno ve skleněné kyvetě o tloušťce 1 cm v rozsahu 200 až 900 nm s krokem 1 nm a v rozsahu 375 až 475 nm s krokem 0,25 nm. Ramanova spektra byla změřena pomocí Ramanova spektrometru (Deltanu Advantage 785 Near- Infrared Raman Spectrometer). Vlnová délka excitačního laserového zdroje byla 785 nm, měřící rozsah cm 1. K interpretaci Ramanových spekter byla použita výpočetní metoda ab-initio. ptimalizace molekul a výpočty spekter byly prováděny programem Gaussian 9. Pou- * Pavel Žvátora získal zvláštní cenu poroty v soutěži o cenu firmy Merck 2008 za nejlepší studentskou vědeckou práci v oboru analytická chemie. 202
2 žitá metoda a báze byla B3LYP/6-31G*. Vypočtená spektra byla porovnána s naměřenými spektry, kdy byly identifikovány nejintenzivnější pásy. Z důvodu posunu vlnočtu při imobilizaci nebo interakci s citrátem bylo v případě podobnosti obou spekter vypočtené spektrum vynásobeno korelačním faktorem 0,96 v ose x. Centrifugace byly prováděny v umělohmotných zkumavkách o objemu 2 ml na centrifuze Eppendorf Centrifuge Vzorky byly odstředěny při otáčkách za minutu po dobu 10 min (odstředivé zrychlení m s 2 ). Sonifikace byla prováděna v ultrazvukové lázni Transsonic 570 (Elma, Německo) při 35 khz. Při měření ph byl používán ph-metr Mettler Toledo s kombinovanou skleněnou elektrodou (InlayÒ 413). Přístroj byl kalibrován pufry o třech hodnotách ph (4,01, 7,00 a 10,00; Merck). Výsledky a diskuse Příprava nanočástic stříbra Nanočástice byly připraveny redukcí AgN 3 citrátem sodným za varu 6. Takto připravené nanočástice poskytovaly dobrý signál v SERS. Touto metodou byly připraveny koloidní roztoky stříbra s širokou distribucí velikosti částic převážně kulovitého tvaru (obr. 2). Maximum absorbance a b Příprava nanočástic Byly připraveny roztoky nanočástic stříbra vzniklé redukcí AgN 3 citrátem sodným. Roztoky byly po přípravě ponechány jeden den v temnu. Ke 2 ml roztoku nanočástic byl poté přidán vodný roztok modelové látky (výsledná koncentrace byla 1, , 3, , 9, , 2, , 5, a 1, mol l 1 ) a výsledný roztok byl po modifikaci ponechán 24 h v temnu. V případě analýzy necentrifugovaných nanočástic bylo změřeno Ramanovo spektrum a pro měření UV-Vis absorpčního spektra byl roztok, z důvodu zachování platnosti Lambertova-Beerova zákona, před měřením 10 zředěn vodou. V případě analýzy centrifugovaných nanočástic byl roztok modifikovaných nanočástic centrifugován, redispergován (v ultrazvukové lázni) v původním objemu vody a poté bylo změřeno Ramanovo spektrum. Pro měření UV-Vis absorpčního spektra byl roztok před měřením 10 zředěn vodou. Při studiu vlivu ph na imobilizaci AcH a 3MPA byly užity dva různé postupy, které se lišily okamžikem přidání látky k roztoku nanočástic a okamžikem, kdy bylo upravováno ph. V prvním případě byla přidána studovaná látka a po 24 h v temnu byly modifikované nanočástice odcentrifugovány a redispergovány ve vodném roztoku HCl nebo NaH podle požadované hodnoty ph. Ve druhém experimentu byl nejprve roztok nemodifikovaných nanočástic odcentrifugován a redispergován ve vodném roztoku HCl nebo NaH podle požadované hodnoty ph. K takto připravenému roztoku nemodifikovaných nanočástic byl přidán vodný roztok studovaných látek a spektra byla měřena po 24 h. V obou případech byly koncentrace látek v měřených roztocích 1, , 9, a 5, mol l 1. Nastavované hodnoty ph byly 1, 4, 7, 10 a 13. Skutečná hodnota ph byla zjišťována pomocí ph-metru. Interakce AcH a 3MPA byly sledovány UV-Vis spektroskopií a povrchem zesíleného Ramanova rozptylu (SERS). Podmínky měření byly shodné jako v předchozím případě. c br. 2. a) Fotografie nanočástic stříbra (TEM); b) rozdělení velikosti těchto nanočástic; c) UV-Vis absorpční spektru nanočástic stříbra připravených redukcí citrátem sodným br. 3. Ramanovo spektrum citrátu (B) (c = mol l 1 ) a SERS spektrum citrátu (A) na povrchu nanočástic stříbra. Jednotlivé označené pásy odpovídají spektru citrátu imobilizovaného na povrchu nanočástic stříbra
3 Tabulka I Hodnoty absorbance a změny vlnové délky absorpčního maxima ( 430 nm) roztoku nanočástic stříbra v závislosti na koncentraci přidané látky. Roztoky nanočástic nebyly přečištěny centrifugací Vazebný atom Látka Koncentrace [mol l 1 ] 1, , , , , , A/ A/ A/ A/ A/ A/ N MENH2 0,666 / 1 0,790 / 2 0,754 / 1 0,742 / 0 0,714 / 6 0,804 / 6 ET3EN 0,750 / 1 0,778 / 3 0,780 / 2 0,753 / 3 0,778 / 3 0,798 / 3 PYR 1,060 / 3 1,099 / 3 1,108 / 3 1,060 / 3 1,091 / 3 1,118 / 3 S C4SH 0,141 / 13 0,175 / 7 0,132 / 1 0,158 / 4 0,495 / 10 0,747 / 7 C12SH 0,714 / 0 0,774 / 0 0,801 / 1 0,790 / 0 0,821 / 1 0,750 / 0 AcH 0,499 / 3 0,653 / 1 0,695 / 2 0,718 / 1 0,729 / 2 0,772 / 1 BZA 0,974 / 4 1,025 / 2 1,096 / 2 1,114 / 2 1,098 / 2 1,114 / 2 /S LIP 0,239 / 14 0,747 / 5 0,787 / 2 0,764 / 2 0,696 / 1 0,713 / 1 3MPA 0,301 / 18 0,836 / 10 0,970 / 12 0,528 / 5 1,002 / 0 1,014 / 2 Tabulka II Hodnoty absorbance a změny vlnové délky absorpčního maxima ( 430 nm) roztoku nanočástic stříbra v závislosti na koncentraci přidané látky. Roztoky nanočástic byly přečištěny centrifugací Vazebný atom Látka Koncentrace [mol l 1 ] 1, , , , , , A/ A/ A/ A/ A/ A/ N MENH2 0,438 / 5 0,484 / 5 0,424 / 5 0,435 / 5 0,328 / 5 0,453 / 5 ET3EN 0,252 / 5 0,277 / 7 0,179 / 8 0,237 / 12 0,155 / 8 0,145 / 9 PYR 0,787 / 0 0,777 / 1 0,802 / 1 0,848 / 1 0,644 / 1 0,859 / 1 S C4SH 0,116 / 4 0,122 / 7 0,144 / 10 0,160 / 10 0,252 / 11 0,575 / 10 C12SH 0,306 / 0 0,441 / 1 0,414 / 1 0,373 / 1 0,418 / 2 0,406 / 1 AcH 0,216 / 8 0,281 / 4 0,367 / 0 0,367 / 1 0,333 / 2 0,442 / 2 BZA 0,404 / 7 0,674 / 3 0,859 / 1 0,870 / 1 0,752 / 2 0,855 / 0 /S LIP 0,227 / 11 0,384 / 2 0,557 / 3 0,501 / 3 0,410 / 0 0,276 / 1 3MPA 0,310 / 19 0,418 / 8 0,720 / 12 0,197 / 12 0,684 / 2 0,639 / 2 takto připravených nanočástic se pohybovalo od 415 do 430 nm. Na obr. 3 je Ramanovo spektrum vodného roztoku citrátu sodného a SERS spektrum citrátu absorbovaného na povrchu nanočástic 10. Koncentrace byla v obou případech stejná. Díky povrchovému zesílení stříbrných nanočástic byly v SERS spektru pozorovány intenzivní signály citrátu. Vliv koncentrace modelových látek na UV-Vis absorpční spektra nanočástic stříbra Byla změřena UV-Vis absorpční spektra připravených roztoků nanočástic jak před modifikací, tak po jejím provedení. Nanočástice byly modifikovány modelovými látkami a výsledky jsou shrnuty v tab. I a II. Přídavek látek ve všech případech způsobil změnu maximální hodnoty absorbance a v řadě případů i posun vlnové délky tohoto maxima 11. interakci studovaných látek s povrchem nanočástic svědčí také to, že posuny vlnové délky absorpčního maxima byly naměřeny i v roztocích modifikovaných nanočástic po centrifugaci, čímž byly z roztoku odstraněny látky nenavázané na povrch nanočástic. Vliv koncentrace modelových látek na SERS nanočástic stříbra V případě modifikace stříbrných nanočástic dusíkatými látkami (MENH2, ET3EN, PYR), došlo k výraznému snížení intenzity SERS signálu (obr. 4) oproti nemodifiko- 204
4 br. 4. SERS spektra (A PYR, B MENH2, C AcH, D nanočástice stříbra), koncentrace látek byla 1, mol l 1. Pásy spektra (D) odpovídají spektru citrátu imobilizovaného na povrchu nanočástic stříbra br. 6. SERS spektra imobilizované 3MPA při koncentraci A) 1, mol l 1 ; B) 9, mol l 1 ; C) 1, mol l 1 vaným nanočásticím, v jejichž spektrech jsou patrny pásy citrátu. V případě látek s jedinou možnou vazbou přes kyslík (AcH a BZA) byly v SERS spektru pozorovány signály citrátu s malými změnami (obr. 4). Změny ve spektrech mohou být způsobeny řadou faktorů, např. možnou interakcí citrátu s karboxylovými kyselinami nebo dusíkatými látkami (MENH2, ET3EN, PYR), nebo částečnou agregací roztoku nanočástic vlivem změny iontové síly tohoto roztoku spolu se změnou ph. Interakce látek vázajících se výhradně přes atom síry (C4SH a C12SH) byla potvrzena posunem valenční vibrace CS z 652 cm 1 v čisté látce (C4SH a C12SH) na 699 cm 1 (C4SH), resp. 741 cm 1 (C12SH). Signál u 699 cm 1 odpovídá konformaci gauche a signál u 741 cm 1 odpovídá konformaci trans (cit. 1 ). V případě látky LIPA byla provázena její vazba na povrch nanočástic absencí valenčního pásu SS (451 cm 1 ) a pásu valenční vibrace cyklu (507 cm 1 ). Toto naznačuje, že se látka vázala na stříbrný povrch přes atomy síry 8. Vazba látky 3MPA přes atom síry byla potvrzena absencí valenčně vibračního pásu CS (670 cm 1 ), který se rozštěpil na dva nové pásy s vlnočty 734 cm 1 a 655 cm 1. Ty přísluší valenčním vibracím CS trans u 734 cm 1 a CS gauche u 655 cm 1 (cit. 1 ) (obr. 5 a 6). Na obr. 6 je také zřetelný pás valenční vibrace C-C u 930 cm 1, který byl přítomen při všech koncentracích. Absence pásu C-CH u 900 cm 1 znamená, že veškerá imobilizovaná látka 3MPA byla přítomna v disociované formě, nezávisle na její koncentraci 1. Vliv ph na UV-Vis absorpční spektra nanočástic stříbra modifikovaných látkami AcH a 3MPA Stabilita citrátových nanočástic stříbra je znázorněna na obr. 7. Hodnota ph byla nastavována roztoky NaH a HCl a změřena ph-metrem. Poté byla změřena UV-Vis absorpční spektra a SERS spektra. Normalizovaná absorbance (obr. 7) byla získána tak, že byl nejprve vypočten rozdíl absorbance roztoku nanočástic po úpravě ph v jejich absorpčním maximu a absorbance u paty tohoto pásu ( max 320 nm). Výsledný rozdíl byl dále dělen hod- A/A 0 1,0 0,8 0,6 0,4 A B 0,2 0, ph br. 5. Schematické znázornění konformace trans a gauche 3MPA imobilizované na povrchu nanočástic stříbra br. 7. Závislost normalizované absorbance ( A/A 0 ) nemodifikovaných citrátových nanočástic. Citrátové nanočástice po úpravě ph pomocí roztoků HCl a NaH (A). Vodný roztok nanočástic stříbra připravených redukcí AgN 3 citrátem sodným (B) 205
5 A/A 0 1,0 0,8 0,6 0,4 0,2 0, br. 8. Závislost normalizované absorbance čistých nanočástic (A) a roztoku těchto nanočástic s přídavky AcH na hodnotě ph. Koncentrace byla (B) 1, mol l 1 ; (C) 9, mol l 1 ; (D) 5, mol l 1. Hodnota ph byla nastavena až po přídavku AcH A B C D ph pufrační kapacitě roztoku nanočástic dochází k posunu ph jednotlivých roztoků směrem k disociační konstantě jednotlivých kyselin (pk a 4,8). Na rozdíl od obr. 7 je patrné, že v případě látek AcH nebo 3MPA dochází ke změně polohy max jednotlivých spekter. Tento fakt je zřejmě zapříčiněn ovlivněním stabilizačního činidla na povrchu nanočástic. Vliv koncentrace přidaných látek na změnu polohy max se projevil nejvýrazněji v neutrální a zásadité oblasti. V případě AcH docházelo při ph 7 k nejnižšímu poklesu při koncentraci látky 5, mol l 1 při stejné koncentraci 3MPA byl při ph 10 pozorován nejvyšší vzrůst max, což lze vysvětlit tak, že v případě 3MPA dochází k výměně molekul citrátu za molekuly 3MPA (cit. 1 ), které přispívají ke stabilizaci vzniklého roztoku. Při ph 13 nedochází v případě přídavků AcH a 3MPA během doby měření k úplné agregaci. Nejmenší pokles max je v obou případech pozorován A/A 0 1,2 1,0 0,8 0,6 0,4 A B C D 0,2 0, ph br. 9. Závislost normalizované absorbance čistých nanočástic (A) a roztoku nanočástic s přídavky 3MPA na hodnotě ph. Její koncentrace byla (B) 1, mol l 1 ; (C) 9, mol l 1 ; (D) 5, mol l 1. Hodnota ph byla nastavena až po přídavku 3MPA br. 10. SERS spektra 3MPA o koncentraci 1, mol l 1. Hodnota ph byla nastavena po přídavcích 3MPA. Spektra byla vzájemně posunuta (pouze v ose y) notou absorbance roztoku nanočástic v absorpčním maximu před změnou ph. Z naměřené závislosti vyplývá, že citrátové nanočástice jsou stabilní v intervalu ph od 4 do 10. Při ph 1,3 a 12,6 docházelo k agregaci nanočástic. Agregace nanočástic je ovlivněna především změnou ph roztoku a částečně také změnou iontové síly tohoto roztoku. Interakce AcH a 3MPA byly sledovány při třech různých koncentracích a při pěti různých hodnotách ph. Přídavky k roztoku nanočástic byly prováděny jednak před úpravou ph roztoku, kdy byla vybraná látka imobilizována na povrch a poté byl sledován vliv změny hodnoty ph na příslušnou interakci s povrchem (obr. 8 a 9) a dále pak po úpravě hodnoty ph, kdy byla rovněž sledována interakce karboxylových kyselin s nanočásticemi o předem připraveném ph, v tomto případě bylo zjištěno, že díky malé br. 11. SERS spektra 3MPA o koncentraci 1, mol l 1. Hodnota ph byla nastavena před přídavky 3MPA. Spektra byla vzájemně posunuta (pouze v ose y) 206
6 při koncentraci látek 9, mol l 1. Lze se domnívat, že je to způsobeno účinnější stabilizací roztoku nanočástic. Vliv ph na SERS spektra nanočástic stříbra modifikovaných AcH a 3MPA Vliv ph v rozsahu hodnot od 1 do 13 byl studován při koncentracích AcH a 3MPA 1, , 9, a 5, mol l 1. V případě AcH nebyl pozorován žádný výrazný vliv ph jednotlivých roztoků na polohu pásů v SERS spektru, kolísala pouze jejich intenzita, tyto změny ale nebyly považovány za významné. V SERS spektrech byly patrné pouze pásy citrátu (obr. 3). Lze se domnívat, že tato interakce je zprostředkována citrátem, nebo že se jedná o dynamický systém, kdy dochází k výměně části citrátu vázaného na povrchu nanočástic s octovou kyselinou v roztoku a naopak. Ukázka naměřených SERS spekter roztoku nanočástic modifikovaných 3MPA o koncentraci 1, mol l 1 při hodnotách ph 1, 4, 7, 10 a 13 je na obr. 10. Hodnoty ph byly nastaveny po centrifugaci. Posun vlnočtu pásu z 903 na 921 cm 1 s rostoucí hodnotou ph odpovídá disociaci karboxylové skupiny za vzniku karboxylátu 12. Podobný efekt lze sledovat u pásů v oblasti cm 1 a 1040 až 1290 cm 1 (cit. 12 ). Změna poměru intenzit pásů u 655 a 734 cm 1 v závislosti na změně koncentrace 3MPA (obr. 6) odpovídá změně konformace této látky na povrchu nanočástic. Tato závislost změny poměru na koncentraci se projevila při ph 4 i při ph 10. Jak ukázala měření (obr. 11), konformace 3MPA na povrchu nanočástic byla nezávislá na hodnotě ph roztoku. Závěr V této práci byly ověřovány interakce vybraných skupin látek s roztokem stříbrných nanočástic stabilizovaných citrátem. Z naměřených spekter je patrné, že interakce závisí na dané funkční skupině. Byla zjištěna silná interakce citrátu s povrchem stříbrných nanočástic, v jejímž důsledku byly schopny z povrchu nanočástic plně vytěsnit citrát pouze látky vázající se přes atom síry (C4SH, C12SH, LIP, 3MPA). V těchto případech se pak jeví SERS spektroskopie jako ideální nástroj pro sledování vazby na stříbrný povrch nanočástic. Připravené nanočástice stříbra stabilizované citrátem byly stabilní v rozmezí ph od 4 do 10. V případě látek MENH2, ET3EN, PYR, AcH a BZA nebyla potvrzena jejich vazba na povrch nanočástic pomocí SERS. Vliv koncentrace a ph byl sledován pouze u AcH a 3MPA. V případě vazby 3MPA prokázala naměřená SERS spektra, že změna její konformace na povrchu závisí pouze na koncentraci 3MPA v roztoku nikoliv na hodnotě ph tohoto roztoku. Experimenty s vlivem ph ukázaly, že pro zlepšení kvality SERS spekter 3MPA je vhodné po přečištění stříbrných nanočástic centrifugací a po interakci s vybranou látkou nastavit ph roztoku na hodnotu kolem 10. Takto získaná spektra se vyznačovala lepším rozlišením jednotlivých pásů a vyšší intenzitou signálu. Totéž platilo i v případě připravených citrátových nanočástic stříbra, kdy SERS spektrum s nejvyšší intenzitou signálu bylo naměřeno po centrifugaci a úpravě ph. Lze se domnívat, že odstraněním přebytečné nenavázané látky z roztoku a volbou vhodného ph lze docílit lepší stabilizaci jednotlivých částic v roztoku, což se může příznivě projevit na kvalitě měřených SERS spekter. Tato práce byla podpořena granty KAN , MŠMT LITERATURA 1. Carot M. L., Macagno V. A., Paredes-livera P., Patrito E. M.: J. Phys. Chem., C 111, 4294 (2007). 2. Imahori H., Fujimoto A., Kang S., Hotta H., Yoshida K., Umeyama T., Matano Y., Isoda S.: Tetrahedron 62, 1955 (2006). 3. Castro J. L., López-Ramírez M. R., Arenas J. F., ter J. C.: J. Raman Spectrosc. 35, 997 (2004). 4. Wang L. R., Fang Y.: Spectrochimica Acta, Part A 63, 614 (2006). 5. Castro J. L., ter J. C., Marcos J. I.: J. Raman Spectrosc. 28, 765 (1997). 6. Aiken J. D., Finke R. G.: J. Mol. Catal., A: Chem. 145, 1 (1999). 7. Lee P. C., Meisel D.: J. Phys. Chem. 86, 3391 (1982). 8. Moskovits M.: M. Rev. Mod. Phys. 1985, Gaussian 03, staženo Bell S. E. J., Sirimuthu N. M. S.: J. Phys. Chem. 109, 7405 (2005). 11. Templeton A. C., Pietron J. J., Murray R. W., Mulvaney P.: J. Phys. Chem., B 104, 564 (2000). 12. Kudelski A.: J. Raman Spectrosc. 34, 853 (2003). P. Žvátora, P. Řezanka, K. Záruba, and V. Král (Department of Analytical Chemistry, Institute of Chemical Technology, Prague): Binding of Selected Compounds to Silver Nanoparticles Better detection limits for some analytes can be obtained by using an appropriate detection method combined with surface immobilization of the receptor. To immobilize analytically important receptors on the nanoparticle surface is often impossible because the receptors do not contain suitable functional groups. In this case various multifunctional spacers can be used in which one group is used for the nanoparticle surface binding and another for immobilization of a receptor. The article deals with modification of silver nanoparticles with various compounds containing different functional groups. 207
STUDIUM POVRCHOVÉ MODIFIKACE STŘÍBRNÝCH NANOČÁSTIC A JEJICH MOŽNÉ VYUŽITÍ V ANALYTICKÉ CHEMII
 STUDIUM POVRCHOVÉ MODIFIKACE STŘÍBRÝCH AOČÁSTIC A JEJICH MOŽÉ VYUŽITÍ V AALYTICKÉ CHEMII Pavel Žvátora, Kamil Záruba, Pavel Řezanka, Vladimír Král Ústav analytické chemie, Fakulta chemicko-inženýrská,
STUDIUM POVRCHOVÉ MODIFIKACE STŘÍBRÝCH AOČÁSTIC A JEJICH MOŽÉ VYUŽITÍ V AALYTICKÉ CHEMII Pavel Žvátora, Kamil Záruba, Pavel Řezanka, Vladimír Král Ústav analytické chemie, Fakulta chemicko-inženýrská,
INTERAKCE MODIFIKOVANÝCH ZLATÝCH NANOČÁSTIC S NUKLEOTIDY. Pavel Řezanka, Kamil Záruba, Vladimír Král
 ITERKCE MDIFIKVÝCH ZLTÝCH ČÁSTIC S UKLETIDY Pavel Řezanka, Kamil Záruba, Vladimír Král Ústav analytické chemie, Fakulta chemicko-inženýrská, Vysoká škola chemicko-technologická, Technická 5, 166 28 Praha
ITERKCE MDIFIKVÝCH ZLTÝCH ČÁSTIC S UKLETIDY Pavel Řezanka, Kamil Záruba, Vladimír Král Ústav analytické chemie, Fakulta chemicko-inženýrská, Vysoká škola chemicko-technologická, Technická 5, 166 28 Praha
Pokročilé cvičení z fyzikální chemie KFC/POK2 Vibrační spektroskopie
 Pokročilé cvičení z fyzikální chemie KFC/POK2 Vibrační spektroskopie Vibrace molekul mohou být měřeny buď pomocí absorpce infračerveného záření, nebo pomocí neelastického rozptylu záření, tzn. Ramanova
Pokročilé cvičení z fyzikální chemie KFC/POK2 Vibrační spektroskopie Vibrace molekul mohou být měřeny buď pomocí absorpce infračerveného záření, nebo pomocí neelastického rozptylu záření, tzn. Ramanova
Molekulová spektroskopie 1. Chemická vazba, UV/VIS
 Molekulová spektroskopie 1 Chemická vazba, UV/VIS 1 Chemická vazba Silová interakce mezi dvěma atomy. Chemické vazby jsou soudržné síly působící mezi jednotlivými atomy nebo ionty v molekulách. Chemická
Molekulová spektroskopie 1 Chemická vazba, UV/VIS 1 Chemická vazba Silová interakce mezi dvěma atomy. Chemické vazby jsou soudržné síly působící mezi jednotlivými atomy nebo ionty v molekulách. Chemická
Vybrané spektroskopické metody
 Vybrané spektroskopické metody a jejich porovnání s Ramanovou spektroskopií Předmět: Kapitoly o nanostrukturách (2012/2013) Autor: Bc. Michal Martinek Školitel: Ing. Ivan Gregora, CSc. Obsah přednášky
Vybrané spektroskopické metody a jejich porovnání s Ramanovou spektroskopií Předmět: Kapitoly o nanostrukturách (2012/2013) Autor: Bc. Michal Martinek Školitel: Ing. Ivan Gregora, CSc. Obsah přednášky
1. Příloha 1 Návod úlohy pro Pokročilé praktikum z biochemie I
 1. Příloha 1 Návod úlohy pro Pokročilé praktikum z biochemie I Vazba bromfenolové modři na sérový albumin Princip úlohy Albumin má unikátní vlastnost vázat menší molekuly mnoha typů. Díky struktuře, tvořené
1. Příloha 1 Návod úlohy pro Pokročilé praktikum z biochemie I Vazba bromfenolové modři na sérový albumin Princip úlohy Albumin má unikátní vlastnost vázat menší molekuly mnoha typů. Díky struktuře, tvořené
Emise vyvolaná působením fotonů nebo částic
 Emise vyvolaná působením fotonů nebo částic PES (fotoelektronová spektroskopie) XPS (rentgenová fotoelektronová spektroskopie), ESCA (elektronová spektroskopie pro chemickou analýzu) UPS (ultrafialová
Emise vyvolaná působením fotonů nebo částic PES (fotoelektronová spektroskopie) XPS (rentgenová fotoelektronová spektroskopie), ESCA (elektronová spektroskopie pro chemickou analýzu) UPS (ultrafialová
Diskutujte, jak široký bude pás spojený s fosforescencí versus fluorescencí. Udělejte odhad v cm -1.
 S použitím modelu volného elektronu (=částice v krabici) spočtěte vlnovou délku a vlnočet nejdlouhovlnějšího elektronového přechodu u molekuly dekapentaenu a oktatetraenu. Diskutujte polohu absorpčního
S použitím modelu volného elektronu (=částice v krabici) spočtěte vlnovou délku a vlnočet nejdlouhovlnějšího elektronového přechodu u molekuly dekapentaenu a oktatetraenu. Diskutujte polohu absorpčního
Identifikace barviv pomocí Ramanovy spektrometrie
 Identifikace barviv pomocí Ramanovy spektrometrie V kriminalistických laboratořích se provádí technická expertíza písemností, která se mimo jiné zabývá zkoumáním použitých psacích prostředků: tiskových
Identifikace barviv pomocí Ramanovy spektrometrie V kriminalistických laboratořích se provádí technická expertíza písemností, která se mimo jiné zabývá zkoumáním použitých psacích prostředků: tiskových
Komplexy rhenistanového anionu s porfyriny
 Komplexy rhenistanového anionu s porfyriny Vladimír Král, Petr Vaňura, Jitka Koukolová Ústav analytické chemie, Vysoká škola chemickotechnologická v Praze, Praha V nukleární medicíně se radionuklidy používají
Komplexy rhenistanového anionu s porfyriny Vladimír Král, Petr Vaňura, Jitka Koukolová Ústav analytické chemie, Vysoká škola chemickotechnologická v Praze, Praha V nukleární medicíně se radionuklidy používají
Derivační spektrofotometrie a rozklad absorpčního spektra
 Derivační spektrofotometrie a rozklad absorpčního spektra Teorie: Derivační spektrofotometrie, využívající derivace absorpční křivky, je obecně používanou metodou pro zvýraznění detailů průběhu záznamu,
Derivační spektrofotometrie a rozklad absorpčního spektra Teorie: Derivační spektrofotometrie, využívající derivace absorpční křivky, je obecně používanou metodou pro zvýraznění detailů průběhu záznamu,
KOMPLEXY EUROPIA(III) LUMINISCENČNÍ VLASTNOSTI A VYUŽITÍ V ANALYTICKÉ CHEMII. Pavla Pekárková
 KOMPLEXY EUROPIA(III) LUMINISCENČNÍ VLASTNOSTI A VYUŽITÍ V ANALYTICKÉ CHEMII Pavla Pekárková Katedra analytické chemie, Přírodovědecká fakulta, Masarykova univerzita, Kotlářská 2, 611 37 Brno E-mail: 78145@mail.muni.cz
KOMPLEXY EUROPIA(III) LUMINISCENČNÍ VLASTNOSTI A VYUŽITÍ V ANALYTICKÉ CHEMII Pavla Pekárková Katedra analytické chemie, Přírodovědecká fakulta, Masarykova univerzita, Kotlářská 2, 611 37 Brno E-mail: 78145@mail.muni.cz
10/21/2013. K. Záruba. Chování a vlastnosti nanočástic ovlivňuje. velikost a tvar (distribuce) povrchové atomy, funkční skupiny porozita stabilita
 Chování a vlastnosti nanočástic ovlivňuje velikost a tvar (distribuce) povrchové atomy, funkční skupiny porozita stabilita K. Záruba Optická mikroskopie Elektronová mikroskopie (SEM, TEM) Fotoelektronová
Chování a vlastnosti nanočástic ovlivňuje velikost a tvar (distribuce) povrchové atomy, funkční skupiny porozita stabilita K. Záruba Optická mikroskopie Elektronová mikroskopie (SEM, TEM) Fotoelektronová
VIBRAČNÍ SPEKTROMETRIE
 VIBRAČNÍ SPEKTROMETRIE (c) -2012 RAMANOVA SPEKTROMETRIE 1 PRINCIP METODY Měří se rozptýlené záření, které vzniká interakcí monochromatického záření z viditelné oblasti s molekulami vzorku za současné změny
VIBRAČNÍ SPEKTROMETRIE (c) -2012 RAMANOVA SPEKTROMETRIE 1 PRINCIP METODY Měří se rozptýlené záření, které vzniká interakcí monochromatického záření z viditelné oblasti s molekulami vzorku za současné změny
Koloidní zlato: tradiční rekvizita alchymistů v minulosti - sofistikovaný (nano)nástroj budoucnosti?
 Koloidní zlato: tradiční rekvizita alchymistů v minulosti - sofistikovaný (nano)nástroj budoucnosti? Vedoucí projektu: Ing. Filip Novotný, Ing. Filip Havel K. Hes - Gymnázium, Praha 6, Nad Alejí 1952 K.
Koloidní zlato: tradiční rekvizita alchymistů v minulosti - sofistikovaný (nano)nástroj budoucnosti? Vedoucí projektu: Ing. Filip Novotný, Ing. Filip Havel K. Hes - Gymnázium, Praha 6, Nad Alejí 1952 K.
Vysoká škola chemicko-technologická v Praze, Ustav analytické chemie, Technická 5, 166 28 Praha 6
 Stanovení konstant stability citrátokomplexů holmia potenciometricky Vaňura Petr, Jedináková-Křížová Věra, Munesawa Yiji Vysoká škola chemicko-technologická v Praze, Ustav analytické chemie, Technická
Stanovení konstant stability citrátokomplexů holmia potenciometricky Vaňura Petr, Jedináková-Křížová Věra, Munesawa Yiji Vysoká škola chemicko-technologická v Praze, Ustav analytické chemie, Technická
Spektroskopické é techniky a mikroskopie. Spektroskopie. Typy spektroskopických metod. Cirkulární dichroismus. Fluorescence UV-VIS
 Spektroskopické é techniky a mikroskopie Spektroskopie metody zahrnující interakce mezi světlem (fotony) a hmotou (elektrony a protony v atomech a molekulách Typy spektroskopických metod IR NMR Elektron-spinová
Spektroskopické é techniky a mikroskopie Spektroskopie metody zahrnující interakce mezi světlem (fotony) a hmotou (elektrony a protony v atomech a molekulách Typy spektroskopických metod IR NMR Elektron-spinová
Ústřední komise Chemické olympiády. 55. ročník 2018/2019 TEST ŠKOLNÍHO KOLA. Kategorie E ŘEŠENÍ
 Ústřední komise Chemické olympiády 55. ročník 2018/2019 TEST ŠKOLNÍHO KOLA Kategorie E ŘEŠENÍ ANORGANICKÁ CHEMIE 16 BODŮ Úloha 1 Vlastnosti sloučenin manganu a chromu 8 bodů 1) Elektronová konfigurace:
Ústřední komise Chemické olympiády 55. ročník 2018/2019 TEST ŠKOLNÍHO KOLA Kategorie E ŘEŠENÍ ANORGANICKÁ CHEMIE 16 BODŮ Úloha 1 Vlastnosti sloučenin manganu a chromu 8 bodů 1) Elektronová konfigurace:
SPEKTROSKOPICKÉ VLASTNOSTI LÁTEK (ZÁKLADY SPEKTROSKOPIE)
 SPEKTROSKOPICKÉ VLASTNOSTI LÁTEK (ZÁKLADY SPEKTROSKOPIE) Elektromagnetické vlnění SVĚTLO Charakterizace záření Vlnová délka - (λ) : jednotky: m (obvykle nm) λ Souvisí s povahou fotonu Charakterizace záření
SPEKTROSKOPICKÉ VLASTNOSTI LÁTEK (ZÁKLADY SPEKTROSKOPIE) Elektromagnetické vlnění SVĚTLO Charakterizace záření Vlnová délka - (λ) : jednotky: m (obvykle nm) λ Souvisí s povahou fotonu Charakterizace záření
Úvod do spektrálních metod pro analýzu léčiv
 Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti Úvod do spektrálních metod pro analýzu léčiv Pavel Matějka, Vadym Prokopec pavel.matejka@vscht.cz pavel.matejka@gmail.com Vadym.Prokopec@vscht.cz
Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti Úvod do spektrálních metod pro analýzu léčiv Pavel Matějka, Vadym Prokopec pavel.matejka@vscht.cz pavel.matejka@gmail.com Vadym.Prokopec@vscht.cz
Charakterizace koloidních disperzí. Pavel Matějka
 Charakterizace koloidních disperzí Pavel Matějka Charakterizace koloidních disperzí 1. Úvod koloidní disperze 2. Spektroskopie kvazielastického rozptylu 1. Princip metody 2. Instrumentace 3. Příklady použití
Charakterizace koloidních disperzí Pavel Matějka Charakterizace koloidních disperzí 1. Úvod koloidní disperze 2. Spektroskopie kvazielastického rozptylu 1. Princip metody 2. Instrumentace 3. Příklady použití
Kurz 1 Úvod k biochemickému praktiku
 Kurz 1 Úvod k biochemickému praktiku Pavla Balínová http://vyuka.lf3.cuni.cz/ Důležité informace Kroužkový asistent: RNDr. Pavla Balínová e-mailová adresa: pavla.balinova@lf3.cuni.cz místnost: 410 studijní
Kurz 1 Úvod k biochemickému praktiku Pavla Balínová http://vyuka.lf3.cuni.cz/ Důležité informace Kroužkový asistent: RNDr. Pavla Balínová e-mailová adresa: pavla.balinova@lf3.cuni.cz místnost: 410 studijní
V001 Dokončení a kalibrace experimentálních zařízení v laboratoři urychlovače Tandetron
 V001 Dokončení a kalibrace experimentálních zařízení v laboratoři urychlovače Tandetron Údaje o provozu urychlovačů v ÚJF AV ČR ( hodiny 2009/hodiny 2008) Urychlovač Celkový počet hodin Analýzy Implantace
V001 Dokončení a kalibrace experimentálních zařízení v laboratoři urychlovače Tandetron Údaje o provozu urychlovačů v ÚJF AV ČR ( hodiny 2009/hodiny 2008) Urychlovač Celkový počet hodin Analýzy Implantace
Spektroskopie v UV-VIS oblasti. UV-VIS spektroskopie. Roztok KMnO 4. pracuje nejčastěji v oblasti 200-800 nm
 Spektroskopie v UV-VIS oblasti UV-VIS spektroskopie pracuje nejčastěji v oblasti 2-8 nm lze měřit i < 2 nm či > 8 nm UV VIS IR Ultra Violet VISible Infra Red Roztok KMnO 4 roztok KMnO 4 je červenofialový
Spektroskopie v UV-VIS oblasti UV-VIS spektroskopie pracuje nejčastěji v oblasti 2-8 nm lze měřit i < 2 nm či > 8 nm UV VIS IR Ultra Violet VISible Infra Red Roztok KMnO 4 roztok KMnO 4 je červenofialový
SPEKTROMETRIE. aneb co jsem se dozvěděla. autor: Zdeňka Baxová
 SPEKTROMETRIE aneb co jsem se dozvěděla autor: Zdeňka Baxová FTIR spektrometrie analytická metoda identifikace látek (organických i anorganických) všech skupenství měříme pohlcení IČ záření (o různé vlnové
SPEKTROMETRIE aneb co jsem se dozvěděla autor: Zdeňka Baxová FTIR spektrometrie analytická metoda identifikace látek (organických i anorganických) všech skupenství měříme pohlcení IČ záření (o různé vlnové
Koloidní zlato. Tradiční rekvizita alchymistů v minulosti sofistikovaný (nano)nástroj budoucnosti?
 Koloidní zlato Tradiční rekvizita alchymistů v minulosti sofistikovaný (nano)nástroj budoucnosti? Dominika Jurdová Gymnázium Velké Meziříčí, D.Jurdova@seznam.cz Tereza Bautkinová Gymnázium Botičská, tereza.bautkinova@gybot.cz
Koloidní zlato Tradiční rekvizita alchymistů v minulosti sofistikovaný (nano)nástroj budoucnosti? Dominika Jurdová Gymnázium Velké Meziříčí, D.Jurdova@seznam.cz Tereza Bautkinová Gymnázium Botičská, tereza.bautkinova@gybot.cz
INSTRUMENTÁLNÍ METODY
 INSTRUMENTÁLNÍ METODY ACH/IM David MILDE, 2014 Dělení instrumentálních metod Spektrální metody (MILDE) Separační metody (JIROVSKÝ) Elektroanalytické metody (JIROVSKÝ) Ostatní: imunochemické, radioanalytické,
INSTRUMENTÁLNÍ METODY ACH/IM David MILDE, 2014 Dělení instrumentálních metod Spektrální metody (MILDE) Separační metody (JIROVSKÝ) Elektroanalytické metody (JIROVSKÝ) Ostatní: imunochemické, radioanalytické,
Chemické výpočty II. Vladimíra Kvasnicová
 Chemické výpočty II Vladimíra Kvasnicová Převod jednotek pmol/l nmol/l µmol/l mmol/l mol/l 10-12 10-9 10-6 10-3 mol/l µg mg g 10-6 10-3 g µl ml dl L 10-6 10-3 10-1 L Cvičení 12) cholesterol (MW=386,7g/mol):
Chemické výpočty II Vladimíra Kvasnicová Převod jednotek pmol/l nmol/l µmol/l mmol/l mol/l 10-12 10-9 10-6 10-3 mol/l µg mg g 10-6 10-3 g µl ml dl L 10-6 10-3 10-1 L Cvičení 12) cholesterol (MW=386,7g/mol):
SPEKTRÁLNÍ METODY. Ing. David MILDE, Ph.D. Katedra analytické chemie Tel.: ; (c) David MILDE,
 SEKTRÁLNÍ METODY Ing. David MILDE, h.d. Katedra analytické chemie Tel.: 585634443; E-mail: david.milde@upol.cz (c) -2008 oužitá a doporučená literatura Němcová I., Čermáková L., Rychlovský.: Spektrometrické
SEKTRÁLNÍ METODY Ing. David MILDE, h.d. Katedra analytické chemie Tel.: 585634443; E-mail: david.milde@upol.cz (c) -2008 oužitá a doporučená literatura Němcová I., Čermáková L., Rychlovský.: Spektrometrické
CHEMIE. Pracovní list č. 7 - žákovská verze Téma: ph. Mgr. Lenka Horutová. Projekt: Student a konkurenceschopnost Reg. číslo: CZ.1.07/1.1.07/03.
 www.projektsako.cz CHEMIE Pracovní list č. 7 - žákovská verze Téma: ph Lektor: Mgr. Lenka Horutová Projekt: Student a konkurenceschopnost Reg. číslo: CZ.1.07/1.1.07/03.0075 Teorie: Pro snadnější výpočet
www.projektsako.cz CHEMIE Pracovní list č. 7 - žákovská verze Téma: ph Lektor: Mgr. Lenka Horutová Projekt: Student a konkurenceschopnost Reg. číslo: CZ.1.07/1.1.07/03.0075 Teorie: Pro snadnější výpočet
ZÁKLADNÍ EXPERIMENTÁLNÍ
 Kurz praktické NMR spektroskopie 10. - 12. říjen 2011, Praha ZÁKLADNÍ EXPERIMENTÁLNÍ POSTUPY NMR ROZTOKŮ A KAPALIN Jana Svobodová Ústav Makromolekulární chemie AV ČR, v.v.i. Bruker 600 Avance III PŘÍSTROJOVÉ
Kurz praktické NMR spektroskopie 10. - 12. říjen 2011, Praha ZÁKLADNÍ EXPERIMENTÁLNÍ POSTUPY NMR ROZTOKŮ A KAPALIN Jana Svobodová Ústav Makromolekulární chemie AV ČR, v.v.i. Bruker 600 Avance III PŘÍSTROJOVÉ
STŘEDNÍ ODBORNÁ ŠKOLA a STŘEDNÍ ODBORNÉ UČILIŠTĚ, Česká Lípa, 28. října 2707, příspěvková organizace
 Název školy: Číslo a název projektu: Číslo a název šablony klíčové aktivity: Označení materiálu: Typ materiálu: STŘEDNÍ ODBORNÁ ŠKOLA a STŘEDNÍ ODBORNÉ UČILIŠTĚ, Česká Lípa, 28. října 2707, příspěvková
Název školy: Číslo a název projektu: Číslo a název šablony klíčové aktivity: Označení materiálu: Typ materiálu: STŘEDNÍ ODBORNÁ ŠKOLA a STŘEDNÍ ODBORNÉ UČILIŠTĚ, Česká Lípa, 28. října 2707, příspěvková
Ústřední komise Chemické olympiády. 55. ročník 2018/2019 TEST ŠKOLNÍHO KOLA. Kategorie E ZADÁNÍ (60 BODŮ) časová náročnost: 120 minut
 Ústřední komise Chemické olympiády 55. ročník 2018/2019 TEST ŠKOLNÍHO KOLA Kategorie E ZADÁNÍ (60 BODŮ) časová náročnost: 120 minut ANORGANICKÁ CHEMIE 16 BODŮ Body celkem Úloha 1 Vlastnosti sloučenin manganu
Ústřední komise Chemické olympiády 55. ročník 2018/2019 TEST ŠKOLNÍHO KOLA Kategorie E ZADÁNÍ (60 BODŮ) časová náročnost: 120 minut ANORGANICKÁ CHEMIE 16 BODŮ Body celkem Úloha 1 Vlastnosti sloučenin manganu
Pufry, pufrační kapacita. Oxidoredukce, elektrodové děje.
 ÚSTAV LÉKAŘSKÉ BIOCHEMIE A LABORATORNÍ DIAGNOSTIKY 1. LF UK Pufry, pufrační kapacita. Oxidoredukce, elektrodové děje. Praktické cvičení z lékařské biochemie Všeobecné lékařství Martin Vejražka, Tomáš Navrátil
ÚSTAV LÉKAŘSKÉ BIOCHEMIE A LABORATORNÍ DIAGNOSTIKY 1. LF UK Pufry, pufrační kapacita. Oxidoredukce, elektrodové děje. Praktické cvičení z lékařské biochemie Všeobecné lékařství Martin Vejražka, Tomáš Navrátil
- Rayleighův rozptyl turbidimetrie, nefelometrie - Ramanův rozptyl. - fluorescence - fosforescence
 ROZPTYLOVÉ a EMISNÍ metody - Rayleighův rozptyl turbidimetrie, nefelometrie - Ramanův rozptyl - fluorescence - fosforescence Ramanova spektroskopie Každá čára Ramanova spektra je svými vlastnostmi závislá
ROZPTYLOVÉ a EMISNÍ metody - Rayleighův rozptyl turbidimetrie, nefelometrie - Ramanův rozptyl - fluorescence - fosforescence Ramanova spektroskopie Každá čára Ramanova spektra je svými vlastnostmi závislá
STANOVENÍ TVARU A DISTRIBUCE VELIKOSTI ČÁSTIC MODELOVÝCH TYPŮ NANOMATERIÁLŮ. Edita BRETŠNAJDROVÁ a, Ladislav SVOBODA a Jiří ZELENKA b
 STANOVENÍ TVARU A DISTRIBUCE VELIKOSTI ČÁSTIC MODELOVÝCH TYPŮ NANOMATERIÁLŮ Edita BRETŠNAJDROVÁ a, Ladislav SVOBODA a Jiří ZELENKA b a UNIVERZITA PARDUBICE, Fakulta chemicko-technologická, Katedra anorganické
STANOVENÍ TVARU A DISTRIBUCE VELIKOSTI ČÁSTIC MODELOVÝCH TYPŮ NANOMATERIÁLŮ Edita BRETŠNAJDROVÁ a, Ladislav SVOBODA a Jiří ZELENKA b a UNIVERZITA PARDUBICE, Fakulta chemicko-technologická, Katedra anorganické
UNIVERZITA PALACKÉHO V OLOMOUCI. Fakulta přírodovědecká. Katedra fyzikální chemie
 UNIVERZITA PALACKÉHO V OLOMOUCI Fakulta přírodovědecká Katedra fyzikální chemie DIPLOMOVÁ PRÁCE Olomouc 2014 Bc. Pavlína Andrýsková UNIVERZITA PALACKÉHO V OLOMOUCI Fakulta přírodovědecká Katedra fyzikální
UNIVERZITA PALACKÉHO V OLOMOUCI Fakulta přírodovědecká Katedra fyzikální chemie DIPLOMOVÁ PRÁCE Olomouc 2014 Bc. Pavlína Andrýsková UNIVERZITA PALACKÉHO V OLOMOUCI Fakulta přírodovědecká Katedra fyzikální
Výpočty koncentrací. objemová % (objemový zlomek) krvi m. Vsložky. celku. Objemy nejsou aditivní!!!
 Výpočty koncentrací objemová % (objemový zlomek) Vsložky % obj. = 100 V celku Objemy nejsou aditivní!!! Příklad: Kolik ethanolu je v 700 ml vodky (40 % obj.)? Kolik promile ethanolu v krvi bude mít muž
Výpočty koncentrací objemová % (objemový zlomek) Vsložky % obj. = 100 V celku Objemy nejsou aditivní!!! Příklad: Kolik ethanolu je v 700 ml vodky (40 % obj.)? Kolik promile ethanolu v krvi bude mít muž
3 Acidobazické reakce
 3 Acidobazické reakce Brønstedova teorie 1. Uveďte explicitní definice podle Brønstedovy teorie. Kyselina je... Báze je... Konjugovaný pár je... 2. Doplňte tabulku a pojmenujte všechny sloučeniny. Kyselina
3 Acidobazické reakce Brønstedova teorie 1. Uveďte explicitní definice podle Brønstedovy teorie. Kyselina je... Báze je... Konjugovaný pár je... 2. Doplňte tabulku a pojmenujte všechny sloučeniny. Kyselina
Základy fotometrie, využití v klinické biochemii
 Základy fotometrie, využití v klinické biochemii Základní vztahy ve fotometrii transmitance (propustnost): T = I / I 0 absorbance: A = log (I 0 / I) = log (1 / T) = log T Lambertův-Beerův zákon A l = e
Základy fotometrie, využití v klinické biochemii Základní vztahy ve fotometrii transmitance (propustnost): T = I / I 0 absorbance: A = log (I 0 / I) = log (1 / T) = log T Lambertův-Beerův zákon A l = e
Opakování
 Slabé vazebné interakce Opakování Co je to atom? Opakování Opakování Co je to atom? Atom je nejmenší částice hmoty, chemicky dále nedělitelná. Skládá se z atomového jádra obsahujícího protony a neutrony
Slabé vazebné interakce Opakování Co je to atom? Opakování Opakování Co je to atom? Atom je nejmenší částice hmoty, chemicky dále nedělitelná. Skládá se z atomového jádra obsahujícího protony a neutrony
PŘÍPRAVA SERS-AKTIVNÍCH MĚDĚNÝCH SUBSTRÁTŮ KATODICKOU REDUKCÍ A VYHODNOCENÍ JEJICH STRUKTURY POMOCÍ MIKROSKOPIE ATOMÁRNÍCH SIL
 PŘÍPRAVA SERS-AKTIVNÍCH MĚDĚNÝCH SUBSTRÁTŮ KATODICKOU REDUKCÍ A VYHODNOCENÍ JEJICH STRUKTURY POMOCÍ MIKROSKOPIE ATOMÁRNÍCH SIL ALŽBĚTA KOKAISLOVÁ a *, SOŇA BRÁZDOVÁ a, VADYM PROKOPEC a, MARTIN ČLUPEK a,
PŘÍPRAVA SERS-AKTIVNÍCH MĚDĚNÝCH SUBSTRÁTŮ KATODICKOU REDUKCÍ A VYHODNOCENÍ JEJICH STRUKTURY POMOCÍ MIKROSKOPIE ATOMÁRNÍCH SIL ALŽBĚTA KOKAISLOVÁ a *, SOŇA BRÁZDOVÁ a, VADYM PROKOPEC a, MARTIN ČLUPEK a,
13. Spektroskopie základní pojmy
 základní pojmy Spektroskopicky významné OPTICKÉ JEVY absorpce absorpční spektrometrie emise emisní spektrometrie rozptyl rozptylové metody Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti
základní pojmy Spektroskopicky významné OPTICKÉ JEVY absorpce absorpční spektrometrie emise emisní spektrometrie rozptyl rozptylové metody Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti
LABORATOŘ OBORU I ÚSTAV ORGANICKÉ TECHNOLOGIE (111) Použití GC-MS spektrometrie
 LABORATOŘ OBORU I ÚSTAV ORGANICKÉ TECHNOLOGIE (111) C Použití GC-MS spektrometrie Vedoucí práce: Doc. Ing. Petr Kačer, Ph.D., Ing. Kamila Syslová Umístění práce: laboratoř 79 Použití GC-MS spektrometrie
LABORATOŘ OBORU I ÚSTAV ORGANICKÉ TECHNOLOGIE (111) C Použití GC-MS spektrometrie Vedoucí práce: Doc. Ing. Petr Kačer, Ph.D., Ing. Kamila Syslová Umístění práce: laboratoř 79 Použití GC-MS spektrometrie
ABSORPČNÍ A EMISNÍ SPEKTRÁLNÍ METODY
 ABSORPČNÍ A EMISNÍ SPEKTRÁLNÍ METODY 1 Fyzikální základy spektrálních metod Monochromatický zářivý tok 0 (W, rozměr m 2.kg.s -3 ): Absorbován ABS Propuštěn Odražen zpět r Rozptýlen s Bilance toků 0 = +
ABSORPČNÍ A EMISNÍ SPEKTRÁLNÍ METODY 1 Fyzikální základy spektrálních metod Monochromatický zářivý tok 0 (W, rozměr m 2.kg.s -3 ): Absorbován ABS Propuštěn Odražen zpět r Rozptýlen s Bilance toků 0 = +
Automatická potenciometrická titrace Klinická a toxikologická analýza Chemie životního prostředí Geologické obory
 Automatická potenciometrická titrace Klinická a toxikologická analýza Chemie životního prostředí Geologické obory Titrace je spolehlivý a celkem nenáročný postup, jak zjistit koncentraci analytu, její
Automatická potenciometrická titrace Klinická a toxikologická analýza Chemie životního prostředí Geologické obory Titrace je spolehlivý a celkem nenáročný postup, jak zjistit koncentraci analytu, její
 Číslo projektu Číslo a název šablony klíčové aktivity Tematická oblast Autor Ročník 3 Obor CZ.1.07/1.5.00/34.0514 III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Metody instrumentální analýzy, vy_32_inovace_ma_11_09
Číslo projektu Číslo a název šablony klíčové aktivity Tematická oblast Autor Ročník 3 Obor CZ.1.07/1.5.00/34.0514 III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Metody instrumentální analýzy, vy_32_inovace_ma_11_09
Povrchová plasmonová rezonance v blízké infračervené oblasti pro studium tvorby multivrstev polyelektrolytů
 Povrchová plasmonová rezonance v blízké infračervené oblasti pro studium tvorby multivrstev polyelektrolytů K. Záruba 1 Úkoly 1. Seznamte se s ovládáním měřicího přístroje (demonstruje asistent: montáž
Povrchová plasmonová rezonance v blízké infračervené oblasti pro studium tvorby multivrstev polyelektrolytů K. Záruba 1 Úkoly 1. Seznamte se s ovládáním měřicího přístroje (demonstruje asistent: montáž
Repetitorium chemie VIII. (2014)
 Repetitorium chemie VIII. (2014) Moderní metody analýzy organických látek se zastávkou u Lambert-Beerova zákona a odhalení tajemství Bradforda/Bradfordové Odhalení tajemství: Protein Concentration Determination
Repetitorium chemie VIII. (2014) Moderní metody analýzy organických látek se zastávkou u Lambert-Beerova zákona a odhalení tajemství Bradforda/Bradfordové Odhalení tajemství: Protein Concentration Determination
Oborový workshop pro SŠ CHEMIE
 PRAKTICKÁ VÝUKA PŘÍRODOVĚDNÝCH PŘEDMĚTŮ NA ZŠ A SŠ CZ.1.07/1.1.30/02.0024 Tento projekt je spolufinancován Evropským sociálním fondem a státním rozpočtem České republiky. Oborový workshop pro SŠ CHEMIE
PRAKTICKÁ VÝUKA PŘÍRODOVĚDNÝCH PŘEDMĚTŮ NA ZŠ A SŠ CZ.1.07/1.1.30/02.0024 Tento projekt je spolufinancován Evropským sociálním fondem a státním rozpočtem České republiky. Oborový workshop pro SŠ CHEMIE
STANOVENÍ CHLORIDŮ. Odměrné argentometrické stanovení chloridů podle Mohra
 STANOVENÍ CHLORIDŮ Odměrné argentometrické stanovení chloridů podle Mohra Cíl práce Stanovte titr odměrného standardního roztoku dusičnanu stříbrného titrací 5 ml standardního srovnávacího roztoku chloridu
STANOVENÍ CHLORIDŮ Odměrné argentometrické stanovení chloridů podle Mohra Cíl práce Stanovte titr odměrného standardního roztoku dusičnanu stříbrného titrací 5 ml standardního srovnávacího roztoku chloridu
OPTIMALIZACE METODY ANODICKÉ ROZPOUŠTĚCÍ VOLTAMETRIE PRO ANALÝZU BIOLOGICKÝCH VZORKŮ S OBSAHEM RTUTI
 Středoškolská technika 212 Setkání a prezentace prací středoškolských studentů na ČVUT OPTIMALIZACE METODY ANODICKÉ ROZPOUŠTĚCÍ VOLTAMETRIE PRO ANALÝZU BIOLOGICKÝCH VZORKŮ S OBSAHEM RTUTI Eliška Marková
Středoškolská technika 212 Setkání a prezentace prací středoškolských studentů na ČVUT OPTIMALIZACE METODY ANODICKÉ ROZPOUŠTĚCÍ VOLTAMETRIE PRO ANALÝZU BIOLOGICKÝCH VZORKŮ S OBSAHEM RTUTI Eliška Marková
MINIATURIZACE PRŮTOKOVÝCH ELEKTROCHEMICKÝCH CEL PRO GENEROVÁNÍ TĚKAVÝCH SLOUČENIN. Jakub Hraníček
 MINIATURIZACE PRŮTOKOVÝCH ELEKTROCHEMICKÝCH CEL PRO GENEROVÁNÍ TĚKAVÝCH SLOUČENIN Jakub Hraníček Katedra analytické chemie, Přírodovědecká fakulta, Univerzita Karlova, Albertov 6, 128 43 Praha 2 E-mail:
MINIATURIZACE PRŮTOKOVÝCH ELEKTROCHEMICKÝCH CEL PRO GENEROVÁNÍ TĚKAVÝCH SLOUČENIN Jakub Hraníček Katedra analytické chemie, Přírodovědecká fakulta, Univerzita Karlova, Albertov 6, 128 43 Praha 2 E-mail:
Roztoky - elektrolyty
 Roztoky - elektrolyty Roztoky - vodné roztoky prakticky vždy vedou elektrický proud Elektrolyty látky, které se štěpí disociují na elektricky nabité částice ionty Původně se předpokládalo, že k disociaci
Roztoky - elektrolyty Roztoky - vodné roztoky prakticky vždy vedou elektrický proud Elektrolyty látky, které se štěpí disociují na elektricky nabité částice ionty Původně se předpokládalo, že k disociaci
COSY + - podmínky měření a zpracování dat ztráta rozlišení ve spektru. inphase dublet, disperzní. antiphase dublet, absorpční
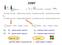 y x COSY 90 y chem. posuv J vazba 90 x : : inphase dublet, disperzní inphase dublet, disperzní antiphase dublet, absorpční antiphase dublet, absorpční diagonální pík krospík + - - + podmínky měření a zpracování
y x COSY 90 y chem. posuv J vazba 90 x : : inphase dublet, disperzní inphase dublet, disperzní antiphase dublet, absorpční antiphase dublet, absorpční diagonální pík krospík + - - + podmínky měření a zpracování
10A1_IR spektroskopie
 C6200-Biochemické metody 10A1_IR spektroskopie Petr Zbořil IR spektroskopie Excitace vibračních a rotačních přechodů Valenční vibrace n Deformační vibrace d IR spektroskopie N atomů = 3N stupňů volnosti
C6200-Biochemické metody 10A1_IR spektroskopie Petr Zbořil IR spektroskopie Excitace vibračních a rotačních přechodů Valenční vibrace n Deformační vibrace d IR spektroskopie N atomů = 3N stupňů volnosti
STANOVENÍ ETHANOLU V ALKOHOLICKÉM NÁPOJI POMOCÍ NIR SPEKTROMETRIE
 STANOVENÍ ETHANOLU V ALKOHOLICKÉM NÁPOJI POMOCÍ NIR SPEKTROMETRIE Úvod Infračervená spektrometrie v blízké oblasti (Near-Infrared Spectrometry NIR spectrometry) je metoda molekulové spektrometrie, která
STANOVENÍ ETHANOLU V ALKOHOLICKÉM NÁPOJI POMOCÍ NIR SPEKTROMETRIE Úvod Infračervená spektrometrie v blízké oblasti (Near-Infrared Spectrometry NIR spectrometry) je metoda molekulové spektrometrie, která
ŘEŠENÍ KONTROLNÍHO TESTU ŠKOLNÍHO KOLA
 Ústřední komise Chemické olympiády 49. ročník 2012/2013 ŠKOLNÍ KOLO kategorie B ŘEŠENÍ KONTROLNÍHO TESTU ŠKOLNÍHO KOLA KONTROLNÍ TEST ŠKOLNÍHO KOLA (60 BODŮ) ANORGANICKÁ CHEMIE 30 BODŮ Úloha 1 Titrační
Ústřední komise Chemické olympiády 49. ročník 2012/2013 ŠKOLNÍ KOLO kategorie B ŘEŠENÍ KONTROLNÍHO TESTU ŠKOLNÍHO KOLA KONTROLNÍ TEST ŠKOLNÍHO KOLA (60 BODŮ) ANORGANICKÁ CHEMIE 30 BODŮ Úloha 1 Titrační
Zápis o rozboru. E skleněné ISE závislé na ph roztoku, lze pomocí kombinované skleněné ISE sestrojit závislost ph na přidávaném
 1 Princip metody Zápis o rozboru Tato laboratorní práce byla rozdělena na tři části.v první bylo úkolem stanovit s pomocí potenciometrické titrace hmotnost kyseliny fosforečné a dihydrogenfosforečnanu
1 Princip metody Zápis o rozboru Tato laboratorní práce byla rozdělena na tři části.v první bylo úkolem stanovit s pomocí potenciometrické titrace hmotnost kyseliny fosforečné a dihydrogenfosforečnanu
Základy NIR spektrometrie a její praktické využití
 Nicolet CZ s.r.o. The world leader in serving science Základy NIR spektrometrie a její praktické využití NIR praktická metoda molekulové spektroskopie, nahrazující pracnější, časově náročnější a dražší
Nicolet CZ s.r.o. The world leader in serving science Základy NIR spektrometrie a její praktické využití NIR praktická metoda molekulové spektroskopie, nahrazující pracnější, časově náročnější a dražší
vzorek1 0.0033390 0.0047277 0.0062653 0.0077811 0.0090141... vzorek 30 0.0056775 0.0058778 0.0066916 0.0076192 0.0087291
 Vzorová úloha 4.16 Postup vícerozměrné kalibrace Postup vícerozměrné kalibrace ukážeme na úloze C4.10 Vícerozměrný kalibrační model kvality bezolovnatého benzinu. Dle následujících kroků na základě naměřených
Vzorová úloha 4.16 Postup vícerozměrné kalibrace Postup vícerozměrné kalibrace ukážeme na úloze C4.10 Vícerozměrný kalibrační model kvality bezolovnatého benzinu. Dle následujících kroků na základě naměřených
nano.tul.cz Inovace a rozvoj studia nanomateriálů na TUL
 Inovace a rozvoj studia nanomateriálů na TUL nano.tul.cz Tyto materiály byly vytvořeny v rámci projektu ESF OP VK: Inovace a rozvoj studia nanomateriálů na Technické univerzitě v Liberci Experimentální
Inovace a rozvoj studia nanomateriálů na TUL nano.tul.cz Tyto materiály byly vytvořeny v rámci projektu ESF OP VK: Inovace a rozvoj studia nanomateriálů na Technické univerzitě v Liberci Experimentální
ZÁKLADNÍ CHEMICKÉ POJMY A ZÁKONY
 ZÁKLADNÍ CHEMICKÉ POJMY A ZÁKONY Klíčová slova: relativní atomová hmotnost (A r ), relativní molekulová hmotnost (M r ), Avogadrova konstanta (N A ), látkové množství (n, mol), molární hmotnost (M, g/mol),
ZÁKLADNÍ CHEMICKÉ POJMY A ZÁKONY Klíčová slova: relativní atomová hmotnost (A r ), relativní molekulová hmotnost (M r ), Avogadrova konstanta (N A ), látkové množství (n, mol), molární hmotnost (M, g/mol),
ANALÝZA BUNĚK POMOCÍ RAMANOVY SPEKTROSKOPIE VLIV MATERIÁLU POUŽITÉHO SUBSTRÁTU
 ANALÝZA BUNĚK POMOCÍ RAMANOVY SPEKTROSKOPIE VLIV MATERIÁLU POUŽITÉHO SUBSTRÁTU Kateřina Štymplová Univerzita Palackého v Olomouci, Česká Republika Abstrakt: Povrchově zesílená Ramanova spektroskopie má
ANALÝZA BUNĚK POMOCÍ RAMANOVY SPEKTROSKOPIE VLIV MATERIÁLU POUŽITÉHO SUBSTRÁTU Kateřina Štymplová Univerzita Palackého v Olomouci, Česká Republika Abstrakt: Povrchově zesílená Ramanova spektroskopie má
ATOMOVÁ SPEKTROMETRIE
 ATOMOVÁ SPEKTROMETRIE Atomová spektrometrie valenčních e - 1. OES (AES). AAS 3. AFS 1 Atomová spektra čárová spektra Tok záření P - množství zářivé energie (Q E ) přenesené od zdroje za jednotku času.
ATOMOVÁ SPEKTROMETRIE Atomová spektrometrie valenčních e - 1. OES (AES). AAS 3. AFS 1 Atomová spektra čárová spektra Tok záření P - množství zářivé energie (Q E ) přenesené od zdroje za jednotku času.
Absorpční fotometrie
 Absorpční fotometrie - v ultrafialové (UV) a viditelné (VIS) oblasti přechody mezi elektronovými stavy +... - v infračervené (IČ) oblasti přechody mezi vibračními stavy +... - v mikrovlnné oblasti přechody
Absorpční fotometrie - v ultrafialové (UV) a viditelné (VIS) oblasti přechody mezi elektronovými stavy +... - v infračervené (IČ) oblasti přechody mezi vibračními stavy +... - v mikrovlnné oblasti přechody
Určení koncentrace proteinu fluorescenční metodou v mikrotitračních destičkách
 Určení koncentrace proteinu fluorescenční metodou v mikrotitračních destičkách Teorie Stanovení celkových proteinů Celkové množství proteinů lze stanovit pomocí několika metod; například: Hartree-Lowryho
Určení koncentrace proteinu fluorescenční metodou v mikrotitračních destičkách Teorie Stanovení celkových proteinů Celkové množství proteinů lze stanovit pomocí několika metod; například: Hartree-Lowryho
Základní parametry 1 H NMR spekter
 LEKCE 1a Základní parametry 1 NMR spekter Počet signálů ve spektru (zjištění počtu skupin chemicky ekvivalentních jader) Integrální intenzita (intenzita pásů závisí na počtu jader) Chemický posun (polohy
LEKCE 1a Základní parametry 1 NMR spekter Počet signálů ve spektru (zjištění počtu skupin chemicky ekvivalentních jader) Integrální intenzita (intenzita pásů závisí na počtu jader) Chemický posun (polohy
FLUORIMETRICKÉ STANOVENÍ FLUORESCEINU
 FLUORIMETRICKÉ STANOVENÍ FLUORESCEINU návod vznikl jako součást bakalářské práce Martiny Vidrmanové Fluorimetrie s využitím spektrofotometru SpectroVis Plus firmy Vernier (http://is.muni.cz/th/268973/prif_b/bakalarska_prace.pdf)
FLUORIMETRICKÉ STANOVENÍ FLUORESCEINU návod vznikl jako součást bakalářské práce Martiny Vidrmanové Fluorimetrie s využitím spektrofotometru SpectroVis Plus firmy Vernier (http://is.muni.cz/th/268973/prif_b/bakalarska_prace.pdf)
Ústřední komise Chemické olympiády. 55. ročník 2018/2019 NÁRODNÍ KOLO. Kategorie E. Zadání praktické části Úloha 2 (30 bodů)
 Ústřední komise Chemické olympiády 55. ročník 2018/2019 NÁRODNÍ KOLO Kategorie E Zadání praktické části Úloha 2 (30 bodů) PRAKTICKÁ ČÁST 30 BODŮ Úloha 2 Stanovení Cu 2+ spektrofotometricky 30 bodů Cu 2+
Ústřední komise Chemické olympiády 55. ročník 2018/2019 NÁRODNÍ KOLO Kategorie E Zadání praktické části Úloha 2 (30 bodů) PRAKTICKÁ ČÁST 30 BODŮ Úloha 2 Stanovení Cu 2+ spektrofotometricky 30 bodů Cu 2+
Teorie kyselin a zásad poznámky 5.A GVN
 Teorie kyselin a zásad poznámky 5A GVN 13 června 2007 Arrheniova teorie platná pouze pro vodní roztoky kyseliny jsou látky schopné ve vodném roztoku odštěpit vodíkový kation H + HCl H + + Cl - CH 3 COOH
Teorie kyselin a zásad poznámky 5A GVN 13 června 2007 Arrheniova teorie platná pouze pro vodní roztoky kyseliny jsou látky schopné ve vodném roztoku odštěpit vodíkový kation H + HCl H + + Cl - CH 3 COOH
ÚSTAV ORGANICKÉ TECHNOLOGIE
 LABORATOŘ OBORU I ÚSTAV ORGANICKÉ TECHNOLOGIE (111) F Imobilizace na alumosilikátové materiály Vedoucí práce: Ing. Eliška Leitmannová, Ph.D. Umístění práce: laboratoř F07, F08 1 Úvod Imobilizace aktivních
LABORATOŘ OBORU I ÚSTAV ORGANICKÉ TECHNOLOGIE (111) F Imobilizace na alumosilikátové materiály Vedoucí práce: Ing. Eliška Leitmannová, Ph.D. Umístění práce: laboratoř F07, F08 1 Úvod Imobilizace aktivních
3 Acidobazické reakce
 3 Acidobazické reakce Brønstedova teorie 1. Uveďte explicitní definice podle Brønstedovy teorie. Kyselina je... Báze je... Konjugovaný pár je... 2. Doplňte tabulku a pojmenujte všechny sloučeniny. Kyselina
3 Acidobazické reakce Brønstedova teorie 1. Uveďte explicitní definice podle Brønstedovy teorie. Kyselina je... Báze je... Konjugovaný pár je... 2. Doplňte tabulku a pojmenujte všechny sloučeniny. Kyselina
Metody charakterizace nanomaterálů I
 Vybrané metody spektráln lní analýzy Metody charakterizace nanomaterálů I RNDr. Věra Vodičková, PhD. Molekulová spektroskopie atomy a molekuly mohou měnit svůj energetický stav přijetím nebo vyzářením
Vybrané metody spektráln lní analýzy Metody charakterizace nanomaterálů I RNDr. Věra Vodičková, PhD. Molekulová spektroskopie atomy a molekuly mohou měnit svůj energetický stav přijetím nebo vyzářením
Odměrná analýza, volumetrie
 Odměrná analýza, volumetrie metoda založená na měření objemu metoda absolutní: stanovení analytu ze změřeného objemu roztoku činidla o přesně známé koncentraci, který je zapotřebí k úplné a stechiometricky
Odměrná analýza, volumetrie metoda založená na měření objemu metoda absolutní: stanovení analytu ze změřeného objemu roztoku činidla o přesně známé koncentraci, který je zapotřebí k úplné a stechiometricky
VLASTNOSTI DRCENÉHO PÓROBETONU
 VLASTNOSTI DRCENÉHO PÓROBETONU (zkoušky provedené ke 4.4.2012) STANOVENÍ ZÁKLADNÍCH FYZIKÁLNÍCH VLASTNOSTÍ 1. Vlhkostní vlastnosti (frakce 2-4): přirozená vlhkost 3,0% hm. nasákavost - 99,3% hm. 2. Hmotnostní
VLASTNOSTI DRCENÉHO PÓROBETONU (zkoušky provedené ke 4.4.2012) STANOVENÍ ZÁKLADNÍCH FYZIKÁLNÍCH VLASTNOSTÍ 1. Vlhkostní vlastnosti (frakce 2-4): přirozená vlhkost 3,0% hm. nasákavost - 99,3% hm. 2. Hmotnostní
Stanovení korozní rychlosti elektrochemickými polarizačními metodami
 Stanovení korozní rychlosti elektrochemickými polarizačními metodami Úvod Měření polarizačního odporu Dílčí děje elektrochemického korozního procesu anodická oxidace kovu a katodická redukce složky prostředí
Stanovení korozní rychlosti elektrochemickými polarizačními metodami Úvod Měření polarizačního odporu Dílčí děje elektrochemického korozního procesu anodická oxidace kovu a katodická redukce složky prostředí
7. Měření fluorescence při excitaci kontinuálním světlem ( steady-state )
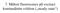 7. Měření fluorescence při excitaci kontinuálním světlem ( steady-state ) Steady-state měření Excitujeme kontinuálním světlem, měříme intenzitu emise (počet emitovaných fotonů) Obvykle nedetekujeme všechny
7. Měření fluorescence při excitaci kontinuálním světlem ( steady-state ) Steady-state měření Excitujeme kontinuálním světlem, měříme intenzitu emise (počet emitovaných fotonů) Obvykle nedetekujeme všechny
Metody nelineární optiky v Ramanově spektroskopii
 Metody nelineární optiky v Ramanově spektroskopii Využití optických nelinearit umožňuje přejít od tradičního studia rozptylu světla na fluktuacích, teplotních elementárních excitacích, ke studiu rozptylu
Metody nelineární optiky v Ramanově spektroskopii Využití optických nelinearit umožňuje přejít od tradičního studia rozptylu světla na fluktuacích, teplotních elementárních excitacích, ke studiu rozptylu
11.Metody molekulové spektrometrie pro kvantitativní analýzu léčiv
 Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti 11.Metody molekulové spektrometrie pro kvantitativní analýzu léčiv Vadym Prokopec Vadym.Prokopec@vscht.cz 11.Metody molekulové spektrometrie
Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti 11.Metody molekulové spektrometrie pro kvantitativní analýzu léčiv Vadym Prokopec Vadym.Prokopec@vscht.cz 11.Metody molekulové spektrometrie
LEKCE 1b. Základní parametry 1 H NMR spekter. Symetrie v NMR spektrech: homotopické, enantiotopické, diastereotopické protony (skupiny)*
 Základní parametry 1 NMR spekter LEKCE 1b Symetrie v NMR spektrech: homotopické, enantiotopické, diastereotopické protony (skupiny)* 3.5 3.0 2.5 2.0 1.5 Základní parametry 1 NMR spekter Počet signálů ve
Základní parametry 1 NMR spekter LEKCE 1b Symetrie v NMR spektrech: homotopické, enantiotopické, diastereotopické protony (skupiny)* 3.5 3.0 2.5 2.0 1.5 Základní parametry 1 NMR spekter Počet signálů ve
Přílohy. NÁZEV: Molekulární modely ve výuce organické chemie na gymnáziu. AUTOR: Milan Marek. KATEDRA: Katedra chemie a didaktiky chemie
 NÁZEV: Molekulární modely ve výuce organické chemie na gymnáziu AUTOR: Milan Marek KATEDRA: Katedra chemie a didaktiky chemie Přílohy Příloha 1 Přehled vzorců a modelů Příloha 2 Nástěnné transparenty modelů
NÁZEV: Molekulární modely ve výuce organické chemie na gymnáziu AUTOR: Milan Marek KATEDRA: Katedra chemie a didaktiky chemie Přílohy Příloha 1 Přehled vzorců a modelů Příloha 2 Nástěnné transparenty modelů
ATOMOVÁ SPEKTROMETRIE
 ATOMOVÁ SPEKTROMETRIE doc. Ing. David MILDE, Ph.D. tel.: 585634443 E-mail: david.milde@upol.cz (c) -017 Doporučená literatura Černohorský T., Jandera P.: Atomová spektrometrie. Univerzita Pardubice 1997.
ATOMOVÁ SPEKTROMETRIE doc. Ing. David MILDE, Ph.D. tel.: 585634443 E-mail: david.milde@upol.cz (c) -017 Doporučená literatura Černohorský T., Jandera P.: Atomová spektrometrie. Univerzita Pardubice 1997.
Jednotné pracovní postupy zkoušení krmiv STANOVENÍ OBSAHU SELENU METODOU ICP-OES
 Strana 1 STANOVENÍ OBSAHU SELENU METODOU ICP-OES 1 Rozsah a účel Postup specifikuje podmínky pro stanovení celkového obsahu selenu v minerálních krmivech a premixech metodou optické emisní spektrometrie
Strana 1 STANOVENÍ OBSAHU SELENU METODOU ICP-OES 1 Rozsah a účel Postup specifikuje podmínky pro stanovení celkového obsahu selenu v minerálních krmivech a premixech metodou optické emisní spektrometrie
Obr. 1. Struktura glukosaminu.
 3. Stanovení glukosaminu ve výživových doplňcích pomocí kapilární elektroforézy Glukosamin (2-amino-2-deoxyglukózamonosacharid je široce distribuován ve tkáních lidského organismu jako složka je klíčovou
3. Stanovení glukosaminu ve výživových doplňcích pomocí kapilární elektroforézy Glukosamin (2-amino-2-deoxyglukózamonosacharid je široce distribuován ve tkáních lidského organismu jako složka je klíčovou
O Minimální počet valencí potřebných ke spojení vícevazných atomů = (24 C + 3 O + 7 N 1) * 2 = 66 valencí
 Jméno a příjmení:_bohumil_dolenský_ Datum:_10.12.2010_ Fakulta:_FCHI_ Kruh:_ÚACh_ 1. Sepište seznam signálů 1 H dle klesajícího chemického posunu (včetně nečistot), uveďte chemický posun, multiplicitu
Jméno a příjmení:_bohumil_dolenský_ Datum:_10.12.2010_ Fakulta:_FCHI_ Kruh:_ÚACh_ 1. Sepište seznam signálů 1 H dle klesajícího chemického posunu (včetně nečistot), uveďte chemický posun, multiplicitu
Jednotné pracovní postupy zkoušení krmiv STANOVENÍ OBSAHU DEKOCHINÁTU METODOU HPLC
 Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU DEKOCHINÁTU METODOU HPLC 1 Rozsah a účel Tato metoda specifikuje podmínky pro stanovení dekochinátu metodou vysokoúčinné kapalinové chromatografie
Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU DEKOCHINÁTU METODOU HPLC 1 Rozsah a účel Tato metoda specifikuje podmínky pro stanovení dekochinátu metodou vysokoúčinné kapalinové chromatografie
ANODA KATODA elektrolyt:
 Ukázky z pracovních listů 1) Naznač pomocí šipek, které částice putují k anodě a které ke katodě. Co je elektrolytem? ANODA KATODA elektrolyt: Zn 2+ Cl - Zn 2+ Zn 2+ Cl - Cl - Cl - Cl - Cl - Zn 2+ Cl -
Ukázky z pracovních listů 1) Naznač pomocí šipek, které částice putují k anodě a které ke katodě. Co je elektrolytem? ANODA KATODA elektrolyt: Zn 2+ Cl - Zn 2+ Zn 2+ Cl - Cl - Cl - Cl - Cl - Zn 2+ Cl -
Postup při interpretaci NMR spekter neznámého vzorku
 Postup při interpretaci NMR spekter neznámého vzorku VŠCT 2017, Bohumil Dolenský, dolenskb@vscht.cz Tento text byl vypracován pro projekt Inovace předmětu Semestrální práce oboru analytická chemie I. Slouží
Postup při interpretaci NMR spekter neznámého vzorku VŠCT 2017, Bohumil Dolenský, dolenskb@vscht.cz Tento text byl vypracován pro projekt Inovace předmětu Semestrální práce oboru analytická chemie I. Slouží
ČESKÉ VYSOKÉ UČENÍ TECHNICKÉ V PRAZE FAKULTA ELEKTROTECHNICKÁ.
 ČESKÉ VYSOKÉ UČENÍ TECHNICKÉ V PRAZE FAKULTA ELEKTROTECHNICKÁ. Protokol o provedeném měření Druh měření Měření vodivosti elektrolytu číslo úlohy 2 Měřený předmět Elektrolyt Měřil Jaroslav ŘEZNÍČEK třída
ČESKÉ VYSOKÉ UČENÍ TECHNICKÉ V PRAZE FAKULTA ELEKTROTECHNICKÁ. Protokol o provedeném měření Druh měření Měření vodivosti elektrolytu číslo úlohy 2 Měřený předmět Elektrolyt Měřil Jaroslav ŘEZNÍČEK třída
Počítačová chemie. výpočetně náročné simulace chemických a biomolekulárních systémů. Zora Střelcová
 Počítačová chemie výpočetně náročné simulace chemických a biomolekulárních systémů Zora Střelcová Národní centrum pro výzkum biomolekul, Masarykova univerzita, Kotlářská 2, 611 37 Brno, Česká Republika
Počítačová chemie výpočetně náročné simulace chemických a biomolekulárních systémů Zora Střelcová Národní centrum pro výzkum biomolekul, Masarykova univerzita, Kotlářská 2, 611 37 Brno, Česká Republika
Rentgenová spektrální analýza Elektromagnetické záření s vlnovou délkou 10-2 až 10 nm
 Rtg. záření: Rentgenová spektrální analýza Elektromagnetické záření s vlnovou délkou 10-2 až 10 nm Vznik rtg. záření: 1. Rtg. záření se spojitým spektrem vzniká při prudkém zabrzdění urychlených elektronů.
Rtg. záření: Rentgenová spektrální analýza Elektromagnetické záření s vlnovou délkou 10-2 až 10 nm Vznik rtg. záření: 1. Rtg. záření se spojitým spektrem vzniká při prudkém zabrzdění urychlených elektronů.
Spektrofotometrické stanovení fosforečnanů ve vodách
 Spektrofotometrické stanovení fosforečnanů ve vodách Úkol: Spektrofotometricky stanovte obsah fosforečnanů ve vodě Chemikálie: 0,07165 g dihydrogenfosforečnan draselný KH 2 PO 4 75 ml kyselina sírová H
Spektrofotometrické stanovení fosforečnanů ve vodách Úkol: Spektrofotometricky stanovte obsah fosforečnanů ve vodě Chemikálie: 0,07165 g dihydrogenfosforečnan draselný KH 2 PO 4 75 ml kyselina sírová H
Optické spektroskopie 1 LS 2014/15
 Optické spektroskopie 1 LS 2014/15 Martin Kubala 585634179 mkubala@prfnw.upol.cz 1.Úvod Velikosti objektů v přírodě Dítě ~ 1 m (10 0 m) Prst ~ 2 cm (10-2 m) Vlas ~ 0.1 mm (10-4 m) Buňka ~ 20 m (10-5 m)
Optické spektroskopie 1 LS 2014/15 Martin Kubala 585634179 mkubala@prfnw.upol.cz 1.Úvod Velikosti objektů v přírodě Dítě ~ 1 m (10 0 m) Prst ~ 2 cm (10-2 m) Vlas ~ 0.1 mm (10-4 m) Buňka ~ 20 m (10-5 m)
CHEMIE. Pracovní list č. 5 - žákovská verze Téma: Vliv teploty na rychlost chemické reakce, teplota tání karboxylových kyselin. Mgr.
 www.projektsako.cz CHEMIE Pracovní list č. 5 - žákovská verze Téma: Vliv teploty na rychlost chemické reakce, teplota tání karboxylových kyselin Lektor: Mgr. Lenka Horutová Projekt: Student a konkurenceschopnost
www.projektsako.cz CHEMIE Pracovní list č. 5 - žákovská verze Téma: Vliv teploty na rychlost chemické reakce, teplota tání karboxylových kyselin Lektor: Mgr. Lenka Horutová Projekt: Student a konkurenceschopnost
