Tepelný stroj a jeho účinnost, Charlesův zákon
|
|
|
- Oldřich Marek
- před 8 lety
- Počet zobrazení:
Transkript
1 1 Tepelný stroj a jeho účinnost, Charlesův zákon Tepelný stroj... Abstrakt Pomůcky: Tepelný stroj PASCO TD-8572, sada plastových trubiček a ventilů, kovová tyč na míchání vody, skleňená nádoba, velká a malá kovová nádoba na vodu, dva stojany, elektrický vařič, Sada závaží, kovová baňka na plyn s gumovou zátkou se dvěma otvory, tlakový senzor PASCO CI-6534A, teploměr PASCO CI-6525, rotační senzor PASCO CI-6538, SCSI rozhraní PASCO SW 750, osobní počítač, program pro datový sběr Data Studio, 1 Pracovní úkoly a jejich řešení 1. V domácí přípravě vyřešte následující úlohu: Uvažujte tepelný stroj naplněný vzduchem, ve kterém se pohybuje válcový píst poloměru r = 2 cm. Hmotnost pístu činí m pist = 400 g. Necháme-li píst, aby vlastní vahou stlačil (ideální) plyn, a zatížíme-li píst závažím o hmotnosti m z = 300 g, pak objem stlačeného plynu (při okolním atmosferickém tlaku p atm = 101, 3 kp a a teplotě 20 C) činí 40 cm 3. Potom zafixujeme objem válce a při konstantním objemu zahřejeme plyn tak, že tlak v pístu bude o patnáct procet vyšší než okolní atmosferický tlak. Pak uvolníme fixaci objemu plynu a píst necháme izotermicky expandovat, až se pozice pístu volně ustálí. Potom z ppomalu odstraníme závaží tak, že nedochází ke změně teploty. Potom opět zafixujeme objem, plyn zchladíme na původní teplotu 20 C. Pak uvolníme fixaci objemu a píst opět zatěžkáváme závažím, aby se izotermicky vrátil do původní polohy. Určete práci, kterou tepelný stroj vykoná během jednoho takového cyklu. Určete teplotu, na kterou jsme plyn v pístu ohřáli. Dále určete účinnost tohoto cyklu. Tuto účinnost porovnejte s maximální možnou účinností pro daný rozdíl teplot, tj. s účinností Carnotova cyklu. Načrtněre a okomentujte pv diagram tohoto cyklu. Molární teplo vzduchu C v při konstantním objemu určete pomocí vztahu C p = M m.c p, kde M m je molární hmotnost vzduchu a c p je měrná tepelná kapacita vzduchu při konstantním tlaku. Z tabuklek lze vyčíst hodnoty M m = 28, 96 g.mol 1, c p = 1, 005 kj.kg 1.K 1. Plocha pístu S = πr 2 = 12, 6 cm 2 = 1, m 2, tlak pistu na plyn p pist = m pistg závaží na plyn činí p z = mzg S = 2,94 N 1, m 2 = 2, 3 kpa. Stav v bodu A: S = 3,92 N 1, m 2 = 3, 1 kpa, tlak p A = p atm + p pist + p z = 101, 3 kp a + 3, 1 kp a + 2, 3 kp a = 106, 7 kp a. V A = 40 cm 3 = m 3. T A = 20 C = 293, 2 K nr = p AV A T A = 106,7 kp a m 3 293,2 K = 1, J.K 1 n = 1, mol Stav v bodu : p = 1, 15 p atm = 116, 5 kp a. V = V A = 40 cm 3 = m 3. T = p V = 319, 2 K nr Stav v bodu C: p C = p A = 106, 7 kp a. V C = nrt C p C = 1, J.K 1.319,2 K = 4, m 3 = 43, 7 cm ,7 kp a T C = T = 319, 2 K Stav v bodu D: p D = p atm + p pist = 104, 4 kp a. V D = nrt D p D = 1, J.K 1.319,2 K = 4, m 3 = 44, 6 cm ,4 kp a T D = T C = T = 319, 2 K
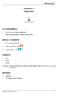
2 2 Stav v bodu : p = nrt V = 1, J.K 1.293,2 K 4, m 3 = 96, 0 kp a. V = V D = 4, m 3 = 44, 6 cm 3. T = T A = 293, 2 K Obrázek 1: Tepelnyý cyklus z úlohy č. 1 Práce vykonaná tepelným strojem: W = pdv + pdv = RnT V dv + W = 1, J.K 1 ln RnT V VD dv = Rn[Tln +T Aln VA ] = Rn.ln VD [T T A] (1) V V V [319, 2 K 293, 2 K] = 0, 041J (2) 40 cm3 Teplo dodané tepelnému stroji: Měrná teplná kapacita vzduchu při konstantním tlaku c p = 1, 005 kj.kg 1.K 1, molární hmotnost vzduchu M m = 28, 96 g.mol 1, poissonova konstanta κ = cp c v = 1, 40. Odtud lze dopočítat molární teplo při konstantním tlaku a při konstantním objemu: C p = M mc p = 28, 96 g.mol 1.1, 005 kj.kg 1.K 1 = 29, 10 J.mol 1.K 1, C v = Mmcp = 28,96 g.mol 1.1,005 kj.kg 1.K 1 = 20, 79 J.mol 1.K 1. κ 1,4 Mezi body A a : Q A = A Mezi body a D: Q D = A C vdt = nc v[t T A] = 1, mol.20, 79 J.mol 1.K 1.[319, 2 K 293, 2 K] = 0, 946 J. pdv = Rn.T ln VD V = 1, J.K 1 ln (3) [319, 2 K] = 0.507J (4) 40 cm3 Tepelné ztráty:
3 3 Mezi body D a : Q D = D Mezi body a A: Q A = D C vdt = nc v[t T D] = 1, mol.20, 79 J.mol 1.K 1.[293, 2 K 319, 2 K] = 0, 946 J. pdv = Rn.T Aln VA V = 1, J.K 1 ln (5) [293, 2 K] = 0.466J (6) 40 cm3 Tepelná účinnost cyklu: Carnotova účinnost: η = W 0, 041 J = Q A + Q D 0, 946 J + 0, 507 J = 2, = 2, 8% (7) η Carnot = 1 TA T = 1 293, 2 K = 1 0, 919 = 0, 081 = 8, 1%. (8) 319, 2 K V domácí přípravě je důležité, aby studenti spočítali alespoň práci tohoto cyklu a tepelnou bilanci v jednotlivých úsecích, aby měli představu o těchto pojmech. Výpočet účinnosti je citlivý na numerickou přesnost, zejména při určování objemů a počtu molů (resp. veličiny nr). Zaokrouhlení o jeden řád může vést ke zcela odlišným výsledkům. 2. Pomocí závaží o hmotnosti 150 g zkalibrujte tlakový senzor a určete rozdíl hmotností pístu P a zavěšeného závaží Z. Uvažte, jestli je možné tento rozdíl při zpracování zanedbat. V domácí přípravě si předem zpočtěte, jakou změnu tlaku způsobí zatěžkání pístu závažím o hmotnosti 150 g, když víte, že průměr pístu činí d = 32, 5mm. Tlak v pístu se kalibruje ve dvou bodech, první bez zývaží na plošině (tlak je pak roven součtu atmosferickému tlaku a tlaku způsobeného vlastní vahou pístu ). Tento tlak sa okalibruje jako 0 kp a. Druhý bod pro kalibraci získáme zatěžkáním pístu, doporučuje se závaží o hmotnost 150 g. Vzhledem k průměru pístu d = 3, 25 cm je příspěvek k tlaku p z = Fz = mz.g. (9) S pist π. d2 4 Pro závaží o hmotnosti 150 g je tlak závaží p z = 0, 15 kg.9, 81 m.c 2. = 1, 77 kp a. (10) π.2, m 2 Při kalibraci je třeba dát pozor, aby jednotky tlaku byly nastaveny jako Pascal, dále musí být citlivost tlakového senzor nastavena jako nízká (low), jinak by byl rozsah senzoru příliš malý. Je také třeba dát pozor, aby při kalibraci nedošlo k záměně kalibračních bodů. Dialog programu Data Studio totiž rozlišuje low point a high point. Rozdíl ve snímaném napětí mezi oběma kalibračními body be měl činit při zátěži 150 g asi 1 V. 3. Uvažujte vzduch jako ideální plyn. Zahříváním baňky s plynem při konstantním tlaku ověřte Charlesův zákon. Výslednou závislost objemu na teplotě znázorněte graficky. Z výsledku měření pak určete přibližný počet molů n plynu v uzavřené soustavě a extrapolací určete objem V 0 celé soustavy při minimálí možné poloze pístu ve válci, tj. pro situaci, kdy se píst dotýká dna válce. Na základě znalosti závislosti objemu na teplotě a počtu molů v soustavě dopočítejte standardní molární objem, tj. objem jednoho molu plynu za normálních podmínek, a porovnejte tento molárí objem s tabulkovou hodnotou. Při zahájení měření na teplotě T Ṽ = π d2 h. = 3, 14 1, m 2.3, m 4 4 =. 305 K byl píst ve výšce h = 33 mm nad dnem válce. To odpovídá objemu. = 2, m 3. = 27 cm 3. Po provedení měření (doba měření byla cca 40 minut) bylo naměřeno přibližně 1400 údajů, které jsou kraficky znázorněny v grafu na obrázku 2. Proložená přímka odpovídá rovnici V (T ) = a.t + b, kde a = cm 3.K 1 ; b = Odtud přímo vyplývá obsolutní hodnota objemu soustavy pži začátku měření V 0 + Ṽ =. 116 cm 3. Výsledná hodnota objemu soustavy při minimální poloze pístu ve válci tedy je V 0. = 116 cm 3 27 cm 3 = 89 cm 3. (11)
4 4 Obrázek 2: Charlesův zákon Po přeškálování objemu tedy máme vztah V = a.t, kde Atmosferický tlak činil 737, 1 T orr = 133, 3.737, 1 P a = 98.3 kp a. a = 0, 343 cm 3 K 1 = nr. (12) p soust V = 0, 343.T Tlakový příspěvek způsobený vlastní vahou pístu byl minimální (< 0.1kP a), proto jej lze zanedbat a do v7po4tu nezahrnout. Ze stavové rovnice ideálního plynu máme a = n = psoust.a R nr p soust, odtud pak dostaneme počet molů = 98, P a.0, m 3 K 1 8, 31 J.K 1.mol 1. = 4, mol. (13) Na základě závislosti 12 víme, že objem soustavy při teplotě 20 C je V 20 = 0, =. 101cm 3 = 1, m 3. Odtud máme objem jednoho V n = 1, m 3. = 24, m 3 mol 1. Hodnota mlárního objemu přitom podle 4, mol tabulek činí V n = 22, 413 m 3 mol Proved te dva cykly tepelného stroje. Pro každý cyklus volte jinou teplotu chladné lázně - pokojovou teplotu a 0 C. Pro každý cyklus určete vykonanou práci, účinnost a Carnotovu účinnost pro daný rozdíl teplot. 2 Poznámky 1. Při manipulaci s kovovou baňkou je třeba dbát, aby gumová zátka byla neustále dobře utěsněna. Tím se zabrání vniknutí vody do systému a potažmo tak i do pístu, čímž by se píst mohl poškodit. ehěm měření nezatlačujte ani nevytahjte gumovou zátku, zkreslovalo by to vásledek měření. 2. Píst nezatěžujte závažím o větší hmotnosti než 150g a nevyvíjejte v pístu relativní tlak větší než 1, 5kP a vzhledem k atmosferickému tlaku. Při větším přetlaku se projevují netěsností ventilů a měření se zkresluje. Průměr pístu činí d = 32, 5mm. 3. Plyn v systému nezahřívejte příliš rychle. Teploměr na prudkou změnu teploty reaguje se zpožděním a výsledek by se tak zkreslil. Při ověřování Charlesova zákona proto volte raději vetší kovovou nádobu na vodu, ve které budete zahřívat kovovou baňku s plynem. Vařič přitom nastavte na nejnižší stupeň. Teplotní růst pak bude pomalejší a měření teploty přesnější.
5 5 4. Při ověřování Charlesova zákona nejdříve začněte zahřívat nádobu s vodou a chvíli počkejte (3-10 min.), než začne růst objem. Teprve potom začněte měřit. Měření provádějte v rozmezí teplot cca 305 K 335 K. Očekávejte, že doma měření může být 40 minut až hodina. Vývoj teploty a tlaku sledujte na VT diagramu. Při měření pozorujte, jestli nedochází ke změně tlaku. Na základě znalosti atmosferického tlaku (zjistěte na barometru v praktiku) a tlaku způsobeného hmotností pístu (viz. úkol č. 2) převed te zjištěnou relativní hodnotu tlaku na hodnotu absolutní. Při zahájení měření odečtěte na stupnici, která se nachází na stěnách válce, polohu pístu. Jelikož tato poloha bude odpovídat nulovému relativnímu objemu určovanému programem Data Studio, budete moci na základě znalosti plochy pístu a po provedení extrapolace naměřených hodnot určit absolutní objem soustavy při minimální poloze pístu. Absolutní objem je nezbytné znát při zpracování úkolu č. 4. ěhem měření mějte na paměti poznámku číslo 3! 5. Při zahřívání vodu v kovové nádobě nikdy neuvádějte až do varu! 6. Před zahájením měření této úlohy si vyzkoušejte, s jakým třením se píst pohybuje v pístnici. To provedete tak, že u tlakového senzoru odpojíte plastovou trubičku, čímž se soutava otevře a píst by měl v pístnici začít stoupat nebo klesat. Směr pohybu pístu závisí na hmotnosti pístua závaží, které je upevněno na druhém konci provázku. V místech, kde se píst zadrhává, je pak tření vyšší a je radno se těmto polohám pístu vyhnout, zejména při jemnějším měření, jako je kalibrace tlakového senzoru. 7. Kalibraci tlakového senzoru provádějte tak, že píst nejdříve necháte nezatěžkaný a v dialogu programu Data Studio pro kalibraci tlakového senzoru tuto hodnotu označíte jako nula. Potom píst zatěžkejte závažím o hmotnosti g, na základě znalosti poloměru pístu dopočtěte příslušnou změnu tlaku a touto hodnotu vložte do zmíněného dialogu programu Data Studio. Tím je tlakový senzor zkalibrován. 8. Rozdíl hmotnosti pístu a závaží na konci provázku zjistěte následovně. Podle poznámky č. 7 zkalibrujte tlakový senzor, potom u tlakového senzoru odpojte plastovou trubici. Tím systém otevřete a tlakový senzor bude ukazovat záporný relativní tlak, který odpovídá atmosferickému tlaku. Pomocí této hodnoty pak již snadno určíte rozdíl hmotnosti pístu a závaží na konci provázku. Po provedení tohoto měření porovnejte zjištěný rozdíl tlaku způsobený hmotností pístu a závaží na konci provázku s atmosferickým tlakem a přesností, se kterou tlakový senzor měří tlak a zvažte, zdali je tento příspěvek k celkovému tlaku pro měření relevantní. 9. Při ověřování Charlesova zákona volte počáteční polohu pístu cca 0, 5 1cm nad minimální možnou polohou pístu. Zabráníte tak zkreslení výsledků měření. Minimální polohu pístu pak určíte pomocí rotačního senzoru. 10. Cykly tepelného stroje provádějte následujícím způsobem: aňku tepelného stroje umístěte do chladné lázně, počkejte, až se poloha pístu ustálí a zahajte měření (= stiskněte Start v programu Data Studio). Potom píst tepelného stroje zatěžkejte závažím, čímž stlačíte plyn ve válci. Potom baňku přemístěte do horké lázně, kterou budete mít připravenou na vařiči, zatížení pístu neměňte a opět vyčkejte, až se poloha pístu ustálí. Děj tedy bude izobarický. Snažte se, aby teplota obou lázní byla pokudmožno konstantn. Po ustálení polohy pístu sejměte závaží, opět nechte ustálit polohu pístu a pak baňku přesuňte zpět do chladné lázně. Vyčkejte, až se systém vrátí do počátečního stavu a pak ukončete měření. Graficky znázorněte a okomentujte pv diagram. Plochu obrazce v pv diagramu, která odpovídá vykonané práci, lze odečíst pomocí programu DataStudio. Rozmyslete, o jaký děj se jedná během zatěžkávání a odlehčování pístu. ěhem zpracování úkolu č. 4 určujte teplotu lázní pomocí dvou externích digitálních teploměrů, protože teploměr PASCO CI-6525 reaguje na změnu teploty příliš pomalu (viz. poznámka 3) a pro určení teploty je tedy nepoužitelný. Při zahájení měření odečtěte na milimetrové stupnici na stěně válce tepelného stroje polohu pístu, obdobně jako při měření úkolu č. 3. Na základě znalosti absolutního objemu soustavy při minimální poloze pístu měřené v úkolu č. 3 pak budete moci určit absolutní objemy během cyklu. Při přípravě chladné lázně o teplotě 0 C použijte led. 11.!! Po zahájení měření úkolu č. 3 neodpojujte plastové hadičky ani žádným jiným způsobem neotvírejte systém, a to až do konce měření úkolu č. 4, aby počet molů v systému, který je měřen v úkolu č. 3 byl stejný i během měření úkolu č. 4. Pokud toto porušíte, budete muset počet molů znovu určit na základě stavové rovnice ideálního plynu a znalosti absolutního objemu soustavy při minimální poloze válce měřené v úkolu č Literatura Reference [1] doc. RNDr. Zlatěk Maršák, CSc., Termodynamika a statistická fyzika, ČVUT Praha, 1995, Třetí vydání [2]
Práce tepelného stroje
 Fyzikální praktikum FJFI ČVUT v Praze Úloha č. 12 : Práce tepelného stroje Jméno: Ondřej Ticháček Pracovní skupina: 6 Kruh: ZS 6 Datum měření: 23.11.2012 Klasifikace: Část I Práce tepelného stroje 1 Zadání
Fyzikální praktikum FJFI ČVUT v Praze Úloha č. 12 : Práce tepelného stroje Jméno: Ondřej Ticháček Pracovní skupina: 6 Kruh: ZS 6 Datum měření: 23.11.2012 Klasifikace: Část I Práce tepelného stroje 1 Zadání
Termodynamika 2. UJOP Hostivař 2014
 Termodynamika 2 UJOP Hostivař 2014 Skupenské teplo tání/tuhnutí je (celkové) teplo, které přijme pevná látka při přechodu na kapalinu během tání nebo naopak Značka Veličina Lt J Nedochází při něm ke změně
Termodynamika 2 UJOP Hostivař 2014 Skupenské teplo tání/tuhnutí je (celkové) teplo, které přijme pevná látka při přechodu na kapalinu během tání nebo naopak Značka Veličina Lt J Nedochází při něm ke změně
3.5 Tepelné děje s ideálním plynem stálé hmotnosti, izotermický děj
 3.5 Tepelné děje s ideálním plynem stálé hmotnosti, izotermický děj a) tepelný děj přechod plynu ze stavu 1 do stavu tepelnou výměnou nebo konáním práce dále uvaž., že hmotnost plynu m = konst. a navíc
3.5 Tepelné děje s ideálním plynem stálé hmotnosti, izotermický děj a) tepelný děj přechod plynu ze stavu 1 do stavu tepelnou výměnou nebo konáním práce dále uvaž., že hmotnost plynu m = konst. a navíc
IDEÁLNÍ PLYN. Stavová rovnice
 IDEÁLNÍ PLYN Stavová rovnice Ideální plyn ) rozměry molekul jsou zanedbatelné vzhledem k jejich vzdálenostem 2) molekuly plynu na sebe působí jen při vzájemných srážkách 3) všechny srážky jsou dokonale
IDEÁLNÍ PLYN Stavová rovnice Ideální plyn ) rozměry molekul jsou zanedbatelné vzhledem k jejich vzdálenostem 2) molekuly plynu na sebe působí jen při vzájemných srážkách 3) všechny srážky jsou dokonale
FYZIKÁLNÍ PRAKTIKUM FJFI ČVUT V PRAZE. Měření Poissonovy konstanty vzduchu. Abstrakt
 FYZIKÁLNÍ PRAKTIKUM FJFI ČVUT V PRAZE Úloha 4: Měření dutých objemů vážením a kompresí plynu Datum měření: 23. 10. 2009 Měření Poissonovy konstanty vzduchu Jméno: Jiří Slabý Pracovní skupina: 1 Ročník
FYZIKÁLNÍ PRAKTIKUM FJFI ČVUT V PRAZE Úloha 4: Měření dutých objemů vážením a kompresí plynu Datum měření: 23. 10. 2009 Měření Poissonovy konstanty vzduchu Jméno: Jiří Slabý Pracovní skupina: 1 Ročník
Laboratorní práce č. 2: Určení měrné tepelné kapacity látky
 Přírodní vědy moderně a interaktivně FYZIKA 4. ročník šestiletého a 2. ročník čtyřletého studia Laboratorní práce č. 2: Určení měrné tepelné kapacity látky Přírodní vědy moderně a interaktivně FYZIKA
Přírodní vědy moderně a interaktivně FYZIKA 4. ročník šestiletého a 2. ročník čtyřletého studia Laboratorní práce č. 2: Určení měrné tepelné kapacity látky Přírodní vědy moderně a interaktivně FYZIKA
d p o r o v t e p l o m ě r, t e r m o č l á n k
 d p o r o v t e p l o m ě r, t e r m o č l á n k Ú k o l : a) Proveďte kalibraci odporového teploměru, termočlánku a termistoru b) Určete teplotní koeficienty odporového teploměru, konstanty charakterizující
d p o r o v t e p l o m ě r, t e r m o č l á n k Ú k o l : a) Proveďte kalibraci odporového teploměru, termočlánku a termistoru b) Určete teplotní koeficienty odporového teploměru, konstanty charakterizující
Cvičení z termomechaniky Cvičení 3.
 Příklad 1 1kg plynu při izobarickém ohřevu o 710 [ C] z teploty 40[ C] vykonal práci 184,5 [kj.kg -1 ]. Vypočítejte molovou hmotnost plynu, množství přivedeného tepla a změnu vnitřní energie ΔT = 710 [K]
Příklad 1 1kg plynu při izobarickém ohřevu o 710 [ C] z teploty 40[ C] vykonal práci 184,5 [kj.kg -1 ]. Vypočítejte molovou hmotnost plynu, množství přivedeného tepla a změnu vnitřní energie ΔT = 710 [K]
9. Struktura a vlastnosti plynů
 9. Struktura a vlastnosti plynů Osnova: 1. Základní pojmy 2. Střední kvadratická rychlost 3. Střední kinetická energie molekuly plynu 4. Stavová rovnice ideálního plynu 5. Jednoduché děje v plynech a)
9. Struktura a vlastnosti plynů Osnova: 1. Základní pojmy 2. Střední kvadratická rychlost 3. Střední kinetická energie molekuly plynu 4. Stavová rovnice ideálního plynu 5. Jednoduché děje v plynech a)
Fyzikální praktikum 1
 Fyzikální praktikum 1 FJFI ČVUT v Praze Úloha: č. 5 - Kalibrace teploměru, skupenské teplo Jméno: Ondřej Finke Datum měření: 6.10.2014 Kruh: FE Skupina: 4 Klasifikace: 1. Pracovní úkoly 1.1 - Kalibrace
Fyzikální praktikum 1 FJFI ČVUT v Praze Úloha: č. 5 - Kalibrace teploměru, skupenské teplo Jméno: Ondřej Finke Datum měření: 6.10.2014 Kruh: FE Skupina: 4 Klasifikace: 1. Pracovní úkoly 1.1 - Kalibrace
Úloha č.1: Stanovení molární tepelné kapacity plynu za konstantního tlaku
 Úloha č.1: Stanovení molární tepelné kapacity plynu za konstantního tlaku Teorie První termodynamický zákon je definován du dq dw (1) kde du je totální diferenciál vnitřní energie a dq a dw jsou neúplné
Úloha č.1: Stanovení molární tepelné kapacity plynu za konstantního tlaku Teorie První termodynamický zákon je definován du dq dw (1) kde du je totální diferenciál vnitřní energie a dq a dw jsou neúplné
Ideální plyn. Stavová rovnice Děje v ideálním plynu Práce plynu, Kruhový děj, Tepelné motory
 Struktura a vlastnosti plynů Ideální plyn Vlastnosti ideálního plynu: Ideální plyn Stavová rovnice Děje v ideálním plynu Práce plynu, Kruhový děj, epelné motory rozměry molekul jsou ve srovnání se střední
Struktura a vlastnosti plynů Ideální plyn Vlastnosti ideálního plynu: Ideální plyn Stavová rovnice Děje v ideálním plynu Práce plynu, Kruhový děj, epelné motory rozměry molekul jsou ve srovnání se střední
Mol. fyz. a termodynamika
 Molekulová fyzika pracuje na základě kinetické teorie látek a statistiky Termodynamika zkoumání tepelných jevů a strojů nezajímají nás jednotlivé částice Molekulová fyzika základem jsou: Látka kteréhokoli
Molekulová fyzika pracuje na základě kinetické teorie látek a statistiky Termodynamika zkoumání tepelných jevů a strojů nezajímají nás jednotlivé částice Molekulová fyzika základem jsou: Látka kteréhokoli
Laboratorní cvičení z fyziky Stavová rovnice plynu
 Autor: Mgr. Ivana Stefanová Jméno souboru: StavRovnice Poslední úprava: 8. května 2016 Obsah Pracovní úkoly...1 Teorie...1 Protokol o měření...2 Pracovní postup...2 Izotermický děj...2 Izochorický děj...2
Autor: Mgr. Ivana Stefanová Jméno souboru: StavRovnice Poslední úprava: 8. května 2016 Obsah Pracovní úkoly...1 Teorie...1 Protokol o měření...2 Pracovní postup...2 Izotermický děj...2 Izochorický děj...2
FJFI ČVUT V PRAZE. Úloha 8: Závislost odporu termistoru na teplotě
 ZÁKLADY FYZIKÁLNÍCH MĚŘENÍ FJFI ČVUT V PRAZE Datum měření: 29. 4. 2009 Pracovní skupina: 3, středa 5:30 Spolupracovali: Monika Donovalová, Štěpán Novotný Jméno: Jiří Slabý Ročník, kruh:. ročník, 2. kruh
ZÁKLADY FYZIKÁLNÍCH MĚŘENÍ FJFI ČVUT V PRAZE Datum měření: 29. 4. 2009 Pracovní skupina: 3, středa 5:30 Spolupracovali: Monika Donovalová, Štěpán Novotný Jméno: Jiří Slabý Ročník, kruh:. ročník, 2. kruh
Fyzikální praktikum FJFI ČVUT v Praze
 Fyzikální praktikum FJFI ČVUT v Praze Úloha 6: Kalibrace teploměru, skupenské teplo Datum měření: 17. 12. 2015 Skupina: 8, čtvrtek 7:30 Vypracoval: Tadeáš Kmenta Klasifikace: Část I Kalibrace rtuťového
Fyzikální praktikum FJFI ČVUT v Praze Úloha 6: Kalibrace teploměru, skupenské teplo Datum měření: 17. 12. 2015 Skupina: 8, čtvrtek 7:30 Vypracoval: Tadeáš Kmenta Klasifikace: Část I Kalibrace rtuťového
LOGO. Struktura a vlastnosti plynů Ideální plyn
 Struktura a vlastnosti plynů Ideální plyn Ideální plyn Protože popsat chování plynů je nad naše možnosti, zavádíme zjednodušený model tzv. ideálního plynu, který má tyto vlastnosti: Částice ideálního plynu
Struktura a vlastnosti plynů Ideální plyn Ideální plyn Protože popsat chování plynů je nad naše možnosti, zavádíme zjednodušený model tzv. ideálního plynu, který má tyto vlastnosti: Částice ideálního plynu
Přijímací zkouška na navazující magisterské studium 2017 Studijní program: Fyzika Studijní obory: FFUM
 Přijímací zkouška na navazující magisterské studium 207 Studijní program: Fyzika Studijní obory: FFUM Varianta A Řešení příkladů pečlivě odůvodněte. Příklad (25 bodů) Nechť (a) Spočtěte lim n x n. (b)
Přijímací zkouška na navazující magisterské studium 207 Studijní program: Fyzika Studijní obory: FFUM Varianta A Řešení příkladů pečlivě odůvodněte. Příklad (25 bodů) Nechť (a) Spočtěte lim n x n. (b)
Základem molekulové fyziky je kinetická teorie látek. Vychází ze tří pouček:
 Molekulová fyzika zkoumá vlastnosti látek na základě jejich vnitřní struktury, pohybu a vzájemného působení částic, ze kterých se látky skládají. Termodynamika se zabývá zákony přeměny různých forem energie
Molekulová fyzika zkoumá vlastnosti látek na základě jejich vnitřní struktury, pohybu a vzájemného působení částic, ze kterých se látky skládají. Termodynamika se zabývá zákony přeměny různých forem energie
Spalování CÍL EXPERIMENTU MODULY A SENZORY POMŮCKY MATERIÁL. Experiment C-5
 Experiment C-5 Spalování CÍL EXPERIMENTU Studium procesu hoření a spalování. Měření hladiny kyslíku v průběhu hoření svíčky. MODULY A SENZORY PC + program NeuLog TM USB modul USB 200 Oxymetr NUL 205 POMŮCKY
Experiment C-5 Spalování CÍL EXPERIMENTU Studium procesu hoření a spalování. Měření hladiny kyslíku v průběhu hoření svíčky. MODULY A SENZORY PC + program NeuLog TM USB modul USB 200 Oxymetr NUL 205 POMŮCKY
Molekulová fyzika a termika. Přehled základních pojmů
 Molekulová fyzika a termika Přehled základních pojmů Kinetická teorie látek Vychází ze tří experimentálně ověřených poznatků: 1) Látky se skládají z částic - molekul, atomů nebo iontů, mezi nimiž jsou
Molekulová fyzika a termika Přehled základních pojmů Kinetická teorie látek Vychází ze tří experimentálně ověřených poznatků: 1) Látky se skládají z částic - molekul, atomů nebo iontů, mezi nimiž jsou
Příklady k zápočtu molekulová fyzika a termodynamika
 Příklady k zápočtu molekulová fyzika a termodynamika 1. Do vody o teplotě t 1 70 C a hmotnosti m 1 1 kg vhodíme kostku ledu o teplotě t 2 10 C a hmotnosti m 2 2 kg. Do soustavy vzápětí přilijeme další
Příklady k zápočtu molekulová fyzika a termodynamika 1. Do vody o teplotě t 1 70 C a hmotnosti m 1 1 kg vhodíme kostku ledu o teplotě t 2 10 C a hmotnosti m 2 2 kg. Do soustavy vzápětí přilijeme další
PLYNNÉ LÁTKY. Mgr. Jan Ptáčník - GJVJ - Fyzika - Termika - 2. ročník
 PLYNNÉ LÁTKY Mgr. Jan Ptáčník - GJVJ - Fyzika - Termika - 2. ročník Ideální plyn Po molekulách ideálního plynu požadujeme: 1.Rozměry molekul ideálního plynu jsou ve srovnání se střední vzdáleností molekul
PLYNNÉ LÁTKY Mgr. Jan Ptáčník - GJVJ - Fyzika - Termika - 2. ročník Ideální plyn Po molekulách ideálního plynu požadujeme: 1.Rozměry molekul ideálního plynu jsou ve srovnání se střední vzdáleností molekul
Kalibrace teploměru, skupenské teplo Abstrakt: V této úloze se studenti seznámí s metodou kalibrace teploměru a na základě svých
 Úloha 6 02PRA1 Fyzikální praktikum 1 Kalibrace teploměru, skupenské teplo Abstrakt: V této úloze se studenti seznámí s metodou kalibrace teploměru a na základě svých měření i ověří Gay-Lussacův zákon.
Úloha 6 02PRA1 Fyzikální praktikum 1 Kalibrace teploměru, skupenské teplo Abstrakt: V této úloze se studenti seznámí s metodou kalibrace teploměru a na základě svých měření i ověří Gay-Lussacův zákon.
TLAK PLYNU V UZAVŘENÉ NÁDOBĚ
 TLAK PLYNU V UZAVŘENÉ NÁDOBĚ Vzdělávací předmět: Fyzika Tematický celek dle RVP: Mechanické vlastnosti tekutin Tematická oblast: Mechanické vlastnosti plynů Cílová skupina: Žák 7. ročníku základní školy
TLAK PLYNU V UZAVŘENÉ NÁDOBĚ Vzdělávací předmět: Fyzika Tematický celek dle RVP: Mechanické vlastnosti tekutin Tematická oblast: Mechanické vlastnosti plynů Cílová skupina: Žák 7. ročníku základní školy
pracovní list studenta Struktura a vlastnosti plynů Stavová rovnice ideálního plynu Vojtěch Beneš
 Výstup RVP: Klíčová slova: pracovní list studenta Struktura a vlastnosti plynů Vojtěch Beneš žák měří vybrané fyzikální veličiny vhodnými metodami, zpracuje a vyhodnotí výsledky měření, aplikuje s porozuměním
Výstup RVP: Klíčová slova: pracovní list studenta Struktura a vlastnosti plynů Vojtěch Beneš žák měří vybrané fyzikální veličiny vhodnými metodami, zpracuje a vyhodnotí výsledky měření, aplikuje s porozuměním
Teplota a její měření
 Teplota a její měření Teplota a její měření Číslo DUM v digitálním archivu školy VY_32_INOVACE_07_03_01 Teplota, Celsiova a Kelvinova teplotní stupnice, převodní vztahy, příklady. Tepelná výměna, měrná
Teplota a její měření Teplota a její měření Číslo DUM v digitálním archivu školy VY_32_INOVACE_07_03_01 Teplota, Celsiova a Kelvinova teplotní stupnice, převodní vztahy, příklady. Tepelná výměna, měrná
Poznámky k cvičením z termomechaniky Cvičení 3.
 Vnitřní energie U Vnitřní energie U je stavová veličina U = U (p, V, T), ale závisí pouze na teplotě (experiment Gay-Lussac / Joule) U = f(t) Pro měrnou vnitřní energii (tedy pro vnitřní energii jednoho
Vnitřní energie U Vnitřní energie U je stavová veličina U = U (p, V, T), ale závisí pouze na teplotě (experiment Gay-Lussac / Joule) U = f(t) Pro měrnou vnitřní energii (tedy pro vnitřní energii jednoho
Závislost odporu termistoru na teplotě
 Fyzikální praktikum pro JCH, Bc Jméno a příjmení: Zuzana Dočekalová Datum: 21.4.2010 Spolupracovník: Aneta Sajdová Obor: Jaderně chemické inženýrství Číslo studenta: 5 (středa 9:30) Ročník: II. Číslo úlohy:
Fyzikální praktikum pro JCH, Bc Jméno a příjmení: Zuzana Dočekalová Datum: 21.4.2010 Spolupracovník: Aneta Sajdová Obor: Jaderně chemické inženýrství Číslo studenta: 5 (středa 9:30) Ročník: II. Číslo úlohy:
Měření Poissonovy konstanty a dutých objemů Abstrakt: V této úloze se studenti seznámí s různými metodami
 FJFI ČVUT v Praze Fyzikální praktikum I Úloha 5 Verze 160927 Měření Poissonovy konstanty a dutých objemů Abstrakt: V této úloze se studenti seznámí s různými metodami měření Poissonovy konstanty, ty použijí
FJFI ČVUT v Praze Fyzikální praktikum I Úloha 5 Verze 160927 Měření Poissonovy konstanty a dutých objemů Abstrakt: V této úloze se studenti seznámí s různými metodami měření Poissonovy konstanty, ty použijí
Fyzika. Pracovní list č. 5 Téma: Měření teploty, relativní vlhkosti, rosného bodu, absolutní vlhkosti. Mgr. Libor Lepík. Student a konkurenceschopnost
 www.projektsako.cz Fyzika Pracovní list č. 5 Téma: Měření teploty, relativní vlhkosti, rosného bodu, absolutní vlhkosti Lektor: Projekt: Reg. číslo: Mgr. Libor Lepík Student a konkurenceschopnost CZ.1.07/1.1.07/03.0075
www.projektsako.cz Fyzika Pracovní list č. 5 Téma: Měření teploty, relativní vlhkosti, rosného bodu, absolutní vlhkosti Lektor: Projekt: Reg. číslo: Mgr. Libor Lepík Student a konkurenceschopnost CZ.1.07/1.1.07/03.0075
Kalorimetrická měření I
 KATEDRA EXPERIMENTÁLNÍ FYZIKY PŘÍRODOVĚDECKÁ FAKULTA UNIVERZITY PALACKÉHO V OLOMOUCI FYZIKÁLNÍ PRAKTIKUM Z MOLEKULOVÉ FYZIKY A TERMODYNAMIKY Kalorimetrická měření I Úvod Teplo Teplo Q je určeno energií,
KATEDRA EXPERIMENTÁLNÍ FYZIKY PŘÍRODOVĚDECKÁ FAKULTA UNIVERZITY PALACKÉHO V OLOMOUCI FYZIKÁLNÍ PRAKTIKUM Z MOLEKULOVÉ FYZIKY A TERMODYNAMIKY Kalorimetrická měření I Úvod Teplo Teplo Q je určeno energií,
du dq dw je totální diferenciál vnitřní energie a respektive práce. Pokud systém může konat pouze objemovou práci platí OCHV
 Úloha č.2: Stanovení učinnosti hořáku, Carnotovy termodynamické účinnosti, reálné vnitřní účinnosti a mechanické účinnosti a z nich vypočtená celková účinnost přeměny tepla na mechanickou energii ve Stirlingově
Úloha č.2: Stanovení učinnosti hořáku, Carnotovy termodynamické účinnosti, reálné vnitřní účinnosti a mechanické účinnosti a z nich vypočtená celková účinnost přeměny tepla na mechanickou energii ve Stirlingově
III. STRUKTURA A VLASTNOSTI PLYNŮ
 III. STRUKTURA A VLASTNOSTI PLYNŮ 3.1 Ideální plyn a) ideální plyn model, předpoklady: 1. rozměry molekul malé (ve srovnání se střední vzdáleností molekul). molekuly na sebe navzálem silově nepůsobí (mimo
III. STRUKTURA A VLASTNOSTI PLYNŮ 3.1 Ideální plyn a) ideální plyn model, předpoklady: 1. rozměry molekul malé (ve srovnání se střední vzdáleností molekul). molekuly na sebe navzálem silově nepůsobí (mimo
1/6. 2. Stavová rovnice, plynová konstanta, Avogadrův zákon, kilomol plynu
 1/6 2. Stavová rovnice, plynová konstanta, Avogadrův zákon, kilomol plynu Příklad: 2.1, 2.2, 2.3, 2.4, 2.5, 2.6, 2.7, 2.8, 2.9, 2.10, 2.11, 2.12, 2.13, 2.14, 2.15, 2.16, 2.17, 2.18, 2.19, 2.20, 2.21, 2.22,
1/6 2. Stavová rovnice, plynová konstanta, Avogadrův zákon, kilomol plynu Příklad: 2.1, 2.2, 2.3, 2.4, 2.5, 2.6, 2.7, 2.8, 2.9, 2.10, 2.11, 2.12, 2.13, 2.14, 2.15, 2.16, 2.17, 2.18, 2.19, 2.20, 2.21, 2.22,
Měření Poissonovy konstanty a dutých objemů Abstrakt: V této úloze se studenti seznámí s různými metodami
 FJFI ČVUT v Praze Fyzikální praktikum I Úloha 5 Verze 171006 Měření Poissonovy konstanty a dutých objemů Abstrakt: V této úloze se studenti seznámí s různými metodami měření Poissonovy konstanty, ty použijí
FJFI ČVUT v Praze Fyzikální praktikum I Úloha 5 Verze 171006 Měření Poissonovy konstanty a dutých objemů Abstrakt: V této úloze se studenti seznámí s různými metodami měření Poissonovy konstanty, ty použijí
PRAKTIKUM I. Oddělení fyzikálních praktik při Kabinetu výuky obecné fyziky MFF UK. Pracoval: Pavel Ševeček stud. skup.: F/F1X/11 dne:
 Oddělení fyzikálních praktik při Kabinetu výuky obecné fyziky MFF UK PRAKTIKUM I. Úloha č. VIII Název: Kalibrace odporového teploměru a termočlánku fázové přechody Pracoval: Pavel Ševeček stud. skup.:
Oddělení fyzikálních praktik při Kabinetu výuky obecné fyziky MFF UK PRAKTIKUM I. Úloha č. VIII Název: Kalibrace odporového teploměru a termočlánku fázové přechody Pracoval: Pavel Ševeček stud. skup.:
Řešení úloh 1. kola 58. ročníku fyzikální olympiády. Kategorie C Autoři úloh: J. Thomas (1, 2, 5, 6, 7), J. Jírů (3), L.
 Řešení úloh 1. kola 58. ročníku fyzikální olympiády. Kategorie C Autoři úloh: J. Thomas (1, 2, 5, 6, 7), J. Jírů (3), L. Ledvina (4) 1.a) Na dosažení rychlosti v 0 potřebuje každý automobil dobu t v 0
Řešení úloh 1. kola 58. ročníku fyzikální olympiády. Kategorie C Autoři úloh: J. Thomas (1, 2, 5, 6, 7), J. Jírů (3), L. Ledvina (4) 1.a) Na dosažení rychlosti v 0 potřebuje každý automobil dobu t v 0
VÝHODY A NEVÝHODY PNEUMATICKÝCH MECHANISMŮ
 VÝHODY A NEVÝHODY PNEUMATICKÝCH MECHANISMŮ Výhody: medium (vzduch) se nachází všude kolem nás možnost využití centrální výroby stlačeného vzduchu v závodě kompresor nemusí pracovat nepřetržitě (stlačený
VÝHODY A NEVÝHODY PNEUMATICKÝCH MECHANISMŮ Výhody: medium (vzduch) se nachází všude kolem nás možnost využití centrální výroby stlačeného vzduchu v závodě kompresor nemusí pracovat nepřetržitě (stlačený
pv = nrt. Lord Celsius udržoval konstantní tlak plynu v uzavřené soustavě. Potom můžeme napsat T, tedy V = C(t t0) = Ct Ct0, (1)
 17. ročník, úloha I. E... absolutní nula (8 bodů; průměr 4,03; řešilo 40 studentů) S experimentálním vybavením dostupným v době Lorda Celsia změřte teplotu absolutní nuly (v Celsiově stupnici). Poradíme
17. ročník, úloha I. E... absolutní nula (8 bodů; průměr 4,03; řešilo 40 studentů) S experimentálním vybavením dostupným v době Lorda Celsia změřte teplotu absolutní nuly (v Celsiově stupnici). Poradíme
Charlesův zákon (pt závislost)
 Charlesův zákon (pt závislost) V této úloze pomocí čidla tlaku plynu GPS-BTA a teploměru TMP-BTA (nebo čidla Go!Temp) objevíme součást stavové rovnice ideálního plynu Charlesův zákon popisující izochorický
Charlesův zákon (pt závislost) V této úloze pomocí čidla tlaku plynu GPS-BTA a teploměru TMP-BTA (nebo čidla Go!Temp) objevíme součást stavové rovnice ideálního plynu Charlesův zákon popisující izochorický
Fyzikální učebna vybavená audiovizuální technikou, interaktivní tabule, fyzikální pomůcky
 Předmět: Náplň: Třída: Počet hodin: Pomůcky: Fyzika (FYZ) Molekulová fyzika, termika 2. ročník, sexta 2 hodiny týdně Fyzikální učebna vybavená audiovizuální technikou, interaktivní tabule, fyzikální pomůcky
Předmět: Náplň: Třída: Počet hodin: Pomůcky: Fyzika (FYZ) Molekulová fyzika, termika 2. ročník, sexta 2 hodiny týdně Fyzikální učebna vybavená audiovizuální technikou, interaktivní tabule, fyzikální pomůcky
Poznámky k semináři z termomechaniky Grafy vody a vodní páry
 Příklad 1 Sytá pára o tlaku 1 [MPa] expanduje izotermicky na tlak 0,1 [MPa]. Znázorněte v diagramech vody a vodní páry. Jelikož se jedná o izotermický děj, je výhodné použít diagram T-s. Dále máme v zadání,
Příklad 1 Sytá pára o tlaku 1 [MPa] expanduje izotermicky na tlak 0,1 [MPa]. Znázorněte v diagramech vody a vodní páry. Jelikož se jedná o izotermický děj, je výhodné použít diagram T-s. Dále máme v zadání,
FYZIKÁLNÍ PRAKTIKUM FJFI ČVUT V PRAZE
 FYZIKÁLNÍ PRAKTIKUM FJFI ČVUT V PRAZE Úloha 3. Vzduchová dráha - ZZE, srážky, impuls síly Autor David Horák Datum měření 21. 11. 2011 Kruh 1 Skupina 7 Klasifikace 1. PRACOVNÍ ÚKOLY: 1) Elastické srážky:
FYZIKÁLNÍ PRAKTIKUM FJFI ČVUT V PRAZE Úloha 3. Vzduchová dráha - ZZE, srážky, impuls síly Autor David Horák Datum měření 21. 11. 2011 Kruh 1 Skupina 7 Klasifikace 1. PRACOVNÍ ÚKOLY: 1) Elastické srážky:
1. Okalibrujte pomocí bodu tání ledu, bodu varu vody a bodu tuhnutí cínu:
 1 Pracovní úkol 1. Okalibrujte pomocí bodu tání ledu, bodu varu vody a bodu tuhnutí cínu: (a) platinovýodporovýteploměr(určetekonstanty R 0, A, B). (b) termočlánek měď-konstantan(určete konstanty a, b,
1 Pracovní úkol 1. Okalibrujte pomocí bodu tání ledu, bodu varu vody a bodu tuhnutí cínu: (a) platinovýodporovýteploměr(určetekonstanty R 0, A, B). (b) termočlánek měď-konstantan(určete konstanty a, b,
Termodynamika. Děj, který není kvazistatický, se nazývá nestatický.
 Termodynamika Zabývá se ději, při nichž se mění tepelná energie v jiné druhy energie (zejména mechanické). Studuje vlastnosti látek bez přihlédnutí k jejich mikrostruktuře. Je vystavěna na axiomech (0.,
Termodynamika Zabývá se ději, při nichž se mění tepelná energie v jiné druhy energie (zejména mechanické). Studuje vlastnosti látek bez přihlédnutí k jejich mikrostruktuře. Je vystavěna na axiomech (0.,
Mechanické pokusy na vzduchové dráze
 Fyzikální praktikum FJFI ČVUT v Praze Úloha č. 3 : Mechanické pokusy na vzduchové dráze Jméno: Ondřej Ticháček Pracovní skupina: 6 Kruh: ZS 6 Datum měření: 14.12.2012 Klasifikace: Část I Mechanické pokusy
Fyzikální praktikum FJFI ČVUT v Praze Úloha č. 3 : Mechanické pokusy na vzduchové dráze Jméno: Ondřej Ticháček Pracovní skupina: 6 Kruh: ZS 6 Datum měření: 14.12.2012 Klasifikace: Část I Mechanické pokusy
HPS - SEŘÍZENÍ PID REGULÁTORU PODLE PŘECHODOVÉ CHARAKTERISTIKY
 Schéma PS - SEŘÍZENÍ PID REGULÁTORU PODLE PŘECODOVÉ CARAKTERISTIKY A1 K1L U1 K1R A2 PC K2L K2R B1 U2 B2 PjR PjR F C1 S1 h L S2 F C2 h R A/D, D/A PŘEVODNÍK A OVLÁDACÍ JEDNOTKA u R u L Obr. 1 Schéma úlohy
Schéma PS - SEŘÍZENÍ PID REGULÁTORU PODLE PŘECODOVÉ CARAKTERISTIKY A1 K1L U1 K1R A2 PC K2L K2R B1 U2 B2 PjR PjR F C1 S1 h L S2 F C2 h R A/D, D/A PŘEVODNÍK A OVLÁDACÍ JEDNOTKA u R u L Obr. 1 Schéma úlohy
STRUKTURA A VLASTNOSTI PLYNŮ POJMY K ZOPAKOVÁNÍ. Testové úlohy varianta A
 Škola: Autor: DUM: Vzdělávací obor: Tematický okruh: Téma: Masarykovo gymnázium Vsetín Mgr. Jitka Novosadová MGV_F_SS_3S3_D09_Z_OPAK_T_Plyny_T Člověk a příroda Fyzika Struktura a vlastnosti plynů Opakování
Škola: Autor: DUM: Vzdělávací obor: Tematický okruh: Téma: Masarykovo gymnázium Vsetín Mgr. Jitka Novosadová MGV_F_SS_3S3_D09_Z_OPAK_T_Plyny_T Člověk a příroda Fyzika Struktura a vlastnosti plynů Opakování
Termodynamika. T [K ]=t [ 0 C] 273,15 T [ K ]= t [ 0 C] termodynamická teplota: Stavy hmoty. jednotka: 1 K (kelvin) = 1/273,16 část termodynamické
![Termodynamika. T [K ]=t [ 0 C] 273,15 T [ K ]= t [ 0 C] termodynamická teplota: Stavy hmoty. jednotka: 1 K (kelvin) = 1/273,16 část termodynamické Termodynamika. T [K ]=t [ 0 C] 273,15 T [ K ]= t [ 0 C] termodynamická teplota: Stavy hmoty. jednotka: 1 K (kelvin) = 1/273,16 část termodynamické](/thumbs/24/2778201.jpg) Termodynamika termodynamická teplota: Stavy hmoty jednotka: 1 K (kelvin) = 1/273,16 část termodynamické teploty trojného bodu vody (273,16 K = 0,01 o C). 0 o C = 273,15 K T [K ]=t [ 0 C] 273,15 T [ K ]=
Termodynamika termodynamická teplota: Stavy hmoty jednotka: 1 K (kelvin) = 1/273,16 část termodynamické teploty trojného bodu vody (273,16 K = 0,01 o C). 0 o C = 273,15 K T [K ]=t [ 0 C] 273,15 T [ K ]=
Úloha 5: Kalibrace rtuťového teploměru plynovým varu vody
 Úloha 5: Kalibrace rtuťového teploměru plynovým teploměrem, měření měrného skupenského tepla varu vody FYZIKÁLNÍ PRAKTIKUM FJFI ČVUT V PRAZE Datum měření: 9.11.2009 Jméno: František Batysta Pracovní skupina:
Úloha 5: Kalibrace rtuťového teploměru plynovým teploměrem, měření měrného skupenského tepla varu vody FYZIKÁLNÍ PRAKTIKUM FJFI ČVUT V PRAZE Datum měření: 9.11.2009 Jméno: František Batysta Pracovní skupina:
6. Jaký je výkon vařiče, který ohřeje 1 l vody o 40 C během 5 minut? Měrná tepelná kapacita vody je W)
 TEPLO 1. Na udržení stále teploty v místnosti se za hodinu spotřebuje 4,2 10 6 J tepla. olik vody proteče radiátorem ústředního topení za hodinu, jestliže má voda při vstupu do radiátoru teplotu 80 ºC
TEPLO 1. Na udržení stále teploty v místnosti se za hodinu spotřebuje 4,2 10 6 J tepla. olik vody proteče radiátorem ústředního topení za hodinu, jestliže má voda při vstupu do radiátoru teplotu 80 ºC
Měření měrné tepelné kapacity látek kalorimetrem
 Měření měrné tepelné kapacity látek kalorimetrem Problém A. Změření kapacity kalorimetru (tzv. vodní hodnota) pomocí elektrického ohřevu s měřeným příkonem. B. Změření měrné tepelné kapacity hliníku směšovací
Měření měrné tepelné kapacity látek kalorimetrem Problém A. Změření kapacity kalorimetru (tzv. vodní hodnota) pomocí elektrického ohřevu s měřeným příkonem. B. Změření měrné tepelné kapacity hliníku směšovací
HYDROSTATICKÝ PARADOX
 HYDROSTATICKÝ PARADOX Vzdělávací předmět: Fyzika Tematický celek dle RVP: Mechanické vlastnosti tekutin Tematická oblast: Mechanické vlastnosti kapalin Cílová skupina: Žák 7. ročníku základní školy Cílem
HYDROSTATICKÝ PARADOX Vzdělávací předmět: Fyzika Tematický celek dle RVP: Mechanické vlastnosti tekutin Tematická oblast: Mechanické vlastnosti kapalin Cílová skupina: Žák 7. ročníku základní školy Cílem
Základní pojmy a jednotky
 Základní pojmy a jednotky Tlak: p = F S [N. m 2 ] [kg. m. s 2. m 2 ] [kg. m 1. s 2 ] [Pa] (1) Hydrostatický tlak: p = h. ρ. g [m. kg. m 3. m. s 2 ] [kg. m 1. s 2 ] [Pa] (2) Převody jednotek tlaku: Bar
Základní pojmy a jednotky Tlak: p = F S [N. m 2 ] [kg. m. s 2. m 2 ] [kg. m 1. s 2 ] [Pa] (1) Hydrostatický tlak: p = h. ρ. g [m. kg. m 3. m. s 2 ] [kg. m 1. s 2 ] [Pa] (2) Převody jednotek tlaku: Bar
Vyhodnocení součinitele alfa z dat naměřených v reálných podmínkách při teplotách 80 C a pokojové teplotě.
 oučinitel odporu Vyhodnocení součinitele alfa z dat naměřených v reálných podmínkách při teplotách 80 C a pokojové teplotě Zadání: Vypočtěte hodnotu součinitele α s platinového odporového teploměru Pt-00
oučinitel odporu Vyhodnocení součinitele alfa z dat naměřených v reálných podmínkách při teplotách 80 C a pokojové teplotě Zadání: Vypočtěte hodnotu součinitele α s platinového odporového teploměru Pt-00
Termodynamika 1. UJOP Hostivař 2014
 Termodynamika 1 UJOP Hostivař 2014 Termodynamika Zabývá se tepelnými ději obecně. Existují 3 termodynamické zákony: 1. Celkové množství energie (všech druhů) izolované soustavy zůstává zachováno. 2. Teplo
Termodynamika 1 UJOP Hostivař 2014 Termodynamika Zabývá se tepelnými ději obecně. Existují 3 termodynamické zákony: 1. Celkové množství energie (všech druhů) izolované soustavy zůstává zachováno. 2. Teplo
1. Okalibrujte pomocí bodu tání ledu, bodu varu vody a bodu tuhnutí cínu:
 1 Pracovní úkoly 1. Okalibrujte pomocí bodu tání ledu, bodu varu vody a bodu tuhnutí cínu: a. platinový odporový teploměr (určete konstanty R 0, A, B) b. termočlánek měď-konstantan (určete konstanty a,
1 Pracovní úkoly 1. Okalibrujte pomocí bodu tání ledu, bodu varu vody a bodu tuhnutí cínu: a. platinový odporový teploměr (určete konstanty R 0, A, B) b. termočlánek měď-konstantan (určete konstanty a,
Cvičení z termomechaniky Cvičení 7 Seminář z termomechaniky
 Příklad 1 Plynová turbína pracuje dle Ericsson-Braytonova oběhu. Kompresor nasává 0,05 [kg.s- 1 ] vzduchu (individuální plynová konstanta 287,04 [J.kg -1 K -1 ]; Poissonova konstanta 1,4 o tlaku 0,12 [MPa]
Příklad 1 Plynová turbína pracuje dle Ericsson-Braytonova oběhu. Kompresor nasává 0,05 [kg.s- 1 ] vzduchu (individuální plynová konstanta 287,04 [J.kg -1 K -1 ]; Poissonova konstanta 1,4 o tlaku 0,12 [MPa]
Mechanika tekutin. Tekutiny = plyny a kapaliny
 Mechanika tekutin Tekutiny = plyny a kapaliny Vlastnosti kapalin Kapaliny mění tvar, ale zachovávají objem jsou velmi málo stlačitelné Ideální kapalina: bez vnitřního tření je zcela nestlačitelná Viskozita
Mechanika tekutin Tekutiny = plyny a kapaliny Vlastnosti kapalin Kapaliny mění tvar, ale zachovávají objem jsou velmi málo stlačitelné Ideální kapalina: bez vnitřního tření je zcela nestlačitelná Viskozita
Cvičení z termomechaniky Cvičení 2. Stanovte objem nádoby, ve které je uzavřený dusík o hmotnosti 20 [kg], teplotě 15 [ C] a tlaku 10 [MPa].
![Cvičení z termomechaniky Cvičení 2. Stanovte objem nádoby, ve které je uzavřený dusík o hmotnosti 20 [kg], teplotě 15 [ C] a tlaku 10 [MPa]. Cvičení z termomechaniky Cvičení 2. Stanovte objem nádoby, ve které je uzavřený dusík o hmotnosti 20 [kg], teplotě 15 [ C] a tlaku 10 [MPa].](/thumbs/25/6795424.jpg) Příklad 1 Stanovte objem nádoby, ve které je uzavřený dusík o hmotnosti 20 [kg], teplotě 15 [ C] a tlaku 10 [MPa]. m 20[kg], t 15 [ C] 288.15 [K], p 10 [MPa] 10.10 6 [Pa], R 8314 [J. kmol 1. K 1 ] 8,314
Příklad 1 Stanovte objem nádoby, ve které je uzavřený dusík o hmotnosti 20 [kg], teplotě 15 [ C] a tlaku 10 [MPa]. m 20[kg], t 15 [ C] 288.15 [K], p 10 [MPa] 10.10 6 [Pa], R 8314 [J. kmol 1. K 1 ] 8,314
VYBRANÉ STATĚ Z PROCESNÍHO INŢENÝRSTVÍ cvičení 12
 UNIVERZITA TOMÁŠE BATI VE ZLÍNĚ FAKULTA APLIKOVANÉ INFORMATIKY VYBRANÉ STATĚ Z PROCESNÍHO INŢENÝRSTVÍ cvičení 2 Termodynamika reálných plynů část 2 Hana Charvátová, Dagmar Janáčová Zlín 203 Tento studijní
UNIVERZITA TOMÁŠE BATI VE ZLÍNĚ FAKULTA APLIKOVANÉ INFORMATIKY VYBRANÉ STATĚ Z PROCESNÍHO INŢENÝRSTVÍ cvičení 2 Termodynamika reálných plynů část 2 Hana Charvátová, Dagmar Janáčová Zlín 203 Tento studijní
1. Změřte teplotní závislost povrchového napětí destilované vody σ v rozsahu teplot od 295 do 345 K metodou bublin.
 1 Pracovní úkoly 1. Změřte teplotní závislost povrchového napětí destilované vody σ v rozsahu teplot od 295 do 35 K metodou bublin. 2. Měřenou závislost znázorněte graficky. Závislost aproximujte kvadratickou
1 Pracovní úkoly 1. Změřte teplotní závislost povrchového napětí destilované vody σ v rozsahu teplot od 295 do 35 K metodou bublin. 2. Měřenou závislost znázorněte graficky. Závislost aproximujte kvadratickou
Cvičení z termodynamiky a statistické fyziky
 Cvičení termodynamiky a statistické fyiky 1Nechť F(x, y=xe y Spočtěte F/ x, F/, 2 F/ x 2, 2 F/ x, 2 F/ x, 2 F/ x 2 2 Bud dω = A(x, ydx+b(x, ydy libovolná diferenciální forma(pfaffián Ukažte, ževpřípadě,žedωjeúplnýdiferenciál(existujefunkce
Cvičení termodynamiky a statistické fyiky 1Nechť F(x, y=xe y Spočtěte F/ x, F/, 2 F/ x 2, 2 F/ x, 2 F/ x, 2 F/ x 2 2 Bud dω = A(x, ydx+b(x, ydy libovolná diferenciální forma(pfaffián Ukažte, ževpřípadě,žedωjeúplnýdiferenciál(existujefunkce
III. STRUKTURA A VLASTNOSTI PLYNŮ
 III. STRUKTURA A VLASTNOSTI PLYNŮ 3.1 Ideální plyn a) ideální plyn model, předpoklady: 1. rozměry molekul malé (ve srovnání se střední vzdáleností molekul). molekuly na sebe navzálem silově nepůsobí (mimo
III. STRUKTURA A VLASTNOSTI PLYNŮ 3.1 Ideální plyn a) ideální plyn model, předpoklady: 1. rozměry molekul malé (ve srovnání se střední vzdáleností molekul). molekuly na sebe navzálem silově nepůsobí (mimo
Úloha 12: Účinnost tepelného stroje
 Úloha 12: Účinnost tepelného stroje FYZIKÁLNÍ PRAKTIKUM FJFI ČVUT V PRAZE Datum měření: 5.10.2009 Jméno: František Batysta Pracovní skupina: 12 Ročník a kroužek: 2. ročník, pond. odp. Spolupracovníci:
Úloha 12: Účinnost tepelného stroje FYZIKÁLNÍ PRAKTIKUM FJFI ČVUT V PRAZE Datum měření: 5.10.2009 Jméno: František Batysta Pracovní skupina: 12 Ročník a kroužek: 2. ročník, pond. odp. Spolupracovníci:
plynu, Měření Poissonovy konstanty vzduchu
 Úloha 4: Měření dutých objemů vážením a kompresí plynu, Měření Poissonovy konstanty vzduchu FYZIKÁLNÍ PRAKTIKUM FJFI ČVUT V PRAZE Datum měření: 2.11.2009 Jméno: František Batysta Pracovní skupina: 11 Ročník
Úloha 4: Měření dutých objemů vážením a kompresí plynu, Měření Poissonovy konstanty vzduchu FYZIKÁLNÍ PRAKTIKUM FJFI ČVUT V PRAZE Datum měření: 2.11.2009 Jméno: František Batysta Pracovní skupina: 11 Ročník
12. Termomechanika par, Clausiova-Clapeyronova rovnice, parní tabulky, základni termodynamické děje v oblasti par
 1/18 12. Termomechanika par, Clausiova-Clapeyronova rovnice, parní tabulky, základni termodynamické děje v oblasti par Příklad: 12.1, 12.2, 12.3, 12.4, 12.5, 12.6, 12.7, 12.8, 12.9, 12.10, 12.11, 12.12,
1/18 12. Termomechanika par, Clausiova-Clapeyronova rovnice, parní tabulky, základni termodynamické děje v oblasti par Příklad: 12.1, 12.2, 12.3, 12.4, 12.5, 12.6, 12.7, 12.8, 12.9, 12.10, 12.11, 12.12,
Termodynamické zákony
 Termodynamické zákony Makroskopická práce termodynamické soustavy Již jsme uvedli, že změna vnitřní energie soustavy je obecně vyvolána dvěma ději: tepelnou výměnou mezi soustavou a okolím a konáním práce
Termodynamické zákony Makroskopická práce termodynamické soustavy Již jsme uvedli, že změna vnitřní energie soustavy je obecně vyvolána dvěma ději: tepelnou výměnou mezi soustavou a okolím a konáním práce
Digitální učební materiál. III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Příjemce podpory Gymnázium, Jevíčko, A. K.
 Digitální učební materiál Číslo projektu CZ.1.07/1.5.00/34.0802 Název projektu Zkvalitnění výuky prostřednictvím ICT Číslo a název šablony klíčové aktivity III/2 Inovace a zkvalitnění výuky prostřednictvím
Digitální učební materiál Číslo projektu CZ.1.07/1.5.00/34.0802 Název projektu Zkvalitnění výuky prostřednictvím ICT Číslo a název šablony klíčové aktivity III/2 Inovace a zkvalitnění výuky prostřednictvím
TERMOMECHANIKA PRO STUDENTY STROJNÍCH FAKULT prof. Ing. Milan Pavelek, CSc. Brno 2013
 Vysoké učení technické v Brně Fakulta strojního inženýrství, Energetický ústav Odbor termomechaniky a techniky prostředí TERMOMECHANIKA PRO STUDENTY STROJNÍCH FAKULT prof. Ing. Milan Pavelek, CSc. Brno
Vysoké učení technické v Brně Fakulta strojního inženýrství, Energetický ústav Odbor termomechaniky a techniky prostředí TERMOMECHANIKA PRO STUDENTY STROJNÍCH FAKULT prof. Ing. Milan Pavelek, CSc. Brno
FYZIKÁLNÍ PRAKTIKUM FJFI ČVUT V PRAZE. Úloha 11: Termická emise elektronů
 FYZIKÁLNÍ PRAKTIKUM FJFI ČVUT V PRAZE Datum měření: 15.4.2011 Jméno: Jakub Kákona Pracovní skupina: 4 Ročník a kroužek: Pa 9:30 Spolupracovníci: Jana Navrátilová Hodnocení: Úloha 11: Termická emise elektronů
FYZIKÁLNÍ PRAKTIKUM FJFI ČVUT V PRAZE Datum měření: 15.4.2011 Jméno: Jakub Kákona Pracovní skupina: 4 Ročník a kroužek: Pa 9:30 Spolupracovníci: Jana Navrátilová Hodnocení: Úloha 11: Termická emise elektronů
Vybrané technologie povrchových úprav. Základy vakuové techniky Doc. Ing. Karel Daďourek 2006
 Vybrané technologie povrchových úprav Základy vakuové techniky Doc. Ing. Karel Daďourek 2006 Střední rychlost plynů Rychlost molekuly v p = (2 k N A ) * (T/M 0 ), N A = 6. 10 23 molekul na mol (Avogadrova
Vybrané technologie povrchových úprav Základy vakuové techniky Doc. Ing. Karel Daďourek 2006 Střední rychlost plynů Rychlost molekuly v p = (2 k N A ) * (T/M 0 ), N A = 6. 10 23 molekul na mol (Avogadrova
pracovní list studenta Kmitání Studium kmitavého pohybu a určení setrvačné hmotnosti tělesa
 pracovní list studenta Kmitání Studium kmitavého pohybu a určení setrvačné hmotnosti tělesa Výstup RVP: Klíčová slova: Eva Bochníčková žák měří vybrané veličiny vhodnými metodami, zpracuje získaná data
pracovní list studenta Kmitání Studium kmitavého pohybu a určení setrvačné hmotnosti tělesa Výstup RVP: Klíčová slova: Eva Bochníčková žák měří vybrané veličiny vhodnými metodami, zpracuje získaná data
Elektroenergetika 1. Termodynamika a termodynamické oběhy
 Termodynamika a termodynamické oběhy Termodynamika Popisuje procesy, které zahrnují změny teploty, přeměny energie a vzájemný vztah mezi tepelnou energií a mechanickou prací Opakování fyziky Termodynamický
Termodynamika a termodynamické oběhy Termodynamika Popisuje procesy, které zahrnují změny teploty, přeměny energie a vzájemný vztah mezi tepelnou energií a mechanickou prací Opakování fyziky Termodynamický
V i s k o z i t a N e w t o n s k ý c h k a p a l i n
 V i s k o z i t a N e w t o n s k ý c h k a p a l i n Ú k o l : Změřit dynamickou viskozitu destilované vody absolutní metodou a její závislost na teplotě relativní metodou. P o t ř e b y : Viz seznam
V i s k o z i t a N e w t o n s k ý c h k a p a l i n Ú k o l : Změřit dynamickou viskozitu destilované vody absolutní metodou a její závislost na teplotě relativní metodou. P o t ř e b y : Viz seznam
Základy vakuové techniky
 Základy vakuové techniky Střední rychlost plynů Rychlost molekuly v p = (2 k N A ) * (T/M 0 ), N A = 6. 10 23 molekul na mol (Avogadrova konstanta), k = 1,38. 10-23 J/K.. Boltzmannova konstanta, T.. absolutní
Základy vakuové techniky Střední rychlost plynů Rychlost molekuly v p = (2 k N A ) * (T/M 0 ), N A = 6. 10 23 molekul na mol (Avogadrova konstanta), k = 1,38. 10-23 J/K.. Boltzmannova konstanta, T.. absolutní
Fyzikální chemie. Magda Škvorová KFCH CN463 magda.skvorova@ujep.cz, tel. 3302. 14. února 2013
 Fyzikální chemie Magda Škvorová KFCH CN463 magda.skvorova@ujep.cz, tel. 3302 14. února 2013 Co je fyzikální chemie? Co je fyzikální chemie? makroskopický přístup: (klasická) termodynamika nerovnovážná
Fyzikální chemie Magda Škvorová KFCH CN463 magda.skvorova@ujep.cz, tel. 3302 14. února 2013 Co je fyzikální chemie? Co je fyzikální chemie? makroskopický přístup: (klasická) termodynamika nerovnovážná
ÚVODNÍ POJMY, VNITŘNÍ ENERGIE, PRÁCE A TEPLO POJMY K ZOPAKOVÁNÍ. Testové úlohy varianta A
 Škola: Autor: DUM: Vzdělávací obor: Tematický okruh: Téma: Masarykovo gymnázium Vsetín Mgr. Jitka Novosadová MGV_F_SS_3S3_D08_Z_OPAK_T_Uvodni_pojmy_vnitrni_energie _prace_teplo_t Člověk a příroda Fyzika
Škola: Autor: DUM: Vzdělávací obor: Tematický okruh: Téma: Masarykovo gymnázium Vsetín Mgr. Jitka Novosadová MGV_F_SS_3S3_D08_Z_OPAK_T_Uvodni_pojmy_vnitrni_energie _prace_teplo_t Člověk a příroda Fyzika
TERMODYNAMIKA Ideální plyn TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY.
 TERMODYNAMIKA Ideální plyn TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY. Ideální plyn je zjednodušená představa skutečného plynu. Je dokonale stlačitelný
TERMODYNAMIKA Ideální plyn TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY. Ideální plyn je zjednodušená představa skutečného plynu. Je dokonale stlačitelný
Poznámky k cvičením z termomechaniky Cvičení 10.
 Příklad 1 Topné těleso o objemu 0,5 [m 3 ], naplněné sytou párou o tlaku 0,15 [MPa], bylo odstaveno. Po nějaké době vychladlo na teplotu 30 C. Určete množství uvolněného tepla a konečný stav páry v tělese.
Příklad 1 Topné těleso o objemu 0,5 [m 3 ], naplněné sytou párou o tlaku 0,15 [MPa], bylo odstaveno. Po nějaké době vychladlo na teplotu 30 C. Určete množství uvolněného tepla a konečný stav páry v tělese.
T0 Teplo a jeho měření
 Teplo a jeho měření 1 Teplo 2 Kalorimetrie Kalorimetr 3 Tepelná kapacita 3.1 Měrná tepelná kapacita Měrná tepelná kapacita při stálém objemu a stálém tlaku Poměr měrných tepelných kapacit 3.2 Molární tepelná
Teplo a jeho měření 1 Teplo 2 Kalorimetrie Kalorimetr 3 Tepelná kapacita 3.1 Měrná tepelná kapacita Měrná tepelná kapacita při stálém objemu a stálém tlaku Poměr měrných tepelných kapacit 3.2 Molární tepelná
Fyzikální praktikum FJFI ČVUT v Praze
 Fyzikální praktikum FJFI ČVUT v Praze Úloha 5: Měření Poissonovy konstanty a dutých objemů Datum měření: 10. 12. 2015 Skupina: 8, čtvrtek 7:30 Vypracoval: Tadeáš Kmenta Klasifikace: Část I Měření Poissonovy
Fyzikální praktikum FJFI ČVUT v Praze Úloha 5: Měření Poissonovy konstanty a dutých objemů Datum měření: 10. 12. 2015 Skupina: 8, čtvrtek 7:30 Vypracoval: Tadeáš Kmenta Klasifikace: Část I Měření Poissonovy
11. Odporový snímač teploty, měřicí systém a bezkontaktní teploměr
 11. Odporový snímač teploty, měřicí systém a bezkontaktní teploměr Otázky k úloze (domácí příprava): Pro jakou teplotu je U = 0 v případě použití převodníku s posunutou nulou dle obr. 1 (senzor Pt 100,
11. Odporový snímač teploty, měřicí systém a bezkontaktní teploměr Otázky k úloze (domácí příprava): Pro jakou teplotu je U = 0 v případě použití převodníku s posunutou nulou dle obr. 1 (senzor Pt 100,
5.4 Adiabatický děj Polytropický děj Porovnání dějů Základy tepelných cyklů První zákon termodynamiky pro cykly 42 6.
 OBSAH Předmluva 9 I. ZÁKLADY TERMODYNAMIKY 10 1. Základní pojmy 10 1.1 Termodynamická soustava 10 1.2 Energie, teplo, práce 10 1.3 Stavy látek 11 1.4 Veličiny popisující stavy látek 12 1.5 Úlohy technické
OBSAH Předmluva 9 I. ZÁKLADY TERMODYNAMIKY 10 1. Základní pojmy 10 1.1 Termodynamická soustava 10 1.2 Energie, teplo, práce 10 1.3 Stavy látek 11 1.4 Veličiny popisující stavy látek 12 1.5 Úlohy technické
Zapojení odporových tenzometrů
 Zapojení odporových tenzometrů Zadání 1) Seznamte se s konstrukcí a použitím lineárních fóliových tenzometrů. 2) Proveďte měření na fóliových tenzometrech zapojených do můstku. 3) Zjistěte rovnici regresní
Zapojení odporových tenzometrů Zadání 1) Seznamte se s konstrukcí a použitím lineárních fóliových tenzometrů. 2) Proveďte měření na fóliových tenzometrech zapojených do můstku. 3) Zjistěte rovnici regresní
Měření měrné telené kapacity pevných látek
 Měření měrné telené kapacity pevných látek Úkol :. Určete tepelnou kapacitu kalorimetru.. Určete měrnou tepelnou kapacitu daných těles. 3. Naměřené hodnoty porovnejte s hodnotami uvedených v tabulkách
Měření měrné telené kapacity pevných látek Úkol :. Určete tepelnou kapacitu kalorimetru.. Určete měrnou tepelnou kapacitu daných těles. 3. Naměřené hodnoty porovnejte s hodnotami uvedených v tabulkách
Úloha č. 3: Přeměna práce Stirlingova motoru na elektrickou energii
 Úloha č. 3: Přeměna práce Stirlingova motoru na elektrickou energii Úvod Tato laboratorní práce je nadstavbou k laboratorním úlohám Stanovení učinnosti hořáku, Carnotovy termodynamické účinnosti, reálné
Úloha č. 3: Přeměna práce Stirlingova motoru na elektrickou energii Úvod Tato laboratorní práce je nadstavbou k laboratorním úlohám Stanovení učinnosti hořáku, Carnotovy termodynamické účinnosti, reálné
FYZIKA I cvičení, FMT 2. POHYB LÁTKY
 FYZIKA I cvičení, FMT 2.1 Kinematika hmotných částic 2. POHYB LÁTKY 2.1.1 2.1.2 2.1.3 2.1.4 2.1.5 2.1.6 Těleso při volném pádu urazí v poslední sekundě dvě třetiny své dráhy. Určete celkovou dráhu volného
FYZIKA I cvičení, FMT 2.1 Kinematika hmotných částic 2. POHYB LÁTKY 2.1.1 2.1.2 2.1.3 2.1.4 2.1.5 2.1.6 Těleso při volném pádu urazí v poslední sekundě dvě třetiny své dráhy. Určete celkovou dráhu volného
HUSTOTA PEVNÝCH LÁTEK
 HUSTOTA PEVNÝCH LÁTEK Hustota látek je základní informací o studované látce. V případě homogenní látky lze i odhadnout druh materiálu s pomocí známých tabulkovaných údajů (s ohledem na barvu a vzhled materiálu
HUSTOTA PEVNÝCH LÁTEK Hustota látek je základní informací o studované látce. V případě homogenní látky lze i odhadnout druh materiálu s pomocí známých tabulkovaných údajů (s ohledem na barvu a vzhled materiálu
Plyn. 11 plynných prvků. Vzácné plyny. He, Ne, Ar, Kr, Xe, Rn Diatomické plynné prvky H 2, N 2, O 2, F 2, Cl 2
 Plyny Plyn T v, K Vzácné plyny 11 plynných prvků He, Ne, Ar, Kr, Xe, Rn 165 Rn 211 N 2 O 2 77 F 2 90 85 Diatomické plynné prvky Cl 2 238 H 2, N 2, O 2, F 2, Cl 2 H 2 He Ne Ar Kr Xe 20 4.4 27 87 120 1 Plyn
Plyny Plyn T v, K Vzácné plyny 11 plynných prvků He, Ne, Ar, Kr, Xe, Rn 165 Rn 211 N 2 O 2 77 F 2 90 85 Diatomické plynné prvky Cl 2 238 H 2, N 2, O 2, F 2, Cl 2 H 2 He Ne Ar Kr Xe 20 4.4 27 87 120 1 Plyn
Technická měření v bezpečnostním inženýrství. Měření teploty, měření vlhkosti vzduchu
 Technická měření v bezpečnostním inženýrství Čís. úlohy: 4 Název úlohy: Měření teploty, měření vlhkosti vzduchu Úkol měření a) Změřte teplotu topné desky IR teploměrem. b) Porovnejte měření teploty skleněným
Technická měření v bezpečnostním inženýrství Čís. úlohy: 4 Název úlohy: Měření teploty, měření vlhkosti vzduchu Úkol měření a) Změřte teplotu topné desky IR teploměrem. b) Porovnejte měření teploty skleněným
STANOVENÍ VLASTNOSTÍ AERAČNÍCH ZAŘÍZENÍ
 STANOVENÍ VLASTNOSTÍ AERAČNÍCH ZAŘÍZENÍ Zadání: 1. Stanovte oxygenační kapacitu a procento využití kyslíku v čisté vodě pro provzdušňovací porézní element instalovaný v plexi válci následujících rozměrů:
STANOVENÍ VLASTNOSTÍ AERAČNÍCH ZAŘÍZENÍ Zadání: 1. Stanovte oxygenační kapacitu a procento využití kyslíku v čisté vodě pro provzdušňovací porézní element instalovaný v plexi válci následujících rozměrů:
TEPELNÉ ÚČINKY EL. PROUDU
 Univerzita Pardubice Fakulta elektrotechniky a informatiky Materiály pro elektrotechniku Laboratorní cvičení č. 1 TEPELNÉ ÚČINKY EL. POUDU Jméno(a): Mikulka oman, Havlíček Jiří Stanoviště: 6 Datum: 19.
Univerzita Pardubice Fakulta elektrotechniky a informatiky Materiály pro elektrotechniku Laboratorní cvičení č. 1 TEPELNÉ ÚČINKY EL. POUDU Jméno(a): Mikulka oman, Havlíček Jiří Stanoviště: 6 Datum: 19.
Měření teplotní roztažnosti
 KATEDRA EXPERIMENTÁLNÍ FYZIKY PŘÍRODOVĚDECKÁ FAKULTA UNIVERZITY PALACKÉHO V OLOMOUCI FYZIKÁLNÍ PRAKTIKUM Z MOLEKULOVÉ FYZIKY A TERMODYNAMIKY Měření teplotní roztažnosti Úvod Zvyšování termodynamické teploty
KATEDRA EXPERIMENTÁLNÍ FYZIKY PŘÍRODOVĚDECKÁ FAKULTA UNIVERZITY PALACKÉHO V OLOMOUCI FYZIKÁLNÍ PRAKTIKUM Z MOLEKULOVÉ FYZIKY A TERMODYNAMIKY Měření teplotní roztažnosti Úvod Zvyšování termodynamické teploty
Stanovení účinnosti spalování biomasy, měření emisí
 3. úloha EZ1 Stanovení účinnosti spalování biomasy, měření emisí Cíl úlohy Orientační stanovení účinnosti tepelného zdroje na biomasu pomocí elektrochemické analýzy kouřových plynů respektive pomocí zjednodušeného
3. úloha EZ1 Stanovení účinnosti spalování biomasy, měření emisí Cíl úlohy Orientační stanovení účinnosti tepelného zdroje na biomasu pomocí elektrochemické analýzy kouřových plynů respektive pomocí zjednodušeného
5. Stejným postupem změřte objem hadičky spojující byretu s měřeným prostorem. Tuto hodnotu odečtěte od výsledku podle bodu 4.
 FYZIKÁLNÍ PRAKTIKUM I FJFI ČVUT v Praze Úloha #4 Poissonova konstanta a měření dutých objemů Datum měření: 6.12.2013 Skupina: 7 Jméno: David Roesel Kroužek: ZS 5 Spolupracovala: Tereza Schönfeldová Klasifikace:
FYZIKÁLNÍ PRAKTIKUM I FJFI ČVUT v Praze Úloha #4 Poissonova konstanta a měření dutých objemů Datum měření: 6.12.2013 Skupina: 7 Jméno: David Roesel Kroužek: ZS 5 Spolupracovala: Tereza Schönfeldová Klasifikace:
pracovní list studenta
 Výstup RVP: Klíčová slova: pracovní list studenta Elektrická energie Vojtěch Beneš žák měří vybrané fyzikální veličiny vhodnými metodami, zpracuje a vyhodnotí výsledky měření, aplikuje s porozuměním termodynamické
Výstup RVP: Klíčová slova: pracovní list studenta Elektrická energie Vojtěch Beneš žák měří vybrané fyzikální veličiny vhodnými metodami, zpracuje a vyhodnotí výsledky měření, aplikuje s porozuměním termodynamické
