Sorpční vlastnosti vláken. Základní pojmy Porózita Sorpční izotermy Sorpce vody Difúze
|
|
|
- Alexandra Ladislava Müllerová
- před 8 lety
- Počet zobrazení:
Transkript
1 Sorpční vlastnosti vláken Základní pojmy Porózita Sorpční izotermy Sorpce vody Difúze
2 Povrchové síly Tělesa-----Molekuly Vzdálenost D r Volná energie interakce W w Síly: 6 W = U * A/ D, U rozměr těles Van der Waalské (dipólové interakce) Elektrostatické Strukturní W = k * T exp( b* D) W = K / D
3 Van der Waalské síly Stejná mocnina vzdálenosti (-6) Interakce mezi dvěma dipóly Interakce dipól indukovaný dipól (Debye síly) Disperzní interakce (Londonovy síly) Působení do 5nm
4 Van der Waalské síly vliv geometrie těles
5 Pojmy I Penetrant (absoptiv a absorbát) Absorbent vlákno Dynamický proces
6 Pojmy II Vlákno obklopeno prostředím, kde se vyskytují molekuly nebo částice jiných látek dochází k celé řadě procesů. Podle znaménka elektrického náboje vlákna a částic jde o elektrostatické přitahování, resp. odpuzování. Vnepřítomnosti makroskopických elektrických nábojů mohou mít částice afinitu k vláknům (jde o rozdíl standardních chemických potenciálů vlákna a částice). Vpřípadě náhodného Brownova pohybu částic bude frekventovaně docházet k interakcím povrchem vlákna a možným vazbám přes vodíkové můstky a van der Waalsovy síly. Makroskopicky se tyto procesy projeví usazováním na povrchu vláken (adsorpce) nebo pronikáním do vláken (difúze), případně transportem přes vlákna
7 Pojmy III Vlákno obklopeno molekulami, resp. částicemi vodní páry, vody, kapalin, plynů a pevných částic: Difúze penetrantů prostředím (obyčejně vodou nebo vzduchem k vláknu. Tento proces je obyčejně dostatečně rychlý. Adsorpce na povrchu vlákna, V řadě případů je adsorpce zkoumána samostatně, protože penetranty výrazně dále do vláken nepronikají resp. jejich pronikání závisí na množství penetrantu na povrchu. Difúze hmotou vlákna, kdy dochází k transportu penetrantů do vláken. Vněkterých případech dochází k zadržování penetrantů na specifických místech ve vlákně a vytvoření vazby s vláknem. Desorpce molekul penetrantu zpět do okolí (resp. přenos penetrantu)
8 Pojmy IV Makroskopickým výsledkem může být usazování penetrantu na povrchu (např. částice prachu), pronikání penetrantu do vlákna (barvení, navlhání), resp. transport penetrantu přes vlákna (odstranění potu) Procesy sorpce mají svoji kinetickou stránku (rychlost změn), rovnovážnou stránku (velikost změn) a termodynamickou stránku (hnací síla změn). Probíhají obyčejně současně, takže jejich oddělené sledování vyžaduje často speciální experimenty.
9 Smáčení a vzlínání Vlákno je s kapalinou pouze v místním styku (např. částečně ponořeno, kapky kapaliny na povrchu atd.). V těchto případech dochází k procesům smáčení, což se projeví ustavením rovnováhy mezi kapalinou a povrchem vlákna. U vlákenných svazků dochází ke vzlínání kapilárním transportem v pórech mezi vlákny. Platí, že: a) smáčení je výsledkem energetických interakcí tří fází tj. pevné látky, kapaliny a okolního vzduchu (plynné fáze) v rovnováze. b) vzlínání souvisí jak s energetickými poměry mezi jednotlivými fázemi, tak i geometrií vlákenného svazku. Tyto procesy jsou důležité také z technologického hlediska, protože ovlivňují řadu zušlechťovacích procesů, přípravu kompozitních struktur a procesy tvorby některých textilních struktur (pojených netkaných textilií).
10 Rovnovážná sorpce O mechanismu interakce molekul penetrantu s povrchem vláknen lze získat informace z tzv. adsorpčních isoterem. Principem je sledování závislosti mezi množstvím penetrantu na povrchu vlákna C P (resp. ve vlákně) a v okolí vlákna C o v rovnováze, kdy došlo k ustálení rozdělení penetrantu mezi vlákno a okolí. Předpokládá se, že v okolí nedochází vlivem sorpčních procesů ke změně koncentrace, tj. C o je konstantní. Experimenty se provádějí při konstantní teplotě.
11 Mechanismy sorpce Fyzikální sorpce Chemisorpce Příklad: sorpce inertního plynu při nízkých teplotách na povrch porézních materiálů. Příklad: reaktivní plyn sorbovaný na aktivních místech povrchu porézního materiálu.
12 Nernstova izoterma Pro případ, kdy se penetrant váže na povrch fyzikálními silami a nebo dochází k jeho rozpouštění ve vlákně platí jednoduchý Nernstův vztah C K *C p = N K N je tzv. rozdělovací koeficient 0 Pro případ adsorpce plynů se tato rovnice označuje jako Henryho vztah (C o je nahrazeno parciálním tlakem plynu p o na styku s povrchem vlákna. Pro překročení jisté koncentrace C o =C om penetrantu v okolí, již vlákno není schopné další molekuly absorbovat a C P = C PM, bez ohledu na C o. Nernstův vztah vyhovuje pro menší hodnoty koncentrace penetrantů v okolí C o.
13 Langmuirova izoterma Pokud se penetrant váže na specifická místa na povrchu vlákna (monomolekulární lokalizovaná sorpce s maximální koncentrací vazných míst S) je C P úměrná také rozdílu S-C P. Po úpravách resultuje Langmuirova izoterma ve tvaru K L * S C P = 1 + K * C K L je konstanta (afinita specifických míst) L o
14 Porovnání izoterem C P Nernst C PM Langmuir C o
15 Složitější izotermy Pro adsorpci řady plynů a par vyhovuje tzv. duální model sorpce jako lineární kombinace Nernstovy a Langmuirovy izotermy (kombinace fyzikální a lokalizované sorpce). V reálných situacích dochází také k obsazování jednoho vazného místa více molekulami penetrantu (vícevrstvá adsorpce). Pro tyto případy vyhovuje např. adsorpční izoterma Brunnauer-Emmett- Teller (BET). V řadě případů nelze oddělit povrchovou adsorpci od absorpce (kde dochází také k difúzi a vazbě penetrantu ve vlákně). Speciální pozornost je věnována sorpci vody a vodních par, protože souvisí jak se zpracovatelností (zejména ve fázi zušlechťování) tak i s fyziologickými projevy vláken.
16 Složitější povrchy Ultramikropóry: průměr méně než 0,5 nm Mikropóry: průměr 0,5 až 2 nm Mezopóry: průměr 2až 50 nm Makropóry: průměr více než 50 nm
17 Typové izotermy I mikroporézní povrch (plnění mikropórů) II neporézní povrch (jedno a pak vícevrstvá sorpce) III slabé interakce IV kapilární kondenzace V slabé interakce (kapilární kondenzace) VI neporézní povrch (adsorpce po vrstvách)
18 Porózita vláken Neporézní látky: malá povrchová plocha Částice: Velikost a povrchová plocha Porézní látky: Středně veliká povrchová plocha Objem a rozměry pórů Aktivní místa: Porosita a koncentrace aktivních míst
19 Typy Pórů Rozvětvený Uzavřený Průchozí Neprůchozí
20 Toky v pórech Knudsenův tok - průměrná volná dráha molekul (plynu) je větší než 3 průměr póru. Dominuje mechanismus kolize p * r molekul plynu se stěnami pórů Fk LS M Poiseuillův tok - průměrná volná dráha molekul (plynu) je menší než průměr póru. Dominuje kolize mezi molekulami plynu p Fp p L S * 4 r * η tlakový spád L s tloušťka pokožky M molekulová hmotnost plynu viskozita plynu F rychlost toku plynu
21 Tvar pórů Cylindrické Štěrbinové Kónické Sférické Lahvovité Intersticiální
22 Sorpce vody I Hydrofilní vlákna porézní (mají k vodě afinitu) jsou schopna vázat a transportovat vodu. Mezi hydrofilní patří všechna vlákna přírodní a chemická obsahující hydrofilní skupiny. Hydrofobní vlákna neporézní (není afinita k vodě) tj. nemožnost vázání vody specifickými vazbami a nesmáčení povrchu vláken. Voda se u svazků těchto vláken šíří kapilárními silami. Voda působí v polymerech především jako plastifikátor snižující teplotu zeskelnění a zvyšující tažnost. Voda ovlivňuje pozitivně také elektrickou vodivost a snižuje měrnou hmotnost.
23 Sorpce vody II Sorpce vody souvisí se složením vláken, stavem jejich povrchu, přístupností hydrofilních skupin, rozvolněností struktury, distribucí pórů, teplotou, časem a : 1.existencí sorpčních center (hydroxylové skupiny u celulózových vláken) 2. přístupností sorpčních center 3. vznikem sekundárních sorpčních center
24 Rovnovážná sorpce vodních par Při sledování rovnovážné absorpce vodních par se konstruují absorpční a desorpční izotermy. Sorpční izoterma pro vodní páru je závislost rovnovážné koncentrace vody ve vlákně C V na relativní vlhkosti vzduchu RH) Cv Desorpce H Absorpce RH
25 Rovnovážná sorpce vodních par - vlákna
26 Konstrukce izoterem Kinetické experimenty, kdy se sleduje při konstantní relativní vlhkosti ovzduší RH závislost koncentrace vodních par C t ve vlákně na čase t. Rovnovážná hodnota C v pro rovnováhu tj. t = E se pak vynáší jako pořadnice do grafu absorpční izotermy. Pokud se začíná od suchého vlákna dochází k jeho vlhčení (absorpci) a pokud se začíná od mokrého vlákna dochází k sušení (desorpci). C t RH = konst. Desorpce Absorpce E H t
27 Hystereze I Rozdíl mezi absorpční a desorpční izotermou při zvolené relativní vlhkosti vzduchu RH se nazývá hystereze. Pro hydrofilní vlákna je hystereze výrazná a pro hydrofóbní vlákna je nízká. Příčinou hystereze je různý počet přístupných vazných míst při sušení mokrého vlákna (více) nebo vlhčení suchého vlákna (méně). K hysterezi dochází také v případě, že ve vlákně jsou póry otevřené na obě strany nebo tzv. lahvovité póry (to může být příčinou hystereze hydrofobních vláken). Příčinou hystereze je také kapilární kondenzace
28 Význam hystereze Hystereze má praktický význam tam, kde se při dané vlhkosti vzduchu požaduje maximální (resp. minimální) vlhkost ve vláknech. Ve zkušebnictví se standardně začíná od vysušených vláken a provádí se vlhčení sohledem na předepsanou vlhkost ovzduší (standardně 65% RH). Z termodynamického hlediska je adsorpce exotermní proces.
29 Tepelné jevy při sorpci vody Pokud je voda absorbována do vláken z vodní páry, dochází nejprve ke kondenzaci na povrchu vláken. Latentní teplo kondenzace (tj. teplo uvolněné při fázové změně z plynné na kapalnou fázi) se pohybuje kolem 2450 Jg -1 vody. S ohledem na relativní vlhkost vzduchu RH je část kondenzované vody transportována do vlákna. Část zůstává na povrchu a je transportována kapilárními silami. Vlivem přítomnosti molekul vody dochází zejména v přístupných oblastech vlákna (amorfní fáze) k tvorbě sekundárních vazeb, což se projeví větší uspořádaností systému a snížením jeho celkové energie. Přebytečná energie se uvolní jako teplo sorpce. Sorpce je tedy exotermní proces doprovázený vývinem tepla.
30 Složky tepla absorpce Voda může být absorbována z vodní páry (teplo Q v ) nebo kapalné vody (bobtnací teplo Q l ). Přechod z parní fáze do vodní je doprovázen vznikem kondenzačního tepla L. Q = L + Q v l bavlna
31 Diferenciální sorpční teplo Diferenciální sorpční teplo Q [Jg -1 vody]. Jde o teplo uvolněné sorpcí 1 g vody na neomezeném počtu vláken při dané vlhkosti ovzduší RH. Čím je vlákno na počátku sorpce sušší tím je teplo Q vyšší. Např. pro viskózu je pro suché vlákno Q=1,17 [Jg - 1 vody] a pro vlákno obsahující 75 % vlhkosti jen 0,24 [Jg -1 vody]
32 Integrální sorpční teplo Integrální sorpční teplo H [Jg -1 vlákna]. Teplo uvolněné při úplném nasycení 1 g vláken při dané vlhkosti. Označuje se také jako teplo smáčecí. Souvisí úzce se schopností vláken vázat vodu. Čím více vody jsou schopna vlákna vázat, tím je H vyšší. Změny integrálního tepla vody s vlhkostí vzduchu (RH)
33 Bobtnání I Obecně lze bobtnání vyjádřit jako relativní změnu průměru (radiální délkové bobtnání S D ) plochy příčného řezu (radiální plošné bobtnání S R ) délky (axiální délkové bobtnání S A ) objemu (objemové bobtnání S V ).
34 Bobtnání II Pro vlákna kruhového průřezu je S = + R 2 2 * S D S D Objemové bobtnání je pro vlákna, která jsou rovnoměrná po délce dáno vztahem S = S + S + S * V R A Při znalosti příčného a podélného bobtnání lze odhadnout objemové bobtnání. Vlivem tvorby vodíkových můstků v amorfních oblastech hydrofilních vláken dochází v výraznému příčnému bobtnání. Podélné bobtnání je výrazně nižší což vede k anizotropii bobtnání A S R
35 Kinetika sorpce Kinetická sledování patří k často používaným nejen proto, že jsou jednoduše realizovatelná ale také proto, že rychlost sorpčních dějů je často praktickým problémem. Z hlediska interpretace se většinou usiluje o izotermní podmínky. Neizotermní kinetické procesy se obtížněji popisují ale jsou v praxi běžné (např. barvení).
36 Transport molekul Základní modely transportu molekul do vláken vycházejí ze známých Fickových zákonů difúze, 2 C Pro nejjednodušší případ difúze do válcového vlákna poloměru r, kdy je na jeho povrchu stálý přebytek penetrantu a difúze probíhá fickovským mechanismem (tj. vyrovnáváním koncentračních rozdílů bez vazby na specifická místa) je řešením diferenciální rovnice difúze součet exponenciál. Pro krátké časy ho lze nahradit odmocninovou závislostí t = D x C 2 M M t R = 4 * D * t π * r 2
37 Ustálený stav K dalšímu zjednodušení dojde, pokud se sleduje ustálená difúze, kdy c D x x = 0 což znamená, že koncentrační gradient je konstantní. Po dosazení do diferenciální rovnice Fickova zákona a úpravách rezultuje vztah mezi tokem pentrantu J množstvím penetrantu za jednotku času J = C / t a koncentračním gradientem ve tvaru dc J = D = dx konst. V systémech, kde platí model duální sorpce se celkový tok J rozkládá na tok J N odpovídající Nernstovu mechanismu a tok J L odpovídající Langmuirovu mechanismu
38 Role struktury I Volno-objemová teorie: dojde k transportu molekuly penetrantu do polymeru jen pokud jsou splněny tyto podmínky: segmenty polymerních řetězců mají postačující energii k vytvoření volného objemu (díry) dostatečné velikosti pro penetrant; molekula penetrantu má dostatečnou energii k přeskoku do tohoto volného objemu; oba tyto děje nastanou současně. Podle této teorie může transport do vláken nastat jen při teplotách dostatečně vysokých pro překonání energetické bariéry bránící oddálení polymerních segmentů. Pod touto teplotou (přechodová teplota difúze T D ), tedy k difúzi prakticky nedochází. Volnoobjemový model difúze vyhovuje pro řadu syntetických vláken se zanedbatelnou porózitou.
39 Teplotní závislost D ln D Při difúzi podle volno-objemového 1/T D 1/T modelu je rozhodující energie pro oddálení polymerních segmentů je závislost na teplotě vyjádřena modelem Williams-Landel-Ferryho (W-L-F) c1 ( T TD ) D = D o exp c2 + T TD kde T D je přechodová teplota difúze a c 1, c 2 jsou konstanty. (Pro amorfní polymery je obyčejně c 1 =17,44 a c 2 =51,6).
40 Role struktury II Pro vlákna přírodní (a dostatečně porézní syntetická vlákna) je vhodný model difúze v pórech (resp. zbotnalých pórech, pokud je např. sledována difúze vodného roztoku barviva). Tento model v podstatě odpovídá Fickovské představě difúze, kdy je hnací silou gradient chemického potenciálu, který lze nahradit gradientem koncentrace. Difúzní koeficient molekul vody ve vzduch je kolem 0,25[cm 2 s -1 ] Difúzní koeficient molekul vody v pórech přírodních vláken kolem 10-7 [cm 2 s -1 ].
41 Teplotní závislost D Charakteristickou pro difúzi v pórech je Arrheniovská závislost difúzního koeficientu na teplotě T vyjádřená jednoduchým výrazem D E = Do * exp RT kde D o je konstanta související s entropií systému, E je aktivační energie difúze a R je univerzální plynová konstanta.
42 Izotermní sorpce Pokud je možné pouze určit celkové množství penetrantu ve vlákně M t v různých časech t používá se pro popis makroskopické kinetiky, tzv. rychlostních modelů typu dm dt t = K * ( M R K je rychlostní konstanta sorpce, M R je rovnovážné množství penetrantu ve vlákně a n je konstanta udávající řád reakce. Obyčejně se pro jednoduchost volí n = 1 (kinetika prvního řádu), kdy po integraci vyjde exponenciální závislost M t = M R M * (1 exp( K * t)) t ) n
43 Izotermní barvení concentration K C=f(t) C eq time Vytahovací křivka je závislost průměrné koncentrace barviva ve vlákně c t a čase t při konstantní teplotě T. Z těchto křivek při různých teplotách je možné určit aktivační parametry a mechanismus barvení.
44 Difuzní modely Řídícím mechanismem je difúze molekul do vlákna. Tento přenosový jev je možno popsat pomocí Fickových zákonů přenosu hmoty
45 PET- disperzní barvivo Známé řešení Fickova zákona pro koncentračně nezávislý difúzní koeficient D a nekonečnou lázeň (koncentrace barviva v lázní je konstantní- platí pro disperzní barviva) has the form c c t 2 gi Dt exp(- ) 2 r =1- i=1 4 g 2 i r poloměr vlákna, c průměrná koncentrace barviva ve vlákně v rovnováze a g i je i-tý kladný kořen Besselovy rovnice prvního druhu nultého řádu (g 1 =5,81 )
46 D = Interpretace D ( 1 X τ ) D l D = k * T 6 * π * η * r Difuzní koeficient D Vlivem komplexního mechanismu barvení jde spíše o rychlostní konstantu než parametr soustavy. Bývá často koncentračně závislý Závisí na porózitě a křivolakosti pórů Einstein- Brownův pohyb ve viskózním prostředí
47 Makroskopické rychlostní modely Formální předpoklady Celková rychlost barvení se dá vyjádřit kinetickou rychlostní rovnicí popisující okamžitou rychlost barvení d c t dt = f(k,c, t) K je rychlostní konstanta
48 Kinetické modely Z analogie s reakční kinetikou lze sestavit rovnici dc t dt = K* (c c ) kde n je konstanta (řád reakce). Pro n=1 exponenciální model Pro n=2 Vickerstaffůvmodel t n
49 PET disperzní barviva Většina kinetických modelů pro tento systém se dá vyjádřit ve tvaru. Pro různé parametry resultují různé modely = [1- exp(-(kt C c c ) ) D ] t Cegarra Puente model: C=1/2 D=1
50 Teplotní závislost Teplotní závislost rychlostní konstanty K (nebo difúzního koeficientu D) je vyjádřena Arrheniovým modelem E K = K0exp(- ) RT K 0 je pre-exponenciální faktor (odpovídá aktivační entropii barvení), E [kj mol -1 ] je aktivační energie barvení a R je universální plynová konstanta.
51 Omezení Použití izotermní kinetiky má výrazná omezení: Je obtížné dodržet izotermní podmínky při vyšších teplotách. Dochází ke strukturním změnám vlivem dlouhodobé tepelné expozice. Praktické barvení probíhá za neizotermních podmínek
52 Neizotermní barvení concentration C=f(F(t)) Neizotermní vytahovací křivka je závislost c t na t pro známý časově teplotní režim ohřevu T(t). Temperature T 1 T 0 T=F(t) θ time t 1 time Praktické barvicí experimenty jsou realizovány v neizotermních podmínkách.
53 Omezení Je možné odhadovat kinetické a aktivační parametry pouze pro vybrané modely. Není možné posuzovat mechanismy barvení. a) Standardní b) Iso-kinetický
54 Kinetický model Neizotermní kinetika se dá popsat obecným modelem d c dt t = K(T) f(c K (T) je tepotně závislá rychlostní konstanta a f(c, c t ) je tepltně nezávislý kinetický člen. Formální integrací pro Vickerstaffův model (n = 2) vychází t, c ) c t = F(t) 1+ c 2 c F(t)
55 Teplotní člen V části lineárního ohřevu platí F(t) = G(t) - G(T0) for T < T1 t < t1 navazující části konstantní teploty je F(t) = K exp(-e/r T 1)(t- t1) + G(T 1) - G(T0) for t t1 0 Symbol G (x) označuje integrál G(x) = K0 Θ Θ je rychlost ohřevu. x 0 exp(-e/rx) dx
56 x Difúze C x x vodních par V řadě případů je zde sorpce doprovázena výrazným bobtnáním vláken, takže množství přístupných míst pro molekuly vody se zvětšuje. Dochází ke shlukování vodních par a vazbě nikoliv molekul, ale těchto shluků. U silně hydrofilních materiálů se tvoří poměrně veliké shluky a difúzní koeficient vody v pórech je vysoký. Pro méně hydrofilní materiály je tendence ke shlukování menší a difúzní koeficient vody v pórech klesá. Fickův zákon modifikovaný pro tvorbu shluků na specifických místně má tvar 2 C C D = + k 1 * C k * S 2 2 x t k 1 a k 2 jsou rychlostní konstanty sorpce a desorpce a S je maximální koncentrace vazných míst pro molekuly vodní páry x x t
Teorie transportu plynů a par polymerními membránami. Doc. Ing. Milan Šípek, CSc. Ústav fyzikální chemie VŠCHT Praha
 Teorie transportu plynů a par polymerními membránami Doc. Ing. Milan Šípek, CSc. Ústav fyzikální chemie VŠCHT Praha Úvod Teorie transportu Difuze v polymerních membránách Propustnost polymerních membrán
Teorie transportu plynů a par polymerními membránami Doc. Ing. Milan Šípek, CSc. Ústav fyzikální chemie VŠCHT Praha Úvod Teorie transportu Difuze v polymerních membránách Propustnost polymerních membrán
Chemie povrchů verze 2013
 Chemie povrchů verze 2013 Definice povrchu složitá, protože v nanoměřítku (na úrovni velikosti atomů) je elektronový obal atomů difúzní většinou definován fyzikální adsorpcí nereaktivních plynů Vlastnosti
Chemie povrchů verze 2013 Definice povrchu složitá, protože v nanoměřítku (na úrovni velikosti atomů) je elektronový obal atomů difúzní většinou definován fyzikální adsorpcí nereaktivních plynů Vlastnosti
Adsorpce. molekulární adsorpce: (g) (s), (l) (s)/(l),... iontová adsorpce Paneth Fajans. výměnná iontová adsorpce, protionty v aluminosilikátech
 Adsorpce 1/15 molekulární adsorpce: (g) (s), (l) (s)/(l),... iontová adsorpce Paneth Fajans výměnná iontová adsorpce, protionty v aluminosilikátech Ar na grafitu adsorpce: na povrch/rozhraní absorpce:
Adsorpce 1/15 molekulární adsorpce: (g) (s), (l) (s)/(l),... iontová adsorpce Paneth Fajans výměnná iontová adsorpce, protionty v aluminosilikátech Ar na grafitu adsorpce: na povrch/rozhraní absorpce:
KATEDRA MATERIÁLOVÉHO INŽENÝRSTVÍ A CHEMIE. 123TVVM transport vodní páry
 KATEDRA MATERIÁLOVÉHO INŽENÝRSTVÍ A CHEMIE 123TVVM transport vodní páry TRANSPORT VODNÍ PÁRY PORÉZNÍM PROSTŘEDÍM: Ve vzduchu obsažená vodní pára samovolně difunduje do míst s nižším parciálním tlakem až
KATEDRA MATERIÁLOVÉHO INŽENÝRSTVÍ A CHEMIE 123TVVM transport vodní páry TRANSPORT VODNÍ PÁRY PORÉZNÍM PROSTŘEDÍM: Ve vzduchu obsažená vodní pára samovolně difunduje do míst s nižším parciálním tlakem až
Počet atomů a molekul v monomolekulární vrstvě
 Počet atomů a molekul v monomolekulární vrstvě ϑ je stupeň pokrytí ϑ = N 1 N 1p N 1 = ϑn 1p ν 1 = 1 4 nv a ν 1ef = γν 1 = γ 1 4 nv a γ je koeficient ulpění () F6450 1 / 23 8kT v a = πm = 8kNa T π M 0 ν
Počet atomů a molekul v monomolekulární vrstvě ϑ je stupeň pokrytí ϑ = N 1 N 1p N 1 = ϑn 1p ν 1 = 1 4 nv a ν 1ef = γν 1 = γ 1 4 nv a γ je koeficient ulpění () F6450 1 / 23 8kT v a = πm = 8kNa T π M 0 ν
2.4 Stavové chování směsí plynů Ideální směs Ideální směs reálných plynů Stavové rovnice pro plynné směsi
 1. ZÁKLADNÍ POJMY 1.1 Systém a okolí 1.2 Vlastnosti systému 1.3 Vybrané základní veličiny 1.3.1 Množství 1.3.2 Délka 1.3.2 Délka 1.4 Vybrané odvozené veličiny 1.4.1 Objem 1.4.2 Hustota 1.4.3 Tlak 1.4.4
1. ZÁKLADNÍ POJMY 1.1 Systém a okolí 1.2 Vlastnosti systému 1.3 Vybrané základní veličiny 1.3.1 Množství 1.3.2 Délka 1.3.2 Délka 1.4 Vybrané odvozené veličiny 1.4.1 Objem 1.4.2 Hustota 1.4.3 Tlak 1.4.4
Při reálném chromatografickém ději nikdy nedojde k ustavení rovnováhy mezi oběma fázemi První ucelená teorie respektující uvedenou skutečnost byla
 Teorie chromatografie - III Příprava předmětu byla podpořena projektem OPPA č. CZ.2.17/3.1.00/33253 4.3.3 Teorie dynamická Při reálném chromatografickém ději nikdy nedojde k ustavení rovnováhy mezi oběma
Teorie chromatografie - III Příprava předmětu byla podpořena projektem OPPA č. CZ.2.17/3.1.00/33253 4.3.3 Teorie dynamická Při reálném chromatografickém ději nikdy nedojde k ustavení rovnováhy mezi oběma
Výzkum vlivu přenosových jevů na chování reaktoru se zkrápěným ložem katalyzátoru. Petr Svačina
 Výzkum vlivu přenosových jevů na chování reaktoru se zkrápěným ložem katalyzátoru Petr Svačina I. Vliv difuze vodíku tekoucím filmem kapaliny na průběh katalytické hydrogenace ve zkrápěných reaktorech
Výzkum vlivu přenosových jevů na chování reaktoru se zkrápěným ložem katalyzátoru Petr Svačina I. Vliv difuze vodíku tekoucím filmem kapaliny na průběh katalytické hydrogenace ve zkrápěných reaktorech
Katedra textilních materiálů ENÍ TEXTILIÍ PŘEDNÁŠKA 4
 PŘEDNÁŠKA 4 PODMÍNKY PRO Vlastnosti charakterizující vnější formu textilií Hmotnost Obchodní hmotnost - je definována jako čistá hmotnost doplněná o obchodní přirážku Čistá hmotnost - je to hmotnost materiálu
PŘEDNÁŠKA 4 PODMÍNKY PRO Vlastnosti charakterizující vnější formu textilií Hmotnost Obchodní hmotnost - je definována jako čistá hmotnost doplněná o obchodní přirážku Čistá hmotnost - je to hmotnost materiálu
Základy vakuové techniky
 Základy vakuové techniky Střední rychlost plynů Rychlost molekuly v p = (2 k N A ) * (T/M 0 ), N A = 6. 10 23 molekul na mol (Avogadrova konstanta), k = 1,38. 10-23 J/K.. Boltzmannova konstanta, T.. absolutní
Základy vakuové techniky Střední rychlost plynů Rychlost molekuly v p = (2 k N A ) * (T/M 0 ), N A = 6. 10 23 molekul na mol (Avogadrova konstanta), k = 1,38. 10-23 J/K.. Boltzmannova konstanta, T.. absolutní
KATEDRA MATERIÁLOVÉHO INŽENÝRSTVÍ A CHEMIE. 123TVVM transport vodní páry
 KATEDRA MATERIÁLOVÉHO INŽENÝRSTVÍ A CHEMIE 123TVVM transport vodní páry Transport vodní páry porézním prostředím: Tepelná vodivost vzduchu: = 0,0262 W m -1 K -1 Tepelná vodivost izolantů: = cca 0,04 W
KATEDRA MATERIÁLOVÉHO INŽENÝRSTVÍ A CHEMIE 123TVVM transport vodní páry Transport vodní páry porézním prostředím: Tepelná vodivost vzduchu: = 0,0262 W m -1 K -1 Tepelná vodivost izolantů: = cca 0,04 W
Teorie chromatografie - I
 Teorie chromatografie - I Veronika R. Meyer Practical High-Performance Liquid Chromatography, Wiley, 2010 http://onlinelibrary.wiley.com/book/10.1002/9780470688427 Příprava předmětu byla podpořena projektem
Teorie chromatografie - I Veronika R. Meyer Practical High-Performance Liquid Chromatography, Wiley, 2010 http://onlinelibrary.wiley.com/book/10.1002/9780470688427 Příprava předmětu byla podpořena projektem
Kapaliny Molekulové vdw síly, vodíkové můstky
 Kapaliny Molekulové vdw síly, vodíkové můstky Metalické roztavené kovy, ionty + elektrony, elektrostatické síly Iontové roztavené soli, FLINAK (LiF + NaF + KF), volně pohyblivé anionty a kationty, iontová
Kapaliny Molekulové vdw síly, vodíkové můstky Metalické roztavené kovy, ionty + elektrony, elektrostatické síly Iontové roztavené soli, FLINAK (LiF + NaF + KF), volně pohyblivé anionty a kationty, iontová
Transportní jevy v plynech Reálné plyny Fázové přechody Kapaliny
 Transportní jevy v plynech Reálné plyny Fázové přechody Kapaliny Hustota toku Zatím jsme studovali pouze soustavy, které byly v rovnovážném stavu není-li soustava v silovém poli, je hustota částic stejná
Transportní jevy v plynech Reálné plyny Fázové přechody Kapaliny Hustota toku Zatím jsme studovali pouze soustavy, které byly v rovnovážném stavu není-li soustava v silovém poli, je hustota částic stejná
Přednáška 4. Tlak nasycených par, odpařování. Materiály pro vakuovou techniku Procesy ve stěnách vak. systémů. Martin Kormunda
 Přednáška 4 Tlak nasycených par, odpařování. Materiály pro vakuovou techniku Procesy ve stěnách vak. systémů. Vypařování Mějme vakuový systém, ve kterém nejsou žádné plyny ani v objemu komory ani na jejích
Přednáška 4 Tlak nasycených par, odpařování. Materiály pro vakuovou techniku Procesy ve stěnách vak. systémů. Vypařování Mějme vakuový systém, ve kterém nejsou žádné plyny ani v objemu komory ani na jejích
Kapaliny Molekulové vdw síly, vodíkové můstky
 Kapaliny Molekulové vdw síly, vodíkové můstky Metalické roztavené kovy, ionty + elektrony, elektrostatické síly Iontové roztavené soli, FLINAK (LiF + NaF + KF), volně pohyblivé anionty a kationty, iontová
Kapaliny Molekulové vdw síly, vodíkové můstky Metalické roztavené kovy, ionty + elektrony, elektrostatické síly Iontové roztavené soli, FLINAK (LiF + NaF + KF), volně pohyblivé anionty a kationty, iontová
Kapaliny Molekulové vdw síly, vodíkové můstky
 Kapaliny Molekulové vdw síly, vodíkové můstky Metalické roztavené kovy, ionty + elektrony, elektrostatické síly Iontové roztavené soli, FLINAK (LiF + NaF + KF), volně pohyblivé anionty a kationty, iontová
Kapaliny Molekulové vdw síly, vodíkové můstky Metalické roztavené kovy, ionty + elektrony, elektrostatické síly Iontové roztavené soli, FLINAK (LiF + NaF + KF), volně pohyblivé anionty a kationty, iontová
Vlastnosti vláken geometrické vlastnosti: mechanické vlastnosti: termické a termomechanické vlastnosti: elektrické vlastnosti: povrchové vlastnosti:
 Vlastnosti vláken Souvisejí s: a) chemickým složením b) způsobem výroby geometrické vlastnosti: délka, jemnost a tvar příčného řezu mechanické vlastnosti: pevnost, tažnost, modul, tuhost, zotavení termické
Vlastnosti vláken Souvisejí s: a) chemickým složením b) způsobem výroby geometrické vlastnosti: délka, jemnost a tvar příčného řezu mechanické vlastnosti: pevnost, tažnost, modul, tuhost, zotavení termické
Vybrané technologie povrchových úprav. Základy vakuové techniky Doc. Ing. Karel Daďourek 2006
 Vybrané technologie povrchových úprav Základy vakuové techniky Doc. Ing. Karel Daďourek 2006 Střední rychlost plynů Rychlost molekuly v p = (2 k N A ) * (T/M 0 ), N A = 6. 10 23 molekul na mol (Avogadrova
Vybrané technologie povrchových úprav Základy vakuové techniky Doc. Ing. Karel Daďourek 2006 Střední rychlost plynů Rychlost molekuly v p = (2 k N A ) * (T/M 0 ), N A = 6. 10 23 molekul na mol (Avogadrova
Metody separace. přírodních látek
 Metody separace přírodních látek (5) Chromatografie; základní definice a klasifikace ruzných metod; kapalinová chromatografie, plynová chromatografie, přístrojová technika. Chromatografie «F(+)d» 1897
Metody separace přírodních látek (5) Chromatografie; základní definice a klasifikace ruzných metod; kapalinová chromatografie, plynová chromatografie, přístrojová technika. Chromatografie «F(+)d» 1897
Struktura polymerů. Příprava (výroba).struktura vlastnosti. Materiálové inženýrství (Nauka o materiálu) Základní představy: přírodní vs.
 Struktura polymerů Základní představy: přírodní vs. syntetické V.Švorčík, vaclav.svorcik@vscht.cz celulóza přírodní kaučuk Příprava (výroba).struktura vlastnosti Materiálové inženýrství (Nauka o materiálu)
Struktura polymerů Základní představy: přírodní vs. syntetické V.Švorčík, vaclav.svorcik@vscht.cz celulóza přírodní kaučuk Příprava (výroba).struktura vlastnosti Materiálové inženýrství (Nauka o materiálu)
Skupenské stavy látek. Mezimolekulární síly
 Skupenské stavy látek Mezimolekulární síly 1 Interakce iont-dipól Např. hydratační (solvatační) interakce mezi Na + (iont) a molekulou vody (dipól). Jde o nejsilnější mezimolekulární (nevazebnou) interakci.
Skupenské stavy látek Mezimolekulární síly 1 Interakce iont-dipól Např. hydratační (solvatační) interakce mezi Na + (iont) a molekulou vody (dipól). Jde o nejsilnější mezimolekulární (nevazebnou) interakci.
VÍTÁM VÁS NA PŘEDNÁŠCE Z PŘEDMĚTU TCT
 VÍTÁM VÁS NA PŘEDNÁŠCE Z PŘEDMĚTU TCT opakování Jeden směr křížem Cros - cros náhodně náhodně náhodně NT ze staplových vláken vlákna pojená pod tryskou Suchá technologie Mokrá technologie vlákna Metody
VÍTÁM VÁS NA PŘEDNÁŠCE Z PŘEDMĚTU TCT opakování Jeden směr křížem Cros - cros náhodně náhodně náhodně NT ze staplových vláken vlákna pojená pod tryskou Suchá technologie Mokrá technologie vlákna Metody
Opakování
 Slabé vazebné interakce Opakování Co je to atom? Opakování Opakování Co je to atom? Atom je nejmenší částice hmoty, chemicky dále nedělitelná. Skládá se z atomového jádra obsahujícího protony a neutrony
Slabé vazebné interakce Opakování Co je to atom? Opakování Opakování Co je to atom? Atom je nejmenší částice hmoty, chemicky dále nedělitelná. Skládá se z atomového jádra obsahujícího protony a neutrony
Fyzikální chemie. Magda Škvorová KFCH CN463 magda.skvorova@ujep.cz, tel. 3302. 14. února 2013
 Fyzikální chemie Magda Škvorová KFCH CN463 magda.skvorova@ujep.cz, tel. 3302 14. února 2013 Co je fyzikální chemie? Co je fyzikální chemie? makroskopický přístup: (klasická) termodynamika nerovnovážná
Fyzikální chemie Magda Škvorová KFCH CN463 magda.skvorova@ujep.cz, tel. 3302 14. února 2013 Co je fyzikální chemie? Co je fyzikální chemie? makroskopický přístup: (klasická) termodynamika nerovnovážná
Voda, pára, vypařování,
 Voda, pára, vypařování, rovnovážná vlhkost MaK 3/2011 Molekula vody a její vlastnosti Základní charakteristiky: Malá(průměr asi 2,8 Å), relativně lehká (M r =18, 015) Polární(vytváří relativně silný dipól),
Voda, pára, vypařování, rovnovážná vlhkost MaK 3/2011 Molekula vody a její vlastnosti Základní charakteristiky: Malá(průměr asi 2,8 Å), relativně lehká (M r =18, 015) Polární(vytváří relativně silný dipól),
9. Chemické reakce Kinetika
 Základní pojmy Kinetické rovnice pro celistvé řády Katalýza Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti reakční mechanismus elementární reakce a molekularita reakce reakční rychlost
Základní pojmy Kinetické rovnice pro celistvé řády Katalýza Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti reakční mechanismus elementární reakce a molekularita reakce reakční rychlost
Mol. fyz. a termodynamika
 Molekulová fyzika pracuje na základě kinetické teorie látek a statistiky Termodynamika zkoumání tepelných jevů a strojů nezajímají nás jednotlivé částice Molekulová fyzika základem jsou: Látka kteréhokoli
Molekulová fyzika pracuje na základě kinetické teorie látek a statistiky Termodynamika zkoumání tepelných jevů a strojů nezajímají nás jednotlivé částice Molekulová fyzika základem jsou: Látka kteréhokoli
PLYNOVÁ CHROMATOGRAFIE (GC)
 PLYNOVÁ CHROMATOGRAFIE (GC) Dělení látek mezi stacionární a mobilní fázi na základě rozdílů v těkavosti a struktuře (separované látky vykazují rozdílnou chromatografickou afinitu) Metoda vhodná pro látky:
PLYNOVÁ CHROMATOGRAFIE (GC) Dělení látek mezi stacionární a mobilní fázi na základě rozdílů v těkavosti a struktuře (separované látky vykazují rozdílnou chromatografickou afinitu) Metoda vhodná pro látky:
2. Úloha difúze v heterogenní katalýze
 2. Úloha difúze v heterogenní katalýze Vnitřní difúze při nerovnoměrné radiální distribuci aktivní složky v částici katalyzátoru Kateřina Horáčková Příčina radiálního aktivitního profilu v katalyzátorové
2. Úloha difúze v heterogenní katalýze Vnitřní difúze při nerovnoměrné radiální distribuci aktivní složky v částici katalyzátoru Kateřina Horáčková Příčina radiálního aktivitního profilu v katalyzátorové
MODELOVÁNÍ. Základní pojmy. Obecný postup vytváření induktivních modelů. Měřicí a řídicí technika magisterské studium FTOP - přednášky ZS 2009/10
 MODELOVÁNÍ základní pojmy a postupy principy vytváření deterministických matematických modelů vybrané základní vztahy používané při vytváření matematických modelů ukázkové příklady Základní pojmy matematický
MODELOVÁNÍ základní pojmy a postupy principy vytváření deterministických matematických modelů vybrané základní vztahy používané při vytváření matematických modelů ukázkové příklady Základní pojmy matematický
Termodynamika (td.) se obecně zabývá vzájemnými vztahy a přeměnami různých druhů
 Termodynamika (td.) se obecně zabývá vzájemnými vztahy a přeměnami různých druhů energií (mechanické, tepelné, elektrické, magnetické, chemické a jaderné) při td. dějích. Na rozdíl od td. cyklických dějů
Termodynamika (td.) se obecně zabývá vzájemnými vztahy a přeměnami různých druhů energií (mechanické, tepelné, elektrické, magnetické, chemické a jaderné) při td. dějích. Na rozdíl od td. cyklických dějů
Molekulová fyzika a termika. Přehled základních pojmů
 Molekulová fyzika a termika Přehled základních pojmů Kinetická teorie látek Vychází ze tří experimentálně ověřených poznatků: 1) Látky se skládají z částic - molekul, atomů nebo iontů, mezi nimiž jsou
Molekulová fyzika a termika Přehled základních pojmů Kinetická teorie látek Vychází ze tří experimentálně ověřených poznatků: 1) Látky se skládají z částic - molekul, atomů nebo iontů, mezi nimiž jsou
KATEDRA MATERIÁLOVÉHO INŽENÝRSTVÍ A CHEMIE. 123TVVM transport kapalné vody
 KATEDRA MATERIÁLOVÉHO INŽENÝRSTVÍ A CHEMIE 123TVVM transport kapalné vody Transport vody porézním prostředím: Souč. tepelné vodivosti vzduchu: = 0,024-0,031 W/mK Souč. tepelné vodivosti izolantů: = cca
KATEDRA MATERIÁLOVÉHO INŽENÝRSTVÍ A CHEMIE 123TVVM transport kapalné vody Transport vody porézním prostředím: Souč. tepelné vodivosti vzduchu: = 0,024-0,031 W/mK Souč. tepelné vodivosti izolantů: = cca
MĚŘENÍ RELATIVNÍ VLHKOSTI. - pro měření relativní vlhkosti se používají metody měření
 MĚŘENÍ RELATIVNÍ VLHKOSTI - pro měření relativní vlhkosti se používají metody měření obsahu vlhkosti vplynech Psychrometrické metody Měření rosného bodu Sorpční metody Rovnovážné elektrolytické metody
MĚŘENÍ RELATIVNÍ VLHKOSTI - pro měření relativní vlhkosti se používají metody měření obsahu vlhkosti vplynech Psychrometrické metody Měření rosného bodu Sorpční metody Rovnovážné elektrolytické metody
TERMOMECHANIKA 1. Základní pojmy
 1 FSI VUT v Brně, Energetický ústav Odbor termomechaniky a techniky prostředí prof. Ing. Milan Pavelek, CSc. TERMOMECHANIKA 1. Základní pojmy OSNOVA 1. KAPITOLY Termodynamická soustava Energie, teplo,
1 FSI VUT v Brně, Energetický ústav Odbor termomechaniky a techniky prostředí prof. Ing. Milan Pavelek, CSc. TERMOMECHANIKA 1. Základní pojmy OSNOVA 1. KAPITOLY Termodynamická soustava Energie, teplo,
ODĚVNÍ KOMFORT TERMOFYZIOLOGICKÝ KOMFORT
 ODĚVNÍ KOMFORT TERMOFYZIOLOGICKÝ KOMFORT ČLOVĚK ODĚV - PROSTŘEDÍ FYZIOLOGICKÉ REAKCE ČLOVĚKA NA OKOLNÍ PROSTŘEDÍ Lidské tělo - nepřetržitý zdroj tepla Bazální metabolismus, teplo je produkováno na základě
ODĚVNÍ KOMFORT TERMOFYZIOLOGICKÝ KOMFORT ČLOVĚK ODĚV - PROSTŘEDÍ FYZIOLOGICKÉ REAKCE ČLOVĚKA NA OKOLNÍ PROSTŘEDÍ Lidské tělo - nepřetržitý zdroj tepla Bazální metabolismus, teplo je produkováno na základě
Vícefázové reaktory. Probublávaný reaktor plyn kapalina katalyzátor. Zuzana Tomešová
 Vícefázové reaktory Probublávaný reaktor plyn kapalina katalyzátor Zuzana Tomešová 2008 Probublávaný reaktor plyn - kapalina - katalyzátor Hydrogenace méně těkavých látek za vyššího tlaku Kolony naplněné
Vícefázové reaktory Probublávaný reaktor plyn kapalina katalyzátor Zuzana Tomešová 2008 Probublávaný reaktor plyn - kapalina - katalyzátor Hydrogenace méně těkavých látek za vyššího tlaku Kolony naplněné
VÝUKOVÝ MODUL MEMBRÁNOVÝCH PROCESŮ TÉMATA PŘEDNÁŠEK
 VÝUKOVÝ MODUL MEMBRÁNOVÝCH PROCESŮ TÉMATA PŘEDNÁŠEK TRANSPORT LÁTEK MEMBRÁNAMI Transport látek porézními membránami - Plouživý tok nestlačitelných tekutin vrstvou částic - Plouživý tok stlačitelných tekutin
VÝUKOVÝ MODUL MEMBRÁNOVÝCH PROCESŮ TÉMATA PŘEDNÁŠEK TRANSPORT LÁTEK MEMBRÁNAMI Transport látek porézními membránami - Plouživý tok nestlačitelných tekutin vrstvou částic - Plouživý tok stlačitelných tekutin
Nultá věta termodynamická
 TERMODYNAMIKA Nultá věta termodynamická 2 Práce 3 Práce - příklady 4 1. věta termodynamická 5 Entalpie 6 Tepelné kapacity 7 Vnitřní energie a entalpie ideálního plynu 8 Výpočet tepla a práce 9 Adiabatický
TERMODYNAMIKA Nultá věta termodynamická 2 Práce 3 Práce - příklady 4 1. věta termodynamická 5 Entalpie 6 Tepelné kapacity 7 Vnitřní energie a entalpie ideálního plynu 8 Výpočet tepla a práce 9 Adiabatický
VLASTNOSTI VLÁKEN. 3. Tepelné vlastnosti vláken
 VLASNOSI VLÁKEN 3. epelné vlastnosti vláken 3.. Úvod epelné vlastnosti vláken jsou velice důležité, neboť jsou rozhodující pro volbu vhodných parametrů zpracování i použití vláken. Závisí na chemickém
VLASNOSI VLÁKEN 3. epelné vlastnosti vláken 3.. Úvod epelné vlastnosti vláken jsou velice důležité, neboť jsou rozhodující pro volbu vhodných parametrů zpracování i použití vláken. Závisí na chemickém
IDEÁLNÍ PLYN. Stavová rovnice
 IDEÁLNÍ PLYN Stavová rovnice Ideální plyn ) rozměry molekul jsou zanedbatelné vzhledem k jejich vzdálenostem 2) molekuly plynu na sebe působí jen při vzájemných srážkách 3) všechny srážky jsou dokonale
IDEÁLNÍ PLYN Stavová rovnice Ideální plyn ) rozměry molekul jsou zanedbatelné vzhledem k jejich vzdálenostem 2) molekuly plynu na sebe působí jen při vzájemných srážkách 3) všechny srážky jsou dokonale
Vlhkost. Voda - skupenství led voda vodní pára. ve stavebních konstrukcích - vše ve vzduchu (uvnitř budov) - vodní pára
 Vlhkost Voda - skupenství led voda vodní pára ve stavebních konstrukcích - vše ve vzduchu (uvnitř budov) - vodní pára Vlhkost ve stavebních konstrukcích nežádoucí účinky... zdroje: srážková v. zemní v.
Vlhkost Voda - skupenství led voda vodní pára ve stavebních konstrukcích - vše ve vzduchu (uvnitř budov) - vodní pára Vlhkost ve stavebních konstrukcích nežádoucí účinky... zdroje: srážková v. zemní v.
Základem molekulové fyziky je kinetická teorie látek. Vychází ze tří pouček:
 Molekulová fyzika zkoumá vlastnosti látek na základě jejich vnitřní struktury, pohybu a vzájemného působení částic, ze kterých se látky skládají. Termodynamika se zabývá zákony přeměny různých forem energie
Molekulová fyzika zkoumá vlastnosti látek na základě jejich vnitřní struktury, pohybu a vzájemného působení částic, ze kterých se látky skládají. Termodynamika se zabývá zákony přeměny různých forem energie
Autokláv reaktor pro promíchávané vícefázové reakce
 Vysoká škola chemicko technologická v Praze Ústav organické technologie (111) Autokláv reaktor pro promíchávané vícefázové reakce Vypracoval : Bc. Tomáš Sommer Předmět: Vícefázové reaktory (prof. Ing.
Vysoká škola chemicko technologická v Praze Ústav organické technologie (111) Autokláv reaktor pro promíchávané vícefázové reakce Vypracoval : Bc. Tomáš Sommer Předmět: Vícefázové reaktory (prof. Ing.
Třífázové trubkové reaktory se zkrápěným ložem katalyzátoru. Roman Snop
 Třífázové trubkové reaktory se zkrápěným ložem katalyzátoru Roman Snop Charakteristika Zkrápěné reaktory jsou nejvhodněji aplikovatelné na provoz heterogenně katalyzovaných reakcí. Nacházejí uplatnění
Třífázové trubkové reaktory se zkrápěným ložem katalyzátoru Roman Snop Charakteristika Zkrápěné reaktory jsou nejvhodněji aplikovatelné na provoz heterogenně katalyzovaných reakcí. Nacházejí uplatnění
Úvod do koroze. (kapitola, která bude společná všem korozním laboratorním pracím a kterou studenti musí znát bez ohledu na to, jakou práci dělají)
 Úvod do koroze (kapitola, která bude společná všem korozním laboratorním pracím a kterou studenti musí znát bez ohledu na to, jakou práci dělají) Koroze je proces degradace kovu nebo slitiny kovů působením
Úvod do koroze (kapitola, která bude společná všem korozním laboratorním pracím a kterou studenti musí znát bez ohledu na to, jakou práci dělají) Koroze je proces degradace kovu nebo slitiny kovů působením
Tepelně vlhkostní mikroklima. Vlhkost v budovách
 Tepelně vlhkostní mikroklima Vlhkost v budovách Zdroje vodní páry stavební vlhkost - vodní pára vázaná v materiálech v důsledku mokrých technologických procesů (chemicky nebo fyzikálně vázaná) zemní vlhkost
Tepelně vlhkostní mikroklima Vlhkost v budovách Zdroje vodní páry stavební vlhkost - vodní pára vázaná v materiálech v důsledku mokrých technologických procesů (chemicky nebo fyzikálně vázaná) zemní vlhkost
Přehled fyzikálních vlastností dřeva
 Dřevo a jeho ochrana Přehled fyzikálních vlastností dřeva cvičení Dřevo a jeho ochrana 2 Charakteristiky dřeva jako materiálu Anizotropie = na směru závislé vlastnosti Pórovitost = porézní materiál Hygroskopicita
Dřevo a jeho ochrana Přehled fyzikálních vlastností dřeva cvičení Dřevo a jeho ochrana 2 Charakteristiky dřeva jako materiálu Anizotropie = na směru závislé vlastnosti Pórovitost = porézní materiál Hygroskopicita
Nauka o materiálu. Přednáška č.10 Difuze v tuhých látkách, fáze a fázové přeměny
 Nauka o materiálu Přednáška č.10 Difuze v tuhých látkách, fáze a fázové přeměny Difuze v tuhých látkách Difuzí nazýváme přesun atomů nebo iontů na vzdálenost větší než je meziatomová vzdálenost. Hnací
Nauka o materiálu Přednáška č.10 Difuze v tuhých látkách, fáze a fázové přeměny Difuze v tuhých látkách Difuzí nazýváme přesun atomů nebo iontů na vzdálenost větší než je meziatomová vzdálenost. Hnací
Reaktory pro systém plyn-kapalina
 Reaktory pro systém plyn-kapalina Vypracoval : Jan Horáček FCHT, ústav 111 Prováděné reakce Rychlé : všechen absorbovaný plyn zreaguje již na fázovém rozhraní (př. : absorpce kyselých plynů : CO 2, H 2
Reaktory pro systém plyn-kapalina Vypracoval : Jan Horáček FCHT, ústav 111 Prováděné reakce Rychlé : všechen absorbovaný plyn zreaguje již na fázovém rozhraní (př. : absorpce kyselých plynů : CO 2, H 2
Zákony ideálního plynu
 5.2Zákony ideálního plynu 5.1.1 Ideální plyn 5.1.2 Avogadrův zákon 5.1.3 Normální podmínky 5.1.4 Boyleův-Mariottův zákon Izoterma 5.1.5 Gay-Lussacův zákon 5.1.6 Charlesův zákon 5.1.7 Poissonův zákon 5.1.8
5.2Zákony ideálního plynu 5.1.1 Ideální plyn 5.1.2 Avogadrův zákon 5.1.3 Normální podmínky 5.1.4 Boyleův-Mariottův zákon Izoterma 5.1.5 Gay-Lussacův zákon 5.1.6 Charlesův zákon 5.1.7 Poissonův zákon 5.1.8
Přednáška 2. Martin Kormunda
 Přednáška 2 Objemové procesy Difuze Tepelná transpirace (efuze) Přenos energie Proudění plynů : proud plynu, vakuová vodivost, vodivost otvoru, potrubí. Proudění plynu netěsnostmi Difuze plynu Veškeré
Přednáška 2 Objemové procesy Difuze Tepelná transpirace (efuze) Přenos energie Proudění plynů : proud plynu, vakuová vodivost, vodivost otvoru, potrubí. Proudění plynu netěsnostmi Difuze plynu Veškeré
6. Stavy hmoty - Plyny
 skupenství plynné plyn x pára (pod kritickou teplotou) stavové chování Ideální plyn Reálné plyny Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti skupenství plynné reálný plyn ve stavu
skupenství plynné plyn x pára (pod kritickou teplotou) stavové chování Ideální plyn Reálné plyny Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti skupenství plynné reálný plyn ve stavu
Typy molekul, látek a jejich vazeb v organismech
 Typy molekul, látek a jejich vazeb v organismech Typy molekul, látek a jejich vazeb v organismech Organismy se skládají z molekul rozličných látek Jednotlivé látky si organismus vytváří sám z jiných látek,
Typy molekul, látek a jejich vazeb v organismech Typy molekul, látek a jejich vazeb v organismech Organismy se skládají z molekul rozličných látek Jednotlivé látky si organismus vytváří sám z jiných látek,
Ústav Anorganické Technologie LABORATORNÍ
 Ústav Anorganické Technologie LABORATORNÍ PRÁCE č.13 Měření permeačních charakteristik kompozitních membrán 1 Teoretická část Mluví-li se o membránách, každý si asi představí tenkou přepážku, která odděluje
Ústav Anorganické Technologie LABORATORNÍ PRÁCE č.13 Měření permeačních charakteristik kompozitních membrán 1 Teoretická část Mluví-li se o membránách, každý si asi představí tenkou přepážku, která odděluje
Dynamické vs. Statické Izotermy Které jsou lepší? Brady Carter Vědecký pracovník Decagon Devices, Inc.
 Dynamické vs. Statické Izotermy Které jsou lepší? Brady Carter Vědecký pracovník Decagon Devices, Inc. Popis Úvod do sorpčních izoterm vlhkosti - Brady Carter Dynamické a statické izotermy - Shelly Schmidt
Dynamické vs. Statické Izotermy Které jsou lepší? Brady Carter Vědecký pracovník Decagon Devices, Inc. Popis Úvod do sorpčních izoterm vlhkosti - Brady Carter Dynamické a statické izotermy - Shelly Schmidt
Plyn. 11 plynných prvků. Vzácné plyny. He, Ne, Ar, Kr, Xe, Rn Diatomické plynné prvky H 2, N 2, O 2, F 2, Cl 2
 Plyny Plyn T v, K Vzácné plyny 11 plynných prvků He, Ne, Ar, Kr, Xe, Rn 165 Rn 211 N 2 O 2 77 F 2 90 85 Diatomické plynné prvky Cl 2 238 H 2, N 2, O 2, F 2, Cl 2 H 2 He Ne Ar Kr Xe 20 4.4 27 87 120 1 Plyn
Plyny Plyn T v, K Vzácné plyny 11 plynných prvků He, Ne, Ar, Kr, Xe, Rn 165 Rn 211 N 2 O 2 77 F 2 90 85 Diatomické plynné prvky Cl 2 238 H 2, N 2, O 2, F 2, Cl 2 H 2 He Ne Ar Kr Xe 20 4.4 27 87 120 1 Plyn
Do známky zkoušky rovnocenným podílem započítávají získané body ze zápočtového testu.
 Podmínky pro získání zápočtu a zkoušky z předmětu Chemicko-inženýrská termodynamika pro zpracování ropy Zápočet je udělen, pokud student splní zápočtový test alespoň na 50 %. Zápočtový test obsahuje 3
Podmínky pro získání zápočtu a zkoušky z předmětu Chemicko-inženýrská termodynamika pro zpracování ropy Zápočet je udělen, pokud student splní zápočtový test alespoň na 50 %. Zápočtový test obsahuje 3
Třífázové trubkové reaktory se zkrápěným ložem katalyzátoru. Předmět: Vícefázové reaktory Jméno: Veronika Sedláková
 Třífázové trubkové reaktory se zkrápěným ložem katalyzátoru Předmět: Vícefázové reaktory Jméno: Veronika Sedláková 3-fázové reakce Autoklávy (diskontinuální) Trubkové reaktory (kontinuální) Probublávané
Třífázové trubkové reaktory se zkrápěným ložem katalyzátoru Předmět: Vícefázové reaktory Jméno: Veronika Sedláková 3-fázové reakce Autoklávy (diskontinuální) Trubkové reaktory (kontinuální) Probublávané
Rychlost chemické reakce A B. time. rychlost = - [A] t. [B] t. rychlost = Reakční rychlost a stechiometrie A + B C; R C = R A = R B A + 2B 3C;
![Rychlost chemické reakce A B. time. rychlost = - [A] t. [B] t. rychlost = Reakční rychlost a stechiometrie A + B C; R C = R A = R B A + 2B 3C; Rychlost chemické reakce A B. time. rychlost = - [A] t. [B] t. rychlost = Reakční rychlost a stechiometrie A + B C; R C = R A = R B A + 2B 3C;](/thumbs/56/39180690.jpg) Rychlost chemické reakce A B time rychlost = - [A] t rychlost = [B] t Reakční rychlost a stechiometrie A + B C; R C = R A = R B A + 2B 3C; 1 1 R A = RB = R 2 3 C Př.: Určete rychlost rozkladu HI v následující
Rychlost chemické reakce A B time rychlost = - [A] t rychlost = [B] t Reakční rychlost a stechiometrie A + B C; R C = R A = R B A + 2B 3C; 1 1 R A = RB = R 2 3 C Př.: Určete rychlost rozkladu HI v následující
Termodynamika a živé systémy. Helena Uhrová
 Termodynamika a živé systémy Helena Uhrová Základní pojmy termodynamiky soustava izolovaná otevřená okolí vlastnosti soustavy znaky popisující soustavu stav rovnováhy tok m či E =0 funkce stavu - soubor
Termodynamika a živé systémy Helena Uhrová Základní pojmy termodynamiky soustava izolovaná otevřená okolí vlastnosti soustavy znaky popisující soustavu stav rovnováhy tok m či E =0 funkce stavu - soubor
Carbovet - mechanismus vyvazování mykotoxinů neschopných adsorpce
 Dos 1654 July 25 nd, 2011 Carbovet - mechanismus vyvazování mykotoxinů neschopných adsorpce Catherine Ionescu Pancosma R&D, Carbovet expert 1 Představení Většina zákazníků požaduje vysvětlení jaký je mechanismus
Dos 1654 July 25 nd, 2011 Carbovet - mechanismus vyvazování mykotoxinů neschopných adsorpce Catherine Ionescu Pancosma R&D, Carbovet expert 1 Představení Většina zákazníků požaduje vysvětlení jaký je mechanismus
Modelování zdravotně významných částic v ovzduší v podmínkách městské zástavby
 Modelování zdravotně významných částic v ovzduší v podmínkách městské zástavby Jiří Pospíšil, Miroslav Jícha pospisil.j@fme.vutbr.cz Vysoké učení technické v Brně Fakulta strojního inženýrství Energetický
Modelování zdravotně významných částic v ovzduší v podmínkách městské zástavby Jiří Pospíšil, Miroslav Jícha pospisil.j@fme.vutbr.cz Vysoké učení technické v Brně Fakulta strojního inženýrství Energetický
VÝUKOVÝ MODUL MEMBRÁNOVÝCH PROCESŮ SYLABY PŘEDNÁŠEK TRANSPORT LÁTEK MEMBRÁNAMI MEMBRÁNOVÉ MATERIÁLY
 VÝUKOVÝ MODUL MEMBRÁNOVÝCH PROCESŮ SYLABY PŘEDNÁŠEK TRANSPORT LÁTEK MEMBRÁNAMI zodpovědni: P. Mikulášek, H. Jiránková, M. Šípek, K. Friess, K. Bouzek Transport látek porézními membránami (P. Mikulášek)
VÝUKOVÝ MODUL MEMBRÁNOVÝCH PROCESŮ SYLABY PŘEDNÁŠEK TRANSPORT LÁTEK MEMBRÁNAMI zodpovědni: P. Mikulášek, H. Jiránková, M. Šípek, K. Friess, K. Bouzek Transport látek porézními membránami (P. Mikulášek)
Plyn. 11 plynných prvků. Vzácné plyny. He, Ne, Ar, Kr, Xe, Rn Diatomické plynné prvky H 2, N 2, O 2, F 2, Cl 2
 Plyny Plyn T v, K Vzácné plyny 11 plynných prvků He, Ne, Ar, Kr, Xe, Rn 165 Rn 211 N 2 O 2 77 F 2 90 85 Diatomické plynné prvky Cl 2 238 H 2, N 2, O 2, F 2, Cl 2 H 2 He Ne Ar Kr Xe 20 4.4 27 87 120 1 Plyn
Plyny Plyn T v, K Vzácné plyny 11 plynných prvků He, Ne, Ar, Kr, Xe, Rn 165 Rn 211 N 2 O 2 77 F 2 90 85 Diatomické plynné prvky Cl 2 238 H 2, N 2, O 2, F 2, Cl 2 H 2 He Ne Ar Kr Xe 20 4.4 27 87 120 1 Plyn
PROCESY V TECHNICE BUDOV 8
 UNIVERZITA TOMÁŠE BATI VE ZLÍNĚ FAKULTA APLIKOVANÉ INFORMATIKY PROCESY V TECHNICE BUDOV 8 Dagmar Janáčová, Hana Charvátová Zlín 2013 Tento studijní materiál vznikl za finanční podpory Evropského sociálního
UNIVERZITA TOMÁŠE BATI VE ZLÍNĚ FAKULTA APLIKOVANÉ INFORMATIKY PROCESY V TECHNICE BUDOV 8 Dagmar Janáčová, Hana Charvátová Zlín 2013 Tento studijní materiál vznikl za finanční podpory Evropského sociálního
Energie v chemických reakcích
 Energie v chemických reakcích Energetická bilance reakce CH 4 + Cl 2 = CH 3 Cl + HCl rozštěpení vazeb vznik nových vazeb V chemických reakcích dochází ke změně vazeb mezi atomy. Vazebná energie uvolnění
Energie v chemických reakcích Energetická bilance reakce CH 4 + Cl 2 = CH 3 Cl + HCl rozštěpení vazeb vznik nových vazeb V chemických reakcích dochází ke změně vazeb mezi atomy. Vazebná energie uvolnění
Sol gel metody, 3. část
 Sol gel metody, 3. část Zdeněk Moravec (hugo@chemi.muni.cz) V posledním díle se podíváme na možnosti, jak připravené materiály charakterizovat a také na možnosti jejich využití v praxi. Metod umožňujících
Sol gel metody, 3. část Zdeněk Moravec (hugo@chemi.muni.cz) V posledním díle se podíváme na možnosti, jak připravené materiály charakterizovat a také na možnosti jejich využití v praxi. Metod umožňujících
Plyn. 11 plynných prvků. Vzácné plyny He, Ne, Ar, Kr, Xe, Rn Diatomické plynné prvky H 2, N 2, O 2, F 2, Cl 2
 Plyny Plyn T v, K 11 plynných prvků Vzácné plyny He, Ne, Ar, Kr, Xe, Rn Diatomické plynné prvky H 2, N 2, O 2, F 2, Cl 2 H 2 20 He 4.4 Ne 27 Ar 87 Kr 120 Xe 165 Rn 211 N 2 77 O 2 90 F 2 85 Cl 2 238 1 Plyn
Plyny Plyn T v, K 11 plynných prvků Vzácné plyny He, Ne, Ar, Kr, Xe, Rn Diatomické plynné prvky H 2, N 2, O 2, F 2, Cl 2 H 2 20 He 4.4 Ne 27 Ar 87 Kr 120 Xe 165 Rn 211 N 2 77 O 2 90 F 2 85 Cl 2 238 1 Plyn
8 Elasticita kaučukových sítí
 8 Elasticita kaučukových sítí Elastomerní polymerní látky (např. kaučuky) tvoří ze / chemické příčné vazby a / fyzikální uzly. Vyznačují se schopností deformovat se již malou silou nejméně o 00 % své původní
8 Elasticita kaučukových sítí Elastomerní polymerní látky (např. kaučuky) tvoří ze / chemické příčné vazby a / fyzikální uzly. Vyznačují se schopností deformovat se již malou silou nejméně o 00 % své původní
Tepelná vodivost. střední rychlost. T 1 > T 2 z. teplo přenesené za čas dt: T 1 T 2. tepelný tok střední volná dráha. součinitel tepelné vodivosti
 Tepelná vodivost teplo přenesené za čas dt: T 1 > T z T 1 S tepelný tok střední volná dráha T součinitel tepelné vodivosti střední rychlost Tepelná vodivost součinitel tepelné vodivosti při T = 300 K součinitel
Tepelná vodivost teplo přenesené za čas dt: T 1 > T z T 1 S tepelný tok střední volná dráha T součinitel tepelné vodivosti střední rychlost Tepelná vodivost součinitel tepelné vodivosti při T = 300 K součinitel
Teorie chromatografie - II
 Teorie chromatografie - II Příprava předmětu byla podpořena projektem OPP č. CZ.2.17/3.1.00/33253 2.2 Interakce mezi molekulami Mezi elektroneutrálními molekulami působí slabé přitažlivé síly, které sdružují
Teorie chromatografie - II Příprava předmětu byla podpořena projektem OPP č. CZ.2.17/3.1.00/33253 2.2 Interakce mezi molekulami Mezi elektroneutrálními molekulami působí slabé přitažlivé síly, které sdružují
102FYZB-Termomechanika
 České vysoké učení technické v Praze Fakulta stavební katedra fyziky 102FYZB-Termomechanika Sbírka úloh (koncept) Autor: Doc. RNDr. Vítězslav Vydra, CSc Poslední aktualizace dne 20. prosince 2018 OBSAH
České vysoké učení technické v Praze Fakulta stavební katedra fyziky 102FYZB-Termomechanika Sbírka úloh (koncept) Autor: Doc. RNDr. Vítězslav Vydra, CSc Poslední aktualizace dne 20. prosince 2018 OBSAH
Membránové potenciály
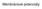 Membránové potenciály Vznik a podstata membránového potenciálu vzniká v důsledku nerovnoměrného rozdělení fyziologických iontů po obou stranách membrány nestejná propustnost membrány pro různé ionty různá
Membránové potenciály Vznik a podstata membránového potenciálu vzniká v důsledku nerovnoměrného rozdělení fyziologických iontů po obou stranách membrány nestejná propustnost membrány pro různé ionty různá
Cvičení 4 Transport plynné a kapalné vody. Transport vodní páry porézním prostředím
 Cvičení 4 Transport plynné a kapalné vody Transport vodní páry porézním prostředím Vzhledem k tepelné vodivosti vody a dalším nepříznivým vlastnostem a účinkům v porézních materiálech je s problémem tepelné
Cvičení 4 Transport plynné a kapalné vody Transport vodní páry porézním prostředím Vzhledem k tepelné vodivosti vody a dalším nepříznivým vlastnostem a účinkům v porézních materiálech je s problémem tepelné
ZÁKLADNÍ MODELY TOKU PORÉZNÍ MEMBRÁNOU
 ZÁKLADNÍ MODELY TOKU PORÉZNÍ MEMBRÁNOU Znázornění odporů způsobujících snižování průtoku permeátu nástřik porézní membrána Druhy odporů R p blokování pórů R p R a R m R a R m R g R cp adsorbce membrána
ZÁKLADNÍ MODELY TOKU PORÉZNÍ MEMBRÁNOU Znázornění odporů způsobujících snižování průtoku permeátu nástřik porézní membrána Druhy odporů R p blokování pórů R p R a R m R a R m R g R cp adsorbce membrána
FYZIKÁLNÍ CHEMIE I: 1. ČÁST KCH/P401
 Univerzita J. E. Purkyně v Ústí nad Labem Přírodovědecká fakulta FYZIKÁLNÍ CHEMIE I: 1. ČÁST KCH/P401 Magda Škvorová Ústí nad Labem 2013 Obor: Toxikologie a analýza škodlivin, Chemie (dvouoborová) Klíčová
Univerzita J. E. Purkyně v Ústí nad Labem Přírodovědecká fakulta FYZIKÁLNÍ CHEMIE I: 1. ČÁST KCH/P401 Magda Škvorová Ústí nad Labem 2013 Obor: Toxikologie a analýza škodlivin, Chemie (dvouoborová) Klíčová
LOGO. Struktura a vlastnosti plynů Ideální plyn
 Struktura a vlastnosti plynů Ideální plyn Ideální plyn Protože popsat chování plynů je nad naše možnosti, zavádíme zjednodušený model tzv. ideálního plynu, který má tyto vlastnosti: Částice ideálního plynu
Struktura a vlastnosti plynů Ideální plyn Ideální plyn Protože popsat chování plynů je nad naše možnosti, zavádíme zjednodušený model tzv. ideálního plynu, který má tyto vlastnosti: Částice ideálního plynu
Interakce mezi kapalinou a vlákenným materiálem
 3. přednáška Interakce mezi kapalinou a vlákenným materiálem OPAKOVÁNÍ Soudržnost dvou spojovaných ploch, tedy vazba mezi pevným povrchem vláken a adhezivem (pojivem) je chápána jako ADHEZE. Primární i
3. přednáška Interakce mezi kapalinou a vlákenným materiálem OPAKOVÁNÍ Soudržnost dvou spojovaných ploch, tedy vazba mezi pevným povrchem vláken a adhezivem (pojivem) je chápána jako ADHEZE. Primární i
5.4 Adiabatický děj Polytropický děj Porovnání dějů Základy tepelných cyklů První zákon termodynamiky pro cykly 42 6.
 OBSAH Předmluva 9 I. ZÁKLADY TERMODYNAMIKY 10 1. Základní pojmy 10 1.1 Termodynamická soustava 10 1.2 Energie, teplo, práce 10 1.3 Stavy látek 11 1.4 Veličiny popisující stavy látek 12 1.5 Úlohy technické
OBSAH Předmluva 9 I. ZÁKLADY TERMODYNAMIKY 10 1. Základní pojmy 10 1.1 Termodynamická soustava 10 1.2 Energie, teplo, práce 10 1.3 Stavy látek 11 1.4 Veličiny popisující stavy látek 12 1.5 Úlohy technické
12. Elektrochemie základní pojmy
 Důležité veličiny Elektroda, článek Potenciometrie Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti Důležité veličiny proud I (ampér - A) náboj Q (coulomb - C) Q t 0 I dt napětí, potenciál
Důležité veličiny Elektroda, článek Potenciometrie Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti Důležité veličiny proud I (ampér - A) náboj Q (coulomb - C) Q t 0 I dt napětí, potenciál
Osnova pro předmět Fyzikální chemie II magisterský kurz
 Osnova pro předmět Fyzikální chemie II magisterský kurz Časový a obsahový program přednášek Týden Obsahová náplň přednášky Pozn. Stavové chování tekutin 1,2a 1, 2a Molekulární přístup kinetická teorie
Osnova pro předmět Fyzikální chemie II magisterský kurz Časový a obsahový program přednášek Týden Obsahová náplň přednášky Pozn. Stavové chování tekutin 1,2a 1, 2a Molekulární přístup kinetická teorie
VI. Nestacionární vedení tepla
 VI. Nestacionární vedení tepla Nestacionární vedení tepla stagnantním prostředím, tj. tělesy a kapalinou, ve které se neprojevuje přirozená konvekce. F. K. rovnice " ρ c p = q + Q! = λ + Q! ( g) 2 ( g)
VI. Nestacionární vedení tepla Nestacionární vedení tepla stagnantním prostředím, tj. tělesy a kapalinou, ve které se neprojevuje přirozená konvekce. F. K. rovnice " ρ c p = q + Q! = λ + Q! ( g) 2 ( g)
5.7 Vlhkost vzduchu 5.7.5 Absolutní vlhkost 5.7.6 Poměrná vlhkost 5.7.7 Rosný bod 5.7.8 Složení vzduchu 5.7.9 Měření vlhkosti vzduchu
 Fázové přechody 5.6.5 Fáze Fázové rozhraní 5.6.6 Gibbsovo pravidlo fází 5.6.7 Fázový přechod Fázový přechod prvního druhu Fázový přechod druhého druhu 5.6.7.1 Clausiova-Clapeyronova rovnice 5.6.8 Skupenství
Fázové přechody 5.6.5 Fáze Fázové rozhraní 5.6.6 Gibbsovo pravidlo fází 5.6.7 Fázový přechod Fázový přechod prvního druhu Fázový přechod druhého druhu 5.6.7.1 Clausiova-Clapeyronova rovnice 5.6.8 Skupenství
Úloha 3-15 Protisměrné reakce, relaxační kinetika... 5. Úloha 3-18 Protisměrné reakce, relaxační kinetika... 6
 3. SIMULTÁNNÍ REAKCE Úloha 3-1 Protisměrné reakce oboustranně prvého řádu, výpočet přeměny... 2 Úloha 3-2 Protisměrné reakce oboustranně prvého řádu, výpočet času... 2 Úloha 3-3 Protisměrné reakce oboustranně
3. SIMULTÁNNÍ REAKCE Úloha 3-1 Protisměrné reakce oboustranně prvého řádu, výpočet přeměny... 2 Úloha 3-2 Protisměrné reakce oboustranně prvého řádu, výpočet času... 2 Úloha 3-3 Protisměrné reakce oboustranně
T0 Teplo a jeho měření
 Teplo a jeho měření 1 Teplo 2 Kalorimetrie Kalorimetr 3 Tepelná kapacita 3.1 Měrná tepelná kapacita Měrná tepelná kapacita při stálém objemu a stálém tlaku Poměr měrných tepelných kapacit 3.2 Molární tepelná
Teplo a jeho měření 1 Teplo 2 Kalorimetrie Kalorimetr 3 Tepelná kapacita 3.1 Měrná tepelná kapacita Měrná tepelná kapacita při stálém objemu a stálém tlaku Poměr měrných tepelných kapacit 3.2 Molární tepelná
2 Tokové chování polymerních tavenin reologické modely
 2 Tokové chování polymerních tavenin reologické modely 2.1 Reologie jako vědní obor Polymerní materiály jsou obvykle zpracovávány v roztaveném stavu, proto se budeme v prvé řadě zabývat jejich tokovým
2 Tokové chování polymerních tavenin reologické modely 2.1 Reologie jako vědní obor Polymerní materiály jsou obvykle zpracovávány v roztaveném stavu, proto se budeme v prvé řadě zabývat jejich tokovým
h nadmořská výška [m]
![h nadmořská výška [m] h nadmořská výška [m]](/thumbs/92/109475205.jpg) Katedra prostředí staveb a TZB KLIMATIZACE, VĚTRÁNÍ Cvičení pro navazující magisterské studium studijního oboru Prostředí staveb Cvičení č. 1 Zpracoval: Ing. Zdeněk GALDA Nové výukové moduly vznikly za
Katedra prostředí staveb a TZB KLIMATIZACE, VĚTRÁNÍ Cvičení pro navazující magisterské studium studijního oboru Prostředí staveb Cvičení č. 1 Zpracoval: Ing. Zdeněk GALDA Nové výukové moduly vznikly za
Chemická vazba. Příčinou nestability atomů a jejich ochoty tvořit vazbu je jejich elektronový obal.
 Chemická vazba Volné atomy v přírodě jen zcela výjimečně (vzácné plyny). Atomy prvků mají snahu se navzájem slučovat a vytvářet molekuly prvků nebo sloučenin. Atomy jsou v molekulách k sobě poutány chemickou
Chemická vazba Volné atomy v přírodě jen zcela výjimečně (vzácné plyny). Atomy prvků mají snahu se navzájem slučovat a vytvářet molekuly prvků nebo sloučenin. Atomy jsou v molekulách k sobě poutány chemickou
Chemická kinetika. Reakce 1. řádu rychlost přímo úměrná koncentraci složky
 Chemická kinetika Chemická kinetika Reakce 0. řádu reakční rychlost nezávisí na čase a probíhá konstantní rychlostí v = k (rychlost se rovná rychlostní konstantě) velmi pomalé reakce (prakticky se nemění
Chemická kinetika Chemická kinetika Reakce 0. řádu reakční rychlost nezávisí na čase a probíhá konstantní rychlostí v = k (rychlost se rovná rychlostní konstantě) velmi pomalé reakce (prakticky se nemění
TERMIKA II. Stacionární vedení s dokonalou i nedokonalou izolací; Obecná rovnice vedení tepla; Přestup a prostup tepla;
 TERMIKA II Šíření tepla vedením, prouděním a zářením; Stacionární vedení s dokonalou i nedokonalou izolací; Nestacionární vedení tepla; Obecná rovnice vedení tepla; Přestup a prostup tepla; 1 Šíření tepla
TERMIKA II Šíření tepla vedením, prouděním a zářením; Stacionární vedení s dokonalou i nedokonalou izolací; Nestacionární vedení tepla; Obecná rovnice vedení tepla; Přestup a prostup tepla; 1 Šíření tepla
3. NEROVNOVÁŽNÉ ELEKTRODOVÉ DĚJE
 3. NEROVNOVÁŽNÉ ELEKTRODOVÉ DĚJE (Elektrochemické články kinetické aspekty) Nerovnovážné elektrodové děje = děje probíhající na elektrodách při průchodu proudu. 3.1. Polarizace Pojem polarizace se používá
3. NEROVNOVÁŽNÉ ELEKTRODOVÉ DĚJE (Elektrochemické články kinetické aspekty) Nerovnovážné elektrodové děje = děje probíhající na elektrodách při průchodu proudu. 3.1. Polarizace Pojem polarizace se používá
9. Struktura a vlastnosti plynů
 9. Struktura a vlastnosti plynů Osnova: 1. Základní pojmy 2. Střední kvadratická rychlost 3. Střední kinetická energie molekuly plynu 4. Stavová rovnice ideálního plynu 5. Jednoduché děje v plynech a)
9. Struktura a vlastnosti plynů Osnova: 1. Základní pojmy 2. Střední kvadratická rychlost 3. Střední kinetická energie molekuly plynu 4. Stavová rovnice ideálního plynu 5. Jednoduché děje v plynech a)
C5250 Chemie životního prostředí II definice pojmů
 C5250 Chemie životního prostředí II definice pojmů Na základě materiálů Ivana Holoubka a Josefa Zemana zpracoval Jiří Kalina. Ekotoxikologie věda studující vlivy chemických, fyzikálních a biologických
C5250 Chemie životního prostředí II definice pojmů Na základě materiálů Ivana Holoubka a Josefa Zemana zpracoval Jiří Kalina. Ekotoxikologie věda studující vlivy chemických, fyzikálních a biologických
Neideální plyny. Z e dr dr dr. Integrace přes hybnosti. Neideální chování
 eideální plyny b H Q(, V, T )... e dp 3... dpdr... dr! h Integrace přes hybnosti QVT (,, ) pmkt! h 3 / e dr dr dr /... U kt... eideální chování p kt r B ( T) r B ( T) r 3 3 Vyšší koeficinety velice složité
eideální plyny b H Q(, V, T )... e dp 3... dpdr... dr! h Integrace přes hybnosti QVT (,, ) pmkt! h 3 / e dr dr dr /... U kt... eideální chování p kt r B ( T) r B ( T) r 3 3 Vyšší koeficinety velice složité
Vodní režim rostlin. Transport vody v xylemu. Kohezní teorie. Transport půda-rostlina-atmosféra. Metody měření. Kavitace
 Vodní režim rostlin Transport vody v xylemu Transport půda-rostlina-atmosféra Kohezní teorie Kavitace Metody měření Longitudinální transport v systému půda-rostlina-atmosféra Hnací síla gradient vodního
Vodní režim rostlin Transport vody v xylemu Transport půda-rostlina-atmosféra Kohezní teorie Kavitace Metody měření Longitudinální transport v systému půda-rostlina-atmosféra Hnací síla gradient vodního
Měření povrchového napětí kapalin a kontaktních úhlů
 2. Přednáška Interakce mezi kapalinou a vlákenným materiálem Měření povrchového napětí kapalin a kontaktních úhlů Eva Kuželová Košťáková KCH, FP, TUL 2019 ADHEZE KAPALIN K PEVNÝM LÁTKÁM Povrchové napětí
2. Přednáška Interakce mezi kapalinou a vlákenným materiálem Měření povrchového napětí kapalin a kontaktních úhlů Eva Kuželová Košťáková KCH, FP, TUL 2019 ADHEZE KAPALIN K PEVNÝM LÁTKÁM Povrchové napětí
ZAKLADY FYZIKALNI CHEMIE HORENí, VÝBUCHU A HAŠENí
 r SDRUŽENí POŽÁRNíHO A BEZPEČNOSTNíHO INžENÝRSTVí. JAROSLAV K,\LOUSEK,.,.,. ZAKLADY FYZIKALNI CHEMIE HORENí, VÝBUCHU A HAŠENí EDICESPBI SPEKTRUM OBSAH. strana 1. FyzikálnÍ chemie v požární ochranč a bezpečnosti
r SDRUŽENí POŽÁRNíHO A BEZPEČNOSTNíHO INžENÝRSTVí. JAROSLAV K,\LOUSEK,.,.,. ZAKLADY FYZIKALNI CHEMIE HORENí, VÝBUCHU A HAŠENí EDICESPBI SPEKTRUM OBSAH. strana 1. FyzikálnÍ chemie v požární ochranč a bezpečnosti
III. STRUKTURA A VLASTNOSTI PLYNŮ
 III. STRUKTURA A VLASTNOSTI PLYNŮ 3.1 Ideální plyn a) ideální plyn model, předpoklady: 1. rozměry molekul malé (ve srovnání se střední vzdáleností molekul). molekuly na sebe navzálem silově nepůsobí (mimo
III. STRUKTURA A VLASTNOSTI PLYNŮ 3.1 Ideální plyn a) ideální plyn model, předpoklady: 1. rozměry molekul malé (ve srovnání se střední vzdáleností molekul). molekuly na sebe navzálem silově nepůsobí (mimo
