METODIKA IDENTIFIKACE PŮVODCŮ FUZARIÓZ KLASU POMOCÍ PCR
|
|
|
- Břetislav Mašek
- před 7 lety
- Počet zobrazení:
Transkript
1 METODIKA IDENTIFIKACE PŮVODCŮ FUZARIÓZ KLASU POMOCÍ PCR Taťána Sumíková, Ludmila Gabrielová-Slezáková, Martin Žabka Výzkumný ústav rostlinné výroby v.v.i. 2009
2 Dedikace Metodika byla financována z projektu QG50076 a výzkumného záměru MZe České republiky Udrţitelné systémy pěstování zemědělských plodin pro produkci kvalitních a bezpečných potravin, krmiv a surovin. Metodika prošla oponentním řízením a získala osvědčení o uznání uplatněné certifikované metodiky vydané Státní rostlinolékařskou správou pod číslem Č.j. SRS /2009 dne O uplatnění metodiky byla uzavřena smlouva s Českou zemědělskou univerzitou v Praze. Oponenti: Mgr. Pavel Matušinský, Ph.D., Zemědělský výzkumný ústav Kroměříţ s.r.o. Mgr. Hana Orságová, Státní rostlinolékařská správa Olomouc Výzkumný ústav rostlinné výroby, v.v.i., Praha, 2009 ISBN:
3 I. Cíl metodiky Cílem navrhované metodiky je uvedení kompletních protokolů k detekci následujících druhů rodu Fusarium F. avenaceum, F. culmorum, F. poae, F. graminearum, F. pseudograminearum, F. sporotrichioides pomocí multiplex PCR. Sekvence pouţitých druhově specifických primerů jsou převzaté z literatury a byly vybrány tak, aby bylo moţné je vzájemně a libovolně kombinovat, coţ umoţňuje detekci jednoho nebo aţ všech šesti výše uvedených druhů v jedné PCR reakci. Reakce jsou optimalizovány pro pouţití v běţné laboratoři molekulární biologie. V metodice je nově zavedena technika pěstování mikromycet ve formě povrchových kultur na celofánu. Tato technika je speciálně určena pro následnou izolaci DNA z houbového mycelia. Technika pěstování povrchových kultur na celofánu umoţňuje optimální manipulaci s napěstovaným myceliem, které se z celofánu snadno odstraní pomocí skalpelu, přičemţ nedochází k neţádoucí kontaminaci vzorku agarovým kultivačním médiem nebo nečistotami z přirozeného substrátu (z napadeného vzorku). II. Vlastní popis metodiky Úvod Onemocnění obilnin, označované jako fuzariózy klasu, způsobené komplexem druhů rodu Fusarium je rozšířené v celé Evropě (Bottalico et Perrone, 2002). Fuzarióza klasu (Fusarium head blight, scab) se projevuje předčasným odumřením klasů nebo jejich zbělením. Hlavními hostiteli jsou pšenice, ječmen a kukuřice. Toto onemocnění je zvláště významné ve vlhkých oblastech. V takových případech můţe dojít k význačným ztrátám na výnosech způsobených sterilitou klásků a nedostatečně vyvinutými obilkami. Je známo přinejmenším 17 druhů tohoto rodu, které se podílejí na vzniku fuzarióz, ale mezi nejčastější a nejvýznamnější patří následující druhy: F. graminearum, F. culmorum, F. avenaceum, F. poae a Microdochium nivale var. nivale a var. majus. V menší míře se vyskytují další druhy rodu Fusarium např. F. tricinctum, F. equiseti, F. acuminatum, F. sambucinum a F. oxysporum (Ioos et al., 2004). F. graminearum je hlavním původcem fuzarióz klasu zejména v teplejších a sušších oblastech, zatímco F. culmorum je dominantní v oblastech chladnějších a vlhčích (Parry et al., 1995). Na území České republiky začíná převaţovat F. graminearum oproti minulým letům, kdy bylo dominantním druhem F. culmorum (Chrpová et al. 2004, Ostrý et al. 2004). Poslední studie ukazují zvyšující se zastoupení druhu F. poae (Remešová et al. 2006). Jedná se o fakultativní nespecifické parazity, kteří také mohou infikovat další části rostlin (Parry et al., 1995, Petrowski et al., 2003, Lemmmens et al., 2004). Poškození klasů tedy můţe být doprovázeno infekcí kořenů, listů nebo následným napadením klíčních rostlin. Nároky těchto patogenů na výţivu nejsou specifické, jedná se o všudypřítomné saprofyty. Limitujícím faktorem pro přechod do parazitické fáze je obvykle vlhkost. Škodlivost fuzarióz spočívá jednak v redukci výnosu, která můţe dosáhnout aţ 70%, ale zejména ve schopnosti mnoha původců fuzarióz produkovat mykotoxiny (Bai et Shaner, 1994). Je známo, ţe fuzáriové mykotoxiny mohou způsobovat váţné zdravotní potíţe jak u člověka, tak u hospodářských zvířat. Následně dochází k projevům chronické nebo akutní mykotoxikózy, např. trávicí potíţe, poruchy plodnosti (Ţabka et Jegorov, 2002). Nejvýznamnější fuzáriové mykotoxiny jsou trichoteceny, zejména deoxynivalenol a nivalenol a zearalenony. Ke tvorbě zdraví škodlivých toxinů v zrnu dochází zejména při infekci druhy F. graminearum a F. culmorum.
4 Přesná detekce jednotlivých původců fuzarióz klasu a zejména stanovení toxinogenních kmenů je nezbytná jak pro pochopení faktorů podílejících se na rozvoji onemocnění a akumulaci toxinů, tak z hlediska ochrany rostlin i zdraví konzumentů. Mykologické určení jednotlivých druhů je dosti obtíţné a relativně časově náročné, proto došlo v poslední době k rozvoji metod zaloţených na PCR reakci. V současnosti jsou známy druhově specifické primery pro mnoho druhů rodu Fusarium např. pro F. avenaceum (Doohan et al., 1998, Turner et al., 1998), F. culmorum a F. graminearum (Nicholson et al.,1998), F. poae (Parry et Nicholson, 1996), F. pseudograminearum (Aoki et O Donnell, 1999) a F. sporotrichioides (Demeke et al., 2004). Efektivnější metodou je pouţití tzv. multiplex PCR tj. PCR reakce, která díky přítomnosti několika primerových párů umoţňuje detekci více druhů současně. Rutinně je moţné detekovat současně 2 14 lokusů. Nutností ovšem je zajistit, aby se amplifikované produkty dostatečně lišily ve svých délkách a bylo je tak moţno bez problémů rozlišit na agarózovém gelu. Neméně důleţitým předpokladem k úspěšnému pouţití multiplex PCR je pečlivá optimalizace reakčních podmínek, zejména zajištění vhodné annealingové teploty a koncentrace jednotlivých primerů. Problémem mohou být také nespecifické produkty, které se amplifikují společně s poţadovanými fragmenty a mohou zkreslovat výsledek reakce. Nicméně při vhodné optimalizaci dochází ke znatelné úspoře času i materiálu. Podstata metodiky Metodika popisuje inovativní přístup pro rychlou a efektivní detekci následujících patogenních druhů rodu Fusarium: F. avenaceum, F. culmorum, F. poae, F. graminearum, F. pseudograminearum a F. sporotrichioides. Jedná se o spojení nového přístupu PCR detekce a nové techniky pěstování mikromycet, speciálně určené pro následnou izolaci houbové DNA. Napadené klasy nebo zrna se omyjí ponořením do 3-5% roztoku NaClO na 2-3 minuty. Tím je vzorek zbaven povrchových nečistot a sekundárních kontaminací, které by mohly být problematické při dalším zpracování vzorků a samotné detekci. Takto připravené vzorky se posléze promyjí ve sterilní destilované vodě za účelem získání suspenze spór či myceliárních fragmentů. Takto získaná suspenze se následně jednoduše rozetře po povrchu připraveného celofánu překrývajícího agarovou ţivnou půdu na Petriho misce. Pomocí skalpelu se narostlé mycelium odebere do plastových 2ml mikrozkumavek (3 kaţdý vzorek), které se vloţí do tekutého dusíku, aby došlo k okamţitému zmraţení. Vzorky se uchovávají v hlubokomrazícím boxu při teplotě -80 C. DNA se z buněk houbového mycelia extrahuje mechanickým rozrušením pletiv a následnou separací od ostatních sloţek, zejména od proteinů, polysacharidů a barviv. Působením cetrimoniumbromidu (CTAB) dochází za přítomnosti chloridu sodného k vytvoření ve vodě rozpustného komplexu CTAB-DNA. Ten se od proteinů a sacharidů oddělí působením směsi chloroformu a isoamylalkoholu a je vyvázán do vodné fáze. DNA se poté z vodné fáze vysráţí pomocí absolutního etanolu a zbytky chloridu sodného a CTAB jsou odstraněny 70% roztokem etanolu. Peletky DNA se rozpustí v pufru TE, tj. velmi zředěném roztoku Tris (trishydroxymethyl) aminomethan a EDTA (kyselina ethylendiamintetraoctová). Tris upravuje ph roztoku a EDTA působí jako chelační činidlo a vyvazuje Mg 2+ ionty, a tím inhibuje činnost nukleáz, enzymů štěpících DNA. Přibliţná koncentrace izolované DNA se stanoví pomocí fluorescence pod UV lampou na agarózovém gelu s ethidiumbromidem, který se váţe na DNA. Fluorescence vyvolaná UV zářením působícím na vázaný ethidiumbromid je úměrná mnoţství DNA. Míra fluorescence
5 vzorku DNA se porovnává s fluorescencí fragmentů o známé koncentraci u markeru Lambda DNA/HindIII. Principem reakce PCR je amplifikace úseku DNA s párem druhově specifických primerů (forward a revers). Nejprve dochází vlivem vysoké teploty k denaturaci dvoušroubovice DNA, poté se podle principu komplementarity na příslušné sekvence DNA naváţou primery. Výsledkem reakce je mnohonásobné zmnoţení úseku DNA označeném na obou koncích pouţitými primery. Produkt PCR reakce se detekuje na agarózovém gelu pod UV lampou po obarvení ethidiumbromidem, který se přidává do gelu při jeho přípravě. V případě multiplex PCR jsou do reakční směsi přidány druhově specifické primery pro více druhů a to umoţňuje detekci několika druhů současně. V případě negativního výsledku PCR pro všechny testované (výše uvedené) druhy, metodika nabízí moţnost klasického postupu detekce na základě morfologických znaků včetně doporučené určovací literatury. Technické vybavení pro mykologickou práci a přípravu vzorků: Petriho misky (skleněné, plastové) celofánová fólie (kruhové výřezy 9 cm v průměru) očkovací mikrobiologické kličky kahan sterilní očkovací box laboratorní sklo (na oplach vzorků a tvorbu suspenze) kultivační termostat (optimum 23 C) binokulární lupa, světelný mikroskop (Olympus BX 51) Chemikálie potřebné pro mykologickou práci a přípravu vzorků: 3-5% vodný roztok NaClO sterilní destilovaná voda agarová kultivační a determinační média (Oxoid, Hi-media nebo vlastní výroba podle uvedené literatury): Bramboro-dextrózový agar - PDA (Booth 1971): brambory 200g dextróza 15g agar 20g destilovaná voda 1000ml Ovesný agar - OA (Samson et al. 1996): ovesné vločky 30g agar 15g destilovaná voda 1000ml Speciální ţivný agar - SNA (Nirenberg 1976): KH 2 PO 4 1g KNO 3 1g MgSO 4. 7 H 2 O 0,5g KCl 0,5g glukóza 0,2g sacharóza 0,2g
6 agar destilovaná voda 20g 1000ml Vybavení nutné pro uchování odebraného mycelia a následnou izolaci DNA: hlubokomrazící box -80 C tekutý dusík homogenizátor QIAGEN a karbidové kuličky centrifuga s otáčkami min otáček/min. s rotorem na plastové mikrozkumavky o objemu 2ml vodní lázeň nebo teplotní blok vortex vybavení na horizontální elektroforézu transluminátor fotodokumentační zařízení automatické pipety a špičky 2 ml plastové mikrozkumavky (Eppendorf) Roztoky a chemikálie potřebné k izolaci DNA metodou CTAB: Extrakční pufr: 0,35M sorbitol 35ml 1M roztoku 0,1M Tris (Tris[hydroxymethyl] aminomethan) 10ml 1M roztoku Tris ph8 5mM EDTA 1ml 0,5M roztoku EDTA ph8 H 2 O doplnit do 100ml 5% roztok sarkosylu N-lauroyl-sarcosine (Sigma) 5g H 2 O 100ml 2% CTAB (lyzující pufr) CTAB (Sigma Aldrich) 2g do 20ml H 2 O 0,2 M Tris (Serva) 20ml 1M roztoku ph8 50mM EDTA (Serva) 10ml 0,5M roztoku ph8 2M NaCl (Serva) 40ml 5M roztoku H 2 O doplnit do 100ml 5% CTAB CTAB (Sigma Aldrich) 5g CTAB do 20ml H 2 O 0,2 M Tris (Serva) 20ml 1M roztoku ph8 50mM EDTA (Serva) 10ml 0,5M roztoku ph8 2M NaCl (Serva) 40ml 5M roztoku H 2 O doplnit do 100ml TE pufr 10mM Tris (Serva) 1mM EDTA (Serva) H 2 O doplnit do 2,5ml 1M roztoku ph8 0,5ml 0,5M roztoku ph8 250ml 0,8% agarózový gel (cca 50 vzorků) Agaróza (Serva) 0,96g 1 TAE pufr 120ml
7 Ethidiumbromid 10mg/ml roztok (Sigma-Aldrich) 1µl 1 TAE pufr TRIS (Serva) EDTA (Serva) ledová CH 3 COOH (Sigma-Aldrich) H 2 O doplnit do 242g do 300ml H 2 O 100ml 0,5M roztoku ph8 57,1ml 0,5M roztoku 1000ml 5M NaCl Absolutní etanol (Serva) vymraţený na -20 C 70% roztok etanolu (Serva) Směs chloroform (Serva): izoamylalkohol (Lachema Brno) 24:1 RNáza Velikostní standard HindIII (Fermentas), včetně loading buffer Vybavení a chemikálie potřebné k determinaci druhů rodu Fusarium pomocí metody PCR: Druhově specifické primery (syntéza firmou Applera podle sekvencí popsaných v uvedených publikacích) viz tabulka 1. dntp (Invitrogen) Qiagen polymeráza včetně pufru a MgCl 2 H 2 O (Sigma Aldrich) Velikostní standard 100bp DNA Ladder (Fermentas), včetně loading buffer PCR plastové zkumavky stripy + víčka nebo PCR destičky + víčka Automatické pipety a špičky Termocykler (UNO II, Biometra) Minicentrifuga Vybavení na horizontální elektroforézu Transluminátor Fotodokumentační zařízení 2% Agarózový gel Agaróza (Serva) 2,4g 1 TAE pufr 120ml Ethidiumbromid 10mg/ml roztok (Sigma-Aldrich) 1µl Tabulka 1. Druh r. Fusarium Označení primerů F. avenaceum Fa F. culmorum FC01 F graminearum Fg16 F. poae FP82 F. sporotrichioides AF330109C F. pseudograminearum FP1 Sekvence primerů (5-3 ) Citace CAA GCA TTG TCG CCA CTC TC GTT TGG CTC TAC CGG GAC TG Doohan et al ATG GTG AAC TCG TGG C CCC TTC TTA CGC CAA TCT CG Nicholson et al CTC CGG ATA TGT TGC GTC AA GGT AGG TAT CCG ACA TGG CAA Nicholson et al CAA GCA AAC AGG CTC TTC ACC Parry et Nicholson TGT TCC ACC TCA GTG ACA GGT T 1996 AAA AGC CCA AAT TGC TGA TG TGG CAT GTT CAT TGT CAC CT Demeke et al CGG GGT AGT TTC ACA TTT CYG Aoki et O Donnell GAG AAT GTG ATG ASG ACA ATA 1999
8 Postup 1. Očištění a příprava vzorku Napadené vzorky se nejprve povrchově očistí ponořením do 3-5% roztoku NaClO. V tomto roztoku se vzorek mírně promíchává po dobu 2-3 minut. Poté se vzorek vyjme a opláchne ve sterilní destilované vodě pro odstranění zbytků roztoku. Tento krok slouţí k odstranění povrchových nečistot. 2. Příprava inokulační suspenze patogena (nebo směsi patogenů) Omytý vzorek se vloţí do sterilní zkumavky, sterilní plastové mikrozkumavky nebo sterilní baňky (dle rozměrů vzorku) se sterilní destilovanou vodou. Celkový objem sterilní destilované vody je závislý na konkrétním vzorku, jeho velikosti a stupni napadení. Pro přípravu očkovací suspenze z malých vzorků (napadené zrno v mikrozkumavce, zkumavce) je optimální pouţití vortexu. Na větší vzorky (napadené klasy v baňce) je vhodné pouţít laboratorní třepačku. Vzorek se 1-3 minuty vortexuje (dle stupně napadení). V případě třepání větších vzorků v baňkách na třepačce se doporučuje třepat minut (dle stupně napadení). 3. Příprava sterilního celofánu Kruhové celofánové výseče (9 cm, dle velikosti Petriho misky) je nejlépe samostatně umístit do skleněných Petriho misek. Pro lepší sterilizaci a pozdější manipulaci při kladení na povrch agaru se celofán zalije nejlépe pomocí střičky destilovanou vodou a to tak, aby došlo k celkovému pokrytí celofánové výseče. Skleněné misky s celofánem se následně vloţí to autoklávu. Sterilní celofán se připraví sterilizací v autoklávu při teplotě 120 C po dobu 20 minut. Po sterilizaci a vychladnutí je celofán připraven pro aplikaci na povrch agaru. 4. Příprava Petriho misek s celofánovou fólií Petriho misky se po nalití kultivačního média (PDA) nechají pozvolna vychladnout. Na povrch ztuhlého kultivačního média se ve sterilních podmínkách (sterilní očkovna, očkovací box) poloţí vysterilizované kruhové výseče celofánové folie pomocí sterilní pinzety. Po přilnutí celofánu na povrch kultivačního media je miska připravena na následnou inokulaci. Obr. 1 Obr. 2 Obr. 3 Obr. 1: Petriho miska s vysterilizovaným celofánem Obr. 2: Vloţení celofánové folie na PDA mediu Obr. 3: Petriho miska s kultivačním médiem a celofánovou fólií připravená k inokulaci 5. Inokulace Petriho misek a kultivace Získaná inokulační suspenze ze vzorku se rozetře očkovací kličkou po povrchu připravených Petriho misek s PDA překrytým celofánovou folií a vloţí do termostatu. Kultivace probíhá po dobu 4 7 dní při teplotě 23 C. Optimální objem rozetřené suspenze se pohybuje v rozmezí μl na povrch Petriho misky.
9 Obr. 4 Obr. 5 Obr. 6 Obr. 7 Obr. 4: Příprava očkovací suspenze z malého vzorku Obr. 5: Příprava očkovací suspenze z větších vzorků Obr. 6: Inokulace suspenze na celofánový povrch Obr. 7: Naočkovaný celofán po 7 dnech kultivace 6. Získání mycelia pro extrakci DNA Narostlé mycelium na celofánové folii se seškrábne pomocí sterilního skalpelu nebo sterilní kličky a vloţí se do 2ml mikrozkumavky (mnoţství odebíraného mycelia přibliţně 1 2 cm, viz obr. 8 11). Pokud nenásleduje bezprostřední extrakce DNA, mikrozkumavky s myceliem se vloţí do tekutého dusíku a posléze se uchovávají v hlubokomrazícím boxu při teplotě -80 C. Obr. 8 Obr. 9 Obr. 10 Obr. 11 Obr. 8 11: Seškrábnutí narostlého mycelia do plastových mikrozkumavek 7. Extrakce DNA Do 2ml mikrozkumavek s myceliem se přidá 400µl extrakčního pufru (jedná-li se o zamraţené vzorky je potřeba postupovat rychle, aby nedošlo k rozmrznutí mycelia). Do kaţdé zkumavky se vloţí jedna karbidová kulička a vzorky se nechají třepat v homogenizátoru po dobu 2 minut při frekvenci 30Hz. Poté se vzorky promíchají na vortexu, přidá se k nim 400µl 2% CTAB a 200µl 5% roztoku sarkosylu. Opět se vortexují a nechají inkubovat ve vodní lázni při teplotě 60 C po dobu 30 minut. Poté je směs ochlazena na laboratorní teplotu. Ke směsi se přidá 1 objem chloroform:isoamylalkohol (v poměru 24:1). Po 10 minutách třepání v ruce jsou vzorky centrifugovány při maximálních otáčkách dalších 10 minut. Vodná fáze se po dokončení centrifugace odebere do nové mikrozkumavky. Ke vzorkům se přidá 400µl 5M roztoku NaCl a 100µl 5% roztoku CTAB, který musí být předehřátý na 60 C a nechají se inkubovat 10 minut při laboratorní teplotě. Po inkubaci se opět přidá 1 objem chloroform:isoamylalkohol a po 10 minutách třepání v ruce se vzorky centrifugují při maximálních otáčkách 10 minut. Vodná fáze se odebere a celý krok se ještě jednou zopakuje. K získanému roztoku se přidá 1ml vymraţeného absolutního etanolu a po lehkém promíchání se vzorky inkubují v lednici při 4 C po dobu minut. Po inkubaci se vzorky centrifugují při maximálních otáčkách po dobu 7 minut. Supernatant se odstraní
10 a k peletce DNA se přidá 500µl 70% etanolu a takto připravené vzorky jsou inkubovány v lednici alespoň 1 hodinu při teplotě +4 C. Poté se vzorky opět centrifugují při maximálních otáčkách po dobu 5 minut, supernatant se odstraní a znovu se přidá 500µl 70% etanolu. Opět následuje inkubace minut při teplotě 4 C. Po další centrifugaci při maximálních otáčkách po dobu 5 minut je odstraněn supernatant a zbytky etanolu se vysuší pomocí vakuové odparky (dokud peletka DNA neskáče při poklepu na uzavřenou ependorfku). DNA se nechá rozpustit v odpovídajícím mnoţství TE pufru ( µl) při teplotě +4 C, nejlépe přes noc. K roztoku DNA se přidá 20µl roztoku RNázy (20mg/ml) a vzorky se inkubují po dobu 10 minut při teplotě 37 C. Kvalita a koncentrace DNA se ověřuje na 0,8% agarózovém gelu. K 1µl DNA se přidá 8µl H 2 O a 2µl loading pufru. Směs se nanese na gel a po minut elektroforézy je DNA vizualizovaná ethidiumbromidem pod UV lampou. Koncentrace DNA se odhaduje srovnáním s velikostním standardem Hind III (6µl). Vzorky se naředí na pracovní koncentraci 50ng/µl. 8. Determinace druhů rodu Fusarium na základě DNA markerů pomocí metody PCR Do PCR zkumavek nebo destiček je napipetována reakční směs. Nejprve se připraví mastermix do zvláštní zkumavky, rozpipetuje se do jednotlivých PCR zkumavek nebo destiček a nakonec se přidá 1µl roztoku DNA o koncentraci 50ng/µl. Reakční směs druhově specifická PCR k detekci jednotlivých druhů: Primer mix forward a revers primer (5µM) 1,5µl dntp (2,5mM) 2µl pufr Qiagen (10 ) 2,5µl MgCl 2 (15mM) 1,5µl Taq polymeráza Qiagen (5U/1µl) 0,2µl H 2 O 16,3µl Templátová DNA 1µl Celkový reakční objem 25µl Reakční směs druhově specifická multiplex PCR k detekci dvou - šesti druhů r. Fusarium současně: Primer mix forward a revers primer (5µM) pro kaţdý 1,5µl* / 1µl** detekovaný druh dntp (2,5mM) 2µl pufr Qiagen (10 ) 2,5µl MgCl 2 (15mM) 1,5µl Taq polymeráza Qiagen (5U/1µl) 0,2µl H 2 O Doplnit do 24µl Templátová DNA 1µl Celkový reakční objem 25µl * mnoţství primerů pro druhy: F. avenaceum, F. culmorum, F. pseudograminearum, F. sporotrichioides ** mnoţství primerů pro druhy: F. poae, F. graminearum Reakce probíhá v termocykleru v následujících reakčních podmínkách: 1 cyklus: 95 C 5 min.
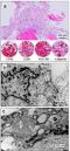
11 35 cyklů: 95 C 30 s. 60 C 30 s. 72 C 40 s. Konečná extense: 72 C 5 min. 10 C 24 h. Velikost produktů PCR reakce pro jednotlivé druhy rodu Fusarium je uvedena na obr. 12. K produktům PCR se přidá 3µl nanášecího pufru (loading buffer) a po promíchání se nanese 12µl směsi na 2% agarózový gel spolu s 6µl délkovým standardem 100bp DNA Ladder (Fermentas). Separace probíhá elektroforézou cca 1,5 hodiny při 50V (delší čas je vhodnější při multiplex PCR, aby došlo k dobrému rozlišení všech produktů). Vizualizace a detekce se provádí pod UV lampou po přidání ethidiumbromidu. Přítomnost produktu amplifikace poţadované délky značí příslušnost k testovanému druhu. Druhová specifita pouţitých primerů byla vybrána na základě publikovaných výsledků výše uvedených autorů (tab. 1) a jejich spolehlivost a specifita byla ověřena na mykologicky určených druzích rodu Fusarium, které lze v našich podmínkách povaţovat za nejčastější původce fuzarióz klasu pšenice tj. F. avenaceum, F. acuminatum, F. culmorum, F. graminearum, F. equiseti, F. poae, F. pseudograminearum a F. sporotrichioides. Obr. 12 Obr. 12: Multiplex PCR 100bp DNA ladder, 1 F. avenaceum, 2 F. culmorum, 3 F. graminearum, 4 F. poae, 5 F. pseudograminearum, 6 F. sporotrichioides, 7 voda 9. Determinace klasickými mykologickými metodami v případě negativního výsledku PCR V případě negativního výsledku PCR se všemi uvedenými druhově specifickými primery se doporučuje k determinaci pouţít tradiční mykologické metody pomocí morfologických znaků (viz literatura pro morfologické určování druhů rodu Fusarium). Pro klasickou mykologickou druhovou determinaci fuzárií je vhodné napěstovat houby na ovesném agaru (OA) nebo bramboro-dextrozovém agaru (PDA) pro pozorování makroskopických znaků kolonií a např. na speciálně ţivném agaru (SNA) pro pozorování mikroskopických znaků. Doporučené kultivační podmínky jsou 24 C a střídání tzv. black light a tmy ve 12 hodinových intervalech. Z makroskopických znaků se hodnotí růstová rychlost kolonie, zbarvení kolonie a zbarvení spodní strany kolonie. Z mikroskopických znaků se hodnotí tvar a velikost konidií a fialid (monofialidy, polyfialidy). U mikrokonidií je důleţitý tvar (kulatý, citronkovitý, oválný, hruškovitý, s papilou), velikost a způsob jejich tvorby v řetízcích nebo ve shlucích. U makrokonidií je důleţitý tvar konidií (vřetenovitý, rovný, silně zakřivený) velikost konidií a tvar apikální a bazální buňky. Dalším znakem je výskyt chlamydospor.
12 III. Srovnání novosti postupů Předloţená metodika shrnuje kompletní protokoly s publikovanými druhově specifickými primery, umoţňující spolehlivou detekci vybraných druhů rodu Fusarium v multiplex PCR reakci. Přestoţe z literatury jsou známy sekvence k detekci mnohých druhů rodu Fusarium, problémem některých publikovaných metod můţe být ne vţdy spolehlivé rozlišení jednotlivých druhů nebo nutnost zdlouhavé optimalizace reakce pro podmínky konkrétní laboratoře. Rovněţ jsou v literatuře známy multiplex PCR reakce k detekci druhů rodu Fusarium, ţádná z prací však nepopisuje současnou detekci následujících druhů: F. avenaceum, F. culmorum, F. poae, F. graminearum, F. pseudograminearum, F. sporotrichioides s různými moţnostmi vzájemné kombinace druhově specifických primerů, coţ umoţňuje detekci 2 aţ 6 druhů, podle vlastního výběru. Metodika dále novým přístupem kultivace hub na celofánech vede k vyšší efektivitě a úspěšnosti detekce. Díky permeabilitě celofánového podkladu můţe houbové mycelium přirozeně růst a čerpat ţiviny z ţivné půdy. Výsledkem je tudíţ přirozeně čistě a rychle napěstované mycelium, prakticky bez kontaktu s agarovým ţivným médiem. Jiţ ve fázi samotné přípravy vzorků, dochází ke zjednodušení manipulace s myceliem. Oproti klasickému způsobu kultivace přímo na agarovém kultivačním médiu odpadá nesnadné a zdlouhavé oddělování houbového mycelia od kultivačního média a především pravděpodobnost kontaminace vzorku ţivným médiem je při správném dodrţení postupu minimální. Houbové mycelium je jednoduchým způsobem lehce oddělitelné od celofánového podkladu a můţe být přímo přeneseno do mikrozkumavek. IV. Popis uplatnění certifikované metodiky Metodika je určená pro studenty České zemědělské univerzity, případně dalších univerzit, zabývajících se studiem mikromycet rodu Fusarium. Jsou zde uvedeny podrobné pracovní protokoly umoţňující detekci šesti druhů rodu Fusarium pomocí multiplex PCR reakce v běţné laboratoři molekulární biologie včetně jejich kultivace. V. Seznam pouţité literatury Aoki T., O Donnell K. (1999): Morphological and molecular characterization of Fusarium pseudograminearum sp nov., formerly recognized as the Group 1 population of F. graminearum. Mycologia 91: Bai G., Shaner G. (1994): Scab of wheat: Prospect of control. Plant disease 78: Bottalico A., Perrone G. (2002): Toxigenic Fusarium species and mycotoxins associated with head blight in small-grain cereals in Europe. European Journal of Plant Pathology 108: Demeke T., Clear R. M., Patrick S. K., Gaba D. (2005): Species-specific PCR-based assays for the detection of Fusarium species and comparison with whole seed agar plate method and trichothecene analysis. International Journal of Food Microbiology 103: Doohan F. M., Parry D. W., Jenkinson P., Nicholson P. (1998): The use of species-specific PCR-based assays to analyze Fusarium ear blight of wheat. Plant Pathology 47: Chrpová J., Šíp V., Sýkorová S., Sychrová E., Matějová E. (2004): Beitrag zur Problematic der Ährenfusariosen bei Getreide. Journal of Applied Botany and Food Quality 78: Ioos R., Belhadj A., Menez M. (2004): Occurrence and distribution of Microdochium nivale and Fusarium species isolated from barley, durum and soft wheat grains in France from 2000 to Mycopathologia 158:
13 Lemmens M., Buerstmayr H., Krska R., Schuhmacher R., Grausgruber H., Ruckenbauer P. (2004): The effect of inoculation treatment and long-term application of moisture on Fusarium head blight symptoms and deoxynivalenol contamination in wheat grains. European Journal of Plant Pathology 110: Nicholson P., Simpson D. R., Weston G., Rezanoor H. N., Lees A. K., Parry D. W., Joyce D. (1998): Detection and quantification of Fusarium culmorum and Fusarium graminearum in cereals using PCR assay. Physiological and Molecular Plant Pathology 53, p Ostrý V., Škarková J., Malíř F., Sýkorová S. (2004): Advances on the Occurence of Toxigenic Fungi and Mycotoxins in the Czech Republic, In: An Overview on Toxigenic Fungi and Mycotoxins in Europe, Logrieco, Antonie, Visconti, Angelo (Eds.) Kluwer 2004, ISBN: Parry D. W., Jenkinson P., Mc. Leod L. (1995): Fusarium ear blight (scab) in small-grain cereals - a review. Plant Pathology 44: Parry D. W., Nicholson P. (1996): Development of a PCR assay to detect Fusarium poae in wheat. Plant Pathology 45, p Petrowski J., Kiecana I., Kaczmarek Z. (2003): Natural occurrence and distribution of Fusarium toxins in contaminated cultivars. European Journal of Plant Pathology 109: Remešová J., Sumíková T., Sychrová E., Matějová E., Chrpová J., Šíp V. (2006): Toxigenic micromycetes of genus Fusarium on wheat isolated in the Czech Republic. In: Sborník abstraktů "XVII. česká a slovenská konference o ochraně rostlin", září 2006, ČZU Praha Turner A. S., Lees A. K., Rezanoor H. N., Nicholson P. (1998): Refinement of PCR-based detection of Fusarium avenaceum and evidence for phenetic relatedness to Fusarium tricinctum. Plant Pathology 47: Ţabka M., Jegorov A. (2002): Comeback of the fungus that gave name to trichothecenes. Chemické listy 96: Literatura pro morfologické určování druhů rodu Fusarium: Booth, C. (1971): The genus Fusarium. 237 p., Kew. Brayford, D. (1993): The identification of Fusarium species. Egham, 118 p. Burgess, L. W., Liddell, C. M., Summerell, B. A. (1988): Laboratory manual for Fusarium research. Sydney, 156 p. Domsch, K. H., Gams, W., Anderson, T. H. (1980): Compendium of soil fungi. Vol p., London etc. Gerlach, W., Nirenberg, H. (1982): The genus Fusarium a pictorial atlas. Berlin & Hamburg, 406p. Leslie, J. F., Summerell, B. A. (2006): The Fusarium Laboratory manual. 388 p., Iowa. Nirenberg, I. H. (1976): Untersuchungen über die morphologische und biologische Differenzierung in der Fusarium Sektion Liseola. Mitt. Biol. Bundesanst. f. Land- u. Forstw. Berlin Dahlem 169: Samson, R. A., Hoekstra, E. S., Frisvad, J. C., Filtenborg, O. (1996). Introduction to foodborne fungi. Baarn & Delft, 322 p. Seifert, K. (1996): FusKey Fusarium interactive key. [ VI. Seznam publikací, které předcházely metodice Remešová J., Sumíková T., Sychrová E., Matějová E., Chrpová J., Šíp V. (2006): Toxigenic micromycetes of genus Fusarium on wheat isolated in the Czech Republic. Sborník
14 příspěvků z XVII. české a slovenské konference o ochraně rostlin, ISBN Chrpová J., Šíp V., Sýkorová S., Sumíková T., Sychrová E. (2007): Occurrence of Fusarium head blight (FHB) in wheat in the Czech Republic and the possibilities of the disease control. Aktuální poznatky v pěstování, šlechtění a ochraně rostlin. Sborník z konference s mezinárodní účastí konané v Brně ve dnech listopadu 2007, ISBN : Sumíková T., Remešová J., Leišová L., Sychrová E., Chrpová J., Šíp V. (2008): Fusarium species associated with FHB on wheat isolated in the Czech republic and their molecular diversity. European Wheat Aneuploid Co-operative Newsletter, Proceedings of the 14th International EWAC Conference 6-10 May 2007, Istanbul, Turkey Slezakova L., Sumikova T., Kocourek F. (2008): The virulence of Fusarium isolates and their ability of mycotoxin production. Journal of Plant Pathology Vol. 90, Supplement 3.
15 Příloha Fusarium culmorum, OA, 7 dní (2 ukázkové kmeny) Fusarium graminearum, OA, 7 dní (2 ukázkové kmeny)
16 Fusarium avenaceum, OA, 7 dní Fusarium avenaceum, OA, 14 dní Fusarium sporotrichioides, OA, 7 dní (2 ukázkové kmeny)
17 Fusarium pseudograminearum, OA, 14 dní Fusarium poae, OA, 7 dní Fusarium culmorum, makrokonidie, OA, 7 dní Fusarium poae, monofialidy s mikrokonidiemi, OA, 7 dní
18 Symptomy napadení houbami rodu Fusarium na klasech pšenice
19 Autoři: Mgr. Taťána Sumíková Mgr. Ludmila Gabrielová-Slezáková Ing. Martin Ţabka, Ph.D. Výzkumný ústav rostlinné výroby, v.v.i. Drnovská Praha 6 Ruzyně Název: Metodika identifikace původců fuzarióz klasu pomocí PCR Vydal: Výzkumný ústav rostlinné výroby, v.v.i. Drnovská Praha 6 Ruzyně Metodika je veřejně přístupná na adrese Náklad: 200 výtisků Vydáno bez jazykové úpravy. Metodika je poskytována bezplatně. Kontakt na autora: sumikova@vurv.cz Výzkumný ústav rostlinné výroby, v.v.i., Praha, 2009 ISBN:
Metodika detekce hub Penicillium expansum, Monilia fructigena, Botrytis cinerea a Neofabraea alba pomocí multiplex PCR
 Metodika detekce hub Penicillium expansum, Monilia fructigena, Botrytis cinerea a Neofabraea alba pomocí multiplex PCR Taťána Sumíková, Ludmila Gabrielová, Martin Žabka Výzkumný ústav rostlinné výroby
Metodika detekce hub Penicillium expansum, Monilia fructigena, Botrytis cinerea a Neofabraea alba pomocí multiplex PCR Taťána Sumíková, Ludmila Gabrielová, Martin Žabka Výzkumný ústav rostlinné výroby
Fusarium a Cylindrocarpon
 Fusarium a Cylindrocarpon Rod Fusarium (česky srpatka) je charakteristický tvorbou vícebuněčných zakřivených makrokonidií, na rozdíl od příbuzného rodu Cylindrocarpon, který má makrokonidie většinou rovné.
Fusarium a Cylindrocarpon Rod Fusarium (česky srpatka) je charakteristický tvorbou vícebuněčných zakřivených makrokonidií, na rozdíl od příbuzného rodu Cylindrocarpon, který má makrokonidie většinou rovné.
Agrotest fyto, s.r.o. Metodika pro zakládání a hodnocení pokusů s umělou inokulací obilnin fuzáriózami klasů
 Agrotest fyto, s.r.o. Metodika pro zakládání a hodnocení pokusů s umělou inokulací obilnin fuzáriózami klasů Kroměříž 2012 2 Metodika vznikla využitím poskytnuté institucionální podpory na dlouhodobý koncepční
Agrotest fyto, s.r.o. Metodika pro zakládání a hodnocení pokusů s umělou inokulací obilnin fuzáriózami klasů Kroměříž 2012 2 Metodika vznikla využitím poskytnuté institucionální podpory na dlouhodobý koncepční
Ing. Kristýna Bezděková Vliv vybraných faktorů na výskyt patogenů Fusarium spp. v zrnu ječmene
 Ing. Kristýna Bezděková Vliv vybraných faktorů na výskyt patogenů Fusarium spp. v zrnu ječmene 24. května 2013, od 9.00 hod, A34 MENDELU AF (budova A) Akce je realizována vrámci klíčové aktivity 02 Interdisciplinární
Ing. Kristýna Bezděková Vliv vybraných faktorů na výskyt patogenů Fusarium spp. v zrnu ječmene 24. května 2013, od 9.00 hod, A34 MENDELU AF (budova A) Akce je realizována vrámci klíčové aktivity 02 Interdisciplinární
Polymerázová řetězová reakce
 Polymerázová řetězová reakce doc. RNDr. Milan Bartoš, Ph.D. bartosm@vfu.cz Přírodovědecká fakulta MU, 2013 Obsah přednášky 1) Co je to PCR, princip, jednotlivé kroky 2) Technické provedení PCR 3) Fyzikální
Polymerázová řetězová reakce doc. RNDr. Milan Bartoš, Ph.D. bartosm@vfu.cz Přírodovědecká fakulta MU, 2013 Obsah přednášky 1) Co je to PCR, princip, jednotlivé kroky 2) Technické provedení PCR 3) Fyzikální
Kvantitativní detekce houbových patogenů v rostlinných pletivech s využitím metod molekulární biologie
 Kvantitativní detekce houbových patogenů v rostlinných pletivech s využitím metod molekulární biologie Leona Leišová Přírodovědecká fakulta UK, Praha 2009 Metody kvantifikace: Nepřímé metody odhad míry
Kvantitativní detekce houbových patogenů v rostlinných pletivech s využitím metod molekulární biologie Leona Leišová Přírodovědecká fakulta UK, Praha 2009 Metody kvantifikace: Nepřímé metody odhad míry
IZOLACE DNA (KIT DNeasy Plant Mini)
 17.1 Izolace DNA (kit DNeasy Plant Mini) Strana 1 IZOLACE DNA (KIT DNeasy Plant Mini) 1 Účel a rozsah Postup slouží k získání deoxyribonukleové kyseliny (DNA) ze vzorku pomocí komerčního kitu DNeasy Plant
17.1 Izolace DNA (kit DNeasy Plant Mini) Strana 1 IZOLACE DNA (KIT DNeasy Plant Mini) 1 Účel a rozsah Postup slouží k získání deoxyribonukleové kyseliny (DNA) ze vzorku pomocí komerčního kitu DNeasy Plant
Jednotné pracovní postupy zkoušení krmiv
 Národní referenční laboratoř Strana KVANTITATIVNÍ STANOVENÍ GENETICKÝCH MODIFIKACÍ METODOU qpcr POMOCÍ ROTOR-GENE PROBE PCR KITU Účel a rozsah Postup slouží ke kvantitativnímu stanovení genetických modifikací
Národní referenční laboratoř Strana KVANTITATIVNÍ STANOVENÍ GENETICKÝCH MODIFIKACÍ METODOU qpcr POMOCÍ ROTOR-GENE PROBE PCR KITU Účel a rozsah Postup slouží ke kvantitativnímu stanovení genetických modifikací
DIAGNOSTICKÝ KIT PRO DETEKCI MINIMÁLNÍ REZIDUÁLNÍ CHOROBY U KOLOREKTÁLNÍHO KARCINOMU
 Úvod IntellMed, s.r.o., Václavské náměstí 820/41, 110 00 Praha 1 DIAGNOSTICKÝ KIT PRO DETEKCI MINIMÁLNÍ REZIDUÁLNÍ CHOROBY U KOLOREKTÁLNÍHO KARCINOMU Jednou z nejvhodnějších metod pro detekci minimální
Úvod IntellMed, s.r.o., Václavské náměstí 820/41, 110 00 Praha 1 DIAGNOSTICKÝ KIT PRO DETEKCI MINIMÁLNÍ REZIDUÁLNÍ CHOROBY U KOLOREKTÁLNÍHO KARCINOMU Jednou z nejvhodnějších metod pro detekci minimální
Kultivační metody stanovení mikroorganismů
 Kultivační metody stanovení mikroorganismů Základní rozdělení půd Syntetická, definovaná media, jednoduché sloučeniny, známé sloţení Komplexní media, vycházejí z ţivočišných nebo rostlinných tkání a pletiv,
Kultivační metody stanovení mikroorganismů Základní rozdělení půd Syntetická, definovaná media, jednoduché sloučeniny, známé sloţení Komplexní media, vycházejí z ţivočišných nebo rostlinných tkání a pletiv,
DETEKCE FUSARIUM LANGSETHIAE MOLEKULÁRNÍMI METODAMI
 JAROSLAV SALAVA, DAVID NOVOTNÝ A IVANA POLIŠENSKÁ DETEKCE FUSARIUM LANGSETHIAE MOLEKULÁRNÍMI METODAMI METODIKA PRO PRAXI Výzkumný ústav rostlinné výroby, v.v.i. 2010 Metodika vznikla za finanční podpory
JAROSLAV SALAVA, DAVID NOVOTNÝ A IVANA POLIŠENSKÁ DETEKCE FUSARIUM LANGSETHIAE MOLEKULÁRNÍMI METODAMI METODIKA PRO PRAXI Výzkumný ústav rostlinné výroby, v.v.i. 2010 Metodika vznikla za finanční podpory
DIAGNOSTICKÝ KIT PRO DETEKCI MINIMÁLNÍ REZIDUÁLNÍ CHOROBY U KARCINOMU PANKREATU
 Úvod IntellMed, s.r.o., Václavské náměstí 820/41, 110 00 Praha 1 DIAGNOSTICKÝ KIT PRO DETEKCI MINIMÁLNÍ REZIDUÁLNÍ CHOROBY U KARCINOMU PANKREATU Jednou z nejvhodnějších metod pro detekci minimální reziduální
Úvod IntellMed, s.r.o., Václavské náměstí 820/41, 110 00 Praha 1 DIAGNOSTICKÝ KIT PRO DETEKCI MINIMÁLNÍ REZIDUÁLNÍ CHOROBY U KARCINOMU PANKREATU Jednou z nejvhodnějších metod pro detekci minimální reziduální
IZOLACE DNA POMOCÍ CTAB PRO STANOVENÍ GMO METODOU PCR
 1253.1 Izolace DNA pomocí CTAB pro stanovení GMO Strana 1 IZOLACE DNA POMOCÍ CTAB PRO STANOVENÍ GMO METODOU PCR 1 Účel a rozsah Postup slouží k získání deoxyribonukleové kyseliny (DNA) ze vzorků krmiv
1253.1 Izolace DNA pomocí CTAB pro stanovení GMO Strana 1 IZOLACE DNA POMOCÍ CTAB PRO STANOVENÍ GMO METODOU PCR 1 Účel a rozsah Postup slouží k získání deoxyribonukleové kyseliny (DNA) ze vzorků krmiv
Izolace genomové DNA ze savčích buněk, stanovení koncentrace DNA pomocí absorpční spektrofotometrie
 Izolace genomové DNA ze savčích buněk, stanovení koncentrace DNA pomocí absorpční spektrofotometrie IZOLACE GENOMOVÉ DNA Deoxyribonukleová kyselina (DNA) představuje základní genetický materiál většiny
Izolace genomové DNA ze savčích buněk, stanovení koncentrace DNA pomocí absorpční spektrofotometrie IZOLACE GENOMOVÉ DNA Deoxyribonukleová kyselina (DNA) představuje základní genetický materiál většiny
Jednotné pracovní postupy zkoušení krmiv STANOVENÍ OBSAHU PROBIOTICKÝCH BAKTERIÍ RODU ENTEROCOCCUS
 Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU PROBIOTICKÝCH BAKTERIÍ RODU ENTEROCOCCUS 1 Rozsah a účel Postup slouží ke stanovení počtu probiotických bakterií v doplňkových látkách, premixech
Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU PROBIOTICKÝCH BAKTERIÍ RODU ENTEROCOCCUS 1 Rozsah a účel Postup slouží ke stanovení počtu probiotických bakterií v doplňkových látkách, premixech
PCR IN DETECTION OF FUNGAL CONTAMINATIONS IN POWDERED PEPPER
 PCR IN DETECTION OF FUNGAL CONTAMINATIONS IN POWDERED PEPPER Trojan V., Hanáček P., Havel L. Department of Plant Biology, Faculty of Agronomy, Mendel University of Agriculture and Forestry in Brno, Zemedelska
PCR IN DETECTION OF FUNGAL CONTAMINATIONS IN POWDERED PEPPER Trojan V., Hanáček P., Havel L. Department of Plant Biology, Faculty of Agronomy, Mendel University of Agriculture and Forestry in Brno, Zemedelska
DIAGNOSTICKÝ KIT PRO DETEKCI MINIMÁLNÍ REZIUDÁLNÍ CHOROBY MRD EGFR
 Úvod IntellMed, s.r.o., Václavské náměstí 820/41, 110 00 Praha 1 DIAGNOSTICKÝ KIT PRO DETEKCI MINIMÁLNÍ REZIUDÁLNÍ CHOROBY MRD EGFR Jednou z nejvhodnějších metod pro detekci minimální reziduální choroby
Úvod IntellMed, s.r.o., Václavské náměstí 820/41, 110 00 Praha 1 DIAGNOSTICKÝ KIT PRO DETEKCI MINIMÁLNÍ REZIUDÁLNÍ CHOROBY MRD EGFR Jednou z nejvhodnějších metod pro detekci minimální reziduální choroby
Braf V600E StripAssay
 Braf V600E StripAssay Kat. číslo 5-570 20 testů 2-8 C Popis stripu: Pracovní postup 1. Izolace DNA Pro izolaci čerstvých nebo mražených biopsií použijte soupravy Qiagen QIAmp DNA Mini nebo Micro. Pro izolaci
Braf V600E StripAssay Kat. číslo 5-570 20 testů 2-8 C Popis stripu: Pracovní postup 1. Izolace DNA Pro izolaci čerstvých nebo mražených biopsií použijte soupravy Qiagen QIAmp DNA Mini nebo Micro. Pro izolaci
Column DNA Lego Kit UNIVERZÁLNÍ SOUPRAVY PRO RYCHLOU IZOLACI ČISTÉ DNA (Katalogové číslo D201 + D202)
 Column DNA Lego Kit UNIVERZÁLNÍ SOUPRAVY PRO RYCHLOU IZOLACI ČISTÉ DNA (Katalogové číslo D201 + D202) Popis Column DNA Lego Kit je základ moderní stavebnicové (Lego) soupravy pro izolaci čisté DNA různého
Column DNA Lego Kit UNIVERZÁLNÍ SOUPRAVY PRO RYCHLOU IZOLACI ČISTÉ DNA (Katalogové číslo D201 + D202) Popis Column DNA Lego Kit je základ moderní stavebnicové (Lego) soupravy pro izolaci čisté DNA různého
Všechna agarová média se sterilizují v autoklávu při 121 C po dobu 15 minut (při tlaku 1,2.10 5 Pa).
 Média pro identifikaci mikroskopických hub Všechna ová média se sterilizují v autoklávu při 121 C po dobu 15 minut (při tlaku 1,2.10 5 Pa). AFPA Aspergillus flavus/parasiticus médium (Aspergillus flavus
Média pro identifikaci mikroskopických hub Všechna ová média se sterilizují v autoklávu při 121 C po dobu 15 minut (při tlaku 1,2.10 5 Pa). AFPA Aspergillus flavus/parasiticus médium (Aspergillus flavus
DETEKCE VNITŘNÍHO GENU RÝŽE FOSFOLIPÁZY D POMOCÍ PCR
 Mgr. Jan Hodek RNDr. Jaroslava Ovesná, CSc. DETEKCE VNITŘNÍHO GENU RÝŽE FOSFOLIPÁZY D POMOCÍ PCR METODIKA PRO PRAXI Výzkumný ústav rostlinné výroby, v.v.i. 2007 Metodika byla vypracována pracovníky Národní
Mgr. Jan Hodek RNDr. Jaroslava Ovesná, CSc. DETEKCE VNITŘNÍHO GENU RÝŽE FOSFOLIPÁZY D POMOCÍ PCR METODIKA PRO PRAXI Výzkumný ústav rostlinné výroby, v.v.i. 2007 Metodika byla vypracována pracovníky Národní
IZOLACE A IDENTIFIKACE PLÍSNÍ
 IZOLACE A IDENTIFIKACE PLÍSNÍ MARCELA PEJCHALOVÁ Univerzita Pardubice Fakulta chemicko-technologická Katedra biologických a biochemických věd Centralizovaný rozvojový projekt MŠMT č. C29: Integrovaný systém
IZOLACE A IDENTIFIKACE PLÍSNÍ MARCELA PEJCHALOVÁ Univerzita Pardubice Fakulta chemicko-technologická Katedra biologických a biochemických věd Centralizovaný rozvojový projekt MŠMT č. C29: Integrovaný systém
RNA Blue REAGENS PRO RYCHLOU PŘÍPRAVU ČISTÉ A NEDEGRADOVANÉ RNA (katalogové číslo R011, R012, R013)
 RNA Blue REAGENS PRO RYCHLOU PŘÍPRAVU ČISTÉ A NEDEGRADOVANÉ RNA (katalogové číslo R011, R012, R013) Upozornění: RNA Blue obsahuje fenol a další toxické komponenty. Při kontaktu s kůží je nutné omytí velkým
RNA Blue REAGENS PRO RYCHLOU PŘÍPRAVU ČISTÉ A NEDEGRADOVANÉ RNA (katalogové číslo R011, R012, R013) Upozornění: RNA Blue obsahuje fenol a další toxické komponenty. Při kontaktu s kůží je nutné omytí velkým
EGFR XL StripAssay. Kat. číslo 5-630. 20 testů 2-8 C
 EGFR XL StripAssay Kat. číslo 5-630 20 testů 2-8 C Popis stripu Pracovní postup 1. Izolace DNA Pro izolaci DNA použijte vhodný izolační kit. Doporučené kity jsou následující: Pro izolaci čerstvých nebo
EGFR XL StripAssay Kat. číslo 5-630 20 testů 2-8 C Popis stripu Pracovní postup 1. Izolace DNA Pro izolaci DNA použijte vhodný izolační kit. Doporučené kity jsou následující: Pro izolaci čerstvých nebo
NRAS StripAssay. Kat. číslo 5-610. 20 testů 2-8 C
 NRAS StripAssay Kat. číslo 5-610 20 testů 2-8 C Popis stripu: Pracovní postup 1. Izolace DNA Pro izolaci DNA musí být použita vhodná metoda vzhledem k typu tkáně vzorku. Pro doporučení vhodné metody kontaktujte
NRAS StripAssay Kat. číslo 5-610 20 testů 2-8 C Popis stripu: Pracovní postup 1. Izolace DNA Pro izolaci DNA musí být použita vhodná metoda vzhledem k typu tkáně vzorku. Pro doporučení vhodné metody kontaktujte
DNA TECHNIKY IDENTIFIKACE ŽIVOČIŠNÝCH DRUHŮ V KRMIVU A POTRAVINÁCH. Michaela Nesvadbová
 DNA TECHNIKY IDENTIFIKACE ŽIVOČIŠNÝCH DRUHŮ V KRMIVU A POTRAVINÁCH Michaela Nesvadbová Význam identifikace živočišných druhů v krmivu a potravinách povinností každého výrobce je řádně a pravdivě označit
DNA TECHNIKY IDENTIFIKACE ŽIVOČIŠNÝCH DRUHŮ V KRMIVU A POTRAVINÁCH Michaela Nesvadbová Význam identifikace živočišných druhů v krmivu a potravinách povinností každého výrobce je řádně a pravdivě označit
α-globin StripAssay Kat. číslo 4-160 10 testů 2-8 C
 α-globin StripAssay Kat. číslo 4-160 10 testů 2-8 C Popis stripů: Pracovní postup Izolace DNA Doporučujeme použít následující kit pro izolaci DNA z plné krve nebo jiných typů vzorků: Spin Micro DNA Extraction
α-globin StripAssay Kat. číslo 4-160 10 testů 2-8 C Popis stripů: Pracovní postup Izolace DNA Doporučujeme použít následující kit pro izolaci DNA z plné krve nebo jiných typů vzorků: Spin Micro DNA Extraction
OPTIMALIZOVANÝ POSTUP PRO DETEKCI GLOMERELLA CINGULATA VE VĚTVÍCH A KMENECH JABLONÍ POMOCÍ MIKROBIOLOGICKÝCH METOD.
 DAVID NOVOTNÝ, IVA KŘÍŽKOVÁ A JIŘINA KRÁTKÁ OPTIMALIZOVANÝ POSTUP PRO DETEKCI GLOMERELLA CINGULATA VE VĚTVÍCH A KMENECH JABLONÍ POMOCÍ MIKROBIOLOGICKÝCH METOD. METODIKA PRO ÚTVARY STÁTNÍ SPRÁVY Výzkumný
DAVID NOVOTNÝ, IVA KŘÍŽKOVÁ A JIŘINA KRÁTKÁ OPTIMALIZOVANÝ POSTUP PRO DETEKCI GLOMERELLA CINGULATA VE VĚTVÍCH A KMENECH JABLONÍ POMOCÍ MIKROBIOLOGICKÝCH METOD. METODIKA PRO ÚTVARY STÁTNÍ SPRÁVY Výzkumný
cdna synthesis kit First-Strand cdna Synthesis System Verze 1.2
 cdna synthesis kit First-Strand cdna Synthesis System Verze 1.2 Obsah soupravy a její skladování Tato souprava pro reverzní transkripci obsahuje reagencie potřebné k provedení reverzní transkripce (RT)
cdna synthesis kit First-Strand cdna Synthesis System Verze 1.2 Obsah soupravy a její skladování Tato souprava pro reverzní transkripci obsahuje reagencie potřebné k provedení reverzní transkripce (RT)
Jednotné pracovní postupy zkoušení krmiv STANOVENÍ OBSAHU KVASINEK RODU SACCHAROMYCES
 Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU KVASINEK RODU SACCHAROMYCES 1 Rozsah a účel Metodika slouží ke stanovení počtu probiotických kvasinek v doplňkových látkách, premixech a krmivech.
Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU KVASINEK RODU SACCHAROMYCES 1 Rozsah a účel Metodika slouží ke stanovení počtu probiotických kvasinek v doplňkových látkách, premixech a krmivech.
TESTOVÁNÍ GMO Praktikum fyziologie rostlin
 Teoretický úvod: TESTOVÁNÍ GMO Praktikum fyziologie rostlin 1 Teoretický úvod: TESTOVÁNÍ GMO Obecně na úvod Určitě jste už slyšeli pojem geneticky modifikovaný organismus (GMO). Úprava vlastností přirozeně
Teoretický úvod: TESTOVÁNÍ GMO Praktikum fyziologie rostlin 1 Teoretický úvod: TESTOVÁNÍ GMO Obecně na úvod Určitě jste už slyšeli pojem geneticky modifikovaný organismus (GMO). Úprava vlastností přirozeně
Praktické cvičení: Izolace a purifikace rekombinantního proteinu
 Praktické cvičení: Izolace a purifikace rekombinantního proteinu Toto blokové praktické cvičení spočívá v teoretickém i praktickém seznámení s rekombinantními proteiny, jejich izolací, purifikací a využitím.
Praktické cvičení: Izolace a purifikace rekombinantního proteinu Toto blokové praktické cvičení spočívá v teoretickém i praktickém seznámení s rekombinantními proteiny, jejich izolací, purifikací a využitím.
Skladištní škůdci- rizika a detekce. Václav Stejskal. Výzkumný ústav rostlinné výroby,v.v.i. Praha stejskal@vurv.cz
 Skladištní škůdci- rizika a detekce Václav Stejskal Výzkumný ústav rostlinné výroby,v.v.i. Praha stejskal@vurv.cz Rizika skladištních škůdců Rizika medicinální a pro bezpečnost potravin - fyzikální kontaminace
Skladištní škůdci- rizika a detekce Václav Stejskal Výzkumný ústav rostlinné výroby,v.v.i. Praha stejskal@vurv.cz Rizika skladištních škůdců Rizika medicinální a pro bezpečnost potravin - fyzikální kontaminace
Sure-MeDIP I. with magnetic beads and MNase. www.krd.cz
 Sure-MeDIP I with magnetic beads and MNase www.krd.cz 1 Obsah soupravy a skladování MeDIP souprava obsahuje reagencie na provedení 25 reakcí. Souprava je rozdělen do dvou částí, jedna je distribuována
Sure-MeDIP I with magnetic beads and MNase www.krd.cz 1 Obsah soupravy a skladování MeDIP souprava obsahuje reagencie na provedení 25 reakcí. Souprava je rozdělen do dvou částí, jedna je distribuována
Braf 600/601 StripAssay
 Braf 600/601 StripAssay Kat. číslo 5-560 20 testů 2-8 C Popis stripu: Pracovní postup Kit umožňuje detekci 9 mutací v genu BRAF (kodón 600 a 601) Další informace najdete v OMIM Online Mendelian Inheritance
Braf 600/601 StripAssay Kat. číslo 5-560 20 testů 2-8 C Popis stripu: Pracovní postup Kit umožňuje detekci 9 mutací v genu BRAF (kodón 600 a 601) Další informace najdete v OMIM Online Mendelian Inheritance
Jaroslava Ovesná, Jan Hodek METODY EXTRAKCE DNA Z ČERSTVÉHO PLODU PAPÁJI A Z KANDOVANÉ PAPÁJI METODIKA PRO PRAXI
 Jaroslava Ovesná, Jan Hodek METODY EXTRAKCE DNA Z ČERSTVÉHO PLODU PAPÁJI A Z KANDOVANÉ PAPÁJI METODIKA PRO PRAXI Výzkumný ústav rostlinné výroby, v.v.i. 2010 Metodika byla vypracována pracovníky Národní
Jaroslava Ovesná, Jan Hodek METODY EXTRAKCE DNA Z ČERSTVÉHO PLODU PAPÁJI A Z KANDOVANÉ PAPÁJI METODIKA PRO PRAXI Výzkumný ústav rostlinné výroby, v.v.i. 2010 Metodika byla vypracována pracovníky Národní
1. Metodika. Protokol č. F1-4 Metodika: Srovnávací analýza efektivity přípravy rekombinantního proteinu ve fermentoru
 Protokol č.: F1-4 Datum: 20.12.2010 Metodika: analýza efektivity přípravy výběr z výsledků ze zkušebních provozů výroby antigenů. Vypracoval: Ing. Václav Filištein, Mgr. Tereza Chrudimská, Spolupracující
Protokol č.: F1-4 Datum: 20.12.2010 Metodika: analýza efektivity přípravy výběr z výsledků ze zkušebních provozů výroby antigenů. Vypracoval: Ing. Václav Filištein, Mgr. Tereza Chrudimská, Spolupracující
Mendelova univerzita v Brně Agronomická fakulta Ústav biologie rostlin
 Mendelova univerzita v Brně Agronomická fakulta Ústav biologie rostlin Inovace laboratorních úloh genetických předmětů metodikami pracujícími s ribonukleovými kyselinami pšenice Metodické návody pro laboratorní
Mendelova univerzita v Brně Agronomická fakulta Ústav biologie rostlin Inovace laboratorních úloh genetických předmětů metodikami pracujícími s ribonukleovými kyselinami pšenice Metodické návody pro laboratorní
MODERNÍ BIOFYZIKÁLNÍ METODY:
 MODERNÍ BIOFYZIKÁLNÍ METODY: POKROČILÉ PRAKTICKÉ VZDĚLÁVÁNÍ V EXPERIMENTÁLNÍ BIOLOGII Operační program Vzdělávání pro konkurenceschopnost Číslo projektu: CZ.1.07/2.3.00/09.0046 Praktický kurz pokročilých
MODERNÍ BIOFYZIKÁLNÍ METODY: POKROČILÉ PRAKTICKÉ VZDĚLÁVÁNÍ V EXPERIMENTÁLNÍ BIOLOGII Operační program Vzdělávání pro konkurenceschopnost Číslo projektu: CZ.1.07/2.3.00/09.0046 Praktický kurz pokročilých
USING OF AUTOMATED DNA SEQUENCING FOR PORCINE CANDIDATE GENES POLYMORFISMS DETECTION
 USING OF AUTOMATED DNA SEQUENCING FOR PORCINE CANDIDATE GENES POLYMORFISMS DETECTION VYUŽITÍ AUTOMATICKÉHO SEKVENOVÁNÍ DNA PRO DETEKCI POLYMORFISMŮ KANDIDÁTNÍCH GENŮ U PRASAT Vykoukalová Z., Knoll A.,
USING OF AUTOMATED DNA SEQUENCING FOR PORCINE CANDIDATE GENES POLYMORFISMS DETECTION VYUŽITÍ AUTOMATICKÉHO SEKVENOVÁNÍ DNA PRO DETEKCI POLYMORFISMŮ KANDIDÁTNÍCH GENŮ U PRASAT Vykoukalová Z., Knoll A.,
IZOLACE DNA PRO STANOVENÍ GMO METODOU PCR (KIT NUCLEOSPIN FOOD)
 1252.1 Izolace DNA pro stanovení GMO metodou Strana 1 IZOLACE DNA PRO STANOVENÍ GMO METODOU PCR (KIT NUCLEOSPIN FOOD) 1 Účel a rozsah Postup slouží k získání deoxyribonukleové kyseliny (DNA) ze vzorku
1252.1 Izolace DNA pro stanovení GMO metodou Strana 1 IZOLACE DNA PRO STANOVENÍ GMO METODOU PCR (KIT NUCLEOSPIN FOOD) 1 Účel a rozsah Postup slouží k získání deoxyribonukleové kyseliny (DNA) ze vzorku
Autoindex nad DNA sekvencemi
 Autoindex nd DNA sekvenemi do. Ing. Jn Holub, Ph.D. ktedr teoretiké informtiky Fkult informčníh tehnologií České vysoké učení tehniké v Prze ENBIK 2014 10. 6. 2014 ENBIK 2014, 10. 5. 2014 J. Holub: Autoindex
Autoindex nd DNA sekvenemi do. Ing. Jn Holub, Ph.D. ktedr teoretiké informtiky Fkult informčníh tehnologií České vysoké učení tehniké v Prze ENBIK 2014 10. 6. 2014 ENBIK 2014, 10. 5. 2014 J. Holub: Autoindex
Izolace nukleových kyselin
 Izolace nukleových kyselin Požadavky na izolaci nukleových kyselin V nativním stavu z přirozeného materiálu v dostatečném množství požadované čistotě. Nukleové kyseliny je třeba zbavit všech látek, které
Izolace nukleových kyselin Požadavky na izolaci nukleových kyselin V nativním stavu z přirozeného materiálu v dostatečném množství požadované čistotě. Nukleové kyseliny je třeba zbavit všech látek, které
MYKOLOGICKÁ ANALÝZA POTRAVIN
 MYKOLOGICKÁ ANALÝZA POTRAVIN a. Souhrn V roce 2011 byl ukončen druhý dvouletý cyklus nově uspořádaného Monitoringu dietární expozice člověka a tím i pozměněného projektu "MYKOMON". Vzhledem k detailnějšímu
MYKOLOGICKÁ ANALÝZA POTRAVIN a. Souhrn V roce 2011 byl ukončen druhý dvouletý cyklus nově uspořádaného Monitoringu dietární expozice člověka a tím i pozměněného projektu "MYKOMON". Vzhledem k detailnějšímu
Optimalizace metody PCR pro její využití na vzorky KONTAMINOVANÝCH PITNÝCH VOD
 Optimalizace metody PCR pro její využití na vzorky KONTAMINOVANÝCH PITNÝCH VOD Dana Vejmelková, Milan Šída, Kateřina Jarošová, Jana Říhová Ambrožová VODÁRENSKÁ BIOLOGIE, 1. 2. 2017 ÚVOD Sledované parametry,
Optimalizace metody PCR pro její využití na vzorky KONTAMINOVANÝCH PITNÝCH VOD Dana Vejmelková, Milan Šída, Kateřina Jarošová, Jana Říhová Ambrožová VODÁRENSKÁ BIOLOGIE, 1. 2. 2017 ÚVOD Sledované parametry,
MagPurix Blood DNA Extraction Kit 200
 MagPurix Blood DNA Extraction Kit 200 Kat. č. ZP02001-48 Doba zpracování: 50-60 minut pro MagPurix 12S 50-70 minut pro MagPurix 24 Použití Souprava MagPurix Blood DNA Extraction Kit 200 je určena pro izolátor
MagPurix Blood DNA Extraction Kit 200 Kat. č. ZP02001-48 Doba zpracování: 50-60 minut pro MagPurix 12S 50-70 minut pro MagPurix 24 Použití Souprava MagPurix Blood DNA Extraction Kit 200 je určena pro izolátor
DETEKCE A IDENTIFIKACE FYTOPATOGENNÍCH BAKTERIÍ METODOU PCR-RFLP
 DETEKCE A IDENTIFIKACE FYTOPATOGENNÍCH BAKTERIÍ METODOU PCR-RFLP Polymerázová řetězová reakce (PCR) je in vitro metoda pro enzymatickou syntézu definované sekvence DNA. Reakce využívá dvou oligonukleotidových
DETEKCE A IDENTIFIKACE FYTOPATOGENNÍCH BAKTERIÍ METODOU PCR-RFLP Polymerázová řetězová reakce (PCR) je in vitro metoda pro enzymatickou syntézu definované sekvence DNA. Reakce využívá dvou oligonukleotidových
IZOLACE DNA PRO STANOVENÍ GMO METODOU PCR (KIT GENELUTE)
 Strana 1 IZOLACE DNA PRO STANOVENÍ GMO METODOU PCR (KIT GENELUTE) 1 Účel a rozsah Postup slouží k získání deoxyribonukleové kyseliny (DNA) ze vzorku pomocí komerčního kitu GenElute. 2 Princip Proces izolace
Strana 1 IZOLACE DNA PRO STANOVENÍ GMO METODOU PCR (KIT GENELUTE) 1 Účel a rozsah Postup slouží k získání deoxyribonukleové kyseliny (DNA) ze vzorku pomocí komerčního kitu GenElute. 2 Princip Proces izolace
Jaroslava Ovesná, Jan Hodek, Lucie Pavlátová,
 Jaroslava Ovesná, Jan Hodek, Lucie Pavlátová, METODIKA DETEKCE GENETICKY MODIFIKOVANÉHO TABÁKU VIRŽINSKÉHO (Nicotina tabacum L. cv. Samsun) S VNESENÝM KVASINKOVÝM MITOTICKÝM AKTIVÁTOREM (gen SpCdc25 z
Jaroslava Ovesná, Jan Hodek, Lucie Pavlátová, METODIKA DETEKCE GENETICKY MODIFIKOVANÉHO TABÁKU VIRŽINSKÉHO (Nicotina tabacum L. cv. Samsun) S VNESENÝM KVASINKOVÝM MITOTICKÝM AKTIVÁTOREM (gen SpCdc25 z
Jednotné pracovní postupy zkoušení krmiv STANOVENÍ OBSAHU MYKOTOXINŮ METODOU LC-MS - FUMONISIN B 1 A B 2
 Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU MYKOTOXINŮ METODOU LC-MS - FUMONISIN B 1 A B 2 1 Rozsah a účel Metoda je vhodná pro stanovení fumonisinů B 1 a B 2 v krmivech. 2 Princip Fumonisiny
Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU MYKOTOXINŮ METODOU LC-MS - FUMONISIN B 1 A B 2 1 Rozsah a účel Metoda je vhodná pro stanovení fumonisinů B 1 a B 2 v krmivech. 2 Princip Fumonisiny
CENÍK SLUŽEB A PRACÍ
 Výzkumný ústav pícninářský, spol. s r.o. Troubsko CENÍK SLUŽEB A PRACÍ 2016 Ceny jsou uvedeny bez DPH Adresa: Výzkumný ústav pícninářský, spol. s r.o. Zahradní 1 664 41 Troubsko Tel.: 547 138 811 E-mail:
Výzkumný ústav pícninářský, spol. s r.o. Troubsko CENÍK SLUŽEB A PRACÍ 2016 Ceny jsou uvedeny bez DPH Adresa: Výzkumný ústav pícninářský, spol. s r.o. Zahradní 1 664 41 Troubsko Tel.: 547 138 811 E-mail:
Havarijní plán PřF UP
 Havarijní plán PřF UP v němž se nakládá s geneticky modifikovanými organismy (GMO), zpracovaný podle 20, odst. 4 zákona č. 78/2004 Sb. pro pracoviště kateder Buněčné biologie a genetiky a Oddělení molekulární
Havarijní plán PřF UP v němž se nakládá s geneticky modifikovanými organismy (GMO), zpracovaný podle 20, odst. 4 zákona č. 78/2004 Sb. pro pracoviště kateder Buněčné biologie a genetiky a Oddělení molekulární
NÁVRH METODIKY PRO TESTOVÁNÍ ODOLNOSTI STAVEBNÍCH HMOT PROTI NAPADENÍ PLÍSNĚMI
 NÁVRH METODIKY PRO TESTOVÁNÍ ODOLNOSTI STAVEBNÍCH HMOT PROTI NAPADENÍ PLÍSNĚMI PROPOSAL OF METHODOLOGY FOR TESTING RESISTANCE OF BUILDING MATERIALS AGAINST MOLD INFESTATION Ilona Kukletová, Ivana Chromková
NÁVRH METODIKY PRO TESTOVÁNÍ ODOLNOSTI STAVEBNÍCH HMOT PROTI NAPADENÍ PLÍSNĚMI PROPOSAL OF METHODOLOGY FOR TESTING RESISTANCE OF BUILDING MATERIALS AGAINST MOLD INFESTATION Ilona Kukletová, Ivana Chromková
Jan Hodek, Jaroslava Ovesná, Lucie Pavlátová. METODIKA DETEKCE GENETICKY MODIFIKOVANÉ PAPÁJI LINIÍ 55-1 a 63-1 METODIKA PRO PRAXI
 Jan Hodek, Jaroslava Ovesná, Lucie Pavlátová METODIKA DETEKCE GENETICKY MODIFIKOVANÉ PAPÁJI LINIÍ 55-1 a 63-1 METODIKA PRO PRAXI Výzkumný ústav rostlinné výroby, v.v.i. 2008 Metodika byla vypracována pracovníky
Jan Hodek, Jaroslava Ovesná, Lucie Pavlátová METODIKA DETEKCE GENETICKY MODIFIKOVANÉ PAPÁJI LINIÍ 55-1 a 63-1 METODIKA PRO PRAXI Výzkumný ústav rostlinné výroby, v.v.i. 2008 Metodika byla vypracována pracovníky
Mendelova univerzita v Brně Agronomická fakulta Ústav biologie rostlin
 Mendelova univerzita v Brně Agronomická fakulta Ústav biologie rostlin Inovace praktických cvičení molekulárně-biologických předmětů o sekvenční úlohy PRACOVNÍ PROTOKOL PRO PŘEDMĚT GENETCKÁ DIVERZITA Vypracováno
Mendelova univerzita v Brně Agronomická fakulta Ústav biologie rostlin Inovace praktických cvičení molekulárně-biologických předmětů o sekvenční úlohy PRACOVNÍ PROTOKOL PRO PŘEDMĚT GENETCKÁ DIVERZITA Vypracováno
Využití metody imunoafinitní chromatografie pro stanovení obsahu deoxynivalenolu v zrnu obilovin METODIKA PRO PRAXI. J. Chrpová a kol.
 Využití metody imunoafinitní chromatografie pro stanovení obsahu deoxynivalenolu v zrnu obilovin METODIKA PRO PRAXI J. Chrpová a kol. Dedikace Metodika vznikla za finanční podpory MZe ČR a je výstupem
Využití metody imunoafinitní chromatografie pro stanovení obsahu deoxynivalenolu v zrnu obilovin METODIKA PRO PRAXI J. Chrpová a kol. Dedikace Metodika vznikla za finanční podpory MZe ČR a je výstupem
Inkubace enzymů se substráty
 Inkubace enzymů se substráty Inkubace redukčních enzymů... 1 Inkubace oxidačních enzymů... 2 Extrakce látek z inkubační směsi... 2 Příprava vzorků k HPLC/UHPLC detekci... 3 Chemikálie a roztoky... 4 Substráty...
Inkubace enzymů se substráty Inkubace redukčních enzymů... 1 Inkubace oxidačních enzymů... 2 Extrakce látek z inkubační směsi... 2 Příprava vzorků k HPLC/UHPLC detekci... 3 Chemikálie a roztoky... 4 Substráty...
Detekce a stanovení Pyrenophora teres v listových pletivech ječmene
 Leona Leišová Detekce a stanovení Pyrenophora teres v listových pletivech ječmene Metodika pro praxi Výzkumný ústav rostlinné výroby, v.v.i. 2007 Metodika vznikla za finanční podpory Mze ČR a je výstupem
Leona Leišová Detekce a stanovení Pyrenophora teres v listových pletivech ječmene Metodika pro praxi Výzkumný ústav rostlinné výroby, v.v.i. 2007 Metodika vznikla za finanční podpory Mze ČR a je výstupem
Určeno pro obecné laboratorní užití. Není určeno pro použití v diagnostických postupech. POUZE PRO POUŽITÍ IN VITRO.
 Určeno pro obecné laboratorní užití. Není určeno pro použití v diagnostických postupech. POUZE PRO POUŽITÍ IN VITRO. PCR Nucleotide Mix Předem připravený roztok ultračistých PCR deoxynukleotidů (datp,
Určeno pro obecné laboratorní užití. Není určeno pro použití v diagnostických postupech. POUZE PRO POUŽITÍ IN VITRO. PCR Nucleotide Mix Předem připravený roztok ultračistých PCR deoxynukleotidů (datp,
Uživatelská příručka
 PGM Barcoding Set 1-8 Navrženo pro PGM ION-TORRENT KÓD PRODUKTU: 2001 (1-8) BALEN9: 32 testů Uživatelská příručka Rev02.2015 Str. 1 Rejstřík 1. POUŽITÍ VÝROBKU 3 2. OBSAH KITU 4 3. SKLADOVÁNÍ 4 4. STABILITA
PGM Barcoding Set 1-8 Navrženo pro PGM ION-TORRENT KÓD PRODUKTU: 2001 (1-8) BALEN9: 32 testů Uživatelská příručka Rev02.2015 Str. 1 Rejstřík 1. POUŽITÍ VÝROBKU 3 2. OBSAH KITU 4 3. SKLADOVÁNÍ 4 4. STABILITA
MagPurix Viral/Pathogen Nucleic Acids Extraction Kit B
 MagPurix Viral/Pathogen Nucleic Acids Extraction Kit B Kat. č. ZP02012 Doba zpracování: 45-60 minut pro MagPurix 12S 45-65 minut pro MagPurix 24 Použití Souprava MagPurix Viral/Pathogen Nucleic Acids Extraction
MagPurix Viral/Pathogen Nucleic Acids Extraction Kit B Kat. č. ZP02012 Doba zpracování: 45-60 minut pro MagPurix 12S 45-65 minut pro MagPurix 24 Použití Souprava MagPurix Viral/Pathogen Nucleic Acids Extraction
Jednotné pracovní postupy zkoušení krmiv STANOVENÍ OBSAHU MYKOTOXINŮ METODOU LC-MS - aflatoxin B1, B2, G1 a G2
 Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU MYKOTOXINŮ METODOU LC-MS - aflatoxin B1, B2, G1 a G2 1 Rozsah a účel Metoda je vhodná pro stanovení aflatoxinů B1, B2, G1 a G2 v krmivech. 2 Princip
Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU MYKOTOXINŮ METODOU LC-MS - aflatoxin B1, B2, G1 a G2 1 Rozsah a účel Metoda je vhodná pro stanovení aflatoxinů B1, B2, G1 a G2 v krmivech. 2 Princip
Nové poznatky k problematice běloklasosti trav
 projekt NAZV č.: QI111C016 Nové poznatky k problematice běloklasosti trav Zdeněk BOTH, Miroslava STREJČKOVÁ Zemědělský výzkum, s. r. o. Výzkumný ústav rostlinné výroby, v. v. i. OSEVA vývoj a výzkum s.r.o.
projekt NAZV č.: QI111C016 Nové poznatky k problematice běloklasosti trav Zdeněk BOTH, Miroslava STREJČKOVÁ Zemědělský výzkum, s. r. o. Výzkumný ústav rostlinné výroby, v. v. i. OSEVA vývoj a výzkum s.r.o.
CYCLER CHECK. Test pro validaci teplotní uniformity cyklérů. Připraveno k použití, prealiquotováno. REF 7104 (10 testů) REF (4 testy)
 CZ Návod k použití CYCLER CHECK Test pro validaci teplotní uniformity cyklérů Připraveno k použití, prealiquotováno REF 7104 (10 testů) REF 71044 (4 testy) Obsah 1. Popis výrobku... 2 2. Materiál... 3
CZ Návod k použití CYCLER CHECK Test pro validaci teplotní uniformity cyklérů Připraveno k použití, prealiquotováno REF 7104 (10 testů) REF 71044 (4 testy) Obsah 1. Popis výrobku... 2 2. Materiál... 3
Tkáňový homogenizátor MagNA Lyser od společnosti Roche
 Izolace RNA Pracovní postup Homogenizace: Pozn. Postup homogenizace platí pouze pro izolaci RNA z nativní tkáně, v případě izolace z buněčné suspenze je tento krok vynechán a začíná se přídavkem homogenizačního
Izolace RNA Pracovní postup Homogenizace: Pozn. Postup homogenizace platí pouze pro izolaci RNA z nativní tkáně, v případě izolace z buněčné suspenze je tento krok vynechán a začíná se přídavkem homogenizačního
MOLEKULÁRNÍ BIOLOGIE. 2. Polymerázová řetězová reakce (PCR)
 MOLEKULÁRNÍ BIOLOGIE 2. Polymerázová řetězová reakce (PCR) Náplň praktik 1. Izolace DNA z buněk bukální sliznice - izolační kit MACHEREY-NAGEL 2. PCR polymerázová řetězová reakce (templát gdna) 3. Restrikční
MOLEKULÁRNÍ BIOLOGIE 2. Polymerázová řetězová reakce (PCR) Náplň praktik 1. Izolace DNA z buněk bukální sliznice - izolační kit MACHEREY-NAGEL 2. PCR polymerázová řetězová reakce (templát gdna) 3. Restrikční
Možnosti snížení rizika napadení obilnin klasovými fuzariózami
 Jana Chrpová a kol. Možnosti snížení rizika napadení obilnin klasovými fuzariózami METODIKA PRO PRAXI Výzkumný ústav rostlinné výroby, v.v.i. 2007 Metodika vznikla za finanční podpory MZe ČR a je výstupem
Jana Chrpová a kol. Možnosti snížení rizika napadení obilnin klasovými fuzariózami METODIKA PRO PRAXI Výzkumný ústav rostlinné výroby, v.v.i. 2007 Metodika vznikla za finanční podpory MZe ČR a je výstupem
VYUŽITÍ AFLP PRO DNA GENOTYPIZACI ROSTLIN
 RNDr. Jaroslava Ovesná, CSc. Mgr. Jan Hodek VYUŽITÍ AFLP PRO DNA GENOTYPIZACI ROSTLIN METODIKA PRO PRAXI Výzkumný ústav rostlinné výroby, v.v.i. 2007 Metodika byla vypracována pracovníky Národní Referenční
RNDr. Jaroslava Ovesná, CSc. Mgr. Jan Hodek VYUŽITÍ AFLP PRO DNA GENOTYPIZACI ROSTLIN METODIKA PRO PRAXI Výzkumný ústav rostlinné výroby, v.v.i. 2007 Metodika byla vypracována pracovníky Národní Referenční
Seminář izolačních technologií
 Seminář izolačních technologií Zpracoval: Karel Bílek a Kateřina Svobodová Podpořeno FRVŠ 2385/2007 a 1305/2009 Úpravy a aktualizace: Pavla Chalupová ÚMFGZ MZLU v Brně 1 Lokalizace jaderné DNA 2 http://www.paternityexperts.com/basicgenetics.html
Seminář izolačních technologií Zpracoval: Karel Bílek a Kateřina Svobodová Podpořeno FRVŠ 2385/2007 a 1305/2009 Úpravy a aktualizace: Pavla Chalupová ÚMFGZ MZLU v Brně 1 Lokalizace jaderné DNA 2 http://www.paternityexperts.com/basicgenetics.html
N Laboratoř hydrobiologie a mikrobiologie
 ÚSTAV TECHNOLOGIE VODY A PROSTŘEDÍ N217019 - Laboratoř hydrobiologie a mikrobiologie Název úlohy: Kultivační stanovení: Stanovení intestinálních enterokoků Vypracováno v rámci projektu: Inovace a restrukturalizace
ÚSTAV TECHNOLOGIE VODY A PROSTŘEDÍ N217019 - Laboratoř hydrobiologie a mikrobiologie Název úlohy: Kultivační stanovení: Stanovení intestinálních enterokoků Vypracováno v rámci projektu: Inovace a restrukturalizace
N217019 - Laboratoř hydrobiologie a mikrobiologie
 ÚSTAV TECHNOLOGIE VODY A PROSTŘEDÍ N217019 - Laboratoř hydrobiologie a mikrobiologie Název úlohy: Kultivační stanovení: Stanovení mikromycet (plísní a kvasinek) Vypracováno v rámci projektu: Inovace a
ÚSTAV TECHNOLOGIE VODY A PROSTŘEDÍ N217019 - Laboratoř hydrobiologie a mikrobiologie Název úlohy: Kultivační stanovení: Stanovení mikromycet (plísní a kvasinek) Vypracováno v rámci projektu: Inovace a
Jednotné pracovní postupy zkoušení krmiv STANOVENÍ AKTIVITY FYTÁZY
 Národní referenční laboratoř Strana 1 STANOVENÍ AKTIVITY FYTÁZY 1 Rozsah a účel Postup specifikuje stanovení fytázové aktivity ve vzorcích krmiva. Tímto postupem se nestanoví rozdíl mezi fytázou přidanou
Národní referenční laboratoř Strana 1 STANOVENÍ AKTIVITY FYTÁZY 1 Rozsah a účel Postup specifikuje stanovení fytázové aktivity ve vzorcích krmiva. Tímto postupem se nestanoví rozdíl mezi fytázou přidanou
Vliv výživy hospodářských zvířat na kvalitu živočišných produktů s důrazem na zdraví člověka
 Vliv výživy hospodářských zvířat na kvalitu živočišných produktů s důrazem na zdraví člověka ODBORNÝ SEMINÁŘ v rámci projektu Aplikace nových poznatků z oblasti výživy hospodářských zvířat do běžné zemědělské
Vliv výživy hospodářských zvířat na kvalitu živočišných produktů s důrazem na zdraví člověka ODBORNÝ SEMINÁŘ v rámci projektu Aplikace nových poznatků z oblasti výživy hospodářských zvířat do běžné zemědělské
ÚLOHA C Klonování PCR produktu do plasmidu
 Jméno a učo: Datum: ÚLOHA C Klonování PCR produktu do plasmidu TEORETICKÝ ÚVOD Při klonování PCR produktů do plasmidů se využívá vlastnosti Taq polymerasy, a jiných non-proofreading polymeras, přidávat
Jméno a učo: Datum: ÚLOHA C Klonování PCR produktu do plasmidu TEORETICKÝ ÚVOD Při klonování PCR produktů do plasmidů se využívá vlastnosti Taq polymerasy, a jiných non-proofreading polymeras, přidávat
Fuzariózy na obilninách. (Fusarium spp.)
 Fuzariózy na obilninách (Fusarium spp.) Úvod Houby rodu Fusarium jsou významnými patogeny většiny zemědělských plodin. U obilovin napadají fuzária paty stébel, listy a klasy. Nejvýznamnější škody vznikají
Fuzariózy na obilninách (Fusarium spp.) Úvod Houby rodu Fusarium jsou významnými patogeny většiny zemědělských plodin. U obilovin napadají fuzária paty stébel, listy a klasy. Nejvýznamnější škody vznikají
USE OF SSR MARKERS TO IMPROVE TECHNOLOGICAL QUALITY IN MALTING BARLEY VYUŽITÍ SSR MARKERŮ PRO ZLEPŠENÍ TECHNOLOGICKÉ JAKOSTI SLADOVNICKÉHO JEČMENE
 USE OF SSR MARKERS TO IMPROVE TECHNOLOGICAL QUALITY IN MALTING BARLEY VYUŽITÍ SSR MARKERŮ PRO ZLEPŠENÍ TECHNOLOGICKÉ JAKOSTI SLADOVNICKÉHO JEČMENE Ježíšková I., Bednář J. Ústav botaniky a fyziologie rostlin,
USE OF SSR MARKERS TO IMPROVE TECHNOLOGICAL QUALITY IN MALTING BARLEY VYUŽITÍ SSR MARKERŮ PRO ZLEPŠENÍ TECHNOLOGICKÉ JAKOSTI SLADOVNICKÉHO JEČMENE Ježíšková I., Bednář J. Ústav botaniky a fyziologie rostlin,
Tkáňové kultury rostlin. Mikropropagace
 Tkáňové kultury rostlin Mikropropagace IN VITRO KULTURY (EXPLANTÁTOVÉ KUTLURY, ROSTLINNÉ EXPLANTÁTY) Izolované rostliny, jejich orgány, pletiva či buňky pěstované in vitro ve sterilních podmínkách Na kultivačních
Tkáňové kultury rostlin Mikropropagace IN VITRO KULTURY (EXPLANTÁTOVÉ KUTLURY, ROSTLINNÉ EXPLANTÁTY) Izolované rostliny, jejich orgány, pletiva či buňky pěstované in vitro ve sterilních podmínkách Na kultivačních
Obsah Protein Gel Electrophoresis Kitu a jeho skladování
 Obsah Protein Gel Electrophoresis Kitu a jeho skladování Protein Gel Electrophoresis Kit obsahuje veškerý potřebný materiál provádění vertikální polyakrilamidové gelové elektroforézy. Experiment provádějí
Obsah Protein Gel Electrophoresis Kitu a jeho skladování Protein Gel Electrophoresis Kit obsahuje veškerý potřebný materiál provádění vertikální polyakrilamidové gelové elektroforézy. Experiment provádějí
Konečná zpráva hodnocení různých způsobů přípravy vzorků pro AMPLICOR HPV test firmy Roche
 Konečná zpráva hodnocení různých způsobů přípravy vzorků pro AMPLICOR HPV test firmy Roche Charakteristika testu: Set AMPLICOR HPV vyráběný firmou Roche je určený pro detekci vysoko-rizikových typů lidských
Konečná zpráva hodnocení různých způsobů přípravy vzorků pro AMPLICOR HPV test firmy Roche Charakteristika testu: Set AMPLICOR HPV vyráběný firmou Roche je určený pro detekci vysoko-rizikových typů lidských
Mykologická analýza potravin
 Mykologická analýza potravin a. Souhrn V roce 2010 byl zahájen druhý dvouletý cyklus nově uspořádaného Monitoringu dietární expozice člověka a tím i pozměněného projektu "MYKOMON". Vzhledem k detailnějšímu
Mykologická analýza potravin a. Souhrn V roce 2010 byl zahájen druhý dvouletý cyklus nově uspořádaného Monitoringu dietární expozice člověka a tím i pozměněného projektu "MYKOMON". Vzhledem k detailnějšímu
Leona Leišová a kol.
 Leona Leišová a kol. Použití metody analýzy mikrosatelitů pro charakterizaci odrůd pšenice, ječmene a ovsa pro potřeby semenářských podniků, šlechtitelských stanic a odrůdového zkušebnictví METODIKA PRO
Leona Leišová a kol. Použití metody analýzy mikrosatelitů pro charakterizaci odrůd pšenice, ječmene a ovsa pro potřeby semenářských podniků, šlechtitelských stanic a odrůdového zkušebnictví METODIKA PRO
5. Bioreaktory. Schematicky jsou jednotlivé typy bioreaktorů znázorněny na obr. 5.1. Nejpoužívanějšími bioreaktory jsou míchací tanky.
 5. Bioreaktory Bioreaktor (fermentor) je nejdůležitější částí výrobní linky biotechnologického procesu. Jde o nádobu různého objemu, ve které probíhá biologický proces. Dochází zde k růstu buněk a tvorbě
5. Bioreaktory Bioreaktor (fermentor) je nejdůležitější částí výrobní linky biotechnologického procesu. Jde o nádobu různého objemu, ve které probíhá biologický proces. Dochází zde k růstu buněk a tvorbě
ODLIŠENÍ ODRŮD PŠENICE OBECNÉ TRITICUM AESTIVUM L. METODOU RAPD
 ODLIŠENÍ ODRŮD PŠENICE OBECNÉ TRITICUM AESTIVUM L. METODOU RAPD Distinguishing of Wheat Varieties (Tritium aestivum L.) by Method RAPD Zuzana Kohutová, Zuzana Kocourková, Hana Vlastníková, Petr Sedlák
ODLIŠENÍ ODRŮD PŠENICE OBECNÉ TRITICUM AESTIVUM L. METODOU RAPD Distinguishing of Wheat Varieties (Tritium aestivum L.) by Method RAPD Zuzana Kohutová, Zuzana Kocourková, Hana Vlastníková, Petr Sedlák
Jednotné pracovní postupy zkoušení krmiv STANOVENÍ OBSAHU MELAMINU A KYSELINY KYANUROVÉ METODOU LC-MS
 Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU MELAMINU A KYSELINY KYANUROVÉ METODOU LC-MS 1 Rozsah a účel Postup je určen pro stanovení obsahu melaminu a kyseliny kyanurové v krmivech. 2 Princip
Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU MELAMINU A KYSELINY KYANUROVÉ METODOU LC-MS 1 Rozsah a účel Postup je určen pro stanovení obsahu melaminu a kyseliny kyanurové v krmivech. 2 Princip
Popis výsledku QC1156/01/2004 Identifikace projektu:
 Popis výsledku QC1156/01/2004 Identifikace projektu: ČÍSLO PROJEKTU QC1156 PROGRAM TÉMA PRIORITA Program I B) Zlepšování biologického potenciálu rostlin a zvířat a jeho efektivní využívání 3) Metody charakterizace
Popis výsledku QC1156/01/2004 Identifikace projektu: ČÍSLO PROJEKTU QC1156 PROGRAM TÉMA PRIORITA Program I B) Zlepšování biologického potenciálu rostlin a zvířat a jeho efektivní využívání 3) Metody charakterizace
Jaroslava Ovesná, Jan Hodek, Lucie Pavlátová. KVALITATIVNÍ STANOVENÍ TRANSGENNÍ LINIE RÝŽE Bt 63 METODOU PCR METODIKA PRO PRAXI
 Jaroslava Ovesná, Jan Hodek, Lucie Pavlátová KVALITATIVNÍ STANOVENÍ TRANSGENNÍ LINIE RÝŽE Bt 63 METODOU PCR METODIKA PRO PRAXI Výzkumný ústav rostlinné výroby, v.v.i. 2009 Metodika byla vypracována pracovníky
Jaroslava Ovesná, Jan Hodek, Lucie Pavlátová KVALITATIVNÍ STANOVENÍ TRANSGENNÍ LINIE RÝŽE Bt 63 METODOU PCR METODIKA PRO PRAXI Výzkumný ústav rostlinné výroby, v.v.i. 2009 Metodika byla vypracována pracovníky
USING MOLECULAR MARKERS FOR GENETIC DIVERSITY TESTING IN SPRING BARLEY WITH DIFFERENT SENSITIVITY AGAINST FHB
 USING MOLECULAR MARKERS FOR GENETIC DIVERSITY TESTING IN SPRING BARLEY WITH DIFFERENT SENSITIVITY AGAINST FHB TESTOVÁNÍ GENETICKÉ DIVERZITY JEČMENE JARNÍHO S RŮZNOU CITLIVOSTÍ VŮČI FHB MOLEKULÁRNÍMI MARKERY
USING MOLECULAR MARKERS FOR GENETIC DIVERSITY TESTING IN SPRING BARLEY WITH DIFFERENT SENSITIVITY AGAINST FHB TESTOVÁNÍ GENETICKÉ DIVERZITY JEČMENE JARNÍHO S RŮZNOU CITLIVOSTÍ VŮČI FHB MOLEKULÁRNÍMI MARKERY
Havarijní plán pro práci s geneticky modifikovanými mikroorganismy Mikrobiologický ústav AV ČR
 Mikrobiologický ústav AV ČR Příloha 6 Havarijní plán 1/5 Havarijní plán pro práci s geneticky modifikovanými mikroorganismy Mikrobiologický ústav AV ČR a) Adresa pracoviště Mikrobiologický ústav AV ČR
Mikrobiologický ústav AV ČR Příloha 6 Havarijní plán 1/5 Havarijní plán pro práci s geneticky modifikovanými mikroorganismy Mikrobiologický ústav AV ČR a) Adresa pracoviště Mikrobiologický ústav AV ČR
Obilniny. Limitované škodlivé organismy a jejich laboratorní stanovení
 Limitované škodlivé organismy a jejich laboratorní stanovení Obilniny Braničnatka plevová Fuzariózy klasů Snětivosti Prašná sněť pšeničná Pruhovitost ječná Skvrnitost Prašná sněť ječná, tvrdá sněť ječná
Limitované škodlivé organismy a jejich laboratorní stanovení Obilniny Braničnatka plevová Fuzariózy klasů Snětivosti Prašná sněť pšeničná Pruhovitost ječná Skvrnitost Prašná sněť ječná, tvrdá sněť ječná
ZDRAVOTNÍ NEZÁVADNOST POTRAVIN
 ZDRAVOTNÍ NEZÁVADNOST POTRAVIN Možnosti stanovení Listeria monocytogenes popis metod a jejich princip Mária Strážiková Aleš Holfeld Obsah Charakteristika Listeria monocytogenes Listerióza Metody detekce
ZDRAVOTNÍ NEZÁVADNOST POTRAVIN Možnosti stanovení Listeria monocytogenes popis metod a jejich princip Mária Strážiková Aleš Holfeld Obsah Charakteristika Listeria monocytogenes Listerióza Metody detekce
DETECTION OF FUNGAL CONTAMINATIONS IN POWDERED PEPPER USING MOLECULAR BIOLOGICAL METHODS
 DETECTION OF FUNGAL CONTAMINATIONS IN POWDERED PEPPER USING MOLECULAR BIOLOGICAL METHODS DETEKCE HOUBOVÝCH KONTAMINACÍ V PRÁŠKOVÉ PAPRICE POMOCÍ MOLEKULÁRNĚ BIOLOGICKÝCH METOD Trojan V., Hanáček P., Havel
DETECTION OF FUNGAL CONTAMINATIONS IN POWDERED PEPPER USING MOLECULAR BIOLOGICAL METHODS DETEKCE HOUBOVÝCH KONTAMINACÍ V PRÁŠKOVÉ PAPRICE POMOCÍ MOLEKULÁRNĚ BIOLOGICKÝCH METOD Trojan V., Hanáček P., Havel
Mykologická analýza potravin
 Mykologická analýza potravin a. Souhrn Rok 2009 byl druhým rokem dvouletého monitorovacího období (2008-2009) nově uspořádaného Monitoringu dietární expozice člověka a tím i pozměněného projektu "MYKOMON".
Mykologická analýza potravin a. Souhrn Rok 2009 byl druhým rokem dvouletého monitorovacího období (2008-2009) nově uspořádaného Monitoringu dietární expozice člověka a tím i pozměněného projektu "MYKOMON".
ACTIVATION OF DEHYDRIN GENES OF GERMINATE PLANTS OF BARLEY TO DROUGHT AND COLD AKTIVACE DEHYDRINOVÝCH GENŮ KLÍČNÍCH ROSTLIN JEČMENE SUCHEM A CHLADEM
 ACTIVATION OF DEHYDRIN GENES OF GERMINATE PLANTS OF BARLEY TO DROUGHT AND COLD AKTIVACE DEHYDRINOVÝCH GENŮ KLÍČNÍCH ROSTLIN JEČMENE SUCHEM A CHLADEM Dokoupilová Z., Holková L., Chloupek O. Ústav pěstování
ACTIVATION OF DEHYDRIN GENES OF GERMINATE PLANTS OF BARLEY TO DROUGHT AND COLD AKTIVACE DEHYDRINOVÝCH GENŮ KLÍČNÍCH ROSTLIN JEČMENE SUCHEM A CHLADEM Dokoupilová Z., Holková L., Chloupek O. Ústav pěstování
MOLEKULÁRNĚ BIOLOGICKÉ METODY V ENVIRONMENTÁLNÍ MIKROBIOLOGII. Martina Nováková, VŠCHT Praha
 MOLEKULÁRNĚ BIOLOGICKÉ METODY V ENVIRONMENTÁLNÍ MIKROBIOLOGII Martina Nováková, VŠCHT Praha MOLEKULÁRNÍ BIOLOGIE V BIOREMEDIACÍCH enumerace FISH průtoková cytometrie klonování produktů PCR sekvenování
MOLEKULÁRNĚ BIOLOGICKÉ METODY V ENVIRONMENTÁLNÍ MIKROBIOLOGII Martina Nováková, VŠCHT Praha MOLEKULÁRNÍ BIOLOGIE V BIOREMEDIACÍCH enumerace FISH průtoková cytometrie klonování produktů PCR sekvenování
Jednotné pracovní postupy zkoušení krmiv STANOVENÍ OBSAHU 5-VINYL - 2-THIOOXAZOLIDONU (GOITRINU) METODOU GC
 Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU 5-VINYL - 2-THIOOXAZOLIDONU (GOITRINU) METODOU GC 1 Rozsah a účel Metoda specifikuje podmínky pro stanovení vinylthiooxazolidonu (dále VOT) v krmivech.
Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU 5-VINYL - 2-THIOOXAZOLIDONU (GOITRINU) METODOU GC 1 Rozsah a účel Metoda specifikuje podmínky pro stanovení vinylthiooxazolidonu (dále VOT) v krmivech.
Spektrofotometrické stanovení fosforečnanů ve vodách
 Spektrofotometrické stanovení fosforečnanů ve vodách Úkol: Spektrofotometricky stanovte obsah fosforečnanů ve vodě Chemikálie: 0,07165 g dihydrogenfosforečnan draselný KH 2 PO 4 75 ml kyselina sírová H
Spektrofotometrické stanovení fosforečnanů ve vodách Úkol: Spektrofotometricky stanovte obsah fosforečnanů ve vodě Chemikálie: 0,07165 g dihydrogenfosforečnan draselný KH 2 PO 4 75 ml kyselina sírová H
Využití rep-pcr v bakteriální taxonomii
 Využití rep-pcr v bakteriální taxonomii Pavel Švec Česká sbírka mikroorganismů Přírodovědecká fakulta MU rep-pcr založeny na shlukové analýze PCR produktů získaných s primery komplementárními k rozptýleným
Využití rep-pcr v bakteriální taxonomii Pavel Švec Česká sbírka mikroorganismů Přírodovědecká fakulta MU rep-pcr založeny na shlukové analýze PCR produktů získaných s primery komplementárními k rozptýleným
NÁVOD K POUŽITÍ PRO HER2 DNA QUANTIFICATION KIT
 IČ: 80 DIČ: CZ80 sales@intellmed.eu NÁVOD K POUŽITÍ PRO HER DNA QUANTIFICATION KIT IČ: 80 DIČ: CZ80 sales@intellmed.eu OBSAH Návod k použití pro HER DNA QUANTIFICATION KIT.... Úvod.... Označení.... Rozsah
IČ: 80 DIČ: CZ80 sales@intellmed.eu NÁVOD K POUŽITÍ PRO HER DNA QUANTIFICATION KIT IČ: 80 DIČ: CZ80 sales@intellmed.eu OBSAH Návod k použití pro HER DNA QUANTIFICATION KIT.... Úvod.... Označení.... Rozsah
Specifická izolace microrna pomocí magnetizovatelných mikročástic
 Název: Školitel: Specifická izolace microrna pomocí magnetizovatelných mikročástic Veronika Vlahová Datum: 21. 3. 214 Reg.č.projektu: CZ.1.7/2.3./2.148 Název projektu: Mezinárodní spolupráce v oblasti
Název: Školitel: Specifická izolace microrna pomocí magnetizovatelných mikročástic Veronika Vlahová Datum: 21. 3. 214 Reg.č.projektu: CZ.1.7/2.3./2.148 Název projektu: Mezinárodní spolupráce v oblasti
CVD-T StripAssay. Kat. číslo 4-360. 20 testů 2-8 C
 CVD-T StripAssay Kat. číslo 4-360 20 testů 2-8 C Popis stripu Pracovní postup Izolace DNA Použijte čerstvou nebo zmraženou krev s EDTA nebo citrátem, jako antikoagulans, vyhněte se krvi s obsahem heparinu.
CVD-T StripAssay Kat. číslo 4-360 20 testů 2-8 C Popis stripu Pracovní postup Izolace DNA Použijte čerstvou nebo zmraženou krev s EDTA nebo citrátem, jako antikoagulans, vyhněte se krvi s obsahem heparinu.
