ZPRÁVA O STAVU PROJEKTU V ROCE 2016
|
|
|
- Vladislav Kučera
- před 6 lety
- Počet zobrazení:
Transkript
1 CAMELIA Datum vydání: 21-JUNE-2017 Zpráva 2016 Verze: 1 CAMELIA SK ZPRÁVA O STAVU PROJEKTU V ROCE 2016 Vydáno dne: 21-JUNE-2016 Autor: ing. Zlata Křístková Schválil: mgr. Marika Chrápavá Verze: 1 + Autor : Zlata Křístková Schválil : Marika Chrápavá Strana 1 (celkem 16)
2 CAMELIA Datum vydání: 16-JUNE-2017 Zpráva 2016 Verze: 1 ŘÍZENÍ DOKUMENTU Záznam změn Datum Autor Verze Popis změny 21-JUNE-2016 Křístková 1 Vytvoření dokumentu Recenzenti Jméno Mgr. Marika Chrápavá Pozice, firma Vedoucí oddělení projektového managementu Princip Tento dokument má dynamickou podstatu, to tedy znamená, že na jeho tvorbě může pracovat několik autorů i recenzentů současně s tím, že každá změna je zaznamenána. Informace o vývoji jsou průběžně doplňovány. Hlavní výhodou je jednotnost a transparentnost, současně odpadá množství nekonzistentních formátů a dokumentů. Autor : Zlata Křístková Schválil : Marika Chrápavá Strana 2 (celkem 16)
3 CAMELIA Datum vydání: 16-JUNE-2017 Zpráva 2016 Verze: 1 OBSAH SEZNAM ZKRATEK Účel dokumentu Základní charakteristika projektu Název projektu Základní charakteristika projektu Cíle projektu Spolupracující centra Etická komise Start projektu Průběh projektu v roce Organizační průběh projektu Setkání center Současný stav projektu Počet záznamů vyplněnost k Reporting Publikační aktivity analytické výstupy CRF Finanční report Hodnocení odborného garanta Hlášení nežádoucích účinků za rok Příloha 1 Struktura CRF Camelia SK Příloha 2 Analytická zpráva za rok Autor : Zlata Křístková Schválil : Marika Chrápavá Strana 3 (celkem 16)
4 CAMELIA Datum vydání: 16-JUNE-2017 Zpráva 2016 Verze: 1 SEZNAM ZKRATEK CML SLS TKI CRF VZP IMA DAS NIL chronická myeloidní leukémie slovenská lékařská společnost inhibitory tyrozinkináz case report form Všeobecná zdravotní pojišťovna imatinib dasatinib nilotinib Autor : Zlata Křístková Schválil : Marika Chrápavá Strana 4 (celkem 16)
5 CAMELIA Datum vydání: 16-JUNE-2017 Zpráva 2016 Verze: 1 1. Účel dokumentu Tento dokument podává souhrnnou zprávu o průběhu projektu CAMELIA SK v roce Hlavním cílem tohoto dokumentu je stručně popsat důležité události v projektu v daném roce. 2. Základní charakteristika projektu 2.1 Název projektu CAMELIA SK 2.2 Základní charakteristika projektu Projekt CAMELIA SK navazuje na úspěšný mezinárodní projekt CAMELIA. Jedná se o klinickou databázi pro sledování pacientů s chronickou myeloidní leukémií (Chronic MyEloid LeukemIA registry). Projekt CAMELIA se v roce 2015 rozštěpil na českou a slovenskou část, přičemž pro publikační účely je možné data z obou databázi i nadále spojovat. Registr Camelia SK slouží ke sběru a vyhodnocování základních epidemiologických a rozšířených klinických dat. Důraz je kladen zejména na hodnocení cytogenetických a molekulárně genetických parametrů. Otevřenost použitého on-line systému sběru a hodnocení dat pak umožňuje rozšiřování datové struktury pro sledování dalších specifických témat. Datová struktura projektu je nastavena pro spolupráci s dalšími regionálními klinickými databázemi a s mezinárodními projekty (European Leukemia Net, EUTOS). Za interpretaci údajů je odpovědná Odborná rada projektu, garantem je Slovenská hematologická a transfuziologická spoločnosť SLS. 2.3 Cíle projektu Primární cíl: Sledování všech pacientů s CML v zapojených hematoonkologických centrech, a to bez ohledu na způsob léčby, sběr a vyhodnocení epidemiologických údajů a údajů o diagnostice, léčbě a výsledcích léčby. Sekundární cíl: Vyhodnocení cytogenetických a molekulárních vyšetření pacientů Odpověď pacientů na léčbu se zaměřením na imatinib a nilotinib jako lék první volby pro farmakoterapii Monitorování pacientů s rezistencí na imatinib Využití výsledků k odborné diskusi týkající se léčby pacientů s CML v běžné klinické praxi Autor : Zlata Křístková Schválil : Marika Chrápavá Strana 5 (celkem 16)
6 CAMELIA Datum vydání: 16-JUNE-2017 Zpráva 2016 Verze: Spolupracující centra Na projektu Camelia SK v současnosti participuje 7 center, které se zabývají léčbou hematoonkologických onemocnění (Tabulka 1). Tabulka 1: Seznam center a kontaktních osob SK Č. Název centra Kontaktní osoba 1 Univerzitná nemocnica Bratislava, Klinika hematológie a transfuziológie 2 Národný onkologický ústav, Bratislava Hematologicko transfuz. oddelenie 4 Univerzitná nemocnica Martin, Klinika hematológie a transfuziológie 5 FNsP F.D.Roosevelta, Banská Bystrica, Hematologicko oddelenie 5 Univerzitná nemocnica L.Pasteura Košice, Klinika hematológie a onkohematológie 6 HEMKO s.r.o., Košice, Hematologická a onkohematologická ambulancia 7 FNsP J. A. Reimana Prešov Hematologické oddelenie MUDr. Zuzana Sninská, Ph. D. Prim. MUDr. Ľudmila Demitrovičová MUDr. Eva Mikušková, PhD. MUDr. Juraj Chudej, PhD. MUDr. Imrich Markuljak MUDr. Natália Štecová Prof. MUDr. Elena Tóthová, CSc. MUDr. Adriana Kafková, Ph.D. Prim. MUDr.Stanislav Palašthy zuzana.sninska@gmail.com ludmila.demitrovicova@nou.sk eva.mikuskova@nou.sk durochudej@pobox.sk markuljak@centrum.sk natalia.stecova@gmail.com etothova@post.sk kafkova1@post.sk palasthy@szm.sk Autor : Zlata Křístková Schválil : Marika Chrápavá Strana 6 (celkem 16)
7 CAMELIA Datum vydání: 16-JUNE-2017 Zpráva 2016 Verze: Etická komise Projekt, vč. protokolu a informovaného souhlasu, byl schválen multicentrickou etickou komisí při Univerzitné nemocnici Bratislava, Nemocnice sv. Cyrila a Metoda dne Start projektu Od svého zahájení v roce 2005 byl registr CAMELIA organizován jako mezinárodní projekt, zapojena byla hematoonkologická centra z České republiky a Slovenské republiky s cílem koordinovat postupy v léčbě CML s ohledem na mezinárodní doporučení a možnosti zapojených pracovišť. V současné době je projekt rozdělen na českou a slovenskou část, přičemž obě dvě části navazují na předchozí etapy společného projektu CAMELIA. Na Slovensku projekt sleduje léčbu CML u celé populace Slovenské republiky díky celkovému pokrytí specializovaných hematoonkologických center. Autor : Zlata Křístková Schválil : Marika Chrápavá Strana 7 (celkem 16)
8 CAMELIA Zpráva 2016 Datum vydání: 21-JUNE-2017 Verze: 1 3. Průběh projektu v roce Organizační průběh projektu Pro rok 2016 bylo podepsáno pokračování smlouvy se společností Novartis. Sběr dat probíhal kontinuálně po celý rok 2016 s nárůstem dat na závěr roku 2016 a v lednu roku Poté následovala etapa čištění a kontroly dat za rok 2016 z důvodu nastavení dalších validačních kritérií, které navrhli projektoví analytici IBA a schválila odborná garantka projektu. Etapa trvala od února 2017 do dubna V květnu 2017 byl zpracován sumární analytický report za rok Setkání center V rámci projektu CAMELIA SK proběhlo setkání center v Bratislave, kde bylo domluveno další pokračování projektu a byla podána informace o přijetí prezentace z dat registru Camelia SK na setkání American Society of Hematology konané v San Diegu ve dnech Současný stav projektu 4.1 Počet záznamů vyplněnost k Statistické výsledky projektu byly zpracovány na exportu k Celkový počet pacientů zadaných do registru byl 853, z toho bylo analyzováno 767 pacientů s potvrzenou Ph/BCR-ABL pozitivitou. Z tohoto počtu pacientů bylo 648 léčeno TKI (viz obr. 1 a obr. 2). Obrázek 1: Celkový počet pacientů v registru Camelia k Obrázek 2: Celkový počet pacientů léčených TKI Autor : Zlata Křístková Schválil : Marika Chrápavá Strana 8 (celkem 16)
9 CAMELIA Datum vydání: 16-JUNE-2017 Zpráva 2016 Verze: Reporting V projektu jsou nastaveny dva typy reportů: měsíční a kvartální Měsíční reporting: Sumarizace údajů o počtu aktuálně a celkově léčených pacientů za jednotlivá zapojená centra (viz obr. 1) Kvartální reporting: Sumarizace údajů o počtu aktuálně a celkově léčených pacientů za jednotlivá zapojená centra, včetně druhu a počtu založených formulářů (viz obr. 3). Obrázek 3: Ukázka kvartálního reportu: Autor : Zlata Křístková Schválil : Marika Chrápavá Strana 9 (celkem 16)
10 CAMELIA Datum vydání: 16-JUNE-2017 Zpráva 2016 Verze: Publikační aktivity analytické výstupy PUBLIKACE V roce 2016 byla přijata prezentace Treatment outcomes in patients treated with tyrosine kinase inhibitors in Slovak registry of chronic myeloid leukemia (Camelia SK) v posterové sekci na setkání American Society of Hematology (San Diego, ). Seznam všech publikací je na webových stránkách projektu : ANALÝZY Analytické zprávy z registru jsou vyvěšovány na stránkách projektu: CRF V průběhu roku 2016 byly provedeny úpravy a rozšíření povinných validačních položek v databázi. Vynucení vyplnění údajů (povinné položky) se týkají zejména následujících údajů: Formulář Léčebná odpověď: - LOP: Položka Molekulárně-genetická odpověď a Léčebná odpověď dle ELN LOP: kontrola, že pacient nemá současně vyplněno Hematologická progrese = ano a Hematologická odpověď = Kompletní Autor : Zlata Křístková Schválil : Marika Chrápavá Strana 10 (celkem 16)
11 CAMELIA Datum vydání: 16-JUNE-2017 Zpráva 2016 Verze: 1 - LOP: kontrola, že pacient nemá současně vyplněno Hematologická progrese = ano a Cytogenetická odpověď = Kompletní - LOP: kontrola, že pacient nemá současně vyplněno Hematologická progrese = ano a Molekulárně-genetická odpověď = VMR, MR4, MR4.5 nebo MR5 - LOP: kontrola, že pacient nemá současně vyplněno Cytogenetická progrese = ano a Cytogenetická odpověď = Kompletní - LOP: kontrola, že pacient nemá současně vyplněno Cytogenetická progrese = ano a Molekulárněgenetická odpověď = VMR, MR4, MR4.5 nebo MR5 - LOP: kontrola, že pacient nemá současně vyplněno Hematologická odpověď = Parciální nebo Není a Cytogenetická odpověď = Kompletní - LOP: kontrola, že pacient nemá současně vyplněno Hematologická odpověď = Parciální nebo Není a Molekulárně-genetická odpověď = VMR, MR4, MR4.5 nebo MR5 - LOP: kontrola, že pacient nemá současně vyplněno Cytogenetická odpověď = Není, Minimální, Malá nebo Velká a Molekulárně-genetická odpověď = VMR, MR4, MR4.5 nebo MR5 - Kontrola, že pacient má založený alespoň 1 formulář Léčebná odpověď/progrese - Stav při zahájení léčby při každém léčebném preparátu podle Aktualizace údajů Přehled léčby Formulář Aktualizace údajů: - Přidání nové povinné otázky Pořadí léčby do formuláře Aktualizace údajů Přehled léčby a do formuláře Léčebná odpověď/progrese - Hodnocení stavu - Kontrola aktualizace údajů u žijících pacientů v posledním roce (tzn., pokud K datu aktualizace pacient = Žije, pak Hodnocení pacienta k datu / poslední kontrola - Kontrola faktického založení formuláře - Aktualizace údajů Přehled léčby: kontrola, že Datum přerušení/ukončení léčby (dd.mm.rrrr) je větší než Datum zahájení léčby (dd.mm.rrrr) - Aktualizace údajů Přehled léčby: kontrola, že Datum zahájení léčby (dd.mm.rrrr) není v žádném z řádků prázdné - Aktualizace údajů Přehled léčby: kontrola, že Datum přerušení/ukončení léčby (dd.mm.rrrr) není prázdné v žádném z řádků předcházejících poslednímu řádku a že není prázdné v posledním řádku, pokud je otázka Léčba neprázdná (tzn. Léčba= Přerušena nebo Léčba= Ukončena ) - Aktualizace údajů: kontrola, že pokud K datu aktualizace pacient= Žije, Hodnocení pacienta k datu / poslední kontrola (dd.mm.rrrr) je větší nebo rovno maximum z Datum zahájení léčby (dd.mm.rrrr), maximum z Datum přerušení/ukončení léčby (dd.mm.rrrr), maximum z Datum hodnocení / zjištění změny (dd.mm.rrrr) z formuláře LOP, maximum z Datum nástupu nežádoucí příhody (dd.mm.rrrr) a maximum z Datum odeznění nežádoucí příhody (dd.mm.rrrr) z formuláře Nežádoucí příhoda, maximum z Datum transplantace (dd.mm.rrrr) z formuláře Transplantace, Datum diagnózy (dd.mm.rrrr) z formuláře Vstupní formulář Autor : Zlata Křístková Schválil : Marika Chrápavá Strana 11 (celkem 16)
12 CAMELIA Datum vydání: 16-JUNE-2017 Zpráva 2016 Verze: 1 - Aktualizace údajů: kontrola, že pokud K datu aktualizace pacient= Zemřel, Datum úmrtí (dd.mm.rrrr) je větší nebo rovno maximum z Datum zahájení léčby (dd.mm.rrrr), maximum z Datum přerušení/ukončení léčby (dd.mm.rrrr), maximum z Datum hodnocení / zjištění změny (dd.mm.rrrr) z formuláře LOP, maximum z Datum nástupu nežádoucí příhody (dd.mm.rrrr) a maximum z Datum odeznění nežádoucí příhody (dd.mm.rrrr) z formuláře Nežádoucí příhoda, maximum z Datum transplantace (dd.mm.rrrr) z formuláře Transplantace, Datum diagnózy (dd.mm.rrrr) z formuláře Vstupní formulář - Aktualizace údajů: kontrola, že pokud K datu aktualizace pacient= Ztracen ze sledování, Datum posledního kontaktu s pacientem je větší nebo rovno maximum z Datum zahájení léčby (dd.mm.rrrr), maximum z Datum přerušení/ukončení léčby (dd.mm.rrrr), maximum z Datum hodnocení / zjištění změny (dd.mm.rrrr) z formuláře LOP, maximum z Datum nástupu nežádoucí příhody (dd.mm.rrrr) a maximum z Datum odeznění nežádoucí příhody (dd.mm.rrrr) z formuláře Nežádoucí příhoda, maximum z Datum transplantace (dd.mm.rrrr) z formuláře Transplantace, Datum diagnózy (dd.mm.rrrr) z formuláře Vstupní formulář - kontrola, že pokud má pacient založený formulář Transplantace, tak má v Aktualizaci údajů Přehled léčby uvedenou léčbu transplantace - Aktualizace údajů: kontrola, že pacient má uvedeno Lék první volby maximálně u jednoho z preparátů (IMA/DAS/NIL) v položce Linie léčby inhibitory tyrosinkináz Formulář Nežádoucí příhoda - Doplnění povinné otázky: NP hlášena na SUKL ano/ne; přidání upozornění Hlášení NP v rámci registru Camelia SK nenahrazuje z legislativy plynoucí povinnost hlásit NP na ŠÚKL. Aktuální CRF je v Příloze č. 1 tohoto dokumentu. Autor : Zlata Křístková Schválil : Marika Chrápavá Strana 12 (celkem 16)
13 CAMELIA Datum vydání: 16-JUNE-2017 Zpráva 2016 Verze: 1 5. Finanční report Financování registru CAMELIA bylo v roce 2016 nastaveno dle podmínek stanovených ve Smlouvě o spolupráci ze dne Tabulka 3: Částky fakturované v roce na základě smlouvy z roku 2016 Služba Datum vystavení Částka (EUR) Etapa č. 1 Kontraktační řízení, protokol, překladové služby, smluvní kontraktace s investigátory, projektový managment, farmakovigilance první část, dílčí analytické výstupy (analýzy center), zpracování posteru, ecrf updatevalidace, služby HelpDesk) Etapa č.2 Náklady na realizaci sběru dat, reporting, Srážky na daň z příjmu Etapa č. 3 analýza dat, vypracování závěrečné zprávy, náklady na realizaci sběru dat - doplatek, farmakovigilance druhá část Srážky na daň z příjmu 191,9 Kontrola kvality dat a doplnění dat za období po zavedení validací v roce Za rok 2016 bylo v období celkem fakturováno ,-EUR za provoz registru a variabilní náklady. 6. Hodnocení odborného garanta Register CAMELIA SK monitoruje celoslovenskú populáciu pacientov s CML. Snahou je zachytiť do registra všetkých diagnostikovaných pacientov, avšak podľa incidencie a vekového priemeru a mediánu sa zdá, že stále nejakí pacienti v registri zahrnutí nie sú. Zbierajú sa základné epidemiologické a rozšírené klinické dáta. Vyhodnocuje sa dosiahnutie hemotologickej, cytogenetickej a molekulovej remisie v presne definovaných časových intervaloch, so zameraním na pacientov liečených inhibítormi tyrozínkinázy. Autor : Zlata Křístková Schválil : Marika Chrápavá Strana 13 (celkem 16)
14 CAMELIA Datum vydání: 16-JUNE-2017 Zpráva 2016 Verze: 1 Na projekte spolupracuje 7 centier, ktoré sa pravidelne zúčastňujú na organizovaných stretnutiach. V priebehu roku 2016 bola snaha o doplnenie všetkých dát u pacientov liečených inhibítormi tyrozínkinázy, pričom spracované dáta boli prijaté vo forme posteru na ASH V roku 2017 plánujeme pokračovať v ďalšom zbere dát a hodnotení liečebných odpovedí. Autor : Zlata Křístková Schválil : Marika Chrápavá Strana 14 (celkem 16)
15 CAMELIA Datum vydání: 16-JUNE-2017 Zpráva 2016 Verze: 1 8. Hlášení nežádoucích účinků za rok 2016 Hlášení Nežádoucích účinků probíhá dle Smlouvy o hlášení nežádoucích účinků ze dne a ze dne V roce 2016 bylo nahlášeno 31 nežádoucích příhod, z toho bylo 16 NP klasifikováno jako SAE a 15 případů klasifikováno jako AE. VĚK/ POHLA VÍ TYP/ POPIS NU ODESLAN É DO NOVARTI SU ID NP 43/F AE/ nehematologická toxicita, otok periférií G /M AE/ nehematologická toxicita, hepatotoxicita G /F AE/ nehematologická toxicita, infekce G /M AE/ hematologická toxicita, anémie G2, neutropenie G3, trombocytopenie G /M SAE/ hematologická toxicita, anémie G3, neutropenie G3, trombocytopenie G4 myelodysplastický syndróm /F SAE/ hematologická toxicita, anémie G2, trombocytopenie G3 transfúzie Ery a Tr /F AE/ nehematologická toxicita, hepatopatia G /M SAE/ nehematologická toxicita G3 chabá paraparéza DK nejasnej eti, závažná sekundárna spinálna stenóza segmentov L2-S1, neuropatia DK ťažkého stupňa 48/F AE/Nehematologická toxicita, dermatitida, G /F AE/Nehematologická toxicita, lumboischiadický syndróm,lumbalgia, G /M SAE/Nehematologická toxicita, Úraz s flegmónou a s následnou amputáciou palca nal.nohe /M AE/Nehematologická toxicita, Chirurgická-Histologicky potvrdený tubulovilozny adenóm rekta-bez dysplazie /M SAE/Nehematologická toxicita, fraktura stavca L1, G /M SAE/Nehematologická toxocita, slabosť, dušnosť, G /F SAE/Hematologická toxicita, Anémie-G4, Neutropénie-G4úmrtí, Trombocytopénie-G /F SAE/Hematologická toxicita, Trombocytopénie, G /M SAE/Hematologická toxicita, Trombocytopénie, G /M SAE/Nehematologická toxicita, CMP hemoragická v oblasti mozočka, Otok priférií-g3, Bolest hlavy-g3, Krvácení-G1, Nevolnost a zvracení-g3 50/M AE/Nehematologická toxicita, Hepatotoxicita vs.polieková, G /M AE/Nehematologická toxicita, Průjem-G2, Kožní toxicita-g Autor : Zlata Křístková Schválil : Marika Chrápavá Strana 15 (celkem 16)
16 CAMELIA Datum vydání: 16-JUNE-2017 Zpráva 2016 Verze: 1 66/F AE/Nehematologická toxicita, Hraničná hodnota bilirubinu priamy a nepriamy, G /M AE/Nehematologická toxicita, Histologicky potvrdený tubulovilozny adenóm rekta-bez dysplazie /F SAE/Hematologická toxicita, úmrtí, Anémie-G4, Neutropénie-G4, Trombocytopénie-G /F SAE/Hematologická toxicita, Trombocytopénie-G /M SAE/Hematologická toxicita, Trombocytopénie-G /M SAE/Nehematologická toxicita, CMP hemoragická v oblasti mozočka /M AE/Nehematologická toxicita, hepatotoxicita vs.polieková-g /M AE/Nehematologická toxicita, črevná viróza /F AE/Nehematologická toxicita, hyperbilirubinemia hraničné hodnoty /F Úmrtí/Pneumonia /M Úmrtí/Jiná Příloha 1 Struktura CRF Camelia SK Příloha 2 Analytická zpráva za rok 2016 Obě přílohy Závěrečné zprávy jsou samostatnými dokumenty. Autor : Zlata Křístková Schválil : Marika Chrápavá Strana 16 (celkem 16)
17 Příloha č.1 Struktura CRF CAMELIA II SK Vstupní formulář 1. Základní záznam 1. *Typ záznamu (výběr) default 1. Základní 2. Rozšířený 2. Datum diagnózy (dd.mm.rrrr) (datum) abs. min:" " 3. *Fáze onemocnění v době diagnózy (výběr) 1. Chronická fáze 2. Akcelerovaná fáze 3. Blastický zvrat 2. Kritéria pro fáze onemocnění:<ul><li>chronická fáze: < 5 % blastů v KD nebo PK, < 15 % blastů + promyelocytů v KD nebo PK, < 20 % bazofilů v PK, 100 trombocytů, nepřítomnost extramed. leukemické infiltrace, s výjimkou HSM</li><li>Akcelerovaná fáze: 10 % - 19 % blastů v KD nebo PK, > 20 % bazofilů v PK, < 100 x 10^9/l trombocytů bez vztahu k terapii, klonální chrom. abnormality v Ph+ buňkách</li><li>blastický zvrat: 20 % blastů v KD nebo PK, extramedulární blastické postižení</li></ul> 1. *Ph / bcr-abl pozitivita potvrzena (ano/ne) 2. Převádět do EuroCML (ano/ne) 3. PSČ bydliště (text) 3. Informovaný souhlas 1. Podepsal pacient informovaný souhlas? (ano/ne) 2. Datum podpisu souhlasu (dd.mm.rrrr) (datum) abs. min:" " 4. Základní údaje pacienta 1. Země narození (výběr) 1. Česká republika 2. Slovenská republika 3. Polsko 4. Ukrajina 5. Jiná 2. Jiná země narození (text) 3. Kouření (výběr) kuřák 2. Kuřák 3. Stop kuřák 4. Neznámo 4. Počet cigaret denně u současného kuřáka (číslo) abs. min:1 max: Rodinný stav (výběr) 1. Nikdy nebyl/a ženatý/vdaná 2. Ženatý/vdaná 3. Rozvedený/á 4. Vdovec/vdova
18 6. Žije pacient v současnosti s partnerem? (výběr) 1. Ano 2. Ne 3. Neznámo 7. Nejvyšší vzdělání (výběr) 1. Základní 2. Střední 3. Vysokoškolské 4. Neznámo 8. Zaměstnání (výběr) zaměstnaný 2. Zaměstnaný na plný úvazek 3. Zaměstnaný na částečný úvazek 4. Neznámo 5. Komorbidity 1. Komorbidity (výběr) 1. Ano 2. Ne 3. Neznámo 2. Neurologické (ano/ne) default 3. Kardiovaskulární (ano/ne) default 4. Hypertenze (ano/ne) default 5. Diabetes (ano/ne) default 6. Chronické onemocnění jater (ano/ne) default 7. Chronické renální onemocnění (ano/ne) default 8. Porucha chování (ano/ne) default 9. Další (ano/ne) default 10. Další - jaké (text) 6. Klinické vyšetření 1. Datum vyšetření (dd.mm.rrrr) (datum) abs. min:" " 2. Symptomy (výběr) 2. Ano 3. Neznámo 3. Úbytek hmotnosti (checkbox) 4. Horečka (checkbox) 5. Bolest břicha (checkbox) 6. Bolest kostí (checkbox) 7. Únava (checkbox) 8. Infekce (checkbox) 9. Hemoragický syndrom (checkbox) 10. Další (checkbox) 11. Specifikujte další symptomy (text) 7. <p> 1. Hmotnost (kg) (desetinné číslo - přesnost: 0) abs. min:0 abs. max:200 min:30 2. Výška (cm) (číslo) abs. min:10 abs. max:300 min:50 max: ECOG/WHO skóre (výběr) Asymptomatický Symptomatický, ale kompletně pohyblivý Symptomatický, < 50% leží v průběhu dne Symptomatický, > 50% leží, ale není upoután na lůžko Upoután na lůžko
19 Úmrtí Neznámo 4. Karnofsky index (výběr) 1. NA - neznámo Pacient je moribundní (pomalu umírá), nemoc rychle pokračuje a léčení nezaznamenává účinné zlepšení (nepomáhá) Pacient je velmi těžce nemocen, je u něho nutná hospitalizace, odborná péče a aktivní podpůrná léčba Pacient je vážně nemocen, nutná je odborná péče a podpůrná léčba, hospitalizace je u něho indikována Pacient je trvale upoután na lůžko, potřebuje nutně lékařskou odbornou péči Omezená výkonnost pacienta, ten není trvale upoután na lůžko, potřebuje však ošetřovatelskou a lékařskou péči Omezená výkonnost pacienta, ten však občas potřebuje cizí pomoc Omezená výkonnost pacienta, samoobslužnost zachována, práceschopnost pacienta Omezená výkonnost pacienta, avšak s vypětím, drobné příznaky nemoci Omezená výkonnost pacienta, minimální projevy choroby Normální stav pacienta, neprojevují se žádné potíže 5. Slezina přesahuje pod žeberní oblouk (cm) (desetinné číslo - přesnost: 0) abs. min:0 abs. max:50 6. Má pacient extramedulární manifestaci onemocnění (mimo jater a sleziny)? (výběr) známo 2. Ano 3. Ne 7. Extramedulární manifestace onemocnění (výběr) 1. Kožní 2. Lymfoidní 3. Kostní 4. CNS 5. Jiné 8. KO + dif. 1. Datum laboratorního vyšetření (dd.mm.rrrr) (datum) abs. min:" " 2. Leukocyty (10e9/l) (desetinné číslo - přesnost: 0) abs. min:0 3. Trombocyty (10e9/l) (desetinné číslo - přesnost: 0) abs. min:0 4. Hemoglobin (g/l) (desetinné číslo - přesnost: 0) abs. min:0 5. Hematokrit (%) (desetinné číslo - přesnost: 0) abs. min:0 min:0 max: MCV (fl) (desetinné číslo - přesnost: 0) abs. min:0 7. Normoblasty (na 100 leu) (desetinné číslo - přesnost: 0) abs. min:0 8. Lymfocyty (%) (desetinné číslo - přesnost: 0) abs. min:0 min:0 max: Monocyty (%) (desetinné číslo - přesnost: 0) abs. min:0 min:0 max: Eozinofily (%) (desetinné číslo - přesnost: 0) abs. min:0 min:0 max: Bazofily (%) (desetinné číslo - přesnost: 0) abs. min:0 min:0 max: Segmenty (%) (desetinné číslo - přesnost: 0) abs. min:0 min:0 max: Tyčky (%) (desetinné číslo - přesnost: 0) abs. min:0 min:0 max: Metamyelocyty (%) (desetinné číslo - přesnost: 0) abs. min:0 min:0 max: Myelocyty (%) (desetinné číslo - přesnost: 0) abs. min:0 min:0 max: Promyelocyty (%) (desetinné číslo - přesnost: 0) abs. min:0 min:0 max: Blasty (%) (desetinné číslo - přesnost: 0) abs. min:0 min:0 max: HLA 1. *HLA vyšetřeno (výběr) 1. Ano
20 2. Ne 2. Byl nalezen HLA identický dárce (výběr) 1. Ano 2. Ne 3. Nalezený dárce (výběr) 1. Příbuzenský 2. Nepříbuzenský 10. Cytologie KD 1. *Vyšetření provedeno (ano/ne) default 2. Datum odběru materiálu (dd.mm.rrrr) (datum) abs. min:" " výpočet 3. Celularita (výběr) stanovena 2. Nízká 3. Normální 4. Vysoká 5. Suchá punkce 4. Blasty (%) (desetinné číslo - přesnost: 0) abs. min:0 min:0 max: Promyelocyty (%) (desetinné číslo - přesnost: 0) abs. min:0 min:0 max: Bazofily (%) (desetinné číslo - přesnost: 0) abs. min:0 min:0 max: Eozinofily (%) (desetinné číslo - přesnost: 0) abs. min:0 min:0 max: Provedena trepanobiopsie (ano/ne) default 9. Dřeňová fibróza (výběr) zadáno 2. Přítomna 3. Nepřítomna 11. Prognostické indexy 1. Věk při diagnóze (roky) (číslo) abs. min:0 výpočet 2. Sokalův index (desetinné číslo - přesnost: 2) výpočet 3. Sokalův index - stupeň rizika (text) výpočet read-only 4. Hasfordův index (EURO SCORE) (desetinné číslo - přesnost: 2) výpočet 5. Hasfordův index - stupeň rizika (text) výpočet read-only 12. <a target="_blank" href=" and_sokal_score/index_eng.html">cml rizikové indexy</a> 1. EUTOS Score (desetinné číslo - přesnost: 2) abs. min:0 min:0 výpočet 2. EUTOS Score - stupeň rizika (text) výpočet read-only 13. <a target="_blank" href=" Score</a> 14. Klasická cytogenetika 1. Datum prvního cytogenetického vyšetření (dd.mm.rrrr) (datum) abs. min:" " 2. *Vyšetření provedeno (ano/ne) default 3. Vyšetřený materiál (výběr) 1. Kostní dřeň 2. Periferní krev 4. Datum odběru materiálu (dd.mm.rrrr) (datum) abs. min:" " výpočet 5. Počet vyšetřených metafází (číslo) abs. min:0 6. Ph chromozom (výběr) 2. Ano 3. Komplexní (variantní) translokace 7. Počet metafází s Ph chromozomem (číslo) abs. min:0 výpočet 8. Procento Ph mitóz (desetinné číslo - přesnost: 0) abs. min:0 výpočet
21 9. Chromozomy zahrnuté do komplexní translokace (text) 10. Přídatné chromozomové změny (výběr) 11. Přídatné změny zjištěny metodou (výběr) 1. Klasická cytogenetika 2. FISH 12. Specifikujte přídatné změny (karyotyp) (text) (výběr) default (výběr) default 15. +Ph (výběr) default 16. i(17q) (výběr) default 17. -Y (výběr) default 18. t(3;21) (výběr) default (výběr)
22 (výběr) default (výběr) default (výběr) default 23. Jiné změny (výběr) default 24. Specifikujte jiné změny (text) 15. FISH 1. *Vyšetření provedeno (ano/ne) default 2. Vyšetřený materiál (výběr) 1. Kostní dřeň 2. Periferní krev 3. Datum odběru materiálu (dd.mm.rrrr) (datum) abs. min:" " výpočet 4. Počet bcr/abl pozitivních buněk (číslo) abs. min:0 5. Počet vyšetřených buněk (číslo) abs. min:0 6. Procento bcr/abl pozitivních buněk (desetinné číslo - přesnost: 0) abs. min:0 výpočet 7. Del 5 abl (výběr) vyšetřeno 2. Ano 3. Ne 8. Del 3 BCR (výběr) vyšetřeno 2. Ano 3. Ne 9. M-FISH (ano/ne) 10. Vypište konečný karyotyp (text) 16. RT-PCR 1. *Vyšetření provedeno (ano/ne) default 2. Datum odběru materiálu (dd.mm.rrrr) (datum) abs. min:" " výpočet 3. Vyšetřený materiál (výběr) 1. Kostní dřeň 2. Periferní krev 4. Výsledek RT-PCR (výběr)
23 1. Pozitivní 2. Negativní 5. Typ transkriptu (výběr) 1. b2a2 2. b3a2 3. b2a3 4. Jiný 6. Specifikujte jiný typ transkriptu (text) 17. QRT-PCR 1. *Vyšetření provedeno (ano/ne) default 2. Metoda (výběr) 1. Q-RT-PCR 2. Real Time (Light Cycler) 3. Vyšetřený materiál (výběr) 1. Kostní dřeň 2. Periferní krev 4. Datum odběru materiálu (dd.mm.rrrr) (datum) abs. min:" " výpočet 5. Kontrolní gen (výběr) 1. ABL 2. ß2M 3. GUS 4. BCR 5. Jiný 6. Neznámý 6. Kontrolní gen - specifikujte (text) 7. BCLR-ABL/kontrolní gen (%) (desetinné číslo - přesnost: 4) abs. min:0 min:0 max: Hodnoceno dle mezinárodní standardní stupnice? (výběr) 1. Ano 2. Ne 3. Neznámo Aktualizace údajů 18. Aktualizace údajů 1. *Hodnocení pacienta k datu / poslední kontrola (dd.mm.rrrr) (datum) abs. min:" " 19. Zařazení do klinické studie 1. Byl pacient zařazen do klinické studie? (výběr) 1. Ano 2. Ne 3. Neznámo 20. Investigator sponsored trial 1. Investigator sponsored trial (ano/ne) 2. Investigator sponsored trial - specifikujte označení studie (text) 21. Company sponsored trial 1. Company sponsored trial (ano/ne) 2. Company sponsored trial - specifikujte označení studie (text) 22. Přehled léčby 1. *Pořadí léčby (číslo) abs. min:1 abs. max: *Typ léčby (výběr) 1. Hydroxyurea 2. Interferon
24 3. Imatinib 4. Transplantace 5. Kombinovaná CHT 6. Jiná 7. Nilotinib 8. Dasatinib 9. Bosutinib 10. Imatinib - generikum 11. Ponatinib 12. Bez léčby 3. Léčba v kombinaci s (výběr) 1. Hydroxyurea 2. Interferon 3. Transplantace 4. Kombinovaná CHT 5. Jiná 6. Nilotinib 7. Dasatinib 8. Ponatinib 9. Bez kombinace 4. Specifikace jiné léčby (text) 5. Datum zahájení léčby (dd.mm.rrrr) (datum) abs. min:" " 6. Dávkování imatinibu (výběr) mg/d mg/d mg/d 4. Jiné 7. Dávkování nilotinibu (výběr) mg/d mg/d mg/d 4. Jiné 8. Dávkování dasatinibu (výběr) mg/d mg/d mg/d mg/d 5. Jiné 9. Dávkování jiné léčby nebo specifikace jiného dávkování imatinibu, dasatinibu, nilotinibu, ponatinibu nebo bosutinibu (text) 10. Důvod nasazení léčby (při zahájení/změně typu léčby) (výběr) 1. První linie léčby 2. Rezistence předchozí léčby 3. Intolerance předchozí léčby 4. Studie 5. Jiný 11. Léčba (výběr) 1. Přerušena 2. Ukončena 12. Datum přerušení/ukončení léčby (dd.mm.rrrr) (datum) abs. min:" " 13. Důvod přerušení léčby (výběr) 1. Progrese
25 2. Rezistence bez progrese 3. Nežádoucí příhoda 4. Odmítnutí 5. Remise 6. Jiný 14. Jiný důvod přerušení léčby - specifikujte (text) 15. Důvod úplného ukončení léčby (výběr) 1. Hematologická rezistence/progrese 2. Cytogenetická rezistence/progrese 3. Molekulární rezistence/progrese 4. Nežádoucí příhody 5. Progrese onemocnění do AF/BZ 6. Alogenní transplantace 7. Úmrtí 8. Jiný 16. Jiný důvod úplného ukončení léčby - specifikujte (text) 17. Byla během léčby zaznamenána NP? (ano/ne) 23. Linie léčby inhibitory tyrosinkináz 1. Linie léčby imatinibem (výběr) 1. Lék první volby 2. Pro selhání nebo netoleranci jiné léčby 2. Linie léčby dasatinibem (výběr) 1. Lék první volby 2. Pro selhání nebo netoleranci jiné léčby 3. Linie léčby nilotinibem (výběr) 1. Lék první volby 2. Pro selhání nebo netoleranci jiné léčby 24. Aktuální stav pacienta 1. *K datu aktualizace pacient (výběr) 1. Žije 2. Zemřel 3. Ztracen ze sledování 25. Pacient zemřel 1. *Datum úmrtí (dd.mm.rrrr) (datum) abs. min:" " 2. *Příčina úmrtí (výběr) 1. Progrese onemocnění (AF/BZ) 2. Základní onemocnění (CML) 3. Úmrtí spojené s transplantací 4. Přidružené onemocnění 5. Jiná 3. Příčina úmrtí - přidružené onemocnění (text) 4. Příčina úmrtí - transplantace (výběr) 1. Úmrtí spojené s transplantací 2. Infekce 3. GvHD 26. Pokud úmrtí pacienta může souviset s podáním imatinibu nebo jiného léčivého přípravku, vyplňte prosím formulář Nežádoucí příhoda. <p></p> 27. Pacient ztracen ze sledování 1. Datum posledního kontaktu s pacientem (datum) abs. min:" " 2. Důvod ztráty follow-up (text) 28. CML a reprodukce 1. Potomek u CML pacienta muže po diagnóze CML (checkbox)
26 2. Těhotenství u CML pacientky ženy (checkbox) Léčebná odpověď/progrese 29. Hodnocení stavu 30. <b>frekvence hodnocení stavu pacienta</b></p><i>- po zahájení léčby TKI v jakékoliv linii či po transplantaci musí být vyplněno hodnocení v 3., 6., 12., 18., 24. měsíci a dále á 1 rok<br>ostatní: á 1 rok<br>- při změně stavu (léčebná odpověď/progrese): ihned! <br></i><p><font color=#cc0000>upozornění: pro správnou funkci automatických výpočtů je nutné vyplňovat formuláře v pořadí odpovídajícím průběhu léčby <br>(tj. nejprve stav při zahájení léčby, poté např. hodnocení po 14 dnech a až pak např. hodnocení po 1 měsíci)</font></p> 1. *Hodnocení stavu pacienta - vztah k léčbě (výběr) 1. Odpověď na probíhající léčbu 2. Stav při zahájení léčby 2. *Datum hodnocení / zjištění změny (dd.mm.rrrr) (datum) abs. min:" " 3. Datum zahájení léčby daným preparátem (dd.mm.rrrr) (datum) výpočet read-only 4. Čas sledování při probíhající léčbě (měsíce) (desetinné číslo - přesnost: 0) výpočet read-only 5. *Pořadí léčby (číslo) abs. min:1 abs. max: Typ léčby (výběr) 1. Imatinib 2. Imatinib - generikum 3. Dasatinib 4. Nilotinib 5. Transplantace 6. Bosutinib 7. Ponatinib 8. Jiná léčba 7. Jiná léčba - specifikace (text) 8. Fáze CML při zahájení léčby (výběr) 1. Chronická fáze 2. Akcelerace 3. Blastický zvrat 31. Pomocná otázka pro zpětné doplnění Stavu při zahájení léčby 1. Jsou zpětně dostupné všechny informace při zahájení léčby? (ano/ne) 32. Hematologická odpověď/progrese 1. *Hematologická odpověď (výběr) ní 2. Parciální 3. Kompletní 4. Nehodnoceno 2. *Hematologická progrese (výběr) 1. Ano 2. Ne 3. Nehodnoceno 3. Hematologická progrese do fáze (výběr) 1. Chronická fáze 2. Akcelerovaná fáze 3. Blastický zvrat 33. Kompletní hematologická odpověď (remise) = CHR<p>- leukocyty < 10 x 10^9/l<br> - trombocyty < 450 x 10^9/l<br>- žádné nezralé formy granulocytů v dif. KO (tj. blasty, promyelocyty a myelocyty)<br> - bazofilů < 5 % v PK<br>- nehmatná slezina<p>parciální
27 hematologická odpověď (remise) = PHR<p>- zlepšení sledovaných parametrů o více než 50% vstupní hodnoty 34. KO + dif. 1. *Datum provedení vyšetření (dd.mm.rrrr) (datum) abs. min:" " 2. *Leukocyty (10e9/l) (desetinné číslo - přesnost: 0) abs. min:0 3. *Trombocyty (10e9/l) (desetinné číslo - přesnost: 0) abs. min:0 4. *Hemoglobin (g/l) (desetinné číslo - přesnost: 0) abs. min:0 5. *MCV (fl) (desetinné číslo - přesnost: 0) abs. min:0 6. Záznam KO při patologickém nálezu pro specifická hodnocení (ano/ne) 7. Hematokrit (%) (desetinné číslo - přesnost: 0) abs. min:0 min:0 max: Normoblasty (na 100 leu) (desetinné číslo - přesnost: 0) abs. min:0 9. Lymfocyty (%) (desetinné číslo - přesnost: 0) abs. min:0 min:0 max: Monocyty (%) (desetinné číslo - přesnost: 0) abs. min:0 min:0 max: Eozinofily (%) (desetinné číslo - přesnost: 0) abs. min:0 min:0 max: Bazofily (%) (desetinné číslo - přesnost: 0) abs. min:0 min:0 max: Segmenty (%) (desetinné číslo - přesnost: 0) abs. min:0 min:0 max: Tyčky (%) (desetinné číslo - přesnost: 0) abs. min:0 min:0 max: Metamyelocyty (%) (desetinné číslo - přesnost: 0) abs. min:0 min:0 max: Myelocyty (%) (desetinné číslo - přesnost: 0) abs. min:0 min:0 max: Promyelocyty (%) (desetinné číslo - přesnost: 0) abs. min:0 min:0 max: Blasty (%) (desetinné číslo - přesnost: 0) abs. min:0 min:0 max: Cytologie KD 1. Záznam cytologie KD pro specifická hodnocení (ano/ne) 2. *Vyšetření provedeno (ano/ne) default 3. Datum odběru materiálu (dd.mm.rrrr) (datum) abs. min:" " 4. Celularita (výběr) stanovena 2. Nízká 3. Normální 4. Vysoká 5. Suchá punkce 5. Blasty (%) (desetinné číslo - přesnost: 0) abs. min:0 min:0 max: Promyelocyty (%) (desetinné číslo - přesnost: 0) abs. min:0 min:0 max: Bazofily (%) (desetinné číslo - přesnost: 0) abs. min:0 min:0 max: Eozinofily (%) (desetinné číslo - přesnost: 0) abs. min:0 min:0 max: Provedena trepanobiopsie (ano/ne) default 10. Dřeňová fibróza (výběr) zadáno 2. Přítomna 3. Nepřítomna 36. Klasická cytogenetika 1. *Vyšetření provedeno (ano/ne) default 2. Vyšetřený materiál (výběr) 1. Kostní dřeň 2. Periferní krev 3. Datum odběru materiálu (dd.mm.rrrr) (datum) abs. min:" " výpočet 4. Počet vyšetřených metafází (číslo) abs. min:0 5. Ph chromozom (výběr) 2. Ano 3. Komplexní (variantní) translokace 6. Počet metafází s Ph chromozomem (číslo) abs. min:0 výpočet
28 7. Procento Ph mitóz (desetinné číslo - přesnost: 0) abs. min:0 výpočet 8. Chromozomy zahrnuté do komplexní translokace (text) 9. Přídatné chromozomové změny (výběr) 10. Přídatné změny zjištěny metodou (výběr) 1. Klasická cytogenetika 2. FISH 11. Specifikujte přídatné změny (karyotyp) (text) (výběr) default (výběr) default 14. +Ph (výběr) default 15. i(17q) (výběr) default 16. -Y (výběr) default 17. t(3;21) (výběr) default (výběr)
29 (výběr) default (výběr) default (výběr) default 22. Jiné změny (výběr) default 23. Specifikujte jiné změny (text) 37. FISH 1. *Vyšetření provedeno (ano/ne) default 2. Vyšetřený materiál (výběr) 1. Kostní dřeň 2. Periferní krev 3. Datum odběru materiálu (dd.mm.rrrr) (datum) abs. min:" " výpočet 4. Počet bcr/abl pozitivních buněk (číslo) abs. min:0 5. Počet vyšetřených buněk (číslo) abs. min:0 6. Procento bcr/abl pozitivních buněk (desetinné číslo - přesnost: 0) abs. min:0 výpočet 7. Del 5 abl (výběr) vyšetřeno 2. Ano 3. Ne 8. Del 3 BCR (výběr) vyšetřeno 2. Ano 3. Ne 9. M-FISH (ano/ne) 10. Vypište konečný karyotyp (text) 38. RT-PCR 1. *Vyšetření provedeno (ano/ne) default 2. Datum odběru materiálu (dd.mm.rrrr) (datum) abs. min:" " výpočet 3. Vyšetřený materiál (výběr) 1. Kostní dřeň 2. Periferní krev
30 4. Výsledek RT-PCR (výběr) 1. Pozitivní 2. Negativní 5. Typ transkriptu (výběr) 1. b2a2 2. b3a2 3. b2a3 4. Jiný 6. Specifikujte jiný typ transkriptu (text) 39. QRT-PCR 1. *Vyšetření provedeno (ano/ne) default 2. Metoda (výběr) 1. Q-RT-PCR 2. Real Time (Light Cycler) 3. Vyšetřený materiál (výběr) 1. Kostní dřeň 2. Periferní krev 4. Datum odběru materiálu (dd.mm.rrrr) (datum) abs. min:" " výpočet 5. Počet kopií kontrolního genu (číslo) abs. min:0 6. BCLR-ABL/kontrolní gen (%) (desetinné číslo - přesnost: 4) abs. min:0 min:0 max: Hodnoceno dle mezinárodní standardní stupnice? (výběr) 1. Ano 2. Ne 3. Neznámo 40. Mutační analýza 1. Datum provedení mutační analýzy (dd.mm.rrrr) (datum) abs. min:" " 2. Typ mutace (výběr) gativní výsledek 2. T315I 3. Y253F/H 4. E255K/V 5. Q252H 6. F359C/V 7. F486S 8. F317L 9. L248V 10. G250E 11. D276G 12. E279K 13. V299L 14. M351T 15. L384M 16. H396P/R 17. G398R 18. Jiná 3. Typ mutace - specifikujte (text) 4. % mutovaných buněk (desetinné číslo - přesnost: 2) abs. min:0 min:0 max: Cytogenetická odpověď / progrese a molekulárně-genetická odpověď / progrese 42. Kriteria hodnocení léčebných odpovědí: <br><a target="_blank" href="
31 UPDATE2013_English.pdf">ELN 2013</a><br><a target="_blank" href="cmlsk_kriteria_odpovedi_2013.pdf">souhrn</a> 1. Klasická cytogenetika - datum minulého odběru (dd.mm.rrrr) (datum) default abs. min:" " 2. Minulé procento Ph mitóz (desetinné číslo - přesnost: 0) default abs. min:-1 min:0 3. FISH - datum minulého odběru (dd.mm.rrrr) (datum) default abs. min:" " 4. FISH - minulé procento bcr/abl pozitivních buněk (desetinné číslo - přesnost: 0) default abs. min:-1 min:0 5. *Cytogenetická odpověď (výběr) default výpočet ní 2. Minimální 3. Malá 4. Velká 5. Kompletní 6. Nehodnoceno 6. *Cytogenetická progrese (výběr) default výpočet 1. Ano 2. Ne 3. Nehodnoceno 7. Cytogenetická odpověď nebo progrese hodnocena (ano/ne) výpočet 8. Cytogenetická odpověď / progrese hodnocena metodou (výběr) výpočet 1. Klasická cytogenetika 2. FISH 9. QRT-PCR - datum minulého odběru materiálu (dd.mm.rrrr) (datum) default abs. min:" " 10. QRT-PCR - minulé (%) (desetinné číslo - přesnost: 4) default abs. min:-1 min:0 11. *Molekulárně-genetická odpověď (výběr) výpočet dosáhnutá 2. Nehodnotitelné 3. VMR 4. MR4 5. MR MR5 12. *Léčebná odpověď dle ELN 2013 (výběr) 1. Optimální 2. Varovné znaky 3. Selhání léčby 43. Pokud je pacient léčen ve 2. linii po selhání imatinibu, můžete odpověď ručně upravit dle <a target="_blank" href="cmlsk_kriteria_odpovedi_2013.pdf"> kritérií hodnocení léčebných odpovědí [3. tabulka na str. 2]</a>. Nežádoucí příhoda 44. Hlášení AE 1. *Datum nástupu nežádoucí příhody (dd.mm.rrrr) (datum) abs. min:" " 2. *Datum odeznění nežádoucí příhody (dd.mm.rrrr) (datum) abs. min:" " 3. V době vyplňování formuláře nežádoucí příhoda stále přetrvává (checkbox) 45. Léčba 1. *Typ léčby v době začátku nežádoucí příhody (výběr) 1. Hydroxyurea 2. Interferon 3. Imatinib
32 4. Transplantace 5. Kombinovaná CHT 6. Jiná 7. Nilotinib 8. Dasatinib 9. Bosutinib 10. Imatinib - generikum 11. Ponatinib 12. Bez léčby 2. *Léčba v kombinaci s (výběr) 1. Hydroxyurea 2. Interferon 3. Transplantace 4. Kombinovaná CHT 5. Jiná 6. Nilotinib 7. Dasatinib 8. Ponatinib 9. Bez kombinace 3. *Specifikace jiné léčby (text) 4. *Dávkování (včetně jednotek) (text) 5. *Může nežádoucí příhoda souviset s podávaným preparátem? (výběr) 1. Ano 2. Ne 3. Nevím 6. *Přerušení/ukončení léčby z důvodu nežádoucí příhody (ano/ne) 7. *Úprava dávkování kvůli nežádoucí příhodě (ano/ne) 46. Typ nežádoucí příhody 1. *Typ nežádoucí příhody (výběr) hematologická toxicita 2. Hematologická toxicita 3. Nehematologická i hematologická toxicita 47. Závažnost nežádoucí příhody 1. *Byla/je nežádoucí příhoda závažná (SAE)? (výběr) 1. Ano 2. Ne 3. Nevím 2. Pacient zemřel (checkbox) 3. Došlo k ohrožení života (checkbox) 4. Přijat do nemocnice nebo hospitalizace prodloužena (checkbox) 5. Došlo k trvalé invaliditě nebo významnému omezení aktivity (checkbox) 6. Teratogenní účinky (checkbox) 7. Jiná lékařsky významná událost (checkbox) 8. *Datum přijetí do nemocnice (dd.mm.rrrr) (datum) abs. min:" " 48. Vývoj stavu pacienta 1. *Vývoj stavu pacienta (s ohledem na nežádoucí příhodu) (výběr) žádoucí příhoda odezněla 2. Nežádoucí příhoda přetrvává 3. Došlo ke zlepšení stavu 4. Došlo ke zhoršení stavu 5. Pacient zemřel 6. Neznámo
33 2. *Byla poskytnuta léčba z důvodu nežádoucí příhody (ano/ne) 3. *Specifikace léčby nežádoucí příhody (text) 4. Poznámky (text) 5. *NP hlášena na ŠÚKL (ano/ne) 6. *Za pravdivost a úplnost informací o nežádoucí příhodě odpovídá (jméno a příjmení lékaře) (text) 7. Tel. kontakt nebo na odpovědného lékaře (text) 49. Hlášení NP v rámci registru Camelia SK nenahrazuje z legislativy plynoucí povinnost hlásit NP na ŠÚKL. 50. Detailní popis nežádoucí příhody 51. <a target="_blank" href=" toxicity Criteria (CTC)</a><br><br>Nehematologická toxicita 1. Otok periferií (checkbox) 2. CTC grade (výběr) Pleural effusion (checkbox) 4. CTC grade (výběr) Průjem (checkbox) 6. CTC grade (výběr) Kožní toxicita (checkbox) 8. CTC grade (výběr) Bolest hlavy (checkbox) 10. CTC grade (výběr) Krvácení (checkbox) 12. CTC grade (výběr) Únava (checkbox) 14. CTC grade (výběr)
34 Nevolnost a zvracení (checkbox) 16. CTC grade (výběr) Infekce (checkbox) 18. CTC grade (výběr) Jiná nehematologická toxicita (checkbox) 20. Specifikujte (text) 21. CTC grade (výběr) Hematologická toxicita 1. Anémie (checkbox) 2. CTC grade (výběr) Neutropenie (checkbox) 4. CTC grade (výběr) Trombocytopenie (checkbox) 6. CTC grade (výběr) Přerušení léčby 1. Délka přerušení léčby kvůli nežádoucí příhodě (dny) (číslo) abs. min:0 2. Neznámo (checkbox) 54. Hospitalizace z důvodu nežádoucí příhody 1. Datum propuštění z nemocnice (dd.mm.rrrr) (datum) abs. min:" " 2. Neznámo (checkbox) Transplantace 55. Transplantace 1. Pořadové číslo transplantace u tohoto pacienta (číslo) abs. min:1 56. Datum transplantace
35 1. *Datum transplantace (dd.mm.rrrr) (datum) abs. min:" " 2. Transplantační centrum (text) 3. Pacient transplantován ve fázi (výběr) 1. Chronická fáze 2. Akcelerovaná fáze 3. Blastická fáze 4. Druhá a vyšší chronická fáze 4. Linie transplantační léčby (výběr) 1. Transplantace plánována jako léčba první volby (pacient veden cíleně k transplantaci) 2. Transplantace pro selhání nebo netoleranci jiné léčby 57. Typ transplantace 1. *Typ transplantace (výběr) 1. Alogenní 2. Autologní 2. Autologní transplantace - typ štěpu (výběr) 1. Kostní dřeň 2. Periferní kmenové buňky 3. CD34 selekce 3. Alogenní transplantace - typ štěpu (výběr) 1. Kostní dřeň 2. Periferní krvetvorné buňky 3. Pupečníková krev 4. Kombinace 4. Alogenní (výběr) 1. Syngenní 2. Příbuzenská 3. Nepříbuzenská 5. HLA shoda (výběr) 1. Shoda 2. 1 neshoda 3. 2 a více neshod 6. Pohlaví dárce (výběr) 1. Muž 2. Žena 3. Neznámo 7. EBMT skóre (výběr) výpočet <a target="_blank" href="cmlsk_ebmt_score.pdf">ebmt risk skóre</a> 1. ECOG/WHO skóre při transplantaci (výběr) Asymptomatický Symptomatický, ale kompletně pohyblivý Symptomatický, < 50% leží v průběhu dne Symptomatický, > 50% leží, ale není upoután na lůžko Upoután na lůžko Neznámo
36 2. Transplantační komorbidity index HCT-CI (číslo) 59. <a target="_blank" href="cmlsk_hct-ci_score.pdf">hct-ci score</a><br><a target="_blank" href=" calculator</a> 60. Manipulace se štěpem 1. Manipulace se štěpem (ano/ne) 2. Selektované CD34+ buňky (ano/ne) 3. T deplece (ano/ne) 4. Jiná manipulace (ano/ne) 5. Specifikujte jinou manipulaci (text) 6. Použitý přípravný režim (výběr) 1. Myeloablativní 2. RIC 7. Typ imunosuprese (text) 61. GVDH 1. Akutní GVHD (ano/ne) 2. Stupeň (výběr) 1. I 2. II 3. III 4. IV 3. Chronická GVHD (ano/ne) 4. Závažnost (výběr) 1. Limitovaná 2. Extenzivní 5. Podány DLI? (ano/ne) 6. Podány TKI po transplantaci? (ano/ne) 7. Důvod podání TKI (výběr) 1. Profylakticky 2. Přetrvávající reziduální nemoc po transpl. 3. Relaps či progrese 8. Poznámka (text) Pacient neodpovídající na léčbu 62. Indikace 1. Důvod vyšetření (výběr) 1. Hematologická rezistence 2. Cytogenetická rezistence 3. Molekulárně genetický relaps 4. Jiný důvod 2. Specifikujte jiný důvod (text) 63. Mutace vazebného místa ABL kinázy 1. Vyšetření provedeno (ano/ne) default 2. Vyšetřený materiál (výběr) 1. Kostní dřeň 2. Periferní krev 3. Datum odběru materiálu (dd.mm.rrrr) (datum) abs. min:" " 4. Metoda RT-PCR (výběr) 1. Přímé sekvenování 2. Sekvenování subklonovaných PCR produktů 5. Přítomna mutace (ano/ne) 6. Definice mutace (mutací) (př. T315I) (text)
37 7. Mutace ověřena restrikční analýzou (ano/ne) 64. Inhibice fosforylace Crkl 1. Vyšetření provedeno (ano/ne) default 2. Vyšetřený materiál (výběr) 1. Kostní dřeň 2. Periferní krev 3. Datum odběru materiálu (dd.mm.rrrr) (datum) abs. min:" " 4. Datum posledního podání imatinibu před odběrem (dd.mm.rrrr) (datum) abs. min:" " 5. Přímý western blot - vyšetřeno (ano/ne) 6. Fosforylovaná forma Crkl (číslo) (desetinné číslo - přesnost: 0) min:0 7. Nefosforylovaná forma Crkl (číslo) (desetinné číslo - přesnost: 0) min:0 8. Kultivační metoda - vyšetřeno (ano/ne) 9. Použitá koncentrace imatinibu (um) (desetinné číslo - přesnost: 0) abs. min:0 10. Inhibice fosforylace (výběr) 1. Úplná 2. Částečná 3. Žádná Další malignity 65. CML sekundární 1. CML sekundární (ano/ne) 66. Primární malignita 1. Diagnóza primární malignity (text) 2. T (výběr) 1. Tis 2. TisD (SD - DCIS) 3. TisL (SL - LCIS) 4. TisP (SP - Paget) 5. Ta 6. T1 7. T1m (1mic) 8. T1a 9. T1a1 10. T1a2 11. T1b 12. T1b1 13. T1b2 14. T1c 15. T2 16. T2a 17. T2b 18. T2c 19. T3 20. T3a 21. T3b 22. T3c 23. T4 24. T4a 25. T4b 26. T4c 27. T4d
38 28. TX 3. N (výběr) 1. N0 2. N1 3. N1m (1mic) 4. N1a 5. N1b 6. N2 7. N2a 8. N2b 9. N2c 10. N3 11. N3a 12. N3b 13. N3c 14. NX 4. M (výběr) 1. M0 2. M1 3. M1a 4. M1b 5. M1c 6. MX 5. Klinické stádium (výběr) známo A 4. 0IS 5. I 6. IA 7. IA1 8. IA2 9. IB 10. IB1 11. IB2 12. IC 13. 1S 14. II 15. IIA 16. IIB 17. IIC 18. III 19. IIIA 20. IIIB 21. IIIC 22. IV 23. IVA 24. IVB 25. IVC 26. IVD 6. Datum stanovení primární malignity (dd.mm.rrrr) (datum) abs. min:" " 67. Léčba primární malignity
39 1. Chemoterapie (ano/ne) 2. Chemoterapie - popis (text) 3. Radioterapie (ano/ne) 4. Radioterapie - popis (text) 5. Jiná terapie (ano/ne) 6. Jiná terapie - popis (text) 7. Stav primární malignity v době zjištění CML (výběr) 1. Bez známek primárního tumoru 2. Známky primárního tumoru 8. Léčba primární malignity v době zjištění CML (ano/ne) 9. Léčba primární maligniity v době zjištění CML - popis (text) 68. Další malignita během léčby CML 1. Další malignita během léčby CML (ano/ne) 69. Sekundární malignita 1. Diagnóza sekundární malignity (text) 2. T (výběr) 1. Tis 2. TisD (SD - DCIS) 3. TisL (SL - LCIS) 4. TisP (SP - Paget) 5. Ta 6. T1 7. T1m (1mic) 8. T1a 9. T1a1 10. T1a2 11. T1b 12. T1b1 13. T1b2 14. T1c 15. T2 16. T2a 17. T2b 18. T2c 19. T3 20. T3a 21. T3b 22. T3c 23. T4 24. T4a 25. T4b 26. T4c 27. T4d 28. TX 3. N (výběr) 1. N0 2. N1 3. N1m (1mic) 4. N1a 5. N1b 6. N2 7. N2a
40 8. N2b 9. N2c 10. N3 11. N3a 12. N3b 13. N3c 14. NX 4. M (výběr) 1. M0 2. M1 3. M1a 4. M1b 5. M1c 6. MX 5. Klinické stádium (výběr) známo A 4. 0IS 5. I 6. IA 7. IA1 8. IA2 9. IB 10. IB1 11. IB2 12. IC 13. 1S 14. II 15. IIA 16. IIB 17. IIC 18. III 19. IIIA 20. IIIB 21. IIIC 22. IV 23. IVA 24. IVB 25. IVC 26. IVD 6. Datum stanovení sekundární malignity (dd.mm.rrrr) (datum) abs. min:" " 70. Léčba sekundární malignity 1. Chemoterapie (ano/ne) 2. Chemoterapie - popis (text) 3. Radioterapie (ano/ne) 4. Radioterapie - popis (text) 5. Jiná terapie (ano/ne) 6. Jiná terapie - popis (text)
Databáze CAMELIA. popis struktury dat a pracovního prostředí. Stav k
 Databáze CAMELIA popis struktury dat a pracovního prostředí Stav k 1. 9. 2012 Zpracoval Institut biostatistiky a analýz, Masarykova univerzita, Kamenice 126/3, 625 00 Brno Databáze CAMELIA Obsah Základní
Databáze CAMELIA popis struktury dat a pracovního prostředí Stav k 1. 9. 2012 Zpracoval Institut biostatistiky a analýz, Masarykova univerzita, Kamenice 126/3, 625 00 Brno Databáze CAMELIA Obsah Základní
ZPRÁVA O STAVU PROJEKTU V ROCE 2014
 CAMELIA SK ZPRÁVA O STAVU PROJEKTU V ROCE 2014 Vydáno dne: 14. 7. 2015 : Mgr. Zuzana Zbožínková, RNDr. Jan Mužík, Ph.D. Schválil: Ing. Petr Brabec, IBA + Schválil : Petr Brabec Strana 1 (celkem 11) ŘÍZENÍ
CAMELIA SK ZPRÁVA O STAVU PROJEKTU V ROCE 2014 Vydáno dne: 14. 7. 2015 : Mgr. Zuzana Zbožínková, RNDr. Jan Mužík, Ph.D. Schválil: Ing. Petr Brabec, IBA + Schválil : Petr Brabec Strana 1 (celkem 11) ŘÍZENÍ
ZPRÁVA O STAVU PROJEKTU V ROCE 2015
 Zpráva 2015 Verze: 1 CAMELIA SK ZPRÁVA O STAVU PROJEKTU V ROCE 2015 Vydáno dne: 18-AUG-2016 : PharmDr. Zuzana Zbožínková Schválil: Ing. Petr Brabec, PhD Verze: 1 + Schválil : Petr Brabec Strana 1 (celkem
Zpráva 2015 Verze: 1 CAMELIA SK ZPRÁVA O STAVU PROJEKTU V ROCE 2015 Vydáno dne: 18-AUG-2016 : PharmDr. Zuzana Zbožínková Schválil: Ing. Petr Brabec, PhD Verze: 1 + Schválil : Petr Brabec Strana 1 (celkem
ZPRÁVA O STAVU PROJEKTU V ROCE 2013
 CAMELIA Datum vydání: 25.2.2014 CAMELIA SK ZPRÁVA O STAVU PROJEKTU V ROCE 2013 Vydáno dne: 25. 2. 2014 : Mgr. Zuzana Zbožínková, RNDr. Jan Mužík, Ph.D. Schválil: Ing. Petr Brabec, IBA +, Jan Mužík Schválil
CAMELIA Datum vydání: 25.2.2014 CAMELIA SK ZPRÁVA O STAVU PROJEKTU V ROCE 2013 Vydáno dne: 25. 2. 2014 : Mgr. Zuzana Zbožínková, RNDr. Jan Mužík, Ph.D. Schválil: Ing. Petr Brabec, IBA +, Jan Mužík Schválil
REGISTR CAMELIA PROJEKTOVÁ ZPRÁVA. Vydáno dne: Autor: Jan Mužík
 REGISTR CAMELIA PROJEKTOVÁ ZPRÁVA Vydáno dne: 30.6.2013 Autor: Jan Mužík CAMELIA OBSAH 1. Účel dokumentu... 3 2. Základní charakteristika projektu... 3 2.1 Popis projektu... 3 2.2 Spolupracující centra...
REGISTR CAMELIA PROJEKTOVÁ ZPRÁVA Vydáno dne: 30.6.2013 Autor: Jan Mužík CAMELIA OBSAH 1. Účel dokumentu... 3 2. Základní charakteristika projektu... 3 2.1 Popis projektu... 3 2.2 Spolupracující centra...
STRUKTURA REGISTRU RENIS
 STRUKTURA REGISTRU RENIS Vstupní data 1. Identifikace při vstupu do registru 1. Datum vstupu do registru (datum) 2. Váhový úbytek za posledních 6 měsíců (kg) (reálné číslo) 3. PS (skóre performance status)
STRUKTURA REGISTRU RENIS Vstupní data 1. Identifikace při vstupu do registru 1. Datum vstupu do registru (datum) 2. Váhový úbytek za posledních 6 měsíců (kg) (reálné číslo) 3. PS (skóre performance status)
Analytický software databáze projektu CAMELIA
 CHRONICKÁ MYELOIDNÍ LEUKÉMIE Analytický software databáze projektu CAMELIA Uživatelská příručka Verze 2.0 Listopad 2010 Česká hematologická společnost ČLS JEP Garant projektu: Česká hematologická společnost
CHRONICKÁ MYELOIDNÍ LEUKÉMIE Analytický software databáze projektu CAMELIA Uživatelská příručka Verze 2.0 Listopad 2010 Česká hematologická společnost ČLS JEP Garant projektu: Česká hematologická společnost
Registr Herceptin Karcinom prsu
 I. Primární diagnostika Registr Herceptin Karcinom prsu Vstupní parametry Rok narození Věk Kód zdravotní pojišťovny (výběr) o 111 o 201 o 205 o 207 o 209 o 211 o 213 o 217 o 222 Datum stanovení diagnózy
I. Primární diagnostika Registr Herceptin Karcinom prsu Vstupní parametry Rok narození Věk Kód zdravotní pojišťovny (výběr) o 111 o 201 o 205 o 207 o 209 o 211 o 213 o 217 o 222 Datum stanovení diagnózy
DIAGNOSTICKÝ A LÉČEBNÝ POSTUP U CHRONICKÉ MYELOIDNÍ LEUKEMIE DOSPĚLÝCH (nebo Algoritmus vyšetření a léčby CML v roce 2008)
 DIAGNOSTICKÝ A LÉČEBNÝ POSTUP U CHRONICKÉ MYELOIDNÍ LEUKEMIE DOSPĚLÝCH (nebo Algoritmus vyšetření a léčby CML v roce 2008) Úvod V České republice každoročně onemocní chronickou myeloidní leukemií (CML)
DIAGNOSTICKÝ A LÉČEBNÝ POSTUP U CHRONICKÉ MYELOIDNÍ LEUKEMIE DOSPĚLÝCH (nebo Algoritmus vyšetření a léčby CML v roce 2008) Úvod V České republice každoročně onemocní chronickou myeloidní leukemií (CML)
MYELOFIBROSA - DIAGNOSTIKA A LÉČEBNÉ MOŽNOSTI
 MYELOFIBROSA - DIAGNOSTIKA A LÉČEBNÉ MOŽNOSTI DEFINICE: chronické myeloproliferativní (klonální) onemocnění charakteristické zmnožením vaziva v kostní dřeni a extramedulární krvetvorbou (první popis -
MYELOFIBROSA - DIAGNOSTIKA A LÉČEBNÉ MOŽNOSTI DEFINICE: chronické myeloproliferativní (klonální) onemocnění charakteristické zmnožením vaziva v kostní dřeni a extramedulární krvetvorbou (první popis -
STRUKTURA REGISTRU MPM
 STRUKTURA REGISTRU MPM 1. Vstupní parametry 1. Kouření (výběr) 1. Kuřák 2. Bývalý kuřák (rok před stanovením DG - dle WHO) 3. Nekuřák 4. Neuvedeno 2. Výška [cm] (reálné číslo) 3. Hmotnost pacienta v době
STRUKTURA REGISTRU MPM 1. Vstupní parametry 1. Kouření (výběr) 1. Kuřák 2. Bývalý kuřák (rok před stanovením DG - dle WHO) 3. Nekuřák 4. Neuvedeno 2. Výška [cm] (reálné číslo) 3. Hmotnost pacienta v době
Lékový registr ALIMTA
 Lékový registr Pravidelný report Maligní pleurální mezoteliom (MPM) Stav registru k datu 31. 3. 2014 Pneumoonkologická centra zapojená v projektu Alimta 1. FN Brno Jihlavská 20, 625 00 Brno - Bohunice
Lékový registr Pravidelný report Maligní pleurální mezoteliom (MPM) Stav registru k datu 31. 3. 2014 Pneumoonkologická centra zapojená v projektu Alimta 1. FN Brno Jihlavská 20, 625 00 Brno - Bohunice
Lékový registr ALIMTA
 Lékový registr Pravidelný report Maligní pleurální mezoteliom (MPM) Stav registru k datu 19. 10. 2015 Pneumoonkologická centra zapojená v projektu Alimta 1. FN Brno Jihlavská 20, 625 00 Brno - Bohunice
Lékový registr Pravidelný report Maligní pleurální mezoteliom (MPM) Stav registru k datu 19. 10. 2015 Pneumoonkologická centra zapojená v projektu Alimta 1. FN Brno Jihlavská 20, 625 00 Brno - Bohunice
VNL. Onemocnění bílé krevní řady
 VNL Onemocnění bílé krevní řady Změny leukocytů V počtu leukocytů Ve vzájemném zastoupení morfologických typů leukocytů Ve funkci leukocytů Reaktivní změny leukocytů Leukocytóza: při bakteriální infekci
VNL Onemocnění bílé krevní řady Změny leukocytů V počtu leukocytů Ve vzájemném zastoupení morfologických typů leukocytů Ve funkci leukocytů Reaktivní změny leukocytů Leukocytóza: při bakteriální infekci
Nežádoucí příhody v klinické studii CMG 2002
 Nežádoucí příhody v klinické studii 2002 Období 4/2002 12/2004 Kamila Havlíková Klinická studie 2002 Nežádoucí příhoda - Adverse Event (AE) Nepříznivá změna zdravotního stavu postihující subjekt hodnocení,
Nežádoucí příhody v klinické studii 2002 Období 4/2002 12/2004 Kamila Havlíková Klinická studie 2002 Nežádoucí příhoda - Adverse Event (AE) Nepříznivá změna zdravotního stavu postihující subjekt hodnocení,
VLIV ČASNÉ BASOFILIE NA PROGNÓZU CML. Autoři: Lucie Benešová, Barbora Maiwaldová. Výskyt
 VLIV ČASNÉ BASOFILIE NA PROGNÓZU CML Autoři: Lucie Benešová, Barbora Maiwaldová Výskyt Chronická myeloidní leukémie je nejčastěji se vyskytujícím myeloproliferativním onemocněním. Obvykle se udává, že
VLIV ČASNÉ BASOFILIE NA PROGNÓZU CML Autoři: Lucie Benešová, Barbora Maiwaldová Výskyt Chronická myeloidní leukémie je nejčastěji se vyskytujícím myeloproliferativním onemocněním. Obvykle se udává, že
Odběr krvetvorných buněk z periferní krve: příprava, průběh a komplikace
 Odběr krvetvorných buněk z periferní krve: příprava, průběh a komplikace Helena Švábová, Andrea Žmijáková Interní hematologická a onkologická klinika FN Brno Separační středisko je součástí Interní hematologické
Odběr krvetvorných buněk z periferní krve: příprava, průběh a komplikace Helena Švábová, Andrea Žmijáková Interní hematologická a onkologická klinika FN Brno Separační středisko je součástí Interní hematologické
Akutní leukémie a myelodysplastický syndrom. Hemato-onkologická klinika FN a LF UP Olomouc
 Akutní leukémie a myelodysplastický syndrom Hemato-onkologická klinika FN a LF UP Olomouc Akutní leukémie (AL) Představují heterogenní skupinu chorob charakterizovaných kumulací klonu nevyzrálých, nádorově
Akutní leukémie a myelodysplastický syndrom Hemato-onkologická klinika FN a LF UP Olomouc Akutní leukémie (AL) Představují heterogenní skupinu chorob charakterizovaných kumulací klonu nevyzrálých, nádorově
VÝROČNÍ ZPRÁVA O ČINNOSTI TKÁŇOVÉHO ZAŘÍZENÍ
 HOO/O13 VÝROČNÍ ZPRÁVA O ČINNOSTI TKÁŇOVÉHO ZAŘÍZENÍ ROK: 6 tkáňové zařízení: Hematologicko - onkologické oddělení Fakultní nemocnice Plzeň alej Svobody 8, Plzeň 34 6 číslo tkáňové banky: odpovědná osoba:
HOO/O13 VÝROČNÍ ZPRÁVA O ČINNOSTI TKÁŇOVÉHO ZAŘÍZENÍ ROK: 6 tkáňové zařízení: Hematologicko - onkologické oddělení Fakultní nemocnice Plzeň alej Svobody 8, Plzeň 34 6 číslo tkáňové banky: odpovědná osoba:
Doplněk MM guidelines: Doplněk č. 1 k doporučení z 9/2012 diagnostika a léčba mnohočetného myelomu
 Doplněk MM guidelines: Doplněk č. 1 k doporučení z 9/2012 diagnostika a léčba mnohočetného myelomu Marta Krejčí XIII. MM workshop a setkání CMG, Mikulov 11.4.2015 Doplněk č. 1 k doporučení z 9/2012: Diagnostika
Doplněk MM guidelines: Doplněk č. 1 k doporučení z 9/2012 diagnostika a léčba mnohočetného myelomu Marta Krejčí XIII. MM workshop a setkání CMG, Mikulov 11.4.2015 Doplněk č. 1 k doporučení z 9/2012: Diagnostika
Nežádoucí příhody v klinické studii CMG 2002
 Nežádoucí příhody v klinické studii 2002 Období 4/2002 3/2006 Kamila Havlíková Klinická studie 2002 Požadavky na hlášení v průběhu klinického hodnocení Povinnosti zkoušejícího: neprodleně (do 15 dnů) hlásit
Nežádoucí příhody v klinické studii 2002 Období 4/2002 3/2006 Kamila Havlíková Klinická studie 2002 Požadavky na hlášení v průběhu klinického hodnocení Povinnosti zkoušejícího: neprodleně (do 15 dnů) hlásit
TULUNG - AVASTIN. Klinický registr pacientů s nemalobuněčným karcinomem plic. Stav registru k datu 26. 3. 2012
 TULUNG - AVASTIN Klinický registr pacientů s nemalobuněčným karcinomem plic Stav registru k datu 26. 3. 2012 Management projektu: Analýza dat: Technické zajištění: Mgr. Karel Hejduk, Ing. Petr Brabec Mgr.
TULUNG - AVASTIN Klinický registr pacientů s nemalobuněčným karcinomem plic Stav registru k datu 26. 3. 2012 Management projektu: Analýza dat: Technické zajištění: Mgr. Karel Hejduk, Ing. Petr Brabec Mgr.
STRUKTURA REGISTRU BREAST
 Vstupní parametry a diagnostika STRUKTURA REGISTRU BREAST 1. Vstupní parametry 1. Kód zdravotní pojišťovny (výběr) 1. 111 2. 201 3. 205 4. 207 5. 209 6. 211 7. 213 8. 217 - do 1.10.2012 9. 222 - do 1.10.2009
Vstupní parametry a diagnostika STRUKTURA REGISTRU BREAST 1. Vstupní parametry 1. Kód zdravotní pojišťovny (výběr) 1. 111 2. 201 3. 205 4. 207 5. 209 6. 211 7. 213 8. 217 - do 1.10.2012 9. 222 - do 1.10.2009
Cytogenetické vyšetřovací metody v onkohematologii Zuzana Zemanová
 Cytogenetické vyšetřovací metody v onkohematologii Zuzana Zemanová Centrum nádorové cytogenetiky Ústav klinické biochemie a laboratorní diagnostiky VFN a 1. LF UK v Praze Klinický význam cytogenetických
Cytogenetické vyšetřovací metody v onkohematologii Zuzana Zemanová Centrum nádorové cytogenetiky Ústav klinické biochemie a laboratorní diagnostiky VFN a 1. LF UK v Praze Klinický význam cytogenetických
TULUNG - AVASTIN. Klinický registr pacientů s nemalobuněčným karcinomem plic. Stav registru k datu 17. 9. 2012
 TULUNG - AVASTIN Klinický registr pacientů s nemalobuněčným karcinomem plic Stav registru k datu 17. 9. 2012 Management projektu: Analýza dat: Technické zajištění: Mgr. Karel Hejduk, Ing. Petr Brabec Mgr.
TULUNG - AVASTIN Klinický registr pacientů s nemalobuněčným karcinomem plic Stav registru k datu 17. 9. 2012 Management projektu: Analýza dat: Technické zajištění: Mgr. Karel Hejduk, Ing. Petr Brabec Mgr.
VÝROČNÍ ZPRÁVA O ČINNOSTI TKÁŇOVÉHO ZAŘÍZENÍ
 VÝROČNÍ ZPRÁVA O ČINNOSTI TKÁŇOVÉHO ZAŘÍZENÍ ROK: 4 tkáňové zařízení: Hematologicko - onkologické oddělení Fakultní nemocnice Plzeň alej Svobody 8, Plzeň 34 6 číslo tkáňové banky: odpovědná osoba: ICCBBA
VÝROČNÍ ZPRÁVA O ČINNOSTI TKÁŇOVÉHO ZAŘÍZENÍ ROK: 4 tkáňové zařízení: Hematologicko - onkologické oddělení Fakultní nemocnice Plzeň alej Svobody 8, Plzeň 34 6 číslo tkáňové banky: odpovědná osoba: ICCBBA
Léčebná doporučení pro pacienty s CML
 Léčebná doporučení pro pacienty s CML Shrnutí doporučení Evropské leukemické sítě (Euroepan LeukemiaNet, ELN) (2013) pro léčbu chronické myeloidní leukémie určené pro pacienty Vydala Obsah Předmluva pracovní
Léčebná doporučení pro pacienty s CML Shrnutí doporučení Evropské leukemické sítě (Euroepan LeukemiaNet, ELN) (2013) pro léčbu chronické myeloidní leukémie určené pro pacienty Vydala Obsah Předmluva pracovní
Hemato-onkologická klinika FNO a LF UP. Transplantace krvetvorných buněk
 Hemato-onkologická klinika FNO a LF UP Transplantace krvetvorných buněk Doney K et al.: Treatment of chronic granulocytic leukemia by chemotherapy, total body irradiation and allogeneic bone marrow transplantation.
Hemato-onkologická klinika FNO a LF UP Transplantace krvetvorných buněk Doney K et al.: Treatment of chronic granulocytic leukemia by chemotherapy, total body irradiation and allogeneic bone marrow transplantation.
Výroční zpráva tkáňového zařízení za rok 2015
 Ústav hematologie a krevní transfuze, p. o. IČO 23736 128 20 Praha 2, U Nemocnice 1 telefon: 224 436 018, E-mail: cryo@uhkt.cz Pracoviště FN Motol, Nová budova kliniky dětské onkologie číslo 23, ulice
Ústav hematologie a krevní transfuze, p. o. IČO 23736 128 20 Praha 2, U Nemocnice 1 telefon: 224 436 018, E-mail: cryo@uhkt.cz Pracoviště FN Motol, Nová budova kliniky dětské onkologie číslo 23, ulice
VÝROČNÍ ZPRÁVA O ČINNOSTI TKÁŇOVÉHO ZAŘÍZENÍ
 VÝROČNÍ ZPRÁVA O ČINNOSTI TKÁŇOVÉHO ZAŘÍZENÍ ROK: 17 tkáňové zařízení: Hematologicko - onkologické oddělení Fakultní nemocnice Plzeň alej Svobody 8, Plzeň 34 číslo tkáňové banky: odpovědná osoba: ICCBBA
VÝROČNÍ ZPRÁVA O ČINNOSTI TKÁŇOVÉHO ZAŘÍZENÍ ROK: 17 tkáňové zařízení: Hematologicko - onkologické oddělení Fakultní nemocnice Plzeň alej Svobody 8, Plzeň 34 číslo tkáňové banky: odpovědná osoba: ICCBBA
LÉČBA RELAPSU MNOHOČETNÉHO MYELOMU. MUDr. Miroslava Schützová. 5. vzdělávací seminář pro nemocné s mnohočetným myelomem, jejich rodinu a přátele
 LÉČBA RELAPSU MNOHOČETNÉHO MYELOMU MUDr. Miroslava Schützová 5. vzdělávací seminář pro nemocné s mnohočetným myelomem, jejich rodinu a přátele 20. - 21. listopadu 2009 Karlova Studánka ČESKÁ MYELOMOVÁ
LÉČBA RELAPSU MNOHOČETNÉHO MYELOMU MUDr. Miroslava Schützová 5. vzdělávací seminář pro nemocné s mnohočetným myelomem, jejich rodinu a přátele 20. - 21. listopadu 2009 Karlova Studánka ČESKÁ MYELOMOVÁ
Projekt CAMELIA Projekt ALERT
 Projekt Alert akutní leukemie klinický registr x Web projektu Diskusní klub projektu Management dat Služby IS Help Zpět Analytické nástroje Prohlížeč dat Expertní služby x Projekt CAMELIA Projekt ALERT
Projekt Alert akutní leukemie klinický registr x Web projektu Diskusní klub projektu Management dat Služby IS Help Zpět Analytické nástroje Prohlížeč dat Expertní služby x Projekt CAMELIA Projekt ALERT
Registr Avastin Nemalobuněčný karcinom plic
 Registr Avastin Nemalobuněčný karcinom plic Formulář: Vstupní parametry Rok narození Věk Pohlaví Kouření o Kuřák o Bývalý kuřák o Nekuřák Hmotnost pacienta v době diagnózy (kg) Hmotnost pacienta v době
Registr Avastin Nemalobuněčný karcinom plic Formulář: Vstupní parametry Rok narození Věk Pohlaví Kouření o Kuřák o Bývalý kuřák o Nekuřák Hmotnost pacienta v době diagnózy (kg) Hmotnost pacienta v době
Terapie hairy-cell leukémie
 Terapie hairy-cell leukémie David Belada, II.interní klinika, OKH FN a LF v Hradci Králové Lymfomové fórum 2010 Grand Hotel Bellevue, Vysoké Tatry 12.-14.3.2010 Úvod Poprvé popsána v roce 1958 (Bouroncle
Terapie hairy-cell leukémie David Belada, II.interní klinika, OKH FN a LF v Hradci Králové Lymfomové fórum 2010 Grand Hotel Bellevue, Vysoké Tatry 12.-14.3.2010 Úvod Poprvé popsána v roce 1958 (Bouroncle
CEBO: (Center for Evidence Based Oncology) Incidence Kostních příhod u nádorů prsu PROJEKT IKARUS. Neintervenční epidemiologická studie
 CEBO: (Center for Evidence Based Oncology) Incidence Kostních příhod u nádorů prsu PROJEKT Neintervenční epidemiologická studie PROTOKOL PROJEKTU Verze: 4.0 Datum: 26.09.2006 Strana 2 PROTOKOL PROJEKTU
CEBO: (Center for Evidence Based Oncology) Incidence Kostních příhod u nádorů prsu PROJEKT Neintervenční epidemiologická studie PROTOKOL PROJEKTU Verze: 4.0 Datum: 26.09.2006 Strana 2 PROTOKOL PROJEKTU
Biologická léčba karcinomu prsu. Prof. MUDr. Jitka Abrahámová, DrSc. Onkologická klinika 1.LF UK a TN KOC (NNB+VFN+TN)
 Biologická léčba karcinomu prsu Prof. MUDr. Jitka Abrahámová, DrSc. Onkologická klinika 1.LF UK a TN KOC (NNB+VFN+TN) Cílená léčba Ca prsu Trastuzumab (HercepNn) AnN HER2 neu pronlátka LapaNnib (Tyverb)
Biologická léčba karcinomu prsu Prof. MUDr. Jitka Abrahámová, DrSc. Onkologická klinika 1.LF UK a TN KOC (NNB+VFN+TN) Cílená léčba Ca prsu Trastuzumab (HercepNn) AnN HER2 neu pronlátka LapaNnib (Tyverb)
VÝROČNÍ ZPRÁVA O ČINNOSTI TKÁŇOVÉHO ZAŘÍZENÍ
 HOO/O1 VÝROČNÍ ZPRÁVA O ČINNOSTI TKÁŇOVÉHO ZAŘÍZENÍ ROK: 218 tkáňové zařízení: Hematologicko - onkologické oddělení Fakultní nemocnice Plzeň alej Svobody 8, Plzeň 4 6 číslo tkáňové banky: odpovědná osoba:
HOO/O1 VÝROČNÍ ZPRÁVA O ČINNOSTI TKÁŇOVÉHO ZAŘÍZENÍ ROK: 218 tkáňové zařízení: Hematologicko - onkologické oddělení Fakultní nemocnice Plzeň alej Svobody 8, Plzeň 4 6 číslo tkáňové banky: odpovědná osoba:
VÝROČNÍ ZPRÁVA O ČINNOSTI TKÁŇOVÉHO ZAŘÍZENÍ
 HOO/O1 VÝROČNÍ ZPRÁVA O ČINNOSTI TKÁŇOVÉHO ZAŘÍZENÍ ROK: 15 tkáňové zařízení: Hematologicko - onkologické oddělení Fakultní nemocnice Plzeň alej Svobody 8, Plzeň 4 6 číslo tkáňové banky: odpovědná osoba:
HOO/O1 VÝROČNÍ ZPRÁVA O ČINNOSTI TKÁŇOVÉHO ZAŘÍZENÍ ROK: 15 tkáňové zařízení: Hematologicko - onkologické oddělení Fakultní nemocnice Plzeň alej Svobody 8, Plzeň 4 6 číslo tkáňové banky: odpovědná osoba:
Léčebná doporučení pro pacienty s CML
 Léčebná doporučení pro pacienty s CML Shrnutí doporučení Evropské leukemické sítě (Euroepan LeukemiaNet, ELN) (2013) pro léčbu chronické myeloidní leukémie určené pro pacienty Vydala CML Advocates Network
Léčebná doporučení pro pacienty s CML Shrnutí doporučení Evropské leukemické sítě (Euroepan LeukemiaNet, ELN) (2013) pro léčbu chronické myeloidní leukémie určené pro pacienty Vydala CML Advocates Network
CORECT - VECTIBIX. Klinický registr pacientů s metastatickým kolorektálním karcinomem. Stav registru k datu
 CORECT - VECTIBIX Klinický registr pacientů s metastatickým kolorektálním karcinomem Stav registru k datu 26. 3. 2012 Management projektu: Analýza dat: Technické zajištění: Mgr. Karel Hejduk, Ing. Petr
CORECT - VECTIBIX Klinický registr pacientů s metastatickým kolorektálním karcinomem Stav registru k datu 26. 3. 2012 Management projektu: Analýza dat: Technické zajištění: Mgr. Karel Hejduk, Ing. Petr
Sledování bezpečnosti v registeru. MUDr. Tomáš Moravec
 Sledování bezpečnosti v registeru MUDr. Tomáš Moravec Jaký je náš cíl v sledování bezpečnosti? naší snahou a cílem je ověření bezpečnostního profilu daného léčivého přípravku a získání nových informací
Sledování bezpečnosti v registeru MUDr. Tomáš Moravec Jaký je náš cíl v sledování bezpečnosti? naší snahou a cílem je ověření bezpečnostního profilu daného léčivého přípravku a získání nových informací
Úvod do problematiky léčby CML pro nemocné s chronickou myeloidní leukemií
 Úvod do problematiky léčby CML pro nemocné s chronickou myeloidní leukemií Prezentace spoluautorů CML Advocates Network Sandy Crainové a Giory Sharfa pod odborným vedením Dr. Timothy Hughese (Univerzita
Úvod do problematiky léčby CML pro nemocné s chronickou myeloidní leukemií Prezentace spoluautorů CML Advocates Network Sandy Crainové a Giory Sharfa pod odborným vedením Dr. Timothy Hughese (Univerzita
Laboratoř rutinního provozu
 Informátor Hemato-onkologické kliniky FNOL 2/2011 é Změna referenčních mezí krevního obrazu pro dospělé a děti Laboratoř rutinního provozu Laboratoř rutinního provozu HOK FNOL sděluje všem žadatelům o
Informátor Hemato-onkologické kliniky FNOL 2/2011 é Změna referenčních mezí krevního obrazu pro dospělé a děti Laboratoř rutinního provozu Laboratoř rutinního provozu HOK FNOL sděluje všem žadatelům o
STRUKTURA REGISTRU OVARIA
 STRUKTURA REGISTRU OVARIA Vstupní údaje 1. Základní data 1. Datum stanovení diagnózy karcinomu ovarií [dd.mm.rrrr] (datum) 2. Výška v době stanovení diagnózy [cm] (číslo) 3. Váha v době stanovení diagnózy
STRUKTURA REGISTRU OVARIA Vstupní údaje 1. Základní data 1. Datum stanovení diagnózy karcinomu ovarií [dd.mm.rrrr] (datum) 2. Výška v době stanovení diagnózy [cm] (číslo) 3. Váha v době stanovení diagnózy
Iclusig (ponatinib) potahované tablety 15 mg, 30 mg a 45 mg* Důležité bezpečnostní informace pro zdravotnické pracovníky
 Edukační materiály Iclusig (ponatinib) potahované tablety 15 mg, 30 mg a 45 mg* Důležité bezpečnostní informace pro zdravotnické pracovníky Tento dokument obsahuje důležité informace o bezpečnosti, s nimiž
Edukační materiály Iclusig (ponatinib) potahované tablety 15 mg, 30 mg a 45 mg* Důležité bezpečnostní informace pro zdravotnické pracovníky Tento dokument obsahuje důležité informace o bezpečnosti, s nimiž
HEMATOLOGIE minulost současnost - budoucnost
 HEMATOLOGIE minulost současnost - budoucnost Doc. MUDr. Jaroslav Čermák, CSc. Ústav hematologie a krevní transfuze, Praha Klepnutm lze upravit styl předlohy podnadpisů. HEMATOLOGIE názory v 60. a 70. letech
HEMATOLOGIE minulost současnost - budoucnost Doc. MUDr. Jaroslav Čermák, CSc. Ústav hematologie a krevní transfuze, Praha Klepnutm lze upravit styl předlohy podnadpisů. HEMATOLOGIE názory v 60. a 70. letech
SBĚR DAT STUDIE DUQUE - ZLOMENINA HORNÍHO KONCE STEHENNÍ KOSTI
 Inclusion Definice Zlomenina krčku SBĚR DAT STUDIE DUQUE - ZLOMENINA HORNÍHO KONCE STEHENNÍ KOSTI Diagnostická kritéria Pacient ve věku 65 let a více + splňující následující tři diagnostická kritéria:
Inclusion Definice Zlomenina krčku SBĚR DAT STUDIE DUQUE - ZLOMENINA HORNÍHO KONCE STEHENNÍ KOSTI Diagnostická kritéria Pacient ve věku 65 let a více + splňující následující tři diagnostická kritéria:
TARCEVA klinický registr
 TARCEVA klinický registr Karcinom pankreatu Stav k datu 10. 4. 2011 Registr Tarceva je podporován výzkumným ý grantem firmy Roche. Česká onkologická společnost Institut biostatistiky a analýz Stav registru
TARCEVA klinický registr Karcinom pankreatu Stav k datu 10. 4. 2011 Registr Tarceva je podporován výzkumným ý grantem firmy Roche. Česká onkologická společnost Institut biostatistiky a analýz Stav registru
Lokální analýza dat Národního registru CMP. Komplexní cerebrovaskulární centrum Fakultní nemocnice Ostrava
 NÁRODNÍ REGISTR CMP Lokální analýza dat Národního registru CMP za rok 2010 Komplexní cerebrovaskulární centrum Fakultní nemocnice Ostrava MUDr. Martin Roubec Garant centra: MUDr. Michal Bar, Ph.D. Garant
NÁRODNÍ REGISTR CMP Lokální analýza dat Národního registru CMP za rok 2010 Komplexní cerebrovaskulární centrum Fakultní nemocnice Ostrava MUDr. Martin Roubec Garant centra: MUDr. Michal Bar, Ph.D. Garant
Podpůrná léčba hematologické toxicity u nemocného s mnohočetným myelomem léčeného lenalidomidovým režimem Kazuistika
 Podpůrná léčba hematologické toxicity u nemocného s mnohočetným myelomem léčeného lenalidomidovým režimem Kazuistika MUDr. Evžen Gregora IX. Národní workshop Mnohočetný myelom Edukační blok Celgene Mikulov
Podpůrná léčba hematologické toxicity u nemocného s mnohočetným myelomem léčeného lenalidomidovým režimem Kazuistika MUDr. Evžen Gregora IX. Národní workshop Mnohočetný myelom Edukační blok Celgene Mikulov
Leukemie a myeloproliferativní onemocnění
 Leukemie a myeloproliferativní onemocnění Myeloproliferativní tumory Klonální onemocnění hematopoetických stem cells charakterizované proliferací jedné nebo více myeloidních řad. Dospělí peak 5. 7. dekáda,
Leukemie a myeloproliferativní onemocnění Myeloproliferativní tumory Klonální onemocnění hematopoetických stem cells charakterizované proliferací jedné nebo více myeloidních řad. Dospělí peak 5. 7. dekáda,
Česká Myelomová Skupina na poli mnohočetného myelomu
 Česká Myelomová Skupina na poli mnohočetného myelomu Vladimír Maisnar IV. interní hematologická klinika LF UK a FN Hradec Králové Lázně Bělohrad, 10. září 2016 Epidemiologická data: MM 1% všech malignit,
Česká Myelomová Skupina na poli mnohočetného myelomu Vladimír Maisnar IV. interní hematologická klinika LF UK a FN Hradec Králové Lázně Bělohrad, 10. září 2016 Epidemiologická data: MM 1% všech malignit,
LEUKÉMIE. Markéta Vojtová
 LEUKÉMIE Markéta Vojtová Trocha patofyziologie 1 Leukémie je zhoubné onemocnění krve Kmenová buňka v kostní dřeni se chromozomálně odchýlí (změní) změněná buňka plodí další již změněné (patologické) buňky
LEUKÉMIE Markéta Vojtová Trocha patofyziologie 1 Leukémie je zhoubné onemocnění krve Kmenová buňka v kostní dřeni se chromozomálně odchýlí (změní) změněná buňka plodí další již změněné (patologické) buňky
Patient s hemato-onkologickým onemocněním: péče v závěru života - umírání v ČR, hospicová péče - zkušenosti jednoho pracoviště
 Patient s hemato-onkologickým onemocněním: péče v závěru života - umírání v ČR, hospicová péče - zkušenosti jednoho pracoviště Jindřich Polívka 1, Jan Švancara 2 1 Hospic Dobrého Pastýře Čerčany 2 Institut
Patient s hemato-onkologickým onemocněním: péče v závěru života - umírání v ČR, hospicová péče - zkušenosti jednoho pracoviště Jindřich Polívka 1, Jan Švancara 2 1 Hospic Dobrého Pastýře Čerčany 2 Institut
CMG LÉČBA RELAPSU, NOVÉ LÉKY, KLINICKÉ STUDIE. MUDr. Miroslava Schützová. Poděbrady 11. září 2010. Hemato-onkologické odd. FN Plzeň NADAČNÍ FOND
 LÉČBA RELAPSU, NOVÉ LÉKY, KLINICKÉ STUDIE MUDr. Miroslava Schützová Hemato-onkologické odd. FN Plzeň Poděbrady 11. září 2010 ČESKÁ MYELOMOVÁ SKUPINA CZECH CMG M Y E L O M A NADAČNÍ FOND GROUP Česká myelomová
LÉČBA RELAPSU, NOVÉ LÉKY, KLINICKÉ STUDIE MUDr. Miroslava Schützová Hemato-onkologické odd. FN Plzeň Poděbrady 11. září 2010 ČESKÁ MYELOMOVÁ SKUPINA CZECH CMG M Y E L O M A NADAČNÍ FOND GROUP Česká myelomová
Léčebné predikce u karcinomu prsu pro rok 2013 chystané novinky
 Léčebné predikce u karcinomu prsu pro rok 2013 chystané novinky Prof. MUDr. Jitka Abrahámová, DrSc Onkologická klinika TN a 1. LF UK KOC (NNB + VFN + TN) St Gallén 2011 Rozsah onemocnění T, N, M ER, PgR
Léčebné predikce u karcinomu prsu pro rok 2013 chystané novinky Prof. MUDr. Jitka Abrahámová, DrSc Onkologická klinika TN a 1. LF UK KOC (NNB + VFN + TN) St Gallén 2011 Rozsah onemocnění T, N, M ER, PgR
SONAR. Vizita 1 (7-10 dní po vzniku CMP)
 SONAR 06.01.2014 Vizita 1 (7-10 dní po vzniku CMP) v Datum Vizity 1 (23880) Datum vzniku CMP (62502) (datum) abs. min:"1.1.1900" Datum Vizity 1 (dd.mm.rrrr) (61555) (datum) abs. min:"1.1.1900" v Osobní
SONAR 06.01.2014 Vizita 1 (7-10 dní po vzniku CMP) v Datum Vizity 1 (23880) Datum vzniku CMP (62502) (datum) abs. min:"1.1.1900" Datum Vizity 1 (dd.mm.rrrr) (61555) (datum) abs. min:"1.1.1900" v Osobní
Nová diagnóza = Studiová indikace. První relaps = Studiová indikace
 Velcade dostupné léčebné protokoly Nová diagnóza = Studiová indikace První relaps = Studiová indikace C M G Velcade dostupné léčebné protokoly Nová diagnóza = Studiová indikace První relaps = Studiová
Velcade dostupné léčebné protokoly Nová diagnóza = Studiová indikace První relaps = Studiová indikace C M G Velcade dostupné léčebné protokoly Nová diagnóza = Studiová indikace První relaps = Studiová
TARCEVA klinický registr
 TARCEVA klinický registr Karcinom pankreatu Stav k datu 10. 10. 2011 Analýza dat: Mgr. Zbyněk Bortlíček Informační technologie: RNDr. Daniel Klimeš, Ph.D. Management projektu: Ing. Petr Brabec, Mgr. Karel
TARCEVA klinický registr Karcinom pankreatu Stav k datu 10. 10. 2011 Analýza dat: Mgr. Zbyněk Bortlíček Informační technologie: RNDr. Daniel Klimeš, Ph.D. Management projektu: Ing. Petr Brabec, Mgr. Karel
ZÁKLADY KLINICKÉ ONKOLOGIE
 Pavel Klener ZÁKLADY KLINICKÉ ONKOLOGIE Galén Autor prof. MUDr. Pavel Klener, DrSc. I. interní klinika klinika hematologie 1. LF UK a VFN, Praha Recenzenti MUDr. Eva Helmichová, CSc. Homolka Premium Care
Pavel Klener ZÁKLADY KLINICKÉ ONKOLOGIE Galén Autor prof. MUDr. Pavel Klener, DrSc. I. interní klinika klinika hematologie 1. LF UK a VFN, Praha Recenzenti MUDr. Eva Helmichová, CSc. Homolka Premium Care
Kazuistika Hodgkinův lymfom
 Kazuistika Hodgkinův lymfom Pavla Štěpánková IV. Interní hematologická klinika FNHK a LFUK, Hradec Králové Regionální seminář Tereziánský dvůr 11.10.2018 19 letá žena Negativní OA 7/2011 febrilie>38st,
Kazuistika Hodgkinův lymfom Pavla Štěpánková IV. Interní hematologická klinika FNHK a LFUK, Hradec Králové Regionální seminář Tereziánský dvůr 11.10.2018 19 letá žena Negativní OA 7/2011 febrilie>38st,
Dosavadní zkušenosti s léčbou lenalidomidem v České republice
 Dosavadní zkušenosti s léčbou lenalidomidem v České republice Luděk Pour Ščudla V., Maisnar V., Gregora E., Schützová M., Špička I., Holánek M., Bačovský J., Straub J., Adam Z., Hájek R. Společná analýza
Dosavadní zkušenosti s léčbou lenalidomidem v České republice Luděk Pour Ščudla V., Maisnar V., Gregora E., Schützová M., Špička I., Holánek M., Bačovský J., Straub J., Adam Z., Hájek R. Společná analýza
Výsledky léčby Waldenströmovy makroglobulinemie na IHOK FN Brno
 C Z E C H G R O U P C Z E C H G R O U P Výsledky léčby Waldenströmovy makroglobulinemie na IHOK FN Brno Luděk Pour IHOK FN Brno 10-11.4. 2015 XIII. Roční setkání CMG C M G Č E S K Á M YE LO M O VÁ S K
C Z E C H G R O U P C Z E C H G R O U P Výsledky léčby Waldenströmovy makroglobulinemie na IHOK FN Brno Luděk Pour IHOK FN Brno 10-11.4. 2015 XIII. Roční setkání CMG C M G Č E S K Á M YE LO M O VÁ S K
Analýza dat LP Revlimid z registru pacientů v ČR
 XII. workshop mnohočetný myelom, hotel Galant, Mikulov 12. dubna 2014 Analýza dat LP Revlimid z registru pacientů v ČR (1.144 pacientů, 2007 3/2014) Vladimír Maisnar za Pacienti léčeni Revlimidem dle center
XII. workshop mnohočetný myelom, hotel Galant, Mikulov 12. dubna 2014 Analýza dat LP Revlimid z registru pacientů v ČR (1.144 pacientů, 2007 3/2014) Vladimír Maisnar za Pacienti léčeni Revlimidem dle center
Přímé sdělení pro zdravotnické pracovníky týkající se spojitosti mezi léčbou Sprycelem (dasatinibem) a plicní arteriální hypertenzí (PAH)
 Přímé sdělení pro zdravotnické pracovníky týkající se spojitosti mezi léčbou Sprycelem (dasatinibem) a plicní arteriální hypertenzí (PAH) Se souhlasem Evropské lékové agentury (EMA) a její
Přímé sdělení pro zdravotnické pracovníky týkající se spojitosti mezi léčbou Sprycelem (dasatinibem) a plicní arteriální hypertenzí (PAH) Se souhlasem Evropské lékové agentury (EMA) a její
Kasuistika onkologický pacient
 Kasuistika onkologický pacient U pana P.P., 68 letého muže, byl diagnostikován metastazující nádor ledviny. Dle provedených vyšetření byly kromě primárního nádoru pravé ledviny diagnostikovány i mnohočetné
Kasuistika onkologický pacient U pana P.P., 68 letého muže, byl diagnostikován metastazující nádor ledviny. Dle provedených vyšetření byly kromě primárního nádoru pravé ledviny diagnostikovány i mnohočetné
Fyzioterapie na transplantační jednotce kostní dřeně Mgr. Michaela Málková, Ph.D.
 Fyzioterapie na transplantační jednotce kostní dřeně Mgr. Michaela Málková, Ph.D. Klinika rehabilitace FN Motol dětská část Transplantace kostní dřeně (TKD) - historie pomocná léčebná metoda již cca 25
Fyzioterapie na transplantační jednotce kostní dřeně Mgr. Michaela Málková, Ph.D. Klinika rehabilitace FN Motol dětská část Transplantace kostní dřeně (TKD) - historie pomocná léčebná metoda již cca 25
Maximalizace efektu léčby relapsu lenalidomidem mnohočetného myelomu v reálné klinické praxi
 Maximalizace efektu léčby relapsu lenalidomidem mnohočetného myelomu v reálné klinické praxi Luděk Pour IHOK FN Brno XII. workshop mnohočetný myelom s mezinárodní účastí Roční setkání České myelomové skupiny
Maximalizace efektu léčby relapsu lenalidomidem mnohočetného myelomu v reálné klinické praxi Luděk Pour IHOK FN Brno XII. workshop mnohočetný myelom s mezinárodní účastí Roční setkání České myelomové skupiny
Jednání KR a VR ČNHP Praha
 Jednání KR a VR ČNHP 21. 2. 2017 Praha Program 10:30 Zahájení Představení registru v Clade-IS (Pavlíčková, 90 min) Postřehy k vyplňování (všichni, 30 min) 12:30 Oběd Propojení registru s WAPPS-Hemo (Ovesná,
Jednání KR a VR ČNHP 21. 2. 2017 Praha Program 10:30 Zahájení Představení registru v Clade-IS (Pavlíčková, 90 min) Postřehy k vyplňování (všichni, 30 min) 12:30 Oběd Propojení registru s WAPPS-Hemo (Ovesná,
Jaké máme leukémie? Akutní myeloidní leukémie (AML) Akutní lymfoblastická leukémie (ALL) Chronické leukémie, myelodysplastický syndrom,
 Akutní myeloidní leukémie (AML) Jaké máme leukémie? Akutní lymfoblastická leukémie (ALL) Chronické leukémie, myelodysplastický syndrom, Chronické leukémie, mnohočetný myelom, Někdy to není tak jednoznačné
Akutní myeloidní leukémie (AML) Jaké máme leukémie? Akutní lymfoblastická leukémie (ALL) Chronické leukémie, myelodysplastický syndrom, Chronické leukémie, mnohočetný myelom, Někdy to není tak jednoznačné
Thalidomid analýza 292 pacientů s MM léčených na IHOK FN Brno
 Thalidomid analýza 292 pacientů s MM léčených na IHOK FN Brno Marta Krejčí, Petra Kaisarová Základní charakteristika souboru (zahájení léčby thalidomidem) Základní charakteristika Pohlaví muži 146 (5.%)
Thalidomid analýza 292 pacientů s MM léčených na IHOK FN Brno Marta Krejčí, Petra Kaisarová Základní charakteristika souboru (zahájení léčby thalidomidem) Základní charakteristika Pohlaví muži 146 (5.%)
Co je to transplantace krvetvorných buněk?
 Co je to transplantace krvetvorných buněk? Transplantace krvetvorných buněk je přenos vlastní (autologní) nebo dárcovské (alogenní) krvetvorné tkáně. Účelem je obnova kostní dřeně po vysoce dávkové chemoterapii
Co je to transplantace krvetvorných buněk? Transplantace krvetvorných buněk je přenos vlastní (autologní) nebo dárcovské (alogenní) krvetvorné tkáně. Účelem je obnova kostní dřeně po vysoce dávkové chemoterapii
Roman Hájek Tomáš Jelínek. Plazmocelulární leukémie (PCL)
 Roman Hájek Tomáš Jelínek Plazmocelulární leukémie (PCL) Definice (1) vzácná forma plazmocelulární dyskrázie nejagresivnější z lidských monoklonálních gamapatií incidence: 0,04/100 000 obyvatel evropské
Roman Hájek Tomáš Jelínek Plazmocelulární leukémie (PCL) Definice (1) vzácná forma plazmocelulární dyskrázie nejagresivnější z lidských monoklonálních gamapatií incidence: 0,04/100 000 obyvatel evropské
Klinické ošetřovatelství
 Klinické ošetřovatelství zdroj www.wikiskripta.eu úprava textu Ing. Petr Včelák vcelak@kiv.zcu.cz Obsah 1 Klinické ošetřovatelství... 3 1.1 Psychiatrická ošetřovatelská péče... 3 1.1.1 Duševní zdraví...
Klinické ošetřovatelství zdroj www.wikiskripta.eu úprava textu Ing. Petr Včelák vcelak@kiv.zcu.cz Obsah 1 Klinické ošetřovatelství... 3 1.1 Psychiatrická ošetřovatelská péče... 3 1.1.1 Duševní zdraví...
Diferenciální diagnostika lymfadenomegalie a splenomegalie. Vít Procházka
 Diferenciální diagnostika lymfadenomegalie a splenomegalie Vít Procházka Motto Sebelepší hematoonkolog se neobejde bez spolupráce s lékařem prvního kontaktu. Mezioborová spolupráce je základem správné
Diferenciální diagnostika lymfadenomegalie a splenomegalie Vít Procházka Motto Sebelepší hematoonkolog se neobejde bez spolupráce s lékařem prvního kontaktu. Mezioborová spolupráce je základem správné
Velcade První výsledky z IHOK FN Brno. Luděk Pour. Roman Hájek, Marta Krejčí,Andrea Křivanová, Lenka Zahradová, Zdeněk Adam CMG
 Velcade První výsledky z IHOK FN Brno Luděk Pour Roman Hájek, Marta Krejčí,Andrea Křivanová, Lenka Zahradová, Zdeněk Adam CZECH CMG M Y E L O M A GROUP Č ESKÁ MYELOMOVÁ SKUPINA Velcade = bortezomib Nobelova
Velcade První výsledky z IHOK FN Brno Luděk Pour Roman Hájek, Marta Krejčí,Andrea Křivanová, Lenka Zahradová, Zdeněk Adam CZECH CMG M Y E L O M A GROUP Č ESKÁ MYELOMOVÁ SKUPINA Velcade = bortezomib Nobelova
Beličková 1, J Veselá 1, E Stará 1, Z Zemanová 2, A Jonášová 2, J Čermák 1
 Beličková 1, J Veselá 1, E Stará 1, Z Zemanová 2, A Jonášová 2, J Čermák 1 1 Ústav hematologie a krevní transfuze, Praha 2 Všeobecná fakultní nemocnice, Praha MDS Myelodysplastický syndrom (MDS) je heterogenní
Beličková 1, J Veselá 1, E Stará 1, Z Zemanová 2, A Jonášová 2, J Čermák 1 1 Ústav hematologie a krevní transfuze, Praha 2 Všeobecná fakultní nemocnice, Praha MDS Myelodysplastický syndrom (MDS) je heterogenní
Chronická myeloproliferativní onemocnění. L. Bourková, OKH FN Brno
 Chronická myeloproliferativní onemocnění L. Bourková, OKH FN Brno Chronická myeloproliferativní onemocnění Chronická myeloidní leukémie (CML) s t(9;22), gen BCR/ABL pozitivní (Chronická granulocytární
Chronická myeloproliferativní onemocnění L. Bourková, OKH FN Brno Chronická myeloproliferativní onemocnění Chronická myeloidní leukémie (CML) s t(9;22), gen BCR/ABL pozitivní (Chronická granulocytární
LEUKÉMIE. Markéta Vojtová
 LEUKÉMIE Markéta Vojtová Zhoubná onemocnění krve LEUKÉMIE akutní chronické myeloidní lymfoidní myeloidní lymfoidní LYMFOMY Hodgkinův non Hodgkinské Leukémie Trocha patofyziologie 1 Leukémie je zhoubné
LEUKÉMIE Markéta Vojtová Zhoubná onemocnění krve LEUKÉMIE akutní chronické myeloidní lymfoidní myeloidní lymfoidní LYMFOMY Hodgkinův non Hodgkinské Leukémie Trocha patofyziologie 1 Leukémie je zhoubné
SEZNAM LABORATORNÍCH VYŠETŘENÍ
 Laboratoř morfologická SME 8/001/01/VERZE 01 SEZNAM LABORATORNÍCH VYŠETŘENÍ Cytologické vyšetření nátěru kostní dřeně Patologické změny krevního obrazu, klinická symptomatologie s možností hematologického
Laboratoř morfologická SME 8/001/01/VERZE 01 SEZNAM LABORATORNÍCH VYŠETŘENÍ Cytologické vyšetření nátěru kostní dřeně Patologické změny krevního obrazu, klinická symptomatologie s možností hematologického
NÁRODNÍ REGISTR CMP. Cévní mozkové příhody epidemiologie, registr IKTA Kalita Z.
 NÁRODNÍ REGISTR CMP Cévní mozkové příhody epidemiologie, registr IKTA Kalita Z.. X.Cerebrovaskulární seminář, 23.9.2011 Kunětická Hora Sympozium firmy ZENTIVA Význam registru Odkud máme informace : ÚZIS
NÁRODNÍ REGISTR CMP Cévní mozkové příhody epidemiologie, registr IKTA Kalita Z.. X.Cerebrovaskulární seminář, 23.9.2011 Kunětická Hora Sympozium firmy ZENTIVA Význam registru Odkud máme informace : ÚZIS
Struktura parametrické dokumentace registru ATTRA Diagnóza: Juvenilní idiopatická artritida
 Struktura parametrické dokumentace registru ATTRA Diagnóza: Juvenilní idiopatická artritida Vstupní údaje... 1 Identifikační údaje pacienta... 1 Identifikační údaje centra... 1 Vstupní vyšetření... 2 Vstupní
Struktura parametrické dokumentace registru ATTRA Diagnóza: Juvenilní idiopatická artritida Vstupní údaje... 1 Identifikační údaje pacienta... 1 Identifikační údaje centra... 1 Vstupní vyšetření... 2 Vstupní
R A P I D EARLY ADMINISTRATION OF ACTIVATED FACTOR VII IN PATIENTS WITH SEVERE BLEEDING ZÁZNAM SUBJEKTU HODNOCENÍ (CRF) Číslo centra.
 R A P I D EARLY ADMINISTRATION OF ACTIVATED FACTOR VII IN PATIENTS WITH SEVERE BLEEDING ZÁZNAM SUBJEKTU HODNOCENÍ (CRF) Číslo centra Číslo pacienta Iniciály pacienta VÝBĚR A VYŘAZENÍ PACIENTŮ Kritéria
R A P I D EARLY ADMINISTRATION OF ACTIVATED FACTOR VII IN PATIENTS WITH SEVERE BLEEDING ZÁZNAM SUBJEKTU HODNOCENÍ (CRF) Číslo centra Číslo pacienta Iniciály pacienta VÝBĚR A VYŘAZENÍ PACIENTŮ Kritéria
Klinická studie CMG 2008
 Klinická studie 2008 Marta Krejčí Interní hematoonkologická klinika FN Brno Název 2008 Multicentrická randomizovaná klinická studie fáze f 3 srovnávaj vající účinnost a bezpečnost kombinované chemoterapie
Klinická studie 2008 Marta Krejčí Interní hematoonkologická klinika FN Brno Název 2008 Multicentrická randomizovaná klinická studie fáze f 3 srovnávaj vající účinnost a bezpečnost kombinované chemoterapie
Název IČO Fakultní nemocnice Brno. PŘÍLOHA č. 2 Vstupní formulář / V-01 / / 4_05 SMLOUVY O POSKYTOVÁNÍ A ÚHRADĚ ZDRAVOTNÍ PÉČE
 IČO 6 5 2 6 9 7 0 5 IČZ smluvního ZZ 7 2 1 0 0 0 0 0 Číslo smlouvy 2 B 7 2 M 0 0 4 Název IČO Fakultní nemocnice Brno PŘÍLOHA č. 2 Vstupní formulář / V-01 / 7.07.07 / 4_05 SMLOUVY O POSKYTOVÁNÍ A ÚHRADĚ
IČO 6 5 2 6 9 7 0 5 IČZ smluvního ZZ 7 2 1 0 0 0 0 0 Číslo smlouvy 2 B 7 2 M 0 0 4 Název IČO Fakultní nemocnice Brno PŘÍLOHA č. 2 Vstupní formulář / V-01 / 7.07.07 / 4_05 SMLOUVY O POSKYTOVÁNÍ A ÚHRADĚ
Lenalidomid. Statistická analýza léčeb z českých center / rmgnew.registry.cz. rmgnew.registry.
 1 Lenalidomid Statistická analýza 1 761 léčeb z českých center 2013 11/2016 Léčebné centrum 2 Celkový počet záznamů N = 1 761 OKH České Budějovice 1,6 KN Liberec 1,8 FNKV Plzeň 3,2 FNKV Praha 8,4 HO Nový
1 Lenalidomid Statistická analýza 1 761 léčeb z českých center 2013 11/2016 Léčebné centrum 2 Celkový počet záznamů N = 1 761 OKH České Budějovice 1,6 KN Liberec 1,8 FNKV Plzeň 3,2 FNKV Praha 8,4 HO Nový
Hlášení těhotenství (formulář)
 Hlášení těhotenství (formulář) OSOBA PODÁVAJÍCÍ HLÁŠENÍ Počáteční Následné sledování Jméno a příjmení: Upřesnění: Lékař (specializace) Lékárník pacient ostatní (upřesněte) Kontaktní adresa: Telefonní číslo:
Hlášení těhotenství (formulář) OSOBA PODÁVAJÍCÍ HLÁŠENÍ Počáteční Následné sledování Jméno a příjmení: Upřesnění: Lékař (specializace) Lékárník pacient ostatní (upřesněte) Kontaktní adresa: Telefonní číslo:
Srovnání dávkování Revlimidu denně a obden
 Srovnání dávkování Revlimidu denně a obden Luděk Pour a Revlimid denně vs obden Úvod Soubor pacientů Toxicita Léčebná odpověď a parametry přežití Závěr Úvod Lenalidomid 25 mg denně účinnější než 50 mg
Srovnání dávkování Revlimidu denně a obden Luděk Pour a Revlimid denně vs obden Úvod Soubor pacientů Toxicita Léčebná odpověď a parametry přežití Závěr Úvod Lenalidomid 25 mg denně účinnější než 50 mg
Nežádoucí účinky nových léků
 Nežádoucí účinky nových léků MUDr. Jan Straub XII. Myeloma workshop Mikulov 12.4. 2014 Nežádoucí účinky nových léků thalidomid bortezomib lenalidomid Obecné shrnutí + výsledky registračních studií Srovnání
Nežádoucí účinky nových léků MUDr. Jan Straub XII. Myeloma workshop Mikulov 12.4. 2014 Nežádoucí účinky nových léků thalidomid bortezomib lenalidomid Obecné shrnutí + výsledky registračních studií Srovnání
Současný stav léčby chronické myeloidní leukemie pomocí inhibitorů tyrozinové kinázy
 Současný stav léčby chronické myeloidní leukemie pomocí inhibitorů tyrozinové kinázy Hana Klamová Ústav hematologie a krevní transfuze, Ústav klinické a experimentální hematologie 1. LF UK, Praha Chronická
Současný stav léčby chronické myeloidní leukemie pomocí inhibitorů tyrozinové kinázy Hana Klamová Ústav hematologie a krevní transfuze, Ústav klinické a experimentální hematologie 1. LF UK, Praha Chronická
RMG = nutná součást dalšího zlepšování péče o pacienty s MM
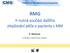 RMG = nutná součást dalšího zlepšování péče o pacienty s MM V. Maisnar za Českou myelomovou skupinu Epidemiologická data MM (dle NOR) 1% všech malignit, 10% hematologických Muži/Ženy = 3/2, medián věku:
RMG = nutná součást dalšího zlepšování péče o pacienty s MM V. Maisnar za Českou myelomovou skupinu Epidemiologická data MM (dle NOR) 1% všech malignit, 10% hematologických Muži/Ženy = 3/2, medián věku:
Analytický report projektu AVASTIN klinický registr
 Analytický report projektu AVASTIN klinický registr Karcinom prsu Stav k datu 10. 4. 2011 Registr Avastin je podporován výzkumným ý grantem firmy Roche. Česká Institut t onkologická biostatistiky společnost
Analytický report projektu AVASTIN klinický registr Karcinom prsu Stav k datu 10. 4. 2011 Registr Avastin je podporován výzkumným ý grantem firmy Roche. Česká Institut t onkologická biostatistiky společnost
Nová diagnóza = Studiová indikace. První relaps = Standardní léčba
 Thalidomid dostupné léčebné protokoly Nová diagnóza = Studiová indikace První relaps = Standardní léčba C M G Thalidomid/dexamethason vs MP for induction therapy and Thalidomide/Intron vs Intron A for
Thalidomid dostupné léčebné protokoly Nová diagnóza = Studiová indikace První relaps = Standardní léčba C M G Thalidomid/dexamethason vs MP for induction therapy and Thalidomide/Intron vs Intron A for
Pomalidomid první rok léčby v ČR
 C Z E C H G R O U P CZECH GROUP 1 Pomalidomid první rok léčby v ČR Luděk Pour IHOK FN Brno XIII. Výroční setkání CMG 10. 4. 2015 Mikulov C M G M Y E L O M A Č E S K Á M YE LO M O VÁ S K U P IN A CMG ČESKÁ
C Z E C H G R O U P CZECH GROUP 1 Pomalidomid první rok léčby v ČR Luděk Pour IHOK FN Brno XIII. Výroční setkání CMG 10. 4. 2015 Mikulov C M G M Y E L O M A Č E S K Á M YE LO M O VÁ S K U P IN A CMG ČESKÁ
Nové znění informací o přípravku výňatky z doporučení výboru PRAC k signálům
 25 February 2016 EMA/PRAC/137776/2016 Corr 1 Pharmacovigilance Risk Assessment Committee (PRAC) Nové znění informací o přípravku výňatky z doporučení výboru PRAC k signálům Přijato na zasedání výboru PRAC
25 February 2016 EMA/PRAC/137776/2016 Corr 1 Pharmacovigilance Risk Assessment Committee (PRAC) Nové znění informací o přípravku výňatky z doporučení výboru PRAC k signálům Přijato na zasedání výboru PRAC
Velcade. Statistická analýza 27 pacientů
 Velcade Statistická analýza 27 pacientů Pacienti začínající s léčbou Velcade v roce 29 Celkový počet záznamz znamů N = 27 Havířov N = 15 55.6 % 11.1 % Pelhřimov N = 3 Opava N = 3 11.1 %. % 11.1 % 11.1
Velcade Statistická analýza 27 pacientů Pacienti začínající s léčbou Velcade v roce 29 Celkový počet záznamz znamů N = 27 Havířov N = 15 55.6 % 11.1 % Pelhřimov N = 3 Opava N = 3 11.1 %. % 11.1 % 11.1
Metodika. Registr pacientů RESET. (REgistr SElárních Tumorů) Stav k 19.09.2011
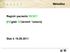 Metodika Registr pacientů RESET (REgistr SElárních Tumorů) Stav k 19.09.2011 Cíl studie Cíl projektu: - Zjistit důležitá data prevalence makroprolaktinomů v ČR a SR - Popsat jednotlivé používané léčebné
Metodika Registr pacientů RESET (REgistr SElárních Tumorů) Stav k 19.09.2011 Cíl studie Cíl projektu: - Zjistit důležitá data prevalence makroprolaktinomů v ČR a SR - Popsat jednotlivé používané léčebné
Farmakovigilance v KH změny a novinky
 Státní ústav pro kontrolu léčiv [ 1 ] Farmakovigilance v KH změny a novinky MUDr. Tomáš Boráň Oddělení klinického hodnocení Farmakovigilance v KH [ 2 ] Obsah CT-3 Aktualizace pokynu KLH-21 DSUR Chyby v
Státní ústav pro kontrolu léčiv [ 1 ] Farmakovigilance v KH změny a novinky MUDr. Tomáš Boráň Oddělení klinického hodnocení Farmakovigilance v KH [ 2 ] Obsah CT-3 Aktualizace pokynu KLH-21 DSUR Chyby v
Hlášení těhotenství (formulář) RO-GNE: HLÁŠENÍ TĚHOTENSTVÍ
 Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že nahlásíte jakékoli nežádoucí účinky, které se u Vás vyskytnou. Zároveň žádáme
Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že nahlásíte jakékoli nežádoucí účinky, které se u Vás vyskytnou. Zároveň žádáme
PŘÍLOHA č. 2 Vstupní formulář / V-01 / / 4_12 SMLOUVY O POSKYTOVÁNÍ A ÚHRADĚ HRAZENÝCH SLUŽEB
 IČO 6 4 2 3 Záčíslí IČO IČZ smluvního ZZ 5 2 Číslo smlouvy 2 A 5 M 3 Název IČO Fakultní nemocnice v Motole PŘÍLOHA č. 2 Vstupní formulář / V-1 / 8.11.11 / 4_12 SMLOUVY O POSKYTOVÁNÍ A ÚHRADĚ HRAZENÝCH
IČO 6 4 2 3 Záčíslí IČO IČZ smluvního ZZ 5 2 Číslo smlouvy 2 A 5 M 3 Název IČO Fakultní nemocnice v Motole PŘÍLOHA č. 2 Vstupní formulář / V-1 / 8.11.11 / 4_12 SMLOUVY O POSKYTOVÁNÍ A ÚHRADĚ HRAZENÝCH
