Devyser CFTR Italia v2. Návod k použití
|
|
|
- Emil Vaněk
- před 6 lety
- Počet zobrazení:
Transkript
1 Devyser CFTR Italia v2 Kat. No.: 8-A032.2 Pro in vitro diagnostiku Návod k použití Strana 1 z 34
2 OBSAH OBSAH 2 1. SEZNÁMENÍ SE SYSTÉMEM DEVYSER ITALIA v2 4 Použití 4 Součástí kitu 4 Postup 4 Background 4 Princip metody 4 2. UPOZORNĚNÍ A BEZPEČNOSTNÍ OPATŘENÍ 5 3. SYMBOLY POUŽITÉ NA NÁLEPKÁCH 6 4. POTŘEBNÝ MATERIÁL Součástí kitu 7 Konfigurace 7 Složky Požadované položky, které nejsou v soupravě 7 Příprava reagencií 7 Extrakce DNA 7 Amplifikace 7 Detekce 7 Size Standard Dye Set Calibration SKLADOVÁNÍ A POŽADAVKY NA POUŽITÍ 9 6. POŽADAVKY NA VZOREK 10 Klinické vzorky 10 DNA extrakce a měření 10 Extrakce DNA z plné krve 10 Extrakce DNA ze suché kapky 11 Postup a skladování 11 Kontroly INSTRUKCE PRO POUŽITÍ Postup Devyser CFTR Italia v Příprava vzorků a amplifikace PCR 12 Příprava vzorků 12 Přidání vzorku 12 Amplifikace Detekce 14 Příprava vzorků 14 Příprava vzorku pro kapilární elektroforézu 14 Příprava přístroje 14 Run Modules ANALÝZA DAT Doporučení správné laboratorní praxe Analýza dat Kit Devyser CFTR Italia v2 16 Zdravé (nemutované) alely 16 Mutantní alely Vyhodnocení 16 Cutoff signály píků 16 Sizing DNA fragmentů 17 Cross-mix ID markery 17 Strana 2 z 34
3 Identifikace cross-mix vzorků 17 Zdravé (nemutované) alely 17 Heterozygótní mutace 17 Homozygótní mutace 17 Alel specifické výjimky 17 Dele14b_17b/Dele17a_18 složený heterozygot 17 Výskyt mutantního píku alely Dele14b_17b 17 Nepřímá detekce krátkých inzercí a delecí (indels) 18 Mutace v místě nasedání primeru a polymorfismy 19 Normální alely detekované v mixu Italia 1 20 Normální (zdravé) alely detekované v mixu Italia Troubleshooting 22 Artefakty PCR 22 Elektroforetické artefakty 23 Copy number varianty VÝKONOSTNÍ CHARAKTERISTIKY 25 Sensitivita 25 Specificita 25 Cross-Reaktivita LIMITACE POSTUPU UPOZORNĚNÍ KUPUJÍCÍMU REFERENCE KONTAKTNÍ INFORMACE HISTORIE REVIZÍ 32 Strana 3 z 34
4 1. SEZNÁMENÍ SE SYSTÉMEM DEVYSER ITALIA v2 Použití Kit Devyser CFTR Italia v2 je určen pro in vitro kvalitativní genotypizaci zdravých a mutantních alel v genu pro transmembránový regulátor cystické fibrózy (CFTR) v lidské genomové DNA. Tento produkt není určen pro samostatnou diagnostiku cystické fibrózy. Součástí kitu Kit Devyser CFTR Italia v2 obsahuje reagencie připravené k použití pro PCR amplifikaci genetických markerů. Postup DNA extrakce: Kit Devyser CFTR Italia v2 byl validován s použitím QIAamp DNA Blood Mini QIAcube Kit (Qiagen, cat.# 51126) a QIAsymphony DSP DNA Midi Kit (Qiagen, cat.# ) pro extrakci DNA z lidské krve (EDTA) a s použitím QIAamp DNA Blood Mini Kit (Qiagen, cat.# 51104) pro extrakci DNA ze suché kapky krve. Amplifikace: Kit Devyser CFTR Italia v2 byl validován s použitím Life Technologies/Thermo Fisher Scientific Veriti Thermal cycler. Detekce: Genetické analyzátory Life Technologies/Thermo Fisher Scientific/ABI (ABI 310, 3130, 3500, 3730) podporující detekci Dye Set DEV-5. Background Cystická Fibróza je dedičné onemocnění postihující děti a mladé dospělé. Od objevu genu CFTR v roce , bylo popsáno více než 1900 mutací a variant v genu CFTR 2. Mutace v CFTR genu může způsobit respirační onemocnění. Další CFTR poruchy způsobené nefunkčností transmembránového regulátoru CF zahrnují kongenitální bilaterální absenci vas (CBAVD), akutní recidivující nebo chronickou pankreatitidu a šířící-se bronchiektázie 3,4. Princip metody Kit Devyser CFTR Italia v2 je založen na multiplexní alelicky specifické PCR amplifikaci a detekci zdravých, nemutovaných, a mutovaných alel v CFTR genu. Alelicky specifická PCR amplifikace generuje fluorescenčně značené fragmenty, které jsou analyzovány kapilární elektroforézou na Genetickém analyzátoru. Amplifikované fragmenty jsou identifikovány podle délky a fluorescenční barvy. Strana 4 z 34
5 2. UPOZORNĚNÍ A BEZPEČNOSTNÍ OPATŘENÍ A. Devyser CFTR Italia v2 byl validován při použití celkového amplifikačního o objemu 12,5 µl. Změna reakčního objemu může vést k nesprávným výsledkům. B. Předejděte mikrobiální kontaminaci při vyjímání alikvotů z reakčních zkumavek. Doporučujeme používat špičky s filtry. C. Nemíchejte reagencie z různých šarží ani z různých zkumavek stejné šarže. D. Nepoužívejte soupravu s prošlou záruční lhůtou. E. Nepoužívejte otevřené nebo poškozené reagenční zkumavky. F. Práce v laboratoři má postupovat jedním směrem. Začíná přípravou reagencií, postupující do prostoru pro extrakci DNA, do prostoru pro amplifikaci DNA a nakonec do prostoru pro detekci. Přípravu reagencií a extrakci DNA provádějte v oddělených prostorách. Přístroje i spotřební materiál mají být lokalizovány pouze v příslušném prostoru a nesmí se přenášet mezi těmito oddělenými prostory. V příslušném prostoru používejte rukavice a při jeho opouštění je vyměňte za nové. Přístroje ani spotřební materiál pro přípravu reagencií nepoužívejte pro extrakci DNA. Přístroje a spotřební materiál pro amplifikaci a detekci nepřenášejte mimo tyto prostory. G. Nakládání s reagenciemi a vzorky, jejich použití, skladování a likvidace musí splňovat požadavky ČSN pro nakládání s biohazardním materiálem. H. Při práci se vzorky a reagenciemi soupravy používejte nepudrované rukavice, laboratorní plášť a ochranu očí. Po skončení práce se vzorky a reagenciemi si řádně omyjte ruce. Strana 5 z 34
6 3. SYMBOLY POUŽITÉ NA NÁLEPKÁCH Šarže Exspirace Počet testů Skladujte při teplotě nižší nebo rovné Katalogové číslo Výrobce In vitro diagnostický medicínský prostředek Strana 6 z 34
7 4. POTŘEBNÝ MATERIÁL 4.1 Součástí kitu Konfigurace Kit Devyser CFTR Italia v2 obsahuje reagencie pro analýzu 48 vzorků. Složky Tabulka 1. Komponenty, které jsou součástí kitu Devyser CFTR Italia v2. Barva víčka Barva Zkumavky Štítek Katal.č. Obsah soupravy Oranžová Čirá PCR Activator 4-A018 2 Fialová Hnědavá Italia 1 4-A229 1 Zlatá Hnědavá Italia 2 4-A Požadované položky, které nejsou v soupravě Příprava reagencií Plast pro termocykler Použijte pipetu a špičky s filtrem nebo dávkovací pipetu s vyměnitelnými špičkami Nepudrované chirurgické rukavice Extrakce DNA Reagencie a přístroje dle požadavků výrobce extrakční soupravy Pipeta nebo dispenzor a špičky s filtry Nepudrované chirurgické rukavice Amplifikace PCR Cycler: Life Technologies/Thermo Fisher Scientific Veriti Thermal cycler. Při použití jiného PCR cycleru musí být dodržen ramp: ohřev 1,6 C/s, chlazení 1,6 C/s. Pipeta nebo dispenzor a špičky s filtry Nepudrované chirurgické rukavice Detekce Life Technologies/Thermo Fisher Scientific/ABI Genetic Analyzer (ABI 310, 3130, 3500, 3730) Metodika je validovaná na polymerech: POP-7 Hi-Di Formamide, čistota pro genetickou analýzu 1x Genetic Analyzer Buffer Pipeta nebo dispenzor a špičky s filtry Nepudrované chirurgické rukavice Strana 7 z 34
8 Size Standard 560 SIZER ORANGE (Devyser Art. No.: 8-A402). 4.3 Dye Set Calibration ABI 3130, 3730: Použijte DEV-5 Dye Set MultiCap kit (Devyser Art. No.: 8-A401) s Any5Dye Dye Set. ABI 3500: Použijte DEV-5 Dye Set MultiCap kit (Devyser Art. No.: 8-A401) a nastavte DEV-5 Dye Set. ABI 310 Matrix file generation: Použijte DEV-5 Dye Set SingleCap kit (Devyser Art. No.: 8-A400). Zvolte soubor modulu GS STR POP4 (1 ml) G5.md5. Detailní instrukce pro Dye set kalibraci je možno stáhnout z Download sekce na webu: a Strana 8 z 34
9 5. 5. SKLADOVÁNÍ A POŽADAVKY NA POUŽITÍ A. Skladujte všechny komponenty při maximální teplotě -18 C. B. Reakční Master Mixy (připravené přidáním Italia 1 a Italia 2 do zkumavek s PCR aktivátorem) mohou být uchovávány při +2 až +8 C 7 dní a pod -18 C 60 dnů. Vyvarujte se opakovanému rozmrazováni a zmrazování. C. Likvidace zbytků reagencií musí být v souladu s legislativou ČR. D. Nemíchejte reagencie z různých šarží. Strana 9 z 34
10 6. POŽADAVKY NA VZOREK Klinické vzorky Kit Devyser CFTR Italia v2 byl validován pro použití s lidskou genomovou DNA izolovanou z plné krve (EDTA) a suchých kapek krve. DNA extrakce a měření Kit Devyser CFTR Italia v2 byl validován s použitím QIAamp DNA Blood Mini Kit (Qiagen, kat. č ) a QIAsymphony DSP DNA Midi Kit (Qiagen, cat.# ) pro extrakci DNA z lidské krve (EDTA) a s použitím QIAamp DNA Blood Mini Kit (Qiagen, cat.# 51104) pro extrakci DNA ze suché kapky krve. Pokud použijete jinou extrační metodu pro izolaci DNA je nutná validace s kitem Devyser CFTR Italia v2 před použitím výsledků k diagnostickým účelům. Konzistentní výsledky jsou dosaženy při dodržení doporučených podmínek PCR a podmínek analýzy (viz sekce ) a s koncentrací DNA mezi 3,75 and 25 ng/pcr reakci (1,5-10 ng genomové DNA/µL vzorek). Pro optimální výsledky je vhodné upravit koncentraci purifikované DNA na 5 ng/µl v 0,1xTE pufru nebo vodě (PCR grade kvality). Koncentrace a čistota DNA je důležitá pro úspěšné testování kitem Devyser CFTR Italia v2. DNA nesmí být kontaminována proteiny, solemi a dalšími PCR inhibitory (např. Zbytkovým ethanolem z extrakce DNA). Nedostatečná kvalita DNA může způsoby neúspěšnou amplifikaci nebo zvýšit signál nežádoucího pozadí během detekce. Přesné a reprodukovatelné měření koncentrace DNA je důležitá, protože přidáním příliš mnoho DNA do PCR reakce může způsobit falešně pozitivní výsledky a příliš malé množství DNA v PCR reakci může naopak způsobit selhání PCR amplifikace a detekce. Kvalitní DNA je důležitá pro přesné a reprodukovatelné stanovení koncentrace DNA ve vzorku. Vzhledem k odchylkám mezi technikami kvantifikace DNA je důležité, aby si uživatel ověřil, že jím používaná technika kvantifikace DNA dává důvěryhodné výsledky, které korelují se skutečnými výsledky získanými při použití kitu Devyser CFTR Italia v2. Uživatel si musí být vědom změn a omezení různých metod kvantifikace DNA. Všechny koncentrace uvedené v tomto manuálu byly stanoveny pomocí Qubit dsdna HS Assay Kit (Life Technologies/Thermo Fisher Scientific, cat.# Q32851/Q32854). Koncentrace DNA stanovená Qubit dsdna HS Assay Kit může být odlišná od koncentrace DNA změřené jinými metodami. Extrakce DNA z plné krve Konzistentní výsledky lze dosáhnout s lidskou genomovou DNA extrahovanou z plné krve (EDTA) pomocí kitu QIAamp DNA Blood Mini QIAcube Kit (Qiagen, cat.# 51126) nebo QIAsymphony DSP DNA Midi Kit (Qiagen, cat.# ). QIAamp DNA Blood Mini QIAcube Kit Použijte protokol se vstupním objemem 200 µl čerstvé plné krve a elucí pomocí 100 µl elučního pufru. Změřte koncentraci purifikované DNA a zřeďte vzorek na 5 ng/µl. Strana 10 z 34
11 QIAsymphony DSP DNA Midi Kit Použijte protokol se vstupním objemem 400 µl čerstvé plné krve a elucí pomocí 200 µl elučního pufru. Změřte koncentraci purifikované DNA a zřeďte vzorek na 5 ng/µl. Extrakce DNA ze suché kapky Konzistentní výsledky lze dosáhnout s lidskou genomovou DNA extrahovanou ze suché kapky pomocí protokolu pro suché kapky uvedeném v manuálu QIAamp DNA Blood Mini Kit (Qiagen, cat.# 51104). Použijte protocol pro suché kapky se vstupním materiálem 2 terčíky 3 mm v průměru a elucí pomocí µl elučního pufru. Postup a skladování Dle pokynů výrobce. Kontroly CFTR zdravá DNA kontrola (Alelický ladder) Doporučejeme použít zdravou DNA kontrolu (nemutovanou DNA) pro každý run jako alelický ladder pro mix Italia 1. Negativní kontrola Doporučujeme použít negativní kontrolu (bez DNA) v každém runu. Pokud detekujete píky v mixu Italia 1 a Italia 2, tak to indikuje kros kontaminaci PCR produktem. Mutovaná pozitivní kontrola Vzorky se známou CFTR mutací mohou být použity jako pozitivní kontrola. Strana 11 z 34
12 7. INSTRUKCE PRO POUŽITÍ 7.1 Postup Devyser CFTR Italia v2 Každý kit Devyser Italia v2 obsahuje reagencie pro 48 vzorků. Reakční master mixy připravte ještě před přípravou vzorků, pokud provedete celou metodu v jediném dni. Pouze pokud extrahujete vzorky DNA den předem, připravte master mixy až den poté. Devyser CFTR Italia v2 byl validován při použití celkového amplifikačního o objemu 12,5 µl. Změna reakčního objemu může vést k nesprávným výsledkům. Reakční Master Mix se připravuje přidáním směsi Italia 1 a Italia 2 do zkumavek s PCR Aktivátorem. Ujistěte se, že jsou oba Italia 1 and Italia 2 před použitím kompletně rozmrazeny. 1. Stočte krátce každou zkumavku. V tomto kroku zkumavky nevortexujte. 2. Přidejte 500 μl příslušného Italia 1 a Italia 2 do zkumavek s PCR Aktivátorem. 3. Opatrně promíchejte reakční master mix několikerým nasátím pipetou od spodu zkumavky. 4. Vortexujte aktivované reakční mixy a lehce stočte. 5. Napipetujte 10 µl smíchaného master mixu do PCR zkumavek. 6. Uzavřete zkumavky a krátce je stočte. 7. Pokračujte krokem 7.2. Smíchaný reakční master mix je stabilní při +2-8 C po dobu 7 dní a při méně než -18 C po dobu 60 dní. Vyvarujte se opakovanému rozmrazováni a zmrazování. 7.2 Příprava vzorků a amplifikace PCR Příprava vzorků Pokud použijete jinou extrační metodu pro izolaci DNA je nutná validace s kitem Devyser CFTR Italia v2 před použitím výsledků k diagnostickým účelům. Konzistentní výsledky jsou dosaženy při dodržení doporučených podmínek PCR a podmínek analýzy (viz tabulka 2-5) a s koncentrací DNA mezi 3,75 and 25 ng/pcr reakci (1,5-10 ng genomové DNA/µL vzorek). Pro optimální výsledky je vhodné upravit koncentraci purifikované DNA na 5 ng/µl v 0,1xTE pufru nebo vodě (PCR grade kvality). Vzorky s nízkou koncentrací DNA mohou být analyzovány, ale je nutné zvýšit počet PCR cyklů z 29 na 31. Neanalyzujte vzorky s koncentrací DNA nad 1,5 ng/μl s použitím 31 počtu PCR cyklů, protože to může způsobit falešně pozitivní signály. Přidání vzorku V prostoru odděleném od prostor pro přípravu reagencií a amplifikaci a detekci. Každý klinický vzorek musí být otestován mixem Italia 2 za účelem detekce mutací, na které je tento kit zacílen. Pro zjištění jestli je detekovaná mutace heterozygótní nebo homozygótní je nutné dotestovat vzorek i mixem Italia Přidejte 2,5 µl vzorku (1,5-10 ng genomové DNA/µL vzorku) do každé PCR zkumavky se smíchaným reakčním master mixu Italia 1 a Italia 2 (z kroku 7.1). 2. Zkumavky uzavřete a krátce stočte. Strana 12 z 34
13 Amplifikace Kit Devyser CFTR Italia v2 byl validován s použitím Life Technologies/Thermo Fisher Scientific Veriti Thermal cycler. Jiné PCR cyclery musí být otestovány a zhodnoceny, že mohou být použity pro diagnostiku kitem Devyser Italia v2. PCR cyclery by měly být pravidelně kalibrovány a udržovány tak, aby byly přesné. Pro Life Technologies/Thermo Fisher Scientific Veriti Thermal cycler: V "Tools Menu" vyberte "Convert a Method". V dalším kroku vyberte "9700 Max Mode" a poté zadejte PCR profil tak, jak je uvedeno níže. Ostatní thermal cyclery: Pro Life Technologies/Thermo Fisher Scientific/ABI GeneAmp PCR System 9700, nastavte ramp speed na MAX. Důležité! Na ostatních cyclerech nastavte Ramping na ohřev 1,6 C/s a chlazení 1,6 C/s. Amplifikační prostor: Naprogramujte termocykler pro amplifikaci dle následujícího teplotního profilu (přečtěte si manuál pro podrobné informace o programování termocykleru): 95 C 15 min 94 C 30 sec - 62 C 60 sec - 72 C 60 - sec for 29 cycles 72 C 15 min 4 C FOREVER 1. Nastavte reakční objem 13 µl. 2. Nastavte ramp na (ohřev 1,6 C/s, chlazení 1,6 C/s). 3. Spusťtte amplifikaci (doba trvání cca 2,5 h). 4. Po amplifikaci vyjměte zkumavky s amplifikační reakcí z termocykleru, vložte je do stojánku. Krátce stočte. Opatrně sejměte víčka, abyste zabránili kontaminaci aerosolem. Amplifikovaný materiál nepřenášejte do před-amplifikačních prostor. Amplifikovaný materiál musí zůstat v amplifikačním a detekčním prostoru. Strana 13 z 34
14 7.3 Detekce Příprava vzorků Řiďte se manuály pro příslušný analyzátor Life Technologies/Thermo Fisher Scientific ohledně údržby a nastavení přístroje. Před spuštěním analýzy soupravou Devyser CFTR Italia v2, přístroj musí být kalibrován na Dye Set DEV-5. Detaily v sekci 4.3. Příprava vzorku pro kapilární elektroforézu 1. Připravte nanášecí směs smícháním 2 µl velikostního standardu (560 SIZER ORANGE) s 100 µl Hi-Di Formamidu (směs stačí pro 6 jamek/zkumavek). 2. Vortexujte 15 s. 3. Do jamek mikrotitrační destičky (nebo do jednotlivých zkumavek v případě ABI 310) napipetujte po 15 μl nanášecí směsi před vložením do analyzátoru. 4. Přidejte 1,5 µl PCR amplifikátu vzorku do příslušné jamky nebo zkumavky s ELFO nanášecí směsí. 5. Uzavřete destičku nebo zkumavky. 6. Krátce centrifugujte destičku nebo zkumavky a ujistěte se, že v roztoku nejsou žádné bublinky. 7. Vložte destičku nabo zkumavky do ABI Genetického analyzátoru. Příprava přístroje Připravte si pracovní protokol s využitím software analyzátoru s následujícím nastavením: Sample ID Dye Set: Any5Dye/DEV-5 Run module Run Modules Doporučené run moduly pro různé typy Genetických analyzátorů Life Technologies/Thermo Fisher Scientific (ABI 310, 3130, 3500, 3730) jsou uvedeny v tabulkách 2-5. Množství PCR produktu nasátého do kapiláry může být upraveno změnou injekčního napětí a injekční doby. Tabulka 2. Nastavení Run modulu pro ABI310 (module file GS STR POP4 (1 ml) G5.md5 ). Run Parameters POP-4 Capillary length 47 cm Run temperature 60 C Injection voltage 15 kv Injection time 5-15 s Run voltage 15 kv Run time 40 min Strana 14 z 34
15 Tabulka 3. Nastavení Run modulu pro ABI Run Parameters POP-4/POP-7 Capillary length 36 cm Run temperature 60 C Injection voltage 1,5 kv Injection time 20 s Run voltage 15 kv Run time 1500 s Tabulka 4. Nastavení Run modulu pro ABI Run Parameters POP-7 Capillary length 50 cm Run temperature 60 C Injection voltage 1,6 kv Injection time 15 s Run voltage 19,5 kv Run time 1500 s Tabulka 5. Nastavení Run modulu pro ABI Run Parameters POP-7 Capillary length 36 cm Run temperature 60 C Injection voltage 1,6 kv Injection time 15 s Run voltage 15 kv Run time 1500 s Strana 15 z 34
16 8. ANALÝZA DAT 8.1 Doporučení správné laboratorní praxe Doporučení správné laboratorní praxe pro molekulární diagnostiku cystické fibrózy a CFTR příbuzné poruchy byly stanoveny, viz odkazy 5-7 v kapitole Analýza dat Každý jedinec má dvě kopie (alely) CFTR genu a je považován za homozygota pro danou sekvenci DNA, pokud mají obě alely stejnou sekvenci. Jedinec je považován za heterozygota pro danou sevenci DNA, pokud se dvě alely liší v dané sekvenci. 8.3 Kit Devyser CFTR Italia v2 Kit Devyser CFTR Italia v2 se používá pro kvalitativní analýzu mutací v CFTR genu. Analýza se provádí dvěma oddělenými Italia v2 mixy (Italia 1 a Italia 2). Mix Italia 1 detekuje nemutované, zdravé alely. Odpovídající mutantní alely jsou detekovány mixem Italia 2. Všechny nalezené nemutované a mutované alely jsou uvedeny v tabulkách 1 a 2. Pro zjištění jestli je detekovaná mutace heterozygótní nebo homozygótní je nutné testovat vzorek oběma mixy. Nepřímá detekce krátkých inzercí a delecí (indely) vyžaduje analýzu výsledků mixem Italia 1. Mix Italia 1 a Italia 2 zahrnují i analýzu dvou polymorfních short tandem repetice (STRs) (ID marker), které umožňují identifikaci obou mixů u analyzovaného vzorku. ID markery amplifikují STR markery na chromozomech 13 a 18 s využitím stejných primerů u obou mixů Italia 1 i Italia 2 (tabulky 6 a 7). Identifikační markery pro detekci pomíchání vzorků použité v kitu Devyser CFTR Italia v2 jsou identické jako ID markery použité ve všech kitech Devyser detekujících CFTR mutace. Zdravé (nemutované) alely PCR fragmenty zdravých DNA sekvencí detekujeme jako modré, zelené a žluté píky v elektroferogramu mixu Italia 1 (tabulka 6). Mutantní alely PCR fragmenty mutantních DNA sekvencí detekujeme jako modré, zelené a žluté píky v elektroferogramu mixu Italia 2 (tabulka 7). 8.4 Vyhodnocení Cutoff signály píků Doporučujeme, aby byl určen cutoff range pro každý přístroj. Nepoužívejte nižší cutoff hodnotu než 200 RFU (ABI 310 a 3130) a 500 RFU (ABI 3730 a 3500). Neanalyzujte vzorky, které mají píky na horní hranici detekce. Dále doporučujeme analyzovat jen takové vzorky, které mají signál ID markerů v mezích nad cutoff hodnotou a pod horní hranicí detekce. Pokud jsou signály ID markerů příliš nízké, tak může být DNA vzorku v PCR reakci příliš nízká. Pokud jsou signály ID markerů příliš vysoké, tak může být množství DNA vzorku v PCR reakci příliš vysoké. Nepřítomnost ID markerů ve vzorku ukazuje na selhání analýzy. Pokud mají ID markery velmi nízké nebo velmi vysoké RFU, měl by být vzorek analyzován s opatrností. Strana 16 z 34
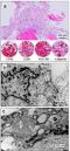
17 Sizing DNA fragmentů PCR fragmenty získané analýzou kitem Devyser CFTR Italia v2 analyzujte společně s ladderem 560 SIZER ORANGE a softwarem pro fragmentační analýzu (např. GeneMapper). Cross-mix ID markery PCR fragmenty reprezentující cross-mix sekvence ID markerů detekujeme jako červené píky v elektroferogramu v obou mixech Italia 1 a Italia 2. Identifikace cross-mix vzorků Délka cross-mix ID markerů detekovaných v mixech Italia 1 a Italia 2 u jednoho vzorku musí být srovnatelné. Každý vzorek musí mít identický profil ID markerů v mixech Italia 1 a Italia 2. Rozdílné ID markery v obou mixech u jednoho vzorku ukazují na pomíchání mixů z dvou různých vzorků. Nepřítomnost ID markerů ve vzorku ukazuje na selhání analýzy. Zdravé (nemutované) alely Vzorek je vyhodnocen jako zdravý (nemutovaný) pro danou alelu, pokud je pík této alely detekován v mixu Italia 1 a stejný pík příslušné alely není detekován v mixu Italia 2. Heterozygótní mutace Vzorek je vyhodnocen jako heterozygótní pro danou alelu, pokud jsou přítomny píky dané alely v obou mixech Italia 1 i Italia 2. Homozygótní mutace Vzorek je vyhodnocen jako homozygótně mutovaný pro danou alelu, pokud je pík této alely detekován v mixu Italia 2 a stejný pík příslušné alely není detekován v mixu Italia 1. Alel specifické výjimky Dele14b_17b/Dele17a_18 složený heterozygot Zdravé alely delecí Dele14b_17b a Dele17a_18 jsou amplifikovány pomocí společného páru primerů specifických pro sekvenci v intronu 19 (ref. název: intron 17) a produktem je fragment o délce 299 bp detekovaný v zelené barvě v panelu Italia 1. V případě složeného heterozygota s genotypem Dele14b_17b/Dele17a_18 nebo homozygótní delece, příslušný fragment zdravé alely nebude v panelu Italia 1 přítomen. Výskyt mutantního píku alely Dele14b_17b U PCR fragmentu CFTRdele14b-17b detekovaného v Italia 2 (Figure 1) se vyskytují stutter píky (píky navíc). Stutter píky pocházejí z co-amplifikace dvou dinukleotidů (2 bp repetice) short tandem repetice (STRs) přímo před zlomovým místem CFTRdele14b-17b v intronu 20 (ref. název: intron 17b). Absolutní délka detekovaných PCR fragmentů se bude lišit mezi jednotlivci v závislosti na skutečném počtu opakování v co-amplifikované STR. Strana 17 z 34
18 Obrázek 1. Bližší pohled na vzorek analyzovaný pomocí Devyser CFTR Italia 2 mix a nesoucí mutaci Dele14b_17b. Nepřímá detekce krátkých inzercí a delecí (indels) Mutace způsobené krátkými inzercemi a deleceni (indels) mezi dvěma protilehlými primery budou mít za následek změny velikosti u všech fragment produkovaných těmito primery. Indel mutace mohou být tedy nepřímo detekovány v Italia 1, přestože jsou přímo detekovány v Italia 2. Jeden příklad falešné mutace detekované v panelu Italia 1 najdete u obrázku 2 (1154insTC). Přesnou identitu detekovaných indels není možno určit pomocí kitu Devyser CFTR Italia v2. Doporučujeme, aby indels byly sekvenovány, aby bylo možno zjistit jejich přesnou identitu. Úplný seznam indel mutací nepřímo zjištěných v Italia 1 lze stáhnout v download sekci na adrese: Strana 18 z 34
19 Obrázek 2. Falešná delece 1154insTC způsobené posunem 2 bp size u R352 amplikonu (exon 8) v panelu Italia 1. Mutace v místě nasedání primeru a polymorfismy Mutace v místě nasedání primerů a polymorfismy mohou ovlivnit funkci jednotlivých PCR primerů použitých v kitu Devyser CFTR Italia v2. Úplný seznam mutací a polymorfismů, které nebyly konkrétně testovány kitem Devyser CFTR Italia v2 lze stáhnout v sekci download na adrese: Strana 19 z 34
20 Normální alely detekované v mixu Italia 1 Tabulka 6. Normální (zdravé) alely detekované v mixu Italia 1. Normální alely jsou uvedeny dle očekávané délky PCR fragmentů. Umístění CFTR genů uvedené v tabulce 6 je stejné jako uvádí databáze mutací cystické fibrózy 2. Použité názvy alel jsou odvozeny od původních názvů mutací a cdna uvedených v tabulce 7. Číslo Normální alela (Italia 1) Umístění v Pozice 2 cdna NM_ (HGVS) Barva píku Délka fragmentu (bp) 1 M1 Exon 1 c.1a Modrá P5 Exon 1 c.14c Modrá CFTRdele1-wt Promotor - Intron 1 - Modrá CFTR-dele2-wt Intron 2 - Modrá Q39 Exon 2 c.115c Modrá S549 Exon 12 c.1645a Modrá Q552 Exon 12 c.1654c Modrá del22-wt Exon 6 - Modrá D110 (c.330c) Exon 4 c.330c Modrá R1066 Exon 20 c.3197g Modrá D110 (c.328g) Exon 4 c.328g Modrá insA-wt Exon 9 - Modrá G1244 Exon 23 c.3731g Modrá c a Intron 11 c a c a 10 Modrá D1152 Exon 21 c.3454g Modrá delA-wt Exon 14 - Modrá G Intron 5 c.579+5g Zelená R352 Exon 8 c.1055g Zelená R1158 Exon 22 c.3472c Zelená G178 Exon 5 c.532g Zelená D579 Exon 13 c.1736a Zelená CFTRdele22,23-wt Intron 24 - Exon 25 - Zelená E585 Exon 13 c.1753g Zelená A Intron 13 c a Zelená delA-wt Exon 27 - Zelená insT-wt Exon 24 - Zelená Dele17a_18-wt Intron Dele14b_17b-wt Intron 19 - Zelená Dele2ins182-wt Intron 1 - Žlutá Dele22_24-wt Intron 24 - Žlutá G1349 Exon 25 c.4046g Žlutá 213 ID1 ID marker 1 Chr Červená ID2 ID marker 2 Chr Červená Úplný seznam indel mutaci, které ovlivňují délku fragmentů a byly detekovány v Italia 1 lze stáhnout v sekci download na adrese: Strana 20 z 34
21 Velikost fragmentů alel se může při elektroforéze lišit v závislosti na přístroji, typu použitého polymeru, na typu použitého size markeru. Délky fragmentů alel uvedených v této tabulce jsou založeny na pozorovaných délkách fragmentů získaných pomocí ABI 3500, POP-7 polymeru a 560 SIZER ORANGE. Normální (zdravé) alely detekované v mixu Italia 2. Tabulka 7. Mutantní alely detekované v mixu Italia 2. Mutantní alely jsou uvedeny dle očekávané délky PCR fragmentů. Použité názvy mutací a cdna uvedených v tabulce 7 jsou uvedeny v souladu se seznamem CFTR2 mutací 8. Pokud není uvedena jiná reference, je umístění CFTR genů uvedené v tabulce 7 stejné jako uvádí databáze mutací cystické fibrózy 2. Mutation legacy name (Italia 2) 8 Umístění v pozice 2 Příslušná normální alela v mixu Italia 1 cdna 8 Barva píku Délka fragmentu (bp) M1V Exon 1 1 c.1a>g Modrá 124 P5L 2 Exon 1 2 c.14c>t Modrá 140 CFTR-dele2 2, Intron 1 4 c _ del2875 Modrá 218 Q39X Exon 2 5 c.115c>t Modrá 251 Dele17a_18 9 Intron 18 - Intron c _ del 9 Modrá 257 S549R(A->C) 2, Exon 12 6 c.1645a>c Modrá 274 Q552X Exon C>T Modrá del22 Exon 6 8 c.720_741del AGGGAGAATGATGATGAAGTAC Modrá 294 CFTRdele1 2 Exon 1 3 c.4_53+69delins299 Modrá 308 D110E 2 Exon 4 9 c.330c>a Modrá 338 R1066H Exon c.3197g>a Modrá 354 D110H Exon 4 11 c.328g>c Modrá 365 G1244E Exon c.3731g>a Modrá 406 c a>g 10 Intron c a>g c a>g 10 Modrá insA Exon 9 12 c.1127_1128insa Modrá 479 D1152H Exon c.3454g>c Modrá delA Exon c.2052dela Modrá G->A Intron 5 17 c.579+5g>a Zelená 124 R352Q Exon 8 18 c.1055g>a Zelená 142 R1158X Exon c.3472c>t Zelená 159 G178R Exon 5 20 c.532g>a Zelená 167 D579G Exon c.1736a>g Zelená 214 E585X Exon c.1753g>t Zelená A->G Intron c a>g Zelená 241 CFTRdele22,23 Intron 24 - Intron c _ del Zelená delA Exon c.4251dela Zelená insT Exon c.3884_3885inst Zelená 276 Strana 21 z 34
22 Dele14b_17b 9 Intron 15 - Intron 20 Dele2ins182 11,12 Intron 1 - Intron 2 Dele22_24 9 Intron 24-3'UTR 28 c _ del 9 Zelená c _ del8108 ins182 11,12 Žlutá c _*3143del instaact 9 Žlutá 204 G1349D Exon c.4046g>a Žlutá 213 ID marker 1 Chr. 13 ID1 Chromosome 13 Červená ID marker 2 Chr. 18 ID2 Chromosome 18 Červená Detekce mutací byla ověřena pomocí klonování DNA sekvencí, které odpovídají těmto konkrétním mutacím. Detekce mutací nebyla potvrzena pomocí lidské genomové DNA z klinického vzorku s mutací. Detekce mutací byla ověřena pomocí klonování DNA sekvencí, které odpovídají těmto konkrétním mutacím. Detekce mutací nebyla potvrzena pomocí lidské genomové DNA z klinického vzorku s mutací. Název cdna byl získán dle doporučení HGVS. Skutečná délka a počet píků detekovaných u Dele14b_17b se mohou lišit mezi jednotlivci v důsledku přítomnosti dvou dinukleotidů STR v amplifikované oblasti (viz obrázek 1 a reference 13). Velikost fragmentů alel se může při elektroforéze lišit v závislosti na přístroji, typu použitého polymeru, na typu použitého size markeru. Délky fragmentů alel uvedených v této tabulce jsou založeny na pozorovaných délkách fragmentů získaných pomocí ABI 3500, POP-7 polymeru a 560 SIZER ORANGE. Troubleshooting Pokud je elektroferogram nízké kvality, data není možné vyhodnotit. PCR produkt můžeme opakovaně nanést do analyzátoru a analyzovat znovu. Výskyt neprůkazných výsledků, je možný z mnoha důvodů:» Překryv barevného signálu mezi kanály» Elektroforetické spiky» Kontaminace DNA: druhý genotyp, PCR amplikony» Koncentrace DNA je příliš vysoká, nebo příliš nízká.» DNA použitá v PCR je degradovaná. Artefakty PCR Stutter píky (obr. 3) jsou detekovány jako samostatné píky, které jsou o jednu nebo několik repetic menší, než aktuální STR alela. Typický stutter pík má obsah menší, než 15% vůči příslušnému STR píku. Obrázek 3. Stutter pík je označen šipkou. Strana 22 z 34
23 -A píky (obr. 4) jsou detekovány jako samostatné píky, které jsou o jeden pár bazí kratší, než PCR produkt s plnou délkou (+A pík). Obrázek 4. -A a +A píky jsou vyznačeny šipkami. Elektroforetické artefakty Průsvity mezi všemi použitými barevnými kanály, které je možné detekovat (obrázek 5.1 a 5.2). Crosstalk se jeví jako stejně vysoké vrcholy v sousedních barevných kanálech a měla by být vyloučena z analýzy. Obrázek 5.1 Průsvit z červeného do žlutého kanálu (barevné kanály jsou ukázány odděleně). Obrázek 5.2 Průsvit ze zeleného do modrého kanálu označený šipkou (překryté barevné kanály). Strana 23 z 34
24 Dye blobs se mohou objevit v rozsahu analýzy (Obr. 6). Obecně platí, že barva dye blobs se objeví jako široký pík bez definovaného vrcholu jedné barvy a vyskytují se v datech relativně brzy na začátku. Obrázek 6. Dye blob označený šipkou. Copy number varianty Identifikační ID markery použité v Devyser CFTR Italia v2 jsou vysoce polymorfní markery, které mohou zobrazit copy number variace (CNVs). CNVs detekované Devyser CFTR Italia v2 by měly být použity pouze pro identifikaci vzorku, a nikoli jako diagnostické markery pro detekci aneuploidie. Obrázek 7 zobrazuje ne-patologickou detekci CNV v ID1. Obrázek 7. Ne-patologická CNV detovaná v ID1 Strana 24 z 34
25 9. VÝKONOSTNÍ CHARAKTERISTIKY Sensitivita Definice: Podíl (%) jedinců s dobře definovaným genetickým onemocněním (mutovaná alela CFTR) a jejichž testované kladné hodnoty v rámci definované rozhodovací meze. Design experimentu: Bylo testováno třicet pět (35) vzorků DNA nesoucích celkem 38 mutací specifických pro Devyser CFTR Italia v2. Vzorky byly předem otestovány jinou používanou metodou. Poznámka: Detekce mutací CFTR-dele2, S549R(A->C), 1259insA a R1066H byla validována s použitím klonovaných DNA sekvencí specificky odpovídajících daným mutacím. Detekce mutací S549R(A->C), 1259insA a R1066H byla potvrzena s použitím lidské genomové DNA z klinických vzorků. Detekce mutace CFTR-dele2 nebyla potvrzena s použitím lidské genomové DNA z klinických vzorků. Výsledek: Kitem Devyser CFTR Italia v2 byly všechny mutace správně identifikovány, a proto je korelace výsledků 100%. > 97 % sensitivita. Specificita Definice: Podíl (%) jedinců, kteří nemají dobře definované genetické onemocnění (nemutované CFTR alely) a jejichž výsledky testu jsou negativní nebo ve vymezené rozhodovací mezi. Design experimentu: Sto deset (110) dárců krve bylo slepě testováno s použitím kitu Devyser CFTR Italia v2. Výsledek: Všechny vzorky daly interpretovatelné výsledky, které splňují kritéria pro interpretaci výsledků. U 109 ze 110 analyzovaných vzorků nebyla kitem Devyser CFTR Italia v2 zachycena žádná mutace. Jeden (1) vzorek byl heterozygótní pro deleci Dele22_24. Tento výsledek byl ověřen jinou zavedenou metodou. Potvrzená delece Dele22_24 byla z výpočtu specificity vyloučena. > 99 % specifita. Strana 25 z 34
26 Cross-Reaktivita Byl nalezen a kitem Devyser CFTR Italia v2 otestován jeden (1) vzorek s potvrzenými CFTR mutacemi (711+5G>T;T/711+1G>T) lokalizovanými v sekvenci primeru použitého v Devyser CFTR Italia v2. Následující cross reaktivity vyly pozorovány při použití kitu Devyser CFTR Italia v2: 1. Přítomnost heterozygótní mutace 711+1G>T může vést k redukci signálu fragmentu 711+5G v Italia Přítomnost homozygótní mutace 711+1G>T může vést k ztrátě fragmentu alely 711+5G v Italia Přítomnost složené mutace 711+5G>T/711+1G>T může vést k interpretaci vzorku jako homozygótního pro mutaci 711+5G>T, protože může dojít ke ztrátě fragmentu normální alely 711+5G v Italia 1. Strana 26 z 34
27 10. LIMITACE POSTUPU A. Používat tento product smí jen osoba vyškolená v technikách PCR a kapilární elektroforézy. B. Kit Devyser CFTR Italia v2 byl validován s použitím Life Technologies/Thermo Fisher Scientific Veriti Thermal cycler. Pokud chcete pro klinickou diagnostiku použít jiný termocykler, je nutná validace soupravy Devyser CFTR Italia v2 pro tento cykler. C. Kit Devyser CFTR Italia v2 byl validován s použitím QIAamp DNA Blood Mini Kit a QIAsymphony DSP DNA Midi Kit pro extrakci DNA z lidské krve (EDTA) a s použitím QIAamp DNA Blood Mini Kit pro extrakci DNA ze suché kapky krve. Další extrakční soupravy nebyly dostatečně validovány a mohou vést k falešně negativním nebo falešně pozitivním výsledkům. D. Devyser CFTR Italia v2 kit musí být používán pouze pro detekci specifických mutací v lidském CFTR genu v souladu s manuálem. Existuje mnoho jiných mutací v genu CFTR, které kit Devyser CFTR Italia v2 nemusí detekovat. Kit nebyl validován pro diagnózu cystické fibrózy. Výsledky získané kitem Devyser CFTR Italia v2 mohou být přímo použity pro konkrétní testovaný vzorek tkáně a materiál. Strana 27 z 34
28 11. UPOZORNĚNÍ KUPUJÍCÍMU Výsledky obdržené pomocí soupravy Devyser CFTR Italia v2 musí být interpretovány s přihlédnutím k dalším laboratorním výsledkům a klinickému obrazu pacienta. Devyser AB nezodpovídá za následná klinická rozhodnutí. LIZ a GeneAmp jsou registrovanými obchodními známkami společnosti Life Technologies Corporation. GeneScan, POP-7 a Hi-Di jsou ochrannými známkami společnosti Life Technologies Corporation. Koupí tohoto produktu nezískáváte licenci k provádění PCR podléhající patentům vlastněným třetí stranou. Strana 28 z 34
29 12. REFERENCE 1 Kerem B, Rommens JM, Buchanan JA, Markiewicz D, Cox TK, Chakravarti A, Buchwald M, and Tsui LC. Identification of the Cystic Fibrosis Gene: Genetic Analysis. Science 1989; 245 (4922): Cystic Fibrosis Mutation Database, Revised Cited Bombieri C, Claustres M, De Boeck K, Derichs N, Dodge J, Girodon E, Sermet I, Schwarz M, Tzetis M, Wilschanski M, Bareil C, Bilton D, Castellani C, Cuppens H, Cutting GR, Drevínek P, Farrell P, Elborn JS, Jarvi K, Kerem B, Kerem E, Knowles M, Macek M Jr, Munck A, Radojkovic D, Seia M, Sheppard DN, Southern KW, Stuhrmann M, Tullis E, Zielenski J, Pignatti PF, Ferec C. Recommendations for the classification of diseases as CFTR-related disorders. J Cyst Fibros Jun; 10 Suppl 2:S Southern KW. Cystic fibrosis and formes frustes of CFTR-related disease. Respiration 2007; 74 (3): Watson MS, Cutting GR, Desnick RJ, Driscoll DA, Klinger K, Mennuti M, Palomaki GE, Popovich BW, Pratt VM, Rohlfs EM, Strom CM, Richards CS, Witt DR, Grody WW. "Cystic fibrosis population carrier screening: 2004 revision of American College of Medical Genetics mutation panel."genet Med. 2004; 6(5): Reaffirmed Schwarz M, Gardner A, Jenkins L, Norbury G, Renwick P, Robinson D. Testing Guidelines for molecular diagnosis of Cystic Fibrosis. Guidelines ratified by the UK Clinical Molecular Genetics Society (13 th July, 2009). 7 Castellani C, Southern KW, Brownlee K, Dankert Roelse J, Duff A, Farrell M, Mehta A, Munck A, Pollitt R, Sermet-Gaudelus I, Wilcken B, Ballmann M, Corbetta C, de Monestrol I, Farrell P, Feilcke M, Férec C, Gartner S, Gaskin K, Hammermann J, Kashirskaya N, Loeber G, Macek M, Mehta G, Reiman A, Rizzotti R, Sammon A, Sands D, Smyth A, Sommerburg O, Torresani T, Travert G, Vernooij A, Elborn S. European best practice guidelines for cystic fibrosis neonatal screening. J Cyst Fibros May; 8(3): List of CFTR2 mutations, Date: 27 February Clinical and Functional Translation of CFTR (CFTR2); available at 9 Tomaiuolo R, Sangiuolo F, Bombieri C, Bonizzato A, Cardillo G, Raia V, D'Apice M.R, Bettin, M.D, Pignatti P.F, Castaldo G, Novelli G. Epidemiology and a novel procedure for large scale analysis of CFTR rearrangements in classic and atypical CF patients: A multicentric Italian study. J Cyst Fibros Sept; 7: Costantino L, Rusconi D, Solda G, Seia M, Paracchini V, Porcaro L, Asselta R, Colombo C,Duga S. Fine Characterization of the Recurrent c a>g Deep-Intronic Mutation in the Cystic Fibrosis Transmembrane Conductance Regulator Gene. Am J Respir Cell Mol Biol May; 48: Taulan M, Girardet A, Guittard C, Altieri J-P, Templin C, Beroud C, des Georges M, Claustres M. Large genomic rearrangements in the CFTR gene contribute to CBAVD. BMC Med Genet Apr; 8:22. Strana 29 z 34
30 12 Férec C, Casals T, Chuzhanova N, Macek Jr M, Bienvenu T, Holubova A, King C, McDevitt T, Castellani C, Farrell PM, Sheridan M, Pantaleo S-J, Loumi O, Messaoud T, Cuppens H, Torricelli F, Cutting GR, Williamson R, Alonso Ramos MJ, Franco Pignatti P, Rague ne`s, O, Cooper DN, Audre zet M-P, Chen J-M. Gross genomic rearrangements involving deletions in the CFTR gene: characterization of six new events from a large cohort of hitherto unidentified cystic fibrosis chromosomes and meta-analysis of the underlying mechanisms. Eur J Hum Genet May; 14 (5): Zielenski J, Markiewicz D, Rininsland F, Rommens J, Tsui LC. A cluster of highly polymorphic dinucleotide repeats in intron 17b of the cystic fibrosis transmembrane conductance regulator (CFTR) gene. Am J Hum Genet Dec; 49(6): Human Genome Variation Society Nomenclature for the description of sequence, Revised Cited Strana 30 z 34
31 13. KONTAKTNÍ INFORMACE Devyser AB Instrumentvägen 19 SE Hägersten ŠVÉDSKO Telefon: Homepage: Technická podpora Phone: Strana 31 z 34
32 14. HISTORIE REVIZÍ Tento pøeklad referenèní anglické verze byl publikován Verze Redakční změny Odstavec 6 Přidání Qubit dsdna HS Assay Kit cat.# Q32854 Odstavec 7 Změna v doporučení o použití Italia 1 a Italia 2 v kapitole 7.2 Přidání vzorku Odstavec 8 Byla přidána informace o použití mixu Italia 1 v kapitole 8.3 Verze Redakční změny Odstavec 4 Aktualizace linku pro download kalibrace Dye Setu Odstavec 8 Aktualizace linku pro download mutací Aktualizace sekce o Elektroforetických artefaktech, která specifikuje průsvity, které mohou nastat u všech použitých berevných kanálů. Byl přidán obrázek 5.1, který ukazuje příklad průsvitu z červeného do žlutého kanálu. Název obrázku 5 "Obrázek 5. Průsvitový pík (ze zeleného do modrého kanálu) označeného šipkou" bylo změněno na: "Obrázek 5.2 Průsvit ze zeleného do modrého kanálu označený šipkou (překryté barevné kanály)." Byla přidána sekce o Copy number variantách Odstavec 8, Tabulka 7 Délka fragment alely 711+5G->A byl změněna z 120 bp na 124 bp. Strana 32 z 34
33 Verze Tabulka 8. Update v kitu Devyser CFTR Italia v2, Italia 1. Normální alela Barva píku v2 Barva píku v1 Délka fragmentu (bp) v2 Délka fragmentu (bp) v1 Změny ve verzi v2 M1 Modrá Zelená Barva píku P5 Modrá Zelená Barva píku CFTRdele1-wt Modrá Zelená Barva píku CFTR-dele2-wt Modrá Modrá Délka fragmentu* 852del22-wt Modrá Nový D110 (c.330c) Modrá Zelená Barva píku D110 (c.328g) Modrá Zelená Barva píku 1259insA-wt Modrá Nový c a Modrá Nový 711+5G Zelená Modrá Barva píku R352 Zelená Modrá Barva píku G178 Zelená Modrá Barva píku Dele2ins182-wt Žlutá Zelená Barva píku Dele22_24-wt Žlutá Modrá Barva píku L997 - Modrá Vyloučené G1349 Žlutá Nový *CFTR-dele2-wt v Italia 1 byla upravena tak, aby se zabránilo nepřímé detekci c del a c delt. Strana 33 z 34
34 Tabulka 9. Update v kitu Devyser CFTR Italia v2, Italia 2. Mutantní alela Název Barva píku v2 Barva píku v1 Délka fragmentu (bp) v2 Délka fragmentu (bp) v1 Změny ve verzi v2 M1V Modrá Zelená Barva píku P5L Modrá Zelená Barva píku L997F - Modrá Vyloučené Dele17a_18 Modrá Zelená Barva píku 852del22 Modrá Nový CFTRdele1 Modrá Zelená Barva píku D110E Modrá Zelená Barva píku D110H Modrá Zelená Barva píku c a>g Modrá Nový 1259insA Modrá Nový 711+5G->A Zelená Modrá Barva píku R352Q Zelená Modrá Barva píku G178R Zelená Modrá Barva píku Dele14b_17b Zelená Zelená Rozsah Dele2ins182 Žlutá Zelená Barva píku Dele22_24 Žlutá Modrá Barva píku G1349D Žlutá Nový Strana 34 z 34
Devyser CFTR Core. Návod k použití
 Devyser CFTR Core Kat. č.: 8-A031 Pro in vitro diagnostiku Návod k použití Strana 1 z 38 OBSAH OBSAH 2 1. SEZNÁMENI SE SYSTÉMEM DEVYSER CORE 4 Použití 4 Obsah soupravy 4 Postup 4 Background 4 Princip metody
Devyser CFTR Core Kat. č.: 8-A031 Pro in vitro diagnostiku Návod k použití Strana 1 z 38 OBSAH OBSAH 2 1. SEZNÁMENI SE SYSTÉMEM DEVYSER CORE 4 Použití 4 Obsah soupravy 4 Postup 4 Background 4 Princip metody
Devyser AZF. Návod k použití
 Devyser AZF Kat.č. 8-A019 Pro in vitro diagnostiku Návod k použití Devyser AZF, Návod k použití, 7-A012-CZ, May-2012 Strana 1 z 20 Devyser AZF, Návod k použití, 7-A012-CZ, May-2012 Strana 2 z 20 Obsah
Devyser AZF Kat.č. 8-A019 Pro in vitro diagnostiku Návod k použití Devyser AZF, Návod k použití, 7-A012-CZ, May-2012 Strana 1 z 20 Devyser AZF, Návod k použití, 7-A012-CZ, May-2012 Strana 2 z 20 Obsah
Devyser UPD-15, Návod k použití, 7-A016-CS, verze Strana 1 z 19 Devyser AB
 č Devyser UPD-15, Návod k použití, 7-A016-CS, verze 2015-05-21 Strana 1 z 19 Obsah Strana 1. Seznámení se systémem Devyser UPD-15 3 2. Upozornění 4 3. Symboly použité na štítcích 5 4. Požadovaný materiál
č Devyser UPD-15, Návod k použití, 7-A016-CS, verze 2015-05-21 Strana 1 z 19 Obsah Strana 1. Seznámení se systémem Devyser UPD-15 3 2. Upozornění 4 3. Symboly použité na štítcích 5 4. Požadovaný materiál
Návod k použití. Devyser Resolution 13 v2 Kat. No.: 8-A Devyser Resolution XY v2 Kat. No.: 8-A012.2-XY. For in vitro Diagnostic Use
 Devyser Resolution 21 v2 Kat. No.: 8-A012.2-21 Devyser Resolution 18 v2 Kat. No.: 8-A012.2-18 Devyser Resolution 13 v2 Kat. No.: 8-A012.2-13 Devyser Resolution XY v2 Kat. No.: 8-A012.2-XY For in vitro
Devyser Resolution 21 v2 Kat. No.: 8-A012.2-21 Devyser Resolution 18 v2 Kat. No.: 8-A012.2-18 Devyser Resolution 13 v2 Kat. No.: 8-A012.2-13 Devyser Resolution XY v2 Kat. No.: 8-A012.2-XY For in vitro
MagPurix Blood DNA Extraction Kit 200
 MagPurix Blood DNA Extraction Kit 200 Kat. č. ZP02001-48 Doba zpracování: 50-60 minut pro MagPurix 12S 50-70 minut pro MagPurix 24 Použití Souprava MagPurix Blood DNA Extraction Kit 200 je určena pro izolátor
MagPurix Blood DNA Extraction Kit 200 Kat. č. ZP02001-48 Doba zpracování: 50-60 minut pro MagPurix 12S 50-70 minut pro MagPurix 24 Použití Souprava MagPurix Blood DNA Extraction Kit 200 je určena pro izolátor
α-globin StripAssay Kat. číslo 4-160 10 testů 2-8 C
 α-globin StripAssay Kat. číslo 4-160 10 testů 2-8 C Popis stripů: Pracovní postup Izolace DNA Doporučujeme použít následující kit pro izolaci DNA z plné krve nebo jiných typů vzorků: Spin Micro DNA Extraction
α-globin StripAssay Kat. číslo 4-160 10 testů 2-8 C Popis stripů: Pracovní postup Izolace DNA Doporučujeme použít následující kit pro izolaci DNA z plné krve nebo jiných typů vzorků: Spin Micro DNA Extraction
Yi TPMT. Diagnostická souprava. Návod k použití. Haasova 27 Brno Česká republika. tel.:
 Yi TPMT Diagnostická souprava Návod k použití Výrobce: YBUX s.r.o. Haasova 27 Brno 616 00 Česká republika IČ 63487951 tel.: +420 541 423 710 e-mail: ybux@ybux.eu Název: Yi TPMT Popis: Diagnostická souprava
Yi TPMT Diagnostická souprava Návod k použití Výrobce: YBUX s.r.o. Haasova 27 Brno 616 00 Česká republika IČ 63487951 tel.: +420 541 423 710 e-mail: ybux@ybux.eu Název: Yi TPMT Popis: Diagnostická souprava
nastavení real-time PCR cykleru Rotor Gene 3000
 Verze: 1.4 Datum poslední revize: 25. 3. 2015 nastavení real-time PCR cykleru Rotor Gene 3000 (Corbett Research) generi biotech OBSAH: 1. Nastavení teplotního profilu a spuštění cykleru... 3 2. Zadání
Verze: 1.4 Datum poslední revize: 25. 3. 2015 nastavení real-time PCR cykleru Rotor Gene 3000 (Corbett Research) generi biotech OBSAH: 1. Nastavení teplotního profilu a spuštění cykleru... 3 2. Zadání
EGFR XL StripAssay. Kat. číslo 5-630. 20 testů 2-8 C
 EGFR XL StripAssay Kat. číslo 5-630 20 testů 2-8 C Popis stripu Pracovní postup 1. Izolace DNA Pro izolaci DNA použijte vhodný izolační kit. Doporučené kity jsou následující: Pro izolaci čerstvých nebo
EGFR XL StripAssay Kat. číslo 5-630 20 testů 2-8 C Popis stripu Pracovní postup 1. Izolace DNA Pro izolaci DNA použijte vhodný izolační kit. Doporučené kity jsou následující: Pro izolaci čerstvých nebo
NRAS StripAssay. Kat. číslo 5-610. 20 testů 2-8 C
 NRAS StripAssay Kat. číslo 5-610 20 testů 2-8 C Popis stripu: Pracovní postup 1. Izolace DNA Pro izolaci DNA musí být použita vhodná metoda vzhledem k typu tkáně vzorku. Pro doporučení vhodné metody kontaktujte
NRAS StripAssay Kat. číslo 5-610 20 testů 2-8 C Popis stripu: Pracovní postup 1. Izolace DNA Pro izolaci DNA musí být použita vhodná metoda vzhledem k typu tkáně vzorku. Pro doporučení vhodné metody kontaktujte
Braf V600E StripAssay
 Braf V600E StripAssay Kat. číslo 5-570 20 testů 2-8 C Popis stripu: Pracovní postup 1. Izolace DNA Pro izolaci čerstvých nebo mražených biopsií použijte soupravy Qiagen QIAmp DNA Mini nebo Micro. Pro izolaci
Braf V600E StripAssay Kat. číslo 5-570 20 testů 2-8 C Popis stripu: Pracovní postup 1. Izolace DNA Pro izolaci čerstvých nebo mražených biopsií použijte soupravy Qiagen QIAmp DNA Mini nebo Micro. Pro izolaci
MagPurix Forensic DNA Extraction Kit
 MagPurix Forensic DNA Extraction Kit Kat. č. ZP02010 Doba zpracování: 40-50 minut pro MagPurix 12S 40-60 minut pro MagPurix 24 Použití Souprava MagPurix Forensic DNA Extraction Kit je určena pro izolátor
MagPurix Forensic DNA Extraction Kit Kat. č. ZP02010 Doba zpracování: 40-50 minut pro MagPurix 12S 40-60 minut pro MagPurix 24 Použití Souprava MagPurix Forensic DNA Extraction Kit je určena pro izolátor
cdna synthesis kit First-Strand cdna Synthesis System Verze 1.2
 cdna synthesis kit First-Strand cdna Synthesis System Verze 1.2 Obsah soupravy a její skladování Tato souprava pro reverzní transkripci obsahuje reagencie potřebné k provedení reverzní transkripce (RT)
cdna synthesis kit First-Strand cdna Synthesis System Verze 1.2 Obsah soupravy a její skladování Tato souprava pro reverzní transkripci obsahuje reagencie potřebné k provedení reverzní transkripce (RT)
Systém pro kvantitativní multiplex amplifikaci DNA PLEXAMP KIT. PXT5 Detekce genomové přestavby genu BRCA2 NÁVOD K POUŽITÍ
 Systém pro kvantitativní multiplex amplifikaci DNA PLEXAMP KIT PXT5 Detekce genomové přestavby genu BRCA2 NÁVOD K POUŽITÍ REFERENCE: PXT5-01.01.25: 25 testů PXT5-01.01.50: 50 testů PXT5-01.01.100: 100
Systém pro kvantitativní multiplex amplifikaci DNA PLEXAMP KIT PXT5 Detekce genomové přestavby genu BRCA2 NÁVOD K POUŽITÍ REFERENCE: PXT5-01.01.25: 25 testů PXT5-01.01.50: 50 testů PXT5-01.01.100: 100
Elucigene CF-EU2v1 Návod k použití
 Elucigene CF-EU2v1 Návod k použití Kat. kód: CF2EUB2 50 testů CF2EUBX 10 testů Pro diagnostické použití in vitro Vyrobeno společností Elucigene Diagnostics. Greenheys House Pencroft Way Manchester Science
Elucigene CF-EU2v1 Návod k použití Kat. kód: CF2EUB2 50 testů CF2EUBX 10 testů Pro diagnostické použití in vitro Vyrobeno společností Elucigene Diagnostics. Greenheys House Pencroft Way Manchester Science
Braf 600/601 StripAssay
 Braf 600/601 StripAssay Kat. číslo 5-560 20 testů 2-8 C Popis stripu: Pracovní postup Kit umožňuje detekci 9 mutací v genu BRAF (kodón 600 a 601) Další informace najdete v OMIM Online Mendelian Inheritance
Braf 600/601 StripAssay Kat. číslo 5-560 20 testů 2-8 C Popis stripu: Pracovní postup Kit umožňuje detekci 9 mutací v genu BRAF (kodón 600 a 601) Další informace najdete v OMIM Online Mendelian Inheritance
Genetický polymorfismus jako nástroj identifikace osob v kriminalistické a soudnělékařské. doc. RNDr. Ivan Mazura, CSc.
 Genetický polymorfismus jako nástroj identifikace osob v kriminalistické a soudnělékařské praxi doc. RNDr. Ivan Mazura, CSc. Historie forenzní genetiky 1985-1986 Alec Jeffreys a satelitní DNA 1980 Ray
Genetický polymorfismus jako nástroj identifikace osob v kriminalistické a soudnělékařské praxi doc. RNDr. Ivan Mazura, CSc. Historie forenzní genetiky 1985-1986 Alec Jeffreys a satelitní DNA 1980 Ray
CVD-T StripAssay. Kat. číslo 4-360. 20 testů 2-8 C
 CVD-T StripAssay Kat. číslo 4-360 20 testů 2-8 C Popis stripu Pracovní postup Izolace DNA Použijte čerstvou nebo zmraženou krev s EDTA nebo citrátem, jako antikoagulans, vyhněte se krvi s obsahem heparinu.
CVD-T StripAssay Kat. číslo 4-360 20 testů 2-8 C Popis stripu Pracovní postup Izolace DNA Použijte čerstvou nebo zmraženou krev s EDTA nebo citrátem, jako antikoagulans, vyhněte se krvi s obsahem heparinu.
NOVÁ VERZE. Systém pro kvantitativní multiplex amplifikaci DNA PLEXAMP KIT. PXT3 Detekce genomové přestavby genů MSH2 a MSH6 NÁVOD K POUŽITÍ
 NOVÁ VERZE Systém pro kvantitativní multiplex amplifikaci DNA PLEXAMP KIT PXT3 Detekce genomové přestavby genů MSH2 a MSH6 NÁVOD K POUŽITÍ REFERENCE: PXT3-02.01.25: 25 testů PXT3-02.01.50: 50 testů PXT3-02.01.100:
NOVÁ VERZE Systém pro kvantitativní multiplex amplifikaci DNA PLEXAMP KIT PXT3 Detekce genomové přestavby genů MSH2 a MSH6 NÁVOD K POUŽITÍ REFERENCE: PXT3-02.01.25: 25 testů PXT3-02.01.50: 50 testů PXT3-02.01.100:
DYNEX nabízí komplexní řešení v oblasti zpracování a analýzy biologických materiálů pomocí molekulárně biologických metod.
 DYNEX nabízí komplexní řešení v oblasti zpracování a analýzy biologických materiálů pomocí molekulárně biologických metod. Od 1.1.2014 DYNEX jediným OFICIÁLNÍM (autorizovaným) distributorem společnosti
DYNEX nabízí komplexní řešení v oblasti zpracování a analýzy biologických materiálů pomocí molekulárně biologických metod. Od 1.1.2014 DYNEX jediným OFICIÁLNÍM (autorizovaným) distributorem společnosti
Uživatelská příručka
 PGM Barcoding Set 1-8 Navrženo pro PGM ION-TORRENT KÓD PRODUKTU: 2001 (1-8) BALEN9: 32 testů Uživatelská příručka Rev02.2015 Str. 1 Rejstřík 1. POUŽITÍ VÝROBKU 3 2. OBSAH KITU 4 3. SKLADOVÁNÍ 4 4. STABILITA
PGM Barcoding Set 1-8 Navrženo pro PGM ION-TORRENT KÓD PRODUKTU: 2001 (1-8) BALEN9: 32 testů Uživatelská příručka Rev02.2015 Str. 1 Rejstřík 1. POUŽITÍ VÝROBKU 3 2. OBSAH KITU 4 3. SKLADOVÁNÍ 4 4. STABILITA
Jednotné pracovní postupy zkoušení krmiv
 Národní referenční laboratoř Strana KVANTITATIVNÍ STANOVENÍ GENETICKÝCH MODIFIKACÍ METODOU qpcr POMOCÍ ROTOR-GENE PROBE PCR KITU Účel a rozsah Postup slouží ke kvantitativnímu stanovení genetických modifikací
Národní referenční laboratoř Strana KVANTITATIVNÍ STANOVENÍ GENETICKÝCH MODIFIKACÍ METODOU qpcr POMOCÍ ROTOR-GENE PROBE PCR KITU Účel a rozsah Postup slouží ke kvantitativnímu stanovení genetických modifikací
Kras XL StripAssay. Kat. číslo 5-680. 20 testů 2-8 C
 Kras XL StripAssay Kat. číslo 5-680 20 testů 2-8 C Popis stripu: Pracovní postup 1. Izolace DNA Musí být použity vhodné metody extrakce DNA, v závislosti na typu vzorku, který má být vyšetřován. Doporučení
Kras XL StripAssay Kat. číslo 5-680 20 testů 2-8 C Popis stripu: Pracovní postup 1. Izolace DNA Musí být použity vhodné metody extrakce DNA, v závislosti na typu vzorku, který má být vyšetřován. Doporučení
CYCLER CHECK. Test pro validaci teplotní uniformity cyklérů. Připraveno k použití, prealiquotováno. REF 7104 (10 testů) REF (4 testy)
 CZ Návod k použití CYCLER CHECK Test pro validaci teplotní uniformity cyklérů Připraveno k použití, prealiquotováno REF 7104 (10 testů) REF 71044 (4 testy) Obsah 1. Popis výrobku... 2 2. Materiál... 3
CZ Návod k použití CYCLER CHECK Test pro validaci teplotní uniformity cyklérů Připraveno k použití, prealiquotováno REF 7104 (10 testů) REF 71044 (4 testy) Obsah 1. Popis výrobku... 2 2. Materiál... 3
MagPurix Viral Nucleic Acid Extraction Kit
 MagPurix Viral Nucleic Acid Extraction Kit Kat. č. ZP02003 Doba zpracování: 40-55 minut pro MagPurix 12S 40-60 minut pro MagPurix 24 Použití Souprava MagPurix Viral Nucleic Acid Extraction Kit je určena
MagPurix Viral Nucleic Acid Extraction Kit Kat. č. ZP02003 Doba zpracování: 40-55 minut pro MagPurix 12S 40-60 minut pro MagPurix 24 Použití Souprava MagPurix Viral Nucleic Acid Extraction Kit je určena
FastFraX TM FMR1 Sizing kit
 FastFraX TM FMR1 Sizing Kit Katalogové číslo: F2-050-V Manuál Pro In vitro diagnostiku Skladování: 2-8 C pro okamžité použití -20 C pro dlouhodobé skladování Chraňte před světlem 1. Úvod Syndrom fragilního
FastFraX TM FMR1 Sizing Kit Katalogové číslo: F2-050-V Manuál Pro In vitro diagnostiku Skladování: 2-8 C pro okamžité použití -20 C pro dlouhodobé skladování Chraňte před světlem 1. Úvod Syndrom fragilního
Verze: 1.2 Datum poslední revize: 24.9.2014. Nastavení real-time PCR cykleru. Light Cycler 480 Instrument. (Roche) generi biotech
 Verze: 1.2 Datum poslední revize: 24.9.2014 Nastavení real-time PCR cykleru Light Cycler 480 Instrument (Roche) generi biotech OBSAH 1. Nastavení teplotního profilu...3 1.1. Nastavení nového teplotního
Verze: 1.2 Datum poslední revize: 24.9.2014 Nastavení real-time PCR cykleru Light Cycler 480 Instrument (Roche) generi biotech OBSAH 1. Nastavení teplotního profilu...3 1.1. Nastavení nového teplotního
DIAGNOSTICKÝ KIT PRO DETEKCI MINIMÁLNÍ REZIDUÁLNÍ CHOROBY U KOLOREKTÁLNÍHO KARCINOMU
 Úvod IntellMed, s.r.o., Václavské náměstí 820/41, 110 00 Praha 1 DIAGNOSTICKÝ KIT PRO DETEKCI MINIMÁLNÍ REZIDUÁLNÍ CHOROBY U KOLOREKTÁLNÍHO KARCINOMU Jednou z nejvhodnějších metod pro detekci minimální
Úvod IntellMed, s.r.o., Václavské náměstí 820/41, 110 00 Praha 1 DIAGNOSTICKÝ KIT PRO DETEKCI MINIMÁLNÍ REZIDUÁLNÍ CHOROBY U KOLOREKTÁLNÍHO KARCINOMU Jednou z nejvhodnějších metod pro detekci minimální
Rapid-VIDITEST Strep A. Jednokrokový kazetový test pro detekci antigenu Steptokoka A ve výtěru z krku. Návod k použití soupravy
 Rapid-VIDITEST Strep A Jednokrokový kazetový test pro detekci antigenu Steptokoka A ve výtěru z krku Návod k použití soupravy Výrobce: VIDIA spol. s r.o., Nad Safinou II 365, Vestec, 252 42 Jesenice u
Rapid-VIDITEST Strep A Jednokrokový kazetový test pro detekci antigenu Steptokoka A ve výtěru z krku Návod k použití soupravy Výrobce: VIDIA spol. s r.o., Nad Safinou II 365, Vestec, 252 42 Jesenice u
MagPurix Viral/Pathogen Nucleic Acids Extraction Kit B
 MagPurix Viral/Pathogen Nucleic Acids Extraction Kit B Kat. č. ZP02012 Doba zpracování: 45-60 minut pro MagPurix 12S 45-65 minut pro MagPurix 24 Použití Souprava MagPurix Viral/Pathogen Nucleic Acids Extraction
MagPurix Viral/Pathogen Nucleic Acids Extraction Kit B Kat. č. ZP02012 Doba zpracování: 45-60 minut pro MagPurix 12S 45-65 minut pro MagPurix 24 Použití Souprava MagPurix Viral/Pathogen Nucleic Acids Extraction
CRP. Axis - Shield. SINGLE TESTS CRP kvantitativní stanovení pomocí přístroje NycoCard Reader II
 Lékařská technika a speciální zdravotní materiál Společnost je zapsána v obchodním rejstříku Městského soudu v Praze, odd. C vložka 1299 Obchodní 110, 251 70 Praha Čestlice Tel. +420 296 328 300 Fax. +420
Lékařská technika a speciální zdravotní materiál Společnost je zapsána v obchodním rejstříku Městského soudu v Praze, odd. C vložka 1299 Obchodní 110, 251 70 Praha Čestlice Tel. +420 296 328 300 Fax. +420
ÚLOHA C Klonování PCR produktu do plasmidu
 Jméno a učo: Datum: ÚLOHA C Klonování PCR produktu do plasmidu TEORETICKÝ ÚVOD Při klonování PCR produktů do plasmidů se využívá vlastnosti Taq polymerasy, a jiných non-proofreading polymeras, přidávat
Jméno a učo: Datum: ÚLOHA C Klonování PCR produktu do plasmidu TEORETICKÝ ÚVOD Při klonování PCR produktů do plasmidů se využívá vlastnosti Taq polymerasy, a jiných non-proofreading polymeras, přidávat
Mentype AMLplex QS. Návod k použití. Důkaz chromozomálních aberací Akutní myeloidní leukémie. Diagnostika in vitro. Vyrobeno v Německu
 Návod k použití Důkaz chromozomálních aberací Akutní myeloidní leukémie Diagnostika in vitro Srpen 2019 45-31220-0010 45-31220-0025 45-31220-0100 45-31220-0400 Biotype GmbH Moritzburger Weg 67 D-01109
Návod k použití Důkaz chromozomálních aberací Akutní myeloidní leukémie Diagnostika in vitro Srpen 2019 45-31220-0010 45-31220-0025 45-31220-0100 45-31220-0400 Biotype GmbH Moritzburger Weg 67 D-01109
Molekulární genetika II zimní semestr 4. výukový týden ( )
 Ústav biologie a lékařské genetiky 1.LF UK a VFN, Praha Molekulární genetika II zimní semestr 4. výukový týden (27.10. 31.10.2008) prenatální DNA diagnostika presymptomatická Potvrzení diagnózy Diagnostika
Ústav biologie a lékařské genetiky 1.LF UK a VFN, Praha Molekulární genetika II zimní semestr 4. výukový týden (27.10. 31.10.2008) prenatální DNA diagnostika presymptomatická Potvrzení diagnózy Diagnostika
SD Rapid test TnI/Myo Duo
 SD Rapid test TnI/Myo Duo Návod k použití soupravy Výrobce: STANDARD DIAGNOSTICS, INC. 156-68 Hagal-dong, Giheung-gu, Yongin-si, Kyonggido, Korea. Tel: +82 31 899 2800, fax: +82 31 899 2840, www.standardia.com
SD Rapid test TnI/Myo Duo Návod k použití soupravy Výrobce: STANDARD DIAGNOSTICS, INC. 156-68 Hagal-dong, Giheung-gu, Yongin-si, Kyonggido, Korea. Tel: +82 31 899 2800, fax: +82 31 899 2840, www.standardia.com
DIAGNOSTICKÝ KIT PRO DETEKCI MINIMÁLNÍ REZIDUÁLNÍ CHOROBY U KARCINOMU PANKREATU
 Úvod IntellMed, s.r.o., Václavské náměstí 820/41, 110 00 Praha 1 DIAGNOSTICKÝ KIT PRO DETEKCI MINIMÁLNÍ REZIDUÁLNÍ CHOROBY U KARCINOMU PANKREATU Jednou z nejvhodnějších metod pro detekci minimální reziduální
Úvod IntellMed, s.r.o., Václavské náměstí 820/41, 110 00 Praha 1 DIAGNOSTICKÝ KIT PRO DETEKCI MINIMÁLNÍ REZIDUÁLNÍ CHOROBY U KARCINOMU PANKREATU Jednou z nejvhodnějších metod pro detekci minimální reziduální
Filozofie validace. Je validace potřebná? Mezinárodní doporučení pro provádění validací ve forenzně genetických laboratořích
 INVESTICE DO ROZVOJE VZDĚLÁVÁNÍ Vzdělávání v oblasti forenzní genetiky reg. č. CZ.1.07/2.3.00/09.0080 Mezinárodní doporučení pro provádění validací ve forenzně genetických laboratořích INVESTICE DO ROZVOJE
INVESTICE DO ROZVOJE VZDĚLÁVÁNÍ Vzdělávání v oblasti forenzní genetiky reg. č. CZ.1.07/2.3.00/09.0080 Mezinárodní doporučení pro provádění validací ve forenzně genetických laboratořích INVESTICE DO ROZVOJE
Rapid-VIDITEST FOB+Tf
 Rapid-VIDITEST FOB+Tf (Jednokrokový kazetový test pro detekci hemoglobinu a transferrinu ve stolici) Návod k použití soupravy Výrobce: VIDIA spol. s r.o., Nad Safinou II 365, Vestec, 252 42 Jesenice u
Rapid-VIDITEST FOB+Tf (Jednokrokový kazetový test pro detekci hemoglobinu a transferrinu ve stolici) Návod k použití soupravy Výrobce: VIDIA spol. s r.o., Nad Safinou II 365, Vestec, 252 42 Jesenice u
Real time PCR detekce Borrelia burgdorferi Sensu Lato
 Real time PCR detekce Borrelia burgdorferi Sensu Lato In vitro diagnostikum -80 až -20 C Viz. obal RT-BBSL-050 Viz. obal POPIS SOUPRAVY Real Time PCR souprava pro detekci Borrelia burgdorferi Sensu Lato
Real time PCR detekce Borrelia burgdorferi Sensu Lato In vitro diagnostikum -80 až -20 C Viz. obal RT-BBSL-050 Viz. obal POPIS SOUPRAVY Real Time PCR souprava pro detekci Borrelia burgdorferi Sensu Lato
Real time PCR detekce bakterií Legionella pneumophila+micdadei, Mycoplasma pneumoniae, Chlamydia pneumoniae a Bordetella pertussis
 Real time PCR detekce bakterií Legionella pneumophila+micdadei, Mycoplasma pneumoniae, Chlamydia pneumoniae a Bordetella pertussis In vitro diagnostikum -80 až -20 C Viz. obal RT-PPX-050 Viz. obal POPIS
Real time PCR detekce bakterií Legionella pneumophila+micdadei, Mycoplasma pneumoniae, Chlamydia pneumoniae a Bordetella pertussis In vitro diagnostikum -80 až -20 C Viz. obal RT-PPX-050 Viz. obal POPIS
Real time PCR detekce bakterií Haemophilus influenzae, Neisseria meningitidis, Streptococcus pneumoniae a Listeria monocytogenes
 Real time PCR detekce bakterií Haemophilus influenzae, Neisseria meningitidis, Streptococcus pneumoniae a Listeria monocytogenes In vitro diagnostikum -80 až -20 C Viz. obal RT-HNSL-050 Viz. obal POPIS
Real time PCR detekce bakterií Haemophilus influenzae, Neisseria meningitidis, Streptococcus pneumoniae a Listeria monocytogenes In vitro diagnostikum -80 až -20 C Viz. obal RT-HNSL-050 Viz. obal POPIS
Využití DNA markerů ve studiu fylogeneze rostlin
 Mendelova genetika v příkladech Využití DNA markerů ve studiu fylogeneze rostlin Ing. Petra VESELÁ Ústav lesnické botaniky, dendrologie a geobiocenologie LDF MENDELU Brno Tento projekt je spolufinancován
Mendelova genetika v příkladech Využití DNA markerů ve studiu fylogeneze rostlin Ing. Petra VESELÁ Ústav lesnické botaniky, dendrologie a geobiocenologie LDF MENDELU Brno Tento projekt je spolufinancován
EUROArray. laboratorní diagnostiku. Praha RNDr. Tereza Gürtlerová. Podtitul, název produktu
 EUROArray DNA Prezentace mikročipy titul pro rutinní laboratorní diagnostiku RNDr. Tereza Gürtlerová Praha 09. 03. 2017 Přehled EUROArray System Princip provedení testu Přehled dostupných kitů EUROArray
EUROArray DNA Prezentace mikročipy titul pro rutinní laboratorní diagnostiku RNDr. Tereza Gürtlerová Praha 09. 03. 2017 Přehled EUROArray System Princip provedení testu Přehled dostupných kitů EUROArray
Sure-MeDIP I. with magnetic beads and MNase. www.krd.cz
 Sure-MeDIP I with magnetic beads and MNase www.krd.cz 1 Obsah soupravy a skladování MeDIP souprava obsahuje reagencie na provedení 25 reakcí. Souprava je rozdělen do dvou částí, jedna je distribuována
Sure-MeDIP I with magnetic beads and MNase www.krd.cz 1 Obsah soupravy a skladování MeDIP souprava obsahuje reagencie na provedení 25 reakcí. Souprava je rozdělen do dvou částí, jedna je distribuována
nastavení real-time PCR cykleru CFX 96 Real-Time System
 Verze: 1.2 Datum poslední revize: 24.9.2014 nastavení real-time PCR cykleru CFX 96 Real-Time System (BioRad) generi biotech OBSAH 1. Spuštění již existujícího či nastavení nového teplotního profilu...3
Verze: 1.2 Datum poslední revize: 24.9.2014 nastavení real-time PCR cykleru CFX 96 Real-Time System (BioRad) generi biotech OBSAH 1. Spuštění již existujícího či nastavení nového teplotního profilu...3
List protokolu QIAsymphony SP
 List protokolu QIAsymphony SP Srpen 2015 Tissue_LC_200_V7_DSP a Tissue_HC_200_V7_DSP (uživatelem validovaný pro použití s minisadou QIAsymphony DSP DNA) Tento dokument Tissue_LC_200_V7_DSP a Tissue_HC_200_V7_DSP
List protokolu QIAsymphony SP Srpen 2015 Tissue_LC_200_V7_DSP a Tissue_HC_200_V7_DSP (uživatelem validovaný pro použití s minisadou QIAsymphony DSP DNA) Tento dokument Tissue_LC_200_V7_DSP a Tissue_HC_200_V7_DSP
nastavení real-time PCR cykléru icycler iq5 Multi-Color Real-Time PCR Detection System
 Verze: 1.0 Datum poslední revize: 2.1.2014 nastavení real-time PCR cykléru icycler iq5 Multi-Color Real-Time PCR Detection System (BioRad) generi biotech OBSAH: 1. Spuštění již existujícího či nastavení
Verze: 1.0 Datum poslední revize: 2.1.2014 nastavení real-time PCR cykléru icycler iq5 Multi-Color Real-Time PCR Detection System (BioRad) generi biotech OBSAH: 1. Spuštění již existujícího či nastavení
Konečná zpráva hodnocení různých způsobů přípravy vzorků pro AMPLICOR HPV test firmy Roche
 Konečná zpráva hodnocení různých způsobů přípravy vzorků pro AMPLICOR HPV test firmy Roche Charakteristika testu: Set AMPLICOR HPV vyráběný firmou Roche je určený pro detekci vysoko-rizikových typů lidských
Konečná zpráva hodnocení různých způsobů přípravy vzorků pro AMPLICOR HPV test firmy Roche Charakteristika testu: Set AMPLICOR HPV vyráběný firmou Roche je určený pro detekci vysoko-rizikových typů lidských
nastavení real-time PCR cykléru CFX 96 Real-Time System
 nastavení real-time PCR cykléru CFX 96 Real-Time System (BioRad) generi biotech OBSAH 1. Spuštění již existujícího či nastavení nového teplotního profilu...3 1.1. Spuštění již uloženého teplotního profilu...3
nastavení real-time PCR cykléru CFX 96 Real-Time System (BioRad) generi biotech OBSAH 1. Spuštění již existujícího či nastavení nového teplotního profilu...3 1.1. Spuštění již uloženého teplotního profilu...3
HR1 BRCA 1/2 NGS IVD KIT
 HR1 BRCA 1/2 NGS IVD KIT Navrženo pro PGM ION-TORRENT KÓD PRODUKTU: PRG-HR1-01 VELIKOST BALENÍ: 16 TEST Uživatelská příručka Rev03.2015 Str. 1 Obsah 1. ÚVOD 3 2. ÚČEL POUŽITÍ 3 3. OBSAH KITU 4 4. SKLADOVÁNÍ
HR1 BRCA 1/2 NGS IVD KIT Navrženo pro PGM ION-TORRENT KÓD PRODUKTU: PRG-HR1-01 VELIKOST BALENÍ: 16 TEST Uživatelská příručka Rev03.2015 Str. 1 Obsah 1. ÚVOD 3 2. ÚČEL POUŽITÍ 3 3. OBSAH KITU 4 4. SKLADOVÁNÍ
BlueWell Intrinsic Factor IgG ELISA Cat.. IF01-96
 BlueWell Intrinsic Factor IgG ELISA Cat.. IF01-96 96 D-tek s.a. rue René Descartes 19 BE-7000 Mons BELGIUM Tel. +32 65 84 18 88 Fax. +32 65 84 26 63 Email: info@d-tek.be Domovská stránka www.d-tek.be R.C.
BlueWell Intrinsic Factor IgG ELISA Cat.. IF01-96 96 D-tek s.a. rue René Descartes 19 BE-7000 Mons BELGIUM Tel. +32 65 84 18 88 Fax. +32 65 84 26 63 Email: info@d-tek.be Domovská stránka www.d-tek.be R.C.
Testovací kity Protrans HLA SBT 1 1.0 Strategie Protrans sekvenování 3 2.0 PROTRANS HLA Sekvenační systém 4 2.0 PROTRANS Sekvenačníí kity (S4, S3,
 Návod k použití Obsah Strana Testovací kity Protrans HLA SBT 1 1.0 Strategie Protrans sekvenování 3 2.0 PROTRANS HLA Sekvenační systém 4 2.0 PROTRANS Sekvenačníí kity (S4, S3, Domino Stones, S2, S1) 4
Návod k použití Obsah Strana Testovací kity Protrans HLA SBT 1 1.0 Strategie Protrans sekvenování 3 2.0 PROTRANS HLA Sekvenační systém 4 2.0 PROTRANS Sekvenačníí kity (S4, S3, Domino Stones, S2, S1) 4
C V C. Návod k použití pro Biofortuna SSPGo TM HLA No Template Control Kit BF-40-02. Revize 2. Červenec 2014
 DOT130v1 Instructions for Use Biofortuna SSPGo TM HLA No Template Control Kit BF-40-02 Strana 1 / 7 Návod k použití pro Biofortuna SSPGo TM HLA No Template Control Kit BF-40-02 Revize 2 Červenec 2014 DOT130v1
DOT130v1 Instructions for Use Biofortuna SSPGo TM HLA No Template Control Kit BF-40-02 Strana 1 / 7 Návod k použití pro Biofortuna SSPGo TM HLA No Template Control Kit BF-40-02 Revize 2 Červenec 2014 DOT130v1
ProFlow Rotavirus-Adenovirus Combi
 KATALOGOVÉ ČÍSLO: PL.3010 (20 testů) ProFlow Rotavirus-Adenovirus Combi ZAMÝŠLENÉ POUŽITÍ ProFlow Rotavirus-Adenovirus je jednoduchý, rychlý imunologický test pro kvalitativní detekci antigenů Rotaviru
KATALOGOVÉ ČÍSLO: PL.3010 (20 testů) ProFlow Rotavirus-Adenovirus Combi ZAMÝŠLENÉ POUŽITÍ ProFlow Rotavirus-Adenovirus je jednoduchý, rychlý imunologický test pro kvalitativní detekci antigenů Rotaviru
Písemná zpráva zadavatele
 Písemná zpráva zadavatele veřejné zakázky zadávané dle zákona č. 137/2006 Sb., o veřejných zakázkách, ve znění účinném ke dni zahájení zadávacího řízení (dále jen ZVZ ). Veřejná zakázka Název: Ostatní
Písemná zpráva zadavatele veřejné zakázky zadávané dle zákona č. 137/2006 Sb., o veřejných zakázkách, ve znění účinném ke dni zahájení zadávacího řízení (dále jen ZVZ ). Veřejná zakázka Název: Ostatní
Chromoprobe Multiprobe - T System
 Návod k použití REF: PMP 009/PMP 008/ PMP 007 Chromoprobe Multiprobe - T System Pouze pro profesionální použití Fluorescenční In Situ Hybridizace (FISH) je technika, která umožňuje detekci DNA sekvencí
Návod k použití REF: PMP 009/PMP 008/ PMP 007 Chromoprobe Multiprobe - T System Pouze pro profesionální použití Fluorescenční In Situ Hybridizace (FISH) je technika, která umožňuje detekci DNA sekvencí
DNA TECHNIKY IDENTIFIKACE ŽIVOČIŠNÝCH DRUHŮ V KRMIVU A POTRAVINÁCH. Michaela Nesvadbová
 DNA TECHNIKY IDENTIFIKACE ŽIVOČIŠNÝCH DRUHŮ V KRMIVU A POTRAVINÁCH Michaela Nesvadbová Význam identifikace živočišných druhů v krmivu a potravinách povinností každého výrobce je řádně a pravdivě označit
DNA TECHNIKY IDENTIFIKACE ŽIVOČIŠNÝCH DRUHŮ V KRMIVU A POTRAVINÁCH Michaela Nesvadbová Význam identifikace živočišných druhů v krmivu a potravinách povinností každého výrobce je řádně a pravdivě označit
Rapid-VIDITEST RSV. (Jednokrokový kazetový test pro in vitro diagnostiku Respiračního syncytiálního viru z nosních výtěrů, výplachů a aspirátů)
 Rapid-VIDITEST RSV (Jednokrokový kazetový test pro in vitro diagnostiku Respiračního syncytiálního viru z nosních výtěrů, výplachů a aspirátů) Návod k použití soupravy Výrobce: VIDIA spol. s r.o., Nad
Rapid-VIDITEST RSV (Jednokrokový kazetový test pro in vitro diagnostiku Respiračního syncytiálního viru z nosních výtěrů, výplachů a aspirátů) Návod k použití soupravy Výrobce: VIDIA spol. s r.o., Nad
Sada artus HBV QS-RGQ
 Sada artus HBV QS-RGQ Výkonnostní charakteristiky Sada artus HBV QS-RGQ, verze 1, 4506363, 4506366 Před samotným testem si ověřte dostupnost nových revizí elektronického značení na adrese www.qiagen.com/products/artushbvrgpcrkitce.aspx.
Sada artus HBV QS-RGQ Výkonnostní charakteristiky Sada artus HBV QS-RGQ, verze 1, 4506363, 4506366 Před samotným testem si ověřte dostupnost nových revizí elektronického značení na adrese www.qiagen.com/products/artushbvrgpcrkitce.aspx.
Určeno pro obecné laboratorní užití. Není určeno pro použití v diagnostických postupech. POUZE PRO POUŽITÍ IN VITRO.
 Určeno pro obecné laboratorní užití. Není určeno pro použití v diagnostických postupech. POUZE PRO POUŽITÍ IN VITRO. PCR Nucleotide Mix Předem připravený roztok ultračistých PCR deoxynukleotidů (datp,
Určeno pro obecné laboratorní užití. Není určeno pro použití v diagnostických postupech. POUZE PRO POUŽITÍ IN VITRO. PCR Nucleotide Mix Předem připravený roztok ultračistých PCR deoxynukleotidů (datp,
Vznešený 2015 QIAsymphony DSP DNA Kits: Charakteristika účinnosti
 Vznešený 2015 QIAsymphony DSP DNA Kits: Charakteristika účinnosti Tento dokument se nazývá Sady QIAsymphony DSP DNA: Charakteristika účinnosti, R4, pro sady verze 1 ě QIAsymphony DSP DNA Kity jsou určené
Vznešený 2015 QIAsymphony DSP DNA Kits: Charakteristika účinnosti Tento dokument se nazývá Sady QIAsymphony DSP DNA: Charakteristika účinnosti, R4, pro sady verze 1 ě QIAsymphony DSP DNA Kity jsou určené
DY D NE N X Hana Vlastníková
 DYNEX Hana Vlastníková Molekulární biologie: Vybavení laboratoře na klíč Přístrojová technika Kompatibilní diagnostické soupravy Profesionální přístup SOP Technická podpora Servis Přístrojové vybavení:
DYNEX Hana Vlastníková Molekulární biologie: Vybavení laboratoře na klíč Přístrojová technika Kompatibilní diagnostické soupravy Profesionální přístup SOP Technická podpora Servis Přístrojové vybavení:
Návrh směrnic pro správnou laboratorní diagnostiku Friedreichovy ataxie.
 Návrh směrnic pro správnou laboratorní diagnostiku Friedreichovy ataxie. Připravila L.Fajkusová Online Mendelian Inheritance in Man: #229300 FRIEDREICH ATAXIA 1; FRDA *606829 FRDA GENE; FRDA Popis onemocnění
Návrh směrnic pro správnou laboratorní diagnostiku Friedreichovy ataxie. Připravila L.Fajkusová Online Mendelian Inheritance in Man: #229300 FRIEDREICH ATAXIA 1; FRDA *606829 FRDA GENE; FRDA Popis onemocnění
TESTOVÁNÍ GMO Praktikum fyziologie rostlin
 Teoretický úvod: TESTOVÁNÍ GMO Praktikum fyziologie rostlin 1 Teoretický úvod: TESTOVÁNÍ GMO Obecně na úvod Určitě jste už slyšeli pojem geneticky modifikovaný organismus (GMO). Úprava vlastností přirozeně
Teoretický úvod: TESTOVÁNÍ GMO Praktikum fyziologie rostlin 1 Teoretický úvod: TESTOVÁNÍ GMO Obecně na úvod Určitě jste už slyšeli pojem geneticky modifikovaný organismus (GMO). Úprava vlastností přirozeně
Fragment Analyzer UNIKÁTNÍ KAPILÁROVÝ FRAGMENTAČNÍ ANALYZÁTOR VÝBORNÉ VÝSLEDKY UNIKÁTNÍ VLASTNOSTI
 Fragment Analyzer UNIKÁTNÍ KAPILÁROVÝ FRAGMENTAČNÍ ANALYZÁTOR VÝBORNÉ VÝSLEDKY UNIKÁTNÍ VLASTNOSTI Výborný přístroj, výborné výsledky Fragmentační analyzátor je automatizovaný kapilárový systém s CE značkou
Fragment Analyzer UNIKÁTNÍ KAPILÁROVÝ FRAGMENTAČNÍ ANALYZÁTOR VÝBORNÉ VÝSLEDKY UNIKÁTNÍ VLASTNOSTI Výborný přístroj, výborné výsledky Fragmentační analyzátor je automatizovaný kapilárový systém s CE značkou
Polymorfismus délky restrikčních fragmentů
 Polymorfismus délky restrikčních fragmentů Princip: Chemikálie: PCR produkt z předchozího praktického cvičení Endonukleáza KpnI 10 U μl -1 Pufr pro KpnI 10 koncentrovaný (Tris-HCl 100 mmol l -1 ph 7,5,
Polymorfismus délky restrikčních fragmentů Princip: Chemikálie: PCR produkt z předchozího praktického cvičení Endonukleáza KpnI 10 U μl -1 Pufr pro KpnI 10 koncentrovaný (Tris-HCl 100 mmol l -1 ph 7,5,
KVANTITATIVNÍ REAL-TIME PCR (q-real-time PCR)
 KVANTITATIVNÍ REAL-TIME PCR (q-real-time PCR) Metoda Real-time PCR slouží pro kvantifikaci DNA a transkripce. Metoda je založena na klasické PCR, ovšem s využitím speciálního cycleru, který v průběhu PCR
KVANTITATIVNÍ REAL-TIME PCR (q-real-time PCR) Metoda Real-time PCR slouží pro kvantifikaci DNA a transkripce. Metoda je založena na klasické PCR, ovšem s využitím speciálního cycleru, který v průběhu PCR
Rapid-VIDITEST. Rota-Adeno Card. (Jednokrokový kazetový test pro in vitro diagnostiku rotavirů a adenovirů) Návod k použití soupravy
 Rapid-VIDITEST Rota-Adeno Card (Jednokrokový kazetový test pro in vitro diagnostiku rotavirů a adenovirů) Návod k použití soupravy Výrobce: VIDIA spol. s r.o., Nad Safinou II č. 365, Vestec, 252 42 Jesenice
Rapid-VIDITEST Rota-Adeno Card (Jednokrokový kazetový test pro in vitro diagnostiku rotavirů a adenovirů) Návod k použití soupravy Výrobce: VIDIA spol. s r.o., Nad Safinou II č. 365, Vestec, 252 42 Jesenice
VÝZNAM NĚKTERÝCH FAKTORŮ PREANALYTICKÉ FÁZE V MOLEKULÁRNÍ BIOLOGII
 VÝZNAM NĚKTERÝCH FAKTORŮ PREANALYTICKÉ FÁZE V MOLEKULÁRNÍ BIOLOGII Plíšková L., Hrochová K., Kutová R. Ústav klinické biochemie a diagnostiky FN Hradec Králové PREANALYTICKÁ FÁZE V MOLEKULÁRNÍ BIOLOGII
VÝZNAM NĚKTERÝCH FAKTORŮ PREANALYTICKÉ FÁZE V MOLEKULÁRNÍ BIOLOGII Plíšková L., Hrochová K., Kutová R. Ústav klinické biochemie a diagnostiky FN Hradec Králové PREANALYTICKÁ FÁZE V MOLEKULÁRNÍ BIOLOGII
Seznam použitých chemikálií
 PŘÍLOHY Tabulky Tabulka č. 1. Přehled výsledků teplot tání pro amplifikáty primeru G3010A. Testování teplot tání rozředěného zásobího roztoku o koncentraci ndna 1ng / 1μl, ředění uvedeno v tabulce. Tabulka
PŘÍLOHY Tabulky Tabulka č. 1. Přehled výsledků teplot tání pro amplifikáty primeru G3010A. Testování teplot tání rozředěného zásobího roztoku o koncentraci ndna 1ng / 1μl, ředění uvedeno v tabulce. Tabulka
IL-6. Laterální imunodifuze pro semikvantitativní měření lidského interleukinu 6 (IL- 6)
 IL-6 Laterální imunodifuze pro semikvantitativní měření lidského interleukinu 6 (IL- 6) Lateralní průtokový imunologický test pro kvantitativní stanovení lidského interleukinu-6 (IL-6), vyhodnocení pomocí
IL-6 Laterální imunodifuze pro semikvantitativní měření lidského interleukinu 6 (IL- 6) Lateralní průtokový imunologický test pro kvantitativní stanovení lidského interleukinu-6 (IL-6), vyhodnocení pomocí
LW Color Compensation Kit Uživatelská příručka
 LW Color Compensation Kit Uživatelská příručka 04 847 148 001 Pro všeobecné použití v laboratoři Obsah 3 (16) Obsah 1 Úvodní informace pro LW Color Compensation Kit... 2 Požadovaný materiál... 2.1 Složení
LW Color Compensation Kit Uživatelská příručka 04 847 148 001 Pro všeobecné použití v laboratoři Obsah 3 (16) Obsah 1 Úvodní informace pro LW Color Compensation Kit... 2 Požadovaný materiál... 2.1 Složení
DIAGNOSTICKÝ KIT PRO DETEKCI MINIMÁLNÍ REZIUDÁLNÍ CHOROBY MRD EGFR
 Úvod IntellMed, s.r.o., Václavské náměstí 820/41, 110 00 Praha 1 DIAGNOSTICKÝ KIT PRO DETEKCI MINIMÁLNÍ REZIUDÁLNÍ CHOROBY MRD EGFR Jednou z nejvhodnějších metod pro detekci minimální reziduální choroby
Úvod IntellMed, s.r.o., Václavské náměstí 820/41, 110 00 Praha 1 DIAGNOSTICKÝ KIT PRO DETEKCI MINIMÁLNÍ REZIUDÁLNÍ CHOROBY MRD EGFR Jednou z nejvhodnějších metod pro detekci minimální reziduální choroby
Rapid-VIDITEST RSV. (Jednokrokový kazetový test pro in vitro diagnostiku Respiračního syncytiálního viru z nosních výtěrů, výplachů a aspirátů)
 Rapid-VIDITEST RSV (Jednokrokový kazetový test pro in vitro diagnostiku Respiračního syncytiálního viru z nosních výtěrů, výplachů a aspirátů) Návod k použití soupravy Výrobce: VIDIA spol. s r.o., Nad
Rapid-VIDITEST RSV (Jednokrokový kazetový test pro in vitro diagnostiku Respiračního syncytiálního viru z nosních výtěrů, výplachů a aspirátů) Návod k použití soupravy Výrobce: VIDIA spol. s r.o., Nad
HbA1c. Axis - Shield. Společnost je zapsána v obchodním rejstříku Městského soudu v Praze, odd. C vložka 1299
 Lékařská technika a speciální zdravotní materiál Společnost je zapsána v obchodním rejstříku Městského soudu v Praze, odd. C vložka 1299 Obchodní 110, 251 70 Praha Čestlice Tel. +420 296 328 300 Fax. +420
Lékařská technika a speciální zdravotní materiál Společnost je zapsána v obchodním rejstříku Městského soudu v Praze, odd. C vložka 1299 Obchodní 110, 251 70 Praha Čestlice Tel. +420 296 328 300 Fax. +420
Rapid-VIDITEST Campylobacter
 Rapid-VIDITEST Campylobacter (Jednokrokový kazetový test pro detekci Campylobacter spp.) Návod k použití soupravy Výrobce: VIDIA spol. s r.o., Nad Safinou II 365, Vestec, 252 42 Jesenice u Prahy, Tel:
Rapid-VIDITEST Campylobacter (Jednokrokový kazetový test pro detekci Campylobacter spp.) Návod k použití soupravy Výrobce: VIDIA spol. s r.o., Nad Safinou II 365, Vestec, 252 42 Jesenice u Prahy, Tel:
HR1 BRCA 1/2 NGS IVD KIT
 HR1 BRCA 1/2 NGS IVD KIT Navrženo pro PGM ION-TORRENT KÓD PRODUKTU: PRG-HR1-01 VELIKOST BALENÍ: 16 TEST Uživatelská příručka Rev05.2015 Str. 1 Obsah 1. ÚVOD 3 2. ÚČEL POUŽITÍ 3 3. OBSAH KITU 4 4. SKLADOVÁNÍ
HR1 BRCA 1/2 NGS IVD KIT Navrženo pro PGM ION-TORRENT KÓD PRODUKTU: PRG-HR1-01 VELIKOST BALENÍ: 16 TEST Uživatelská příručka Rev05.2015 Str. 1 Obsah 1. ÚVOD 3 2. ÚČEL POUŽITÍ 3 3. OBSAH KITU 4 4. SKLADOVÁNÍ
Rapid-VIDITEST Adenovirus Resp.
 Rapid-VIDITEST Adenovirus Resp. (Jednokrokový kazetový test pro in vitro diagnostiku Adenoviru z nosních výtěrů, výplachů a aspirátů) Návod k použití soupravy Výrobce: VIDIA spol. s r.o., Nad Safinou II
Rapid-VIDITEST Adenovirus Resp. (Jednokrokový kazetový test pro in vitro diagnostiku Adenoviru z nosních výtěrů, výplachů a aspirátů) Návod k použití soupravy Výrobce: VIDIA spol. s r.o., Nad Safinou II
NÁVOD K POUŽITÍ PRO HER2 DNA QUANTIFICATION KIT
 IČ: 80 DIČ: CZ80 sales@intellmed.eu NÁVOD K POUŽITÍ PRO HER DNA QUANTIFICATION KIT IČ: 80 DIČ: CZ80 sales@intellmed.eu OBSAH Návod k použití pro HER DNA QUANTIFICATION KIT.... Úvod.... Označení.... Rozsah
IČ: 80 DIČ: CZ80 sales@intellmed.eu NÁVOD K POUŽITÍ PRO HER DNA QUANTIFICATION KIT IČ: 80 DIČ: CZ80 sales@intellmed.eu OBSAH Návod k použití pro HER DNA QUANTIFICATION KIT.... Úvod.... Označení.... Rozsah
MOLEKULÁRNÍ BIOLOGIE. 2. Polymerázová řetězová reakce (PCR)
 MOLEKULÁRNÍ BIOLOGIE 2. Polymerázová řetězová reakce (PCR) Náplň praktik 1. Izolace DNA z buněk bukální sliznice - izolační kit MACHEREY-NAGEL 2. PCR polymerázová řetězová reakce (templát gdna) 3. Restrikční
MOLEKULÁRNÍ BIOLOGIE 2. Polymerázová řetězová reakce (PCR) Náplň praktik 1. Izolace DNA z buněk bukální sliznice - izolační kit MACHEREY-NAGEL 2. PCR polymerázová řetězová reakce (templát gdna) 3. Restrikční
Proflow Adenovirus. KATALOGOVÉ ČÍSLO: PL.3011 (20 testů)
 KATALOGOVÉ ČÍSLO: PL.3011 (20 testů) Proflow Adenovirus ZAMÝŠLENÉ POUŽITÍ Proflow Adenovirus je jednoduchý, rychlý imunologický test pro kvalitativní detekci antigenu Adenoviru ve vzorku stolice. Tento
KATALOGOVÉ ČÍSLO: PL.3011 (20 testů) Proflow Adenovirus ZAMÝŠLENÉ POUŽITÍ Proflow Adenovirus je jednoduchý, rychlý imunologický test pro kvalitativní detekci antigenu Adenoviru ve vzorku stolice. Tento
Manuál. Verze Duben Novinka v detekci chromozomálních aberací spojených s akutní myeloidní leukémií. Mentype AMLplex QS Duben 2015 LEUGAAMLv2cz
 Mentype AMLplex QS Manuál Novinka v detekci chromozomálních aberací spojených s akutní myeloidní leukémií Verze Duben 2015 Vyrobeno v Německu Biotype Diagnostic GmbH vyvíjí, vyrábí a prodává vlastní detekční
Mentype AMLplex QS Manuál Novinka v detekci chromozomálních aberací spojených s akutní myeloidní leukémií Verze Duben 2015 Vyrobeno v Německu Biotype Diagnostic GmbH vyvíjí, vyrábí a prodává vlastní detekční
PŘÍPRAVA REAGENCIÍ A STABILITA:
 REF 816A 10 lahviček z nichž každá obsahuje 0,5ml LAtrol Abnormální kontroly REF 816N 10 lahviček z nichž každá obsahuje 1,0ml LAtrol Normální kontroly UŽITÍ: LAtrol Abnormální kontrolní plazma (REF 816A)
REF 816A 10 lahviček z nichž každá obsahuje 0,5ml LAtrol Abnormální kontroly REF 816N 10 lahviček z nichž každá obsahuje 1,0ml LAtrol Normální kontroly UŽITÍ: LAtrol Abnormální kontrolní plazma (REF 816A)
Tkáňový homogenizátor MagNA Lyser od společnosti Roche
 Izolace RNA Pracovní postup Homogenizace: Pozn. Postup homogenizace platí pouze pro izolaci RNA z nativní tkáně, v případě izolace z buněčné suspenze je tento krok vynechán a začíná se přídavkem homogenizačního
Izolace RNA Pracovní postup Homogenizace: Pozn. Postup homogenizace platí pouze pro izolaci RNA z nativní tkáně, v případě izolace z buněčné suspenze je tento krok vynechán a začíná se přídavkem homogenizačního
Manuál. Vyrobeno v Německu. AMLGAv3cz xxx* *xxx definuje velikost balení
 Manuál Novinka v detekci chromozomálních aberací spojených s akutní myeloidní leukémií 45-31220-0xxx* *xxx definuje velikost balení Vyrobeno v Německu Biotype Diagnostic GmbH vyvíjí, vyrábí a prodává vlastní
Manuál Novinka v detekci chromozomálních aberací spojených s akutní myeloidní leukémií 45-31220-0xxx* *xxx definuje velikost balení Vyrobeno v Německu Biotype Diagnostic GmbH vyvíjí, vyrábí a prodává vlastní
POUŽITÍ PRINCIPY STANOVENÍ
 NOW Malaria TEST POUŽITÍ Binax NOW Malaria TEST je rychlá imunochromatografická metoda pro kvalitativní stanovení antigenů Plasmodium falciparum (PF), Plasmodium vivax (PV), Plasmodium malariae (PM) a
NOW Malaria TEST POUŽITÍ Binax NOW Malaria TEST je rychlá imunochromatografická metoda pro kvalitativní stanovení antigenů Plasmodium falciparum (PF), Plasmodium vivax (PV), Plasmodium malariae (PM) a
CHORUS CARDIOLIPIN-G
 CHORUS CARDIOLIPIN-G 86046 (36 testů) Výrobce: DIESSE Diagnostica Senese Via delle Rose 10 53035 Monteriggioni (Siena) Itálie OBSAH 1 Úvod... 3 2 Princip testu... 3 3 Složení soupravy... 3 4 Další potřebné
CHORUS CARDIOLIPIN-G 86046 (36 testů) Výrobce: DIESSE Diagnostica Senese Via delle Rose 10 53035 Monteriggioni (Siena) Itálie OBSAH 1 Úvod... 3 2 Princip testu... 3 3 Složení soupravy... 3 4 Další potřebné
NGS analýza dat. kroužek, Alena Musilová
 NGS analýza dat kroužek, 16.12.2016 Alena Musilová Typy NGS experimentů Název Materiál Cílí na..? Cíl experimentu? amplikon DNA malý počet vybraných genů hledání variant exom DNA všechny geny hledání
NGS analýza dat kroužek, 16.12.2016 Alena Musilová Typy NGS experimentů Název Materiál Cílí na..? Cíl experimentu? amplikon DNA malý počet vybraných genů hledání variant exom DNA všechny geny hledání
HISTO TYPE B*27 Q. Souprava pro tkáňovou typizaci HLA alel na molekulárně genetickém základě
 CZ Návod k použití HISTO TYPE B*27 Q Souprava pro tkáňovou typizaci HLA alel na molekulárně genetickém základě Návody v elektronické podobě najdete na www.bag-healthcare.com IVD REF 728200 HISTO TYPE B*27
CZ Návod k použití HISTO TYPE B*27 Q Souprava pro tkáňovou typizaci HLA alel na molekulárně genetickém základě Návody v elektronické podobě najdete na www.bag-healthcare.com IVD REF 728200 HISTO TYPE B*27
Cystická fibróza. Iveta Valášková ivalskova@fnbrno.cz. Fakultní nemocnice Brno Oddělení lékařské genetiky
 Cystická fibróza Iveta Valášková ivalskova@fnbrno.cz Fakultní nemocnice Brno Oddělení lékařské genetiky Cystická fibróza nejčastěji se vyskytující autozomálně recesivní dědičná metabolická porucha v zakavkazské
Cystická fibróza Iveta Valášková ivalskova@fnbrno.cz Fakultní nemocnice Brno Oddělení lékařské genetiky Cystická fibróza nejčastěji se vyskytující autozomálně recesivní dědičná metabolická porucha v zakavkazské
Seznam vyšetření. Detekce markerů: F2 (protrombin) G20210A, F5 Leiden (G1691A), MTHFR C677T, MTHFR A1298C, PAI-1 4G/5G, F5 Cambridge a Hong Kong
 VD.PCE 02 Laboratorní příručka Příloha č. 2: Seznam vyšetření Molekulární hematologie a hematoonkologie Detekce markerů: F2 (protrombin) G20210A, F5 Leiden (G1691A), MTHFR C677T, MTHFR A1298C, PAI-1 4G/5G,
VD.PCE 02 Laboratorní příručka Příloha č. 2: Seznam vyšetření Molekulární hematologie a hematoonkologie Detekce markerů: F2 (protrombin) G20210A, F5 Leiden (G1691A), MTHFR C677T, MTHFR A1298C, PAI-1 4G/5G,
MagPurix Bacterial DNA Extraction Kit
 MagPurix Bacterial DNA Extraction Kit Kat. č. ZP02006 Doba zpracování: 55-65 minut pro MagPurix 12S 55-75 minut pro MagPurix 24 Použití Souprava MagPurix Bacterial DNA Extraction Kit je určena pro izolátor
MagPurix Bacterial DNA Extraction Kit Kat. č. ZP02006 Doba zpracování: 55-65 minut pro MagPurix 12S 55-75 minut pro MagPurix 24 Použití Souprava MagPurix Bacterial DNA Extraction Kit je určena pro izolátor
List protokolu QIAsymphony SP
 Únor 2017 List protokolu QIAsymphony SP circdna_2000_dsp_v1 a circdna_4000_dsp_v1 Tento dokument je Listem protokolu QIAsymphony circdna_2000_dsp_v1 a circdna_4000_dsp_v1, verze 1, R1 Sample to Insight
Únor 2017 List protokolu QIAsymphony SP circdna_2000_dsp_v1 a circdna_4000_dsp_v1 Tento dokument je Listem protokolu QIAsymphony circdna_2000_dsp_v1 a circdna_4000_dsp_v1, verze 1, R1 Sample to Insight
Rapid-VIDITEST FOB. (Jednokrokový blisterový test pro detekci hemoglobinu ve stolici) Návod k použití soupravy
 Rapid-VIDITEST FOB (Jednokrokový blisterový test pro detekci hemoglobinu ve stolici) Návod k použití soupravy Výrobce: VIDIA spol. s r.o., Nad Safinou II 365, Vestec, 252 42 Jesenice u Prahy, Tel: 261
Rapid-VIDITEST FOB (Jednokrokový blisterový test pro detekci hemoglobinu ve stolici) Návod k použití soupravy Výrobce: VIDIA spol. s r.o., Nad Safinou II 365, Vestec, 252 42 Jesenice u Prahy, Tel: 261
Návod k použití CRC RAScan Combination Kit
 Návod k použití CRC RAScan Combination Kit Souprava SURVEYOR Scan KRAS a NRAS Exons 2, 3 & 4 CE IVD se systémy Tento návod k použití si důkladně přečtěte před použitím tohoto produktu. Uschovejte si tento
Návod k použití CRC RAScan Combination Kit Souprava SURVEYOR Scan KRAS a NRAS Exons 2, 3 & 4 CE IVD se systémy Tento návod k použití si důkladně přečtěte před použitím tohoto produktu. Uschovejte si tento
Polymorfismus délky restrikčních fragmentů (RFLP)
 ÚSTAV LÉKAŘSKÉ BIOCHEMIE A LABORATORNÍ DIAGNOSTIKY 1. LF UK Polymorfismus délky restrikčních fragmentů (RFLP) Praktické cvičení z lékařské biochemie Všeobecné lékařství Martin Vejražka 2017/18 Obsah POLYMORFISMUS
ÚSTAV LÉKAŘSKÉ BIOCHEMIE A LABORATORNÍ DIAGNOSTIKY 1. LF UK Polymorfismus délky restrikčních fragmentů (RFLP) Praktické cvičení z lékařské biochemie Všeobecné lékařství Martin Vejražka 2017/18 Obsah POLYMORFISMUS
Mgr. et Mgr. Lenka Falková. Laboratoř agrogenomiky. Ústav morfologie, fyziologie a genetiky zvířat Mendelova univerzita
 Mgr. et Mgr. Lenka Falková Laboratoř agrogenomiky Ústav morfologie, fyziologie a genetiky zvířat Mendelova univerzita 9. 9. 2015 Šlechtění Užitek hospodářská zvířata X zájmová zvířata Zemědělství X chovatelství
Mgr. et Mgr. Lenka Falková Laboratoř agrogenomiky Ústav morfologie, fyziologie a genetiky zvířat Mendelova univerzita 9. 9. 2015 Šlechtění Užitek hospodářská zvířata X zájmová zvířata Zemědělství X chovatelství
Validace sérologických testů výrobcem. Vidia spol. s r.o. Ing. František Konečný IV/2012
 Validace sérologických testů výrobcem Vidia spol. s r.o. Ing. František Konečný IV/2012 Legislativa Zákon č. 123/2000 Sb. o zdravotnických prostředcích ve znění pozdějších předpisů Nařízení vlády č. 453/2004
Validace sérologických testů výrobcem Vidia spol. s r.o. Ing. František Konečný IV/2012 Legislativa Zákon č. 123/2000 Sb. o zdravotnických prostředcích ve znění pozdějších předpisů Nařízení vlády č. 453/2004
Laboratoř sekvenace DNA Servisní laboratoř biologické sekce PřF UK
 Laboratoř sekvenace DNA Založena 2003, momentálně jsme 2 zaměstnankyně, máme dvě spolupracovnice na DPP a jsme finančně soběstačné, včetně platů. Rok Počet sekvenací Počet fragmentací 2009 10 700 8 100
Laboratoř sekvenace DNA Založena 2003, momentálně jsme 2 zaměstnankyně, máme dvě spolupracovnice na DPP a jsme finančně soběstačné, včetně platů. Rok Počet sekvenací Počet fragmentací 2009 10 700 8 100
Seznam vyšetření. Nesrážlivá periferní krev nebo kostní dřeň
 VD.PCE 08 Laboratorní příručka Příloha č. 1: Seznam vyšetření Molekulární hematologie a hematoonkologie Vyšetření mutačního stavu IgV H u CLL Detekce přestavby IgV H u jiných B lymfoproliferací RNA nebo
VD.PCE 08 Laboratorní příručka Příloha č. 1: Seznam vyšetření Molekulární hematologie a hematoonkologie Vyšetření mutačního stavu IgV H u CLL Detekce přestavby IgV H u jiných B lymfoproliferací RNA nebo
