Mendelova Univerzita v Brně Lesnická a dřevařská fakulta
|
|
|
- Přemysl Doležal
- před 9 lety
- Počet zobrazení:
Transkript
1 Mendelova Univerzita v Brně Lesnická a dřevařská fakulta Laboratorní postupy pro zpracování půdních vzorků (schématické postupy pro práci v laboratoři) Obory Lesnictví a Arboristika garant doc. Dr. Ing. Dušan Vavříček vypracoval Ing. Aleš Kučera, Ph.D.
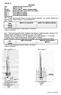
2 Stanovení půdní katalázy: metodický postup Pomůcky: Jankův vápnoměr; analytické váhy s přesností měření min. 0,1 g; hliníková váženka pro odvážení množství vzorku, laboratorní lžička 1. Princip metody je měření produkce O 2 rozkladem H 2 O 2. Základní pomůckou je Jankův vápnoměr. 2. Potřebné reagencie: 3% roztok peroxidu vodíku 3. Navážka: humusové horizonty 5g; minerální horizonty 10g, vždy vzorky čerstvé, s původní vlhkostí, přesáté přes síto s velikostí ok 5 mm. 4. Navážený vzorek vsypeme do vyvíjecí nádoby (viz obr.) a přilijeme 50 ml destilované vody. Množství destilované vody odměřujeme odměrným válcem. 5. Do reakční baňky Jankova vápnoměru (viz obrázek) nalijeme 20 ml 3% H 2 O 2 a vyvíjecí nádobu dobře zazátkujeme zátkou, ve které je umístěna reakční baňka. 6. Trojcestný kohout nastavíme tak, aby mohl z hadice reakční baňky uniknout vzduch ven do místnosti. Po několika sekundách nastavíme trojcestný kohout tak, aby z měrného válce mohl vzduch unikat ven do mísnosti. 7. Zkontrolujeme, je li na stupnici měrného válce hladina vody na hodnotě 0, pokud není, upravíme hladinu vody vhodnou manipulací se zásobní lahví (za uvolněné tlačky na hadici od zásobní lahve) tak, aby voda do válce buď natékala nebo z něj vytékala do zásobní lahve. Hladina vody musí být na hodnotě 0 v obou polovinách měrného válce. 8. Trojcestný kohout nastavíme tak, aby byla spojena hadice vedoucí od vyvíjecí nádoby s prostorem nad hladinou odměrného válce. 9. Poznačíme si aktuální čas a nakloníme uzavřenou vyvíjecí nádobu tak, aby veškerý H 2 O 2 vytekl do půdní suspenze. 10. Obsah vyvíjecí nádoby opatrně krouživým pohybem promísíme. 11. Po 15 min. zaznamenáme výšku hladiny vodního sloupce v měrném válci. V případě intenzivní produkce kyslíku zmírníme tlak v celé soustavě upuštěním vody do zásobní lahve z pravého vyrovnávajícího válce Jankova vápnoměru. 12. Pro udávání výsledků vycházíme z toho, že dílek rovný jedné desetině stupnice (0,1!!!) představuje 5 ml nově produkovaného kyslíku. V případě výchozí navážky 10 g výsledek dělíme dvěma. 13. Výsledek přepočteme na produkci O 2 za 15 min na 5 g sušiny půdního vzorku. 14. Vyhodnocení viz tabulka 39 Metodických postupů Hodnocení lesních půd podle aktivity půdní katalázy [ml O 2. 5g min 1 ] ml g min 1 aktivity půdní katalázy Méně než 5 Velmi slabá 5 15 Slabá Střední Vysoká Více než 60 Velmi vysoká
3
4 Stanovení půdních celuláz: metodický postup Pomůcky: sterilizovaný filtrační papír, 3x petriho misky, skleněná tyčinka, destilovaná voda 1. Nastříháme proužky filtračního papíru do rozměrů 5 x 1 cm. 2. Do Petriho misky vsypeme půdní vzorek s původní vlhkostí a laboratorní lžičkou jej rovnoměrně rozprostřeme v přibližně 5 mm silné vrstvě 3. Na vzorek položíme 3 proužky filtračního papíru. K jejich dokonalému přilnutí k povrchu půdního vzorku proužky jemně přitlačíme skleněnou tyčinkou. Je li vzorek tak suchý, že filtrační papír nesmáčí, opatrně jej navlhčíme destilovanou vodou pomocí střičky. 4. Označíme víčko i boky Petriho misky lihovým fixem a uzavřenou Petriho misku dáme k inkubaci. 5. Každý sudý týden (vždy při dalším laboratorním cvičení) pomocí střičky vzorek opatrně provlhčíme destilovanou vodou. 6. V určitý den (6 týdnů od založení měření) stanovíme procento úbytku celulózy. Do výpočtu zahrnujeme pouze plochu zcela rozložené celulózy. Při kolonizaci půdními houbami celulóza zcela zmizí nebo je zakryta mycelii jednotlivých druhů mikromycet. Při kolonizaci bakteriemi a aktinomycetami zůstává na povrchu vzorku sliznatá, mokvavá vrstvička. Částečně rozložená celulóza indikuje neukončený rozklad a do výpočtu se nezahrnuje. 7. K zjištění přesného procenta úbytku použijeme rastr 5 x 1 cm rozdělený na 20 stejných políček 5 x 5 mm. Každé políčko představuje 5% plochy proužku. 8. Kvantifikaci ukončeného rozkladu celulózy provedeme u všech tří jednotlivých papírků 9. Z daných tří hodnot spočítáme aritmetický průměr. Kde: Výpočet: A = P/T A míra aktivity půdních celuláz, P aritmetický průměr úbytků celulózy (procento úbytku plochy) T doba inkubace v týdnech Hodnocení lesních půd podle aktivity půdních celuláz A aktivity půdních celuláz 0 Žádná 0 1 Velmi slabá 1 2 Slabá 2 5 Střední 5 10 Vysoká > 10 Velmi vysoká
5 Stanovení sušiny: metodický postup Pomůcky: hliníková vysoušečka; analytické váhy; laboratorní lžička, exsikátor 1. Zvážíme prázdnou vysoušečku, zaznamenáme číslo misky (zpravidla vyražené z dolní strany misky na dně). 2. Do hliníkové vysoušecí misky se vloží vzorek s původní vlhkostí. V případě horizontu měli Oh se vkládá přibližně 3 5 g vzorku, v případě humusového A horizontu ± 5 g a v případě podpovrchových a substrátových horizontů 8 10 g; 3. Vzorky ve vysoušečce se zváží na analytických vahách s nejvyšší dosažitelnou přesností; 4. Vzorky se suší při teplotě 105 C po dobu 2 3 hodin; 5. Vysoušečka se vzorkem se vyjme ze sušárny; 6. Po zchladnutí v exsikátoru se vzorek v zavíčkované vysoušečce zváží. Výpočet množství sušiny a obsahu vody ve vzorku: s = [(m 2 m 0 )/(m 1 m 0 )]. 100 [%] w = [(m 1 m 2 )/(m 1 m 0 )]. 100 [%] kde: s: hmotnostní podíl sušiny ve vzorku w: hmotnostní vlhkost pro chemickou analýzu m 0 : hmotnost prázdné vysoušečky v g m 1 : hmotnost vysoušečky se vzorkem před vysušením v g m 2 : hmotnost vysoušečky se vzorkem po vysušení v g
6 Stanovení hydrofyzikálních vlastností půdy: metodický postup Pomůcky: fyzikální váleček s víčky; analytické váhy; nasávací zařízení; hodinové sklo; filtrační papír Postup analýzy fyzikálního válečku: Poznámka: Veškerá vážení provádíme vždy na stejných vahách! Fyzikální váleček je předem zvážený z prvního cvičení předmětu pedologie a jeho hmotnost je zaznamenána 1. Z řádně odebraného fyzikálního válečku sejmeme nejprve spodní víčko, a na jeho místo přiložíme suchý filtrační papír. Poté váleček i s papírem otočíme a sejmeme i druhé víčko. 2. Váleček s čerstvým vzorkem bez víček zvážíme na analytických vahách. A hodnotu zaznamenáme. 3. Zvážený váleček i s filtračním papírem umístíme na nasávací zařízení (plechová vanička s vodou a s dřevem obaleným filtračním papírem). 4. Váleček přikryjeme hodinovým sklem a necháme nasávat vodu do druhého dne. 5. Druhý den si připravíme tři suché filtrační papíry (pozn.: po nasávání by vzorek ve válečku měl mít lesklý povrch). 6. Po hodině odsávání váleček umístíme i s původním filtračním papírem na nové tři suché filtrační papíry a opět přikryjeme hodinovým sklem. 7. Po druhé hodině odsávání fyzikální váleček i s původním filtračním papírem (bez hodinového skla) zvážíme. Tuto hodnotu zaznamenáme. 8. Váleček umístíme i s původním filtračním papírem do sušárny a necháme sušit. Při příštím cvičení zvážíme váleček s vysušeným půdním vzorkem a s původním filtračním papírem. 9. Fyzikální váleček vysypeme a očistíme, aby byl připraven k dalšímu použití. Výpočet hodnot hydrofyzikálních vlastností: maximální kapilární kapacita Θ MKK, měrná hmotnost ρ s, objemová hmotnost ρ w, objemová hmotnost redukovaná ρ d, pórovitost P, hmotností vlhkost w, objemová vlhkost Θ, provzdušněnost (okamžitá) A, minimální vzdušná kapacita A MKK, nasycenost půdních pórů R NP : Viz Laboratorní postupy při zjišťování půdních vlastností analýzy prováděné v rámci pedologického praktika ( materialy ke stazeni/):
7 Výpočet objemové hmotnosti ρw ρw = (b a)/v [g.cm 3 ] kde b hmotnost válečku s neporušeným vzorkem v původním stavu, a hmotnost válečku s víčky a V objem vzorku. Výpočet objemové hmotnosti redukované ρd ρd = (c a)/v [g.cm 3 ] kde c hmotnost válečku se vzorkem vysušeným do konstantní hmotnosti, a hmotnost válečku s víčky a V objem vzorku.
8 Stanovení měrné hmotnosti: metodický postup pozn.: všechna vážený provádíme na stejných vahách z důvodu možných rozdílů v kalibraci vah. pomůcky: Gay Lussacův pyknometr se zátkou; analytické váhy; střička s destilovanou vodou; malá nálevka; drátek; vařič; 1. Základní pomůckou je čistý Gay Lussacův očíslovaný pyknometr s příslušnou zátkou se stejným číslem. Číslo je potřeba nezaměnit a hlídat vždy příslušnou zátku k příslušnému pyknometru. 2. Pyknometr naplníme destilovanou vodou po okraj, aby voda svým meniskem přesahovala kraj hrdla. 3. Pyknometr uzavřeme tak, že krouživým pohybem zátku zasuneme, aby voda prostříkla podélnou kapilárou zátky a v pyknometru ani v zátce nezbyl žádný vzduch. 4. Pyknometr po povrchu osušíme a zvážíme. 5. Pyknometru vyprázdníme a umístíme na váhu. Do hrdla vložíme malou nálevku a vynulujeme hodnotu váhy (značkou tare nebo zero ). Poté pomocí lžičky, nálevky a drátku vpravíme do pyknometru půdní vzorek ve formě jemnozemě I vysušený do konstantní hmotnosti. Přesnou hodnotu navážky zaznamenáme. Přibližná hodnota navážky by se měla pohybovat mezi cca 8 15 g. 6. Pyknometr naplníme asi z 1/4 až 1/3 vodou a umístíme na plotnu, kde vzorek zahříváme do varu. Při zahřívání je nutno dbát na nevykypění obsahu pyknometru. Suspenzi vaříme cca min, až na hladině neplave žádná část půdního vzorku. 7. Pyknometr necháme vychladnout na pokojovou teplotu, doplníme destilovanou vodou a zazátkujeme stejným způsobem jako při prvním vážení. 8. Pyknometr se vzorkem a s vodou vážíme. Výpočet: ρ s = m 1 /(m 1 + m 2 m 3 ) [g.cm 3 ] kde m 1 hmotnost vzorku vysušeného do konstantní hmotnosti (navážka vzatá ke stanovení), m 2 hmotnost pyknometru s destilovanou vodou a m 3 hmotnost pyknometru s rozvařeným vzorkem a s destilovanou vodou.
9 Stanovení procentického podílu humusových látek (ztráta žíháním): metodický postup pozn.: tato metoda patří v současnosti k metodám orientačním, její výhodou je rychlost, nenáročnost a jednoduchá interpretovatelnost. pomůcky: tyglík; laboratorní lžička; muflová pec; analytické váhy; kovové kleště; exsikátor 1. Vzorek jemnozemě I vysušený do konstantní hmotnosti nasypeme do předem zváženého a očíslovaného tyglíku, a to přibližně do ½ 2/3 jeho výšky. Přesnou hodnotu navážky zaznamenáme. 2. Tyglík se vzorkem vložíme do muflovací pece s nastavenou teplotou 550 C. 3. Po dosažení teploty necháme vzorek v muflovací peci po dobu 30 min. 4. Po vyžíhání se vzorek z vnitřního prostoru muflovací pece vyjme kovovými kleštěmi a vloží do exsikátoru. Po vychladnutí se tyglík opět zváží. Výpočet: y = (m1 m2)/m1 * 100 [% kde m 1 hmotnost vzorku vysušeného do konstantní hmotnosti a m 2 hmotnost vzorku po vyžíhání. Vyhodnocení: Humus (%) Půdní horizont Méně než 1 Velmi slabě humózní 1 2 Slabě humózní 2 5 Humózní 5 20 Silně humózní Více než 20 Velmi silně humózní
10 Stanovení půdní acidity aktivní a potenciálně výměnné: metodický postup pomůcky: 2x kádinka o objemu 50 ml; 2x míchací tyčinka; odměrný válec 25 ml; ph metr; laboratorní lžička; analytické váhy reagencie: destilovaná voda KCl 1M 1. Do dvou kádinek navážíme 10 g jemnozemě I, jednu kádinku označíme lihovým fixem značkou ph/h 2 O, druhou ph/kcl. 2. Do kádinky se značkou ph/h 2 O přilijeme 25 ml destilované vody (odměříme pipetou), suspenzi zamícháme skleněnou tyčinkou a necháme dvě hodiny odstát. Obsah občas zamícháme. 3. Do kádinky se značkou ph/kcl přilijeme 25 ml 1 mol KCl, obsah zamícháme a necháme odstát minimálně dvě hodiny (pozn.: metodický postup udává odstát do druhého dne, ale z důvodu časové omezenosti v rámci cvičení tento metodický krok nebudeme provádět. Suspenze se nechá odstát do konce laboratorního cvičení, kdy se provede měření jako poslední úkon). 4. Po dvou hodinách vložíme do suspenze vzorku vodou elektrodu ph metru a po ustálení hodnoty na displeji zapíšeme hodnotu jako ph/h 2 O. Měření se provádí na zkalibrovaném ph metru (kalibraci provádí vyučující nebo laboratorní asistent); vlastní proměření vzorku provádí vyučující nebo laboratorní asistent. 5. Před koncem cvičení vložíme do suspenze vzorku s KCl elektrodu ph metru a po ustálení hodnoty na displeji zapíšeme hodnotu jako ph/kcl. Vyhodnocení: PH/KCl PH/H2O Typ reakce Více než 7,0 Více než 7,2 Mírně alkalická 6,1 7,0 6,6 7,2 Neutrální 5,1 6,0 5,6 6,5 Mírně kyselá 4,1 5,0 4,5 5,5 Středně kyselá 3,0 4,0 3,5 4,4 Silně kyselá Méně než 3,0 Méně než 3,5 Velmi silně kyselá
11 Stanovení sorpčních vlastností půdy: metodický postup pozn.: Sorpční vlastnosti sestávají z několika dílčích veličin, z nichž některé zjišťujeme laboratorním stanovením (hydrolytická acidita, obsah výměnných bazí) a některé výpočtem (kationtová výměnná kapacita, stupeň nasycenosti sorpčního komplexu bazickými kationty) Stanovení hydrolytické acidity (Ha): Pomůcky: PE vzorkovnice se závitem; váženka na odvážení vzorků; laboratorní lžička; třepací zařízení; filtrační souprava (nálevka, filtrační papír, kádinka min. 50 ml, ocelový kruh a stojan); byreta 50 n. 100 ml s nálevkou pro nalévání NaOH do byrety; erlen mayerova baňka; pipeta 50 ml nedělená s nasávacím zařízením Potřebné reagencie: 1 mol roztok octanu sodného (CH 3 COONa) 1 % roztok fenolftaleinu (acidobazický indikátor) 0,1 mol roztok NaOH 1. Do PE vzorkovnice o obsahu 250 ml navážíme 20 g vzorku upraveného ve formě jemnozemě I. 2. Přilijeme 50 ml CH 3 COONa (množství odměříme odměrným válcem), vzorkovnici zazátkujeme a necháme na třepačce třepat 1 h. 3. Připravíme si filtrační soupravu (kádinka min. 100 ml, nálevka, ocelový kruh a stojan, filtrační papír). 4. Po hodině třepání suspenzi přefiltrujeme. 5. Z filtrátu odebereme pipetou 25 ml do erlen mayerovy baňky (o obsahu 100 ml). 6. Přidáme 2 3 kapky fenolftaleinu a titrujeme 0,1 mol roztokem NaOH do slabě růžového zbarvení. 7. Povedeme výpočet hodnoty Ha kde: a... spotřebované množství NaOH k titraci [ml] c(naoh)... koncentrace NaOH (0,1) přepočet na 1000 g zeminy K... korekce na octan sodný (1,75) [mmol.kg 1 ] g... navážka vzatá ke stanovení [g]. V případě, že filtrátu ke stanovení bereme 25 ml, tj. ½ z původní navážky (abychom stanovovali hodnotu S pro celý vzorek, museli bychom z filtrátu odebrat 50 ml, což není možné kvůli ztrátám část roztoku zůstane ve filtračním papíře, část v zemině), g je rovno polovině původní navážky a do jmenovatele tedy dosadíme hodnotu 2,5 (g/2)! f... faktor NaOH
12 Stanovení obsahu výměnných bazí (S): Pomůcky: PE vzorkovnice se závitem; váženka na odvážení vzorků; laboratorní lžička; třepací zařízení; filtrační souprava (nálevka, filtrační papír, kádinka min. 50 ml, ocelový kruh a stojan); byreta 50 n. 100 ml s nálevkou pro nalévání NaOH do byrety; erlen mayerova baňka; pipeta 250 ml nedělená s nasávacím zařízením Potřebné reagencie: 0,1 mol HCl 0,1 mol NaOH 1% roztok fenolftaleinu (acidobazický indikátor) 1. Do PE vzorkovnice o obsahu 250 ml navážíme 5 g vzorku upraveného ve formě jemnozemě I. 2. Přilijeme 50 ml HCl (množství odměříme odměrným válcem), vzorkovnici zazátkujeme a necháme na třepačce třepat 1 h. 3. Připravíme si filtrační soupravu (kádinka min. 100 ml, nálevka, ocelový kruh a stojan, filtrační papír). 4. Po hodině třepání suspenzi přefiltrujeme. 5. Z filtrátu odebereme pipetou 25 ml do erlen mayerovy baňky (o obsahu 250 ml). 6. Přidáme 2 3 kapky fenolftaleinu a titrujeme 0,1 mol roztokem NaOH do slabě růžového zbarvení. 7. Povedeme výpočet hodnoty S [mmol.kg 1 ] kde: a... množství HCl spotřebovaného ke stanovení [ml] f1... faktor HCl (f1 = 1) b... množství NaOH spotřebovaného k titraci [ml] f2... faktor NaOH M... molarita roztoků g... navážka půdy ke stanovení. V případě, že filtrátu ke stanovení bereme 25 ml, tj. ½ z původní navážky (abychom stanovovali hodnotu S pro celý vzorek, museli bychom z filtrátu odebrat 50 ml, což není možné kvůli ztrátám část roztoku zůstane ve filtračním papíře, část v zemině), g je rovno polovině původní navážky a do jmenovatele tedy dosadíme hodnotu 2,5 (g/2)!
13 Výpočet ostatních veličin půdní sorpce: T = Ha + S [mmol. kg 1] kde: T = kationtová výměnná kapacita Ha = hydrolytická acidita S = obsah výměnných bazí V = S T.100 [%] kde: V = stupeň nasycenosti sorpčního komplexu bazickými kationty Vyhodnocení: Hodnocení stupně nasycení sorpčního komplexu lesních půd bazickými kationty V (%) Stupeň nasycení bazickými kationy Více než 90 Plně nasycená Vysoce nasycená Nasycená Mírně nasycená Vysoce nenasycená méně než 10 Extrémně nenasycená Hodnocení maximální sorpční kapacity výměnných bazických kationů lesních půd T (mmol.1000 g 1) Sorpční kapacita Více než 350 Velmi vysoká Vysoká Střední Nízká Méně než 80 Velmi nízká Hodnocení okamžitého obsahu výměnných bazických kationů lesních půd S (mmol.1000g 1) Obsah výměnných bazických kationů Více než 315 Velmi vysoký Vysoký Střední Nízký Méně než 25 Velmi nízký
Nadaní žáci Pracovní sešit. Půda a krajina Půdní vlastnosti II.
 Poznámky: Nadaní žáci 2017 Pracovní sešit Půda a krajina Půdní vlastnosti II. Tento pracovní sešit vznikl jako součást vzdělávacího programu, který je realizován díky podpoře dotačního programu MŠMT Podpora
Poznámky: Nadaní žáci 2017 Pracovní sešit Půda a krajina Půdní vlastnosti II. Tento pracovní sešit vznikl jako součást vzdělávacího programu, který je realizován díky podpoře dotačního programu MŠMT Podpora
Nadaní žáci Pracovní sešit. Půda a krajina Půdní vlastnosti I.
 Poznámky: Nadaní žáci 2017 Pracovní sešit Půda a krajina Půdní vlastnosti I. Tento pracovní sešit vznikl jako součást vzdělávacího programu, který je realizován díky podpoře dotačního programu MŠMT Podpora
Poznámky: Nadaní žáci 2017 Pracovní sešit Půda a krajina Půdní vlastnosti I. Tento pracovní sešit vznikl jako součást vzdělávacího programu, který je realizován díky podpoře dotačního programu MŠMT Podpora
1. Stanovení půdní reakce
 1. Stanovení půdní reakce 1.1. Teoretický úvod Půdní reakce je základní fyzikálně-chemická vlastnost půd. Je určována koncentrací vodíkových iontů, které vodných roztocích tvoří kationty H 3 O +. Koncentrace
1. Stanovení půdní reakce 1.1. Teoretický úvod Půdní reakce je základní fyzikálně-chemická vlastnost půd. Je určována koncentrací vodíkových iontů, které vodných roztocích tvoří kationty H 3 O +. Koncentrace
LABORATORNÍ POSTUPY PŘI ZJIŠŤOVÁNÍ PŮDNÍCH VLASTNOSTÍ ANALÝZY PROVÁDĚNÉ V RÁMCI PEDOLOGICKÉHO PRAKTIKA
 LABORATORNÍ POSTUPY PŘI ZJIŠŤOVÁNÍ PŮDNÍCH VLASTNOSTÍ ANALÝZY PROVÁDĚNÉ V RÁMCI PEDOLOGICKÉHO PRAKTIKA V rámci pedologických praktik posluchači provádí analýzy půdních vlastností, jejichž postupy jsou
LABORATORNÍ POSTUPY PŘI ZJIŠŤOVÁNÍ PŮDNÍCH VLASTNOSTÍ ANALÝZY PROVÁDĚNÉ V RÁMCI PEDOLOGICKÉHO PRAKTIKA V rámci pedologických praktik posluchači provádí analýzy půdních vlastností, jejichž postupy jsou
LABORATORNÍ POSTUPY PŘI ZJIŠŤOVÁNÍ PŮDNÍCH VLASTNOSTÍ ANALÝZY PROVÁDĚNÉ V RÁMCI PEDOLOGICKÉHO PRAKTIKA
 LABORATORNÍ POSTUPY PŘI ZJIŠŤOVÁNÍ PŮDNÍCH VLASTNOSTÍ ANALÝZY PROVÁDĚNÉ V RÁMCI PEDOLOGICKÉHO PRAKTIKA V rámci pedologických praktik posluchači provádí analýzy půdních vlastností jejichž postupy jsou níže
LABORATORNÍ POSTUPY PŘI ZJIŠŤOVÁNÍ PŮDNÍCH VLASTNOSTÍ ANALÝZY PROVÁDĚNÉ V RÁMCI PEDOLOGICKÉHO PRAKTIKA V rámci pedologických praktik posluchači provádí analýzy půdních vlastností jejichž postupy jsou níže
Sešit pro laboratorní práci z chemie
 Sešit pro laboratorní práci z chemie téma: Příprava roztoků a měření ph autor: ing. Alena Dvořáková vytvořeno při realizaci projektu: Inovace školního vzdělávacího programu biologie a chemie registrační
Sešit pro laboratorní práci z chemie téma: Příprava roztoků a měření ph autor: ing. Alena Dvořáková vytvořeno při realizaci projektu: Inovace školního vzdělávacího programu biologie a chemie registrační
CHEMIE Pracovní list č.3 žákovská verze Téma: Acidobazická titrace Mgr. Lenka Horutová Student a konkurenceschopnost
 www.projektsako.cz CHEMIE Pracovní list č.3 žákovská verze Téma: Acidobazická titrace Lektor: Projekt: Reg. číslo: Mgr. Lenka Horutová Student a konkurenceschopnost CZ.1.07/1.1.07/03.0075 Teorie: Základem
www.projektsako.cz CHEMIE Pracovní list č.3 žákovská verze Téma: Acidobazická titrace Lektor: Projekt: Reg. číslo: Mgr. Lenka Horutová Student a konkurenceschopnost CZ.1.07/1.1.07/03.0075 Teorie: Základem
Návody pokusů k 2. laboratornímu cvičení Určeno pro žáky ZŠ
 Návody pokusů k 2. laboratornímu cvičení Určeno pro žáky ZŠ Obsah: 3. stanoviště analýza potravin...1 3.1 Škrob v potravinách...1 3.2 Stanovení ph vybraných potravin...2 3.3 Stanovení cukernatosti potravin...3
Návody pokusů k 2. laboratornímu cvičení Určeno pro žáky ZŠ Obsah: 3. stanoviště analýza potravin...1 3.1 Škrob v potravinách...1 3.2 Stanovení ph vybraných potravin...2 3.3 Stanovení cukernatosti potravin...3
NEUTRALIZAČNÍ ODMĚRNÁ ANALÝZA (TITRACE)
 NEUTRALIZAČNÍ ODMĚRNÁ ANALÝZA (TITRACE) Cíle a princip: Stanovit TITR (přesnou koncentraci) odměrného roztoku kyseliny nebo zásady pomocí známé přesné koncentrace již stanoveného odměrného roztoku. Podstatou
NEUTRALIZAČNÍ ODMĚRNÁ ANALÝZA (TITRACE) Cíle a princip: Stanovit TITR (přesnou koncentraci) odměrného roztoku kyseliny nebo zásady pomocí známé přesné koncentrace již stanoveného odměrného roztoku. Podstatou
č.. 6: Tento projekt je spolufinancován Evropským sociálním fondem a Státním rozpočtem ČR InoBio CZ.1.07/2.2.00/28.0018
 Pedologické praktikum - téma č.. 6: Práce v pedologické laboratoři - půdní fyzika Tento projekt je spolufinancován Evropským sociálním fondem a Státním rozpočtem ČR InoBio CZ.1.07/2.2.00/28.0018 Půdní
Pedologické praktikum - téma č.. 6: Práce v pedologické laboratoři - půdní fyzika Tento projekt je spolufinancován Evropským sociálním fondem a Státním rozpočtem ČR InoBio CZ.1.07/2.2.00/28.0018 Půdní
Chelatometrie. Stanovení tvrdosti vody
 Chelatometrie Stanovení tvrdosti vody CHELATOMETRIE Cheláty (vnitřně komplexní sloučeniny; řecky chelé = klepeto) jsou komplexní sloučeniny, kde centrální ion je členem jednoho nebo více vznikajících kruhů.
Chelatometrie Stanovení tvrdosti vody CHELATOMETRIE Cheláty (vnitřně komplexní sloučeniny; řecky chelé = klepeto) jsou komplexní sloučeniny, kde centrální ion je členem jednoho nebo více vznikajících kruhů.
Metodika stanovení kyselinové neutralizační kapacity v pevných odpadech
 Metodika stanovení kyselinové neutralizační kapacity v pevných odpadech 1 Princip Principem zkoušky je stanovení vodného výluhu při různých přídavcích kyseliny dusičné nebo hydroxidu sodného a následné
Metodika stanovení kyselinové neutralizační kapacity v pevných odpadech 1 Princip Principem zkoušky je stanovení vodného výluhu při různých přídavcích kyseliny dusičné nebo hydroxidu sodného a následné
Sorpční charakteristiky půdy stanovení KVK podle Bowera, stanovení hydrolytické acidity, výpočet S,V
 Sorpční charakteristiky půdy stanovení KVK podle Bowera, stanovení hydrolytické acidity, výpočet S,V Sorpční vlastnosti půdy sorpce půdy schopnost půdy zadržovat ve svém sorpčním komplexu prvky a živiny,
Sorpční charakteristiky půdy stanovení KVK podle Bowera, stanovení hydrolytické acidity, výpočet S,V Sorpční vlastnosti půdy sorpce půdy schopnost půdy zadržovat ve svém sorpčním komplexu prvky a živiny,
Praktické ukázky analytických metod ve vinařství
 Praktické ukázky analytických metod ve vinařství Ing. Mojmír Baroň Stanovení v moštu Stanovení ph a veškerých titrovatelných kyselin Stanovení ph Princip: Hodnota ph je záporný dekadický logaritmus aktivity
Praktické ukázky analytických metod ve vinařství Ing. Mojmír Baroň Stanovení v moštu Stanovení ph a veškerých titrovatelných kyselin Stanovení ph Princip: Hodnota ph je záporný dekadický logaritmus aktivity
Vážení, odměřování objemů
 Vážení, odměřování objemů Vážení K nezbytnému vybavení každé laboratoře patří váhy, pomocí kterých určujeme množství dané látky. Princip vážení je znám po staletí. Jde o srovnávací metodu, kdy se srovnává
Vážení, odměřování objemů Vážení K nezbytnému vybavení každé laboratoře patří váhy, pomocí kterých určujeme množství dané látky. Princip vážení je znám po staletí. Jde o srovnávací metodu, kdy se srovnává
Tento projekt je spolufinancován Evropským sociálním fondem a Státním rozpočtem ČR InoBio CZ.1.07/2.2.00/28.0018
 Tento projekt je spolufinancován Evropským sociálním fondem a Státním rozpočtem ČR InoBio CZ.1.07/2.2.00/28.0018 METODY ZJIŠŤOVÁNÍ KVALITY SUBSTRÁTŮ PRO PĚSTOVÁNÍ SADEBNÍHO MATERIÁLU LESNÍCH DŘEVIN (pomocný
Tento projekt je spolufinancován Evropským sociálním fondem a Státním rozpočtem ČR InoBio CZ.1.07/2.2.00/28.0018 METODY ZJIŠŤOVÁNÍ KVALITY SUBSTRÁTŮ PRO PĚSTOVÁNÍ SADEBNÍHO MATERIÁLU LESNÍCH DŘEVIN (pomocný
KARBOXYLOVÉ KYSELINY
 LABORATORNÍ PRÁCE Č. 28 KARBOXYLOVÉ KYSELINY PRINCIP Karboxylové kyseliny jsou látky, které ve své molekule obsahují jednu nebo více karboxylových skupin. Odvozují se od nich dva typy derivátů, substituční
LABORATORNÍ PRÁCE Č. 28 KARBOXYLOVÉ KYSELINY PRINCIP Karboxylové kyseliny jsou látky, které ve své molekule obsahují jednu nebo více karboxylových skupin. Odvozují se od nich dva typy derivátů, substituční
Název: Acidobazické indikátory
 Název: Acidobazické indikátory Autor: Mgr. Jiří Vozka, Ph.D. Název školy: Gymnázium Jana Nerudy, škola hl. města Prahy Předmět, mezipředmětové vztahy: chemie, biologie, fyzika Ročník: 3. (1. ročník vyššího
Název: Acidobazické indikátory Autor: Mgr. Jiří Vozka, Ph.D. Název školy: Gymnázium Jana Nerudy, škola hl. města Prahy Předmět, mezipředmětové vztahy: chemie, biologie, fyzika Ročník: 3. (1. ročník vyššího
Ústřední komise Chemické olympiády. 55. ročník 2018/2019 ŠKOLNÍ KOLO. Kategorie C ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ)
 Ústřední komise Chemické olympiády 55. ročník 2018/2019 ŠKOLNÍ KOLO Kategorie C ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ) PRAKTICKÁ ČÁST 40 BODŮ Autor RNDr. Jan Břížďala Gymnázium Třebíč RNDr. Jan Havlík, Ph.D.
Ústřední komise Chemické olympiády 55. ročník 2018/2019 ŠKOLNÍ KOLO Kategorie C ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ) PRAKTICKÁ ČÁST 40 BODŮ Autor RNDr. Jan Břížďala Gymnázium Třebíč RNDr. Jan Havlík, Ph.D.
Ústřední komise Chemické olympiády. 55. ročník 2018/2019 KRAJSKÉ KOLO. Kategorie A ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ) Časová náročnost 120 minut
 Ústřední komise Chemické olympiády 55. ročník 2018/2019 KRAJSKÉ KOLO Kategorie A ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ) Časová náročnost 120 minut Úloha 1 Příprava Mohrovy soli 15 bodů Mezi podvojné soli patří
Ústřední komise Chemické olympiády 55. ročník 2018/2019 KRAJSKÉ KOLO Kategorie A ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ) Časová náročnost 120 minut Úloha 1 Příprava Mohrovy soli 15 bodů Mezi podvojné soli patří
I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í
 I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY Laboratorní práce č. 10 Bílkoviny Pro potřeby projektu
I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY Laboratorní práce č. 10 Bílkoviny Pro potřeby projektu
Gymnázium a Střední odborná škola, Rokycany, Mládežníků 1115
 Gymnázium a Střední odborná škola, Rokycany, Mládežníků 1115 Číslo projektu: CZ.1.07/1.5.00/34.0410 Číslo šablony: 19 Název materiálu: Ročník: Identifikace materiálu: Jméno autora: Předmět: Tématický celek:
Gymnázium a Střední odborná škola, Rokycany, Mládežníků 1115 Číslo projektu: CZ.1.07/1.5.00/34.0410 Číslo šablony: 19 Název materiálu: Ročník: Identifikace materiálu: Jméno autora: Předmět: Tématický celek:
Úloha č.2 Vážení. Jméno: Datum provedení: TEORETICKÝ ÚVOD
 Jméno: Obor: Datum provedení: TEORETICKÝ ÚVOD Jednou ze základních operací v biochemické laboratoři je vážení. Ve většině případů právě přesnost a správnost navažovaného množství látky má vliv na výsledek
Jméno: Obor: Datum provedení: TEORETICKÝ ÚVOD Jednou ze základních operací v biochemické laboratoři je vážení. Ve většině případů právě přesnost a správnost navažovaného množství látky má vliv na výsledek
ODMĚRNÁ ANALÝZA - TITRACE
 LABORATORNÍ PRÁCE Č. 35 ODMĚRNÁ ANALÝZA - TITRACE PRINCIP Odměrnou analýzou (titrací) se stanovuje obsah určité složky ve vzorku. Podstatou odměrného stanovení je chemická reakce mezi odměrným roztokem
LABORATORNÍ PRÁCE Č. 35 ODMĚRNÁ ANALÝZA - TITRACE PRINCIP Odměrnou analýzou (titrací) se stanovuje obsah určité složky ve vzorku. Podstatou odměrného stanovení je chemická reakce mezi odměrným roztokem
FYZIKÁLNÍ A CHEMICKÝ ROZBOR PITNÉ VODY
 LABORATORNÍ PRÁCE Č. 13 FYZIKÁLNÍ A CHEMICKÝ ROZBOR PITNÉ VODY PRINCIP V přírodě se vyskytující voda není nikdy čistá, obsahuje vždy určité množství rozpuštěných látek, plynů a nerozpuštěných pevných látek.
LABORATORNÍ PRÁCE Č. 13 FYZIKÁLNÍ A CHEMICKÝ ROZBOR PITNÉ VODY PRINCIP V přírodě se vyskytující voda není nikdy čistá, obsahuje vždy určité množství rozpuštěných látek, plynů a nerozpuštěných pevných látek.
Hydroxidy a indikátory demonstrační
 název typ: zařazení: Pomůcky: Chemikálie: Postup: pozorování rovnice, vysvětlení Hydroxidy a indikátory demonstrační Hydroxidy. Indikátory. 3 zkumavky, kapátko NaOH(C), fenolftalein, lakmus, ph papírek
název typ: zařazení: Pomůcky: Chemikálie: Postup: pozorování rovnice, vysvětlení Hydroxidy a indikátory demonstrační Hydroxidy. Indikátory. 3 zkumavky, kapátko NaOH(C), fenolftalein, lakmus, ph papírek
ÚLOHA 1: Stanovení koncentrace kyseliny ve vzorku potenciometrickou titrací
 UPOZORNĚNÍ V tabulkách pro jednotlivé úlohy jsou uvedeny předpokládané pomůcky, potřebné pro vypracování experimentální části úlohy. Některé pomůcky (lžička, váženka, stopky, elmag. míchadélko, tyčinka
UPOZORNĚNÍ V tabulkách pro jednotlivé úlohy jsou uvedeny předpokládané pomůcky, potřebné pro vypracování experimentální části úlohy. Některé pomůcky (lžička, váženka, stopky, elmag. míchadélko, tyčinka
Sešit pro laboratorní práci z chemie
 Sešit pro laboratorní práci z chemie téma: Příprava oxidu měďnatého autor: ing. Alena Dvořáková vytvořeno při realizaci projektu: Inovace školního vzdělávacího programu biologie a chemie registrační číslo
Sešit pro laboratorní práci z chemie téma: Příprava oxidu měďnatého autor: ing. Alena Dvořáková vytvořeno při realizaci projektu: Inovace školního vzdělávacího programu biologie a chemie registrační číslo
Ústřední komise Chemické olympiády. 55. ročník 2018/2019 ŠKOLNÍ KOLO. Kategorie B ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ)
 Ústřední komise Chemické olympiády 55. ročník 2018/2019 ŠKOLNÍ KOLO Kategorie B ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ) PRAKTICKÁ ČÁST 40 BODŮ Autor Bc. Lukáš Tomaník VŠCHT Praha RNDr. Petr Holzhauser, Ph.D.
Ústřední komise Chemické olympiády 55. ročník 2018/2019 ŠKOLNÍ KOLO Kategorie B ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ) PRAKTICKÁ ČÁST 40 BODŮ Autor Bc. Lukáš Tomaník VŠCHT Praha RNDr. Petr Holzhauser, Ph.D.
č.. 7: Tento projekt je spolufinancován Evropským sociálním fondem a Státním rozpočtem ČR InoBio CZ.1.07/2.2.00/
 Pedologické praktikum - téma č.. 7: Práce v pedologické laboratoři - půdní chemie Tento projekt je spolufinancován Evropským sociálním fondem a Státním rozpočtem ČR InoBio CZ.1.07/2.2.00/28.0018 Půdní
Pedologické praktikum - téma č.. 7: Práce v pedologické laboratoři - půdní chemie Tento projekt je spolufinancován Evropským sociálním fondem a Státním rozpočtem ČR InoBio CZ.1.07/2.2.00/28.0018 Půdní
Speciální botanika (obor-les) Hodnocení přírodních poměrů vybraného území. Floristický soupis
 Speciální botanika (obor-les) Hodnocení přírodních poměrů vybraného území Floristický soupis Obor: lesnictví Ročník: 1. (let. semestr) Vypracoval: Vojtěch Horák Akademický rok: 2012/2013 0 1.Úvod Cílem
Speciální botanika (obor-les) Hodnocení přírodních poměrů vybraného území Floristický soupis Obor: lesnictví Ročník: 1. (let. semestr) Vypracoval: Vojtěch Horák Akademický rok: 2012/2013 0 1.Úvod Cílem
Neutralizační (acidobazické) titrace
 Neutralizační (acidobazické) titrace Neutralizační titrace jsou založeny na reakci mezi kyselinou a zásadou. V podstatě se vždy jedná o reakci iontů H + s ionty OH - podle schematu: H + + OH - H O V průběhu
Neutralizační (acidobazické) titrace Neutralizační titrace jsou založeny na reakci mezi kyselinou a zásadou. V podstatě se vždy jedná o reakci iontů H + s ionty OH - podle schematu: H + + OH - H O V průběhu
53. ročník 2016/2017
 Ústřední komise Chemické olympiády 53. ročník 2016/2017 OKRESNÍ KOLO kategorie D ZADÁNÍ PRAKTICKÉ ČÁSTI časová náročnost: 90 minut Úloha 1 Yamadův univerzální indikátor 30 bodů Úvod Univerzální acidobazické
Ústřední komise Chemické olympiády 53. ročník 2016/2017 OKRESNÍ KOLO kategorie D ZADÁNÍ PRAKTICKÉ ČÁSTI časová náročnost: 90 minut Úloha 1 Yamadův univerzální indikátor 30 bodů Úvod Univerzální acidobazické
Projekt Pospolu. Stanovení jílovitých podílů podle ČSN EN A1 Zkouška s methylenovou modří
 Projekt Pospolu Stanovení jílovitých podílů podle ČSN EN 933-9+A1 Zkouška s methylenovou modří Autorem materiálu a všech jeho částí, není-li uvedeno jinak, je Tomáš Táborský. Jako jedna z hlavních složek
Projekt Pospolu Stanovení jílovitých podílů podle ČSN EN 933-9+A1 Zkouška s methylenovou modří Autorem materiálu a všech jeho částí, není-li uvedeno jinak, je Tomáš Táborský. Jako jedna z hlavních složek
Návod k laboratornímu cvičení. Fenoly
 Návod k laboratornímu cvičení Fenoly Úkol č. 1: Příprava fenolátu sodného Pomůcky: váhy, kádinka, zkumavky Chemikálie: 10% roztok hydroxidu sodného NaOH (C), 5%roztok kyseliny chlorovodíkové HCl (C, X
Návod k laboratornímu cvičení Fenoly Úkol č. 1: Příprava fenolátu sodného Pomůcky: váhy, kádinka, zkumavky Chemikálie: 10% roztok hydroxidu sodného NaOH (C), 5%roztok kyseliny chlorovodíkové HCl (C, X
Návod k laboratornímu cvičení. Bílkoviny
 Úkol č. 1: Důkazy bílkovin ve vaječném bílku a) natvrdo uvařené vejce s kyselinou dusičnou Pomůcky: Petriho miska, pipeta, nůž. Návod k laboratornímu cvičení Bílkoviny Chemikálie: koncentrovaná kyselina
Úkol č. 1: Důkazy bílkovin ve vaječném bílku a) natvrdo uvařené vejce s kyselinou dusičnou Pomůcky: Petriho miska, pipeta, nůž. Návod k laboratornímu cvičení Bílkoviny Chemikálie: koncentrovaná kyselina
LABORATORNÍ STANOVENÍ SÍRANŮ VE VODNÉM ROZTOKU
 LABORATORNÍ STANOVENÍ SÍRANŮ VE VODNÉM ROZTOKU Cílem práce je stanovit koncentraci síranů v neznámém vzorku postupem A, B a C a porovnat jednotlivé metody mezi sebou. Protokol musí osahovat veškeré výpočty
LABORATORNÍ STANOVENÍ SÍRANŮ VE VODNÉM ROZTOKU Cílem práce je stanovit koncentraci síranů v neznámém vzorku postupem A, B a C a porovnat jednotlivé metody mezi sebou. Protokol musí osahovat veškeré výpočty
Ústřední komise Chemické olympiády. 55. ročník 2018/2019 KRAJSKÉ KOLO. Kategorie E ZADÁNÍ PRAKTICKÉ ČÁSTI (50 BODŮ)
 Ústřední komise Chemické olympiády 55. ročník 2018/2019 KRAJSKÉ KOLO Kategorie E ZADÁNÍ PRAKTICKÉ ČÁSTI (50 BODŮ) Úloha 1 Stanovení Bi 3+ a Zn 2+ ve směsi 50 bodů Chelatometricky lze stanovit ionty samostatně,
Ústřední komise Chemické olympiády 55. ročník 2018/2019 KRAJSKÉ KOLO Kategorie E ZADÁNÍ PRAKTICKÉ ČÁSTI (50 BODŮ) Úloha 1 Stanovení Bi 3+ a Zn 2+ ve směsi 50 bodů Chelatometricky lze stanovit ionty samostatně,
Ústřední komise Chemické olympiády. 53. ročník 2016/2017. KRAJSKÉ KOLO kategorie C. ŘEŠENÍ PRAKTICKÉ ČÁSTI (40 bodů) časová náročnost: 120 minut
 Ústřední komise Chemické olympiády 53. ročník 2016/2017 KRAJSKÉ KOLO kategorie C ŘEŠENÍ PRAKTICKÉ ČÁSTI (40 bodů) časová náročnost: 120 minut Úloha 1 Rychlá příprava mědi 20 bodů 1. Fe + CuSO 4 Cu + FeSO
Ústřední komise Chemické olympiády 53. ročník 2016/2017 KRAJSKÉ KOLO kategorie C ŘEŠENÍ PRAKTICKÉ ČÁSTI (40 bodů) časová náročnost: 120 minut Úloha 1 Rychlá příprava mědi 20 bodů 1. Fe + CuSO 4 Cu + FeSO
Termochemie. Úkol: A. Určete změnu teploty při rozpouštění hydroxidu sodného B. Určete reakční teplo reakce zinku s roztokem měďnaté soli
 1. Termochemie Úkol: Určete změnu teploty při rozpouštění hydroxidu sodného B. Určete reakční teplo reakce zinku s roztokem měďnaté soli Pomůcky : a) kádinky, teploměr, odměrný válec, váženka, váhy, kalorimetr,
1. Termochemie Úkol: Určete změnu teploty při rozpouštění hydroxidu sodného B. Určete reakční teplo reakce zinku s roztokem měďnaté soli Pomůcky : a) kádinky, teploměr, odměrný válec, váženka, váhy, kalorimetr,
Laboratorní cvičení z kinetiky chemických reakcí
 Laboratorní cvičení z kinetiky chemických reakcí LABORATORNÍ CVIČENÍ 1. Téma: Ovlivňování průběhu reakce změnou koncentrace látek. podmínek průběhu reakce. Jednou z nich je změna koncentrace výchozích
Laboratorní cvičení z kinetiky chemických reakcí LABORATORNÍ CVIČENÍ 1. Téma: Ovlivňování průběhu reakce změnou koncentrace látek. podmínek průběhu reakce. Jednou z nich je změna koncentrace výchozích
13/sv. 8 (85/503/EHS) Tato směrnice je určena členským státům.
 62 31985L0503 L 308/12 ÚŘEDNÍ VĚSTNÍK EVROPSKÝCH SPOLEČENSTVÍ 20.11.1985 PRVNÍ SMĚRNICE KOMISE ze dne 25. října 1985 o metodách pro analýzu potravinářských kaseinů a kaseinátů (85/503/EHS) KOMISE EVROPSKÝCH
62 31985L0503 L 308/12 ÚŘEDNÍ VĚSTNÍK EVROPSKÝCH SPOLEČENSTVÍ 20.11.1985 PRVNÍ SMĚRNICE KOMISE ze dne 25. října 1985 o metodách pro analýzu potravinářských kaseinů a kaseinátů (85/503/EHS) KOMISE EVROPSKÝCH
1. Cvičení Fyzikální vlastnosti půdy
 1. Cvičení Fyzikální vlastnosti půdy Pedologie v tropech Ing. Petra Hubová hubova@af.czu.cz č.dv. 234 Porušený x neporušený půdní vzorek Odběr neporušeného půdního vzorku Rozbor neporušeného půdního vzorku
1. Cvičení Fyzikální vlastnosti půdy Pedologie v tropech Ing. Petra Hubová hubova@af.czu.cz č.dv. 234 Porušený x neporušený půdní vzorek Odběr neporušeného půdního vzorku Rozbor neporušeného půdního vzorku
Stanovení izoelektrického bodu kaseinu
 Stanovení izoelektrického bodu kaseinu Shlukování koloidních částic do větších celků makroskopických rozměrů nazýváme koagulací. Ke koagulaci koloidních roztoků bílkovin dochází porušením solvatačního
Stanovení izoelektrického bodu kaseinu Shlukování koloidních částic do větších celků makroskopických rozměrů nazýváme koagulací. Ke koagulaci koloidních roztoků bílkovin dochází porušením solvatačního
Vodík, kyslík a jejich sloučeniny
 I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY Laboratorní práce č. 8 Vodík, kyslík a jejich sloučeniny
I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY Laboratorní práce č. 8 Vodík, kyslík a jejich sloučeniny
Neutralizace kyseliny zásadou
 Neutralizace kyseliny zásadou Metodický list pro učitele Časový harmonogram a) doba na přípravu - 10 minut b) doba na provedení - 15 minut Pomůcky a) chemikálie - kyselina chlorovodíková - hydroxid sodný
Neutralizace kyseliny zásadou Metodický list pro učitele Časový harmonogram a) doba na přípravu - 10 minut b) doba na provedení - 15 minut Pomůcky a) chemikálie - kyselina chlorovodíková - hydroxid sodný
Odměrná analýza, volumetrie
 Odměrná analýza, volumetrie metoda založená na měření objemu metoda absolutní: stanovení analytu ze změřeného objemu roztoku činidla o přesně známé koncentraci, který je zapotřebí k úplné a stechiometricky
Odměrná analýza, volumetrie metoda založená na měření objemu metoda absolutní: stanovení analytu ze změřeného objemu roztoku činidla o přesně známé koncentraci, který je zapotřebí k úplné a stechiometricky
Jazykové gymnázium Pavla Tigrida, Ostrava-Poruba Název projektu: Podpora rozvoje praktické výchovy ve fyzice a chemii
 Datum: Jazykové gymnázium Pavla Tigrida, Ostrava-Poruba Název projektu: Podpora rozvoje praktické výchovy ve fyzice a chemii Laboratorní cvičení č. Tlak vzduchu: Teplota vzduchu: Bílkoviny(proteiny) Vlhkost
Datum: Jazykové gymnázium Pavla Tigrida, Ostrava-Poruba Název projektu: Podpora rozvoje praktické výchovy ve fyzice a chemii Laboratorní cvičení č. Tlak vzduchu: Teplota vzduchu: Bílkoviny(proteiny) Vlhkost
53. ročník 2016/2017
 Ústřední komise Chemické olympiády 53. ročník 2016/2017 OKRESNÍ KOLO kategorie D ŘEŠENÍ PRAKTICKÉ ČÁSTI časová náročnost: 90 minut Úloha 1 Yamadův univerzální indikátor 30 bodů Úkoly: 1. Doplněná Tabulka
Ústřední komise Chemické olympiády 53. ročník 2016/2017 OKRESNÍ KOLO kategorie D ŘEŠENÍ PRAKTICKÉ ČÁSTI časová náročnost: 90 minut Úloha 1 Yamadův univerzální indikátor 30 bodů Úkoly: 1. Doplněná Tabulka
Laboratorní pomůcky, chemické nádobí
 Laboratorní pomůcky, chemické nádobí Laboratorní sklo: měkké (tyčinky, spojovací trubice, kapiláry) tvrdé označení SIMAX (většina varného a odměrného skla) Zahřívání skla: Tenkostěnné nádoby (kádinky,
Laboratorní pomůcky, chemické nádobí Laboratorní sklo: měkké (tyčinky, spojovací trubice, kapiláry) tvrdé označení SIMAX (většina varného a odměrného skla) Zahřívání skla: Tenkostěnné nádoby (kádinky,
Ústřední komise Chemické olympiády. 55. ročník 2018/2019 ŠKOLNÍ KOLO. Kategorie B ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ)
 Ústřední komise Chemické olympiády 55. ročník 2018/2019 ŠKOLNÍ KOLO Kategorie B ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ) PRAKTICKÁ ČÁST 40 BODŮ Autor Bc. Lukáš Tomaník VŠCHT Praha RNDr. Petr Holzhauser, Ph.D.
Ústřední komise Chemické olympiády 55. ročník 2018/2019 ŠKOLNÍ KOLO Kategorie B ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ) PRAKTICKÁ ČÁST 40 BODŮ Autor Bc. Lukáš Tomaník VŠCHT Praha RNDr. Petr Holzhauser, Ph.D.
Ústřední komise Chemické olympiády. 56. ročník 2019/2020 ŠKOLNÍ KOLO. Kategorie A. Praktická část Zadání 40 bodů
 Ústřední komise Chemické olympiády 56. ročník 2019/2020 ŠKOLNÍ KOLO Kategorie A Praktická část Zadání 40 bodů PRAKTICKÁ ČÁST 40 BODŮ Autor Doc. Ing. Petr Exnar, CSc. Technická univerzita v Liberci Recenze
Ústřední komise Chemické olympiády 56. ročník 2019/2020 ŠKOLNÍ KOLO Kategorie A Praktická část Zadání 40 bodů PRAKTICKÁ ČÁST 40 BODŮ Autor Doc. Ing. Petr Exnar, CSc. Technická univerzita v Liberci Recenze
Kurz 1 Úvod k biochemickému praktiku
 Kurz 1 Úvod k biochemickému praktiku Pavla Balínová http://vyuka.lf3.cuni.cz/ Důležité informace Kroužkový asistent: RNDr. Pavla Balínová e-mailová adresa: pavla.balinova@lf3.cuni.cz místnost: 410 studijní
Kurz 1 Úvod k biochemickému praktiku Pavla Balínová http://vyuka.lf3.cuni.cz/ Důležité informace Kroužkový asistent: RNDr. Pavla Balínová e-mailová adresa: pavla.balinova@lf3.cuni.cz místnost: 410 studijní
Termodynamika - určení měrné tepelné kapacity pevné látky
 I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY Laboratorní práce č. 3 Termodynamika - určení měrné
I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY Laboratorní práce č. 3 Termodynamika - určení měrné
I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í LABORATORNÍ PRÁCE Č. 6 PRÁCE S PLYNY
 LABORATORNÍ PRÁCE Č. 6 PRÁCE S PLYNY Mezi nejrozšířenější práce s plyny v laboratoři patří příprava a důkazy oxidu uhličitého CO 2, kyslíku O 2, vodíku H 2, oxidu siřičitého SO 2 a amoniaku NH 3. Reakcí
LABORATORNÍ PRÁCE Č. 6 PRÁCE S PLYNY Mezi nejrozšířenější práce s plyny v laboratoři patří příprava a důkazy oxidu uhličitého CO 2, kyslíku O 2, vodíku H 2, oxidu siřičitého SO 2 a amoniaku NH 3. Reakcí
Ministerstvo školství, mládeže a tělovýchovy Ústřední komise Chemické olympiády. 46. ročník 2009/2010. KRAJSKÉ KOLO kategorie D
 Ministerstvo školství, mládeže a tělovýchovy Ústřední komise Chemické olympiády 46. ročník 2009/2010 KRAJSKÉ KOLO kategorie D ŘEŠENÍ SOUTĚŽNÍCH ÚLOH TEORETICKÁ ČÁST (60 bodů) Úloha 1 Vlastnosti prvků 26
Ministerstvo školství, mládeže a tělovýchovy Ústřední komise Chemické olympiády 46. ročník 2009/2010 KRAJSKÉ KOLO kategorie D ŘEŠENÍ SOUTĚŽNÍCH ÚLOH TEORETICKÁ ČÁST (60 bodů) Úloha 1 Vlastnosti prvků 26
Jednotné pracovní postupy zkoušení krmiv STANOVENÍ OBSAHU MĚDI, ŽELEZA, MANGANU A ZINKU METODOU FAAS
 Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU MĚDI, ŽELEZA, MANGANU A ZINKU METODOU FAAS 1 Účel a rozsah Tato metoda specifikuje podmínky pro stanovení obsahu mědi, manganu, zinku a železa ve
Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU MĚDI, ŽELEZA, MANGANU A ZINKU METODOU FAAS 1 Účel a rozsah Tato metoda specifikuje podmínky pro stanovení obsahu mědi, manganu, zinku a železa ve
I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í LABORATORNÍ PRÁCE Č. 14 SRÁŽECÍ REAKCE
 LABORATORNÍ PRÁCE Č. 14 SRÁŽECÍ REAKCE PRINCIP Srážecí reakce je reakce, při níž se alespoň jeden z produktů vylučuje z reakční směsi ve formě tuhé fáze (sraženiny). A + (aq) + B - (aq) AB (s) (Reakce
LABORATORNÍ PRÁCE Č. 14 SRÁŽECÍ REAKCE PRINCIP Srážecí reakce je reakce, při níž se alespoň jeden z produktů vylučuje z reakční směsi ve formě tuhé fáze (sraženiny). A + (aq) + B - (aq) AB (s) (Reakce
I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í
 I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY Laboratorní práce č. 9 Lipidy Pro potřeby projektu
I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY Laboratorní práce č. 9 Lipidy Pro potřeby projektu
č.. 5: Tento projekt je spolufinancován Evropským sociálním fondem a Státním rozpočtem ČR InoBio CZ.1.07/2.2.00/
 Pedologické praktikum - téma č.. 5: Práce v pedologické laboratoři - pravidla práce, bezpečnost práce, udávání výsledků analýz Tento projekt je spolufinancován Evropským sociálním fondem a Státním rozpočtem
Pedologické praktikum - téma č.. 5: Práce v pedologické laboratoři - pravidla práce, bezpečnost práce, udávání výsledků analýz Tento projekt je spolufinancován Evropským sociálním fondem a Státním rozpočtem
Ústřední komise Chemické olympiády. 55. ročník 2018/2019 NÁRODNÍ KOLO. Kategorie E. Zadání praktické části Úloha 2 (30 bodů)
 Ústřední komise Chemické olympiády 55. ročník 2018/2019 NÁRODNÍ KOLO Kategorie E Zadání praktické části Úloha 2 (30 bodů) PRAKTICKÁ ČÁST 30 BODŮ Úloha 2 Stanovení Cu 2+ spektrofotometricky 30 bodů Cu 2+
Ústřední komise Chemické olympiády 55. ročník 2018/2019 NÁRODNÍ KOLO Kategorie E Zadání praktické části Úloha 2 (30 bodů) PRAKTICKÁ ČÁST 30 BODŮ Úloha 2 Stanovení Cu 2+ spektrofotometricky 30 bodů Cu 2+
Ústřední komise Chemické olympiády. 55. ročník 2018/2019 NÁRODNÍ KOLO. Kategorie E. Zadání praktické části Úloha 1 (20 bodů)
 Ústřední komise Chemické olympiády 55. ročník 2018/2019 NÁRODNÍ KOLO Kategorie E Zadání praktické části Úloha 1 (20 bodů) PRAKTICKÁ ČÁST 20 BODŮ Úloha 1 Stanovení Ni 2+ a Ca 2+ ve směsi konduktometricky
Ústřední komise Chemické olympiády 55. ročník 2018/2019 NÁRODNÍ KOLO Kategorie E Zadání praktické části Úloha 1 (20 bodů) PRAKTICKÁ ČÁST 20 BODŮ Úloha 1 Stanovení Ni 2+ a Ca 2+ ve směsi konduktometricky
Ústřední komise Chemické olympiády. 53. ročník 2016/2017. KRAJSKÉ KOLO kategorie C. ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ) časová náročnost: 120 minut
 Ústřední komise Chemické olympiády 53. ročník 2016/2017 KRAJSKÉ KOLO kategorie C ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ) časová náročnost: 120 minut Zadání praktické části krajského kola ChO kat. C 2016/2017
Ústřední komise Chemické olympiády 53. ročník 2016/2017 KRAJSKÉ KOLO kategorie C ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ) časová náročnost: 120 minut Zadání praktické části krajského kola ChO kat. C 2016/2017
Návod k laboratornímu cvičení. Oddělování složek směsí I
 Návod k laboratornímu cvičení Oddělování složek směsí I Úkol č. 1: Usazování Pomůcky: dělící nálevka, držák, svorka, stojan, kádinka Chemikálie: voda, potravinářské barvivo, olej 1. Dělící nálevku upevníme
Návod k laboratornímu cvičení Oddělování složek směsí I Úkol č. 1: Usazování Pomůcky: dělící nálevka, držák, svorka, stojan, kádinka Chemikálie: voda, potravinářské barvivo, olej 1. Dělící nálevku upevníme
Jazykové gymnázium Pavla Tigrida, Ostrava-Poruba Název projektu: Podpora rozvoje praktické výchovy ve fyzice a chemii
 Datum: Jazykové gymnázium Pavla Tigrida, Ostrava-Poruba Název projektu: Podpora rozvoje praktické výchovy ve fyzice a chemii Tlak vzduchu: Teplota vzduchu: Laboratorní cvičení č. Oddělování složek směsí
Datum: Jazykové gymnázium Pavla Tigrida, Ostrava-Poruba Název projektu: Podpora rozvoje praktické výchovy ve fyzice a chemii Tlak vzduchu: Teplota vzduchu: Laboratorní cvičení č. Oddělování složek směsí
látka Obr. k úkolům 1 a 2 Obr. k úkolu 3
 cvičení: A Téma: Základní vlastnosti organických látek Cíl: Teplota varu a tání Pomůcky: žákovská souprava, teploměr, skleněná trubička, Chemikálie: ethanol CH 3 CH 2 OH, aceton CH 3 COCH 3, naftalen Úkol
cvičení: A Téma: Základní vlastnosti organických látek Cíl: Teplota varu a tání Pomůcky: žákovská souprava, teploměr, skleněná trubička, Chemikálie: ethanol CH 3 CH 2 OH, aceton CH 3 COCH 3, naftalen Úkol
Jazykové gymnázium Pavla Tigrida, Ostrava-Poruba Název projektu: Podpora rozvoje praktické výchovy ve fyzice a chemii
 Datum: Jazykové gymnázium Pavla Tigrida, Ostrava-Poruba Název projektu: Podpora rozvoje praktické výchovy ve fyzice a chemii Laboratorní cvičení č. Tlak vzduchu: Teplota vzduchu: Vodík a kyslík Vlhkost
Datum: Jazykové gymnázium Pavla Tigrida, Ostrava-Poruba Název projektu: Podpora rozvoje praktické výchovy ve fyzice a chemii Laboratorní cvičení č. Tlak vzduchu: Teplota vzduchu: Vodík a kyslík Vlhkost
I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í
 I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY Laboratorní práce č. 8 Sacharidy Pro potřeby projektu
I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY Laboratorní práce č. 8 Sacharidy Pro potřeby projektu
Laboratorní cvičení z lékařské chemie II
 Laboratorní cvičení z lékařské chemie II 1. ročník, všeobecné lékařství Ústav lékařské chemie a biochemie Lékařská fakulta v Plzni, Univerzita Karlova Jméno: Potvrzení o účasti na praktikách Studijní skupina:
Laboratorní cvičení z lékařské chemie II 1. ročník, všeobecné lékařství Ústav lékařské chemie a biochemie Lékařská fakulta v Plzni, Univerzita Karlova Jméno: Potvrzení o účasti na praktikách Studijní skupina:
Název: Redoxní titrace - manganometrie
 Název: Redoxní titrace - manganometrie Autor: RNDr. Markéta Bludská Název školy: Gymnázium Jana Nerudy, škola hl. města Prahy Předmět, mezipředmětové vztahy: chemie a její aplikace, matematika Ročník:
Název: Redoxní titrace - manganometrie Autor: RNDr. Markéta Bludská Název školy: Gymnázium Jana Nerudy, škola hl. města Prahy Předmět, mezipředmětové vztahy: chemie a její aplikace, matematika Ročník:
Stanovení kritické micelární koncentrace
 Stanovení kritické micelární koncentrace TEORIE KONDUKTOMETRIE Měrná elektrická vodivost neboli konduktivita je fyzikální veličinou, která popisuje schopnost látek vést elektrický proud. Látky snadno vedoucí
Stanovení kritické micelární koncentrace TEORIE KONDUKTOMETRIE Měrná elektrická vodivost neboli konduktivita je fyzikální veličinou, která popisuje schopnost látek vést elektrický proud. Látky snadno vedoucí
Jednotné pracovní postupy zkoušení krmiv STANOVENÍ OBSAHU 5-VINYL - 2-THIOOXAZOLIDONU (GOITRINU) METODOU GC
 Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU 5-VINYL - 2-THIOOXAZOLIDONU (GOITRINU) METODOU GC 1 Rozsah a účel Metoda specifikuje podmínky pro stanovení vinylthiooxazolidonu (dále VOT) v krmivech.
Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU 5-VINYL - 2-THIOOXAZOLIDONU (GOITRINU) METODOU GC 1 Rozsah a účel Metoda specifikuje podmínky pro stanovení vinylthiooxazolidonu (dále VOT) v krmivech.
STANOVENÍ SIŘIČITANŮ VE VÍNĚ
 STANOVENÍ SIŘIČITANŮ VE VÍNĚ CÍLE ÚLOHY: seznámit se s principy izotachoforézy a jodometrické titrace kvantitativně stanovit siřičitany v bílém víně oběma metodami POUŽITÉ VYBAVENÍ: Chemikálie: ITP 10mM
STANOVENÍ SIŘIČITANŮ VE VÍNĚ CÍLE ÚLOHY: seznámit se s principy izotachoforézy a jodometrické titrace kvantitativně stanovit siřičitany v bílém víně oběma metodami POUŽITÉ VYBAVENÍ: Chemikálie: ITP 10mM
ODDĚLOVÁNÍ SLOŽEK SMĚSÍ, PŘÍPRAVA ROZTOKU URČITÉHO SLOŽENÍ
 ODDĚLOVÁNÍ SLOŽEK SMĚSÍ, PŘÍPRAVA ROZTOKU URČITÉHO SLOŽENÍ PaedDr. Ivana Töpferová Střední průmyslová škola, Mladá Boleslav, Havlíčkova 456 CZ.1.07/1.5.00/34.0861 MODERNIZACE VÝUKY Anotace: laboratorní
ODDĚLOVÁNÍ SLOŽEK SMĚSÍ, PŘÍPRAVA ROZTOKU URČITÉHO SLOŽENÍ PaedDr. Ivana Töpferová Střední průmyslová škola, Mladá Boleslav, Havlíčkova 456 CZ.1.07/1.5.00/34.0861 MODERNIZACE VÝUKY Anotace: laboratorní
Červené zelí a červená řepa jako přírodní indikátory ph
 Zvyšování kvality výuky v přírodních a technických oblastech CZ.1.07/1.128/02.0055 Červené zelí a červená řepa jako přírodní indikátory ph (laboratorní práce) Označení: EU-Inovace-BFCh-Ch-10 Předmět: Biologicko-fyzikálně
Zvyšování kvality výuky v přírodních a technických oblastech CZ.1.07/1.128/02.0055 Červené zelí a červená řepa jako přírodní indikátory ph (laboratorní práce) Označení: EU-Inovace-BFCh-Ch-10 Předmět: Biologicko-fyzikálně
Jednotné pracovní postupy zkoušení krmiv STANOVENÍ OBSAHU VÁPNÍKU MANGANOMETRICKY
 Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU VÁPNÍKU MANGANOMETRICKY 1 Rozsah a účel Tato metoda specifikuje podmínky pro stanovení celkového obsahu vápníku v krmivech, krmných směsích a premixech.
Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU VÁPNÍKU MANGANOMETRICKY 1 Rozsah a účel Tato metoda specifikuje podmínky pro stanovení celkového obsahu vápníku v krmivech, krmných směsích a premixech.
RUŠENÁ KRYSTALIZACE A SUBLIMACE
 LABORATORNÍ PRÁCE Č. 5 RUŠENÁ KRYSTALIZACE A SUBLIMACE KRYSTALIZACE PRINCIP Krystalizace je důležitý postup při získávání čistých tuhých látek z jejich roztoků. Tuhá látka se rozpustí ve vhodném rozpouštědle.
LABORATORNÍ PRÁCE Č. 5 RUŠENÁ KRYSTALIZACE A SUBLIMACE KRYSTALIZACE PRINCIP Krystalizace je důležitý postup při získávání čistých tuhých látek z jejich roztoků. Tuhá látka se rozpustí ve vhodném rozpouštědle.
Návod k laboratornímu cvičení. Alkaloidy a steroidy
 Návod k laboratornímu cvičení Úkol č. 1: Sublimace kofeinu Alkaloidy a steroidy Pomůcky: 2 hodinová sklíčka, elektrický vařič, siťka, stojan s kruhem, filtrační papír Chemikálie: suché čajové lístky (černý,
Návod k laboratornímu cvičení Úkol č. 1: Sublimace kofeinu Alkaloidy a steroidy Pomůcky: 2 hodinová sklíčka, elektrický vařič, siťka, stojan s kruhem, filtrační papír Chemikálie: suché čajové lístky (černý,
UHLOVODÍKY A HALOGENDERIVÁTY
 LABORATORNÍ PRÁCE Č. 25 UHLOVODÍKY A HALOGENDERIVÁTY PRINCIP Uhlovodíky jsou nejjednodušší organické sloučeniny, jejichž molekuly jsou tvořeny pouze uhlíkem a vodíkem. Uhlovodíky klasifikujeme z několika
LABORATORNÍ PRÁCE Č. 25 UHLOVODÍKY A HALOGENDERIVÁTY PRINCIP Uhlovodíky jsou nejjednodušší organické sloučeniny, jejichž molekuly jsou tvořeny pouze uhlíkem a vodíkem. Uhlovodíky klasifikujeme z několika
Vzdušné x Hydraulické
 VÁPNO A STANOVENÍ PH Stavební hmoty I Není vápno jako vápno!!! Vzdušné x Hydraulické Vzdušné vápno Užíváno již od starověku, na našem území od období Velké Moravy (technologický import) Pálené vápno -
VÁPNO A STANOVENÍ PH Stavební hmoty I Není vápno jako vápno!!! Vzdušné x Hydraulické Vzdušné vápno Užíváno již od starověku, na našem území od období Velké Moravy (technologický import) Pálené vápno -
VLHKOST A NASÁKAVOST STAVEBNÍCH MATERIÁLŮ. Stavební hmoty I Cvičení 7
 VLHKOST A NASÁKAVOST STAVEBNÍCH MATERIÁLŮ Stavební hmoty I Cvičení 7 STANOVENÍ VLHKOSTI STAVEBNÍCH MATERIÁLŮ PROTOKOL Č.7 Stanovení vlhkosti stavebních materiálů a výrobků sušením při zvýšené teplotě dle
VLHKOST A NASÁKAVOST STAVEBNÍCH MATERIÁLŮ Stavební hmoty I Cvičení 7 STANOVENÍ VLHKOSTI STAVEBNÍCH MATERIÁLŮ PROTOKOL Č.7 Stanovení vlhkosti stavebních materiálů a výrobků sušením při zvýšené teplotě dle
STANOVENÍ CHLORIDŮ. Odměrné argentometrické stanovení chloridů podle Mohra
 STANOVENÍ CHLORIDŮ Odměrné argentometrické stanovení chloridů podle Mohra Cíl práce Stanovte titr odměrného standardního roztoku dusičnanu stříbrného titrací 5 ml standardního srovnávacího roztoku chloridu
STANOVENÍ CHLORIDŮ Odměrné argentometrické stanovení chloridů podle Mohra Cíl práce Stanovte titr odměrného standardního roztoku dusičnanu stříbrného titrací 5 ml standardního srovnávacího roztoku chloridu
Oddělování složek směsí filtrace pomocí žákovské soupravy pro chemii
 Zvyšování kvality výuky v přírodních a technických oblastech CZ.1.07/1.128/02.0055 Oddělování složek směsí filtrace pomocí žákovské soupravy pro chemii (laboratorní práce) Označení: EU-Inovace-Ch-8-03
Zvyšování kvality výuky v přírodních a technických oblastech CZ.1.07/1.128/02.0055 Oddělování složek směsí filtrace pomocí žákovské soupravy pro chemii (laboratorní práce) Označení: EU-Inovace-Ch-8-03
T É M A: SRÁŽENÍ, GRAVIMETRIE. Spolupracoval/a: ANOTACE: TEORIE: VÁŽKOVÁ ANALÝZA (GRAVIMETRIE)
 SEMINÁŘ STUDENT CHEMIE T É M A: Vypracoval/a: Spolupracoval/a: SRÁŽENÍ, GRAVIMETRIE Třída: Datum: ANOTACE: V této laboratorní práci se žáci seznámí s využití metody srážení v kvantitativní analýze tzv.
SEMINÁŘ STUDENT CHEMIE T É M A: Vypracoval/a: Spolupracoval/a: SRÁŽENÍ, GRAVIMETRIE Třída: Datum: ANOTACE: V této laboratorní práci se žáci seznámí s využití metody srážení v kvantitativní analýze tzv.
Vliv ředění na kyselost/zásaditost roztoků pomocí čidla kyselosti ph
 Zvyšování kvality výuky v přírodních a technických oblastech CZ.1.07/1.1.28/02.0055 Vliv ředění na kyselost/zásaditost roztoků pomocí čidla kyselosti ph (laboratorní práce) Označení: EU-Inovace-Ch-8-11
Zvyšování kvality výuky v přírodních a technických oblastech CZ.1.07/1.1.28/02.0055 Vliv ředění na kyselost/zásaditost roztoků pomocí čidla kyselosti ph (laboratorní práce) Označení: EU-Inovace-Ch-8-11
Dovednosti/Schopnosti. - orientuje se v ČL, který vychází z Evropského lékopisu;
 Jednotka učení 4a: Stanovení obsahu Ibuprofenu 1. diferencování pracovního úkolu Handlungswissen Charakteristika pracovní činnosti Pracovní postup 2. HINTERFRAGEN 3. PŘIŘAZENÍ... Sachwissen Charakteristika
Jednotka učení 4a: Stanovení obsahu Ibuprofenu 1. diferencování pracovního úkolu Handlungswissen Charakteristika pracovní činnosti Pracovní postup 2. HINTERFRAGEN 3. PŘIŘAZENÍ... Sachwissen Charakteristika
Spektrofotometrické stanovení fosforečnanů ve vodách
 Spektrofotometrické stanovení fosforečnanů ve vodách Úkol: Spektrofotometricky stanovte obsah fosforečnanů ve vodě Chemikálie: 0,07165 g dihydrogenfosforečnan draselný KH 2 PO 4 75 ml kyselina sírová H
Spektrofotometrické stanovení fosforečnanů ve vodách Úkol: Spektrofotometricky stanovte obsah fosforečnanů ve vodě Chemikálie: 0,07165 g dihydrogenfosforečnan draselný KH 2 PO 4 75 ml kyselina sírová H
Titrace a odměrné nádobí
 Titrace a odměrné nádobí Titrace patří k nejjednodušším metodám analytické chemie bez nároků na přístrojové vybavení. Dodnes jsou pro jednodušší analýzy využívány v praxi. Klíčové pro správné provádění
Titrace a odměrné nádobí Titrace patří k nejjednodušším metodám analytické chemie bez nároků na přístrojové vybavení. Dodnes jsou pro jednodušší analýzy využívány v praxi. Klíčové pro správné provádění
VÁPNO A STANOVENÍ PH. Stavební hmoty I
 VÁPNO A STANOVENÍ PH Stavební hmoty I Není vápno jako vápno!!! Vzdušné x Hydraulické Vzdušné vápno Užíváno již od starověku, na našem území od období Velké Moravy (technologický import) Pálené vápno -
VÁPNO A STANOVENÍ PH Stavební hmoty I Není vápno jako vápno!!! Vzdušné x Hydraulické Vzdušné vápno Užíváno již od starověku, na našem území od období Velké Moravy (technologický import) Pálené vápno -
Návod k laboratornímu cvičení. Cukry(sacharidy)
 Návod k laboratornímu cvičení Cukry(sacharidy) Úkol č. 1: Odlišení glukosy a fruktosy Pomůcky: zkumavky, lžička na chemikálie, kádinka, stojan, držák, kruh, síťka, plynový kahan, zápalky Chemikálie: fruktosa,
Návod k laboratornímu cvičení Cukry(sacharidy) Úkol č. 1: Odlišení glukosy a fruktosy Pomůcky: zkumavky, lžička na chemikálie, kádinka, stojan, držák, kruh, síťka, plynový kahan, zápalky Chemikálie: fruktosa,
SILNIČNÍ A GEOTECHNICKÁ LABORATOŘ
 Inovace studijního oboru Geotechnika reg. č. CZ.1.07/2.2.00/28.0009 SILNIČNÍ A GEOTECHNICKÁ LABORATOŘ podklady do cvičení PŮDNÍ OBJEMOVÝ DENZITOMETR Ing. Marek Mohyla Místnost: C 315 Telefon: 597 321 362
Inovace studijního oboru Geotechnika reg. č. CZ.1.07/2.2.00/28.0009 SILNIČNÍ A GEOTECHNICKÁ LABORATOŘ podklady do cvičení PŮDNÍ OBJEMOVÝ DENZITOMETR Ing. Marek Mohyla Místnost: C 315 Telefon: 597 321 362
Jednotné pracovní postupy zkoušení krmiv STANOVENÍ OBSAHU KOBALTU METODOU ICP-MS
 Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU KOBALTU METODOU ICP-MS 1 Rozsah a účel Metoda specifikuje podmínky pro stanovení celkového obsahu kobaltu v krmivech metodou hmotnostní spektrometrie
Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU KOBALTU METODOU ICP-MS 1 Rozsah a účel Metoda specifikuje podmínky pro stanovení celkového obsahu kobaltu v krmivech metodou hmotnostní spektrometrie
CZ.1.07/1.1.28/
 Projekt: Zavádění moderních trendů do výuky potravinářské chemie Reg.č.: CZ.1.07/1.1.28/01.0024 Výukový materiál pro obor Analýza potravin ANALYTICKÁ CHEMIE 2. ročník Autor: Ing. Dana Kovaříková V Pardubicích
Projekt: Zavádění moderních trendů do výuky potravinářské chemie Reg.č.: CZ.1.07/1.1.28/01.0024 Výukový materiál pro obor Analýza potravin ANALYTICKÁ CHEMIE 2. ročník Autor: Ing. Dana Kovaříková V Pardubicích
Ústřední komise Chemické olympiády. 50. ročník 2013/2014. OKRESNÍ KOLO kategorie D ŘEŠENÍ SOUTĚŽNÍCH ÚLOH
 Ústřední komise Chemické olympiády 50. ročník 2013/2014 OKRESNÍ KOLO kategorie D ŘEŠENÍ SOUTĚŽNÍCH ÚLOH TEORETICKÁ ČÁST (70 BODŮ) Informace pro hodnotitele Ve výpočtových úlohách jsou uvedeny dílčí výpočty
Ústřední komise Chemické olympiády 50. ročník 2013/2014 OKRESNÍ KOLO kategorie D ŘEŠENÍ SOUTĚŽNÍCH ÚLOH TEORETICKÁ ČÁST (70 BODŮ) Informace pro hodnotitele Ve výpočtových úlohách jsou uvedeny dílčí výpočty
Reakce kyselin a zásad
 seminář 6. 1. 2011 Chemie Reakce kyselin a zásad Známe několik teorií, které charakterizují definují kyseliny a zásady. Nejstarší je Arrheniova teorie, která je platná pro vodné prostředí, podle které
seminář 6. 1. 2011 Chemie Reakce kyselin a zásad Známe několik teorií, které charakterizují definují kyseliny a zásady. Nejstarší je Arrheniova teorie, která je platná pro vodné prostředí, podle které
HYDROXYDERIVÁTY - ALKOHOLY
 LABORATORNÍ PRÁCE Č. 26 HYDROXYDERIVÁTY - ALKOHOLY PRINCIP Hydroxyderiváty jsou kyslíkaté deriváty uhlovodíků, které vznikají náhradou jednoho nebo více atomů vodíku v molekule uhlovodíku hydroxylovou
LABORATORNÍ PRÁCE Č. 26 HYDROXYDERIVÁTY - ALKOHOLY PRINCIP Hydroxyderiváty jsou kyslíkaté deriváty uhlovodíků, které vznikají náhradou jednoho nebo více atomů vodíku v molekule uhlovodíku hydroxylovou
Návod k laboratornímu cvičení. Efektní pokusy
 Návod k laboratornímu cvičení Efektní pokusy Úkol č. 1: Chemikova zahrádka Pomůcky: skleněná vana, lžička na chemikálie. Chemikálie: vodní sklo, síran zinečnatý ZnSO 4 (X i ), síran železnatý FeSO 4, chlorid
Návod k laboratornímu cvičení Efektní pokusy Úkol č. 1: Chemikova zahrádka Pomůcky: skleněná vana, lžička na chemikálie. Chemikálie: vodní sklo, síran zinečnatý ZnSO 4 (X i ), síran železnatý FeSO 4, chlorid
Ústřední komise Chemické olympiády. 55. ročník 2018/2019 ŠKOLNÍ KOLO. Kategorie A ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ)
 Ústřední komise Chemické olympiády 55. ročník 2018/2019 ŠKOLNÍ KOLO Kategorie A ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ) PRAKTICKÁ ČÁST 40 BODŮ Autor Mgr. Filip Smrčka Masarykova univerzita, Brno prof. RNDr. Přemysl
Ústřední komise Chemické olympiády 55. ročník 2018/2019 ŠKOLNÍ KOLO Kategorie A ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ) PRAKTICKÁ ČÁST 40 BODŮ Autor Mgr. Filip Smrčka Masarykova univerzita, Brno prof. RNDr. Přemysl
CHEMIE. Pracovní list č. 7 - žákovská verze Téma: ph. Mgr. Lenka Horutová. Projekt: Student a konkurenceschopnost Reg. číslo: CZ.1.07/1.1.07/03.
 www.projektsako.cz CHEMIE Pracovní list č. 7 - žákovská verze Téma: ph Lektor: Mgr. Lenka Horutová Projekt: Student a konkurenceschopnost Reg. číslo: CZ.1.07/1.1.07/03.0075 Teorie: Pro snadnější výpočet
www.projektsako.cz CHEMIE Pracovní list č. 7 - žákovská verze Téma: ph Lektor: Mgr. Lenka Horutová Projekt: Student a konkurenceschopnost Reg. číslo: CZ.1.07/1.1.07/03.0075 Teorie: Pro snadnější výpočet
Střední průmyslová škola, Karviná. Protokol o zkoušce
 č.1 Stanovení dusičnanů ve vodách fotometricky Předpokládaná koncentrace 5 20 mg/l navážka KNO 3 (g) Příprava kalibračního standardu Kalibrace slepý vzorek kalibrační roztok 1 kalibrační roztok 2 kalibrační
č.1 Stanovení dusičnanů ve vodách fotometricky Předpokládaná koncentrace 5 20 mg/l navážka KNO 3 (g) Příprava kalibračního standardu Kalibrace slepý vzorek kalibrační roztok 1 kalibrační roztok 2 kalibrační
