Neutralizace kyseliny zásadou
|
|
|
- Naděžda Blažková
- před 8 lety
- Počet zobrazení:
Transkript
1 Neutralizace kyseliny zásadou Metodický list pro učitele Časový harmonogram a) doba na přípravu - 10 minut b) doba na provedení - 15 minut Pomůcky a) chemikálie - kyselina chlorovodíková - hydroxid sodný - destilovaná voda - chlorid sodný - metyloranž b) potřeby - dvě kádinky 250 cm 3 - odměrný válec 100 cm 3 - skleněná tyčinka - hodinové sklíčko - lihový kahan - zápalky - azbestová síťka - stojan - bílá podložka c) přístroje - PH-BTA ph Sensor čidlo kyselosti - rozhraní Vernier GO!Link - počítač s programem Logger Lite Informace o nebezpečnosti použitých chemikálií 1
2 Přípravné kroky připravit roztoky: - 10% roztok kyseliny chlorovodíkové - 5% roztok hydroxidu sodného - roztok metyloranže Interaktivní výukový materiál související s pokusem - viz prezentace - Roztoky kyselé, zásadité - prezentace.pptx Použitá literatura: KARGER, I. a kol. Chemie I pro 8. ročník základní školy a nižší ročníky víceletých gymnázií. Olomouc: Prodos, ISBN BENEŠ, P. a kol. Základy chemie 1 pro 2. stupeň základní školy, nižší ročníky víceletých gymnázií a střední školy. 1. vydání. Praha: Fortuna, ISBN LOS, P. a kol. Nebojte se chemie 1. díl - chemie pro základní a občanskou školu. 1. vydání. Praha: Scientia, ISBN Metodika pokusu Cíl: žáci umí pracovat s indikátory, znají barevné přechody indikátorů a umí pracovat se senzorem ph. Cílem této úlohy je z roztoku kyseliny a zásady připravit neutrální roztok a jeho odpařením získat sůl. Měření ph provedeme jednak orientačně pomocí indikátoru metyloranže, ale také měřením v počítači v programu Logger Lite za pomoci PH-BTA ph Sensor čidla kyselosti. Výstupy RVP: orientuje se na stupnici ph, změří reakci roztoku univerzálním indikátorem a uvede příklady uplatňování neutralizace v praxi Cílová skupina: žák ZŠ - 8. ročník Náročnost: nízká 2
3 Klíčová slova: indikátor, metyloranž, ph stupnice, kyselina chlorovodíková, hydroxid sodný Poučení o bezpečnosti práce ke konkrétnímu pokusu Aktivitu lze provádět buď demonstračním způsobem v hodině chemie, nebo ji mohou žáci provádět samostatně vedlejším efektem je pak upevňování měřících a praktických dovedností. Pracovní postup: - v první kádince rozpustíme 3 g chloridu sodného ve 100 cm 3 destilované vody a přidáme několik kapek metyloranže - postavíme na bílou podložku - do druhé kádinky odměříme 50 cm 3 roztoku kyseliny chlorovodíkové a opět přidáme několik kapek metyloranže - nyní provedeme přesné měření ph senzorem Vernier PH-BTA - do počítače připojíme rozhraní Vernier GO!Link a do jeho vstupu zapojíme ph senzor Vernier - spustíme program Logger Lite - změříme hodnotu ph v roztoku kyseliny chlorovodíkové a výsledek měření zaznamenáme do připravené tabulky - v odměrném válci odměříme 50 cm 3 roztoku hydroxidu sodného - po malých kapkách přidáváme tento roztok hydroxidu k roztoku kyseliny v kádince - po každém přidání zamícháme skleněnou tyčinkou - sledujeme změnu zbarvení indikátoru - zbarvení v kádince, ve které sléváme roztok kyseliny a hydroxidu, srovnáváme se zbarvením v kádince s roztokem soli na bílé podložce - jakmile se obě zbarvení srovnají, práci přerušíme - provedeme přesné měření ph senzorem Vernier PH-BTA - senzor zasuneme do nově vzniklého roztoku a výsledek měření opět zaznamenáme do připravené tabulky - část vzniklého roztoku nalijeme na hodinové sklíčko - na azbestové síťce nad kahanem opatrně odpařujeme - za malou chvíli se voda odpaří a na sklíčku můžeme pozorovat bílý povlak 3
4 Závěr: V okamžiku sjednocení zbarvení roztoků je vzniklý roztok neutrální. Z kyselého (červeného) roztoku jsme neutralizací roztokem zásady získali roztok neutrální (oranžový). Na sklíčku odpařením tohoto neutrálního roztoku vznikne sodná sůl kyseliny chlorovodíkové chlorid sodný. Ukázka naměřených hodnot: Obrazovka monitoru před začátkem měření Tabulka měření: roztok kyseliny chlorovodíkové zbarvení hodnota ph - na začátku měření červené 5 - na konci měření oranžové 7 4
5 Pedagogicko-podpůrné činnosti Lze zdůraznit mezipředmětové vztahy a přesah do vzdělávacích předmětů: Biologie zdravá výživa - ph našeho organismu normální hladina ph našeho těla je mírně zásaditá (od 7,36 do 7,44) Zoologie - citlivost vodních živočichů na ph prostředí př.: Pedologie mlži snáší prostředí - 6 ph čolci - 5 ph okouni - 5 ph - kyselost půdy Kontrolní materiál pro zpětnou vazbu Otázky pro zpětnou vazbu: 1. Co je to neutralizace? 2. Kdy je roztok kyselý, zásaditý nebo neutrální? 3. Jakými způsoby můžeme zjistit hodnoty ph roztoků? 4. Jak se v kyselém a neutrálním prostředí zbarví indikátor metyloranž? 5. Jak se v kyselém, zásaditém a neutrálním prostředí zbarví indikátor lakmus? 6. Zapište chemickou rovnici: hydroxid sodný (zásada) reaguje s kyselinou chlorovodíkovou (kyselina) za vzniku chloridu sodného (sůl) a vody. Řešení: 1. neutralizace je reakce kyseliny se zásadou a vzniká sůl dané kyseliny a voda 2. kyselý pod 7 ph, zásaditý nad 7 ph, neutrální = 7 ph 5
6 3. orientační měření pomocí indikátorů (lakmus, fenolftalein, metyloranž), přesně ph metry 4. kyselé červeně, neutrální oranžově, zásadité - žluté 5. kyselé prostředí červeně, neutrální - fialově, zásadité - modře 6. NaOH + HCl NaCl + H 2O Fotodokumentace Čidlo kyselosti PH-BTA ph Sensor 6
7 Rozhraní Vernier GO!Link Ukázka měření ph 7
8 Protokol o provedeném pokusu - číslo protokolu Ch 18/8 - ověření provedeno a zapsáno v třídní knize 8. třídy dne Autoři pokusu: Ing. Marie Smičková, Mgr. Jitka Slavíčková Autor prezentace: Ing. Marie Smičková Uvedený pokus je reálný v podmínkách ZŠ. 8
Důkaz kyselin. Metodický list pro učitele. Časový harmonogram. a) doba na přípravu - 10 minut b) doba na provedení 10 minut.
 Důkaz kyselin Metodický list pro učitele Časový harmonogram a) doba na přípravu - 10 minut b) doba na provedení 10 minut Pomůcky a) chemikálie - kyselina dusičná - kyselina chlorovodíková - kyselina citronová
Důkaz kyselin Metodický list pro učitele Časový harmonogram a) doba na přípravu - 10 minut b) doba na provedení 10 minut Pomůcky a) chemikálie - kyselina dusičná - kyselina chlorovodíková - kyselina citronová
Příprava vápenné vody
 Příprava vápenné vody Metodický list pro učitele Časový harmonogram a) doba na přípravu - 10 minut b) doba na provedení - 10 minut Pomůcky a) chemikálie - oxid vápenatý - voda b) potřeby - kádinka 2 ks
Příprava vápenné vody Metodický list pro učitele Časový harmonogram a) doba na přípravu - 10 minut b) doba na provedení - 10 minut Pomůcky a) chemikálie - oxid vápenatý - voda b) potřeby - kádinka 2 ks
Důkaz uhličitanu ve vodním kameni
 Důkaz uhličitanu ve vodním kameni Časový harmonogram a) doba na přípravu - 10 minut b) doba na provedení - 10 minut Metodický list pro učitele Pomůcky a) chemikálie - ocet b) potřeby - varná konvice zanesená
Důkaz uhličitanu ve vodním kameni Časový harmonogram a) doba na přípravu - 10 minut b) doba na provedení - 10 minut Metodický list pro učitele Pomůcky a) chemikálie - ocet b) potřeby - varná konvice zanesená
Rozklad uhličitanu vápenatého kyselinou
 Časový harmonogram Rozklad uhličitanu vápenatého kyselinou a) doba na přípravu - 10 minut b) doba na provedení - 10 minut Pomůcky a) chemikálie - kyselina chlorovodíková b) potřeby - kádinka - vápenec
Časový harmonogram Rozklad uhličitanu vápenatého kyselinou a) doba na přípravu - 10 minut b) doba na provedení - 10 minut Pomůcky a) chemikálie - kyselina chlorovodíková b) potřeby - kádinka - vápenec
Nasycený roztok. Metodický list pro učitele. Časový harmonogram. a) doba na přípravu - 10 minut b) doba na provedení - 10 minut.
 Nasycený roztok Metodický list pro učitele Časový harmonogram a) doba na přípravu - 10 minut b) doba na provedení - 10 minut Pomůcky a) chemikálie - modrá skalice (pentahydrát síranu měďnatého) - voda
Nasycený roztok Metodický list pro učitele Časový harmonogram a) doba na přípravu - 10 minut b) doba na provedení - 10 minut Pomůcky a) chemikálie - modrá skalice (pentahydrát síranu měďnatého) - voda
Ředění kyseliny sírové
 Ředění kyseliny sírové Metodický list pro učitele Časový harmonogram a) doba na přípravu - 10 minut b) doba na provedení - 5 minut Pomůcky a) chemikálie - kyselina sírová - voda b) potřeby - kádinky 500
Ředění kyseliny sírové Metodický list pro učitele Časový harmonogram a) doba na přípravu - 10 minut b) doba na provedení - 5 minut Pomůcky a) chemikálie - kyselina sírová - voda b) potřeby - kádinky 500
Měření obsahu kyslíku a oxidu uhličitého ve vzduchu
 Měření obsahu kyslíku a oxidu uhličitého ve vzduchu Časový harmonogram Metodický list pro učitele a) doba na přípravu - 5 minut b) doba na provedení - 5 minut na začátku vyučovací hodiny a 5 minut na konci
Měření obsahu kyslíku a oxidu uhličitého ve vzduchu Časový harmonogram Metodický list pro učitele a) doba na přípravu - 5 minut b) doba na provedení - 5 minut na začátku vyučovací hodiny a 5 minut na konci
Vlastnosti kyseliny sírové
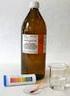 Vlastnosti kyseliny sírové Metodický list pro učitele Časový harmonogram a) doba na přípravu - 10 minut b) doba na provedení - 10 minut Pomůcky a) chemikálie - kyselina sírová - voda - kostka cukru b)
Vlastnosti kyseliny sírové Metodický list pro učitele Časový harmonogram a) doba na přípravu - 10 minut b) doba na provedení - 10 minut Pomůcky a) chemikálie - kyselina sírová - voda - kostka cukru b)
Sublimace jodu. Metodický list pro učitele. Časový harmonogram. a) doba na přípravu - 10 minut b) doba na provedení - 20 minut.
 Sublimace jodu Metodický list pro učitele Časový harmonogram a) doba na přípravu - 10 minut b) doba na provedení - 20 minut Pomůcky a) chemikálie - jod znečištěný pískem b) potřeby - kádinka - hodinové
Sublimace jodu Metodický list pro učitele Časový harmonogram a) doba na přípravu - 10 minut b) doba na provedení - 20 minut Pomůcky a) chemikálie - jod znečištěný pískem b) potřeby - kádinka - hodinové
Kyseliny a zásady měření ph indikátory a senzorem ph Vernier Laboratorní práce
 Kyseliny a zásady měření ph indikátory a senzorem ph Vernier Laboratorní práce VY_52_INOVACE_204 Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Chemie Ročník: 8.,9. Kyseliny a zásady měření ph indikátory
Kyseliny a zásady měření ph indikátory a senzorem ph Vernier Laboratorní práce VY_52_INOVACE_204 Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Chemie Ročník: 8.,9. Kyseliny a zásady měření ph indikátory
Vliv ředění na kyselost/zásaditost roztoků pomocí čidla kyselosti ph
 Zvyšování kvality výuky v přírodních a technických oblastech CZ.1.07/1.1.28/02.0055 Vliv ředění na kyselost/zásaditost roztoků pomocí čidla kyselosti ph (laboratorní práce) Označení: EU-Inovace-Ch-8-11
Zvyšování kvality výuky v přírodních a technických oblastech CZ.1.07/1.1.28/02.0055 Vliv ředění na kyselost/zásaditost roztoků pomocí čidla kyselosti ph (laboratorní práce) Označení: EU-Inovace-Ch-8-11
Koroze železa. Metodický list pro učitele. Časový harmonogram. Dlouhodobé:
 Koroze železa Metodický list pro učitele Časový harmonogram Dlouhodobé: a) doba na přípravu - 5 minut b) doba na provedení - 5 minut, c) vyhodnocení za týden - 5 minut Pomůcky a) chemikálie - benzín -
Koroze železa Metodický list pro učitele Časový harmonogram Dlouhodobé: a) doba na přípravu - 5 minut b) doba na provedení - 5 minut, c) vyhodnocení za týden - 5 minut Pomůcky a) chemikálie - benzín -
Neutralizace, měření senzorem ph Vernier Laboratorní práce
 Neutralizace, měření senzorem ph Vernier Laboratorní práce VY_52_INOVACE_209 Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Chemie Ročník: 8.,9. Neutralizace, měření senzorem ph Vernier Laboratorní
Neutralizace, měření senzorem ph Vernier Laboratorní práce VY_52_INOVACE_209 Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Chemie Ročník: 8.,9. Neutralizace, měření senzorem ph Vernier Laboratorní
Filtrace znečištěné vody
 Filtrace znečištěné vody Metodický list pro učitele Časový harmonogram a) doba na přípravu - 10 minut b) doba na provedení - 10 minut Pomůcky a) chemikálie - kalná vody z rybníka - 200 ml b) potřeby -
Filtrace znečištěné vody Metodický list pro učitele Časový harmonogram a) doba na přípravu - 10 minut b) doba na provedení - 10 minut Pomůcky a) chemikálie - kalná vody z rybníka - 200 ml b) potřeby -
Studium kyselosti a zásaditosti roztoků kolem nás
 Zvyšování kvality výuky v přírodních a technických oblastech CZ.1.07/1.1.28/02.0055 Studium kyselosti a zásaditosti roztoků kolem nás (laboratorní práce) Označení: EU-Inovace-Ch-8-10 Předmět: Chemie Cílová
Zvyšování kvality výuky v přírodních a technických oblastech CZ.1.07/1.1.28/02.0055 Studium kyselosti a zásaditosti roztoků kolem nás (laboratorní práce) Označení: EU-Inovace-Ch-8-10 Předmět: Chemie Cílová
Inovace výuky chemie. ph a neutralizace. Ch 8/09
 Inovace výuky chemie ph a neutralizace Ch 8/09 Vzdělávací oblast: Vzdělávací obor: Tematický okruh: Cílová skupina: Klíčová slova: Očekávaný výstup: Člověk a příroda Chemie Anorganické sloučeniny 8. ročník
Inovace výuky chemie ph a neutralizace Ch 8/09 Vzdělávací oblast: Vzdělávací obor: Tematický okruh: Cílová skupina: Klíčová slova: Očekávaný výstup: Člověk a příroda Chemie Anorganické sloučeniny 8. ročník
Název: Acidobazické indikátory
 Název: Acidobazické indikátory Autor: Mgr. Jiří Vozka, Ph.D. Název školy: Gymnázium Jana Nerudy, škola hl. města Prahy Předmět, mezipředmětové vztahy: chemie, biologie, fyzika Ročník: 3. (1. ročník vyššího
Název: Acidobazické indikátory Autor: Mgr. Jiří Vozka, Ph.D. Název školy: Gymnázium Jana Nerudy, škola hl. města Prahy Předmět, mezipředmětové vztahy: chemie, biologie, fyzika Ročník: 3. (1. ročník vyššího
Červené zelí a červená řepa jako přírodní indikátory ph
 Zvyšování kvality výuky v přírodních a technických oblastech CZ.1.07/1.128/02.0055 Červené zelí a červená řepa jako přírodní indikátory ph (laboratorní práce) Označení: EU-Inovace-BFCh-Ch-10 Předmět: Biologicko-fyzikálně
Zvyšování kvality výuky v přírodních a technických oblastech CZ.1.07/1.128/02.0055 Červené zelí a červená řepa jako přírodní indikátory ph (laboratorní práce) Označení: EU-Inovace-BFCh-Ch-10 Předmět: Biologicko-fyzikálně
Návod k laboratornímu cvičení. Fenoly
 Návod k laboratornímu cvičení Fenoly Úkol č. 1: Příprava fenolátu sodného Pomůcky: váhy, kádinka, zkumavky Chemikálie: 10% roztok hydroxidu sodného NaOH (C), 5%roztok kyseliny chlorovodíkové HCl (C, X
Návod k laboratornímu cvičení Fenoly Úkol č. 1: Příprava fenolátu sodného Pomůcky: váhy, kádinka, zkumavky Chemikálie: 10% roztok hydroxidu sodného NaOH (C), 5%roztok kyseliny chlorovodíkové HCl (C, X
Kapitola: Přírodní látky Téma: Vitamíny. Cíl: Porovnat průběh a rychlost rozpouštění pevných forem vitamínu C v kyselině chlorovodíkové
 Sledování rozpustnosti vitamínu C v žaludeční kyselině demonstrační pokus VY_52_Inovace_244 Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Chemie Ročník: 8, 9 Kapitola: Přírodní látky Téma: Vitamíny
Sledování rozpustnosti vitamínu C v žaludeční kyselině demonstrační pokus VY_52_Inovace_244 Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Chemie Ročník: 8, 9 Kapitola: Přírodní látky Téma: Vitamíny
Měření ph nápojů a roztoků
 Měření ph nápojů a roztoků vzorová úloha (ZŠ) Jméno Třída.. Datum.. 1 Teoretický úvod Kyselý nebo zásaditý roztok? Proč je ocet považován za kyselý roztok? Ocet obsahuje nadbytek (oxoniových kationtů).
Měření ph nápojů a roztoků vzorová úloha (ZŠ) Jméno Třída.. Datum.. 1 Teoretický úvod Kyselý nebo zásaditý roztok? Proč je ocet považován za kyselý roztok? Ocet obsahuje nadbytek (oxoniových kationtů).
Sacharidy - důkaz organických látek v přírodních materiálech pomocí žákovské soupravy pro chemii
 Zvyšování kvality výuky v přírodních a technických oblastech CZ.1.07/1.1.28/02.0055 Sacharidy - důkaz organických látek v přírodních materiálech pomocí žákovské soupravy pro chemii (laboratorní práce)
Zvyšování kvality výuky v přírodních a technických oblastech CZ.1.07/1.1.28/02.0055 Sacharidy - důkaz organických látek v přírodních materiálech pomocí žákovské soupravy pro chemii (laboratorní práce)
Měření ph nápojů a roztoků
 Měření ph nápojů a roztoků vzorová úloha (SŠ) Jméno Třída.. Datum.. 1 Teoretický úvod Kyselý nebo zásaditý roztok? Proč je ocet považován za kyselý roztok? Ocet obsahuje nadbytek (oxoniových kationtů).
Měření ph nápojů a roztoků vzorová úloha (SŠ) Jméno Třída.. Datum.. 1 Teoretický úvod Kyselý nebo zásaditý roztok? Proč je ocet považován za kyselý roztok? Ocet obsahuje nadbytek (oxoniových kationtů).
Příprava roztoku o dané koncentraci Laboratorní práce
 Příprava o dané koncentraci Laboratorní práce VY_52_INOVACE_197 Vzdělávací oblast: Člověk a příroda Vzdělávací obor:chemie Ročník: 8, 9 Příprava o dané koncentraci Laboratorní práce Jméno Třída..Datum
Příprava o dané koncentraci Laboratorní práce VY_52_INOVACE_197 Vzdělávací oblast: Člověk a příroda Vzdělávací obor:chemie Ročník: 8, 9 Příprava o dané koncentraci Laboratorní práce Jméno Třída..Datum
CHEMIE Pracovní list č.3 žákovská verze Téma: Acidobazická titrace Mgr. Lenka Horutová Student a konkurenceschopnost
 www.projektsako.cz CHEMIE Pracovní list č.3 žákovská verze Téma: Acidobazická titrace Lektor: Projekt: Reg. číslo: Mgr. Lenka Horutová Student a konkurenceschopnost CZ.1.07/1.1.07/03.0075 Teorie: Základem
www.projektsako.cz CHEMIE Pracovní list č.3 žákovská verze Téma: Acidobazická titrace Lektor: Projekt: Reg. číslo: Mgr. Lenka Horutová Student a konkurenceschopnost CZ.1.07/1.1.07/03.0075 Teorie: Základem
Tento materiál byl vytvořen v rámci projektu Operačního programu Vzdělávání pro konkurenceschopnost.
 Tento materiál byl vytvořen v rámci projektu Operačního programu Vzdělávání pro konkurenceschopnost. Projekt MŠMT ČR Číslo projektu Název projektu školy Klíčová aktivita III/2 EU PENÍZE ŠKOLÁM CZ.1.07/1.4.00/21.2146
Tento materiál byl vytvořen v rámci projektu Operačního programu Vzdělávání pro konkurenceschopnost. Projekt MŠMT ČR Číslo projektu Název projektu školy Klíčová aktivita III/2 EU PENÍZE ŠKOLÁM CZ.1.07/1.4.00/21.2146
Půdy vlastnosti II. (laboratorní práce)
 Zvyšování kvality výuky v přírodních a technických oblastech CZ.1.07/1.1.28/02.0055 Půdy vlastnosti II. (laboratorní práce) Označení: EU-Inovace-Př-9-39 Předmět: přírodopis Cílová skupina: 9. třída Autor:
Zvyšování kvality výuky v přírodních a technických oblastech CZ.1.07/1.1.28/02.0055 Půdy vlastnosti II. (laboratorní práce) Označení: EU-Inovace-Př-9-39 Předmět: přírodopis Cílová skupina: 9. třída Autor:
Autor: Mgr. Stanislava Bubíková. Datum (období) tvorby: 12. 4. 2013. Ročník: osmý
 ph Autor: Mgr. Stanislava Bubíková Datum (období) tvorby: 12. 4. 2013 Ročník: osmý Vzdělávací oblast: Člověk a příroda / Chemie / Anorganické sloučeniny 1 Anotace: Žáci se seznámí se základní vlastností
ph Autor: Mgr. Stanislava Bubíková Datum (období) tvorby: 12. 4. 2013 Ročník: osmý Vzdělávací oblast: Člověk a příroda / Chemie / Anorganické sloučeniny 1 Anotace: Žáci se seznámí se základní vlastností
NEUTRALIZAČNÍ ODMĚRNÁ ANALÝZA (TITRACE)
 NEUTRALIZAČNÍ ODMĚRNÁ ANALÝZA (TITRACE) Cíle a princip: Stanovit TITR (přesnou koncentraci) odměrného roztoku kyseliny nebo zásady pomocí známé přesné koncentrace již stanoveného odměrného roztoku. Podstatou
NEUTRALIZAČNÍ ODMĚRNÁ ANALÝZA (TITRACE) Cíle a princip: Stanovit TITR (přesnou koncentraci) odměrného roztoku kyseliny nebo zásady pomocí známé přesné koncentrace již stanoveného odměrného roztoku. Podstatou
Tento materiál byl vytvořen v rámci projektu Operačního programu Vzdělávání pro konkurenceschopnost.
 Tento materiál byl vytvořen v rámci projektu Operačního programu Vzdělávání pro konkurenceschopnost. Projekt MŠMT ČR Číslo projektu Název projektu školy Klíčová aktivita III/2 EU PENÍZE ŠKOLÁM CZ.1.07/1.4.00/21.2146
Tento materiál byl vytvořen v rámci projektu Operačního programu Vzdělávání pro konkurenceschopnost. Projekt MŠMT ČR Číslo projektu Název projektu školy Klíčová aktivita III/2 EU PENÍZE ŠKOLÁM CZ.1.07/1.4.00/21.2146
Obsah soli v potravinách Laboratorní práce
 Obsah soli v potravinách Laboratorní práce VY_52_INOVACE_214 Vzdělávací oblast: Člověk a příroda Vzdělávací obor:chemie Ročník: 8, 9 Obsah soli v potravinách Laboratorní práce Jméno Třída..Datum Úkol:
Obsah soli v potravinách Laboratorní práce VY_52_INOVACE_214 Vzdělávací oblast: Člověk a příroda Vzdělávací obor:chemie Ročník: 8, 9 Obsah soli v potravinách Laboratorní práce Jméno Třída..Datum Úkol:
CHEMIE. Pracovní list č. 7 - žákovská verze Téma: ph. Mgr. Lenka Horutová. Projekt: Student a konkurenceschopnost Reg. číslo: CZ.1.07/1.1.07/03.
 www.projektsako.cz CHEMIE Pracovní list č. 7 - žákovská verze Téma: ph Lektor: Mgr. Lenka Horutová Projekt: Student a konkurenceschopnost Reg. číslo: CZ.1.07/1.1.07/03.0075 Teorie: Pro snadnější výpočet
www.projektsako.cz CHEMIE Pracovní list č. 7 - žákovská verze Téma: ph Lektor: Mgr. Lenka Horutová Projekt: Student a konkurenceschopnost Reg. číslo: CZ.1.07/1.1.07/03.0075 Teorie: Pro snadnější výpočet
Trojské trumfy. pražským školám BARVY U ŽIVOČICHŮ A ROSTLIN. projekt CZ.2.17/3.1.00/32718 EVROPSKÝ SOCIÁLNÍ FOND
 EVROPSKÝ SOCIÁLNÍ FOND PRAHA & EU INVESTUJEME DO VAŠÍ BUDOUCNOSTI Pracovní Didaktický list balíček č. 7 č. 9 Trojské trumfy pražským školám projekt CZ.2.17/3.1.00/32718 BARVY U ŽIVOČICHŮ A ROSTLIN A B?
EVROPSKÝ SOCIÁLNÍ FOND PRAHA & EU INVESTUJEME DO VAŠÍ BUDOUCNOSTI Pracovní Didaktický list balíček č. 7 č. 9 Trojské trumfy pražským školám projekt CZ.2.17/3.1.00/32718 BARVY U ŽIVOČICHŮ A ROSTLIN A B?
Bílkoviny (laboratorní práce)
 Zvyšování kvality výuky v přírodních a technických oblastech CZ.1.07/1.128/02.0055 Bílkoviny (laboratorní práce) Označení: EU-Inovace-Ch-9-08 Předmět: chemie Cílová skupina: 9. třída Autor: Mgr. Simona
Zvyšování kvality výuky v přírodních a technických oblastech CZ.1.07/1.128/02.0055 Bílkoviny (laboratorní práce) Označení: EU-Inovace-Ch-9-08 Předmět: chemie Cílová skupina: 9. třída Autor: Mgr. Simona
Sešit pro laboratorní práci z chemie
 Sešit pro laboratorní práci z chemie téma: Příprava roztoků a měření ph autor: ing. Alena Dvořáková vytvořeno při realizaci projektu: Inovace školního vzdělávacího programu biologie a chemie registrační
Sešit pro laboratorní práci z chemie téma: Příprava roztoků a měření ph autor: ing. Alena Dvořáková vytvořeno při realizaci projektu: Inovace školního vzdělávacího programu biologie a chemie registrační
Změna teploty varu roztoku demonstrační pokus VY_52_Inovace_222 Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Chemie Ročník: 8
 Změna teploty varu roztoku demonstrační pokus VY_52_Inovace_222 Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Chemie Ročník: 8 Kapitola: Směsi Téma: Roztoky Cíl: Sledovat zvyšování teploty varu
Změna teploty varu roztoku demonstrační pokus VY_52_Inovace_222 Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Chemie Ročník: 8 Kapitola: Směsi Téma: Roztoky Cíl: Sledovat zvyšování teploty varu
1. Chemický turnaj. kategorie mladší žáci 30.11. 2012. Zadání úloh
 1. Chemický turnaj kategorie mladší žáci 30.11. 2012 Zadání úloh Vytvořeno v rámci projektu OPVK CZ.1.07/1.1.26/01.0034,,Zkvalitňování výuky chemie a biologie na GJO spolufinancovaného Evropským sociálním
1. Chemický turnaj kategorie mladší žáci 30.11. 2012 Zadání úloh Vytvořeno v rámci projektu OPVK CZ.1.07/1.1.26/01.0034,,Zkvalitňování výuky chemie a biologie na GJO spolufinancovaného Evropským sociálním
53. ročník 2016/2017
 Ústřední komise Chemické olympiády 53. ročník 2016/2017 OKRESNÍ KOLO kategorie D ZADÁNÍ PRAKTICKÉ ČÁSTI časová náročnost: 90 minut Úloha 1 Yamadův univerzální indikátor 30 bodů Úvod Univerzální acidobazické
Ústřední komise Chemické olympiády 53. ročník 2016/2017 OKRESNÍ KOLO kategorie D ZADÁNÍ PRAKTICKÉ ČÁSTI časová náročnost: 90 minut Úloha 1 Yamadův univerzální indikátor 30 bodů Úvod Univerzální acidobazické
Kyselost a zásaditost vodných roztoků
 Kyselost a zásaditost vodných roztoků Autorem materiálu a všech jeho částí, není-li uvedeno jinak, je. Mgr. Vlastimil Vaněk. Dostupné z Metodického portálu www.rvp.cz, ISSN: 1802-4785, financovaného z
Kyselost a zásaditost vodných roztoků Autorem materiálu a všech jeho částí, není-li uvedeno jinak, je. Mgr. Vlastimil Vaněk. Dostupné z Metodického portálu www.rvp.cz, ISSN: 1802-4785, financovaného z
LP č. 6 - BÍLKOVINY. Autor: Mgr. Stanislava Bubíková. Datum (období) tvorby: 28. 2. 2013. Ročník: devátý
 LP č. 6 - BÍLKOVINY Autor: Mgr. Stanislava Bubíková Datum (období) tvorby: 28. 2. 2013 Ročník: devátý Vzdělávací oblast: Člověk a příroda / Chemie / Organické sloučeniny 1 Anotace: Žáci prakticky ověří
LP č. 6 - BÍLKOVINY Autor: Mgr. Stanislava Bubíková Datum (období) tvorby: 28. 2. 2013 Ročník: devátý Vzdělávací oblast: Člověk a příroda / Chemie / Organické sloučeniny 1 Anotace: Žáci prakticky ověří
ph půdy Zvyšování kvality výuky v přírodních a technických oblastech CZ.1.07/1.1.28/02.0055 (laboratorní práce) Označení: EU-Inovace-BFCh-Ch-04
 Zvyšování kvality výuky v přírodních a technických oblastech CZ.1.07/1.1.28/02.0055 (laboratorní práce) Označení: EU-Inovace-BFCh-Ch-04 Předmět: Biologická, fyzikální a chemická praktika Cílová skupina:
Zvyšování kvality výuky v přírodních a technických oblastech CZ.1.07/1.1.28/02.0055 (laboratorní práce) Označení: EU-Inovace-BFCh-Ch-04 Předmět: Biologická, fyzikální a chemická praktika Cílová skupina:
ROZDĚLENÍ SLOUČENIN INDIKÁTORY VZNIK HYDROXIDŮ A KYSELIN
 ROZDĚLENÍ SLOUČENIN INDIKÁTORY VZNIK HYDROXIDŮ A KYSELIN PROJEKT EU PENÍZE ŠKOLÁM OPERAČNÍ PROGRAM VZDĚLÁVÁNÍ PRO KONKURENCESCHOPNOST VY_52_INOVACE_190 VZDĚLÁVACÍ OBLAST: ČLOVĚK A PŘÍRODA VZDĚLÁVACÍ OBOR:
ROZDĚLENÍ SLOUČENIN INDIKÁTORY VZNIK HYDROXIDŮ A KYSELIN PROJEKT EU PENÍZE ŠKOLÁM OPERAČNÍ PROGRAM VZDĚLÁVÁNÍ PRO KONKURENCESCHOPNOST VY_52_INOVACE_190 VZDĚLÁVACÍ OBLAST: ČLOVĚK A PŘÍRODA VZDĚLÁVACÍ OBOR:
Kyselé deště a jejich vliv na povrchové vody
 Zvyšování kvality výuky v přírodních a technických oblastech CZ.1.07/1.1.28/02.0055 Kyselé deště a jejich vliv na povrchové vody (laboratorní práce) Označení: EU-Inovace-BFCh-Ch-06 Předmět: Biologická,
Zvyšování kvality výuky v přírodních a technických oblastech CZ.1.07/1.1.28/02.0055 Kyselé deště a jejich vliv na povrchové vody (laboratorní práce) Označení: EU-Inovace-BFCh-Ch-06 Předmět: Biologická,
Hydroxidy a indikátory demonstrační
 název typ: zařazení: Pomůcky: Chemikálie: Postup: pozorování rovnice, vysvětlení Hydroxidy a indikátory demonstrační Hydroxidy. Indikátory. 3 zkumavky, kapátko NaOH(C), fenolftalein, lakmus, ph papírek
název typ: zařazení: Pomůcky: Chemikálie: Postup: pozorování rovnice, vysvětlení Hydroxidy a indikátory demonstrační Hydroxidy. Indikátory. 3 zkumavky, kapátko NaOH(C), fenolftalein, lakmus, ph papírek
53. ročník 2016/2017
 Ústřední komise Chemické olympiády 53. ročník 2016/2017 OKRESNÍ KOLO kategorie D ŘEŠENÍ PRAKTICKÉ ČÁSTI časová náročnost: 90 minut Úloha 1 Yamadův univerzální indikátor 30 bodů Úkoly: 1. Doplněná Tabulka
Ústřední komise Chemické olympiády 53. ročník 2016/2017 OKRESNÍ KOLO kategorie D ŘEŠENÍ PRAKTICKÉ ČÁSTI časová náročnost: 90 minut Úloha 1 Yamadův univerzální indikátor 30 bodů Úkoly: 1. Doplněná Tabulka
Měření ph látek pomocí čidla kyselosti ph
 Zvyšování kvality výuky v přírodních a technických oblastech CZ.1.07/1.1.28/02.0055 Měření ph látek pomocí čidla kyselosti ph (laboratorní práce) Označení: EU-Inovace-Ch-8-09 Předmět: Chemie Cílová skupina:
Zvyšování kvality výuky v přírodních a technických oblastech CZ.1.07/1.1.28/02.0055 Měření ph látek pomocí čidla kyselosti ph (laboratorní práce) Označení: EU-Inovace-Ch-8-09 Předmět: Chemie Cílová skupina:
Termochemie. Úkol: A. Určete změnu teploty při rozpouštění hydroxidu sodného B. Určete reakční teplo reakce zinku s roztokem měďnaté soli
 1. Termochemie Úkol: Určete změnu teploty při rozpouštění hydroxidu sodného B. Určete reakční teplo reakce zinku s roztokem měďnaté soli Pomůcky : a) kádinky, teploměr, odměrný válec, váženka, váhy, kalorimetr,
1. Termochemie Úkol: Určete změnu teploty při rozpouštění hydroxidu sodného B. Určete reakční teplo reakce zinku s roztokem měďnaté soli Pomůcky : a) kádinky, teploměr, odměrný válec, váženka, váhy, kalorimetr,
2.12 Vyvíjení CO 2 bublinky kolem nás. Projekt Trojlístek
 2. Vlastnosti látek a chemické reakce 2.12 Vyvíjení CO 2 bublinky kolem nás. Projekt úroveň 1 2 3 1. Předmět výuky Metodika je určena pro vzdělávací obsah vzdělávacího předmětu Chemie. Chemie 2. Cílová
2. Vlastnosti látek a chemické reakce 2.12 Vyvíjení CO 2 bublinky kolem nás. Projekt úroveň 1 2 3 1. Předmět výuky Metodika je určena pro vzdělávací obsah vzdělávacího předmětu Chemie. Chemie 2. Cílová
Návod k laboratornímu cvičení. Efektní pokusy
 Návod k laboratornímu cvičení Efektní pokusy Úkol č. 1: Chemikova zahrádka Pomůcky: skleněná vana, lžička na chemikálie. Chemikálie: vodní sklo, síran zinečnatý ZnSO 4 (X i ), síran železnatý FeSO 4, chlorid
Návod k laboratornímu cvičení Efektní pokusy Úkol č. 1: Chemikova zahrádka Pomůcky: skleněná vana, lžička na chemikálie. Chemikálie: vodní sklo, síran zinečnatý ZnSO 4 (X i ), síran železnatý FeSO 4, chlorid
REAKCE V ANORGANICKÉ CHEMII
 REAKCE V ANORGANICKÉ CHEMII PaedDr. Ivana Töpferová Střední průmyslová škola, Mladá Boleslav, Havlíčkova 456 CZ.1.07/1.5.00/34.0861 MODERNIZACE VÝUKY Anotace: laboratorní práce z anorganické chemie, realizace
REAKCE V ANORGANICKÉ CHEMII PaedDr. Ivana Töpferová Střední průmyslová škola, Mladá Boleslav, Havlíčkova 456 CZ.1.07/1.5.00/34.0861 MODERNIZACE VÝUKY Anotace: laboratorní práce z anorganické chemie, realizace
Název: Tajná písma. Výukové materiály. Téma: Organické a anorganické látky a indikátory. Úroveň: 2. stupeň ZŠ
 Název: Tajná písma Výukové materiály Téma: Organické a anorganické látky a indikátory Úroveň: 2. stupeň ZŠ Tematický celek: Vidět a poznat neviditelné Předmět (obor): chemie Doporučený věk žáků: 13 14
Název: Tajná písma Výukové materiály Téma: Organické a anorganické látky a indikátory Úroveň: 2. stupeň ZŠ Tematický celek: Vidět a poznat neviditelné Předmět (obor): chemie Doporučený věk žáků: 13 14
Půda a kyselé deště. Zvyšování kvality výuky v přírodních a technických oblastech CZ.1.07/1.1.28/02.0055. (laboratorní práce)
 Zvyšování kvality výuky v přírodních a technických oblastech CZ.1.07/1.1.28/02.0055 Půda a kyselé deště (laboratorní práce) Označení: EU-Inovace-BFCh-Ch-05 Předmět: Biologická, fyzikální a chemická praktika
Zvyšování kvality výuky v přírodních a technických oblastech CZ.1.07/1.1.28/02.0055 Půda a kyselé deště (laboratorní práce) Označení: EU-Inovace-BFCh-Ch-05 Předmět: Biologická, fyzikální a chemická praktika
Neutralizace prezentace
 Neutralizace prezentace VY_52_INOVACE_207 Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Chemie Ročník: 8,9 Projekt EU peníze školám Operačního programu Vzdělávání pro konkurenceschopnost Z daných
Neutralizace prezentace VY_52_INOVACE_207 Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Chemie Ročník: 8,9 Projekt EU peníze školám Operačního programu Vzdělávání pro konkurenceschopnost Z daných
Název: Kyselé a zásadité 1
 Název: Kyselé a zásadité 1 1) Co mají společného? Podívejte se na následující potraviny a zkuste zapřemýšlet, co mají společného: Společnou vlastností těchto potravin je: Které další látky jsou kyselé?
Název: Kyselé a zásadité 1 1) Co mají společného? Podívejte se na následující potraviny a zkuste zapřemýšlet, co mají společného: Společnou vlastností těchto potravin je: Které další látky jsou kyselé?
Kyselé deště, rozpouštění CO 2 ve vodě
 Kyselé deště, rozpouštění CO 2 ve vodě vzorová úloha (ZŠ) Jméno Třída.. Datum.. 1 Teoretický úvod Cílem úlohy je zjistit hodnotu ph teplé a studené vody vlivem rozpouštění CO 2 ve vodě. Podobný děj probíhá
Kyselé deště, rozpouštění CO 2 ve vodě vzorová úloha (ZŠ) Jméno Třída.. Datum.. 1 Teoretický úvod Cílem úlohy je zjistit hodnotu ph teplé a studené vody vlivem rozpouštění CO 2 ve vodě. Podobný děj probíhá
I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í
 I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY Laboratorní práce č. 10 Bílkoviny Pro potřeby projektu
I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY Laboratorní práce č. 10 Bílkoviny Pro potřeby projektu
I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í
 I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY Laboratorní práce č. 9 Lipidy Pro potřeby projektu
I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY Laboratorní práce č. 9 Lipidy Pro potřeby projektu
VÝŽIVA LIDSTVA Mléko a zdraví
 GYMNÁZIUM JANA OPLETALA LITOVEL Odborná práce přírodovědného kroužku VÝŽIVA LIDSTVA Mléko a zdraví Vypracovali: Martina Hubáčková, Petra Vašíčková, Pavla Kubíčková, Michaela Pavlovská, Jitka Tichá, Petra
GYMNÁZIUM JANA OPLETALA LITOVEL Odborná práce přírodovědného kroužku VÝŽIVA LIDSTVA Mléko a zdraví Vypracovali: Martina Hubáčková, Petra Vašíčková, Pavla Kubíčková, Michaela Pavlovská, Jitka Tichá, Petra
FYZIKÁLNÍ A CHEMICKÝ ROZBOR PITNÉ VODY
 LABORATORNÍ PRÁCE Č. 13 FYZIKÁLNÍ A CHEMICKÝ ROZBOR PITNÉ VODY PRINCIP V přírodě se vyskytující voda není nikdy čistá, obsahuje vždy určité množství rozpuštěných látek, plynů a nerozpuštěných pevných látek.
LABORATORNÍ PRÁCE Č. 13 FYZIKÁLNÍ A CHEMICKÝ ROZBOR PITNÉ VODY PRINCIP V přírodě se vyskytující voda není nikdy čistá, obsahuje vždy určité množství rozpuštěných látek, plynů a nerozpuštěných pevných látek.
Návod k laboratornímu cvičení. Cukry(sacharidy)
 Návod k laboratornímu cvičení Cukry(sacharidy) Úkol č. 1: Odlišení glukosy a fruktosy Pomůcky: zkumavky, lžička na chemikálie, kádinka, stojan, držák, kruh, síťka, plynový kahan, zápalky Chemikálie: fruktosa,
Návod k laboratornímu cvičení Cukry(sacharidy) Úkol č. 1: Odlišení glukosy a fruktosy Pomůcky: zkumavky, lžička na chemikálie, kádinka, stojan, držák, kruh, síťka, plynový kahan, zápalky Chemikálie: fruktosa,
Potenciometrické stanovení disociační konstanty
 Potenciometrické stanovení disociační konstanty TEORIE Elektrolytická disociace kyseliny HA ve vodě vede k ustavení disociační rovnováhy: HA + H 2O A - + H 3O +, kterou lze charakterizovat disociační konstantou
Potenciometrické stanovení disociační konstanty TEORIE Elektrolytická disociace kyseliny HA ve vodě vede k ustavení disociační rovnováhy: HA + H 2O A - + H 3O +, kterou lze charakterizovat disociační konstantou
ORGANICKÁ CHEMIE Laboratorní práce č. 3
 Téma: Hydroxyderiváty uhlovodíků ORGANICKÁ CHEMIE Laboratorní práce č. 3 Úkol 1: Dokažte přítomnost ethanolu ve víně. Ethanol bezbarvá kapalina, která je základní součástí alkoholických nápojů. Ethanol
Téma: Hydroxyderiváty uhlovodíků ORGANICKÁ CHEMIE Laboratorní práce č. 3 Úkol 1: Dokažte přítomnost ethanolu ve víně. Ethanol bezbarvá kapalina, která je základní součástí alkoholických nápojů. Ethanol
Ústřední komise Chemické olympiády. 55. ročník 2018/2019 ŠKOLNÍ KOLO. Kategorie C ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ)
 Ústřední komise Chemické olympiády 55. ročník 2018/2019 ŠKOLNÍ KOLO Kategorie C ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ) PRAKTICKÁ ČÁST 40 BODŮ Autor RNDr. Jan Břížďala Gymnázium Třebíč RNDr. Jan Havlík, Ph.D.
Ústřední komise Chemické olympiády 55. ročník 2018/2019 ŠKOLNÍ KOLO Kategorie C ZADÁNÍ PRAKTICKÉ ČÁSTI (40 BODŮ) PRAKTICKÁ ČÁST 40 BODŮ Autor RNDr. Jan Břížďala Gymnázium Třebíč RNDr. Jan Havlík, Ph.D.
Návod k laboratornímu cvičení. Bílkoviny
 Úkol č. 1: Důkazy bílkovin ve vaječném bílku a) natvrdo uvařené vejce s kyselinou dusičnou Pomůcky: Petriho miska, pipeta, nůž. Návod k laboratornímu cvičení Bílkoviny Chemikálie: koncentrovaná kyselina
Úkol č. 1: Důkazy bílkovin ve vaječném bílku a) natvrdo uvařené vejce s kyselinou dusičnou Pomůcky: Petriho miska, pipeta, nůž. Návod k laboratornímu cvičení Bílkoviny Chemikálie: koncentrovaná kyselina
Bádáme v kroužku chemie
 Bádáme v kroužku chemie Tento modul obsahuje náměty aktivit, které jsou vhodné pro realizaci ve volnočasových kroužcích chemie na základní škole, popř. na nižším stupni osmiletého gymnázia. Autor: Mgr.
Bádáme v kroužku chemie Tento modul obsahuje náměty aktivit, které jsou vhodné pro realizaci ve volnočasových kroužcích chemie na základní škole, popř. na nižším stupni osmiletého gymnázia. Autor: Mgr.
2.01 Aerobní/anaerobní reakce aneb kvasinky v akci. Projekt Trojlístek
 2. Vlastnosti látek a chemické reakce 2.01 Aerobní/anaerobní reakce aneb kvasinky v akci. Projekt úroveň 1 2 3 1. Předmět výuky Metodika je určena pro vzdělávací obsah vzdělávacího předmětu Chemie. Chemie
2. Vlastnosti látek a chemické reakce 2.01 Aerobní/anaerobní reakce aneb kvasinky v akci. Projekt úroveň 1 2 3 1. Předmět výuky Metodika je určena pro vzdělávací obsah vzdělávacího předmětu Chemie. Chemie
STUPNĚ ph NEUTRALIZACE PROJEKT EU PENÍZE ŠKOLÁM OPERAČNÍ PROGRAM VZDĚLÁVÁNÍ PRO KONKURENCESCHOPNOST
 STUPNĚ ph NEUTRALIZACE PROJEKT EU PENÍZE ŠKOLÁM OPERAČNÍ PROGRAM VZDĚLÁVÁNÍ PRO KONKURENCESCHOPNOST MĚŘÍME STUPEŇ KYSELOSTI STUPNICE ph SLOUŽÍ K URČOVÁNÍ STUPNĚ KYSELOSTI NEBO ZÁSADITOSTI HODNOCENÍ JE
STUPNĚ ph NEUTRALIZACE PROJEKT EU PENÍZE ŠKOLÁM OPERAČNÍ PROGRAM VZDĚLÁVÁNÍ PRO KONKURENCESCHOPNOST MĚŘÍME STUPEŇ KYSELOSTI STUPNICE ph SLOUŽÍ K URČOVÁNÍ STUPNĚ KYSELOSTI NEBO ZÁSADITOSTI HODNOCENÍ JE
Návod k laboratornímu cvičení. Alkoholy
 Úkol č. 1: Ověřování fyzikálních vlastností alkoholů Návod k laboratornímu cvičení Alkoholy Pomůcky: 3 velké zkumavky - A,B,C, hodinové sklíčko, kapátko nebo skleněná tyčinka Chemikálie: etanol (F), etan-1,2-
Úkol č. 1: Ověřování fyzikálních vlastností alkoholů Návod k laboratornímu cvičení Alkoholy Pomůcky: 3 velké zkumavky - A,B,C, hodinové sklíčko, kapátko nebo skleněná tyčinka Chemikálie: etanol (F), etan-1,2-
SOLI VZNIK PROJEKT EU PENÍZE ŠKOLÁM OPERAČNÍ PROGRAM VZDĚLÁVÁNÍ PRO KONKURENCESCHOPNOST
 SOLI VZNIK PROJEKT EU PENÍZE ŠKOLÁM OPERAČNÍ PROGRAM VZDĚLÁVÁNÍ PRO KONKURENCESCHOPNOST SOLI SOLI JSOU CHEMICKÉ SLOUČENINY SLOŽENÉ Z KATIONTŮ KOVŮ A ANIONTŮ KYSELIN 1. NEUTRALIZACÍ VZNIK SOLÍ 2. REAKCÍ
SOLI VZNIK PROJEKT EU PENÍZE ŠKOLÁM OPERAČNÍ PROGRAM VZDĚLÁVÁNÍ PRO KONKURENCESCHOPNOST SOLI SOLI JSOU CHEMICKÉ SLOUČENINY SLOŽENÉ Z KATIONTŮ KOVŮ A ANIONTŮ KYSELIN 1. NEUTRALIZACÍ VZNIK SOLÍ 2. REAKCÍ
Gymnázium a Střední odborná škola, Rokycany, Mládežníků 1115
 Gymnázium a Střední odborná škola, Rokycany, Mládežníků 1115 Číslo projektu: CZ.1.07/1.5.00/34.0410 Číslo šablony: 19 Název materiálu: Ročník: Identifikace materiálu: Jméno autora: Předmět: Tématický celek:
Gymnázium a Střední odborná škola, Rokycany, Mládežníků 1115 Číslo projektu: CZ.1.07/1.5.00/34.0410 Číslo šablony: 19 Název materiálu: Ročník: Identifikace materiálu: Jméno autora: Předmět: Tématický celek:
Laboratorní cvičení z kinetiky chemických reakcí
 Laboratorní cvičení z kinetiky chemických reakcí LABORATORNÍ CVIČENÍ 1. Téma: Ovlivňování průběhu reakce změnou koncentrace látek. podmínek průběhu reakce. Jednou z nich je změna koncentrace výchozích
Laboratorní cvičení z kinetiky chemických reakcí LABORATORNÍ CVIČENÍ 1. Téma: Ovlivňování průběhu reakce změnou koncentrace látek. podmínek průběhu reakce. Jednou z nich je změna koncentrace výchozích
1.08 Tvrdost vody. Projekt Trojlístek
 1. Chemie a společnost 1.08. Projekt úroveň 1 2 3 1. Předmět výuky Metodika je určena pro vzdělávací obsah vzdělávacího předmětu Chemie. Chemie 2. Cílová skupina Metodika je určena pro žáky 2. stupně ZŠ
1. Chemie a společnost 1.08. Projekt úroveň 1 2 3 1. Předmět výuky Metodika je určena pro vzdělávací obsah vzdělávacího předmětu Chemie. Chemie 2. Cílová skupina Metodika je určena pro žáky 2. stupně ZŠ
Název: Barvy chromu. Autor: Mgr. Jiří Vozka, Ph.D. Název školy: Gymnázium Jana Nerudy, škola hl. města Prahy
 Název: Barvy chromu Autor: Mgr. Jiří Vozka, Ph.D. Název školy: Gymnázium Jana Nerudy, škola hl. města Prahy Předmět, mezipředmětové vztahy: chemie, biologie Ročník: 3. Tématický celek: Systematická anorganická
Název: Barvy chromu Autor: Mgr. Jiří Vozka, Ph.D. Název školy: Gymnázium Jana Nerudy, škola hl. města Prahy Předmět, mezipředmětové vztahy: chemie, biologie Ročník: 3. Tématický celek: Systematická anorganická
Typy chemických reakcí Laboratorní práce
 Typy chemických reakcí Laboratorní práce VY_52_INOVACE_212 Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Chemie Ročník: 9 Typy chemických reakcí Laboratorní práce Jméno Třída..Datum Úkol: Proveďte
Typy chemických reakcí Laboratorní práce VY_52_INOVACE_212 Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Chemie Ročník: 9 Typy chemických reakcí Laboratorní práce Jméno Třída..Datum Úkol: Proveďte
Praktické ukázky analytických metod ve vinařství
 Praktické ukázky analytických metod ve vinařství Ing. Mojmír Baroň Stanovení v moštu Stanovení ph a veškerých titrovatelných kyselin Stanovení ph Princip: Hodnota ph je záporný dekadický logaritmus aktivity
Praktické ukázky analytických metod ve vinařství Ing. Mojmír Baroň Stanovení v moštu Stanovení ph a veškerých titrovatelných kyselin Stanovení ph Princip: Hodnota ph je záporný dekadický logaritmus aktivity
chemie Měření ph elektrolytů, hydrolýza solí Cíle Podrobnější rozbor cílů Zařazení do výuky Časová náročnost Zadání úlohy Návaznost experimentů
 Měření ph elektrolytů, hydrolýza solí pracovní návod s metodickým komentářem pro učitele připravil M. Škavrada chemie 07 úloha číslo Cíle Cílem tohoto laboratorního cvičení je měření ph silných a slabých
Měření ph elektrolytů, hydrolýza solí pracovní návod s metodickým komentářem pro učitele připravil M. Škavrada chemie 07 úloha číslo Cíle Cílem tohoto laboratorního cvičení je měření ph silných a slabých
Jazykové gymnázium Pavla Tigrida, Ostrava-Poruba Název projektu: Podpora rozvoje praktické výchovy ve fyzice a chemii
 Datum: Jazykové gymnázium Pavla Tigrida, Ostrava-Poruba Název projektu: Podpora rozvoje praktické výchovy ve fyzice a chemii Laboratorní cvičení č. Tlak vzduchu: Teplota vzduchu: Bílkoviny(proteiny) Vlhkost
Datum: Jazykové gymnázium Pavla Tigrida, Ostrava-Poruba Název projektu: Podpora rozvoje praktické výchovy ve fyzice a chemii Laboratorní cvičení č. Tlak vzduchu: Teplota vzduchu: Bílkoviny(proteiny) Vlhkost
I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í
 I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY Laboratorní práce č. 8 Sacharidy Pro potřeby projektu
I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY Laboratorní práce č. 8 Sacharidy Pro potřeby projektu
I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í LABORATORNÍ PRÁCE Č. 6 PRÁCE S PLYNY
 LABORATORNÍ PRÁCE Č. 6 PRÁCE S PLYNY Mezi nejrozšířenější práce s plyny v laboratoři patří příprava a důkazy oxidu uhličitého CO 2, kyslíku O 2, vodíku H 2, oxidu siřičitého SO 2 a amoniaku NH 3. Reakcí
LABORATORNÍ PRÁCE Č. 6 PRÁCE S PLYNY Mezi nejrozšířenější práce s plyny v laboratoři patří příprava a důkazy oxidu uhličitého CO 2, kyslíku O 2, vodíku H 2, oxidu siřičitého SO 2 a amoniaku NH 3. Reakcí
Ústřední komise Chemické olympiády. 55. ročník 2018/2019 KRAJSKÉ KOLO. Kategorie E ZADÁNÍ PRAKTICKÉ ČÁSTI (50 BODŮ)
 Ústřední komise Chemické olympiády 55. ročník 2018/2019 KRAJSKÉ KOLO Kategorie E ZADÁNÍ PRAKTICKÉ ČÁSTI (50 BODŮ) Úloha 1 Stanovení Bi 3+ a Zn 2+ ve směsi 50 bodů Chelatometricky lze stanovit ionty samostatně,
Ústřední komise Chemické olympiády 55. ročník 2018/2019 KRAJSKÉ KOLO Kategorie E ZADÁNÍ PRAKTICKÉ ČÁSTI (50 BODŮ) Úloha 1 Stanovení Bi 3+ a Zn 2+ ve směsi 50 bodů Chelatometricky lze stanovit ionty samostatně,
Dovednosti/Schopnosti. - orientuje se v ČL, který vychází z Evropského lékopisu;
 Jednotka učení 4a: Stanovení obsahu Ibuprofenu 1. diferencování pracovního úkolu Handlungswissen Charakteristika pracovní činnosti Pracovní postup 2. HINTERFRAGEN 3. PŘIŘAZENÍ... Sachwissen Charakteristika
Jednotka učení 4a: Stanovení obsahu Ibuprofenu 1. diferencování pracovního úkolu Handlungswissen Charakteristika pracovní činnosti Pracovní postup 2. HINTERFRAGEN 3. PŘIŘAZENÍ... Sachwissen Charakteristika
Funkce chemického pokusu ve výuce chemie
 Funkce chemického pokusu ve výuce Funkce vyplývají ze struktury pokusu a charakteristiky výuky a vzhledem k cílům výuky Informativní Formativní Metodologická Vyberte si každý jednu chemickou reakci (z
Funkce chemického pokusu ve výuce Funkce vyplývají ze struktury pokusu a charakteristiky výuky a vzhledem k cílům výuky Informativní Formativní Metodologická Vyberte si každý jednu chemickou reakci (z
Stanovení celkové kyselosti nápojů potenciometrickou titrací
 Stanovení celkové kyselosti nápojů potenciometrickou titrací Princip metody U acidobazických titrací se využívají dva druhy indikace bodu ekvivalence - vizuální a instrumentální. K vizuální indikaci bodu
Stanovení celkové kyselosti nápojů potenciometrickou titrací Princip metody U acidobazických titrací se využívají dva druhy indikace bodu ekvivalence - vizuální a instrumentální. K vizuální indikaci bodu
Oborový workshop pro ZŠ CHEMIE
 PRAKTICKÁ VÝUKA PŘÍRODOVĚDNÝCH PŘEDMĚTŮ NA ZŠ A SŠ CZ.1.07/1.1.30/02.0024 Tento projekt je spolufinancován Evropským sociálním fondem a státním rozpočtem České republiky. Oborový workshop pro ZŠ CHEMIE
PRAKTICKÁ VÝUKA PŘÍRODOVĚDNÝCH PŘEDMĚTŮ NA ZŠ A SŠ CZ.1.07/1.1.30/02.0024 Tento projekt je spolufinancován Evropským sociálním fondem a státním rozpočtem České republiky. Oborový workshop pro ZŠ CHEMIE
Reakce kyselin a zásad
 seminář 6. 1. 2011 Chemie Reakce kyselin a zásad Známe několik teorií, které charakterizují definují kyseliny a zásady. Nejstarší je Arrheniova teorie, která je platná pro vodné prostředí, podle které
seminář 6. 1. 2011 Chemie Reakce kyselin a zásad Známe několik teorií, které charakterizují definují kyseliny a zásady. Nejstarší je Arrheniova teorie, která je platná pro vodné prostředí, podle které
Moravské gymnázium Brno s.r.o. RNDr. Miroslav Štefan. Chemie obecná síla kyselin a zásad. Datum tvorby 11.12.2013
 Číslo projektu CZ.1.07/1.5.00/34.0743 Název školy Autor Tematická oblast Ročník Moravské gymnázium Brno s.r.o. RNDr. Miroslav Štefan Chemie obecná síla kyselin a zásad 1. ročník Datum tvorby 11.12.2013
Číslo projektu CZ.1.07/1.5.00/34.0743 Název školy Autor Tematická oblast Ročník Moravské gymnázium Brno s.r.o. RNDr. Miroslav Štefan Chemie obecná síla kyselin a zásad 1. ročník Datum tvorby 11.12.2013
Vzdělávací oblast: Člověk a příroda. Vyučovací předmět: Chemie. Třída: tercie. Očekávané výstupy. Poznámky. Přesahy. Žák: Průřezová témata
 Vzdělávací oblast: Člověk a příroda Vyučovací předmět: Chemie Třída: tercie Očekávané výstupy Uvede příklady chemického děje a čím se zabývá chemie Rozliší tělesa a látky Rozpozná na příkladech fyzikální
Vzdělávací oblast: Člověk a příroda Vyučovací předmět: Chemie Třída: tercie Očekávané výstupy Uvede příklady chemického děje a čím se zabývá chemie Rozliší tělesa a látky Rozpozná na příkladech fyzikální
STŘEDNÍ ODBORNÁ ŠKOLA a STŘEDNÍ ODBORNÉ UČILIŠTĚ, Česká Lípa, 28. října 2707, příspěvková organizace. Digitální učební materiály
 Název školy Číslo projektu Název projektu Klíčová aktivita Označení materiálu: Typ materiálu: Předmět, ročník, obor: Tematická oblast: Téma: Jméno a příjmení autora: STŘEDNÍ ODBORNÁ ŠKOLA a STŘEDNÍ ODBORNÉ
Název školy Číslo projektu Název projektu Klíčová aktivita Označení materiálu: Typ materiálu: Předmět, ročník, obor: Tematická oblast: Téma: Jméno a příjmení autora: STŘEDNÍ ODBORNÁ ŠKOLA a STŘEDNÍ ODBORNÉ
ODMĚRNÁ ANALÝZA - TITRACE
 LABORATORNÍ PRÁCE Č. 35 ODMĚRNÁ ANALÝZA - TITRACE PRINCIP Odměrnou analýzou (titrací) se stanovuje obsah určité složky ve vzorku. Podstatou odměrného stanovení je chemická reakce mezi odměrným roztokem
LABORATORNÍ PRÁCE Č. 35 ODMĚRNÁ ANALÝZA - TITRACE PRINCIP Odměrnou analýzou (titrací) se stanovuje obsah určité složky ve vzorku. Podstatou odměrného stanovení je chemická reakce mezi odměrným roztokem
Člověk a příroda - chemie volitelný předmět
 Vyučovací předmět: Období ročník: Učební texty: Člověk a příroda - chemie volitelný předmět 3. období 9. ročník Pro manuál pokusů byly vybrány pokusy z publikací: Seminář a praktikum z chemie (SPN Praha;
Vyučovací předmět: Období ročník: Učební texty: Člověk a příroda - chemie volitelný předmět 3. období 9. ročník Pro manuál pokusů byly vybrány pokusy z publikací: Seminář a praktikum z chemie (SPN Praha;
LP č. 5 - SACHARIDY. Autor: Mgr. Stanislava Bubíková. Datum (období) tvorby: 28. 2. 2013. Ročník: devátý
 LP č. 5 - SACHARIDY Autor: Mgr. Stanislava Bubíková Datum (období) tvorby: 28. 2. 2013 Ročník: devátý Vzdělávací oblast: Člověk a příroda / Chemie / Organické sloučeniny 1 Anotace: Žáci si prakticky vyzkouší
LP č. 5 - SACHARIDY Autor: Mgr. Stanislava Bubíková Datum (období) tvorby: 28. 2. 2013 Ročník: devátý Vzdělávací oblast: Člověk a příroda / Chemie / Organické sloučeniny 1 Anotace: Žáci si prakticky vyzkouší
Ústřední komise Chemické olympiády. 50. ročník 2013/2014. OKRESNÍ KOLO kategorie D ŘEŠENÍ SOUTĚŽNÍCH ÚLOH
 Ústřední komise Chemické olympiády 50. ročník 2013/2014 OKRESNÍ KOLO kategorie D ŘEŠENÍ SOUTĚŽNÍCH ÚLOH TEORETICKÁ ČÁST (70 BODŮ) Informace pro hodnotitele Ve výpočtových úlohách jsou uvedeny dílčí výpočty
Ústřední komise Chemické olympiády 50. ročník 2013/2014 OKRESNÍ KOLO kategorie D ŘEŠENÍ SOUTĚŽNÍCH ÚLOH TEORETICKÁ ČÁST (70 BODŮ) Informace pro hodnotitele Ve výpočtových úlohách jsou uvedeny dílčí výpočty
LP č. 3 - ESTERY. Autor: Mgr. Stanislava Bubíková. Datum (období) tvorby: 27. 12. 2012. Ročník: devátý
 LP č. 3 - ESTERY Autor: Mgr. Stanislava Bubíková Datum (období) tvorby: 27. 12. 2012 Ročník: devátý Vzdělávací oblast: Člověk a příroda / Chemie / Organické sloučeniny 1 Anotace: Žáci prakticky vyzkouší
LP č. 3 - ESTERY Autor: Mgr. Stanislava Bubíková Datum (období) tvorby: 27. 12. 2012 Ročník: devátý Vzdělávací oblast: Člověk a příroda / Chemie / Organické sloučeniny 1 Anotace: Žáci prakticky vyzkouší
Název práce: Rostlinná buňka a látky v ní obsažené. Odstavce Vzdělávací cíl, Pomůcky a Inovace viz následující strana
 Datum: 30. 12. 2012 Projekt: Využití ICT techniky především v uměleckém vzdělávání Registrační číslo: CZ.1.07/1.5.00/34.1013 Číslo DUM: VY_32_INOVACE_270 Škola: Akademie - VOŠ, Gymn. a SOŠUP Světlá nad
Datum: 30. 12. 2012 Projekt: Využití ICT techniky především v uměleckém vzdělávání Registrační číslo: CZ.1.07/1.5.00/34.1013 Číslo DUM: VY_32_INOVACE_270 Škola: Akademie - VOŠ, Gymn. a SOŠUP Světlá nad
2.03 Endotermní/exotermní děje. Projekt Trojlístek
 2. Vlastnosti látek a chemické reakce 2.03 Endotermní/exotermní děje. Projekt úroveň 1 2 3 1. Předmět výuky Metodika je určena pro vzdělávací obsah vzdělávacího předmětu Chemie. Chemie 2. Cílová skupina
2. Vlastnosti látek a chemické reakce 2.03 Endotermní/exotermní děje. Projekt úroveň 1 2 3 1. Předmět výuky Metodika je určena pro vzdělávací obsah vzdělávacího předmětu Chemie. Chemie 2. Cílová skupina
VZNIK SOLÍ, NEUTRALIZACE
 VZNIK SOLÍ, NEUTRALIZACE Autor: Mgr. Stanislava Bubíková Datum (období) tvorby: 25. 4. 2013 Ročník: osmý Vzdělávací oblast: Člověk a příroda / Chemie / anorganické sloučeniny 1 Anotace: Žáci se seznámí
VZNIK SOLÍ, NEUTRALIZACE Autor: Mgr. Stanislava Bubíková Datum (období) tvorby: 25. 4. 2013 Ročník: osmý Vzdělávací oblast: Člověk a příroda / Chemie / anorganické sloučeniny 1 Anotace: Žáci se seznámí
Ústřední komise Chemické olympiády. 42. ročník. KRAJSKÉ KOLO Kategorie D. SOUTĚŽNÍ ÚLOHY TEORETICKÉ ČÁSTI Časová náročnost: 60 minut
 Ústřední komise Chemické olympiády 42. ročník 2005 2006 KRAJSKÉ KOLO Kategorie D SOUTĚŽNÍ ÚLOHY TEORETICKÉ ČÁSTI Časová náročnost: 60 minut Institut dětí a mládeže Ministerstva školství, mládeže a tělovýchovy
Ústřední komise Chemické olympiády 42. ročník 2005 2006 KRAJSKÉ KOLO Kategorie D SOUTĚŽNÍ ÚLOHY TEORETICKÉ ČÁSTI Časová náročnost: 60 minut Institut dětí a mládeže Ministerstva školství, mládeže a tělovýchovy
Sešit pro laboratorní práci z chemie
 Sešit pro laboratorní práci z chemie téma: Příprava oxidu měďnatého autor: ing. Alena Dvořáková vytvořeno při realizaci projektu: Inovace školního vzdělávacího programu biologie a chemie registrační číslo
Sešit pro laboratorní práci z chemie téma: Příprava oxidu měďnatého autor: ing. Alena Dvořáková vytvořeno při realizaci projektu: Inovace školního vzdělávacího programu biologie a chemie registrační číslo
POČÍTAČEM PODPOROVANÝ EXPERIMENT JAROSLAV VYSKOČIL, ONDŘEJ KOŠEK
 POČÍTAČEM PODPOROVANÝ EXPERIMENT JAROSLAV VYSKOČIL, ONDŘEJ KOŠEK Ondřej Košek Jaroslav Vyskočil OBSAH Jaké místo má počítačem podporovaný experiment ve výuce? Konkrétní měřící systémy, jejich představení
POČÍTAČEM PODPOROVANÝ EXPERIMENT JAROSLAV VYSKOČIL, ONDŘEJ KOŠEK Ondřej Košek Jaroslav Vyskočil OBSAH Jaké místo má počítačem podporovaný experiment ve výuce? Konkrétní měřící systémy, jejich představení
CHEMIE - ÚVOD. Autor: Mgr. Stanislava Bubíková. Datum (období) tvorby: 13. 2. 2012. Ročník: osmý
 Autor: Mgr. Stanislava Bubíková CHEMIE - ÚVOD Datum (období) tvorby: 13. 2. 2012 Ročník: osmý Vzdělávací oblast: Člověk a příroda / Chemie / Pozorování, pokus a bezpečnost práce 1 Anotace: Žáci se seznámí
Autor: Mgr. Stanislava Bubíková CHEMIE - ÚVOD Datum (období) tvorby: 13. 2. 2012 Ročník: osmý Vzdělávací oblast: Člověk a příroda / Chemie / Pozorování, pokus a bezpečnost práce 1 Anotace: Žáci se seznámí
