Laboratorní návod - Stanovení molární hmotnosti snadno těkavé látky metodou Viktora Meyera 1
|
|
|
- Filip Netrval
- před 8 lety
- Počet zobrazení:
Transkript
1 Laboratorní návod - Stanovení molární hmotnosti snadno těkavé látky metodou Viktora Meyera 1 Molární hmotnost M látky je definována jako podíl hmotnosti m a odpovídajícího látkového množství n Jednotkou molární hmotnosti M v soustavě SI je kg mol -1. Látkové množství udává počet částic s tím, že jeden mol obsahuje počet částic daný hodnotou Avogadrovy konstanty (6, mol -1 ). Metoda V. Meyera je zajímavou aplikací Avogadrova zákona, podle kterého stejná látková množství různých plynných látek, které se chovají jako ideální plyn, zaujímají za stejné teploty a tlaku stejný objem. Metoda spočívá v tom, že do objemu vzduchu uzavřeného v trubici vpravíme známé množství kapalné látky, která se vypaří a promění v přehřátou páru. Pára této látky má během expanze přibližně stejnou teplotu a tlak jako vzduch, který tlačí před sebou. Po ukončení děje, kdy se předpokládáme pístový tok plynů aparaturou, zaujme pára stejný prostor, jako měl vzduch, který vytlačila. Vzduch je vytlačen do termostatovaného prostoru umožňujícího změření objemu (teplota nemusí být nutně stejná jako teplota pece, jen nesmí docházet ke změnám rozložení teploty v jednotlivých místech aparatury). Platnost Avogadrova zákona se předpokládá v celé aparatuře a proto platí, že látkové množství vytlačeného vzduchu, u kterého změříme objem, je stejné, jako látkové množství vypařené látky, jejíž molární hmotnost zjišťujeme. Proto můžeme ze stavových veličin vytlačeného vzduchu vypočítat za předpokladu ideálního chování molární hmotnost zkoumané látky. Při atmosférickém tlaku (tzn. hodnoty do řádově 100 kpa) lze popsat chování plynů a par s dobrou přesností stavovou rovnicí ideálního plynu kde molární hmotnost M je stanovovaná veličina.měřenými veličinami jsou objem vzduchu V v byretě při tlaku p a termodynamické teplotě T (teplota v byretě). Vzduch je vypuzen z přístroje do plynové byrety párou kapaliny, jejíž molární hmotnost zjišťujeme, kdy známé její hmotnost m. V rovnici (4.2) značí R molární (univerzální) plynovou konstantu, která je přírodní konstantou a má pro všechny plyny stejnou hodnotu R = 8,3143 (± 0,0012) J mol -1 K - 1. Úpravou rovnice (4.2) obdržíme pro molární hmotnost měřené látky výraz Metoda je rychlá a přesná, není však vhodná ke stanovení molární hmotnosti látek, které za daných podmínek podléhají disociaci nebo asociaci. 1 Nedílnou součástí tohoto návodu je doplněk popisující statistické zpracování naměřených dat
2 Pokusné zařízení Základní částí přístroje je výparná baňka zasunutá do elektrické pece (obr. 4.1). Dno baňky je převrstveno skleněnými kuličkami. Baňka je opatřena trubicí, v jejíž horní části je šikmo umístěno otáčivé shazovací zařízení, jímž se vzorek kapaliny zatavený ve skleněné ampulce (baničce) spouští do výparné baňky. Ve vyhřátém prostoru výparné baňky ampulka praskne a Obr. 4.1 Obr. 4.2 páry zkoumané látky vypudí vzduch, který se odvádí bočním vývodem do plynové byrety naplněné vodou. Ke spodnímu konci byrety je připojena vyrovnávací nádoba k eliminaci vypařením vzniklého rozdílu mezi tlakem uvnitř přístroje a barometrickým tlakem. Teplota vypuzeného vzduchu se odečítá na teploměru umístěném v temperačním plášti plynové byrety. Postup práce POVINNOSTÍ STUDENTA JE POUŽÍVAT OCHRANNÝ ŠTÍT NEBO OCHRANNÉ BRÝLE A TO V KAŽDÉ FÁZI PŘÍPRAVY BANIČEK A PRÁCE S APARATUROU!!!!! Přípravné práce Pec zapínáme na pokyn asistenta hned na začátku pracovního dne, neboť musí vyhřívat 1 až 2 hodiny před zahájením vlastního měření. Teplotu pece nastavíme asi na 220 až 230 C, pokud asistent neudá jinak. Neměňte nastavení regulátoru teploty pece!!! Nastavení parametrů regulátoru je velice zdlouhavá a komplikovaná záležitost. Zatímco roztápíme pec, ethanolem vyčistíme a poté vysušíme výparnou baňku a skleněné kuličky. Na dno suché baňky nasypeme skleněné kuličky asi do výše 2 cm a baňku upevníme v peci tak, aby její dno bylo asi 15 cm nad dnem pece (nejteplejší místo v peci!). Otvor v peci okolo stopky výparné baňky zakryjte. Dále je třeba očistit zábrus shazovacího zařízení od případných střípků a namazat ho. Pokud jsou výparná baňka či kuličky mokré, je nutné výparnou baňku s kuličkami vysušit. To se provádí tak, že výparná baňka se boční olivkou připojí k vodní vývěvě, jádro spouštěcího zařízení se zasune do zábrusu a do horního otvoru
3 výparné baňky se zasune dlouhá trubice provlečená zátkou, která umožňuje vysušení výparné baňky proudícím vzduchem (viz bod 7 níže uvedeného postupu práce s aparaturou). Bez zbytečné prodlevy je pak potřeba zahájit výrobu prázdných baniček, následně je plnit, vážit a posléze zahájit měření, kdy se změří dva až třikrát pro kontrolu vzorek toluenu a následně minimálně desetkrát neznámý vzorek. Je třeba si vypracovat efektivní postup práce, aby nedocházelo k časovým ztrátám. Vzorky kapaliny se zatavují do malých skleněných ampulek, které se zhotovují z připravené kapilární trubičky za použití kahanu následujícím způsobem. Kapilární trubičku ohřejeme na jednom místě malým svítivým plamenem a po jejím změknutí ji ihned vytáhneme (mimo plamen!) v tenkou kapiláru. Totéž opakujeme na místě vzdáleném asi o 15 mm, takže nám mezi oběma kapilárami vznikne malá banička. Nyní stačí nyní jednu z kapilár odtavit, druhou zkrátit na cca 50 mm a ampulka je hotova. Celý postup je naznačen na obr Jsou-li ampulky tenkostěnné, váží kolem 60 mg. Jestliže váží více než 100 mg, při pokusech zpravidla obtížně praskají. Správnou velikost ampulek určíme orientačním pokusem. Navážka má vytlačit do byrety 20 až 30 cm 3 vzduchu. Vyrobené a zvážené prázdné ampulky, které uchováváme ve stojánku s očíslovanými pozicemi, aby nedošlo k záměně, se následně plní toluenem nebo vzorkem. Ampulku uchopíme do pinzety, mírně ji ohřejeme nad malým svítivým plamenem a pak rychle ponoříme konec kapilárního hrdla do kapaliny a vyčkáme, až se malé množství látky vsaje do nádobky. Nasátou kapalinu setřeseme na dno nádobky a znovu opatrně zahříváme, až kapalina začne vřít a vypudí z nádobky vzduch. V tom okamžiku znovu rychle ponoříme ampulku do lahvičky se vzorkem. Většinou se tím celá naplní. Pokud v ampulce zůstává větší vzduchová bublina, musíme vyvařování opakovat. Hrdélko naplněné ampulky pečlivě osušíme, ampulku případně zchladíme ponořením jejího tělíčka do studené vody a otevřený konec kapiláry rychle zatavíme. Potom ampulku osušíme a znovu zvážíme. Važte vždy na stejných vahách! Nezapomeňte na kontrolu nulové polohy. Po ustálení teploty v peci je možné začít s měřením. Správnost postupu a přesnost práce si ověříme na známé látce (toluen, aceton apod.), potom teprve přikročíme ke stanovení molární hmotnosti neznámého vzorku, se kterým se provede minimálně 10 měření. Z hlediska využití času je efektivní zahájit měření s naplněnými baničkami co nejdříve, přičemž je zbytečné čekat až do doby, než jsou naplněné všechny baničky. Je záhodno začít s měřením už ve chvíli, kdy jsou k dispozici cca tři naplněné baničky. Čas k naplnění zbylých baniček je k dispozici během odsávání par z výparné baňky mezi jednotlivými experimenty (viz níže). Postup měření na aparatuře 1. Pomocí silikonové hadičky spojíme byretu s výparnou baňkou. 2. Do spouštěcího zařízení se ve vodorovné poloze vloží hrdlem k rukojeti naplněná, zatavená a zvážená banička se vzorkem (Obr. 4.3.) a celé zařízení se zasune do boční trubice výparné baňky. (Obr. 4.4.) Aby zařízení těsnilo, je nutné předem opatřit zábrusy tenkou vrstvou mazacího tuku (zmíněno výše) a udržovat je prosté hrubých nečistot. Pokud je zařízení znečištěné mazacím tukem uvnitř, banička se přilepí a nevypadne.
4 Obr Vsunutí baničky do shazovacího zařízení Obr Vhazovací zařízení připraveno k akci 3. Horní konec výparné trubice se uzavře zátkou. Byretu i výparnou baňku spojíme s vnější atmosférou otočením trojcestného kohoutu do příslušné polohy. Vyrovnávací nádobu byrety upevníme tak, aby se hladina vody v byretě ustálila přibližně na počátku stupnice. Počkáme cca 5 minut na vytemperování (pokud nedojde k ustálení teploty, došlo by v aparatuře k objemovým změnám plynu v důsledku změn teploty a to by vedlo k nepřesnému určení vytlačeného objemu). Po vyrovnání tlaku a teploty a nastavení polohy hladiny se kohout přetočí tak, aby zůstala průchozí pouze cesta mezi výparnou baňkou a byretou, ale zároveň byl zaslepen zavzdušňovací otvor. 4. Nyní vyzkoušíme, zda přístroj těsní a teplota v peci zůstává stálá. O tom se přesvědčíme snížením vyrovnávací baňky plynové byrety. Jestliže meniskus po počátečním malém poklesu zůstává nadále na témže místě, můžeme zahájit měření (pro jistotu můžeme umístit vyrovnávací nádobu i nad hladinu vody v byretě a ani v tomto případě nesmí docházet k vyrovnání hladin v tomto případě pozor na vniknutí kapaliny z byrety do výparné baňky!!!!!!!!). Netěsní-li trojcestný kohout nebo jádro spouštěcího zařízení, očistíme zábrus od starého tuku (v případě nutnosti rozpouštědlem - např. toluen) a znovu
5 naneseme slabou vrstvu tuku. Netěsnost může způsobovat i zátka v horním otvoru výparné baňky popř. spojení mezi byretou a výparnou baňkou. 5. Pokud aparatura těsní, vyrovnáme hladiny v byretě a vyrovnávací nádobce a zjistíme počáteční polohu menisku v byretě. Pokud to není přesně nula, hodnotu si poznamenáme, abychom ji mohli odečíst na konci měření od konečné polohy menisku a získali tak správnou hodnotu vytlačeného objemu. Vyrovnávací nádobku vrátíme do stojanu 6. Nyní pootočíme spouštěcí zařízení o 180 a tím spustíme ampulku do výparné baňky (Obr. 4.5). Při spouštění baničky je nutné spouštěcí zařízení i horní zátku přidržovat, ev. zajistit gumičkou, aby přetlak par po prasknutí baňky nevyrazil shazovací zařízení nebo zátku z výparné trubice. Ampulka zpravidla po několika vteřinách praskne a hladina vody v byretě rychle klesá. Se zařízením manipulujte opatrně a s citem. Je to jenom sklo! Obr Spuštění baničky Po přibližném ustálení menisku vyrovnáme co nejpřesněji hladiny v byretě a ve vyrovnávací nádobě, vyčkáme do úplného ustálení menisku a odečteme objem vytlačeného vzduchu (nezapomeneme případně na odečtenou počáteční polohu menisku). Zaznamenáme si hodnoty teploty v byretě a atmosférického tlaku, který zjistíme na digitálním barometru. 7. Z trubice vyjmeme horní zátku a na dno baňky zavedeme odsávací trubici. Rozpojíme hadičku mezi byretou a výparnou baňkou a na boční olivku výparné baňky připojíme hadici připojující vodní vývěvu. Výparnou baňkou, která přitom zůstává v peci, prosáváme po 10 minut vzduch. Tím je přístroj připraven k dalšímu měření, to znamená, že je možné začít s novou baničkou znovu od bodu jedna tohoto postupu. Pokud by se páry neodsávaly, začaly by při dalších měřeních kondenzovat v částech výparné trubice,
6 které jsou mimo pec, a to by způsobilo prudké oscilace menisku v byretě a bylo by nemožné přesně určit objem vytlačeného plynu. Zpracování naměřených údajů a vyhodnocení a) Výpočet bez korekcí: Do rovnice (4.3) dosadíme všechny experimentální údaje a konstantu R v soustavě SI, za p dosadíme atmosférický tlak. Výsledek uvedeme do protokolu. b) Přesnější výpočet s korekcemi: Pro přesnější výpočet musíme brát v úvahu dvě skutečnosti: 1. Vzduch vytlačený z výparné baňky je ve vodní byretě dosycován vodní parou, která se vypařuje z vodní hladiny a ze zbytků vody ulpělé na stěnách vodní byrety po poklesu hladiny. Je-li např. laboratorní vzduch (jehož teplota je přibližně rovna teplotě vodní byrety) nasycen z 60 %, pak se vzduch může dosytit maximálně na 100 % (kdy je parciální tlak vody roven tenzi vodní páry). Za tlak p dosadíme atmosférický tlak p', od kterého je odečtena korekce na vypařenou vodu kde u je nasycená tenze par vody při teplotě byrety. Tato korekce nepřesáhne 2,5 %, normálně se pohybuje mezi 1 a 2 %. 2. Páry látky v blízkosti bodu varu se nechovají jako ideální plyn. Zaujímají objem asi o 1% menší než by zaujímalo stejné množství ideálního plynu. Korekce na neidealitu a korekce na vlhkost se téměř kompenzují. Pro přesná měření bychom korekci na neidealitu určili např. z Redlichovy-Kwongovy rovnice nebo pomocí kompresibilitního diagramu. K tomu účelu bychom však museli stanovit i teplotu v peci. Vzhledem k tomu, že uvedené jevy se navzájem kompenzují, nebudeme uvažovat žádnou korekci, a výpočet molární hmotnosti se provede přímo z rovnice ideálního plynu (tj. rovnice 4.3). Výsledky pro vzorek i toluen upravíme do tabulky, ve které uvedeme pro každé jednotlivé měření číslo pokusu, navážku, objem odečtený na byretě, atmosférický tlak, teplotu a vypočtenou hodnotu molární hmotnosti.
7 Záhlaví tabulky: poř.č. m [g[ T [K] P [kpa] V [ml] M [g/mol] Minimálně 10 získaných hodnot molární hmotnosti vzorku zpracujete i statisticky. To znamená, že se vypočítá aritmetický průměr a určí interval spolehlivosti na úrovni 95%, to znamená interval, v kterém leží skutečná hodnota s pravděpodobností 95%. Postup statistického zpracování naměřených dat je popsán v kapitole Zpracování naměřených dat, která je k nalezení mezi návody k jednotlivým pracím na www stránce ÚFCH. Osnova postupu práce: 1. Vyhřívání pece s baňky s kuličkami. 2. Výroba a vážení prázdných ampulek, jejich plnění a opětovné zvážení. 3. Odsátí par vodní vývěvou. 4. Pokus: a) uzavření aparatury, kontrola těsnosti a vyrovnání hladin, zjištění počáteční polohy menisku b) spuštění ampulky, c) vyrovnání hladin a odečtení objemu, teploty a tlaku, d) otevření a odsátí par z aparatury. Přesnost a zdroje chyb Chyba stanovení v tomto provedení činí ± 1%. Zdroje chyb: Ampulky nepraskají: Jsou příliš silnostěnné; málo naplněné; jsou nedokonale zatavené nebo výparná baňka je málo vyhřátá, což může být zaviněno tím, že je umístěna na chladnějším místě v peci. Meniskus zvolna klesá: Ulomila se pouze špička ampulky a páry difundují pomalu hrdlem nádobky, výsledky jsou příliš vysoké. Meniskus zvolna stoupá: Za dlouhou dobu, kterou pokus trvá, část par se dostane do chladnější části výparné baňky, zkondenzuje a tím se zmenší objem. Pokus je nutno opakovat. Oscilace polohy menisku: Nedokonale vysušená výparná baňka s kuličkami. Tento jev je často doprovázen kondenzací vzorku na trubici výparné baňky nad pecí. Vyšší výsledky naměříme také v tom případě, když teplota v peci během pokusu klesla. Výsledky jsou příliš nízké: Teplota v peci během pokusu stoupla, vzorek byl vlhký nebo baňka či kuličky nebyly suché.
7 Tenze par kapalin. Obr. 7.1 Obr. 7.2
 7 Tenze par kapalin Tenze par (neboli tlak sytých, případně nasycených par) je tlak v jednosložkovém systému, kdy je za dané teploty v rovnováze fáze plynná s fází kapalnou nebo pevnou. Tenze par je nejvyšší
7 Tenze par kapalin Tenze par (neboli tlak sytých, případně nasycených par) je tlak v jednosložkovém systému, kdy je za dané teploty v rovnováze fáze plynná s fází kapalnou nebo pevnou. Tenze par je nejvyšší
Stanovení měrného tepla pevných látek
 61 Kapitola 10 Stanovení měrného tepla pevných látek 10.1 Úvod O teple se dá říci, že souvisí s energií neuspořádaného pohybu molekul. Úhrnná pohybová energie neuspořádaného pohybu molekul, pohybu postupného,
61 Kapitola 10 Stanovení měrného tepla pevných látek 10.1 Úvod O teple se dá říci, že souvisí s energií neuspořádaného pohybu molekul. Úhrnná pohybová energie neuspořádaného pohybu molekul, pohybu postupného,
FYZIKÁLNÍ PRAKTIKUM FJFI ČVUT V PRAZE. Měření Poissonovy konstanty vzduchu. Abstrakt
 FYZIKÁLNÍ PRAKTIKUM FJFI ČVUT V PRAZE Úloha 4: Měření dutých objemů vážením a kompresí plynu Datum měření: 23. 10. 2009 Měření Poissonovy konstanty vzduchu Jméno: Jiří Slabý Pracovní skupina: 1 Ročník
FYZIKÁLNÍ PRAKTIKUM FJFI ČVUT V PRAZE Úloha 4: Měření dutých objemů vážením a kompresí plynu Datum měření: 23. 10. 2009 Měření Poissonovy konstanty vzduchu Jméno: Jiří Slabý Pracovní skupina: 1 Ročník
Kalorimetrická měření I
 KATEDRA EXPERIMENTÁLNÍ FYZIKY PŘÍRODOVĚDECKÁ FAKULTA UNIVERZITY PALACKÉHO V OLOMOUCI FYZIKÁLNÍ PRAKTIKUM Z MOLEKULOVÉ FYZIKY A TERMODYNAMIKY Kalorimetrická měření I Úvod Teplo Teplo Q je určeno energií,
KATEDRA EXPERIMENTÁLNÍ FYZIKY PŘÍRODOVĚDECKÁ FAKULTA UNIVERZITY PALACKÉHO V OLOMOUCI FYZIKÁLNÍ PRAKTIKUM Z MOLEKULOVÉ FYZIKY A TERMODYNAMIKY Kalorimetrická měření I Úvod Teplo Teplo Q je určeno energií,
Úloha č.1: Stanovení molární tepelné kapacity plynu za konstantního tlaku
 Úloha č.1: Stanovení molární tepelné kapacity plynu za konstantního tlaku Teorie První termodynamický zákon je definován du dq dw (1) kde du je totální diferenciál vnitřní energie a dq a dw jsou neúplné
Úloha č.1: Stanovení molární tepelné kapacity plynu za konstantního tlaku Teorie První termodynamický zákon je definován du dq dw (1) kde du je totální diferenciál vnitřní energie a dq a dw jsou neúplné
Fyzikální praktikum FJFI ČVUT v Praze
 Fyzikální praktikum FJFI ČVUT v Praze Úloha 5: Měření Poissonovy konstanty a dutých objemů Datum měření: 10. 12. 2015 Skupina: 8, čtvrtek 7:30 Vypracoval: Tadeáš Kmenta Klasifikace: Část I Měření Poissonovy
Fyzikální praktikum FJFI ČVUT v Praze Úloha 5: Měření Poissonovy konstanty a dutých objemů Datum měření: 10. 12. 2015 Skupina: 8, čtvrtek 7:30 Vypracoval: Tadeáš Kmenta Klasifikace: Část I Měření Poissonovy
Měření povrchového napětí
 Měření povrchového napětí Úkol : 1. Změřte pomocí kapilární elevace povrchové napětí daných kapalin při dané teplotě. 2. Změřte pomocí kapkové metody povrchové napětí daných kapalin při dané teplotě. Pomůcky
Měření povrchového napětí Úkol : 1. Změřte pomocí kapilární elevace povrchové napětí daných kapalin při dané teplotě. 2. Změřte pomocí kapkové metody povrchové napětí daných kapalin při dané teplotě. Pomůcky
Laboratorní pomůcky, chemické nádobí
 Laboratorní pomůcky, chemické nádobí Laboratorní sklo: měkké (tyčinky, spojovací trubice, kapiláry) tvrdé označení SIMAX (většina varného a odměrného skla) Zahřívání skla: Tenkostěnné nádoby (kádinky,
Laboratorní pomůcky, chemické nádobí Laboratorní sklo: měkké (tyčinky, spojovací trubice, kapiláry) tvrdé označení SIMAX (většina varného a odměrného skla) Zahřívání skla: Tenkostěnné nádoby (kádinky,
4 STANOVENÍ KINEMATICKÉ A DYNAMICKÉ VISKOZITY OVOCNÉHO DŽUSU
 Laboratorní cvičení z předmětu Reologie potravin a kosmetických prostředků 4 STANOVENÍ KINEMATICKÉ A DYNAMICKÉ VISKOZITY OVOCNÉHO DŽUSU (KAPILÁRNÍ VISKOZIMETR UBBELOHDE) 1. TEORIE: Ve všech kapalných látkách
Laboratorní cvičení z předmětu Reologie potravin a kosmetických prostředků 4 STANOVENÍ KINEMATICKÉ A DYNAMICKÉ VISKOZITY OVOCNÉHO DŽUSU (KAPILÁRNÍ VISKOZIMETR UBBELOHDE) 1. TEORIE: Ve všech kapalných látkách
HUSTOTA PEVNÝCH LÁTEK
 HUSTOTA PEVNÝCH LÁTEK Hustota látek je základní informací o studované látce. V případě homogenní látky lze i odhadnout druh materiálu s pomocí známých tabulkovaných údajů (s ohledem na barvu a vzhled materiálu
HUSTOTA PEVNÝCH LÁTEK Hustota látek je základní informací o studované látce. V případě homogenní látky lze i odhadnout druh materiálu s pomocí známých tabulkovaných údajů (s ohledem na barvu a vzhled materiálu
215.1.9 - REKTIFIKACE DVOUSLOŽKOVÉ SMĚSI, VÝPOČET ÚČINNOSTI
 215.1.9 - REKTIFIKACE DVOUSLOŽKOVÉ SMĚSI, VÝPOČET ÚČINNOSTI ÚVOD Rektifikace je nejčastěji používaným procesem pro separaci organických látek. Je široce využívána jak v chemické laboratoři, tak i v průmyslu.
215.1.9 - REKTIFIKACE DVOUSLOŽKOVÉ SMĚSI, VÝPOČET ÚČINNOSTI ÚVOD Rektifikace je nejčastěji používaným procesem pro separaci organických látek. Je široce využívána jak v chemické laboratoři, tak i v průmyslu.
Tři experimenty, které se nevejdou do školní třídy. Mgr. Kateřina Vondřejcová
 Tři experimenty, které se nevejdou do školní třídy Mgr. Kateřina Vondřejcová Centrum talentů M&F&I, Univerzita Hradec Králové, 2010 1.. experiiment:: Změř s Thallésem výšku svojjíí školly Obr. 1: Thalés
Tři experimenty, které se nevejdou do školní třídy Mgr. Kateřina Vondřejcová Centrum talentů M&F&I, Univerzita Hradec Králové, 2010 1.. experiiment:: Změř s Thallésem výšku svojjíí školly Obr. 1: Thalés
Struktura a vlastnosti kapalin
 I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY Laboratorní práce č. 7 Struktura a vlastnosti kapalin
I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY Laboratorní práce č. 7 Struktura a vlastnosti kapalin
Na libovolnou plochu o obsahu S v atmosférickém vzduchu působí kolmo tlaková síla, kterou vypočítáme ze vztahu: F = pa. S
 MECHANICKÉ VLASTNOSTI PLYNŮ. Co už víme o plynech? Vlastnosti ply nů: 1) jsou snadno stlačitelné a rozpínavé 2) nemají vlastní tvar ani vlastní objem 3) jsou tekuté 4) jsou složeny z částic, které se neustále
MECHANICKÉ VLASTNOSTI PLYNŮ. Co už víme o plynech? Vlastnosti ply nů: 1) jsou snadno stlačitelné a rozpínavé 2) nemají vlastní tvar ani vlastní objem 3) jsou tekuté 4) jsou složeny z částic, které se neustále
Fyzikální praktikum FJFI ČVUT v Praze
 Fyzikální praktikum FJFI ČVUT v Praze Úloha 6: Kalibrace teploměru, skupenské teplo Datum měření: 17. 12. 2015 Skupina: 8, čtvrtek 7:30 Vypracoval: Tadeáš Kmenta Klasifikace: Část I Kalibrace rtuťového
Fyzikální praktikum FJFI ČVUT v Praze Úloha 6: Kalibrace teploměru, skupenské teplo Datum měření: 17. 12. 2015 Skupina: 8, čtvrtek 7:30 Vypracoval: Tadeáš Kmenta Klasifikace: Část I Kalibrace rtuťového
Mechanické vlastnosti kapalin a plynů. opakování
 Mechanické vlastnosti kapalin a plynů opakování 1 Jakým směrem se šíří tlak? 2 Chlapci si zhotovili model hydraulického lisu podle obrázku. Na písty ručních stříkaček působí stejnou silou. Který chlapec
Mechanické vlastnosti kapalin a plynů opakování 1 Jakým směrem se šíří tlak? 2 Chlapci si zhotovili model hydraulického lisu podle obrázku. Na písty ručních stříkaček působí stejnou silou. Který chlapec
1. Změřte teplotní závislost povrchového napětí destilované vody σ v rozsahu teplot od 295 do 345 K metodou bublin.
 1 Pracovní úkoly 1. Změřte teplotní závislost povrchového napětí destilované vody σ v rozsahu teplot od 295 do 35 K metodou bublin. 2. Měřenou závislost znázorněte graficky. Závislost aproximujte kvadratickou
1 Pracovní úkoly 1. Změřte teplotní závislost povrchového napětí destilované vody σ v rozsahu teplot od 295 do 35 K metodou bublin. 2. Měřenou závislost znázorněte graficky. Závislost aproximujte kvadratickou
Úloha č.2 Vážení. Jméno: Datum provedení: TEORETICKÝ ÚVOD
 Jméno: Obor: Datum provedení: TEORETICKÝ ÚVOD Jednou ze základních operací v biochemické laboratoři je vážení. Ve většině případů právě přesnost a správnost navažovaného množství látky má vliv na výsledek
Jméno: Obor: Datum provedení: TEORETICKÝ ÚVOD Jednou ze základních operací v biochemické laboratoři je vážení. Ve většině případů právě přesnost a správnost navažovaného množství látky má vliv na výsledek
T0 Teplo a jeho měření
 Teplo a jeho měření 1 Teplo 2 Kalorimetrie Kalorimetr 3 Tepelná kapacita 3.1 Měrná tepelná kapacita Měrná tepelná kapacita při stálém objemu a stálém tlaku Poměr měrných tepelných kapacit 3.2 Molární tepelná
Teplo a jeho měření 1 Teplo 2 Kalorimetrie Kalorimetr 3 Tepelná kapacita 3.1 Měrná tepelná kapacita Měrná tepelná kapacita při stálém objemu a stálém tlaku Poměr měrných tepelných kapacit 3.2 Molární tepelná
Mol. fyz. a termodynamika
 Molekulová fyzika pracuje na základě kinetické teorie látek a statistiky Termodynamika zkoumání tepelných jevů a strojů nezajímají nás jednotlivé částice Molekulová fyzika základem jsou: Látka kteréhokoli
Molekulová fyzika pracuje na základě kinetické teorie látek a statistiky Termodynamika zkoumání tepelných jevů a strojů nezajímají nás jednotlivé částice Molekulová fyzika základem jsou: Látka kteréhokoli
Kalibrace teploměru, skupenské teplo Abstrakt: V této úloze se studenti seznámí s metodou kalibrace teploměru a na základě svých
 Úloha 6 02PRA1 Fyzikální praktikum 1 Kalibrace teploměru, skupenské teplo Abstrakt: V této úloze se studenti seznámí s metodou kalibrace teploměru a na základě svých měření i ověří Gay-Lussacův zákon.
Úloha 6 02PRA1 Fyzikální praktikum 1 Kalibrace teploměru, skupenské teplo Abstrakt: V této úloze se studenti seznámí s metodou kalibrace teploměru a na základě svých měření i ověří Gay-Lussacův zákon.
TLAK PLYNU V UZAVŘENÉ NÁDOBĚ
 TLAK PLYNU V UZAVŘENÉ NÁDOBĚ Vzdělávací předmět: Fyzika Tematický celek dle RVP: Mechanické vlastnosti tekutin Tematická oblast: Mechanické vlastnosti plynů Cílová skupina: Žák 7. ročníku základní školy
TLAK PLYNU V UZAVŘENÉ NÁDOBĚ Vzdělávací předmět: Fyzika Tematický celek dle RVP: Mechanické vlastnosti tekutin Tematická oblast: Mechanické vlastnosti plynů Cílová skupina: Žák 7. ročníku základní školy
FYZIKÁLNÍ PRAKTIKUM FJFI ČVUT V PRAZE. Úloha 5: Kalibrace rtuťového teploměru plynovým teploměrem
 FYZIKÁLNÍ PRAKTIKUM FJFI ČVUT V PRAZE Úloha 5: Kalibrace rtuťového teploměru plynovým teploměrem Měření měrného skupenského tepla varu vody Datum měření: 30. 10. 2009 Jméno: Jiří Slabý Pracovní skupina:
FYZIKÁLNÍ PRAKTIKUM FJFI ČVUT V PRAZE Úloha 5: Kalibrace rtuťového teploměru plynovým teploměrem Měření měrného skupenského tepla varu vody Datum měření: 30. 10. 2009 Jméno: Jiří Slabý Pracovní skupina:
Teplota. fyzikální veličina značka t
 Teplota fyzikální veličina značka t Je to vlastnost předmětů a okolí, kterou je člověk schopen vnímat a přiřadit jí pocity studeného, teplého či horkého. Jak se tato vlastnost jmenuje? Teplota Naše pocity
Teplota fyzikální veličina značka t Je to vlastnost předmětů a okolí, kterou je člověk schopen vnímat a přiřadit jí pocity studeného, teplého či horkého. Jak se tato vlastnost jmenuje? Teplota Naše pocity
Termodynamika - určení měrné tepelné kapacity pevné látky
 I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY Laboratorní práce č. 3 Termodynamika - určení měrné
I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY Laboratorní práce č. 3 Termodynamika - určení měrné
plynu, Měření Poissonovy konstanty vzduchu
 Úloha 4: Měření dutých objemů vážením a kompresí plynu, Měření Poissonovy konstanty vzduchu FYZIKÁLNÍ PRAKTIKUM FJFI ČVUT V PRAZE Datum měření: 2.11.2009 Jméno: František Batysta Pracovní skupina: 11 Ročník
Úloha 4: Měření dutých objemů vážením a kompresí plynu, Měření Poissonovy konstanty vzduchu FYZIKÁLNÍ PRAKTIKUM FJFI ČVUT V PRAZE Datum měření: 2.11.2009 Jméno: František Batysta Pracovní skupina: 11 Ročník
HYDROSTATICKÝ TLAK. 1. K počítači připojíme pomocí kabelu modul USB.
 HYDROSTATICKÝ TLAK Vzdělávací předmět: Fyzika Tematický celek dle RVP: Mechanické vlastnosti tekutin Tematická oblast: Mechanické vlastnosti kapalin Cílová skupina: Žák 7. ročníku základní školy Cílem
HYDROSTATICKÝ TLAK Vzdělávací předmět: Fyzika Tematický celek dle RVP: Mechanické vlastnosti tekutin Tematická oblast: Mechanické vlastnosti kapalin Cílová skupina: Žák 7. ročníku základní školy Cílem
Praktikum I Mechanika a molekulová fyzika
 Oddělení fyzikálních praktik při Kabinetu výuky obecné fyziky MFF UK Praktikum I Mechanika a molekulová fyzika Úloha č. IV Název: Určení závislosti povrchového napětí na koncentraci povrchově aktivní látky
Oddělení fyzikálních praktik při Kabinetu výuky obecné fyziky MFF UK Praktikum I Mechanika a molekulová fyzika Úloha č. IV Název: Určení závislosti povrchového napětí na koncentraci povrchově aktivní látky
1. Měření hustoty látek. Úkol 1: Stanovte hustotu tělesa přímou metodou a pomocí Tabulek určete druh látky, z níž je těleso zhotoveno.
 1. Měření hustoty látek Úkol 1: Stanovte hustotu tělesa přímou metodou a pomocí Tabulek určete druh látky, z níž je těleso zhotoveno. BROŽ, J. Základy fyzikálních měření. 1. vyd. Praha: SPN, 1983, čl.
1. Měření hustoty látek Úkol 1: Stanovte hustotu tělesa přímou metodou a pomocí Tabulek určete druh látky, z níž je těleso zhotoveno. BROŽ, J. Základy fyzikálních měření. 1. vyd. Praha: SPN, 1983, čl.
Mechanika tekutin. Tekutiny = plyny a kapaliny
 Mechanika tekutin Tekutiny = plyny a kapaliny Vlastnosti kapalin Kapaliny mění tvar, ale zachovávají objem jsou velmi málo stlačitelné Ideální kapalina: bez vnitřního tření je zcela nestlačitelná Viskozita
Mechanika tekutin Tekutiny = plyny a kapaliny Vlastnosti kapalin Kapaliny mění tvar, ale zachovávají objem jsou velmi málo stlačitelné Ideální kapalina: bez vnitřního tření je zcela nestlačitelná Viskozita
Fyzikální praktikum 1
 Fyzikální praktikum 1 FJFI ČVUT v Praze Úloha: č. 5 - Kalibrace teploměru, skupenské teplo Jméno: Ondřej Finke Datum měření: 6.10.2014 Kruh: FE Skupina: 4 Klasifikace: 1. Pracovní úkoly 1.1 - Kalibrace
Fyzikální praktikum 1 FJFI ČVUT v Praze Úloha: č. 5 - Kalibrace teploměru, skupenské teplo Jméno: Ondřej Finke Datum měření: 6.10.2014 Kruh: FE Skupina: 4 Klasifikace: 1. Pracovní úkoly 1.1 - Kalibrace
Měření teplotní roztažnosti
 KATEDRA EXPERIMENTÁLNÍ FYZIKY PŘÍRODOVĚDECKÁ FAKULTA UNIVERZITY PALACKÉHO V OLOMOUCI FYZIKÁLNÍ PRAKTIKUM Z MOLEKULOVÉ FYZIKY A TERMODYNAMIKY Měření teplotní roztažnosti Úvod Zvyšování termodynamické teploty
KATEDRA EXPERIMENTÁLNÍ FYZIKY PŘÍRODOVĚDECKÁ FAKULTA UNIVERZITY PALACKÉHO V OLOMOUCI FYZIKÁLNÍ PRAKTIKUM Z MOLEKULOVÉ FYZIKY A TERMODYNAMIKY Měření teplotní roztažnosti Úvod Zvyšování termodynamické teploty
SEZNAM POKUSŮ TEPLO 1 NÁVODY NA POKUSY MĚŘENÍ TEPLOT. Měření teplot. Používání teploměru. (1.1.) Kalibrace teploměru. (1.2.
 TEPLO TA1 419.0008 TEPLO 1 SEZNAM POKUSŮ MĚŘENÍ TEPLOT Měření teplot. Používání teploměru. (1.1.) Kalibrace teploměru. (1.2.) KALORIMETRIE Teplotní rovnováha. (2.1.) Studium kalorimetru. (2.2.) Křivka
TEPLO TA1 419.0008 TEPLO 1 SEZNAM POKUSŮ MĚŘENÍ TEPLOT Měření teplot. Používání teploměru. (1.1.) Kalibrace teploměru. (1.2.) KALORIMETRIE Teplotní rovnováha. (2.1.) Studium kalorimetru. (2.2.) Křivka
13/sv. 8 (85/503/EHS) Tato směrnice je určena členským státům.
 62 31985L0503 L 308/12 ÚŘEDNÍ VĚSTNÍK EVROPSKÝCH SPOLEČENSTVÍ 20.11.1985 PRVNÍ SMĚRNICE KOMISE ze dne 25. října 1985 o metodách pro analýzu potravinářských kaseinů a kaseinátů (85/503/EHS) KOMISE EVROPSKÝCH
62 31985L0503 L 308/12 ÚŘEDNÍ VĚSTNÍK EVROPSKÝCH SPOLEČENSTVÍ 20.11.1985 PRVNÍ SMĚRNICE KOMISE ze dne 25. října 1985 o metodách pro analýzu potravinářských kaseinů a kaseinátů (85/503/EHS) KOMISE EVROPSKÝCH
Měření měrné telené kapacity pevných látek
 Měření měrné telené kapacity pevných látek Úkol :. Určete tepelnou kapacitu kalorimetru.. Určete měrnou tepelnou kapacitu daných těles. 3. Naměřené hodnoty porovnejte s hodnotami uvedených v tabulkách
Měření měrné telené kapacity pevných látek Úkol :. Určete tepelnou kapacitu kalorimetru.. Určete měrnou tepelnou kapacitu daných těles. 3. Naměřené hodnoty porovnejte s hodnotami uvedených v tabulkách
látka Obr. k úkolům 1 a 2 Obr. k úkolu 3
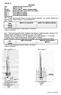 cvičení: A Téma: Základní vlastnosti organických látek Cíl: Teplota varu a tání Pomůcky: žákovská souprava, teploměr, skleněná trubička, Chemikálie: ethanol CH 3 CH 2 OH, aceton CH 3 COCH 3, naftalen Úkol
cvičení: A Téma: Základní vlastnosti organických látek Cíl: Teplota varu a tání Pomůcky: žákovská souprava, teploměr, skleněná trubička, Chemikálie: ethanol CH 3 CH 2 OH, aceton CH 3 COCH 3, naftalen Úkol
Stanovení hustoty pevných a kapalných látek
 55 Kapitola 9 Stanovení hustoty pevných a kapalných látek 9.1 Úvod Hustota látky ρ je hmotnost její objemové jednotky, definované vztahem: ρ = dm dv, kde dm = hmotnost objemového elementu dv. Pro homogenní
55 Kapitola 9 Stanovení hustoty pevných a kapalných látek 9.1 Úvod Hustota látky ρ je hmotnost její objemové jednotky, definované vztahem: ρ = dm dv, kde dm = hmotnost objemového elementu dv. Pro homogenní
KATEDRA MATERIÁLOVÉHO INŽENÝRSTVÍ A CHEMIE. 123TVVM transport vodní páry
 KATEDRA MATERIÁLOVÉHO INŽENÝRSTVÍ A CHEMIE 123TVVM transport vodní páry TRANSPORT VODNÍ PÁRY PORÉZNÍM PROSTŘEDÍM: Ve vzduchu obsažená vodní pára samovolně difunduje do míst s nižším parciálním tlakem až
KATEDRA MATERIÁLOVÉHO INŽENÝRSTVÍ A CHEMIE 123TVVM transport vodní páry TRANSPORT VODNÍ PÁRY PORÉZNÍM PROSTŘEDÍM: Ve vzduchu obsažená vodní pára samovolně difunduje do míst s nižším parciálním tlakem až
Měření měrného skupenského tepla tání ledu
 KATEDRA EXPERIMENTÁLNÍ FYZIKY PŘÍRODOVĚDECKÁ FAKULTA UNIVERZITY PALACKÉHO V OLOMOUCI FYZIKÁLNÍ PRAKTIKUM Z MOLEKULOVÉ FYZIKY A TERMODYNAMIKY Měření měrného skupenského tepla tání ledu Úvod Tání, měrné
KATEDRA EXPERIMENTÁLNÍ FYZIKY PŘÍRODOVĚDECKÁ FAKULTA UNIVERZITY PALACKÉHO V OLOMOUCI FYZIKÁLNÍ PRAKTIKUM Z MOLEKULOVÉ FYZIKY A TERMODYNAMIKY Měření měrného skupenského tepla tání ledu Úvod Tání, měrné
Charlesův zákon (pt závislost)
 Charlesův zákon (pt závislost) V této úloze pomocí čidla tlaku plynu GPS-BTA a teploměru TMP-BTA (nebo čidla Go!Temp) objevíme součást stavové rovnice ideálního plynu Charlesův zákon popisující izochorický
Charlesův zákon (pt závislost) V této úloze pomocí čidla tlaku plynu GPS-BTA a teploměru TMP-BTA (nebo čidla Go!Temp) objevíme součást stavové rovnice ideálního plynu Charlesův zákon popisující izochorický
LEE: Stanovení viskozity glycerolu pomocí dvou metod v kosmetickém produktu
 LEE: Stanovení viskozity glycerolu pomocí dvou metod v kosmetickém produktu Jsi chemikem ve farmaceutické společnosti, mezi jejíž činnosti, mimo jiné, patří analýza glycerolu pro kosmetické produkty. Dnešní
LEE: Stanovení viskozity glycerolu pomocí dvou metod v kosmetickém produktu Jsi chemikem ve farmaceutické společnosti, mezi jejíž činnosti, mimo jiné, patří analýza glycerolu pro kosmetické produkty. Dnešní
Jazykové gymnázium Pavla Tigrida, Ostrava-Poruba Název projektu: Podpora rozvoje praktické výchovy ve fyzice a chemii
 Datum: Jazykové gymnázium Pavla Tigrida, Ostrava-Poruba Název projektu: Podpora rozvoje praktické výchovy ve fyzice a chemii Tlak vzduchu: Teplota vzduchu: Laboratorní cvičení č. Oddělování složek směsí
Datum: Jazykové gymnázium Pavla Tigrida, Ostrava-Poruba Název projektu: Podpora rozvoje praktické výchovy ve fyzice a chemii Tlak vzduchu: Teplota vzduchu: Laboratorní cvičení č. Oddělování složek směsí
STANOVENÍ PROPUSTNOSTI OBALOVÝCH MATERIÁLŮ PRO VODNÍ PÁRU
 STANOVENÍ PROPUSTNOSTI OBALOVÝCH MATERIÁLŮ PRO VODNÍ PÁRU Úvod Obecná teorie propustnosti polymerních obalových materiálů je zmíněna v návodu pro stanovení propustnosti pro kyslík. Na tomto místě je třeba
STANOVENÍ PROPUSTNOSTI OBALOVÝCH MATERIÁLŮ PRO VODNÍ PÁRU Úvod Obecná teorie propustnosti polymerních obalových materiálů je zmíněna v návodu pro stanovení propustnosti pro kyslík. Na tomto místě je třeba
CHEMIE. Pracovní list č. 5 - žákovská verze Téma: Vliv teploty na rychlost chemické reakce, teplota tání karboxylových kyselin. Mgr.
 www.projektsako.cz CHEMIE Pracovní list č. 5 - žákovská verze Téma: Vliv teploty na rychlost chemické reakce, teplota tání karboxylových kyselin Lektor: Mgr. Lenka Horutová Projekt: Student a konkurenceschopnost
www.projektsako.cz CHEMIE Pracovní list č. 5 - žákovská verze Téma: Vliv teploty na rychlost chemické reakce, teplota tání karboxylových kyselin Lektor: Mgr. Lenka Horutová Projekt: Student a konkurenceschopnost
GEODÉZIE II. metody Trigonometrická metoda Hydrostatická nivelace Barometrická nivelace GNSS metoda. Trigonometricky určen. ení. Princip určen.
 Vysoká škola báňská technická univerzita Ostrava Hornicko-geologická fakulta Institut geodézie a důlního měřictví GEODÉZIE II Ing. Hana Staňková, Ph.D. 3. URČOV OVÁNÍ VÝŠEK metody Trigonometrická metoda
Vysoká škola báňská technická univerzita Ostrava Hornicko-geologická fakulta Institut geodézie a důlního měřictví GEODÉZIE II Ing. Hana Staňková, Ph.D. 3. URČOV OVÁNÍ VÝŠEK metody Trigonometrická metoda
TEPLO PŘIJATÉ A ODEVZDANÉ TĚLESEM PŘI TEPELNÉ VÝMĚNĚ
 TEPLO PŘIJATÉ A ODEVZDANÉ TĚLESEM PŘI TEPELNÉ VÝMĚNĚ Vzdělávací předmět: Fyzika Tematický celek dle RVP: Energie Tematická oblast: Vnitřní energie. Teplo Cílová skupina: Žák 8. ročníku základní školy Cílem
TEPLO PŘIJATÉ A ODEVZDANÉ TĚLESEM PŘI TEPELNÉ VÝMĚNĚ Vzdělávací předmět: Fyzika Tematický celek dle RVP: Energie Tematická oblast: Vnitřní energie. Teplo Cílová skupina: Žák 8. ročníku základní školy Cílem
4. Kolmou tlakovou sílu působící v kapalině na libovolně orientovanou plochu S vyjádříme jako
 1. Pojem tekutiny je A) synonymem pojmu kapaliny B) pojmem označujícím souhrnně kapaliny a plyny C) synonymem pojmu plyny D) označením kapalin se zanedbatelnou viskozitou 2. Příčinou rozdílné tekutosti
1. Pojem tekutiny je A) synonymem pojmu kapaliny B) pojmem označujícím souhrnně kapaliny a plyny C) synonymem pojmu plyny D) označením kapalin se zanedbatelnou viskozitou 2. Příčinou rozdílné tekutosti
Měření Poissonovy konstanty a dutých objemů Abstrakt: V této úloze se studenti seznámí s různými metodami
 FJFI ČVUT v Praze Fyzikální praktikum I Úloha 5 Verze 171006 Měření Poissonovy konstanty a dutých objemů Abstrakt: V této úloze se studenti seznámí s různými metodami měření Poissonovy konstanty, ty použijí
FJFI ČVUT v Praze Fyzikální praktikum I Úloha 5 Verze 171006 Měření Poissonovy konstanty a dutých objemů Abstrakt: V této úloze se studenti seznámí s různými metodami měření Poissonovy konstanty, ty použijí
Laboratorní práce č. 2: Určení povrchového napětí kapaliny
 Přírodní vědy moderně a interaktivně SEMINÁŘ FYZIKY Laboratorní práce č. 2: Určení povrchového napětí kapaliny G Gymnázium Hranice Přírodní vědy moderně a interaktivně SEMINÁŘ FYZIKY G Gymnázium Hranice
Přírodní vědy moderně a interaktivně SEMINÁŘ FYZIKY Laboratorní práce č. 2: Určení povrchového napětí kapaliny G Gymnázium Hranice Přírodní vědy moderně a interaktivně SEMINÁŘ FYZIKY G Gymnázium Hranice
Vybrané technologie povrchových úprav. Základy vakuové techniky Doc. Ing. Karel Daďourek 2006
 Vybrané technologie povrchových úprav Základy vakuové techniky Doc. Ing. Karel Daďourek 2006 Střední rychlost plynů Rychlost molekuly v p = (2 k N A ) * (T/M 0 ), N A = 6. 10 23 molekul na mol (Avogadrova
Vybrané technologie povrchových úprav Základy vakuové techniky Doc. Ing. Karel Daďourek 2006 Střední rychlost plynů Rychlost molekuly v p = (2 k N A ) * (T/M 0 ), N A = 6. 10 23 molekul na mol (Avogadrova
Stanovení kritické micelární koncentrace
 Stanovení kritické micelární koncentrace TEORIE KONDUKTOMETRIE Měrná elektrická vodivost neboli konduktivita je fyzikální veličinou, která popisuje schopnost látek vést elektrický proud. Látky snadno vedoucí
Stanovení kritické micelární koncentrace TEORIE KONDUKTOMETRIE Měrná elektrická vodivost neboli konduktivita je fyzikální veličinou, která popisuje schopnost látek vést elektrický proud. Látky snadno vedoucí
5b MĚŘENÍ VISKOZITY KAPALIN POMOCÍ PADAJÍCÍ KULIČKY
 Laboratorní cvičení z předmětu Reologie potravin a kosmetických prostředků 5b MĚŘENÍ VISKOZITY KAPALIN POMOCÍ PADAJÍCÍ KULIČKY 1. TEORIE: Měření viskozity pomocí padající kuličky patří k nejstarším metodám
Laboratorní cvičení z předmětu Reologie potravin a kosmetických prostředků 5b MĚŘENÍ VISKOZITY KAPALIN POMOCÍ PADAJÍCÍ KULIČKY 1. TEORIE: Měření viskozity pomocí padající kuličky patří k nejstarším metodám
Základy vakuové techniky
 Základy vakuové techniky Střední rychlost plynů Rychlost molekuly v p = (2 k N A ) * (T/M 0 ), N A = 6. 10 23 molekul na mol (Avogadrova konstanta), k = 1,38. 10-23 J/K.. Boltzmannova konstanta, T.. absolutní
Základy vakuové techniky Střední rychlost plynů Rychlost molekuly v p = (2 k N A ) * (T/M 0 ), N A = 6. 10 23 molekul na mol (Avogadrova konstanta), k = 1,38. 10-23 J/K.. Boltzmannova konstanta, T.. absolutní
Hydrochemie koncentrace látek (výpočty)
 1 Atomová hmotnostní konstanta/jednotka m u Relativní atomová hmotnost Relativní molekulová hmotnost Látkové množství (mol) 1 mol je takové množství látky, které obsahuje tolik částic, kolik je atomů ve
1 Atomová hmotnostní konstanta/jednotka m u Relativní atomová hmotnost Relativní molekulová hmotnost Látkové množství (mol) 1 mol je takové množství látky, které obsahuje tolik částic, kolik je atomů ve
Medundcké 'il1~~thorii kapalin Cll plynů demoru,trovl.illlhi!lll@ii1liioci imprcnfbovahýdm prostředlkť!! - plasf@vý4:h hlihvi
 Veletrh nápadů učitelů fyziky Medundcké 'il1~~thorii kapalin Cll plynů demoru,trovl.illlhi!lll@ii1liioci imprcnfbovahýdm prostředlkť!! - plasf@vý4:h hlihvi Věra Novobilská l. Ověření Pasclllova zókona
Veletrh nápadů učitelů fyziky Medundcké 'il1~~thorii kapalin Cll plynů demoru,trovl.illlhi!lll@ii1liioci imprcnfbovahýdm prostředlkť!! - plasf@vý4:h hlihvi Věra Novobilská l. Ověření Pasclllova zókona
ZMĚNY SKUPENSTVÍ LÁTEK
 ZMĚNY SKUPENSTVÍ LÁTEK TÁNÍ A TUHNUTÍ - OSNOVA Kapilární jevy příklad Skupenské přeměny látek Tání a tuhnutí Teorie s video experimentem Příklad KAPILÁRNÍ JEVY - OPAKOVÁNÍ KAPILÁRNÍ JEVY - PŘÍKLAD Jak
ZMĚNY SKUPENSTVÍ LÁTEK TÁNÍ A TUHNUTÍ - OSNOVA Kapilární jevy příklad Skupenské přeměny látek Tání a tuhnutí Teorie s video experimentem Příklad KAPILÁRNÍ JEVY - OPAKOVÁNÍ KAPILÁRNÍ JEVY - PŘÍKLAD Jak
Vážení, odměřování objemů
 Vážení, odměřování objemů Vážení K nezbytnému vybavení každé laboratoře patří váhy, pomocí kterých určujeme množství dané látky. Princip vážení je znám po staletí. Jde o srovnávací metodu, kdy se srovnává
Vážení, odměřování objemů Vážení K nezbytnému vybavení každé laboratoře patří váhy, pomocí kterých určujeme množství dané látky. Princip vážení je znám po staletí. Jde o srovnávací metodu, kdy se srovnává
Vlastnosti kapalin. Povrchová vrstva kapaliny
 Struktura a vlastnosti kapalin Vlastnosti kapalin, Povrchová vrstva kapaliny Jevy na rozhraní pevného tělesa a kapaliny Kapilární jevy, Teplotní objemová roztažnost Vlastnosti kapalin Kapalina - tvoří
Struktura a vlastnosti kapalin Vlastnosti kapalin, Povrchová vrstva kapaliny Jevy na rozhraní pevného tělesa a kapaliny Kapilární jevy, Teplotní objemová roztažnost Vlastnosti kapalin Kapalina - tvoří
Laboratorní práce č. 1: Přibližné určení průměru molekuly kyseliny olejové
 Přírodní vědy moderně a interaktivně FYZIKA 4. ročník šestiletého a 2. ročník čtyřletého studia Laboratorní práce č. 1: Přibližné určení průměru molekuly kyseliny olejové ymnázium Přírodní vědy moderně
Přírodní vědy moderně a interaktivně FYZIKA 4. ročník šestiletého a 2. ročník čtyřletého studia Laboratorní práce č. 1: Přibližné určení průměru molekuly kyseliny olejové ymnázium Přírodní vědy moderně
DESTILAČNÍ ZKOUŠKA PALIV
 VYSOKÁ ŠKOLA CHEMICKO-TECHNOLOGICKÁ V PRAZE Fakulta technologie ochrany prostředí Ústav technologie ropy a alternativních ativních paliv DESTILAČNÍ ZKOUŠKA PALIV Laboratorní cvičení ÚVOD Destilační zkouška
VYSOKÁ ŠKOLA CHEMICKO-TECHNOLOGICKÁ V PRAZE Fakulta technologie ochrany prostředí Ústav technologie ropy a alternativních ativních paliv DESTILAČNÍ ZKOUŠKA PALIV Laboratorní cvičení ÚVOD Destilační zkouška
002. Pokles teploty ochlazením - chladicí účinky těkavých kapalin
 002. Pokles teploty ochlazením - chladicí účinky těkavých kapalin Oblast dle RVP: Člov?k a p?íroda Obor: fyzika Mezipředmětové vztahy: biologie, ekologie Klíčová slova: vnit?ní energie, skupenství látek,
002. Pokles teploty ochlazením - chladicí účinky těkavých kapalin Oblast dle RVP: Člov?k a p?íroda Obor: fyzika Mezipředmětové vztahy: biologie, ekologie Klíčová slova: vnit?ní energie, skupenství látek,
PRAKTIKUM... Oddělení fyzikálních praktik při Kabinetu výuky obecné fyziky MFF UK. Odevzdal dne: Seznam použité literatury 0 1. Celkem max.
 Oddělení fyzikálních praktik při Kabinetu výuky obecné fyziky MFF UK PRAKTIKUM... Úloha č. Název: Pracoval: stud. skup. dne Odevzdal dne: Možný počet bodů Udělený počet bodů Práce při měření 0 5 Teoretická
Oddělení fyzikálních praktik při Kabinetu výuky obecné fyziky MFF UK PRAKTIKUM... Úloha č. Název: Pracoval: stud. skup. dne Odevzdal dne: Možný počet bodů Udělený počet bodů Práce při měření 0 5 Teoretická
HYDROSTATICKÝ PARADOX
 HYDROSTATICKÝ PARADOX Vzdělávací předmět: Fyzika Tematický celek dle RVP: Mechanické vlastnosti tekutin Tematická oblast: Mechanické vlastnosti kapalin Cílová skupina: Žák 7. ročníku základní školy Cílem
HYDROSTATICKÝ PARADOX Vzdělávací předmět: Fyzika Tematický celek dle RVP: Mechanické vlastnosti tekutin Tematická oblast: Mechanické vlastnosti kapalin Cílová skupina: Žák 7. ročníku základní školy Cílem
DUM č. 12 v sadě. 10. Fy-1 Učební materiály do fyziky pro 2. ročník gymnázia
 projekt GML Brno Docens DUM č. 12 v sadě 10. Fy-1 Učební materiály do fyziky pro 2. ročník gymnázia Autor: Vojtěch Beneš Datum: 03.05.2014 Ročník: 1. ročník Anotace DUMu: Kapaliny, změny skupenství Materiály
projekt GML Brno Docens DUM č. 12 v sadě 10. Fy-1 Učební materiály do fyziky pro 2. ročník gymnázia Autor: Vojtěch Beneš Datum: 03.05.2014 Ročník: 1. ročník Anotace DUMu: Kapaliny, změny skupenství Materiály
VYPAŘOVÁNÍ POMŮCKY NASTAVENÍ MĚŘICÍHO ZAŘÍZENÍ. Vzdělávací předmět: Fyzika. Tematický celek dle RVP: Energie. Tematická oblast: Změny skupenství látek
 VYPAŘOVÁNÍ Vzdělávací předmět: Fyzika Tematický celek dle RVP: Energie Tematická oblast: Změny skupenství látek Cílová skupina: Žák 8. ročníku základní školy Cílem pokusu je sledování změny teploty tělesa
VYPAŘOVÁNÍ Vzdělávací předmět: Fyzika Tematický celek dle RVP: Energie Tematická oblast: Změny skupenství látek Cílová skupina: Žák 8. ročníku základní školy Cílem pokusu je sledování změny teploty tělesa
Jednotné pracovní postupy zkoušení krmiv STANOVENÍ OBSAHU 5-VINYL - 2-THIOOXAZOLIDONU (GOITRINU) METODOU GC
 Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU 5-VINYL - 2-THIOOXAZOLIDONU (GOITRINU) METODOU GC 1 Rozsah a účel Metoda specifikuje podmínky pro stanovení vinylthiooxazolidonu (dále VOT) v krmivech.
Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU 5-VINYL - 2-THIOOXAZOLIDONU (GOITRINU) METODOU GC 1 Rozsah a účel Metoda specifikuje podmínky pro stanovení vinylthiooxazolidonu (dále VOT) v krmivech.
ρ = měrný odpor, ρ [Ω m] l = délka vodiče
![ρ = měrný odpor, ρ [Ω m] l = délka vodiče ρ = měrný odpor, ρ [Ω m] l = délka vodiče](/thumbs/28/12887427.jpg) 7 Kapitola 2 Měření elektrických odporů 2 Úvod Ohmův zákon definuje ohmický odpor, zkráceně jen odpor, R elektrického vodiče jako konstantu úměrnosti mezi stejnosměrným proudem I, který protéká vodičem
7 Kapitola 2 Měření elektrických odporů 2 Úvod Ohmův zákon definuje ohmický odpor, zkráceně jen odpor, R elektrického vodiče jako konstantu úměrnosti mezi stejnosměrným proudem I, který protéká vodičem
Látkové množství n poznámky 6.A GVN
 Látkové množství n poznámky 6.A GVN 10. září 2007 charakterizuje látky z hlediska počtu částic (molekul, atomů, iontů), které tato látka obsahuje je-li v tělese z homogenní látky N částic, pak látkové
Látkové množství n poznámky 6.A GVN 10. září 2007 charakterizuje látky z hlediska počtu částic (molekul, atomů, iontů), které tato látka obsahuje je-li v tělese z homogenní látky N částic, pak látkové
Č e s k ý m e t r o l o g i c k ý i n s t i t u t Okružní 31, 638 00
 Č e s k ý m e t r o l o g i c k ý i n s t i t u t Okružní 31, 638 00 Brno Český metrologický institut (dále jen ČMI ), jako orgán věcně a místně příslušný ve věci stanovování metrologických a technických
Č e s k ý m e t r o l o g i c k ý i n s t i t u t Okružní 31, 638 00 Brno Český metrologický institut (dále jen ČMI ), jako orgán věcně a místně příslušný ve věci stanovování metrologických a technických
MECHANIKA KAPALIN A PLYNŮ. Mgr. Jan Ptáčník - GJVJ - Fyzika - Mechanika - 1. ročník
 MECHANIKA KAPALIN A PLYNŮ Mgr. Jan Ptáčník - GJVJ - Fyzika - Mechanika - 1. ročník Mechanika kapalin a plynů Hydrostatika - studuje podmínky rovnováhy kapalin. Aerostatika - studuje podmínky rovnováhy
MECHANIKA KAPALIN A PLYNŮ Mgr. Jan Ptáčník - GJVJ - Fyzika - Mechanika - 1. ročník Mechanika kapalin a plynů Hydrostatika - studuje podmínky rovnováhy kapalin. Aerostatika - studuje podmínky rovnováhy
KATEDRA MATERIÁLOVÉHO INŽENÝRSTVÍ A CHEMIE. 123TVVM transport vodní páry
 KATEDRA MATERIÁLOVÉHO INŽENÝRSTVÍ A CHEMIE 123TVVM transport vodní páry Transport vodní páry porézním prostředím: Tepelná vodivost vzduchu: = 0,0262 W m -1 K -1 Tepelná vodivost izolantů: = cca 0,04 W
KATEDRA MATERIÁLOVÉHO INŽENÝRSTVÍ A CHEMIE 123TVVM transport vodní páry Transport vodní páry porézním prostředím: Tepelná vodivost vzduchu: = 0,0262 W m -1 K -1 Tepelná vodivost izolantů: = cca 0,04 W
PROCESY V TECHNICE BUDOV cvičení 3, 4
 UNIVERZITA TOMÁŠE ATI VE ZLÍNĚ FAKULTA APLIKOVANÉ INFORMATIKY PROCESY V TECHNICE UDOV cvičení 3, 4 část Hana Charvátová, Dagmar Janáčová Zlín 013 Tento studijní materiál vznikl za finanční podpory Evropského
UNIVERZITA TOMÁŠE ATI VE ZLÍNĚ FAKULTA APLIKOVANÉ INFORMATIKY PROCESY V TECHNICE UDOV cvičení 3, 4 část Hana Charvátová, Dagmar Janáčová Zlín 013 Tento studijní materiál vznikl za finanční podpory Evropského
KDE VZÍT PLYNY? Václav Piskač, Brno 2014
 KDE VZÍT PLYNY? Václav Piskač, Brno 2014 Tento článek se zabývá možnostmi, jak pro školní experimenty s plyny získat něco jiného než vzduch. V dalším budu předpokládat, že nemáte kamarády ve výzkumném
KDE VZÍT PLYNY? Václav Piskač, Brno 2014 Tento článek se zabývá možnostmi, jak pro školní experimenty s plyny získat něco jiného než vzduch. V dalším budu předpokládat, že nemáte kamarády ve výzkumném
Měření Poissonovy konstanty a dutých objemů Abstrakt: V této úloze se studenti seznámí s různými metodami
 FJFI ČVUT v Praze Fyzikální praktikum I Úloha 5 Verze 160927 Měření Poissonovy konstanty a dutých objemů Abstrakt: V této úloze se studenti seznámí s různými metodami měření Poissonovy konstanty, ty použijí
FJFI ČVUT v Praze Fyzikální praktikum I Úloha 5 Verze 160927 Měření Poissonovy konstanty a dutých objemů Abstrakt: V této úloze se studenti seznámí s různými metodami měření Poissonovy konstanty, ty použijí
34_Mechanické vlastnosti kapalin... 2 Pascalův zákon _Tlak - příklady _Hydraulické stroje _PL: Hydraulické stroje - řešení...
 34_Mechanické vlastnosti kapalin... 2 Pascalův zákon... 2 35_Tlak - příklady... 2 36_Hydraulické stroje... 3 37_PL: Hydraulické stroje - řešení... 4 38_Účinky gravitační síly Země na kapalinu... 6 Hydrostatická
34_Mechanické vlastnosti kapalin... 2 Pascalův zákon... 2 35_Tlak - příklady... 2 36_Hydraulické stroje... 3 37_PL: Hydraulické stroje - řešení... 4 38_Účinky gravitační síly Země na kapalinu... 6 Hydrostatická
Praktikum I Mechanika a molekulová fyzika
 Oddělení fyzikálních praktik při Kabinetu výuky obecné fyziky MFF UK Praktikum I Mechanika a molekulová fyzika Úloha č. XIX Název: Pád koule ve viskózní kapalině Pracoval: Matyáš Řehák stud.sk.: 16 dne:
Oddělení fyzikálních praktik při Kabinetu výuky obecné fyziky MFF UK Praktikum I Mechanika a molekulová fyzika Úloha č. XIX Název: Pád koule ve viskózní kapalině Pracoval: Matyáš Řehák stud.sk.: 16 dne:
Řízení robota senzorem teploty II. Tematický celek: Termodynamika. Komplexní úloha - 2. část:
 Název: Řízení robota senzorem teploty II. Tematický celek: Termodynamika. Komplexní úloha - 2. část: Použijte konstrukci robota popsanou v rvs_i_29. Naprogramujte robota tak, aby rozhodl, které z kapalných
Název: Řízení robota senzorem teploty II. Tematický celek: Termodynamika. Komplexní úloha - 2. část: Použijte konstrukci robota popsanou v rvs_i_29. Naprogramujte robota tak, aby rozhodl, které z kapalných
Taková vrstva suspenze je nazývána fluidní vrstvou. Její existence je vymezena přesně definovanou oblastí mimovrstvové rychlosti tekutiny,
 8 Fluidace Lenka Schreiberová I Základní vztahy a definice Fluidace je děj, při kterém tekutina proudící ve směru opačném směru zemské tíže vytváří spolu s pevnými částicemi suspenzi. Suspenze může vyplňovat
8 Fluidace Lenka Schreiberová I Základní vztahy a definice Fluidace je děj, při kterém tekutina proudící ve směru opačném směru zemské tíže vytváří spolu s pevnými částicemi suspenzi. Suspenze může vyplňovat
Vyjadřování přesnosti v metrologii
 Vyjadřování přesnosti v metrologii Měření soubor činností, jejichž cílem je stanovit hodnotu veličiny. Výsledek měření hodnota získaná měřením přisouzená měřené veličině. Chyba měření výsledek měření mínus
Vyjadřování přesnosti v metrologii Měření soubor činností, jejichž cílem je stanovit hodnotu veličiny. Výsledek měření hodnota získaná měřením přisouzená měřené veličině. Chyba měření výsledek měření mínus
du dq dw je totální diferenciál vnitřní energie a respektive práce. Pokud systém může konat pouze objemovou práci platí OCHV
 Úloha č.2: Stanovení učinnosti hořáku, Carnotovy termodynamické účinnosti, reálné vnitřní účinnosti a mechanické účinnosti a z nich vypočtená celková účinnost přeměny tepla na mechanickou energii ve Stirlingově
Úloha č.2: Stanovení učinnosti hořáku, Carnotovy termodynamické účinnosti, reálné vnitřní účinnosti a mechanické účinnosti a z nich vypočtená celková účinnost přeměny tepla na mechanickou energii ve Stirlingově
Pexeso Laboratorní pomůcky
 Pexeso Laboratorní pomůcky Hana Cídlová, Eva Lomovcivová Katedra chemie Pedagogické fakulty Masarykovy univerzity v Brně, Česká republika e-mail: cidlova@centrum.cz Milé děti! Připravily jsme pro Vás zábavnou
Pexeso Laboratorní pomůcky Hana Cídlová, Eva Lomovcivová Katedra chemie Pedagogické fakulty Masarykovy univerzity v Brně, Česká republika e-mail: cidlova@centrum.cz Milé děti! Připravily jsme pro Vás zábavnou
VYUŽITÍ MULTIFUNKČNÍHO KALIBRÁTORU PRO ZKRÁCENOU ZKOUŠKU PŘEPOČÍTÁVAČE MNOŽSTVÍ PLYNU
 VYUŽITÍ MULTIFUNKČNÍHO KALIBRÁTORU PRO ZKRÁCENOU ZKOUŠKU PŘEPOČÍTÁVAČE MNOŽSTVÍ PLYNU potrubí průtokoměr průtok teplota tlak Přepočítávač množství plynu 4. ročník mezinárodní konference 10. a 11. listopadu
VYUŽITÍ MULTIFUNKČNÍHO KALIBRÁTORU PRO ZKRÁCENOU ZKOUŠKU PŘEPOČÍTÁVAČE MNOŽSTVÍ PLYNU potrubí průtokoměr průtok teplota tlak Přepočítávač množství plynu 4. ročník mezinárodní konference 10. a 11. listopadu
KAPALINY. Mgr. Jan Ptáčník - GJVJ - Fyzika - Sekunda
 KAPALINY Mgr. Jan Ptáčník - GJVJ - Fyzika - Sekunda Vlastnosti molekul kapalin V neustálém pohybu Ve stejných vzdálenostech, nejsou ale vázány Působí na sebe silami: odpudivé x přitažlivé Vlastnosti kapalin
KAPALINY Mgr. Jan Ptáčník - GJVJ - Fyzika - Sekunda Vlastnosti molekul kapalin V neustálém pohybu Ve stejných vzdálenostech, nejsou ale vázány Působí na sebe silami: odpudivé x přitažlivé Vlastnosti kapalin
1/6. 2. Stavová rovnice, plynová konstanta, Avogadrův zákon, kilomol plynu
 1/6 2. Stavová rovnice, plynová konstanta, Avogadrův zákon, kilomol plynu Příklad: 2.1, 2.2, 2.3, 2.4, 2.5, 2.6, 2.7, 2.8, 2.9, 2.10, 2.11, 2.12, 2.13, 2.14, 2.15, 2.16, 2.17, 2.18, 2.19, 2.20, 2.21, 2.22,
1/6 2. Stavová rovnice, plynová konstanta, Avogadrův zákon, kilomol plynu Příklad: 2.1, 2.2, 2.3, 2.4, 2.5, 2.6, 2.7, 2.8, 2.9, 2.10, 2.11, 2.12, 2.13, 2.14, 2.15, 2.16, 2.17, 2.18, 2.19, 2.20, 2.21, 2.22,
Demonstrace hydrostatického paradoxu pomocí plastových lahví a LabQuest Vernier
 Demonstrace hydrostatického paradoxu pomocí plastových lahví a LabQuest Vernier ČENĚK KODEJŠKA Přírodovědecká fakulta Univerzity Palackého, Olomouc Úvod Při podrobném zkoumání problematiky demonstrace
Demonstrace hydrostatického paradoxu pomocí plastových lahví a LabQuest Vernier ČENĚK KODEJŠKA Přírodovědecká fakulta Univerzity Palackého, Olomouc Úvod Při podrobném zkoumání problematiky demonstrace
IDEÁLNÍ PLYN. Stavová rovnice
 IDEÁLNÍ PLYN Stavová rovnice Ideální plyn ) rozměry molekul jsou zanedbatelné vzhledem k jejich vzdálenostem 2) molekuly plynu na sebe působí jen při vzájemných srážkách 3) všechny srážky jsou dokonale
IDEÁLNÍ PLYN Stavová rovnice Ideální plyn ) rozměry molekul jsou zanedbatelné vzhledem k jejich vzdálenostem 2) molekuly plynu na sebe působí jen při vzájemných srážkách 3) všechny srážky jsou dokonale
CVIČENÍ 3: VODNÍ PROVOZ (POKRAČOVÁNÍ), MINERÁLNÍ VÝŽIVA. Pokus č. 1: Stanovení celkové a kutikulární transpirace listů analýzou transpirační křivky
 CVIČENÍ 3: VODNÍ PROVOZ (POKRAČOVÁNÍ), MINERÁLNÍ VÝŽIVA Pokus č. 1: Stanovení celkové a kutikulární transpirace listů analýzou transpirační křivky Analýza transpiračních křivek, založená na vážení odříznutých
CVIČENÍ 3: VODNÍ PROVOZ (POKRAČOVÁNÍ), MINERÁLNÍ VÝŽIVA Pokus č. 1: Stanovení celkové a kutikulární transpirace listů analýzou transpirační křivky Analýza transpiračních křivek, založená na vážení odříznutých
Molekulová fyzika a termika. Přehled základních pojmů
 Molekulová fyzika a termika Přehled základních pojmů Kinetická teorie látek Vychází ze tří experimentálně ověřených poznatků: 1) Látky se skládají z částic - molekul, atomů nebo iontů, mezi nimiž jsou
Molekulová fyzika a termika Přehled základních pojmů Kinetická teorie látek Vychází ze tří experimentálně ověřených poznatků: 1) Látky se skládají z částic - molekul, atomů nebo iontů, mezi nimiž jsou
Univerzita obrany. Měření součinitele tření potrubí K-216. Laboratorní cvičení z předmětu HYDROMECHANIKA. Protokol obsahuje 14 listů
 Univerzita obrany K-216 Laboratorní cvičení z předmětu HYDROMECHANIKA Měření součinitele tření potrubí Protokol obsahuje 14 listů Vypracoval: Vít Havránek Studijní skupina: 21-3LRT-C Datum zpracování:5.5.2011
Univerzita obrany K-216 Laboratorní cvičení z předmětu HYDROMECHANIKA Měření součinitele tření potrubí Protokol obsahuje 14 listů Vypracoval: Vít Havránek Studijní skupina: 21-3LRT-C Datum zpracování:5.5.2011
7. MECHANIKA TEKUTIN - statika
 7. - statika 7.1. Základní vlastnosti tekutin Obecným pojem tekutiny jsou myšleny. a. Mají společné vlastnosti tekutost, částice jsou od sebe snadno oddělitelné, nemají vlastní stálý tvar apod. Reálné
7. - statika 7.1. Základní vlastnosti tekutin Obecným pojem tekutiny jsou myšleny. a. Mají společné vlastnosti tekutost, částice jsou od sebe snadno oddělitelné, nemají vlastní stálý tvar apod. Reálné
1. Okalibrujte pomocí bodu tání ledu, bodu varu vody a bodu tuhnutí cínu:
 1 Pracovní úkoly 1. Okalibrujte pomocí bodu tání ledu, bodu varu vody a bodu tuhnutí cínu: a. platinový odporový teploměr (určete konstanty R 0, A, B) b. termočlánek měď-konstantan (určete konstanty a,
1 Pracovní úkoly 1. Okalibrujte pomocí bodu tání ledu, bodu varu vody a bodu tuhnutí cínu: a. platinový odporový teploměr (určete konstanty R 0, A, B) b. termočlánek měď-konstantan (určete konstanty a,
Vážení. práce s předvážkami práce s přesnými vahami práce s analytickými vahami příklad vážení na analytických vahách prasárničky...
 LEKCE 2 Vážení práce s předvážkami práce s přesnými vahami práce s analytickými vahami příklad vážení na analytických vahách prasárničky... Předvážky (váhy přenosné) xxx slouží xxx k orientačnímu navažování
LEKCE 2 Vážení práce s předvážkami práce s přesnými vahami práce s analytickými vahami příklad vážení na analytických vahách prasárničky... Předvážky (váhy přenosné) xxx slouží xxx k orientačnímu navažování
pv = nrt. Lord Celsius udržoval konstantní tlak plynu v uzavřené soustavě. Potom můžeme napsat T, tedy V = C(t t0) = Ct Ct0, (1)
 17. ročník, úloha I. E... absolutní nula (8 bodů; průměr 4,03; řešilo 40 studentů) S experimentálním vybavením dostupným v době Lorda Celsia změřte teplotu absolutní nuly (v Celsiově stupnici). Poradíme
17. ročník, úloha I. E... absolutní nula (8 bodů; průměr 4,03; řešilo 40 studentů) S experimentálním vybavením dostupným v době Lorda Celsia změřte teplotu absolutní nuly (v Celsiově stupnici). Poradíme
VLHKOST A NASÁKAVOST STAVEBNÍCH MATERIÁLŮ. Stavební hmoty I Cvičení 7
 VLHKOST A NASÁKAVOST STAVEBNÍCH MATERIÁLŮ Stavební hmoty I Cvičení 7 STANOVENÍ VLHKOSTI STAVEBNÍCH MATERIÁLŮ PROTOKOL Č.7 Stanovení vlhkosti stavebních materiálů a výrobků sušením při zvýšené teplotě dle
VLHKOST A NASÁKAVOST STAVEBNÍCH MATERIÁLŮ Stavební hmoty I Cvičení 7 STANOVENÍ VLHKOSTI STAVEBNÍCH MATERIÁLŮ PROTOKOL Č.7 Stanovení vlhkosti stavebních materiálů a výrobků sušením při zvýšené teplotě dle
Měření měrné tepelné kapacity látek kalorimetrem
 Měření měrné tepelné kapacity látek kalorimetrem Problém A. Změření kapacity kalorimetru (tzv. vodní hodnota) pomocí elektrického ohřevu s měřeným příkonem. B. Změření měrné tepelné kapacity hliníku směšovací
Měření měrné tepelné kapacity látek kalorimetrem Problém A. Změření kapacity kalorimetru (tzv. vodní hodnota) pomocí elektrického ohřevu s měřeným příkonem. B. Změření měrné tepelné kapacity hliníku směšovací
ZMĚNY SKUPENSTVÍ LÁTEK ČÁST 01
 ZMĚNY SKUPENSTVÍ LÁTEK ČÁST 01 A) Výklad: Změny skupenství látky Látka se může vyskytovat ve třech různých skupenstvích PEVNÉM, KAPALNÉM nebo PLYNNÉM. Např. voda (H 2 O)- může se vyskytovat jako krystalický
ZMĚNY SKUPENSTVÍ LÁTEK ČÁST 01 A) Výklad: Změny skupenství látky Látka se může vyskytovat ve třech různých skupenstvích PEVNÉM, KAPALNÉM nebo PLYNNÉM. Např. voda (H 2 O)- může se vyskytovat jako krystalický
Stanovení viskozity skla v intervalu 10 2 až 10 5 dpas
 Návod na laboratorní práci: Stanovení viskozity skla v intervalu 10 2 až 10 5 dpas Vedoucí práce: Dr.Ing. Martin Míka, Ing. František Lahodný, Ph.D. telefon 220444102 Místo: laboratoře A14 a A15 Úvod Viskozita
Návod na laboratorní práci: Stanovení viskozity skla v intervalu 10 2 až 10 5 dpas Vedoucí práce: Dr.Ing. Martin Míka, Ing. František Lahodný, Ph.D. telefon 220444102 Místo: laboratoře A14 a A15 Úvod Viskozita
Práce tepelného stroje
 Fyzikální praktikum FJFI ČVUT v Praze Úloha č. 12 : Práce tepelného stroje Jméno: Ondřej Ticháček Pracovní skupina: 6 Kruh: ZS 6 Datum měření: 23.11.2012 Klasifikace: Část I Práce tepelného stroje 1 Zadání
Fyzikální praktikum FJFI ČVUT v Praze Úloha č. 12 : Práce tepelného stroje Jméno: Ondřej Ticháček Pracovní skupina: 6 Kruh: ZS 6 Datum měření: 23.11.2012 Klasifikace: Část I Práce tepelného stroje 1 Zadání
1 Tlaková ztráta při toku plynu výplní
 I Základní vztahy a definice 1 Tlaková ztráta při toku plynu výplní Proudění plynu (nebo kapaliny) nehybnou vrstvou částic má řadu aplikací v chemické technoloii. Částice tvořící vrstvu mohou být kuličky,
I Základní vztahy a definice 1 Tlaková ztráta při toku plynu výplní Proudění plynu (nebo kapaliny) nehybnou vrstvou částic má řadu aplikací v chemické technoloii. Částice tvořící vrstvu mohou být kuličky,
6. Mechanika kapalin a plynů
 6. Mechanika kapalin a plynů 1. Definice tekutin 2. Tlak 3. Pascalův zákon 4. Archimedův zákon 5. Rovnice spojitosti (kontinuity) 6. Bernoulliho rovnice 7. Fyzika letu Tekutiny: jejich rozdělení, jejich
6. Mechanika kapalin a plynů 1. Definice tekutin 2. Tlak 3. Pascalův zákon 4. Archimedův zákon 5. Rovnice spojitosti (kontinuity) 6. Bernoulliho rovnice 7. Fyzika letu Tekutiny: jejich rozdělení, jejich
