LICENČNÍ SMLOUVA POSKYTOVANÁ KVÝKONU PRÁVAUŽÍT ŠKOLNÍ DÍLO
|
|
|
- Barbora Němečková
- před 8 lety
- Počet zobrazení:
Transkript
1
2
3
4
5 LICENČNÍ SMLOUVA POSKYTOVANÁ KVÝKONU PRÁVAUŽÍT ŠKOLNÍ DÍLO uzavřená mezi smluvními stranami: 1. Pan/paní Jméno apříjmení: Bc. Jiří Polický Bytem: Příkopy 1105, Náchod Narozen/a (datum amísto): , Náchod (dále jen "autor") a 2. Vysoké učení technické vbrně Fakulta elektrotechniky akomunikačních technologií se sídlem Údolní 244/53, Brno 2 jejímž jménem jedná na základě písemného pověření děkanem fakulty: Ing. Edita Hejátková (dále jen "nabyvatel") Článek 1 Specifikace školního díla 1. Předmětem této smlouvy je vysokoškolská kvalifikační práce (VŠKP): dizertační práce diplomová práce bakalářská práce jiná práce, jejíž druh je specifikován jako... (dále jen VŠKP nebo dílo) Název VŠKP: Využití uhlíkových nanotrubic pro realizaci elektrod tlustovrstvých senzorů Vedoucí/školitel VŠKP: Ing. Jan Prášek, Ph.D. Ústav: Ústav mikroelektroniky Datum obhajoby VŠKP:... VŠKP odevzdal autor nabyvateli v: tištěné formě - počet exemplářů 2 elektronické formě - počet exemplářů 1 2. Autor prohlašuje, ževytvořil samostatnou vlastní tvůrčí činností dílo shora popsané aspecifikované.autor dále prohlašuje, že přizpracovávání díla se sám nedostal do rozporu sautorským zákonem apředpisy souvisejícími aže je dílo dílem původním. 3. Dílo je chráněno jako dílo dle autorského zákona vplatném znění. 4. Autor potvrzuje, že listinná aelektronická verze díla je identická.
6 Článek 2 Udělení licenčního oprávnění 1. Autor touto smlouvou poskytuje nabyvateli oprávnění (licenci) kvýkonu práva uvedené dílo nevýdělečně užít, archivovat azpřístupnit ke studijním, výukovým avýzkumným účelům včetně pořizovaní výpisů, opisů arozmnoženin. 2. Licence je poskytována celosvětově, pro celou dobu trvání autorských amajetkových práv kdílu. 3. Autor souhlasí se zveřejněním díla vdatabázi přístupné vmezinárodní síti ihned po uzavření této smlouvy 1rok po uzavření této smlouvy 3roky po uzavření této smlouvy 5let po uzavření této smlouvy 10 let po uzavření této smlouvy (z důvodu utajení vněmobsažených informací) 4. Nevýdělečné zveřejňování díla nabyvatelem vsouladu sustanovením 47b zákona č. 111/1998 Sb., vplatném znění, nevyžaduje licenci anabyvatel je kněmu povinen aoprávněn ze zákona. Článek 3 Závěrečná ustanovení 1. Smlouva je sepsána ve třech vyhotoveních splatností originálu, přičemž po jednom vyhotovení obdrží autor anabyvatel, další vyhotovení je vloženo do VŠKP. 2. Vztahy mezi smluvními stranami vzniklé aneupravené touto smlouvou se řídí autorským zákonem, občanským zákoníkem, vysokoškolským zákonem, zákonem oarchivnictví, vplatném znění apopř. dalšími právními předpisy. 3. Licenční smlouva byla uzavřena na základě svobodné apravé vůle smluvních stran, splným porozuměním jejímu textu idůsledkům, nikoliv vtísni aza nápadně nevýhodných podmínek. 4. Licenční smlouva nabývá platnosti aúčinnosti dnem jejího podpisu oběma smluvními stranami. VBrně dne: Nabyvatel Autor
7 ABSTRAKT Tato práce se zabývá problematikou detekce těžkých kovů s použitím miniaturizovaných tlustovrstvých senzorů. Pracovní elektroda pro tyto senzory byla připravena pomocí tlustovrstvé pasty za použití prášku s uhlíkovými nanotrubicemi, pojiva a ředidla. Vyrobené elektrody byly proměřeny při detekci iontů olova a kadmia v tříelektrodovém systému diferenčně pulzní voltametrií v acetátovém pufru. Získané výsledky byly porovnány s uhlíkovou elektrodou vytvořenou ze speciální komerční tlustovrstvé polymerní pasty. Na závěr je zde popsána i možnost aktivace povrchu pracovní elektrody kyselinou dusičnou a ověření detekce těžkých kovů na reálném biologickém vzorku. ABSTRACT This work covers an area of heavy metals detection by miniaturized thick film sensors. Working electrode of these sensors was fabricated using thick film paste that was prepared as a nanocomposition of carbon nanotubes powder, suitable vehicle and a thinner. The response of fabricated electrodes to cadmium and lead ions was measured using differential pulse voltammetry in an acetate buffer solution using a three electrode sytem. The results were compared with the carbon electrode made from special commercial thick film polymer paste. Finally the possibility of working electrode surface activation with nitric acid and heavy metals on real biological sample detection is described here. KLÍČOVÁ SLOVA Tištěná elektroda, Senzor, Uhlíkové nanotrubice, Těžké kovy, Diferenční pulzní voltametrie KEYWORDS Thick film electrode, Sensor, Carbon nanotubes, Heavy metals, Diferential pulse voltamettry
8 BIBLIOGRAFICKÁ CITACE POLICKÝ, J. Využití uhlíkových nanotrubic pro realizaci elektrod tlustovrstvých senzorů. Brno: Vysoké učení technické v Brně, Fakulta elektrotechniky a komunikačních technologií, s. Vedoucí diplomové práce Ing. Jan Prášek, Ph.D. PROHLÁŠENÍ AUTORA O PŮVODNOSTI DÍLA: Prohlašuji, že jsem tuto vysokoškolskou kvalifikační práci vypracoval samostatně pod vedením vedoucího diplomové práce, s použitím odborné literatury a dalších informačních zdrojů, které jsou všechny citovány v práci a uvedeny v seznamu literatury. Jako autor uvedené diplomové práce dále prohlašuji, že v souvislosti s vytvořením této diplomové práce jsem neporušil autorská práva třetích osob, zejména jsem nezasáhl nedovoleným způsobem do cizích autorských práv osobnostních a jsem si plně vědom následků porušení ustanovení 11 a následujících autorského zákona č. 121/2000 Sb., včetně možných trestněprávních důsledků vyplývajících z ustanovení 152 trestního zákona č. 140/1961 Sb. V Brně dne podpis autora PODĚKOVÁNÍ Děkuji vedoucímu diplomové práce Ing. Janu Práškovi, Ph.D., doc. Ing. Jaromíru Hubálkovi, Ph.D. a Ing. Janě Chomoucké, Ph.D. za účinnou metodickou, pedagogickou a odbornou pomoc a další cenné rady při zpracování diplomové práce. V Brně dne podpis autora
9 Vysoké učení technické v Brně Fakulta elektrotechniky a komunikačních technologií Ústav mikroelektroniky POPISNÝ SOUBOR ZÁVEREČNÉ PRÁCE Autor: Název závěrečné práce: Název závěrečné práce ENG: Anotace závěrečné práce: Anotace závěrečné práce ENG: Bc. Jiří Polický Využití uhlíkových nanotrubic pro realizaci elektrod tlustovrstvých senzorů Carbon nanotubes utilization for fabrication of thick-film sensors electrodes Tato práce se zabývá problematikou detekce těžkých kovů s použitím miniaturizovaných tlustovrstvých senzorů. Pracovní elektroda pro tyto senzory byla připravena pomocí tlustovrstvé pasty za použití prášku s uhlíkovými nanotrubicemi, pojiva a ředidla. Vyrobené elektrody byly proměřeny při detekci iontů olova a kadmia v tříelektrodovém systému diferenčně pulzní voltametrií v acetátovém pufru. Získané výsledky byly porovnány s uhlíkovou elektrodou vytvořenou ze speciální komerční tlustovrstvé polymerní pasty. Na závěr je zde popsána i možnost aktivace povrchu pracovní elektrody kyselinou dusičnou a ověření detekce těžkých kovů na reálném biologickém vzorku. This work covers an area of heavy metals detection by miniaturized thick film sensors. Working electrode of these sensors was fabricated using thick film paste that was prepared as a nanocomposition of carbon nanotubes powder, suitable vehicle and a thinner. The response of fabricated electrodes to cadmium and lead ions was measured using differential pulse voltammetry in an acetate buffer solution using a three electrode
10 sytem. The results were compared with the carbon electrode made from special commercial thick film polymer paste. Finally the possibility of working electrode surface activation with nitric acid and heavy metals on real biological sample detection is described here. Klíčová slova: Klíčová slova ENG: Tištěná elektroda, Senzor, Uhlíkové nanotrubice, Těžké kovy, Diferenční pulzní voltametrie. Thick film electrode, Sensor, Carbon nanotubes, Heavy metals, Diferential pulse voltamettry Typ závěrečné práce: Datový formát elektronické verze: Jazyk závěrečné práce: Přidělovaný titul: Vedoucí závěrečné práce: diplomová formát pdf český Ing. Ing. Jan Prášek, Ph.D. Škola: Fakulta: Vysoké učení technické v Brně Fakulta elektrotechniky a komunikačních technologií Ústav: Studijní program: Studijní obor: Ústav mikroelektroniky Elektrotechnika, elektronika, komunikační a řídicí technika Mikroelektronika
11 OBSAH 1 ÚVOD ELEKTROCHEMIE ELEKTROCHEMICKÉ ANALYTICKÉ METODY Elektrochemický článek Potenciometrie Polarografie Voltametrie NESTACIONÁRNÍ ELEKTROCHEMICKÉ METODY Lineární voltametrie Cyklická voltametrie Amperometrie POUŽÍVANÉ ELEKTRODY HYGIENICKÉ LIMITY UHLÍKOVÉ NANOTRUBICE VÝROBA CNT Laserové odpařování Metoda uhlíkového oblouku (Arc Discharge Production) Depozice chemických par (CVD) Depozice chemických par v plazmatu (PECVD) MĚŘICÍ APARATURA MĚŘICÍ CELA VÝROBA VLASTNÍCH PRACOVNÍCH ELEKTROD ELEKTROCHEMICKÉ SENZORY EXPERIMENTÁLNÍ ČÁST REALIZACE PRACOVNÍCH ELEKTROD POVRCH ELEKTROD PRAKTICKÉ MĚŘENÍ Základní roztok Nastavení potenciostatu MĚŘENÍ IONTŮ OLOVA MĚŘENÍ IONTŮ KADMIA DETEKČNÍ LIMITY LEPTÁNÍ ELEKTROD POUŽITÉ CHEMIKÁLIE MĚŘENÍ REÁLNÝCH VZORKŮ ZÁVĚR LITERATURA
12 Seznam obrázků Obr. 1 Rozdělení elektroanalytických metod [10] Obr. 2 Příklad uspořádání elektrochemického článku [12] Obr. 3 Schéma a realizace základního uspořádání elektrochemické cely pro potenciometrická měření [10] Obr. 4 Jaroslav Heyrovský [2] Obr. 5 Příklad polarizační křivky základního elektrolytu [12] Obr. 6 Vložený potenciál a měřený signál v diferenční pulzní voltametrii [12] Obr. 7 Schematické znázornění elektrochemické rozpouštěcí analýzy (I - koncentrační fáze, II rozpouštěcí fáze) [12] Obr. 8 Průběh potenciálu a) a proudová odezva b) v SW voltametrii [12] Obr. 9 Katodicko-anodický voltamogram [18] Obr. 10 Rotující disková elektroda (RDE) [12] Obr. 11 Model uhlíkových nanotrubic a) jednostěnná CNT b) vícestěnná CNT [25] Obr. 12 Chirální vektor [28] Obr. 13 Struktury a) lenošky (armchair), b) cikcak (zigzag), c) chirální (chiral) [28] Obr. 14 Experimentální zařízení pro syntézu uhlíkových nanotrubiček laserovým odpařováním [28] Obr. 15 Měřící cela [12] Obr. 16 Zapojení měřicí aparatury v a) dvouelektrodovém a b) tříelektrodovém uspořádání [12] Obr. 17 Měřicí cela použita při experimentu (vpravo detail) Obr. 18 Princip sítotisku [26] Obr. 19 Příklad komerčně vyráběného senzoru AC1.W*.R* [31] Obr. 21 a) sítotiskový poloautomat Tesla UL 1505 A, b) pec pro výpal tlustých vrstev BTU TFF Obr. 20 Geometrická plocha elektrody stanovená na Olympus SZ
13 Obr. 22 Substrát s elektrodami MW Obr. 23 Elektroda MW Obr. 24 SEM 15kV, zvětšení 25kx, MW Obr. 25 SEM 15kV, zvětšení 25kx, MW Obr. 26 SEM 15kV, zvětšení 25kx, MW Obr. 27 SEM 15kV, zvětšení 25kx, MW Obr. 28 SEM 15kV, zvětšení 25kx, MW Obr. 29 SEM 15kV, zvětšení 25kx, DW Obr. 30 SEM 15kV, zvětšení 25kx, BQ Obr. 31 SEM 2kV, zvětšení 25kx, MW Obr. 32 Ruční přenosný potenciostat PalmSens Obr. 33 Měřicí pracoviště Obr. 34 Nastavení metody DPV na potenciostatu PalmSens (nastavené parametry - vpravo)41 Obr. 35 Příklad odezvy elektrody MW1 při stanovení Pb získané pomocí DPV Obr. 36 Kalibrační křivky WE měřené na iontech Pb Obr. 37 Příklad odezvy elektrody MW1 na přídavky Cd získané pomocí DPV Obr. 38 Kalibrační křivky WE získané při stanovení kadmia v roztoku Obr. 39 Měření detekčního limitu olova elektrody MW Obr. 40 Měření detekčního limitu kadmia elektrody MW Obr. 41 Leptací lázeň kyseliny dusičné Obr. 42 Vliv leptání elektrody na její proudovou odezvu - MW Obr. 43 Měření reálných vzorků elektrodou MW
14 Seznam tabulek Tab. 1 Limitní hodnoty upravující množství znečištění Tab. 2 Složení past pro výrobu WE elektrod Tab. 3 Poměr složek acetátového pufru v závislost na ph Tab. 4 Proudové odezvy v závislosti na leptání
15 Úvod 1 Úvod S nárůstem produkce výroby roste stále více odpadů, které tato industriální část průmyslu vytváří. S tím souvisí i množství nebezpečných látek, které ovlivňují životní prostředí a v konečném důsledku i lidské zdraví (znečištění pitných zdrojů, dusičnany v zemědělské půdě atd.). Proto je nutné množství těchto látek monitorovat a dohlížet na dodržování předepsaných limitů. K detekci a stanovení koncentrace látky v roztoku se kromě jiných, převážně optických technik využívá elektrochemické analýzy založené na polarografii a voltametrii [1]. Polarografie byla velmi oblíbenou a přesnou metodou minulého století. Její objev je spojen se jménem prof. Jaroslava Heyrovského, který za tento objev obdržel v roce 1959 Nobelovu cenu [2]. Jedná se o měření analytu za použití rtuťové kapkové elektrody. Dnes se z důvodu toxicity rtuti od této metody ustupuje a přechází se na voltametrii využívající tuhých elektrod. Ke sledování a rozborům látek je převážně nutné rozsáhlé laboratorní vybavení, které nás limituje nejen svými rozměry, ale i provozními náklady. S rostoucí integrací se v současné době daří vyrobit velmi rychlá a komplexní elektronická zařízení ve formě přenosných přístrojů. Omezujícím prvkem v měřicí sestavě ovšem zůstává elektrodový systém využívaný při detekci. Z tohoto důvodu je snaha nahradit klasické elektrody elektrodami miniaturizovanými. Jednou z možností je vytvářet elektrody pomocí technologie tlustých vrstev [3], [4], [5]. Jedná se o relativně levný nevakuový proces vytváření vrstev specifických vlastností. Zpočátku byla tato technologie využívána pro výrobu hybridních integrovaných obvodů převážně v prototypové a malosériové výrobě [3]. S masivním nárůstem CMOS technologie a se zdokonalující se technologií povrchové montáže se tlusté vrstvy pro výrobu integrovaných obvodů dostaly do pozadí. Nově si své místo našly na poli nekonvenčních aplikací, jako jsou topné elementy, rychlotavné pojistky, displeje, senzory, apod. [5], [6]. Se snahou miniaturizace senzorů, dochází ke zmenšování aktivních ploch jednotlivých elektrod. To má za následek zhoršení parametrů celého měřicího systému, především zhoršení detekčních limitů a citlivosti [7]. Možnost jak tyto parametry opět zlepšit, je zvýšit aktivní plochu elektrod užitím nanomateriálů, jako jsou například uhlíkové nanotrubice a nanotyčinky [8]. Vytváření nanostrukturovaných povrchů elektrod je možné přímým růstem uhlíkových nanotrubic přímo na substrátu, jak je popsáno v [8] a [9]. Jednodušší metodou je příprava pasty s obsahem nanomateriálů ve formě prášku, který je smíchán s vhodným pojivem a nanesen na předem připravený substrát sítotiskem, máčením, dispenzerem, nástřikem atd
16 Úvod Tato práce se zabývá možností zvětšení aktivní plochy pracovních elektrod miniaturních elektrochemických senzorů při zachování jejich geometrických rozměrů vytvořením nanostrukturovaného povrchu elektrod. Zvětšení aktivního povrchu je docíleno vytvořením polymerní tlustovrstvé pasty s využitím uhlíkových nanotrubic. Cílem je vytvořit pracovní elektrodu, která se bude svými detekčními schopnostmi při detekci těžkých kovů blížit klasické polarografické elektrodě
17 Elektrochemie 2 Elektrochemie 2.1 Elektrochemické analytické metody Elektrochemické analytické metody jsou založeny na měření některé elektrické veličiny (napětí na elektrodách, elektrický proud, vodivost roztoku, relativní permitivita). Měřená veličina musí být jednoznačně určena. Rozdělení elektroanalytických metod je na obr. 1. Obr. 1 Rozdělení elektroanalytických metod [10] Většina elektroanalytických metod je založena na redoxní reakci. Jsou to takové reakce při kterých dochází k výmněně elektoronů mezi reakčními složkami, čímž dochází k oxidaci nebo redukci. [10], [11], [12]. Redoxní reakce D (1) Oxidace: ztráta elektronů probíhající na anodě Redukce: příjem elektronů probíhající na katodě Oxidační činidlo: akceptor elektronů, D Redukční činidlo: donor elektronů, D Vedení elektrického proudu: Vodiče první třídy kovy přenos náboje zajišťují elektrony
18 Elektrochemie Vodiče druhé třídy elektrolyty přenos náboje zajišťují ionty Systém s kombinovanou vodivostí je elektrodový proces (elektrolýza) [10], [13] Elektrochemický článek Základním prvkem elektrochemických analytických metod založených na redoxní reakci je elektrochemický článek (obr. 2). Obě elektrody jsou v systému fyzicky odděleny. Přenos elektronů mezi elektrodami je umožněn vnějším vodičem. Elektroda je zde pevná vodivá fáze v kontaktu s roztokem elektrolytu. Reakce probíhají na rozhraní pevné a vodivé fáze. Solný můstek zajišťuje vodivé spojení mezi elektrodami, ale brání promíchání roztoků [10], [11], [12]. Obr. 2 Příklad uspořádání elektrochemického článku [12] Vztah definovaný mezi potenciálem kovové elektrody a aktivitou jejich iontů v roztoku na jejím povrchu je dán Nernstovou rovnicí. Výsledkem je elektrodový potenciál charakterizující elektrodu [10], [12], [14]. (2) kde E elektrický potenciál elektrody E 0 standardní elektrodový potenciál R molární plynová konstanta (8,314 J/K/mol) T teplota v kelvinech (teplota ve C + 273,15)
19 Elektrochemie n počet vyměněných elektronů F Faradayova konstanta (96485 C/mol) a aktivita oxidované nebo redukované formy U zředěných roztoků se místo aktivity dosazuje relativní látková koncentrace Potenciometrie Analytická metoda, při které se koncentrace analytu stanovuje z napětí elektrochemického článku tvořeného indikační elektrodou ponořenou v analyzovaném roztoku a referenční elektrodou spojenou s analyzovaným roztokem pomocí solného můstku (obr. 3). Měřeným článkem neteče elektrický proud rovnovážná potenciometrie [10], [11]. Obr. 3 Schéma a realizace základního uspořádání elektrochemické cely pro potenciometrická měření [10] Polarografie Polarografie je světově spojena českým jménem profesora Jaroslava Heyrovského (obr. 4), který za objev polarografie dostal v roce 1959 Nobelovu cenu za chemii [2]. Tradiční polarografie prošla za dobu své existence rozsáhlým vývojem. V současné době v laboratořích převládá v používání voltametrických technik s eliminací nabíjecího proudu a s akumulací analytu. Jako polarografie se označuje z historických důvodů voltametrie používající jako pracovní elektrodu rtuťovou kapající elektrodu. Obr. 4 Jaroslav Heyrovský [2] Obě metody, polarografie i voltametrie, jsou založeny na měření polarizačních křivek (příklad viz obr. 5), což vyjadřuje závislost proudu tekoucího pracovní elektrodou na vloženém potenciálu. Chybí-li v roztoku látka, která by způsobovala redoxní reakci, dochází k polarizaci pracovní elektrody a proud jí neteče. V opačném případě, je velikost anodického nebo katodického proudu mírou koncentrace depolarizátoru [12]
20 Elektrochemie Obr. 5 Příklad polarizační křivky základního elektrolytu [12] Voltametrie Voltametrie, stejně jako polarografie, využívá měření polarizačních křivek. Jedná se o stacionární metodu, tzn., že měření není závislé na čase. Při voltametrii se pro měření používají zásadně tuhé elektrody z různých materiálů (obvykle elektrody platinové, zlaté a uhlíkové). Časté je použití rotujících diskových elektrod, kde se depolarizátor dostává k povrchu rotující diskové elektrody konvektivně-difúzním transportem. Konvekcí (prouděním) se dostává depolarizátor do blízkosti povrchu elektrody, kde se utváří tenká difúzní vrstva. Pro konvektivně-difúzní limitní proud platí Levičova rovnice (3) [12] ve tvaru: π ν ω (3) kde I l konvektivně difúzní limitní proud, k numerická konstanta, z počet vyměňovaných elektronů, F Faradayova konstanta, r poloměr diskové elektrody, D difúzní koeficient, ν kinematická viskozita roztoku, ω úhlová rychlost otáčení elektrody, c koncentrace depolarizátoru. Z rovnice (3) vyplývá, že užitečný signál (difúzní proud) je přímo úměrný koncentraci roztoku. Při voltametrické analýze se zpravidla polarizuje elektroda v obou směrech (od kladnějších k záporným potenciálům a naopak) z důvodu hystereze měření (rozpouštěcí voltametrie) [10], [11], [12], [13]
21 Elektrochemie Diferenční pulzní voltametrie (DPV) V kombinaci s předchozím elektrolytickým nahromaděním analytu na elektrodě je podle [15] a [16] diferenční pulzní voltametrie považována za nejvýhodnější elektrochemickou metodou. Měří se zde diference proudu těsně před začátkem a těsně před koncem potenciálového pulzu (obr. 6). Výhodou pulzních technik je potlačení nabíjecího kapacitního proudu, dochází však i k mírnému útlumu užitečného (faradaického) proudu, avšak tento pokles není tak strmý, jako u proudu kapacitního. Důsledkem odlišného průběhu poklesu kapacitního, resp. faradaického proudu s časem je, že při měření s využitím skokových potenciálových pulzů měřený proud po určitý krátký časový okamžik odpovídá pouze faradickému proudu. Diferenční pulzní voltametrií lze stanovit koncentrace analytů až 10-8 mol l -1. Je-li před počátkem měření učiněn akumulační krok, lze teoreticky meze stanovitelnosti posunout až na hodnoty mol l -1 [11], [12], [15], [16]. -E [V] I2 I1 [A] Obr. 6 Vložený potenciál a měřený signál v diferenční pulzní voltametrii [12] Rozpouštěcí (stripping) voltametrie Metoda slučuje výhodu předběžného akumulování látky na povrchu elektrody s následným voltametrickým měřením množství vyloučeného povlaku (obr. 7). Tato metoda umožňuje zvýšení citlivosti koncentrace až o několik řádů. Výhodné je provádět zakoncentrování analytu elektrolyticky. K provedení rozpouštěcího kroku lze použít jakékoliv elektrochemické techniky. V současné době se rozpouštěcí analýza nejčastěji kombinuje s DPV. Elektrolytické nahromadění analytu na elektrodě se většinou provádí na konstantním potenciálu, který se volí tak, aby elektrodová reakce probíhala dostatečnou rychlostí. Dalšího podstatného zcitlivění lze dosáhnout zpětným periodickým přepínáním polarizačního napětí na potenciál akumulace elektrolytu. Roztokem se během předběžné elektrolýzy míchá, aby se
22 Elektrochemie zajistil konstantní přísun analytu z roztoku. Následně získaná rozpouštěcí křivka má tvar vrcholu (píku). Potenciál maxima vrcholu E 1/2 kvalitativně určuje daný analyt, výška vrcholu (resp. plocha vrcholu) odpovídá koncentraci látky (obr. 7). [12], [15], [16], [17] Obr. 7 Schematické znázornění elektrochemické rozpouštěcí analýzy (I - koncentrační fáze, II rozpouštěcí fáze) [12] Možnosti akumulace analytu [15]: - akumulace kovů ve formě amalgámu do rtuťové visící kapky nebo do filmu rtuti polarografie, - akumulace kovu na tuhé elektrodě v podobě filmu (stanovení rtuti) voltametrie, - depozice na povrchu elektrody v podobě málo rozpustné sloučeniny (AgCl), - adsorpce analytu na povrchu elektrody (stanovení nitrobenzenu), - nakoncentrování extrakcí (stanovení Pb, Zn, Cd v pitné vodě), - zakoncentrování analytu pomocí iontové výměny. Square wave voltametrie (SWV) Od klasické AC polarografie se SW voltametrie liší tím, že se místo sinusového napětí superponovaného na lineárně rostoucí DC napětí superponuje malé obdélníkové napětí (obr. 8a). Proud se měří jen těsně před změnou znaménka pravoúhlého signálu (maximálně potlačena nabíjecí složka proudu). Získaný měřený signál má tvar vrcholu (obr. 8b). Mez stanovitelnosti pro reverzibilní systémy činí asi mol.l -1, pro ireverzibilní systémy asi 10-6 mol.l -1 [11], [12], [15], [16]
23 Elektrochemie Obr. 8 Průběh potenciálu a) a proudová odezva b) v SW voltametrii [12] 2.2 Nestacionární elektrochemické metody Při nestacionárních elektrochemických metodách je měřená veličina funkcí času. Při potenciostatických metodách je měřena časová závislost proudu na nastaveném potenciálu, při galvanostatických metodách je sledována časová odezva potenciálu v závislosti na nastaveném vstupním proudu [12] Lineární voltametrie Nestacionární technika s lineárně rostoucím potenciálem. Elektroda se zde polarizuje rychleji než v případě klasické voltametrie a to 10 až 1000 mv/s. Rychlá změna potenciálu způsobí vyčerpání analytu v celém okolí elektrody. Výsledným signálem lineární polarografie je vrchol na křivce (vytvoří se maximum), kde jeho potenciál udává kvalitativní parametr a velikost je úměrná koncentraci. Metoda lineární voltametrie slouží rovněž ke studiu kinetiky elektrodových reakcí [12] Cyklická voltametrie Při cyklování vstupního potenciálového impulzu ve tvaru rovnoramenného trojúhelníku můžeme studovat reverzibilitu měřeného systému. Studuje se zde fáze redukce a následná oxidace analytu. Výsledkem měření je katodicko anodická křivka (obr. 9). Při reverzibilní elektrodové reakci se získá stejně vysoký katodický i anodický vrchol (pík) [12], [15], [18]
24 Elektrochemie Legenda: Obr. 9 Katodicko-anodický voltamogram [18] 1. neprobíhá žádný děj 2. počátek oxidačního procesu 3. maximum anodického proudu 4. pokles anodického proudu s vyčerpáním oxidované formy 5. počátek redoxního děje 6. redukce látky na elektrodě 7. maximum katodického proudu 8. pokles katodického proudu s vyčerpáním redukované formy Amperometrie Jedná se o metodu odvozenou od voltametrie. Detekce analytu je provedena velikostí protékajícího proudu pracovní elektrodou, na kterou je přiložen konstantní potenciál zvolen tak, aby elektrodou tekl limitní proud. [12]
25 Elektrochemie 2.3 Používané elektrody Elektrody I. druhu Obvykle se používají jako pracovní elektrody (WE), jsou polarizovatelné. Na elektrodách probíhají reakce přenosu elektronu mezi kovem a kationtem, aniontem nebo elektricky neutrální částicí roztoku. Půlvlnový potenciál závisí na aktivitě vlastních iontů (dle Nernstovy rovnice). Příklad elektrody I. druhu je tuhá stříbrná, platinová a uhlíková elektroda, například ve tvaru rotující diskové elektrody obr. 10, [10], [12], [19]. Obr. 10 Rotující disková elektroda (RDE) [12] Elektrody II. druhu Jsou nejčastěji používané jako nepolarizovatelné referenční elektrody (RE). Tyto elektrody se skládají ze tří fází (kov pokrytý jeho málo rozpustnou solí ponořený do roztoku obsahující aniont této soli solný můstek 2.1.1). Elektrodová reakce je kombinací dílčích reakcí na obou rozhraních. Potenciál elektrody je řízen koncentrací aniontu, se kterým kationty elektrody tvoří nerozpustnou sloučeninu. Příklad: kalomelová elektroda (Hg Hg 2 Cl 2 K +, Cl -, H 2 O), argentchloridová elektroda (Ag AgCl K +,Cl -, H 2 O), merkursulfátová elektroda (Hg Hg 2 SO 4 K +, SO 2-4, H 2 O) [12], [19]. Elektrody oxidačně redukční Elektrody jsou složené z inertního vodiče elektronů (kovy Pt, Au, nebo Hg a grafit) ponořeného do roztoku obou oxidačních forem jedné látky. Elektroda zprostředkovává výměnu elektronů mezi oxidovanou a redukovanou formou. Rozdíl od elektrod I. druhu je, že oba oxidační stavy mohou být v různých koncentracích [12], [19]
26 Elektrochemie Polymerní elektrody Trojfázová soustava tvořená vodičem elektronů pokrytým filmem elektronově, nebo iontově vodivým polymerem [19]. Elektrody iontově selektivní (membránové) Elektrody založené na vzniku potenciálu na membráně, jež je pro různé ionty různě propustná. Elektroda je tvořena membránou oddělující vnější (měřený) a vnitřní roztok. Potenciál elektrody je určen výměnou iontů mezi membránou a roztokem (nikoli redoxní reakcí) [12]. 2.4 Hygienické limity Limitní hodnoty znečištění vodních zdrojů určují vyhlášky vydané českou republikou v roce 2004, jedná se o vyhlášku č. 252/2004 Sb. upravující hygienické požadavky na pitnou a teplou vodu a četnost a rozsah kontroly pitné vody. Další vyhláškou č. 275/2004 Sb.. Jedná se o vyhlášku o požadavcích na jakost a zdravotní nezávadnost balených vod a o způsobu jejich úpravy. Limitní hodnoty z těchto vyhlášek jsou shrnuty v tab. 1. Tab. 1 Limitní hodnoty upravující množství znečištění pitná voda balených přírodních minerálních vod kojenecké a pramenité vody koncentrace Prvek Značka µg/l µmol/l Měď Cu ,480 Olovo Pb 10 0,483 Kadmium Cd 5 0,445 Rtuť Hg 1 0,050 Měď Cu ,480 Olovo Pb 10 0,483 Kadmium Cd 3 0,267 Rtuť Hg 1 0,050 Měď Cu ,496 Olovo Pb 5 0,241 Kadmium Cd 2 0,178 Rtuť Hg 0,5 0,025 podle [20] podle [21] podle [21]
27 Uhlíkové nanotrubice 3 Uhlíkové nanotrubice Z Levičovy rovnice (3) vyplývá, že jestliže chceme vyrobit miniaturizovanou elektrodu s co nejmenším průměrem a chceme-li zároveň dosáhnout vysoké proudové odezvy je nutné zvětšit aktivní povrch elektrody. Jediným možným řešením je zvětšovat elektrodu ve třetím rozměru, tj. dosáhnout co nejvíce porézního povrchu. Vhodným materiálem jsou uhlíkové nanotrubice, které mohou na povrchu elektrody vytvářet strukturu připomínající les (v ideálním případě přímého růstu CNTs na elektrodě). Uhlíkové nanotrubice mají jedinečné vlastnosti, jedná se o válcovitou strukturu seskupení atomů uhlíku o průměru několik nanometrů (1/50000 šíře lidského vlasu) a délky až několik mikrometrů [22].. Dělí se na jednostěnné (single-wall nanotube SWNTs) a vícestěnné (multi-wall nanotube - MWNTs), jak je zobrazeno na obr. 11. I přesto, že se o nanostrukturách ve svém článku zmiňují fyzikální chemici Radushkevich a Lukyanovich již v roce 1952 [23] a Oberlina, Endoa a Koyama v roce 1976, většina akademické populace přisuzuje objev nanotrubic složených z grafitového uhlíku Sumio Iijima (NEC) z roku 1991 [24]. Obr. 11 Model uhlíkových nanotrubic a) jednostěnná CNT b) vícestěnná CNT [25] Struktura nanotrubice může být vytvořena zabalením graphenu do bezešvého válce. Graphen je rovinná síť vzájemně propojených atomů uhlíku uspořádaných do tvaru šestiúhelníků, podobně jako u pláství medu [19]. Podle směru stočení grafitového archu rozdělujeme nanotrubice do tří základních skupin podle struktury. Jak ukazuje obr. 12 a obr. 13 rozeznáváme strukturu chirální (chiral) - n m 0, lenošky (armchair) - n = m 0 a cikcak (zigzag) - n 0, m = 0. Závislost elektrických vlastností uhlíkových nanotrubic závisí na směru chirálního vektoru, je považována za vodič, je-li n-m dělitelné třemi, v jiných
28 Uhlíkové nanotrubice případech se jedná o polovodič. Průměr uhlíkové SWNT je dán d = (n 2 + m 2 + nm) 1/2.0,0783 [nm]. Teoreticky by vodiče z nanotrubic mohly mít proudovou hustotu až A.cm -2, což odpovídá přibližně 1000 násobku vodivosti kovů, jako jsou stříbro a měď. [27], [28], [29] C h = na 1 + ma 2 ZIGZAG Obr. 12 Chirální vektor [28] Obr. 13 Struktury a) lenošky (armchair), b) cikcak (zigzag), c) chirální (chiral) [28] Uhlíkové nanotrubice jsou nejsilnější a nejtužší materiál na zemi. Vícestěnné uhlíkové nanotrubice dosahují pevnost v tahu až 63 gigapascalů, měrná pevnost nanotrubic je až kn.m.kg -1 (uhlíková ocel 154 kn.m.kg -1 ). Tepelná vodivost nanotrubic je výborná v podélném směru až 6000 W.m.K -1 (měď 385 W.m.K -1 ). Teplotní stabilita uhlíkových
29 Uhlíkové nanotrubice nanotrubic je odhadnuta až na 2800 C ve vakuu [19], [23], [24]. Jelikož se jedná o materiál, který má jedny z nejlepších mechanických a elektrických vlastností, je hojně využíván např. jako hrot skenovacího mikroskopu [30], jako elektrody kapacitorů [4], apod. 3.1 Výroba CNT Uhlíkové nanotrubice je možné vyrobit několika možnými způsoby [28]: laserovým odpařováním, metodou uhlíkového oblouku, depozicí chemických par (CVD), depozice chemických par v plazmatu (PECVD) Laserové odpařování Si trubička obsahující argon (Ar) a grafitový terčík jsou zahřáty na 1200 C. V trubičce, je vodou chlazený měděný kolektor. Grafitový terčík obsahuje malé množství kobaltu a niklu, které působí jako katalytické jádro pro tvoření trubiček (obr. 14). Svazek pulzního laseru dopadá na grafitový terčík a tím odpařuje uhlík z grafitu. Argon transportuje atomy uhlíku z horké zóny k Cu kolektoru na kterém kondenzuje, tzn. růst vícestěnných nanotrubic o průměru 20 nm, délky až 100 µm a počtu plášťů [27], [28] Obr. 14 Experimentální zařízení pro syntézu uhlíkových nanotrubiček laserovým odpařováním [28] Metoda uhlíkového oblouku (Arc Discharge Production) Další možností výroby CNTs je syntéza pomocí uhlíkového oblouku. Na uhlíkové elektrody od průměru 6-12 mm, které jsou od sebe vzdáleny 1-4 mm. V okolí elektrod je atmosféra hélia v podtlaku. Stejnosměrné napětí vkládané na elektrody je v rozsahu 20 až 25 V. Atomy uhlíku jsou vystřelovány z anody a na katodě vytvářejí nanotrubice. K vytváření SWNTs je nutné použít katalyzátor - kobalt, nikl nebo železo. Není-li použit
30 Uhlíkové nanotrubice katalyzátor, vytvářejí se MWNTs. Touto metodou je možné vytvořit trubičky o průměru 1 až 5 nm a délky 1 µm. [27] Depozice chemických par (CVD) Na substrátu je vrstva kritických částic (Ni, Co, Fe, Mo), velikost těchto částic určuje velikost nanotrubic. Tento substrát je umístěn v reaktoru při teplotě 700 C. Do reaktoru jsou přivedeny dva plyny inertní (N, H) a hydrokarbonový plyn obsahující uhlík (acetylen C 2 H 2, metan CH 4, etan - C 2 H 6 ) Depozice chemických par v plazmatu (PECVD) Při uhlíkovém výboji v parách hydrokarbonových plynů při teplotě 1100 C dochází k rozkladu tohoto plynu a vznikají atomy uhlíku, které kondenzují na chladnějším místě. Takto vytvořené trubičky jsou s otevřenými konci, k čemuž při jiných metodách nedochází. [27]
31 Měřící aparatura 4 Měřicí aparatura 4.1 Měřicí cela Měřicí aparatura je sestavena z baňky s analyzovaným roztokem, elektrod a voltametrického analyzátoru (obr. 15). [12] AE RE WE Obr. 15 Měřící cela [12] Zapojení analyzátoru a elektrod je možné provést dvěma základními způsoby. Jedná se o dvouelektrodové a tříelektrodové zapojení. Při dvouelektrodovém zapojení dochází k úbytku napětí při průchodu elektrického proudu roztokem (tvoří el. odpor), a proto není znám přesný potenciál pracovní elektrody (obr. 16a). V praxi se více využívá zapojení se třemi elektrodami (obr. 16b). Elektrický článek je zde rozšířen o pomocnou elektrodu. Proud teče mezi pomocnou a pracovní elektrodou a skutečný potenciál napětí se měří mezi
32 Měřící aparatura referenční elektrodou a pracovní elektrodou za bezproudového stavu. V této práci bylo v praktickém měření použito tříelektrodového zapojení obr. 17. Obr. 16 Zapojení měřicí aparatury v a) dvouelektrodovém a b) tříelektrodovém uspořádání [12] Referenční elektroda Pomocná elektroda Obr. 17 Měřicí cela použita při experimentu (vpravo detail) 4.2 Výroba vlastních pracovních elektrod Pravcovní elektroda Pro výrobu vlastních pracovních elektrod byla zvolena tlustovrstvá technologie (TLV). Jedná se o aditivní nevakuový proces, který zajišťuje optimální rozměry pracovní elektrody a možnost reprodukovatelně nanášet požadované materiály na substrát. Pomocí sítotisku (obr. 18) je stěrkou protlačena připravená pasta skrz síto s vytvořeným motivem na substrát,
33 Měřící aparatura nejčastěji korundovou keramiku (Al 2 O 3 ), nebo sklo. Hlavní požadavek na nanášenou pastu je správná viskozita umožňující správnou depozici. Pasta je složena z lakové a pojivové složky. Při výpalu dochází k odpaření lakové složky a pojivová složka se vytvrdí - zajišťuje konzistentnost po výpalu. Podle použitého materiálu matrice můžeme TLV pasty rozdělit na anorganické a polymerní. Jejich základním rozdílem je teplota pro vytvrzování natištěné vrstvy. Polymerní se vytvrzují do teploty přibližně 200 C, vrstvy z anorganických past se vypalují při teplotách nad 800 C. Nevýhody polymerních past je omezená pracovní teplota a špatná odolnost vůči vlhkosti. Tloušťka nanášené vrstvy se pohybuje v rozměrech 5 až 80 mikrometrů. [26] Obr. 18 Princip sítotisku [26] 4.3 Elektrochemické senzory Elektrochemický senzor se skládá ze dvou až čtyř elektrod. Nejčastější konfigurace je senzor obsahující tři elektrody. Jedná se o referenční elektrodu elektroda II. druhu (popsáno v kap. 2.3), nejčastěji Ag/AgCl elektroda, pomocnou elektrodu I. druhu též popsané v kap a elektrodu pracovní. Všechny tyto elektrody je možné udělat planární technologií na společném substrátu. [5] Tříelektrodové elektrochemické senzory na bázi tlustých vrstev jsou vyráběny např. firmou BVT Technologies, a.s. obr. 19 [31]. U těchto komerčně vyrobených senzorů je pracovní elektroda z Pt, Au, nebo kombinace AuPd pasty a dalších, referenční elektroda nejčastěji z AgPd nebo Ag/AgCl pasty. Pomocná elektroda je tvořena PtAu nebo PtPd pastou (viz. katalogový list k senzorům typu AC1.W*.R*)
34 Měřící aparatura Obr. 19 Příklad komerčně vyráběného senzoru AC1.W*.R* [31] Požadavky na vlastnosti senzorů podle [5]: Jednoznačná závislost výstupní veličiny na veličině měřené. Velká citlivost senzoru. Vhodný průběh statických charakteristik. Velká přesnost a časová stálost. Minimální závislost na vlivech okolního prostředí (mimo vlivů měřených). Minimální zatěžování měřeného objektu. Vysoká spolehlivost. Velmi nízká pořizovací cena a nízké náklady na provoz. Jednoduchá obsluha a údržba. Vlastnosti senzorů podle [5]: Statické vlastnosti: o Statická přenosová charakteristika (kalibrační křivka) udává vztah mezi vstupní a měřenou veličinou. o Citlivost je definována jako sklon statické přenosové charakteristiky
35 Měřící aparatura o Limit detekce (práh citlivosti, dolní hranice měřícího rozsahu) je nejnižší hodnota měřené veličiny, která může být senzorem detekována. o Plný rozsah (horní hranice měřícího rozsahu) je nejvyšší hodnota měřené veličiny, která může být senzorem detekována. o Dynamický rozsah je dán intervalem dolní a horní hranicí měřícího rozsahu, tj. mezi limitem detekce a plným rozsahem. o Linearita udává maximální odchylku kteréhokoliv kalibračního bodu od odpovídajícího bodu na ideální statické přenosové charakteristice. o Hystereze je maximální rozdíl ve vstupu při jakékoliv hodnotě měřeného rozsahu, kdy hodnota je měřena nejdříve zvyšováním a poté snižováním měřené veličiny (nebo naopak). o Rozlišení nejmenší inkrement výstupu senzoru, který senzor zaznamená při změně výstupu. Odpovídá absolutní nebo relativní chybě senzoru. o Reprodukovatelnost je dána odchylkou mezi naměřenými hodnotami, které byly měřené při neměnné vstupní veličině a neměnných rušivých vlivech v krátkém časovém sledu. Dynamické vlastnosti: o Přechodová charakteristika je průběh výstupní veličiny v závislosti na čase při skokové změně vstupní veličiny. o Frekvenční charakteristika udává závislost přenosu a fázového úhlu na frekvenci, tj. rozdíl amplitudy a fáze výstupního signálu oproti signálu vstupnímu v závislosti na frekvenci
36 Experimentální část 5 Experimentální část Cílem experimentální části je realizace miniaturizované pracovní elektrody (WE) elektrochemického senzoru s proudovou odezvou odpovídající standardní elektrochemické pracovní elektrodě, která má několikanásobně větší geometrickou plochu. Zvětšení aktivního povrchu elektrody při zachování minimálních geometrických rozměrů bude realizováno využitím uhlíkových nanotrubic, které budou použity jako funkční složka při výrobě vlastních polymerních TLV past. Charakterizace realizovaných elektrod bude provedena při stanovení těžkých kovů (diferenčně pulzní voltametrií) obsažených v roztoku (detekce iontů olova a kadmia). Na závěr budou výsledky porovnány s komerčně dodávanou polymerní tlustovrstvou pastou speciálně určenou pro výrobu WE senzorů. 5.1 Realizace pracovních elektrod K výrobě pracovních elektrod bylo použito několik různých typů uhlíkových nanotrubic, které byly zakoupeny od firmy Sigma-Aldrich [32]. Tab. 2 Složení past pro výrobu WE elektrod MWCNT1 (MW1) MWCNT2 (MW2) MWCNT3 (MW3) MWCNT4 (MW4) MWCNT5 (MW5) MWCNT6 (MW6) množství typ označení výrobce 750 mg MWCNTs Sigma-Aldrich 2,3g CV59 pojivo ESL 800ul 402 ředidlo ESL 750 mg MWCNTs Sigma-Aldrich 2,3g 520 pojivo ESL 800ul 116 ředidlo ESL 200 mg MWCNTs Sigma-Aldrich 2,3g CV59 pojivo ESL 500 ul 402 ředidlo ESL 500 mg MWCNTs Sigma-Aldrich 3g CV59 pojivo ESL 600ul 402 ředidlo ESL 300 mg MWCNTs Sigma-Aldrich 2,3g CV59 pojivo ESL 1000 ul 402 ředidlo ESL 2g MWCNTs Sigma-Aldrich 2g CV59 pojivo ESL 700ul 402 ředidlo ESL
37 Experimentální část 750mg MWCNTs Sigma-Aldrich MWCNT7 (MW7) PMMA Polymetylmetakrylát pojivo aceton ředidlo 150 mg DWCNTs Sigma-Aldrich DWCNT1 (DW1) 3,5g CV59 pojivo ESL 300 ul 402 ředidlo ESL BQ (BQ221) komerční polymerní pasta na uhlíkovém základě DuPont Pro elektrody MW1, MW2, MW6 a MW7 byl požit typ (Sigma-Aldrich), jedná se o vícestěnné nanotrubice deponované pomocí CVD o průměru nm, síle stěny 5 40 nm a délce 0,5-2 µm. CNTs pro výrobu elektrody MW6 byly funkcionalizovány ferrocenem, který se již dříve ukázal jako možnost pro zlepšení odezvy elektrody [33]. Elektroda MW3 byla vyrobena z vícestěnných nanotrubic složených ze 3 až 19 vrstev graphenu (viz. kap. 3) s označením (Sigma-Aldrich). Nanotrubice jsou vyrobené pomocí CVD, délka nanotrubic je 0,5-200 µm, průměr 7-15 nm a síla stěny 3-6 nm. Hustota přibližně 2,1 g/ml. Na výrobu pasty pro elektrodu MW4 byly použity vícestěnné nanotrubice vyrobené pomocí CVD za přítomnosti HCl. Rozměry trubic jsou délka 2,5-20µm, průměr 6 13 nm, a jsou složeny ze 7 až 13 graphenových vrstev. Do pasty MW5 byly použity nanotrubice (Sigma-Aldrich) vyrobené pomocí CVD o délce 0,5 200 µm, průměru nm a síle stěny 5 15 nm. Elektroda DW1 byla vyrobena za použití dvoustěnných uhlíkových nanotrubic (Sigma-Aldrich). Dodaný prášek obsahuje 50-80% DWNT a 10-40% ostatních uhlíkových nanotrubic. Rozměry jsou: délka 50 µm, průměr 5 nm a síla stěny 1,3 až 2 nm. Nanotrubice byly vyrobeny pomocí CVD. Aby bylo možné připravit pastu správných parametrů pro technologický postup nanášení aktivní vrstvy pracovní elektrody sítotiskem, bylo nutné na přípravu past použít vhodné pojivo a ředidlo v poměru uvedeném v tab. 2. Pro přípravu past byla použita dvě pojiva od firmy firmy ESL ElectroScience [34]: 1. CV59 je pryskyřice rozpuštěná v BCA (butyl carbitol acetát). Pasta za použití tohoto pojiva musí byt po aplikaci zasušena a vypálena při teplotě 150 C po dobu 30 minut jedná se o polyamidovou pryskyřici rozpuštěnou v methyl-pyrrolidonu. Takto vytvořená pasta musí byt vysušena po dobu 15 minut při teplotě 125 C a následně vytvrzena v peci při teplotě 275 C po dobu 30 minut
38 Experimentální část Elektroda BQ byla vyrobena pomocí speciální komerční pasty BQ221 dodané firmou DuPont [35]. Jedná se o kompozitní vodivou uhlíkovou polymerní pastu pro výrobu pracovních elektrod biosenzorů s vysokou citlivostí. Pasta se pyšní nízkou rezistivitou, vysokou citlivostí a dlouhou životností. Pasty byly na předem připravený substrát naneseny pomocí sítotisku na keramickou destičku (Al 2 O 3 ), jak je popsáno v odstavci 4.2. Poloměr apertury v sítu byl 0,7 mm, což odpovídá ploše elektrody 1,54 mm 2. Přesná plocha elektrody 1,65 mm 2 (viz. obr. 20) byla změřena na Olympus SZ 61. Na tisk pasty bylo využito sítotiskového poloautomatu Tesla UL 1505 A (obr. 21a). Keramická destička obsahuje celkem 14 elektrod. Pro snazší dělení byla destička narýhována laserem (obr. 22). Další technologickou operací byl výpal. Dobu a teplotu výpalu udává každý výrobce dané pasty v jejím katalogovém listu, U námi připravených past byl tento údaj od výrobce dohledán v parametrech pojiva. Pec na výpal tlustovrstvých elektrod je zobrazena na obr. 21b. Analýza povrchu elektrod provedená elektronovým rastrovacím mikroskopem je zobrazena na obrázcích v kap Obr. 20 Geometrická plocha elektrody stanovená na Olympus SZ 61 Obr. 21 a) sítotiskový poloautomat Tesla UL 1505 A, b) pec pro výpal tlustých vrstev BTU TFF
39 Experimentální část Pracovní elektroda s MWNT Krycí vrstva ESL 4917 Vodivá vrstva ESL 9562-G 7,2 mm Obr. 22 Substrát s elektrodami MW1 Výjimkou při nanášení pasty na substrát byla elektroda MW7 (obr. 23), zde nebylo možné použít sítotisku, protože docházelo k velice rychlému odpařování ředidla (aceton) a tím způsobené tuhnutí pasty. Proto byla pasta na elektrodu nanesena špachtlí, tudíž u této elektrody nelze určit přesnou plochu elektrody. Obr. 23 Elektroda MW7 5.2 Povrch elektrod K analýze povrchu elektrod bylo použito rastrovacího elektronového mikroskopu Tescan Mira II. Na obr. 24 až obr. 30 jsou zobrazeny povrchy elektrod za použití urychlovacího napětí elektronů 15kV a nastaveného zvětšení 25 tisíc krát. Po zkoumání těchto obrázků bylo prokázáno, že při takto vysokém urychlovacím napětí dochází k prosvícení vrchních vrstev struktury. Proto je na obrázcích zobrazena pouze vnitřní struktura aktivního povrchu. I přesto je možné si z obrázků udělat představu o odlišnostech ve struktuře jednotlivých elektrod. Na všech snímcích je možné rozeznat uhlíkové nanotrubice obalené pojivem. Na obr. 31je snímek elektrody MW7 při urychlovacím napětím elektronů pouze 2kV. Je zde patrný povrch velice hustě pokrytý CNTs
40 Experimentální část Obr. 24 SEM 15kV, zvětšení 25kx, MW1 Obr. 25 SEM 15kV, zvětšení 25kx, MW3 Obr. 26 SEM 15kV, zvětšení 25kx, MW4 Obr. 27 SEM 15kV, zvětšení 25kx, MW5 Obr. 28 SEM 15kV, zvětšení 25kx, MW6 Obr. 29 SEM 15kV, zvětšení 25kx, DW1-38 -
41 Experimentální část Obr. 30 SEM 15kV, zvětšení 25kx, BQ221 Obr. 31 SEM 2kV, zvětšení 25kx, MW7 5.3 Praktické měření Měření probíhalo v tříelektrodovém zapojení v měřící cele popsané v kap Referenční elektroda byla použita Ag/AgCl SESV 17 (Elektrochemické Detektory, Turnov, Česká republika), pomocná elektroda byla platinová UMMPTB11 (Sycopel Scientific Limited, UK). Všechny dosažené výsledky byly měřeny na ručním přenosném potenciostatu obr. 32 od firmy Palm Instruments [36]. Celkový pohled na měřicí pracoviště je na obr. 33. Obr. 32 Ruční přenosný potenciostat PalmSens
42 Experimentální část Obr. 33 Měřicí pracoviště Základní roztok Měření probíhalo v acetátovém pufru o ph 5,4. Roztok je složen z a ml 0,2 M CH 3 COOH a (200 - a) ml 0,2 M CH 3 COONa. Poměr složek v závislosti na kyselosti je v tab. 3. Tab. 3 Poměr složek acetátového pufru v závislost na ph ph [-] 3,6 3,8 4 4,2 4,4 4,6 4,8 5 5,2 5,4 5,6 a [ml] Nastavení potenciostatu Měření bylo prováděno pomocí přenosného potenciostatu PalmSens (obr. 32) s použitím originálního softwaru dodávaného k přístroji. Potenciostat byl připojen k PC pomocí USB rozhraní. Měření probíhalo v rozsahu napětí od -1 V do 0 V (obr. 34). V první fázi, kdy je na elektrodu vložen záporný potenciál, dojde k redukci iontů na elektrodě. Při snižování napětí směrem k 0 V dojde ke zpětné oxidaci, tj. vyloučení iontů z elektrody zpět do roztoku. Směr redoxní reakce byl experimentálně ověřen v [37]
43 Experimentální část Obr. 34 Nastavení metody DPV na potenciostatu PalmSens (nastavené parametry - vpravo) 5.4 Měření iontů olova Pro měření pracovních elektrod byl jako přídavek těžkého kovu do pufru zvolen 10 mmol.l -1 octan olovnatý (CH 3 COO) 2 Pb namíchaný v acetátovém pufru. Postup měření byl zvolen tak, že byl v první řadě proměřen čistý pufr, bez jakéhokoliv přídavku, poté se postupovalo s přídavky 10 µl popř. 20 µl 10 mmol.l -1 roztoku s obsahem iontů olova. Po každém zvýšení koncentrace analytu, byla měřicí cela promíchána a teprve po té bylo spuštěno další měření. Změřený půlvlnový potenciál olova E 1/2 = -0,568 V viz. obr. 35. Příklad změřeného voltamogramu na elektrodě MW1 s přídavky olova je na obr. 35. V legendě je zaznamenán objemový přídavek 10 mmol.l -1 (CH 3 COO) 2 Pb v 5 ml acetátového pufru
44 Experimentální část Pufr 10µl_Pb 20µl_Pb 30µl_Pb 40µl_Pb 50µl_Pb 60µl_Pb 70µl_Pb 80µl_Pb 90µl_Pb 100µl_Pb 110µl_Pb 30 I [ua] µl_Pb 130µl_Pb 140µl_Pb 150µl_Pb U [V] -0,9-0,8-0,7-0,6-0,5-0,4-0,3-0,2-0,1 0 0 Obr. 35 Příklad odezvy elektrody MW1 při stanovení Pb získané pomocí DPV J [na.mm -2 ] MW1 MW4 MW6 MW8 DW1 MW3 MW5 MW7 BQ ,02 0,04 0,06 0,08 0,1 0,12 0,14 0,16 0,18 0,2 koncentrace [µmol.l -1 ] Obr. 36 Kalibrační křivky WE měřené na iontech Pb
45 Experimentální část Na obr. 36 jsou výsledné kalibrační křivky měřených elektrod. Pro lepší porovnatelnost je proudová odezva elektrod přepočtena na proudovou hustotu. Nejlepších výsledků dosáhly elektrody označené MW1, MW6 a elektroda BQ, vyrobena z komerční TLV pasty. Dle tab. 2 můžeme vidět, že elektrody MW1 a MW6 mají podobné složení (liší se poměry jednotlivých složek). CNTs pro výrobu elektrody MW6 jsou navíc pro možné zvýšení odezvy funkcionalizovány ferrocenem. 5.5 Měření iontů kadmia Měření iontů kadmia bylo analogické s měřením iontů olova popsané v kap Standardem pro měření byl 10 mmol.l -1 CdCl 2 v acetátovém pufru (PH 5,4). Změřené kalibrační křivky v závislosti na koncentraci iontů kadmia jsou zobrazeny na obr. 37. Výsledný souhrn kalibračních křivek je na obr. 38. V porovnání s kalibračními křivkami měřenými na iontech olova je u kadmia několikanásobně menší odezva u všech elektrod. Nejlepších výsledků je opět dosaženo s elektrodami MW1, MW6 a BQ. Změřený půlvlnový potenciál kadmia E 1/2 = -0,818 V. U elektrod MW6 bylo díky funkcionalizaci ferrocenem předpokládáno zvýšení proudové odezvy v porovnání s elektrodami MW1. Tento předpoklad nebyl naplněn buď z důvodu použitého pojiva nebo nebyla modifikace ferrocenem úspěšná. pufr 5µl_Cd 10µl_Cd 20µl_Cd 30µl_Cd 40µl_Cd 50µl_Cd 60µl_Cd 70µl_Cd 80µl_Cd 90µl_Cd 100µl_Cd 110µl_Cd 120µl_Cd 130µl_Cd 140µl_Cd 150µl_Cd 9 I [ua] U [V] -0,9-0,8-0,7-0,6-0,5-0,4-0,3-0,2-0,1 0 0 Obr. 37 Příklad odezvy elektrody MW1 na přídavky Cd získané pomocí DPV
46 Experimentální část J [na.mm -2 ] MW1 MW3 MW4 MW5 MW6 BQ ,02 0,04 0,06 0,08 0,1 0,12 0,14 0,16 0,18 0,2 koncentrace [µmol.l -1 ] Obr. 38 Kalibrační křivky WE získané při stanovení kadmia v roztoku 5.6 Detekční limity Pro vyhodnocení detekčního limitu byla zvolena elektroda MW1, se kterou bylo dosaženo největší citlivosti (18,13 µa při koncentraci olova 199,64 µmol.l -1 a 6,69 µa při koncentraci kadmia 199,64 µmol.l -1 ). Při měření olova je rozlišovací schopnost již při přídavku 5 µl (obr. 39). To odpovídá koncentraci olova v roztoku 10 µmol.l -1. Při měření kadmia je možné vrchol rozlišit až při druhém přídavku, to znamená celkový objem přídavku je 10 µl roztoku kadmia o koncentraci 10 mmol.l -1. Celková koncentrace iontů kadmia v 5 ml acetátového pufru je 20 µmol.l
47 Experimentální část pufr 10µl_Pb 5µl_Pb 20µl_Pb 1,4 I [ua] 1,2 1 0,8 0,6 0,4 0,2-1 U [V] -0,9-0,8-0,7-0,6-0,5-0,4-0,3-0,2-0,1 0 Obr. 39 Měření detekčního limitu olova elektrody MW1 0 pufr 10µl_Cd 5µl_Cd 20µl_Cd 0,8 I [ua] 0,7 0,6 0,5 0,4 0,3 0,2 0,1-1 U [V] -0,9-0,8-0,7-0,6-0,5-0,4-0,3-0,2-0,1 0 0 Obr. 40 Měření detekčního limitu kadmia elektrody MW1-45 -
48 Experimentální část 5.7 Leptání elektrod Další experiment byl proveden na základě úvahy, že při výrobě elektrod s uhlíkovými nanotrubicemi, dochází k usazení nanotrubic blíže k substrátu a vytlačení pojivové složky tlustovrstvé pasty k aktivnímu povrchu. To částečně vyplývá z plnění pasty, které je vzhledem k charakteru nanotrubic ve velkém váhovém nepoměru (viz tab. 2). Analyzovaná látka proto nemá možnost přímé interakce s nanotrubicemi. Pro eliminaci tohoto efektu byla zvolena metoda, kdy byla elektroda leptána po definovanou dobu v kyselině, která rozpustila a odplavila vrchní část zakryté elektrody. Vzhledem k tomu, že jsou CNTs velice odolné vůči chemikáliím (kap. 3), není předpoklad, že by vlivem působení kyseliny došlo k poškození nanotrubic. Pro leptání byla zvolena 65% kyselina dusičná, která byla promíchávána a zahřívána na 40 C (obr. 41). Doba leptání byla zvolena 60 s. Obr. 41 Leptací lázeň kyseliny dusičné K měření bylo použito stejné techniky se shodným nastavením, jako u předchozího měření popsaného v kap. 5.4 a 5.5. Měření proběhlo na jedné koncentraci, kdy byl do 5 ml acetátového pufru napipetován přídavek 70 µl roztoku 10 mmol.l -1 (CH 3 COO) 2 Pb a 70 µl 10 mmol.l -1 CdCl 2. Vliv leptání elektrody MW1 na její proudovou odezvu je uveden na obr. 42. Z uvedeného výsledku vyplývá, že je proudová odezva leptané elektrody několikrát větší, než při měření elektrodou, která není takto upravena. Tab. 4 názorně ukazuje hodnotu
U = E a - E k + IR Znamená to, že vložené napětí je vyrovnáváno
 Voltametrie a polarografie Princip. Do roztoku vzorku (elektrolytu) jsou ponořeny dvě elektrody (na rozdíl od potenciometrie prochází obvodem el. proud) - je vytvořen elektrochemický článek. Na elektrody
Voltametrie a polarografie Princip. Do roztoku vzorku (elektrolytu) jsou ponořeny dvě elektrody (na rozdíl od potenciometrie prochází obvodem el. proud) - je vytvořen elektrochemický článek. Na elektrody
Příloha 1. Náleţitosti a uspořádání textové části VŠKP
 Příloha 1 Náleţitosti a uspořádání textové části VŠKP Náležitosti a uspořádání textové části VŠKP je určeno v tomto pořadí: a) titulní list b) zadání VŠKP c) abstrakt v českém a anglickém jazyce, klíčová
Příloha 1 Náleţitosti a uspořádání textové části VŠKP Náležitosti a uspořádání textové části VŠKP je určeno v tomto pořadí: a) titulní list b) zadání VŠKP c) abstrakt v českém a anglickém jazyce, klíčová
TLUSTOVRSTVÉ SENZORY PRO DETEKCI TĚŽKÝCH KOVŮ
 VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ BRNO UNIVERSITY OF TECHNOLOGY FAKULTA ELEKTROTECHNIKY A KOMUNIKAČNÍCH TECHNOLOGIÍ ÚSTAV MIKROELEKTRONIKY FACULTY OF ELECTRICAL ENGINEERING AND COMMUNICATION DEPARTMENT OF
VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ BRNO UNIVERSITY OF TECHNOLOGY FAKULTA ELEKTROTECHNIKY A KOMUNIKAČNÍCH TECHNOLOGIÍ ÚSTAV MIKROELEKTRONIKY FACULTY OF ELECTRICAL ENGINEERING AND COMMUNICATION DEPARTMENT OF
VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ BRNO UNIVERSITY OF TECHNOLOGY NÁVRH STRATEGIE ROZVOJE MALÉ RODINNÉ FIRMY THE DEVELOPMENT OF SMALL FAMILY OWNED COMPANY
 VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ BRNO UNIVERSITY OF TECHNOLOGY FAKULTA PODNIKATELSKÁ ÚSTAV FACULTY OF BUSINESS AND MANAGEMENT INSTITUT OF NÁVRH STRATEGIE ROZVOJE MALÉ RODINNÉ FIRMY THE DEVELOPMENT OF SMALL
VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ BRNO UNIVERSITY OF TECHNOLOGY FAKULTA PODNIKATELSKÁ ÚSTAV FACULTY OF BUSINESS AND MANAGEMENT INSTITUT OF NÁVRH STRATEGIE ROZVOJE MALÉ RODINNÉ FIRMY THE DEVELOPMENT OF SMALL
Galvanický článek. Li Rb K Na Be Sr Ca Mg Al Be Mn Zn Cr Fe Cd Co Ni Sn Pb H Sb Bi As CU Hg Ag Pt Au
 Řada elektrochemických potenciálů (Beketova řada) v níž je napětí mezi dvojicí kovů tím větší, čím větší je jejich vzdálenost v této řadě. Prvek více vlevo vytěsní z roztoku kov nacházející se vpravo od
Řada elektrochemických potenciálů (Beketova řada) v níž je napětí mezi dvojicí kovů tím větší, čím větší je jejich vzdálenost v této řadě. Prvek více vlevo vytěsní z roztoku kov nacházející se vpravo od
Uhlíkové struktury vázající ionty těžkých kovů
 Uhlíkové struktury vázající ionty těžkých kovů 7. června/june 2013 9:30 h 17:30 h Laboratoř metalomiky a nanotechnologií, Mendelova univerzita v Brně a Středoevropský technologický institut Budova D, Zemědělská
Uhlíkové struktury vázající ionty těžkých kovů 7. června/june 2013 9:30 h 17:30 h Laboratoř metalomiky a nanotechnologií, Mendelova univerzita v Brně a Středoevropský technologický institut Budova D, Zemědělská
3. NEROVNOVÁŽNÉ ELEKTRODOVÉ DĚJE
 3. NEROVNOVÁŽNÉ ELEKTRODOVÉ DĚJE (Elektrochemické články kinetické aspekty) Nerovnovážné elektrodové děje = děje probíhající na elektrodách při průchodu proudu. 3.1. Polarizace Pojem polarizace se používá
3. NEROVNOVÁŽNÉ ELEKTRODOVÉ DĚJE (Elektrochemické články kinetické aspekty) Nerovnovážné elektrodové děje = děje probíhající na elektrodách při průchodu proudu. 3.1. Polarizace Pojem polarizace se používá
OPTIMALIZACE ELEKTRODOVÉHO SYSTÉMU TLUSTOVRSTVÉHO ELEKTROCHEMICKÉHO SENZORU
 VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ BRNO UNIVERSITY OF TECHNOLOGY FAKULTA ELEKTROTECHNIKY A KOMUNIKAČNÍCH TECHNOLOGIÍ ÚSTAV MIKROELEKTRONIKY FACULTY OF ELECTRICAL ENGINEERING AND COMMUNICATION DEPARTMENT OF
VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ BRNO UNIVERSITY OF TECHNOLOGY FAKULTA ELEKTROTECHNIKY A KOMUNIKAČNÍCH TECHNOLOGIÍ ÚSTAV MIKROELEKTRONIKY FACULTY OF ELECTRICAL ENGINEERING AND COMMUNICATION DEPARTMENT OF
12. Elektrochemie základní pojmy
 Důležité veličiny Elektroda, článek Potenciometrie Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti Důležité veličiny proud I (ampér - A) náboj Q (coulomb - C) Q t 0 I dt napětí, potenciál
Důležité veličiny Elektroda, článek Potenciometrie Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti Důležité veličiny proud I (ampér - A) náboj Q (coulomb - C) Q t 0 I dt napětí, potenciál
OPTIMALIZACE METODY ANODICKÉ ROZPOUŠTĚCÍ VOLTAMETRIE PRO ANALÝZU BIOLOGICKÝCH VZORKŮ S OBSAHEM RTUTI
 Středoškolská technika 212 Setkání a prezentace prací středoškolských studentů na ČVUT OPTIMALIZACE METODY ANODICKÉ ROZPOUŠTĚCÍ VOLTAMETRIE PRO ANALÝZU BIOLOGICKÝCH VZORKŮ S OBSAHEM RTUTI Eliška Marková
Středoškolská technika 212 Setkání a prezentace prací středoškolských studentů na ČVUT OPTIMALIZACE METODY ANODICKÉ ROZPOUŠTĚCÍ VOLTAMETRIE PRO ANALÝZU BIOLOGICKÝCH VZORKŮ S OBSAHEM RTUTI Eliška Marková
Na www.studijni-svet.cz zaslal(a): Téra2507. Elektrochemické metody
 Na www.studijni-svet.cz zaslal(a): Téra2507 Elektrochemické metody Elektrolýza Do roztoku elektrolytu ponoříme dvě elektrody a vložíme na ně dostatečně velké vnější stejnosměrné napětí. Roztok elektrolytu
Na www.studijni-svet.cz zaslal(a): Téra2507 Elektrochemické metody Elektrolýza Do roztoku elektrolytu ponoříme dvě elektrody a vložíme na ně dostatečně velké vnější stejnosměrné napětí. Roztok elektrolytu
Název: Stanovení železa ve vzorcích krve pomocí diferenční pulzní voltametrie
 Název: Stanovení železa ve vzorcích krve pomocí diferenční pulzní voltametrie Školitel: MVDr. Ludmila Krejčová Datum: 24.2. 2012 Reg.č.projektu: CZ.1.07/2.3.00/20.0148 Název projektu: Mezinárodní spolupráce
Název: Stanovení železa ve vzorcích krve pomocí diferenční pulzní voltametrie Školitel: MVDr. Ludmila Krejčová Datum: 24.2. 2012 Reg.č.projektu: CZ.1.07/2.3.00/20.0148 Název projektu: Mezinárodní spolupráce
Bakalářská práce bakalářský studijní obor Teleinformatika
 VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ Fakulta elektrotechniky a komunikačních technologií Ústav telekomunikací Bakalářská práce bakalářský studijní obor Teleinformatika Student: Bílek Petr ID: 78462 Ročník: 3
VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ Fakulta elektrotechniky a komunikačních technologií Ústav telekomunikací Bakalářská práce bakalářský studijní obor Teleinformatika Student: Bílek Petr ID: 78462 Ročník: 3
Elektrody pro snímání biologických potenciálů. X31ZLE Základy lékařské elektroniky Jan Havlík Katedra teorie obvodů
 Elektrody pro snímání biologických potenciálů X31ZLE Základy lékařské elektroniky Jan Havlík Katedra teorie obvodů xhavlikj@fel.cvut.cz Spojení elektroda elektrolyt organismus vodič 2. třídy (ionty) přívodní
Elektrody pro snímání biologických potenciálů X31ZLE Základy lékařské elektroniky Jan Havlík Katedra teorie obvodů xhavlikj@fel.cvut.cz Spojení elektroda elektrolyt organismus vodič 2. třídy (ionty) přívodní
Laboratorní práce č. 8: Elektrochemické metody stanovení korozní rychlosti
 Laboratorní práce č. 8: Elektrochemické metody stanovení korozní rychlosti Cíl práce: Cílem laboratorní úlohy Elektrochemické metody stanovení korozní rychlosti je stanovení korozní rychlosti oceli v prostředí
Laboratorní práce č. 8: Elektrochemické metody stanovení korozní rychlosti Cíl práce: Cílem laboratorní úlohy Elektrochemické metody stanovení korozní rychlosti je stanovení korozní rychlosti oceli v prostředí
Elektrochemické metody
 Elektrochemické metody Konduktometrie Coulometrie Potenciometrie, Iontově selektivní elektrody (ISE) Voltametrie (Ampérometrie, Polarografie) Biosenzory Petr Breinek Elektrochemie_N2012 Elektrochemie Elektrochemie
Elektrochemické metody Konduktometrie Coulometrie Potenciometrie, Iontově selektivní elektrody (ISE) Voltametrie (Ampérometrie, Polarografie) Biosenzory Petr Breinek Elektrochemie_N2012 Elektrochemie Elektrochemie
Úvod do koroze. (kapitola, která bude společná všem korozním laboratorním pracím a kterou studenti musí znát bez ohledu na to, jakou práci dělají)
 Úvod do koroze (kapitola, která bude společná všem korozním laboratorním pracím a kterou studenti musí znát bez ohledu na to, jakou práci dělají) Koroze je proces degradace kovu nebo slitiny kovů působením
Úvod do koroze (kapitola, která bude společná všem korozním laboratorním pracím a kterou studenti musí znát bez ohledu na to, jakou práci dělají) Koroze je proces degradace kovu nebo slitiny kovů působením
Vysoké učení technické v brně Fakulta elektrotechniky a komunikačních technologií Ústav mikroelektroniky
 Vysoké učení technické v brně Fakulta elektrotechniky a komunikačních technologií Ústav mikroelektroniky Ing. Jan Prášek TLUSTOVRSTVÉ SENZORY PRO DETEKCI TĚŽKÝCH KOVŮ THICK-FILM SENSORS FOR HEAVY METALS
Vysoké učení technické v brně Fakulta elektrotechniky a komunikačních technologií Ústav mikroelektroniky Ing. Jan Prášek TLUSTOVRSTVÉ SENZORY PRO DETEKCI TĚŽKÝCH KOVŮ THICK-FILM SENSORS FOR HEAVY METALS
Elektrochemický potenciál Standardní vodíková elektroda Oxidačně-redukční potenciály
 Elektrochemický potenciál Standardní vodíková elektroda Oxidačně-redukční potenciály Elektrochemie rovnováhy a děje v soustavách nesoucích elektrický náboj Krystal kovu ponořený do destilované vody + +
Elektrochemický potenciál Standardní vodíková elektroda Oxidačně-redukční potenciály Elektrochemie rovnováhy a děje v soustavách nesoucích elektrický náboj Krystal kovu ponořený do destilované vody + +
Oxidace a redukce. Hoření = slučování s kyslíkem = oxidace. 2 Mg + O 2 2 MgO S + O 2 SO 2. Redukce = odebrání kyslíku
 Oxidace a redukce Hoření = slučování s kyslíkem = oxidace 2 Mg + O 2 2 MgO S + O 2 SO 2 Redukce = odebrání kyslíku Fe 2 O 3 + 3 C 2 Fe + 3 CO CuO + H 2 Cu + H 2 O 1 Oxidace a redukce Širší pojem oxidace
Oxidace a redukce Hoření = slučování s kyslíkem = oxidace 2 Mg + O 2 2 MgO S + O 2 SO 2 Redukce = odebrání kyslíku Fe 2 O 3 + 3 C 2 Fe + 3 CO CuO + H 2 Cu + H 2 O 1 Oxidace a redukce Širší pojem oxidace
VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ
 VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ BRNO UNIVERSITY OF TECHNOLOGY FAKULTA ELEKTROTECHNIKY A KOMUNIKAČNÍCH TECHNOLOGIÍ ÚSTAV MIKROELEKTRONIKY FACULTY OF ELECTRICAL ENGINEERING AND COMMUNICATION DEPARTMENT OF
VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ BRNO UNIVERSITY OF TECHNOLOGY FAKULTA ELEKTROTECHNIKY A KOMUNIKAČNÍCH TECHNOLOGIÍ ÚSTAV MIKROELEKTRONIKY FACULTY OF ELECTRICAL ENGINEERING AND COMMUNICATION DEPARTMENT OF
Oxidace a redukce. Objev kyslíku nový prvek, vyvrácení flogistonové teorie. Hoření = slučování s kyslíkem = oxidace. 2 Mg + O 2 2 MgO S + O 2 SO 2
 Oxidace a redukce Objev kyslíku nový prvek, vyvrácení flogistonové teorie Hoření = slučování s kyslíkem = oxidace 2 Mg + O 2 2 MgO S + O 2 SO 2 Lavoisier Redukce = odebrání kyslíku Fe 2 O 3 + 3 C 2 Fe
Oxidace a redukce Objev kyslíku nový prvek, vyvrácení flogistonové teorie Hoření = slučování s kyslíkem = oxidace 2 Mg + O 2 2 MgO S + O 2 SO 2 Lavoisier Redukce = odebrání kyslíku Fe 2 O 3 + 3 C 2 Fe
Voltametrie (laboratorní úloha)
 Voltametrie (laboratorní úloha) Teorie: Voltametrie (přesněji volt-ampérometrie) je nejčastěji používaná elektrochemická metoda, kdy se na pracovní elektrodu (rtuť, platina, zlato, uhlík, amalgamy,...)
Voltametrie (laboratorní úloha) Teorie: Voltametrie (přesněji volt-ampérometrie) je nejčastěji používaná elektrochemická metoda, kdy se na pracovní elektrodu (rtuť, platina, zlato, uhlík, amalgamy,...)
Elektrolýza. (procesy v elektrolytických článcích) ch) Základní pojmy a představy z elektrolýzy. V rovnováze E = 0 (I = 0)
 Elektrolýza (procesy v elektrolytických článcích) ch) V rovnováze Základní pojmy a představy z elektrolýzy E = (I = ) Ag Ag + ϕ Ag Ag E RT F r = E + + ln aag + Ag / Ag roztok AgNO 3 Po připojení zdroje
Elektrolýza (procesy v elektrolytických článcích) ch) V rovnováze Základní pojmy a představy z elektrolýzy E = (I = ) Ag Ag + ϕ Ag Ag E RT F r = E + + ln aag + Ag / Ag roztok AgNO 3 Po připojení zdroje
TLUSTOVRSTVÉ SENZORY PRO DETEKCI TĚŢKÝCH KOVŮ
 VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ BRNO UNIVERSITY OF TECHNOLOGY FAKULTA ELEKTROTECHNIKY A KOMUNIKAČNÍCH TECHNOLOGIÍ ÚSTAV MIKROELEKTRONIKY FACULTY OF ELECTRICAL ENGINEERING AND COMMUNICATION DEPARTMENT OF
VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ BRNO UNIVERSITY OF TECHNOLOGY FAKULTA ELEKTROTECHNIKY A KOMUNIKAČNÍCH TECHNOLOGIÍ ÚSTAV MIKROELEKTRONIKY FACULTY OF ELECTRICAL ENGINEERING AND COMMUNICATION DEPARTMENT OF
Automatická potenciometrická titrace Klinická a toxikologická analýza Chemie životního prostředí Geologické obory
 Automatická potenciometrická titrace Klinická a toxikologická analýza Chemie životního prostředí Geologické obory Titrace je spolehlivý a celkem nenáročný postup, jak zjistit koncentraci analytu, její
Automatická potenciometrická titrace Klinická a toxikologická analýza Chemie životního prostředí Geologické obory Titrace je spolehlivý a celkem nenáročný postup, jak zjistit koncentraci analytu, její
VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ BRNO UNIVERSITY OF TECHNOLOGY
 VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ BRNO UNIVERSITY OF TECHNOLOGY FAKULTA ELEKTROTECHNIKY A KOMUNIKAČNÍCH TECHNOLOGIÍ ÚSTAV MIKROELEKTRONIKY FACULTY OF ELECTRICAL ENGINEERING AND COMMUNICATION DEPARTMENT OF
VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ BRNO UNIVERSITY OF TECHNOLOGY FAKULTA ELEKTROTECHNIKY A KOMUNIKAČNÍCH TECHNOLOGIÍ ÚSTAV MIKROELEKTRONIKY FACULTY OF ELECTRICAL ENGINEERING AND COMMUNICATION DEPARTMENT OF
Elektrody pro snímání biologických potenciálů. A6M31LET Lékařská technika Jan Havlík Katedra teorie obvodů
 Elektrody pro snímání biologických potenciálů A6M31LET Lékařská technika Jan Havlík Katedra teorie obvodů xhavlikj@fel.cvut.cz Elektroda rozhraní dvou světů elektroda je součástí rozhraní dvou světů světa
Elektrody pro snímání biologických potenciálů A6M31LET Lékařská technika Jan Havlík Katedra teorie obvodů xhavlikj@fel.cvut.cz Elektroda rozhraní dvou světů elektroda je součástí rozhraní dvou světů světa
Inovace profesní přípravy budoucích učitelů chemie
 Inovace profesní přípravy budoucích učitelů chemie I n v e s t i c e d o r o z v o j e v z d ě l á v á n í CZ.1.07/2.2.00/15.0324 Tento projekt je spolufinancován Evropským sociálním fondem a státním rozpočtem
Inovace profesní přípravy budoucích učitelů chemie I n v e s t i c e d o r o z v o j e v z d ě l á v á n í CZ.1.07/2.2.00/15.0324 Tento projekt je spolufinancován Evropským sociálním fondem a státním rozpočtem
GALAVANICKÝ ČLÁNEK. V běžné životě používáme název baterie. Odborné pojmenování pro baterii je galvanický článek.
 GALAVANICKÝ ČLÁNEK V běžné životě používáme název baterie. Odborné pojmenování pro baterii je galvanický článek. Galvanický článek je zařízení, které využívá redoxní reakce jako zdroj energie. Je zdrojem
GALAVANICKÝ ČLÁNEK V běžné životě používáme název baterie. Odborné pojmenování pro baterii je galvanický článek. Galvanický článek je zařízení, které využívá redoxní reakce jako zdroj energie. Je zdrojem
Konduktometrie. Potenciometrie, Iontově selektivní elektrody (ISE) Voltametrie (Ampérometrie, Polarografie)
 Elektrochemické metody Konduktometrie Coulometrie Potenciometrie, Iontově selektivní elektrody (ISE) Voltametrie (Ampérometrie, Polarografie) Biosenzory Petr Breinek Elektrochemie-I 2012 Elektrochemie
Elektrochemické metody Konduktometrie Coulometrie Potenciometrie, Iontově selektivní elektrody (ISE) Voltametrie (Ampérometrie, Polarografie) Biosenzory Petr Breinek Elektrochemie-I 2012 Elektrochemie
Oxidace a redukce. Objev kyslíku nový prvek, vyvrácení flogistonové teorie. Hoření = slučování s kyslíkem = oxidace. 2 Mg + O 2 2 MgO S + O 2 SO 2
 Oxidace a redukce Objev kyslíku nový prvek, vyvrácení flogistonové teorie Hoření = slučování s kyslíkem = oxidace 2 Mg + O 2 2 MgO S + O 2 SO 2 Antoine Lavoisier (1743-1794) Redukce = odebrání kyslíku
Oxidace a redukce Objev kyslíku nový prvek, vyvrácení flogistonové teorie Hoření = slučování s kyslíkem = oxidace 2 Mg + O 2 2 MgO S + O 2 SO 2 Antoine Lavoisier (1743-1794) Redukce = odebrání kyslíku
GRAFEN VERSUS MWCNT; POROVNÁNÍ DVOU FOREM UHLÍKU V DETEKCI TĚŽKÉHO KOVU. Název: Školitel: Mgr. Dana Fialová. Datum: 15.3.2013
 Název: Školitel: GRAFEN VERSUS MWCNT; POROVNÁNÍ DVOU FOREM UHLÍKU V DETEKCI TĚŽKÉHO KOVU Mgr. Dana Fialová Datum: 15.3.2013 Reg.č.projektu: CZ.1.07/2.3.00/20.0148 Název projektu: Mezinárodní spolupráce
Název: Školitel: GRAFEN VERSUS MWCNT; POROVNÁNÍ DVOU FOREM UHLÍKU V DETEKCI TĚŽKÉHO KOVU Mgr. Dana Fialová Datum: 15.3.2013 Reg.č.projektu: CZ.1.07/2.3.00/20.0148 Název projektu: Mezinárodní spolupráce
Biosenzory Ondřej Wiewiorka
 Elektrochemické analytické metody Základy elektrochemie Potenciometrie Voltametrie a Polarografie Amperometrie Coulometrie Konduktometrie Biosenzory Ondřej Wiewiorka Co je to elektroanalýza? Elektrochemie
Elektrochemické analytické metody Základy elektrochemie Potenciometrie Voltametrie a Polarografie Amperometrie Coulometrie Konduktometrie Biosenzory Ondřej Wiewiorka Co je to elektroanalýza? Elektrochemie
Chemické metody přípravy tenkých vrstev
 Chemické metody přípravy tenkých vrstev verze 2013 Povrchové filmy monomolekulární Langmuirovy filmy PAL (povrchově aktivní látky) na polární kapalině (vodě), 0,205 nm 2 na 1 molekulu, tloušťka dána délkou
Chemické metody přípravy tenkých vrstev verze 2013 Povrchové filmy monomolekulární Langmuirovy filmy PAL (povrchově aktivní látky) na polární kapalině (vodě), 0,205 nm 2 na 1 molekulu, tloušťka dána délkou
Autokláv reaktor pro promíchávané vícefázové reakce
 Vysoká škola chemicko technologická v Praze Ústav organické technologie (111) Autokláv reaktor pro promíchávané vícefázové reakce Vypracoval : Bc. Tomáš Sommer Předmět: Vícefázové reaktory (prof. Ing.
Vysoká škola chemicko technologická v Praze Ústav organické technologie (111) Autokláv reaktor pro promíchávané vícefázové reakce Vypracoval : Bc. Tomáš Sommer Předmět: Vícefázové reaktory (prof. Ing.
STEJNOSMĚRNÝ PROUD Galvanické články TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY.
 STEJNOSMĚRNÝ PROUD Galvanické články TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY. Galvanické články Většina kovů ponořených do vody nebo elektrolytu
STEJNOSMĚRNÝ PROUD Galvanické články TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY. Galvanické články Většina kovů ponořených do vody nebo elektrolytu
Modifikace uhlíkové pastové elektrody pro stanovení stříbrných iontů
 Název: Školitel: Modifikace uhlíkové pastové elektrody pro stanovení stříbrných iontů Mgr. Dana Dospivová Datum: 24.2.212 Reg.č.projektu: CZ.1.7/2.3./2.148 Název projektu: Mezinárodní spolupráce v oblasti
Název: Školitel: Modifikace uhlíkové pastové elektrody pro stanovení stříbrných iontů Mgr. Dana Dospivová Datum: 24.2.212 Reg.č.projektu: CZ.1.7/2.3./2.148 Název projektu: Mezinárodní spolupráce v oblasti
OPTIMALIZACE ELEKTRODOVÉHO SYSTÉMU TLUSTOVRSTVÉHO ELEKTROCHENICKÉHO SENZORU
 VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ BRNO UNIVERSITY OF TECHNOLOGY FAKULTA ELEKTROTECHNIKY A KOMUNIKAČNÍCH TECHNOLOGIÍ ÚSTAV MIKROELEKTRONIKY FACULTY OF ELECTRICAL ENGINEERING AND COMMUNICATION DEPARTMENT OF
VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ BRNO UNIVERSITY OF TECHNOLOGY FAKULTA ELEKTROTECHNIKY A KOMUNIKAČNÍCH TECHNOLOGIÍ ÚSTAV MIKROELEKTRONIKY FACULTY OF ELECTRICAL ENGINEERING AND COMMUNICATION DEPARTMENT OF
Principy chemických snímačů
 Principy chemických snímačů Název školy: SPŠ Ústí nad Labem, středisko Resslova Autor: Ing. Pavel Votrubec Název: VY_32_INOVACE_05_AUT_99_principy_chemickych_snimacu.pptx Téma: Principy chemických snímačů
Principy chemických snímačů Název školy: SPŠ Ústí nad Labem, středisko Resslova Autor: Ing. Pavel Votrubec Název: VY_32_INOVACE_05_AUT_99_principy_chemickych_snimacu.pptx Téma: Principy chemických snímačů
UNIVERZITA KARLOVA V PRAZE Přírodovědecká fakulta. Katedra analytické chemie Andrea Hájková, Vlastimil Vyskočil, Jiří Barek
 UNIVERZITA KARLOVA V PRAZE Přírodovědecká fakulta Katedra analytické chemie Andrea Hájková, Vlastimil Vyskočil, Jiří Barek Výrobní dokumentace a Technický popis funkčního vzorku kombinovaného miniaturizovaného
UNIVERZITA KARLOVA V PRAZE Přírodovědecká fakulta Katedra analytické chemie Andrea Hájková, Vlastimil Vyskočil, Jiří Barek Výrobní dokumentace a Technický popis funkčního vzorku kombinovaného miniaturizovaného
VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ BRNO UNIVERSITY OF TECHNOLOGY OPTIMALIZACE ELEKTROD TLUSTOVRSTVÝCH SENZORŮ ELECTRODES OPTIMIZATION OF THICK-FILM SENSORS
 VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ BRNO UNIVERSITY OF TECHNOLOGY FAKULTA ELEKTROTECHNIKY A KOMUNIKAČNÍCH TECHNOLOGIÍ ÚSTAV MIKROELEKTRONIKY FACULTY OF ELECTRICAL ENGINEERING AND COMMUNICATION DEPARTMENT OF
VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ BRNO UNIVERSITY OF TECHNOLOGY FAKULTA ELEKTROTECHNIKY A KOMUNIKAČNÍCH TECHNOLOGIÍ ÚSTAV MIKROELEKTRONIKY FACULTY OF ELECTRICAL ENGINEERING AND COMMUNICATION DEPARTMENT OF
Průvodka. CZ.1.07/1.5.00/34.0802 Zkvalitnění výuky prostřednictvím ICT. III/2 Inovace a zkvalitnění výuky prostřednictvím ICT. Pořadí DUMu v sadě 07
 Průvodka Číslo projektu Název projektu Číslo a název šablony klíčové aktivity CZ.1.07/1.5.00/34.0802 Zkvalitnění výuky prostřednictvím ICT III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Příjemce
Průvodka Číslo projektu Název projektu Číslo a název šablony klíčové aktivity CZ.1.07/1.5.00/34.0802 Zkvalitnění výuky prostřednictvím ICT III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Příjemce
STŘÍKANÉ PRACOVNÍ ELEKTRODY ELEKTROCHEMICKÝCH SENZORŮ SPRAY-COATED WORKING ELECTRODES OF ELECTROCHEMICAL SENSORS
 VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ BRNO UNIVERSITY OF TECHNOLOGY FAKULTA ELEKTROTECHNIKY A KOMUNIKAČNÍCH TECHNOLOGIÍ ÚSTAV MIKROELEKTRONIKY FACULTY OF ELECTRICAL ENGINEERING AND COMMUNICATION DEPARTMENT OF
VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ BRNO UNIVERSITY OF TECHNOLOGY FAKULTA ELEKTROTECHNIKY A KOMUNIKAČNÍCH TECHNOLOGIÍ ÚSTAV MIKROELEKTRONIKY FACULTY OF ELECTRICAL ENGINEERING AND COMMUNICATION DEPARTMENT OF
ELEKTROLÝZA. Autor: Mgr. Stanislava Bubíková. Datum (období) tvorby: 13. 3. 2012. Ročník: osmý
 Autor: Mgr. Stanislava Bubíková ELEKTROLÝZA Datum (období) tvorby: 13. 3. 2012 Ročník: osmý Vzdělávací oblast: Člověk a příroda / Chemie / Chemické reakce 1 Anotace: Žáci se seznámí s elektrolýzou. V rámci
Autor: Mgr. Stanislava Bubíková ELEKTROLÝZA Datum (období) tvorby: 13. 3. 2012 Ročník: osmý Vzdělávací oblast: Člověk a příroda / Chemie / Chemické reakce 1 Anotace: Žáci se seznámí s elektrolýzou. V rámci
Elektrolytické vylučování mědi (galvanoplastika)
 Elektrolytické vylučování mědi (galvanoplastika) 1. Úvod Často se setkáváme s požadavkem na zhotovení kopie uměleckého nebo muzejního sbírkového předmětu. Jednou z možností je použití galvanoplastické
Elektrolytické vylučování mědi (galvanoplastika) 1. Úvod Často se setkáváme s požadavkem na zhotovení kopie uměleckého nebo muzejního sbírkového předmětu. Jednou z možností je použití galvanoplastické
instrumentální Většina instrumentálních metod vyžaduje kalibraci. Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti
 Kvantitativní analýza - instrumentální Většina instrumentálních metod vyžaduje kalibraci. Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti Důležité pojmy Metody kalibrace Metoda kalibrační
Kvantitativní analýza - instrumentální Většina instrumentálních metod vyžaduje kalibraci. Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti Důležité pojmy Metody kalibrace Metoda kalibrační
TECHNOLOGICKÉ PROCESY PŘI VÝROBĚ POLOVODIČOVÝCH PRVKŮ III.
 TECHNOLOGICKÉ PROCESY PŘI VÝROBĚ POLOVODIČOVÝCH PRVKŮ III. NANÁŠENÍ VRSTEV V mikroelektronice se nanáší tzv. tlusté a tenké vrstvy. a) Tlusté vrstvy: Používají se v hybridních integrovaných obvodech. Nanáší
TECHNOLOGICKÉ PROCESY PŘI VÝROBĚ POLOVODIČOVÝCH PRVKŮ III. NANÁŠENÍ VRSTEV V mikroelektronice se nanáší tzv. tlusté a tenké vrstvy. a) Tlusté vrstvy: Používají se v hybridních integrovaných obvodech. Nanáší
Katedra chemie FP TUL Chemické metody přípravy vrstev
 Chemické metody přípravy vrstev Metoda sol-gel Historie nejstarší příprava silikagelu 1939 patent na výrobu antireflexních vrstev na fotografické čočky 60. léta studium vrstev SiO 2 a TiO 2 70. léta výroba
Chemické metody přípravy vrstev Metoda sol-gel Historie nejstarší příprava silikagelu 1939 patent na výrobu antireflexních vrstev na fotografické čočky 60. léta studium vrstev SiO 2 a TiO 2 70. léta výroba
Stanovení korozní rychlosti elektrochemickými polarizačními metodami
 Stanovení korozní rychlosti elektrochemickými polarizačními metodami Úvod Měření polarizačního odporu Dílčí děje elektrochemického korozního procesu anodická oxidace kovu a katodická redukce složky prostředí
Stanovení korozní rychlosti elektrochemickými polarizačními metodami Úvod Měření polarizačního odporu Dílčí děje elektrochemického korozního procesu anodická oxidace kovu a katodická redukce složky prostředí
Metody kalibrace. Důležité pojmy. Metoda kalibrační křivky (external standards)
 Důležité pojmy Metody kalibrace Metoda kalibrační křivky (external standards) připravíme sérii kalibračních roztoků stanovovaného analytu, pokrývající zamýšlený koncentrační rozsah snažíme se, aby bylo
Důležité pojmy Metody kalibrace Metoda kalibrační křivky (external standards) připravíme sérii kalibračních roztoků stanovovaného analytu, pokrývající zamýšlený koncentrační rozsah snažíme se, aby bylo
Datum: 21. 8. 2013 Projekt: Využití ICT techniky především v uměleckém vzdělávání Registrační číslo: CZ.1.07./1.5.00/34.
 Datum: 21. 8. 2013 Projekt: Využití ICT techniky především v uměleckém vzdělávání Registrační číslo: CZ.1.07./1.5.00/34.1013 Číslo DUM: VY_32_INOVACE_93 Škola: Akademie VOŠ, Gymn. a SOŠUP Světlá nad Sázavou
Datum: 21. 8. 2013 Projekt: Využití ICT techniky především v uměleckém vzdělávání Registrační číslo: CZ.1.07./1.5.00/34.1013 Číslo DUM: VY_32_INOVACE_93 Škola: Akademie VOŠ, Gymn. a SOŠUP Světlá nad Sázavou
DOUTNAVÝ VÝBOJ. Další technologie využívající doutnavý výboj
 DOUTNAVÝ VÝBOJ Další technologie využívající doutnavý výboj Plazma doutnavého výboje je využíváno v technologiích depozice povlaků nebo modifikace povrchů. Jedná se zejména o : - depozici povlaků magnetronovým
DOUTNAVÝ VÝBOJ Další technologie využívající doutnavý výboj Plazma doutnavého výboje je využíváno v technologiích depozice povlaků nebo modifikace povrchů. Jedná se zejména o : - depozici povlaků magnetronovým
Metodický pokyn č. 1/09 pro odevzdávání, ukládání a zpřístupňování vysokoškolských závěrečných prací
 Metodický pokyn č. 1/09 pro odevzdávání, ukládání a zpřístupňování vysokoškolských závěrečných prací Článek I. Úvodní ustanovení (1) Pro účely této směrnice se vysokoškolskými závěrečnými pracemi rozumí
Metodický pokyn č. 1/09 pro odevzdávání, ukládání a zpřístupňování vysokoškolských závěrečných prací Článek I. Úvodní ustanovení (1) Pro účely této směrnice se vysokoškolskými závěrečnými pracemi rozumí
ELEKTRICKÝ PROUD V KAPALINÁCH
 ELEKTRICKÝ PROUD V KPLINÁCH 1. Elektrolyt a elektrolýza elektrolyt kapalina, která může vést elektrický proud (musí obsahovat ionty kyselin, zásad nebo solí - rozpuštěné nebo roztavené) elektrolýza proces,
ELEKTRICKÝ PROUD V KPLINÁCH 1. Elektrolyt a elektrolýza elektrolyt kapalina, která může vést elektrický proud (musí obsahovat ionty kyselin, zásad nebo solí - rozpuštěné nebo roztavené) elektrolýza proces,
BRNO UNIVERSITY OF TECHNOLOGY FAKULTA ELEKTROTECHNIKY A KOMUNIKAČNÍCH TECHNOLOGIÍ ÚSTAV MIKROELEKTRONIKY
 VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ BRNO UNIVERSITY OF TECHNOLOGY FAKULTA ELEKTROTECHNIKY A KOMUNIKAČNÍCH TECHNOLOGIÍ ÚSTAV MIKROELEKTRONIKY FACULTY OF ELECTRICAL ENGINEERING AND COMMUNICATION DEPARTMENT OF
VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ BRNO UNIVERSITY OF TECHNOLOGY FAKULTA ELEKTROTECHNIKY A KOMUNIKAČNÍCH TECHNOLOGIÍ ÚSTAV MIKROELEKTRONIKY FACULTY OF ELECTRICAL ENGINEERING AND COMMUNICATION DEPARTMENT OF
ELEKTROCHEMIE A KOROZE Ing. Jiří Vondrák, DrSc. ÚACH AV ČR
 ELEKTROCHEMIE A KOROZE Ing. Jiří Vondrák, DrSc. ÚACH AV ČR Elektrochemie: chemické reakce vyvolané elektrickým proudem a naopak vznik elektrického proudu z chemických reakcí Historie: L. Galvani - žabí
ELEKTROCHEMIE A KOROZE Ing. Jiří Vondrák, DrSc. ÚACH AV ČR Elektrochemie: chemické reakce vyvolané elektrickým proudem a naopak vznik elektrického proudu z chemických reakcí Historie: L. Galvani - žabí
VY_32_INOVACE_6/15_ČLOVĚK A PŘÍRODA. Předmět: Fyzika Ročník: 6. Poznámka: Vodiče a izolanty Vypracoval: Pták
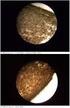 VY_32_INOVACE_6/15_ČLOVĚK A PŘÍRODA Předmět: Fyzika Ročník: 6. Poznámka: Vodiče a izolanty Vypracoval: Pták Izolant je látka, která nevede elektrický proud izolant neobsahuje volné částice s elektrický
VY_32_INOVACE_6/15_ČLOVĚK A PŘÍRODA Předmět: Fyzika Ročník: 6. Poznámka: Vodiče a izolanty Vypracoval: Pták Izolant je látka, která nevede elektrický proud izolant neobsahuje volné částice s elektrický
Allotropické modifikace uhlíku
 Allotropické modifikace uhlíku 1 Elektrody na bázi uhlíku Homogenní Spektrální uhlík (grafit) Skelný uhlík (glassy carbon) Pyrolytický grafit Uhlíková vlákna Fulereny (1985) Nanotrubičky (1991) Diamant
Allotropické modifikace uhlíku 1 Elektrody na bázi uhlíku Homogenní Spektrální uhlík (grafit) Skelný uhlík (glassy carbon) Pyrolytický grafit Uhlíková vlákna Fulereny (1985) Nanotrubičky (1991) Diamant
5.0 ZJIŠŤOVÁNÍ FÁZOVÝCH PŘEMĚN
 5.0 ZJIŠŤOVÁNÍ FÁZOVÝCH PŘEMĚN Metody zkoumání fázových přeměn v kovech a slitinách jsou založeny na využití změn převážně fyzikálních vlastností, které fázovou přeměnu a s ní spojenou změnu struktury
5.0 ZJIŠŤOVÁNÍ FÁZOVÝCH PŘEMĚN Metody zkoumání fázových přeměn v kovech a slitinách jsou založeny na využití změn převážně fyzikálních vlastností, které fázovou přeměnu a s ní spojenou změnu struktury
Návod pro laboratorní úlohu: Závislost citlivosti plynových vodivostních senzorů na teplotě
 Návod pro laboratorní úlohu: Závislost citlivosti plynových vodivostních senzorů na teplotě Náplní laboratorní úlohy je proměření základních parametrů plynových vodivostních senzorů: i) el. odpor a ii)
Návod pro laboratorní úlohu: Závislost citlivosti plynových vodivostních senzorů na teplotě Náplní laboratorní úlohy je proměření základních parametrů plynových vodivostních senzorů: i) el. odpor a ii)
= vědní disciplína zabývající se ději a rovnováhami v soustavách, ve kterých se vyskytují elektricky nabité částice
 Otázka: Elektrochemie Předmět: Chemie Přidal(a): j. Elektrochemie = vědní disciplína zabývající se ději a rovnováhami v soustavách, ve kterých se vyskytují elektricky nabité částice Př. soustav s el. nábojem
Otázka: Elektrochemie Předmět: Chemie Přidal(a): j. Elektrochemie = vědní disciplína zabývající se ději a rovnováhami v soustavách, ve kterých se vyskytují elektricky nabité částice Př. soustav s el. nábojem
Elektrochemie. 2. Elektrodový potenciál
 Elektrochemie 1. Poločlánky Ponoříme-li kov do roztoku jeho solí mohou nastav dva různé děje: a. Do roztoku se z kovu uvolňují kationty (obr. a), na elektrodě vzniká převaha elektronů. Elektroda se tedy
Elektrochemie 1. Poločlánky Ponoříme-li kov do roztoku jeho solí mohou nastav dva různé děje: a. Do roztoku se z kovu uvolňují kationty (obr. a), na elektrodě vzniká převaha elektronů. Elektroda se tedy
Přehled veličin elektrických obvodů
 Přehled veličin elektrických obvodů Ing. Martin Černík, Ph.D Projekt ESF CZ.1.7/2.2./28.5 Modernizace didaktických metod a inovace. Elektrický náboj - základní vlastnost některých elementárních částic
Přehled veličin elektrických obvodů Ing. Martin Černík, Ph.D Projekt ESF CZ.1.7/2.2./28.5 Modernizace didaktických metod a inovace. Elektrický náboj - základní vlastnost některých elementárních částic
Aplikace AAS ACH/APAS. David MILDE, Úvod
 Aplikace AAS ACH/APAS David MILDE, 2017 Úvod AAS: v podstatě 4atomizační techniky: plamenová atomizace (FA), elektrotermická atomizace (ETA), generování těkavých hydridů (HG), určené pro stanovení As,
Aplikace AAS ACH/APAS David MILDE, 2017 Úvod AAS: v podstatě 4atomizační techniky: plamenová atomizace (FA), elektrotermická atomizace (ETA), generování těkavých hydridů (HG), určené pro stanovení As,
2.4 Stavové chování směsí plynů Ideální směs Ideální směs reálných plynů Stavové rovnice pro plynné směsi
 1. ZÁKLADNÍ POJMY 1.1 Systém a okolí 1.2 Vlastnosti systému 1.3 Vybrané základní veličiny 1.3.1 Množství 1.3.2 Délka 1.3.2 Délka 1.4 Vybrané odvozené veličiny 1.4.1 Objem 1.4.2 Hustota 1.4.3 Tlak 1.4.4
1. ZÁKLADNÍ POJMY 1.1 Systém a okolí 1.2 Vlastnosti systému 1.3 Vybrané základní veličiny 1.3.1 Množství 1.3.2 Délka 1.3.2 Délka 1.4 Vybrané odvozené veličiny 1.4.1 Objem 1.4.2 Hustota 1.4.3 Tlak 1.4.4
VOLTAMPEROMETRIE. Stanovení rozpuštěného kyslíku
 VOLTAMPEROMETRIE Stanovení rozpuštěného kyslíku Inovace předmětu probíhá v rámci projektu CZ.1.07/2.2.00/28.0302 Inovace studijních programů AF a ZF MENDELU směřující k vytvoření mezioborové integrace.
VOLTAMPEROMETRIE Stanovení rozpuštěného kyslíku Inovace předmětu probíhá v rámci projektu CZ.1.07/2.2.00/28.0302 Inovace studijních programů AF a ZF MENDELU směřující k vytvoření mezioborové integrace.
VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ
 VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ BRNO UNIVERSITY OF TECHNOLOGY FAKULTA ELEKTROTECHNIKY A KOMUNIKAČNÍCH TECHNOLOGIÍ ÚSTAV MIKROELEKTRONIKY FACULTY OF ELECTRICAL ENGINEERING AND COMMUNICATION DEPARTMENT OF
VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ BRNO UNIVERSITY OF TECHNOLOGY FAKULTA ELEKTROTECHNIKY A KOMUNIKAČNÍCH TECHNOLOGIÍ ÚSTAV MIKROELEKTRONIKY FACULTY OF ELECTRICAL ENGINEERING AND COMMUNICATION DEPARTMENT OF
elektrické filtry Jiří Petržela filtry založené na jiných fyzikálních principech
 Jiří Petržela filtry založené na jiných fyzikálních principech piezoelektrický jev při mechanickém namáhání krystalu ve správném směru na něm vzniká elektrické napětí po přiložení elektrického napětí se
Jiří Petržela filtry založené na jiných fyzikálních principech piezoelektrický jev při mechanickém namáhání krystalu ve správném směru na něm vzniká elektrické napětí po přiložení elektrického napětí se
Elektrický proud v elektrolytech
 Elektrolytický vodič Elektrický proud v elektrolytech Vezěe nádobu s destilovanou vodou (ta nevede el. proud) a vlože do ní dvě elektrody, které připojíe do zdroje stejnosěrného napětí. Do vody nasypee
Elektrolytický vodič Elektrický proud v elektrolytech Vezěe nádobu s destilovanou vodou (ta nevede el. proud) a vlože do ní dvě elektrody, které připojíe do zdroje stejnosěrného napětí. Do vody nasypee
PRAKTIKUM III. Oddělení fyzikálních praktik při Kabinetu výuky obecné fyziky MFF UK. Pracoval: Jan Polášek stud. skup. 11 dne 23.4.2009.
 Oddělení fyzikálních praktik při Kabinetu výuky obecné fyziky MFF UK PRAKTIKUM III Úloha č. XXVI Název: Vláknová optika Pracoval: Jan Polášek stud. skup. 11 dne 23.4.2009 Odevzdal dne: Možný počet bodů
Oddělení fyzikálních praktik při Kabinetu výuky obecné fyziky MFF UK PRAKTIKUM III Úloha č. XXVI Název: Vláknová optika Pracoval: Jan Polášek stud. skup. 11 dne 23.4.2009 Odevzdal dne: Možný počet bodů
Mikro a nanotribologie materiály, výroba a pohon MEMS
 Tribologie Mikro a nanotribologie materiály, výroba a pohon MEMS vypracoval: Tomáš Píza Obsah - Co je to MEMS - Materiály pro MEMS - Výroba MEMS - Pohon MEMS Co to je MEMS - zkratka z anglických slov Micro-Electro-Mechanical-Systems
Tribologie Mikro a nanotribologie materiály, výroba a pohon MEMS vypracoval: Tomáš Píza Obsah - Co je to MEMS - Materiály pro MEMS - Výroba MEMS - Pohon MEMS Co to je MEMS - zkratka z anglických slov Micro-Electro-Mechanical-Systems
VEDENÍ ELEKTRICKÉHO PROUDU V LÁTKÁCH
 VEDENÍ ELEKTRICKÉHO PROUDU V LÁTKÁCH Jan Hruška TV-FYZ Ahoj, tak jsme tady znovu a pokusíme se Vám vysvětlit problematiku vedení elektrického proudu v látkách. Co je to vlastně elektrický proud? Na to
VEDENÍ ELEKTRICKÉHO PROUDU V LÁTKÁCH Jan Hruška TV-FYZ Ahoj, tak jsme tady znovu a pokusíme se Vám vysvětlit problematiku vedení elektrického proudu v látkách. Co je to vlastně elektrický proud? Na to
Elektroanalytické metody
 Elektroanalytické metody Elektroanalytické metody (EAM) zkoumají elektrochemické chování roztoku analytu v závislosti na jeho složení a koncentraci. Analyzovaný roztok je v kontaktu s elektrodami, které
Elektroanalytické metody Elektroanalytické metody (EAM) zkoumají elektrochemické chování roztoku analytu v závislosti na jeho složení a koncentraci. Analyzovaný roztok je v kontaktu s elektrodami, které
Elektrochemie. Zn, + + e. red. 1 Standardní vodíková elektroda je elektroda vytvořená z platiny, pokrytá platinovou černí, sycená plynným
 ÚSTAV LÉKAŘSKÉ BIOCHEMIE 1 LF UK Elektrochemie v biochemii Martin Vejražka Praha, 8 Elektrodové děje Ponoříme-li do roztoku kovového iontu (např Cu ) elektrodu ze stejného kovu (v daném případě mědi),
ÚSTAV LÉKAŘSKÉ BIOCHEMIE 1 LF UK Elektrochemie v biochemii Martin Vejražka Praha, 8 Elektrodové děje Ponoříme-li do roztoku kovového iontu (např Cu ) elektrodu ze stejného kovu (v daném případě mědi),
Návod pro laboratorní úlohu: Komerční senzory plynů a jejich testování
 Návod pro laboratorní úlohu: Komerční senzory plynů a jejich testování Úkol měření: 1) Proměřte závislost citlivosti senzoru TGS na koncentraci vodíku 2) Porovnejte vaši citlivostní charakteristiku s charakteristikou
Návod pro laboratorní úlohu: Komerční senzory plynů a jejich testování Úkol měření: 1) Proměřte závislost citlivosti senzoru TGS na koncentraci vodíku 2) Porovnejte vaši citlivostní charakteristiku s charakteristikou
Příprava grafénu. Petr Jelínek
 Příprava grafénu Petr Jelínek Schéma prezentace Úvod do tématu Provedené experimenty - příprava grafénu - charakterizace Plánovaná činnost - experimenty Závěr 2 Pohled do historie 1960 HOPG (Arthur Moore)
Příprava grafénu Petr Jelínek Schéma prezentace Úvod do tématu Provedené experimenty - příprava grafénu - charakterizace Plánovaná činnost - experimenty Závěr 2 Pohled do historie 1960 HOPG (Arthur Moore)
SNÍMAČE PRO MĚŘENÍ TEPLOTY
 SNÍMAČE PRO MĚŘENÍ TEPLOTY 10.1. Kontaktní snímače teploty 10.2. Bezkontaktní snímače teploty 10.1. KONTAKTNÍ SNÍMAČE TEPLOTY Experimentální metody přednáška 10 snímač je připevněn na měřený objekt 10.1.1.
SNÍMAČE PRO MĚŘENÍ TEPLOTY 10.1. Kontaktní snímače teploty 10.2. Bezkontaktní snímače teploty 10.1. KONTAKTNÍ SNÍMAČE TEPLOTY Experimentální metody přednáška 10 snímač je připevněn na měřený objekt 10.1.1.
Kurz 1 Úvod k biochemickému praktiku
 Kurz 1 Úvod k biochemickému praktiku Pavla Balínová http://vyuka.lf3.cuni.cz/ Důležité informace Kroužkový asistent: RNDr. Pavla Balínová e-mailová adresa: pavla.balinova@lf3.cuni.cz místnost: 410 studijní
Kurz 1 Úvod k biochemickému praktiku Pavla Balínová http://vyuka.lf3.cuni.cz/ Důležité informace Kroužkový asistent: RNDr. Pavla Balínová e-mailová adresa: pavla.balinova@lf3.cuni.cz místnost: 410 studijní
Universální přenosný potenciostat (nanopot)
 Universální přenosný potenciostat (nanopot) (funkční vzorek 2014) Autoři: Michal Pavlík, Jiří Háze, Lukáš Fujcik, Vilém Kledrowetz, Marek Bohrn, Marian Pristach, Vojtěch Dvořák Funkční vzorek universálního
Universální přenosný potenciostat (nanopot) (funkční vzorek 2014) Autoři: Michal Pavlík, Jiří Háze, Lukáš Fujcik, Vilém Kledrowetz, Marek Bohrn, Marian Pristach, Vojtěch Dvořák Funkční vzorek universálního
Funkční vzorek. Geofyzikální ústředna GU100 modulární ústředna pro záznam dat v autonomním i síťovém režimu
 Technická univerzita v Liberci Ústav pro nanomateriály, pokročilé technologie a inovace Evidenční list funkčního vzorku stupeň utajení: bez utajení Funkční vzorek Geofyzikální ústředna GU100 modulární
Technická univerzita v Liberci Ústav pro nanomateriály, pokročilé technologie a inovace Evidenční list funkčního vzorku stupeň utajení: bez utajení Funkční vzorek Geofyzikální ústředna GU100 modulární
Potenciometrie. Obr.1 Schema základního uspořádání elektrochemické cely pro potenciometrická měření
 Potenciometrie 1.Definice Rovnovážná potenciometrie je analytickou metodou, při níž se analyt stanovuje ze změřeného napětí elektrochemického článku, tvořeného indikační elektrodou ponořenou do analyzovaného
Potenciometrie 1.Definice Rovnovážná potenciometrie je analytickou metodou, při níž se analyt stanovuje ze změřeného napětí elektrochemického článku, tvořeného indikační elektrodou ponořenou do analyzovaného
Mikrosenzory a mikroelektromechanické systémy
 Mikrosenzory a mikroelektromechanické systémy Ing. Jaromír Hubálek, Ph.D. Ústav mikroelektroniky U7/104 Tel. 54114 6163 hubalek@feec.vutbr.cz http://www.umel.feec.vutbr.cz/~hubalek Obsah Úvod do senzorové
Mikrosenzory a mikroelektromechanické systémy Ing. Jaromír Hubálek, Ph.D. Ústav mikroelektroniky U7/104 Tel. 54114 6163 hubalek@feec.vutbr.cz http://www.umel.feec.vutbr.cz/~hubalek Obsah Úvod do senzorové
