Cytologický gynekologický screening a diagnostika. Vyšetření HPV
|
|
|
- Silvie Hájková
- před 9 lety
- Počet zobrazení:
Transkript
1 Příručka pro odběr primárních vzorků Klinická laboratoř společnosti GYNEKO spol. s r.o. Cytologický gynekologický screening a diagnostika Vyšetření okultního krvácení ve stolici (faecal occult blood, FOB) Vyšetření spermatu nativní spermiogram Vyšetření HPV POV - příručka pro odběr primárních vzorků - 5.doc Strana 1 (celkem 17)
2 Cytologický gynekologický screening a diagnostika a1) Název vyšetření... 2 a2) Vzor formuláře prohlášení o souhlasu pacienta... 2 a3) Pokyny pacientům k jejich osobní přípravě před odběrem vzorků... 2 a4) Informaci pro uživatele služeb laboratoře o účelu a vhodnosti nabízených služeb... 2 b1) Postup pro přípravu pacienta před odběrem vzorku... 2 b2) Způsob označování primárního vzorku... 3 b3) VLASTNÍ POSTUP pro odběr primárního vzorku... 3 b4) Kontraindikace odběru vzorku... 4 c1) Pokyny pro vyplnění žádanky... 4 c2) Pokyny pro druh a množství primárního vzorku... 4 c3) Instrukce pro načasování odběru... 4 c4) Pokyny pro zacházení se vzorkem mezi jeho odběrem a přijetím do laboratoře... 4 c5) Pokyny pro označování primárních vzorků... 4 c6) Klinické informace... 4 c7) Pozitivní identifikace pacienta... 4 c8) Autorizace osoby provádějící odběr primárního vzorku... 5 c9) Pokyny pro bezpečnou likvidaci materiálů použitých při odběru vzorku... 5 d1) Instrukce pro skladování po vyšetření vzorků v laboratoři... 5 d2) Informace o časovém rozpětí, kdy je možné požadovat dodatečné vyšetření... 5 d3) Informace o možných dodatečných vyšetřeních... 5 d4) Instrukce pro opakované nebo další vyšetření... 5 a1) Název vyšetření Cytologický gynekologický screening a diagnostika a2) Vzor formuláře prohlášení o souhlasu pacienta Prohlášení o souhlasu k odběru vzorku se u vyšetření nepoužívá. a3) Pokyny pacientům k jejich osobní přípravě před odběrem vzorků Návody předávané pacientovi nejsou použity. a4) Informaci pro uživatele služeb laboratoře o účelu a vhodnosti nabízených služeb Cytologický gynekologický screening je mikroskopické vyšetření případných buněčných změn na děložním čípku a tyto změny jsou diagnostikovány podle standardu Bethesda (Diane Salomon, Ritu Nayar: The Bethesda System for Reporting Cervical Cytology. Definitions, criteria and explanatory notes). Cílem vyšetření je sekundární prevence karcinomu děložního hrdla, její diagnostika. b1) Postup pro přípravu pacienta před odběrem vzorku Zvláštní osobní příprava pacienta před odběrem vzorku není nutná, resp. je plně v kompetenci ošetřujícího gynekologa. Vzorek by se neměl odebírat při menses a dále je nutné respektovat pokyny v b4) - Kontraindikace odběru vzorku. POV - příručka pro odběr primárních vzorků - 5.doc Strana 2 (celkem 17)
3 b2) Způsob označování primárního vzorku Vzorek pacienta musí být označen tak, aby byl jednoznačně identifikován a spojen se žádankou. Označení lze provést: 1) jménem a příjmením pacienta 2) rodným číslem pacienta a identifikační značkou (zkratkou) lékaře, který vyšetření požaduje (viz také kapitola c5) Pokyny pro označování primárních vzorků) 3) značkou lékaře a pořadovým číslem skla 4) pouze pořadovým číslem skla; v tomto případě se jedná o vzorky z ordinací Gyneko a číselné řady se nepřekrývají Vzhledem k tomu, že cytologická skla představují specifické nosiče vzorků, které nelze s žádným dalším vyšetřením v laboratoři zaměnit, není nutné označovat vzorek požadavkem na vyšetření. Tento požadavek se vypíše na přiložené žádance. b3) VLASTNÍ POSTUP pro odběr primárního vzorku 1) Zavést vaginální zrcadlo. 2) Aplikovat na 30 vteřin 3-5% kyselinu octovou. 3) Provést kolposkopii. V případě, že plánujeme použití Lugolova roztoku, musíme odebrat cytologii před kolposkopií. 4) Štětičkou nebo Ayre špachtlí provést stěr na sklo s matovaným okrajem, označeným číselným kódem ( kód i číselnou řadu přiděluje laboratoř ). Snažíme se postihnout maximální plochu transformační zóny. Sklo držíme v levé ruce a buňky z nástroje přeneseme na průhlednou část skla blíže k matované části. 5) Za pomocí cytobrushe provést krouživým pohybem stěr z endocervixu. Cytobrush otočíme o 180, zanořený pokud možno na hloubku pracovní části nástroje. Nástroje se snažit zavést v ose čípku, aby se co nejvíce předešlo krvácení. Poté opět rotačním pohybem o 180 přenést buňky na sklo. Rotace má být v opačném směru, než byla v čípku. Buňky z endocervixu přenést od matované části na vzdálenější průhlednou část stejného skla. 6) Ihned (do 20-ti vteřin) sklo fixovat v metanolu nebo etanolu 90% nebo isopropylalkoholu 70 % nebo postřikem vhodným fixačním sprejem ze vzdálenosti cm. Náplň kyvety vyměňovat po fixaci 2 x 10 preparátů. 7) Při použití kyvety s alkoholy, ponechat sklo v kyvetě minimálně 20 min. Poté sklo nechat uschnout na vhodné podložce. 8) Pečlivě vyplnit žádanku. Nevyplněné nebo nezatržené kolonky automaticky znamenají, že se jev nevyskytl!!! 9) Všechna odebraná skla vložit do transportní krabičky, správně označené. Ke krabičce přiložit vyplněné žádanky od skel, které jsou v krabičce obsaženy. 10) Krabičku předat předem dohodnutým a definovaným způsobem laboratoři. Pokyny pro odběr vzorku: vzorek by se měl odebírat: 1) minimálně 48 hod po vaginální medikaci, vaginálních kontraceptivech po vag. výplaších 2) alespoň 24 hodin po coitu 3) minimálně 6 týdnů od porodu 4) minimálně po 1 týdnu aplikace estrogenů při léčbě atrofie 5) minimálně 3 týdny od traumatu cervixu ( instrumentační výkony na čípku ) POV - příručka pro odběr primárních vzorků - 5.doc Strana 3 (celkem 17)
4 b4) Kontraindikace odběru vzorku V následujících vyjmenovaných případech se nedoporučuje cytologické vyšetření, nebo vyšetření až po případném přeléčení (nález další postup). 1) Rozpadající se nekrotický viditelný tumor biopsie 2) Výrazná atrofie týdenní přeléčení estrogeny 3) Polyp histologie 4) Těžká mukopurulentní cervicitis přeléčení 5) Puerperium cytologické vyšetření lze provést nejdříve 4 týdny po porodu, nejlépe však 6 týdnů po porodu c1) Pokyny pro vyplnění žádanky Formulář žádosti o vyšetření (žádanka) musí být jednoznačně vyplněn; nevyplněné položky jsou laboratoří interpretovány jako jev se nevyskytl. Zvláštní pozornost je třeba věnovat identifikaci klienta a identifikaci požadujícího lékaře. c2) Pokyny pro druh a množství primárního vzorku Provádí se stěr z endocervixu za pomocí špachtle a cytobrushe. Podrobný postup je uveden v kapitole b3) - Postup pro odběr primárního vzorku. Kritériem pro odmítnutí vzorku je: - vzorek nevyhovující pokynům v odst. b3 jehož (nedostatečná) kvalita by mohla mít vliv na výsledek vyšetření - vzorek, který nelze jednoznačně identifikovat c3) Instrukce pro načasování odběru Instrukce pro načasování odběru nejsou u vyšetření nutné, odběr ovšem není možný v období menses. c4) Pokyny pro zacházení se vzorkem mezi jeho odběrem a přijetím do laboratoře Primární vzorky cytologická skla jsou po fixaci stabilní. Lze je přepravovat při běžné teplotě a zdržení vzorku mezi odběrem a vyšetřením nemá vliv na kvalitu výsledku. c5) Pokyny pro označování primárních vzorků Primární vzorky (skla) musí být označena značkou lékaře nebo identifikací pacienta. (viz b2)) Značky (zkratky lékařů) jsou přidělovány laboratoří, seznam zkratek je uveden v příloze SOP. Identifikace skla (rodným číslem pacienta) musí být shodná s žádankou (viz také požadavky týkající se pozitivní identifikace pacientů v kapitole c7). Vzorky s neshodným označením budou z dalšího zpracování vyloučeny. c6) Klinické informace Klinické informace, které potřebuje laboratoř, jsou uvedeny na žádance. c7) Pozitivní identifikace pacienta Pozitivní identifikace pacienta je v laboratoři zajištěna následujícími provozními kroky: 1) při příjmu vzorků se provádí kontrola (shoda) identifikačních znaků pacienta na žádance a na biologickém materiálu 2) každý vzorek a žádanka dostane unikátní laboratorní číslo, shodné s číslem v laboratorním informačním systému POV - příručka pro odběr primárních vzorků - 5.doc Strana 4 (celkem 17)
5 3) přiřazené laboratorní číslo je uvedeno na zprávě o vyšetření pro zpětnou kontrolu 4) žádný vyšetřovací postup nepoužívá ředění nebo dělení vzorku, tudíž nejsou potřebná opatření na označování dalších vzorkovnic c8) Autorizace osoby provádějící odběr primárního vzorku Odběr primárního vzorku provádí ošetřující lékař gynekolog; identifikace lékaře musí být součástí vyplněné žádanky. c9) Pokyny pro bezpečnou likvidaci materiálů použitých při odběru vzorku Při odběru vzorku nevzniká nebezpečný odpad, avšak kartáček na odběr vzorku je po použití infekční. d1) Instrukce pro skladování po vyšetření vzorků v laboratoři Vyšetřené vzorky jsou stabilní za normální teploty a skladují se v přepravních boxech v archivu. d2) Informace o časovém rozpětí, kdy je možné požadovat dodatečné vyšetření Vyšetřené vzorky (skla) jsou dlouhodobě stabilní a je možné kdykoliv provést opakované nebo dodatečné vyšetření. d3) Informace o možných dodatečných vyšetřeních Dodatečná vyšetření k metodě nejsou k dispozici. d4) Instrukce pro opakované nebo další vyšetření Interval pro opakované nebo další vyšetření vychází v zásadě z doporučení IBA (viz IBA) obsaženého v datovém auditu (viz datový audit). Uživatelé programu Intellipat mohou využít doporučení, které generuje SW, ale konečné rozhodnutí a odpovědnost je na ošetřujícím gynekologovi. V souladu s datovým auditem ovšem také laboratoř musí vznést každé čtvrtletí dotaz na osud pacientky na ošetřujícího gynekologa, viz tabulka dotaz na osud pacientky. Interval pro vydávání výsledku vyšetření Horní hranice pro odeslání výsledků je stanovena datovým auditem screeningu karcinomu děložního hrdla a činí 3 týdny. Zdroj: Datový audit screeningu karcinomu děložního hrdla, Institut biostatistiky a analýz Masarykovy university, Brno, 2008 Autorský kolektiv: RNDr. Ing. Karel Chroust, Ph.D., Bc. Ondřej Májek, Mgr. Daniel Klimeš, Ing. Petr Brabec, doc. RNDr. Ladislav Dušek, Ph.D. Odpovědnost za uvolňování a předávání výsledků vyšetření Pracovník k metodě odpovídá za přenos výsledků do informačního systému, za distribuci (předání) výsledků pak nese odpovědnost pověřený pracovník. K distribuci je oprávněn výsledky uvolnit pouze vedoucí laboratoře, případně jeho zástupce. POV - příručka pro odběr primárních vzorků - 5.doc Strana 5 (celkem 17)
6 Vysvětlivky: IBA Institut biostatistiky a analýz Lékařské a Přírodovědecké fakulty Masarykovy univerzity Datový audit Datový audit a informační zázemí organizovaných programů screeningu zhoubných nádorových onemocnění v České republice Vyšetření okultního krvácení ve stolici (faecal occult blood, FOB) a1) Název vyšetření... 6 a2) Vzor formuláře prohlášení o souhlasu pacienta... 6 a3) Pokyny pacientům k jejich osobní přípravě před odběrem vzorků... 6 a4) Informaci pro uživatele služeb laboratoře o účelu a vhodnosti nabízených služeb... 6 b1) Postup pro přípravu pacienta před odběrem vzorku... 7 b2) Způsob označování primárního vzorku... 7 b3) VLASTNÍ POSTUP pro odběr primárního vzorku... 7 c1) Pokyny pro vyplnění žádanky... 7 c2) Pokyny pro druh a množství primárního vzorku... 7 c3) Instrukce pro načasování odběru... 7 c4) Pokyny pro zacházení se vzorkem mezi jeho odběrem a přijetím do laboratoře... 7 c5) Pokyny pro označování primárních vzorků... 8 c6) Klinické informace... 8 c7) Pozitivní identifikace pacienta... 8 c8) Autorizace osoby provádějící odběr primárního vzorku... 8 c9) Pokyny pro bezpečnou likvidaci materiálů použitých při odběru vzorku... 8 d1) Instrukce pro skladování po vyšetření vzorků v laboratoři... 8 d2) Informace o časovém rozpětí, kdy je možné požadovat dodatečné vyšetření... 8 d3) Informace o možných dodatečných vyšetřeních... 8 d4) Instrukce pro opakované nebo další vyšetření... 8 a1) Název vyšetření Vyšetření okultního krvácení ve stolici (faecal occult blood, FOB) a2) Vzor formuláře prohlášení o souhlasu pacienta Prohlášení o souhlasu k odběru vzorku se u vyšetření nepoužívá. a3) Pokyny pacientům k jejich osobní přípravě před odběrem vzorků Speciální osobní příprava pacienta před odběrem vzorku není nutná, což je také výhodou tohoto postupu vyšetření. a4) Informaci pro uživatele služeb laboratoře o účelu a vhodnosti nabízených služeb FOB test je kvalitativní test pro detekci okultního krvácení ve vzorcích lidské stolice v případech suspektního krvácení z dolní části trávicího traktu. POV - příručka pro odběr primárních vzorků - 5.doc Strana 6 (celkem 17)
7 b1) Postup pro přípravu pacienta před odběrem vzorku U pacientů se nepožaduje speciální dieta před odběrem vzorku stolice. V době testování by pacient ovšem obecně neměl užívat léky způsobující gastrointestinální poškození (např. nesteroidní antirevmatika). b2) Způsob označování primárního vzorku Vzorek pacienta je označen minimálně rodným číslem pacienta popř. pořadovým číslem v daný pracovní den.. Vzhledem k tomu, že vzorkovnice na stanovení FOB představují specifické nosiče vzorků, které nelze s žádným dalším vyšetřením v laboratoři zaměnit, není nutné označovat vzorek požadavkem na vyšetření. Tento požadavek se vypíše na přiložené žádance. b3) VLASTNÍ POSTUP pro odběr primárního vzorku 1) otevřít vzorkovnici, ve víčku se nachází odběrová tyčinka 2) krouživým pohybem tyčinky odebrat ze 3 až 6 míst stolice vzorek; dostačující je kulička velikosti černého pepře 3) upozornění: větší množství může zanést filtr ve víčku 4) upozornění: řídká stolice nemusí na tyčince dobře ulpět 5) odběrovou tyčinku se vzorkem zasunout do lahvičky a pečlivě uzavřít 6) důkladně protřepat 7) před předáním lékaři uchovat vzorkovnici v temnu při teplotě 2-25 C 8) vzorkovnici předat lékaři nejpozději druhý den po odběru Vlastní postup pro odběr primárního vzorku je včetně nákresu uváděn přímo na žádance k vyšetření. c1) Pokyny pro vyplnění žádanky Formulář žádosti o vyšetření (žádanka) musí být jednoznačně vyplněn; nevyplněné položky jsou laboratoří interpretována jako nepožadováno. Zvláštní pozornost je třeba věnovat identifikaci klienta a identifikaci požadujícího lékaře. c2) Pokyny pro druh a množství primárního vzorku vzorek stolice velikosti hlavičky černého pepře, detaily viz b3) Kritériem pro odmítnutí vzorku je: - vzorek nevyhovující pokynům v odst. b3 jehož (nedostatečná) kvalita by mohla mít vliv na výsledek vyšetření - vzorek, který nelze jednoznačně identifikovat c3) Instrukce pro načasování odběru Načasování odběru není pro vyšetření kritické, ale pacient by měl dodržovat pokyny uvedené v kapitole b3) Postup pro odběr primárního vzorku. c4) Pokyny pro zacházení se vzorkem mezi jeho odběrem a přijetím do laboratoře Vzorek je stabilní 5 dní v temnu při teplotě 2-25 C. POV - příručka pro odběr primárních vzorků - 5.doc Strana 7 (celkem 17)
8 c5) Pokyny pro označování primárních vzorků Primární vzorky (vzorkovnice se štětečkem a vzorkem v pufru) se ihned po dodání označí shodně s žádankou. Identifikace vzorku (rodným číslem pacienta) musí být shodná s žádankou (viz také požadavky týkající se pozitivní identifikace pacientů v kapitole c7). Vzorky s neshodným označením budou z dalšího zpracování vyloučeny. c6) Klinické informace Laboratoř nepotřebuje pro vyšetření žádné klinické informace o pacientovi. Interpretace výsledků je záležitostí ošetřujícího lékaře. c7) Pozitivní identifikace pacienta Pozitivní identifikace pacienta je v laboratoři zajištěna následujícími provozními kroky: 1) při příjmu vzorků se provádí kontrola (shoda) identifikačních znaků pacienta na žádance a na biologickém materiálu, po kontrole je vzorek ihned označen datem příjmu a laboratorním číslem 2) vzorek a žádanka jsou jednoznačně označeny tak, aby nemohlo dojít k záměně 3) existuje jednoznačná vazba mezi žádankou a zprávou o vyšetření 4) žádný vyšetřovací postup nepoužívá ředění nebo dělení vzorku, tudíž nejsou potřebná opatření na označování dalších vzorkovnic c8) Autorizace osoby provádějící odběr primárního vzorku Odběr primárního vzorku provádí pacient klient; na žádance ovšem musí být jednoznačná identifikace ošetřujícího lékaře. c9) Pokyny pro bezpečnou likvidaci materiálů použitých při odběru vzorku Při odběru vzorku nevzniká nebezpečný odpad. d1) Instrukce pro skladování po vyšetření vzorků v laboratoři Primární vzorek anebo části vzorku po vyšetření nelze skladovat. d2) Informace o časovém rozpětí, kdy je možné požadovat dodatečné vyšetření Dodatečná vyšetření nelze provést. Pro zabezpečení kvality se namátkově vyšetřuje vzorek duplicitně (dvěma laboranty). d3) Informace o možných dodatečných vyšetřeních Laboratoř žádné dodatečné vyšetření neprovádí. V případě pozitivního výsledku doporučí ošetřujícímu lékaři odeslat pacienta na gastroenterologické vyšetření. d4) Instrukce pro opakované nebo další vyšetření Opakované vyšetření nelze provést na původním vzorku; nutno odebrat vzorek nový. POV - příručka pro odběr primárních vzorků - 5.doc Strana 8 (celkem 17)
9 Interval pro vydávání výsledku vyšetření Vzorky pro stanovení FOB se přijímají do laboratoře tak, aby mohly být analyzovány nejpozději do 5-ti kalendářních dnů od data odběru. Zpráva o vyšetření je vystavena vždy v den analýzy a tentýž den odeslána zákazníkovi. Odpovědnost za uvolňování a předávání výsledků vyšetření Pracovník k metodě odpovídá za přenos výsledků do informačního systému, za distribuci (předání) výsledků pak nese odpovědnost pověřený pracovník. K distribuci je oprávněn výsledky uvolnit pouze vedoucí laboratoře, případně jeho zástupce. Vyšetření spermatu nativní spermiogram a1) Název vyšetření... 9 a2) Vzor formuláře prohlášení o souhlasu pacienta... 9 a3) Pokyny pacientům k jejich osobní přípravě před odběrem vzorků... 9 a4) Informaci pro uživatele služeb laboratoře o účelu a vhodnosti nabízených služeb b1) Postup pro přípravu pacienta před odběrem vzorku b2) Způsob označování primárního vzorku b3) VLASTNÍ POSTUP pro odběr primárního vzorku c1) Pokyny pro vyplnění žádanky c2) Pokyny pro druh a množství primárního vzorku c3) Instrukce pro načasování odběru c4) Pokyny pro zacházení se vzorkem mezi jeho odběrem a přijetím do laboratoře c5) Pokyny pro označování primárních vzorků c6) Klinické informace c7) Pozitivní identifikace pacienta c8) Autorizace osoby provádějící odběr primárního vzorku c9) Pokyny pro bezpečnou likvidaci materiálů použitých při odběru vzorku d1) Instrukce pro skladování po vyšetření vzorků v laboratoři d2) Informace o časovém rozpětí, kdy je možné požadovat dodatečné vyšetření d3) Informace o možných dodatečných vyšetřeních d4) Instrukce pro opakované nebo další vyšetření a1) Název vyšetření Vyšetření spermatu nativní spermiogram a2) Vzor formuláře prohlášení o souhlasu pacienta Prohlášení o souhlasu k odběru vzorku se u vyšetření nepoužívá. a3) Pokyny pacientům k jejich osobní přípravě před odběrem vzorků Speciální osobní příprava pacienta před odběrem vzorku není nutná, avšak je nutné dbát pokynů podle kapitoly b1) - Postup pro přípravu pacienta před odběrem vzorku. POV - příručka pro odběr primárních vzorků - 5.doc Strana 9 (celkem 17)
10 a4) Informaci pro uživatele služeb laboratoře o účelu a vhodnosti nabízených služeb Vyšetření spermatu nativní spermiogram slouží k vyšetření kvality spermatu a porovnání výsledků s obecně přijímanými limity (World Health Organisation, WHO). b1) Postup pro přípravu pacienta před odběrem vzorku Před vyšetřením je nutné dodržet 4-5 dnů bez ejakulace, min však 48 hodin. Hraniční hodnoty podle doporučení WHO jsou 2 až 7 dní. b2) Způsob označování primárního vzorku Vzorek pacienta musí být označen minimálně rodným číslem a jménem pacienta (klienta). Vzhledem k tomu, že vzorkovnice na vyšetření spermatu představují specifické nosiče vzorků, které nelze s žádným dalším vyšetřením v laboratoři zaměnit, není nutné označovat vzorek požadavkem na vyšetření. Tento požadavek se vypíše na přiložené žádance. b3) VLASTNÍ POSTUP pro odběr primárního vzorku 1) Vzorek má být získán čistou masturbací, aby nemohla uniknout první porce ejakulátu, nejbohatší na spermie, mimo nádobu. Vzorek nesmí být jakkoliv znečištěn, například slinami, poševními sekrety nebo získáním z kondomu. Získání ejakulátu z přerušované soulože není akceptováno. 2) Veškeré množství ejakulátu má být odebráno do běžné čisté, vymyté nádoby se širokým hrdlem uzávěrem (nebo standardní vzorkovnice, kterou vydá pacientovi laboratoř), která nemusí být sterilní, ale musí však být zbavena jakýchkoliv zbytků dezinfekce a chemikálií. Stačí kvalitní proplach, umytí a vysušení. 3) Vzhledem k variabilitě vzorku by měl být odebrán druhý vzorek ejakulátu v intervalu ne dříve než za týden a ne později než za tři týdny. c1) Pokyny pro vyplnění žádanky Formulář žádosti o vyšetření (žádanka) musí být jednoznačně vyplněn; nevyplněné položky jsou laboratoří interpretována jako nepožadováno. Zvláštní pozornost je třeba věnovat identifikaci klienta a identifikaci požadujícího lékaře. c2) Pokyny pro druh a množství primárního vzorku Odebírá se ejakulát, jehož množství je dáno fyziologicky / zdravotním stavem klienta. Kritériem pro odmítnutí vzorku je: - vzorek nevyhovující pokynům v odst. b3 jehož (nedostatečná) kvalita by mohla mít vliv na výsledek vyšetření - vzorek, který nelze jednoznačně identifikovat c3) Instrukce pro načasování odběru Načasování odběru není pro vyšetření kritické, ale pacient by měl dodržovat pokyny uvedené v kapitole b3) Postup pro odběr primárního vzorku. POV - příručka pro odběr primárních vzorků - 5.doc Strana 10 (celkem 17)
11 c4) Pokyny pro zacházení se vzorkem mezi jeho odběrem a přijetím do laboratoře Transport ke zpracování nesmí trvat déle než 1 hod. od odběru. Čím kratší čas uplyne mezi odběrem a zpracováním, tím přesnější je výsledek. Nádobka musí být transportována při teplotě blízké tělesné hranice od 20 do 40 C. c5) Pokyny pro označování primárních vzorků Primární vzorky (vzorkovnice s ejakulátem) se označují popř. kontrolují v laboratoři ihned po dodání ve shodně s žádankou, resp. pop případné identifikaci pacienta. c6) Klinické informace Laboratoř nepotřebuje pro vyšetření žádné klinické informace o pacientovi. Interpretace výsledků je záležitostí ošetřujícího lékaře. c7) Pozitivní identifikace pacienta Pozitivní identifikace pacienta je v laboratoři zajištěna následujícími provozními kroky: 1) při příjmu vzorků se provádí kontrola (shoda) identifikačních znaků pacienta na požadavkovém listu (žádance) a na biologickém materiálu; po kontrole je vzorek ihned označen časem a datem příjmu a laboratorním číslem 2) vzorek a žádanka jsou jednoznačně označeny tak, aby nemohlo dojít k záměně 3) existuje jednoznačná vazba mezi žádankou a zprávou o vyšetření 4) vzorkovnice použité na ředění vzorku ( kepíky ) jsou označeny shodně s původním vzorkem c8) Autorizace osoby provádějící odběr primárního vzorku Odběr primárního vzorku provádí pacient klient. Pracovník na příjmu vzorků v laboratoři stvrzuje svým podpisem na žádance správnost údajů, viz také kapitoly c7 pozitivní identifikace pacienta. c9) Pokyny pro bezpečnou likvidaci materiálů použitých při odběru vzorku Při odběru vzorku nevzniká nebezpečný odpad. d1) Instrukce pro skladování po vyšetření vzorků v laboratoři Primární vzorek anebo části vzorku po vyšetření nelze skladovat. d2) Informace o časovém rozpětí, kdy je možné požadovat dodatečné vyšetření Dodatečná vyšetření nelze provést vzhledem k životnosti nativního vzorku. Pro zabezpečení kvality se namátkově vyšetřuje vzorek duplicitně (dvěma laboranty). d3) Informace o možných dodatečných vyšetřeních Dodatečná vyšetření k metodě nejsou k dispozici. POV - příručka pro odběr primárních vzorků - 5.doc Strana 11 (celkem 17)
12 d4) Instrukce pro opakované nebo další vyšetření Opakované vyšetření nelze provést na původním vzorku; nutno odebrat vzorek nový. Vzhledem k variabilitě vzorku by měl být odebrán druhý vzorek ejakulátu v intervalu ne dříve než za týden a ne později než za tři týdny. (viz. text na žádance). Interval pro vydávání výsledku vyšetření Vzorky pro vyšetření spermatu se přijímají do laboratoře tak, aby mohly být analyzovány ihned, zpravidla v určený den v týdnu (čtvrtek). Vzorky musí být zpracovány ihned, výsledky se předávají tentýž den. Odpovědnost za předávání výsledků vyšetření Pracovník k metodě odpovídá za přenos výsledků do informačního systému, za distribuci (předání) výsledků pak nese odpovědnost pověřený pracovník. K distribuci je oprávněn výsledky uvolnit pouze vedoucí laboratoře, případně jeho zástupce. Vyšetření vysoce rizikových papillomavirů (HR HPV) pomocí testu cobas 4800 a1) Název vyšetření a2) Vzor formuláře prohlášení o souhlasu pacienta a3) Pokyny pacientům k jejich osobní přípravě před odběrem vzorku a4) Informaci pro uživatele služeb laboratoře o účelu a vhodnosti nabízených služeb a5) Indikace použití testu cobas 4800 HPV b1) Postup pro přípravu pacienta před odběrem vzorku b2) Způsob označování primárního vzorku b3) Vlastní postup pro odběr primárního vzorku b4) Kontraindikace odběru vzorku c1) Pokyny pro vyplnění žádanky c2) Pokyny pro druh a množství primárního vzorku c3) Instrukce pro načasování odběru c4) Pokyny pro zacházení se vzorkem mezi jeho odběrem a přijetím do laboratoře c5) Pokyny pro označování primárních vzorků c6) Klinické informace c7) Pozitivní identifikace pacienta c8) Autorizace osoby provádějící odběr primárního vzorku c9) Pokyny pro bezpečnou likvidaci materiálů použitých při odběru vzorku d1) Instrukce pro skladování po vyšetření vzorku v laboratoři d2) Informace o časovém rozpětí, kdy je možné požadovat dodatečné vyšetření d3) Informace o možných dodatečných vyšetřeních d4) Instrukce pro opakované nebo další vyšetření a1) Název vyšetření Vyšetření vysoce rizikových papillomavirů (HR HPV) pomocí testu cobas 4800 šetření POV - příručka pro odběr primárních vzorků - 5.doc Strana 12 (celkem 17)
13 a2)vzor formuláře prohlášení o souhlasu pacienta Prohlášení o souhlasu k odběru vzorku se u vyšetření nepoužívá. a3) Pokyny pacientům k jejich osobní přípravě před odběrem vzorku Návody předávané pacientovi nejsou použity. a4) Informace pro uživatele služeb laboratoře o účelu a vhodnosti nabízených služeb Průkaz genomu Hight Risk HPV v cervikálních buňkách (detekce virů typu 16 a 18 a skupiny virů 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 66, 68). a5) Indikace použití testu cobas 4800 HPV Vyšetření umožňuje vyhodnotit charakter infekce virem HPV a prognózu nemocných. Dle ASCCP 2006, USA (Consensus Guidelines for the Management of Women With Abnormal Cervical Screening Tests) a konsenzu odborníků z kolposkopické a onkogynekologické sekce ČGPS společně se Společností českých patologů jsou indikace použití testu cobas 4800 HPV následující: - screening pacientek s výsledky cytologie ASC-US (atypické šupinovité buňky neurčitého významu) pro stanovení nutnosti provedení kolposkopie. - u žen s ASC-H (atypické dlaždicovité buňky naznačující HSIL, tj. high grade squamous intraepitelial lesion) - u žen s LSIL (low grade squamous intraepitelial lesion) - u žen s atypickými žlázovými buňkami (AGC) - při screeningu karcinomu děložního hrdla u žen nad 30 let (pouze určení HR HPV) - u žen s histologickou diagnózou CIN-1, které předcházela cytologie ASC-US, ASC-H nebo LSIL - u žen s histologickou diagnózou CIN-2,3 po léčbě - u žen s ASC-US ve věku do 30 let a starších žen plánujících těhotenství s anamnézou abnormální onkologická cytologie nebo konizace pro prekancerózu - u žen s ASC-US nad 30 let a mladších žen neplánujících těhotenství (preferovat u žen s anamnézou abnormální onkologická cytologie, SIL nebo konizace pro prekancerózu) - u žen s ASC-H do 30 let a starších žen plánujících těhotenství s normální kolposkopií - u žen s ASC-H nad 30 let a mladších žen neplánujících těhotenství s normální kolposkopií - u žen s AGC-NOS do 30 let a starších žen plánujících těhotenství - u žen s AGC-NOS nad 30 let a mladších žen neplánujících těhotenství - u žen s AGC-NEO do 30 let a starších žen plánujících těhotenství po expertní kolposkopii s HGL vyloučenou - u žen s AGC-NEO nad 30 let a mladších žen neplánujících těhotenství po expertní kolposkopii s výsledkem normální - u žen s LSIL nad 30 let a neplánujících těhotenství po kolposkopii s ATZ ne plně vizualizovatelnou U žen ve věku 30 let a starších lze test cobas 4800 HPV využít ke stanovení přítomnosti nebo nepřítomnosti genotypů HPV 16 a 18. Tyto informace společně s lékařským vyhodnocením anamnézy cytologie, dalších rizikových faktorů a odborných zásad lze použít jako vodítko pří léčbě pacientek. b1) Postup pro přípravu pacienta před odběrem vzorku POV - příručka pro odběr primárních vzorků - 5.doc Strana 13 (celkem 17)
14 Zvláštní osobní příprava pacienta před odběrem vzorku není nutná, resp. je plně v kompetenci ošetřujícího gynekologa. Vzorek by se neměl odebírat při menses a dále je nutné respektovat pokyny v b4) Kontraindikace odběru vzorku. b2) Způsob označování primárního vzorku Vzorek pacienta musí být označen tak, aby byl jednoznačně identifikován a spojen se žádankou. Označení lze provést: 1) jménem a příjmením pacienta 2) rodným číslem pacienta 3) kombinace předchozích dvou možností b3) Vlastní postup pro odběr primárního vzorku 1) Umístěte Rovers Cervex-Brush (odběrový kartáček) na endocervikální kanál. Jemně zatlačte kartáč proti děložnímu čípku. Udržujte jemný tlak, tyčinku držte mezi palcem a ukazovákem a otočte kartáč pětkrát ve směru hodinových ručiček. 2) Zatlačením palce na zadní stranu kartáčku jednoduše odpojte celý kartáč z tyčinky do lahvičky s konzervačním médiem (cobas PCR cell collection media). 3) Umístěte víčko na lahvičku a utáhněte. Označte lahvičku a žádanku. 4) Umístěte lahvičky do sáčku a spolu s přiloženou žádankou (tak, aby nedošlo ke kontaminaci)odešlete do laboratoře. Viz také obrazovou předlohu v Příloze 1 POV. b4) Kontraindikace odběru vzorku Cervex-Brush by neměl být používán v prvních 10 týdnech těhotenství u těhotných. Odběr by také neměl být prováděn během menstruace (viz b1)). c1) Pokyny pro vyplnění žádanky Formulář žádosti o vyšetření (žádanka) musí být jednoznačně vyplněn; nevyplněné položky jsou laboratoří interpretovány jako,,jev se nevyskytl. Zvláštní pozornost je třeba věnovat identifikaci klienta a identifikaci požadujícího lékaře. c2) Pokyny pro druh a množství primárního vzorku Provádí se stěr z endocervixu za pomocí odběrového kartáčku Cervex-Brush. Podrobný postup je uveden v kapitole b3) Postup pro odběr primárního vzorku. Kritériem pro odmítnutí vzorku je: - vzorek nevyhovující pokynům v odst. b3 jehož nedostatečná kvalita by mohla mít vliv na výsledek měření o tomto nemůže rozhodnout pracovník na příjmu, ale takový vzorek je na základě kontroly přítomnosti â-globinu odmítnut přístrojem - vzorek, který nelze jednoznačně identifikovat - viditelně poškozená vzorkovnice - nadbytečné množství krve nehodnotí pracovník na příjmu, ale takový vzorek je následně odmítnut přístrojem - vzorkovnice s obsahem menším než 3ml Používaný odběrový systém POV - příručka pro odběr primárních vzorků - 5.doc Strana 14 (celkem 17)
15 Pro odběry jsou používány komerční lahvičky s konzervačním médiem (cobas PCR cell collection media PCR odběrové buněčné medium cobas), které je možné si spolu s odběrovými kartáčky a transportními sáčky vyžádat v laboratoři na tel. čísle nebo Lahvičky s odběrovým médiem do odběru skladujte dle informací na lhvičce C. c3) Instrukce pro načasování odběru Instrukce pro načasování odběru nejsou u vyšetření nutné, odběr by ovšem neměl být prováděn v období menstruace. (viz také b4), b1)). c4) Pokyny pro zacházení se vzorkem mezi jeho odběrem a přijetím do laboratoře Vzorek je stabilní 6 měsíců při teplotě 2-8 C nebo při teplotě do 30 C. Materiál musí být dopraven v určených a neporušených vzorkovnicích opatřených identifikačním štítkem a papírovou žádankou. Vzhledem ke stabilitě vzorků (c4)) se převoz vzorků do laboratoře provádí bez chlazení, při normální teplotě. c5) Pokyny pro označování primárních vzorků Primární vzorky (odběrové lahvičky) musí být označeny identifikací pacienta. (viz. b2) Identifikace primárního vzorku musí být shodná s žádankou. Vzorky s neshodným označením budou z dalšího zpracování vyloučeny (c2)). c6) Klinické informace Laboratoř nepotřebuje pro vyšetření žádné klinické informace o pacientovi. Interpretace výsledků je záležitostí ošetřujícího lékaře. c7) Pozitivní identifikace pacienta Pozitivní identifikace pacienta je v laboratoři zajištěna následujícími provozními kroky: 1) Při příjmu vzorku se provádí kontrola (shoda) identifikačních znaků pacienta na žádance a na vzorkovnici s odebraným biologickým materiálem. 2) Po kontrole je vzorek ihned označen datem příjmu a laboratorním číslem. 3) Vzorek a žádanka jsou jednoznačně označeny tak, aby nemohlo dojít k záměně. 4) Existuje jednoznačná vazba mezi žádankou a zprávou o vyšetření. 5) Vyšetřovací postup nepoužívá ředění nebo dělení vzorku, tudíž nejsou potřebná opatření na označování dalších vzorkovnic. c8) Autorizace osoby provádějící odběr primárního vzorku Odběr primárního vzorku provádí ošetřující lékař gynekolog; jednoznačná identifikace lékaře musí být součástí vyplněné žádanky (jméno, adresa, IČP). c9) Pokyny pro bezpečnou likvidaci materiálů použitých při odběru vzorku Kartáček na odběr vzorku je po použití infekční a je povinností odebírajícího lékaře zajistit jeho likvidaci s ohledem na tuto skutečnost. Jiný nebezpečný odpad při odběru nevzniká. d1) Instrukce pro skladování po vyšetření vzorku v laboratoři Vzorek je po vyšetření ihned likvidován v souladu s Provozním řádem laboratoře. POV - příručka pro odběr primárních vzorků - 5.doc Strana 15 (celkem 17)
16 Skladování vzorku po vyšetření je možné pouze pro účely interní kontroly kvality a to nejdéle po dobu 6 měsíců při teplotě 2-8 C nebo při teplotě do 30 C (c4)). d2) Informace o časovém rozpětí, kdy je možné požadovat dodatečné vyšetření Vzorky jsou po vyšetření ihned likvidovány, opakovaná ani dodatečná vyšetření se neprovádějí. d3) Informace o možných dodatečných vyšetřeních Dodatečná vyšetření k metodě nejsou k dispozici. d4) Instrukce pro opakované nebo další vyšetření Interval pro opakované nebo další vyšetření určuje ošetřující lékař. Pro opakované vyšetření je nutno odebrat vzorek nový. Interval pro vydávání výsledku vyšetření Výsledky vyšetření vzorků jsou dodávané nejpozději do 14 dnů od přijetí vzorku laboratoří výhradně odesílajícímu lékaři. Odpovědnost za uvolňování a předávání výsledků vyšetření Výsledky jsou po kontrole odpovědným VŠ pracovníkem (PK Příloha 6) uvolněny a vydávají se v tištěné formě. Přílohy Příloha 1 - Postup pro odběr vzorků dle SOP4 Dokument Jméno Datum Podpis Vypracoval: Miloslava Dümlerová Kontroloval: Schválil: Kateřina Blahová Radka Zgabajová Jitka Kvaššay MUDr. Petr Mičulka Mgr.Vladimíra Holubová Rozdělovník Jméno Datum Podpis 1 manažer kvality 2 laboratoř 3 Přezkoumal Jméno Datum Podpis POV - příručka pro odběr primárních vzorků - 5.doc Strana 16 (celkem 17)
17 Seznámení s dokumentací Jméno Datum Podpis 1 MUDr. Ingrid Švarcová 2 Dana Šperlingová 3 Jana Šabršulová 4 Ludmila Holubcová 5 Petra Janotová 6 Kateřina Blahová 7 Dana Vojtášková POV - příručka pro odběr primárních vzorků - 5.doc Strana 17 (celkem 17)
Cytologický gynekologický screening a diagnostika
 Příručka pro odběr primárních vzorků Klinická laboratoř společnosti GYNEKO spol. s r.o. Cytologický gynekologický screening a diagnostika Vyšetření okultního krvácení ve stolici (faecal occult blood, FOB)
Příručka pro odběr primárních vzorků Klinická laboratoř společnosti GYNEKO spol. s r.o. Cytologický gynekologický screening a diagnostika Vyšetření okultního krvácení ve stolici (faecal occult blood, FOB)
Příručka pro odběr primárních vzorků. BIOLAB Praha Laboratoř Vsetín. Cytologický gynekologický screening a diagnostika
 Příručka pro odběr primárních vzorků BIOLAB Praha Cytologický gynekologický screening a diagnostika Vyšetření spermatu nativní spermiogram Vyšetření HPV Kontaktní informace: BIOLAB Praha Nemocniční 945,
Příručka pro odběr primárních vzorků BIOLAB Praha Cytologický gynekologický screening a diagnostika Vyšetření spermatu nativní spermiogram Vyšetření HPV Kontaktní informace: BIOLAB Praha Nemocniční 945,
Příručka pro odběr primárních vzorků. Klinická laboratoř společnosti GYNEKO spol. s r.o. Cytologický gynekologický screening a diagnostika
 Příručka pro odběr primárních vzorků Klinická laboratoř společnosti GYNEKO spol. s r.o. Cytologický gynekologický screening a diagnostika Vyšetření okultního krvácení ve stolici (faecal occult blood, FOB)
Příručka pro odběr primárních vzorků Klinická laboratoř společnosti GYNEKO spol. s r.o. Cytologický gynekologický screening a diagnostika Vyšetření okultního krvácení ve stolici (faecal occult blood, FOB)
BIOLAB Praha. Cytologický gynekologický screening a diagnostika. Vyšetření HPV
 Příručka pro odběr primárních vzorků BIOLAB Praha Cytologický gynekologický screening a diagnostika Vyšetření spermatu nativní spermiogram Vyšetření HPV Kontaktní informace: BIOLAB Praha Nemocniční 945,
Příručka pro odběr primárních vzorků BIOLAB Praha Cytologický gynekologický screening a diagnostika Vyšetření spermatu nativní spermiogram Vyšetření HPV Kontaktní informace: BIOLAB Praha Nemocniční 945,
Konsensus pro řešení abnormálních nálezů ve skríningu cervikálních karcinomů
 Konsensus pro řešení abnormálních nálezů ve skríningu cervikálních karcinomů Členové panelu Sekce kolposkopie a cervikální patologie ČGPS MUDr. Vladimír Dvořák (místopředseda sekce) Doc. MUDr. Pavel Freitag,
Konsensus pro řešení abnormálních nálezů ve skríningu cervikálních karcinomů Členové panelu Sekce kolposkopie a cervikální patologie ČGPS MUDr. Vladimír Dvořák (místopředseda sekce) Doc. MUDr. Pavel Freitag,
Laboratorní příručka
 Typ dokumentu: Příručka Zpracoval/datum/podpis: 25. 5. 2014 Přezkoumal/datum/podpis: 3. 6. 2014 Schválil/datum/podpis: 3. 6. 2014 Číslo verze: 02 Číslo výtisku: 01 Platnost od: 1. 7. 2014 Verze: 02 Změna
Typ dokumentu: Příručka Zpracoval/datum/podpis: 25. 5. 2014 Přezkoumal/datum/podpis: 3. 6. 2014 Schválil/datum/podpis: 3. 6. 2014 Číslo verze: 02 Číslo výtisku: 01 Platnost od: 1. 7. 2014 Verze: 02 Změna
DIAGNOSTICKO TERAPEUTICKÝ ALGORITMUS CERVIKÁLNÍCH INTRAEPITELIÁLNÍCH NEOPLÁZIÍ L.ŠEVČÍK, P.GRAF, S.ĎURIANOVÁ
 Porodnicko-gynekologická klinika FN a LF OU v Ostravě přednosta: Doc. MUDr. Vít Unzeitig, CSc. DIAGNOSTICKO TERAPEUTICKÝ ALGORITMUS CERVIKÁLNÍCH INTRAEPITELIÁLNÍCH NEOPLÁZIÍ L.ŠEVČÍK, P.GRAF, S.ĎURIANOVÁ
Porodnicko-gynekologická klinika FN a LF OU v Ostravě přednosta: Doc. MUDr. Vít Unzeitig, CSc. DIAGNOSTICKO TERAPEUTICKÝ ALGORITMUS CERVIKÁLNÍCH INTRAEPITELIÁLNÍCH NEOPLÁZIÍ L.ŠEVČÍK, P.GRAF, S.ĎURIANOVÁ
Datové rozhraní pro předávání dat cervikálního screeningu k centrálnímu zpracování Verze 1.2 (1.12.2008)
 Datové rozhraní pro předávání dat cervikálního screeningu k centrálnímu zpracování Verze 1.2 (1.12.2008) EXPORTNÍ SOUBORY Cytologické vyšetření Soubor obsahuje jeden záznam pro každé provedené screeningové
Datové rozhraní pro předávání dat cervikálního screeningu k centrálnímu zpracování Verze 1.2 (1.12.2008) EXPORTNÍ SOUBORY Cytologické vyšetření Soubor obsahuje jeden záznam pro každé provedené screeningové
Prekancerózy cervicis uteri
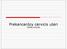 Prekancerózy cervicis uteri Ondřej Kuchyňa Epidemiologie Incidence ca cervicis uteri se u nás dlouhodobě pohybuje okolo 20/100 000 obyvatel /rok. Evropská unie 12.8/100 000/rok Primární prevence- preventivní
Prekancerózy cervicis uteri Ondřej Kuchyňa Epidemiologie Incidence ca cervicis uteri se u nás dlouhodobě pohybuje okolo 20/100 000 obyvatel /rok. Evropská unie 12.8/100 000/rok Primární prevence- preventivní
Řízení preanalytické fáze, principy a odpovědnost
 Řízení preanalytické fáze, principy a odpovědnost dnost MUDr. Miroslav Verner Nemocnice České Budějovice a.s. Centrální laboratoře České Budějovice 30.9.2009, e-medica Problémy tradičních dominantně děděných
Řízení preanalytické fáze, principy a odpovědnost dnost MUDr. Miroslav Verner Nemocnice České Budějovice a.s. Centrální laboratoře České Budějovice 30.9.2009, e-medica Problémy tradičních dominantně děděných
Příručka pro odběr primárních vzorků cytologické laboratoře
 Gynekologicko porodní oddělení Standardní operační postup organizační Počet stran textu: 15 Počet příloh: 1 Název dokumentu: cytologické laboratoře Zpracoval: Zkontroloval: Schválil:... Ing. Ludmila Švandová
Gynekologicko porodní oddělení Standardní operační postup organizační Počet stran textu: 15 Počet příloh: 1 Název dokumentu: cytologické laboratoře Zpracoval: Zkontroloval: Schválil:... Ing. Ludmila Švandová
SCREENINGOVÉ PROGRAMY V ČR Z POHLEDU VZP ČR
 SCREENINGOVÉ PROGRAMY V ČR Z POHLEDU VZP ČR 5.12. 2013 MUDr. HANA ŠUSTKOVÁ, VZP ČR OBSAH 1. Screening karcinomu děložního hrdla 2. Mamografický screening 3. Screening kolorektálního karcinomu 4. Projekt
SCREENINGOVÉ PROGRAMY V ČR Z POHLEDU VZP ČR 5.12. 2013 MUDr. HANA ŠUSTKOVÁ, VZP ČR OBSAH 1. Screening karcinomu děložního hrdla 2. Mamografický screening 3. Screening kolorektálního karcinomu 4. Projekt
Indikátory kvality v programu screeningu karcinomu děložního hrdla v ČR O. Májek, J. Dušková, A. Beková, L. Dušek, V. Dvořák
 Indikátory kvality v programu screeningu karcinomu děložního hrdla v ČR O. Májek, J. Dušková, A. Beková, L. Dušek, V. Dvořák Úvod Účinnost screeningové cytologie Finsko a Švédsko: organizované programy
Indikátory kvality v programu screeningu karcinomu děložního hrdla v ČR O. Májek, J. Dušková, A. Beková, L. Dušek, V. Dvořák Úvod Účinnost screeningové cytologie Finsko a Švédsko: organizované programy
LABORATORNÍ PŘÍRUČKA LP
 GYN-CYT s.r.o platnost od 1.7.2015 strana 1 / 12 GYN-CYT s.r.o. Gynekologická ordinace a laboratoř gynekologické cytologie U Nemocnice 380/III 377 38 Jindřichův Hradec IČ 28118511 LABORATORNÍ PŘÍRUČKA
GYN-CYT s.r.o platnost od 1.7.2015 strana 1 / 12 GYN-CYT s.r.o. Gynekologická ordinace a laboratoř gynekologické cytologie U Nemocnice 380/III 377 38 Jindřichův Hradec IČ 28118511 LABORATORNÍ PŘÍRUČKA
A - ÚVOD. A1 Předmluva. A2 Obsah. Vážené kolegyně, vážení kolegové, vážení klienti,
 Vznikající záznamy: 0 Strana: 1 z 13 A - ÚVOD A1 Předmluva Vážené kolegyně, vážení kolegové, vážení klienti, tato laboratorní příručka je věnována všem, kteří potřebují informace o naší laboratoři, o naší
Vznikající záznamy: 0 Strana: 1 z 13 A - ÚVOD A1 Předmluva Vážené kolegyně, vážení kolegové, vážení klienti, tato laboratorní příručka je věnována všem, kteří potřebují informace o naší laboratoři, o naší
Laboratorní příručka
 Hvězdova 1073/33, 140 00 Praha 4 Laboratorní příručka Výtisk č.:01 Počet stran: 6 Datum vydání: 18.8.2016 Datum účinnosti: 18.8.2016 Zrušovací ustanovení: / Zpracoval Schválil Jméno Ing.Kristýna Chaloupková
Hvězdova 1073/33, 140 00 Praha 4 Laboratorní příručka Výtisk č.:01 Počet stran: 6 Datum vydání: 18.8.2016 Datum účinnosti: 18.8.2016 Zrušovací ustanovení: / Zpracoval Schválil Jméno Ing.Kristýna Chaloupková
LABORATORNÍ PŘÍRUČKA
 Verze:1.0 str. 1 PROKOPEC COP s.r.o. Centrum onkologické prevence v gynekologii Gynekologická ordinace a laboratoř gynekologické cytologie U Tří lvů 4 370 01, České Budějovice IČO 28159632 LABORATORNÍ
Verze:1.0 str. 1 PROKOPEC COP s.r.o. Centrum onkologické prevence v gynekologii Gynekologická ordinace a laboratoř gynekologické cytologie U Tří lvů 4 370 01, České Budějovice IČO 28159632 LABORATORNÍ
LABORATORNÍ PŘÍRUČKA
 LABORATORNÍ PŘÍRUČKA MDgK- plus spol. s r.o. Vydání č. 1 schválila dne: 21.12. 2011 MUDr. Jarmila Klusáková, PhD, Datum platnosti: 22.12. 2012 Stránka 1 z 8 OBSAH: 1. ÚVOD....3 2. INFORMACE O LABORATOŘI
LABORATORNÍ PŘÍRUČKA MDgK- plus spol. s r.o. Vydání č. 1 schválila dne: 21.12. 2011 MUDr. Jarmila Klusáková, PhD, Datum platnosti: 22.12. 2012 Stránka 1 z 8 OBSAH: 1. ÚVOD....3 2. INFORMACE O LABORATOŘI
je nutno páchat sebevraždu? Lenka Čeganová, Laboratoř Trutnov
 Selhání cervikovaginální cytologie je ntno páchat sebevražd? Lenka Čeganová, Laboratoř Trtnov Cervikovaginální cytologie Žádný test v historii nebyl úspěšnější v boji s rakovino Ale: cervikovaginální
Selhání cervikovaginální cytologie je ntno páchat sebevražd? Lenka Čeganová, Laboratoř Trtnov Cervikovaginální cytologie Žádný test v historii nebyl úspěšnější v boji s rakovino Ale: cervikovaginální
Závěrečná zpráva. Zkoušení způsobilosti v lékařské mikrobiologii (Externí hodnocení kvality) PT#M/20-2/2017 (č. 997)
 Státní zdravotní ústav Expertní skupina pro zkoušení způsobilosti Poskytovatel programů zkoušení způsobilosti akreditovaný ČIA dle ČSN EN ISO/IEC 17043, reg. č. 7001 Šrobárova 48, 100 42 Praha 10 Vinohrady
Státní zdravotní ústav Expertní skupina pro zkoušení způsobilosti Poskytovatel programů zkoušení způsobilosti akreditovaný ČIA dle ČSN EN ISO/IEC 17043, reg. č. 7001 Šrobárova 48, 100 42 Praha 10 Vinohrady
Jiří Sláma Onkogynekologické centrum VFN a 1. LF UK, Praha. nsc.uzis.cz
 Optimalizace programu screeningu karcinomu děložního hrdla zavedením detekce genomu lidského papilomaviru pomocí samoodběrových sad u žen dlouhodobě se neúčastnících stávajícího screeningu Cervix registrační
Optimalizace programu screeningu karcinomu děložního hrdla zavedením detekce genomu lidského papilomaviru pomocí samoodběrových sad u žen dlouhodobě se neúčastnících stávajícího screeningu Cervix registrační
Závěrečná zpráva. Zkoušení způsobilosti v lékařské mikrobiologii (Externí hodnocení kvality) PT#M/20-2/2016 (č. 952)
 Státní zdravotní ústav Expertní skupina pro zkoušení způsobilosti Poskytovatel programů zkoušení způsobilosti akreditovaný ČIA dle ČSN EN ISO/IEC 17043, reg. č. 7001 Šrobárova 48, 100 42 Praha 10 Vinohrady
Státní zdravotní ústav Expertní skupina pro zkoušení způsobilosti Poskytovatel programů zkoušení způsobilosti akreditovaný ČIA dle ČSN EN ISO/IEC 17043, reg. č. 7001 Šrobárova 48, 100 42 Praha 10 Vinohrady
Indikátory kvality v programu screeningu karcinomu děložního hrdla v ČR
 Indikátory kvality v programu screeningu karcinomu děložního hrdla v ČR analýza screeningových vyšetření do roku 2013 J. Dušková, A. Beková, O. Májek, L. Dušek, V. Dvořák Podíl vzorků s neuspokojivou kvalitou
Indikátory kvality v programu screeningu karcinomu děložního hrdla v ČR analýza screeningových vyšetření do roku 2013 J. Dušková, A. Beková, O. Májek, L. Dušek, V. Dvořák Podíl vzorků s neuspokojivou kvalitou
Laboratorní příručka.
 Kód dokumentu: LP 001 vydání: 04 Počet stran: 14 Rozdělovník Výtisk č. Umístění Odpovědná osoba Podpis 1 Pracovna lékařů Hana Rusová Název dokumentu: www.hvozd.com Autor dokumentu: MUDr. Jiří Vorlíček,
Kód dokumentu: LP 001 vydání: 04 Počet stran: 14 Rozdělovník Výtisk č. Umístění Odpovědná osoba Podpis 1 Pracovna lékařů Hana Rusová Název dokumentu: www.hvozd.com Autor dokumentu: MUDr. Jiří Vorlíček,
1. Indráková Vanda Změna č.1 na listech č. 1, 3, 4,
 Standardizovaný operační postup (SOP) Číslo dokumentu: SOP-522 Vydání: 2. Výtisk: 1. Zpracoval: MUDr. Koudová Monika Název: Ověřil: ODBĚR BIOLOGICKÉHO MATERIÁLU PRO MOLEKULÁRNĚ GENETICKÉ VYŠETŘENÍ: Mgr.
Standardizovaný operační postup (SOP) Číslo dokumentu: SOP-522 Vydání: 2. Výtisk: 1. Zpracoval: MUDr. Koudová Monika Název: Ověřil: ODBĚR BIOLOGICKÉHO MATERIÁLU PRO MOLEKULÁRNĚ GENETICKÉ VYŠETŘENÍ: Mgr.
LABORATORNÍ PŘÍRUČKA
 LABORATORNÍ PŘÍRUČKA A. Úvod A-1 Předmluva Tato laboratorní příručka je základním dokumentem naší laboratoře pro zlepšení komunikace s uživateli našich služeb. Má sloužit jako obecný průvodce pro spolupráci
LABORATORNÍ PŘÍRUČKA A. Úvod A-1 Předmluva Tato laboratorní příručka je základním dokumentem naší laboratoře pro zlepšení komunikace s uživateli našich služeb. Má sloužit jako obecný průvodce pro spolupráci
Laboratorní příručka. www.hvozd.com
 Kód dokumentu: LP 001 vydání: 02 Počet stran: 14 Rozdělovník Výtisk č. Umístění Odpovědná osoba Podpis 1 Pracovna lékařů Hana Rusová Název dokumentu: Laboratorní příručka www.hvozd.com Autor dokumentu:
Kód dokumentu: LP 001 vydání: 02 Počet stran: 14 Rozdělovník Výtisk č. Umístění Odpovědná osoba Podpis 1 Pracovna lékařů Hana Rusová Název dokumentu: Laboratorní příručka www.hvozd.com Autor dokumentu:
Sběr dat a výsledky programu screeningu karcinomu děložního hrdla. RNDr. Ondřej Májek, doc. RNDr. Ladislav Dušek, Ph.D.
 Sběr dat a výsledky programu screeningu karcinomu děložního hrdla RNDr. Ondřej Májek, doc. RNDr. Ladislav Dušek, Ph.D. Struktura informační podpory screeningového programu Zpracovatel dat a poskytovatel
Sběr dat a výsledky programu screeningu karcinomu děložního hrdla RNDr. Ondřej Májek, doc. RNDr. Ladislav Dušek, Ph.D. Struktura informační podpory screeningového programu Zpracovatel dat a poskytovatel
Laboratorní příručka
 Školní 146, Příbram VIII, 26101, tel. 318628219, e-mail cygysro@seznam.cz Laboratorní příručka CYGY s.r.o. Nestátní zdravotnické zařízení IČO 29011043 Gynekologická ordinace primární péče s cytologickou
Školní 146, Příbram VIII, 26101, tel. 318628219, e-mail cygysro@seznam.cz Laboratorní příručka CYGY s.r.o. Nestátní zdravotnické zařízení IČO 29011043 Gynekologická ordinace primární péče s cytologickou
Národní program cervikálního screeningu v České republice
 Národní program cervikálního screeningu v České republice Přehled zaslaných dat k 13.1.2015 Report pro centrum Přerov - DIMOLab s.r.o. IČ: 25860844 Masarykova univerzita, Institut biostatistiky a analýz,
Národní program cervikálního screeningu v České republice Přehled zaslaných dat k 13.1.2015 Report pro centrum Přerov - DIMOLab s.r.o. IČ: 25860844 Masarykova univerzita, Institut biostatistiky a analýz,
Rocheáda v rozhodování aneb testování HPV ve screeningu cervikálního karcinomu 2013
 Rocheáda v rozhodování aneb testování HPV ve screeningu cervikálního karcinomu 2013 Igor Blanárik, Olga Bálková, Roche s.r.o., Diagnostics Division Konference AACL, Praha, 22. března 2013 Detekce HPV a
Rocheáda v rozhodování aneb testování HPV ve screeningu cervikálního karcinomu 2013 Igor Blanárik, Olga Bálková, Roche s.r.o., Diagnostics Division Konference AACL, Praha, 22. března 2013 Detekce HPV a
Laboratorní příručka Patologického oddělení
 Typ dokumentu: Laboratorní příručka Číslo dokumentu: LP Oblast využití: Patologické oddělení Platnost od: 1.10. 2013 Verze č.: 1 Interval revizí: 1 rok Název dokumentu Laboratorní příručka Patologického
Typ dokumentu: Laboratorní příručka Číslo dokumentu: LP Oblast využití: Patologické oddělení Platnost od: 1.10. 2013 Verze č.: 1 Interval revizí: 1 rok Název dokumentu Laboratorní příručka Patologického
KOLOREKTÁLNÍ KARCINOM: VÝZVA PRO ZDRAVÝ ŽIVOTNÍ STYL, SCREENING A ORGANIZACI LÉČEBNÉ PÉČE
 KOLOREKTÁLNÍ KARCINOM: VÝZVA PRO ZDRAVÝ ŽIVOTNÍ STYL, SCREENING A ORGANIZACI LÉČEBNÉ PÉČE Brno, 29. května 2015: Moravská metropole se již počtvrté stává hostitelem mezinárodní konference Evropské dny
KOLOREKTÁLNÍ KARCINOM: VÝZVA PRO ZDRAVÝ ŽIVOTNÍ STYL, SCREENING A ORGANIZACI LÉČEBNÉ PÉČE Brno, 29. května 2015: Moravská metropole se již počtvrté stává hostitelem mezinárodní konference Evropské dny
Závěrečná zpráva. Zkoušení způsobilosti v lékařské mikrobiologii (Externí hodnocení kvality) PT#M/32/2010 (č. 677) Identifikace herpetických virů
 Státní zdravotní ústav Expertní skupina pro zkoušení způsobilosti Organizátor programů zkoušení způsobilosti akreditovaný ČIA, reg. č. 7001 Šrobárova 48, 100 42 Praha 10 Vinohrady Závěrečná zpráva Zkoušení
Státní zdravotní ústav Expertní skupina pro zkoušení způsobilosti Organizátor programů zkoušení způsobilosti akreditovaný ČIA, reg. č. 7001 Šrobárova 48, 100 42 Praha 10 Vinohrady Závěrečná zpráva Zkoušení
Zdravotnické laboratoře. MUDr. Marcela Šimečková
 Zdravotnické laboratoře MUDr. Marcela Šimečková Český institut pro akreditaci o.p.s. 14.2.2006 Obsah sdělení Zásady uvedené v ISO/TR 22869- připravené technickou komisí ISO/TC 212 Procesní uspořádání normy
Zdravotnické laboratoře MUDr. Marcela Šimečková Český institut pro akreditaci o.p.s. 14.2.2006 Obsah sdělení Zásady uvedené v ISO/TR 22869- připravené technickou komisí ISO/TC 212 Procesní uspořádání normy
Laboratorní příručka
 Kód dokumentu: LP 001 Vydání: 4. Počet stran: 14 Datum vydání 22.10.2014 Rozdělovník Výtisk č. Umístění Odpovědná osoba Podpis 1. Vedoucí laboratoře MUDr. Milan Cihlář A. Úvod a obsah A.1 - Úvod Vážení,
Kód dokumentu: LP 001 Vydání: 4. Počet stran: 14 Datum vydání 22.10.2014 Rozdělovník Výtisk č. Umístění Odpovědná osoba Podpis 1. Vedoucí laboratoře MUDr. Milan Cihlář A. Úvod a obsah A.1 - Úvod Vážení,
LABORATORNÍ PŘÍRUČKA. Obsah
 LABORATORNÍ PŘÍRUČKA Obsah LABORATORNÍ PŘÍRUČKA... 1 1 Úvod... 3 2 Informace o laboratoři... 3 2.1 Identifikace laboratoře a důležité údaje... 3 2.2 Základní informace o laboratoři... 4 2.3 Zaměření laboratoře...
LABORATORNÍ PŘÍRUČKA Obsah LABORATORNÍ PŘÍRUČKA... 1 1 Úvod... 3 2 Informace o laboratoři... 3 2.1 Identifikace laboratoře a důležité údaje... 3 2.2 Základní informace o laboratoři... 4 2.3 Zaměření laboratoře...
Laboratorní příručka
 Neřízená dokumentace Laboratorní příručka CYGY s.r.o. Nestátní zdravotnické zařízení IČO 29011043 Cytologická laboratoř Školní 146, 26101 Příbram VIII LP005 Platí od 1.5.2019 Laboratorní příručka - vydání
Neřízená dokumentace Laboratorní příručka CYGY s.r.o. Nestátní zdravotnické zařízení IČO 29011043 Cytologická laboratoř Školní 146, 26101 Příbram VIII LP005 Platí od 1.5.2019 Laboratorní příručka - vydání
Cytologické a histologické vyšetření. Tento výukový materiál vznikl za přispění Evropské unie, státního rozpočtu ČR a Středočeského kraje
 Cytologické a histologické vyšetření Tento výukový materiál vznikl za přispění Evropské unie, státního rozpočtu ČR a Středočeského kraje Duben 2011 Tondrová Irena Bc. CYTOLOGICKÉ A HISTOLOGICKÉ VYŠETŘENÍ
Cytologické a histologické vyšetření Tento výukový materiál vznikl za přispění Evropské unie, státního rozpočtu ČR a Středočeského kraje Duben 2011 Tondrová Irena Bc. CYTOLOGICKÉ A HISTOLOGICKÉ VYŠETŘENÍ
Bioptická vyšetření materiálu z oblasti děložního čípku
 Bioptická vyšetření materiálu z oblasti děložního čípku klinicko-patologický seminář Podřipská nemocnice Roudnice n.labem 16. května 2005 MUDr. Jan Šťastný Diagnoza s.r.o. Progresivní změny na čípku Pseudotumory
Bioptická vyšetření materiálu z oblasti děložního čípku klinicko-patologický seminář Podřipská nemocnice Roudnice n.labem 16. května 2005 MUDr. Jan Šťastný Diagnoza s.r.o. Progresivní změny na čípku Pseudotumory
LABORATORNÍ PŘÍRUČKA
 Laboratorní příručka Strana: 1 LABORATORNÍ PŘÍRUČKA A - Úvod Tato laboratorní příručka má sloužit jako obecný průvodce pro spolupráci snaší laboratoří a jako informativní materiál o poskytovaných službách.
Laboratorní příručka Strana: 1 LABORATORNÍ PŘÍRUČKA A - Úvod Tato laboratorní příručka má sloužit jako obecný průvodce pro spolupráci snaší laboratoří a jako informativní materiál o poskytovaných službách.
Hodnocení adresného zvaní občanů do screeningových programů v ČR
 Datová základna realizace screeningových programů CZ.03.2.63/0.0/0.0/15_039/0007216 Hodnocení adresného zvaní občanů do screeningových programů v ČR Výsledky nad daty do 31.12. 2017 L. Dušek jménem kolektivu
Datová základna realizace screeningových programů CZ.03.2.63/0.0/0.0/15_039/0007216 Hodnocení adresného zvaní občanů do screeningových programů v ČR Výsledky nad daty do 31.12. 2017 L. Dušek jménem kolektivu
Odběry vzorků u pacientů s podezřením na infekci krevního řečiště
 Odběry vzorků u pacientů s podezřením na infekci krevního řečiště Eva Krejčí Centrum klinických laboratoří, Zdravotní ústav se sídlem v Ostravě Lékařská fakulta Ostravské univerzity Infekce krevního řečiště
Odběry vzorků u pacientů s podezřením na infekci krevního řečiště Eva Krejčí Centrum klinických laboratoří, Zdravotní ústav se sídlem v Ostravě Lékařská fakulta Ostravské univerzity Infekce krevního řečiště
VÝUKOVÉ VYUŽITÍ INFORMAČNÍCH SYSTÉMŮ PRO PROGRAMY SCREENINGU ZHOUBNÝCH NÁDORŮ PRSU, TLUSTÉHO STŘEVA A KONEČNÍKU A HRDLA DĚLOŽNÍHO
 VÝUKOVÉ VYUŽITÍ INFORMAČNÍCH SYSTÉMŮ PRO PROGRAMY SCREENINGU ZHOUBNÝCH NÁDORŮ PRSU, TLUSTÉHO STŘEVA A KONEČNÍKU A HRDLA DĚLOŽNÍHO O. Májek, J. Daneš, M. Zavoral, V. Dvořák, D. Klimeš, D. Schwarz, J. Gregor,
VÝUKOVÉ VYUŽITÍ INFORMAČNÍCH SYSTÉMŮ PRO PROGRAMY SCREENINGU ZHOUBNÝCH NÁDORŮ PRSU, TLUSTÉHO STŘEVA A KONEČNÍKU A HRDLA DĚLOŽNÍHO O. Májek, J. Daneš, M. Zavoral, V. Dvořák, D. Klimeš, D. Schwarz, J. Gregor,
Laboratorní příručka HistoCyt s.r.o.
 , Verze: 02 Datum vydání: 19.02.2012 Datum účinnosti: 19.02.2012 Zrušovací ustanovení: nahrazuje verzi 01 ze dne 1.8.2011. Počet stran: 11 Zpracoval Schválil Jméno Marcela Princová MUDr. Ivan Princ Funkce
, Verze: 02 Datum vydání: 19.02.2012 Datum účinnosti: 19.02.2012 Zrušovací ustanovení: nahrazuje verzi 01 ze dne 1.8.2011. Počet stran: 11 Zpracoval Schválil Jméno Marcela Princová MUDr. Ivan Princ Funkce
Odběrový manuál (Výtah z laboratorní příručky) Cytologická a bioptická laboratoř MUDr. Pavla Formánka
 Odběrový manuál (Výtah z laboratorní příručky) Cytologická a bioptická laboratoř MUDr. Pavla Formánka 1 Obsah 1 Obsah...2 2 Úvod...4 3 Informace o laboratoři...4 3.1 Základní informace...4 3.2 Zaměření
Odběrový manuál (Výtah z laboratorní příručky) Cytologická a bioptická laboratoř MUDr. Pavla Formánka 1 Obsah 1 Obsah...2 2 Úvod...4 3 Informace o laboratoři...4 3.1 Základní informace...4 3.2 Zaměření
Odběry biologického materiálu. Markéta Vojtová VOŠZ a SZŠ Hradec Králové
 Odběry biologického materiálu Markéta Vojtová VOŠZ a SZŠ Hradec Králové Vyšetření biologického materiálu 1 Určení správné diagnozy a následné terapie Informace, které doplňují anamnestické údaje, fyzikální
Odběry biologického materiálu Markéta Vojtová VOŠZ a SZŠ Hradec Králové Vyšetření biologického materiálu 1 Určení správné diagnozy a následné terapie Informace, které doplňují anamnestické údaje, fyzikální
LABORATORNÍ PŘÍRUČKA
 Verze:2.1 str. 1 z 11 PROKOPEC COP s.r.o. Laboratoř gynekologické cytologie U Tří lvů 294/4 370 01, České Budějovice IČO 28159632 LABORATORNÍ PŘÍRUČKA Autor: Bc. Štěpán Prokopec, Mgr. Kuralová Schválil:
Verze:2.1 str. 1 z 11 PROKOPEC COP s.r.o. Laboratoř gynekologické cytologie U Tří lvů 294/4 370 01, České Budějovice IČO 28159632 LABORATORNÍ PŘÍRUČKA Autor: Bc. Štěpán Prokopec, Mgr. Kuralová Schválil:
Nové možnosti v diagnostice prekanceróz a karcinomu děložního hrdla Jiří Sláma
 Nové možnosti v diagnostice prekanceróz a karcinomu děložního hrdla Jiří Sláma Onkogynekologické centrum Gynekologicko porodnická klinika VFN a 1. LF UK Praha Případ ze studie ATHENA 44 let 1987 2002 roční
Nové možnosti v diagnostice prekanceróz a karcinomu děložního hrdla Jiří Sláma Onkogynekologické centrum Gynekologicko porodnická klinika VFN a 1. LF UK Praha Případ ze studie ATHENA 44 let 1987 2002 roční
P 02 Laboratorní příručka
 P02 Laboratorní příručka Výtisk číslo: 1 Vydání: 3 Počet stran: 15 P 02 Laboratorní příručka Platnost končí dne 31. 12. 2013 Zpracoval Schválil Jméno MVDr. Dag Rejthar Marta Křížová Podpis Datum 14.10.2011
P02 Laboratorní příručka Výtisk číslo: 1 Vydání: 3 Počet stran: 15 P 02 Laboratorní příručka Platnost končí dne 31. 12. 2013 Zpracoval Schválil Jméno MVDr. Dag Rejthar Marta Křížová Podpis Datum 14.10.2011
Preventivní programy v onkologii. Prof. MUDr. Jan Žaloudík, CSc. Masarykův onkologický ústav Brno
 Preventivní programy v onkologii Prof. MUDr. Jan Žaloudík, CSc. Masarykův onkologický ústav Brno mediální obraz onkologie dnes.. skutečné pojištění.. onkologie zítra snad prevence, časný záchyt, cena /přínos
Preventivní programy v onkologii Prof. MUDr. Jan Žaloudík, CSc. Masarykův onkologický ústav Brno mediální obraz onkologie dnes.. skutečné pojištění.. onkologie zítra snad prevence, časný záchyt, cena /přínos
Konečná zpráva hodnocení různých způsobů přípravy vzorků pro AMPLICOR HPV test firmy Roche
 Konečná zpráva hodnocení různých způsobů přípravy vzorků pro AMPLICOR HPV test firmy Roche Charakteristika testu: Set AMPLICOR HPV vyráběný firmou Roche je určený pro detekci vysoko-rizikových typů lidských
Konečná zpráva hodnocení různých způsobů přípravy vzorků pro AMPLICOR HPV test firmy Roche Charakteristika testu: Set AMPLICOR HPV vyráběný firmou Roche je určený pro detekci vysoko-rizikových typů lidských
Laboratorní příručka Cytologická laboratoř Porodnicko-gynekologické kliniky FNO
 Fakultní nemocnice Ostrava 17. listopadu 1790, 708 52 Ostrava-Poruba Cytologická laboratoř Porodnicko-gynekologické kliniky FNO Evid. značka: Identifikace: Identifikace výtisku: Rozdělovník: Nahrazuje:
Fakultní nemocnice Ostrava 17. listopadu 1790, 708 52 Ostrava-Poruba Cytologická laboratoř Porodnicko-gynekologické kliniky FNO Evid. značka: Identifikace: Identifikace výtisku: Rozdělovník: Nahrazuje:
Závěrečná zpráva. PT#M/7/2019 (č. 1061) Sérologie CMV. Zkoušení způsobilosti v lékařské mikrobiologii (Externí hodnocení kvality)
 Státní zdravotní ústav Expertní skupina pro zkoušení způsobilosti Poskytovatel zkoušení způsobilosti akreditovaný ČIA podle ČSN EN ISO/IEC 17043, reg. č. 7001 Šrobárova 48, 100 42 Praha 10 Vinohrady Závěrečná
Státní zdravotní ústav Expertní skupina pro zkoušení způsobilosti Poskytovatel zkoušení způsobilosti akreditovaný ČIA podle ČSN EN ISO/IEC 17043, reg. č. 7001 Šrobárova 48, 100 42 Praha 10 Vinohrady Závěrečná
LABORATORNÍ PŘÍRUČKA
 LABORATORNÍ PŘÍRUČKA Laboratoř MDgK- plus Stránka 1 z 9 OBSAH: 1. ÚVOD....3 2. INFORMACE O LABORATOŘI 3 2.1. Základní informace o laboratoři...3 2.2. Zaměření laboratoře a spektrum nabízených služeb...
LABORATORNÍ PŘÍRUČKA Laboratoř MDgK- plus Stránka 1 z 9 OBSAH: 1. ÚVOD....3 2. INFORMACE O LABORATOŘI 3 2.1. Základní informace o laboratoři...3 2.2. Zaměření laboratoře a spektrum nabízených služeb...
MUDr.M.Doleželová 23/10/2010 1
 23/10/2010 1 Historie a představení společnosti Orion Diagnostica Oy je společností náležící k Orion Group, jedné z předních finských společností zabývajících se péčí o zdraví. Orion Diagnostica Oy byla
23/10/2010 1 Historie a představení společnosti Orion Diagnostica Oy je společností náležící k Orion Group, jedné z předních finských společností zabývajících se péčí o zdraví. Orion Diagnostica Oy byla
SMĚRNICE ÚSTAVU. Tabulka provedených revizí a změn. Laboratorní příručka Vydání 1. Změna:0 Datum změny: Ústav patologie
 Fakultní nemocnic e Královské Vinohrady, Šrobárova 50, Praha 10 Ústav patologie SMĚRNICE ÚSTAVU Číslo : LP-86500-01/2011 Platnost směrnice: od 15.4.2011 ročně Počet příloh: Interval revizí: schválení Místo
Fakultní nemocnic e Královské Vinohrady, Šrobárova 50, Praha 10 Ústav patologie SMĚRNICE ÚSTAVU Číslo : LP-86500-01/2011 Platnost směrnice: od 15.4.2011 ročně Počet příloh: Interval revizí: schválení Místo
VYROCNI ZPRAVA 2014. Centrum onkologické prevence pro ženy, s.r.o. Cyto l og i cká l aboratoř. Za období 1. ledna 31. prosince 2014. 1 z 8.
 Centrum onko l og i cké prevence pro ženy, s. r. o. Cyto l og i cká l aboratoř Hrus i cká 2538, Praha 4 VYROCNI ZPRAVA 2014 Centrum onkologické prevence pro ženy, s.r.o. Za období 1. ledna 31. prosince
Centrum onko l og i cké prevence pro ženy, s. r. o. Cyto l og i cká l aboratoř Hrus i cká 2538, Praha 4 VYROCNI ZPRAVA 2014 Centrum onkologické prevence pro ženy, s.r.o. Za období 1. ledna 31. prosince
Příloha č.5 Seznam PCR vyšetření
 Příloha č.5 Seznam PCR vyšetření Obsah Virus hepatitidy B - kvalitativní průkaz... 2 Virus hepatitidy B - kvantita... 2 Virus hepatitidy C kvalitativní průkaz... 3 Virus hepatitidy C - kvantita... 3 Virus
Příloha č.5 Seznam PCR vyšetření Obsah Virus hepatitidy B - kvalitativní průkaz... 2 Virus hepatitidy B - kvantita... 2 Virus hepatitidy C kvalitativní průkaz... 3 Virus hepatitidy C - kvantita... 3 Virus
PATOLOGICKO ANATOMICKÉ ODDĚLENÍ LABORATORNÍ PŘÍRUČKA
 PATOLOGICKO ANATOMICKÉ ODDĚLENÍ LABORATORNÍ PŘÍRUČKA Verze č. 4 Vlastník procesu: Patologicko-anatomické oddělení Účinnost od: 6. 6. 2016 Jméno Funkce Datum Podpis Zpracoval: MUDr. Barbora Studená Manažerka
PATOLOGICKO ANATOMICKÉ ODDĚLENÍ LABORATORNÍ PŘÍRUČKA Verze č. 4 Vlastník procesu: Patologicko-anatomické oddělení Účinnost od: 6. 6. 2016 Jméno Funkce Datum Podpis Zpracoval: MUDr. Barbora Studená Manažerka
LABORATORNÍ PŘÍRUČKA
 LABORATORNÍ PŘÍRUČKA A. Úvod A-1 Předmluva Tato laboratorní příručka je základním dokumentem naší laboratoře pro zlepšení komunikace s uživateli našich služeb. Má sloužit jako obecný průvodce pro spolupráci
LABORATORNÍ PŘÍRUČKA A. Úvod A-1 Předmluva Tato laboratorní příručka je základním dokumentem naší laboratoře pro zlepšení komunikace s uživateli našich služeb. Má sloužit jako obecný průvodce pro spolupráci
Pokyny pro pacienty. Seznam pokynů pro pacienty
 Pokyny pro pacienty (dle Příručky kvality OKBH MNMK) Seznam pokynů pro pacienty Pokyny: příprava před odběrem žilní krve Pokyny: odběr vzorku moče na vyšetření močového sedimentu Pokyny: pro 24 hod. sběr
Pokyny pro pacienty (dle Příručky kvality OKBH MNMK) Seznam pokynů pro pacienty Pokyny: příprava před odběrem žilní krve Pokyny: odběr vzorku moče na vyšetření močového sedimentu Pokyny: pro 24 hod. sběr
LABORATORNÍ PŘÍRUČKA
 ONMB, a.s., nemocnice Středočeského kraje Dokument LP 01 Kopie č. 1/1 Strana 1/24 Úsek: PAO Cytologie Určení: lékaři, zdravotní laboranti, zdravotní sestry Vypracoval: Bc. Nikol Kávová Datum: 21.6.2012
ONMB, a.s., nemocnice Středočeského kraje Dokument LP 01 Kopie č. 1/1 Strana 1/24 Úsek: PAO Cytologie Určení: lékaři, zdravotní laboranti, zdravotní sestry Vypracoval: Bc. Nikol Kávová Datum: 21.6.2012
Hyperkeratóza ve stěrech z děložního hrdla - definice a její význam. Iva Kinkorová Luňáčková
 Hyperkeratóza ve stěrech z děložního hrdla - definice a její význam Iva Kinkorová Luňáčková XXV. Cytologický den, 11.10.2017 Definice hyperkeratóza je ochranná proliferační odpověď dlaždicového epitelu,
Hyperkeratóza ve stěrech z děložního hrdla - definice a její význam Iva Kinkorová Luňáčková XXV. Cytologický den, 11.10.2017 Definice hyperkeratóza je ochranná proliferační odpověď dlaždicového epitelu,
Jak probíhá testování?
 Jak probíhá testování? 1 1. Výběr koní Koně jsou k testování vybráni jednou z následujících metod: výběr umístěných koní (tj. medailové pozice; v soutěži družstev vždy alespoň jeden soutěžící z umístěného
Jak probíhá testování? 1 1. Výběr koní Koně jsou k testování vybráni jednou z následujících metod: výběr umístěných koní (tj. medailové pozice; v soutěži družstev vždy alespoň jeden soutěžící z umístěného
Laboratorní příručka laboratoří oddělení patologie
 Druh a číslo dokumentu: Pokyn oddělení Nemocnice s poliklinikou Purkyňova 1849, 470 77 Vydání: 1 Verze: 1 Platnost od: Celkový počet stran: 17 Název dokumentu: Rozdělovník Verze Umístění Odpovědná osoba
Druh a číslo dokumentu: Pokyn oddělení Nemocnice s poliklinikou Purkyňova 1849, 470 77 Vydání: 1 Verze: 1 Platnost od: Celkový počet stran: 17 Název dokumentu: Rozdělovník Verze Umístění Odpovědná osoba
Závěrečná zpráva. Zkoušení způsobilosti v lékařské mikrobiologii (Externí hodnocení kvality) PT#M/20-2/2018 (č. 1043)
 Státní zdravotní ústav Expertní skupina pro zkoušení způsobilosti Poskytovatel programů zkoušení způsobilosti akreditovaný ČIA dle ČSN EN ISO/IEC 17043, reg. č. 7001 Šrobárova 48, 100 42 Praha 10 Vinohrady
Státní zdravotní ústav Expertní skupina pro zkoušení způsobilosti Poskytovatel programů zkoušení způsobilosti akreditovaný ČIA dle ČSN EN ISO/IEC 17043, reg. č. 7001 Šrobárova 48, 100 42 Praha 10 Vinohrady
Laboratorní příručka Cytologické laboratoře
 CGOP, s.r.o. Cytologická laboratoř Praha 2, Vocelova 603/5, PSČ 120 00 Autor laboratorní příručky: MUDr. Alena Beková, M.I.A.C. Vedoucí cytologické laboratoře Podpis: Laboratorní příručku kontroloval:
CGOP, s.r.o. Cytologická laboratoř Praha 2, Vocelova 603/5, PSČ 120 00 Autor laboratorní příručky: MUDr. Alena Beková, M.I.A.C. Vedoucí cytologické laboratoře Podpis: Laboratorní příručku kontroloval:
Systém podpory prevence vybraných nádorových onemocnění v ČR screeningové programy
 Příloha č. 4 - Vzorové dopisy a) Přední strana Zde vedle loga MZ Vážený pane, muž varianta 1 (50-70 let; bez K) neabsolvoval toto pro Vaše zdraví důležité preventivní vyšetření: V České republice každoročně
Příloha č. 4 - Vzorové dopisy a) Přední strana Zde vedle loga MZ Vážený pane, muž varianta 1 (50-70 let; bez K) neabsolvoval toto pro Vaše zdraví důležité preventivní vyšetření: V České republice každoročně
Cytologické vyšetření
 Cytologie Cytologické vyšetření mikroskopické vyšetření jednotlivých buněk rozetřených na podložním skle - chybí kontinuita vyšetřované tkáně v histologickém řezu Materiál a způsoby odběru tekutý materiál
Cytologie Cytologické vyšetření mikroskopické vyšetření jednotlivých buněk rozetřených na podložním skle - chybí kontinuita vyšetřované tkáně v histologickém řezu Materiál a způsoby odběru tekutý materiál
Evropské asociace proti rakovině děložního čípku
 Evropské asociace proti rakovině děložního čípku Založena 2002, řízena představenstvem 125 institucí ze 34 zemí Cíl: šířit informace o karcinomu hrdla děložního a možnostech prevence tohoto onemocnění
Evropské asociace proti rakovině děložního čípku Založena 2002, řízena představenstvem 125 institucí ze 34 zemí Cíl: šířit informace o karcinomu hrdla děložního a možnostech prevence tohoto onemocnění
dokument: LP : 2016/06
 G Pokyny a instrukce G 1 Pokyny a instrukce pro lékaře G 1.1 Pokyny pro vyšetření orálního glukózového tolerančního testu (ogtt) Úvodní informace Diagnostika diabetes mellitus (DM) a porušené glukózové
G Pokyny a instrukce G 1 Pokyny a instrukce pro lékaře G 1.1 Pokyny pro vyšetření orálního glukózového tolerančního testu (ogtt) Úvodní informace Diagnostika diabetes mellitus (DM) a porušené glukózové
Laboratorní příručka Cytologické laboratoře
 CGOP, s.r.o. Praha 2, Vocelova 603/5, PSČ 120 00 Autor laboratorní příručky: MUDr. Alena Beková, M.I.A.C. Vedoucí cytologické laboratoře Podpis: Laboratorní příručku kontroloval: Mgr. Lucie Panýrová Manažer
CGOP, s.r.o. Praha 2, Vocelova 603/5, PSČ 120 00 Autor laboratorní příručky: MUDr. Alena Beková, M.I.A.C. Vedoucí cytologické laboratoře Podpis: Laboratorní příručku kontroloval: Mgr. Lucie Panýrová Manažer
Organizace a výsledky zdravotních screeningových programů v ČR
 Centrum pro rozvoj technologické platformy registrů Národního zdravotnického informačního systému, modernizace vytěžování jejich obsahu a rozšíření jejich informační kapacity. CZ.03.4.74/0.0/0.0/15_019/0002748
Centrum pro rozvoj technologické platformy registrů Národního zdravotnického informačního systému, modernizace vytěžování jejich obsahu a rozšíření jejich informační kapacity. CZ.03.4.74/0.0/0.0/15_019/0002748
LABORATORNÍ PŘÍRUČKA
 DOKUMENTACE QMS PK 02 Laboratorní příručka Typ dokumentace: Interní Verze: 02 Autor (jméno, datum, podpis): MUDr. Jan Šťastný, vedoucí laboratoře Eva Závorková, vedoucí laborantka Schválil (jméno, datum,
DOKUMENTACE QMS PK 02 Laboratorní příručka Typ dokumentace: Interní Verze: 02 Autor (jméno, datum, podpis): MUDr. Jan Šťastný, vedoucí laboratoře Eva Závorková, vedoucí laborantka Schválil (jméno, datum,
Ceník služeb GYNEKO spol. s r.o. Ceník služeb nehrazených zdravotní pojišťovnou. Dokument Jméno Datum Podpis Vypracoval: Jitka Kaňáková 18. 10.
 Ceník služeb nehrazených zdravotní pojišťovnou Dokument Jméno Datum Podpis Vypracoval: Jitka Kaňáková 18. 10. 2012 Kontroloval: Schválil: Miloslava Dümlerová MUDr. Tomáš Malík Rozdělovník Jméno Datum Podpis
Ceník služeb nehrazených zdravotní pojišťovnou Dokument Jméno Datum Podpis Vypracoval: Jitka Kaňáková 18. 10. 2012 Kontroloval: Schválil: Miloslava Dümlerová MUDr. Tomáš Malík Rozdělovník Jméno Datum Podpis
Laboratorní příručka. Oddělení Patologické anatomie. Nemocnice s poliklinikou. Nový Jičín 1.11.2011. Verze 01
 Laboratorní příručka Oddělení Patologické anatomie Nemocnice s poliklinikou Nový Jičín 1.11.2011 Verze 01 1 A. Úvod A-1 Předmluva Vážené kolegyně, vážení kolegové, Předkládáme Vám nabídku našich služeb,
Laboratorní příručka Oddělení Patologické anatomie Nemocnice s poliklinikou Nový Jičín 1.11.2011 Verze 01 1 A. Úvod A-1 Předmluva Vážené kolegyně, vážení kolegové, Předkládáme Vám nabídku našich služeb,
Laboratorní příručka
 Strana: 1/19 Evidenční číslo výtisku: 1 Interval revizí: 1 rok Platí od: 6.1.2015 Nahrazuje: Laboratorní příručku, verze 1 s platností od 4.3.2013 do 6.1.2015 Zpracoval Přezkoumal Schválil Jméno MUDr.
Strana: 1/19 Evidenční číslo výtisku: 1 Interval revizí: 1 rok Platí od: 6.1.2015 Nahrazuje: Laboratorní příručku, verze 1 s platností od 4.3.2013 do 6.1.2015 Zpracoval Přezkoumal Schválil Jméno MUDr.
Závěrečná zpráva. PT#M/11/2017 (č. 965) Identifikace respiračních virů. Zkoušení způsobilosti v lékařské mikrobiologii (Externí hodnocení kvality)
 Státní zdravotní ústav Expertní skupina pro zkoušení způsobilosti Poskytovatel programů zkoušení způsobilosti akreditovaný ČIA podle ČSN EN ISO/IEC 17043 reg. č. 7001 Šrobárova 48, 100 42 Praha 10 Vinohrady
Státní zdravotní ústav Expertní skupina pro zkoušení způsobilosti Poskytovatel programů zkoušení způsobilosti akreditovaný ČIA podle ČSN EN ISO/IEC 17043 reg. č. 7001 Šrobárova 48, 100 42 Praha 10 Vinohrady
Systém podpory prevence vybraných nádorových onemocnění v ČR screeningové programy
 toto pro Vaše zdraví důležité preventivní vyšetření: vyšetření zaměřené na včasný záchyt zhoubného nádoru děložního čípku. V České republice každoročně onemocní zhoubným nádorem děložního čípku přibližně
toto pro Vaše zdraví důležité preventivní vyšetření: vyšetření zaměřené na včasný záchyt zhoubného nádoru děložního čípku. V České republice každoročně onemocní zhoubným nádorem děložního čípku přibližně
Závěrečná zpráva. PT#M/24/2018 (č.1025) Sérologie Helicobacter pylori. Zkoušení způsobilosti v lékařské mikrobiologii (Externí hodnocení kvality)
 Státní zdravotní ústav Expertní skupina pro zkoušení způsobilosti Poskytovatel zkoušení způsobilosti akreditovaný ČI podle ČSN EN ISO/IE 17043, reg. č. 7001 Šrobárova 48, 100 42 Praha 10 Vinohrady Závěrečná
Státní zdravotní ústav Expertní skupina pro zkoušení způsobilosti Poskytovatel zkoušení způsobilosti akreditovaný ČI podle ČSN EN ISO/IE 17043, reg. č. 7001 Šrobárova 48, 100 42 Praha 10 Vinohrady Závěrečná
Laboratorní příručka
 Cytologická laboratoř MUDr. Milan Dušek Výtisk číslo: 1 Vydání: 3 Počet stran: 8 Laboratorní příručka Nabývá účinnosti dne 1. 7. 2014 Toto vydání nahrazuje vydání 2. z 1. 8. 2011 a nabývá účinnosti dne
Cytologická laboratoř MUDr. Milan Dušek Výtisk číslo: 1 Vydání: 3 Počet stran: 8 Laboratorní příručka Nabývá účinnosti dne 1. 7. 2014 Toto vydání nahrazuje vydání 2. z 1. 8. 2011 a nabývá účinnosti dne
LABORATORNÍ PŘÍRUČKA
 LABORATORNÍ PŘÍRUČKA A. ÚVOD A-1 ÚVODNÍ SLOVO Tato laboratorní příručka je základním dokumentem naší laboratoře pro zlepšení komunikace s uživateli našich služeb. Má sloužit jako obecný průvodce pro spolupráci
LABORATORNÍ PŘÍRUČKA A. ÚVOD A-1 ÚVODNÍ SLOVO Tato laboratorní příručka je základním dokumentem naší laboratoře pro zlepšení komunikace s uživateli našich služeb. Má sloužit jako obecný průvodce pro spolupráci
LABORATORNÍ PŘÍRUČKA Verze: 2.6 Kód: LP COPCB Počet stran: 10
 Verze:2.6 Neřízená kopie str. 1 z 10 PROKOPEC COP s.r.o. Laboratoř gynekologické cytologie U Tří lvů 294/4 370 01, České Budějovice IČO 28159632 LABORATORNÍ PŘÍRUČKA Verze: 2.6 Kód: LP COPCB 2015-02-01
Verze:2.6 Neřízená kopie str. 1 z 10 PROKOPEC COP s.r.o. Laboratoř gynekologické cytologie U Tří lvů 294/4 370 01, České Budějovice IČO 28159632 LABORATORNÍ PŘÍRUČKA Verze: 2.6 Kód: LP COPCB 2015-02-01
Oficiální výsledky Národního programu mamografického screeningu v roce 2011
 Oficiální výsledky Národního programu mamografického screeningu v roce 2011 Jan Daneš, Helena Bartoňková, Miroslava Skovajsová Analýza dat: Ondřej Májek, Daniel Klimeš, Ladislav Dušek Úvod V České republice
Oficiální výsledky Národního programu mamografického screeningu v roce 2011 Jan Daneš, Helena Bartoňková, Miroslava Skovajsová Analýza dat: Ondřej Májek, Daniel Klimeš, Ladislav Dušek Úvod V České republice
Hodnocení adresného zvaní občanů do onkologických screeningových programů ČR
 Hodnocení adresného zvaní občanů do onkologických screeningových programů ČR Vypracoval Institut biostatistiky a analýz, Lékařská a Přírodovědecká fakulta, Masarykova univerzita, Brno. Ve spolupráci s
Hodnocení adresného zvaní občanů do onkologických screeningových programů ČR Vypracoval Institut biostatistiky a analýz, Lékařská a Přírodovědecká fakulta, Masarykova univerzita, Brno. Ve spolupráci s
DIAGNOSTIKA A MONITOROVÁNÍ INFEKCÍ ZPŮSOBENÉ LIDSKÝMI PAPILLOMAVIRY VYSOCE RIZIKOVÉHO TYPU POMOCÍ REAL TIME PCR
 DIAGNOSTIKA A MONITOROVÁNÍ INFEKCÍ ZPŮSOBENÉ LIDSKÝMI PAPILLOMAVIRY VYSOCE RIZIKOVÉHO TYPU POMOCÍ REAL TIME PCR Michaela Kavanová, DiS. tel.: +420 221 985 476 mobil: +420 725 004 523 e-mail: michaela.kavanova@synlab.cz
DIAGNOSTIKA A MONITOROVÁNÍ INFEKCÍ ZPŮSOBENÉ LIDSKÝMI PAPILLOMAVIRY VYSOCE RIZIKOVÉHO TYPU POMOCÍ REAL TIME PCR Michaela Kavanová, DiS. tel.: +420 221 985 476 mobil: +420 725 004 523 e-mail: michaela.kavanova@synlab.cz
Odběr, zpracování a uchování klinických vzorků
 Obecně Výsledky laboratorních testů, zejména RT-PCR závisí na druhu klinického materiálu, odběru, uchování a transportu. Nejpodrobnější informace o přítomnosti infekčního agens poskytne analýza klinického
Obecně Výsledky laboratorních testů, zejména RT-PCR závisí na druhu klinického materiálu, odběru, uchování a transportu. Nejpodrobnější informace o přítomnosti infekčního agens poskytne analýza klinického
Screening pro prevenci karcinomu hrdla děložního v 21. století
 Screening pro prevenci karcinomu hrdla děložního v 21. století Ruth Tachezy ÚHKT,, NRL pro PV www.papillomavirus papillomavirus.cz Od objevu po průkaz etiologické souvislosti 1983 izolován prvníhpv z karcinomu
Screening pro prevenci karcinomu hrdla děložního v 21. století Ruth Tachezy ÚHKT,, NRL pro PV www.papillomavirus papillomavirus.cz Od objevu po průkaz etiologické souvislosti 1983 izolován prvníhpv z karcinomu
Mikroskopie versus kultivace, kdy, komu a proč? Jan Kestřánek PGK, FNHK
 Mikroskopie versus kultivace, kdy, komu a proč? Jan Kestřánek PGK, FNHK Vulvovaginální dyskomfort Akutní vulvovaginální dyskomfort (AVD): obtíže v oblasti zevního genitálu a pochvy jako je výtok, svědění
Mikroskopie versus kultivace, kdy, komu a proč? Jan Kestřánek PGK, FNHK Vulvovaginální dyskomfort Akutní vulvovaginální dyskomfort (AVD): obtíže v oblasti zevního genitálu a pochvy jako je výtok, svědění
Kontakt Telefon: 485 313 020 Služba : 485 313 033 ATB : 485 313 029
 Klinický materiál odeslaný do laboratoře je zpracován dle standardních postupů (SOP) a vyšetření je kódováno dle sazebníku zdravotnických. O dalším vyšetřovacím postupu rozhoduje lékař se specializovanou
Klinický materiál odeslaný do laboratoře je zpracován dle standardních postupů (SOP) a vyšetření je kódováno dle sazebníku zdravotnických. O dalším vyšetřovacím postupu rozhoduje lékař se specializovanou
PŘÍPRAVA ZDRAVOTNICKÝCH PROSTŘEDKŮ KE STERILIZACI
 Identifikační číslo Oblast působnosti a druh Verze 04 SOP_CHN_0009_4 l. Dodatky 0 Revize dokumentu ll. Ročně lll. SOP Přílohy Úsek platnosti lll. PŘÍPRAVA ZDRAVOTNICKÝCH PROSTŘEDKŮ KE STERILIZACI Jméno
Identifikační číslo Oblast působnosti a druh Verze 04 SOP_CHN_0009_4 l. Dodatky 0 Revize dokumentu ll. Ročně lll. SOP Přílohy Úsek platnosti lll. PŘÍPRAVA ZDRAVOTNICKÝCH PROSTŘEDKŮ KE STERILIZACI Jméno
LABORATORNÍ PŘÍRUČKA
 DOKUMENTACE QMS PK 02 Laboratorní příručka Typ dokumentace: Verze: 03 Autor (jméno, datum, podpis): Schválil (jméno, datum, podpis): Interní MUDr. Jan Šťastný, vedoucí laboratoře Lenka Vithová, vedoucí
DOKUMENTACE QMS PK 02 Laboratorní příručka Typ dokumentace: Verze: 03 Autor (jméno, datum, podpis): Schválil (jméno, datum, podpis): Interní MUDr. Jan Šťastný, vedoucí laboratoře Lenka Vithová, vedoucí
Závěrečná zpráva. PT#M/9-2/2016 (č.945) Sérologie lymeské borreliózy. Zkoušení způsobilosti v lékařské mikrobiologii (Externí hodnocení kvality)
 Státní zdravotní ústav Expertní skupina pro zkoušení způsobilosti Poskytovatel programů zkoušení způsobilosti akreditovaný ČIA podle ČSN EN ISO/IEC 17043, reg č 7001 Šrobárova 48, 100 42 Praha 10 Vinohrady
Státní zdravotní ústav Expertní skupina pro zkoušení způsobilosti Poskytovatel programů zkoušení způsobilosti akreditovaný ČIA podle ČSN EN ISO/IEC 17043, reg č 7001 Šrobárova 48, 100 42 Praha 10 Vinohrady
Závěrečná zpráva. Zkoušení způsobilosti v lékařské mikrobiologii (Externí hodnocení kvality)
 Státní zdravotní ústav Expertní skupina pro zkoušení způsobilosti Poskytovatel programů zkoušení způsobilosti akreditovaný ČIA podle ČSN EN ISO/IEC 17043, reg. č. 7001 Šrobárova 48, 100 42 Praha 10 Vinohrady
Státní zdravotní ústav Expertní skupina pro zkoušení způsobilosti Poskytovatel programů zkoušení způsobilosti akreditovaný ČIA podle ČSN EN ISO/IEC 17043, reg. č. 7001 Šrobárova 48, 100 42 Praha 10 Vinohrady
Preanalytická fáze na rozhraní mezi klinickým
 Preanalytická fáze na rozhraní mezi klinickým oddělením a laboratoří Sedlák T., Plačková M., Stýborová I., Bunešová M. ÚKBP UK 2. LF a FN Motol, Praha 30. 5. 1. 6. 2010 BIOLAB 2010 Hradec Králové Spolehlivý
Preanalytická fáze na rozhraní mezi klinickým oddělením a laboratoří Sedlák T., Plačková M., Stýborová I., Bunešová M. ÚKBP UK 2. LF a FN Motol, Praha 30. 5. 1. 6. 2010 BIOLAB 2010 Hradec Králové Spolehlivý
KLINICKÁ HODNOCENÍ S LPMT POŽADAVKY NA VSTUPNÍ MATERIÁL LIDSKÉ TKÁNĚ A BUŇKY
 Požadavky na vstupní materiál lidské tkáně a buňky 1 KLINICKÁ HODNOCENÍ S LPMT POŽADAVKY NA VSTUPNÍ MATERIÁL LIDSKÉ TKÁNĚ A BUŇKY MUDr. Ivana Koblihová Inspektor lidských tkání a buněk Požadavky na vstupní
Požadavky na vstupní materiál lidské tkáně a buňky 1 KLINICKÁ HODNOCENÍ S LPMT POŽADAVKY NA VSTUPNÍ MATERIÁL LIDSKÉ TKÁNĚ A BUŇKY MUDr. Ivana Koblihová Inspektor lidských tkání a buněk Požadavky na vstupní
Závěrečná zpráva. Zkoušení způsobilosti v lékařské mikrobiologii (Externí hodnocení kvality)
 Státní zdravotní ústav Expertní skupina pro zkoušení způsobilosti Poskytovatel programů zkoušení způsobilosti akreditovaný ČIA podle ČSN EN ISO/IEC 17043, reg. č. 7001 Šrobárova 48, 100 42 Praha 10 Vinohrady
Státní zdravotní ústav Expertní skupina pro zkoušení způsobilosti Poskytovatel programů zkoušení způsobilosti akreditovaný ČIA podle ČSN EN ISO/IEC 17043, reg. č. 7001 Šrobárova 48, 100 42 Praha 10 Vinohrady
Laboratorní příručka
 Kód dokumentu: Bioptická a cytologická LP Vydání: 2 Počet stran: 15 Datum vydání: 3.4.2013 Revize LP Datum revize Jméno a podpis Datum revize Jméno a podpis Zpracoval: MUDr. Pavla Vysoudilová Manažer kvality
Kód dokumentu: Bioptická a cytologická LP Vydání: 2 Počet stran: 15 Datum vydání: 3.4.2013 Revize LP Datum revize Jméno a podpis Datum revize Jméno a podpis Zpracoval: MUDr. Pavla Vysoudilová Manažer kvality
LABORATORNÍ PŘÍRUČKA
 LABORATORNÍ PŘÍRUČKA A. Úvod A-1 Předmluva Tato laboratorní příručka je základním dokumentem naší laboratoře pro zlepšení komunikace s uživateli našich služeb. Má sloužit jako obecný průvodce pro spolupráci
LABORATORNÍ PŘÍRUČKA A. Úvod A-1 Předmluva Tato laboratorní příručka je základním dokumentem naší laboratoře pro zlepšení komunikace s uživateli našich služeb. Má sloužit jako obecný průvodce pro spolupráci
