-agonists mirabegron.
|
|
|
- Karel Beran
- před 8 lety
- Počet zobrazení:
Transkript
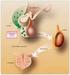
1 MUDr. Michaela Matoušková Urocentrum Praha Souhrn Matoušková M.. Remedia 2013; 23: Více než 400 milionů obyvatel planety trpí symptomy hyperaktivního močového měchýře (OAB overactive bladder). V léčbě hyperaktivního močového měchýře jsou farmakologickou léčbou volby antimuskarinové látky, v České republice v první linii neretardované lékové formy, ve druhé linii dlouhodobě působící léčivé přípravky a jejich kombinace s léky první linie. Limitující pro terapii jsou především jejich nežádoucí účinky, které vedou k relativně nízké compliance pacientů. U části pacientů však není dosaženo dostatečného efektu i přes jejich dobrou spolupráci. Se zcela odlišným mechanismem účinku se nově setkáváme u mirabegronu, který je selektivním agonistou -adrenoreceptorů. byl vyvinut pro léčbu hyperaktivního močového měchýře. Celosvětově bylo do randomizovaných studií s mirabegronem zařazeno více než pacientů. v dávce 50 mg vedl k významnému zmírnění symptomů hyperaktivního močového měchýře (snížení počtu epizod inkontinence a počtu mikcí) ve srovnání s placebem, ale i ve srovnání s retardovanou formou močového spasmolytika (tolterodinem). Zmírnění symptomů vede ke zlepšení kvality života. Nežádoucí účinky jsou srovnatelné s podáním placeba. tak představuje novou terapeutickou možnost v léčbě hyperaktivního močového měchýře s dobrou účinností a snášenlivostí. Klíčová slova: hyperaktivní močový měchýř močová spasmolytika -mimetika mirabegron. Summary Matouskova M.. Remedia 2013; 23: More than 400 million people worldwide suffer from symptoms of overactive bladder (OAB). Antimuscarinic agents represent the pharmacological treatment of choice in OAB. In the Czech Republic, first line treatment involves non-sustained formulations and second line treatment consists of long-acting drugs and their combination with first-line drugs. Treatment limiting factors mainly include the undesirable effects of these drugs, which lead to relatively low patient compliance. However, some patients fail to achieve a sufficient effect despite their good cooperation., a selective -adrenergic receptor agonist, thus represents a drug with a completely different mechanism of action. has been developed precisely for the treatment of overactive bladder. Worldwide, randomized trials with mirabegron have involved more than patients. 50 mg resulted in a significant alleviation of the symptoms of overactive bladder (reducing the number of incontinence episodes and the frequency of micturition) compared with placebo, but also compared with a sustained form of urinary antispasmodic (tolterodine). Alleviation of symptoms improves quality of life. The side effects are similar to placebo. represents a new therapeutic option in the treatment of overactive bladder with good efficacy and tolerability. Key words: overactive bladder urinary antispasmodics -agonists mirabegron. Farmakologická skupina patří mezi urologika, močová spasmolytika, ATC kód: G04BD12. Je první molekulou, která ovlivňuje detruzor (hladkou svalovinu močového měchýře) cestou agonismu -adrenergních receptorů. Chemický strukturní a sumární vzorec mirabegronu uvádí obr. 1. Mechanismus účinku, farmakodynamika je selektivní agonista - -adrenoreceptorů. Aktivací -adrenoreceptorů v dochází prostřednictvím enzymu adenylátcyklázy ke zvýšení koncentrace cyklického adenosin monofosfátu (camp) a k následnému uvolnění. Výsledkem je zlepšení plnicí funkce močového měchýře (obr. 2). má nízkou aktivitu vůči dalším dvěma adrenoreceptorům β 1 a β 2, stejně tak i vůči ostatním receptorům (např. α 1A, a transportéry NA/DA). V lidském močovém měchýři jsou vysoce (až z 97 %) exprimovány právě -adrenoreceptory (obr. 3) [1]. Na zvířecím modelu byl prokázán relaxační účinek a snížení frekvence močení. Po podání mirabegronu se zvýšil mikční objem a snížila se frekvence kontrakcí bez mikce, neměl však vliv na mikční tlak a objem reziduální moče. V průběhu plnicí fáze převládá stimulace sympatických nervů. Noradrenalin se uvolňuje z nervových zakončení, tím dochází k aktivaci β-adrenoreceptorů ve svalovině močového měchýře a k jejímu následnému uvolnění. Během mikční fáze je močový měchýř ovládán převážně parasympatickou nervovou soustavou. Acetylcholin uvolněný z pánevních nervových zakončení stimuluje cholinergní receptory a M 3, tím navozuje kontrakci močového měchýře. Aktivace dráhy navíc inhibuje vzestup hladiny camp, vyvolaný prostřednictvím -adrenoreceptorů. Aktivace -adrenoreceptorů proto nezasahuje do mikčního procesu (obr. 4). C 21 H 24 N 4 O 2 S m. h. 396,506 Obr. 1 Chemický strukturní vzorec mirabegronu. 253
2 -adrenoreceptor mirabegron camp zvyšuje relaxaci aktivace -adrenoreceptoru mirabegronem detruzor Metabolismus Biotransfomace mirabegronu probíhá více cestami dealkylací, oxidací, glukuronidací a amidovou hydrolýzou. je hlavní cirkulující složkou po podání jediné dávky 14 C-mirabegronu. V plazmě jsou detekovatelné dva hlavní metabolity glukuronidy fáze 2, které představují 16 % a 11 % celkové expozice. Oba jsou farmakologicky neaktivní. neinhibuje metabolismus současně podávaných léčiv, která jsou metabolizována enzymy cytochromu P450. Omezenou úlohu v eliminaci mají CYP2D6 a CYP3A4 při oxidačním metabolismu. Kromě CYP3A4 a CYP2D6 jsou do metabolismu zapojeny butyrylcholinesteráza, uridin difosfo-glukuronosyltransferáza (UGT) a pravděpodobně i alkoholdehydrogenáza (ADH). Obr. 2 Mechanismus účinku mirabegronu. Selektivní agonista mirabegron aktivuje -adrenoreceptory v močovém měchýři, čímž dochází ke zvýšení koncentrace camp. Vlivem camp nastává relaxace hladké svaloviny močového měchýře. camp cyklický adenosin monofosfát; detruzor hladká svalovina močového měchýře Farmakokinetické vlastnosti Základní farmakokinetické parametry mirabegronu jsou shrnuty v tab. 1. Absorpce Po podání per os dosahuje mirabegron maximální plazmatické koncentrace (c max ) za 3 4 hodiny. Absolutní biologická dostupnost je 35 % při dávce 50 mg. Průměrná hodnota c max a AUC se zvyšuje více než dávka, proporcionálně v celém rozpětí dávkování. V celkové populaci mužů a žen vedlo dvojnásobné zvýšení dávky z 50 mg na 100 mg mirabegronu ke zvýšení hodnoty c max přibližně 2,9násobně a AUC tau 2,6násobně, zatímco čtyřnásobné zvýšení dávky z 50 mg na 200 mg mirabegronu zvýšilo hodnoty c max přibližně 8,4krát a AUC tau 6,5krát. Ustálených koncentrací je dosaženo do 7 dnů při dávkování mirabegronu jednou denně. Při pravidelném denním podávání je plazmatická koncentrace léčiva v ustáleném stavu přibližně dvojnásobná oproti podání jediné dávky. Současné podání tablety o dávce 50 mg spolu s jídlem s vysokým obsahem tuku snížilo c max mirabegronu o 45 % a AUC o 17 %. Potrava s nízkým obsahem tuku snížila c max mirabegronu o 75 % a AUC o 51 %. je možné užívat v doporučené dávce spolu s jídlem nebo nezávisle na jídle. Distribuce je rozsáhle distribuován v organismu. Distribuční objem v ustáleném stavu (Vss) je přibližně 1670 l. Přibližně v 71 % se váže na proteiny lidské plazmy. Vykazuje středně vysokou afinitu k albuminu a α 1 -kyselému glykoproteinu. proniká do červených krvinek a koncentrace 14 C-mirabegronu in vitro byla v erytrocytech dvojnásobná oproti plazmě. extracelulární část intracelulární část Exkrece Celková tělesná clearance (CL tot ) z plazmy je přibližně 57 l/h. Terminální eliminační poločas (t 1/2 ) je přibližně 50 hodin. Renální clearance (CL R ) představuje přibližně 13 l/h, to odpovídá téměř 25 % hodnoty CL tot. Renální eliminace mirabegronu probíhá primárně prostřednictvím aktivní tubulární sekrece spolu s glomerulární filtrací. Vylučování nezměněného mirabegronu močí závisí na dávce a pohybuje se přibližně od 6,0 % po denní dávce 25 mg až do 12,2 % po denní dávce 100 mg. Po podání 160 mg 14 C-mirabegronu zdravým dobrovolníkům bylo přibližně 55 % radionuklidu získáno zpět v moči a 34 % ve stolici. Nezměněný mirabegron odpovídal za 45 % radioaktivity moči, což ukazuje na přítomnost metabolitů. Nezměněný mirabegron odpovídal za většinu radioaktivity ve stolici. místo důležité pro aktivitu receptoru a pro interakci s ligandy NH 2 S-S COOH buněčná membrána Obr. 3 Struktura lidského -adrenoreceptoru; volně podle [17] Yasuhiko, et al.,
3 detruzor Závislost na věku a pohlaví Hodnoty c max a AUC mirabegronu a jeho metabolitů po opakovaném podání perorální dávky u starších dobrovolníků ( 65 let) byly podobné jako u mladších (18 45 let). Hodnoty c max a AUC jsou přibližně o 40 % až 50 % vyšší u žen než u mužů. Rozdíly mezi pohlavími v hodnotách c max a AUC jsou připisovány rozdílům v tělesné hmotnosti a v biologické dostupnosti. Klinické zkušenosti Na studie fáze II (BLOSSOM [2] a DRAGON [3]) navázaly studie fáze III. Účinnost a bezpečnost byla ověřena ve 41 klinických studiích s více než 10 tisíci pacienty se symptomy dolních močových cest, kteří se účastnili studií fáze I, II a III; 622 z nich užívalo mirabegron déle než jeden rok. Studie fáze III 178-CL-046, 178-CL a 178-CL-074 byly 12týdenní, studie 178-CL-049 byla roční. Všechny probíhaly v Evropě, Severní Americe a Austrálii. Studie 046 je komparátorem kontrolovaná studie [4], v níž mirabegron v dávce 50 mg výrazně snížil frekvenci močení (ve srovnání s placebem, p < 0,05) a tolterodin ve standardní dávce (4 mg) nebyl v tomto cílovém ukazateli signifikantně účinnější než placebo. 50 mg dále významně (p < 0,05) zvýšil objem vymočené moči během jednoho M 3 Ach M 3 M3 M2 M 3 M 3 kontrakce M2 Ach snížení relaxace vymočení a signifikantně (p < 0,05) snížil počet epizod inkontinence. Studie 047 [5, 6] rovněž dokládá signifikantní snížení počtu epizod inkontinence za 24 hodin (-1,47 mirabegron vs. -1,13 placebo; p < 0,05) a výrazné snížení frekvence močení během 24 hodin (-1,66 mirabegron vs. -1,05 placebo; p < 0,05). v dávce 50 mg dále statisticky významně zvýšil objem vymočené moči (18,2 ml mirabegron vs. 7,0 ml placebo; p < 0,05). Studie 074 [7] sledovala podání mirabegronu v dávce 25 nebo 50 mg vs. placebo. v dávce 25 mg i 50 mg signifikantně snížil počet epizod inkontinence za 24 hodin (-1,36 mirabegron 25 mg, -1,38 mirabegron 50 mg vs. -0,96 placebo; p < 0,05) a výrazně snížil frekvenci močení za 24 hodin (-1,65 mirabegron 25 mg, -1,60 mirabegron 50 mg vs. -1,18 placebo; p < 0,05), což byly předem definované primární cílové ukazatele této studie. v dávce 50 mg pak dále statisticky významně zvýšil objem vymočené moči (20,7 ml mirabegron 50 mg, 12,8 ml mirabegron 25 mg vs. 8,3 ml placebo; p < 0,05 pro 50 mg). Navíc mirabegron 50 mg zlepšil kvalitu života pacientů s OAB měřenou pomocí vizuální analogové škály TS-VAS (+1,88 mirabegron vs. +1,05 placebo; p < 0,001) nebo pomocí specifického dotazníku OAB-q (obtěžování symptomy OAB výraznější snížení ve prospěch mirabegronu -18,8 vs. -16,0 placebo; p = 0,028). Studie 049 [8], mezinárodní, multicentrická, dvojitě zaslepená, randomizovaná studie s paralelními skupinami, kontrolovaná aktivním komparátorem, dlouhodobě sledovala bezpečnost léčby mirabegronem. Celkový bezpečnostní profil mirabegronu byl velmi dobrý a srovnatelný s placebem a s výsledky zaznamenanými v ostatních kratších studiích fáze III. navíc znamenal 3 4krát nižší výskyt sucha v ústech (nejtypičtější a nejčastější nežádoucí účinek antimuskarinik) ve srovnání s tolterodinem. 50 mg si zachovával účinnost na všechny symptomy OAB po celou dobu sledování srovnatelnou s výsledky časově kratších studií fáze III. Metaanalýza tří studií fáze III s 4611 pacienty [9] dokládá lepší, odlišný bezpečnostní profil léčby a nižší výskyt: sucha v ústech ve srovnání s tolterodinem (1,7 % vs. 10,1 %) a s ostatními antimuskariniky (29,6 %); Tab. 1 ZÁKLADNÍ FARMAKOKINETICKÉ PARAMETRY MIRABEGRONU absorpce NA β3 β3 relaxace Obr. 4 Ovlivnění močového měchýře prostřednictvím receptorů, M 3 a. Ach acetylcholin; NA noradrenalin; detruzor hladká svalovina močového měchýře biologická dostupnost F (%) maximální plazmatická koncentrace C max po jednorázové dávce 50 mg (ng/ml) čas dosažení maximální plazmatické koncentrace t max (h) vazba na plazmatické proteiny metabolismus indukce hepatálních enzymů eliminační poločas t 1/2 (h) 50 podle [16] SPC Betmiga, hod., na dávce závislá 35 (při dávce 50 mg) 41,6 3 4 ano, 71 %, středně vysoká afinita k albuminu a α 1 -kyselému glykoproteinu více cest: dealkylace, oxidace, glukuronidace, amidová hydrolýza ne 255
4 lepší ostatní terapie tolterodin ER 4 mg fesoterodin 4 mg fesoterodin 8 mg oxybutynin ER 10 mg oxybutynin ER 15 mg oxybutynin ER 5 mg oxybutynin IR 10 mg oxybutynin IR 15 mg oxybutynin IR 9 mg placebo solifenacin 10 mg solifenacin 5 mg tolterodin IR 4 mg trospium 60 mg trospium 40 mg 1, Graf 1 Relativní riziko sucha v ústech při užívání antimuskarinika a nebo placeba versus léčba mirabegronem 50 mg; podle [10] Maman, et al., Čím dále v pravé části grafu se uvedená hodnota nachází, tím více je z hlediska daného nežádoucího účinku lepší mirabegron 50 mg ve srovnání s danou terapií. IR immediate release, okamžité uvolňování; ER extended release, prodloužené uvolňování pruritu ve srovnání s tolterodinem (0,2 % vs. 1,4 %) a s ostatními antimuskariniky (15,4 %); retence moči ve srovnání s tolterodinem (0,1 % vs. 0,6 %) a s ostatními antimuskariniky (1,1 %). Nepřímé srovnání na základě Network meta-analysis s dostupnými antimuskariniky (Mixed Treatment Comparison; MTC) bylo provedeno s celkem 40 studiemi ( pacientů). Grafy 1 a 2 srovnávají výskyt sucha v ústech a obstipace u pacientů léčených antimuskariniky, mirabegronem či placebem [10]. Zařazení do současné palety léčiv Farmakologickou léčbou volby nemocných s příznaky OAB je podání močových spasmolytik. V první linii léčby jsou neretardované lékové formy (s okamžitým uvolňováním léčiva) oxybutynin, propiverin, trospium, tolterodin. Možné je i v první linii podání tricyklických antidepresiv; lze využít jejich kombinovaného účinku (centrální a periferní anticholinergní efekt, blokáda aktivity transportního systému na presynaptické membráně vychytávající zpětně noradrenalin a serotonin) a také centrálního sedativního účinku imipramin. Možné je podání inhibitorů fosfodiesterázy 5. typu (PDI5) tadalafil, sildenafil. Pokud se nedostaví požadovaný efekt léčby nebo pacient léčbu netoleruje pro výskyt nežádoucích účinků, volí urolog lepší mirabegron 50 mg 4,168 4,436 9,700 6,795 7,864 4,130 14,069 10,778 10,078 4,229 7,042 5,672 4,481 39,208 nebo urogynekolog léčivé přípravky s prodlouženým uvolňováním účinných látek zařazených do druhé linie léčby tolterodin, solifenacin, darifenacin, fesoterodin, oxybutynin v transdermální náplasti. V léčbě bývají k dotitrování účinku kombinovány léčivé přípravky 1. a 2. linie. lepší ostatní terapie tolterodin ER 4 mg fesoterodin 4 mg fesoterodin 8 mg oxybutynin ER 10 mg oxybutynin ER 15 mg oxybutynin ER 5 mg oxybutynin IR 15 mg oxybutynin IR 9 mg placebo solifenacin 10 mg solifenacin 5 mg tolterodin IR 4 mg trospium 40 mg trospium 60 mg Po selhání 2. linie léčby část pacientů rezignuje a své obtíže [11, 12] řeší pouze preskripcí a používáním hygienických pomůcek. Po selhání veškerých možností farmakoterapie přichází na řadu chirurgická léčba, např. aplikace botulotoxinu do sliznice močového měchýře a různé augmentace močového měchýře (náhrada střevem nebo žaludkem). Na podkladě podrobné analýzy III. fáze studie 046 u selektované skupiny pacientů s předcházející léčbou antimuskariniky, kteří přerušili terapii buď pro nedostatečnou snášenlivost nebo nedostačující účinek, zaznamenala přibližně polovina pacientů přínos z léčby mirabegronem (graf 3). Předchozí terapie zahrnovala tolterodin, solifenacin, oxybutynin, trospium, darifenacin, propiverin, fesoterodin [13]. Zdá se tedy, že máme k dispozici přípravek, který za dobré snášenlivosti může být využit při selhání 2. linie léčby hyperaktivního močového měchýře, eventuálně v kombinaci s předcházející terapií. Zkoušeny jsou i další přípravky ve skupině, např. solabegron [14]. Indikace je indikován k symptomatické léčbě urgence, zvýšené frekvence močení a/nebo urgentní inkontinence, jež se mohou vyskytnout u dospělých pacientů se syndromem hyperaktivního močového měchýře (OAB). Dávkování Doporučená dávka pro dospělé pacienty je 50 mg mirabegronu jednou denně, s jídlem nebo nezávisle na jídle. lepší mirabegron 50 mg 1,109 1,066 1,926 1,021 2,158 2,459 1,614 0,989 0,732 4,369 2,501 1,034 1,692 7, Graf 2 Relativní riziko zácpy při užívání antimuskarinika a nebo placeba versus léčba mirabegronem 50 mg; podle [10] Maman, et al., Čím dále v pravé části grafu se uvedená hodnota nachází, tím více je z hlediska daného nežádoucího účinku lepší mirabegron 50 mg ve srovnání s danou terapií. IR immediate release, okamžité uvolňování; ER extended release, prodloužené uvolňování 256
5 průměrná změna od výchozí hodnoty 0-0,5-1,0-1,5-2,0 placebo mirabegron 50 mg tolterodin SR 4 mg epizody inkontinence za 24 hod. -1,17-1,57 * -1,27 NS Graf 3 Průměrná změna v epizodách inkontinence a počtu mikcí za jeden den ve srovnání s počátkem terapie u pacientů dříve léčených antimuskariniky; podle [13] Khullar, et al., NS není statisticky významný rozdíl v porovnání s placebem; *statisticky významné zlepšení v porovnání s placebem; jako aktivní kontrola byl použit tolterodin SR 4 mg Insuficience ledvin a jater Jediná dávka mirabegronu 100 mg podaná u dobrovolníků s mírnou insuficiencí ledvin zvýšila c max o 6 %, se střední insuficiencí ledvin o 23 % a se závažnou insuficiencí o 92 %. nebyl studován u pacientů v terminálním stadiu onemocnění ledvin (GFR < 15 ml/min/1,73 m 2 či u pacientů na hemodialýze) nebo se závažným poškozením jater (Childovo-Pughovo skóre C), a proto se jeho používání u těchto skupin pacientů nedoporučuje. Hypertenze nebyl hodnocen u pacientů s těžkou neléčenou hypertenzí (systolický TK 180 mm Hg a/nebo diastolický TK 110 mm Hg). Jeho používání se u této populace pacientů nedoporučuje. U pacientů s hypertenzí 2. stupně (systolický TK 160 mm Hg a/nebo diastolický TK 100 mm Hg) je k dispozici omezené množství údajů. Pacienti s vrozeným nebo získaným prodloužením intervalu QT Při používání mirabegronu v terapeutických dávkách nebylo v klinických studiích prokázáno klinicky relevantní prodloužení intervalu QT. Vzhledem k tomu, že pacienti se známou anamnézou prodloužení intervalu QT nebo pacienti, kteří užívají léky, o kterých je známo, že prodlužují interval QT, nebyli do těchto studií zařazeni, není účinek mirabegronu u těchto pacientů znám. Při podávání mirabegronu těmto pacientům je třeba dbát zvýšené opatrnosti. Těhotenství O používání mirabegronu u těhotných žen je k dispozici omezené množství údajů. průměrná změna od výchozí hodnoty 0-0,5-1,0-1,5-2,0 počet mikcí za 24 hod. -1,34-1,93 * -1,59 NS Studie na zvířatech prokázaly reprodukční toxicitu. se nedoporučuje podávat těhotným ženám a ženám, které mohou otěhotnět a nepoužívají antikoncepci. Kojení se vylučuje do mléka hlodavců, a proto se předpokládá, že bude přítomný v lidském mateřském mléce. Nebyly provedeny žádné studie, které by posoudily vliv mirabegronu na tvorbu mléka u lidí, jeho přítomnost v lidském mateřském mléce nebo jeho účinky na kojené dítě. Ve farmakokinetických pokusech na potkanech dochází přibližně k 1,7násobnému zvýšení koncentrace mirabegronu nebo jeho metabolitů v mateřském mléce. Během kojení by mirabegron neměl být podáván. Fertilita Nebyly zjištěny žádné s léčbou související účinky mirabegronu na fertilitu zvířat. Vliv mirabegronu na lidskou fertilitu nebyl stanoven. Ovlivnění pozornosti nemá žádný nebo má zanedbatelný vliv na schopnost řídit nebo obsluhovat stroje. Kontraindikace Kontraindikací léčby mirabegronem je hypersenzitivita na léčivou látku nebo na kteroukoli pomocnou látku. nemá kontraindikace obdobné skupině antimuskarinik. Nežádoucí účinky Bezpečnost mirabegronu byla hodnocena u 8433 pacientů s OAB. Z nich 5648 dostalo nejméně jednu dávku mirabegronu ve fázích II a III klinického zkoušení, 622 pacientů dostávalo mirabegron nejméně jeden rok (365 dní). Ve třech 12týdenních dvojitě zaslepených studiích fáze III kontrolovaných placebem dokončilo léčbu mirabegronem 88 % pacientů. Pro nežádoucí účinky přerušila léčbu 4 % pacientů. Většina nežádoucích účinků byla mírné až střední závažnosti. Nejčastějšími nežádoucími účinky hlášenými u pacientů léčených mirabegronem 50 mg jsou tachykardie a infekce močových cest. Tachykardie se vyskytla u 1,2 % pacientů, k přerušení léčby vedla tachykardie u 0,1 % pacientů. Frekvence infekcí močových cest byla 2,9 %, u žádného z pacientů nebyla důvodem k přerušení léčby. Nežádoucí účinky pozorované v průběhu jednoroční studie s aktivním komparátorem (tolterodinem) byly typem a závažností obdobné s kontrolovanými studiemi fáze III. Lékové interakce je transportován a metabolizován více cestami. je substrátem cytochromu P450 (CYP) 3A4, CYP2D6, butyrylcholinesterázy, uridin difosfo-glukuronosyltransferázy (UGT), efluxního transportéru P-glykoproteinu (P-gp) a influxních organických kationových transportérů (OCT) OCT1, OCT2 a OCT3. Studie mirabegronu využívající lidské jaterní mikrozomy a rekombinantní lidské CYP enzymy ukázaly, že mirabegron je mírný a časově závislý inhibitor CYP2D6 a slabý inhibitor CYP3A [15]. při vysokých koncentracích inhiboval transport léku zprostředkovaný P-gp. Účinek mirabegronu na transportéry je slabý inhibitor P-gp. U zdravých dobrovolníků mirabegron zvýšil u substrátu P-gp digoxinu c max o 29 % a AUC o 27 %. Pacientům, kteří začínají užívat kombinaci mirabegronu a digoxinu, by měla být zpočátku předepsána nejnižší dávka digoxinu. K získání požadovaného klinického účinku je třeba monitorovat sérové koncentrace digoxinu a použít je pro titraci dávky digoxinu. Při kombinaci mirabegronu se substráty citlivými k P-gp, jako je např. dabigatran, by měl být zvažován potenciál pro inhibici substrátu P-gp mirabegronem. Jiné interakce Nebyly zjištěny žádné klinicky významné interakce při současném podávání mirabegronu s terapeutickými dávkami solifenacinu, tamsulosinu, warfarinu, metforminu nebo v kombinaci s perorálně podávanými kontraceptivy obsahujícími ethinylestradiol a levonorgestrel. Žádná úprava dávkování se nedoporučuje. 258
6 Literatura [1] Astellas Pharma Global Development, Inc (APGD). Advisory Committee Briefing Document. (YM178) for the Treatment of Overactive Bladder. April 5, Available at: fda.gov/downloads/advisorycommittees/committeesmeetingmaterials/drugs/reproductive- HealthDrugsAdvisoryCommittee/UCM pdf [2] Chapple CR, Yamaguchi O, Ridder A, et al. Clinical proof of concept study (BLOSSOM) shows novel adrenoceptor agonist YM178 is effective and well tolerated in the treatment of symptoms of overactive bladder. Poster presented at the European Association of Urology Annual Meeting Poster 674. [3] Chapple CR, JJ Wyndaele JJ, van Kerrebroeck P, et al. Dose-ranging study of once-daily mirabegron (YM178), a novel selective -adrenoceptor agonist, in patients with overactive bladder (OAB). Poster presented at the European Association of Urology Annual Meeting Poster 774. [4] Khullar V, Amarenco G, Angulo JC, et al. Efficacy and tolerability of mirabegron, a -adrenoceptor agonist, in patients with overactive bladder: Results from a randomised European-Australian Phase 3 trial (SCORPIO). Eur Urol 2013; 63: [5] Nitti V, Herschorn S, Auerbach S, et al. The efficacy and safety of mirabegron in patients with overactive bladder syndrome results from a North-American Phase III trial. Poster presented at the European Association of Urology Annual Meeting Poster 885. [6] Nitti VW, Auerbach S, Martin N, et al. Results of a Randomized Phase III Trial of in Patients with Overactive Bladder. J Urol 2012; Oct 16. pii: S (12) doi: /j. juro [7] van Kerrebroeck P, Barkin J, Castro-Diaz D, et al. Randomised, Double-blind, Placebo-controlled Phase III Study to Assess the Efficacy and Safety of 25 mg and 50 mg Once-daily in Overactive Bladder (OAB). 42nd Annual Meeting of the International Continence Society, October 15-19, 2012, Beijing, China. Abstract Search on Congress-Webpage: Abstracts/AbstractsSearch.aspx? EventID=134. Download-date: 2012/08/21 (2012), p. Abstr [8] Chapple CR, Kaplan SA, Mitcheson D, et al. Randomized, double-blind, active-controlled phase 3 study to assess 12-month safety and efficacy of mirabegron, a -adrenoceptor agonist, in overactive bladder. Eur Urol 2013; 63: [9] Nitti V, Chapple CR, Amarenco G, et al. The incidence of antimuscarinic-associated side effects in overactive bladder (OAB) patients treated with mirabegron: Results of a pooled analysis of 3 randomised phase 3 trials. 28th Annual Congress of the European Association of Urology, March 15-19, 2013, Milan, Italy. Congress-Website: - download-date: 2013/02/19 (2013), p. Abstr [10] Maman K, Aballea S, Nazir J, et al. Comparative efficacy and safety of treatments for the management of overactive bladder: A systematic literature review and mixed treatment comparison. Value in Health 16: A180, Abstr. PUK1 (2013). [11] Linnér L, Schioler H, Samuelsson E, et al. Low persistence of anticholinergic drug use in Sweden. Eur J Clin Pharmacol 2011; 67: [12] Wagg A, Compion G, Fahey A, Siddiqui E. Persistence with prescribed antimuscarinic therapy for overactive bladder: a UK experience. BJU Int 2012; 110: doi: /j X x. Epub 2012 Mar 12. [13] Khullar V, et al. Efficacy of mirabegron in patients with and without prior antimuscarinic therapy for overactive bladder (OAB): Post-hoc analysis of a prospective, randomised European-Australian phase III trial. European Urology Supplements 2012; 11: e684. [14] Ohlstein EH, von Keitz A, Michel MC. A multicenter, doubleblind, randomized, placebo-controlled trial of the -adrenoceptor agonist solabegron for overactive bladder. Eur Urol 2012; 62: [15] Tyagi P, Tyagi V., a -adrenoceptor agonist for the potential treatment of urinary frequency, urinary incontinence or urgency associated with overactive bladder. Drugs 2010; 13: [16] Betmiga: Summary of product characteristics (SPC) available at docs/cs_cz/document_library/epar_-_product_ Information/human/002388/WC pdf [17] Yasuhiko I, Naoki A, Yukio H. Beta3-Adrenoceptor Agonists: Possible Role in the Treatment of Overactive Bladder. Korean J Urol 2010; 51:
Vesicare 5 mg potahované tablety
 Sp. zn. sukls74933/2013 SOUHR ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Vesicare 5 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Vesicare 5 mg, potahované tablety: Jedna tableta obsahuje 5 mg
Sp. zn. sukls74933/2013 SOUHR ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Vesicare 5 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Vesicare 5 mg, potahované tablety: Jedna tableta obsahuje 5 mg
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakákoli podezření
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakákoli podezření
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Belsanor 5 mg potahované tablety Belsanor 10 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Belsanor 5 mg potahované tablety: Jedna tableta obsahuje
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Belsanor 5 mg potahované tablety Belsanor 10 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Belsanor 5 mg potahované tablety: Jedna tableta obsahuje
Pomocná látka se známým účinkem: Jedna tableta obsahuje 75 mg monohydrátu laktosy. Úplný seznam pomocných látek viz bod 6.1.
 sp.zn.: sukls81995/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Loratadin-ratiopharm 10 mg Tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje loratadinum 10 mg. Pomocná látka se
sp.zn.: sukls81995/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Loratadin-ratiopharm 10 mg Tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje loratadinum 10 mg. Pomocná látka se
STÁTNÍ ÚSTAV PRO KONTROLU LÉČIV Šrobárova 48, 100 41 PRAHA 10 tel.: 272 185 111, fax.: 271 732 377, e-mail: posta@sukl.cz
 STÁTNÍ ÚSTAV PRO KONTROLU LÉČIV Šrobárova 48, 100 41 PRAHA 10 tel.: 272 185 111, fax.: 271 732 377, e-mail: posta@sukl.cz SUKLS21047/2010 V souladu s ustanovením 39o zákona č. 48/1997 Sb., o veřejném zdravotním
STÁTNÍ ÚSTAV PRO KONTROLU LÉČIV Šrobárova 48, 100 41 PRAHA 10 tel.: 272 185 111, fax.: 271 732 377, e-mail: posta@sukl.cz SUKLS21047/2010 V souladu s ustanovením 39o zákona č. 48/1997 Sb., o veřejném zdravotním
Jedna tableta s prodlouženým uvolňováním obsahuje 0,4 mg tamsulosini hydrochloridum, což odpovídá 0,367 mg tamsulosinum.
 sp.zn.sukls48957/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Tamsulosin HCl Teva 0,4 mg tablety s prodlouženým uvolňováním 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta s prodlouženým uvolňováním
sp.zn.sukls48957/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Tamsulosin HCl Teva 0,4 mg tablety s prodlouženým uvolňováním 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta s prodlouženým uvolňováním
mirabegron profily léčiv MUDr. Viktor Vik; MUDr. Tomáš Doležal, Ph.D.* Úvod Mechanismus účinku a farmakodynamické vlastnosti
 mirabegron MUDr. Viktor Vik; MUDr. Tomáš Doležal, Ph.D.* Urologické oddělení, Thomayerova nemocnice, Praha; *Institut pro zdravotní ekonomiku a technology assessment (iheta) a Farmakologický ústav 2. LF
mirabegron MUDr. Viktor Vik; MUDr. Tomáš Doležal, Ph.D.* Urologické oddělení, Thomayerova nemocnice, Praha; *Institut pro zdravotní ekonomiku a technology assessment (iheta) a Farmakologický ústav 2. LF
PŘÍLOHA III ÚPRAVY SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE. Tyto změny k SPC a příbalové informace jsou platné v den Rozhodnutí Komise
 PŘÍLOHA III ÚPRAVY SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE Tyto změny k SPC a příbalové informace jsou platné v den Rozhodnutí Komise Po Rozhodnutí Komise aktualizuje národní kompetentní autorita
PŘÍLOHA III ÚPRAVY SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE Tyto změny k SPC a příbalové informace jsou platné v den Rozhodnutí Komise Po Rozhodnutí Komise aktualizuje národní kompetentní autorita
Děti a mladiství Pro podávání přípravku Urorec u dětí a mladistvých neexistuje žádná relevantní indikace.
 1. NÁZEV PŘÍPRAVKU Urorec 4 mg tvrdé tobolky 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tvrdá tobolka obsahuje 4 mg silodosinum. Úplný seznam pomocných látek viz bod 6.1. 3. LÉKOVÁ FORMA Tvrdá tobolka.
1. NÁZEV PŘÍPRAVKU Urorec 4 mg tvrdé tobolky 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tvrdá tobolka obsahuje 4 mg silodosinum. Úplný seznam pomocných látek viz bod 6.1. 3. LÉKOVÁ FORMA Tvrdá tobolka.
SOUHRN ÚDAJŮ O PŘÍPRAVKU. Jedna tvrdá tobolka s prodlouženým uvolňováním obsahuje tolterodini hydrogenotartras 4 mg (odpovídá tolterodinum 2,74 mg).
 1. NÁZEV PŘÍPRAVKU DETRUSITOL SR 4 mg tvrdé tobolky s prodlouženým uvolňováním SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tvrdá tobolka s prodlouženým uvolňováním obsahuje tolterodini
1. NÁZEV PŘÍPRAVKU DETRUSITOL SR 4 mg tvrdé tobolky s prodlouženým uvolňováním SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tvrdá tobolka s prodlouženým uvolňováním obsahuje tolterodini
Desloratadin STADA 5 mg jsou modré, kulaté, bikonvexní potahované tablety o průměru přibližně 6,5 mm.
 Sp.zn.sukls74932/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Desloratadin STADA 5 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna potahovaná tableta obsahuje desloratadinum 5 mg.
Sp.zn.sukls74932/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Desloratadin STADA 5 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna potahovaná tableta obsahuje desloratadinum 5 mg.
Bezpečnost a účinnost přípravku Neoclarityn 5 mg potahované tablety u dětí mladších 12 let nebyla dosud stanovena. Nejsou dostupné žádné údaje.
 1. NÁZEV PŘÍPRAVKU Neoclarityn 5 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje desloratadinum 5 mg. Pomocná látka se známým účinkem: Tento přípravek obsahuje laktózu.
1. NÁZEV PŘÍPRAVKU Neoclarityn 5 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje desloratadinum 5 mg. Pomocná látka se známým účinkem: Tento přípravek obsahuje laktózu.
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 sp.zn.sukls63588/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Claritine 10 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje loratadinum 10 mg. Pomocná látka se známým účinkem:
sp.zn.sukls63588/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Claritine 10 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje loratadinum 10 mg. Pomocná látka se známým účinkem:
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Desloratadin +pharma 5 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje desloratadinum v množství 5 mg. Úplný seznam pomocných
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Desloratadin +pharma 5 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje desloratadinum v množství 5 mg. Úplný seznam pomocných
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakákoli podezření
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakákoli podezření
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Emselex 7,5 mg, tablety s prodlouženým uvolňováním 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje 7,5 mg darifenacinum (jako hydrobromid)
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Emselex 7,5 mg, tablety s prodlouženým uvolňováním 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje 7,5 mg darifenacinum (jako hydrobromid)
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Urorec 4 mg tvrdé tobolky 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tvrdá tobolka obsahuje silodosinum 4 mg. Úplný seznam pomocných látek viz
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Urorec 4 mg tvrdé tobolky 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tvrdá tobolka obsahuje silodosinum 4 mg. Úplný seznam pomocných látek viz
Světle červené, ploché, kulaté, skvrnité tablety, na jedné straně označené písmenem K.
 1. NÁZEV PŘÍPRAVKU Aerius 2,5 mg tablety dispergovatelné v ústech 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta dispergovatelná v ústech obsahuje desloratadinum 2,5 mg. Pomocné látky se známým
1. NÁZEV PŘÍPRAVKU Aerius 2,5 mg tablety dispergovatelné v ústech 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta dispergovatelná v ústech obsahuje desloratadinum 2,5 mg. Pomocné látky se známým
SOUHRN ÚDAJŮ O PŘÍPRAVKU. Jedna tableta obsahuje 10 mg loratadinum. Jedna 10 mg tableta loratadinu obsahuje 71,3 mg monohydrátu laktosy.
 sp.zn. sukls138016/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU CLARITINE Tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje 10 mg loratadinum. Jedna 10 mg tableta loratadinu obsahuje
sp.zn. sukls138016/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU CLARITINE Tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje 10 mg loratadinum. Jedna 10 mg tableta loratadinu obsahuje
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 sp.zn.sukls40560/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Claritine 1mg/ml sirup 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden ml sirupu obsahuje loratadinum 1 mg. Pomocná látka se známým účinkem:
sp.zn.sukls40560/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Claritine 1mg/ml sirup 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden ml sirupu obsahuje loratadinum 1 mg. Pomocná látka se známým účinkem:
FARMAKOKINETIKA PODÁNÍ LÉČIVA (JEDNORÁZOVÉ, OPAKOVANÉ) Pavel Jeřábek
 FARMAKOKINETIKA PODÁNÍ LÉČIVA (JEDNORÁZOVÉ, OPAKOVANÉ) Pavel Jeřábek METABOLIZACE ZPŮSOBY APLIKACE Sublingvální nitroglycerin ph ionizace, lipofilita, ochrana před prvním průchodem játry, rychlá resorpce
FARMAKOKINETIKA PODÁNÍ LÉČIVA (JEDNORÁZOVÉ, OPAKOVANÉ) Pavel Jeřábek METABOLIZACE ZPŮSOBY APLIKACE Sublingvální nitroglycerin ph ionizace, lipofilita, ochrana před prvním průchodem játry, rychlá resorpce
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Resolor 1 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna potahovaná tableta obsahuje 1 mg prucalopridum (ve formě prucalopridi
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Resolor 1 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna potahovaná tableta obsahuje 1 mg prucalopridum (ve formě prucalopridi
Obecné aspekty lékových interakcí
 Obecné aspekty lékových interakcí výskyt, rozdělení, hlavní mechanismy a důsledky lékových interakcí PharmDr. Josef Suchopár 18. 6. 2014 Lékové interakce: skutečný problém nebo fáma? Velká Británie (Pirmohamed,
Obecné aspekty lékových interakcí výskyt, rozdělení, hlavní mechanismy a důsledky lékových interakcí PharmDr. Josef Suchopár 18. 6. 2014 Lékové interakce: skutečný problém nebo fáma? Velká Británie (Pirmohamed,
Příloha č. 3 k rozhodnutí o prodloužení registrace sp.zn.sukls10638/2011 a příloha k sp.zn. sukls246529/2010, sukls242130/2011, sukls46873/2012
 Příloha č. 3 k rozhodnutí o prodloužení registrace sp.zn.sukls10638/2011 a příloha k sp.zn. sukls246529/2010, sukls242130/2011, sukls46873/2012 1. NÁZEV PŘÍPRAVKU Ewofex 120 mg potahované tablety SOUHRN
Příloha č. 3 k rozhodnutí o prodloužení registrace sp.zn.sukls10638/2011 a příloha k sp.zn. sukls246529/2010, sukls242130/2011, sukls46873/2012 1. NÁZEV PŘÍPRAVKU Ewofex 120 mg potahované tablety SOUHRN
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU CLARITINE Sirup 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden ml sirupu obsahuje 1 mg loratadinum. Jeden ml loratadinového sirupu obsahuje 600 mg sacharosy.
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU CLARITINE Sirup 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden ml sirupu obsahuje 1 mg loratadinum. Jeden ml loratadinového sirupu obsahuje 600 mg sacharosy.
Základní informace o hyperaktivním močovém měchýři (OAB)
 Informace pro pacienty Čeština Základní informace o hyperaktivním močovém měchýři (OAB) Podtržená slova jsou vysvětlena ve slovníčku pojmů. Co je to močový měchýř? Močový měchýř slouží jako rezervoár pro
Informace pro pacienty Čeština Základní informace o hyperaktivním močovém měchýři (OAB) Podtržená slova jsou vysvětlena ve slovníčku pojmů. Co je to močový měchýř? Močový měchýř slouží jako rezervoár pro
Farmakokinetika. Farmakokinetika (pharmacon + kinetikos) Farmakodynamika. 26. února Popisuje osud léčiva v těle Co dělá tělo s lékem
 Ústav farmakologie LF UP v Olomouc 26. února 29 Základní pojmy (pharmacon + kinetikos) Popisuje osud léčiva v těle Co dělá tělo s lékem Základní pojmy Farmakodynamika Popisuje účinek léku na organismus
Ústav farmakologie LF UP v Olomouc 26. února 29 Základní pojmy (pharmacon + kinetikos) Popisuje osud léčiva v těle Co dělá tělo s lékem Základní pojmy Farmakodynamika Popisuje účinek léku na organismus
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 sp. zn. sukls211402/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Alfuzostad 10 mg tablety s prodlouženým uvolňováním 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje alfuzosini hydrochloridum10
sp. zn. sukls211402/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Alfuzostad 10 mg tablety s prodlouženým uvolňováním 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje alfuzosini hydrochloridum10
Tableta s prodlouženým uvolňováním. Popis přípravku : bílé, kulaté, nepotahované tablety se zkosenými hranami.
 Příloha č.2 k rozhodnutí o změně registrace sp. zn. sukls37077/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Alfuzostad 10 mg tablety s prodlouženým uvolňováním 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Příloha č.2 k rozhodnutí o změně registrace sp. zn. sukls37077/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Alfuzostad 10 mg tablety s prodlouženým uvolňováním 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Karbapenemy v intenzivní péči K. Urbánek
 Karbapenemy v intenzivní péči K. Urbánek Ústav farmakologie Lékařská fakulta Univerzity Palackého a Fakultní nemocnice Olomouc Rozdělení Skupina I Skupina II ertapenem, panipenem, tebipenem omezený účinek
Karbapenemy v intenzivní péči K. Urbánek Ústav farmakologie Lékařská fakulta Univerzity Palackého a Fakultní nemocnice Olomouc Rozdělení Skupina I Skupina II ertapenem, panipenem, tebipenem omezený účinek
3 LÉKOVÁ FORMA Tableta s prodlouženým uvolňováním. Růžové, kulaté bikonvexní tablety s vyraženým '35' na jedné straně, na druhé straně hladké.
 Příloha č. 3 k rozhodnutí o registraci sp.zn.sukls200469/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 NÁZEV LÉČIVÉHO PŘÍPRAVKU Portora 35 mg tablety s prodlouženým uvolňováním 2 KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Příloha č. 3 k rozhodnutí o registraci sp.zn.sukls200469/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 NÁZEV LÉČIVÉHO PŘÍPRAVKU Portora 35 mg tablety s prodlouženým uvolňováním 2 KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Jedna dávka přípravku Neoclarityn tableta dispergovatelná v ústech obsahuje desloratadinum 2,5 mg.
 1 NÁZEV PŘÍPRAVKU Neoclarityn 2,5 mg tablety dispergovatelné v ústech 2 KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka přípravku Neoclarityn tableta dispergovatelná v ústech obsahuje desloratadinum 2,5
1 NÁZEV PŘÍPRAVKU Neoclarityn 2,5 mg tablety dispergovatelné v ústech 2 KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka přípravku Neoclarityn tableta dispergovatelná v ústech obsahuje desloratadinum 2,5
Osud xenobiotik v organismu. M. Balíková
 Osud xenobiotik v organismu M. Balíková JED-NOXA-DROGA-XENOBIOTIKUM Látka, která po vstřebání do krve vyvolá chorobné změny v organismu Toxické účinky: a) přechodné b) trvale poškozující c) fatální Vzájemné
Osud xenobiotik v organismu M. Balíková JED-NOXA-DROGA-XENOBIOTIKUM Látka, která po vstřebání do krve vyvolá chorobné změny v organismu Toxické účinky: a) přechodné b) trvale poškozující c) fatální Vzájemné
Tvrdá tobolka se světle modrým víčkem a světle modrým tělem.
 Příloha č. 3 k rozhodnutí o registraci sp.zn. sukls127013/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Orlistat Polpharma 60 mg, tvrdé tobolky 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tvrdá tobolka
Příloha č. 3 k rozhodnutí o registraci sp.zn. sukls127013/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Orlistat Polpharma 60 mg, tvrdé tobolky 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tvrdá tobolka
Příloha č. 3 k rozhodnutí o prodloužení registrace sp.zn. sukls122181/2011 a příloha k sp. zn. sukls91704/2011
 Příloha č. 3 k rozhodnutí o prodloužení registrace sp.zn. sukls122181/2011 a příloha k sp. zn. sukls91704/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU SANDOMIGRAN 0,5 mg obalené tablety 2. KVALITATIVNÍ
Příloha č. 3 k rozhodnutí o prodloužení registrace sp.zn. sukls122181/2011 a příloha k sp. zn. sukls91704/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU SANDOMIGRAN 0,5 mg obalené tablety 2. KVALITATIVNÍ
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 3 k rozhodnutí o registraci sp.zn. sukls42544-6/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Pexogies 0,088 mg tablety Pexogies 0,18 mg tablety Pexogies 0,7 mg tablety 2. KVALITATIVNÍ A
Příloha č. 3 k rozhodnutí o registraci sp.zn. sukls42544-6/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Pexogies 0,088 mg tablety Pexogies 0,18 mg tablety Pexogies 0,7 mg tablety 2. KVALITATIVNÍ A
Oranžová tobolka č. 2 (tvrdá želatinová), která obsahuje bílé nebo nažloutlé granule.
 Příloha č. 2 k rozhodnutí o změně registrace sp.zn. sukls151812/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU TAMIPRO 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tobolka obsahuje 0,4 mg tamsulosini
Příloha č. 2 k rozhodnutí o změně registrace sp.zn. sukls151812/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU TAMIPRO 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tobolka obsahuje 0,4 mg tamsulosini
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU CLARITINE 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Tablety: Jedna tableta obsahuje 10 mg loratadinum. Sirup: Jeden ml sirupu obsahuje 1 mg loratadinum. Pomocné
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU CLARITINE 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Tablety: Jedna tableta obsahuje 10 mg loratadinum. Sirup: Jeden ml sirupu obsahuje 1 mg loratadinum. Pomocné
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Aerius 5 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje desloratadinum v množství 5 mg. Úplný seznam pomocných
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Aerius 5 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje desloratadinum v množství 5 mg. Úplný seznam pomocných
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 sp.zn.sukls25947/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Ditropan 5 mg Tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje oxybutynini hydrochloridum 5 mg v jedné tabletě. Pomocné
sp.zn.sukls25947/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Ditropan 5 mg Tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje oxybutynini hydrochloridum 5 mg v jedné tabletě. Pomocné
5-HMT FARMAKOLOGICKÝ PROFIL. doc. MUDr. Roman Zachoval, Ph.D. Urologické oddělení Fakultní Thomayerovy nemocnice, Praha
 FESTERDI VÉ ATICLIERGIKUM PR LÉČBU YPERAKTIVÍ MČVÉ MĚCÝŘE doc. MUDr. Roman Zachoval, Ph.D. Urologické oddělení Fakultní Thomayerovy nemocnice, Praha Autor v přehledném článku referuje o fesoteridinu, novém
FESTERDI VÉ ATICLIERGIKUM PR LÉČBU YPERAKTIVÍ MČVÉ MĚCÝŘE doc. MUDr. Roman Zachoval, Ph.D. Urologické oddělení Fakultní Thomayerovy nemocnice, Praha Autor v přehledném článku referuje o fesoteridinu, novém
Parkinsonova choroba - pohled urologa (symptomatologie, diagnostika, léčba) Roman Zachoval
 Parkinsonova choroba - pohled urologa (symptomatologie, diagnostika, léčba) Roman Zachoval Urologické oddělení Thomayerova nemocnice Topografie bazálních ganglií Topografie bazálních ganglií Patofyziologie
Parkinsonova choroba - pohled urologa (symptomatologie, diagnostika, léčba) Roman Zachoval Urologické oddělení Thomayerova nemocnice Topografie bazálních ganglií Topografie bazálních ganglií Patofyziologie
Preskripční omezení urologických a uroonkologických léčivých přípravků, platné k 1. 8. 2015
 182 Preskripční omezení urologických a uroonkologických léčivých přípravků, platné k 1. 8. 2015 V posledních týdnech došlo k opakovaným kontrolám zdravotními pojišťovnami. Revize byly zaměřeny na dodržování
182 Preskripční omezení urologických a uroonkologických léčivých přípravků, platné k 1. 8. 2015 V posledních týdnech došlo k opakovaným kontrolám zdravotními pojišťovnami. Revize byly zaměřeny na dodržování
PŘÍLOHA III RELEVANTNÍ ČÁSTI SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE. Poznámka: Tyto úpravy souhrnu údajů o přípravku a
 PŘÍLOHA III RELEVANTNÍ ČÁSTI SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE Poznámka: Tyto úpravy souhrnu údajů o přípravku a příbalové informace jsou platné v okamžiku přijetí rozhodnutí Komisí. Poté,
PŘÍLOHA III RELEVANTNÍ ČÁSTI SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE Poznámka: Tyto úpravy souhrnu údajů o přípravku a příbalové informace jsou platné v okamžiku přijetí rozhodnutí Komisí. Poté,
Příloha č. 2 k rozhodnutí o změně registrace sp.zn.sukls13958/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU
 1. NÁZEV PŘÍPRAVKU Zofran Příloha č. 2 k rozhodnutí o změně registrace sp.zn.sukls13958/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Ondansetronum, 16 mg v jednom čípku. 3. LÉKOVÁ
1. NÁZEV PŘÍPRAVKU Zofran Příloha č. 2 k rozhodnutí o změně registrace sp.zn.sukls13958/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Ondansetronum, 16 mg v jednom čípku. 3. LÉKOVÁ
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 2 k rozhodnutí o změně registrace sp.zn. sukls6044/2010 1. NÁZEV PŘÍPRAVKU Mucosolvan pro dospělé sirup SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 5 ml sirupu obsahuje
Příloha č. 2 k rozhodnutí o změně registrace sp.zn. sukls6044/2010 1. NÁZEV PŘÍPRAVKU Mucosolvan pro dospělé sirup SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 5 ml sirupu obsahuje
METABOLISMUS NIKOTINU U ČLOVĚKA
 METABOLISMUS NIKOTINU U ČLOVĚKA Z. Zloch Ústav hygieny LF UK Plzeň Výskyt nikotinu Cigaretový tabák obs. 1 1.5 % nikotinu, tj. 95 % všech přítomných alkaloidů Minoritní alkaloidy: nornikotin, anatabin,
METABOLISMUS NIKOTINU U ČLOVĚKA Z. Zloch Ústav hygieny LF UK Plzeň Výskyt nikotinu Cigaretový tabák obs. 1 1.5 % nikotinu, tj. 95 % všech přítomných alkaloidů Minoritní alkaloidy: nornikotin, anatabin,
Příloha č. 2 k rozhodnutí o převodu registrace sp.zn. sukls167006/2012, sukls167014/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 2 k rozhodnutí o převodu registrace sp.zn. sukls167006/2012, sukls167014/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Solasfera 5 mg, potahované tablety Solasfera 10 mg, potahované tablety
Příloha č. 2 k rozhodnutí o převodu registrace sp.zn. sukls167006/2012, sukls167014/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Solasfera 5 mg, potahované tablety Solasfera 10 mg, potahované tablety
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU XATRAL UNO tablety s prodlouženým uvolňováním 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivá látka: Alfuzosini hydrochloridum 10 mg v jedné tabletě. Úplný seznam
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU XATRAL UNO tablety s prodlouženým uvolňováním 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivá látka: Alfuzosini hydrochloridum 10 mg v jedné tabletě. Úplný seznam
Sp.zn.sukls88807/2015
 Sp.zn.sukls88807/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU NORMAGLYC 500 mg, potahované tablety NORMAGLYC 850 mg, potahované tablety NORMAGLYC 1000 mg, potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ
Sp.zn.sukls88807/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU NORMAGLYC 500 mg, potahované tablety NORMAGLYC 850 mg, potahované tablety NORMAGLYC 1000 mg, potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ
Jedna transdermální náplast obsahuje 36 mg oxybutyninum. Plocha náplasti je 39 cm 2 a uvolňuje nominálně 3,9 mg oxybutyninu za 24 hodin.
 1. NÁZEV PŘÍPRAVKU Kentera 3,9 mg/24 hodin, transdermální náplast 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna transdermální náplast obsahuje 36 mg oxybutyninum. Plocha náplasti je 39 cm 2 a uvolňuje
1. NÁZEV PŘÍPRAVKU Kentera 3,9 mg/24 hodin, transdermální náplast 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna transdermální náplast obsahuje 36 mg oxybutyninum. Plocha náplasti je 39 cm 2 a uvolňuje
CZ PAR QUETIAPINUM. Seroquel. UK/W/0004/pdWS/001. NL/W/0004/pdWS/001
 CZ PAR Název (léčivá látka/ přípravek) Číslo procedury QUETIAPINUM Seroquel UK/W/0004/pdWS/001 NL/W/0004/pdWS/001 ART. NÁZVY PŘÍPRAVKŮ KLINICKÝCH STUDIÍ INN DRŽITELÉ PŘÍPRAVKŮ KLINICKÝCH STUDIÍ SCHVÁLENÉ
CZ PAR Název (léčivá látka/ přípravek) Číslo procedury QUETIAPINUM Seroquel UK/W/0004/pdWS/001 NL/W/0004/pdWS/001 ART. NÁZVY PŘÍPRAVKŮ KLINICKÝCH STUDIÍ INN DRŽITELÉ PŘÍPRAVKŮ KLINICKÝCH STUDIÍ SCHVÁLENÉ
SOUHRN ÚDAJŮ O PŘÍPRAVKU. 1. NÁZEV PŘÍPRAVKU VINPOCETIN-RICHTER tablety
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU VINPOCETIN-RICHTER tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Vinpocetinum 5 mg v 1 tabletě. Pomocné látky: monohydrát laktosy. 3. LÉKOVÁ FORMA Tablety.
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU VINPOCETIN-RICHTER tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Vinpocetinum 5 mg v 1 tabletě. Pomocné látky: monohydrát laktosy. 3. LÉKOVÁ FORMA Tablety.
Příloha č. 3 k rozhodnutí o prodloužení registrace sp.zn. sukls52815/2009
 Příloha č. 3 k rozhodnutí o prodloužení registrace sp.zn. sukls52815/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU LEVOPRONT sirup 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivá látka: levodropropizinum
Příloha č. 3 k rozhodnutí o prodloužení registrace sp.zn. sukls52815/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU LEVOPRONT sirup 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivá látka: levodropropizinum
2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 g masti obsahuje calcitriolum 0,003 mg (3 mikrogramy). Úplný seznam pomocných látek viz bod 6.1.
 Sp. zn. sukls155368/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Silkis mast 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 g masti obsahuje calcitriolum 0,003 mg (3 mikrogramy). Úplný seznam pomocných
Sp. zn. sukls155368/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Silkis mast 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 g masti obsahuje calcitriolum 0,003 mg (3 mikrogramy). Úplný seznam pomocných
Porovnání účinnosti a vedlejších účinků anticholinergik při léčbě OAB
 241 Porovnání účinnosti a vedlejších účinků anticholinergik při léčbě OAB MUDr. Pavel Verner Urocentrum, Praha Je podán přehled účinnosti, vedlejších účinků, možných lékových interakcí a jsou diskutovány
241 Porovnání účinnosti a vedlejších účinků anticholinergik při léčbě OAB MUDr. Pavel Verner Urocentrum, Praha Je podán přehled účinnosti, vedlejších účinků, možných lékových interakcí a jsou diskutovány
SOUHRN ÚDAJŮ O PŘÍPRAVKU. 400 mg + 40 mg. čípky PROCTO-GLYVENOL. 50 mg/g + 20 mg/g. rektální krém
 sp.zn. sukls74884/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PROCTO-GLYVENOL 400 mg + 40 mg čípky PROCTO-GLYVENOL 50 mg/g + 20 mg/g rektální krém 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Čípky: Jeden
sp.zn. sukls74884/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PROCTO-GLYVENOL 400 mg + 40 mg čípky PROCTO-GLYVENOL 50 mg/g + 20 mg/g rektální krém 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Čípky: Jeden
Příloha č. 3 k rozhodnutí o prodloužení registrace sp.zn. sukls 212259/2010, sukls212261/2010 a příloha k sp. zn. sukls170374/2010
 Příloha č. 3 k rozhodnutí o prodloužení registrace sp.zn. sukls 212259/2010, sukls212261/2010 a příloha k sp. zn. sukls170374/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Ondansetron Arrow 4 mg Ondansetron
Příloha č. 3 k rozhodnutí o prodloužení registrace sp.zn. sukls 212259/2010, sukls212261/2010 a příloha k sp. zn. sukls170374/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Ondansetron Arrow 4 mg Ondansetron
SOUHR ÚDAJŮ O PŘÍPRAVKU. Vesicare perorální suspenze obsahuje solifenacini succinas 1 mg/ml, což odpovídá solifenacinum 0,75 mg/ml.
 SOUHR ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Vesicare 1 mg/ml perorální suspenze 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Vesicare perorální suspenze obsahuje solifenacini succinas 1 mg/ml, což odpovídá solifenacinum
SOUHR ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Vesicare 1 mg/ml perorální suspenze 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Vesicare perorální suspenze obsahuje solifenacini succinas 1 mg/ml, což odpovídá solifenacinum
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Sp.zn.sukls193313/2014 1. NÁZEV PŘÍPRAVKU TAMALIS 10 mg tablety SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje: rupatadinum 10 mg (ve formě fumarátu) Pomocné látky
Sp.zn.sukls193313/2014 1. NÁZEV PŘÍPRAVKU TAMALIS 10 mg tablety SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje: rupatadinum 10 mg (ve formě fumarátu) Pomocné látky
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 2 k rozhodnutí o změně registrace sp.zn. sukls6046/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Mucosolvan long effect Tvrdé tobolky s prodlouženým uvolňováním 2. KVALITATIVNÍ A KVANTITATIVNÍ
Příloha č. 2 k rozhodnutí o změně registrace sp.zn. sukls6046/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Mucosolvan long effect Tvrdé tobolky s prodlouženým uvolňováním 2. KVALITATIVNÍ A KVANTITATIVNÍ
FARMAKOTERAPIE PORUCH MOČENÍ. Roman Zachoval
 FARMAKOTERAPIE PORUCH MOČENÍ Roman Zachoval NOVINKY VE FARMAKOTERAPII HYPERAKTIVNÍHO MOČOVÉHO MĚCHÝŘE (OAB) - mirabegron - darifenacin Perzistence (%) Přerušení farmakoterapie u různých skupin léčiv: OAB
FARMAKOTERAPIE PORUCH MOČENÍ Roman Zachoval NOVINKY VE FARMAKOTERAPII HYPERAKTIVNÍHO MOČOVÉHO MĚCHÝŘE (OAB) - mirabegron - darifenacin Perzistence (%) Přerušení farmakoterapie u různých skupin léčiv: OAB
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU ellaone 30 mg tableta 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje 30 mg ulipristali acetas. Pomocné látky se známým účinkem:
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU ellaone 30 mg tableta 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje 30 mg ulipristali acetas. Pomocné látky se známým účinkem:
Farmakokinetická analýza
 Farmakokinetická analýza Doc. PharmDr. František Štaud, Ph.D. Katedra farmakologie a toxikologie Univerzita Karlova v Praze Farmaceutická fakulta v Hradci Králové PK analýza Vliv organismu na lék Vliv
Farmakokinetická analýza Doc. PharmDr. František Štaud, Ph.D. Katedra farmakologie a toxikologie Univerzita Karlova v Praze Farmaceutická fakulta v Hradci Králové PK analýza Vliv organismu na lék Vliv
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 sp.zn. sukls86344/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU VENORUTON FORTE tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta Venorutonu Forte obsahuje 500 mg oxerutinum (O-beta-hydroxyethyl-rutosid).
sp.zn. sukls86344/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU VENORUTON FORTE tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta Venorutonu Forte obsahuje 500 mg oxerutinum (O-beta-hydroxyethyl-rutosid).
sp.zn.sukls188553/2014
 sp.zn.sukls188553/2014 1. NÁZEV PŘÍPRAVKU SOUHRN ÚDAJŮ O PŘÍPRAVKU tablety s prodlouženým uvolňováním. 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta s prodlouženým uvolňováním obsahuje pentoxifyllinum
sp.zn.sukls188553/2014 1. NÁZEV PŘÍPRAVKU SOUHRN ÚDAJŮ O PŘÍPRAVKU tablety s prodlouženým uvolňováním. 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta s prodlouženým uvolňováním obsahuje pentoxifyllinum
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 sp.zn. sukls144430/2014 1. Název přípravku Ebrantil 30 retard Ebrantil 60 retard Tvrdé tobolky s prodlouženým uvolňováním SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. Kvalitativní a kvantitativní složení Jedna tobolka
sp.zn. sukls144430/2014 1. Název přípravku Ebrantil 30 retard Ebrantil 60 retard Tvrdé tobolky s prodlouženým uvolňováním SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. Kvalitativní a kvantitativní složení Jedna tobolka
Příloha I. Vědecké závěry a zdůvodnění změny v registraci
 Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy / aktualizovaných zpráv o bezpečnosti (PSUR)
Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy / aktualizovaných zpráv o bezpečnosti (PSUR)
Příloha č. 3 k rozhodnutí o převodu registrace sp. zn. sukls198549/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 3 k rozhodnutí o převodu registrace sp. zn. sukls198549/2010 1. NÁZEV PŘÍPRAVKU LANBICA 50 mg Potahované tablety SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 potahovaná
Příloha č. 3 k rozhodnutí o převodu registrace sp. zn. sukls198549/2010 1. NÁZEV PŘÍPRAVKU LANBICA 50 mg Potahované tablety SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 potahovaná
Vývoj nových léčiv. Preklinický výzkum Klinický výzkum
 Vývoj nových léčiv Preklinický výzkum Klinický výzkum Úvod Léčivo = nejprověřenější potravina vstupující do organismu Ideální léčivo kvalitní, účinné, bezpečné a dostupné Financování výzkumu léčiv souvislost
Vývoj nových léčiv Preklinický výzkum Klinický výzkum Úvod Léčivo = nejprověřenější potravina vstupující do organismu Ideální léčivo kvalitní, účinné, bezpečné a dostupné Financování výzkumu léčiv souvislost
CZ PAR. QUETIAPINI FUMARAS Seroquel. UK/W/0004/pdWS/001 NL/W/0004/pdWS/001
 Název (léčivá látka/přípravek) CZ PAR QUETIAPINI FUMARAS Seroquel Číslo procedury UK/W/0004/pdWS/001 NL/W/0004/pdWS/001 ART. NÁZEV INN DRŽITEL SCHVÁLENÉ INDIKACE ATC KÓD LÉKOVÁ FORMA, SÍLA INDIKAČNÍ SKUPINA
Název (léčivá látka/přípravek) CZ PAR QUETIAPINI FUMARAS Seroquel Číslo procedury UK/W/0004/pdWS/001 NL/W/0004/pdWS/001 ART. NÁZEV INN DRŽITEL SCHVÁLENÉ INDIKACE ATC KÓD LÉKOVÁ FORMA, SÍLA INDIKAČNÍ SKUPINA
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Sp.zn. sukls277451/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Azelastin COMOD 0,5 mg/ml oční kapky, roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Azelastini hydrochloridum 0,05 % (0,50 mg/ml) Jedna
Sp.zn. sukls277451/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Azelastin COMOD 0,5 mg/ml oční kapky, roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Azelastini hydrochloridum 0,05 % (0,50 mg/ml) Jedna
Indikace přípravku Zetamac v ordinaci praktického lékaře
 Indikace přípravku Zetamac v ordinaci praktického lékaře MUDr. Igor Karen 13.10. 2009 Zetamac léková forma azithromycinum 2g granule s prodlouženým uvolňováním pro přípravu perorální suspenze s příchutí
Indikace přípravku Zetamac v ordinaci praktického lékaře MUDr. Igor Karen 13.10. 2009 Zetamac léková forma azithromycinum 2g granule s prodlouženým uvolňováním pro přípravu perorální suspenze s příchutí
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 sp. zn. sukls111315/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Protradon 100 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje tramadoli hydrochloridum 100 mg. Úplný seznam
sp. zn. sukls111315/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Protradon 100 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje tramadoli hydrochloridum 100 mg. Úplný seznam
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakákoli podezření
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakákoli podezření
Vesicare 5 mg potahované tablety
 Příloha č. 2a k rozhodnutí o změně registrace sp. zn. sukls148391/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Vesicare 5 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Vesicare 5 mg:
Příloha č. 2a k rozhodnutí o změně registrace sp. zn. sukls148391/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Vesicare 5 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Vesicare 5 mg:
DOPADY ZMĚNY ANTIMUSKARINIKA NA KVALITU ŽIVOTA U PACIENTŮ S HYPERAKTIVNÍM MĚCHÝŘEM VÝSLEDKY STUDIE VEST
 106 DOPADY ZMĚNY ANTIMUSKARINIKA NA KVALITU ŽIVOTA U PACIENTŮ S HYPERAKTIVNÍM MĚCHÝŘEM VÝSLEDKY STUDIE VEST The impact of changing antimuscarinics on quality of live in patients with overactive bladder
106 DOPADY ZMĚNY ANTIMUSKARINIKA NA KVALITU ŽIVOTA U PACIENTŮ S HYPERAKTIVNÍM MĚCHÝŘEM VÝSLEDKY STUDIE VEST The impact of changing antimuscarinics on quality of live in patients with overactive bladder
Jedna potahovaná tableta obsahuje levocetirizini dihydrochloridum 5 mg (což odpovídá 4,2 mg levocetirizinum).
 Sp.zn.sukls82355/2012 SOUHRN ÚDAJU O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Levocetirizin Actavis 5 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna potahovaná tableta obsahuje levocetirizini
Sp.zn.sukls82355/2012 SOUHRN ÚDAJU O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Levocetirizin Actavis 5 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna potahovaná tableta obsahuje levocetirizini
Příloha č.3 k rozhodnutí o změně registrace sp.zn.sukls98466/2010 a příloha k sp.zn.sukls164928/2009, sukls164929/2009
 Příloha č.3 k rozhodnutí o změně registrace sp.zn.sukls98466/2010 a příloha k sp.zn.sukls164928/2009, sukls164929/2009 1. NÁZEV PŘÍPRAVKU Kapidin 10 mg Kapidin 20 mg Potahované tablety SOUHRN ÚDAJŮ O PŘÍPRAVKU
Příloha č.3 k rozhodnutí o změně registrace sp.zn.sukls98466/2010 a příloha k sp.zn.sukls164928/2009, sukls164929/2009 1. NÁZEV PŘÍPRAVKU Kapidin 10 mg Kapidin 20 mg Potahované tablety SOUHRN ÚDAJŮ O PŘÍPRAVKU
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU Borgal 200/40 mg/ml injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 ml obsahuje: Léčivé látky: Sulfadoxinum 200 mg Trimethoprimum
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU Borgal 200/40 mg/ml injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 ml obsahuje: Léčivé látky: Sulfadoxinum 200 mg Trimethoprimum
Příloha II. Vědecké závěry a zdůvodnění změny podmínek rozhodnutí o registraci
 Příloha II Vědecké závěry a zdůvodnění změny podmínek rozhodnutí o registraci 21 Vědecké závěry Celkové závěry vědeckého hodnocení přípravků Oxynal a Targin a souvisejících názvů (viz příloha I) Podkladové
Příloha II Vědecké závěry a zdůvodnění změny podmínek rozhodnutí o registraci 21 Vědecké závěry Celkové závěry vědeckého hodnocení přípravků Oxynal a Targin a souvisejících názvů (viz příloha I) Podkladové
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Atosiban SUN 6,75 mg/0,9 ml injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna injekční lahvička s 0,9 ml roztoku obsahuje atosibanum
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Atosiban SUN 6,75 mg/0,9 ml injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna injekční lahvička s 0,9 ml roztoku obsahuje atosibanum
Osud léčiv v organismu, aplikace léčiv. T.Sechser
 Osud léčiv v organismu, aplikace léčiv T.Sechser Institut klinické a experimentální medicíny 6R 2LK 1.3.2007 tosc@volny.cz PROGRAM PREZENTACE Transport látek mebránami Absorpce, biologická dostupnost,
Osud léčiv v organismu, aplikace léčiv T.Sechser Institut klinické a experimentální medicíny 6R 2LK 1.3.2007 tosc@volny.cz PROGRAM PREZENTACE Transport látek mebránami Absorpce, biologická dostupnost,
Výsledky léčby sibutraminem v iniciální šestitýdenní fázi studie SCOUT. MUDr. Igor Karen
 Výsledky léčby sibutraminem v iniciální šestitýdenní fázi studie SCOUT MUDr. Igor Karen 1 První výsledky studie SCOUT Všichni lékaři se setkávají ve svých praxích s obézními pacienty Někteří již kardiovaskulární
Výsledky léčby sibutraminem v iniciální šestitýdenní fázi studie SCOUT MUDr. Igor Karen 1 První výsledky studie SCOUT Všichni lékaři se setkávají ve svých praxích s obézními pacienty Někteří již kardiovaskulární
1. NÁZEV PŘÍPRAVKU. Orgalutran 0,25 mg/0,5 ml injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
 1. NÁZEV PŘÍPRAVKU Orgalutran 0,25 mg/0,5 ml injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Předplněná injekční stříkačka obsahuje 0,25 mg ganirelixum v 0,5 ml vodného roztoku. Léčivá látka ganirelixum
1. NÁZEV PŘÍPRAVKU Orgalutran 0,25 mg/0,5 ml injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Předplněná injekční stříkačka obsahuje 0,25 mg ganirelixum v 0,5 ml vodného roztoku. Léčivá látka ganirelixum
Příloha č. 3 k rozhodnutí o převodu registrace sp.zn. sukls62363/2011 a sukls62355/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 3 k rozhodnutí o převodu registrace sp.zn. sukls62363/2011 a sukls62355/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Procto-Glyvenol 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Čípky:Tribenosidum
Příloha č. 3 k rozhodnutí o převodu registrace sp.zn. sukls62363/2011 a sukls62355/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Procto-Glyvenol 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Čípky:Tribenosidum
Obsah 1 Úvod 2 Variabilita lékové odpovědi 3 Klinické využití určování koncentrace léčiv
 Obsah 1 Úvod... 11 2 Variabilita lékové odpovědi... 14 2.1 Faktory variability... 14 2.2 Vliv onemocnění... 17 2.2.1 Chronické srdeční selhání... 17 2.2.2 Snížená funkce ledvin... 18 2.2.3 Snížená funkce
Obsah 1 Úvod... 11 2 Variabilita lékové odpovědi... 14 2.1 Faktory variability... 14 2.2 Vliv onemocnění... 17 2.2.1 Chronické srdeční selhání... 17 2.2.2 Snížená funkce ledvin... 18 2.2.3 Snížená funkce
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU FLUMIREX
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU FLUMIREX 2. KVALITATIVNÍ I KVANTITATIVNÍ SLOŽENÍ Fluoxetini hydrochloridum 22,36 mg (odp. 20 mg fluoxetinu) v 1 tobolce. Pomocné látky viz 6.1. 3. LÉKOVÁ FORMA
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU FLUMIREX 2. KVALITATIVNÍ I KVANTITATIVNÍ SLOŽENÍ Fluoxetini hydrochloridum 22,36 mg (odp. 20 mg fluoxetinu) v 1 tobolce. Pomocné látky viz 6.1. 3. LÉKOVÁ FORMA
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 2 k rozhodnutí o změně registrace sp. zn. sukls25846/2010 a sukls25848/2010 a příloha ke sp. zn. sukls156917/2010 a sukls157010/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 NÁZEV PŘÍPRAVKU Pentasa Sachet
Příloha č. 2 k rozhodnutí o změně registrace sp. zn. sukls25846/2010 a sukls25848/2010 a příloha ke sp. zn. sukls156917/2010 a sukls157010/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 NÁZEV PŘÍPRAVKU Pentasa Sachet
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 sp.zn.sukls204047/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU VOLTAREN FORTE 2,32% gel 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 g přípravku Voltaren Forte 2,32% obsahuje diclofenacum diethylaminum
sp.zn.sukls204047/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU VOLTAREN FORTE 2,32% gel 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 g přípravku Voltaren Forte 2,32% obsahuje diclofenacum diethylaminum
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 3 k rozhodnutí o prodloužení registrace sp.zn. sukls6972/2006 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PARALEN 500 SUP čípky 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden čípek obsahuje Paracetamolum
Příloha č. 3 k rozhodnutí o prodloužení registrace sp.zn. sukls6972/2006 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PARALEN 500 SUP čípky 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden čípek obsahuje Paracetamolum
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 3 k rozhodnutí o registraci sp.zn. sukls187009/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU ARTAXIN 625 mg, tvrdé tobolky 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tobolka obsahuje glucosaminum
Příloha č. 3 k rozhodnutí o registraci sp.zn. sukls187009/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU ARTAXIN 625 mg, tvrdé tobolky 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tobolka obsahuje glucosaminum
Sp.zn. sukls20326/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU
 Sp.zn. sukls20326/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Solifenacin G.L.Pharma 5 mg, potahované tablety Solifenacin G.L.Pharma 10 mg, potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Sp.zn. sukls20326/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Solifenacin G.L.Pharma 5 mg, potahované tablety Solifenacin G.L.Pharma 10 mg, potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Sp. zn. sukls230046/2016 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Azelastin COMOD 0,5 mg/ml oční kapky, roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Azelastini hydrochloridum 0,05 % (0,50 mg/ml) Jedna
Sp. zn. sukls230046/2016 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Azelastin COMOD 0,5 mg/ml oční kapky, roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Azelastini hydrochloridum 0,05 % (0,50 mg/ml) Jedna
Příloha č.3 k rozhodnutí o registraci sp.zn. sukls48796/2009
 Příloha č.3 k rozhodnutí o registraci sp.zn. sukls48796/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU GLUCOPHAGE XR 750 mg tablety s prodlouženým uvolňováním 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Příloha č.3 k rozhodnutí o registraci sp.zn. sukls48796/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU GLUCOPHAGE XR 750 mg tablety s prodlouženým uvolňováním 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Jedna tableta obsahuje bisulepini hydrochloridum 2,25 mg (bisulepinum 2 mg).
 sp. zn. sukls298106/2018 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Dithiaden 2 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje bisulepini hydrochloridum 2,25 mg (bisulepinum
sp. zn. sukls298106/2018 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Dithiaden 2 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje bisulepini hydrochloridum 2,25 mg (bisulepinum
SOUHRN ÚDAJŮ O PŘÍPRAVKU. MINIRIN Melt 240 μg Perorální lyofilizát
 Příloha č. 2 ke sdělení sp.zn. sukls239195-96/2010 a sukls25698/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 NÁZEV PŘÍPRAVKU MINIRIN Melt 60 μg MINIRIN Melt 120 μg MINIRIN Melt 240 μg Perorální lyofilizát 2 KVALITATIVNÍ
Příloha č. 2 ke sdělení sp.zn. sukls239195-96/2010 a sukls25698/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 NÁZEV PŘÍPRAVKU MINIRIN Melt 60 μg MINIRIN Melt 120 μg MINIRIN Melt 240 μg Perorální lyofilizát 2 KVALITATIVNÍ
Broskvově zbarvené oválné bikonvexní potahované tablety, po obou stranách hladké.
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU FEXIGRA TABLETY 120 mg FEXIGRA TABLETY 180 mg Potahované tablety 2. KVANTITATIVNÍ A KVALITATIVNÍ SLOŽENÍ FEXIGRA TABLETY 120 mg FEXIGRA TABLETY 180
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU FEXIGRA TABLETY 120 mg FEXIGRA TABLETY 180 mg Potahované tablety 2. KVANTITATIVNÍ A KVALITATIVNÍ SLOŽENÍ FEXIGRA TABLETY 120 mg FEXIGRA TABLETY 180
sp. zn. sukls178963/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU FAMOSAN 10 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
 sp. zn. sukls178963/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU FAMOSAN 10 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna potahovaná tableta obsahuje famotidinum 10 mg. Pomocné
sp. zn. sukls178963/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU FAMOSAN 10 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna potahovaná tableta obsahuje famotidinum 10 mg. Pomocné
Dospělí: Jeden čípek ráno, večer a po každém vyprázdnění střev. Zavést do rekta zaobleným koncem.
 sp.zn. sukls186765/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PREPARATION H čípky 23 mg / 69 mg 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivé látky: Faecis extractum fluidum 1,00 % hmot., t.j. 23
sp.zn. sukls186765/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PREPARATION H čípky 23 mg / 69 mg 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivé látky: Faecis extractum fluidum 1,00 % hmot., t.j. 23
