Moderní biofyzikální přístupy v experimentální biologii
|
|
|
- Julie Bártová
- před 6 lety
- Počet zobrazení:
Transkript
1 Oddělení funkční genomiky a proteomiky Ústav experimentální biologie, Přírodovědecká fakulta Masarykova univerzita Praktický kurz Moderní biofyzikální přístupy v experimentální biologii Místo konání: Brno, Univerzitní kampus Bohunice blok A2, seminární místnost 1.21 Datum: Začátek vždy v 9:00 Vedoucí kurzu: Mgr. Ctirad Hofr Ph.D hofr@sci.muni.cz Kurz je organizován v rámci projektu OP VK Moderní biofyzikální metody: pokročilé vzdělávání v experimentální biologii registrační číslo CZ.1.07/2.3.00/
2 Časový plán Moderní biofyzikální přístupy v experimentální biologii Úterý Středa Čtvrtek Úvod organizace kurzu Anisotropie fluorescence přednáška Fluorescenční mikroskopie přednáška Měření spektrálních charakteristik proteinů a DNA návod Skupina A Nanophotemeter 2.Stanovení koncentrace proteinů Bradfordové metodou návod Skupina B Spektrofotometr záměna skupin A a B na stanovištích 1 a 2 5. Příprava fluorescenčně značeného proteinu Skupina A, B návod 6. Předvedení měření anizotropie fluorescence Skupina A, B 9. Příprava mikroskopických preparátů pro lokalizaci transgenních proteinů (každý si připraví vlastní preparát) návod 10. Sledování připravených preparátů rostlin obsahujících GFP a RFP v živých buňkách za použití fluorescenční mikroskopie Skupina A, B oběd záměna skupin záměna skupin záměna skupin Vliv ph a teploty na spektrální vlastnosti fluorescenčních sond návod Skupina C (3 účastníci) Fluorimetr Fmax4 4. Fluorescenční stanovení koncentrace DNA návod Skupina D (3 účastníci) SpectroVis záměna skupin C a D na stanovištích 3 a 4 7. Vizualizace makromolekul při horizontální elektroforetické separaci (EMSA) návod 8. Agarosová elektroforéza sledovaná v reálném čase Skupina C, D společně 11. Měření vlastní fluorescence aminokyselin a proteinů Skupina C návod 12. Stanovení koncentrace DNA a proteinu za použití komerčně dostupných kitů 1 návod Skupina D Záměna skupin C a D na stanovištích 11 a 12
3 Měření spektrálních charakteristik a stanovení koncentrace DNA a proteinů Spektroskopie v UV oblasti umožňuje stanovit koncentraci a čistotu biologických molekul. Molekuly DNA mají absorpční maximum kolem 260 nm, molekuly proteinů kolem 280 nm. Pro přímé spektrální určení koncentrace se využívá Lambert-Beerova zákona pro monochromatické světlo, který lze zapsat ve tvaru A = c.ε za předpokladu, že měříme v 1 cm kyvetě a známe extinkční koeficient ε, který má jednotku [M -1 cm -1 ] pro molární koncentraci nebo [ml.mg -1 cm -1 ] pro koncentraci v mg/ml. V případě, že neznáme extinkční koeficient, můžeme pro určení koncentrace DNA o vysoké molekulární hmotnosti použít zjednodušeného předpokladu, že roztok dvouřetězcové DNA o absorbanci 1 má koncentraci 50 µg/ml a pro převod na molární koncentraci nukleotidu DNA pak vztah 320 µg/ml = 1 mm. Pro určení koncentrace proteinů spektroskopicky lze využít absorbance proteinů při 280 nm. Jestliže známe primární sekvenci aminokyselin proteinu, lze extinkční koeficient vypočítat Ze změřené absorbance pak určíme koncentraci proteinu. Znalost extinkčního koeficientu není nutná v případě univerzální Bradfordové metody. Bradfordové metoda je v současnosti nejrozšířenější způsob určování koncentrace proteinu. Bradfordové metoda využívá posunu absorpčního maxima Coomasie Blue po vazbě na protein. Za použití kalibrační křivky se známou koncentrací proteinu lze určit skutečnou koncentraci neznámého proteinu nebo směsi proteinů. Materiál DNA DNA (Salmon sperm; přibližná koncentrace = 7,5 mg/ml) Oligonukleotid CNF2_Bot (5 GTTATCCTTTGAGGGTTTAG; přibližná koncentrace = 0,02 mg/ml) BSA (hovězí sérový albumin; ε = ml mg -1 cm -1, MW = 66430; přibližná koncentrace 5 mg/ml) TE pufr, destilovaná voda Bradford reagent (BioRad) Kyvety a spektrofotometr 1. Připravte roztok DNA v TE pufru ze zásobního roztoku tak, aby bylo možno přesně určit koncentraci DNA. 2. Změřte absorpční spektrum DNA v rozsahu vlnových délek 220 až 350 nm. 3. Určete polohu absorpčního maxima. 4. Stanovte přesnou koncentraci DNA v zásobním roztoku z hodnoty absorbance naředěného roztoku při 260 nm. Koncentraci vyjádřete v mg/ml a v OD/mL. 5. Nařeďte roztok oligonukleotidu v TE pufru ze zásobního roztoku tak, aby bylo spektroskopicky možno přesně stanovit jeho koncentraci. 6. Změřte absorpční spektrum v rozsahu vlnových délek 220 až 600 nm. 7. Nastavení NanoPhotometer: Functions Wavescan nastavte min a max λ OK Blank - vzorek 8. Na základě zadané sekvence oligonukleotidu stanovte extinkční koeficient ε 260 a spektroskopicky určete jeho koncentraci Změřte spektrum značeného oligonukleotidu ve stejném rozsahu vlnových délek a porovnejte jej se spektrem neznačeného oligonukleotidu.
4 Protein UV spektroskopie 1. Připravte roztok BSA v TE pufru ze zásobního roztoku tak, aby bylo možno přesně určit koncentraci BSA. 2. Změřte absorpční spektrum BSA v rozsahu vlnových délek 240 až 350 nm: Nastavení přístroje Beckman DU 730 :Wavelength Scan Options λ nastavit hodnoty min a max λ OK blank - vzorek 3. Určete polohu absorpčního maxima. 4. Stanovte přesnou molární koncentraci BSA v zásobním roztoku z hodnoty absorbance naředěného roztoku při 280 nm. Bradfordové metoda 1. Připravte standardní kalibrační křivku pro měření koncentrace proteinu Bradfordové metodu. 2. Změřte koncentraci BSA pomocí této metody. 3. Vezměte roztok reakčního Bradfordové činidla z lednice a nechte jej zahřát na pokojovou teplotu a promíchejte. 4. Připravte roztoky blanku a standardů BSA o celkovém objemu 1mL do mikrozkumavek tak, že do 980 µl reakčního Bradfordové činidla přidejte vždy 20 µl TE pufru nebo 20 µl mg/ml, 0.25 mg/ml, 0.5 mg/ml, 0.75 mg/ml, 1 mg/ml a 1.5 mg/ml standardů. 5. Současně připravte stejným způsobem roztok BSA ze zásobného roztoku, který jste naředili tak, aby bylo možno přesně určit jeho koncentraci. 6. Všechny roztoky dobře promíchejte a nechte inkubovat 5 min při pokojové teplotě. Inkubace by neměla přesáhnout 1h. 7. Nastavení spektrofotometru: Beckman DU 530: Protein assay Bradford STD Curve Units: mg/ml tlačítko MORE Create table vypište hodnoty koncentrací standardů od nejmenší Entry Done Změřte absorbanci blanku Změřte absorbanci roztoku standardů. Při měření postupujte od nejnižší koncentrace standardu k nejvyšší. Po posledním standardu se vytvoří kalibrační křivka. Změňte rovnici: Next formula Entry Done Beckman DU 730: Protein Assay Analysis Bradford Start Standard Curve Standards Setup - vypište hodnoty koncentrací standardů od nejmenší přes Edit concentration Done změřte absorbanci blanku, poté standardů. Změňte rovnici na Non-linear - Done 8. Změřte absorbanci blanku, jednoho standardu (pro kontrolu) a poté neznámého vzorku a pomocí kalibrační křivky určete jeho koncentraci. 9. Porovnejte hodnoty koncentrace zásobního roztoku BSA určené spektroskopicky při 280 nm a pomocí Bradfordové metody.
5 Vliv ph a teploty na spektrální vlastnosti fluoroforů V tomto experimentu je ukázán vliv ph na fluorescenci a absorpci fluorescenční značky fluoresceinu rozpuštěné ve stejné koncentraci v roztocích o různém ph. Je rovněž demonstrován vliv teploty na intenzitu fluorescence. Materiál Fluorescein - NIST-traceable standard - 50 µm (Molecular Probes, Invitrogen) Pufr 5 (20 mm MES, ph 5.0) Pufr 7 (50 mm fosfát sodný, ph 7.0) Pufr 9 (50 mm glycin, ph 9.0) Spektrofluorometr vybavený kryostatem (chlazenou vodní lázní) Kyveta Postup 1. Připravte vzorky fluoresceinu x naředěním roztoku NIST standardu jeho přidáním 1,5 µl do 1499 µl roztoku pufru 5, pufru 7 a pufru 9 a následným dalším naředěním (150 µl 1000x zřeď. roztoku do 1350 µl příslušného pufru). 2. Změřte excitační spektra vzorků při λ(em) = 515 nm 3. Změřte emisní spektra vzorků při λ(ex) = 488 nm 4. Změřte spektra při 20, 25 a 37 C. Výsledky Obr. 1: Vliv ph na excitační a emisní spektrum fluoresceinu. Při změně pufru z ph 7 na ph 5 a při zvýšení teploty dochází ke snížení intenzity fluorescence fluoresceinu.
6 Fluorescenční stanovení koncentrace DNA Určení koncentrace DNA je často základním krokem při analýze biologického materiálu a je součástí mnoha laboratorních protokolů. Znalost přesné koncentrace DNA je důležitá pro celou řadu technik (např. sekvenování, klonování cdna, transkripce RNA). Koncentrace DNA je nejčastěji měřena UV spektroskopií, určením hodnoty absorbance při 260 nm (Abs 260 = 1 pro dvouřetězcovou DNA o koncentraci 50 µg/ml; v 1 cm kyvetě). Ke kvantifikaci nižších koncentrací DNA, než jsou detekovatelné za použití UV spektroskopie lze použít fluorescenční sondy, které se vážou na dvouřetězcovou DNA a vykazují několikanásobný nárůst intenzity fluorescence po navázání. K sondám, které lze použít ke stanovení koncentrace DNA patří GelStar. Tato fluorescenční sonda má excitační maximum kolem 493 nm a emituje v oblasti 530 nm. Materiál Spektrofluorometr SpectroVis Plus (Vernier) Kyveta (2 ml) Roztok DNA (Salmon sperm) GelStar (10000x) 1x TE pufr Destilovaná voda Příprava roztoků 1x TE: 10 mm Tris-HCl 1 mm EDTA ph 8,0 100x GelStar 2 µl zásobního 10000x koncentrovaného roztoku GelStar nařeďte na objem 200 µl 1x TE pufrem Standardní roztok DNA Abs 260 = 0,369 koncentrace =?
7 Vytvoření standardní křivky 1. Připravte následná ředění roztoku DNA v 1X TE s koncentrací: 5 ng/µl, 2,5 ng/µl, 1,25 ng/µl, 0,625 ng/µl, 0,3125 ng/µl po 1mL) 2. Připravte blank: 1 ml 1x TE pufru 3. Ke každé koncentraci 1mL standardního roztoku DNA a k blanku přidejte vždy 20 µl 100x GelStar roztoku a 980 µl 1xTE pufru. Promíchejte a postupně pipetujte do kyvety. Celková koncentrace DNA standardů v kyvetě je nyní poloviční (2,50, 1,25,... ng/µl) 4. Všechny standardy a vzorky s GelStar uchovejte v temnu až do měření. 5. Zapněte spektrofluorometr podle návodu. 6. Spusťte program Logger Pro Změřte intenzitu fluorescence Experiment Change units Spectrometer Fluorescence excitační vlnová délka 8. Změřte nejdříve intenzitu fluorescence blanku, následně standardy: vložte kyvetu, měření spustíte tlačítkem Collect a zastavíte Stop 9. Hodnoty intenzity zapište do tabulky a vyneste do grafu hodnoty intenzity fluorescence standardů na koncentraci vzorku. Měření neznámého vzorku 1. Nařeďte neznámý vzorek v 1x TE na celkový objem 1mL. Objem v eppendorfce: 0,5 ml 2. Přidejte 20 µl 100x GelStar a 980 µl 1xTE pufru. 3. Změřte intenzitu fluorescence neznámého vzorku. 4. Určete podle standardní křivky koncentraci DNA v neznámém vzorku. Výsledky Stanovení koncentrace DNA v původním neředěném neznámém vzorku.
8 Fluorescenční značení proteinu Fluorescenční značení proteinu bude provedeno za použití soupravy Alexa Fluor 594 Protein Labeling Kit. Proteiny značené tímto fluoroforem vykazují excitační maximum 590 nm a emisní maximum 617 nm. Alexa Fluor 594 je ve formě NHS (sukcinimidyl) esteru viz Obr. 1. Za použití následujícího postupu lze fluorescenčně naznačit 0.1 až 1 mg proteinu. Příprava proteinu Obr. 1 AlexaFluor 594 Pro optimální efektivitu značení by měl být protein ve fosfátovém pufru bez amonných inontů a primárních aminů. V případě, že protein je v jiném pufru (Trisový, glycinový), je možno dialýzou pufr změnit. Výsledná koncentrace roztoku proteinu na značení by měla být 2 mg/ml. Materiál Alexa Fluor 594 Mikrozkumavka s magnetickým míchadlem Roztok proteinu ve fosfátovém pufru (Thyroglobulin, MW = , extinkční koeficient ε = M -1 cm -1, zásobní koncentrace 10 mg/ml) 1M roztok hydrogenuhličitanu sodného (NaHCO 3, MW = 84), 1ml Fosfátový pufr (50 mm NaCl, 50 mm fosfát sodný) Kolona s náplní Sephadex G-25 Kyvety NanoPhotometer (Implen) Značení proteinu 1. Do mikrokyvety napipetujte 50 µl roztoku proteinu (c= 10 mg/ml). Jestliže je koncentrace proteinu vyšší než 2 mg/ml, roztok se naředí přidáním fosfátového pufru na výslednou koncentraci 2 mg/ml. 2. Zkumavku s fluorescenční značkou nechte zahřát na laboratorní teplotu. Přidejte 25 µl 1M NaHCO 3 a promíchejte pipetováním nahoru a dolů. Odpipetujte do mikrozkumavky s proteinem a promíchejte pipetováním nahoru a dolů. 3. Vše nechte míchat v mikrozkumavce s magnetickým míchadlem po dobu 30 minut při laboratorní teplotě.
9 minut před koncem inkubace připravte kolonu pro separaci proteinu a nenavázané fluorescenční značky. Purifikace proteinu Náplň kolony Sephadex G-25 umožňuje gelovou filtrací oddělit nenavázanou fluorescenční značku od proteinu podle rozdílné velikosti a molekulové hmotnosti. 1. Kolonu umístěte do stojánku, odstraňte víčko a zátku a nechte obsah kolony vykapat. 2. Promyjte kolonu 5 ml fofátového pufru. 3. Opatrně naneste reakční směs proteinu a značky pipetou do středu kolony. Použijte 100 µl fosfátového pufru k vypláchnutí mikrozkumavky s reakční směsí a opět naneste na kolonu. Roztok nechte zaputovat do kolony. 4. Po 1 ml přidávejte fosfátový pufr. Postupně jímejte frakce vytékající z kolony do mikrozkumavek po 1 ml. Po cca 2-3 ml začíná vytékat značený protein. Zachyťte značený protein do jedné frakce. 5. Vzorek (frakci se zachyceným značeným proteinem) proměřte na spektrofotometru. Na základě absorpčního spektra určete, jaké množství proteinu bylo naznačeno a jaký je stupeň značení. Nastavení spektrofotometru: Functions Wave scan interval vlnových délek ( nm) vložte kyvetu s blankem Blank vložte kyvetu se vzorkem Sample Options Graph scale upravit rozsah osy y, aby byly píky viditelné kde je molární extinkční koeficient značky Alexa Fluor 594 při 590 nm a Cm molární koncentrace proteinu, (ředění: pokud jste ředili do kyvety) Výsledky Získané množství proteinu a stupeň značení.
10 Vizualizace makromolekul při elektroforetické separaci Fluorescenční značení lze využít při sledování elektroforetické migrace makromolekul. V případě, že jsou protein a DNA naznačeny rozdílnou fluorescenční značkou, lze nezávisle detekovat polohu DNA a proteinů a sledovat jejich vzájemnou interakci. Materiál DNA fragment s navázanou fluorescenční značkou Rhodamin Red X (excitace 572 nm, emise 595 nm) protein s navázanou fluorescenční značkou Alexa Fluor 488 (excitace 496 nm, emise 519 nm) roztok akrylamidu 30% (akrylamid : bisakrylamid ~ 37:1) Upozornění: Akrylamid je neurotoxin. Je nutno pracovat v rukavicích! 5X TBE (450 mm Tris, 450 mm kys. boritá, 10 mm EDTA) 30% APS (ammonium persulfate) TEMED (N, N, N -tetramethylethylendiamin) Fosfátový pufr (50 mm NaCl, 50 mm fosfát sodný) ddh 2 O n-butanol nasycený vodou (45 ml n-butanolu smíchano s 5 ml ddh 2 O) mikrozkumavky 6x nanášecí pufr (0.15% orange G, 60% glycerol, 10 mm Tris-HCl ph 7.6, 60 mm EDTA) aparatura pro horizontální elektroforézu fluorescenční scanner FLA-7000 Postup 1. Připravte směs pro horizontální akrylamidový gel tak, že smícháte odpovídající množství zásobního roztoku akrylamidu (neurotoxin!), 5X TBE a ddh2o, aby výsledná koncentrace akrylamidu byla 5 % v 0.25X TBE a celkový objem směsi byl 80 ml. Jednotlivé složky přidávejte v pořadí: ddh 2 O, 5x TBE, dále 400 µl 30% APS a 26,4 µl TEMED a až nakonec 30% akrylamid. Dobře promíchejte, nalijte do formy a nasaďte hřebínek na 10 jamek. Směs se po nalití do formy přelije vrstvou n-butanolu, aby mohlo dojít k polymeraci bez přístupu vzduchu. Nechte 1 hodinu polymerizovat na stole. 2. Připravte roztok fluorescenčně značené DNA ve fosfátovém pufru tak, aby byla jeho výsledná koncentrace 1,5 pmol/µl (zásobní DNA: vysušených 30 pmol) 3. Připravte roztok fluorescenčně značeného proteinu ve fosfátovém pufru tak, aby byla jeho koncentrace 3 pmol/µl. (zásobní protein: přibližně 7,5 pmol/µl bude upřesněno) 4. Připravte vzorky do mikrozkumavek podle následující tabulky bez přídavku nanášecího pufru:
11 zkumavka číslo: pouze DNA DNA : protein 1:2 1:4 1:6 1:8 1:12 1:16 1:20 1:24 DNA (1,5 pmol/μl) pouze protein protein (3 pmol/μl) fosfátový pufr x nanášecí pufr Nechte 10 minut inkubovat za laboratorní teploty. 6. Sestavte aparaturu pro horizontální elektroforézu a naplňte ji 0.25X TBE pufrem (cca 1,5 l). 7. Ke každému vzorku přidejte 6x nanášecí pufr podle tabulky. 8. Vložte gel do elektroforetické vany. 9. Naneste vzorky na gel v pořadí jako je v tabulce. 10. Spusťte elektroforézu při napětí 40 V. Po 30 minutách zvyšte napětí na 90 V a nechte pokračovat dalších 90 minut. 11. Detekujte fluorescenci značené DNA na fluorescenčním scanneru s nastavením budícího záření a detekčního filtru na Rhodamin red-x [ROX]. 12. Detekujte fluorescenci značeného proteinu na fluorescenčním scanneru s nastavením budícího záření a detekčního filtru na Alexa fluor [Alexa488]. 13. Porovnejte obě výsledná zobrazení a určete oblasti, ve kterých se vyskytují komplexy vzniklé vazbou proteinu na DNA. Obr. 1 Příklad překryvu zobrazení při různém fluorescenčním značení DNA a proteinu
12 Stanovení koncentrace DNA a proteinu pomocí mikrofluorometru Materiál Quant-iT dsdna BR Assay Kit, Quant-iT ssdna Assay Kit, Quant-iT protein Assay Kit Standardy dsdna, ssdna a proteinu Vzorek dsdna, ssdna a proteinu o neznámé koncentraci Qubit mikrozkumavky Mikrofluorometr Qubit (Invitrogen) Postup 1. Připravte si cca 1 ml Working solution smícháním Quant-iT reagent a Quant-iT buffer v poměru 1:200 (1 µl reagent : 200 µl buffer) zvlášť pro ssdna, dsdna a protein 2. Připravte standardy smícháním 190 µl Working solution + 10 µl příslušného standardu #1 a #2 (#3 pro protein) 3. Připravte vzorek o neznámé koncentraci ve dvou mikrozkumavkách smícháním 195 µl Working solution + 5 µl vzorku 4. Standardy i vzorky krátce promíchejte na vortexu (2-3 sec), opatrně - ve vzorku nesmí být bublinky!! 5. Inkubace 5-10 minut při laboratorní teplotě 6. Zapněte Qubit fluorometr, vyberte příslušnou metodu (metoda v přístroji musí mít stejný název jako kit, který používáte), nová kalibrace (standardy), poté změřte neznámý vzorek (od každé zkumavky 3 měření) Pozn.: Měření by mělo probíhat za laboratorní teploty (22-28 C). Teplota vzorků by měla být stejná, proto nedržte zkumavku se vzorkem před měřením dlouho v rukách, po každém měření zkumavku ihned vytáhněte z přístroje a mezi jednotlivými měřeními ji ponechte inkubovat alespoň 30 sec při laboratorní teplotě. Výsledky Stanovení koncentrace DNA a RNA v neznámých vzorcích.
13 Vlastní fluorescence proteinů Vlastní fluorescenci proteinů je způsobena aromatickými aminokyselinami v nich obsaženými: tryptofanem (Trp), tyrozinem (Tyr) a fenylalaninem (Phe). Dominující je fluorescence tryptofanu, naopak prakticky vůbec se neuplatňuje fenylalanin. V této úloze jsou změřena fluorescenční excitační a emisní spektra albuminu a čistého tryptofanu, tyrozinu a fenylalaninu. Vlastnosti L-tryptofanu MW = 204,23 absorpční maximum: λ exmax = 295 nm fluorescenční emisní maximum: λ emmax = 353 nm emise Trp je vysoce závislá na polaritě a okolním prostředí Vlastnosti L-tyrozinu MW = 181,19 absorpční maximum: λ exmax = 275 nm fluorescenční emisní maximum: λ emmax = 304 nm emise Tyr je relativně málo citlivá na polaritu rozpouštědla Vlastnosti L-fenylalaninu MW = 165,19 absorpční maximum: λ exmax = 260 nm fluorescenční emisní maximum: λ emmax = 282 nm emise Phe je strukturovaná Fluorescence proteinů je obvykle excitována při 280 nm nebo při delších vlnových délkách, takže fenylalanin není ve většině experimentů excitován. Navíc je kvantový výtěžek fluorescence Phe velmi malý (kolem 0,02). Tryptofanovou fluorescenci v proteinech lze selektivně excitovat při nm. Materiál L-tryptofan (Applichem), L-tyrozin (Applichem), L-fenylalanin (Applichem) Hovězí sérový albumin (BSA, MW = 67000) pufr A (120 mmol/l NaCl, 10 mmol/l KCl, 30 mmol/l Tris HCl, ph 7,4) Postup 1. Připravené zásobní roztoky 10 mm Trp, 2 mm Tyr, 10 mm Phe a 0,25 mmol/l albumin pro vlastní měření nařeďte pufrem A na koncentrace: 5 µμ Trp, 20 µm Tyr, 200 µm Phe a 0.6 µm albumin 2. Změřte excitační a emisní spektra vzorků za podmínek uvedených v tabulce.
14 excitační spektrum emisní spektrum λ em (nm) λ ex (nm) λ ex (nm) λ em (nm) L-tryptofan L-tyrozin L-fenylalanin albumin Výsledky Změřená excitační a emisní spektra vlastní fluorescence tryptofanu (Trp), tyrozinu (Tyr), fenylalaninu (Phe) a albuminu v pufru A jsou na Obr.1 a Obr 2. Z výsledných spekter je zřejmé, že prakticky veškerá vlastní fluorescence albuminu pochází od tryptofanu. Měření byla provedena na spektrofluorometru FluoroMax-4. Intenzita fluorescence 1.2x x x x x x PHE ALB TRP TYR λ (nm ) Obr. 1 Excitační spektra 5 µm Trp (λ em = 350 nm), 20 µm Tyr (λ em = 300 nm), 200µM Phe (λ em = 280 nm) a 0.6 µm albuminu (λ em = 350 nm). 1.2x x10 6 ALB TRP Intenzita fluorescence 8.0x x x x10 5 PHE TYR λ (nm ) Obr. 2 Emisní spektra 5 µm Trp (λ ex = 280 nm), 20 µm Tyr (λ ex = 270 nm), 200 µm Phe (λ ex = 250 nm) a 0.6 µm albuminu (λ ex = 280 nm).
15 Studium vazby molekul za použití anizotropie fluorescence Změna anizotropie fluorescence je používána při popisu vzájemné interakce molekul. V případě, že se fragment DNA s fluorescenční značkou volně pohybuje (rotuje) v roztoku, je pozorovaná anizotropie relativně nízká. V případě, že dojde ke vzniku komplexu DNA a proteinu, dochází k výraznému snížení pohyblivosti DNA s fluorescenční značkou, což má za následek zvýšení anizotropie fluorescence. Při titrování roztoku fluorescenčně značené DNA roztokem DNA-vazebného proteinu dochází k postupné vazbě molekul proteinu na vazebná místa jednotlivých molekul DNA a tedy k postupnému zvyšování anizotropie fluorescence. Protein se na vazebná místa na DNA váže až do okamžiku, kdy je koncentrace proteinu tak vysoká, že jsou všechny molekuly DNA obsazeny. V tomto momentě anizotropie fluorescence dosáhne maximální hodnoty a přestane se dále zvyšovat. Koncetrace proteinu, při které hodnota anizotropie fluorescence tvoří 50 % maximální hodnoty, se nazývá disociační konstanta (Kd). Ta reprezentuje afinitu (sílu vazby) konkrétního proteinu k DNA. Studium změn Kd v závislosti např. na iontové síle či teplotě umožňuje získat cenné poznatky o povaze komplexu protein-dna a o mechanismu, jakým spolu obě makromolekuly interagují. Materiál 30 pmol vysušeného fragmentu DNA (GTTAGG) 4 značeného Rhodaminem Red X (λ ex = 572, λ em = 591 nm) Roztoky proteinu (lidský telomer-vazebný protein TRF1, MW = 110 kda) o koncentracích 1µM a 20µM Pufr P (20mM HEPES, 180mM KCl, 0,1mM EDTA, 3mM MgCl 2, ph 8.0) 1M DTT Spektrofluorometr vybavený polarizátory pro měření anizotropie fluorescence Mikrokyveta s magnetickým míchadlem
16 Postup 1) Resuspendovat vysušenou DNA v 1,5 ml pufru P a důkladně vortexovat. Výsledná koncentrace DNA bude 20nM. 2) Pufrem P naředit resuspendovanou DNA na 2nM, resp. 10nM roztok o objemu 1,5 ml. Přidat 1.5 µl 1M DTT. Roztok přenést do kyvety. Kyvetu při manipulaci odzátkovávat jen na nezbytně dlouhou dobu, aby bylo zamezeno vnášení částic prachu do vzorku. 3) Na fluorimetru 5x změřit anizotropii fluorescence pomocí funkce batch experiment a nastavení uloženém v souboru./redx_titrator/p0.xml (λ ex = 572 nm, λ em = 591 nm, šířka štěrbin 8/8 nm). Hodnoty anizotropie zaznamenat do tabulky v software SigmaPlot. 4) Postupně přidávat 1µM roztok proteinu tak, aby celkový objem přidaného roztoku byl 3, 5, 10, 20 a 50 µl. Po každém přídavku 5x změřit hodnotu anizotropie fluorescence a zaznamenat do tabulky v software SigmaPlot. 5) Postupně přidávat 20 µm roztok proteinu tak, aby celkový objem přidaného roztoku byl 3, 5, 10 a 20 µl. Po každém přídavku 5x změřit hodnotu anizotropie fluorescence a zaznamenat v software SigmaPlot. 6) V software SigmaPlot provést úpravu hodnot anizotropie na změnu objemu po přídavku roztoků proteinu. 7) Pomocí software SigmaPlot vynést do grafu závislost korigovaných hodnot anizotropie fluorescence na koncentraci přidaného proteinu. 8) Pomocí software SigmaPlot analyzovat křivku vazby proteinu a stanovit disociační konstantu Kd. Kd = 17 ± 1 nm Obr. 1. Závislost anizotropie fluorescence značeného fragmentu DNA na koncentraci proteinu.
17 Pokročilé biofyzikální přístupy v experimentální biologii 2012: Fluorescenční mikroskopie při lokalizaci transgenních proteinů exprimovaných a) v semenáčcích Arabidopsis thaliana b) v listech Nicotiana benthamiana Cíl praktické úĺohy: Teorie: a) osvojení si protokolu pro přípravu preparátu pro in vivo mikroskopii a analýzu distribuce fluorescenčních proteinů v semenáčcích A. thaliana b) praktický nácvik infiltrace bakteriální kultury do listů N. benthamiana a příprava mikroskopického preparátu z transientně transformovaných listů. Fluorescenční proteinové markery jako je například GFP a RFP jsou využívány pro analýzu lokalizace proteinů zájmu v buněčných strukturách. Základní princip je takový, že se vytvoří fúzní gen, ve kterém je v totožném čtecím rámci exprimován marker a cílový protein jako jediná molekula. Expresní vektory s fúzními geny jsou u rostlin nejčastěji založené na vnášení T-DNA do rostlinného genomu. V případě semenáčků procházejí rostliny selekčním tlakem na přítomnost transgenu a jsou tak upřednostněni stabilní transformanti. U agroinfiltrace do listů není žádná taková selekce prováděna a pozorujeme pouze transientní expresi, která je po určité době umlčena. Exprimované cílové proteiny jsou lokalizovány podle signálních sekvencí a v místě kumulace pozorujeme po excitaci fluorescenční signál (viz přiložené excitační a emisní spektra GFP a RFP). RFP GFP Dotazy směřujte na nebo 21286@mail.muni.cz
18 Postup při přípravě preparátu pro in vivo mikroskopii a analýze distribuce fluorescenčních proteinů v semenáčcích A. thaliana: Materiál je nutné udržovat ve fyziologicky blízkých podmínkách, proto připravíme tzv. biochamber obsahující rostlinné kultivační medium Murashinge/Skoog (MS). Vzorky jsou uzavřeny biofolií, která propouští vzduch. 1. Oboustranná lepící páska je vystřihnuta do tvaru čtverce, jehož strana je asi 24mm ~ krátké straně krycího skla. V tomto čtverci je pak vyříznuto okénko, jak ukazuje schéma, a páska je nalepena na KRYCÍ sklo. lepící páska lepící páska nalepená na krycím skle 2. Dovnitř tohoto okénka napipetujeme 20µl MS media a vložíme 2-3 dny staré semenáčky Arabidopsis, které byly ve svislé poloze pěstovány na agarové plotně obsahující MS medium. Tyto semenáčky obsahují protein GFP nebo GFP fúzován s AtTRB1 proteinem. 3. Okénko zakryjeme biofolií. 4. Takto připravený preparát je přilepen páskou na nosič obsahující otvor pro cirkulaci vzduchu, a to biofolií směrem do otvoru. Preparát vložíme do mikroskopu krycím sklem směrem k objektivu. V této komůrce semenáčky Arabidopsis rostou až několik dní. 5. Preparát obsahující GFP pozorujeme na fluorescenčním mikroskopu nejdříve v procházejícím světle, následně pak pod filtrem specifickým pro GFP/FITC. Mikroskopie jaderného proteinu AtTRB1 byla provedena v časovém rozmezí asi 2 hod. Každých 30sec byl materiál proskenován v 15-ti optických rovinách odpovídajícím 0,4µm. Dotazy směřujte na nebo 21286@mail.muni.cz
19 Postup při infiltraci bakteriální kultury do listů N. benthamiana a přípravě mikroskopického preparátu z transientně transformovaných listů 1. kolonie agrobakteriálního klonu se odpíchne do 5ml media a kultivuje se do OD600 = Pokud je OD vyšší kultura se na požadovanou koncentraci naředí (cca 24h) 2. napěstovaná kultura se stočí ve výkyvném rotoru (8000 RPM) a pak se rozsuspenduje ve stejném objemu infiltračního media (10mM MES, 10mM MgCl2, ph~5.7, sterilní) 3. pro samotnou infiltraci se kultura smíchá se stejně připraveným pomocným kmenem agromabteria p19 nebo HcPro, které potlačují mechanizmy umlčování genů. Kultury se smíchají v poměru 1:1 a nechají odpočívat 10 min na ledu 4. žlutou špičkou se naruší spodní epidermis listu a 1ml inzulinkou se vlačí bakteriální suspenze do pletiva. Infiltrovaná oblast listu se označí fixou a místo vpichu se prorazí skrz. (Rostliny by měly být 4-6 týdnů vzrostlé, cca 30 cm, dobře zalité před infiltrací a pouze primární listy by měly být infiltrovány. 5. Analýza se provádí po 3 4 dnech buď na listových výsečích nebo sloupnuté epidermis. Dotazy směřujte na nebo 21286@mail.muni.cz
Praktický kurz. Moderní biofyzikální přístupy v experimentální biologii
 Oddělení funkční genomiky a proteomiky Ústav experimentální biologie, Přírodovědecká fakulta Masarykova univerzita Praktický kurz Moderní biofyzikální přístupy v experimentální biologii Místo konání: Brno,
Oddělení funkční genomiky a proteomiky Ústav experimentální biologie, Přírodovědecká fakulta Masarykova univerzita Praktický kurz Moderní biofyzikální přístupy v experimentální biologii Místo konání: Brno,
Pokročilé biofyzikální přístupy v experimentální biologii
 Molekulální komplexy chromatinu CEITEC, Masarykova univerzita Praktický kurz Pokročilé biofyzikální přístupy v experimentální biologii Místo konání: Brno, Univerzitní kampus Bohunice blok A2, seminární
Molekulální komplexy chromatinu CEITEC, Masarykova univerzita Praktický kurz Pokročilé biofyzikální přístupy v experimentální biologii Místo konání: Brno, Univerzitní kampus Bohunice blok A2, seminární
Určení koncentrace proteinu fluorescenční metodou v mikrotitračních destičkách
 Určení koncentrace proteinu fluorescenční metodou v mikrotitračních destičkách Teorie Stanovení celkových proteinů Celkové množství proteinů lze stanovit pomocí několika metod; například: Hartree-Lowryho
Určení koncentrace proteinu fluorescenční metodou v mikrotitračních destičkách Teorie Stanovení celkových proteinů Celkové množství proteinů lze stanovit pomocí několika metod; například: Hartree-Lowryho
1. Příloha 1 Návod úlohy pro Pokročilé praktikum z biochemie I
 1. Příloha 1 Návod úlohy pro Pokročilé praktikum z biochemie I Vazba bromfenolové modři na sérový albumin Princip úlohy Albumin má unikátní vlastnost vázat menší molekuly mnoha typů. Díky struktuře, tvořené
1. Příloha 1 Návod úlohy pro Pokročilé praktikum z biochemie I Vazba bromfenolové modři na sérový albumin Princip úlohy Albumin má unikátní vlastnost vázat menší molekuly mnoha typů. Díky struktuře, tvořené
Praktický kurz Pokročilé biofyzikální přístupy v genomice a proteomice. 12.-13. května 2010
 www.modernibiofyzika.cz Oddělení funkční genomiky a proteomiky Ústav experimentální biologie, Přírodovědecká fakulta Masarykova univerzita Praktický kurz Pokročilé biofyzikální přístupy v genomice a proteomice
www.modernibiofyzika.cz Oddělení funkční genomiky a proteomiky Ústav experimentální biologie, Přírodovědecká fakulta Masarykova univerzita Praktický kurz Pokročilé biofyzikální přístupy v genomice a proteomice
Obsah Protein Gel Electrophoresis Kitu a jeho skladování
 Obsah Protein Gel Electrophoresis Kitu a jeho skladování Protein Gel Electrophoresis Kit obsahuje veškerý potřebný materiál provádění vertikální polyakrilamidové gelové elektroforézy. Experiment provádějí
Obsah Protein Gel Electrophoresis Kitu a jeho skladování Protein Gel Electrophoresis Kit obsahuje veškerý potřebný materiál provádění vertikální polyakrilamidové gelové elektroforézy. Experiment provádějí
2) Připravte si 3 sady po šesti zkumavkách. Do všech zkumavek pipetujte 0.2 ml roztoku BAPNA o různé koncentraci podle tabulky.
 CVIČENÍ Z ENZYMOLOGIE 1) Stanovení Michaelisovy konstanty trypsinu pomocí chromogenního substrátu. Aktivita trypsinu se určí změřením rychlosti hydrolýzy chromogenního substrátu BAPNA (Nα-benzoyl-L-arginin-p-nitroanilid)
CVIČENÍ Z ENZYMOLOGIE 1) Stanovení Michaelisovy konstanty trypsinu pomocí chromogenního substrátu. Aktivita trypsinu se určí změřením rychlosti hydrolýzy chromogenního substrátu BAPNA (Nα-benzoyl-L-arginin-p-nitroanilid)
IZOLACE, SEPARACE A DETEKCE PROTEINŮ I. Vlasta Němcová, Michael Jelínek, Jan Šrámek
 IZOLACE, SEPARACE A DETEKCE PROTEINŮ I Vlasta Němcová, Michael Jelínek, Jan Šrámek Studium aktinu, mikrofilamentární složky cytoskeletu pomocí dvou metod: detekce přímo v buňkách - fluorescenční barvení
IZOLACE, SEPARACE A DETEKCE PROTEINŮ I Vlasta Němcová, Michael Jelínek, Jan Šrámek Studium aktinu, mikrofilamentární složky cytoskeletu pomocí dvou metod: detekce přímo v buňkách - fluorescenční barvení
Pokročilé biofyzikální metody v experimentální biologii
 Pokročilé biofyzikální metody v experimentální biologii Ctirad Hofr 1/1 Proč biofyzikální metody? Biofyzikální metody využívají fyzikální principy ke studiu biologických systémů Poskytují kvantitativní
Pokročilé biofyzikální metody v experimentální biologii Ctirad Hofr 1/1 Proč biofyzikální metody? Biofyzikální metody využívají fyzikální principy ke studiu biologických systémů Poskytují kvantitativní
Tkáňový homogenizátor MagNA Lyser od společnosti Roche
 Izolace RNA Pracovní postup Homogenizace: Pozn. Postup homogenizace platí pouze pro izolaci RNA z nativní tkáně, v případě izolace z buněčné suspenze je tento krok vynechán a začíná se přídavkem homogenizačního
Izolace RNA Pracovní postup Homogenizace: Pozn. Postup homogenizace platí pouze pro izolaci RNA z nativní tkáně, v případě izolace z buněčné suspenze je tento krok vynechán a začíná se přídavkem homogenizačního
SDS polyakrylamidová gelová elektroforéza (SDS PAGE)
 SDS polyakrylamidová gelová elektroforéza (SDS PAGE) Princip SDS polyakrylamidová gelová elektroforéza slouží k separaci proteinů na základě jejich velikosti (molekulové hmotnosti). Zahřátím vzorku za
SDS polyakrylamidová gelová elektroforéza (SDS PAGE) Princip SDS polyakrylamidová gelová elektroforéza slouží k separaci proteinů na základě jejich velikosti (molekulové hmotnosti). Zahřátím vzorku za
Izolace genomové DNA ze savčích buněk, stanovení koncentrace DNA pomocí absorpční spektrofotometrie
 Izolace genomové DNA ze savčích buněk, stanovení koncentrace DNA pomocí absorpční spektrofotometrie IZOLACE GENOMOVÉ DNA Deoxyribonukleová kyselina (DNA) představuje základní genetický materiál většiny
Izolace genomové DNA ze savčích buněk, stanovení koncentrace DNA pomocí absorpční spektrofotometrie IZOLACE GENOMOVÉ DNA Deoxyribonukleová kyselina (DNA) představuje základní genetický materiál většiny
2) Připravte si 7 sad po pěti zkumavkách. Do všech zkumavek pipetujte 0.2 ml roztoku BAPNA o různé koncentraci podle tabulky.
 CVIČENÍ Z ENZYMOLOGIE 1) Stanovení Michaelisovy konstanty trypsinu pomocí chromogenního substrátu. Aktivita trypsinu se určí změřením rychlosti hydrolýzy chromogenního substrátu BAPNA (Nα-benzoyl-L-arginin-p-nitroanilid)
CVIČENÍ Z ENZYMOLOGIE 1) Stanovení Michaelisovy konstanty trypsinu pomocí chromogenního substrátu. Aktivita trypsinu se určí změřením rychlosti hydrolýzy chromogenního substrátu BAPNA (Nα-benzoyl-L-arginin-p-nitroanilid)
SDS-PAGE elektroforéza
 SDS-PAGE elektroforéza Příprava gelu... 1 Recept na 0.75 mm gel (1 gel/2 gely)... 2 Recept na 1.5 mm gel (1 gel/2 gely)... 2 Příprava vzorku... 3 Elektroforéza... 3 Barvení gelů Blue Silver... 4 Chemikálie
SDS-PAGE elektroforéza Příprava gelu... 1 Recept na 0.75 mm gel (1 gel/2 gely)... 2 Recept na 1.5 mm gel (1 gel/2 gely)... 2 Příprava vzorku... 3 Elektroforéza... 3 Barvení gelů Blue Silver... 4 Chemikálie
Absorpční spektroskopie při biologické analýze molekul
 Absorpční spektroskopie při biologické analýze molekul Pokročilé biofyzikální metody v experimentální biologii Ctirad Hofr 8.11.2007 7 1 UV spektroskopie DNA a proteinů Všechny atomy absorbují v UV oblasti
Absorpční spektroskopie při biologické analýze molekul Pokročilé biofyzikální metody v experimentální biologii Ctirad Hofr 8.11.2007 7 1 UV spektroskopie DNA a proteinů Všechny atomy absorbují v UV oblasti
Barevné principy absorpce a fluorescence
 Barevné principy absorpce a fluorescence Pokročilé biofyzikální metody v experimentální biologii Ctirad Hofr 27.9.2007 2 1 Světlo je elektromagnetické vlnění Skládá se z elektrické složky a magnetické
Barevné principy absorpce a fluorescence Pokročilé biofyzikální metody v experimentální biologii Ctirad Hofr 27.9.2007 2 1 Světlo je elektromagnetické vlnění Skládá se z elektrické složky a magnetické
Barevné principy absorpce a fluorescence
 Barevné principy absorpce a fluorescence Pokročilé biofyzikální metody v experimentální biologii Ctirad Hofr Světlo je elektromagnetické vlnění Skládá se z elektrické složky a magnetické složky, které
Barevné principy absorpce a fluorescence Pokročilé biofyzikální metody v experimentální biologii Ctirad Hofr Světlo je elektromagnetické vlnění Skládá se z elektrické složky a magnetické složky, které
Elektroforéza v přítomnosti SDS SDS PAGE
 Elektroforéza v přítomnosti SDS SDS PAGE Elektroforéza v přítomnosti SDS SDS PAGE je jednoduchá, rychlá a reprodukovatelná metoda pro kvalifikovanou charakterizaci a srovnání bílkovin.tato metoda separuje
Elektroforéza v přítomnosti SDS SDS PAGE Elektroforéza v přítomnosti SDS SDS PAGE je jednoduchá, rychlá a reprodukovatelná metoda pro kvalifikovanou charakterizaci a srovnání bílkovin.tato metoda separuje
FLUORIMETRICKÉ STANOVENÍ FLUORESCEINU
 FLUORIMETRICKÉ STANOVENÍ FLUORESCEINU návod vznikl jako součást bakalářské práce Martiny Vidrmanové Fluorimetrie s využitím spektrofotometru SpectroVis Plus firmy Vernier (http://is.muni.cz/th/268973/prif_b/bakalarska_prace.pdf)
FLUORIMETRICKÉ STANOVENÍ FLUORESCEINU návod vznikl jako součást bakalářské práce Martiny Vidrmanové Fluorimetrie s využitím spektrofotometru SpectroVis Plus firmy Vernier (http://is.muni.cz/th/268973/prif_b/bakalarska_prace.pdf)
Cvičení ke kurzu Obecná ekotoxikologie. Úloha A - Stanovení ekotoxicity v testu klíčení rostlin
 Cvičení ke kurzu Obecná ekotoxikologie Nutné potřeby, které studenti přinesou s sebou do cvičení: - Tento návod - Poznámkový sešit, psací potřeby - Nůžky - Pravítko (s milimetrovým rozlišením) - Přezůvky
Cvičení ke kurzu Obecná ekotoxikologie Nutné potřeby, které studenti přinesou s sebou do cvičení: - Tento návod - Poznámkový sešit, psací potřeby - Nůžky - Pravítko (s milimetrovým rozlišením) - Přezůvky
ÚSTAV ORGANICKÉ TECHNOLOGIE
 LABORATOŘ OBORU I ÚSTAV ORGANICKÉ TECHNOLOGIE (111) F Imobilizace na alumosilikátové materiály Vedoucí práce: Ing. Eliška Leitmannová, Ph.D. Umístění práce: laboratoř F07, F08 1 Úvod Imobilizace aktivních
LABORATOŘ OBORU I ÚSTAV ORGANICKÉ TECHNOLOGIE (111) F Imobilizace na alumosilikátové materiály Vedoucí práce: Ing. Eliška Leitmannová, Ph.D. Umístění práce: laboratoř F07, F08 1 Úvod Imobilizace aktivních
Stanovení koncentrace (kvantifikace) proteinů
 Stanovení koncentrace (kvantifikace) proteinů Bioanalytické metody Prof. RNDr. Pavel Peč, CSc. Úvod Kritéria výběru metod stanovení koncentrace proteinů jsou založena na možnostech pro vlastní analýzu,
Stanovení koncentrace (kvantifikace) proteinů Bioanalytické metody Prof. RNDr. Pavel Peč, CSc. Úvod Kritéria výběru metod stanovení koncentrace proteinů jsou založena na možnostech pro vlastní analýzu,
DIAGNOSTICKÝ KIT PRO DETEKCI MINIMÁLNÍ REZIDUÁLNÍ CHOROBY U KOLOREKTÁLNÍHO KARCINOMU
 Úvod IntellMed, s.r.o., Václavské náměstí 820/41, 110 00 Praha 1 DIAGNOSTICKÝ KIT PRO DETEKCI MINIMÁLNÍ REZIDUÁLNÍ CHOROBY U KOLOREKTÁLNÍHO KARCINOMU Jednou z nejvhodnějších metod pro detekci minimální
Úvod IntellMed, s.r.o., Václavské náměstí 820/41, 110 00 Praha 1 DIAGNOSTICKÝ KIT PRO DETEKCI MINIMÁLNÍ REZIDUÁLNÍ CHOROBY U KOLOREKTÁLNÍHO KARCINOMU Jednou z nejvhodnějších metod pro detekci minimální
Oborový workshop pro SŠ CHEMIE
 PRAKTICKÁ VÝUKA PŘÍRODOVĚDNÝCH PŘEDMĚTŮ NA ZŠ A SŠ CZ.1.07/1.1.30/02.0024 Tento projekt je spolufinancován Evropským sociálním fondem a státním rozpočtem České republiky. Oborový workshop pro SŠ CHEMIE
PRAKTICKÁ VÝUKA PŘÍRODOVĚDNÝCH PŘEDMĚTŮ NA ZŠ A SŠ CZ.1.07/1.1.30/02.0024 Tento projekt je spolufinancován Evropským sociálním fondem a státním rozpočtem České republiky. Oborový workshop pro SŠ CHEMIE
Ústřední komise Chemické olympiády. 55. ročník 2018/2019 NÁRODNÍ KOLO. Kategorie E. Zadání praktické části Úloha 2 (30 bodů)
 Ústřední komise Chemické olympiády 55. ročník 2018/2019 NÁRODNÍ KOLO Kategorie E Zadání praktické části Úloha 2 (30 bodů) PRAKTICKÁ ČÁST 30 BODŮ Úloha 2 Stanovení Cu 2+ spektrofotometricky 30 bodů Cu 2+
Ústřední komise Chemické olympiády 55. ročník 2018/2019 NÁRODNÍ KOLO Kategorie E Zadání praktické části Úloha 2 (30 bodů) PRAKTICKÁ ČÁST 30 BODŮ Úloha 2 Stanovení Cu 2+ spektrofotometricky 30 bodů Cu 2+
7. Měření fluorescence při excitaci kontinuálním světlem ( steady-state )
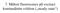 7. Měření fluorescence při excitaci kontinuálním světlem ( steady-state ) Steady-state měření Excitujeme kontinuálním světlem, měříme intenzitu emise (počet emitovaných fotonů) Obvykle nedetekujeme všechny
7. Měření fluorescence při excitaci kontinuálním světlem ( steady-state ) Steady-state měření Excitujeme kontinuálním světlem, měříme intenzitu emise (počet emitovaných fotonů) Obvykle nedetekujeme všechny
Western blotting. 10% APS 20,28 µl 40,56 µl 81,12 µl 20,28 µl 40,56 µl 81,12 µl
 Western blotting 1. Příprava gelu složení aparatury hustotu gelu volit podle velikosti proteinů příprava rozdělovacího gelu: 10% 12% počet gelů 1 2 4 1 2 4 objem 6 ml 12 ml 24 ml 6 ml 12 ml 24 ml 40% akrylamid
Western blotting 1. Příprava gelu složení aparatury hustotu gelu volit podle velikosti proteinů příprava rozdělovacího gelu: 10% 12% počet gelů 1 2 4 1 2 4 objem 6 ml 12 ml 24 ml 6 ml 12 ml 24 ml 40% akrylamid
Sbohem, paní Bradfordová
 Sbohem, paní Bradfordová aneb IČ spektroskopie ve službách kvantifikace proteinů Mgr. Stanislav Kukla Merck spol. s r. o. Agenda 1 Zhodnocení současných možností kvantifikace proteinů Bradfordové metoda
Sbohem, paní Bradfordová aneb IČ spektroskopie ve službách kvantifikace proteinů Mgr. Stanislav Kukla Merck spol. s r. o. Agenda 1 Zhodnocení současných možností kvantifikace proteinů Bradfordové metoda
Braf V600E StripAssay
 Braf V600E StripAssay Kat. číslo 5-570 20 testů 2-8 C Popis stripu: Pracovní postup 1. Izolace DNA Pro izolaci čerstvých nebo mražených biopsií použijte soupravy Qiagen QIAmp DNA Mini nebo Micro. Pro izolaci
Braf V600E StripAssay Kat. číslo 5-570 20 testů 2-8 C Popis stripu: Pracovní postup 1. Izolace DNA Pro izolaci čerstvých nebo mražených biopsií použijte soupravy Qiagen QIAmp DNA Mini nebo Micro. Pro izolaci
DIAGNOSTICKÝ KIT PRO DETEKCI MINIMÁLNÍ REZIDUÁLNÍ CHOROBY U KARCINOMU PANKREATU
 Úvod IntellMed, s.r.o., Václavské náměstí 820/41, 110 00 Praha 1 DIAGNOSTICKÝ KIT PRO DETEKCI MINIMÁLNÍ REZIDUÁLNÍ CHOROBY U KARCINOMU PANKREATU Jednou z nejvhodnějších metod pro detekci minimální reziduální
Úvod IntellMed, s.r.o., Václavské náměstí 820/41, 110 00 Praha 1 DIAGNOSTICKÝ KIT PRO DETEKCI MINIMÁLNÍ REZIDUÁLNÍ CHOROBY U KARCINOMU PANKREATU Jednou z nejvhodnějších metod pro detekci minimální reziduální
fenanthrolinem Příprava
 1 ÚLOHA 9: Spektrofotometrické fenanthrolinem studium komplexu Fe(II) s 1,10- Příprava 2. 3. 4. 5. 6. Zopakujte si základní pojmy z optiky - elektromagnetické záření a jeho šíření absorbujícím prostředím,
1 ÚLOHA 9: Spektrofotometrické fenanthrolinem studium komplexu Fe(II) s 1,10- Příprava 2. 3. 4. 5. 6. Zopakujte si základní pojmy z optiky - elektromagnetické záření a jeho šíření absorbujícím prostředím,
Jednotné pracovní postupy zkoušení krmiv
 Národní referenční laboratoř Strana KVANTITATIVNÍ STANOVENÍ GENETICKÝCH MODIFIKACÍ METODOU qpcr POMOCÍ ROTOR-GENE PROBE PCR KITU Účel a rozsah Postup slouží ke kvantitativnímu stanovení genetických modifikací
Národní referenční laboratoř Strana KVANTITATIVNÍ STANOVENÍ GENETICKÝCH MODIFIKACÍ METODOU qpcr POMOCÍ ROTOR-GENE PROBE PCR KITU Účel a rozsah Postup slouží ke kvantitativnímu stanovení genetických modifikací
TESTOVÁNÍ GMO Praktikum fyziologie rostlin
 Teoretický úvod: TESTOVÁNÍ GMO Praktikum fyziologie rostlin 1 Teoretický úvod: TESTOVÁNÍ GMO Obecně na úvod Určitě jste už slyšeli pojem geneticky modifikovaný organismus (GMO). Úprava vlastností přirozeně
Teoretický úvod: TESTOVÁNÍ GMO Praktikum fyziologie rostlin 1 Teoretický úvod: TESTOVÁNÍ GMO Obecně na úvod Určitě jste už slyšeli pojem geneticky modifikovaný organismus (GMO). Úprava vlastností přirozeně
S filtračními papíry a membránou je nutno manipulovat pinzetou s tupým koncem.
 Western Blotting Příprava blotovacího sendviče... 1 Blotování... 2 Kontrola přenesení proteinů na membránu... 2 Blokování membrány... 2 Aplikace protilátek... 2 Vizualizace... 3 Vyvolání filmu... 4 Chemikálie
Western Blotting Příprava blotovacího sendviče... 1 Blotování... 2 Kontrola přenesení proteinů na membránu... 2 Blokování membrány... 2 Aplikace protilátek... 2 Vizualizace... 3 Vyvolání filmu... 4 Chemikálie
Jednotné pracovní postupy zkoušení krmiv STANOVENÍ OBSAHU DEKOCHINÁTU METODOU HPLC
 Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU DEKOCHINÁTU METODOU HPLC 1 Rozsah a účel Tato metoda specifikuje podmínky pro stanovení dekochinátu metodou vysokoúčinné kapalinové chromatografie
Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU DEKOCHINÁTU METODOU HPLC 1 Rozsah a účel Tato metoda specifikuje podmínky pro stanovení dekochinátu metodou vysokoúčinné kapalinové chromatografie
Kurz 1 Úvod k biochemickému praktiku
 Kurz 1 Úvod k biochemickému praktiku Pavla Balínová http://vyuka.lf3.cuni.cz/ Důležité informace Kroužkový asistent: RNDr. Pavla Balínová e-mailová adresa: pavla.balinova@lf3.cuni.cz místnost: 410 studijní
Kurz 1 Úvod k biochemickému praktiku Pavla Balínová http://vyuka.lf3.cuni.cz/ Důležité informace Kroužkový asistent: RNDr. Pavla Balínová e-mailová adresa: pavla.balinova@lf3.cuni.cz místnost: 410 studijní
METODY STUDIA PROTEINŮ
 METODY STUDIA PROTEINŮ Mgr. Vlasta Němcová vlasta.furstova@tiscali.cz OBSAH PŘEDNÁŠKY 1) Stanovení koncentrace proteinu 2) Stanovení AMK sekvence proteinu Hmotnostní spektrometrie Edmanovo odbourávání
METODY STUDIA PROTEINŮ Mgr. Vlasta Němcová vlasta.furstova@tiscali.cz OBSAH PŘEDNÁŠKY 1) Stanovení koncentrace proteinu 2) Stanovení AMK sekvence proteinu Hmotnostní spektrometrie Edmanovo odbourávání
Column DNA Lego Kit UNIVERZÁLNÍ SOUPRAVY PRO RYCHLOU IZOLACI ČISTÉ DNA (Katalogové číslo D201 + D202)
 Column DNA Lego Kit UNIVERZÁLNÍ SOUPRAVY PRO RYCHLOU IZOLACI ČISTÉ DNA (Katalogové číslo D201 + D202) Popis Column DNA Lego Kit je základ moderní stavebnicové (Lego) soupravy pro izolaci čisté DNA různého
Column DNA Lego Kit UNIVERZÁLNÍ SOUPRAVY PRO RYCHLOU IZOLACI ČISTÉ DNA (Katalogové číslo D201 + D202) Popis Column DNA Lego Kit je základ moderní stavebnicové (Lego) soupravy pro izolaci čisté DNA různého
Bakteriální bioluminiscenční test. Stanovení účinnosti čištění odpadních vod pomocí bakteriálního bioluminiscenčního testu
 Bakteriální bioluminiscenční test Stanovení účinnosti čištění odpadních vod pomocí bakteriálního bioluminiscenčního testu BBTT Cíl: Stanovit účinek odpadních vod na bakterie Vibrio fischeri. Principem
Bakteriální bioluminiscenční test Stanovení účinnosti čištění odpadních vod pomocí bakteriálního bioluminiscenčního testu BBTT Cíl: Stanovit účinek odpadních vod na bakterie Vibrio fischeri. Principem
Identifikace mikroorganismů pomocí sekvence jejich genu pro 16S rrna
 Praktická úloha Identifikace mikroorganismů pomocí sekvence jejich genu pro 16S rrna Pro spolehlivou identifikaci mikroorganismů pomocí genetických metod se velmi často využívá stanovení nukleotidové sekvence
Praktická úloha Identifikace mikroorganismů pomocí sekvence jejich genu pro 16S rrna Pro spolehlivou identifikaci mikroorganismů pomocí genetických metod se velmi často využívá stanovení nukleotidové sekvence
NRAS StripAssay. Kat. číslo 5-610. 20 testů 2-8 C
 NRAS StripAssay Kat. číslo 5-610 20 testů 2-8 C Popis stripu: Pracovní postup 1. Izolace DNA Pro izolaci DNA musí být použita vhodná metoda vzhledem k typu tkáně vzorku. Pro doporučení vhodné metody kontaktujte
NRAS StripAssay Kat. číslo 5-610 20 testů 2-8 C Popis stripu: Pracovní postup 1. Izolace DNA Pro izolaci DNA musí být použita vhodná metoda vzhledem k typu tkáně vzorku. Pro doporučení vhodné metody kontaktujte
Polymorfismus délky restrikčních fragmentů (RFLP)
 ÚSTAV LÉKAŘSKÉ BIOCHEMIE A LABORATORNÍ DIAGNOSTIKY 1. LF UK Polymorfismus délky restrikčních fragmentů (RFLP) Praktické cvičení z lékařské biochemie Všeobecné lékařství Martin Vejražka 2017/18 Obsah POLYMORFISMUS
ÚSTAV LÉKAŘSKÉ BIOCHEMIE A LABORATORNÍ DIAGNOSTIKY 1. LF UK Polymorfismus délky restrikčních fragmentů (RFLP) Praktické cvičení z lékařské biochemie Všeobecné lékařství Martin Vejražka 2017/18 Obsah POLYMORFISMUS
Úvod. Náplň práce. Úkoly
 Název práce: Zkouška disoluce pevných lékových forem Vedoucí práce: Doc. Ing. Petr Zámostný, Ph.D. Jméno zástupce: Ing. Jan Patera Umístění práce: S25b Úvod Uvolňování léčiva z tuhých perorálních lékových
Název práce: Zkouška disoluce pevných lékových forem Vedoucí práce: Doc. Ing. Petr Zámostný, Ph.D. Jméno zástupce: Ing. Jan Patera Umístění práce: S25b Úvod Uvolňování léčiva z tuhých perorálních lékových
1. Metodika. Protokol č. F1-4 Metodika: Srovnávací analýza efektivity přípravy rekombinantního proteinu ve fermentoru
 Protokol č.: F1-4 Datum: 20.12.2010 Metodika: analýza efektivity přípravy výběr z výsledků ze zkušebních provozů výroby antigenů. Vypracoval: Ing. Václav Filištein, Mgr. Tereza Chrudimská, Spolupracující
Protokol č.: F1-4 Datum: 20.12.2010 Metodika: analýza efektivity přípravy výběr z výsledků ze zkušebních provozů výroby antigenů. Vypracoval: Ing. Václav Filištein, Mgr. Tereza Chrudimská, Spolupracující
EGFR XL StripAssay. Kat. číslo 5-630. 20 testů 2-8 C
 EGFR XL StripAssay Kat. číslo 5-630 20 testů 2-8 C Popis stripu Pracovní postup 1. Izolace DNA Pro izolaci DNA použijte vhodný izolační kit. Doporučené kity jsou následující: Pro izolaci čerstvých nebo
EGFR XL StripAssay Kat. číslo 5-630 20 testů 2-8 C Popis stripu Pracovní postup 1. Izolace DNA Pro izolaci DNA použijte vhodný izolační kit. Doporučené kity jsou následující: Pro izolaci čerstvých nebo
Fluorescenční mikroskopie
 Fluorescenční mikroskopie Pokročilé biofyzikální metody v experimentální biologii Ctirad Hofr 1 VYUŽITÍ FLUORESCENCE, PŘÍMÁ FLUORESCENCE, PŘÍMÁ A NEPŘÍMA IMUNOFLUORESCENCE, BIOTIN-AVIDINOVÁ METODA IMUNOFLUORESCENCE
Fluorescenční mikroskopie Pokročilé biofyzikální metody v experimentální biologii Ctirad Hofr 1 VYUŽITÍ FLUORESCENCE, PŘÍMÁ FLUORESCENCE, PŘÍMÁ A NEPŘÍMA IMUNOFLUORESCENCE, BIOTIN-AVIDINOVÁ METODA IMUNOFLUORESCENCE
Moderní nástroje pro zobrazování biologicky významných molekul pro zajištění zdraví. René Kizek
 Moderní nástroje pro zobrazování biologicky významných molekul pro zajištění zdraví René Kizek 12.04.2013 Fluorescence je fyzikálně chemický děj, který je typem luminiscence. Luminiscence se dále dělí
Moderní nástroje pro zobrazování biologicky významných molekul pro zajištění zdraví René Kizek 12.04.2013 Fluorescence je fyzikálně chemický děj, který je typem luminiscence. Luminiscence se dále dělí
Izolace nukleových kyselin
 Izolace nukleových kyselin Požadavky na izolaci nukleových kyselin V nativním stavu z přirozeného materiálu v dostatečném množství požadované čistotě. Nukleové kyseliny je třeba zbavit všech látek, které
Izolace nukleových kyselin Požadavky na izolaci nukleových kyselin V nativním stavu z přirozeného materiálu v dostatečném množství požadované čistotě. Nukleové kyseliny je třeba zbavit všech látek, které
Mikrokalorimetrie. Izotermální titrační mikrokalorimetrie
 Labolatoř molekulárních komplexů chromatinu CEITEC a Přírodovědecká fakulta, Masarykova univerzita www.modernibiofyzika.cz Praktický kurz Pokročilé biofyzikální přístupy v genomice a proteomice 30. května
Labolatoř molekulárních komplexů chromatinu CEITEC a Přírodovědecká fakulta, Masarykova univerzita www.modernibiofyzika.cz Praktický kurz Pokročilé biofyzikální přístupy v genomice a proteomice 30. května
IZOLACE DNA (KIT DNeasy Plant Mini)
 17.1 Izolace DNA (kit DNeasy Plant Mini) Strana 1 IZOLACE DNA (KIT DNeasy Plant Mini) 1 Účel a rozsah Postup slouží k získání deoxyribonukleové kyseliny (DNA) ze vzorku pomocí komerčního kitu DNeasy Plant
17.1 Izolace DNA (kit DNeasy Plant Mini) Strana 1 IZOLACE DNA (KIT DNeasy Plant Mini) 1 Účel a rozsah Postup slouží k získání deoxyribonukleové kyseliny (DNA) ze vzorku pomocí komerčního kitu DNeasy Plant
SPEKTROSKOPICKÉ VLASTNOSTI LÁTEK (ZÁKLADY SPEKTROSKOPIE)
 SPEKTROSKOPICKÉ VLASTNOSTI LÁTEK (ZÁKLADY SPEKTROSKOPIE) Elektromagnetické vlnění SVĚTLO Charakterizace záření Vlnová délka - (λ) : jednotky: m (obvykle nm) λ Souvisí s povahou fotonu Charakterizace záření
SPEKTROSKOPICKÉ VLASTNOSTI LÁTEK (ZÁKLADY SPEKTROSKOPIE) Elektromagnetické vlnění SVĚTLO Charakterizace záření Vlnová délka - (λ) : jednotky: m (obvykle nm) λ Souvisí s povahou fotonu Charakterizace záření
cdna synthesis kit First-Strand cdna Synthesis System Verze 1.2
 cdna synthesis kit First-Strand cdna Synthesis System Verze 1.2 Obsah soupravy a její skladování Tato souprava pro reverzní transkripci obsahuje reagencie potřebné k provedení reverzní transkripce (RT)
cdna synthesis kit First-Strand cdna Synthesis System Verze 1.2 Obsah soupravy a její skladování Tato souprava pro reverzní transkripci obsahuje reagencie potřebné k provedení reverzní transkripce (RT)
Fluorescenční rezonanční přenos energie
 Fluorescenční rezonanční přenos energie Pokročilé biofyzikální metody v experimentální biologii Ctirad Hofr 1 Přenos excitační energie Přenos elektronové energie se uskutečňuje mechanismy zářivými nebo
Fluorescenční rezonanční přenos energie Pokročilé biofyzikální metody v experimentální biologii Ctirad Hofr 1 Přenos excitační energie Přenos elektronové energie se uskutečňuje mechanismy zářivými nebo
DIAGNOSTICKÝ KIT PRO DETEKCI MINIMÁLNÍ REZIUDÁLNÍ CHOROBY MRD EGFR
 Úvod IntellMed, s.r.o., Václavské náměstí 820/41, 110 00 Praha 1 DIAGNOSTICKÝ KIT PRO DETEKCI MINIMÁLNÍ REZIUDÁLNÍ CHOROBY MRD EGFR Jednou z nejvhodnějších metod pro detekci minimální reziduální choroby
Úvod IntellMed, s.r.o., Václavské náměstí 820/41, 110 00 Praha 1 DIAGNOSTICKÝ KIT PRO DETEKCI MINIMÁLNÍ REZIUDÁLNÍ CHOROBY MRD EGFR Jednou z nejvhodnějších metod pro detekci minimální reziduální choroby
Téma: Testy životaschopnosti a Počítání buněk
 LRR/BUBV vičení z buněčné biologie Úloha č. 3 Téma: Testy životaschopnosti a Počítání Úvod: Při práci s buňkami je jedním ze základních sledovaných parametrů stanovení jejich životaschopnosti (viability).
LRR/BUBV vičení z buněčné biologie Úloha č. 3 Téma: Testy životaschopnosti a Počítání Úvod: Při práci s buňkami je jedním ze základních sledovaných parametrů stanovení jejich životaschopnosti (viability).
Anizotropie fluorescence
 Anizotropie fluorescence Pokročilé biofyzikální metody v experimentální biologii Ctirad Hofr 6 1 Jev anizotropie Jestliže dochází k excitaci světlem kmitajícím v jedné rovině, emise fluorescence se často
Anizotropie fluorescence Pokročilé biofyzikální metody v experimentální biologii Ctirad Hofr 6 1 Jev anizotropie Jestliže dochází k excitaci světlem kmitajícím v jedné rovině, emise fluorescence se často
KOMPLEXY EUROPIA(III) LUMINISCENČNÍ VLASTNOSTI A VYUŽITÍ V ANALYTICKÉ CHEMII. Pavla Pekárková
 KOMPLEXY EUROPIA(III) LUMINISCENČNÍ VLASTNOSTI A VYUŽITÍ V ANALYTICKÉ CHEMII Pavla Pekárková Katedra analytické chemie, Přírodovědecká fakulta, Masarykova univerzita, Kotlářská 2, 611 37 Brno E-mail: 78145@mail.muni.cz
KOMPLEXY EUROPIA(III) LUMINISCENČNÍ VLASTNOSTI A VYUŽITÍ V ANALYTICKÉ CHEMII Pavla Pekárková Katedra analytické chemie, Přírodovědecká fakulta, Masarykova univerzita, Kotlářská 2, 611 37 Brno E-mail: 78145@mail.muni.cz
Spektroskopie v UV-VIS oblasti. UV-VIS spektroskopie. Roztok KMnO 4. pracuje nejčastěji v oblasti 200-800 nm
 Spektroskopie v UV-VIS oblasti UV-VIS spektroskopie pracuje nejčastěji v oblasti 2-8 nm lze měřit i < 2 nm či > 8 nm UV VIS IR Ultra Violet VISible Infra Red Roztok KMnO 4 roztok KMnO 4 je červenofialový
Spektroskopie v UV-VIS oblasti UV-VIS spektroskopie pracuje nejčastěji v oblasti 2-8 nm lze měřit i < 2 nm či > 8 nm UV VIS IR Ultra Violet VISible Infra Red Roztok KMnO 4 roztok KMnO 4 je červenofialový
Sure-MeDIP I. with magnetic beads and MNase. www.krd.cz
 Sure-MeDIP I with magnetic beads and MNase www.krd.cz 1 Obsah soupravy a skladování MeDIP souprava obsahuje reagencie na provedení 25 reakcí. Souprava je rozdělen do dvou částí, jedna je distribuována
Sure-MeDIP I with magnetic beads and MNase www.krd.cz 1 Obsah soupravy a skladování MeDIP souprava obsahuje reagencie na provedení 25 reakcí. Souprava je rozdělen do dvou částí, jedna je distribuována
α-globin StripAssay Kat. číslo 4-160 10 testů 2-8 C
 α-globin StripAssay Kat. číslo 4-160 10 testů 2-8 C Popis stripů: Pracovní postup Izolace DNA Doporučujeme použít následující kit pro izolaci DNA z plné krve nebo jiných typů vzorků: Spin Micro DNA Extraction
α-globin StripAssay Kat. číslo 4-160 10 testů 2-8 C Popis stripů: Pracovní postup Izolace DNA Doporučujeme použít následující kit pro izolaci DNA z plné krve nebo jiných typů vzorků: Spin Micro DNA Extraction
Fluorescenční sondy. Fluorescenční sondy. Indikátory pro anorganické ionty. Fluorescenční sondy pro využití v analytické chemii, medicíně a biologii
 Fluorescenční sondy Fluorescenční sondy vnější fluorofory, které se ke sledovaným molekulám, iontům, atd. váží nekovalentní vazbou změna fluorescenční vlastností (intenzita emise, posun emisního maxima,
Fluorescenční sondy Fluorescenční sondy vnější fluorofory, které se ke sledovaným molekulám, iontům, atd. váží nekovalentní vazbou změna fluorescenční vlastností (intenzita emise, posun emisního maxima,
ÚLOHA C Klonování PCR produktu do plasmidu
 Jméno a učo: Datum: ÚLOHA C Klonování PCR produktu do plasmidu TEORETICKÝ ÚVOD Při klonování PCR produktů do plasmidů se využívá vlastnosti Taq polymerasy, a jiných non-proofreading polymeras, přidávat
Jméno a učo: Datum: ÚLOHA C Klonování PCR produktu do plasmidu TEORETICKÝ ÚVOD Při klonování PCR produktů do plasmidů se využívá vlastnosti Taq polymerasy, a jiných non-proofreading polymeras, přidávat
PLANÁRNÍ (PLOŠNÁ) CHROMATOGRAFIE
 PLANÁRNÍ (PLOŠNÁ) CHROMATOGRAFIE Tenkovrstvá chromatografie je technika pro identifikaci a separaci směsi organických látek Identifikace složek směsi (nutné použít standard) analysa frakcí sbíraných během
PLANÁRNÍ (PLOŠNÁ) CHROMATOGRAFIE Tenkovrstvá chromatografie je technika pro identifikaci a separaci směsi organických látek Identifikace složek směsi (nutné použít standard) analysa frakcí sbíraných během
kovem. reakce probíhá u řady
 Spektrometrická analýza CÍL CVIČENÍ a) Zvládnout obsluhu automatizovaného spektrometru, sledování kinetiky enzymové reakce a inhibice enzymové aktivity těžkým kovem. b) Zvládnout základy spektrometrické
Spektrometrická analýza CÍL CVIČENÍ a) Zvládnout obsluhu automatizovaného spektrometru, sledování kinetiky enzymové reakce a inhibice enzymové aktivity těžkým kovem. b) Zvládnout základy spektrometrické
Stanovení α-amylázy v moči
 Stanovení α-amylázy v moči α-amyláza je produkována především pankreatem a také ve slinných žlázách a normálně je odváděna do zažívacího traktu. Do krve se dostává fyziologicky jen nepatrné množství. Vzhledem
Stanovení α-amylázy v moči α-amyláza je produkována především pankreatem a také ve slinných žlázách a normálně je odváděna do zažívacího traktu. Do krve se dostává fyziologicky jen nepatrné množství. Vzhledem
Metoda Live/Dead aneb využití fluorescenční mikroskopie v bioaugmentační praxi. Juraj Grígel Inovativní sanační technologie ve výzkumu a praxi
 Metoda Live/Dead aneb využití fluorescenční mikroskopie v bioaugmentační praxi Juraj Grígel Inovativní sanační technologie ve výzkumu a praxi Co je to vlastně ta fluorescence? Některé látky (fluorofory)
Metoda Live/Dead aneb využití fluorescenční mikroskopie v bioaugmentační praxi Juraj Grígel Inovativní sanační technologie ve výzkumu a praxi Co je to vlastně ta fluorescence? Některé látky (fluorofory)
FLUORESCENČNÍ MIKROSKOP
 FLUORESCENČNÍ MIKROSKOP na gymnáziu Pierra de Coubertina v Táboře Pavla Trčková, kabinet Biologie, GPdC Tábor Co je fluorescence Fluorescence je jev spočívající v tom, že některé látky (fluorofory) po
FLUORESCENČNÍ MIKROSKOP na gymnáziu Pierra de Coubertina v Táboře Pavla Trčková, kabinet Biologie, GPdC Tábor Co je fluorescence Fluorescence je jev spočívající v tom, že některé látky (fluorofory) po
Praktický kurz Pokročilé biofyzikální přístupy v genomice a proteomice května 2011
 www.modernibiofyzika.cz Oddělení funkční genomiky a proteomiky Ústav experimentální biologie, Přírodovědecká fakulta Masarykova univerzita Praktický kurz Pokročilé biofyzikální přístupy v genomice a proteomice
www.modernibiofyzika.cz Oddělení funkční genomiky a proteomiky Ústav experimentální biologie, Přírodovědecká fakulta Masarykova univerzita Praktický kurz Pokročilé biofyzikální přístupy v genomice a proteomice
Využití a princip fluorescenční mikroskopie
 Využití a princip fluorescenční mikroskopie fyzikálně chemický děj Fluorescence typem luminiscence (elektroluminiscence, fotoluminiscence, radioluminiscence a chemiluminiscenci) patří mezi fotoluminiscenční
Využití a princip fluorescenční mikroskopie fyzikálně chemický děj Fluorescence typem luminiscence (elektroluminiscence, fotoluminiscence, radioluminiscence a chemiluminiscenci) patří mezi fotoluminiscenční
MagPurix Viral/Pathogen Nucleic Acids Extraction Kit B
 MagPurix Viral/Pathogen Nucleic Acids Extraction Kit B Kat. č. ZP02012 Doba zpracování: 45-60 minut pro MagPurix 12S 45-65 minut pro MagPurix 24 Použití Souprava MagPurix Viral/Pathogen Nucleic Acids Extraction
MagPurix Viral/Pathogen Nucleic Acids Extraction Kit B Kat. č. ZP02012 Doba zpracování: 45-60 minut pro MagPurix 12S 45-65 minut pro MagPurix 24 Použití Souprava MagPurix Viral/Pathogen Nucleic Acids Extraction
INFRAČERVENÁ SPEKTROMETRIE A BIOSLOŽKY PALIV
 VYSOKÁ ŠKOLA CHEMICKO-TECHNOLOGICKÁ V PRAZE Fakulta technologie ochrany prostředí Ústav technologie ropy a alternativních paliv INFRAČERVENÁ SPEKTROMETRIE A BIOSLOŽKY PALIV Laboratorní cvičení ÚVOD V několika
VYSOKÁ ŠKOLA CHEMICKO-TECHNOLOGICKÁ V PRAZE Fakulta technologie ochrany prostředí Ústav technologie ropy a alternativních paliv INFRAČERVENÁ SPEKTROMETRIE A BIOSLOŽKY PALIV Laboratorní cvičení ÚVOD V několika
SPEKTROFOTOMETR (NÁVOD K OBSLUZE)
 SPEKTROFOTOMETR (NÁVOD K OBSLUZE) 1. Obecná charakteristika spektrofotometru Spektrofotometr umožňuje stanovovat vlastnosti vzorku, např. koncentrace určité látky v roztoku, na základě pohlcování světla
SPEKTROFOTOMETR (NÁVOD K OBSLUZE) 1. Obecná charakteristika spektrofotometru Spektrofotometr umožňuje stanovovat vlastnosti vzorku, např. koncentrace určité látky v roztoku, na základě pohlcování světla
Práce se spektrometrem SpectroVis Plus Vernier
 informace pro učitele Práce se spektrometrem SpectroVis Plus Vernier Aleš Mareček Kvinta úloha Měřené veličiny Přístroj SpectroVis Plus umožní studovat viditelnou část spektra a část blízké infračervené
informace pro učitele Práce se spektrometrem SpectroVis Plus Vernier Aleš Mareček Kvinta úloha Měřené veličiny Přístroj SpectroVis Plus umožní studovat viditelnou část spektra a část blízké infračervené
LRR/BUBCV CVIČENÍ Z BUNĚČNÉ BIOLOGIE 3. TESTY ŽIVOTASCHOPNOSTI A POČÍTÁNÍ BUNĚK
 LRR/BUBCV CVIČEÍ Z BUĚČÉ BILGIE 3. TESTY ŽIVTASCHPSTI A PČÍTÁÍ BUĚK TERETICKÝ ÚVD: Při práci s buňkami je jedním ze základních sledovaných parametrů stanovení jejich životaschopnosti (viability). Tímto
LRR/BUBCV CVIČEÍ Z BUĚČÉ BILGIE 3. TESTY ŽIVTASCHPSTI A PČÍTÁÍ BUĚK TERETICKÝ ÚVD: Při práci s buňkami je jedním ze základních sledovaných parametrů stanovení jejich životaschopnosti (viability). Tímto
Základy fotometrie, využití v klinické biochemii
 Základy fotometrie, využití v klinické biochemii Základní vztahy ve fotometrii transmitance (propustnost): T = I / I 0 absorbance: A = log (I 0 / I) = log (1 / T) = log T Lambertův-Beerův zákon A l = e
Základy fotometrie, využití v klinické biochemii Základní vztahy ve fotometrii transmitance (propustnost): T = I / I 0 absorbance: A = log (I 0 / I) = log (1 / T) = log T Lambertův-Beerův zákon A l = e
Derivační spektrofotometrie a rozklad absorpčního spektra
 Derivační spektrofotometrie a rozklad absorpčního spektra Teorie: Derivační spektrofotometrie, využívající derivace absorpční křivky, je obecně používanou metodou pro zvýraznění detailů průběhu záznamu,
Derivační spektrofotometrie a rozklad absorpčního spektra Teorie: Derivační spektrofotometrie, využívající derivace absorpční křivky, je obecně používanou metodou pro zvýraznění detailů průběhu záznamu,
Úvod k biochemickému. mu praktiku. Vladimíra Kvasnicová
 Úvod k biochemickému mu praktiku Vladimíra Kvasnicová organizace praktik pravidla bezpečné práce v laboratoři laboratorní vybavení práce s automatickou pipetou návody: viz. aplikace Výuka automatická pipeta
Úvod k biochemickému mu praktiku Vladimíra Kvasnicová organizace praktik pravidla bezpečné práce v laboratoři laboratorní vybavení práce s automatickou pipetou návody: viz. aplikace Výuka automatická pipeta
PROTOKOL WESTERN BLOT
 WESTERN BLOT 1. PŘÍPRAVA ELEKTROFORETICKÉ APARATURY Saponátem a vodou se důkladně umyjí skla, plastové vložky a hřebínek, poté se důkladně opláchnou deionizovanou/destilovanou vodou a etanolem a nechají
WESTERN BLOT 1. PŘÍPRAVA ELEKTROFORETICKÉ APARATURY Saponátem a vodou se důkladně umyjí skla, plastové vložky a hřebínek, poté se důkladně opláchnou deionizovanou/destilovanou vodou a etanolem a nechají
MagPurix Blood DNA Extraction Kit 200
 MagPurix Blood DNA Extraction Kit 200 Kat. č. ZP02001-48 Doba zpracování: 50-60 minut pro MagPurix 12S 50-70 minut pro MagPurix 24 Použití Souprava MagPurix Blood DNA Extraction Kit 200 je určena pro izolátor
MagPurix Blood DNA Extraction Kit 200 Kat. č. ZP02001-48 Doba zpracování: 50-60 minut pro MagPurix 12S 50-70 minut pro MagPurix 24 Použití Souprava MagPurix Blood DNA Extraction Kit 200 je určena pro izolátor
PROTEINOVÁ DENATURUJÍCÍ ELEKTROFORÉZA (SDS PAGE)
 PROTEINOVÁ DENATURUJÍCÍ ELEKTROFORÉZA (SDS PAGE) Denaturující proteinová elektroforéza (SDS PAGE - SDS Protein Acrylamide Gel Electrophoresis) je metoda, která se používá k separaci proteinů podle velikosti,
PROTEINOVÁ DENATURUJÍCÍ ELEKTROFORÉZA (SDS PAGE) Denaturující proteinová elektroforéza (SDS PAGE - SDS Protein Acrylamide Gel Electrophoresis) je metoda, která se používá k separaci proteinů podle velikosti,
Úloha č. 1 Odměřování objemů, ředění roztoků Strana 1. Úkol 1. Ředění roztoků. Teoretický úvod - viz návod
 Úloha č. 1 Odměřování objemů, ředění roztoků Strana 1 Teoretický úvod Uveďte vzorec pro: výpočet směrodatné odchylky výpočet relativní chyby měření [%] Použitý materiál, pomůcky a přístroje Úkol 1. Ředění
Úloha č. 1 Odměřování objemů, ředění roztoků Strana 1 Teoretický úvod Uveďte vzorec pro: výpočet směrodatné odchylky výpočet relativní chyby měření [%] Použitý materiál, pomůcky a přístroje Úkol 1. Ředění
Molekulová spektroskopie 1. Chemická vazba, UV/VIS
 Molekulová spektroskopie 1 Chemická vazba, UV/VIS 1 Chemická vazba Silová interakce mezi dvěma atomy. Chemické vazby jsou soudržné síly působící mezi jednotlivými atomy nebo ionty v molekulách. Chemická
Molekulová spektroskopie 1 Chemická vazba, UV/VIS 1 Chemická vazba Silová interakce mezi dvěma atomy. Chemické vazby jsou soudržné síly působící mezi jednotlivými atomy nebo ionty v molekulách. Chemická
ELEKTROFORETICKÉ METODY
 ELEKTROFORETICKÉ METODY ELEKTROFORETICKÁ SEPARACE AMINOKYSELIN NA PAPÍROVÉM NOSIČI Aminokyseliny lze rozdělit elektroforézou na papíře. Protože molekulová hmotnost jednotlivých aminokyselin není příliš
ELEKTROFORETICKÉ METODY ELEKTROFORETICKÁ SEPARACE AMINOKYSELIN NA PAPÍROVÉM NOSIČI Aminokyseliny lze rozdělit elektroforézou na papíře. Protože molekulová hmotnost jednotlivých aminokyselin není příliš
Adsorpce barviva na aktivním uhlí
 Adsorpce barviva na aktivním uhlí TEORIE ABSORBANCE Prochází-li světelný tok monochromatických paprsků o intenzitě I 0 určitým prostředím dojde k pohlcení jisté části záření a intenzita záření se sníží
Adsorpce barviva na aktivním uhlí TEORIE ABSORBANCE Prochází-li světelný tok monochromatických paprsků o intenzitě I 0 určitým prostředím dojde k pohlcení jisté části záření a intenzita záření se sníží
Interakce proteinu p53 s genomovou DNA v kontextu chromatinu glioblastoma buněk
 MASARYKOVA UNIVERZITA V BRNĚ Přírodovědecká fakulta Ústav experimentální biologie Oddělení genetiky a molekulární biologie Interakce proteinu p53 s genomovou DNA v kontextu chromatinu glioblastoma buněk
MASARYKOVA UNIVERZITA V BRNĚ Přírodovědecká fakulta Ústav experimentální biologie Oddělení genetiky a molekulární biologie Interakce proteinu p53 s genomovou DNA v kontextu chromatinu glioblastoma buněk
Braf 600/601 StripAssay
 Braf 600/601 StripAssay Kat. číslo 5-560 20 testů 2-8 C Popis stripu: Pracovní postup Kit umožňuje detekci 9 mutací v genu BRAF (kodón 600 a 601) Další informace najdete v OMIM Online Mendelian Inheritance
Braf 600/601 StripAssay Kat. číslo 5-560 20 testů 2-8 C Popis stripu: Pracovní postup Kit umožňuje detekci 9 mutací v genu BRAF (kodón 600 a 601) Další informace najdete v OMIM Online Mendelian Inheritance
Příprava roztoků, absorpční spektrofotometrie
 Příprava roztoků, absorpční spektrofotometrie Příprava roztoků Roztoky jsou homogenní soustavy složené ze dvou či více složek. Složení roztoků (tedy údaje o kvantitativním zastoupení jednotlivých složek)
Příprava roztoků, absorpční spektrofotometrie Příprava roztoků Roztoky jsou homogenní soustavy složené ze dvou či více složek. Složení roztoků (tedy údaje o kvantitativním zastoupení jednotlivých složek)
pracovní list studenta Komplexní sloučeniny Stanovení koncentrace kationtů přechodných kovů
 Výstup RVP: Klíčová slova: pracovní list studenta Komplexní sloučeniny Stanovení koncentrace kationtů přechodných kovů Aleš Mareček žák se seznámí s moderními metodami kvantitativní analýzy (práce propojuje
Výstup RVP: Klíčová slova: pracovní list studenta Komplexní sloučeniny Stanovení koncentrace kationtů přechodných kovů Aleš Mareček žák se seznámí s moderními metodami kvantitativní analýzy (práce propojuje
Polymorfismus délky restrikčních fragmentů
 Polymorfismus délky restrikčních fragmentů Princip: Chemikálie: PCR produkt z předchozího praktického cvičení Endonukleáza KpnI 10 U μl -1 Pufr pro KpnI 10 koncentrovaný (Tris-HCl 100 mmol l -1 ph 7,5,
Polymorfismus délky restrikčních fragmentů Princip: Chemikálie: PCR produkt z předchozího praktického cvičení Endonukleáza KpnI 10 U μl -1 Pufr pro KpnI 10 koncentrovaný (Tris-HCl 100 mmol l -1 ph 7,5,
Studium komplexace -cyklodextrinu s diclofenacem s využitím NMR spektroskopie
 Jména: Datum: Studium komplexace -cyklodextrinu s diclofenacem s využitím NMR spektroskopie Cílem laboratorního cvičení je prozkoumat interakce léčiva diclofenac s -cyklodextrinem v D 2 O při tvorbě komplexu
Jména: Datum: Studium komplexace -cyklodextrinu s diclofenacem s využitím NMR spektroskopie Cílem laboratorního cvičení je prozkoumat interakce léčiva diclofenac s -cyklodextrinem v D 2 O při tvorbě komplexu
Obr. 1. Struktura glukosaminu.
 3. Stanovení glukosaminu ve výživových doplňcích pomocí kapilární elektroforézy Glukosamin (2-amino-2-deoxyglukózamonosacharid je široce distribuován ve tkáních lidského organismu jako složka je klíčovou
3. Stanovení glukosaminu ve výživových doplňcích pomocí kapilární elektroforézy Glukosamin (2-amino-2-deoxyglukózamonosacharid je široce distribuován ve tkáních lidského organismu jako složka je klíčovou
STANOVENÍ ANTIOXIDAČNÍ KAPACITY METODOU FOTOCHEMILUMINISCENCE NA PŘÍSTROJI PHOTOCHEM
 STANOVENÍ ANTIOXIDAČNÍ KAPACITY METODOU FOTOCHEMILUMINISCENCE NA PŘÍSTROJI PHOTOCHEM ANTIOXIDAČNÍ KAPACITA ČAJŮ Princip metodiky: Analyzátor Photochem je určen pro stanovení antioxidační kapacity vybraných
STANOVENÍ ANTIOXIDAČNÍ KAPACITY METODOU FOTOCHEMILUMINISCENCE NA PŘÍSTROJI PHOTOCHEM ANTIOXIDAČNÍ KAPACITA ČAJŮ Princip metodiky: Analyzátor Photochem je určen pro stanovení antioxidační kapacity vybraných
Jednotné pracovní postupy zkoušení krmiv STANOVENÍ OBSAHU SEMDURAMICINU METODOU HPLC
 Strana 1 STANOVENÍ OBSAHU SEMDURAMICINU METODOU HPLC 1 Rozsah a účel Postup specifikuje podmínky pro stanovení obsahu semduramicinu v krmivech metodou vysokoúčinné kapalinové chromatografie (HPLC) v koncentračním
Strana 1 STANOVENÍ OBSAHU SEMDURAMICINU METODOU HPLC 1 Rozsah a účel Postup specifikuje podmínky pro stanovení obsahu semduramicinu v krmivech metodou vysokoúčinné kapalinové chromatografie (HPLC) v koncentračním
HbA1c. Axis - Shield. Společnost je zapsána v obchodním rejstříku Městského soudu v Praze, odd. C vložka 1299
 Lékařská technika a speciální zdravotní materiál Společnost je zapsána v obchodním rejstříku Městského soudu v Praze, odd. C vložka 1299 Obchodní 110, 251 70 Praha Čestlice Tel. +420 296 328 300 Fax. +420
Lékařská technika a speciální zdravotní materiál Společnost je zapsána v obchodním rejstříku Městského soudu v Praze, odd. C vložka 1299 Obchodní 110, 251 70 Praha Čestlice Tel. +420 296 328 300 Fax. +420
Protokoly Transformace plasmidu do elektrokompetentních buněk BL21 Pracovní postup:
 Protokoly Pracovní potřeby, pufry a chemikálie jsou uvedeny na konci protokolu. Pracovní postupy jsou odvozeny od těchto kitů: Champion pet160 Directional TOPO Expression Kit with Lumio Technology (Invitrogen)
Protokoly Pracovní potřeby, pufry a chemikálie jsou uvedeny na konci protokolu. Pracovní postupy jsou odvozeny od těchto kitů: Champion pet160 Directional TOPO Expression Kit with Lumio Technology (Invitrogen)
Uživatelská příručka
 PGM Barcoding Set 1-8 Navrženo pro PGM ION-TORRENT KÓD PRODUKTU: 2001 (1-8) BALEN9: 32 testů Uživatelská příručka Rev02.2015 Str. 1 Rejstřík 1. POUŽITÍ VÝROBKU 3 2. OBSAH KITU 4 3. SKLADOVÁNÍ 4 4. STABILITA
PGM Barcoding Set 1-8 Navrženo pro PGM ION-TORRENT KÓD PRODUKTU: 2001 (1-8) BALEN9: 32 testů Uživatelská příručka Rev02.2015 Str. 1 Rejstřík 1. POUŽITÍ VÝROBKU 3 2. OBSAH KITU 4 3. SKLADOVÁNÍ 4 4. STABILITA
nano.tul.cz Inovace a rozvoj studia nanomateriálů na TUL
 Inovace a rozvoj studia nanomateriálů na TUL nano.tul.cz Tyto materiály byly vytvořeny v rámci projektu ESF OP VK: Inovace a rozvoj studia nanomateriálů na Technické univerzitě v Liberci Experimentální
Inovace a rozvoj studia nanomateriálů na TUL nano.tul.cz Tyto materiály byly vytvořeny v rámci projektu ESF OP VK: Inovace a rozvoj studia nanomateriálů na Technické univerzitě v Liberci Experimentální
Stanovení cholesterolu ve vaječném žloutku a mléce kapilární elektroforézou
 Stanovení cholesterolu ve vaječném žloutku a mléce kapilární elektroforézou Úkol Stanovte obsah cholesterolu ve vaječném žloutku a mléce pomocí kapilární elektroforézy. Teoretická část Cholesterol je steroidní
Stanovení cholesterolu ve vaječném žloutku a mléce kapilární elektroforézou Úkol Stanovte obsah cholesterolu ve vaječném žloutku a mléce pomocí kapilární elektroforézy. Teoretická část Cholesterol je steroidní
CS Úřední věstník Evropské unie L 54/89
 26.2.2009 CS Úřední věstník Evropské unie L 54/89 c) při vlnové délce mezi 230 a 320 nm se nesmí spektrum vzestupné části, vrcholu a sestupné části píku zkoušeného vzorku lišit od ostatních částí spektra
26.2.2009 CS Úřední věstník Evropské unie L 54/89 c) při vlnové délce mezi 230 a 320 nm se nesmí spektrum vzestupné části, vrcholu a sestupné části píku zkoušeného vzorku lišit od ostatních částí spektra
