Vazba a struktura. by Chemie - Úterý,?ervenec 16, Otázka: Vazba a struktura. P?edm?
|
|
|
- Dušan Bárta
- před 10 lety
- Počet zobrazení:
Transkript
1 Vazba a struktura by Chemie - Úterý,?ervenec 16, Otázka: Vazba a struktura P?edm?t: Chemie P?idal(a): Lenka CHEMICKÉ VAZBY = síly, kterými jsou k sob? navzájem vázány slou?ené atomy v molekule, pop?. v krystalové struktu?e - v p?evážné v?tšin? jde o sdílení dvojic elektron? s opa?ným spinem neboli vazebných elektronových pár? - pouze vzácné plyny jsou tvo?eny volnými, neslou?enými, atomy - ke vzniku a št?pení chem. vazeb dochází p?i chemických reakcích - disocia?ní energie = energie pot?ebná k rozšt?pení chem. vazby - vazebná energie = energie, která se uvolní p?i vzniku vazby - p?. H? - p?echod elektron? z atom. orbitalu do molekulového orbitalu p?i vzniku molekuly z volných atom? je spojen se snížením energie systému, které je p?í?inou chemické vazby page 1 / 11
2 (takový mol. orbital je vazebný) obsazením 2. mol. orbitalu by vedlo ke zvýšení energie (ke snížení hustoty mezi jádry) (tzv. protivazebný neboli antivazebný orbital) - délka vazby = mezijaderná vzdálenost - vznik chem. vazby: I. dojde k p?iblížení -> sražení -> pr?niku obaly II. uplat?ují se p?itažlivé síly jádra do míst s vyšší e hustotou III. uplat?ují se i odpudivé síly mezi jádry IV. dojde k vyrovnání p?íslušných atomových jader a elektron? - 2 základní typy vazeb: 1) vazba iontová její podstatou jsou elektrostatické síly p?sobící mezi opa?n? nabitými ionty 2) vazba kovalentní oba atomy sdílí spole?n? 1 vazebný elektronový pár, kdy každý partner poskytne 1 elektron s opa?ným spinem - hodnota vazebné energie závisí na tom, jakých dalších vazeb se ú?astní atomy spojené posuzovanou vazbou - rozd?lení vazeb násobnosti: 1) jednoduché každý atom poskytne 1 valen?ní elektron (tzn. vznikne 1 elektronový pár) - je to tém?? vždy vazba? (=sigma) výjimkou je t?eba molekula B? (existuje page 2 / 11
3 za vysokých teplot), v níž je nutno p?edpokládat jednoduchou vazbu? 2) dvojná každý atom poskytne 2 valen?ní elektrony (tzn. vzniknou 2 elektronové páry) - vazba? a? 3) trojná každý atom poskytne 3 valen?ní elektrony N=N - vazba?,? a? 4)?tverná pouze u komplexních slou?enin rhodia a molybdenu - vaznost udává?íslo, vyjad?ující kolik kovalentních vazeb daný atom vytvá?í - vazba? vzniká pravd?podobn? na spojnici jader, kde je nejvyšší hustota valen?ních elektron? - vyzna?uje se osovou soum?rností - je podmín?na obsazením vazebného molekulového orbitalu? - m?že vzniknout p?ekryvem 2 orbital? s, nebo kombinací 2 orbital? p, pop?. orbitalu p a orbitalu s - vazba? je symetricky rozložena nad spojnicí jader - m?že vzniknout z p?ekryvu 2 orbital? p - pevnost chemické vazby roste s násobností page 3 / 11
4 - kovalentní vazba = vzniká p?ekryvem 2 orbital? každý poskytne 1 elektron - výsledkem vzájemného p?itahování elektron? a jader je potom p?itahování jader k míst?m se zvýšenou elektronovou hustotou tzn. k sob? navzájem - elektronegativita X - schopnost atomu p?itahovat vazebné elektrony - její hodnota závisí na tom, se kterým atomem a jakým zp?sobem (ox.?íslo, hybridizace) je daný atom vázán - prvky: - elektropozitivní - elektronegativní - v molekule složené ze dvou atom? s r?znou elektronegativitou p?evládá u atomu s v?tší elektronegativitou záporný náboj a u druhého kladný -> vytvá?í tzv. dipól - polarita kovalentní vazby - ve stejnojaderných dvouatomových molekulách p?sobí ob? jádra na elektrony naprosto stejn? => prostorové rozd?lení el. hustoty je v okolí obou jader stejné - nepolární vazba rozdíl elektronegativit je menší než 0,4 - nej?ast?jší slou?eniny H?, O?, N? - polární vazba rozdíl elektronegativit je od 0,4 do 1,7 - H?O, HCl - iontová vazba extrémn? polární p?. chlorid sodný Na?Cl page 4 / 11
5 - valen?ní elektron jednoho atomu je vtažen do valen?ní vrstvy druhého a vzniká elektronicky nabytá?ástice - mezi atomy, jejichž elektronegativity se liší aspo? o 1,7 - koordina?n?-kovalentní vazba (donor akceptorová nebo také dativní vazba) - donor = dárce, akceptor = p?íjemce - liší se ve vzniku - ve vlastnostech se neliší od kovalentní - p?i vzniku má 1 reaktant volný celý elektronový pár a 2. pouze p?ijímá (má volný orbital) - p?. reakce trimethylaminu s kationtem vodíku - kovová vazba elektronový plyn kov vytvo?í krystalovou m?ížku a ten plyn vytvo?í volné valen?ní elektrony -> elektrony jsou delokalizovány - asi 80% prvk? jsou kovy - krystal kovu se skládá z kationt?, uspo?ádaných v krystalové m?ížce kationty jsou ve svých polohách udržovány nábojem voln? pohyblivých valen?ních el. slabé vazebné interakce - van der waalsovy síly p?. molekula grafitu - jejich podstatou je vzájemné p?sobení molekulových dipól? jak stálých tak indukovaných - u molekul nebo atom?, které nemají stálý dipól, mohou vést okamžité nerovnom?rnosti v rozložení elektron? ke vzniku do?asných dipól?, jejichž vzájemné p?sobení má za následek p?itahování molekul page 5 / 11
6 - vodíkové m?stky vznikají mezi H + F, O, N - zakresluje se: F-H.F-H (2 molekuly kys. fluorovodíkové) - ovliv?ují fyzikální vlastnosti látek (var, tání, rozpustnost) - mají v?tší sílu než van der waalsovy síly - vliv chemické vazby na vlastnosti látek: - látky s kovalentní nepolární vazbou jsou nerozpustné ve vod? a rozpustné v nepolárních rozpoušt?dlech a nevedou el. proud - látky s polární a iontovou vazbou jsou rozpustné ve vod? a nerozpustné v polárních rozpoušt?dlech v roztoku nebo tavenin? vedou el. proud - látky s kovovou vazbou vedou el. proud a teplo, jsou kujné a tažné - struktura krystal?: - pevné látky, které mají pravidelné uspo?ádání základních?ástic (atom?, molekul nebo iont?)?ili krystalovou strukturu, mohou vytvá?et soum?rná t?lesa nazývaná krystaly - krystaly se v?tšinou vyskytují jako polykrystaly složení z velkého po?tu malých krystalk?, v nichž jsou?ástice uspo?ádány pravideln?, ale poloha krystalk? je nahodilá - monokrystaly krystalické látky, které se vyskytují jako jednotlivé krystaly v?tších rozm?r? - pravidelný tvar krystal? je projevem zákonitosti jejich vnit?ního uspo?ádání - povrch krystal? je složen z rovinných krystalových ploch, protínajících se v hranách a hrany se stýkají ve vrcholech - 2 plochy svírají vždy stejný úhel page 6 / 11
7 - podle soum?rnosti se krystaly rozd?lují do 7 krystalových soustav: jednoklonné, trojklonné, koso?tvere?né, klencové, šestere?né,?tvere?né, krychlové - základní bu?ka jednoduché seskupení?ástic tvo?ících stavební jednotku krystalu - krystaly: 1) iontové vysoká teplota - vedou v roztoku el. proud (umož?uje to pohyblivé ionty), v pevném skupenství jsou nevodivé - jsou k?ehké - v?tšinou se rozpoušt?jí v rozpoušt?dlech z polárních molekul 2) atomové (kovalentní) - velmi tvrdé, nerozpustné - nevedou el. proud - vysoká teplota tání - diamant 3) molekulové spojené van der waalsovýmy silami nebo m?stky - tvo?í molekuly prvk? (p?. N?), jednoduché oxidy, hydridy,?etné organické molekuly a makromolekuly - nízká teplota tání, t?kavé, nevodivé, rozpustné v nepolárních rozpoušt?dlech 4) n?co mezi atomovými a molekulovými = vrstevnaté 5) kovové uspo?ádání: - krychlová plošn? centrovaná základní bu?ka (p?. Al) - šestere?ná základní b. (p?. Mg) page 7 / 11
8 - krychlová t?sn? centrovaná b. (p?. alkalické kovy) - alotropie prvky, které mohou mít n?kolik r?zných krystalových forem - p?. diamant nebo grafit pop?. fosfor - polymorfie alotropie u slou?enin - p?. uhli?itan vápenatý - izomorfní (stejnotvaré) látky krystalizují spole?n? ze sm?si svých nasycených roztok? nebo travenin a vytvá?í tak sm?sné krystaly, ve kterých se mohou vyskytovat v libovolných pom?rech - p?edpokladem izomorfie je stejný typ krystalové struktury a malé rozdíly ve velikosti iont? - amorfní (beztvaré) látky uspo?ádání?ástic je bu? zcela nepravidelné nebo jsou vytvo?eny velmi malé oblasti s pravidelnou strukturou - podobné ztuhlým kapalinám - p?. sklo MOLEKULA - i pro molekulu existuje orbitalový model, ve kterém je chování jednotlivých elektron? v molekule popsáno pomocí jednoelektronových vlnových funkcí molekulových orbital? - ke znázorn?ní el. hustoty se používají hrani?ní plochy a mapy elektronových hustot neboli vrstevnicové diagramy page 8 / 11
9 - i pro molekulu platí výstavbový princip, Pauliho princip a Hundovo pravidlo - polovina rozdíl? po?tu elektron? ve vazebných a protivazebných orbitalech udává?ád vazby dvouatomových molekul veli?inu charakterizující násobnost a pevnost vazby - u t?í atomových molekul se uplat?uje d?ležitá vlastnost kovalentní vazby její sm?r totožný se sm?rem spojnice atomových jader vázaných atom? - vazebný úhel = úhel, který svírají 2 vazby vycházející z jednoho jádra - jednoduchý odhad tvaru molekuly a velikosti vazebných úhl? je založený na p?edstav? odpuzování valen?ních elektronových dvojic - jednoduchá kovalentní vazba p?edstavuje zhušt?ní elektron? na spojnici vázaných jader protože se el. navzájem odpuzují, tak jsou vazby vycházející z jednoho atomu orientovány tak, aby tato zhušt?ní byla co nejdále od sebe a vazebné úhly m?ly tak co nejv?tší hodnotu - 2 vazebné elektronové páry nejmenší energie odpovídá maximální vazebný úhel (180 ) -> molekula je lineární - 3 vazebné elektronové páry atomová jádra jsou ve vrcholech rovnostranného trojúhelníku (v jeho st?edu je jedno jádro) vazebný úhel je n?které molekuly (p?. NH?) obsahuje ve valen?ní vrstv? centrálního atomu krom? vazebných el. pár? i volné (nevazebné) el. páry page 9 / 11
10 - metoda delokalizovaných molekulových orbital? vychází z toho, že el. v molekulových orbitalech nejsou lokalizovány mezi dvojice atom?, ale jsou delokalizovány ( rozprost?eny ) p?es n?kolik atom? tím se liší klasické p?edstav?, že dva el. spole?né dv?ma atom?m odpovídají jedné chemické vazb? - metoda lokalizovaných molekulových orbital? poskytuje názorn?jší popis molekulové geometrie - používají se hybridní orbitaly, které jsou p?izp?sobeny geometrii molekuly - hybridní orbitaly získají se lineární kombinací (hybridizací) atomových orbital? valen?ní vrstvy centrálního atomu - p?i výpo?tu lokalizovaných molekulových orbital? se hybridní atomové orbitaly centrálního atomu kombinují s atomovými orbitaly jiných atom? molekuly - hybridizace: - type hybridizace: - hybridizace sp (lineární neboli diagonální) - u t?íatomových molekul - hybridizace sp²(trigonální) - hybridizace sp³ (tetraedrická) - je to matematická metoda (ne reálný proces) - používají se at. orbitaly, které se p?íliš neliší energií - typ hybridizace se volí podle tvaru molekuly - hybridizací se nem?ní po?et orbital? - vaznost atomu (neboli vaznost prvku) je definována jako po?et kovalentních vazeb, které z n?ho page 10 / 11
11 Powered by TCPDF ( Vazba a struktura vycházejí - rozhoduje o ní snížení energie spojené s vytvo?ením daného po?tu vazeb - pro ur?ování vaznosti prvk? 2. a 3. periody se používá oktetové pravidlo zd?vod?uje stálost molekul tím, že vázané atomy sdílením elektron? nebývají relativn? stalé konfigurace vzácného plynu - vytvá?í se tolik vazeb, aby vázané atomy m?ly práv? tuto konfiguraci = elektronový oktet molekulových - k vazb? dochází tehdy, pokud vazebné ú?inky elektron? ve vazebných orbitalech nejsou kompenzovány obsazením protivazebných molekulových orbital? - nelze vždy posuzovat jenom podle po?tu atomových orbital? obsazených jedním elektronem v jeho základním stavu - struktura složit?jších molekul - lineární p?. oxid uhli?itý všechny valen?ní elektrony atomu uhlíku se ú?astní vazby - lomená p?. oxid si?i?itý atom síry má volný elektronový pár - k mnohotvárnosti molekul význa?n? p?ispívá možnost?et?zení atom? - d?sledkem je existence izomer? (látky se stejným souhrnným vzorcem, ale lišícím se strukturou) PDF generated by Kalin's PDF Creation Station page 11 / 11
3) Vazba a struktura. Na www.studijni-svet.cz zaslal(a): Lenka
 Na www.studijni-svet.cz zaslal(a): Lenka CHEMICKÍ VAZBA = síly, kterými jsou k sobě navzájem vázány sloučené atomy v molekule, popř. v krystalové struktuře - v převážné většině jde o sdílení dvojic elektronů
Na www.studijni-svet.cz zaslal(a): Lenka CHEMICKÍ VAZBA = síly, kterými jsou k sobě navzájem vázány sloučené atomy v molekule, popř. v krystalové struktuře - v převážné většině jde o sdílení dvojic elektronů
 Chemická vazba Něco málo opakování Něco málo opakování Co je to atom? Něco málo opakování Co je to atom? Atom je nejmenší částice hmoty, chemicky dále nedělitelná. Skládá se z atomového jádra obsahujícího
Chemická vazba Něco málo opakování Něco málo opakování Co je to atom? Něco málo opakování Co je to atom? Atom je nejmenší částice hmoty, chemicky dále nedělitelná. Skládá se z atomového jádra obsahujícího
Chemická vazba. Příčinou nestability atomů a jejich ochoty tvořit vazbu je jejich elektronový obal.
 Chemická vazba Volné atomy v přírodě jen zcela výjimečně (vzácné plyny). Atomy prvků mají snahu se navzájem slučovat a vytvářet molekuly prvků nebo sloučenin. Atomy jsou v molekulách k sobě poutány chemickou
Chemická vazba Volné atomy v přírodě jen zcela výjimečně (vzácné plyny). Atomy prvků mají snahu se navzájem slučovat a vytvářet molekuly prvků nebo sloučenin. Atomy jsou v molekulách k sobě poutány chemickou
Atom a molekula - maturitní otázka z chemie
 Atom a molekula - maturitní otázka z chemie by jx.mail@centrum.cz - Pond?lí, Únor 09, 2015 http://biologie-chemie.cz/atom-a-molekula-maturitni-otazka-z-chemie/ Otázka: Atom a molekula P?edm?t: Chemie P?idal(a):
Atom a molekula - maturitní otázka z chemie by jx.mail@centrum.cz - Pond?lí, Únor 09, 2015 http://biologie-chemie.cz/atom-a-molekula-maturitni-otazka-z-chemie/ Otázka: Atom a molekula P?edm?t: Chemie P?idal(a):
Mgr. Jakub Janíček VY_32_INOVACE_Ch1r0118
 Chemická vazba Mgr. Jakub Janíček VY_32_INOVACE_Ch1r0118 Chemická vazba Většina atomů má tendenci se spojovat do větších celků (molekul), v nichž jsou vzájemně vázané chemickou vazbou. Chemická vazba je
Chemická vazba Mgr. Jakub Janíček VY_32_INOVACE_Ch1r0118 Chemická vazba Většina atomů má tendenci se spojovat do větších celků (molekul), v nichž jsou vzájemně vázané chemickou vazbou. Chemická vazba je
Opakování
 Slabé vazebné interakce Opakování Co je to atom? Opakování Opakování Co je to atom? Atom je nejmenší částice hmoty, chemicky dále nedělitelná. Skládá se z atomového jádra obsahujícího protony a neutrony
Slabé vazebné interakce Opakování Co je to atom? Opakování Opakování Co je to atom? Atom je nejmenší částice hmoty, chemicky dále nedělitelná. Skládá se z atomového jádra obsahujícího protony a neutrony
Teorie chemické vazby a molekulární geometrie Molekulární geometrie VSEPR
 Geometrie molekul Lewisovy vzorce poskytují informaci o tom které atomy jsou spojeny vazbou a o jakou vazbu se jedná (topologie molekuly). Geometrické uspořádání molekuly je charakterizováno: Délkou vazeb
Geometrie molekul Lewisovy vzorce poskytují informaci o tom které atomy jsou spojeny vazbou a o jakou vazbu se jedná (topologie molekuly). Geometrické uspořádání molekuly je charakterizováno: Délkou vazeb
- anomálie vody - nejvyšší hustota p?i 4 C hlavní význam pro vodní organismy
 Voda - seminární práce by Chemie -?tvrtek, Prosinec 19, 2013 http://biologie-chemie.cz/voda-seminarni-prace/ Otázka: Voda - seminární práce P?edm?t: Chemie P?idal(a): MrLuciprd VODA základní podmínka života
Voda - seminární práce by Chemie -?tvrtek, Prosinec 19, 2013 http://biologie-chemie.cz/voda-seminarni-prace/ Otázka: Voda - seminární práce P?edm?t: Chemie P?idal(a): MrLuciprd VODA základní podmínka života
Teorie hybridizace. Vysvětluje vznik energeticky rovnocenných kovalentních vazeb a umožňuje předpovědět prostorový tvar molekul.
 Chemická vazba co je chemická vazba charakteristiky chemické vazby jak vzniká vazba znázornění chemické vazby kovalentní a koordinační vazba vazba σ a π jednoduchá, dvojná a trojná vazba polarita vazby
Chemická vazba co je chemická vazba charakteristiky chemické vazby jak vzniká vazba znázornění chemické vazby kovalentní a koordinační vazba vazba σ a π jednoduchá, dvojná a trojná vazba polarita vazby
CHEMICKÁ VAZBA. Autor: Mgr. Stanislava Bubíková. Datum (období) tvorby: Ročník: osmý
 Autor: Mgr. Stanislava Bubíková CHEMICKÁ VAZBA Datum (období) tvorby: 13. 11. 01 Ročník: osmý Vzdělávací oblast: Člověk a příroda / Chemie / Částicové složení látek a chemické prvky; chemické reakce 1
Autor: Mgr. Stanislava Bubíková CHEMICKÁ VAZBA Datum (období) tvorby: 13. 11. 01 Ročník: osmý Vzdělávací oblast: Člověk a příroda / Chemie / Částicové složení látek a chemické prvky; chemické reakce 1
Vazby v pevných látkách
 Vazby v pevných látkách Hlavní body 1. Tvorba pevných látek 2. Van der Waalsova vazba elektrostatická interakce indukovaných dipólů 3. Iontová vazba elektrostatická interakce iontů 4. Kovalentní vazba
Vazby v pevných látkách Hlavní body 1. Tvorba pevných látek 2. Van der Waalsova vazba elektrostatická interakce indukovaných dipólů 3. Iontová vazba elektrostatická interakce iontů 4. Kovalentní vazba
Průvodka. CZ.1.07/1.5.00/ Zkvalitnění výuky prostřednictvím ICT. III/2 Inovace a zkvalitnění výuky prostřednictvím ICT
 Průvodka Číslo projektu Název projektu Číslo a název šablony klíčové aktivity CZ.1.07/1.5.00/34.0802 Zkvalitnění výuky prostřednictvím ICT III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Příjemce
Průvodka Číslo projektu Název projektu Číslo a název šablony klíčové aktivity CZ.1.07/1.5.00/34.0802 Zkvalitnění výuky prostřednictvím ICT III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Příjemce
Chemie. Mgr. Petra Drápelová Mgr. Jaroslava Vrbková. Gymnázium, SOŠ a VOŠ Ledeč nad Sázavou
 Chemie Mgr. Petra Drápelová Mgr. Jaroslava Vrbková Gymnázium, SOŠ a VOŠ Ledeč nad Sázavou CHEMICKÁ VAZBA VY_32_INOVACE_03_3_07_CH Gymnázium, SOŠ a VOŠ Ledeč nad Sázavou CHEMICKÁ VAZBA Volné atomy v přírodě
Chemie Mgr. Petra Drápelová Mgr. Jaroslava Vrbková Gymnázium, SOŠ a VOŠ Ledeč nad Sázavou CHEMICKÁ VAZBA VY_32_INOVACE_03_3_07_CH Gymnázium, SOŠ a VOŠ Ledeč nad Sázavou CHEMICKÁ VAZBA Volné atomy v přírodě
Ch - Elektronegativita, chemická vazba
 Ch - Elektronegativita, chemická vazba Autor: Mgr. Jaromír Juřek Kopírování a jakékoliv další využití výukového materiálu je povoleno pouze s využitím odkazu na www.jarjurek.cz. VARIACE 1 Tento dokument
Ch - Elektronegativita, chemická vazba Autor: Mgr. Jaromír Juřek Kopírování a jakékoliv další využití výukového materiálu je povoleno pouze s využitím odkazu na www.jarjurek.cz. VARIACE 1 Tento dokument
Molekuly 1 12/4/2011. Molekula definice IUPAC. Molekuly. Proč existují molekuly? Kosselův model. Představy o molekulách
 1/4/011 Molekuly 1 Molekula definice IUPC elektricky neutrální entita sestávající z více nežli jednoho atomu. Přesně, molekula, v níž je počet atomů větší nežli jedna, musí odpovídat snížení na ploše potenciální
1/4/011 Molekuly 1 Molekula definice IUPC elektricky neutrální entita sestávající z více nežli jednoho atomu. Přesně, molekula, v níž je počet atomů větší nežli jedna, musí odpovídat snížení na ploše potenciální
Předmět: Ročník: Vytvořil: Datum: CHEMIE PRVNÍ Mgr. Tomáš MAŇÁK 15. června 2013. Název zpracovaného celku: CHEMICKÁ VAZBA
 Předmět: Ročník: Vytvořil: Datum: CHEMIE PRVNÍ Mgr. Tomáš MAŇÁK 15. června 2013 Název zpracovaného celku: CHEMICKÁ VAZBA CHEMICKÁ VAZBA (chemical bond) CHEMICKÉ VAZBY soudržné síly působící mezi jednotlivými
Předmět: Ročník: Vytvořil: Datum: CHEMIE PRVNÍ Mgr. Tomáš MAŇÁK 15. června 2013 Název zpracovaného celku: CHEMICKÁ VAZBA CHEMICKÁ VAZBA (chemical bond) CHEMICKÉ VAZBY soudržné síly působící mezi jednotlivými
Skupenské stavy látek. Mezimolekulární síly
 Skupenské stavy látek Mezimolekulární síly 1 Interakce iont-dipól Např. hydratační (solvatační) interakce mezi Na + (iont) a molekulou vody (dipól). Jde o nejsilnější mezimolekulární (nevazebnou) interakci.
Skupenské stavy látek Mezimolekulární síly 1 Interakce iont-dipól Např. hydratační (solvatační) interakce mezi Na + (iont) a molekulou vody (dipól). Jde o nejsilnější mezimolekulární (nevazebnou) interakci.
Chemická vazba. John Dalton Amadeo Avogadro
 Chemická vazba John Dalton 1766-1844 Amadeo Avogadro 1776-1856 Výpočet molekuly 2, metoda valenční vazby Walter eitler 1904-1981 Fritz W. London 1900-1954 Teorie molekulových orbitalů Friedrich und 1896-1997
Chemická vazba John Dalton 1766-1844 Amadeo Avogadro 1776-1856 Výpočet molekuly 2, metoda valenční vazby Walter eitler 1904-1981 Fritz W. London 1900-1954 Teorie molekulových orbitalů Friedrich und 1896-1997
Periodická tabulka prvků
 Periodická tabulka prvků 17. století s objevem dalších a dalších prvků nutnost systematizace J. W. Döberreiner (1829) teorie o triádách prvků triáda kovů (lithium, sodík, draslík reagují podobným způsobem)
Periodická tabulka prvků 17. století s objevem dalších a dalších prvků nutnost systematizace J. W. Döberreiner (1829) teorie o triádách prvků triáda kovů (lithium, sodík, draslík reagují podobným způsobem)
2.3 CHEMICKÁ VAZBA. Molekula bílého fosforu P 4 a kyseliny sírové H 2 SO 4. Předpona piko p je dílčí jednotkou a udává velikost m.
 2.3 CHEMICKÁ VAZBA Spojováním dvou a více atomů vznikají molekuly. Jestliže dochází ke spojování výhradně atomů téhož chemického prvku, pak se jedná o molekuly daného prvku (vodíku H 2, dusíku N 2, ozonu
2.3 CHEMICKÁ VAZBA Spojováním dvou a více atomů vznikají molekuly. Jestliže dochází ke spojování výhradně atomů téhož chemického prvku, pak se jedná o molekuly daného prvku (vodíku H 2, dusíku N 2, ozonu
Chemická vazba. Důvody pro vazbu = menší energie atomů ve vázaném stavu než energie jednotlivých oddělených atomů
 Chemická vazba Důvody pro vazbu = menší energie atomů ve vázaném stavu než energie jednotlivých oddělených atomů Mechanismus tvorby vazby = sdílení, předávání nebo redistribuce valenčních elektronů Model
Chemická vazba Důvody pro vazbu = menší energie atomů ve vázaném stavu než energie jednotlivých oddělených atomů Mechanismus tvorby vazby = sdílení, předávání nebo redistribuce valenčních elektronů Model
John Dalton Amadeo Avogadro
 Spojením atomů vznikají molekuly... John Dalton 1766 1844 Amadeo Avogadro 1776 1856 Výpočet molekuly 2, metoda valenční vazby Walter eitler 1904 1981 Fritz W. London 1900 1954 Teorie molekulových orbitalů
Spojením atomů vznikají molekuly... John Dalton 1766 1844 Amadeo Avogadro 1776 1856 Výpočet molekuly 2, metoda valenční vazby Walter eitler 1904 1981 Fritz W. London 1900 1954 Teorie molekulových orbitalů
Chemická vazba. Molekula vodíku. Elektronová teorie. Oktetové pravidlo (Kossel, Lewis, 1916) Pevnost vazby vazebná energie.
 Elektronová teorie ktetové pravidlo (Kossel, Lewis, 1916) Chemická vazba sdílení 2 valenčních e - opačného spinu 2 atomy za vzniku stabilní elektronové konfigurace vzácného plynu Spojení atomů prvků v
Elektronová teorie ktetové pravidlo (Kossel, Lewis, 1916) Chemická vazba sdílení 2 valenčních e - opačného spinu 2 atomy za vzniku stabilní elektronové konfigurace vzácného plynu Spojení atomů prvků v
Valenční elektrony a chemická vazba
 Valenční elektrony a chemická vazba Ve vnější energetické hladině se nacházejí valenční elektrony, které se mohou podílet na tvorbě chemické vazby. Valenční elektrony často znázorňujeme pomocí teček kolem
Valenční elektrony a chemická vazba Ve vnější energetické hladině se nacházejí valenční elektrony, které se mohou podílet na tvorbě chemické vazby. Valenční elektrony často znázorňujeme pomocí teček kolem
Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 08.03.2013 Číslo DUMu: VY_32_INOVACE_09_Ch_OB Ročník: I. Vzdělávací oblast: Přírodovědné
 Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 08.03.2013 Číslo DUMu: VY_32_INOVACE_09_Ch_OB Ročník: I. Vzdělávací oblast: Přírodovědné vzdělávání Vzdělávací obor: Chemie Tematický okruh: Obecná
Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 08.03.2013 Číslo DUMu: VY_32_INOVACE_09_Ch_OB Ročník: I. Vzdělávací oblast: Přírodovědné vzdělávání Vzdělávací obor: Chemie Tematický okruh: Obecná
Chemická vazba. Důvody pro vazbu = menší energie atomů ve vázaném stavu než energie jednotlivých oddělených atomů
 Chemická vazba Důvody pro vazbu = menší energie atomů ve vázaném stavu než energie jednotlivých oddělených atomů Mechanismus tvorby vazby = sdílení, předávání nebo redistribuce valenčních elektronů Model
Chemická vazba Důvody pro vazbu = menší energie atomů ve vázaném stavu než energie jednotlivých oddělených atomů Mechanismus tvorby vazby = sdílení, předávání nebo redistribuce valenčních elektronů Model
Skupenské stavy. Kapalina Částečně neuspořádané Volný pohyb částic nebo skupin částic Částice blíže u sebe
 Skupenské stavy Plyn Zcela neuspořádané Hodně volného prostoru Zcela volný pohyb částic Částice daleko od sebe Kapalina Částečně neuspořádané Volný pohyb částic nebo skupin částic Částice blíže u sebe
Skupenské stavy Plyn Zcela neuspořádané Hodně volného prostoru Zcela volný pohyb částic Částice daleko od sebe Kapalina Částečně neuspořádané Volný pohyb částic nebo skupin částic Částice blíže u sebe
Mezimolekulové interakce
 Mezimolekulové interakce Interakce molekul reaktivně vzniká či zaniká kovalentní vazba překryv elektronových oblaků, mění se vlastnosti nereaktivně vznikají molekulové komplexy slabá, nekovalentní, nechemická,
Mezimolekulové interakce Interakce molekul reaktivně vzniká či zaniká kovalentní vazba překryv elektronových oblaků, mění se vlastnosti nereaktivně vznikají molekulové komplexy slabá, nekovalentní, nechemická,
17. Elektrický proud v polovodiích, užití polovodiových souástek
 17. Elektrický proud v polovodiích, užití polovodiových souástek Polovodie se od kov liší pedevším tím, že mají vtší rezistivitu (10-2.m až 10 9.m) (kovy 10-8.m až 10-6.m). Tato rezistivita u polovodi
17. Elektrický proud v polovodiích, užití polovodiových souástek Polovodie se od kov liší pedevším tím, že mají vtší rezistivitu (10-2.m až 10 9.m) (kovy 10-8.m až 10-6.m). Tato rezistivita u polovodi
Překryv orbitalů. Vznik vazby překryvem orbitalů na dvou různých atomech A, B Obsazeno dvojicí elektronů Ψ = Ψ A Ψ Β
 Překryv orbitalů Vznik vazby překryvem orbitalů na dvou různých atomech A, B Obsazeno dvojicí elektronů Ψ = Ψ A Ψ Β Podmínky překryvu: Vhodná symetrie, znaménko vlnové funkce Vhodná energie, srovnatelná,
Překryv orbitalů Vznik vazby překryvem orbitalů na dvou různých atomech A, B Obsazeno dvojicí elektronů Ψ = Ψ A Ψ Β Podmínky překryvu: Vhodná symetrie, znaménko vlnové funkce Vhodná energie, srovnatelná,
Gymnázium, Milevsko, Masarykova 183 Školní vzdělávací program (ŠVP) pro vyšší stupeň osmiletého studia a čtyřleté studium 4.
 Vyučovací předmět - Chemie Vzdělávací obor - Člověk a příroda Gymnázium, Milevsko, Masarykova 183 Školní vzdělávací program (ŠVP) pro vyšší stupeň osmiletého studia a čtyřleté studium 4. ročník - seminář
Vyučovací předmět - Chemie Vzdělávací obor - Člověk a příroda Gymnázium, Milevsko, Masarykova 183 Školní vzdělávací program (ŠVP) pro vyšší stupeň osmiletého studia a čtyřleté studium 4. ročník - seminář
Orbitaly, VSEPR 1 / 18
 rbitaly, VSEPR Rezonanční struktury, atomové a molekulové orbitaly, hybridizace, určování tvaru molekuly pomocí teorie VSEPR, úvod do symetrie molekul, dipólový moment 1 / 18 Formální náboj Rozdíl mezi
rbitaly, VSEPR Rezonanční struktury, atomové a molekulové orbitaly, hybridizace, určování tvaru molekuly pomocí teorie VSEPR, úvod do symetrie molekul, dipólový moment 1 / 18 Formální náboj Rozdíl mezi
Orbitaly, VSEPR. Zdeněk Moravec, 16. listopadu / 21
 rbitaly, VSEPR Rezonanční struktury, atomové a molekulové orbitaly, hybridizace, určování tvaru molekuly pomocí teorie VSEPR, úvod do symetrie molekul, dipólový moment Zdeněk Moravec, http://z-moravec.net
rbitaly, VSEPR Rezonanční struktury, atomové a molekulové orbitaly, hybridizace, určování tvaru molekuly pomocí teorie VSEPR, úvod do symetrie molekul, dipólový moment Zdeněk Moravec, http://z-moravec.net
ATOMOVÉ JÁDRO. Nucleus Složení: Proton. Neutron 1 0 n částice bez náboje Proton + neutron = NUKLEON PROTONOVÉ číslo: celkový počet nukleonů v jádře
 ATOM 1 ATOM Hmotná částice Dělit lze: Fyzikálně ANO Chemicky Je z nich složena každá látka Složení: Atomové jádro (protony, neutrony) Elektronový obal (elektrony) NE Elektroneutrální částice: počet protonů
ATOM 1 ATOM Hmotná částice Dělit lze: Fyzikálně ANO Chemicky Je z nich složena každá látka Složení: Atomové jádro (protony, neutrony) Elektronový obal (elektrony) NE Elektroneutrální částice: počet protonů
Inovace studia molekulární a buněčné biologie reg. č. CZ.1.07/2.2.00/
 Inovace studia molekulární a buněčné biologie reg. č. CZ.1.07/2.2.00/07.0354 Předmět: LRR/CHPB1/Chemie pro biology 1 Chemická vazba II Mgr. Karel Doležal Dr. Cíl přednášky: seznámit posluchače s principem
Inovace studia molekulární a buněčné biologie reg. č. CZ.1.07/2.2.00/07.0354 Předmět: LRR/CHPB1/Chemie pro biology 1 Chemická vazba II Mgr. Karel Doležal Dr. Cíl přednášky: seznámit posluchače s principem
I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í CHEMICKÁ VAZBA
 CHEMICKÁ VAZBA Chemická vazba = síla, která drží atomy ve sloučenině, podílejí se na ní valenční elektrony Elektronové vzorce (užívané pro s and p prvky): valenční elektrony jsou znázorněny tečkami kolem
CHEMICKÁ VAZBA Chemická vazba = síla, která drží atomy ve sloučenině, podílejí se na ní valenční elektrony Elektronové vzorce (užívané pro s and p prvky): valenční elektrony jsou znázorněny tečkami kolem
Vodík - maturitní otázka z chemie
 Vodík - maturitní otázka z chemie by jx.mail@centrum.cz - St?eda, Únor 18, 2015 http://biologie-chemie.cz/vodik-maturitni-otazka-z-chemie/ Otázka: Vodík P?edm?t: Chemie P?idal(a): Ivana K. Zna?ka: H El.
Vodík - maturitní otázka z chemie by jx.mail@centrum.cz - St?eda, Únor 18, 2015 http://biologie-chemie.cz/vodik-maturitni-otazka-z-chemie/ Otázka: Vodík P?edm?t: Chemie P?idal(a): Ivana K. Zna?ka: H El.
Úvod do studia organické chemie
 Úvod do studia organické chemie 1828... Wöhler... uměle připravil močovinu Organická chemie - chemie sloučenin uhlíku a vodíku, případně dalších prvků (O, N, X, P, S) Příčiny stability uhlíkových řetězců:
Úvod do studia organické chemie 1828... Wöhler... uměle připravil močovinu Organická chemie - chemie sloučenin uhlíku a vodíku, případně dalších prvků (O, N, X, P, S) Příčiny stability uhlíkových řetězců:
Chemická vazba. Důvody pro vazbu = menší energie atomů ve vázaném stavu než energie jednotlivých oddělených atomů
 Chemická vazba Důvody pro vazbu = menší energie atomů ve vázaném stavu než energie jednotlivých oddělených atomů Mechanismus tvorby vazby = sdílení, předávání nebo redistribuce valenčních elektronů Model
Chemická vazba Důvody pro vazbu = menší energie atomů ve vázaném stavu než energie jednotlivých oddělených atomů Mechanismus tvorby vazby = sdílení, předávání nebo redistribuce valenčních elektronů Model
Gymnázium Jiřího Ortena, Kutná Hora
 Předmět: Seminář chemie (SCH) Náplň: Obecná chemie, anorganická chemie, chemické výpočty, základy analytické chemie Třída: 3. ročník a septima Počet hodin: 2 hodiny týdně Pomůcky: Vybavení odborné učebny,
Předmět: Seminář chemie (SCH) Náplň: Obecná chemie, anorganická chemie, chemické výpočty, základy analytické chemie Třída: 3. ročník a septima Počet hodin: 2 hodiny týdně Pomůcky: Vybavení odborné učebny,
Jádro se skládá z kladně nabitých protonů a neutrálních neutronů -> nukleony
 Otázka: Atom a molekula Předmět: Chemie Přidal(a): Dituse Atom = základní stavební částice všech látek Skládá se ze 2 částí: o Kladně nabité jádro o Záporně nabitý elektronový obal Jádro se skládá z kladně
Otázka: Atom a molekula Předmět: Chemie Přidal(a): Dituse Atom = základní stavební částice všech látek Skládá se ze 2 částí: o Kladně nabité jádro o Záporně nabitý elektronový obal Jádro se skládá z kladně
02 Nevazebné interakce
 02 Nevazebné interakce Nevazebné interakce Druh chemické vazby Určují 3D konfiguraci makromolekul, účastní se mnoha biologických procesů, zodpovědné za uspořádání molekul v krystalu Síla nevazebných interakcí
02 Nevazebné interakce Nevazebné interakce Druh chemické vazby Určují 3D konfiguraci makromolekul, účastní se mnoha biologických procesů, zodpovědné za uspořádání molekul v krystalu Síla nevazebných interakcí
Částicové složení látek atom,molekula, nuklid a izotop
 Částicové složení látek atom,molekula, nuklid a izotop ATOM základní stavební částice všech hmotných těles jádro 100 000x menší než atom působí jaderné síly p + n 0 [1] e - stejný počet protonů a elektronů
Částicové složení látek atom,molekula, nuklid a izotop ATOM základní stavební částice všech hmotných těles jádro 100 000x menší než atom působí jaderné síly p + n 0 [1] e - stejný počet protonů a elektronů
vzrst elektronegativity
 Chemické názvosloví Chemické prvky (zjednodušen jen prvky) jsou látky složené z atom o stejném protonovém ísle (poet proton v jáde atomu). Každému prvku písluší uritý mezinárodní název a od nho odvozený
Chemické názvosloví Chemické prvky (zjednodušen jen prvky) jsou látky složené z atom o stejném protonovém ísle (poet proton v jáde atomu). Každému prvku písluší uritý mezinárodní název a od nho odvozený
Úvod do strukturní analýzy farmaceutických látek
 Úvod do strukturní analýzy farmaceutických látek Garant předmětu: Vyučující: doc. Ing. Bohumil Dolenský, Ph.D. prof. RNDr. Pavel Matějka, Ph.D., A136, linka 3687, matejkap@vscht.cz doc. Ing. Bohumil Dolenský,
Úvod do strukturní analýzy farmaceutických látek Garant předmětu: Vyučující: doc. Ing. Bohumil Dolenský, Ph.D. prof. RNDr. Pavel Matějka, Ph.D., A136, linka 3687, matejkap@vscht.cz doc. Ing. Bohumil Dolenský,
Metalografie ocelí a litin
 Metalografie ocelí a litin Metalografie se zabývá pozorováním a zkoumáním vnitřní stavby neboli struktury kovů a slitin. Dále také stanoví, jak tato struktura souvisí s chemickým složením, teplotou a tepelným
Metalografie ocelí a litin Metalografie se zabývá pozorováním a zkoumáním vnitřní stavby neboli struktury kovů a slitin. Dále také stanoví, jak tato struktura souvisí s chemickým složením, teplotou a tepelným
Metodika pro učitele Chemická vazba pro ZŠ (teoretické cvičení s tablety)
 Metodika pro učitele Chemická vazba pro ZŠ (teoretické cvičení s tablety) Základní charakteristika výukového programu: Délka: 3 vyučovací hodiny; možnost vybrat pouze určité kapitoly Věková kategorie:
Metodika pro učitele Chemická vazba pro ZŠ (teoretické cvičení s tablety) Základní charakteristika výukového programu: Délka: 3 vyučovací hodiny; možnost vybrat pouze určité kapitoly Věková kategorie:
anorganických sloučenin Iontové rovnice MUDr.Jan Pláteník, PhD Stavba hmoty: Atom Molekula Ion Sloučenina
 Opakování názvosloví anorganických sloučenin Iontové rovnice MUDr.Jan Pláteník, PhD Stavba hmoty: Atom Molekula Ion Sloučenina Směs (dispersní soustava) 1 Atom Nejmenšíčástice prvku, která vykazuje jeho
Opakování názvosloví anorganických sloučenin Iontové rovnice MUDr.Jan Pláteník, PhD Stavba hmoty: Atom Molekula Ion Sloučenina Směs (dispersní soustava) 1 Atom Nejmenšíčástice prvku, která vykazuje jeho
Vyšší odborná škola, Obchodní akademie a Střední odborná škola EKONOM, o. p. s. Litoměřice, Palackého 730/1
 DUM Základy přírodních věd DUM III/2-T3-2-20 Téma: Test obecná chemie Střední škola Rok: 2012 2013 Varianta: A Test obecná chemie Zpracoval: Mgr. Pavel Hrubý Mgr. Josef Kormaník TEST Otázka 1 OsO 4 je
DUM Základy přírodních věd DUM III/2-T3-2-20 Téma: Test obecná chemie Střední škola Rok: 2012 2013 Varianta: A Test obecná chemie Zpracoval: Mgr. Pavel Hrubý Mgr. Josef Kormaník TEST Otázka 1 OsO 4 je
Voda polární rozpouštědlo
 VY_32_INVACE_30_BEN05.notebook Voda polární rozpouštědlo Temacká oblast : Chemie anorganická chemie Datum vytvoření: 2. 8. 2012 Ročník: 2. ročník čtyřletého gymnázia (sexta osmiletého gymnázia) Stručný
VY_32_INVACE_30_BEN05.notebook Voda polární rozpouštědlo Temacká oblast : Chemie anorganická chemie Datum vytvoření: 2. 8. 2012 Ročník: 2. ročník čtyřletého gymnázia (sexta osmiletého gymnázia) Stručný
Molekulová spektroskopie 1. Chemická vazba, UV/VIS
 Molekulová spektroskopie 1 Chemická vazba, UV/VIS 1 Chemická vazba Silová interakce mezi dvěma atomy. Chemické vazby jsou soudržné síly působící mezi jednotlivými atomy nebo ionty v molekulách. Chemická
Molekulová spektroskopie 1 Chemická vazba, UV/VIS 1 Chemická vazba Silová interakce mezi dvěma atomy. Chemické vazby jsou soudržné síly působící mezi jednotlivými atomy nebo ionty v molekulách. Chemická
Metodika pro učitele Chemická vazba pro SŠ (teoretické cvičení s tablety)
 Metodika pro učitele Chemická vazba pro SŠ (teoretické cvičení s tablety) Základní charakteristika výukového programu: Délka: 4 5 vyučovacích hodin; možnost vybrat pouze určité kapitoly Věková kategorie:
Metodika pro učitele Chemická vazba pro SŠ (teoretické cvičení s tablety) Základní charakteristika výukového programu: Délka: 4 5 vyučovacích hodin; možnost vybrat pouze určité kapitoly Věková kategorie:
DOUČOVÁNÍ KVINTA CHEMIE
 1. ÚVOD DO STUDIA CHEMIE 1) Co studuje chemie? 2) Rozděl chemii na tři důležité obory. DOUČOVÁNÍ KVINTA CHEMIE 2. NÁZVOSLOVÍ ANORGANICKÝCH SLOUČENIN 1) Pojmenuj: BaO, N 2 0, P 4 O 10, H 2 SO 4, HMnO 4,
1. ÚVOD DO STUDIA CHEMIE 1) Co studuje chemie? 2) Rozděl chemii na tři důležité obory. DOUČOVÁNÍ KVINTA CHEMIE 2. NÁZVOSLOVÍ ANORGANICKÝCH SLOUČENIN 1) Pojmenuj: BaO, N 2 0, P 4 O 10, H 2 SO 4, HMnO 4,
6.3.2 Periodická soustava prvků, chemické vazby
 6.3. Periodická soustava prvků, chemické vazby Předpoklady: 060301 Nejjednodušší atom: vodík s jediným elektronem v obalu. Ostatní prvky mají více protonů v jádře i více elektronů v obalu změny oproti
6.3. Periodická soustava prvků, chemické vazby Předpoklady: 060301 Nejjednodušší atom: vodík s jediným elektronem v obalu. Ostatní prvky mají více protonů v jádře i více elektronů v obalu změny oproti
Tvary víceatomových molekul. Nevazebné mezimolekulové interakce
 Tvary víceatomových molekul Nevazebné mezimolekulové interakce Lewisovy vzorce kovalentních sloučenin ybridizace atomových orbitalů (A) Tvary molekul metoda VSEPR Dipólový moment Van der Waalsovy síly
Tvary víceatomových molekul Nevazebné mezimolekulové interakce Lewisovy vzorce kovalentních sloučenin ybridizace atomových orbitalů (A) Tvary molekul metoda VSEPR Dipólový moment Van der Waalsovy síly
VLASTNOSTI LÁTEK. Autor: Mgr. Stanislava Bubíková. Datum (období) tvorby: Ročník: osmý
 Autor: Mgr. Stanislava Bubíková VLASTNOSTI LÁTEK Datum (období) tvorby: 27. 3. 2012 Ročník: osmý Vzdělávací oblast: Člověk a příroda / Chemie / Pozorování, pokus a bezpečnost práce 1 Anotace: Žáci se seznámí
Autor: Mgr. Stanislava Bubíková VLASTNOSTI LÁTEK Datum (období) tvorby: 27. 3. 2012 Ročník: osmý Vzdělávací oblast: Člověk a příroda / Chemie / Pozorování, pokus a bezpečnost práce 1 Anotace: Žáci se seznámí
Gymnázium Jiřího Ortena, Kutná Hora
 Předmět: Náplň: Třída: Počet hodin: Pomůcky: Chemie (CHE) Obecná chemie 1. ročník a kvinta 2 hodiny týdně Školní tabule, interaktivní tabule, tyčinkové a kalotové modely molekul, zpětný projektor, transparenty,
Předmět: Náplň: Třída: Počet hodin: Pomůcky: Chemie (CHE) Obecná chemie 1. ročník a kvinta 2 hodiny týdně Školní tabule, interaktivní tabule, tyčinkové a kalotové modely molekul, zpětný projektor, transparenty,
Struktura Molekul a Chemická Vazba
 Struktura Molekul a Chemická Vazba Slučováním atomů vznikají molekuly na základě chemické vazby. (~100 atomů ~10 6 různých molekul) Elektronová teorie chemické vazby: každý atom se snaží dosáhnout elektronové
Struktura Molekul a Chemická Vazba Slučováním atomů vznikají molekuly na základě chemické vazby. (~100 atomů ~10 6 různých molekul) Elektronová teorie chemické vazby: každý atom se snaží dosáhnout elektronové
Na Zemi tvoří vodík asi 15 % atomů všech prvků. Chemické slučování je děj, při kterém z látek jednodušších vznikají látky složitější.
 Nejjednodušší prvek. Na Zemi tvoří vodík asi 15 % atomů všech prvků. Chemické slučování je děj, při kterém z látek jednodušších vznikají látky složitější. Vodík tvoří dvouatomové molekuly, je lehčí než
Nejjednodušší prvek. Na Zemi tvoří vodík asi 15 % atomů všech prvků. Chemické slučování je děj, při kterém z látek jednodušších vznikají látky složitější. Vodík tvoří dvouatomové molekuly, je lehčí než
12.CHALKOGENY A HALOGENY
 12.CHALKOGENY A HALOGENY Chalkogeny ( česky se jedná o prvky ) 1) Popiš obecnou charakteristiku dané skupiny (počet valenčních elektronů, obecná elektronová konfigurace valenční vrstvy, způsoby dosažení
12.CHALKOGENY A HALOGENY Chalkogeny ( česky se jedná o prvky ) 1) Popiš obecnou charakteristiku dané skupiny (počet valenčních elektronů, obecná elektronová konfigurace valenční vrstvy, způsoby dosažení
12. Struktura a vlastnosti pevných látek
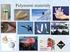 12. Struktura a vlastnosti pevných látek Osnova: 1. Látky krystalické a amorfní 2. Krystalová mřížka, příklady krystalových mřížek 3. Poruchy krystalových mřížek 4. Druhy vazeb mezi atomy 5. Deformace
12. Struktura a vlastnosti pevných látek Osnova: 1. Látky krystalické a amorfní 2. Krystalová mřížka, příklady krystalových mřížek 3. Poruchy krystalových mřížek 4. Druhy vazeb mezi atomy 5. Deformace
Složení látek a chemická vazba Číslo variace: 1
 Složení látek a chemická vazba Číslo variace: 1 Zkoušecí kartičku si PODEPIŠ a zapiš na ni ČÍSLO VARIACE TESTU (číslo v pravém horním rohu). Odpovědi zapiš na zkoušecí kartičku, do testu prosím nepiš.
Složení látek a chemická vazba Číslo variace: 1 Zkoušecí kartičku si PODEPIŠ a zapiš na ni ČÍSLO VARIACE TESTU (číslo v pravém horním rohu). Odpovědi zapiš na zkoušecí kartičku, do testu prosím nepiš.
Veličiny- základní N A. Látkové množství je dáno podílem N částic v systému a Avogadrovy konstanty NA
 YCHS, XCHS I. Úvod: plán přednášek a cvičení, podmínky udělení zápočtu a zkoušky. Základní pojmy: jednotky a veličiny, základy chemie. Stavba atomu a chemická vazba. Skupenství látek, chemické reakce,
YCHS, XCHS I. Úvod: plán přednášek a cvičení, podmínky udělení zápočtu a zkoušky. Základní pojmy: jednotky a veličiny, základy chemie. Stavba atomu a chemická vazba. Skupenství látek, chemické reakce,
Periodický systém víceelektronové systémy elektronová konfigurace periodický systém periodicita fyzikálních a chemických vlastností
 Periodický systém víceelektronové systémy elektronová konfigurace periodický systém periodicita fyzikálních a chemických vlastností obrázky molekul a Lewisovy vzorce molekul v této přednášce čerpány z:
Periodický systém víceelektronové systémy elektronová konfigurace periodický systém periodicita fyzikálních a chemických vlastností obrázky molekul a Lewisovy vzorce molekul v této přednášce čerpány z:
MŘÍŽKY A VADY. Vnitřní stavba materiálu
 Poznámka: tyto materiály slouží pouze pro opakování STT žáků SPŠ Na Třebešíně, Praha 10;s platností do r. 2016 v návaznosti na platnost norem. Zákaz šířění a modifikace těchto materálů. Děkuji Ing. D.
Poznámka: tyto materiály slouží pouze pro opakování STT žáků SPŠ Na Třebešíně, Praha 10;s platností do r. 2016 v návaznosti na platnost norem. Zákaz šířění a modifikace těchto materálů. Děkuji Ing. D.
Inovace studia molekulární a buněčné biologie
 Investice do rozvoje vzdělávání Inovace studia molekulární a buněčné biologie Tento projekt je spolufinancován Evropským sociálním fondem a státním rozpočtem České republiky. Investice do rozvoje vzdělávání
Investice do rozvoje vzdělávání Inovace studia molekulární a buněčné biologie Tento projekt je spolufinancován Evropským sociálním fondem a státním rozpočtem České republiky. Investice do rozvoje vzdělávání
Průvodka. CZ.1.07/1.5.00/ Zkvalitnění výuky prostřednictvím ICT. III/2 Inovace a zkvalitnění výuky prostřednictvím ICT
 Průvodka Číslo projektu Název projektu Číslo a název šablony klíčové aktivity CZ.1.07/1.5.00/34.0802 Zkvalitnění výuky prostřednictvím ICT III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Příjemce
Průvodka Číslo projektu Název projektu Číslo a název šablony klíčové aktivity CZ.1.07/1.5.00/34.0802 Zkvalitnění výuky prostřednictvím ICT III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Příjemce
Protonové číslo Z - udává počet protonů v jádře atomu, píše se jako index vlevo dole ke značce prvku
 Stavba jádra atomu Protonové Z - udává protonů v jádře atomu, píše se jako index vlevo dole ke značce prvku Neutronové N - udává neutronů v jádře atomu Nukleonové A = Z + N, udává nukleonů (protony + neutrony)
Stavba jádra atomu Protonové Z - udává protonů v jádře atomu, píše se jako index vlevo dole ke značce prvku Neutronové N - udává neutronů v jádře atomu Nukleonové A = Z + N, udává nukleonů (protony + neutrony)
Struktura atomů a molekul
 Struktura atomů a molekul Obrazová příloha Michal Otyepka tento text byl vysázen systémem L A TEX2 ε ii Úvod Dokument obsahuje všechny obrázky tak, jak jsou uvedeny ve druhém vydání skript Struktura atomů
Struktura atomů a molekul Obrazová příloha Michal Otyepka tento text byl vysázen systémem L A TEX2 ε ii Úvod Dokument obsahuje všechny obrázky tak, jak jsou uvedeny ve druhém vydání skript Struktura atomů
Biochemie žákovská sada Obj. číslo
 Biochemie žákovská sada Obj. číslo 204.5041 Strana 1 z 28 Karty k základním strukturám od R. S. Lowrieho, studijního ředitele, Oxford School. Úvod Systém molekulárních modelů umožňuje vytvářet struktury
Biochemie žákovská sada Obj. číslo 204.5041 Strana 1 z 28 Karty k základním strukturám od R. S. Lowrieho, studijního ředitele, Oxford School. Úvod Systém molekulárních modelů umožňuje vytvářet struktury
anorganických sloučenin Iontové rovnice MUDr. Jan Pláteník, PhD. Stavba hmoty: Atom Molekula Ion Sloučenina
 Opakování názvosloví anorganických sloučenin Iontové rovnice MUDr. Jan Pláteník, PhD. Stavba hmoty: Atom Molekula Ion Sloučenina Směs (dispersní soustava) 1 Atom Nejmenšíčástice prvku, která vykazuje jeho
Opakování názvosloví anorganických sloučenin Iontové rovnice MUDr. Jan Pláteník, PhD. Stavba hmoty: Atom Molekula Ion Sloučenina Směs (dispersní soustava) 1 Atom Nejmenšíčástice prvku, která vykazuje jeho
Historie. - elektrizace tením (elektron = jantar) - Magnetismus magnetovec pitahuje železo. procházející proud vytváí magnetické pole
 Historie Staréecko: elektrizace tením (elektron = jantar) Magnetismus magnetovec pitahuje železo Hans Christian Oersted objevil souvislost mezi elektinou a magnetismem procházející proud vytváí magnetické
Historie Staréecko: elektrizace tením (elektron = jantar) Magnetismus magnetovec pitahuje železo Hans Christian Oersted objevil souvislost mezi elektinou a magnetismem procházející proud vytváí magnetické
Masarykova střední škola zemědělská a Vyšší odborná škola, Opava, příspěvková organizace
 Číslo projektu Číslo materiálu Název školy Autor Průřezové téma Tematický celek CZ.1.07/1.5.00/34.0565 VY_32_INOVACE_345_PSP a chemická vazba Masarykova střední škola zemědělská a Vyšší odborná škola,
Číslo projektu Číslo materiálu Název školy Autor Průřezové téma Tematický celek CZ.1.07/1.5.00/34.0565 VY_32_INOVACE_345_PSP a chemická vazba Masarykova střední škola zemědělská a Vyšší odborná škola,
Prvky 14. Skupiny (Tetrely)
 Prvky 14. Skupiny (Tetrely) 19.1.2011 p 2 prvky C nekov Si, Ge polokov Sn, Pb kov ns 2 np 2 Na vytvoření kovalentních vazeb ve sloučeninách poskytují 2, nebo 4 elektrony Všechny prvky jsou pevné látky
Prvky 14. Skupiny (Tetrely) 19.1.2011 p 2 prvky C nekov Si, Ge polokov Sn, Pb kov ns 2 np 2 Na vytvoření kovalentních vazeb ve sloučeninách poskytují 2, nebo 4 elektrony Všechny prvky jsou pevné látky
Periodický systém víceelektronové systémy elektronová konfigurace periodický systém periodicita fyzikálních a chemických vlastností
 Periodický systém víceelektronové systémy elektronová konfigurace periodický systém periodicita fyzikálních a chemických vlastností obrázky molekul a Lewisovy vzorce molekul v této přednášce čerpány z:
Periodický systém víceelektronové systémy elektronová konfigurace periodický systém periodicita fyzikálních a chemických vlastností obrázky molekul a Lewisovy vzorce molekul v této přednášce čerpány z:
ZŠ ÚnO, Bratří Čapků 1332
 Animovaná chemie Top-Hit Analytická chemie Analýza anorganických látek Důkaz aniontů Důkaz kationtů Důkaz kyslíku Důkaz vody Gravimetrická analýza Hmotnostní spektroskopie Chemická analýza Nukleární magnetická
Animovaná chemie Top-Hit Analytická chemie Analýza anorganických látek Důkaz aniontů Důkaz kationtů Důkaz kyslíku Důkaz vody Gravimetrická analýza Hmotnostní spektroskopie Chemická analýza Nukleární magnetická
Nekovalentní interakce
 Nekovalentní interakce Jan Řezáč UOCHB AV ČR 31. října 2017 Jan Řezáč (UOCHB AV ČR) Nekovalentní interakce 31. října 2017 1 / 28 Osnova 1 Teorie 2 Typy nekovalentních interakcí 3 Projevy v chemii 4 Výpočty
Nekovalentní interakce Jan Řezáč UOCHB AV ČR 31. října 2017 Jan Řezáč (UOCHB AV ČR) Nekovalentní interakce 31. října 2017 1 / 28 Osnova 1 Teorie 2 Typy nekovalentních interakcí 3 Projevy v chemii 4 Výpočty
Předmět: CHEMIE Ročník: 8. ŠVP Základní škola Brno, Hroznová 1. Výstupy předmětu
 Chemie ukázka chemického skla Chemie přírodní věda, poznat chemické sklo a pomůcky, zásady bezpečné práce práce s dostupnými a běžně používanými látkami (směsmi). Na základě piktogramů žák posoudí nebezpečnost
Chemie ukázka chemického skla Chemie přírodní věda, poznat chemické sklo a pomůcky, zásady bezpečné práce práce s dostupnými a běžně používanými látkami (směsmi). Na základě piktogramů žák posoudí nebezpečnost
Test vlastnosti látek a periodická tabulka
 DUM Základy přírodních věd DUM III/2-T3-2-08 Téma: Test vlastnosti látek a periodická tabulka Střední škola Rok: 2012 2013 Varianta: A Zpracoval: Mgr. Pavel Hrubý Mgr. Josef Kormaník TEST Test vlastnosti
DUM Základy přírodních věd DUM III/2-T3-2-08 Téma: Test vlastnosti látek a periodická tabulka Střední škola Rok: 2012 2013 Varianta: A Zpracoval: Mgr. Pavel Hrubý Mgr. Josef Kormaník TEST Test vlastnosti
Typy molekul, látek a jejich vazeb v organismech
 Typy molekul, látek a jejich vazeb v organismech Typy molekul, látek a jejich vazeb v organismech Organismy se skládají z molekul rozličných látek Jednotlivé látky si organismus vytváří sám z jiných látek,
Typy molekul, látek a jejich vazeb v organismech Typy molekul, látek a jejich vazeb v organismech Organismy se skládají z molekul rozličných látek Jednotlivé látky si organismus vytváří sám z jiných látek,
Do této skupiny patří dusík, fosfor, arsen, antimon a bismut. Společnou vlastností těchto prvků je pět valenčních elektronů v orbitalech ns a np:
 PRVKY PÁTÉ SKUPINY Do této skupiny patří dusík, fosfor, arsen, antimon a bismut. Společnou vlastností těchto prvků je pět valenčních elektronů v orbitalech ns a np: Obecná konfigurace: ns np Nejvyšší kladné
PRVKY PÁTÉ SKUPINY Do této skupiny patří dusík, fosfor, arsen, antimon a bismut. Společnou vlastností těchto prvků je pět valenčních elektronů v orbitalech ns a np: Obecná konfigurace: ns np Nejvyšší kladné
Struktura elektronového obalu
 Projekt: Inovace oboru Mechatronik pro Zlínský kraj Registrační číslo: CZ.1.07/1.1.08/03.0009 Struktura elektronového obalu Představy o modelu atomu se vyvíjely tak, jak se zdokonalovaly možnosti vědy
Projekt: Inovace oboru Mechatronik pro Zlínský kraj Registrační číslo: CZ.1.07/1.1.08/03.0009 Struktura elektronového obalu Představy o modelu atomu se vyvíjely tak, jak se zdokonalovaly možnosti vědy
ZŠ ÚnO, Bratří Čapků 1332
 Úvodní obrazovka Menu (vlevo nahoře) Návrat na hlavní stránku Obsah Výsledky Poznámky Záložky edunet Konec Chemie 1 (pro 12-16 let) LangMaster Obsah (střední část) výběr tématu - dvojklikem v seznamu témat
Úvodní obrazovka Menu (vlevo nahoře) Návrat na hlavní stránku Obsah Výsledky Poznámky Záložky edunet Konec Chemie 1 (pro 12-16 let) LangMaster Obsah (střední část) výběr tématu - dvojklikem v seznamu témat
