Imunoterapie metastazujícího melanomu
|
|
|
- Natálie Kadlecová
- před 8 lety
- Počet zobrazení:
Transkript
1 183 Imunoterapie metastazujícího melanomu Ivana Krajsová Dermatovenerologická klinika VFN v Praze Aktivace imunitního systému je velmi důležitým krokem v léčebné strategii metastazujícího melanomu a větší pochopení funkce kontrolních bodů imunity vedlo k vývoji řady checkpoint inhibitorů. Ipilimumab, monoklonální protilátka proti CTLA-4 byl první lék, který prokázal zlepšení přežití u pacientů s metastazujícím melanomem. Medián celkového přežití (OS) u pacientů léčených ipilimumabem byl, při porovnání s pacienty léčenými gp100 vakcínou, delší (10,9 proti 6,4 měsíce) a také pacienti léčení ipilimumabem a DTIC měli, proti pacientům léčeným samotným DTIC zlepšené OS (11,2 proti 9,1 měsíce). Většina nežádoucích účinků vyvolaných léčbou ipilimumabem jsou imunitně zprostředkované a mezi nejčastější patří gastrointestinální a kožní toxicita, endokrinopatie a hepatotoxicita. Koncem roku 2014 byly schváleny FDA pembrolizumab a nivolumab, nové monoklonální protilátky proti dalšímu významnému kontrolnímu bodu imunity PD-1 receptoru. Vstupujeme do nové éry v léčbě melanomu, ale nemůžeme říci, že je problematika léčby melanomu vyřešena. Je nutný další výzkum v oblasti biomarkerů a kombinované léčby, včetně optimálního dávkování i doby terapie. Klíčová slova: melanom, imunoterapie, anti CTLA-4. Immunotherapy for metastatic melanoma Activation of the immune system is very important step in the treatment strategy of metastatic melanoma and greater understanding of function of the immune checkpoints led to the development of several immune checkpoint inhibitors. Ipilimumab, an anti-ctla-4 monoclonal antibody, was the first agent to demonstrate a survival benefit in patients with metastatic cutaneous melanoma. The median OS rate for patients treated with ipilimumab was, compared with patients receiving a gp100 vaccine longer (10.9 versus 6.4 months), and also patients treated with ipilimumab and DTIC compared with those treated with DTIC alone had improved OS (median OS 11.2 versus 9.1 months.) The majority of ipilimumab-related adverse events are immune related, and the most common are gastrointenstinal and skin toxicity, endocrinopathy and hepatotoxicity. New monoclonal antibody against other important immunity checkpoint PD-1 receptor, pembrolizumab and nivolumab, got FDA approval at the end of We are approaching the new era of the treatment of melanoma but we cannot say, that we resolved the problem. Further research of biomarkers, combination therapies and also optimal dosing, and duration of treatment is needed. Key words: melanoma, immunotherapy, anti CTLA-4. Onkologie 2015; 9(4): Úvod Imunoterapie má již dlouhodobě v léčbě pokročilého i metastazujícího melanomu své nezastupitelné místo. Lepší pochopení principů vzájemné interakce nádoru a imunitního systému hostitele umožnilo postupný rozvoj imunoterapeutických postupů a přechod od nespecifické imunoterapie v imunoterapii specifickou, zaměřenou na konkrétní cíle. Jednou z cest, která umožňuje rozvoj nádoru, je únik nádorových buněk před detekcí imunitním systémem. Nádorová tolerance může být způsobena nízkou imunogenicitou samotného nádoru, ale také jeho schopností tlumit imunitní reakce. Vznik nádorové tolerance je velmi složitý a komplexní proces, kterého se účastní řada mechanizmů. Na jejím vzniku se mohou podílet také některé kontrolní body imunity tzv. checkpoints, mezi které patří cytotoxický T-lymfocytární antigen4 (CTLA-4) a programmed death-1 (PD-1) receptory a ligand PD-1 receptoru programmed death ligand-1 (PD-L1). Fyziologickou funkcí těchto receptorů je zpětnovazebný mechanizmus, ochrana před nadměrnou imunitní reakcí, před vyvoláním autoimunity. Jejich aktivace chrání organizmus před vznikem autoimunitních reakcí, ale současně umožňuje navození nádorové tolerance. Vývoj nových monoklonálních protilátek inhibujících receptory CTLA-4 a PD-1 znamenal možnost regulace T buněčné aktivace a proliferace s navazujícím ovlivněním T buněčné protinádorové imunitní reakce. Klinické studie s monoklonálními protilátkami, proti CTLA-4 ipilimumabem a proti PD-1 pembrolizumabem a nivolumabem, prokázaly jejich účinnost v léčbě metastazujícího melanomu. Rok 2011 je v moderní léčbě metastazujícího melanomu považován za zásadní. FDA byl schválen nový lék ipilimumab, který jako první v historii prokázal schopnost statisticky významného prodloužení celkového přežívání (OS) pacientů s metastazujícím melanomem. Velmi brzy následovalo schválení i dalších léků pegylovaného interferonu alfa pro adjuvantní léčbu pokročilého melanomu a BRAF a MEK inhibitorů, vemurafenibu, dabrafenibu a trametinibu pro terapii BRAF pozitivních melanomů. V roce 2014 byly schváleny monoklonální protilátky proti PD-1 receptoru pembrolizumab a nivolumab. Ve studiích fáze III prokazují četné a dlouhodobé léčebné odpovědi i prodloužení celkového přežití a mírnou, dobře zvládnutelnou toxicitu. Imunoterapie metastazujícího melanomu pomocí inhibice receptoru CTLA-4 Cytotoxický T lymfocytární antigen 4 (CTLA-4) je považován za významný kontrolní bod imunitního systému, jehož úkolem je ochrana před nadměrnou aktivací imunitního systému, před vznikem autoimunitních reakcí. Tento zpětnovazebný mechanizmus ale současně umožňuje vznik nádorové tolerance, protože usnadňuje únik nádorových buněk před protinádorovou T lymfocytární imunitní reakcí. Blokáda CTLA-4 receptoru ipilimumabem prodlužuje aktivaci T lymfocytů a obnovuje jejich proliferaci, čímž zesiluje T buněčné imunitní reakce a podporuje účinnou protinádorovou imunitní odpověď. Již první studie fáze II s ipilimumabem, plně humánní IgG1 monoklonální protilátkou, která blokuje CTLA-4 receptor, naznačovaly, že tento
2 184 Přehledové články Graf 1. Analýza přežití pacientů léčených ipilimumabem v rámci 12 klinických studií (převzato z 5) Medián OS 11,4 měsíců (95 % CI 10,7 12,1) křížky označují censorované pacienty způsob aktivace imunitního systému dokáže příznivě ovlivnit celkové přežívání (OS) pacientů s metastazujícím melanomem (1). Byla to velmi překvapivá pozorování, protože do té doby se prodloužení celkového přežití nemocných s metastazujícím melanomem zdálo nedostižným cílem. Zásadní pro klinické využití ipilimumabu byly výsledky Hodiho studie fáze III publikované v NEJM v roce 2010 (2). Studie porovnávala účinnost terapie ipilimumabem v kombinaci s gp100 vakcínou, ipilimumabem samotným a samotnou gp100 vakcínou a prokázala významné prodloužení OS. Ipilimumab byl podáván v dávce 3 mg/ kg. Medián celkového přežití byl u pacientů léčených ipilimumabem + gp100 vakcínou 10,0 měsíců, u pacientů léčených ipilimumabem 10,1 měsíců, zatímco u pacientů léčených samotnou vakcínou byl pouze 6,4 měsíců (p < 0,001). U pacientů, léčených ipilimumabem, došlo ke snížení rizika o 32 resp. 34 % proti léčbě samotnou vakcínou. Ještě pozoruhodnější bylo zlepšení dlouhodobého přežití. Při hodnocení po 24 měsících od zahájení léčby přežívalo 21,6 a 23,5 % pacientů léčených ipilimumabem a pouze 13,7 % pacientů léčených gp100 vakcínou. Podobné výsledky potvrdila i další studie fáze III hodnotící účinnost kombinované léčby ipilimumabem s DTIC proti léčbě samotným DTIC u nemocných v první linii léčby metastazujícího melanomu (3). Primárním cílem bylo hodnocení OS, které bylo signifikantně delší ve skupině nemocných léčených ipilimumabem s DTIC 11,2 měsíců proti 9,1 měsícům u pacientů, kteří dostávali pouze DTIC (p < 0,001). Jeden rok po zahájení léčby přežívalo 47,3 % proti 36,3 % nemocných, 2 roky 28,5 % proti 17,9 % a 3 roky 20,8 % proti 12,2 %. Ipilimumab v léčbě metastazujícího melanomu byl zkoušen v řadě studií fáze II a III v různém dávkování i v různých léčebných schématech. V listopadu 2014 byly v Annals of Oncology publikovány zajímavé výsledky studie BMS 025 (C. Lebbé a kolektiv) aktualizující pěti až šestileté sledování a přežití pacientů, původně léčených ipilimumabem ve studiích fáze II. Cílem bylo zhodnotit medián doby přežití a četnost přežití od podání první dávky ipilimumabu v původních studiích k červnu 2013 a zhodnocení nežádoucích účinků léčby. Do studie bylo zařazeno 248 pacientů, u 93 byla zahájena nová léčba ipilimumabem, 91 nemocných pokračovalo v udržovací léčbě, a 58 bylo sledováno bez léčby. Pětileté přežití u pacientů léčených v druhé či další linii léčby ze studií BMS , 008 a 022 bylo 12,3% pro ipilimumab v dávce 0,3mg/kg, 16,5 % pro ipilimumab 3 mg/kg a 18,2 28,4 % u dávek 10mg/kg. U nemocných, kteří dostávali ipilimumab v první linii léčby společně s budesonidem či placebem studie CA , bylo dosaženo pětileté přežití u 37,7 % ve skupině ipilimumab + placebo a u 49,5 % ve skupině ipilimumab + budesonid. Nebyly popsány žádné neočekávané nežádoucí účinky léčby, shodovaly se s běžně pozorovanými v jiných studiích (4). Podrobně budou zmíněny v kapitole věnované této problematice. Výsledky studie BMS mají svá omezení, protože byla analyzována data různě projektovaných studií, s různými populacemi pacientů i odlišným dávkováním. Přesto je možné pozorovat stejný trend jako v dalších ipilimumabových studiích, tedy dlouhé trvání dosažených léčebných odpovědí i dlouhodobé přežívání léčených pacientů. V této studii 82,6 % nemocných, kteří žili 3 roky po zahájení léčby, žili i v odstupu 5 let (4). Také další analýza studií fáze II a III s ipilimumabem v léčbě metastazujícího melanomu zpracovaná Schadendorfem a publikovaná v únoru 2015 v JCO (Journal of Clinical Oncology) potvrzuje dlouhodobý efekt léčby. Hodnoceno bylo celkem pacientů z 12 klinických studií. Medián OS byl 11,4 měsíce a 3 roky přežívalo 22 % nemocných (graf 1). Na křivce OS je patrné plateau objevující se v odstupu 3 let od zahájení léčby. Potvrzuje, že většina nemocných léčených ipilimumabem, kteří přežívají 36 měsíců a déle, má vysokou šanci na dlouhodobé přežití (5). Praktické využití ipilimumabu Ipilimumab pod firemním názvem Yervoy je v současné době v ČR schválen pro terapii metastazujícího melanomu v druhé a další linii léčby, tedy po předchozím selhání chemoterapie a v případě BRAF pozitivních nádorů po selhání léčby BRAF inhibitory a chemoterapií. Smí být aplikován pouze v rámci stanovených onkologických center (obrazek 1). Yervoy je podáván v dávce 3 mg/kg intravenózně v 90 minut trvající infuzi, celkem 4 v třítýdenních intervalech, celá léčba trvá 9 týdnů. Léčebný účinek nastupuje většinou výrazně později než u chemoterapie, která se projevuje přímým cytostatickým účinkem. Ipilimumab nejprve zablokuje receptor CTLA-4 a teprve poté dochází k aktivaci a proliferaci T lymfocytů následované protinádorovou T imunitní reakcí. Infiltrace nádoru T lymfocyty může v některých případech způsobit i zvětšení ložiska a imitovat progresi onemocnění. Jsou popisovány i případy vzniku nových ložisek při současné stabilizaci nebo zmenšování ostatních. V jiných případech nenastane objektivní zmenšení nádorových mas, podle RECIST či WHO kritérií, přesto nedochází k progresi a onemocnění může zůstávat i mnoho let stabilizované. Vzhledem k odlišnostem v charakteru léčebných odpovědí byla navržena nová hodnotící kritéria označovaná jako immune related response criteria (irrc). Zhodnocení léčebných odpovědí se provádí nejdříve v rozmezí týdnů po první dávce ipilimumabu a dále ve 12týdenních intervalech. Nežádoucí účinky imunoterapie anti CTLA-4 a jejich léčba Léčba ipilimumabem je spojena s nežádoucími účinky, které jsou vyvolané aktivací imunitního systému. Za normálních okolností Onkologie 2015; 9(4)
3 185 Obrázek 1. Metastazující melanom prvních 6 9 týdnů po úvodní dávce ipilimumabu, pouze v omezeném počtu případů dochází k jejich vzniku až v odstupu týdnů nebo měsíců po zahájení léčby. Doba trvání nežádoucích účinků se pohybuje nejčastěji mezi 4,3 7,7 týdny, nejdůležitější pro jejich rychlý ústup je včasné rozpoznání a zahájení léčby (8). Terapie jednotlivých iraes se řídí charakterem postižení jednotlivých orgánů i jejich závažností. Lékem volby, zejména u stupně 3 a 4 jsou systémově podávané kortikoidy. Nejčastěji je při léčbě ipilimumabem popisována kožní toxicita, ale za nejzávažnější je nutné považovat postižení gastrointestinálního traktu. Obrázek 2. Kožní toxicita při léčbě ipilimumabem receptor CTLA-4 reguluje, tlumí imunitní reakce a chrání před vznikem autoimunity. Zablokování CTLA-4 ipilimumabem tak může spustit širokou škálu autoimunitních reakcí zaměřených na různé orgány. Označují se jako immune-related adverse events (iraes) a jsou typickými nežádoucími účinky této léčby. Jejich charakter odpovídá principu léčby zesílení T buněčné reaktivity. Studie věnovaná účinnosti léčby ipilimumabem při použití různých dávek 0,3 3,0 10,0 mg/kg naznačila, že se zvyšující se dávkou stoupá nejen účinnost ale i toxicita léčby (6). Dávka 10 mg/kg je spojena zejména s vyšší četností nežádoucích účinků v oblasti GIT. Retrospektivní analýza proběhlých a ukončených studií s různými dávkami ipilimumabu ukázala, že iraes byly popisovány asi u 64 % léčených pacientů, ale komplikace vedoucí ke smrti nemocných byly nižší než 1 % (7). Nejčastěji popisovanými nežádoucími účinky jsou: gastrointestinální (GIT) a kožní toxicita, dále hepatotoxicita a endokrinní toxicita. Méně často se objevuje oftalmologická či neurologická toxicita a velmi vzácně byly zaznamenány nežádoucí účinky postihující respirační nebo genitourinární trakt. Většina iraes bývá popisována již v průběhu indukční léčby tedy během GIT toxicita Gastrointenstinální toxicita patří mezi typické nežádoucí účinky léčby ipilimumabem a je pro ni charakteristický pestrý klinický obraz. Může se projevovat pouze neurčitými nevýraznými bolestmi břicha, nechutenstvím či nauzeou, zvýrazněnou střevní peristaltikou, ale také zvracením a průjmy. Průjmovitou stolici je možné považovat za dominantní příznak GIT toxicity. Bývá popisována u % léčených pacientů. Potíže začínají většinou náhle velmi řídkou až vodnatou stolicí, která se může opakovat krátce po sobě s následným několikahodinovým vymizením příznaků a poté návratem potíží. Průjmy se objevují převážně mezi 5 12 týdnem od zahájení léčby, nejčastěji tedy po druhé nebo třetí dávce ipilimumabu. Neléčená, průjmovitá stolice se trvale zhoršuje a může vést k těžké kolitidě s ulceracemi, případně i k perforaci střeva. Správně léčená GIT toxicita naopak odeznívá většinou v průběhu 4 týdnů. Na základě tíže postižení, hodnoceného podle CTCAE (Common Terminology Criteria for Adverse Events) kritérií verze 3 nebo 4, lékař rozhodne o dalším léčebném postupu. Při mírném postižení stupně 1 a 2 může být dostačující pouze symptomatická léčba, dostatečná hydratace, střevo šetřící dieta a případně loperamid, živočišné uhlí a podobné přípravky. Je však nutný pečlivý monitoring pacienta a odložení další dávky ipilimumabu do odeznění příznaků nebo zmírnění na stupeň 1. Pokud potíže neustupují a přetrvává závažnost stupně 2 nebo se průjmy zhoršují, je vhodné zvážit koloskopii, vyloučení infekční etiologie, ale zejména je vhodné již v této fázi zahájit podávání kortikosteroidů. Při průjmech stupně 3 a 4 nebo při potvrzené kolitidě musí být trvale ukončena terapie ipilimumabem a musí být zahájeno podávání kortikosteroidů ve vysokých dávkách, nejlépe methyprednisolon v úvodní dávce 2 mg/ kg i.v. a dále dle stavu pacienta udržovací léčba
4 186 Přehledové články v dávkách 1 2 mg/kg. Teprve po ústupu příznaků a zmírnění potíží je možné velmi pomalu dávky kortikoidů snižovat. Ke kompletnímu vysazení steroidů by nemělo dojít dříve než za 30 dní, vhodnější je postupné snižování dávky až v rozmezí dní, jinak hrozí recidiva potíží (9). Pro léčbu průjmů je možné někdy využít také budenosid v dávce 9 mg denně. Jeho profylaktické podávání ale vzniku GIT toxicity zabránit nedokáže, jak prokázala studie BMS Ve vzácných případech rezistence k léčbě kortikoidy je nutné aplikovat infliximab v dávce 5 mg/kg. Základem léčby GIT toxicity je včasné rozpoznání příznaků a včasné zahájení odpovídající léčby. Ještě před zahájením podávání ipilimumabu je nezbytné nemocné správně instruovat o nutnosti okamžitě informovat ošetřujícího lékaře o vzniku průjmu či zažívacích potíží. Důležité je primárně každý průjem vzniklý v průběhu léčby ipilimumabem považovat za komplikaci léčby a odpovídajícím způsobem léčit. Kožní toxicita Nejčastějším nežádoucím účinkem léčby ipilimumabem je kožní toxicita, popisovaná u 40 60% pacientů. Ve většině případů nezpůsobuje nemocným závažné potíže. Patří mezi nejčasněji vznikající nežádoucí účinky, objevuje se často již po první nebo druhé dávce ipilimumabu. Typickým příznakem je svědění kůže, které může, ale nemusí být provázeno kožními projevy a bývá popisováno až u 30 % nemocných. Pokud dojde ke kožnímu postižení, projevuje se většinou makulopapulozním exantémem postihujícím různé partie těla (obrázek 2). Příznakem kožní toxicity může být také vznik vitiliga, objevující se u 4 11 % nemocných, jako příznak autoimunitní reakce proti melanocytům. Byly popsány případy exacerbace atopického ekzému, ložiskové defluvium nebo vznik kožní sarkoidózy. Velmi vzácně, v méně než 1 % případů, je popisována závažnější kožní toxicita v podobě Stevens-Johnsonova syndromu či Lyelova syndromu, dále fotosenzitivita nebo DRESS syndrom (drug reaction and eosinophilia with systemic symptoms). Léčba kožní toxicity je závislá na charakteru a tíži postižení. Většinou je dostačující lokální léčba kortikoidními externy, u těžších případů kožní toxicity je vhodné systémové podání kortikoidů (10). Pouze závažná kožní toxicita vyžaduje trvalé ukončení léčby ipilimumabem. Hepatotoxicita Hepatotoxicita bývá často asymptomatická, bez subjektivních potíží, detekovatelná pouze průkazem elevace jaterních testů. Je proto nezbytné v průběhu léčby ipilimumabem pečlivě monitorovat hodnoty transamináz a bilirubinu. Objevuje se většinou v rozmezí 3 9 týdnů od zahájení léčby. V diferenciální diagnostice je nutné vyloučit infekční hepatitidy či jaterní metastázy. U závažné hepatotoxicity stupně 3 a 4, která je indikací k trvalému ukončení léčby ipilimumabem, jsou lékem volby opět systémově podávané kortikoidy, nejčastěji methylpredniosolon v dávce 1 2 mg/kg. Základem úspěšnosti léčby je její včasné zahájení a pomalé postupné vysazování. Při správné léčbě většinou dochází k normalizaci jaterních funkcí v průběhu 4 týdnů. Ve vzácných případech rezistence k terapii kortikoidy je indikováno podávání mycophenolat mofetilu (9, 10). Endokrinní toxicita Typickými a nejčastějšími endokrinopatiemi vyvolanými léčbou ipilimumabem jsou autoimunní thyreoiditida, hypofyzitida a insuficience nadledvin, objevující se asi u 4 8 % pacientů (2). První příznaky nastupují většinou až ke konci léčby mezi týdnem a projevují se výraznou únavou, bolestmi hlavy, závratěmi, poruchami zraku, ztrátou libida a řadou dalších ne zcela specifických příznaků. Nejčastěji mohou připomínat metastatické postižení CNS. Etiologii potíží v těchto případech snadno odhalí vyšetření hladin minerálů, kortizolu, ft3, ft4, TSH a případně pohlavních hormonů. Při podezření na hypofyzitidu je doporučováno CT či MR CNS se zaměřením na oblast tureckého sedla. Nejúčinnější léčbou je hormonální substituce odpovídající zjištěné endokrinopatii tedy nejčastěji podávání thyroxinu nebo kortizolu, méně často také sexuálních hormonů. Na rozdíl od předchozích nežádoucích účinků bývají autoimunitně vyvolané endokrinopatie dlouhodobé, většinou s trvalou potřebou hormonální substituce (11). Méně časté nežádoucí účinky Byly popsány i případy postižení dalších orgánů, vyskytující se ale většinou v méně než 1 % případů. Jedná se například o neurologickou toxicitu v podobě senzorické i motorické neuropatie nebo myastenie gravis. Zcela ojediněle byly zaznamenány případy Guillain-Barré syndromu. Oční toxicita se projevuje převážně vznikem uveitidy, episkleritidy nebo iritidy. V jejich léčbě je většinou dostačující lokální aplikace steroidů, vzácně je nutná systémová léčba kortikoidy. Byly popsány také ojedinělé případy plicní toxicity v podobě atypických pneumonií nebo plicní sarkoidózy (9). Základem úspěšnosti léčby nežádoucích účinků je jejich včasná diagnostika a včasné zahájení léčby. Obecně jsou lékem volby kortikoidy, u toxicity stupně 3 a vyšší většinou v iniciální dávce 2 mg/kg intravenózně s postupným poklesem na 1 mg/kg a následným přechodem na perorální podávání. I když se může zdát například léčba průjmů kortikoidy přinejmenším zvláštní, je zcela nezbytná, protože etiologicky jsou tyto průjmy vyvolané autoimunitní reakcí v oblasti GIT. Vždy je nutné pomalé vysazování léčby, jinak hrozí recidiva potíží. Závěr Metastazující melanom je vysoce rezistentní ke klasickým léčebným postupům jako je chemoterapie nebo aktinoterapie. Ještě v nedávné době se medián přežití těchto pacientů pohyboval na úrovni 6 9 měsíců a 5 let přežívalo maximálně 10 % nemocných. Zavedení cílené imunoterapie zaměřené na kontrolní body imunity znamenalo zcela nový směr v léčbě tohoto onemocnění. V současné době jsou v klinické praxi největší zkušenosti s terapií inhibitorem CTLA-4 ipilimumabem. Jeho klinická aktivita, v léčbě metastazujícího melanomu, představuje zcela nové možnosti terapie tohoto agresivního onemocnění. Hlavním přínosem ipilimumabu je dlouhá doba trvání léčebných odpovědí a významné prodloužení celkového přežití (12). Pět let přežívá % nemocných. Koncem roku 2014 byly pro léčbu metastazujícího melanomu schváleny další dva imunoterapeutické preparáty, zaměřené na inhibici receptoru PD-1, pembrolizumab (KeyTruda) a nivolumab (Opdivo). V ČR je dostupná léčba pembrolizumabem v rámci specifického léčebného programu u nemocných u kterých selhala předchozí léčba ipilimumabem a nivolumab zatím v rámci klinických studií ve stejné indikaci. V letošním roce i následujících letech jsou očekávány výsledky řady klinických studií s kombinovanou léčbou ipilimumab plus nivolumab, či kombinace imunoterapie s léčbou BRAF inhibitory, s chemoterapií nebo s aktinoterapií. Probíhají a připravují se také studie s využitím ipilimumabu, nivolumabu i pembrolizumabu v adjuvantním podávání u nemocných po operaci pokročilého kožního melanomu a první předběžné výsledky naznačují jejich účinnost i v této indikaci. I když vstupujeme do nové éry v léčbě metastazujícího melanomu, stále nemůžeme říci, že tato problematika byla vyřešena. Hlavní otázkou imunoterapie zůstává nalezení prediktivních faktorů, biomarkerů, které by lépe označily nemocné profitující z této léčby, nalezení optimálního dávkování i optimálního léčebného schématu. Onkologie 2015; 9(4)
5 189 Literatura 1. O Day SJ, Maio M, Chiarion-Sileni V, Gajewski TF, Pehamberger H, Bondarenko IN, Queirolo P, Lundgren L, Mikhailov S, Roman L, Verschraegen C, Humphrey R, Ibrahim R, de Pril V, Hoos A, Wolchok JD. Ann Oncol. 2010; 21(8): doi: /annonc/mdq013. Epub 2010 Feb Hodi FS, O Day SJ, McDermott DF, Weber RW, Sosman JA, Haanen JB, Gonzalez R, Robert C, Schadendorf D, Hassel JC, Akerley W, van den Eertwegh AJ, Lutzky J, Lorigan P, Vaubel JM, Linette GP, Hogg D, Ottensmeier CH, Lebbe C, Peschel C, Quirt I, Clark JI, Wolchok JD, Weber JS, Tian J, Yellin MJ, Nichol GM, Hoos A, Urba WJ.: N Engl J Med. 2010; 363(8): doi: /NEJMoa Epub 2010 Jun Robert C, Thomas L, Bondarenko I, O Day S, Weber J, Garbe C, Lebbe C, Baurain JF, Testori A, Grob JJ, Davidson N, Richards J, Maio M, Hauschild A, Miller WH Jr, Gascon P, Lotem M, Harmankaya K, Ibrahim R, Francis S, Chen TT, Humphrey R, Hoos A, Wolchok JD.: N Engl J Med. 2011; 364(26): doi: /NEJMoa Epub 2011 Jun Lebbé C, Weber JS, Maio M, Neyns B, Wolchok JD, et al. Survival follow-up and ipilimumab retreatment of patients with advanced melanoma who received ipilimumab in prior phase II studies. Annals of Oncology, 2014; 25(11): Schadendorf D, Hodi FS, Robert C, Wolchok JD, et al. Pooled Analysis of Long-Term Survival Data From Phase II and Phase III Trials of Ipilimumab in Unresectable or Metastatic Melanoma. J Clin Oncol, 2015, doi: /JCO Wolchok JD, Neyns B, Lebbé C, et al. Ipilimumab momnotherapy in patients with pretrreated advanced melanoma: a randomized double-blind, multicentre, phase 2, dose ranging study. The Lancet Oncology, 2010; 11: Ibrahim R, Berman D, DePril V, et al. Ipilimumab safety profil: summary of findings from completed trials in advanced melanoma. J Clin Oncol.2011; 29(Suppl): Abstract Andrews S, Holden R. Characteristics and management of immune-related adverse efects associated with ipilimumab, a new immunotherapy for metastatic melanoma. Cancer management and Research, 2012; 4: Scarpati GV, Fusciello C, Sabbatino F, Pepe S, et al. Ipilimumab in the treatment of metastatic melanoma: management of adverse events. OncoTargets and Therapy, 2014; 7: Mavropoulos JC, Wang TS. Managing skin toxicities from new melanoma drug. Current Treatment Options in Oncology, 2014; 15: Tarhini A. Scientifica (Cairo). 2013; 2013: doi: /2013/ Epub 2013 Apr McDermott D, Lebbé C, Hodi FS, Balch MC, et al. Durable benefit and the potential for long term survival with immunotherapy in advanced melanoma. Cancer Treatment Reviews, 2014; (40): Článek přijat redakcí: Článek přijat k publikaci: MUDr. Ivana Krajsová, MBA Dermatovenerologická klinika VFN v Praze U Nemocnice 499/2, Praha Ivana.Krajsova@vfn.cz
Význam imunitního systému a možnosti imunoterapie u maligního melanomu
 PŘEHLED Význam imunitního systému a možnosti imunoterapie u maligního melanomu Importance of the Immune System and Immunotherapeutic Options in Malignant Melanoma Krajsová I. Dermatovenerologická klinika
PŘEHLED Význam imunitního systému a možnosti imunoterapie u maligního melanomu Importance of the Immune System and Immunotherapeutic Options in Malignant Melanoma Krajsová I. Dermatovenerologická klinika
11. ZHOUBNÉ NOVOTVARY KŮŽE (C43-44)
 11. ZHOUBNÉ NOVOTVARY KŮŽE (C43-44) 11.1 Zhoubný melanom kůže (C43) 11.1.1 Adjuvantní léčba V adjuvantní léčbě maligního melanomu se stále používá interferon alfa. Je nutné připustit hraniční benefit této
11. ZHOUBNÉ NOVOTVARY KŮŽE (C43-44) 11.1 Zhoubný melanom kůže (C43) 11.1.1 Adjuvantní léčba V adjuvantní léčbě maligního melanomu se stále používá interferon alfa. Je nutné připustit hraniční benefit této
Možnosti léčby kastračně rezistentního metastatického karcinomu prostaty
 Možnosti léčby kastračně rezistentního metastatického karcinomu prostaty Iveta Kolářová Oddělení klinické a radiační onkologie Pardubice Multiscan s.r.o. Pardubická krajská nemocnice, a.s. Pardubice 19.9.2012
Možnosti léčby kastračně rezistentního metastatického karcinomu prostaty Iveta Kolářová Oddělení klinické a radiační onkologie Pardubice Multiscan s.r.o. Pardubická krajská nemocnice, a.s. Pardubice 19.9.2012
11. ZHOUBNÉ NOVOTVARY KŮŽE (C43-44)
 11. ZHOUBNÉ NOVOTVARY KŮŽE (C43-44) 11.1 Zhoubný melanom kůže (C43) 11.1.1 Adjuvantní léčba V adjuvantní léčbě maligního melanomu se stále používá interferon alfa. Je nutné připustit hraniční benefit této
11. ZHOUBNÉ NOVOTVARY KŮŽE (C43-44) 11.1 Zhoubný melanom kůže (C43) 11.1.1 Adjuvantní léčba V adjuvantní léčbě maligního melanomu se stále používá interferon alfa. Je nutné připustit hraniční benefit této
11. ZHOUBNÉ NOVOTVARY KŮŽE (C43-44)
 11. ZHOUBNÉ NOVOTVARY KŮŽE (C43-44) 11.1 Zhoubný melanom kůže (C43) 11.1.1 Adjuvantní léčba V adjuvantní léčbě maligního melanomu se stále používá interferon alfa. Je nutné připustit hraniční benefit této
11. ZHOUBNÉ NOVOTVARY KŮŽE (C43-44) 11.1 Zhoubný melanom kůže (C43) 11.1.1 Adjuvantní léčba V adjuvantní léčbě maligního melanomu se stále používá interferon alfa. Je nutné připustit hraniční benefit této
11. ZHOUBNÉ NOVOTVARY KŮŽE (C43-44)
 11. 11.1 Zhoubný melanom kůže (C43) 11.1.1 Adjuvantní léčba V adjuvantní léčbě maligního melanomu je standardem cílená léčba s kombinací BRAF a MEK inhibitoru a imunoterapie s checkpoint inhibitory. Z
11. 11.1 Zhoubný melanom kůže (C43) 11.1.1 Adjuvantní léčba V adjuvantní léčbě maligního melanomu je standardem cílená léčba s kombinací BRAF a MEK inhibitoru a imunoterapie s checkpoint inhibitory. Z
Edukační materiál. Yervoy (ipilimumab) Časté otázky Brožura pro. zdravotníky
 Edukační materiál Yervoy (ipilimumab) Časté otázky Brožura pro zdravotníky Přípravek YERVOY je indikován k léčbě pokročilého melanomu (neresekovatelného nebo metastazujícího) u dospělých. 1 Tento léčivý
Edukační materiál Yervoy (ipilimumab) Časté otázky Brožura pro zdravotníky Přípravek YERVOY je indikován k léčbě pokročilého melanomu (neresekovatelného nebo metastazujícího) u dospělých. 1 Tento léčivý
Ipilimumab v léčbě melanomu
 MUDr. Monika Arenbergerová, Ph.D.; MUDr. Alena Fialová; prof. MUDr. Petr Arenberger, DrSc., MBA Dermatovenerologická klinika 3. LF UK a FNKV, Praha Souhrn Arenbergerová M, Fialová A, Arenberger P.. Remedia
MUDr. Monika Arenbergerová, Ph.D.; MUDr. Alena Fialová; prof. MUDr. Petr Arenberger, DrSc., MBA Dermatovenerologická klinika 3. LF UK a FNKV, Praha Souhrn Arenbergerová M, Fialová A, Arenberger P.. Remedia
Pokroky v imunoterapii maligního melanomu
 přehled Pokroky v imunoterapii maligního melanomu Advances in Immunother apy of Malignant Melanoma Krajsová I. Dermatovenerologická klinika 1. LF UK a VFN v Praze Souhrn Rozvoj imunoterapie dramaticky
přehled Pokroky v imunoterapii maligního melanomu Advances in Immunother apy of Malignant Melanoma Krajsová I. Dermatovenerologická klinika 1. LF UK a VFN v Praze Souhrn Rozvoj imunoterapie dramaticky
3.3 KARCINOM SLINIVKY BŘIŠNÍ
 3.3 KARCINOM SLINIVKY BŘIŠNÍ Epidemiologie Zhoubné nádory pankreatu se vyskytují převážně ve vyšším věku po 60. roce života, převážně u mužů. Zhoubné nádory pankreatu Incidence a mortalita v České republice
3.3 KARCINOM SLINIVKY BŘIŠNÍ Epidemiologie Zhoubné nádory pankreatu se vyskytují převážně ve vyšším věku po 60. roce života, převážně u mužů. Zhoubné nádory pankreatu Incidence a mortalita v České republice
IMUNOTERAPIE NÁDORŮ MOČOVÉHO MĚCHÝŘE. Michaela Matoušková
 IMUNOTERAPIE NÁDORŮ MOČOVÉHO MĚCHÝŘE Michaela Matoušková IMUNOTERAPIE ZN Z UROTELU lokalizovaná onemocnění - BCG VAKCÍNA pokročilá onemocnění BCG VAKCÍNA po instilaci vazba BCG k fibronektinu produkovanému
IMUNOTERAPIE NÁDORŮ MOČOVÉHO MĚCHÝŘE Michaela Matoušková IMUNOTERAPIE ZN Z UROTELU lokalizovaná onemocnění - BCG VAKCÍNA pokročilá onemocnění BCG VAKCÍNA po instilaci vazba BCG k fibronektinu produkovanému
Systémová léčba lokálně pokročilých a metastatických GEP-NET
 Systémová léčba lokálně pokročilých a metastatických GEP-NET Jiří Tomášek Masarykův onkologický ústav, Brno Vzácné nádory a raritní stavy v oblasti GITu Seminář pro onkology, gastroenterology,radiology
Systémová léčba lokálně pokročilých a metastatických GEP-NET Jiří Tomášek Masarykův onkologický ústav, Brno Vzácné nádory a raritní stavy v oblasti GITu Seminář pro onkology, gastroenterology,radiology
Novinky v léčbě pacientů s pokročilým maligním melanomem
 Novinky v léčbě pacientů s pokročilým maligním melanomem MUDr. Radek Lakomý, Ph.D.; MUDr. Alexandr Poprach; prof. MUDr. Rostislav Vyzula, CSc. LF MU a Masarykův onkologický ústav, Klinika komplexní onkologické
Novinky v léčbě pacientů s pokročilým maligním melanomem MUDr. Radek Lakomý, Ph.D.; MUDr. Alexandr Poprach; prof. MUDr. Rostislav Vyzula, CSc. LF MU a Masarykův onkologický ústav, Klinika komplexní onkologické
Nežádoucí účinky moderní imunoterapie a jejich řešení v klinické praxi
 PŘEHLED Nežádoucí účinky moderní imunoterapie a jejich řešení v klinické praxi Side- effects of Modern Immunotherapy and How to Solve Them in the Clinics Lakomý R., Poprach A. Klinika komplexní onkologické
PŘEHLED Nežádoucí účinky moderní imunoterapie a jejich řešení v klinické praxi Side- effects of Modern Immunotherapy and How to Solve Them in the Clinics Lakomý R., Poprach A. Klinika komplexní onkologické
Nežádoucí účinky novodobé léčby maligního melanomu a jejich léčba/ management
 PŘEHLED Nežádoucí účinky novodobé léčby maligního melanomu a jejich léčba/ management Adverse Effects of Modern Treatment of Malignant Melanoma and their Treatment/ Management Kopecký J. 1, Kubeček O.
PŘEHLED Nežádoucí účinky novodobé léčby maligního melanomu a jejich léčba/ management Adverse Effects of Modern Treatment of Malignant Melanoma and their Treatment/ Management Kopecký J. 1, Kubeček O.
KEYTRUDA. (pembrolizumab) Seznam důležitých imunitně zprostředkovaných nežádoucích účinků a jejich příznaků, včetně opatření a léčby
 Edukační materiál KEYTRUDA (pembrolizumab) Seznam důležitých imunitně zprostředkovaných nežádoucích účinků a jejich příznaků, včetně opatření a léčby Brožura pro Zdravotnického pracovníka Tento léčivý
Edukační materiál KEYTRUDA (pembrolizumab) Seznam důležitých imunitně zprostředkovaných nežádoucích účinků a jejich příznaků, včetně opatření a léčby Brožura pro Zdravotnického pracovníka Tento léčivý
Toxicita imunoterapie
 Aneta Kyllarová, Ondřej Kubeček, Petronela Trojanová, Veronika Molnárová, Peter Priester, Jindřich Kopecký Klinika onkologie a radioterapie FN a LF Hradec Králové, Karlova univerzita V poslední dekádě
Aneta Kyllarová, Ondřej Kubeček, Petronela Trojanová, Veronika Molnárová, Peter Priester, Jindřich Kopecký Klinika onkologie a radioterapie FN a LF Hradec Králové, Karlova univerzita V poslední dekádě
15. ZHOUBNÉ NÁDORY KŮŽE (C43, C44)
 15. ZHOUBNÉ NÁDORY KŮŽE (C43, C44) 15.1 Zhoubný melanom kůže (C43) 15.1.1 Adjuvantní léčba V adjuvantní léčbě maligního melanomu se stále používá interferon alfa. Je nutné připustit hraniční benefit této
15. ZHOUBNÉ NÁDORY KŮŽE (C43, C44) 15.1 Zhoubný melanom kůže (C43) 15.1.1 Adjuvantní léčba V adjuvantní léčbě maligního melanomu se stále používá interferon alfa. Je nutné připustit hraniční benefit této
Desloratadin STADA 5 mg jsou modré, kulaté, bikonvexní potahované tablety o průměru přibližně 6,5 mm.
 Sp.zn.sukls74932/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Desloratadin STADA 5 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna potahovaná tableta obsahuje desloratadinum 5 mg.
Sp.zn.sukls74932/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Desloratadin STADA 5 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna potahovaná tableta obsahuje desloratadinum 5 mg.
Imunoterapie u bronchogenního karcinomu a její perspektivy
 PŘEHLED Imunoterapie u bronchogenního karcinomu a její perspektivy Immunotherapy of Bronchogenic Carcinoma and Its Perspectives Koubková L. Pneumologická klinika 2. LF UK a FN v Motole, Praha Souhrn Imunoterapie
PŘEHLED Imunoterapie u bronchogenního karcinomu a její perspektivy Immunotherapy of Bronchogenic Carcinoma and Its Perspectives Koubková L. Pneumologická klinika 2. LF UK a FN v Motole, Praha Souhrn Imunoterapie
Příloha č. 2 k rozhodnutí o změně registrace sp.zn.sukls114374/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 2 k rozhodnutí o změně registrace sp.zn.sukls114374/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU LOPERON cps 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Loperamidi hydrochloridum 2 mg v jedné
Příloha č. 2 k rozhodnutí o změně registrace sp.zn.sukls114374/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU LOPERON cps 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Loperamidi hydrochloridum 2 mg v jedné
Několik poznámek k diagnostice a léčbě diferencovaných karcinomů štítné žlázy (DTC) Otakar Kraft, Martin Havel Klinika nukleární medicíny FN Ostrava
 Několik poznámek k diagnostice a léčbě diferencovaných karcinomů štítné žlázy (DTC) Otakar Kraft, Martin Havel Klinika nukleární medicíny FN Ostrava 51. Dny nukleární medicíny Seč 12.-14.11.2014 Úvod Cíle
Několik poznámek k diagnostice a léčbě diferencovaných karcinomů štítné žlázy (DTC) Otakar Kraft, Martin Havel Klinika nukleární medicíny FN Ostrava 51. Dny nukleární medicíny Seč 12.-14.11.2014 Úvod Cíle
XOFIGO (RADIUM-223 DICHLORID) V LÉČBĚ METASTATICKÉHO KASTRAČNĚ REZISTENTNÍHO KARCINOMU PROSTATY
 NÁDORY PROSTATY 63 XOFIGO (RADIUM-223 DICHLORID) V LÉČBĚ METASTATICKÉHO KASTRAČNĚ REZISTENTNÍHO KARCINOMU PROSTATY Kolektiv autorů Úvod Léčivý přípravek (radium-223 dichlorid) byl 13. listopadu 2013 schválen
NÁDORY PROSTATY 63 XOFIGO (RADIUM-223 DICHLORID) V LÉČBĚ METASTATICKÉHO KASTRAČNĚ REZISTENTNÍHO KARCINOMU PROSTATY Kolektiv autorů Úvod Léčivý přípravek (radium-223 dichlorid) byl 13. listopadu 2013 schválen
Možnosti léčby CRPC s časem přibývají
 Možnosti léčby CRPC s časem přibývají Jana Katolická Onkologicko-chirurgické oddělení Fakultní nemocnice u Sv. Anny Mnoho studií - jen čtyři nové léky Enzalutamid Abirateron + prednison Cabazitaxel Radium-223
Možnosti léčby CRPC s časem přibývají Jana Katolická Onkologicko-chirurgické oddělení Fakultní nemocnice u Sv. Anny Mnoho studií - jen čtyři nové léky Enzalutamid Abirateron + prednison Cabazitaxel Radium-223
Nežádoucí účinky cílené léčby renálního karcinomu. Svoboda T., Říčař J., Vokurka S. FN Plzeň
 Nežádoucí účinky cílené léčby renálního karcinomu Svoboda T., Říčař J., Vokurka S. FN Plzeň Aplikace systémové léčby Urologie = chirurgický základ Onkologie = od své podstaty interní ve všech složkách,
Nežádoucí účinky cílené léčby renálního karcinomu Svoboda T., Říčař J., Vokurka S. FN Plzeň Aplikace systémové léčby Urologie = chirurgický základ Onkologie = od své podstaty interní ve všech složkách,
Comparison of response rates in relapsed/refractory MM
 Lenalidomid Lenalidomid Imunomodulační látka patřící mezi sloučeniny zvané IMiDy. Sloučenina strukturou podobná Thalidomidu s účinkem antiangiogenním, imunomodulačním a přímým protinádorovým. Comparison
Lenalidomid Lenalidomid Imunomodulační látka patřící mezi sloučeniny zvané IMiDy. Sloučenina strukturou podobná Thalidomidu s účinkem antiangiogenním, imunomodulačním a přímým protinádorovým. Comparison
Ipilimumab je plně lidská monoklonální protilátka anti-ctla-4 (IgG1κ) produkovaná ovariálními buňkami čínského křečíka rekombinantní DNA technologií.
 1. NÁZEV PŘÍPRAVKU YERVOY 5 mg/ml koncentrát pro infuzní roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden ml koncentrátu obsahuje ipilimumabum 5 mg. Jedna 10 ml lahvička obsahuje ipilimumabum 50 mg.
1. NÁZEV PŘÍPRAVKU YERVOY 5 mg/ml koncentrát pro infuzní roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden ml koncentrátu obsahuje ipilimumabum 5 mg. Jedna 10 ml lahvička obsahuje ipilimumabum 50 mg.
OBSAH. Proč monitoring CL. Jaký monitoring CL. Diskuze (?)
 www.recetox.cz www.mou.cz Návrh monitoringu cytostatik na pracovištích v ČR www.cytostatika.cz Luděk Bláha, Pavel Odráška, Lenka Doležalová a kol. 14. Kongres Nemocničních lékárníků (listopad 2010, Hradec
www.recetox.cz www.mou.cz Návrh monitoringu cytostatik na pracovištích v ČR www.cytostatika.cz Luděk Bláha, Pavel Odráška, Lenka Doležalová a kol. 14. Kongres Nemocničních lékárníků (listopad 2010, Hradec
Jedna tvrdá tobolka obsahuje loperamidi hydrochloridum 2 mg.
 Sp.zn.sukls97430/2013 1.NÁZEV LÉČIVÉHO PŘÍPRAVKU Tannex 2 mg tvrdé tobolky 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tvrdá tobolka obsahuje loperamidi hydrochloridum 2 mg. Pomocná látka se známým účinkem:
Sp.zn.sukls97430/2013 1.NÁZEV LÉČIVÉHO PŘÍPRAVKU Tannex 2 mg tvrdé tobolky 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tvrdá tobolka obsahuje loperamidi hydrochloridum 2 mg. Pomocná látka se známým účinkem:
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 sp.zn.: sukls179784/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU IMODIUM 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Loperamidi hydrochloridum 2 mg v jedné tobolce Úplný seznam pomocných látek viz bod
sp.zn.: sukls179784/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU IMODIUM 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Loperamidi hydrochloridum 2 mg v jedné tobolce Úplný seznam pomocných látek viz bod
Orofaciální karcinomy - statistické zhodnocení úspěšnosti léčby
 Orofaciální karcinomy - statistické zhodnocení úspěšnosti léčby Autor: David Diblík, Martina Kopasová, Školitel: MUDr. Richard Pink, Ph.D. Výskyt Zhoubné (maligní) nádory v oblasti hlavy a krku (orofaciální
Orofaciální karcinomy - statistické zhodnocení úspěšnosti léčby Autor: David Diblík, Martina Kopasová, Školitel: MUDr. Richard Pink, Ph.D. Výskyt Zhoubné (maligní) nádory v oblasti hlavy a krku (orofaciální
Příloha č. 2 k rozhodnutí o změně registrace sp.zn. sukls106353/2011
 Příloha č. 2 k rozhodnutí o změně registrace sp.zn. sukls106353/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRVKU Lopacut 2 mg, potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje
Příloha č. 2 k rozhodnutí o změně registrace sp.zn. sukls106353/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRVKU Lopacut 2 mg, potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje
Evropský konsensus pro použití lenalidomidu v RRMM v roce 2011 a léčebné postupy v ČR
 Evropský konsensus pro použití lenalidomidu v RRMM v roce 2011 a léčebné postupy v ČR Ivan Špička I. interní klinika klinika hematologie 1. LF a VFN Univerzita Karlova v Praze Léčebný cíl pro pacienty
Evropský konsensus pro použití lenalidomidu v RRMM v roce 2011 a léčebné postupy v ČR Ivan Špička I. interní klinika klinika hematologie 1. LF a VFN Univerzita Karlova v Praze Léčebný cíl pro pacienty
Nespecifické střevní záněty u dětí
 Nespecifické střevní záněty u dětí Autor: Filipová V., Školitel: Mihál V., Prof. MUDr. CSc. Nespecifické střevní záněty (NSZ, anglicky IBD Inflammatory Bowel Disease) jsou onemocnění, která postihují především
Nespecifické střevní záněty u dětí Autor: Filipová V., Školitel: Mihál V., Prof. MUDr. CSc. Nespecifické střevní záněty (NSZ, anglicky IBD Inflammatory Bowel Disease) jsou onemocnění, která postihují především
Vliv způsobu podání bortezomibu na účinnost a bezpečnost léčby pacientů s mnohočetným myelomem. MUDr. P. Pavlíček FN KV a 3.
 Vliv způsobu podání bortezomibu na účinnost a bezpečnost léčby pacientů s mnohočetným myelomem MUDr. P. Pavlíček FN KV a 3. LF UK Praha Tato prezentace vznikla s finanční podporou společnosti Johnson &
Vliv způsobu podání bortezomibu na účinnost a bezpečnost léčby pacientů s mnohočetným myelomem MUDr. P. Pavlíček FN KV a 3. LF UK Praha Tato prezentace vznikla s finanční podporou společnosti Johnson &
Maligní melanom a nové možnosti jeho léčby
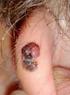 Viera Bajčiová Klinika dětské onkologie FN a LF MU Brno Léčba pokročilého a metastatického melanomu dosáhla v posledních pěti letech revolučních změn. Po desetiletích stagnace a hledání nových možností
Viera Bajčiová Klinika dětské onkologie FN a LF MU Brno Léčba pokročilého a metastatického melanomu dosáhla v posledních pěti letech revolučních změn. Po desetiletích stagnace a hledání nových možností
II. Interní klinika, odd. gastroenterologie, FNKV, 3.LF UK Hnaníček J., Mandys V., Kment M., Zádorová Z.
 II. Interní klinika, odd. gastroenterologie, FNKV, 3.LF UK Hnaníček J., Mandys V., Kment M., Zádorová Z. Copaxon - spouštěcí faktor ulcerózní kolitidy? hypotéza: může copaxon indukovat ulcerózní kolitidu?
II. Interní klinika, odd. gastroenterologie, FNKV, 3.LF UK Hnaníček J., Mandys V., Kment M., Zádorová Z. Copaxon - spouštěcí faktor ulcerózní kolitidy? hypotéza: může copaxon indukovat ulcerózní kolitidu?
Novinky v léčbě. Úvod: Srdeční selhání epidemie 21. století. Prof. MUDr. Jindřich Špinar, CSc., FESC Interní kardiologická klinika FN Brno
 Novinky v léčbě Úvod: Srdeční selhání epidemie 21. století Prof. MUDr. Jindřich Špinar, CSc., FESC Interní kardiologická klinika FN Brno PARADIGM-HF: Design studie Randomizace n=8442 Dvojitě slepá Léčebná
Novinky v léčbě Úvod: Srdeční selhání epidemie 21. století Prof. MUDr. Jindřich Špinar, CSc., FESC Interní kardiologická klinika FN Brno PARADIGM-HF: Design studie Randomizace n=8442 Dvojitě slepá Léčebná
Časté otázky. Brožura pro. zdravotníky
 Časté otázky Brožura pro zdravotníky Přípravek YERVOY je indikován k léčbě pokročilého melanomu (neresekovatelného nebo metastazujícího) u dospělých. 1 Yervoy podléhá dalšímu sledování, které umožní rychlé
Časté otázky Brožura pro zdravotníky Přípravek YERVOY je indikován k léčbě pokročilého melanomu (neresekovatelného nebo metastazujícího) u dospělých. 1 Yervoy podléhá dalšímu sledování, které umožní rychlé
HEREDITÁRNÍ ANGIOEDÉM KAZUISTIKA
 HEREDITÁRNÍ ANGIOEDÉM KAZUISTIKA Ústav klinické imunologie a alergologie Univerzitní centrum pro primární imunodeficience LF MU a FN u sv. Anny v Brně Alena Plodíková Ivana Denková Helena Horáková 1 Hereditární
HEREDITÁRNÍ ANGIOEDÉM KAZUISTIKA Ústav klinické imunologie a alergologie Univerzitní centrum pro primární imunodeficience LF MU a FN u sv. Anny v Brně Alena Plodíková Ivana Denková Helena Horáková 1 Hereditární
Bezpečnost a účinnost přípravku Neoclarityn 5 mg potahované tablety u dětí mladších 12 let nebyla dosud stanovena. Nejsou dostupné žádné údaje.
 1. NÁZEV PŘÍPRAVKU Neoclarityn 5 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje desloratadinum 5 mg. Pomocná látka se známým účinkem: Tento přípravek obsahuje laktózu.
1. NÁZEV PŘÍPRAVKU Neoclarityn 5 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje desloratadinum 5 mg. Pomocná látka se známým účinkem: Tento přípravek obsahuje laktózu.
1 Buněčný cyklus a apoptóza (z. Kleibi)..
 1 Buněčný cyklus a apoptóza (z. Kleibi).. 1.1 Buněčný cyklus 1.1.1 Mitogenní signalizace a zahájení buněčného cyklu 1.1.2 G1 fáze buněčného cyklu a její reštrikční bod 1.1.3 S fáze: replikace DNA 1.1.4
1 Buněčný cyklus a apoptóza (z. Kleibi).. 1.1 Buněčný cyklus 1.1.1 Mitogenní signalizace a zahájení buněčného cyklu 1.1.2 G1 fáze buněčného cyklu a její reštrikční bod 1.1.3 S fáze: replikace DNA 1.1.4
Edukační materiál. YERVOY (ipilimumab) Důležitá upozornění k předcházení závažných následků možných nežádoucích účinků léčivého přípravku YERVOY
 Edukační materiál YERVOY (ipilimumab) Důležitá upozornění k předcházení závažných následků možných nežádoucích účinků léčivého přípravku YERVOY Přípravek YERVOY (ipilimumab) je indikován k léčbě pokročilého
Edukační materiál YERVOY (ipilimumab) Důležitá upozornění k předcházení závažných následků možných nežádoucích účinků léčivého přípravku YERVOY Přípravek YERVOY (ipilimumab) je indikován k léčbě pokročilého
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Desloratadin +pharma 5 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje desloratadinum v množství 5 mg. Úplný seznam pomocných
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Desloratadin +pharma 5 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje desloratadinum v množství 5 mg. Úplný seznam pomocných
Revlimid v léčbě myelomu u nemocných s renální insuficiencí MUDr. Jan Straub
 Revlimid v léčbě myelomu u nemocných s renální insuficiencí MUDr. Jan Straub Updated December 2009. 1 Závěry s ASH 2009 Len-Dex u rr MM s úpravou dávkování v závislosti na stupni renální insuficience Soubor
Revlimid v léčbě myelomu u nemocných s renální insuficiencí MUDr. Jan Straub Updated December 2009. 1 Závěry s ASH 2009 Len-Dex u rr MM s úpravou dávkování v závislosti na stupni renální insuficience Soubor
Kazuistika ČUS. MUDr. PharmDr Jan Dvořák RTO klinika FNKV, 3. LF UK
 Kazuistika ČUS MUDr. PharmDr Jan Dvořák RTO klinika FNKV, 3. LF UK Pacient S.U. Dg. C61 v roce 2009, 56 let 8/2009 biopsie GLS 9 (4+5), PSA 8.22 μg/l 11/2009 RAPE, pt2c pn0(5 uzlin) M0, GS 7 (4+3), R0
Kazuistika ČUS MUDr. PharmDr Jan Dvořák RTO klinika FNKV, 3. LF UK Pacient S.U. Dg. C61 v roce 2009, 56 let 8/2009 biopsie GLS 9 (4+5), PSA 8.22 μg/l 11/2009 RAPE, pt2c pn0(5 uzlin) M0, GS 7 (4+3), R0
Jedna tableta s prodlouženým uvolňováním obsahuje 0,4 mg tamsulosini hydrochloridum, což odpovídá 0,367 mg tamsulosinum.
 sp.zn.sukls48957/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Tamsulosin HCl Teva 0,4 mg tablety s prodlouženým uvolňováním 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta s prodlouženým uvolňováním
sp.zn.sukls48957/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Tamsulosin HCl Teva 0,4 mg tablety s prodlouženým uvolňováním 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta s prodlouženým uvolňováním
Příloha č. 3 k rozhodnutí o prodloužení registrace sp. zn.:sukls167009/2008 a příloha k sp.zn. sukls80895/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 3 k rozhodnutí o prodloužení registrace sp. zn.:sukls167009/2008 a příloha k sp.zn. sukls80895/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU LODRONAT 520 potahované tablety 2. KVALITATIVNÍ
Příloha č. 3 k rozhodnutí o prodloužení registrace sp. zn.:sukls167009/2008 a příloha k sp.zn. sukls80895/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU LODRONAT 520 potahované tablety 2. KVALITATIVNÍ
Nádorová. onemocnění plic ONKOLOGIE IVANA PÁLKOVÁ JANA SKŘIČKOVÁ
 ONKOLOGIE Nádorová onemocnění plic Každá epocha lidských dějin má své dominující nemoci. V minulém století to byla, vedle civilizačních chorob, především nádorová onemocnění. Změnu nelze očekávat ani ve
ONKOLOGIE Nádorová onemocnění plic Každá epocha lidských dějin má své dominující nemoci. V minulém století to byla, vedle civilizačních chorob, především nádorová onemocnění. Změnu nelze očekávat ani ve
JAK SLEDOVAT KVALITU KOLOSKOPICKÉHO CENTRA? Petr Vítek
 JAK SLEDOVAT KVALITU KOLOSKOPICKÉHO CENTRA? Petr Vítek Obsah sdělení Proč sledovat kvalitu koloskopie? Indikátory kvality koloskopie a jejich měření Co sledovat v praxi? Quality means doing it right when
JAK SLEDOVAT KVALITU KOLOSKOPICKÉHO CENTRA? Petr Vítek Obsah sdělení Proč sledovat kvalitu koloskopie? Indikátory kvality koloskopie a jejich měření Co sledovat v praxi? Quality means doing it right when
Příloha II. Vědecké závěry
 Příloha II Vědecké závěry 11 Vědecké závěry Po zvážení revidovaného konečného doporučení Farmakovigilančního výboru pro posuzování rizik léčiv (PRAC) ze dne 10. července 2014 týkajícího se léčivých přípravků
Příloha II Vědecké závěry 11 Vědecké závěry Po zvážení revidovaného konečného doporučení Farmakovigilančního výboru pro posuzování rizik léčiv (PRAC) ze dne 10. července 2014 týkajícího se léčivých přípravků
Václav Hořejší Ústav molekulární genetiky AV ČR. IMUNITNÍ SYSTÉM vs. NÁDORY
 Václav Hořejší Ústav molekulární genetiky AV ČR IMUNITNÍ SYSTÉM vs. NÁDORY PROTINÁDOROVÁ IMUNITA - HISTORIE 1891 W. Coley - otec imunoterapie 1957 F.M. Burnet hypotéza imunitního dozoru 1976 A.W. Bruce
Václav Hořejší Ústav molekulární genetiky AV ČR IMUNITNÍ SYSTÉM vs. NÁDORY PROTINÁDOROVÁ IMUNITA - HISTORIE 1891 W. Coley - otec imunoterapie 1957 F.M. Burnet hypotéza imunitního dozoru 1976 A.W. Bruce
Jedna dávka přípravku Neoclarityn tableta dispergovatelná v ústech obsahuje desloratadinum 2,5 mg.
 1 NÁZEV PŘÍPRAVKU Neoclarityn 2,5 mg tablety dispergovatelné v ústech 2 KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka přípravku Neoclarityn tableta dispergovatelná v ústech obsahuje desloratadinum 2,5
1 NÁZEV PŘÍPRAVKU Neoclarityn 2,5 mg tablety dispergovatelné v ústech 2 KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka přípravku Neoclarityn tableta dispergovatelná v ústech obsahuje desloratadinum 2,5
zdravotníky Časté otázky Brožura pro
 koncentrát pro přípravu Časté otázky Brožura pro zdravotníky Přípravek YERVOY je indikován k léčbě pokročilého melanomu (neresekovatelného nebo metastazujícího) u dospělých, kteří už absolvovali jinou
koncentrát pro přípravu Časté otázky Brožura pro zdravotníky Přípravek YERVOY je indikován k léčbě pokročilého melanomu (neresekovatelného nebo metastazujícího) u dospělých, kteří už absolvovali jinou
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Aerius 5 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje desloratadinum v množství 5 mg. Úplný seznam pomocných
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Aerius 5 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje desloratadinum v množství 5 mg. Úplný seznam pomocných
Možnosti léčby CRPC. Michaela Matoušková
 Možnosti léčby CRPC Michaela Matoušková Pokročilý karcinom prostaty prevalence CaP 65215 pokročilý CaP st. III 8492 st. IV 5884 14376 CRPC cca 900-1000 Zdroj dat www.uroweb.cz CRPC Kastrační hladina testosteronu
Možnosti léčby CRPC Michaela Matoušková Pokročilý karcinom prostaty prevalence CaP 65215 pokročilý CaP st. III 8492 st. IV 5884 14376 CRPC cca 900-1000 Zdroj dat www.uroweb.cz CRPC Kastrační hladina testosteronu
Protokol pro léčbu karcinomu tlustého střeva
 1 Klinika onkologie a radioterapie FN Hradec Králové Platnost od: 2.1.2013 Dokument: standardní léčebný postup - verze 2013 Počet stran: 6 Přílohy: nejsou Protokol pro léčbu karcinomu tlustého střeva Schválili:
1 Klinika onkologie a radioterapie FN Hradec Králové Platnost od: 2.1.2013 Dokument: standardní léčebný postup - verze 2013 Počet stran: 6 Přílohy: nejsou Protokol pro léčbu karcinomu tlustého střeva Schválili:
Norifaz 35 mg potahované tablety
 Příloha č. 3 k rozhodnutí o registraci sp. zn. sukls18991/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Norifaz 35 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna potahovaná tableta
Příloha č. 3 k rozhodnutí o registraci sp. zn. sukls18991/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Norifaz 35 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna potahovaná tableta
Betalaktamy v intenzivní péči z pohledu farmakologa
 Betalaktamy v intenzivní péči z pohledu farmakologa K. Urbánek Ústav farmakologie Lékařská fakulta Univerzity Palackého a Fakultní nemocnice Olomouc Přehled karbapenemů Karbapenemová antibiotika Skupina
Betalaktamy v intenzivní péči z pohledu farmakologa K. Urbánek Ústav farmakologie Lékařská fakulta Univerzity Palackého a Fakultní nemocnice Olomouc Přehled karbapenemů Karbapenemová antibiotika Skupina
Renální karcinom přehled léčby pokročilého a metastatického onemocnění
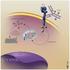 Renální karcinom přehled léčby pokročilého a metastatického onemocnění Doc. MUDr. Tomáš Büchler, Ph.D. Onkologická klinika 1. LF UK a Thomayerovy nemocnice, Praha Souhrn Büchler T.. Remedia 2013; 23 (Supl.
Renální karcinom přehled léčby pokročilého a metastatického onemocnění Doc. MUDr. Tomáš Büchler, Ph.D. Onkologická klinika 1. LF UK a Thomayerovy nemocnice, Praha Souhrn Büchler T.. Remedia 2013; 23 (Supl.
Příbalová informace: informace pro pacienta. Norethisteron Zentiva 5 mg, tablety norethisteroni acetas
 sp. zn. sukls127842/2015 Příbalová informace: informace pro pacienta Norethisteron Zentiva 5 mg, tablety norethisteroni acetas Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
sp. zn. sukls127842/2015 Příbalová informace: informace pro pacienta Norethisteron Zentiva 5 mg, tablety norethisteroni acetas Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU YERVOY 5 mg/ml koncentrát pro infuzní roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden ml koncentrátu obsahuje ipilimumabum 5 mg. Jedna 10 ml
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU YERVOY 5 mg/ml koncentrát pro infuzní roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden ml koncentrátu obsahuje ipilimumabum 5 mg. Jedna 10 ml
Příloha č. 2 k rozhodnutí o změně registrace sp. zn. sukls20675/2011 a příloha ke sp. zn. sukls155771/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 2 k rozhodnutí o změně registrace sp. zn. sukls20675/2011 a příloha ke sp. zn. sukls155771/2011 1. NÁZEV PŘÍPRAVKU LODRONAT 520 potahované tablety SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A
Příloha č. 2 k rozhodnutí o změně registrace sp. zn. sukls20675/2011 a příloha ke sp. zn. sukls155771/2011 1. NÁZEV PŘÍPRAVKU LODRONAT 520 potahované tablety SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A
CELIAKIE. MUDr. Denisa Pavlovská, Doc. MUDr. Jarmila Skotáková, CSc.
 CELIAKIE MUDr. Denisa Pavlovská, Doc. MUDr. Jarmila Skotáková, CSc. MUDr. Helena Masaříková LF MU, Klinika dětské radiologie, FN Brno LF MU, Klinika dětské radiologie, FN Brno DEFINICE celoživotní, geneticky
CELIAKIE MUDr. Denisa Pavlovská, Doc. MUDr. Jarmila Skotáková, CSc. MUDr. Helena Masaříková LF MU, Klinika dětské radiologie, FN Brno LF MU, Klinika dětské radiologie, FN Brno DEFINICE celoživotní, geneticky
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakákoli podezření
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakákoli podezření
Analýzy pro Jihomoravský kraj
 Příloha č. 11 zprávy ČOS: Podklady pro plánování nákladů léčebné péče v onkologii - analýzy dostupných populačních dat v ČR Analýzy pro Jihomoravský kraj Koncept zprávy, metodika výpočtů a celkové populační
Příloha č. 11 zprávy ČOS: Podklady pro plánování nákladů léčebné péče v onkologii - analýzy dostupných populačních dat v ČR Analýzy pro Jihomoravský kraj Koncept zprávy, metodika výpočtů a celkové populační
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU. Somatuline P.R. 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Somatuline P.R. 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Lyofilizát: 1 dávka obsahuje Léčivá látka: Lanreotidi acetas odp. lanreotidum 0,030 g Pomocné látky:
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Somatuline P.R. 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Lyofilizát: 1 dávka obsahuje Léčivá látka: Lanreotidi acetas odp. lanreotidum 0,030 g Pomocné látky:
Udržovací léčba: zamířeno na anti-vegf léčbu Alan Sandler
 Udržovací léčba: zamířeno na anti-vegf léčbu Alan Sandler Department of Hematology/Oncology Oregon Health and Science University Knight Cancer Institute Portland, OR, USA Medián OS (měsíce) Studie v 1.linii
Udržovací léčba: zamířeno na anti-vegf léčbu Alan Sandler Department of Hematology/Oncology Oregon Health and Science University Knight Cancer Institute Portland, OR, USA Medián OS (měsíce) Studie v 1.linii
Eva Havrdová et al. Roztroušená skleróza. v praxi. Galén
 Eva Havrdová et al. Roztroušená skleróza v praxi Galén Hlavní autorka a pořadatelka prof. MUDr. Eva Havrdová, CSc. Neurologická klinika 1. LF UK a VFN, Praha Recenzent MUDr. Jiří Piťha Centrum pro diagnostiku
Eva Havrdová et al. Roztroušená skleróza v praxi Galén Hlavní autorka a pořadatelka prof. MUDr. Eva Havrdová, CSc. Neurologická klinika 1. LF UK a VFN, Praha Recenzent MUDr. Jiří Piťha Centrum pro diagnostiku
Hodnocení segmentu centrové léčby z dat plátců zdravotní péče. Společné pracoviště ÚZIS ČR a IBA MU
 Hodnocení segmentu centrové léčby z dat plátců zdravotní péče Společné pracoviště ÚZIS ČR a IBA MU Realita současné české medicíny: úspěšné výsledky léčby = podstatné prodlužování doby života pacienta
Hodnocení segmentu centrové léčby z dat plátců zdravotní péče Společné pracoviště ÚZIS ČR a IBA MU Realita současné české medicíny: úspěšné výsledky léčby = podstatné prodlužování doby života pacienta
Asymptomatické stenózy víme už jak postupovat? D. Krajíčková Neurologická klinika LU UK a FN v Hradci Králové
 Asymptomatické stenózy víme už jak postupovat? D. Krajíčková Neurologická klinika LU UK a FN v Hradci Králové Prevalence asymptomatické stenózy Prevalence asymptomatické stenózy (AS) > 70 % v populaci
Asymptomatické stenózy víme už jak postupovat? D. Krajíčková Neurologická klinika LU UK a FN v Hradci Králové Prevalence asymptomatické stenózy Prevalence asymptomatické stenózy (AS) > 70 % v populaci
Kombinované režimy v imunoterapii
 Přehled Kombinované režimy v imunoterapii Combined Regimens in Immunother apy Melichar B., Spisarová M. Onkologická klinika LF UP a FN Olomouc Souhrn Příchod imunoterapie mění náš pohled na obecnou strategii
Přehled Kombinované režimy v imunoterapii Combined Regimens in Immunother apy Melichar B., Spisarová M. Onkologická klinika LF UP a FN Olomouc Souhrn Příchod imunoterapie mění náš pohled na obecnou strategii
Nové chemoterapeutické režimy u karcinomu prsu. Miloš Holánek, Ji í Vysko il KKOP, MOÚ Brno
 Nové chemoterapeutické režimy u karcinomu prsu Miloš Holánek, Jií Vyskoil KKOP, MOÚ Brno Úvod Terapeutické modality u karcinomu prsu: - chirurgická léba -hormonoterapie -radioterapie - chemoterapie - cílená
Nové chemoterapeutické režimy u karcinomu prsu Miloš Holánek, Jií Vyskoil KKOP, MOÚ Brno Úvod Terapeutické modality u karcinomu prsu: - chirurgická léba -hormonoterapie -radioterapie - chemoterapie - cílená
Pomalidomid první rok léčby v ČR
 C Z E C H G R O U P CZECH GROUP 1 Pomalidomid první rok léčby v ČR Luděk Pour IHOK FN Brno XIII. Výroční setkání CMG 10. 4. 2015 Mikulov C M G M Y E L O M A Č E S K Á M YE LO M O VÁ S K U P IN A CMG ČESKÁ
C Z E C H G R O U P CZECH GROUP 1 Pomalidomid první rok léčby v ČR Luděk Pour IHOK FN Brno XIII. Výroční setkání CMG 10. 4. 2015 Mikulov C M G M Y E L O M A Č E S K Á M YE LO M O VÁ S K U P IN A CMG ČESKÁ
Světle červené, ploché, kulaté, skvrnité tablety, na jedné straně označené písmenem K.
 1. NÁZEV PŘÍPRAVKU Aerius 2,5 mg tablety dispergovatelné v ústech 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta dispergovatelná v ústech obsahuje desloratadinum 2,5 mg. Pomocné látky se známým
1. NÁZEV PŘÍPRAVKU Aerius 2,5 mg tablety dispergovatelné v ústech 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta dispergovatelná v ústech obsahuje desloratadinum 2,5 mg. Pomocné látky se známým
The Cost Study of First- line Treatment of Metastatic Colorectal Carcinoma with Bevacizumab- containing Regimen in the Czech Republic
 PŮVODNÍ PRÁCE Analýza nákladů na 1. linii léčby metastatického kolorektálního karcinomu při podání režimů s bevacizumabem data z reálné klinické praxe v České republice The Cost Study of First- line Treatment
PŮVODNÍ PRÁCE Analýza nákladů na 1. linii léčby metastatického kolorektálního karcinomu při podání režimů s bevacizumabem data z reálné klinické praxe v České republice The Cost Study of First- line Treatment
Co mě může potkat při návratu onemocnění. Nové přístupy biologická léčba karcinomu prostaty. MUDr. Hana Študentová, Ph.D.
 Co mě může potkat při návratu onemocnění. Nové přístupy biologická léčba karcinomu prostaty MUDr. Hana Študentová, Ph.D. Obsah Obecný úvod Androgenní signalizace Možnosti systémové léčby Závěr Koho se
Co mě může potkat při návratu onemocnění. Nové přístupy biologická léčba karcinomu prostaty MUDr. Hana Študentová, Ph.D. Obsah Obecný úvod Androgenní signalizace Možnosti systémové léčby Závěr Koho se
Klinická data bevacizumabu v úvodní léčbě karcinomu vaječníků: GOG-0218
 Klinická data bevacizumabu v úvodní léčbě karcinomu vaječníků: GOG-0218 Professor Bradley J. Monk Division of Gynecologic Oncology Department of Obstetrics and Gynecology Creighton University School of
Klinická data bevacizumabu v úvodní léčbě karcinomu vaječníků: GOG-0218 Professor Bradley J. Monk Division of Gynecologic Oncology Department of Obstetrics and Gynecology Creighton University School of
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 3 k rozhodnutí o registraci sp.zn.:sukls4358/2009, sukls4359/2009, sukls4361/2009, sukls4362/2009 Příloha č. 3 ke sdělení sp.zn.: sukls128253/2011, sukls128483/2011, sukls128487/2011, sukls128489/2011,
Příloha č. 3 k rozhodnutí o registraci sp.zn.:sukls4358/2009, sukls4359/2009, sukls4361/2009, sukls4362/2009 Příloha č. 3 ke sdělení sp.zn.: sukls128253/2011, sukls128483/2011, sukls128487/2011, sukls128489/2011,
STÁTNÍ ÚSTAV PRO KONTROLU LÉČIV Šrobárova 48, 100 41 PRAHA 10 tel. 272 185 111, fax 271 732 377, e-mail: posta@sukl.cz
 STÁTNÍ ÚSTAV PRO KONTROLU LÉČIV Šrobárova 48, 100 41 PRAHA 10 tel. 272 185 111, fax 271 732 377, e-mail: posta@sukl.cz V souladu s ustanovením 39o zákona č. 48/1997 Sb., o veřejném zdravotním pojištění,
STÁTNÍ ÚSTAV PRO KONTROLU LÉČIV Šrobárova 48, 100 41 PRAHA 10 tel. 272 185 111, fax 271 732 377, e-mail: posta@sukl.cz V souladu s ustanovením 39o zákona č. 48/1997 Sb., o veřejném zdravotním pojištění,
Sp.zn.sukls88807/2015
 Sp.zn.sukls88807/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU NORMAGLYC 500 mg, potahované tablety NORMAGLYC 850 mg, potahované tablety NORMAGLYC 1000 mg, potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ
Sp.zn.sukls88807/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU NORMAGLYC 500 mg, potahované tablety NORMAGLYC 850 mg, potahované tablety NORMAGLYC 1000 mg, potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 3 k rozhodnutí o registraci sp.zn. sukls42544-6/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Pexogies 0,088 mg tablety Pexogies 0,18 mg tablety Pexogies 0,7 mg tablety 2. KVALITATIVNÍ A
Příloha č. 3 k rozhodnutí o registraci sp.zn. sukls42544-6/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Pexogies 0,088 mg tablety Pexogies 0,18 mg tablety Pexogies 0,7 mg tablety 2. KVALITATIVNÍ A
Parenterální výživa v onkologii a kdy domů? (kriteria pro aplikaci v domácí péči) Viktor Maňásek Komplexní onkologické centrum Nový Jičín
 Parenterální výživa v onkologii a kdy domů? (kriteria pro aplikaci v domácí péči) Viktor Maňásek Komplexní onkologické centrum Nový Jičín Odhad přežití onkologicky nemocných dle nutričních parametrů Diagnostic
Parenterální výživa v onkologii a kdy domů? (kriteria pro aplikaci v domácí péči) Viktor Maňásek Komplexní onkologické centrum Nový Jičín Odhad přežití onkologicky nemocných dle nutričních parametrů Diagnostic
INDIVIDUÁLNÍ ZDRAVOTNÍ PÉČE PRO NEJNÁROČNĚJŠÍ
 INDIVIDUÁLNÍ ZDRAVOTNÍ PÉČE PRO NEJNÁROČNĚJŠÍ CO PŘINÁŠÍ PRIVÁTNÍ ZDRAVOTNÍ PÉČE Hlavním cílem centra privátní zdravotní péče AGEL+ je zajištění nadstandardní organizace služeb v oblasti individuální péče
INDIVIDUÁLNÍ ZDRAVOTNÍ PÉČE PRO NEJNÁROČNĚJŠÍ CO PŘINÁŠÍ PRIVÁTNÍ ZDRAVOTNÍ PÉČE Hlavním cílem centra privátní zdravotní péče AGEL+ je zajištění nadstandardní organizace služeb v oblasti individuální péče
Kolorektální karcinom (karcinom tlustého střeva a konečníku)
 Kolorektální karcinom (karcinom tlustého střeva a konečníku) Autor: Hanáčková Veronika Výskyt Kolorektální karcinom (označován jako CRC) je jedním z nejčastějších nádorů a ve všech vyspělých státech jeho
Kolorektální karcinom (karcinom tlustého střeva a konečníku) Autor: Hanáčková Veronika Výskyt Kolorektální karcinom (označován jako CRC) je jedním z nejčastějších nádorů a ve všech vyspělých státech jeho
Sp.zn.sukls113275/2013, sukls113277/2013, sukls113278/2013, sukls113279/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Sp.zn.sukls113275/2013, sukls113277/2013, sukls113278/2013, sukls113279/2013 1. NÁZEV PŘÍPRAVKU SOUHRN ÚDAJŮ O PŘÍPRAVKU Vitamin D 3 Radaydrug 800 IU potahované tablety Vitamin D 3 Radaydrug 1 000 IU potahované
Sp.zn.sukls113275/2013, sukls113277/2013, sukls113278/2013, sukls113279/2013 1. NÁZEV PŘÍPRAVKU SOUHRN ÚDAJŮ O PŘÍPRAVKU Vitamin D 3 Radaydrug 800 IU potahované tablety Vitamin D 3 Radaydrug 1 000 IU potahované
Důležité bezpečnostní informace pro zdravotnické pracovníky
 Edukační materiály BAVENCIO (avelumab) 20 mg/ml koncentrát pro infuzní roztok Důležité bezpečnostní informace pro zdravotnické pracovníky Tento dokument obsahuje důležité informace o bezpečnosti, s nimiž
Edukační materiály BAVENCIO (avelumab) 20 mg/ml koncentrát pro infuzní roztok Důležité bezpečnostní informace pro zdravotnické pracovníky Tento dokument obsahuje důležité informace o bezpečnosti, s nimiž
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 2 k rozhodnutí o změně registrace sp. zn. sukls25846/2010 a sukls25848/2010 a příloha ke sp. zn. sukls156917/2010 a sukls157010/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 NÁZEV PŘÍPRAVKU Pentasa Sachet
Příloha č. 2 k rozhodnutí o změně registrace sp. zn. sukls25846/2010 a sukls25848/2010 a příloha ke sp. zn. sukls156917/2010 a sukls157010/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 NÁZEV PŘÍPRAVKU Pentasa Sachet
Srovnání dávkování Revlimidu denně a obden
 Srovnání dávkování Revlimidu denně a obden Luděk Pour a Revlimid denně vs obden Úvod Soubor pacientů Toxicita Léčebná odpověď a parametry přežití Závěr Úvod Lenalidomid 25 mg denně účinnější než 50 mg
Srovnání dávkování Revlimidu denně a obden Luděk Pour a Revlimid denně vs obden Úvod Soubor pacientů Toxicita Léčebná odpověď a parametry přežití Závěr Úvod Lenalidomid 25 mg denně účinnější než 50 mg
Edukační materiál. OPDIVO (nivolumab) Riziko imunitně podmíněných nežádoucích účinků a jejich zvládání
 Edukační materiál OPDIVO (nivolumab) Přípravek OPDIVO je indikován k léčbě různých typů nádorů, v monoterapii nebo v kombinaci s ipilimumabem. Kompletní seznam schválených indikací a informace o tom, u
Edukační materiál OPDIVO (nivolumab) Přípravek OPDIVO je indikován k léčbě různých typů nádorů, v monoterapii nebo v kombinaci s ipilimumabem. Kompletní seznam schválených indikací a informace o tom, u
Stanovení autoprotilátek proti TSH receptoru
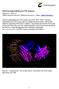 Stanovení autoprotilátek proti TSH receptoru Fejfárková Z., Pikner R. Oddělení klinických laboratoří, Klatovská nemocnice a.s., Klatovy, pikner@nemkt.cz Stanovení autoprotilátek proti TSH receptoru (anti
Stanovení autoprotilátek proti TSH receptoru Fejfárková Z., Pikner R. Oddělení klinických laboratoří, Klatovská nemocnice a.s., Klatovy, pikner@nemkt.cz Stanovení autoprotilátek proti TSH receptoru (anti
Stejně jako antibiotika
 Stejně jako antibiotika Účinek statinů LDL partikule LDL receptory Statiny syntéza jaterní cholesterol biliární cholesterol cholesterol z potravy Klíčové statinové studie a spektrum rizika Zvýšení absolutního
Stejně jako antibiotika Účinek statinů LDL partikule LDL receptory Statiny syntéza jaterní cholesterol biliární cholesterol cholesterol z potravy Klíčové statinové studie a spektrum rizika Zvýšení absolutního
Nová antiinfekční léčiva. Karolína Hronová, Ondřej Slanař Farmakologický ústav 1.LFUK
 Nová antiinfekční léčiva Karolína Hronová, Ondřej Slanař Farmakologický ústav 1.LFUK Vývoj nových ATB Tlak na vývoj nových ATB-nárůst multirezistentních kmenů Vývoj nových léčiv-1 z 5ti léčiv, které dosáhnou
Nová antiinfekční léčiva Karolína Hronová, Ondřej Slanař Farmakologický ústav 1.LFUK Vývoj nových ATB Tlak na vývoj nových ATB-nárůst multirezistentních kmenů Vývoj nových léčiv-1 z 5ti léčiv, které dosáhnou
Léčba lokalizovaného a lokálně pokročilého karcinomu prostaty (ct1-3 N0 M0)
 4.3. ZHOUBNÝ NOVOTVAR PROSTATY Léčba lokalizovaného a lokálně pokročilého karcinomu prostaty (ct1-3 N0 M0) Léčba nízce rizikového (ct1-2a a GS 6 a PSA < 10 μg/l) a středně rizikového (ct2b-c a/nebo GS
4.3. ZHOUBNÝ NOVOTVAR PROSTATY Léčba lokalizovaného a lokálně pokročilého karcinomu prostaty (ct1-3 N0 M0) Léčba nízce rizikového (ct1-2a a GS 6 a PSA < 10 μg/l) a středně rizikového (ct2b-c a/nebo GS
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č.2 k rozhodnutí o změně registrace sp.zn. sukls 145753/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Betaserc 16 tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje 16 mg
Příloha č.2 k rozhodnutí o změně registrace sp.zn. sukls 145753/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Betaserc 16 tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje 16 mg
SOUHRN ÚDAJŮ O PŘÍPRAVKU. Jeden sáček obsahuje macrogolum 4000 4 g (LaxBalance jablko) nebo 10 g (LaxBalance grapefruit, LaxBalance citrón).
 Sp.zn.sukls85836/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU LaxBalance jablko 4 g LaxBalance grapefruit 10 g LaxBalance citrόn 10 g prášek pro perorální roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Sp.zn.sukls85836/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU LaxBalance jablko 4 g LaxBalance grapefruit 10 g LaxBalance citrόn 10 g prášek pro perorální roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Edukační materiál. OPDIVO (nivolumab) Riziko imunitně podmíněných nežádoucích účinků a jejich zvládání
 Edukační materiál Přípravek OPDIVO je indikován k léčbě různých typů nádorů, v monoterapii nebo v kombinaci s ipilimumabem. Kompletní seznam schválených indikací a informace o tom, u jakých pacientů je
Edukační materiál Přípravek OPDIVO je indikován k léčbě různých typů nádorů, v monoterapii nebo v kombinaci s ipilimumabem. Kompletní seznam schválených indikací a informace o tom, u jakých pacientů je
Karcinom prostaty screening. Dalibor Pacík LF MU FN Brno
 Karcinom prostaty screening Dalibor Pacík LF MU FN Brno Screening komu jak kdy skončit U.S. Preventative Services Task Force Recommendation Co je USPSTF? Panel PL a epidemiologů podporovaný US Department
Karcinom prostaty screening Dalibor Pacík LF MU FN Brno Screening komu jak kdy skončit U.S. Preventative Services Task Force Recommendation Co je USPSTF? Panel PL a epidemiologů podporovaný US Department
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 SOUHRN ÚDAJŮ O PŘÍPRAVKU Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakákoli podezření na nežádoucí
SOUHRN ÚDAJŮ O PŘÍPRAVKU Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakákoli podezření na nežádoucí
SOUHRN ÚDAJŮ O PŘÍPRAVKU. Jeden gram gelu obsahuje calcipotriolum 50 mikrogramů (jako monohydrát) a betamethasonum 0,5 mg (jako dipropionát).
 Sp.zn.sukls13650/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Xamiol 50 mikrogramů/g + 0,5 mg/g gel 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden gram gelu obsahuje calcipotriolum 50 mikrogramů (jako
Sp.zn.sukls13650/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Xamiol 50 mikrogramů/g + 0,5 mg/g gel 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden gram gelu obsahuje calcipotriolum 50 mikrogramů (jako
