F - Změny skupenství látek
|
|
|
- Květa Bláhová
- před 8 lety
- Počet zobrazení:
Transkript
1 F - Změny skupenství látek Určeno jako učební text pro studenty dálkového studia a jako shrnující text pro studenty denního studia. VARIACE 1 Tento dokument byl kompletně vytvořen, sestaven a vytištěn v programu dosystem - EduBase. Více informací o programu naleznete na
2 ± Změny skupenství látek Změny skupenství látek O tom, v kterém skupenství se nalézá určitá látka, rozhoduje její teplota a tlak. Tání a tuhnutí Zahříváme-li pevnou látku, mění se při dosažení teploty tání v kapalinu. Naopak při ochlazování začne kapalina při teplotě tuhnutí přecházet v látku pevnou. Každá chemicky čistá krystalická látka taje i tuhne při určité teplotě. Látky beztvaré (amorfní) nemají určitou teplotu tání. Tání krystalických látek je způsobeno zvyšováním vnitřní energie částic, což následně způsobí jejich rychlejší pohyb a tedy jejich uvolnění z krystalické mřížky. Chemicky čistá krystalická látka, zahřátá na teplotu tání, nezvyšuje při dalším ohřívání svoji teplotu, dokud všechna látka neroztaje. Obdobně po celou dobu tuhnutí se teplota látky nemění. Měrné skupenské teplo tání Měrné skupenské teplo tání (značka l t) je množství tepla, které musíme dodat jednomu kilogramu pevné krystalické látky zahřáté na teplotu tání, aby se změnila na kapalinu o téže teplotě. Pozn.: Skupenské teplo tání (značka L t) je množství tepla, které musíme dodat pevné krystalické látce zahřáté na teplotu tání, aby se změnila na kapalinu o téže teplotě. Základní jednotkou měrného skupenského tepla je joule na kilogram [J/kg]. Množství tepla, nutného k přeměně tělesa z pevné látky o hmotnosti m, která je zahřáta na teplotu tání, v látku kapalnou, se nazývá skupenské teplo tání a vypočteme ho podle vzorce L t = m. l t Většina látek při tuhnutí svůj objem zmenšuje. Výjimku tvoří voda a několi dalších látek. Vypařování kapalin Kapaliny se vypařují na svém volném povrchu při jakékoliv teplotě. Vypařování lze urychlit: zvýšením teploty kapaliny odsáváním par vzniklých nad kapalinou zvětšením volného povrchu kapaliny Syté páry, kapalnění Je-li kapalina v uzavřené nádobě, páry nemohou unikat, jejich hustota a tlak se stále zvětšují. Při určité teplotě bude z kapaliny unikat právě tolik molekul, kolik se jich bude vracet zpět. Pára nad kapalinou se v tu chvíli nazývá sytá pára. Kapalina a její sytá pára jsou v tomto okamžiku v rovnováze. Sytá pára má při určité teplotě nad kapalinou určitý tlak. Vypaří-li se všechna kapalina v nádobě a my dále budeme zvyšovat teplotu, vzniká tzv. pára přehřátá. Všechny plyny jsou silně přehřátými parami. Plyny lze za velmi nízkých teplot zkapalnět. Např. na zkapalnění kyslíku ho musíme ochladit až na teplotu -119 C. Sublimace 1 z 8
3 Sublimace je jev, při kterém se pevná látka mění přímo na plynnou. Např. mokré prádlo i za mrazu "uschne". Ve skutečnosti ale zmrzne a led se následně přemění na páru. Opačným jevem, tedy přeměnnou skupenství plynného na pevné, je desublimace. Var Zahříváme-li kapalinu, stoupá tlak jejích sytých par. Dosáhne-li tlak sytých par atmosférického tlaku, nastává var. Při varu se kapalina vypařuje nejen z povrchu, ale z celého jejího objemu. Zvýšením tlaku se teplota varu zvyšuje, naopak snížením talku se teplota varu snižuje. Tohoto jevu se využívá např. při konstrukci tzv. tlakových hrnců. Měrné skupenské teplo varu Měrné skupenské teplo varu určité látky (značka l v) je určeno množstvím tepla, které musíme dodat jednomu kilogramu kapaliny zahřáté na normální teplotu varu, aby se změnila na páru o téže teplotě. Obdobně jako u tání zde platí vzorec: L v = m. l v Dojde-li ke kondenzaci (kapalnění) páry za stejných podmínek (teplota a tlak), jako byly při varu, je měrné skupenské teplo kondenzační rovno měrnému skupenskému teplu varu. Voda má značné měrné skupenské teplo varu. Tohoto jevu se využívá při vytápění domů, železničních vagónů, ale i při ochlazování. Např. v létě se kropí ulice vodou; po dešti se vždy ochladí; lidské tělo se ochlazuje vypařováním potu. Naopak vlivem tepla uvolněného při kapalnění vodních par se např. před deštěm zpravidla oteplí. Vlhkost vzduchu a její měření Atmosférický vzduch obsahuje za každé teploty vodní páry, které způsobují jeho vlhkost. Absolutní vlhkost vzduchu je určena počtem kilogramů vodní páry v jednom metru krychlovém vzduchu. Platí tedy vzorec: F = m V Jednotkou absolutní vlhkosti vzduchu je kilogram na metr krychlový [kg/m 3 ]. Je-li vzduch za dané teploty vodními parami plně nasycen, má největší (maximální) vlhkost, kterou označujeme F m. Údaj absolutní vlhkosti není vždy dostatečný. Např. za chladného rána v létě se nám vzduch zdá dosti vlhký, celá příroda je svěží. Avšak při téže absolutní vlhkosti v parném létě se nám vzduch zdá suchý, vše v přírodě usychá. Proto zavádíme pojem relativní vlhkost. Relativní (poměrná) vlhkost vzduchu je určena poměrem absolutní vlhkosti vzduchu F a maximální absolutní vlhkosti F m,která by byla možná za dané teploty. Platí tedy vzorec: f = F.100% F m Dokonale suchý vzduch (bez vodních par) má relativní vlhkost 0 %. Je-li vzduch parami nasycen, je jeho relativní vlhkost 100 %. Nejpříznivější podmínky pro člověka jsou při teplotě 20 C. Relativní vlhkost se měří vlhkoměry (hygrometry). Hlavním měřícím prvkem v těchto přístrojích bývá odmaštěný lidský vlas. Ukázkové příklady: Příklad 1: Určete teplo, které musíme dodat 8,5 kg železa zahřátého na teplotu tání, aby roztálo, je-li 2 z 8
4 měrné skupenské teplo tání železa 280 kj/kg. Řešení: m = 8,5 kg l t = 280 kj/kg = J/kg L t =? [J] L t = m. l t L t = 8, L t = J = 2,38 MJ Železu musíme dodat teplo o velikosti 2,38 MJ. Příklad 2: Led o hmotnosti 6,2 kg a o počáteční teplotě -25 o C se přeměnil za normálního tlaku na vodu teploty 0 o C (objemu V 2). Určete teplo, které soustava přijala od svého okolí během celého děje. Měrná tepelná kapacita ledu je 2,1 kj/kg. o C, měrné skupenské teplo tání ledu je 334 kj/kg. Řešení: m = 6,2 kg t 1 = -25 C t 2 = 0 C c = 2,1 kj/kg. C = J/kg. C l t = 334 kj/kg = J/kg Q =? [J] Nejprve spočítáme teplo potřebné k ohřátí ledu z teploty -25 C na teplotu 0 C: Q 1 = m. c. (t 2 - t 1) Q 1 = 6, (0 - (-25)) = Q 1 = J Nyní spočítáme teplo potřebné k přeměně ledu na vodu o téže teplotě: L t = m. l t L t = 6, = L t = J Celkové dodané teplo odpovídá součtu vypočtených tepel: Q = Q 1 + L t Q = J J = J = 2,4 MJ (po zaokrouhlení) Soustava přijala od svého okolí teplo o velikosti asi 2,4 MJ. Příklad 3: Pára o hmotnosti 5,2 kg a o počáteční teplotě 100 o C zkondenzovala na vodu a ta se při postupném ochlazování změnila až na led o teplotě -25 o C. Jaké teplo se při tom uvolnilo? Měrná tepelná kapacita ledu je 2,1 kj/kg. o C, měrná tepelná kapacita vody je 4,2 kj/kg. o C, měrné skupenské teplo tání ledu je 334 kj/kg, měrné skupenské teplo varu vody je kj/kg. Řešení: m = 5,2 kg t 1 = 100 t 2 = -25 C 3 z 8
5 c L = 2,4 kj/kg. C = J/kg. C c V = 4,2 kj/kg. C = J/kg. C l t = 334 kj/kg = J/kg l v = kj/kg = J/kg Q =? [J] Celkové teplo je tvořeno skupenským teplem L v uvolněným při kondenzaci páry, dále teplem Q 1 uvolněným při ochlazení vody z teploty 100 C na teplotu 0 C, pak teplem L t uvolněným při změně vody na led a nakonec teplem Q 2 uvolněným při ochlazení ledu z teploty 0 C na teplotu -25 C: Q = m. l v + m. c v. (t 1 - t 0) + m. l t + m. c L. (t 0 - t 2) Q = m. [l V + c V. (t 1 - t 0) + l t + c L. (t 0 - t 2)] Po dosazení: Q = 5,2. [ (100-0) (0 - (-25))] Q = J = 16 MJ (po zaokrouhlení) Celkově se uvolnilo teplo o velikosti asi 16 MJ. ± Změny skupenství látek - procvičovací příklady 1. V chladničce se vyrobí za 2 hodiny led o hmotnosti 5,5 kg a o teplotě 0 o C z vody o počáteční teplotě 6 o C. Jak velké teplo bylo odbráno vodě chladicím zařízením? Měrná tepelná kapacita vody je 4,2 kj/kg. o C, měrné skupenské teplo tání ledu je 334 kj/kg. 1,96 MJ 2. Jak velký objem má voda, která vznikne, roztaje-li led o hmotnosti 1,1 kg? Hustota vody je kg/m 3 a hustota ledu je 900 kg/m 3. 1,1 dm 3 3. Voda o hmotnosti 470 g a o počáteční teplotě 75 o C se mísí s ledem o hmotnosti 55 g a o počáteční teplotě 0 o C. Po roztání ledu se teplota ustálila na 58 o C. Určete měrné skupenské teplo tání ledu. Měrná tepelná kapacita vody je 4,2 kj/kg. o C. 367 KJ/kg 4. Jak velké teplo je třeba dodat vodě o hmotnosti 5,6 kg a o teplotě 100 o C, aby se přeměnila v páru téže teploty? Měrné skupenské teplo vypařování vody je kj/kg. 12,9 MJ Určete teplo, které musíme dodat 3,5 kg železa zahřátého na teplotu tání, aby roztálo, je-li měrné skupenské teplo tání železa 280 kj/kg. 980 kj Do vody o hmotnosti 8,0 kg a o počáteční teplotě 64 o C byly vhozeny kousky ledu o celkové hmotnosti 2,8 kg a o počáteční teplotě 0 o C. Určete teplotu vody po roztání ledu. Měrná tepelná kapacita vody je 4,2 kj/kg. o C, měrné skupenské teplo tání ledu je 334 kj/kg. 26,8 C z 8
6 7. Ve vodě o hmotnosti 820 g a o počáteční teplotě 12 o C zkapalní vodní pára o hmotnosti 25 g a o počáteční teplotě 100 o C. Určete výslednou teplotu vody. Měrná tepelná kapacita vody je 4,2 kj/kg. o C, měrné skupenské teplo varu vody je kj/kg. 31 C 8. Jaké teplo přijme ocelový předmět o hmotnosti 180 kg a o teplotě tání o C, jestliže roztaje a teplota taveniny se nezmění? Měrně skupenské teplo tání oceli je 260 kj/kg. 47 MJ 9. Ve vodě o hmotnosti 1,4 kg má roztát led o hmotnosti 260 g a o počáteční teplotě 0 oc. Jaká je nejnižší možná počáteční teplota vody? Měrná tepelná kapacita vody je 4,2 kj/kg. o C a měrné skupenské teplo tání ledu je 334 kj/kg. 14,8 C 10. Do vody o hmotnosti 3,5 kg a o teplotě 40 o C byl vložen led o hmotnosti 2,2 kg a o teplotě 0 o C. Určete hmotnost ledu, který roztaje. Předpokládáme, že tepelná výměna nastala jen mezi vodou a ledem. Měrná tepelná kapacita vody je 4,2 kj/kg. o C, měrné skupenské teplo tání ledu je 334 kj/kg. 1,8 kg 11. Mokré prádlo má hmotnost 48 kg, z toho 10 % hmotnosti je voda. Jak velké teplo voda při vypaření přijala, jestliže na odpaření vody o hmotnosti 1 kg se za dané teploty potřebuje přibližně teplo kj? 11 MJ 12. K ochlazení nápojů se použilo ledu o hmotnosti 1,3 kg a o teplotě 0 o C. Jak velké teplo odevzdaly chlazené nápoje ledu, jestliže všechen led roztál ve vodu o teplotě 0 oc. Měrné skupenské teplo tání ledu je 334 kj/kg. 434 kj 13. V tepelně izolované nádobě je voda o hmotnosti 4,2 kg a teplotě 16 o C. Vodu zahříváme a při teplotě 100 o C se hmotnost vody vypařováním sníží o 10 %. Jak velké celkové teplo při tom voda přijme? Vypařování při teplotách nižších než 100 o C a tepelné ztráty do okolí neuvažujeme. Měrná tepelná kapacita vody je 4,2 kj/kg. o C a měrné skupenské teplo varu vody je kj/kg. 2,43 MJ 14. Led o hmotnosti 4 kg a o počáteční teplotě -8 o C roztaje na vodu o teplotě 0 o C. Voda vzniklá z ledu se dále zahřeje na teplotu 100 o C a při této teplotě se vypaří při normálním tlaku 100 kpa na páru o teplotě 100 o C. Určete celkové teplo, které soustava přijala, ve všech třech dějích. Měrná tepelná kapacita ledu je 2,1 kj/kg. o C, měrná tepelná kapacita vody je 4,2 kj/kg. o C, měrné skupenské teplo tání ledu je 334 kj/kg, měrné skupenské teplo varu vody je kj/kg. 12,1 MJ z 8
7 15. Určete hmotnost ledu počáteční teploty 0 o C, který může roztát ve vodě o hmotnosti 4,7 kg a o počáteční teplotě 65 o C. Měrná tepelná kapacita vody je 4,2 kj/kg. o C a měrné skupenské teplo tání ledu je 334 kj/kg. 3,8 kg Voda o hmotnosti kg má objem 1,1 m 3. Jaký objem má led, který vznikne zmrznutím této vody, je-li hustota ledu 920 kg/m 3? 1,2 m Jaké teplo přijme voda o hmotnosti 5,6 kg a o teplotě 0 o C, je-li přivedena do varu a přemění se v sytou páru o teplotě 100 o C při normálním tlaku 100 kpa? Měrná tepelná kapacita vody je 4,2 kj/kg. o C a měrné skupenské teplo varu vody při normálním tlaku je kj/kg. 15 MJ 18. Těleso ze železa o hmotnosti 1,5 kg bylo ponořeno do vroucí vody a ohřálo se na teplotu 100 o C. Potom bylo vloženo do nádoby většího objemu naplněné ledovou drtí o teplotě 0 o C a ochlazeno na tuto teplotu. Určete hmotnost ledu, který při tom roztál. Předpokládáme, že tepelná výměna nastala jen mezi tělesem a ledem. Měrné skupenské teplo tání ledu je 334 kj/kg a měrná tepelná kapacita železa je 0,450 kj/kg. o C. 202 g 19. V tepelně izolované nádobě je led o hmotnosti 1,2 kg a o teplotě 0 o C. Do nádoby přidáme vodu o teplotě 100 o C tak, že led v nádobě roztaje a výsledná teplota vody v nádobě je 0 o C. Určete hmotnost přidané vody. Měrná tepelná kapacita vody je 4,2 kj/kg. o C, měrné skupenské teplo tání ledu je 334 kj/kg. 0,95 kg 20. Led o hmotnosti 5,5 kg a o počáteční teplotě -15 o C se má přeměnit ve vodní páru o teplotě 100 o C. Určete teplo, které je třeba dodat. Měrná tepelná kapacita ledu je 2,1 kj/kg. o C, měrná tepelná kapacita vody je 4,2 kj/kg. o C, měrné skupenské teplo tání ledu je 334 kj/kg, měrné skupenské teplo varu vody je kj/kg. 16,75 MJ 21. Led o hmotnosti 3,0 kg a o počáteční teplotě -20 o C se přeměnil za normálního tlaku na vodu teploty 0 o C (objemu V 2). Určete teplo, které soustava přijala od svého okolí během celého děje. Měrná tepelná kapacita ledu je 2,1 kj/kg. o C, měrné skupenské teplo tání ledu je 334 kj/kg. 1,13 MJ 22. Ocelový odlitek o hmotnosti 260 kg má teplotu tání. Jaké skupenské teplo přijme k roztavení? Měrné skupenské teplo tání oceli je 258 kj/kg. 67,1 MJ Jak velké teplo dodá svému okolí voda o teplotě 0 o C a o hmotnosti 145 g, která zmrzne na led o teplotě 0 o C? Měrné skupenské teplo tání ledu je 334 kj/kg. 48,4 kj z 8
8 24. Kus ledu o hmotnosti 3,0 kg a o teplotě -10 o C se má přeměnit na vodu o teplotě 25 oc. Jaké teplo přijme při tom led a následně vzniklá voda od svého okolí? Měrná tepelná kapacita ledu je 2,1 kj/kg. o C, měrné skupenské teplo tání ledu je 334 kj/kg, měrná tepelná kapacita vody je 4,2 kj/kg. o C. 1,38 MJ Jak velký objem má voda, která vznikne, roztaje-li led o objemu 1,1 dm 3? Hustota vody je kg/m 3 a hustota ledu je 900 kg/m 3. 0,99 litru V tělese parního ústředního topení zkapalní za hodinu sytá pára o hmotnosti 2,9 kg a počáteční teplotě 100 o C na vodu, jejíž teplota se sníží na 75 o C. Jaké celkové teplo odevzdá soustava vytápěné místnosti? Měrná tepelná kapacita vody je 4,2 kj/kg. o C, měrné skupenské teplo varu vody je kj/kg. 6,86 MJ 27. Vodní pára o teplotě 100 o C zkapalní ve vodě o hmotnosti 1,2 kg a o počáteční teplotě 12 o C. Jak velkou hmotnost má vodní pára, jestliže teplota vody stoupne na 84 o C. Měrná tepelná kapacita vody je 4,2 kj/kg. o C, měrné skupenské teplo varu vody je kj/kg. 156 g 28. V tepelně izolované nádobě je led o hmotnosti 2,5 kg a o teplotě 0 o C. Do nádoby přivádíme sytou vodní páru o teplotě 100 o C tak, že led roztaje a výsledná teplota vody je 0 o C. Určete hmotnost přivedené vodní páry. Měrná tepelná kapacita vody je 4,2 kj/kg. o C, měrné skupenské teplo tání ledu je 334 kj/kg, měrné skupenské teplo varu vody je kj/kg. 0,31 kg 29. Voda o hmotnosti 2,4 kg a o teplotě 84 o C se ohřeje na teplotu 100 o C a přemění se na páru téže teploty. Určete teplo, které soustava přijala od svého okolí během celého děje. Měrná tepelná kapacita vody je 4,2 kj/kg. o C a měrné skupenské teplo varu vody je kj/kg. 5,6 MJ 30. Pára o hmotnosti 8 kg a o počáteční teplotě 100 o C zkondenzovala na vodu a ta se při postupném ochlazování změnila až na led o teplotě -15 o C. Jaké teplo se při tom uvolnilo? Měrná tepelná kapacita ledu je 2,1 kj/kg. o C, měrná tepelná kapacita vody je 4,2 kj/kg. o C, měrné skupenské teplo tání ledu je 334 kj/kg, měrné skupenské teplo varu vody je kj/kg. 24,4 MJ 31. Jak velké teplo dodá vodní pára o hmotnosti 5,5 kg a teplotě 100 o C svému okolí, jestliže zkapalní a vzniklá voda se ochladí na 0 o C. Měrná tepelná kapacita vody je 4,2 kj/kg. o C, měrné skupenské teplo varu vody je kj/kg. 14,7 MJ z 8
9 32. Při kolika stupních bude vařit voda na Mont Everestu (8 847 m), když na každých 1000 m výšky klesne teplota varu vody asi o 2,9 o C? 74,3 C 33. Za jeden den se při teplém počasí odpaří z lidského těla až 2,1 kg vody. Voda o hmotnosti 1 kg se za určité teploty přemění v páru téže teploty, přijme-li ze svého okolí přibližně teplo kj. Jak velké teplo odevzdá tělo na odpaření potu za jeden den? 4,83 MJ Jaké teplo odvzdá svému okolí sytá vodní pára o hmotnosti 28 kg a teplotě 100 o C, zkapalní-li na vodu téže teploty? Měrné skupenské teplo varu vody je kj/kg. 63,3 MJ z 8
10 Obsah Změny skupenství látek 1 Změny skupenství látek - procvičovací příklady :29:58 Vytištěno v programu dosystem - EduBase (
Vnitřní energie pevné látky < Vnitřní energie kapaliny < Vnitřní energie plynu (nejmenší energie)
 Změny skupenství Při změně tělesa z pevné látky na kapalinu nebo z kapaliny na plyn se jeho vnitřní energie zvyšuje musíme dodávat teplo (zahřívat). Při změně tělesa z plynu na kapalinu, nebo z kapaliny
Změny skupenství Při změně tělesa z pevné látky na kapalinu nebo z kapaliny na plyn se jeho vnitřní energie zvyšuje musíme dodávat teplo (zahřívat). Při změně tělesa z plynu na kapalinu, nebo z kapaliny
F8 - Změny skupenství Číslo variace: 1
 F8 - Změny skupenství Číslo variace: 1 1. K vypařování kapaliny dochází: při každé teplotě v celém jejím objemu pouze při teplotě 100 C v celém objemu kapaliny pouze při normální teplotě a normálním tlaku
F8 - Změny skupenství Číslo variace: 1 1. K vypařování kapaliny dochází: při každé teplotě v celém jejím objemu pouze při teplotě 100 C v celém objemu kapaliny pouze při normální teplotě a normálním tlaku
Název DUM: Změny skupenství v příkladech
 Základní škola národního umělce Petra Bezruče, Frýdek-Místek, tř. T. G. Masaryka 454 Zpracováno v rámci OP VK - EU peníze školám Jednička ve vzdělávání CZ.1.07/1.4.00/21.2759 Název DUM: Změny skupenství
Základní škola národního umělce Petra Bezruče, Frýdek-Místek, tř. T. G. Masaryka 454 Zpracováno v rámci OP VK - EU peníze školám Jednička ve vzdělávání CZ.1.07/1.4.00/21.2759 Název DUM: Změny skupenství
SKUPENSKÉ PŘEMĚNY POJMY K ZOPAKOVÁNÍ. Testové úlohy varianta A
 Škola: Autor: DUM: Vzdělávací obor: Tematický okruh: Téma: Masarykovo gymnázium Vsetín Mgr. Jitka Novosadová MGV_F_SS_3S3_D11_Z_OPAK_T_Skupenske_premeny_T Člověk a příroda Fyzika Skupenské přeměny Opakování
Škola: Autor: DUM: Vzdělávací obor: Tematický okruh: Téma: Masarykovo gymnázium Vsetín Mgr. Jitka Novosadová MGV_F_SS_3S3_D11_Z_OPAK_T_Skupenske_premeny_T Člověk a příroda Fyzika Skupenské přeměny Opakování
ZMĚNY SKUPENSTVÍ LÁTEK
 ZMĚNY SKUPENSTVÍ LÁTEK TÁNÍ A TUHNUTÍ - OSNOVA Kapilární jevy příklad Skupenské přeměny látek Tání a tuhnutí Teorie s video experimentem Příklad KAPILÁRNÍ JEVY - OPAKOVÁNÍ KAPILÁRNÍ JEVY - PŘÍKLAD Jak
ZMĚNY SKUPENSTVÍ LÁTEK TÁNÍ A TUHNUTÍ - OSNOVA Kapilární jevy příklad Skupenské přeměny látek Tání a tuhnutí Teorie s video experimentem Příklad KAPILÁRNÍ JEVY - OPAKOVÁNÍ KAPILÁRNÍ JEVY - PŘÍKLAD Jak
23_ 2 24_ 2 25_ 2 26_ 4 27_ 5 28_ 5 29_ 5 30_ 7 31_
 Obsah 23_ Změny skupenství... 2 24_ Tání... 2 25_ Skupenské teplo tání... 2 26_ Anomálie vody... 4 27_ Vypařování... 5 28_ Var... 5 29_ Kapalnění... 5 30_ Jak určíš skupenství látky?... 7 31_ Tepelné motory:...
Obsah 23_ Změny skupenství... 2 24_ Tání... 2 25_ Skupenské teplo tání... 2 26_ Anomálie vody... 4 27_ Vypařování... 5 28_ Var... 5 29_ Kapalnění... 5 30_ Jak určíš skupenství látky?... 7 31_ Tepelné motory:...
TEPELNÉ JEVY. Mgr. Jan Ptáčník - GJVJ - Fyzika - Tercie
 TEPELNÉ JEVY Mgr. Jan Ptáčník - GJVJ - Fyzika - Tercie Vnitřní energie tělesa Každé těleso se skládá z látek. Látky se skládají z částic. neustálý neuspořádaný pohyb kinetická energie vzájemné působení
TEPELNÉ JEVY Mgr. Jan Ptáčník - GJVJ - Fyzika - Tercie Vnitřní energie tělesa Každé těleso se skládá z látek. Látky se skládají z částic. neustálý neuspořádaný pohyb kinetická energie vzájemné působení
Digitální učební materiál
 Evidenční číslo materiálu: 516 Digitální učební materiál Autor: Mgr. Pavel Kleibl Datum: 22. 1. 2013 Ročník: 8. Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Fyzika Tematický okruh: Energie Téma:
Evidenční číslo materiálu: 516 Digitální učební materiál Autor: Mgr. Pavel Kleibl Datum: 22. 1. 2013 Ročník: 8. Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Fyzika Tematický okruh: Energie Téma:
F - příprava na 4. zápočtový test
 F - příprava na 4. zápočtový test Určeno pro studenty dálkového studia VARIACE 1 Tento dokument byl kompletně vytvořen, sestaven a vytištěn v programu dosystem - EduBase. Více informací o programu naleznete
F - příprava na 4. zápočtový test Určeno pro studenty dálkového studia VARIACE 1 Tento dokument byl kompletně vytvořen, sestaven a vytištěn v programu dosystem - EduBase. Více informací o programu naleznete
1) Skupenství fáze, forma, stav. 2) 3 druhy skupenství (1 látky): pevné (led) kapalné (voda) plynné (vodní pára)
 SKUPENSTVÍ 1) Skupenství fáze, forma, stav 2) 3 druhy skupenství (1 látky): pevné (led) kapalné (voda) plynné (vodní pára) 3) Pevné látky nemění tvar, objem částice blízko sebe, pohybují se kolem urč.
SKUPENSTVÍ 1) Skupenství fáze, forma, stav 2) 3 druhy skupenství (1 látky): pevné (led) kapalné (voda) plynné (vodní pára) 3) Pevné látky nemění tvar, objem částice blízko sebe, pohybují se kolem urč.
Řešení: Fázový diagram vody
 Řešení: 1) Menší hustota ledu v souladu s Archimédovým zákonem zapříčiňuje plování jedu ve vodě. Vodní nádrže a toky tudíž zamrzají shora (od hladiny). Kdyby hustota ledu byla větší než hustota vody, docházelo
Řešení: 1) Menší hustota ledu v souladu s Archimédovým zákonem zapříčiňuje plování jedu ve vodě. Vodní nádrže a toky tudíž zamrzají shora (od hladiny). Kdyby hustota ledu byla větší než hustota vody, docházelo
Laboratorní práce č. 2: Určení měrného skupenského tepla tání ledu
 Přírodní vědy moderně a interaktivně FYZIKA 1. ročník šestiletého studia Laboratorní práce č. 2: Určení měrného skupenského tepla tání ledu ymnázium Přírodní vědy moderně a interaktivně FYZIKA 1. ročník
Přírodní vědy moderně a interaktivně FYZIKA 1. ročník šestiletého studia Laboratorní práce č. 2: Určení měrného skupenského tepla tání ledu ymnázium Přírodní vědy moderně a interaktivně FYZIKA 1. ročník
F - Elektrická práce, elektrický výkon, účinnost
 F - Elektrická práce, elektrický výkon, účinnost rčeno jako učební text pro studenty dálkového studia a jako shrnující text pro studenty denního studia. VAIACE Tento dokument byl kompletně vytvořen, sestaven
F - Elektrická práce, elektrický výkon, účinnost rčeno jako učební text pro studenty dálkového studia a jako shrnující text pro studenty denního studia. VAIACE Tento dokument byl kompletně vytvořen, sestaven
LOGO. Změny skupenství
 Změny skupenství Látka existuje ve třech skupenstvích Pevném Kapalném Plynném Látka může přecházet z jednoho skupenství do druhého. Existují tedy tyto změny skupenství: Změny skupenství plyn sublimace
Změny skupenství Látka existuje ve třech skupenstvích Pevném Kapalném Plynném Látka může přecházet z jednoho skupenství do druhého. Existují tedy tyto změny skupenství: Změny skupenství plyn sublimace
Termika. Autor: Mgr. Jaromír JUŘEK Kopírování a jakékoliv další využití výukového materiálu je povoleno pouze s uvedením odkazu na www.jarjurek.cz.
 Variace 1 Termika Autor: Mgr. Jaromír JUŘEK Kopírování a jakékoliv další využití výukového materiálu je povoleno pouze s uvedením odkazu na www.jarjurek.cz. 1. Termika - nauka o tepelných jevech Vnitřní
Variace 1 Termika Autor: Mgr. Jaromír JUŘEK Kopírování a jakékoliv další využití výukového materiálu je povoleno pouze s uvedením odkazu na www.jarjurek.cz. 1. Termika - nauka o tepelných jevech Vnitřní
Zavádění inovativních metod a výukových materiálů do přírodovědných předmětů na Gymnáziu v Krnově
 Zavádění inovativních metod a výukových materiálů do přírodovědných předmětů na Gymnáziu v Krnově 06_6_ Změny skupenství látek Ing. Jakub Ulmann 6 Změny skupenství látek 6.1 Tání 6.2 Tuhnutí 6.3 Změna
Zavádění inovativních metod a výukových materiálů do přírodovědných předmětů na Gymnáziu v Krnově 06_6_ Změny skupenství látek Ing. Jakub Ulmann 6 Změny skupenství látek 6.1 Tání 6.2 Tuhnutí 6.3 Změna
(test version, not revised) 24. listopadu 2010
 Změny skupenství (test version, not revised) Petr Pošta pposta@karlin.mff.cuni.cz 24. listopadu 2010 Obsah Tání Tuhnutí Sublimace a desublimace Vypařování a var. Kondenzace Sytá pára Fázový diagram Vodní
Změny skupenství (test version, not revised) Petr Pošta pposta@karlin.mff.cuni.cz 24. listopadu 2010 Obsah Tání Tuhnutí Sublimace a desublimace Vypařování a var. Kondenzace Sytá pára Fázový diagram Vodní
6. Jaký je výkon vařiče, který ohřeje 1 l vody o 40 C během 5 minut? Měrná tepelná kapacita vody je W)
 TEPLO 1. Na udržení stále teploty v místnosti se za hodinu spotřebuje 4,2 10 6 J tepla. olik vody proteče radiátorem ústředního topení za hodinu, jestliže má voda při vstupu do radiátoru teplotu 80 ºC
TEPLO 1. Na udržení stále teploty v místnosti se za hodinu spotřebuje 4,2 10 6 J tepla. olik vody proteče radiátorem ústředního topení za hodinu, jestliže má voda při vstupu do radiátoru teplotu 80 ºC
Kalorimetrická rovnice, skupenské přeměny
 Základní škola Nový Bor, náměstí Míru 128, okres Česká Lípa, příspěvková organizace e mail: info@zsnamesti.cz; www.zsnamesti.cz; telefon: 487 722 010; fax: 487 722 378 Registrační číslo: CZ.1.07/1.4.00/21.3267
Základní škola Nový Bor, náměstí Míru 128, okres Česká Lípa, příspěvková organizace e mail: info@zsnamesti.cz; www.zsnamesti.cz; telefon: 487 722 010; fax: 487 722 378 Registrační číslo: CZ.1.07/1.4.00/21.3267
SKUPENSTVÍ LÁTEK Prima - Fyzika
 SKUPENSTVÍ LÁTEK Prima - Fyzika Skupenství látek Pevné skupenství Skupenství látek Skupenství látek Pevné skupenství Kapalné skupenství Skupenství látek Pevné skupenství Kapalné skupenství Plynné skupenství
SKUPENSTVÍ LÁTEK Prima - Fyzika Skupenství látek Pevné skupenství Skupenství látek Skupenství látek Pevné skupenství Kapalné skupenství Skupenství látek Pevné skupenství Kapalné skupenství Plynné skupenství
Měření měrného skupenského tepla tání ledu
 KATEDRA EXPERIMENTÁLNÍ FYZIKY PŘÍRODOVĚDECKÁ FAKULTA UNIVERZITY PALACKÉHO V OLOMOUCI FYZIKÁLNÍ PRAKTIKUM Z MOLEKULOVÉ FYZIKY A TERMODYNAMIKY Měření měrného skupenského tepla tání ledu Úvod Tání, měrné
KATEDRA EXPERIMENTÁLNÍ FYZIKY PŘÍRODOVĚDECKÁ FAKULTA UNIVERZITY PALACKÉHO V OLOMOUCI FYZIKÁLNÍ PRAKTIKUM Z MOLEKULOVÉ FYZIKY A TERMODYNAMIKY Měření měrného skupenského tepla tání ledu Úvod Tání, měrné
POZNÁMKA: V USA se používá ještě Fahrenheitova teplotní stupnice. Převodní vztahy jsou vzhledem k volbě základních bodů složitější: 9 5
 TEPLO, TEPLOTA Tepelný stav látek je charakterizován veličinou termodynamická teplota T Jednotkou je kelvin T K Mezi Celsiovou a Kelvinovou teplotní stupnicí existuje převodní vztah T 73,5C t POZNÁMKA:
TEPLO, TEPLOTA Tepelný stav látek je charakterizován veličinou termodynamická teplota T Jednotkou je kelvin T K Mezi Celsiovou a Kelvinovou teplotní stupnicí existuje převodní vztah T 73,5C t POZNÁMKA:
DUM č. 12 v sadě. 10. Fy-1 Učební materiály do fyziky pro 2. ročník gymnázia
 projekt GML Brno Docens DUM č. 12 v sadě 10. Fy-1 Učební materiály do fyziky pro 2. ročník gymnázia Autor: Vojtěch Beneš Datum: 03.05.2014 Ročník: 1. ročník Anotace DUMu: Kapaliny, změny skupenství Materiály
projekt GML Brno Docens DUM č. 12 v sadě 10. Fy-1 Učební materiály do fyziky pro 2. ročník gymnázia Autor: Vojtěch Beneš Datum: 03.05.2014 Ročník: 1. ročník Anotace DUMu: Kapaliny, změny skupenství Materiály
Vzdělávací materiál. vytvořený v projektu OP VK CZ.1.07/1.5.00/ Anotace. Změny skupenství látek - tání, tuhnutí VY_32_INOVACE_F0114.
 Vzdělávací materiál vytvořený v projektu OP VK Název školy: Gymnázium, Zábřeh, náměstí Osvobození 20 Číslo projektu: Název projektu: Číslo a název klíčové aktivity: CZ.1.07/1.5.00/34.0211 Zlepšení podmínek
Vzdělávací materiál vytvořený v projektu OP VK Název školy: Gymnázium, Zábřeh, náměstí Osvobození 20 Číslo projektu: Název projektu: Číslo a název klíčové aktivity: CZ.1.07/1.5.00/34.0211 Zlepšení podmínek
VÝUKOVÝ MATERIÁL. 0301 Ing. Yvona Bečičková Tematická oblast. Termika Číslo a název materiálu VY_32_INOVACE_0301_0215 Anotace
 VÝUKOVÝ MATERIÁL Identifikační údaje školy Vyšší odborná škola a Střední škola, Varnsdorf, příspěvková organizace Bratislavská 2166, 407 47 Varnsdorf, IČO: 18383874 www.vosassvdf.cz, tel. +420412372632
VÝUKOVÝ MATERIÁL Identifikační údaje školy Vyšší odborná škola a Střední škola, Varnsdorf, příspěvková organizace Bratislavská 2166, 407 47 Varnsdorf, IČO: 18383874 www.vosassvdf.cz, tel. +420412372632
STRUKTURA PEVNÝCH LÁTEK A KAPALIN
 STRUKTURA PEVNÝCH LÁTEK A KAPALIN 19. ZMĚNY SKUPENSTVÍ, FÁZOVÝ DIAGRAM Autor: Ing. Eva Jančová DESS SOŠ a SOU spol. s r. o. SKUPENSTVÍ - Skupenství neboli stav je konkrétní forma látky, charakterizovaná
STRUKTURA PEVNÝCH LÁTEK A KAPALIN 19. ZMĚNY SKUPENSTVÍ, FÁZOVÝ DIAGRAM Autor: Ing. Eva Jančová DESS SOŠ a SOU spol. s r. o. SKUPENSTVÍ - Skupenství neboli stav je konkrétní forma látky, charakterizovaná
3.2 Látka a její skupenství
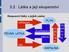 3.2 Látka a její skupenství Skupenství látky a jejich změny sublimace PEVNÁ LÁTKA tání desublimace tuhnutí PLYN vy pa řo vá ní KAPALINA zka pal ňo vá ní Látka a změna vnitřní energie Změna vnitřní energie
3.2 Látka a její skupenství Skupenství látky a jejich změny sublimace PEVNÁ LÁTKA tání desublimace tuhnutí PLYN vy pa řo vá ní KAPALINA zka pal ňo vá ní Látka a změna vnitřní energie Změna vnitřní energie
Termodynamika 2. UJOP Hostivař 2014
 Termodynamika 2 UJOP Hostivař 2014 Skupenské teplo tání/tuhnutí je (celkové) teplo, které přijme pevná látka při přechodu na kapalinu během tání nebo naopak Značka Veličina Lt J Nedochází při něm ke změně
Termodynamika 2 UJOP Hostivař 2014 Skupenské teplo tání/tuhnutí je (celkové) teplo, které přijme pevná látka při přechodu na kapalinu během tání nebo naopak Značka Veličina Lt J Nedochází při něm ke změně
STRUKTURA KAPALIN STRUKTURA KAPALIN
 Předmět: Ročník: Vytvořil: Datum: FYZIKA PRVNÍ MGR. JÜTTNEROVÁ 18. 5. 2013 Název zpracovaného celku: STRUKTURA KAPALIN STRUKTURA KAPALIN Struktura kapalin, povrchová vrstva kapaliny: Každá molekula kapaliny
Předmět: Ročník: Vytvořil: Datum: FYZIKA PRVNÍ MGR. JÜTTNEROVÁ 18. 5. 2013 Název zpracovaného celku: STRUKTURA KAPALIN STRUKTURA KAPALIN Struktura kapalin, povrchová vrstva kapaliny: Každá molekula kapaliny
Energie. Název sady DUM. Člověk a příroda. Vzdělávací oblast. Fyzika. Autor, datum vytvoření Mgr. Zbyněk Šostý, 2012. interaktivní tabule
 Název DUM: Skupenství látek Název sady DUM Číslo DUM Vzdělávací oblast Vzdělávací obor Energie VY_32_INOVACE_14_S1 12 Člověk a příroda Fyzika Ročník 8. Autor, datum vytvoření Mgr. Zbyněk Šostý, 2012 Doporučená
Název DUM: Skupenství látek Název sady DUM Číslo DUM Vzdělávací oblast Vzdělávací obor Energie VY_32_INOVACE_14_S1 12 Člověk a příroda Fyzika Ročník 8. Autor, datum vytvoření Mgr. Zbyněk Šostý, 2012 Doporučená
[381 m/s] 12. Ocelovou součást o hmotnosti m z = 4 kg, měrném teple c z = 420 J/kgK, zahřátou na teplotu t z = 900 C ponoříme do olejové lázně o
![[381 m/s] 12. Ocelovou součást o hmotnosti m z = 4 kg, měrném teple c z = 420 J/kgK, zahřátou na teplotu t z = 900 C ponoříme do olejové lázně o [381 m/s] 12. Ocelovou součást o hmotnosti m z = 4 kg, měrném teple c z = 420 J/kgK, zahřátou na teplotu t z = 900 C ponoříme do olejové lázně o](/thumbs/27/11706382.jpg) 3 - Termomechanika 1. Hustota vzduchu při tlaku p l = 0,2 MPa a teplotě t 1 = 27 C je ρ l = 2,354 kg/m 3. Jaká je jeho hustota ρ 0 při tlaku p 0 = 0,1MPa a teplotě t 0 = 0 C [1,29 kg/m 3 ] 2. Určete objem
3 - Termomechanika 1. Hustota vzduchu při tlaku p l = 0,2 MPa a teplotě t 1 = 27 C je ρ l = 2,354 kg/m 3. Jaká je jeho hustota ρ 0 při tlaku p 0 = 0,1MPa a teplotě t 0 = 0 C [1,29 kg/m 3 ] 2. Určete objem
ABSOLVENTSKÁ PRÁCE ZÁKLADNÍ ŠKOLA, ŠKOLNÍ 24, BYSTRÉ 9. ROČNÍK. Změny skupenství. Filip Skalský, David Řehůřek
 ABSOLVENTSKÁ PRÁCE ZÁKLADNÍ ŠKOLA, ŠKOLNÍ 24, 569 92 BYSTRÉ 9. ROČNÍK Změny skupenství Filip Skalský, David Řehůřek ŠKOLNÍ ROK 2011/2012 Prohlašujeme, že jsme absolventskou práci vypracovali samostatně
ABSOLVENTSKÁ PRÁCE ZÁKLADNÍ ŠKOLA, ŠKOLNÍ 24, 569 92 BYSTRÉ 9. ROČNÍK Změny skupenství Filip Skalský, David Řehůřek ŠKOLNÍ ROK 2011/2012 Prohlašujeme, že jsme absolventskou práci vypracovali samostatně
Molekulová fyzika a termika
 Molekulová fyzika a termika Fyzika 1. ročník Vzdělávání pro konkurenceschopnost Inovace výuky oboru Informační technologie MěSOŠ Klobouky u Brna Mgr. Petr Kučera 1 Obsah témat v kapitole Molekulová fyzika
Molekulová fyzika a termika Fyzika 1. ročník Vzdělávání pro konkurenceschopnost Inovace výuky oboru Informační technologie MěSOŠ Klobouky u Brna Mgr. Petr Kučera 1 Obsah témat v kapitole Molekulová fyzika
CELKOVÉ OPAKOVÁNÍ UČIVA + ZÁPIS DO ŠKOLNÍHO SEŠITU část 03 VNITŘNÍ ENERGIE, TEPLO.
 CELKOVÉ OPAKOVÁNÍ UČIVA + ZÁPIS DO ŠKOLNÍHO SEŠITU část 03 VNITŘNÍ ENERGIE, TEPLO. 01) Složení látek opakování učiva 6. ročníku: Všechny látky jsou složeny z částic nepatrných rozměrů (tj. atomy, molekuly,
CELKOVÉ OPAKOVÁNÍ UČIVA + ZÁPIS DO ŠKOLNÍHO SEŠITU část 03 VNITŘNÍ ENERGIE, TEPLO. 01) Složení látek opakování učiva 6. ročníku: Všechny látky jsou složeny z částic nepatrných rozměrů (tj. atomy, molekuly,
Názvosloví Kvalita Výroba Kondenzace Teplosměnná plocha
 Názvosloví Kvalita Výroba Kondenzace Teplosměnná plocha Názvosloví páry Pro správné pochopení funkce parních systémů musíme znát základní pojmy spojené s párou. Entalpie Celková energie, příslušná danému
Názvosloví Kvalita Výroba Kondenzace Teplosměnná plocha Názvosloví páry Pro správné pochopení funkce parních systémů musíme znát základní pojmy spojené s párou. Entalpie Celková energie, příslušná danému
Termika. Nauka o teple se zabývá měřením teploty, tepla a tepelnými ději.
 Termika Nauka o teple se zabývá měřením teploty, tepla a tepelnými ději. 1. Vnitřní energie Brownův pohyb a difúze látek prokazují, že částice látek jsou v neustálém neuspořádaném pohybu. Proto mají kinetickou
Termika Nauka o teple se zabývá měřením teploty, tepla a tepelnými ději. 1. Vnitřní energie Brownův pohyb a difúze látek prokazují, že částice látek jsou v neustálém neuspořádaném pohybu. Proto mají kinetickou
ZMĚNY SKUPENSTVÍ LÁTEK ČÁST 01
 ZMĚNY SKUPENSTVÍ LÁTEK ČÁST 01 A) Výklad: Změny skupenství látky Látka se může vyskytovat ve třech různých skupenstvích PEVNÉM, KAPALNÉM nebo PLYNNÉM. Např. voda (H 2 O)- může se vyskytovat jako krystalický
ZMĚNY SKUPENSTVÍ LÁTEK ČÁST 01 A) Výklad: Změny skupenství látky Látka se může vyskytovat ve třech různých skupenstvích PEVNÉM, KAPALNÉM nebo PLYNNÉM. Např. voda (H 2 O)- může se vyskytovat jako krystalický
12. Termomechanika par, Clausiova-Clapeyronova rovnice, parní tabulky, základni termodynamické děje v oblasti par
 1/18 12. Termomechanika par, Clausiova-Clapeyronova rovnice, parní tabulky, základni termodynamické děje v oblasti par Příklad: 12.1, 12.2, 12.3, 12.4, 12.5, 12.6, 12.7, 12.8, 12.9, 12.10, 12.11, 12.12,
1/18 12. Termomechanika par, Clausiova-Clapeyronova rovnice, parní tabulky, základni termodynamické děje v oblasti par Příklad: 12.1, 12.2, 12.3, 12.4, 12.5, 12.6, 12.7, 12.8, 12.9, 12.10, 12.11, 12.12,
Základní poznatky. Teplota Vnitřní energie soustavy Teplo
 Molekulová fyzika a termika Základní poznatky Základní poznatky Teplota Vnitřní energie soustavy Teplo Termika = část fyziky zabývající se studiem vlastností látek a jejich změn souvisejících s teplotou
Molekulová fyzika a termika Základní poznatky Základní poznatky Teplota Vnitřní energie soustavy Teplo Termika = část fyziky zabývající se studiem vlastností látek a jejich změn souvisejících s teplotou
VNITŘNÍ ENERGIE. Mgr. Jan Ptáčník - GJVJ - Fyzika - 2. ročník - Termika
 VNITŘNÍ ENERGIE Mgr. Jan Ptáčník - GJVJ - Fyzika - 2. ročník - Termika Zákon zachování energie Ze zákona zachování mechanické energie platí: Ek + Ep = konst. Ale: Vnitřní energie tělesa Každé těleso má
VNITŘNÍ ENERGIE Mgr. Jan Ptáčník - GJVJ - Fyzika - 2. ročník - Termika Zákon zachování energie Ze zákona zachování mechanické energie platí: Ek + Ep = konst. Ale: Vnitřní energie tělesa Každé těleso má
Základní škola národního umělce Petra Bezruče, Frýdek-Místek, tř. T. G. Masaryka 454. Název DUM: Teplo v příkladech I
 Základní škola národního umělce Petra Bezruče, Frýdek-Místek, tř. T. G. Masaryka 454 Zpracováno v rámci OP VK - EU peníze školám Jednička ve vzdělávání CZ.1.07/1.4.00/21.2759 Název DUM: Teplo v příkladech
Základní škola národního umělce Petra Bezruče, Frýdek-Místek, tř. T. G. Masaryka 454 Zpracováno v rámci OP VK - EU peníze školám Jednička ve vzdělávání CZ.1.07/1.4.00/21.2759 Název DUM: Teplo v příkladech
Ch - Rozlišování látek
 Ch - Rozlišování látek Autor: Mgr. Jaromír JUŘEK Kopírování a jakékoliv další využití výukového materiálu je povoleno pouze s uvedením odkazu na www.jarjurek.cz. VARIACE 1 Tento dokument byl kompletně
Ch - Rozlišování látek Autor: Mgr. Jaromír JUŘEK Kopírování a jakékoliv další využití výukového materiálu je povoleno pouze s uvedením odkazu na www.jarjurek.cz. VARIACE 1 Tento dokument byl kompletně
Mol. fyz. a termodynamika
 Molekulová fyzika pracuje na základě kinetické teorie látek a statistiky Termodynamika zkoumání tepelných jevů a strojů nezajímají nás jednotlivé částice Molekulová fyzika základem jsou: Látka kteréhokoli
Molekulová fyzika pracuje na základě kinetické teorie látek a statistiky Termodynamika zkoumání tepelných jevů a strojů nezajímají nás jednotlivé částice Molekulová fyzika základem jsou: Látka kteréhokoli
Příklady k zápočtu molekulová fyzika a termodynamika
 Příklady k zápočtu molekulová fyzika a termodynamika 1. Do vody o teplotě t 1 70 C a hmotnosti m 1 1 kg vhodíme kostku ledu o teplotě t 2 10 C a hmotnosti m 2 2 kg. Do soustavy vzápětí přilijeme další
Příklady k zápočtu molekulová fyzika a termodynamika 1. Do vody o teplotě t 1 70 C a hmotnosti m 1 1 kg vhodíme kostku ledu o teplotě t 2 10 C a hmotnosti m 2 2 kg. Do soustavy vzápětí přilijeme další
Vnitřní energie, práce a teplo
 Vnitřní energie, práce a teplo Míček upustíme z výšky na podlahu o Míček padá zvětšuje se, zmenšuje se. Celková mechanická energie se - o Míček se od země odrazí a stoupá vzhůru zvětšuje se, zmenšuje se.
Vnitřní energie, práce a teplo Míček upustíme z výšky na podlahu o Míček padá zvětšuje se, zmenšuje se. Celková mechanická energie se - o Míček se od země odrazí a stoupá vzhůru zvětšuje se, zmenšuje se.
Doprovodné otázky pro studenty, kvízy, úkoly aj.
 Doprovodné otázky pro studenty, kvízy, úkoly aj. Otázky: 1. Jak se projeví menší hustota ledu v porovnání s vodou při zamrzání vodních nádrží a toků? 2. Jaký jev se nazývá anomálie vody? 3. Vysvětlete
Doprovodné otázky pro studenty, kvízy, úkoly aj. Otázky: 1. Jak se projeví menší hustota ledu v porovnání s vodou při zamrzání vodních nádrží a toků? 2. Jaký jev se nazývá anomálie vody? 3. Vysvětlete
TÉMA: Molekulová fyzika a tepelné děje v plynech VNITŘNÍ ENERGIE TĚLESA
 U.. vnitřní energie tělesa ( termodynamické soustavy) je celková kinetická energie neuspořádaně se pohybujících částic tělesa ( molekul, atomů, iontů) a celková potenciální energie vzájemné polohy těchto
U.. vnitřní energie tělesa ( termodynamické soustavy) je celková kinetická energie neuspořádaně se pohybujících částic tělesa ( molekul, atomů, iontů) a celková potenciální energie vzájemné polohy těchto
V izolované soustavě nedochází k výměně tepla s okolím. Dokonalá izolovaná soustava neexistuje, nejvíce se jí blíží kalorimetr nebo termoska.
 Teplo a vnitřní energie pracovní list Vnitřní energie Všechny tělesa se skládají z částic, které vykonávají neustálý a neuspořádaný pohyb a které na sebe navzájem silově působí. Částice uvnitř všech těles
Teplo a vnitřní energie pracovní list Vnitřní energie Všechny tělesa se skládají z částic, které vykonávají neustálý a neuspořádaný pohyb a které na sebe navzájem silově působí. Částice uvnitř všech těles
ZÁKLADNÍ ŠKOLA KOLÍN II., KMOCHOVA 943 škola s rozšířenou výukou matematiky a přírodovědných předmětů
 ZÁKLADNÍ ŠKOLA KOLÍN II., KMOCHOVA 943 škola s rozšířenou výukou matematiky a přírodovědných předmětů Autor Číslo materiálu Mgr. Vladimír Hradecký 8_F_1_13 Datum vytvoření 2. 11. 2011 Druh učebního materiálu
ZÁKLADNÍ ŠKOLA KOLÍN II., KMOCHOVA 943 škola s rozšířenou výukou matematiky a přírodovědných předmětů Autor Číslo materiálu Mgr. Vladimír Hradecký 8_F_1_13 Datum vytvoření 2. 11. 2011 Druh učebního materiálu
1/ Vlhký vzduch
 1/5 16. Vlhký vzduch Příklad: 16.1, 16.2, 16.3, 16.4, 16.5, 16.6, 16.7, 16.8, 16.9, 16.10, 16.11, 16.12, 16.13, 16.14, 16.15, 16.16, 16.17, 16.18, 16.19, 16.20, 16.21, 16.22, 16.23 Příklad 16.1 Teplota
1/5 16. Vlhký vzduch Příklad: 16.1, 16.2, 16.3, 16.4, 16.5, 16.6, 16.7, 16.8, 16.9, 16.10, 16.11, 16.12, 16.13, 16.14, 16.15, 16.16, 16.17, 16.18, 16.19, 16.20, 16.21, 16.22, 16.23 Příklad 16.1 Teplota
Termodynamika 1. UJOP Hostivař 2014
 Termodynamika 1 UJOP Hostivař 2014 Termodynamika Zabývá se tepelnými ději obecně. Existují 3 termodynamické zákony: 1. Celkové množství energie (všech druhů) izolované soustavy zůstává zachováno. 2. Teplo
Termodynamika 1 UJOP Hostivař 2014 Termodynamika Zabývá se tepelnými ději obecně. Existují 3 termodynamické zákony: 1. Celkové množství energie (všech druhů) izolované soustavy zůstává zachováno. 2. Teplo
T0 Teplo a jeho měření
 Teplo a jeho měření 1 Teplo 2 Kalorimetrie Kalorimetr 3 Tepelná kapacita 3.1 Měrná tepelná kapacita Měrná tepelná kapacita při stálém objemu a stálém tlaku Poměr měrných tepelných kapacit 3.2 Molární tepelná
Teplo a jeho měření 1 Teplo 2 Kalorimetrie Kalorimetr 3 Tepelná kapacita 3.1 Měrná tepelná kapacita Měrná tepelná kapacita při stálém objemu a stálém tlaku Poměr měrných tepelných kapacit 3.2 Molární tepelná
V izolované soustavě nedochází k výměně tepla s okolím. Dokonalá izolovaná soustava neexistuje, nejvíce se jí blíží kalorimetr nebo termoska.
 Teplo a vnitřní energie pracovní list Vnitřní energie Všechny tělesa se skládají z částic, které vykonávají neustálý a neuspořádaný pohyb a které na sebe navzájem silově působí. Částice uvnitř všech těles
Teplo a vnitřní energie pracovní list Vnitřní energie Všechny tělesa se skládají z částic, které vykonávají neustálý a neuspořádaný pohyb a které na sebe navzájem silově působí. Částice uvnitř všech těles
1/6. 2. Stavová rovnice, plynová konstanta, Avogadrův zákon, kilomol plynu
 1/6 2. Stavová rovnice, plynová konstanta, Avogadrův zákon, kilomol plynu Příklad: 2.1, 2.2, 2.3, 2.4, 2.5, 2.6, 2.7, 2.8, 2.9, 2.10, 2.11, 2.12, 2.13, 2.14, 2.15, 2.16, 2.17, 2.18, 2.19, 2.20, 2.21, 2.22,
1/6 2. Stavová rovnice, plynová konstanta, Avogadrův zákon, kilomol plynu Příklad: 2.1, 2.2, 2.3, 2.4, 2.5, 2.6, 2.7, 2.8, 2.9, 2.10, 2.11, 2.12, 2.13, 2.14, 2.15, 2.16, 2.17, 2.18, 2.19, 2.20, 2.21, 2.22,
2.6.4 Kapalnění, sublimace, desublimace
 264 Kapalnění, sublimace, desublimace Předpoklady: 2603 Kapalnění (kondenzace) Snižování eploy páry pára se mění v kapalinu Kde dochází ke kondenzaci? na povrchu kapaliny, na povrchu pevné láky (orosení
264 Kapalnění, sublimace, desublimace Předpoklady: 2603 Kapalnění (kondenzace) Snižování eploy páry pára se mění v kapalinu Kde dochází ke kondenzaci? na povrchu kapaliny, na povrchu pevné láky (orosení
EU peníze středním školám digitální učební materiál
 EU peníze středním školám digitální učební materiál Číslo projektu: Číslo a název šablony klíčové aktivity: Tematická oblast, název DUMu: Autor: CZ.1.07/1.5.00/34.0515 III/2 Inovace a zkvalitnění výuky
EU peníze středním školám digitální učební materiál Číslo projektu: Číslo a název šablony klíčové aktivity: Tematická oblast, název DUMu: Autor: CZ.1.07/1.5.00/34.0515 III/2 Inovace a zkvalitnění výuky
Ideální plyn. Stavová rovnice Děje v ideálním plynu Práce plynu, Kruhový děj, Tepelné motory
 Struktura a vlastnosti plynů Ideální plyn Vlastnosti ideálního plynu: Ideální plyn Stavová rovnice Děje v ideálním plynu Práce plynu, Kruhový děj, epelné motory rozměry molekul jsou ve srovnání se střední
Struktura a vlastnosti plynů Ideální plyn Vlastnosti ideálního plynu: Ideální plyn Stavová rovnice Děje v ideálním plynu Práce plynu, Kruhový děj, epelné motory rozměry molekul jsou ve srovnání se střední
Vnitřní energie, práce, teplo.
 Vnitřní energie, práce, teplo. Vnitřní energie tělesa Částice uvnitř látek mají kinetickou a potenciální energii. Je to energie uvnitř tělesa, proto ji nazýváme vnitřní energie. Značíme ji písmenkem U
Vnitřní energie, práce, teplo. Vnitřní energie tělesa Částice uvnitř látek mají kinetickou a potenciální energii. Je to energie uvnitř tělesa, proto ji nazýváme vnitřní energie. Značíme ji písmenkem U
Termodynamika. T [K ]=t [ 0 C] 273,15 T [ K ]= t [ 0 C] termodynamická teplota: Stavy hmoty. jednotka: 1 K (kelvin) = 1/273,16 část termodynamické
![Termodynamika. T [K ]=t [ 0 C] 273,15 T [ K ]= t [ 0 C] termodynamická teplota: Stavy hmoty. jednotka: 1 K (kelvin) = 1/273,16 část termodynamické Termodynamika. T [K ]=t [ 0 C] 273,15 T [ K ]= t [ 0 C] termodynamická teplota: Stavy hmoty. jednotka: 1 K (kelvin) = 1/273,16 část termodynamické](/thumbs/24/2778201.jpg) Termodynamika termodynamická teplota: Stavy hmoty jednotka: 1 K (kelvin) = 1/273,16 část termodynamické teploty trojného bodu vody (273,16 K = 0,01 o C). 0 o C = 273,15 K T [K ]=t [ 0 C] 273,15 T [ K ]=
Termodynamika termodynamická teplota: Stavy hmoty jednotka: 1 K (kelvin) = 1/273,16 část termodynamické teploty trojného bodu vody (273,16 K = 0,01 o C). 0 o C = 273,15 K T [K ]=t [ 0 C] 273,15 T [ K ]=
SBÍRKA ŘEŠENÝCH FYZIKÁLNÍCH ÚLOH
 SBÍRKA ŘEŠENÝCH FYZIKÁLNÍCH ÚLOH MECHANIKA MOLEKULOVÁ FYZIKA A TERMIKA ELEKTŘINA A MAGNETISMUS KMITÁNÍ A VLNĚNÍ OPTIKA FYZIKA MIKROSVĚTA TERMODYNAMICKÁ TEPLOTNÍ STUPNICE, TEPLOTA 1) Převeďte hodnoty v
SBÍRKA ŘEŠENÝCH FYZIKÁLNÍCH ÚLOH MECHANIKA MOLEKULOVÁ FYZIKA A TERMIKA ELEKTŘINA A MAGNETISMUS KMITÁNÍ A VLNĚNÍ OPTIKA FYZIKA MIKROSVĚTA TERMODYNAMICKÁ TEPLOTNÍ STUPNICE, TEPLOTA 1) Převeďte hodnoty v
Tepelná vodivost. střední rychlost. T 1 > T 2 z. teplo přenesené za čas dt: T 1 T 2. tepelný tok střední volná dráha. součinitel tepelné vodivosti
 Tepelná vodivost teplo přenesené za čas dt: T 1 > T z T 1 S tepelný tok střední volná dráha T součinitel tepelné vodivosti střední rychlost Tepelná vodivost součinitel tepelné vodivosti při T = 300 K součinitel
Tepelná vodivost teplo přenesené za čas dt: T 1 > T z T 1 S tepelný tok střední volná dráha T součinitel tepelné vodivosti střední rychlost Tepelná vodivost součinitel tepelné vodivosti při T = 300 K součinitel
Pomůcky, které poskytuje sbírka fyziky, a audiovizuální technika v učebně fyziky, interaktivní tabule a i-učebnice
 Předmět: Náplň: Třída: Počet hodin: Pomůcky: Fyzika (FYZ) Práce a energie, tepelné jevy, elektrický proud, zvukové jevy Tercie 1+1 hodina týdně Pomůcky, které poskytuje sbírka fyziky, a audiovizuální technika
Předmět: Náplň: Třída: Počet hodin: Pomůcky: Fyzika (FYZ) Práce a energie, tepelné jevy, elektrický proud, zvukové jevy Tercie 1+1 hodina týdně Pomůcky, které poskytuje sbírka fyziky, a audiovizuální technika
EU PENÍZE ŠKOLÁM Operační program Vzdělávání pro konkurenceschopnost
 ZÁKLADNÍ ŠKOLA OLOMOUC příspěvková organizace MOZARTOVA 48, 779 00 OLOMOUC tel.: 585 427 142, 775 116 442; fax: 585 422 713 e-mail: kundrum@centrum.cz; www.zs-mozartova.cz Projekt: ŠKOLA RADOSTI, ŠKOLA
ZÁKLADNÍ ŠKOLA OLOMOUC příspěvková organizace MOZARTOVA 48, 779 00 OLOMOUC tel.: 585 427 142, 775 116 442; fax: 585 422 713 e-mail: kundrum@centrum.cz; www.zs-mozartova.cz Projekt: ŠKOLA RADOSTI, ŠKOLA
2_ Práce _ Slovní úlohy: _ Práce a kladky _ Výkon _ Výkon - příklady _ PL: MECHANICKÁ PRÁCE A VÝKON...
 2_ Práce... 2 3. - 4._ Slovní úlohy:... 3 5_ Práce a kladky... 4 6._ Výkon... 5 7_ Výkon - příklady... 6 8_ PL: MECHANICKÁ PRÁCE A VÝKON... 7 9_ Výpočet práce z výkonu a času:... 8 10_ Energie... 9 Energie
2_ Práce... 2 3. - 4._ Slovní úlohy:... 3 5_ Práce a kladky... 4 6._ Výkon... 5 7_ Výkon - příklady... 6 8_ PL: MECHANICKÁ PRÁCE A VÝKON... 7 9_ Výpočet práce z výkonu a času:... 8 10_ Energie... 9 Energie
Fyzikální vzdělávání. 1. ročník. Učební obor: Kuchař číšník Kadeřník. Implementace ICT do výuky č. CZ.1.07/1.1.02/02.0012 GG OP VK
 Fyzikální vzdělávání 1. ročník Učební obor: Kuchař číšník Kadeřník 1 2 Termika 2.1Teplota, teplotní roztažnost látek 2.2 Teplo a práce, přeměny vnitřní energie tělesa 2.3 Tepelné motory 2.4 Struktura pevných
Fyzikální vzdělávání 1. ročník Učební obor: Kuchař číšník Kadeřník 1 2 Termika 2.1Teplota, teplotní roztažnost látek 2.2 Teplo a práce, přeměny vnitřní energie tělesa 2.3 Tepelné motory 2.4 Struktura pevných
5.7 Vlhkost vzduchu 5.7.5 Absolutní vlhkost 5.7.6 Poměrná vlhkost 5.7.7 Rosný bod 5.7.8 Složení vzduchu 5.7.9 Měření vlhkosti vzduchu
 Fázové přechody 5.6.5 Fáze Fázové rozhraní 5.6.6 Gibbsovo pravidlo fází 5.6.7 Fázový přechod Fázový přechod prvního druhu Fázový přechod druhého druhu 5.6.7.1 Clausiova-Clapeyronova rovnice 5.6.8 Skupenství
Fázové přechody 5.6.5 Fáze Fázové rozhraní 5.6.6 Gibbsovo pravidlo fází 5.6.7 Fázový přechod Fázový přechod prvního druhu Fázový přechod druhého druhu 5.6.7.1 Clausiova-Clapeyronova rovnice 5.6.8 Skupenství
Změna skupenství, Tání a tuhnutí, Sublimace a desublimace Vypařování a kapalnění Sytá pára, Fázový diagram, Vodní pára
 Zěny skupenství átek Zěna skupenství, Tání a tuhnutí, Subiace a desubiace Vypařování a kapanění Sytá pára, Fázový diagra, Vodní pára Zěna skupenství = fyzikání děj, při které se ění skupenství átky Skupenství
Zěny skupenství átek Zěna skupenství, Tání a tuhnutí, Subiace a desubiace Vypařování a kapanění Sytá pára, Fázový diagra, Vodní pára Zěna skupenství = fyzikání děj, při které se ění skupenství átky Skupenství
Změna skupenství - přehled Převzato z materiálů ZŠ Ondřejov - http://www.zsondrejov.cz/vyuka/
 Změna skupenství - přehled Převzato z materiálů ZŠ Ondřejov - http://www.zsondrejov.cz/vyuka/ Skupenství látek Látky se vyskytují ve třech skupenstvích pevné, kapalné, plynné. Základní vlastnosti látek
Změna skupenství - přehled Převzato z materiálů ZŠ Ondřejov - http://www.zsondrejov.cz/vyuka/ Skupenství látek Látky se vyskytují ve třech skupenstvích pevné, kapalné, plynné. Základní vlastnosti látek
h nadmořská výška [m]
![h nadmořská výška [m] h nadmořská výška [m]](/thumbs/92/109475205.jpg) Katedra prostředí staveb a TZB KLIMATIZACE, VĚTRÁNÍ Cvičení pro navazující magisterské studium studijního oboru Prostředí staveb Cvičení č. 1 Zpracoval: Ing. Zdeněk GALDA Nové výukové moduly vznikly za
Katedra prostředí staveb a TZB KLIMATIZACE, VĚTRÁNÍ Cvičení pro navazující magisterské studium studijního oboru Prostředí staveb Cvičení č. 1 Zpracoval: Ing. Zdeněk GALDA Nové výukové moduly vznikly za
Test vlastnosti látek a periodická tabulka
 DUM Základy přírodních věd DUM III/2-T3-2-08 Téma: Test vlastnosti látek a periodická tabulka Střední škola Rok: 2012 2013 Varianta: A Zpracoval: Mgr. Pavel Hrubý Mgr. Josef Kormaník TEST Test vlastnosti
DUM Základy přírodních věd DUM III/2-T3-2-08 Téma: Test vlastnosti látek a periodická tabulka Střední škola Rok: 2012 2013 Varianta: A Zpracoval: Mgr. Pavel Hrubý Mgr. Josef Kormaník TEST Test vlastnosti
Laboratorní práce č. 2: Určení měrné tepelné kapacity látky
 Přírodní vědy moderně a interaktivně FYZIKA 4. ročník šestiletého a 2. ročník čtyřletého studia Laboratorní práce č. 2: Určení měrné tepelné kapacity látky Přírodní vědy moderně a interaktivně FYZIKA
Přírodní vědy moderně a interaktivně FYZIKA 4. ročník šestiletého a 2. ročník čtyřletého studia Laboratorní práce č. 2: Určení měrné tepelné kapacity látky Přírodní vědy moderně a interaktivně FYZIKA
4IS09F8 změna skupenství.notebook. Registrační číslo projektu: CZ.1.07/1.4.00/21.3075. Šablona: III/2. Sada: VY_32_INOVACE_4IS Pořadové číslo: 09
 Registrační číslo projektu: CZ.1.07/1.4.00/21.3075 Šablona: III/2 Sada: VY_32_INOVACE_4IS Pořadové číslo: 09 Ověření ve výuce Třída: 8.A Datum: 20.2.2013 1 Změna skupenství Předmět: Fyzika Ročník: 8. ročník
Registrační číslo projektu: CZ.1.07/1.4.00/21.3075 Šablona: III/2 Sada: VY_32_INOVACE_4IS Pořadové číslo: 09 Ověření ve výuce Třída: 8.A Datum: 20.2.2013 1 Změna skupenství Předmět: Fyzika Ročník: 8. ročník
Pomůcky, které poskytuje sbírka fyziky, a audiovizuální technika v učebně fyziky, interaktivní tabule
 Předmět: Náplň: Třída: Počet hodin: Pomůcky: Fyzika (FYZ) Práce a energie, tepelné jevy, elektrický proud, zvukové jevy Tercie 1+1 hodina týdně Pomůcky, které poskytuje sbírka fyziky, a audiovizuální technika
Předmět: Náplň: Třída: Počet hodin: Pomůcky: Fyzika (FYZ) Práce a energie, tepelné jevy, elektrický proud, zvukové jevy Tercie 1+1 hodina týdně Pomůcky, které poskytuje sbírka fyziky, a audiovizuální technika
Termika termika - teplota, teplo a práce termodynamické zákony tepelná vodivost - tepelná kapacita skupenské teplo
 Termika termika - teplota, teplo a práce termodynamické zákony tepelná vodivost - tepelná kapacita skupenské teplo teplo, teplota, práce, tepelná vodivost Teplo část vnitřní energie tělesa = součet kinetické
Termika termika - teplota, teplo a práce termodynamické zákony tepelná vodivost - tepelná kapacita skupenské teplo teplo, teplota, práce, tepelná vodivost Teplo část vnitřní energie tělesa = součet kinetické
Vnitřní energie. Teplo. Tepelná výměna.
 Vnitřní energie. Teplo. Tepelná výměna. A) Výklad: Vnitřní energie vnitřní energie označuje součet celkové kinetické energie částic (tj. rotační + vibrační + translační energie) a celkové polohové energie
Vnitřní energie. Teplo. Tepelná výměna. A) Výklad: Vnitřní energie vnitřní energie označuje součet celkové kinetické energie částic (tj. rotační + vibrační + translační energie) a celkové polohové energie
2_ Mechanická práce _Slovní úlohy _ Práce a kladky _ Výkon _ Výkon - příklady _ PL: MECHANICKÁ PRÁCE A VÝKON...
 2_ Mechanická práce... 2 3.- 4._Slovní úlohy... 2 5_ Práce a kladky... 4 6._ Výkon... 4 7_ Výkon - příklady... 5 8_ PL: MECHANICKÁ PRÁCE A VÝKON... 6 9_ Výpočet práce z výkonu a času:... 7 10_ Energie...
2_ Mechanická práce... 2 3.- 4._Slovní úlohy... 2 5_ Práce a kladky... 4 6._ Výkon... 4 7_ Výkon - příklady... 5 8_ PL: MECHANICKÁ PRÁCE A VÝKON... 6 9_ Výpočet práce z výkonu a času:... 7 10_ Energie...
KLIMATIZACE A PRŮMYSLOVÁ VZDUCHOTECHNIKA VYBRANÉ PŘÍKLADY KE CVIČENÍ I.
 KLIMATIZACE A PRŮMYSLOVÁ VZDUCHOTECHNIKA VYBRANÉ PŘÍKLADY KE CVIČENÍ I. Ing. Jan Schwarzer, Ph.D.. Praha 2011 Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti 1 Obsah 1 Obsah... 2 2 Označení...3
KLIMATIZACE A PRŮMYSLOVÁ VZDUCHOTECHNIKA VYBRANÉ PŘÍKLADY KE CVIČENÍ I. Ing. Jan Schwarzer, Ph.D.. Praha 2011 Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti 1 Obsah 1 Obsah... 2 2 Označení...3
II. VNITŘNÍ ENERGIE, PRÁCE A TEPLO
 II. VNITŘNÍ ENERGIE, PRÁCE A TEPLO 2.1 Vnitřní energie tělesa a) celková energie (termodynamické) soustavy E tvořena kinetickou energií E k jejího makroskopického pohybu jako celku potenciální energií
II. VNITŘNÍ ENERGIE, PRÁCE A TEPLO 2.1 Vnitřní energie tělesa a) celková energie (termodynamické) soustavy E tvořena kinetickou energií E k jejího makroskopického pohybu jako celku potenciální energií
Půdní voda. *vyplňuje póry v půdách. *nevytváří souvislou hladinu. *je důležitá pro růst rostlin.
 PODPOVRCHOVÁ VODA Půdní voda *vyplňuje póry v půdách. *nevytváří souvislou hladinu. *je důležitá pro růst rostlin. Podzemní voda hromadí se na horninách, které jsou málo propustné pro vodu vytváří souvislou
PODPOVRCHOVÁ VODA Půdní voda *vyplňuje póry v půdách. *nevytváří souvislou hladinu. *je důležitá pro růst rostlin. Podzemní voda hromadí se na horninách, které jsou málo propustné pro vodu vytváří souvislou
MOLEKULOVÁ FYZIKA A TERMODYNAMIKA
 MOLEKULOVÁ FYZIKA A TERMODYNAMIKA 2 metody zkoumání látek na základě vnějších projevů: I. KINETICKÁ TEORIE LÁTEK -studium vlastností látek na základě vnitřní struktury, pohybu a vzájemného působení jednotlivých
MOLEKULOVÁ FYZIKA A TERMODYNAMIKA 2 metody zkoumání látek na základě vnějších projevů: I. KINETICKÁ TEORIE LÁTEK -studium vlastností látek na základě vnitřní struktury, pohybu a vzájemného působení jednotlivých
Fyzika je přírodní věda, která zkoumá a popisuje zákonitosti přírodních jevů.
 Fyzika je přírodní věda, která zkoumá a popisuje zákonitosti přírodních jevů. Násobky jednotek název značka hodnota kilo k 1000 mega M 1000000 giga G 1000000000 tera T 1000000000000 Tělesa a látky Tělesa
Fyzika je přírodní věda, která zkoumá a popisuje zákonitosti přírodních jevů. Násobky jednotek název značka hodnota kilo k 1000 mega M 1000000 giga G 1000000000 tera T 1000000000000 Tělesa a látky Tělesa
Vnitřní energie, teplo, změny skupenství Pracovní listy pro samostatnou práci
 Vnitřní energie, teplo, změny skupenství Pracovní listy pro samostatnou práci Oblast: Člověk a příroda Předmět: Fyzika Tematický okruh: Tělesa, látky a síla Ročník: 8. Klíčová slova: změny skupenství,
Vnitřní energie, teplo, změny skupenství Pracovní listy pro samostatnou práci Oblast: Člověk a příroda Předmět: Fyzika Tematický okruh: Tělesa, látky a síla Ročník: 8. Klíčová slova: změny skupenství,
Kalorimetrická rovnice
 Kalorimetrická rovnice Kalorimetr je zařízení umožňující pokusně provádět tepelnou výměnu mezi tělesy a měřit potřebné tepelné veličiny skládá se ze dvou nádobek do sebe vložených mezi stěnami nádobek
Kalorimetrická rovnice Kalorimetr je zařízení umožňující pokusně provádět tepelnou výměnu mezi tělesy a měřit potřebné tepelné veličiny skládá se ze dvou nádobek do sebe vložených mezi stěnami nádobek
Cvičení z termomechaniky Cvičení 2. Stanovte objem nádoby, ve které je uzavřený dusík o hmotnosti 20 [kg], teplotě 15 [ C] a tlaku 10 [MPa].
![Cvičení z termomechaniky Cvičení 2. Stanovte objem nádoby, ve které je uzavřený dusík o hmotnosti 20 [kg], teplotě 15 [ C] a tlaku 10 [MPa]. Cvičení z termomechaniky Cvičení 2. Stanovte objem nádoby, ve které je uzavřený dusík o hmotnosti 20 [kg], teplotě 15 [ C] a tlaku 10 [MPa].](/thumbs/25/6795424.jpg) Příklad 1 Stanovte objem nádoby, ve které je uzavřený dusík o hmotnosti 20 [kg], teplotě 15 [ C] a tlaku 10 [MPa]. m 20[kg], t 15 [ C] 288.15 [K], p 10 [MPa] 10.10 6 [Pa], R 8314 [J. kmol 1. K 1 ] 8,314
Příklad 1 Stanovte objem nádoby, ve které je uzavřený dusík o hmotnosti 20 [kg], teplotě 15 [ C] a tlaku 10 [MPa]. m 20[kg], t 15 [ C] 288.15 [K], p 10 [MPa] 10.10 6 [Pa], R 8314 [J. kmol 1. K 1 ] 8,314
3 pokusy z termiky. Vojtěch Jelen Fyzikální seminář LS 2014
 3 pokusy z termiky Vojtěch Jelen Fyzikální seminář LS 2014 Obsah 1. Pokus online 2. Měření teploty cihly 3. Vypařování střely 1. Kalorimetrie Zabývá se měřením tepla a studuje vlastnosti látek a jejich
3 pokusy z termiky Vojtěch Jelen Fyzikální seminář LS 2014 Obsah 1. Pokus online 2. Měření teploty cihly 3. Vypařování střely 1. Kalorimetrie Zabývá se měřením tepla a studuje vlastnosti látek a jejich
Stanovení měrného tepla pevných látek
 61 Kapitola 10 Stanovení měrného tepla pevných látek 10.1 Úvod O teple se dá říci, že souvisí s energií neuspořádaného pohybu molekul. Úhrnná pohybová energie neuspořádaného pohybu molekul, pohybu postupného,
61 Kapitola 10 Stanovení měrného tepla pevných látek 10.1 Úvod O teple se dá říci, že souvisí s energií neuspořádaného pohybu molekul. Úhrnná pohybová energie neuspořádaného pohybu molekul, pohybu postupného,
FAKULTA STAVEBNÍ VUT V BRNĚ PŘIJÍMACÍ ŘÍZENÍ PRO AKADEMICKÝ ROK 2006 2007
 TEST Z FYZIKY PRO PŘIJÍMACÍ ZKOUŠKY ČÍSLO FAST-F-2006-01 1. Převeďte 37 mm 3 na m 3. a) 37 10-9 m 3 b) 37 10-6 m 3 c) 37 10 9 m 3 d) 37 10 3 m 3 e) 37 10-3 m 3 2. Voda v řece proudí rychlostí 4 m/s. Kolmo
TEST Z FYZIKY PRO PŘIJÍMACÍ ZKOUŠKY ČÍSLO FAST-F-2006-01 1. Převeďte 37 mm 3 na m 3. a) 37 10-9 m 3 b) 37 10-6 m 3 c) 37 10 9 m 3 d) 37 10 3 m 3 e) 37 10-3 m 3 2. Voda v řece proudí rychlostí 4 m/s. Kolmo
Výukový materiál zpracován v rámci projektu EU peníze školám
 Výukový materiál zpracován v rámci projektu EU peníze školám Registrační číslo projektu: CZ.1.07/1.5.00/34.0996 Šablona: III/2 č. materiálu: VY_32_INOVACE_374 Jméno autora: Třída/ročník: Mgr. Alena Krejčíková
Výukový materiál zpracován v rámci projektu EU peníze školám Registrační číslo projektu: CZ.1.07/1.5.00/34.0996 Šablona: III/2 č. materiálu: VY_32_INOVACE_374 Jméno autora: Třída/ročník: Mgr. Alena Krejčíková
UČIVO. Termodynamická teplota. První termodynamický zákon Přenos vnitřní energie
 PŘEDMĚT: FYZIKA ROČNÍK: SEXTA VÝSTUP UČIVO MEZIPŘEDM. VZTAHY, PRŮŘEZOVÁ TÉMATA, PROJEKTY, KURZY POZNÁMKY Zná 3 základní poznatky kinetické teorie látek a vysvětlí jejich praktický význam Vysvětlí pojmy
PŘEDMĚT: FYZIKA ROČNÍK: SEXTA VÝSTUP UČIVO MEZIPŘEDM. VZTAHY, PRŮŘEZOVÁ TÉMATA, PROJEKTY, KURZY POZNÁMKY Zná 3 základní poznatky kinetické teorie látek a vysvětlí jejich praktický význam Vysvětlí pojmy
PROCESY V TECHNICE BUDOV 8
 UNIVERZITA TOMÁŠE BATI VE ZLÍNĚ FAKULTA APLIKOVANÉ INFORMATIKY PROCESY V TECHNICE BUDOV 8 Dagmar Janáčová, Hana Charvátová Zlín 2013 Tento studijní materiál vznikl za finanční podpory Evropského sociálního
UNIVERZITA TOMÁŠE BATI VE ZLÍNĚ FAKULTA APLIKOVANÉ INFORMATIKY PROCESY V TECHNICE BUDOV 8 Dagmar Janáčová, Hana Charvátová Zlín 2013 Tento studijní materiál vznikl za finanční podpory Evropského sociálního
F - Mechanika tuhého tělesa
 F - Mechanika tuhého tělesa Učební text pro studenty dálkového studia a shrnující text pro studenty denního studia. VARIACE 1 Tento dokument byl kompletně vytvořen, sestaven a vytištěn v programu dosystem
F - Mechanika tuhého tělesa Učební text pro studenty dálkového studia a shrnující text pro studenty denního studia. VARIACE 1 Tento dokument byl kompletně vytvořen, sestaven a vytištěn v programu dosystem
VÝUKOVÝ MATERIÁL Ing. Yvona Bečičková Tematická oblast. Termika Číslo a název materiálu VY_32_INOVACE_0301_0220 Anotace
 VÝUKOVÝ MATERIÁL Identifikační údaje školy Vyšší odborná škola a Střední škola, Varnsdorf, příspěvková organizace Bratislavská 2166, 407 47 Varnsdorf, IČO: 18383874 www.vosassvdf.cz, tel. +420412372632
VÝUKOVÝ MATERIÁL Identifikační údaje školy Vyšší odborná škola a Střední škola, Varnsdorf, příspěvková organizace Bratislavská 2166, 407 47 Varnsdorf, IČO: 18383874 www.vosassvdf.cz, tel. +420412372632
FYZIKA 6. ročník 2. část
 FYZIKA 6. ročník 2. část 23_Hmotnost tělesa... 2 24_Rovnoramenné váhy.... 3 25_Hustota... 4 26_Výpočet hustoty látky... 4 27_Výpočet hustoty látky příklady... 6 28_Výpočet hmotnosti tělesa příklady...
FYZIKA 6. ročník 2. část 23_Hmotnost tělesa... 2 24_Rovnoramenné váhy.... 3 25_Hustota... 4 26_Výpočet hustoty látky... 4 27_Výpočet hustoty látky příklady... 6 28_Výpočet hmotnosti tělesa příklady...
Vnitřní energie, práce a teplo
 Vnitřní energie, práce a teplo Zákon zachování mechanické energie V izolované soustavě těles je v každém okamžiku úhrnná mechanická energie stálá. Mění se navzájem jen potenciální energie E p a kinetická
Vnitřní energie, práce a teplo Zákon zachování mechanické energie V izolované soustavě těles je v každém okamžiku úhrnná mechanická energie stálá. Mění se navzájem jen potenciální energie E p a kinetická
Fyzika - Sexta, 2. ročník
 - Sexta, 2. ročník Fyzika Výchovné a vzdělávací strategie Kompetence komunikativní Kompetence k řešení problémů Kompetence sociální a personální Kompetence občanská Kompetence k podnikavosti Kompetence
- Sexta, 2. ročník Fyzika Výchovné a vzdělávací strategie Kompetence komunikativní Kompetence k řešení problémů Kompetence sociální a personální Kompetence občanská Kompetence k podnikavosti Kompetence
Fyzika. Pracovní list č. 5 Téma: Měření teploty, relativní vlhkosti, rosného bodu, absolutní vlhkosti. Mgr. Libor Lepík. Student a konkurenceschopnost
 www.projektsako.cz Fyzika Pracovní list č. 5 Téma: Měření teploty, relativní vlhkosti, rosného bodu, absolutní vlhkosti Lektor: Projekt: Reg. číslo: Mgr. Libor Lepík Student a konkurenceschopnost CZ.1.07/1.1.07/03.0075
www.projektsako.cz Fyzika Pracovní list č. 5 Téma: Měření teploty, relativní vlhkosti, rosného bodu, absolutní vlhkosti Lektor: Projekt: Reg. číslo: Mgr. Libor Lepík Student a konkurenceschopnost CZ.1.07/1.1.07/03.0075
Termomechanika cvičení
 KATEDRA ENERGETICKÝCH STROJŮ A ZAŘÍZENÍ Termomechanika cvičení 1. cvičení Ing. Michal Volf / 18.02.2019 Informace o cvičení Ing. Michal Volf Email: volfm@kke.zcu.cz Konzultace: po vzájemné dohodě prezentace
KATEDRA ENERGETICKÝCH STROJŮ A ZAŘÍZENÍ Termomechanika cvičení 1. cvičení Ing. Michal Volf / 18.02.2019 Informace o cvičení Ing. Michal Volf Email: volfm@kke.zcu.cz Konzultace: po vzájemné dohodě prezentace
STRUKTURA PEVNÝCH LÁTEK A KAPALIN
 STRUKTURA PEVNÝCH LÁTEK A KAPALIN 10. VLHKOST VZDUCHU Autor: Ing. Eva Jančová DESS SOŠ a SOU spol. s r. o. VLHKOST VZDUCHU - Vlhkost je základní vlastnost vzduchu. - Vlhkost vzduchu udává, jaké množství
STRUKTURA PEVNÝCH LÁTEK A KAPALIN 10. VLHKOST VZDUCHU Autor: Ing. Eva Jančová DESS SOŠ a SOU spol. s r. o. VLHKOST VZDUCHU - Vlhkost je základní vlastnost vzduchu. - Vlhkost vzduchu udává, jaké množství
FYZIKA 6. ročník 2. část
 FYZIKA 6. ročník 2. část 23_Hmotnost tělesa... 2 24_Rovnoramenné váhy.... 3 25_Hustota... 4 26_Výpočet hustoty látky... 4 27_Výpočet hustoty látky příklady... 6 28_Výpočet hmotnosti tělesa příklady...
FYZIKA 6. ročník 2. část 23_Hmotnost tělesa... 2 24_Rovnoramenné váhy.... 3 25_Hustota... 4 26_Výpočet hustoty látky... 4 27_Výpočet hustoty látky příklady... 6 28_Výpočet hmotnosti tělesa příklady...
Transportní jevy v plynech Reálné plyny Fázové přechody Kapaliny
 Transportní jevy v plynech Reálné plyny Fázové přechody Kapaliny Hustota toku Zatím jsme studovali pouze soustavy, které byly v rovnovážném stavu není-li soustava v silovém poli, je hustota částic stejná
Transportní jevy v plynech Reálné plyny Fázové přechody Kapaliny Hustota toku Zatím jsme studovali pouze soustavy, které byly v rovnovážném stavu není-li soustava v silovém poli, je hustota částic stejná
