DIAGNÓZA JEDNODUCHÝCH A SMÍŠ ÍŠENÝCH PORUCH ACIDOBAZICKÉ ROVNOVÁHY. A. Kazda. Katedra klinické biochemie, IPVZ Praha UKBLD 1.
|
|
|
- Dominik Daniel Malý
- před 7 lety
- Počet zobrazení:
Transkript
1 DIAGNÓZA JEDNODUCHÝCH A SMÍŠ ÍŠENÝCH PORUCH ACIDOBAZICKÉ ROVNOVÁHY A. Kazda Katedra klinické biochemie, IPVZ Praha UKBLD 1. LF UK a VFN
2 Záznamový list acidobazické regulace Graf acidobazické regulace (M. Engliš,, Prakt. lék. l 1972)
3 Pufrové systémy slouží k okamžit itému modulování výchylky ph tělesných t lesných tekutin chemickou reakcí. Pufr je tvořen en slabou kyselinou a její solí.. Slabá kyselina disociuje v roztoku málo, m její sůl l disociuje prakticky zcela. pufry v krvi kyselina baze % zastoupení obsažen hydrogen uhličitanový itanový hemoglobinový H CO 2 3 oxyhemoglobin HCO plazma deoxyhemoglobin 35 erytrocyty fosfátový H 2 PO- 4 HPO erytrocyty (plazma) proteiny -COOH -COO - 7 plazma (erytrocyty)
4 Vztah mezi ph a pufry popisuje Henderson-Hasselbachova Hasselbachova rovnice: [sůl] ph = pk + log [kyselina] Henderson-Hasselbachova Hasselbachova rovnice pro hydrogenuhličitanový itanový pufr: ph = pk + log [HCO -3 ] [H 2 CO 3 ] Koncentrace kyseliny uhličit ité se vyjadřuje jako funkce pco 2 ph = pk + log [HCO -3 ] α. pco 2 α = koeficient rozpustnosti oxidu uhličit itého, 0,0306 mol torr -1, tj. 0,2295 mol kpa -1 pk = přiblip ibližně 6,1
5 tkáně CO 2 CO 2 plíce CO 2 + H 2 O (800) H 2 CO 3 (1) H + + HCO -3 (0,03) Interakční reakce HCO -3 H 2 CO 3 H + Buf HBuf Retence CO 2 HCO -3 H 2 CO 3 CO 2 + H 2 O H + Buf HBuf Příklad zátěžz ěže e hydrogenuhličitanov itanového pufru: neschopnost vydýchat potřebn ebné množstv ství CO 2. ZátěžZ se přenp enáší na všechny v pufrové systémy.
6 Základní veličiny iny a jejich referenční meze ph 7,36-7,44 7,44 p CO a 2 4,8 5,9 kpa HCO - 3 akt mmol/l BE B BE ECT -2,5 až a +2,5 mmol/l -2,5 až a +2,5 mmol/l
7 Záznamový list acidobazické regulace Graf acidobazické regulace (M. Engliš, Prakt. lék. 1972)
8 Problémy interpretace acidobazických poruch při i klasickém m hodnocení Identifikace různých r zných příčin p metabolických poruch acidobazické rovnováhy (ABR) a určen ení jejich kvantitativního podílu je problémem interpretace acidobazických nálezů. Jsou užívány u dva systémy: metabolická acidóza/alkal za/alkalóza jsou diagnostikovány ny podle 1. zvýšen ení/snížení koncentrace bikarbonátů [HCO 3- ], 2. hodnoty base deficit/base excess (BE) Oba systémy jsou významně limitovány: 1. první omezení: [HCO 3- ] a BE (stejně i ph) jsou určov ovány v plazmě několika proměnnými. Ty se mohou měnit m nezávisle jedna na druhé.. Současn asně mohou existovat alkalizující i acidifikující vlivy. Smíš íšené abnormality mohou unikat poznání, pokud se jejich vliv na [HCO 3- ], BE a ph ruší ší. 2. druhé omezení: je v jejich neschopnosti identifikovat různr zné primárn rní příčiny metabolických acidóz z a alkalóz. BE ani [HCO 3- ] nedávaj vají přímou mou informaci o individuáln lní primárn rní příčině metabolických poruch.
9 Stav acidobazické rovnováhy v tělesných tekutinách Stav acidobazické rovnováhy v tělesných t lesných tekutinách je určov ován n nezávisle proměnnými veličinami. inami. V plazmě in vivo patří mezi tyto nezávisl vislé veličiny: iny: 1. PCO 2 je určován nezávisle proměnnými veličinami 2. Diference silných iontů (SID). Je to diference mezi sumou všechv silných (plně disociovaných, chemicky nereagujících) ch) kationů (Na +, K +, Ca 2+, Mg 2+ ) a všemi v silnými aniony (Cl - a další silné aniony) 3. Koncentrace netěkavých kavých slabých kyselin (A tot ), tj. suma látkových koncentrací negativních nábojn bojů albuminu a anorganického fosforu. Žádná z další ších acidobazických proměnných nných (tj. ph,[hco 3- ], BE) se nemůž ůže e změnit primárn rně.. Jsou to závislé hodnoty,, které se měním jen v závislosti z na změně nezávisle proměnných veličin. in. P. A. Stewart, V. Fencl
10 Dělení acidobazických poruch dle Stewarta modifikováno Fenclem Porucha I. Respirační II. Nerespirační - metabolická 1. Abnormáln lní SID a. Voda nadbytek/deficit b. Dysbalance silných aniontů - Chloridy nadbytek/deficit ACIDÓZA PCO 2 SID [Na + ] [Cl - ] ALKALÓZA PCO 2 SID [Na + ] [Cl - ] - Neidentifikované anionty nadbytek III. 2. Netěkav kavé slabé kyseliny a. Sérový S albumin b. Anorganické fosfáty [UA - ] - [Pi] - [Alb] - Fencl et al. Am. JRespir Crit Care 2000;162(6): Funk. Wien Clin Wschr 2007;119(13-14):390 14):
11 Metabolické AB poruchy dle Stewartova modelu a jejich klinické příčiny Diagnóza diluční acidóza koncentrační alkalóza hyperchloremická acidóza hypochloremická alkalóza acidóza ze zvýšen ení UA - hyperfofatemická acidóza hypoalbuminemická alkalóza Klinická příčina každá příčina hyponatrémie každá příčina hypernatrémie - infuze roztoků bohatých na Cl - (NaCl, Ringer) - průjem - tubulárn rní poškozen kození při i akutním či i chronickém m renáln lním m selhání - renáln lní tubulárn rní acidózy - kompenzace chronické RAL - ztráta ta žaludeční šťávy - diuretika - kompenzace chronické RAC - uremie, ketoacidóza, laktacidóza, intoxikace (salicyláty, metanol, etylalkohol) - každá příčina zvýšen ení fosfátu (předev edevším m renáln lní selhání) - jaterní insuficience, malnutrice, nefrotický sd., poraněné plochy Funk. Wien Clin Wschr 2007;119(13-14):390 14):
12 mmol/l Na + Cl - HCO K + Alb - SID Ca 2+ Mg 2+ Ca Mg Pi - UA - Diference silných iontů - SID vše e mmol/l jen albumin g/l SID = [Na + ] + [K + ] + [Ca 2+ ] + [Mg 2+ ] ([CI - ] + [UA - ]) SID = [HCO 3 -]] x [Alb] x [Pi]
13
14
15 Chloridový anion korigovaný Výpočet určuje, uje, jak by se při p i aktuáln lní hypo-,, resp. hypernatrémii, změnila nila hodnota plazmatických (sérových) chloridů,, kdyby došlo k normalizaci natrémie. Výpočtem tem se tedy zjišťuje, zda při p i aktuáln lní dysbalanci natrémie je hodnota chloridů změněna na více v nebo méně, m, než odpovídá změně natrémie. [Cl - ] korig = [Cl - ] zjišť x [Na + ] norm /[Na + ] zjišť
16 Ve vztahu Na + : Cl - mohou existovat varianty ovlivňuj ující acidobazickou rovnováhu: 1. Diluční acidóza: snížen ení S_Na + + odpovídaj dající pokles S_Cl - 2. Koncentrační alkalóza: zvýšen ení S_Na + + odpovídaj dající vzestup S_Cl - 3. Hyperchloridemická acidóza: zvýšen ení S_Cl - + S_Na + v referenčních mezích 4. Hypochloridemická alkalóza: snížen ení S_Cl - + S_Na + v referenčních mezích 5. Diluční acidóza + hyperchloridemická acidóza: snížen ení S_Na + + relativně menší snížen ení S_Cl - 6. Diluční acidóza + hypochloridemická alkalóza: snížen ení S_Na + + relativně větší snížen ení S_Cl - 7. Koncentrační alkalóza + hypochloridemická alkalóza za: zvýšen ení S_Na + + relativně menší zvýšen ení S_Cl - 8. Koncentrační alkalóza + hyperchloridemická acidóza: zvýšen ení S_Na + + relativně větší zvýšen ení S_Cl -
17 Příklady hyper erchloridemických acidóz z a hypochloridemických alkalóz, dilučních acidóz z a koncentračních ch alkalóz a jejich vzájemných kombinací Situace Na + K + Ca Ca 2+ Mg 2+ Cl Cl - Cl - korig fyziologická 140 4,4 2,0 0, hyperchloridemická acidóza 140 4,4 2,0 0, hypochloridemická alkalóza 140 4,4 2,0 0, diluční acidóza (nadbytek vody, 15% pokles koncentrací) 119 3,7 1,7 0,7 86,7 102 diluční acidóza + hyperchloridemická acidóza 119 3,7 1,7 0, ,1 diluční acidóza + hypochloridemická alkalóza 119 3,7 1,7 0, ,4 koncentrační alkalóza (deficit vody, 15% zvýšen ení koncentrací) 161 5,1 2,3 0,9 117,3 102 koncentrační alkalóza + hypochloridemická alkalóza 161 5,1 2,3 0, ,5 koncentrační alkalóza + hyperchloridemická acidóza 161 5,1 2,3 0, ,1
18 Klasifikace poruch natriového a chloridového ho iontu P_Na + measured (mmol/l) P_Cl - measured (mmol/)
19 Klasifikace poruch natriového a chloridového ho iontu P_Na + measured (mmol/l) A B C P_Cl - measured (mmol/) A. P_Na P_Cl - 80 Diluční acidóza + hypochloridemická alkalóza B. P_Na P_Cl - 90 Diluční acidóza C. P_Na P_Cl Diluční acidóza + hyperchloridemická acidóza
20 mmol/l Na + Cl - 50 K + Ca 2+ Mg 2+ Ca Mg HCO - 3 Alb - Pi - UA - UA - Neměř ěřené anionty UA - mmol/l [UA - ] = [Na + ] + [K + ] + [Ca 2+ ] + [Mg 2+ ] ([CI - ] + SID)
21 NEMĚŘ ĚŘENÉ ANIONY KORIGOVANÉ - UA mmol/l UA - korig. [UA - ] = ([Na + ] + [K + ] + [Ca 2+ ] + [Mg 2+ ] - [Cl - ] SID) x [Na] + norm./[na + ] zjišť.
22 mmol/l Cl - Na + HCO K + Alb - ANION GAP AG Ca 2+ Mg 2+ mmol/l Pi - UA - AG - AG = [Na + ] + [K + ] ([Cl - ] + [HCO - 3 ]) AG = [Na + ] ([Cl - ] + [HCO - 3 ]) AG korig = AG x ([Alb] norm [Alb] zjišť ) (kde [Alb] norm [Alb] zjišť představují normáln lní a zjištěný plazmatic matický albumin v g/l)
23 ANION GAP KORIGOVANÝ - AG AG korig AG = [Na + ] + [K + ] ([Cl - ] + [HCO 3- ]) AG korig = AG x ([Alb] norm [Alb] zji zjišť koncentrace v plazmě (ionty mmol/l, l, albumin g/l) g Na + K + Cl - HCO - 3 UA - Alb AG AG korig fyziologický stav hypoalbuminémie mie hypoalbuminémie mie + zvýšen ení laktátu tu
24 Biochemické parametry potřebn ebné při i hodnocení acidobazického nálezun 1. Acidobazické: ph, pco 2, BE, HCO 3 - aktuáln lní 2. Pro výpočty nezávisle proměnných veličin in hodnoty v séru (plazmě): Na+, K+, Cl-,, P, Ca, Mg, albumin 3. K doplnění informací: laktát, t, kyslíkov kové parametry, ph moče, ketonurie, urea, kreatinin
25 parametr anion gap (AG, aniontové okno) strong ion difference (SID) korigované chloridy neměř ěřené anionty náboj albuminu náboj na fosfátech referenční meze mmol/l ,2 (pro ph 7,4 a P_alb 40 g/l) 1,8 (pro ph 7,4 a P_fosfáty 1,0 mmol/l) Jabor 2007
26 Nemocný č.. 1, diagnóza: Bronchopneumonie. Cirhosis hepatis. Chron. ethylismus. Měřené parametry Vypočítan tané parametry Na mmol/l HCO - 3 K + 5,2 mmol/l AG Ca 1,6 mmol/l AG Mg 0,6 mmol/l BE Cl - 98 mmol/l SID Pi 0,9 mmol/l Cl Albumin 16 g/l UA ph 7,40 pco 2 5,2 kpa Hodnocení: Nález ABR je v mezích fyziologických hodnot. AG zjist. AG korig. Cl - korig. UA - korig. 24 mmol/l 8 mmol/l 15,3 mmol/l 0 mmol/l 30 mmol/l 111 mmol/l 8 mmol/l Hodnota SID je snížena jako výsledek nadbytku vody v plazmě ([Na + ] = 125 mmol/l) i nadbytku Cl - (zřejmý až z hodnoty Cl - korig ) Tato acidóza se smíšenou příčinou je zcela kompenzovaná hypoalbuminemickou alkalózou. Hodnoty BE a [HCO 3- ] jsou normální. Na hypoalbuminemickou alkalózu upozorňuje pokles AG zjist. Závěr: Smíšená porucha. Acidóza z nadbytku vody a hypechloridemie + hypoalbuminemická alkalóza.
27 Klasifikace poruch natriového a chloridového iontu P_Na + measured (mmol/l) A P_Cl - measured (mmol/) A. P_Na P_Cl - 98 Diluční acidóza a hypochloredemická alkalóza
28 Nemocný č.. 2, diagnóza: Stav po operaci pro ulcus pylori penetrans ad vesicam felleam. V dvoutýdenním m pooperačním m období průjmy, dehydratace, zmatenost, spavost. Vyšet etření v 3. týdnu, dosud několik n řidších stolic denně,, diuréza kolem 1500 ml/den. Měřené parametry [Na ] 159 mmol/l [urea ] 29 mmol/l [HCO 3 ] [K + ] 4,6 mmol/l [kreat] 390 mmol/l Ag zjišť [Ca] 2,1 mmol/l [lakt ] 2,2 mmol/l Ag korig [Mg] 0,87 mmol/l BE b [Cl ] 112 mmol/l BE ect [Pi] 2,5 mmol/l SID [Alb] 32 g/l [Cl ] korig pco 2 5,13 kpa [UA ] korig ph 7,410 Vypočítan tané parametry 25,5 mmol/l 26,1 mmol/l 28,1 mmol/l +1 mmol/l + 1,3 mmol/l 38,7 mmol/l 98,6 mmol/l 14 mmol/l Hodnocení: Nález ABR je v mezích fyziologických hodnot. hodnoty AG a UA jsou zvýšeny složka MAC hypernatrémie, hypoalbuminémie mie (hypochloridemie korig.) složka MAL protikladné vlivy na SID se vyrovnávaj vají Závěr: Smíš íšená porucha. MAC při p i renáln lní insuficienci, hyperfosfatemie, MAL z více příčin. p
29 Nemocný č.. 3, diagnóza: Přeložen en na chirurgickou kliniku z interní s dg. Menetrierovy choroby s recidivující hematemézou a melenou, hypoproteinemické otoky. Krátce po přijetí hemorhagický šok, v němžn bylo provedeno následujn sledující vyšet etření: Měřené parametry [Na ] 148 mmol/l p a O 2 6,3 kpa [HCO 3 ] [K + ] 2,3 mmol/l [urea ] 11 mmol Ag zjišť [Ca] 1,7 mmol/l [lakt] 10,5 mmol Ag korig [Mg] 0,6 mmol/l [celk. bílk.] 31 g/l BE b [Cl ] 102 mmol/l [hemogl] 40 g/l BE ect [Pi ] 1,0 mmol/l SID [Alb] 15 g/l [Cl ] korig ph 7,504 [UA ] korig pco 2 3,5 kpa Vypočítan tané parametry 20,3 mmol/l 28 mmol/l 34,2 mmol/l -33 mmol/l -2,3 mmol/l 26,3 mmol/l 95,9 mmol/l 22,8 mmol/l Hodnocení: Nález ABR je v oblasti respirační alkalózy. acidifikující vlivy - hyperlaktátemie temie (zvýšen ení AG, UA, pokles SID) alkalizující vlivy - hypernatrémie, hypochloridemie, hypoalbuminémie mie Závěr: Smíš íšená porucha. Výsledkem působenp sobení protikladných vlivů acidifikujících ch a alkalizujících ch je jen mírný m pokles BE, MAC a MAL zůstz stávají skryty. RAL je důsledkem extrémn mní hypoxémie (anémie, PaO 2, laktát). t).
30 Nemocná č. 4 43letá žena, přelop eložená z III. interní kliniky VFN na kliniku AR, kde byla sledována ve dnech Diagnózy: Proteinokalorická malnutrice, v.s. mentáln lní anorexie Iatrogenní pneumotorax, respirační insuficience Sekundárn rní anémie Hypoproteinemické edémy a trofické defekty kůžk ůže Chronický zánět z t ledvin a oligurie asystolie, resuscitace, umělá plicní ventilace Léčba mj.: Furosemid 1-3x mg/d
31 Nemocná č. 4 laboratorní nálezy a léčbal Parametr Ref. meze S-Na mmol/l 3,8-5,0 S-K + mmol/l S-Cl ,3 4,3 5,0 4,6 2,5 4,4 4,3 3,7 4, Cl - korig mmol/l ,5 96,5 95,3 ph 7,36-7,44 7,44 7,32 7,36 7,38 7,37 7,43 7,37 7,41 7,44 7,47 BE albumin alb/alk -2,5-+2,5 mmol/l g/l mmol/l du-na + mmol/d du-k + mmol/d +2,3 +4,1 +3,0 +2,4 +7,9 +6,7 +9,9 +15,5 +14, , , , , du-cl mmol/d
32 Nemocná č. 4 - hodnocení Dny 1-3: 1 diluční acidóza + hypoalbuminemická alkalóza Dny 4-6: 4 hypoalbuminemická alkalóza Dny 7-9: 7 koncentrační alkalóza + hypochloremická alkalóza + hypoalbuminemická alkalóza Na ph mám vliv trvalá hyperkapnie (6,6-8,7 kpa) Nemocná nešet etří Cl - ani v období hypochloremické alkalózy (léčba furosemidem, chronická renáln lní insuficience, clearance kreatininu /korig./ 0,63-0,65 0,65 ml/s.)
33 Výpočty k diferenciáln lní diagnóze metabolických poruch 1. Vliv iontů (efekt elektrolytů) ) na BE (EEBE) EEBE mmol/l = Na + - Cl Vliv albuminu na BE (AlbBE) AlbBE mmol/l = (42 Alb)/4 Story DA et al. B J Anaesth 2004;92(1):54-60
34 Příklad použit ití jednoduchých výpočtů Měřené parametry Na mmol/l K + 5,5 mmol/l Cl mmol/l laktát - 3 mmol/l albumin 26 g/l ph 7,12 pco 2 4,6 kpa Vypočítané parametry HCO mmol/l BE - 17 mmol/l EE BE = -10 mmol/l Alb (42 26)/4 = BE +4 mmol/l laktát BE 1-3= -2 mmol/l Složky ovlivňuj ující BE Korekce podílu hyoalbuminemické MAL Odečtení efektu elektrolytů Odečtení vlivu laktátu = - 21 mmol/l = - 11 mmol/l = - 9 mmol/l Hodnocení BE: po odečtení všech složek podílejících se na hodnotě BE je výsledná hodnota stále ještě negativní (-9 mmol/l). To lze vysvětlit pouze zvýšením UA-, na němž se vedle laktátu podílejí další složky. V souladu s tímto závěrem z rem je zvýšen ení AG korig : AG korig = ( ,5) ( ) + 4 = 26,5 Závěr: r: na nálezu n ABR se podílej lejí vlivy acidifikující,, změny v [Na + ] a [Cl - ], zvýšen ení UA - (kromě laktátu tu další vlivy) a hypoalbuminemická MAL. Story DA et al. B J Anaesth 2004;92(1): Funk GCH. Wien Klin Wschr 2007;119(13-14):390 14):
35 ZÁVĚRY 1. Dopočítávan vané acidobazické parametry (HCO - 3 i BE), stejně tak jako ph jsou závislé na hodnotách nezávisle proměnných, mezi které patří pco 2, diference silných bází b (SID) a koncentrace netěkavých slabých kyselin (A ). (A tot ). 2. Hodnocení těchto chto parametrů,, doplněné o další výpočty ze sloupce anionů, především m o korigované chloridy (Cl - korig ) a neměř ěřené aniony (UA - ) umožň žňuje rozpoznat smíš íšené poruchy vnitřního prostřed edí. 3. Změny ny hodnot Na+ a Cl- ovlivňuj ují acidobazický nález. n Tyto změny ny mohou vést v k poruchám m buď jednoduchým nebo smíš íšeným. Jejich vliv na acidobazický nález n se můžm ůže e buď zesilovat nebo naopak rušit. Ke správn vné diagnóze přispp ispívá buď výpočet korigovaných chloridů nebo jednodušší odečten tení z grafu. Diferencování jednoduchých a smíš íšených poruch vnitřního prostřed edí má význam nejen diagnostický, ale i terapeutický.
36
Acidobazické regulace
 ZÁKLADY OBECNÉ A KLINICKÉ BIOCHEMIE 2004 Acidobazické regulace Antonín Kazda kapitola ve skriptech 3.8 Klasifikace acidobazických ch poruch Porucha ACIDOSA ALKALOSA I. Respirační PCO2 II. Nerespirační
ZÁKLADY OBECNÉ A KLINICKÉ BIOCHEMIE 2004 Acidobazické regulace Antonín Kazda kapitola ve skriptech 3.8 Klasifikace acidobazických ch poruch Porucha ACIDOSA ALKALOSA I. Respirační PCO2 II. Nerespirační
Acidobazická rovnováha vývoj interpretace nálezn. lezů. A. Kazda
 Acidobazická rovnováha vývoj interpretace nálezn lezů A. Kazda Vyšet etřování acidobazické rovnováhy před p r. 1956 Bylo měřm ěřeno ph krve a vyšet etřen en celkový CO 2 (Total CO 2 ) např. van Slykeovým
Acidobazická rovnováha vývoj interpretace nálezn lezů A. Kazda Vyšet etřování acidobazické rovnováhy před p r. 1956 Bylo měřm ěřeno ph krve a vyšet etřen en celkový CO 2 (Total CO 2 ) např. van Slykeovým
Acidobazická rovnováha
 Acidobazická rovnováha Klepnutím lze upravit styl předlohy podnadpisů. MUDr. Jiří Dvorský, NMB Vnitřní prostředí Pod pojmem vnitřní prostředí chápeme extracelulární tekutinu (včetně jejího složení) omývající
Acidobazická rovnováha Klepnutím lze upravit styl předlohy podnadpisů. MUDr. Jiří Dvorský, NMB Vnitřní prostředí Pod pojmem vnitřní prostředí chápeme extracelulární tekutinu (včetně jejího složení) omývající
3.8. Acidobazická regulace
 3.8. Acidobazická regulace Tabulka 3.8. 1: Referenční intervaly Parametr Muži Ženy ph 7,37 7,43 7,37 7,43 pco 2 (kpa) 4,7 6,0 4,3 5,7 - aktuální HCO 3 (mmol/l) 23,6 27,6 21,8 27,2 - standardní HCO 3 (mmol/l)
3.8. Acidobazická regulace Tabulka 3.8. 1: Referenční intervaly Parametr Muži Ženy ph 7,37 7,43 7,37 7,43 pco 2 (kpa) 4,7 6,0 4,3 5,7 - aktuální HCO 3 (mmol/l) 23,6 27,6 21,8 27,2 - standardní HCO 3 (mmol/l)
Acidobazická rovnováha 11
 Acidobazická rovnováha 11 Iontogram krevní plazmy, AG, SID, BB s, pufrační systémy, hydrogenuhličitanový pufr. Poruchy acidobazické rovnováhy. 1. Jaký je princip měření a? 2. Které kyslíkové parametry
Acidobazická rovnováha 11 Iontogram krevní plazmy, AG, SID, BB s, pufrační systémy, hydrogenuhličitanový pufr. Poruchy acidobazické rovnováhy. 1. Jaký je princip měření a? 2. Které kyslíkové parametry
Vyšetřování a léčba poruch acidobazické rovnováhy
 Vyšetřování a léčba poruch acidobazické rovnováhy Vladimír Soška Oddělení klinické biochemie Fyziologické hodnoty ABR Parametr Jednotka Normální meze Kritické hodnoty ph 7.35-7.45 < 7.1; > 7.6 pco 2 kpa
Vyšetřování a léčba poruch acidobazické rovnováhy Vladimír Soška Oddělení klinické biochemie Fyziologické hodnoty ABR Parametr Jednotka Normální meze Kritické hodnoty ph 7.35-7.45 < 7.1; > 7.6 pco 2 kpa
ABR a iontového hospodářství
 Poruchy acidobazické rovnováhy Patobiochemie a diagnostika poruch ABR a iontového hospodářství Připojte se! Room name: ABR http://b.socrative.com Regulace kyselosti vnitřního prostředí CO 2 NH 3 tvorba
Poruchy acidobazické rovnováhy Patobiochemie a diagnostika poruch ABR a iontového hospodářství Připojte se! Room name: ABR http://b.socrative.com Regulace kyselosti vnitřního prostředí CO 2 NH 3 tvorba
ABR a iontového hospodářství
 Poruchy acidobazické rovnováhy Patobiochemie a diagnostika poruch ABR a iontového hospodářství Regulace kyselosti vnitřního prostředí CO 2 NH 3 tvorba močoviny glutaminu H + HCO - 3 Martin Vejražka, 2007
Poruchy acidobazické rovnováhy Patobiochemie a diagnostika poruch ABR a iontového hospodářství Regulace kyselosti vnitřního prostředí CO 2 NH 3 tvorba močoviny glutaminu H + HCO - 3 Martin Vejražka, 2007
Stewart Fenclův koncept hodnocení poruch ABR
 Stewart Fenclův koncept hodnocení poruch ABR František Duška Klinika anesteziologie a resuscitace a Ústav lék. chemie a biochemie 3. LF UK Motto: Republika nepotřebuje chemiky! Roberspierre při vynášení
Stewart Fenclův koncept hodnocení poruch ABR František Duška Klinika anesteziologie a resuscitace a Ústav lék. chemie a biochemie 3. LF UK Motto: Republika nepotřebuje chemiky! Roberspierre při vynášení
Poruchy vnitřního prostředí. v intenzivní medicíně
 Poruchy vnitřního prostředí v intenzivní medicíně Vnitřní prostředí = extracelulární tekutina (plazma, intersticiální tekutina) Poruchy objemu a osmolality Poruchy iontů (Na, K, Ca, Mg, Cl) Poruchy acidobazické
Poruchy vnitřního prostředí v intenzivní medicíně Vnitřní prostředí = extracelulární tekutina (plazma, intersticiální tekutina) Poruchy objemu a osmolality Poruchy iontů (Na, K, Ca, Mg, Cl) Poruchy acidobazické
Plasma a většina extracelulární
 Acidobazická rovnováha Tato prezentace je přístupná online Fyziologické ph Plasma a většina extracelulární tekutiny ph = 7,40 ± 0,02 Význam stálého ph Na ph závisí vlastnosti bílkovin aktivita enzymů struktura
Acidobazická rovnováha Tato prezentace je přístupná online Fyziologické ph Plasma a většina extracelulární tekutiny ph = 7,40 ± 0,02 Význam stálého ph Na ph závisí vlastnosti bílkovin aktivita enzymů struktura
Acidobazická rovnováha a její vztahy k iontovému hospodářství. Klinické aplikace.
 Text použit s laskavým svolením autora. Acidobazická rovnováha a její vztahy k iontovému hospodářství. Klinické aplikace. Antonín Jabor Oddělení klinické biochemie Nemocnice Kladno Část 1. Relevantní parametry
Text použit s laskavým svolením autora. Acidobazická rovnováha a její vztahy k iontovému hospodářství. Klinické aplikace. Antonín Jabor Oddělení klinické biochemie Nemocnice Kladno Část 1. Relevantní parametry
Produkce kyselin v metabolismu Těkavé: 15,000 mmol/den kyseliny uhličité, vyloučena plícemi jako CO 2 Netěkavé kyseliny (1 mmol/kg/den) jsou vyloučeny
 Vnitřní prostředí a acidobazická rovnováha 13.12.2004 Vnitřní prostředí Sestává z posuzování složení extracelulární tekutiny z hlediska izohydrie (= optimální koncentrace ph) izoionie (= optimální koncentrace
Vnitřní prostředí a acidobazická rovnováha 13.12.2004 Vnitřní prostředí Sestává z posuzování složení extracelulární tekutiny z hlediska izohydrie (= optimální koncentrace ph) izoionie (= optimální koncentrace
Monitoring vnitřního prostředí pacienta
 Monitoring vnitřního prostředí pacienta MVDr. Leona Raušerová -Lexmaulová, Ph.D. Klinika chorob psů a koček VFU Brno Vnitřní prostředí Voda Ionty Bílkoviny Cukry Tuky Důležité faktory Obsah vody Obsah
Monitoring vnitřního prostředí pacienta MVDr. Leona Raušerová -Lexmaulová, Ph.D. Klinika chorob psů a koček VFU Brno Vnitřní prostředí Voda Ionty Bílkoviny Cukry Tuky Důležité faktory Obsah vody Obsah
Zpět k základům: poruchy acidobazické rovnováhy a vnitřního prostředí u komplikovaného pacienta Antonín Jabor, Janka Franeková
 Zpět k základům: poruchy acidobazické rovnováhy a vnitřního prostředí u komplikovaného pacienta Antonín Jabor, Janka Franeková PLM IKEM a 3. LF, UK Praha 7.10. 08:50 7.10 12:17 7.10. 16:44 8.10. 02:00
Zpět k základům: poruchy acidobazické rovnováhy a vnitřního prostředí u komplikovaného pacienta Antonín Jabor, Janka Franeková PLM IKEM a 3. LF, UK Praha 7.10. 08:50 7.10 12:17 7.10. 16:44 8.10. 02:00
Acidobazická rovnováha H+ a ph Vodíkový iont se skládá z protonu, kolem něhož neobíhá žádný elektron. Proto je vodíkový iont velmi malý a je
 Acidobazická rovnováha 14.4.2004 H+ a ph Vodíkový iont se skládá z protonu, kolem něhož neobíhá žádný elektron. Proto je vodíkový iont velmi malý a je extrémně reaktivní. Má proto velmi hluboký vliv na
Acidobazická rovnováha 14.4.2004 H+ a ph Vodíkový iont se skládá z protonu, kolem něhož neobíhá žádný elektron. Proto je vodíkový iont velmi malý a je extrémně reaktivní. Má proto velmi hluboký vliv na
Jana Fauknerová Matějčková
 Jana Fauknerová Matějčková kyselina (HA) acidóza (acidémie) báze (B ) alkalóza (alkalémie) pufr ph = pk + log cs / ca koncentrace [H + ] v krvi udržována pomocí plic, ledvin a jater okolo 40 nm ph = log
Jana Fauknerová Matějčková kyselina (HA) acidóza (acidémie) báze (B ) alkalóza (alkalémie) pufr ph = pk + log cs / ca koncentrace [H + ] v krvi udržována pomocí plic, ledvin a jater okolo 40 nm ph = log
Acidobazická rovnováha (ABR)
 Acidobazická rovnováha (ABR) Definice ph ph = log c(h + ) ph = 7,4 c(h + ) = 40 nm (H + ) = ph kyselina látka odštěpující H + (Arrhenius) nebo donor H + (Brönsted) zásada látka odštěpující OH (Arrhenius)
Acidobazická rovnováha (ABR) Definice ph ph = log c(h + ) ph = 7,4 c(h + ) = 40 nm (H + ) = ph kyselina látka odštěpující H + (Arrhenius) nebo donor H + (Brönsted) zásada látka odštěpující OH (Arrhenius)
P. Schneiderka, Ústav patologické fyziologie LFUP a OKB FN Olomouc
 P. Schneiderka, Ústav patologické fyziologie LFUP a OKB FN Olomouc Acidobazický stav organismu Verze 27.9. 2012 Úvod Za průkopníka znalostí o acidobazickém stavu organismu (ABS) lze považovat amerického
P. Schneiderka, Ústav patologické fyziologie LFUP a OKB FN Olomouc Acidobazický stav organismu Verze 27.9. 2012 Úvod Za průkopníka znalostí o acidobazickém stavu organismu (ABS) lze považovat amerického
Vliv infuzních roztoků na acidobazickou rovnováhu. Antonín Jabor IKEM Praha
 Vliv infuzních roztoků na acidobazickou rovnováhu Antonín Jabor IKEM Praha Fyziologický roztok Fyziologický roztok Incidence hyperchloridemie na konci operace je častá, je spojena s metabolickou acidózou,
Vliv infuzních roztoků na acidobazickou rovnováhu Antonín Jabor IKEM Praha Fyziologický roztok Fyziologický roztok Incidence hyperchloridemie na konci operace je častá, je spojena s metabolickou acidózou,
Acidobazický stav organismu
 Acidobazický stav organismu Doc. MUDr. Petr Schneiderka CSc. Tvorba a ověření e-learningového prostředí pro integraci výuky preklinických a klinických předmětů na LF UP a FZV UP Reg. č.: CZ.1.07/2.2.00/15.0313
Acidobazický stav organismu Doc. MUDr. Petr Schneiderka CSc. Tvorba a ověření e-learningového prostředí pro integraci výuky preklinických a klinických předmětů na LF UP a FZV UP Reg. č.: CZ.1.07/2.2.00/15.0313
Výpočty koncentrací. objemová % (objemový zlomek) krvi m. Vsložky. celku. Objemy nejsou aditivní!!!
 Výpočty koncentrací objemová % (objemový zlomek) Vsložky % obj. = 100 V celku Objemy nejsou aditivní!!! Příklad: Kolik ethanolu je v 700 ml vodky (40 % obj.)? Kolik promile ethanolu v krvi bude mít muž
Výpočty koncentrací objemová % (objemový zlomek) Vsložky % obj. = 100 V celku Objemy nejsou aditivní!!! Příklad: Kolik ethanolu je v 700 ml vodky (40 % obj.)? Kolik promile ethanolu v krvi bude mít muž
VNITŘNÍ PROSTŘEDÍ. Biochemický ústav LF MU (V.P.) 2007
 1 VNITŘNÍ PROSTŘEDÍ Biochemický ústav LF MU (V.P.) 2007 2 Vnitřní prostředí: Claude Bernard, 1878: Co je vnitřní prostředí? Je to krev, ve skutečnosti však nikoliv celá, nýbrž tekutá část krve, krevní
1 VNITŘNÍ PROSTŘEDÍ Biochemický ústav LF MU (V.P.) 2007 2 Vnitřní prostředí: Claude Bernard, 1878: Co je vnitřní prostředí? Je to krev, ve skutečnosti však nikoliv celá, nýbrž tekutá část krve, krevní
Chloridy v séru. Patofyziologické mechanismy ovlivňující koncentraci. Příčiny hypochlorémie. Nedostatečný přívod Zcela neslaná dieta
 Chloridy v séru Abstrakt Chloridy jsou hlavním aniontem extracelulární tekutiny, jejich koncentrace v séru je nižší než v arteriální krvi. Stanovení koncentrace chloridů v séru je základem pro interpretaci
Chloridy v séru Abstrakt Chloridy jsou hlavním aniontem extracelulární tekutiny, jejich koncentrace v séru je nižší než v arteriální krvi. Stanovení koncentrace chloridů v séru je základem pro interpretaci
Klinická fyziologie ABR sekce Základy oboru edukační lekce. Michal Horáček KARIM 2. LF UK a FN v Motole Praha
 Klinická fyziologie ABR sekce Základy oboru edukační lekce Michal Horáček KARIM 2. LF UK a FN v Motole Praha Hlavní ukazatel ABR: ph (resp. a[h + ]) ph = pondus hydrogenii, potential of hydrogen = vodíkový
Klinická fyziologie ABR sekce Základy oboru edukační lekce Michal Horáček KARIM 2. LF UK a FN v Motole Praha Hlavní ukazatel ABR: ph (resp. a[h + ]) ph = pondus hydrogenii, potential of hydrogen = vodíkový
PARENTERÁLNÍ VÝŽIVA 1
 PARENTERÁLNÍ VÝŽIVA 1 2 3 4 5 6 7 8 9 10 Cukr a tuk: 1/ glukosa je (aerobně) metabolizována na acetyl-coa. Jeho nadbytek, neodbouraný v Krebsově cyklu, může být přeměněn na mastné kyseliny (ev. na cholesterol)
PARENTERÁLNÍ VÝŽIVA 1 2 3 4 5 6 7 8 9 10 Cukr a tuk: 1/ glukosa je (aerobně) metabolizována na acetyl-coa. Jeho nadbytek, neodbouraný v Krebsově cyklu, může být přeměněn na mastné kyseliny (ev. na cholesterol)
Diagnostika a léčba poruch acidobazické rovnováhy. J. Vymětal 3. interní klinika nefrologická, revmatologická a endokrinologická
 Diagnostika a léčba poruch acidobazické rovnováhy J. Vymětal 3. interní klinika nefrologická, revmatologická a endokrinologická ph alkalita/acidita vnitřního prostředí 7,4 ± 0,04 mmol/l pco 2 respirační
Diagnostika a léčba poruch acidobazické rovnováhy J. Vymětal 3. interní klinika nefrologická, revmatologická a endokrinologická ph alkalita/acidita vnitřního prostředí 7,4 ± 0,04 mmol/l pco 2 respirační
tělní buňky tělní tekutiny krev erythrocyty 7.28 thrombocyty 7.0 žaludeční šťáva buňky kosterního svalstva duodenální šťáva
 Acidobazická rovnováha homeostasa H + iontů Regulace vnitřního prostředí Udržování osmotické koncetrace solí, minerálů, eáů, Vztahy acidobazické rovnováhy Stálost = acidobazická rovnováha (stav) Regulace
Acidobazická rovnováha homeostasa H + iontů Regulace vnitřního prostředí Udržování osmotické koncetrace solí, minerálů, eáů, Vztahy acidobazické rovnováhy Stálost = acidobazická rovnováha (stav) Regulace
Existují ideální iontové roztoky pro pacienty se SBS? Michal Žourek DPV Praha
 Existují ideální iontové roztoky pro pacienty se SBS? Michal Žourek DPV Praha 16.11.2007 Osnova Vstřebávání základních látek z GIT Hodnocení ABR Hodnocení změn: Na, K, Cl, Ca, P, Mg SBS a funkční změny
Existují ideální iontové roztoky pro pacienty se SBS? Michal Žourek DPV Praha 16.11.2007 Osnova Vstřebávání základních látek z GIT Hodnocení ABR Hodnocení změn: Na, K, Cl, Ca, P, Mg SBS a funkční změny
Diagnostika poruch acidobazické rovnováhy
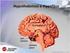 Návod do cvičení Diagnostika poruch acidobazické rovnováhy Úvod Stálost tzv. vnitřního prostředí je nezbytnou podmínkou života vyšších organismů. Důležitá je zejména hodnota ph. Na hodnotě ph závisí mimo
Návod do cvičení Diagnostika poruch acidobazické rovnováhy Úvod Stálost tzv. vnitřního prostředí je nezbytnou podmínkou života vyšších organismů. Důležitá je zejména hodnota ph. Na hodnotě ph závisí mimo
Diagnostika a léčba poruch acidobazické rovnováhy. J. Vymětal 3. interní klinika nefrologická, revmatologická a endokrinologická
 Diagnostika a léčba poruch acidobazické rovnováhy J. Vymětal 3. interní klinika nefrologická, revmatologická a endokrinologická ph alkalita/acidita vnitřního prostředí 7,4 ± 0,04 mmol/l pco 2 respirační
Diagnostika a léčba poruch acidobazické rovnováhy J. Vymětal 3. interní klinika nefrologická, revmatologická a endokrinologická ph alkalita/acidita vnitřního prostředí 7,4 ± 0,04 mmol/l pco 2 respirační
Hlavní ukazatele acidobazické rovnováhy
 Hlavní ukazatele acidobazické rovnováhy Pro vyšetření parametrů acidobazické rovnováhy (ABR) se odebírá krev arteriální nebo arterilizovaná. Arteriální krev se odebírá z artérií do heparinizovaných zkumavek
Hlavní ukazatele acidobazické rovnováhy Pro vyšetření parametrů acidobazické rovnováhy (ABR) se odebírá krev arteriální nebo arterilizovaná. Arteriální krev se odebírá z artérií do heparinizovaných zkumavek
rovnováha mezi acidifikujícími a alkalizujícími vlivy
 AB balance; úvod do patofy- siologických aspektů AB balance; introduction into pathophysiological aspects Prof. Dr. V. Pelouch, CSc. Co je acidobazická rovnováha? rovnováha mezi acidifikujícími a alkalizujícími
AB balance; úvod do patofy- siologických aspektů AB balance; introduction into pathophysiological aspects Prof. Dr. V. Pelouch, CSc. Co je acidobazická rovnováha? rovnováha mezi acidifikujícími a alkalizujícími
BILANČNÍ PŘÍSTUP K MODELOVÁNÍ ACIDOBAZICKÉ ROVNOVÁHY A PŘENOSU KREVNÍCH PLYNŮ
 BILANČNÍ PŘÍSTUP K MODELOVÁNÍ ACIDOBAZICKÉ ROVNOVÁHY A PŘENOSU KREVNÍCH PLYNŮ Jiří Kofránek, Michal Andrlík, Stanislav Matoušek Anotace Navazujeme na popis našeho přístupu k modelování acidobazické rovnováhy
BILANČNÍ PŘÍSTUP K MODELOVÁNÍ ACIDOBAZICKÉ ROVNOVÁHY A PŘENOSU KREVNÍCH PLYNŮ Jiří Kofránek, Michal Andrlík, Stanislav Matoušek Anotace Navazujeme na popis našeho přístupu k modelování acidobazické rovnováhy
Acidobazická rovnováha. H. Vaverková
 Acidobazická rovnováha H. Vaverková Acidobazická rovnováha ph arteriální krve a intersticiální tekutiny normálně kolísá v rozmezí 7,35-7,45 ph kompatibilní s životem: 6,8-7,8 ph < 7,35 = acidóza, ph >7,45
Acidobazická rovnováha H. Vaverková Acidobazická rovnováha ph arteriální krve a intersticiální tekutiny normálně kolísá v rozmezí 7,35-7,45 ph kompatibilní s životem: 6,8-7,8 ph < 7,35 = acidóza, ph >7,45
2 Roztoky elektrolytů. Osmotický tlak
 Roztoky elektrolytů. Osmotický tlak 1. Doplněním uvedených schémat vyjádřete rozdílné chování různých typů látek po jejich rozpuštění ve vodě. Použijte symboly AB(aq), A + (aq), B - (aq). [s pevná fáze,
Roztoky elektrolytů. Osmotický tlak 1. Doplněním uvedených schémat vyjádřete rozdílné chování různých typů látek po jejich rozpuštění ve vodě. Použijte symboly AB(aq), A + (aq), B - (aq). [s pevná fáze,
Acidobazická rovnováha pro pokročilé. František Duška KAR FNKV
 Acidobazická rovnováha pro pokročilé František Duška KAR FNKV Republika nepotřebuje chemiky! Roberspierre při vynášení rozsudku trestu smrti nad Lavoisierem 8. května 1794 28 letý muž, alkoholik. Přichází
Acidobazická rovnováha pro pokročilé František Duška KAR FNKV Republika nepotřebuje chemiky! Roberspierre při vynášení rozsudku trestu smrti nad Lavoisierem 8. května 1794 28 letý muž, alkoholik. Přichází
KAZUISTIKY Z LABORATORNÍ MEDICÍNY
 KAZUISTIKY Z LABORATORNÍ MEDICÍNY Jaroslav Racek Ústav klinické biochemie a hematologie LF UK a FN v Plzni Dialog 2019, zámek Valeč, 7. 9. 4. 2019 KAZUISTIKA I O T R AVA M E T F O R M I N E M A A C E I
KAZUISTIKY Z LABORATORNÍ MEDICÍNY Jaroslav Racek Ústav klinické biochemie a hematologie LF UK a FN v Plzni Dialog 2019, zámek Valeč, 7. 9. 4. 2019 KAZUISTIKA I O T R AVA M E T F O R M I N E M A A C E I
Akutní stavy Ztráty vody a iont byly hrazeny infúzemi glukózy nebo pitím vody. Vznikající hypoosmolalita ECT vedla k p esunu ásti vody z ECT do ICT.
 Strana 1 (celkem 6 Strana 1 (celkem 6) Odd lení laboratorní medicíny nemocnice Šternberk Jívavská 20, 78516, eská Republika Tel 585087308 fax 585087306 E-mail olm@nemstbk.cz info:www.nemstbk.cz/olm ----------------------------------------------
Strana 1 (celkem 6 Strana 1 (celkem 6) Odd lení laboratorní medicíny nemocnice Šternberk Jívavská 20, 78516, eská Republika Tel 585087308 fax 585087306 E-mail olm@nemstbk.cz info:www.nemstbk.cz/olm ----------------------------------------------
Acidobazická rovnováha
 Acidobazická rovnováha... přístupy Motol, 2019-04-16 Jak to vypadá v realitě? pouze arteriální odběry 15 000 nálezů ABL 800 Radiometer BEECT ABIC APH ACO2 7,8 18 7,6 7,4 7,2 16 14 12 10 7,0 8 6,8 6,6 6,4
Acidobazická rovnováha... přístupy Motol, 2019-04-16 Jak to vypadá v realitě? pouze arteriální odběry 15 000 nálezů ABL 800 Radiometer BEECT ABIC APH ACO2 7,8 18 7,6 7,4 7,2 16 14 12 10 7,0 8 6,8 6,6 6,4
Vybrané klinicko-biochemické hodnoty
 Vybrané klinicko-biochemické hodnoty Obecným výsledkem laboratorního vyšetření je naměřená hodnota, která může být fyziologická, zvýšená či snížená. Abychom zjištěnou hodnotu mohli takto zařadit, je třeba
Vybrané klinicko-biochemické hodnoty Obecným výsledkem laboratorního vyšetření je naměřená hodnota, která může být fyziologická, zvýšená či snížená. Abychom zjištěnou hodnotu mohli takto zařadit, je třeba
Acidobazická rovnováha - jasně a jednoduše
 Acidobazická rovnováha - jasně a jednoduše Michal Horáček KARIM 2. LF UK v FNM Praha ph, resp. a[h + ] rovnice 4. řádu: 3 nezávisle proměnné, 5 rychlostních konstant po zjednodušení: Acidobazická rovnováha
Acidobazická rovnováha - jasně a jednoduše Michal Horáček KARIM 2. LF UK v FNM Praha ph, resp. a[h + ] rovnice 4. řádu: 3 nezávisle proměnné, 5 rychlostních konstant po zjednodušení: Acidobazická rovnováha
ZÁKLADNÍ CHEMICKÉ POJMY A ZÁKONY
 ZÁKLADNÍ CHEMICKÉ POJMY A ZÁKONY Klíčová slova: relativní atomová hmotnost (A r ), relativní molekulová hmotnost (M r ), Avogadrova konstanta (N A ), látkové množství (n, mol), molární hmotnost (M, g/mol),
ZÁKLADNÍ CHEMICKÉ POJMY A ZÁKONY Klíčová slova: relativní atomová hmotnost (A r ), relativní molekulová hmotnost (M r ), Avogadrova konstanta (N A ), látkové množství (n, mol), molární hmotnost (M, g/mol),
Jana Fauknerová Matějčková
 Jana Fauknerová Matějčková převody jednotek výpočet ph ph vodných roztoků ph silných kyselin a zásad ph slabých kyselin a zásad, disociační konstanta, pk ph pufrů koncentace 1000mg př. g/dl mg/l = = *10000
Jana Fauknerová Matějčková převody jednotek výpočet ph ph vodných roztoků ph silných kyselin a zásad ph slabých kyselin a zásad, disociační konstanta, pk ph pufrů koncentace 1000mg př. g/dl mg/l = = *10000
Klasické nebo Stewartovo hodnocení poruch ABR?
 Klasické nebo Stewartovo hodnocení poruch ABR? Neboli naše mezery v acidobazi M. Kratochvíl, KARIM FN Brno Definice ph: záporný dekadický logaritmus koncentrace oxoniových iontů (40 nmol/l) Kyselina: donor
Klasické nebo Stewartovo hodnocení poruch ABR? Neboli naše mezery v acidobazi M. Kratochvíl, KARIM FN Brno Definice ph: záporný dekadický logaritmus koncentrace oxoniových iontů (40 nmol/l) Kyselina: donor
Infúze. Markéta Vojtová. VOŠZ a SZŠ Hradec Králové
 Infúze Markéta Vojtová VOŠZ a SZŠ Hradec Králové Infúze Podání většího množství tekutin parenterální cestou Tekutiny Léky Elektrolyty Vitamíny Nutrice Úpravy ABR Doplnění cirkulujícího objemu tekutin Vyvolání
Infúze Markéta Vojtová VOŠZ a SZŠ Hradec Králové Infúze Podání většího množství tekutin parenterální cestou Tekutiny Léky Elektrolyty Vitamíny Nutrice Úpravy ABR Doplnění cirkulujícího objemu tekutin Vyvolání
3 Acidobazické reakce
 3 Acidobazické reakce Brønstedova teorie 1. Uveďte explicitní definice podle Brønstedovy teorie. Kyselina je... Báze je... Konjugovaný pár je... 2. Doplňte tabulku a pojmenujte všechny sloučeniny. Kyselina
3 Acidobazické reakce Brønstedova teorie 1. Uveďte explicitní definice podle Brønstedovy teorie. Kyselina je... Báze je... Konjugovaný pár je... 2. Doplňte tabulku a pojmenujte všechny sloučeniny. Kyselina
Soli. ph roztoků solí - hydrolýza
 Soli Soli jsou iontové sloučeniny vzniklé neutralizační reakcí. Např. NaCl je sůl vzniklá reakcí kyseliny HCl a zásady NaOH. Př.: Napište neutralizační reakce jejichž produktem jsou CH 3 COONa, NaCN, NH
Soli Soli jsou iontové sloučeniny vzniklé neutralizační reakcí. Např. NaCl je sůl vzniklá reakcí kyseliny HCl a zásady NaOH. Př.: Napište neutralizační reakce jejichž produktem jsou CH 3 COONa, NaCN, NH
Pavel Suk ARK, FN u svatéanny v Brně
 Pavel Suk ARK, FN u svatéanny v Brně anamnéza, klinika jaká porucha ABR je nejpravděpodobnější? vyvolávající porucha? jiné příčiny? smíšené poruchy ABR kompenzace? je adekvátní? klinická významnost? dynamika?
Pavel Suk ARK, FN u svatéanny v Brně anamnéza, klinika jaká porucha ABR je nejpravděpodobnější? vyvolávající porucha? jiné příčiny? smíšené poruchy ABR kompenzace? je adekvátní? klinická významnost? dynamika?
Cca případu ročně. Zvolit si způsob. Detailně plánovat. Moc se tím nechlubit. Držet se plánu. Soukromí. Štěstí
 Lucky Losers Cca 1 300 případu ročně Zvolit si způsob Detailně plánovat Moc se tím nechlubit Držet se plánu Soukromí Štěstí Příběhy obyčejného šílenství lidí, kteří to přežili, aby to zkusili znovu a
Lucky Losers Cca 1 300 případu ročně Zvolit si způsob Detailně plánovat Moc se tím nechlubit Držet se plánu Soukromí Štěstí Příběhy obyčejného šílenství lidí, kteří to přežili, aby to zkusili znovu a
Toxické metabolity glykolaldehyd, kys. glykolová, kys. glyoxylová, kys. štavelová
 Marek Protuš C 2 H 6 O 2 Alkohol 1,2-ethandiol bezbarvá viskózní tekutina nasládlé chuti netoxický Molární hmotnost 62,068 g/mol Teplota tání 12,9 C Teplota varu 197,3 C Hustota 1,113 g/cm 3 Rozpustnost
Marek Protuš C 2 H 6 O 2 Alkohol 1,2-ethandiol bezbarvá viskózní tekutina nasládlé chuti netoxický Molární hmotnost 62,068 g/mol Teplota tání 12,9 C Teplota varu 197,3 C Hustota 1,113 g/cm 3 Rozpustnost
9. Poruchy metabolismu draslíku 14. Acidózy 15. Alkalózy. Draslík ) Regulace K mezi tělem a zevním prostředím
 9. Poruchy metabolismu draslíku 14. Acidózy 15. Alkalózy Prof. MUDr. Zuzana Kubová, CSc. Ústav patologické fyziologie, Lékařská fakulta UK v Hradci Králové Draslík K hl. ICT kation 160 mmol/l konc. v séru
9. Poruchy metabolismu draslíku 14. Acidózy 15. Alkalózy Prof. MUDr. Zuzana Kubová, CSc. Ústav patologické fyziologie, Lékařská fakulta UK v Hradci Králové Draslík K hl. ICT kation 160 mmol/l konc. v séru
3 Acidobazické reakce
 3 Acidobazické reakce Brønstedova teorie 1. Uveďte explicitní definice podle Brønstedovy teorie. Kyselina je... Báze je... Konjugovaný pár je... 2. Doplňte tabulku a pojmenujte všechny sloučeniny. Kyselina
3 Acidobazické reakce Brønstedova teorie 1. Uveďte explicitní definice podle Brønstedovy teorie. Kyselina je... Báze je... Konjugovaný pár je... 2. Doplňte tabulku a pojmenujte všechny sloučeniny. Kyselina
Seznam vyšetření biochemie a hematologie
 Seznam vyšetření biochemie a hematologie BIOCHEMICKÁ VYŠETŘENÍ NÁZEV: Glukosa POUŽITÍ: Stanovení koncentrace glukosy v séru (plazmě) a v moči JEDNOTKY KONCENTRACE: mmol/l (sérum, plazma) g% (sbíraná moč)
Seznam vyšetření biochemie a hematologie BIOCHEMICKÁ VYŠETŘENÍ NÁZEV: Glukosa POUŽITÍ: Stanovení koncentrace glukosy v séru (plazmě) a v moči JEDNOTKY KONCENTRACE: mmol/l (sérum, plazma) g% (sbíraná moč)
Projekt: Digitální učební materiály ve škole, registrační číslo projektu CZ.1.07/1.5.00/34.0527
 Projekt: Digitální učební materiály ve škole, registrační číslo projektu CZ.1.07/1.5.00/34.0527 Příjemce: Střední zdravotnická škola a Vyšší odborná škola zdravotnická, Husova 3, 371 60 České Budějovice
Projekt: Digitální učební materiály ve škole, registrační číslo projektu CZ.1.07/1.5.00/34.0527 Příjemce: Střední zdravotnická škola a Vyšší odborná škola zdravotnická, Husova 3, 371 60 České Budějovice
Acido-bázická rovnováha (ABR)
 1 Acido-bázická rovnováha (ABR) Vladimír Kollárik II. klinika anestéziológie a intenzívnej medicíny Fakultná nemocnica s poliklinikou F. D. Roosevelta Banská Bystrica CEEA 2017 Košice, 2 3 Prečo je dôležitý
1 Acido-bázická rovnováha (ABR) Vladimír Kollárik II. klinika anestéziológie a intenzívnej medicíny Fakultná nemocnica s poliklinikou F. D. Roosevelta Banská Bystrica CEEA 2017 Košice, 2 3 Prečo je dôležitý
Seznam vyšetření biochemie a hematologie
 Seznam vyšetření biochemie a hematologie BIOCHEMIE NÁZEV: Glukosa POUŽITÍ: Stanovení koncentrace glukosy v séru (plazmě) a v moči JEDNOTKY KONCENTRACE: mmol/l (sérum, plazma) g% (sbíraná moč) g (odpad
Seznam vyšetření biochemie a hematologie BIOCHEMIE NÁZEV: Glukosa POUŽITÍ: Stanovení koncentrace glukosy v séru (plazmě) a v moči JEDNOTKY KONCENTRACE: mmol/l (sérum, plazma) g% (sbíraná moč) g (odpad
analyzátor POCT Parametry acidobazické rovnováhy a ionty
 email: inlab@inlab.cz analyzátor POCT Parametry acidobazické rovnováhy a ionty Sodík, draslík, chloridy, ionizovaný vápník, ph a pco 2: Prvky jsou měřeny potenciometricky ion selektivními elektrodami.
email: inlab@inlab.cz analyzátor POCT Parametry acidobazické rovnováhy a ionty Sodík, draslík, chloridy, ionizovaný vápník, ph a pco 2: Prvky jsou měřeny potenciometricky ion selektivními elektrodami.
3 Acidobazické reakce
 3 Acidobazické reakce Brønstedova teorie 1. Uveďte explicitní definice podle Brønstedovy teorie. Kyselina je... Báze je... Konjugovaný pár je... 2. Doplňte tabulku a pojmenujte všechny sloučeniny. Kyselina
3 Acidobazické reakce Brønstedova teorie 1. Uveďte explicitní definice podle Brønstedovy teorie. Kyselina je... Báze je... Konjugovaný pár je... 2. Doplňte tabulku a pojmenujte všechny sloučeniny. Kyselina
Veterinární analyzátor POCT Parametry acidobazické rovnováhy a ionty
 email: inlab@inlab.cz Veterinární analyzátor POCT Parametry acidobazické rovnováhy a ionty Sodík, draslík, chloridy, ionizovaný vápník, ph a pco 2: Prvky jsou měřeny potenciometricky ion selektivními elektrodami.
email: inlab@inlab.cz Veterinární analyzátor POCT Parametry acidobazické rovnováhy a ionty Sodík, draslík, chloridy, ionizovaný vápník, ph a pco 2: Prvky jsou měřeny potenciometricky ion selektivními elektrodami.
 Renální tubulární acidózy Akutní selhání ledvin Prerenální syndrom je dán schopností ledvin udržet v organismu sůl a vodu tváří v tvář zaznamenané hypoperfúzi ledvin. Při obnovení renální hemodynamiky
Renální tubulární acidózy Akutní selhání ledvin Prerenální syndrom je dán schopností ledvin udržet v organismu sůl a vodu tváří v tvář zaznamenané hypoperfúzi ledvin. Při obnovení renální hemodynamiky
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 sp.zn. sukls212686/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Chlorid sodný 0,9% Braun Infuzní roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 000 ml roztoku obsahuje: natrii chloridum Koncentrace
sp.zn. sukls212686/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Chlorid sodný 0,9% Braun Infuzní roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 000 ml roztoku obsahuje: natrii chloridum Koncentrace
František Duška DIABETICKÁ KETOACIDÓZA
 František Duška www.duska.eu DIABETICKÁ KETOACIDÓZA Přehled Povaha acidobazické poruchy role hyperchloridémie Vývoj poruchy v průběhu (protokolizované) léčby Specifika DKA v UK Narozdíl od ČR častá diagnóza:
František Duška www.duska.eu DIABETICKÁ KETOACIDÓZA Přehled Povaha acidobazické poruchy role hyperchloridémie Vývoj poruchy v průběhu (protokolizované) léčby Specifika DKA v UK Narozdíl od ČR častá diagnóza:
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 sp.zn. sukls176277/2011 a sp.zn. sukls129930/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Chlorid sodný 10% Braun koncentrát pro infuzní roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 ml koncentrátu
sp.zn. sukls176277/2011 a sp.zn. sukls129930/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Chlorid sodný 10% Braun koncentrát pro infuzní roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 ml koncentrátu
Vnitřní rozdělení tělních tekutin
 Vnitřní prostředí Spolu s krevním oběhem, plícemi, ledvinami zajišťuje tkáním přísun kyslíku, živin a odsun katabolitů regulace osmolality,, iontového složení, acidobazické rovnováhy a teploty normální
Vnitřní prostředí Spolu s krevním oběhem, plícemi, ledvinami zajišťuje tkáním přísun kyslíku, živin a odsun katabolitů regulace osmolality,, iontového složení, acidobazické rovnováhy a teploty normální
Biochemické vyšetření
 Biochemické vyšetření Biochemické vyšetření ke zjištění malnutricí z nedostatku Biochemické vyšetření malnutricí z nadbytečného příjmu vyšetření z nadbytku Plasmatické proteiny Hodnocení k určení proteinových
Biochemické vyšetření Biochemické vyšetření ke zjištění malnutricí z nedostatku Biochemické vyšetření malnutricí z nadbytečného příjmu vyšetření z nadbytku Plasmatické proteiny Hodnocení k určení proteinových
Příloha č. 2 k rozhodnutí o změně registrace sp.zn.sukls43951/2010
 Příloha č. 2 k rozhodnutí o změně registrace sp.zn.sukls43951/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Hydrogenuhličitan sodný 4,2% (w/v) - BRAUN infuzní roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ
Příloha č. 2 k rozhodnutí o změně registrace sp.zn.sukls43951/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Hydrogenuhličitan sodný 4,2% (w/v) - BRAUN infuzní roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ
Chemické výpočty II. Vladimíra Kvasnicová
 Chemické výpočty II Vladimíra Kvasnicová Převod jednotek pmol/l nmol/l µmol/l mmol/l mol/l 10-12 10-9 10-6 10-3 mol/l µg mg g 10-6 10-3 g µl ml dl L 10-6 10-3 10-1 L Cvičení 12) cholesterol (MW=386,7g/mol):
Chemické výpočty II Vladimíra Kvasnicová Převod jednotek pmol/l nmol/l µmol/l mmol/l mol/l 10-12 10-9 10-6 10-3 mol/l µg mg g 10-6 10-3 g µl ml dl L 10-6 10-3 10-1 L Cvičení 12) cholesterol (MW=386,7g/mol):
Homeostáza vody a iontů
 Homeostáza vody a iontů 1 Homeostasa Je stálost vnitřního prostředí Tělesna teplota distribuce vody ph Koncentrace iontů, glukosy, Základní regulační mechanismus je zpětná vazba 2 3 Voda v lidském těle
Homeostáza vody a iontů 1 Homeostasa Je stálost vnitřního prostředí Tělesna teplota distribuce vody ph Koncentrace iontů, glukosy, Základní regulační mechanismus je zpětná vazba 2 3 Voda v lidském těle
RENÁLNÍ INSUFICIENCE TRANSPLANTACE LEDVIN. Markéta Vojtová VOŠZ a SZŠ Hradec králové
 RENÁLNÍ INSUFICIENCE TRANSPLANTACE LEDVIN Markéta Vojtová VOŠZ a SZŠ Hradec králové Renální insuficience 1 Neschopnost ledvin plnit svoji funkci Vylučování dusíkatých látek kyselých katabolitů Vody Elektrolytů
RENÁLNÍ INSUFICIENCE TRANSPLANTACE LEDVIN Markéta Vojtová VOŠZ a SZŠ Hradec králové Renální insuficience 1 Neschopnost ledvin plnit svoji funkci Vylučování dusíkatých látek kyselých katabolitů Vody Elektrolytů
1. Poruchy glomerulární filtrace
 LEDVINY 1. Poruchy glomerulární filtrace 2. Nefrotický syndrom 3. Poruchy činnosti tubulů 4. Oligurie, polyurie 5. Nefrolithiasis 6. Průtok krve ledvinou a jeho poruchy 7. Akutní selhání ledvin 8. Chronické
LEDVINY 1. Poruchy glomerulární filtrace 2. Nefrotický syndrom 3. Poruchy činnosti tubulů 4. Oligurie, polyurie 5. Nefrolithiasis 6. Průtok krve ledvinou a jeho poruchy 7. Akutní selhání ledvin 8. Chronické
Diabetická ketoacidóza a edém mozku
 Diabetická ketoacidóza a edém mozku Michal Šitina, Jan Maňák Klinika gerontologická a metabolická FN Hradec Králové Interní JIP Kazuistika muž 40 let, DM 1. typu nalezen v motelu soporozní, výrazná dehydatace,
Diabetická ketoacidóza a edém mozku Michal Šitina, Jan Maňák Klinika gerontologická a metabolická FN Hradec Králové Interní JIP Kazuistika muž 40 let, DM 1. typu nalezen v motelu soporozní, výrazná dehydatace,
 OBECNÁ CHEMIE František Zachoval CHEMICKÉ ROVNOVÁHY 1. Rovnovážný stav, rovnovážná konstanta a její odvození Dlouhou dobu se chemici domnívali, že jakákoliv chem.
OBECNÁ CHEMIE František Zachoval CHEMICKÉ ROVNOVÁHY 1. Rovnovážný stav, rovnovážná konstanta a její odvození Dlouhou dobu se chemici domnívali, že jakákoliv chem.
Intoxikace metanolem a odběr orgánů. Peter Sklienka KARIM FN Ostrava
 Intoxikace metanolem a odběr orgánů Peter Sklienka KARIM FN Ostrava Intoxikace a odběr orgánů Problém transplantace orgánů od intoxikovaných dárců: Legislativa Orgánově specifická toxicita Možný transfer
Intoxikace metanolem a odběr orgánů Peter Sklienka KARIM FN Ostrava Intoxikace a odběr orgánů Problém transplantace orgánů od intoxikovaných dárců: Legislativa Orgánově specifická toxicita Možný transfer
SCHVÁLENO SL \TN STĺ-\\! PRO kontrolu LĚČ\J. Příloha č. 2 k rozhodnutí o změně registrace sp.zn.suk1s44379/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 2 k rozhodnutí o změně registrace sp.zn.suk1s44379/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU SL \TN STĺ-\\! PRO kontrolu LĚČ\J SCHVÁLENO I 2-05- 2010 1. NÁZEV PŘÍPRAVKU Hydrogenuhličitan sodný 8,4% (w/v)
Příloha č. 2 k rozhodnutí o změně registrace sp.zn.suk1s44379/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU SL \TN STĺ-\\! PRO kontrolu LĚČ\J SCHVÁLENO I 2-05- 2010 1. NÁZEV PŘÍPRAVKU Hydrogenuhličitan sodný 8,4% (w/v)
Faktory ovlivňující úspěšnost embryologické laboratoře
 Faktory ovlivňující úspěšnost embryologické laboratoře P. Trávník Sanatorium REPROMEDA s.r.o. 1 Úspěšnost AR ovlivňuje řada faktorů, něco jsme věděli, některé jsme poznali v průběhu let 1990 Sanatorium
Faktory ovlivňující úspěšnost embryologické laboratoře P. Trávník Sanatorium REPROMEDA s.r.o. 1 Úspěšnost AR ovlivňuje řada faktorů, něco jsme věděli, některé jsme poznali v průběhu let 1990 Sanatorium
Těžká laktátová acidosa. Daniel Nalos, Věra Vondráková, Pavel Neumann. KAPIM Ústí nad Labem
 Těžká laktátová acidosa Daniel Nalos, Věra Vondráková, Pavel Neumann. KAPIM Ústí nad Labem Anamnesa 74 letá paní, žijící ve společné domácnosti s manželem, v chronické medikaci Letrox 1 tbl. Cilkanol 1tbl,
Těžká laktátová acidosa Daniel Nalos, Věra Vondráková, Pavel Neumann. KAPIM Ústí nad Labem Anamnesa 74 letá paní, žijící ve společné domácnosti s manželem, v chronické medikaci Letrox 1 tbl. Cilkanol 1tbl,
Krevní plazma organické a anorganické součásti, význam minerálů a bílkovin krevní plazmy. Somatologie Mgr. Naděžda Procházková
 Krevní plazma organické a anorganické součásti, význam minerálů a bílkovin krevní plazmy. Somatologie Mgr. Naděžda Procházková Krevní plazma definice: Tekutá složka krve Nažloutlá, vazká tekutina Složení
Krevní plazma organické a anorganické součásti, význam minerálů a bílkovin krevní plazmy. Somatologie Mgr. Naděžda Procházková Krevní plazma definice: Tekutá složka krve Nažloutlá, vazká tekutina Složení
NEMOCNÝ S JATERNÍ CIRHÓZOU kazuistika jako prostředek výuky klinické biochemie
 NEMOCNÝ S JATERNÍ CIRHÓZOU kazuistika jako prostředek výuky klinické biochemie Jaroslav Racek Ústav klinické biochemie a hematologie LF UK a FN v Plzni Pracovní den Sekce biochemických laborantů ČSKB,
NEMOCNÝ S JATERNÍ CIRHÓZOU kazuistika jako prostředek výuky klinické biochemie Jaroslav Racek Ústav klinické biochemie a hematologie LF UK a FN v Plzni Pracovní den Sekce biochemických laborantů ČSKB,
sp.zn. sukls62825/2018 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Ardeaelytosol H 1/1 infuzní roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
 sp.zn. sukls62825/2018 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Ardeaelytosol H 1/1 infuzní roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1000 ml infuzního roztoku obsahuje: Natrii chloridum Kalii
sp.zn. sukls62825/2018 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Ardeaelytosol H 1/1 infuzní roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1000 ml infuzního roztoku obsahuje: Natrii chloridum Kalii
sp.zn. sukls62825/2018 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Ardeaelytosol F 1/1 9 g/l infuzní roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
 sp.zn. sukls62825/2018 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Ardeaelytosol F 1/1 9 g/l infuzní roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1000 ml infuzního roztoku obsahuje: Natrii chloridum
sp.zn. sukls62825/2018 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Ardeaelytosol F 1/1 9 g/l infuzní roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1000 ml infuzního roztoku obsahuje: Natrii chloridum
OŠETŘOVATELSTVÍ PRO STŘEDNÍ ZDRAVOTNICKÉ ŠKOLY 2. ROČNÍK / 2. díl
 OŠETŘOVATELSTVÍ PRO STŘEDNÍ ZDRAVOTNICKÉ ŠKOLY 2. ROČNÍK / 2. díl Hlavní autorka a editorka: PhDr. Jarmila Kelnarová, Ph.D. Autorský kolektiv: PhDr. Jarmila Kelnarová, Ph.D., Mgr. Martina Cahová, Mgr.
OŠETŘOVATELSTVÍ PRO STŘEDNÍ ZDRAVOTNICKÉ ŠKOLY 2. ROČNÍK / 2. díl Hlavní autorka a editorka: PhDr. Jarmila Kelnarová, Ph.D. Autorský kolektiv: PhDr. Jarmila Kelnarová, Ph.D., Mgr. Martina Cahová, Mgr.
Vladimír Šrámek ARK, FNUSA v Brně Colors of Sepsis,
 hypernatrémie Vladimír Šrámek ARK, FNUSA v Brně Colors of Sepsis, 29.1.-1.2.2019 proč jsem vybral toto téma regulace Na + je zásadní pro homeostázu regulace a léčba poruch ostatních iontů jsou méně komplikované
hypernatrémie Vladimír Šrámek ARK, FNUSA v Brně Colors of Sepsis, 29.1.-1.2.2019 proč jsem vybral toto téma regulace Na + je zásadní pro homeostázu regulace a léčba poruch ostatních iontů jsou méně komplikované
Seznam vyšetření biochemie a hematologie
 Seznam vyšetření biochemie a hematologie BIOCHEMIE NÁZEV: Glukosa POUŽITÍ: Stanovení koncentrace glukosy v séru (plazmě) a v moči JEDNOTKY KONCENTRACE: mmol/l (sérum, plazma) g% (sbíraná moč) g (odpad
Seznam vyšetření biochemie a hematologie BIOCHEMIE NÁZEV: Glukosa POUŽITÍ: Stanovení koncentrace glukosy v séru (plazmě) a v moči JEDNOTKY KONCENTRACE: mmol/l (sérum, plazma) g% (sbíraná moč) g (odpad
Změny osmolality vnitřního prostředí vyšetřovací metody a interpretace
 Změny osmolality vnitřního prostředí vyšetřovací metody a interpretace Voda a elektrolyty jsou hlavními složkami vnitřního prostředí. Tělesná voda celková tělesná voda CTV je 50 70 % celkové tělesné hmotnosti
Změny osmolality vnitřního prostředí vyšetřovací metody a interpretace Voda a elektrolyty jsou hlavními složkami vnitřního prostředí. Tělesná voda celková tělesná voda CTV je 50 70 % celkové tělesné hmotnosti
Renální tubulární acidózy VKP
 Akutní selhání ledvin Renální tubulární acidózy VKP- 31.3.2008 Způsobeno významným poklesem glomerulární filtrace a exkrečních funkcí obou ledvin náhle vzniklá neschopnost ledvin přiměřeně regulovat solnou
Akutní selhání ledvin Renální tubulární acidózy VKP- 31.3.2008 Způsobeno významným poklesem glomerulární filtrace a exkrečních funkcí obou ledvin náhle vzniklá neschopnost ledvin přiměřeně regulovat solnou
Globální respirační insuficience kazuistika
 Globální respirační insuficience kazuistika Radovan Uvízl Klinika anestezie, resuscitace a intenzivní medicíny LF UP a FN Tvorba a ověření e-learningového prostředí pro integraci výuky preklinických a
Globální respirační insuficience kazuistika Radovan Uvízl Klinika anestezie, resuscitace a intenzivní medicíny LF UP a FN Tvorba a ověření e-learningového prostředí pro integraci výuky preklinických a
VO V DA D A VODN D Í BIL I AN A CE C
 VODA A VODNÍ BILANCE Voda Základní složka živého organismu Hlavní funkce vody: Prostřed edí pro životní děje Rozpouštědlo pro živiny Tepelné hospodářstv ství Udržen ení koloidů v rozpuštěném m stavu Reaktant
VODA A VODNÍ BILANCE Voda Základní složka živého organismu Hlavní funkce vody: Prostřed edí pro životní děje Rozpouštědlo pro živiny Tepelné hospodářstv ství Udržen ení koloidů v rozpuštěném m stavu Reaktant
Jana Fauknerová Matějčková
 Jana Fauknerová Matějčková po 2 arteriální krev 13,33 kpa (100 mm Hg) venózní krev 5,33 kpa (40 mm Hg) pco 2 arteriální krev 5,33 kpa (40 mm Hg) venózní krev 6,13 kpa (46 mm Hg) Hb váže 4 molekuly kyslíku
Jana Fauknerová Matějčková po 2 arteriální krev 13,33 kpa (100 mm Hg) venózní krev 5,33 kpa (40 mm Hg) pco 2 arteriální krev 5,33 kpa (40 mm Hg) venózní krev 6,13 kpa (46 mm Hg) Hb váže 4 molekuly kyslíku
Městnavé srdeční selhání Centrální žilní tlak
 Městnavé srdeční selhání Centrální žilní tlak Radovan Uvízl Klinika anestezie, resuscitace a intenzivní medicíny LF UP a FN Tvorba a ověření e-learningového prostředí pro integraci výuky preklinických
Městnavé srdeční selhání Centrální žilní tlak Radovan Uvízl Klinika anestezie, resuscitace a intenzivní medicíny LF UP a FN Tvorba a ověření e-learningového prostředí pro integraci výuky preklinických
Příloha č.2 k rozhodnutí o změně registrace sp.zn. sukls42312/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č.2 k rozhodnutí o změně registrace sp.zn. sukls42312/2012 1. NÁZEV PŘÍPRAVKU SOUHRN ÚDAJŮ O PŘÍPRAVKU bez 2 mmol/l 3 mmol/l 4 mmol/l Roztok pro hemofiltraci 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Příloha č.2 k rozhodnutí o změně registrace sp.zn. sukls42312/2012 1. NÁZEV PŘÍPRAVKU SOUHRN ÚDAJŮ O PŘÍPRAVKU bez 2 mmol/l 3 mmol/l 4 mmol/l Roztok pro hemofiltraci 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Biochemické a hematologické metody a jejich interpretace
 Biochemické a hematologické metody a jejich interpretace OBSAH Str. ABR 1 Albumin 15 ALP 17 ALT 18 Amniová tekutina na fosfolipidy 19 Amoniak 20 AMS 22 Anorganický fosfor (ip) 24 AT III 26 Apolipoprotein
Biochemické a hematologické metody a jejich interpretace OBSAH Str. ABR 1 Albumin 15 ALP 17 ALT 18 Amniová tekutina na fosfolipidy 19 Amoniak 20 AMS 22 Anorganický fosfor (ip) 24 AT III 26 Apolipoprotein
Chronické selhání ledvin. Kamil Ševela
 Chronické selhání ledvin Kamil Ševela CHRONICKÉ SELHÁNÍ LEDVIN: perfúze ledvin: 20 25% minutového srdečního výdeje renální selhání je vždy spojeno s katabolizmem bílkovin: otoky dušnost zvýšená incidence
Chronické selhání ledvin Kamil Ševela CHRONICKÉ SELHÁNÍ LEDVIN: perfúze ledvin: 20 25% minutového srdečního výdeje renální selhání je vždy spojeno s katabolizmem bílkovin: otoky dušnost zvýšená incidence
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Resical prášek pro přípravu perorální nebo rektální suspenze 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ prášku obsahuje: 1 g prášku obsahuje: Calcii polystyrensulfonas
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Resical prášek pro přípravu perorální nebo rektální suspenze 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ prášku obsahuje: 1 g prášku obsahuje: Calcii polystyrensulfonas
Autor kapitoly: MUDr.Pavel Pick, Ústav klinické biochemie VFN a 1.LF UK Praha
 Poruchy acidobazické regulace Autor kapitoly: MUDr.Pavel Pick, Ústav klinické biochemie VFN a 1.LF UK Praha 1. Úvod Poruchy acidobazické regulace (ABR) jsou stavy, které vznikají v úzké souvislosti se
Poruchy acidobazické regulace Autor kapitoly: MUDr.Pavel Pick, Ústav klinické biochemie VFN a 1.LF UK Praha 1. Úvod Poruchy acidobazické regulace (ABR) jsou stavy, které vznikají v úzké souvislosti se
LCH/PAK01. 5 hodin cvičení
 Studijní program : Porodní asistence bakalářské studium - kombinovaná forma Název předmětu : Klinická biochemie Rozvrhová zkratka : LCH/PAK01 Rozvrh výuky : 5 hodin přednášek 5 hodin cvičení Zařazení výuky
Studijní program : Porodní asistence bakalářské studium - kombinovaná forma Název předmětu : Klinická biochemie Rozvrhová zkratka : LCH/PAK01 Rozvrh výuky : 5 hodin přednášek 5 hodin cvičení Zařazení výuky
REHYDRATACE TELAT NENÍ JEN OTÁZKOU PŘÍJMU TEKUTIN
 REHYDRATACE TELAT NENÍ JEN OTÁZKOU PŘÍJMU TEKUTIN ELEKTROLYTY ACETÁT ENERGIE (dextróza a glycin) OBOHACENO LAKTOFERINEM PRŮJEM U TELAT DŮSLEDKY ZTRÁT STOLICÍ STAVY KE KOREKCI DEHYDRATACE Hypoxie Svaly
REHYDRATACE TELAT NENÍ JEN OTÁZKOU PŘÍJMU TEKUTIN ELEKTROLYTY ACETÁT ENERGIE (dextróza a glycin) OBOHACENO LAKTOFERINEM PRŮJEM U TELAT DŮSLEDKY ZTRÁT STOLICÍ STAVY KE KOREKCI DEHYDRATACE Hypoxie Svaly
Anorganické látky v buňkách - seminář. Petr Tůma některé slidy převzaty od V. Kvasnicové
 Anorganické látky v buňkách - seminář Petr Tůma některé slidy převzaty od V. Kvasnicové Zastoupení prvků v přírodě anorganická hmota kyslík (O) 50% křemík (Si) 25% hliník (Al) 7% železo (Fe) 5% vápník
Anorganické látky v buňkách - seminář Petr Tůma některé slidy převzaty od V. Kvasnicové Zastoupení prvků v přírodě anorganická hmota kyslík (O) 50% křemík (Si) 25% hliník (Al) 7% železo (Fe) 5% vápník
Elektrochemie. Předmět elektrochemie: disociace (roztoky elektrolytů, taveniny solí) vodivost. jevy na rozhraní s/l (elektrolýza, články)
 Elektrochemie 1/30 Předmět elektrochemie: disociace (roztoky elektrolytů, taveniny solí) vodivost jevy na rozhraní s/l (elektrolýza, články) Vodiče: vodivost způsobena pohybem elektronů uvnitř mřížky:
Elektrochemie 1/30 Předmět elektrochemie: disociace (roztoky elektrolytů, taveniny solí) vodivost jevy na rozhraní s/l (elektrolýza, články) Vodiče: vodivost způsobena pohybem elektronů uvnitř mřížky:
