Acidobazická rovnováha (ABR)
|
|
|
- Miroslava Dvořáková
- před 9 lety
- Počet zobrazení:
Transkript
1 Acidobazická rovnováha (ABR) Definice ph ph = log c(h + ) ph = 7,4 c(h + ) = 40 nm (H + ) = ph kyselina látka odštěpující H + (Arrhenius) nebo donor H + (Brönsted) zásada látka odštěpující OH (Arrhenius) nebo akceptor H + (Brönsted) disociační konstanta HA H + + A K = [H + ] x [A ] / [HA] pk = log K pufry systémy zmírňující výkyvy ph po přidání kyseliny nebo zásady Zdroj kyselin: Osud kyselin: Zdroj zásad: hlavně metabolismus další metabolické přeměny nebo vyloučení z organismu hlavně potrava Metabolické kyseliny (tj. netěkavé vylučovány ledvinami) glukóza kyselina mléčná laktát + H + mastné kyseliny ketolátky: kyselina acetoctová acetacetát + H + (pk = 3,8) kyselina βhydroxymáselná βhydroxybutyrát + H + (pk = 4,4) aminokyseliny obsahující síru (Cys, Met): SH H 2 SO 4 sulfát + 2 H + fosfolipidy H 3 PO 4 2 H + + HPO 4 2 (pk 3 = 12,7 do třetího stupně nedisociuje) (denně vyloučeno: 70 mmol netěkavých kyselin, hlavně fosfátů a sulfátů) Respirační kyselina (tj. těkavá: vydýchatelná vylučována plícemi) CO 2 + H 2 O H 2 CO 3 HCO 3 + H + (denně vyloučeno: mmol CO 2 ) Potraviny a) acidifikující organismus: volné kyseliny nebo látky, jejichž metabolismem kyseliny vznikají (normálně jsou většinou kompletně zoxidovány na CO 2 a vodu); při překročení kapacity pufrů: ph (viz. vylučování kyselin z organismu ledvinami: ph moči je kyselejší než ph krve = kyseliny jsou odpadním produktem metabolismu) b) alkalizující organismus: dodávají do těla báze, přispívají ke zvýšení koncentrace HCO 3 (ovoce, zelenina obsahují soli organických kyselin) Pořadí systémů zodpovídajících za udržování ABR: 1. pufry (regulují především výkyvy ph při běžném metabolismu: krátkodobá, akutní regulace několik sec.) 2. plíce (rychlá regulace pco 2 minuty, hodiny) 3. ledviny (zadržování nebo vylučování H + vliv na vylučování nebo vstřebávání HCO 3 ) Na udržování ph krve se podílí také játra (syntéza močoviny, přeměna laktátu) a myokard (oxidace ketolátek). játra: a) NH 4 + močovina + 2 H + okyselení organismu CO NH 4 + CO(NH 2 ) H + + H 2 O H + + HCO 3 H 2 O + CO 2 (spotřeba HCO 3 ) b) NH 4 + syntéza glutaminu netvoří se H +, glutamin je vychytáván ledvinami vylučování H + ve formě NH 4 + 1
2 Pufry celkem bikarbonátový: HCO 3 / CO 2! otevřený systém: neustále vylučován a opět doplňován mtb! * fosfátový: HPO 2 4 / H 2 PO 4 anorganický nebo organicky vázaný (= estery: meziprodukty mtb) hemoglobin: Hb / HbH + pk (HHbO 2 ) = 6,17 pk (HHb) = 7,82 proteiny: proteiny / proteinh + (viz. kyselé a zásadité aminokyseliny) HandersonHasselbalchova rovnice ph = pk + log c s / c k c s báze pufru c k nedisociovaná slabá kyselina ph = pk + log (HCO 3 / CO 2 ) = pk + log (HPO 2 4 / H 2 PO 4 ) = pk + log (Hb / HbH + ) 7,4 = pk H2CO3 + log (HCO 3 / α x pco 2 ) = pk H2PO4 + log (HPO 2 4 / H 2 PO 4 ) = pk HbH + log (Hb / HbH + ) α = faktor konverze přepočet tlaku CO 2 na molární koncentraci v mmol/l jeli pco 2 v kpa α = 0,226 jeli pco 2 v Torr α = 0,03 pufry nejlépe pufrují při ph = pk ± 1 ph = pk + log (1 / 1) ph = pk při c s = c k ph = pk + log (10 / 1) ph = pk + 1 při c s = 10x vyšší než c k ph = pk + log (1 / 10) ph = pk 1 při c s = 10x nižší než c k Ze vztahu mezi hodnotami ph a pk lze naopak také vypočítat poměr koncentrací báze / kyselina: při ph > pk je c s > c k (viz. např. ph = pk + 1) rovnováha reakce HA H + + A je posunuta vpravo ph < pk je c s < c k (viz. např. ph = pk 1) rovnováha reakce HA H + + A je posunuta vlevo ph = pk je c s = c k reakce zleva do prava a zpět probíhá stejně rychle složení pufračních systémů (poměr báze / kyselina) lze pro dané ph tělních tekutin odhadnout z pk HA pk H2CO3 = 6,1 HCO 3 / CO 2 20 / 1 při ph = 7,4 7,4 = (6,1 + log 20) = 6,1 + 1,3 = 7,4 pk H2PO4 7,0 HPO 4 2 / H 2 PO 4 v krvi (ph = 7,4) převažuje HPO 4 2, v moči (ph = 6) H 2 PO 4 (ph > pk) (báze) (ph < pk) (kys.) * [HCO 3 ] / [CO 2 ] 20 / 1 = 20 přídavek H + HCO 3 + H + H 2 CO 3 H 2 O + CO 2 (tj. HCO 3 a CO 2 ) [HCO 3 ] / [CO 2 ] (20 1) / (1 + 1) = 19 / 2 = 9,5 ale CO 2 je vydýchán ( otevřený systém ) [HCO 3 ] / [CO 2 ] (20 1) / (1 + 0) = 19 / 1 = 19 poměr [HCO 3 ] / [CO 2 ] se změní nepatrně pouze malá změna ph hydrogenuhličitan = bicarbonicum (lat.), bicarbonate (angl.) 2
3 Hlavní pufrační systémy lokalizace pufry komentář ISF bikarbonátový pufruje metabolické kyseliny fosfátový proteiny nízká koncentrace malý význam nízká koncentrace malý význam krev bikarbonátový pufruje metabolické kyseliny hemoglobin plazmatické proteiny fosfátový pufruje CO 2 (vznik kyseliny uhličité) minoritní ICF proteiny významný pufr fosfátový nízká koncentrace malý význam významný pufr moč fosfátový odpovídá za většinu tzv. titrovatelné acidity moči amoniakální významný: odstraňování aminodusíku i protonů; kation! Pufry krve pufr plazma erytrocyty celkem HCO 3 / CO 2 35 % 18 % 53 % Hb / HbH + 35 % 35 % plazmatické proteiny 7 % 7 % anorganický fosfát 1 % 1 % 2 % organický fosfát 3 % 3 % 43 % 57 % 100 % Vylučování CO 2 plícemi viz. Biochemie krve a dýchání Vylučování protonů ledvinami (koncentrační gradient: v moči je až 1000x vyšší koncentrace protonů než v buňce) proximální tubulus: vylučování H + výměnou za vstřebaný Na + (luminální membrána, antiport) Na/KATPáza na bazální straně distální tubulus: aktivní (ATP) sekrece H + proximální tubulus: Na + HCO 3 Na + (vstřebává se) a H + (vylučován) H + + HCO 3 H 2 CO 3 H 2 CO 3 H 2 O + CO 2 CO 2 se vstřebá a v tubulární buňce opět rozpadne na H + a HCO 3 kyselá moč: a) vstřebávání HCO 3 b) pufrování fosfátovým pufrem (ph moči < pk H2PO4 ): H + + HPO 4 2 H 2 PO 4 c) vylučování H + ve formě NH 4 + Vylučování H + a K + ledvinami je stimulováno aldosteronem (výměna H + za vstřebaný Na +!). resorpce HCO 3 Kalémie acidóza vyplavování K + z buněk hyperkalémie ztráty K + močí (při následné rychlé alkalizaci organismu se K + vrací do buňky, což vede k hypokalémii nebezpečí hlavně pro srdce přenos signálu na membráně) alkalóza K + nahrazuje nedostatek H + v buňkách pokles K + v krvi hypokalémie; místo H + se do moči vylučuje K + (výměnou za Na + ) 3
4 Pufrování moči 1) za každý vyloučený H + se vstřebá 1 HCO 3 (pk = 6,1) 2) v kyselé moči: nadbytek H + + HPO 4 2 H 2 PO 4 vylučování spolu s kationtem (pk = 6,7 7,2) 3) vylučovaný aminodusík váže H + : NH 3 + H + NH 4 + (chronická acidóza méně urey, více NH 4 + ) vylučování aminodusíku může být silně redukováno nebo naopak velmi zvýšeno ( aktivity glutaminázy v ledvinách = při chronické acidóze); glutamináza štěpí Gln na Glu a NH 4 + vyloučen do moče Jako H 2 PO 4 se vyloučí 20 mmol H + (tzv. titrovatelná acidita moči), jako NH mmol H + za den. (pk NH4+ = 9,3; tj. v moči je amoniak protonizován, reakce NH 4 + H + + NH 3 probíhá zprava do leva) Resorpce fosfátů do krve parathirin, kalcitonin: inhibují resorpci kalcitriol: aktivuje resorpci Fyziologické hodnoty ABR (dle NČLP) ph 7,36 7,44 po 2 8,9 14,7 kpa pco 2 4,80 5,90 kpa [HCO 3 ] 24 ± 2 mm BE 0 ± 2,5 mm (base excess = nadbytek bází; jeli hodnota negativní, jde o nedostatek bází) Poruchy ABR (akutní nebo kompenzované) klinicky definovány podle změn bikarbonátového systému a) respirační = primární poruchou je změna pco 2 (porucha respirace) hyper nebo hypokapnie b) metabolické = primární poruchou je změna koncentrace HCO 3 ( pufrováním metabolických kyselin nebo zvýšeným vylučováním / ztrátami z organismu) acidóza nahromadění kyselých nebo ztráta alkalických metabolitů alkalóza nahromadění alkalických nebo ztráta kyselých metabolitů Kompenzace snaha organismu o normalizaci ph při delším trvání poruchy jeden systém nahrazuje porušenou funkci systému jiného. Cílem je vrátit ph co nejblíže k fyziologické hodnotě. respirační poruchy jsou kompenzovány ledvinami kyselá nebo alkalická moč (3 5 dní) metabolické poruchy jsou kompenzovány plícemi hyper nebo hypoventilace (12 24 hodin) nebo korigovány ledvinami (korekce) Příčiny acidózy respirační: hypoventilace ( pco 2 ) metabolická: vážné průjmy ( HCO 3 ), DM (ketoacidóza), vytrvalé cvičení, hypoxie ( laktátu), urémie Příčiny alkalózy respirační: hyperventilace ( pco 2 ) metabolická: zvracení ( HCl), alkalizující léky 4
5 Respirační acidóza (RAc) příčina: hypoventilace CO 2 + H 2 O H 2 CO 3 HCO 3 + H + H + + Hb HbH + nárůst pco 2 pokles ph nárůst HCO 3 a úbytek bází jiných pufrů, hlavně Hb BE = 0 při po 2 laktátu (kombinace s MAc) kompenzace: vstřebávání HCO 3 ledvinami (kyselá moč) pozitivní BE (= pufrování úbytek báze) Při pco 2 dochází k aktivaci dechového centra, jeho vnímavost však klesá při hodnotách pco 2 nad 8 kpa jediným stimulem se pak stává po 2. Respirační alkalóza (RAl) příčina: hyperventilace CO 2 + H 2 O H 2 CO 3 HCO 3 + H + HbH + Hb + H + (= pufrování nárůst báze) pokles pco 2 vzrůst ph úbytek HCO 3 a nárůst bází jiných pufrů BE = 0 alkalické ph: protein + Ca 2+ Caproteinát + 2 H + pokles konc. Ca 2+ v plazmě (otevření Na + kanálů a zvýšení excitability tetanické křeče) kompenzace: zvýšené vylučování HCO 3 ledvinami negativní BE Metabolická acidóza (MAc) příčina: 1) nadprodukce kyselin (H + ) v metabolismu (ketolátky, laktát, otravy) vysoký anion gap 2) zvýšené vylučování HCO 3 normální anion gap (tzv. hyperchloremická MAc) Anion gap (AG) je hodnota důležitá pro diferenciální diagnostiku. ad1) metabolismus H + H + + HCO 3 H 2 CO 3 H 2 O + CO 2 a H + + báze nebikarbonátových pufrů (= pufrování) hyperventilace (= kompenzace) pokles BE (HCO 3 i jiných bází) + kyselá moč zvýšené vstřebávání HCO 3 ad2) ztráty HCO 3 např. při průjmech, inhibitory CA pokles ph negativní BE kyselá moč ( fosfáty a NH 4 + ), snížené vylučování HCO 3 hluboké dýchání (stimulace dechového centra vysokou koncentrací H + ) později pco 2 (komp.) kompenzace: hyperventilace další pokles HCO 3 Nejčastější je laktátová acidóza (nedostatečná oxygenace krve a tkání, porucha odbourávání laktátu) 5
6 Metabolická alkalóza (MAl) = závažná porucha (hůře snášena i kompenzována než MAc) příčina: 1) zvýšené vylučování protonů (např. zvracení, vstřebávání NaHCO 3 = mineralokortikoidů) 2) zvýšený přísun alkálií H + CO 2 + H 2 O H 2 CO 3 HCO 3 + H + další pufry H + (= pufrování HCO 3 aj. bází pufrů pozitivní BE) protein + Ca 2+ Caproteinát + 2 H + pokles konc. Ca 2+ otevírá Na + kanály zvýšená excitabilita tetanické křeče zvýšení ph pozitivní BE K + v krvi tzv. hypokalemická alkalóza (nadměrné vylučování K + močí) poruchy srdečního rytmu kompenzace: hypoventilace (nedokonalá kompenzace hyperkapnie a hypoxemie) pco 2 Vladimíra Kvasnicová 6
ABR a iontového hospodářství
 Poruchy acidobazické rovnováhy Patobiochemie a diagnostika poruch ABR a iontového hospodářství Regulace kyselosti vnitřního prostředí CO 2 NH 3 tvorba močoviny glutaminu H + HCO - 3 Martin Vejražka, 2007
Poruchy acidobazické rovnováhy Patobiochemie a diagnostika poruch ABR a iontového hospodářství Regulace kyselosti vnitřního prostředí CO 2 NH 3 tvorba močoviny glutaminu H + HCO - 3 Martin Vejražka, 2007
ABR a iontového hospodářství
 Poruchy acidobazické rovnováhy Patobiochemie a diagnostika poruch ABR a iontového hospodářství Připojte se! Room name: ABR http://b.socrative.com Regulace kyselosti vnitřního prostředí CO 2 NH 3 tvorba
Poruchy acidobazické rovnováhy Patobiochemie a diagnostika poruch ABR a iontového hospodářství Připojte se! Room name: ABR http://b.socrative.com Regulace kyselosti vnitřního prostředí CO 2 NH 3 tvorba
Plasma a většina extracelulární
 Acidobazická rovnováha Tato prezentace je přístupná online Fyziologické ph Plasma a většina extracelulární tekutiny ph = 7,40 ± 0,02 Význam stálého ph Na ph závisí vlastnosti bílkovin aktivita enzymů struktura
Acidobazická rovnováha Tato prezentace je přístupná online Fyziologické ph Plasma a většina extracelulární tekutiny ph = 7,40 ± 0,02 Význam stálého ph Na ph závisí vlastnosti bílkovin aktivita enzymů struktura
Acidobazická rovnováha H+ a ph Vodíkový iont se skládá z protonu, kolem něhož neobíhá žádný elektron. Proto je vodíkový iont velmi malý a je
 Acidobazická rovnováha 14.4.2004 H+ a ph Vodíkový iont se skládá z protonu, kolem něhož neobíhá žádný elektron. Proto je vodíkový iont velmi malý a je extrémně reaktivní. Má proto velmi hluboký vliv na
Acidobazická rovnováha 14.4.2004 H+ a ph Vodíkový iont se skládá z protonu, kolem něhož neobíhá žádný elektron. Proto je vodíkový iont velmi malý a je extrémně reaktivní. Má proto velmi hluboký vliv na
Produkce kyselin v metabolismu Těkavé: 15,000 mmol/den kyseliny uhličité, vyloučena plícemi jako CO 2 Netěkavé kyseliny (1 mmol/kg/den) jsou vyloučeny
 Vnitřní prostředí a acidobazická rovnováha 13.12.2004 Vnitřní prostředí Sestává z posuzování složení extracelulární tekutiny z hlediska izohydrie (= optimální koncentrace ph) izoionie (= optimální koncentrace
Vnitřní prostředí a acidobazická rovnováha 13.12.2004 Vnitřní prostředí Sestává z posuzování složení extracelulární tekutiny z hlediska izohydrie (= optimální koncentrace ph) izoionie (= optimální koncentrace
Jana Fauknerová Matějčková
 Jana Fauknerová Matějčková kyselina (HA) acidóza (acidémie) báze (B ) alkalóza (alkalémie) pufr ph = pk + log cs / ca koncentrace [H + ] v krvi udržována pomocí plic, ledvin a jater okolo 40 nm ph = log
Jana Fauknerová Matějčková kyselina (HA) acidóza (acidémie) báze (B ) alkalóza (alkalémie) pufr ph = pk + log cs / ca koncentrace [H + ] v krvi udržována pomocí plic, ledvin a jater okolo 40 nm ph = log
Diagnostika poruch acidobazické rovnováhy
 Návod do cvičení Diagnostika poruch acidobazické rovnováhy Úvod Stálost tzv. vnitřního prostředí je nezbytnou podmínkou života vyšších organismů. Důležitá je zejména hodnota ph. Na hodnotě ph závisí mimo
Návod do cvičení Diagnostika poruch acidobazické rovnováhy Úvod Stálost tzv. vnitřního prostředí je nezbytnou podmínkou života vyšších organismů. Důležitá je zejména hodnota ph. Na hodnotě ph závisí mimo
tělní buňky tělní tekutiny krev erythrocyty 7.28 thrombocyty 7.0 žaludeční šťáva buňky kosterního svalstva duodenální šťáva
 Acidobazická rovnováha homeostasa H + iontů Regulace vnitřního prostředí Udržování osmotické koncetrace solí, minerálů, eáů, Vztahy acidobazické rovnováhy Stálost = acidobazická rovnováha (stav) Regulace
Acidobazická rovnováha homeostasa H + iontů Regulace vnitřního prostředí Udržování osmotické koncetrace solí, minerálů, eáů, Vztahy acidobazické rovnováhy Stálost = acidobazická rovnováha (stav) Regulace
Acidobazická rovnováha
 Acidobazická rovnováha Klepnutím lze upravit styl předlohy podnadpisů. MUDr. Jiří Dvorský, NMB Vnitřní prostředí Pod pojmem vnitřní prostředí chápeme extracelulární tekutinu (včetně jejího složení) omývající
Acidobazická rovnováha Klepnutím lze upravit styl předlohy podnadpisů. MUDr. Jiří Dvorský, NMB Vnitřní prostředí Pod pojmem vnitřní prostředí chápeme extracelulární tekutinu (včetně jejího složení) omývající
Vyšetřování a léčba poruch acidobazické rovnováhy
 Vyšetřování a léčba poruch acidobazické rovnováhy Vladimír Soška Oddělení klinické biochemie Fyziologické hodnoty ABR Parametr Jednotka Normální meze Kritické hodnoty ph 7.35-7.45 < 7.1; > 7.6 pco 2 kpa
Vyšetřování a léčba poruch acidobazické rovnováhy Vladimír Soška Oddělení klinické biochemie Fyziologické hodnoty ABR Parametr Jednotka Normální meze Kritické hodnoty ph 7.35-7.45 < 7.1; > 7.6 pco 2 kpa
Acidobazická rovnováha 11
 Acidobazická rovnováha 11 Iontogram krevní plazmy, AG, SID, BB s, pufrační systémy, hydrogenuhličitanový pufr. Poruchy acidobazické rovnováhy. 1. Jaký je princip měření a? 2. Které kyslíkové parametry
Acidobazická rovnováha 11 Iontogram krevní plazmy, AG, SID, BB s, pufrační systémy, hydrogenuhličitanový pufr. Poruchy acidobazické rovnováhy. 1. Jaký je princip měření a? 2. Které kyslíkové parametry
Výpočty koncentrací. objemová % (objemový zlomek) krvi m. Vsložky. celku. Objemy nejsou aditivní!!!
 Výpočty koncentrací objemová % (objemový zlomek) Vsložky % obj. = 100 V celku Objemy nejsou aditivní!!! Příklad: Kolik ethanolu je v 700 ml vodky (40 % obj.)? Kolik promile ethanolu v krvi bude mít muž
Výpočty koncentrací objemová % (objemový zlomek) Vsložky % obj. = 100 V celku Objemy nejsou aditivní!!! Příklad: Kolik ethanolu je v 700 ml vodky (40 % obj.)? Kolik promile ethanolu v krvi bude mít muž
Poruchy vnitřního prostředí. v intenzivní medicíně
 Poruchy vnitřního prostředí v intenzivní medicíně Vnitřní prostředí = extracelulární tekutina (plazma, intersticiální tekutina) Poruchy objemu a osmolality Poruchy iontů (Na, K, Ca, Mg, Cl) Poruchy acidobazické
Poruchy vnitřního prostředí v intenzivní medicíně Vnitřní prostředí = extracelulární tekutina (plazma, intersticiální tekutina) Poruchy objemu a osmolality Poruchy iontů (Na, K, Ca, Mg, Cl) Poruchy acidobazické
Jana Fauknerová Matějčková
 Jana Fauknerová Matějčková převody jednotek výpočet ph ph vodných roztoků ph silných kyselin a zásad ph slabých kyselin a zásad, disociační konstanta, pk ph pufrů koncentace 1000mg př. g/dl mg/l = = *10000
Jana Fauknerová Matějčková převody jednotek výpočet ph ph vodných roztoků ph silných kyselin a zásad ph slabých kyselin a zásad, disociační konstanta, pk ph pufrů koncentace 1000mg př. g/dl mg/l = = *10000
3.8. Acidobazická regulace
 3.8. Acidobazická regulace Tabulka 3.8. 1: Referenční intervaly Parametr Muži Ženy ph 7,37 7,43 7,37 7,43 pco 2 (kpa) 4,7 6,0 4,3 5,7 - aktuální HCO 3 (mmol/l) 23,6 27,6 21,8 27,2 - standardní HCO 3 (mmol/l)
3.8. Acidobazická regulace Tabulka 3.8. 1: Referenční intervaly Parametr Muži Ženy ph 7,37 7,43 7,37 7,43 pco 2 (kpa) 4,7 6,0 4,3 5,7 - aktuální HCO 3 (mmol/l) 23,6 27,6 21,8 27,2 - standardní HCO 3 (mmol/l)
Chemické výpočty II. Vladimíra Kvasnicová
 Chemické výpočty II Vladimíra Kvasnicová Převod jednotek pmol/l nmol/l µmol/l mmol/l mol/l 10-12 10-9 10-6 10-3 mol/l µg mg g 10-6 10-3 g µl ml dl L 10-6 10-3 10-1 L Cvičení 12) cholesterol (MW=386,7g/mol):
Chemické výpočty II Vladimíra Kvasnicová Převod jednotek pmol/l nmol/l µmol/l mmol/l mol/l 10-12 10-9 10-6 10-3 mol/l µg mg g 10-6 10-3 g µl ml dl L 10-6 10-3 10-1 L Cvičení 12) cholesterol (MW=386,7g/mol):
3 Acidobazické reakce
 3 Acidobazické reakce Brønstedova teorie 1. Uveďte explicitní definice podle Brønstedovy teorie. Kyselina je... Báze je... Konjugovaný pár je... 2. Doplňte tabulku a pojmenujte všechny sloučeniny. Kyselina
3 Acidobazické reakce Brønstedova teorie 1. Uveďte explicitní definice podle Brønstedovy teorie. Kyselina je... Báze je... Konjugovaný pár je... 2. Doplňte tabulku a pojmenujte všechny sloučeniny. Kyselina
3 Acidobazické reakce
 3 Acidobazické reakce Brønstedova teorie 1. Uveďte explicitní definice podle Brønstedovy teorie. Kyselina je... Báze je... Konjugovaný pár je... 2. Doplňte tabulku a pojmenujte všechny sloučeniny. Kyselina
3 Acidobazické reakce Brønstedova teorie 1. Uveďte explicitní definice podle Brønstedovy teorie. Kyselina je... Báze je... Konjugovaný pár je... 2. Doplňte tabulku a pojmenujte všechny sloučeniny. Kyselina
Anorganické látky v buňkách - seminář. Petr Tůma některé slidy převzaty od V. Kvasnicové
 Anorganické látky v buňkách - seminář Petr Tůma některé slidy převzaty od V. Kvasnicové Zastoupení prvků v přírodě anorganická hmota kyslík (O) 50% křemík (Si) 25% hliník (Al) 7% železo (Fe) 5% vápník
Anorganické látky v buňkách - seminář Petr Tůma některé slidy převzaty od V. Kvasnicové Zastoupení prvků v přírodě anorganická hmota kyslík (O) 50% křemík (Si) 25% hliník (Al) 7% železo (Fe) 5% vápník
Diagnostika a léčba poruch acidobazické rovnováhy. J. Vymětal 3. interní klinika nefrologická, revmatologická a endokrinologická
 Diagnostika a léčba poruch acidobazické rovnováhy J. Vymětal 3. interní klinika nefrologická, revmatologická a endokrinologická ph alkalita/acidita vnitřního prostředí 7,4 ± 0,04 mmol/l pco 2 respirační
Diagnostika a léčba poruch acidobazické rovnováhy J. Vymětal 3. interní klinika nefrologická, revmatologická a endokrinologická ph alkalita/acidita vnitřního prostředí 7,4 ± 0,04 mmol/l pco 2 respirační
Acidobazické regulace
 ZÁKLADY OBECNÉ A KLINICKÉ BIOCHEMIE 2004 Acidobazické regulace Antonín Kazda kapitola ve skriptech 3.8 Klasifikace acidobazických ch poruch Porucha ACIDOSA ALKALOSA I. Respirační PCO2 II. Nerespirační
ZÁKLADY OBECNÉ A KLINICKÉ BIOCHEMIE 2004 Acidobazické regulace Antonín Kazda kapitola ve skriptech 3.8 Klasifikace acidobazických ch poruch Porucha ACIDOSA ALKALOSA I. Respirační PCO2 II. Nerespirační
PARENTERÁLNÍ VÝŽIVA 1
 PARENTERÁLNÍ VÝŽIVA 1 2 3 4 5 6 7 8 9 10 Cukr a tuk: 1/ glukosa je (aerobně) metabolizována na acetyl-coa. Jeho nadbytek, neodbouraný v Krebsově cyklu, může být přeměněn na mastné kyseliny (ev. na cholesterol)
PARENTERÁLNÍ VÝŽIVA 1 2 3 4 5 6 7 8 9 10 Cukr a tuk: 1/ glukosa je (aerobně) metabolizována na acetyl-coa. Jeho nadbytek, neodbouraný v Krebsově cyklu, může být přeměněn na mastné kyseliny (ev. na cholesterol)
Diagnostika a léčba poruch acidobazické rovnováhy. J. Vymětal 3. interní klinika nefrologická, revmatologická a endokrinologická
 Diagnostika a léčba poruch acidobazické rovnováhy J. Vymětal 3. interní klinika nefrologická, revmatologická a endokrinologická ph alkalita/acidita vnitřního prostředí 7,4 ± 0,04 mmol/l pco 2 respirační
Diagnostika a léčba poruch acidobazické rovnováhy J. Vymětal 3. interní klinika nefrologická, revmatologická a endokrinologická ph alkalita/acidita vnitřního prostředí 7,4 ± 0,04 mmol/l pco 2 respirační
Acidobazická rovnováha. H. Vaverková
 Acidobazická rovnováha H. Vaverková Acidobazická rovnováha ph arteriální krve a intersticiální tekutiny normálně kolísá v rozmezí 7,35-7,45 ph kompatibilní s životem: 6,8-7,8 ph < 7,35 = acidóza, ph >7,45
Acidobazická rovnováha H. Vaverková Acidobazická rovnováha ph arteriální krve a intersticiální tekutiny normálně kolísá v rozmezí 7,35-7,45 ph kompatibilní s životem: 6,8-7,8 ph < 7,35 = acidóza, ph >7,45
Hlavní ukazatele acidobazické rovnováhy
 Hlavní ukazatele acidobazické rovnováhy Pro vyšetření parametrů acidobazické rovnováhy (ABR) se odebírá krev arteriální nebo arterilizovaná. Arteriální krev se odebírá z artérií do heparinizovaných zkumavek
Hlavní ukazatele acidobazické rovnováhy Pro vyšetření parametrů acidobazické rovnováhy (ABR) se odebírá krev arteriální nebo arterilizovaná. Arteriální krev se odebírá z artérií do heparinizovaných zkumavek
Monitoring vnitřního prostředí pacienta
 Monitoring vnitřního prostředí pacienta MVDr. Leona Raušerová -Lexmaulová, Ph.D. Klinika chorob psů a koček VFU Brno Vnitřní prostředí Voda Ionty Bílkoviny Cukry Tuky Důležité faktory Obsah vody Obsah
Monitoring vnitřního prostředí pacienta MVDr. Leona Raušerová -Lexmaulová, Ph.D. Klinika chorob psů a koček VFU Brno Vnitřní prostředí Voda Ionty Bílkoviny Cukry Tuky Důležité faktory Obsah vody Obsah
Acidobazická rovnováha a její poruchy
 Kyseliny y vs. báze Acidobazická rovnováha a její poruchy definice: BronstedLowry (192) normální A:B poměr 1:20 Kyselina: H donor Báze: H akceptor síla je definována jako tendence odevzdat (popř. přijmout)
Kyseliny y vs. báze Acidobazická rovnováha a její poruchy definice: BronstedLowry (192) normální A:B poměr 1:20 Kyselina: H donor Báze: H akceptor síla je definována jako tendence odevzdat (popř. přijmout)
Jana Fauknerová Matějčková
 Jana Fauknerová Matějčková po 2 arteriální krev 13,33 kpa (100 mm Hg) venózní krev 5,33 kpa (40 mm Hg) pco 2 arteriální krev 5,33 kpa (40 mm Hg) venózní krev 6,13 kpa (46 mm Hg) Hb váže 4 molekuly kyslíku
Jana Fauknerová Matějčková po 2 arteriální krev 13,33 kpa (100 mm Hg) venózní krev 5,33 kpa (40 mm Hg) pco 2 arteriální krev 5,33 kpa (40 mm Hg) venózní krev 6,13 kpa (46 mm Hg) Hb váže 4 molekuly kyslíku
Metabolismus aminokyselin 2. Vladimíra Kvasnicová
 Metabolismus aminokyselin 2 Vladimíra Kvasnicová Odbourávání AMK 1) odstranění aminodusíku z molekuly AMK 2) detoxikace uvolněné aminoskupiny 3) metabolismus uhlíkaté kostry AMK 7 produktů 7 degradačních
Metabolismus aminokyselin 2 Vladimíra Kvasnicová Odbourávání AMK 1) odstranění aminodusíku z molekuly AMK 2) detoxikace uvolněné aminoskupiny 3) metabolismus uhlíkaté kostry AMK 7 produktů 7 degradačních
 Renální tubulární acidózy Akutní selhání ledvin Prerenální syndrom je dán schopností ledvin udržet v organismu sůl a vodu tváří v tvář zaznamenané hypoperfúzi ledvin. Při obnovení renální hemodynamiky
Renální tubulární acidózy Akutní selhání ledvin Prerenální syndrom je dán schopností ledvin udržet v organismu sůl a vodu tváří v tvář zaznamenané hypoperfúzi ledvin. Při obnovení renální hemodynamiky
P. Schneiderka, Ústav patologické fyziologie LFUP a OKB FN Olomouc
 P. Schneiderka, Ústav patologické fyziologie LFUP a OKB FN Olomouc Acidobazický stav organismu Verze 27.9. 2012 Úvod Za průkopníka znalostí o acidobazickém stavu organismu (ABS) lze považovat amerického
P. Schneiderka, Ústav patologické fyziologie LFUP a OKB FN Olomouc Acidobazický stav organismu Verze 27.9. 2012 Úvod Za průkopníka znalostí o acidobazickém stavu organismu (ABS) lze považovat amerického
Acidobazická rovnováha a její vztahy k iontovému hospodářství. Klinické aplikace.
 Text použit s laskavým svolením autora. Acidobazická rovnováha a její vztahy k iontovému hospodářství. Klinické aplikace. Antonín Jabor Oddělení klinické biochemie Nemocnice Kladno Část 1. Relevantní parametry
Text použit s laskavým svolením autora. Acidobazická rovnováha a její vztahy k iontovému hospodářství. Klinické aplikace. Antonín Jabor Oddělení klinické biochemie Nemocnice Kladno Část 1. Relevantní parametry
Acidobazický stav organismu
 Acidobazický stav organismu Doc. MUDr. Petr Schneiderka CSc. Tvorba a ověření e-learningového prostředí pro integraci výuky preklinických a klinických předmětů na LF UP a FZV UP Reg. č.: CZ.1.07/2.2.00/15.0313
Acidobazický stav organismu Doc. MUDr. Petr Schneiderka CSc. Tvorba a ověření e-learningového prostředí pro integraci výuky preklinických a klinických předmětů na LF UP a FZV UP Reg. č.: CZ.1.07/2.2.00/15.0313
VNITŘNÍ PROSTŘEDÍ. Biochemický ústav LF MU (V.P.) 2007
 1 VNITŘNÍ PROSTŘEDÍ Biochemický ústav LF MU (V.P.) 2007 2 Vnitřní prostředí: Claude Bernard, 1878: Co je vnitřní prostředí? Je to krev, ve skutečnosti však nikoliv celá, nýbrž tekutá část krve, krevní
1 VNITŘNÍ PROSTŘEDÍ Biochemický ústav LF MU (V.P.) 2007 2 Vnitřní prostředí: Claude Bernard, 1878: Co je vnitřní prostředí? Je to krev, ve skutečnosti však nikoliv celá, nýbrž tekutá část krve, krevní
Propojení metabolických drah. Alice Skoumalová
 Propojení metabolických drah Alice Skoumalová Metabolické stavy 1. Resorpční fáze po dobu vstřebávání živin z GIT (~ 2 h) glukóza je hlavní energetický zdroj 2. Postresorpční fáze mezi jídly (~ 2 h po
Propojení metabolických drah Alice Skoumalová Metabolické stavy 1. Resorpční fáze po dobu vstřebávání živin z GIT (~ 2 h) glukóza je hlavní energetický zdroj 2. Postresorpční fáze mezi jídly (~ 2 h po
3 Acidobazické reakce
 3 Acidobazické reakce Brønstedova teorie 1. Uveďte explicitní definice podle Brønstedovy teorie. Kyselina je... Báze je... Konjugovaný pár je... 2. Doplňte tabulku a pojmenujte všechny sloučeniny. Kyselina
3 Acidobazické reakce Brønstedova teorie 1. Uveďte explicitní definice podle Brønstedovy teorie. Kyselina je... Báze je... Konjugovaný pár je... 2. Doplňte tabulku a pojmenujte všechny sloučeniny. Kyselina
Vliv infuzních roztoků na acidobazickou rovnováhu. Antonín Jabor IKEM Praha
 Vliv infuzních roztoků na acidobazickou rovnováhu Antonín Jabor IKEM Praha Fyziologický roztok Fyziologický roztok Incidence hyperchloridemie na konci operace je častá, je spojena s metabolickou acidózou,
Vliv infuzních roztoků na acidobazickou rovnováhu Antonín Jabor IKEM Praha Fyziologický roztok Fyziologický roztok Incidence hyperchloridemie na konci operace je častá, je spojena s metabolickou acidózou,
Těžká laktátová acidosa. Daniel Nalos, Věra Vondráková, Pavel Neumann. KAPIM Ústí nad Labem
 Těžká laktátová acidosa Daniel Nalos, Věra Vondráková, Pavel Neumann. KAPIM Ústí nad Labem Anamnesa 74 letá paní, žijící ve společné domácnosti s manželem, v chronické medikaci Letrox 1 tbl. Cilkanol 1tbl,
Těžká laktátová acidosa Daniel Nalos, Věra Vondráková, Pavel Neumann. KAPIM Ústí nad Labem Anamnesa 74 letá paní, žijící ve společné domácnosti s manželem, v chronické medikaci Letrox 1 tbl. Cilkanol 1tbl,
Homeostáza vody a iontů
 Homeostáza vody a iontů 1 Homeostasa Je stálost vnitřního prostředí Tělesna teplota distribuce vody ph Koncentrace iontů, glukosy, Základní regulační mechanismus je zpětná vazba 2 3 Voda v lidském těle
Homeostáza vody a iontů 1 Homeostasa Je stálost vnitřního prostředí Tělesna teplota distribuce vody ph Koncentrace iontů, glukosy, Základní regulační mechanismus je zpětná vazba 2 3 Voda v lidském těle
Mendelova zemědělská a lesnická univerzita v Brně Agronomická fakulta Ústav morfologie, fyziologie a genetiky zvířat
 Mendelova zemědělská a lesnická univerzita v Brně Agronomická fakulta Ústav morfologie, fyziologie a genetiky zvířat Ukazatele acidobazické rovnováhy krve jalovic v průběhu výkrmu Bakalářská práce Vedoucí
Mendelova zemědělská a lesnická univerzita v Brně Agronomická fakulta Ústav morfologie, fyziologie a genetiky zvířat Ukazatele acidobazické rovnováhy krve jalovic v průběhu výkrmu Bakalářská práce Vedoucí
KAZUISTIKY Z LABORATORNÍ MEDICÍNY
 KAZUISTIKY Z LABORATORNÍ MEDICÍNY Jaroslav Racek Ústav klinické biochemie a hematologie LF UK a FN v Plzni Dialog 2019, zámek Valeč, 7. 9. 4. 2019 KAZUISTIKA I O T R AVA M E T F O R M I N E M A A C E I
KAZUISTIKY Z LABORATORNÍ MEDICÍNY Jaroslav Racek Ústav klinické biochemie a hematologie LF UK a FN v Plzni Dialog 2019, zámek Valeč, 7. 9. 4. 2019 KAZUISTIKA I O T R AVA M E T F O R M I N E M A A C E I
Intermediární metabolismus. Vladimíra Kvasnicová
 Intermediární metabolismus Vladimíra Kvasnicová Vztahy v intermediárním metabolismu (sacharidy, lipidy, proteiny) 1. po jídle (přísun energie z vnějšku) oxidace CO 2, H 2 O, urea + ATP tvorba zásob glykogen,
Intermediární metabolismus Vladimíra Kvasnicová Vztahy v intermediárním metabolismu (sacharidy, lipidy, proteiny) 1. po jídle (přísun energie z vnějšku) oxidace CO 2, H 2 O, urea + ATP tvorba zásob glykogen,
2 Roztoky elektrolytů. Osmotický tlak
 Roztoky elektrolytů. Osmotický tlak 1. Doplněním uvedených schémat vyjádřete rozdílné chování různých typů látek po jejich rozpuštění ve vodě. Použijte symboly AB(aq), A + (aq), B - (aq). [s pevná fáze,
Roztoky elektrolytů. Osmotický tlak 1. Doplněním uvedených schémat vyjádřete rozdílné chování různých typů látek po jejich rozpuštění ve vodě. Použijte symboly AB(aq), A + (aq), B - (aq). [s pevná fáze,
Acidobazická rovnováha - jasně a jednoduše
 Acidobazická rovnováha - jasně a jednoduše Michal Horáček KARIM 2. LF UK v FNM Praha ph, resp. a[h + ] rovnice 4. řádu: 3 nezávisle proměnné, 5 rychlostních konstant po zjednodušení: Acidobazická rovnováha
Acidobazická rovnováha - jasně a jednoduše Michal Horáček KARIM 2. LF UK v FNM Praha ph, resp. a[h + ] rovnice 4. řádu: 3 nezávisle proměnné, 5 rychlostních konstant po zjednodušení: Acidobazická rovnováha
 OBECNÁ CHEMIE František Zachoval CHEMICKÉ ROVNOVÁHY 1. Rovnovážný stav, rovnovážná konstanta a její odvození Dlouhou dobu se chemici domnívali, že jakákoliv chem.
OBECNÁ CHEMIE František Zachoval CHEMICKÉ ROVNOVÁHY 1. Rovnovážný stav, rovnovážná konstanta a její odvození Dlouhou dobu se chemici domnívali, že jakákoliv chem.
FYZIOLOGIE VYLUČOVÁNÍ - exkrece
 FYZIOLOGIE VYLUČOVÁNÍ - exkrece Ex. látek narušující stálost vnitřního prostředí - zbytky a zplodiny metabolizmu - látky momentálně nadbytečné - látky cizorodé (léky, drogy, toxiny...) Ex. fce několika
FYZIOLOGIE VYLUČOVÁNÍ - exkrece Ex. látek narušující stálost vnitřního prostředí - zbytky a zplodiny metabolizmu - látky momentálně nadbytečné - látky cizorodé (léky, drogy, toxiny...) Ex. fce několika
Stewart Fenclův koncept hodnocení poruch ABR
 Stewart Fenclův koncept hodnocení poruch ABR František Duška Klinika anesteziologie a resuscitace a Ústav lék. chemie a biochemie 3. LF UK Motto: Republika nepotřebuje chemiky! Roberspierre při vynášení
Stewart Fenclův koncept hodnocení poruch ABR František Duška Klinika anesteziologie a resuscitace a Ústav lék. chemie a biochemie 3. LF UK Motto: Republika nepotřebuje chemiky! Roberspierre při vynášení
Integrace metabolických drah v organismu. Zdeňka Klusáčková
 Integrace metabolických drah v organismu Zdeňka Klusáčková Hydrolýza a resorpce základních složek potravy Přehled hlavních metabolických drah Biochemie výživy A) resorpční fáze (přísun živin) glukóza hlavní
Integrace metabolických drah v organismu Zdeňka Klusáčková Hydrolýza a resorpce základních složek potravy Přehled hlavních metabolických drah Biochemie výživy A) resorpční fáze (přísun živin) glukóza hlavní
Funkční anatomie ledvin Clearance
 Funkční anatomie ledvin Clearance doc. MUDr. Markéta Bébarová, Ph.D. Fyziologický ústav Lékařská fakulta Masarykovy univerzity Tato prezentace obsahuje pouze stručný výtah nejdůležitějších pojmů a faktů.
Funkční anatomie ledvin Clearance doc. MUDr. Markéta Bébarová, Ph.D. Fyziologický ústav Lékařská fakulta Masarykovy univerzity Tato prezentace obsahuje pouze stručný výtah nejdůležitějších pojmů a faktů.
Metabolismus aminokyselin - testík na procvičení - Vladimíra Kvasnicová
 Metabolismus aminokyselin - testík na procvičení - Vladimíra Kvasnicová Vyberte esenciální aminokyseliny a) Asp, Glu b) Val, Leu, Ile c) Ala, Ser, Gly d) Phe, Trp Vyberte esenciální aminokyseliny a) Asp,
Metabolismus aminokyselin - testík na procvičení - Vladimíra Kvasnicová Vyberte esenciální aminokyseliny a) Asp, Glu b) Val, Leu, Ile c) Ala, Ser, Gly d) Phe, Trp Vyberte esenciální aminokyseliny a) Asp,
Vybrané klinicko-biochemické hodnoty
 Vybrané klinicko-biochemické hodnoty Obecným výsledkem laboratorního vyšetření je naměřená hodnota, která může být fyziologická, zvýšená či snížená. Abychom zjištěnou hodnotu mohli takto zařadit, je třeba
Vybrané klinicko-biochemické hodnoty Obecným výsledkem laboratorního vyšetření je naměřená hodnota, která může být fyziologická, zvýšená či snížená. Abychom zjištěnou hodnotu mohli takto zařadit, je třeba
Biochemie kosti. Anatomie kosti. Kostní buňky. Podpůrná funkce. Udržování homeostasy minerálů. Sídlo krvetvorného systému
 Biochemie kosti Podpůrná funkce Udržování homeostasy minerálů Sídlo krvetvorného systému Anatomie kosti Haversovy kanálky okostice lamely oddělené lakunami Kostní buňky Osteoblasty Osteocyty Osteoklasty
Biochemie kosti Podpůrná funkce Udržování homeostasy minerálů Sídlo krvetvorného systému Anatomie kosti Haversovy kanálky okostice lamely oddělené lakunami Kostní buňky Osteoblasty Osteocyty Osteoklasty
ZÁKLADNÍ CHEMICKÉ POJMY A ZÁKONY
 ZÁKLADNÍ CHEMICKÉ POJMY A ZÁKONY Klíčová slova: relativní atomová hmotnost (A r ), relativní molekulová hmotnost (M r ), Avogadrova konstanta (N A ), látkové množství (n, mol), molární hmotnost (M, g/mol),
ZÁKLADNÍ CHEMICKÉ POJMY A ZÁKONY Klíčová slova: relativní atomová hmotnost (A r ), relativní molekulová hmotnost (M r ), Avogadrova konstanta (N A ), látkové množství (n, mol), molární hmotnost (M, g/mol),
9. Poruchy metabolismu draslíku 14. Acidózy 15. Alkalózy. Draslík ) Regulace K mezi tělem a zevním prostředím
 9. Poruchy metabolismu draslíku 14. Acidózy 15. Alkalózy Prof. MUDr. Zuzana Kubová, CSc. Ústav patologické fyziologie, Lékařská fakulta UK v Hradci Králové Draslík K hl. ICT kation 160 mmol/l konc. v séru
9. Poruchy metabolismu draslíku 14. Acidózy 15. Alkalózy Prof. MUDr. Zuzana Kubová, CSc. Ústav patologické fyziologie, Lékařská fakulta UK v Hradci Králové Draslík K hl. ICT kation 160 mmol/l konc. v séru
Metabolismus aminokyselin. Vladimíra Kvasnicová
 Metabolismus aminokyselin Vladimíra Kvasnicová Aminokyseliny aminokyseliny přijímáme v potravě ve formě proteinů: důležitá forma organicky vázaného dusíku, který tak může být v těle využit k syntéze dalších
Metabolismus aminokyselin Vladimíra Kvasnicová Aminokyseliny aminokyseliny přijímáme v potravě ve formě proteinů: důležitá forma organicky vázaného dusíku, který tak může být v těle využit k syntéze dalších
METABOLISMUS SACHARIDŮ
 METABOLISMUS SACHARIDŮ PRINCIP Rozštěpené sacharidy vstřebávání střevní sliznicí do krevního oběhu dopraveny vrátnicovou žílou do jater. V játrech enzymaticky hexózy štěpeny na GLUKÓZU vyplavována do krve
METABOLISMUS SACHARIDŮ PRINCIP Rozštěpené sacharidy vstřebávání střevní sliznicí do krevního oběhu dopraveny vrátnicovou žílou do jater. V játrech enzymaticky hexózy štěpeny na GLUKÓZU vyplavována do krve
Exkrece = Exkrety Exkrementy
 Vylučovací soustava Vylučovací soustava Exkrece = vylučování vylučování odpadních produktů tkáňového metabolismu z těla ven Exkrety tekuté odpadní látky x Exkrementy tuhé odpadní látky Hlavní exkrety:
Vylučovací soustava Vylučovací soustava Exkrece = vylučování vylučování odpadních produktů tkáňového metabolismu z těla ven Exkrety tekuté odpadní látky x Exkrementy tuhé odpadní látky Hlavní exkrety:
Biochemický ústav LF MU (E.T.) 2013
 Roztoky elektrolytů: ph, hydrolýza solí, pufry Biochemický ústav LF MU (E.T.) 2013 1 Pojmy, jejichž znalost ze střední školy je nezbytná pro porozumění přednášené látce : elektrolyty, jejich chování, typy
Roztoky elektrolytů: ph, hydrolýza solí, pufry Biochemický ústav LF MU (E.T.) 2013 1 Pojmy, jejichž znalost ze střední školy je nezbytná pro porozumění přednášené látce : elektrolyty, jejich chování, typy
Teorie kyselin a zásad poznámky 5.A GVN
 Teorie kyselin a zásad poznámky 5A GVN 13 června 2007 Arrheniova teorie platná pouze pro vodní roztoky kyseliny jsou látky schopné ve vodném roztoku odštěpit vodíkový kation H + HCl H + + Cl - CH 3 COOH
Teorie kyselin a zásad poznámky 5A GVN 13 června 2007 Arrheniova teorie platná pouze pro vodní roztoky kyseliny jsou látky schopné ve vodném roztoku odštěpit vodíkový kation H + HCl H + + Cl - CH 3 COOH
Hospodaření s vodou a minerály, ledviny, moč. Helena Brodská
 ZÁKLADY OBECNÉ A KLINICKÉ BIOCHEMIE 2004 Hospodaření s vodou a minerály, ledviny, moč Helena Brodská kapitola ve skriptech - 3.7 Tělesná voda-rozložení Celková tělesná voda /CTV/ 55-60% hmotnosti organismu.
ZÁKLADY OBECNÉ A KLINICKÉ BIOCHEMIE 2004 Hospodaření s vodou a minerály, ledviny, moč Helena Brodská kapitola ve skriptech - 3.7 Tělesná voda-rozložení Celková tělesná voda /CTV/ 55-60% hmotnosti organismu.
Metabolismus kyslíku v organismu
 Metabolismus kyslíku v organismu Účinná respirace/oxygenace tkání záleží na dostatečném po 2 ve vdechovaném vzduchu ventilaci / perfuzi výměně plynů v plicích vazbě kyslíku na hemoglobin srdečním výdeji
Metabolismus kyslíku v organismu Účinná respirace/oxygenace tkání záleží na dostatečném po 2 ve vdechovaném vzduchu ventilaci / perfuzi výměně plynů v plicích vazbě kyslíku na hemoglobin srdečním výdeji
SOUSTAVA VYLUČOVACÍ. vylučovací soustava = ledviny + odvodné cesty močové vylučovací soustava = ledviny + močovody + močový měchýř + močová trubice
 SOUSTAVA VYLUČOVACÍ Funkce vylučovací soustavy a způsoby vylučování odpadních látek u živočichů Při látkové přeměně v buňkách a tělních dutinách živočichů vznikají odpadní látky, které musí být u organismu
SOUSTAVA VYLUČOVACÍ Funkce vylučovací soustavy a způsoby vylučování odpadních látek u živočichů Při látkové přeměně v buňkách a tělních dutinách živočichů vznikají odpadní látky, které musí být u organismu
ECT = tekutina mimo buňky ICT = tekutina v buňkách
 DRASLÍ ( i sodík ) VE ZDRAVÍ A NEMOCI seminář pro U3V Ondřej Veselý Ústav patologické fyziologie LF UP Dětská endokrinologická ambulance Svitavy 1 Zastoupení + v organismu 98% draslíku je v buňkách nejvýznamnější
DRASLÍ ( i sodík ) VE ZDRAVÍ A NEMOCI seminář pro U3V Ondřej Veselý Ústav patologické fyziologie LF UP Dětská endokrinologická ambulance Svitavy 1 Zastoupení + v organismu 98% draslíku je v buňkách nejvýznamnější
Acidobazická rovnováha vývoj interpretace nálezn. lezů. A. Kazda
 Acidobazická rovnováha vývoj interpretace nálezn lezů A. Kazda Vyšet etřování acidobazické rovnováhy před p r. 1956 Bylo měřm ěřeno ph krve a vyšet etřen en celkový CO 2 (Total CO 2 ) např. van Slykeovým
Acidobazická rovnováha vývoj interpretace nálezn lezů A. Kazda Vyšet etřování acidobazické rovnováhy před p r. 1956 Bylo měřm ěřeno ph krve a vyšet etřen en celkový CO 2 (Total CO 2 ) např. van Slykeovým
Sůl kyseliny mléčné - konečný produkt anaerobního metabolismu
 Biochemické vyšetření ve sportu Laktát Sůl kyseliny mléčné - konečný produkt anaerobního metabolismu V klidu 0,8 mmol/l (0,5-1,5 mmol/l) Tvorba laktátu = přetížení aerobního způsobu zisku energie a přestup
Biochemické vyšetření ve sportu Laktát Sůl kyseliny mléčné - konečný produkt anaerobního metabolismu V klidu 0,8 mmol/l (0,5-1,5 mmol/l) Tvorba laktátu = přetížení aerobního způsobu zisku energie a přestup
Toxické metabolity glykolaldehyd, kys. glykolová, kys. glyoxylová, kys. štavelová
 Marek Protuš C 2 H 6 O 2 Alkohol 1,2-ethandiol bezbarvá viskózní tekutina nasládlé chuti netoxický Molární hmotnost 62,068 g/mol Teplota tání 12,9 C Teplota varu 197,3 C Hustota 1,113 g/cm 3 Rozpustnost
Marek Protuš C 2 H 6 O 2 Alkohol 1,2-ethandiol bezbarvá viskózní tekutina nasládlé chuti netoxický Molární hmotnost 62,068 g/mol Teplota tání 12,9 C Teplota varu 197,3 C Hustota 1,113 g/cm 3 Rozpustnost
Regulace glykémie. Jana Mačáková
 Regulace glykémie Jana Mačáková Katedra fyziologie a patofyziologie LF OU Ústav patologické fyziologie LF UP Název projektu: Tvorba a ověření e-learningového prostředí pro integraci výuky preklinických
Regulace glykémie Jana Mačáková Katedra fyziologie a patofyziologie LF OU Ústav patologické fyziologie LF UP Název projektu: Tvorba a ověření e-learningového prostředí pro integraci výuky preklinických
REAKCE: 1) ACIDOBAZICKÉ Acidum = kyselina Baze = zásada. Využití: V analytické kvantitativní chemii v odměrné analýze
 KYSELINY A ZÁSADY 1 REAKCE: 1) ACIDOBAZICKÉ Acidum = kyselina Baze = zásada Využití: V analytické kvantitativní chemii v odměrné analýze A) ALKALIMETRIE = odměrný roztok je zásada B) ACIDIMETRIE = odměrný
KYSELINY A ZÁSADY 1 REAKCE: 1) ACIDOBAZICKÉ Acidum = kyselina Baze = zásada Využití: V analytické kvantitativní chemii v odměrné analýze A) ALKALIMETRIE = odměrný roztok je zásada B) ACIDIMETRIE = odměrný
Acidobazická rovnováha
 Kyseliny vs. báze Acidobazická rovnováha definice: BronstedLowry (192) normální A:B pomr 1:20 Kyselina: H donor Báze: H akceptor síla je definována jako tendence odevzdat (pop. pijmout) hydrogenový iont
Kyseliny vs. báze Acidobazická rovnováha definice: BronstedLowry (192) normální A:B pomr 1:20 Kyselina: H donor Báze: H akceptor síla je definována jako tendence odevzdat (pop. pijmout) hydrogenový iont
glukóza *Ivana FELLNEROVÁ, PřF UP Olomouc*
 Prezentace navazuje na základní znalosti Biochemie, stavby a transportu přes y Doplňující prezentace: Proteiny, Sacharidy, Stavba, Membránový transport, Symboly označující animaci resp. video (dynamická
Prezentace navazuje na základní znalosti Biochemie, stavby a transportu přes y Doplňující prezentace: Proteiny, Sacharidy, Stavba, Membránový transport, Symboly označující animaci resp. video (dynamická
Klinická fyziologie a farmakologie jater a ledvin. Eva Kieslichová KARIP, Transplantcentrum
 Klinická fyziologie a farmakologie jater a ledvin Eva Kieslichová KARIP, Transplantcentrum 2 5% tělesné hmotnosti 25 30% srdečního výdeje játra obsahují 10-15% celkového krevního objemu játra hepatocyty
Klinická fyziologie a farmakologie jater a ledvin Eva Kieslichová KARIP, Transplantcentrum 2 5% tělesné hmotnosti 25 30% srdečního výdeje játra obsahují 10-15% celkového krevního objemu játra hepatocyty
Hydrochemie Oxid uhličitý a jeho iontové formy, ph, NK
 1 Oxid uhličitý - CO 2 původ: atmosférický - neznečištěný vzduch 0,03 obj. % CO 2 biogenní aerobní a anaerobní rozklad OL hlubinný magma, termický rozklad uhličitanových minerálů, rozklad uhličitanových
1 Oxid uhličitý - CO 2 původ: atmosférický - neznečištěný vzduch 0,03 obj. % CO 2 biogenní aerobní a anaerobní rozklad OL hlubinný magma, termický rozklad uhličitanových minerálů, rozklad uhličitanových
fce jater: (chem. továrna, jako 1. dostává všechny látky vstřebané GIT) METABOLICKÁ (jsou metabolicky nejaktivnější tkání v těle)
 JÁTRA ústřední orgán intermed. metabolismu, vysoká schopnost regenerace krevní oběh játry: (protéká 20% veškeré krve, 10-30% okysl.tep.krve, která zajišťuje výživu buněk, zbytek-portální krev) 1. funkční
JÁTRA ústřední orgán intermed. metabolismu, vysoká schopnost regenerace krevní oběh játry: (protéká 20% veškeré krve, 10-30% okysl.tep.krve, která zajišťuje výživu buněk, zbytek-portální krev) 1. funkční
Acido-bázická rovnováha (ABR)
 1 Acido-bázická rovnováha (ABR) Vladimír Kollárik II. klinika anestéziológie a intenzívnej medicíny Fakultná nemocnica s poliklinikou F. D. Roosevelta Banská Bystrica CEEA 2017 Košice, 2 3 Prečo je dôležitý
1 Acido-bázická rovnováha (ABR) Vladimír Kollárik II. klinika anestéziológie a intenzívnej medicíny Fakultná nemocnica s poliklinikou F. D. Roosevelta Banská Bystrica CEEA 2017 Košice, 2 3 Prečo je dôležitý
Projekt: Digitální učební materiály ve škole, registrační číslo projektu CZ.1.07/1.5.00/34.0527
 Projekt: Digitální učební materiály ve škole, registrační číslo projektu CZ.1.07/1.5.00/34.0527 Příjemce: Střední zdravotnická škola a Vyšší odborná škola zdravotnická, Husova 3, 371 60 České Budějovice
Projekt: Digitální učební materiály ve škole, registrační číslo projektu CZ.1.07/1.5.00/34.0527 Příjemce: Střední zdravotnická škola a Vyšší odborná škola zdravotnická, Husova 3, 371 60 České Budějovice
Obecná patofyziologie ledvin
 Obecná patofyziologie ledvin 1 Vztah mezi koncentrací látek v plazmě a jejich vylučováním v ledvinách Obecné schéma zpětnovazebního řízení (obr 1) 1 Vztah mezi koncentrací látek v plazmě a jejich vylučováním
Obecná patofyziologie ledvin 1 Vztah mezi koncentrací látek v plazmě a jejich vylučováním v ledvinách Obecné schéma zpětnovazebního řízení (obr 1) 1 Vztah mezi koncentrací látek v plazmě a jejich vylučováním
[ ] d[ Y] rychlost REAKČNÍ KINETIKA X Y
![[ ] d[ Y] rychlost REAKČNÍ KINETIKA X Y [ ] d[ Y] rychlost REAKČNÍ KINETIKA X Y](/thumbs/78/77051926.jpg) REAKČNÍ KINETIKA Faktory ovlivňující rychlost chemických reakcí Chemická povaha reaktantů - reaktivita Fyzikální stav reaktantů homogenní vs. heterogenní reakce Teplota 10 C zvýšení rychlosti 2x 3x zýšení
REAKČNÍ KINETIKA Faktory ovlivňující rychlost chemických reakcí Chemická povaha reaktantů - reaktivita Fyzikální stav reaktantů homogenní vs. heterogenní reakce Teplota 10 C zvýšení rychlosti 2x 3x zýšení
Renální tubulární acidózy VKP
 Akutní selhání ledvin Renální tubulární acidózy VKP- 31.3.2008 Způsobeno významným poklesem glomerulární filtrace a exkrečních funkcí obou ledvin náhle vzniklá neschopnost ledvin přiměřeně regulovat solnou
Akutní selhání ledvin Renální tubulární acidózy VKP- 31.3.2008 Způsobeno významným poklesem glomerulární filtrace a exkrečních funkcí obou ledvin náhle vzniklá neschopnost ledvin přiměřeně regulovat solnou
LEDVINOVÁ KONTROLA HOMEOSTÁZY
 LEDVINOVÁ KONTROLA HOMEOSTÁZY Doc. MUDr. Květoslava Dostálová, CSc. Ústav patologické fyziologie LF UP Název projektu: Tvorba a ověření e-learningového prostředí pro integraci výuky preklinických a klinických
LEDVINOVÁ KONTROLA HOMEOSTÁZY Doc. MUDr. Květoslava Dostálová, CSc. Ústav patologické fyziologie LF UP Název projektu: Tvorba a ověření e-learningového prostředí pro integraci výuky preklinických a klinických
Metabolismus bílkovin. Václav Pelouch
 ZÁKLADY OBECNÉ A KLINICKÉ BIOCHEMIE 2004 Metabolismus bílkovin Václav Pelouch kapitola ve skriptech - 3.2 Výživa Vyvážená strava člověka musí obsahovat: cukry (50 55 %) tuky (30 %) bílkoviny (15 20 %)
ZÁKLADY OBECNÉ A KLINICKÉ BIOCHEMIE 2004 Metabolismus bílkovin Václav Pelouch kapitola ve skriptech - 3.2 Výživa Vyvážená strava člověka musí obsahovat: cukry (50 55 %) tuky (30 %) bílkoviny (15 20 %)
Elektrochemie. Předmět elektrochemie: disociace (roztoky elektrolytů, taveniny solí) vodivost. jevy na rozhraní s/l (elektrolýza, články)
 Elektrochemie 1/30 Předmět elektrochemie: disociace (roztoky elektrolytů, taveniny solí) vodivost jevy na rozhraní s/l (elektrolýza, články) Vodiče: vodivost způsobena pohybem elektronů uvnitř mřížky:
Elektrochemie 1/30 Předmět elektrochemie: disociace (roztoky elektrolytů, taveniny solí) vodivost jevy na rozhraní s/l (elektrolýza, články) Vodiče: vodivost způsobena pohybem elektronů uvnitř mřížky:
CZ.1.07/1.5.00/34.0802 Zkvalitnění výuky prostřednictvím ICT. Protolytické děje VY_32_INOVACE_18_15. Mgr. Věra Grimmerová. grimmerova@gymjev.
 Průvodka Číslo projektu Název projektu Číslo a název šablony klíčové aktivity CZ.1.07/1.5.00/34.0802 Zkvalitnění výuky prostřednictvím ICT III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Příjemce
Průvodka Číslo projektu Název projektu Číslo a název šablony klíčové aktivity CZ.1.07/1.5.00/34.0802 Zkvalitnění výuky prostřednictvím ICT III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Příjemce
BILANČNÍ PŘÍSTUP K MODELOVÁNÍ ACIDOBAZICKÉ ROVNOVÁHY A PŘENOSU KREVNÍCH PLYNŮ
 BILANČNÍ PŘÍSTUP K MODELOVÁNÍ ACIDOBAZICKÉ ROVNOVÁHY A PŘENOSU KREVNÍCH PLYNŮ Jiří Kofránek, Michal Andrlík, Stanislav Matoušek Anotace Navazujeme na popis našeho přístupu k modelování acidobazické rovnováhy
BILANČNÍ PŘÍSTUP K MODELOVÁNÍ ACIDOBAZICKÉ ROVNOVÁHY A PŘENOSU KREVNÍCH PLYNŮ Jiří Kofránek, Michal Andrlík, Stanislav Matoušek Anotace Navazujeme na popis našeho přístupu k modelování acidobazické rovnováhy
Klasické nebo Stewartovo hodnocení poruch ABR?
 Klasické nebo Stewartovo hodnocení poruch ABR? Neboli naše mezery v acidobazi M. Kratochvíl, KARIM FN Brno Definice ph: záporný dekadický logaritmus koncentrace oxoniových iontů (40 nmol/l) Kyselina: donor
Klasické nebo Stewartovo hodnocení poruch ABR? Neboli naše mezery v acidobazi M. Kratochvíl, KARIM FN Brno Definice ph: záporný dekadický logaritmus koncentrace oxoniových iontů (40 nmol/l) Kyselina: donor
Regenerace ve sportu biologické veličiny. MUDr.Kateřina Kapounková
 Regenerace ve sportu biologické veličiny MUDr.Kateřina Kapounková Biologické veličiny pro řízení zatížení Srdeční frekvence Laktát Močovina Kreatinkináza Amoniak Hematokrit a hemoglobin Glukóza Minerály
Regenerace ve sportu biologické veličiny MUDr.Kateřina Kapounková Biologické veličiny pro řízení zatížení Srdeční frekvence Laktát Močovina Kreatinkináza Amoniak Hematokrit a hemoglobin Glukóza Minerály
Úvod k biochemickému. mu praktiku. Vladimíra Kvasnicová
 Úvod k biochemickému mu praktiku Vladimíra Kvasnicová organizace praktik pravidla bezpečné práce v laboratoři laboratorní vybavení práce s automatickou pipetou návody: viz. aplikace Výuka automatická pipeta
Úvod k biochemickému mu praktiku Vladimíra Kvasnicová organizace praktik pravidla bezpečné práce v laboratoři laboratorní vybavení práce s automatickou pipetou návody: viz. aplikace Výuka automatická pipeta
Odbourávání a syntéza glukózy
 Odbourávání a syntéza glukózy Josef Fontana EB - 54 Obsah přednášky Glukóza význam glukózy pro buňku, glykémie role glukózy v metabolismu transport glukózy přes buněčné membrány enzymy fosforylující a
Odbourávání a syntéza glukózy Josef Fontana EB - 54 Obsah přednášky Glukóza význam glukózy pro buňku, glykémie role glukózy v metabolismu transport glukózy přes buněčné membrány enzymy fosforylující a
Biologický materiál je tvořen vzorky tělních tekutin, tělesných sekretů, exkretů a tkání.
 Otázka: Druhy biologického materiálu Předmět: Biologie Přidal(a): moni.ka Druhy biologického materiálu Biologický materiál je tvořen vzorky tělních tekutin, tělesných sekretů, exkretů a tkání. Tělní tekutiny
Otázka: Druhy biologického materiálu Předmět: Biologie Přidal(a): moni.ka Druhy biologického materiálu Biologický materiál je tvořen vzorky tělních tekutin, tělesných sekretů, exkretů a tkání. Tělní tekutiny
Příloha č. 2 k rozhodnutí o změně registrace sp.zn.sukls43951/2010
 Příloha č. 2 k rozhodnutí o změně registrace sp.zn.sukls43951/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Hydrogenuhličitan sodný 4,2% (w/v) - BRAUN infuzní roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ
Příloha č. 2 k rozhodnutí o změně registrace sp.zn.sukls43951/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Hydrogenuhličitan sodný 4,2% (w/v) - BRAUN infuzní roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ
Roztoky - elektrolyty
 Roztoky - elektrolyty Roztoky - vodné roztoky prakticky vždy vedou elektrický proud Elektrolyty látky, které se štěpí disociují na elektricky nabité částice ionty Původně se předpokládalo, že k disociaci
Roztoky - elektrolyty Roztoky - vodné roztoky prakticky vždy vedou elektrický proud Elektrolyty látky, které se štěpí disociují na elektricky nabité částice ionty Původně se předpokládalo, že k disociaci
VYBRANÉ BIOCHEMICKÉ A FYZIOLOGICKÉ HODNOTY JEDNOTLIVÝCH DRUHŮ ZVÍŘAT MVDr. Vladimír Kopřiva,Ph.D DOPLŇKOVÝ STUDIJNÍ MATERIÁL KÓD AKTIVITY 2110/4-4 up.
 VYBRANÉ BIOCHEMICKÉ A FYZIOLOGICKÉ HODNOTY JEDNOTLIVÝCH DRUHŮ ZVÍŘAT MVDr. Vladimír Kopřiva,Ph.D DOPLŇKOVÝ STUDIJNÍ MATERIÁL KÓD AKTIVITY 2110/4-4 up. BIOCHEMICKÉ HODNOTY U VYBRANÝCH DRUHŮ ZVÍŘAT (SKOT,PRASE,
VYBRANÉ BIOCHEMICKÉ A FYZIOLOGICKÉ HODNOTY JEDNOTLIVÝCH DRUHŮ ZVÍŘAT MVDr. Vladimír Kopřiva,Ph.D DOPLŇKOVÝ STUDIJNÍ MATERIÁL KÓD AKTIVITY 2110/4-4 up. BIOCHEMICKÉ HODNOTY U VYBRANÝCH DRUHŮ ZVÍŘAT (SKOT,PRASE,
Přehled energetického metabolismu
 Přehled energetického metabolismu Josef Fontana EB 40 Obsah přednášky Důležité termíny energetického metabolismu Základní schéma energetického metabolismu Hlavní metabolické dráhy energetického metabolismu
Přehled energetického metabolismu Josef Fontana EB 40 Obsah přednášky Důležité termíny energetického metabolismu Základní schéma energetického metabolismu Hlavní metabolické dráhy energetického metabolismu
5. Příjem, asimilace a fyziologické dopady anorganického dusíku. 5. Příjem, asimilace a fyziologické dopady anorganického dusíku
 5. Příjem, asimilace a fyziologické dopady anorganického dusíku Zdroje dusíku dostupné v půdě: Amonné ionty + Dusičnany = největší zdroj dusíku v půdě Organický dusík (aminokyseliny, aminy, ureidy) zpracování
5. Příjem, asimilace a fyziologické dopady anorganického dusíku Zdroje dusíku dostupné v půdě: Amonné ionty + Dusičnany = největší zdroj dusíku v půdě Organický dusík (aminokyseliny, aminy, ureidy) zpracování
VÁPNÍK A JEHO VÝZNAM
 VÁPNÍK A JEHO VÝZNAM MUDr. Barbora Schutová, 2009 Ústav normální, patologické a klinické fyziologie, 3. LF UK Pozn.: Obrázky byly z důvodu autorských práv odstraněny nebo nahrazeny textem VÁPNÍK A JEHO
VÁPNÍK A JEHO VÝZNAM MUDr. Barbora Schutová, 2009 Ústav normální, patologické a klinické fyziologie, 3. LF UK Pozn.: Obrázky byly z důvodu autorských práv odstraněny nebo nahrazeny textem VÁPNÍK A JEHO
Acidobazické reakce. 1. Arrheniova teorie. 2. Neutralizace
 Acidobazické reakce 1. Arrheniova teorie Kyseliny látky schopné ve vodných roztocích odštěpit H + např: HCl H + + Cl -, obecně HB H + + B - Zásady látky schopné ve vodných roztocích poskytovat OH - např.
Acidobazické reakce 1. Arrheniova teorie Kyseliny látky schopné ve vodných roztocích odštěpit H + např: HCl H + + Cl -, obecně HB H + + B - Zásady látky schopné ve vodných roztocích poskytovat OH - např.
Klinická fyziologie ABR sekce Základy oboru edukační lekce. Michal Horáček KARIM 2. LF UK a FN v Motole Praha
 Klinická fyziologie ABR sekce Základy oboru edukační lekce Michal Horáček KARIM 2. LF UK a FN v Motole Praha Hlavní ukazatel ABR: ph (resp. a[h + ]) ph = pondus hydrogenii, potential of hydrogen = vodíkový
Klinická fyziologie ABR sekce Základy oboru edukační lekce Michal Horáček KARIM 2. LF UK a FN v Motole Praha Hlavní ukazatel ABR: ph (resp. a[h + ]) ph = pondus hydrogenii, potential of hydrogen = vodíkový
Autor kapitoly: MUDr.Pavel Pick, Ústav klinické biochemie VFN a 1.LF UK Praha
 Poruchy acidobazické regulace Autor kapitoly: MUDr.Pavel Pick, Ústav klinické biochemie VFN a 1.LF UK Praha 1. Úvod Poruchy acidobazické regulace (ABR) jsou stavy, které vznikají v úzké souvislosti se
Poruchy acidobazické regulace Autor kapitoly: MUDr.Pavel Pick, Ústav klinické biochemie VFN a 1.LF UK Praha 1. Úvod Poruchy acidobazické regulace (ABR) jsou stavy, které vznikají v úzké souvislosti se
DIAGNÓZA JEDNODUCHÝCH A SMÍŠ ÍŠENÝCH PORUCH ACIDOBAZICKÉ ROVNOVÁHY. A. Kazda. Katedra klinické biochemie, IPVZ Praha UKBLD 1.
 DIAGNÓZA JEDNODUCHÝCH A SMÍŠ ÍŠENÝCH PORUCH ACIDOBAZICKÉ ROVNOVÁHY A. Kazda Katedra klinické biochemie, IPVZ Praha UKBLD 1. LF UK a VFN Záznamový list acidobazické regulace Graf acidobazické regulace (M.
DIAGNÓZA JEDNODUCHÝCH A SMÍŠ ÍŠENÝCH PORUCH ACIDOBAZICKÉ ROVNOVÁHY A. Kazda Katedra klinické biochemie, IPVZ Praha UKBLD 1. LF UK a VFN Záznamový list acidobazické regulace Graf acidobazické regulace (M.
Analyt Proxim. tubulus Henleova klička Distální tubulus a sběrný kanálek Voda NaCl KCl (sekrece) HCO 3
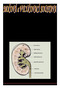 - vylučování se součastní = plíce (voda, CO2 ) viz dýchací soustava 2. ročník = kůží ( NaCl, voda, mastné kyseliny )viz. kůže 1. ročník = játry a trávicím ústrojím (zbytky potravy, žluč.) viz. trávicí
- vylučování se součastní = plíce (voda, CO2 ) viz dýchací soustava 2. ročník = kůží ( NaCl, voda, mastné kyseliny )viz. kůže 1. ročník = játry a trávicím ústrojím (zbytky potravy, žluč.) viz. trávicí
