INDIKACE Používá se k náhradě krevní ztráty a pro léčbu anémie.
|
|
|
- Lenka Kopecká
- před 7 lety
- Počet zobrazení:
Transkript
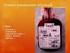
1 ERYTROCYTY BEZ BUFFY-COATU RESUSPENDOVANÉ EBR (Příbalový leták) Výrobce EBR - Hematologicko-transfúzní oddělení, Nemocnice Znojmo C 2074 Je to transfuzní přípravek získaný z plné krve odstřeďováním, odstraněním plazmy a buffy-coatu a následnou resuspenzí erytrocytů ve vhodném výživném roztoku. Hematokrit je v rozmezí ,70. Každá jednotka na konci zpracování obsahuje minimálně 43g hemoglobinu. Jednotka obsahuje veškeré, erytrocyty, kromě 10 ml až 30 ml z původního množství erytrocytů v jednotce. Obsah leukocytů v jednotce je nižší než 1,2x10 9 /l a průměrný obsah trombocytů v jednotce je nižší než 10x109/l. PŘÍPRAVA Antikoagulační roztok: CPD, objem 63 ml. Příprava probíhá 2-6 hod. po odběru. Po odstředění plné krve je oddělena od erytrocytů plazma a vrstva buffy-coatu (o hmotnosti 86-96g včetně vaku). Výživný roztok: ADSOL nebo SAGM, objem 100 ml. Po pečlivém promíchání s výživným roztokem je EBR uchováván při teplotě 2-6oC. OZNAČOVÁNÍ V označení na obalu (vaku) je uveden: - Název a sídlo výrobce, identifikační číslo ZTS - Číslo přípravku (identifikační odběrové číslo) i v podobě čárového kódu - Název přípravku EBR i v podobě čárového kódu - Krevní skupina ABO, Rh poz. nebo neg. i v podobě čárového kódu - Objem v ml - Způsob odběru, zpracování - Datum odběru i v čárovém kódu - Doba použitelnosti - Pokyny pro skladování - Vyhovuje v předepsaných testech - Složení a objem přidaného výživného roztoku,odběrový roztok - Teplota uchovávání, - Že krev se nesmí použít pro transfuzi, pokud je přítomna nadměrná hemolýza či jiné známky znehodnocení, - Že se přípravek musí podávat přes filtr o velikosti pórů 170um až 200um. UCHOVÁVÁNÍ A STABILITA Uchovávat při teplotě 2oC až 6oC. Doba uchovávání v závislosti na použitém antikoagulačním a výživném roztoku. EBR jsou odebírány do antikoagulačního roztoku CPD, výživného roztoku ADSOL nebo SAGM (Fy BAXTER), maximální doba uchovávání je 42 dnů. Vaky se SAGM od jiných výrobců je maximální doba uchovávání 35 dní. Odstranění buffy-coatu během zpracování snižuje tvorbu mikroagregátů. DOPRAVA Validovaný systém dopravy zajišťuje, aby do konce maxim. doby dopravy 24 hod teplota nepřevýšila 10oC. Pro přepravu v dopravním prostředku bez možnosti chlazení je vyžadováno použití chlazených termoboxů. INDIKACE Používá se k náhradě krevní ztráty a pro léčbu anémie. UPOZORNĚNÍ Kompatibilita erytrocytů s uvažovaným příjemcem se musí ověřit vhodným předtransfuzním vyšetřením. Podávání resuspendovaných erytrocytů bez buffy-coatu se nedoporučuje u:
2 - různých typů nesnášenlivosti plazmy - výměnné transfuze u novorozenců, pokud se přípravek nepoužije do 7 dní od odběru a výživný roztok se nenahradí čerstvou zmrazenou plazmou v den použití. NEŽÁDOUCÍ ÚČINKY - oběhové přetížení - hemolytické potransfuzní reakce - nehemolytická potransfuzní reakce (hlavně zimnice, horečka, kopřivka), ale vzácněji než po transfuzní resuspendovaných erytrocytů, - možný přenos syfilis, pokud byla plná krev uchovávána při 4oC méně než 96 h, - přenos virů (hepatitidy, HIV apod.) je možný bez ohledu na pečlivý výběr dárců a skríningová vyšetření, - vzácně přenos protozoí (např.malárie), - aloimunizace proti HLA a erytrocytovým antigenům, - sepse způsobená náhodnou bakteriální kontaminací, - biochemické odchylky při masivní transfuzi, např.hyperkalémie, - potransfuzní purpura, - akutní poškození plic vyvolané transfuzí. Platnost od:
3 ERYTROCYTY BEZ BUFFY-COATU RESUSPENDOVANÉ DELEUKOTIZOVANÉ ERD Výrobce ERD Hematologicko - transfúzní oddělení, Nemocnice Znojmo C 2074 Erytrocyty resuspendované, deleukotizované, kterými se rozumí erytrocyty z jednotlivého odběru plné krve, ze kterého je odstraněn velký podíl plazmy a ze kterého jsou odstraněny leukocyty a je přidán resuspenzní roztok. Hematokrit je v rozmezí ,70. Každá jednotka na konci zpracování obsahuje minimálně 40g hemoglobinu, obsah leukocytů v jednotce je nižší než 1x106/TU. PŘÍPRAVA Antikoagulační roztok: CPD, objem 63 ml. Příprava probíhá 2-6 hod. po odběru. Po odstředění plné krve je oddělena od erytrocytů plazma a vrstva buffy-coatu (o hmotnosti 86-96g včetně vaku). Výživný roztok: SAGM, objem 100 ml. Vyrobenou EBR filtrujeme přes leukocytární filtr, čímž odstraníme zbylé leukocyty až do požadovaného rozmezí. Způsob filtrace pre-storage. OZNAČOVÁNÍ štítek viz příloha V označení na obalu (vaku) je uveden: - Název a sídlo výrobce, identifikační číslo ZTS - Číslo přípravku (identifikační odběrové číslo) i v podobě čárového kódu - Název přípravku ERD i v podobě čárového kódu - Krevní skupina ABO, Rh poz. nebo neg. i v podobě čárového kódu - Objem v ml - Způsob odběru, zpracování - Datum odběru i v čárovém kódu - Doba použitelnosti - Pokyny pro skladování - Vyhovuje v předepsaných testech - Složení a objem přidaného výživného roztoku,odběrový roztok - Teplota uchovávání - krev se nesmí použít pro transfuzi, pokud je přítomna nadměrná hemolýza či jiné známky znehodnocení, UCHOVÁVÁNÍ A STABILITA Uchovávat při teplotě 2oC až 6oC. Při poklesu teploty pod 1stC se přípravek nesmí použít k transfúzi. Doba uchovávání v závislosti na použitém antikoagulačním a výživném roztoku. ERD jsou odebírány do antikoagulačního roztoku CPD a výživného roztoku SAGM (Fy Fenwal), maximální doba uchovávání je 42 dnů, vaky s roztokem SAGM od jiných výrobců 35 dní maximální doba uchovávání. VAROVÁNÍ Jen na předpis lékaře! Přípravek nesmí být používán po uplynutí doby exspirace vyznačené na štítku vaku. Přípravek musí být uchováván mimo dosah dětí. DOPRAVA Validovaný systém dopravy zajišťuje, aby do konce maxim. doby dopravy 24 hod teplota nepřevýšila 10 o C. Pro přepravu v dopravním prostředku bez možnosti chlazení je vyžadováno použití chlazených termoboxů.
4 Při poklesu teploty pod 1stC se přípravek nesmí použít k aplikaci. INDIKACE Používá se u pacientů v případě: a) nehemolytické postransfúzní reakce: - při opakovaných febrilních nehemolytických reakcích, anebo - při průkazu cytotoxických HLA protilátek b) riziko aloimunizace - při chronických substitucích transfúzními přípravky - před a po orgánových transplantacích (transplantacích kostní dřeně, srdce, ledvin, jater apod.) c) riziko infekce CMV u CMV seronegativních příjemců - před a po orgánových transplantacích - u imunosuprimovaných pacientů - u nedonošených dětí a novorozenců - u těhotných žen - u dětí po operacích srdce a velkých cév UPOZORNĚNÍ Kompatibilita erytrocytů s uvažovaným příjemcem se musí ověřit vhodným předtransfuzním vyšetřením. Při podávání krevní transfúze musí lékař dodržovat legislativně stanovený postup provádění transfúze a striktně dodržovat veškeré zásady pro zajištění bezpečnosti krevního převodu. Přípravek se podává transfúzní soupravou se vřazeným filtrem. Přípravek nesmí být používán po uplynutí doby exspirace vyznačené na štítku vaku. Celková doba aplikace TP nesmí překročit 4hod. Erytrocytové přípravky je vhodné před aplikací nechat alespoň ½ hod. temperovat na pokojovou teplotu. Mísení medikamentů s transfúzním přípravkem není přípustně. KONTRAINDIKACE Každá transfúze, která není přísně indikována, je kontraindikována. Opatrnost při různých typech intolerance plazmy a ostatních krevních složek NEŽÁDOUCÍ ÚČINKY - oběhové přetížení - hemolytické potransfuzní reakce - nehemolytická potransfuzní reakce (hlavně zimnice, horečka, kopřivka) - možný přenos syfilis, pokud byla ERD uchovávána při 4 o C méně než 96 h, - přenos virů (hepatitidy, HIV apod.) je možný bez ohledu na pečlivý výběr dárců a skríningová vyšetření, - vzácně přenos protozoí (např.malárie), - aloimunizace proti HLA a erytrocytovým antigenům, - sepse způsobená náhodnou bakteriální kontaminací, - biochemické odchylky při masivní transfuzi, např.hyperkalémie, - potransfuzní purpura, - akutní poškození plic vyvolané transfúzí /TRALI/ - přenos jiných patogenů, které nejsou testovány Platnost do:
5 ZMRAZENÁ ČERSTVÁ PLAZMA P [Příbalový leták] Výrobce P Hematologicko - transfúzní oddělení, Nemocnice Znojmo C 2074 Je to přípravek získaný z plné krve, nebo plazmaferézou zmrazený do 6 hodin po odběru na teplotu - 30 o C v jádře během 60 minut a dále uchovávána při teplotě - 25 o C a nižší. VLASTNOSTI Tento přípravek obsahuje normální plazmatické hladiny stabilních koagulačních faktorů, albuminu a imunoglobulinu. Obsahuje nejméně 70% původního faktoru VIII a nejméně podobné množství dalších labilních koagulačních faktorů a přirozených inhibitorů. PŘÍPRAVA a) Z plné krve Plazma je oddělena od odebrané plné krve za použití krevního vaku s připojenými vaky pro rozdělení krve na složky. Je využíváno rychlého odstřeďování. Separace z plné krve je dokončena během 6 hod po odběru. Zmrazování se provádí v šokovém zmrazovači, v němž dojde k úplnému zmrazení během jedné hodiny na teplotu pod -30oC. b) Přístrojovou plazmaferézou OZNAČOVÁNÍ V označení na obalu (vaku) je uveden: - Název a sídlo výrobce, identifikační číslo ZTS - Číslo přípravku (identifikační odběrové číslo) i v podobě čárového kódu - Název přípravku P i v podobě čárového kódu - Krevní skupina ABO, Rh poz. nebo neg. i v podobě čárového kódu - Objem v ml - Způsob odběru, zpracování - Datum odběru i v čárovém kódu - Doba použitelnosti - Pokyny pro skladování - Vyhovuje v předepsaných testech - Odběrový roztok Plazma prošlá karanténou - Čerstvě zmražená plazma klinická - prošlá karanténou. Štítek je nalepen na vak s plazmou. UCHOVÁVÁNÍ A STABILITA Transfúzní přípravek - P je uchováván dle Rady Evropy No.R (95)15 pro rok 2006: - při teplotě - 25 o C a nižší je doba exspirace 36 měsíců. - při teplotě -18 o C až -25 o C je doba exspirace 3 měsíce DOPRAVA: Teplota uchovávání musí být udržována i během přepravy. Při přejímání plazmy je nutné ověřit, že vaky zůstaly při přepravě zmrzlé. Pokud plazma není určena k okamžitému použití, je uložena při teplotě -25oC. INDIKACE: - Koagulační poruchy, především v těch klinických situací, kde je přítomen kombinovaný deficit koagulačních faktorů, pokud není k dispozici vhodný přípravek, v němž byly viry inaktivovány. - K léčbě trombotické, trombocytopenické purpury (TTP) - Hlavní užití jako výchozí surovina pro frakcionaci.
6 UPOZORNĚNÍ: Zmrazenou čerstvou plazmu není vhodné používat: - K pouhé úpravě objemového deficitu při absenci deficitu koagulačních faktorů ani jako zdroj imunoglobulinů. - Tam kde je k dispozici alternativní výrobek, v němž byly inaktivovány viry. - U nemocných s nesnášenlivostí proti plazmatickým bílkovinám. Používá se skupinově kompatibilní plazma. Používá se bezprostředně po rozmrazení. Opakovaně se nezmrazuje. Před použitím se rozmrazí v řádně kontrolovaném prostředí, ověří se neporušenost vaku. Po rozmrazení nesmí být viděn nerozpuštěný kryoprotein. NEŽÁDOUCÍ ÚČINKY: - Citronánová toxicita při rychlé transfuzi velkých objemů. - Nehemolytické potransfuzní reakce (především zimnice, horečka, kopřivka) - Přenos virů (hepatitidy, HIV, apod.) je možný bez ohledu na pečlivý výběr dárců a screeningová vyšetření. - Sepse způsobená náhodnou bakteriální kontaminací. - Akutní poškození plic související s transfuzí. Platnost od :
7 TROMOBOCYTY Z PLNÉ KRVE V NÁHRADNÍM ROZTOKU [Příbalový leták] VýrobceTAD - Hematologicko - transfúzní oddělení, Nemocnice Znojmo C 2074 Je to přípravek získaný z plné krve, který obsahuje většinu původního obsahu trombocytů v terapeuticky účinné formě. VLASTNOSTI V závislosti na metodě přípravy kolísá obsah trombocytů v jedné jednotce mezi 45x109 až 85x109 ( v průměru 70x109) v 50 ml až 60 ml dispenzního roztoku. Podobně kolísá o obsah leukocytů mezi 0,05x109 až 1,0x109 a obsah erytrocytů mezi 0,2x109 až 1,0x109 na jednotku, pokud se neprovádějí další postupy ke snížení těchto počtů. Množství trombocytů ve standardní dávce pro dospělé odpovídá množství získanému ze čtyř až šesti jednotek plné krve. PŘÍPRAVA 1a. Příprava plazmy bohaté na trombocyty Princip: jednotka čerstvé krve se odstřeďuje tak, aby v plazmě zůstal optimální počet trombocytů a počty leukocytů a erytrocytů byly sníženy na definovanou úroveň. Klíčové body metody jsou: - účinnost odstřeďování definována jako gamin, - standardizace teploty krve při odstřeďování, - zabránění, že dojde k rozvíření vrstev jednotlivých složek, - průtok při oddělování plazmy by neměl být příliš rychlý a separace musí být ukončena 8mm až 10mm nad povrchem vrstvy erytrocytů 1b. Příprava trombocytů z plazmy bohaté na trombocyty Princip: trombocyty v plazmě bohaté na trombocyty sedimentují rychlým odstřeďováním, odstraní se supernatantní plazma chudá na trombocyty až na zbylých 50ml až 70ml, nakonec je umožněno, aby se rozpadly agregáty trombocytů a trombocyty jsou pak resuspendovány. 2. Příprava trombocytů z buffy-coatu Princip: čerstvá jednotka plné krve se odstřeďuje tak, že trombocyty primárně sedimentují do vrstvy buffy-coatu společně s leukocyty. Buffy-coat se oddělí a dále zpracuje tak, aby se získal koncentrát trombocytů. Jednotlivé buffy-coaty nebo jejich směs (směs ze 4 až 10-ti jednotek obsahujících kompatibilní krevní skupiny) se ředí plazmou nebo výživným roztokem. Po pečlivém promíchání se vak s jedním buffy-coatem nebo vak se směsným buffy-coatem odstřeďuje tak, že trombocyty zůstávají v supernatantu, ale erytrocyty a leukocyty sedimentují na dno vaku. Klíčové body této metody jsou podobné bodům zmíněným v odstv. 1a příprava plazmy bohaté na trombocyty. Deleukotizované trombocytové přípravky mohou být připraveny filtrací, doporučuje se deleukotizace před uchováváním /nejlépe do 6hod. po oddělení). OZNAČOVÁNÍ V označení na obalu (vaku) je uveden: - Název a sídlo výrobce - Číslo odběru (u směsných trombocytů je nutné zavést systém označování, který umožní identifikaci původních dárců) - Název přípravku P i v podobě čárového kódu - Krevní skupina ABO, - přítomnost znaku Rh(D) - Rh (D) pozitivní, nepřítomnost znaku Rh (D) Rh(D) negativní - Objem v ml a průměrné množství trombocytů - Datum odběru a doba použitelnosti - Pokyny pro skladování - zda je přípravek deleukotizován či nikoliv - složení antikoag. Nebo přídavného roztoku - že se přípravek musí podávat přes filtr o velikosti pórů 170 um až 200um.
8 UCHOVÁVÁNÍ A STABILITA Trombocyty se musí uchovávat za podmínek, které zaručují zachování jejich životnosti. Míchání trombocytů během uchovávání musí být natolik účinné, aby zaručovalo dostupnost kyslíku, ale aby bylo zároveň co nejšetrnější. Teplota uchovávání má být 20stC až 24stC. Životnost je za optimálních podmínek zachovávána až 7 dní. Nicméně se v současně nedoporučuje delší uchovávání než 5 dní. DOPRAVA: Teplota během přepravy v termoboxech s pokojovou teplotou. Pokud se bezprostředně nepoužijí k transfúzi, by měly být uchovávány za doporučených podmínek a až do použití by měly být míchány. INDIKACE: Rozhodnutí podat trombocyty by nemělo být založeno pouze na nízkém počtu trombocytů. Za jednoznačnou Indikaci lze považovat pouze přítomnost těžké trombocytopenie s klinicky významným krvácením přisuzovaným úbytku trombocytů. Všechny další indikace jsou více či méně relativní a závislé na klinickém stavu nemocného. UPOZORNĚNÍ: Jestliže se trombocyty smíchají před začátkem doby uchovávání (buffy-coat či suspenze trombocytů), mohou se skladovat až 5 dní od odběru. Jestliže se trombocyty smíchají až po době uchovávání, měly by se podat co nejdříve, ale ne později než 6hod. po smíchání. NEŽÁDOUCÍ ÚČINKY: - nehemolytická potransfuzní reakce (hlavně zimnice, horečka, kopřivka). Výskyt lze omezit použitím deleukotizovaných trombocytových přípravků - přenos virů (hepatitidy, HIV apod.) je možný bez ohledu na pečlivý výběr dárců a skríningová vyšetření, rizika přenosu CMV mohou být snížena deleukotizací - možný přenos syfilis - vzácně přenos protozoí (např.malárie), - aloimunizace proti HLA a HPA - sepse způsobená náhodnou bakteriální kontaminací, - biochemické odchylky při masivní transfuzi, např.hyperkalémie, - potransfuzní purpura, - akutní poškození plic vyvolané transfuzí, pokud jsou trombocyty nesuspendovány v plazmě Platnost od:
9 Informace pro použití trombocytů Transfuzní přípravek: Trombocyty z aferézy deleukotizované, v náhradním roztoku Zkratka: TADR Výrobce: Hematologicko transfuzní oddělení, Nemocnice Znojmo, MUDr.J. Janského 11, Znojmo , tel. kontakt Transfuzní přípravek byl vyroben za dodržení platných legislativních postupů a kontrol jakosti. Definice: Transfuzní přípravek získaný trombocytaferézou od jednoho dárce pomocí separátoru krevních elementů, deleukotizovaný. Trombocyty jsou resuspendovány ve směsi plazmy a náhradního roztoku pro uchování trombocytů InterSol (PAS III). Přípravek obsahuje: trombocyty minimálně 2x10 11 na 1 transfuzní jednotku (TU) resuspendované v plazmě a náhradním roztoku, reziduální leukocyty v množství menším než 1x10/6 antikoagulační roztok ACD-A (složení v 1000ml roztoku: Acidum citricum monohydricum 8,0g, Natrii citras dihydricus 22,0g, Glucosum monohydricum 24,5g ) náhradní roztok pro trombocyty InterSol (PAS III). Složení: Natrii citras 3,18g, Dinatr.phosphas anhydr. 3,05g, Natr. dihydrogenphosphas dihydr. 1,05g, Natrii acetas trihydr. 4,42g, Natrii chlorid 4,52g, Agua ad inject. ad 1000ml) Skladování: TADR se uchovává za neustálého čeření na třepačce (agitátoru) v termoboxu při teplotě od +20st.C do +24st.C nejdéle po dobu 5 dní. Datum exspirace uvedeno na štítku. Po transportu na oddělení neprodleně aplikujte! Trombocytový koncentrát je nutno podat nejpozději do 1 hod. po dodání. Transport: V transportních termoboxech při teplotě +20st.C až +24st.C. Po příjmu by se měly TAD uchovávat za doporučených podmínek za neustálého čeření, pokud se bezprostředně nepoužijí k transfuzi. Indikace: Za jednoznačnou indikaci lze považovat těžkou trombocytopenii s klinicky významným krvácením přisuzovaným deficitu trombocytů a trombocytopatie při klinicky významném krvácení. Substituce trombocytů před operačními výkony u pacientů s trombocytopenií. Dále podání v případě výskytu nehemolytické potransfuzní reakce v anamnéze, rizika aloimunizace nebo rizika infekce CMV u CMV séronegativního příjemce transfuze trombocytů. Kontraindikace: Hemolyticko-uremický syndrom, trombotická trombocytopenická purpura (TTP), heparinem indukovaná trombocytopenie. Nedoporučuje se použití trombocytů od příbuzných nemocného nebo jiných HLA shodných jedinců, kteří jsou potenciálními dárci krvetvorných buněk. Možné nežádoucí účinky: nehemolytická potransfuzní reakce (hlavně zimnice, horečka, kopřivka) výskyt lze omezit podáním deleukotizovaných trombocytárních přípravků aloimunizace, především proti HLA a HPA antigenům při použití deleukotizovaných trombocytárních přípravků je riziko aloimunizace minimální, pokud jsou i ostatní podané přípravky deleukotizovány možný přenos infekčních patogenů (virů hepatitidy, HIV, EBV, CMV, protozoí) i přes pečlivý výběr dárců a povinná screeningová vyšetření dárců na HIV-1,2, HBV, HCV, syfilis) potransfuzní purpura bakteriálně toxická reakce TRALI ( akutní poškození plic vyvolané transfuzí) TA-GvHD ( s transfuzí asociovaná reakce štěpu proti hostiteli) TRIM (imunomodulační účinek vázaný na transfuzi) Upozornění: Před podáním transfuzního přípravku proveďte kontrolu vzhledu přípravku se zaměřením na agregáty trombocytů ( sraženiny) a neporušenost vaku. Aplikace přípravků pomocí transfúzního setu. Platnost od:
TRANSFUZNÍ PŘÍPRAVKY
 TRANSFUZNÍ PŘÍPRAVKY vyrobené HTO Nemocnice Pardubického kraje, a.s. Orlickoústecké nemocnice PŘÍBALOVÉ INFORMACE Verze 1/2015 Obsah: Erytrocyty bez buffy - coatu resuspendované EBR... 2 Plazma z plné
TRANSFUZNÍ PŘÍPRAVKY vyrobené HTO Nemocnice Pardubického kraje, a.s. Orlickoústecké nemocnice PŘÍBALOVÉ INFORMACE Verze 1/2015 Obsah: Erytrocyty bez buffy - coatu resuspendované EBR... 2 Plazma z plné
TRANSFUZNÍ PŘÍPRAVKY vyrobené HTO
 TRANSFUZNÍ PŘÍPRAVKY vyrobené HTO Orlickoústecká nemocnice PŘÍBALOVÉ INFORMACE Verze 1/2017 Erytrocyty bez buffy-coatu resuspendované EBR... 2 Plazma z plné krve P... 3 Plazma z plné krve k frakcionaci
TRANSFUZNÍ PŘÍPRAVKY vyrobené HTO Orlickoústecká nemocnice PŘÍBALOVÉ INFORMACE Verze 1/2017 Erytrocyty bez buffy-coatu resuspendované EBR... 2 Plazma z plné krve P... 3 Plazma z plné krve k frakcionaci
Autologní transfuzní přípravky
 Autologní transfuzní přípravky Erytrocyty pro autotransfuzi (Autologní odběr: Erytrocyty bez buffy - coatu resuspendované AEBR) Trombocyty z aferézy pro autotransfuzi (Autologní odběr: Trombocyty z aferézy)
Autologní transfuzní přípravky Erytrocyty pro autotransfuzi (Autologní odběr: Erytrocyty bez buffy - coatu resuspendované AEBR) Trombocyty z aferézy pro autotransfuzi (Autologní odběr: Trombocyty z aferézy)
Autologní transfuzní přípravky
 Informace o transfuzním přípravku ČTĚTE POZORNĚ! Transfuzní přípravek, který jste obdrželi, byl vyroben za dodržení všech definovaných postupů pro výrobu, kontrolu a zabezpečování jakosti. K jeho znehodnocení
Informace o transfuzním přípravku ČTĚTE POZORNĚ! Transfuzní přípravek, který jste obdrželi, byl vyroben za dodržení všech definovaných postupů pro výrobu, kontrolu a zabezpečování jakosti. K jeho znehodnocení
SEZNAM VYRÁBĚNÝCH TRANSFUZNÍCH PŘÍPRAVKŮ
 SEZNAM VYRÁBĚNÝCH TRANSFUZNÍCH PŘÍPRAVKŮ Červenec 2017 Krajská zdravotní, a.s. - MASARYKOVA NEMOCNICE v Ústí nad Labem, o.z. Sociální péče 3316/12A 401 13 Ústí nad Labem http://www.kzcr.eu Tel: +420 477
SEZNAM VYRÁBĚNÝCH TRANSFUZNÍCH PŘÍPRAVKŮ Červenec 2017 Krajská zdravotní, a.s. - MASARYKOVA NEMOCNICE v Ústí nad Labem, o.z. Sociální péče 3316/12A 401 13 Ústí nad Labem http://www.kzcr.eu Tel: +420 477
Srpen Krajská zdravotní, a.s. prim. MUDr. Jiří Masopust tel.: lékaři tel.
 Kontakt Krajská zdravotní, a.s. Masarykova nemocnice v Ústí nad Labem, o.z. Transfuzní oddělení Sociální péče 3316/12A 401 13 Ústí nad Labem SEZNAM VYRÁBĚNÝCH TRANSFUZNÍCH PŘÍPRAVKŮ prim. MUDr. Jiří Masopust
Kontakt Krajská zdravotní, a.s. Masarykova nemocnice v Ústí nad Labem, o.z. Transfuzní oddělení Sociální péče 3316/12A 401 13 Ústí nad Labem SEZNAM VYRÁBĚNÝCH TRANSFUZNÍCH PŘÍPRAVKŮ prim. MUDr. Jiří Masopust
Erytrocyty bez buffy coatu resuspendované z plné krve( EBR)
 Poslední revize 24.10.2013 Erytrocyty bez buffy coatu resuspendované z plné krve( EBR) Vlastnosti: Transfúzní přípravek vyrobený ze 450ml + - 10% plné krve odebrané vždy od jednoho dárce do 63ml CPD (složení:
Poslední revize 24.10.2013 Erytrocyty bez buffy coatu resuspendované z plné krve( EBR) Vlastnosti: Transfúzní přípravek vyrobený ze 450ml + - 10% plné krve odebrané vždy od jednoho dárce do 63ml CPD (složení:
Erytrocyty bez buffy coatu resuspendované EBR
 Erytrocyty bez buffy coatu resuspendované EBR Charakteristika: Výrobek získaný z lidské krve dárců, odebrané aseptickým způsobem do vaku s antikoagulačním roztokem CPD, po odstranění většiny plazmy, leukocytů
Erytrocyty bez buffy coatu resuspendované EBR Charakteristika: Výrobek získaný z lidské krve dárců, odebrané aseptickým způsobem do vaku s antikoagulačním roztokem CPD, po odstranění většiny plazmy, leukocytů
Systém řízení kvality, SVP a výroba TP
 Systém řízení kvality, SVP a výroba TP Pacasová R. Transfuzní a tkáňové oddělení FN Brno LF MU bakalářské studium Zdravotní laborant, 2015 Legislativa ZTS - EU Výrobu transfuzních přípravků v Evropě (EU)
Systém řízení kvality, SVP a výroba TP Pacasová R. Transfuzní a tkáňové oddělení FN Brno LF MU bakalářské studium Zdravotní laborant, 2015 Legislativa ZTS - EU Výrobu transfuzních přípravků v Evropě (EU)
Transfuzní přípravky
 Transfuzní přípravky Transfuzní přípravky lidská krev a její složky zpracované pro podání transfuzí za účelem léčení nebo předcházení nemoci erytrocyty, trombocyty, granulocyty, plazma. Jedná se o individuálně
Transfuzní přípravky Transfuzní přípravky lidská krev a její složky zpracované pro podání transfuzí za účelem léčení nebo předcházení nemoci erytrocyty, trombocyty, granulocyty, plazma. Jedná se o individuálně
Trombocytové přípravky v náhradních roztocích
 Trombocytové transfuzní přípravky v náhradních roztocích - zkušenosti TO KNL, a.s. Maříková Š., Řehořová L., Procházková R. Transfuzní oddělení, Krajská nemocnice Liberec, a.s. 6. STŘEŠOVICKÝ TRANSFUZNÍ
Trombocytové transfuzní přípravky v náhradních roztocích - zkušenosti TO KNL, a.s. Maříková Š., Řehořová L., Procházková R. Transfuzní oddělení, Krajská nemocnice Liberec, a.s. 6. STŘEŠOVICKÝ TRANSFUZNÍ
Roční výkaz o činnosti poskytovatele ZS A (MZ) 1-01
 Ministerstvo zdravotnictví Schváleno ČSÚ pro Ministerstvo zdravotnictví. ČV 126/14 ze dne 30.10.2013 v rámci Programu statistických zjišťování na rok 2014. Vyplněný výkaz předložte pracovišti státní statistické
Ministerstvo zdravotnictví Schváleno ČSÚ pro Ministerstvo zdravotnictví. ČV 126/14 ze dne 30.10.2013 v rámci Programu statistických zjišťování na rok 2014. Vyplněný výkaz předložte pracovišti státní statistické
OPRAVA ČESKÉHO OBRANNÉHO STANDARDU
 OPRAVA ČESKÉHO OBRANNÉHO STANDARDU. Označení a název opravovaného ČOS 653,. vydání MINIMÁLNÍ POŽADAVKY NA KREV, DÁRCE KRVE, VYBAVENÍ PRO KREVNÍ TRANSFUZI A OZNAČOVÁNÍ KREVNÍCH SKUPIN 2. Oprava č.. Část
OPRAVA ČESKÉHO OBRANNÉHO STANDARDU. Označení a název opravovaného ČOS 653,. vydání MINIMÁLNÍ POŽADAVKY NA KREV, DÁRCE KRVE, VYBAVENÍ PRO KREVNÍ TRANSFUZI A OZNAČOVÁNÍ KREVNÍCH SKUPIN 2. Oprava č.. Část
Roční výkaz o činnosti ZZ A (MZ) 1-01
 Ministerstvo zdravotnictví Schváleno ČSÚ pro Ministerstvo zdravotnictví. ČV 177/10 ze dne 20.10.2009 v rámci Programu statistických zjišťování na rok 2010. Vyplněný výkaz laskavě předložte pracovišti státní
Ministerstvo zdravotnictví Schváleno ČSÚ pro Ministerstvo zdravotnictví. ČV 177/10 ze dne 20.10.2009 v rámci Programu statistických zjišťování na rok 2010. Vyplněný výkaz laskavě předložte pracovišti státní
Spolupráce transfuziologa a anesteziologa/intenzivisty - cesta k účelné hemoterapii
 Spolupráce transfuziologa a anesteziologa/intenzivisty - cesta k účelné hemoterapii Hana Lejdarová TTO FN Brno XXIV. Kongres ČSARIM, 7. 9.9.2017, Brno Proč? Nestačí údaje na žádance? Máme na konzultaci
Spolupráce transfuziologa a anesteziologa/intenzivisty - cesta k účelné hemoterapii Hana Lejdarová TTO FN Brno XXIV. Kongres ČSARIM, 7. 9.9.2017, Brno Proč? Nestačí údaje na žádance? Máme na konzultaci
Fakultní nemocnice a Lékařská fakulta UK Hradec Králové
 Deleukotizace transfuzních přípravků - dočká se český pacient? V. Řeháček k Transfuzní oddělení Fakultní nemocnice a Lékařská fakulta UK Hradec Králové STŘEŠOVICKÝ TRANSFUZNÍ DEN, Praha, 22. 23. LISTOPADU
Deleukotizace transfuzních přípravků - dočká se český pacient? V. Řeháček k Transfuzní oddělení Fakultní nemocnice a Lékařská fakulta UK Hradec Králové STŘEŠOVICKÝ TRANSFUZNÍ DEN, Praha, 22. 23. LISTOPADU
PRVKY BEZPEČNOSTI Č VE VÝROBĚ TRANSFUZNÍCH PŘÍPRAVKŮ
 PRVKY BEZPEČNOSTI Č FAKULTNÍ NEMOCNICE BRNO VE VÝROBĚ TRANSFUZNÍCH PŘÍPRAVKŮ EVA TESAŘOVÁ 6. STŘEŠOVICKÝ TRANSFUZNÍ DEN, PRAHA, 22.11.2012 1 BEZPEČNÁ HEMOTERAPIE Bezpečné postupy Bezpečné produkty Implementaci
PRVKY BEZPEČNOSTI Č FAKULTNÍ NEMOCNICE BRNO VE VÝROBĚ TRANSFUZNÍCH PŘÍPRAVKŮ EVA TESAŘOVÁ 6. STŘEŠOVICKÝ TRANSFUZNÍ DEN, PRAHA, 22.11.2012 1 BEZPEČNÁ HEMOTERAPIE Bezpečné postupy Bezpečné produkty Implementaci
Transfuzní lékařství SEMINÁŘ
 Transfuzní lékařství SEMINÁŘ Fakultní nemocnice Olomouc - komise účelné hemoterapie Transfuzní oddělení příprava transfúzních přípravků laboratoř testů slučitelnosti skladování transfúzních přípravků imunohematologické
Transfuzní lékařství SEMINÁŘ Fakultní nemocnice Olomouc - komise účelné hemoterapie Transfuzní oddělení příprava transfúzních přípravků laboratoř testů slučitelnosti skladování transfúzních přípravků imunohematologické
Potransfuzní reakce. Rozdělení potransfuzních reakcí a komplikací
 Potransfuzní reakce Potransfuzní reakcí rozumíme nežádoucí účinek podaného transfuzního přípravku. Od roku 2005 (dle platné legislativy) rozlišujeme: závažná nežádoucí příhoda ( vzniká v souvislosti s
Potransfuzní reakce Potransfuzní reakcí rozumíme nežádoucí účinek podaného transfuzního přípravku. Od roku 2005 (dle platné legislativy) rozlišujeme: závažná nežádoucí příhoda ( vzniká v souvislosti s
Racionální hemoterapie
 Racionální hemoterapie motto racionální hemoterapie: podat správný přípravek správnému pacientovi správnou technikou ve správnou chvíli Léčivé přípravky z krve transfuzní přípravky: vyráběné v rámci TO
Racionální hemoterapie motto racionální hemoterapie: podat správný přípravek správnému pacientovi správnou technikou ve správnou chvíli Léčivé přípravky z krve transfuzní přípravky: vyráběné v rámci TO
Organizace transfuzní služby. I.Sulovská
 Organizace transfuzní služby I.Sulovská Transfuzní oddělení Výroba transfuzních přípravků (TP) řízena zákony, vyhláškami a metodickými pokyny 2 druhy TO: výrobci TP odběrová střediska Výrobci TP mají uděleno
Organizace transfuzní služby I.Sulovská Transfuzní oddělení Výroba transfuzních přípravků (TP) řízena zákony, vyhláškami a metodickými pokyny 2 druhy TO: výrobci TP odběrová střediska Výrobci TP mají uděleno
Transfuziologie. medici
 Transfuziologie medici Základní informace o transfúzním oddělení Bezpečnost transfúze závisí především na výběru vhodného dárce a poodběrovém serologickém vyšetření Poučení pro dárce - na začátku. Osobní
Transfuziologie medici Základní informace o transfúzním oddělení Bezpečnost transfúze závisí především na výběru vhodného dárce a poodběrovém serologickém vyšetření Poučení pro dárce - na začátku. Osobní
Organizace skladování a výdeje transfuzních přípravků Sekundární výroba SIMONA HOHLOVÁ TRANSFUZNÍ A TKÁŇOVÉ ODDĚLENÍ
 Organizace skladování a výdeje transfuzních přípravků Sekundární výroba SIMONA HOHLOVÁ TRANSFUZNÍ A TKÁŇOVÉ ODDĚLENÍ Osnova Definice + obecné poznámky Příjem na sklad Skladování Monitorování Výdej Transport
Organizace skladování a výdeje transfuzních přípravků Sekundární výroba SIMONA HOHLOVÁ TRANSFUZNÍ A TKÁŇOVÉ ODDĚLENÍ Osnova Definice + obecné poznámky Příjem na sklad Skladování Monitorování Výdej Transport
 Transfúze krve Krevní transfúze je proces, během kterého je do krevního oběhu příjemce vpravena krev nebo krevní složky od dárce je možné ji považovat za specifický případ transplantace orgánu. Dárcovství
Transfúze krve Krevní transfúze je proces, během kterého je do krevního oběhu příjemce vpravena krev nebo krevní složky od dárce je možné ji považovat za specifický případ transplantace orgánu. Dárcovství
Kontroly jakosti v ZTS. MVDr. Naďa Poloková TTO FN Brno
 Kontroly jakosti v ZTS MVDr. Naďa Poloková TTO FN Brno 1 Kontrola kvality (jakosti) - definice Kvalita (jakost) je pojmem pro zpravidla kladné vlastnosti výrobku nebo služby. Kvalitní výrobek nebo služba
Kontroly jakosti v ZTS MVDr. Naďa Poloková TTO FN Brno 1 Kontrola kvality (jakosti) - definice Kvalita (jakost) je pojmem pro zpravidla kladné vlastnosti výrobku nebo služby. Kvalitní výrobek nebo služba
PŘÍLOHA č. 1 TRANSFUZNÍ PŘÍPRAVKY ČÍSLO OOP: Andersová, Sasková DNE: VYPRACOVAL: Obsah
 PŘÍLOHA č. 1 TRANSFUZNÍ PŘÍPRAVKY SPISOVÁ ZNAČKA: SUKLS156267/2018 ČÍSLO OOP: 01-18 VYŘIZUJE: Vysekalová VYPRACOVAL: Andersová, Sasková DNE: 29.3.2018 Obsah 1) Přehled výkonů a přípravků zahrnutých do
PŘÍLOHA č. 1 TRANSFUZNÍ PŘÍPRAVKY SPISOVÁ ZNAČKA: SUKLS156267/2018 ČÍSLO OOP: 01-18 VYŘIZUJE: Vysekalová VYPRACOVAL: Andersová, Sasková DNE: 29.3.2018 Obsah 1) Přehled výkonů a přípravků zahrnutých do
Mgr. Dagmar Chátalova
 Mgr. Dagmar Chátalova Transfuze - převod lidské krve nebo krevních přípravků od jednoho člověka ( dárce ) do krevního oběhu druhého člověka ( příjemce ) Indikace při ztrátě krve úraz, operace,těžký porod,
Mgr. Dagmar Chátalova Transfuze - převod lidské krve nebo krevních přípravků od jednoho člověka ( dárce ) do krevního oběhu druhého člověka ( příjemce ) Indikace při ztrátě krve úraz, operace,těžký porod,
Návod k vyplnění výročních zpráv o závažných nežádoucích reakcích a závažných nežádoucích událostech:
 Návod k vyplnění výročních zpráv o závažných nežádoucích reakcích a závažných nežádoucích událostech: Prázdné tabulky (vzory) z vyhlášky 143/2008 Sb. jsou k dispozici na webových stránkách SÚKLu: http://www.sukl.cz/zdravotnicka-zarizeni/formulare
Návod k vyplnění výročních zpráv o závažných nežádoucích reakcích a závažných nežádoucích událostech: Prázdné tabulky (vzory) z vyhlášky 143/2008 Sb. jsou k dispozici na webových stránkách SÚKLu: http://www.sukl.cz/zdravotnicka-zarizeni/formulare
ČOS 650003 1. vydání ČESKÝ OBRANNÝ STANDARD MINIMÁLNÍ POŽADAVKY NA KREV, DÁRCE KRVE, VYBAVENÍ PRO KREVNÍ TRANSFUZI A OZNAČOVÁNÍ KREVNÍCH SKUPIN
 ČESKÝ OBRANNÝ STANDARD MINIMÁLNÍ POŽADAVKY NA KREV, DÁRCE KRVE, VYBAVENÍ PRO KREVNÍ TRANSFUZI A OZNAČOVÁNÍ KREVNÍCH SKUPIN (VOLNÁ STRANA) 2 ČESKÝ OBRANNÝ STANDARD MINIMÁLNÍ POŽADAVKY NA KREV, DÁRCE KRVE,
ČESKÝ OBRANNÝ STANDARD MINIMÁLNÍ POŽADAVKY NA KREV, DÁRCE KRVE, VYBAVENÍ PRO KREVNÍ TRANSFUZI A OZNAČOVÁNÍ KREVNÍCH SKUPIN (VOLNÁ STRANA) 2 ČESKÝ OBRANNÝ STANDARD MINIMÁLNÍ POŽADAVKY NA KREV, DÁRCE KRVE,
c) příjemcem osoba, která obdržela transfuzi krve nebo krevních
 L 256/32 Úřední věstník Evropské unie 1.10.2005 SMĚRNICE KOMISE 2005/61/ES ze dne 30. září 2005, kterou se provádí směrnice Evropského parlamentu a Rady 2002/98/ES, pokud jde o požadavky na sledovatelnost
L 256/32 Úřední věstník Evropské unie 1.10.2005 SMĚRNICE KOMISE 2005/61/ES ze dne 30. září 2005, kterou se provádí směrnice Evropského parlamentu a Rady 2002/98/ES, pokud jde o požadavky na sledovatelnost
Dárcovství krve a typy odběrů MUDr. Simona Hohlová
 Dárcovství krve a typy odběrů MUDr. Simona Hohlová Transfuzní a tkáňové oddělení Osnova Dárcovství krve o obecné principy o propagace dárcovství a oceňování dárců krve o registry dárců krve a jejích složek
Dárcovství krve a typy odběrů MUDr. Simona Hohlová Transfuzní a tkáňové oddělení Osnova Dárcovství krve o obecné principy o propagace dárcovství a oceňování dárců krve o registry dárců krve a jejích složek
SOUHRN ÚDAJŮ O PŘÍPRAVKU. Obsah anti-d imunoglobulinu obsaženého v přípravku PARTOBULIN SDF je stanoven metodou dle Evropského lékopisu.
 Příloha č. 2 k rozhodnutí o změně registrace sp. zn. sukls215609/2010 1. NÁZEV PŘÍPRAVKU SOUHRN ÚDAJŮ O PŘÍPRAVKU PARTOBULIN SDF Lidský anti-d imunoglobulin k intramuskulárnímu podání. 2. KVALITATIVNÍ
Příloha č. 2 k rozhodnutí o změně registrace sp. zn. sukls215609/2010 1. NÁZEV PŘÍPRAVKU SOUHRN ÚDAJŮ O PŘÍPRAVKU PARTOBULIN SDF Lidský anti-d imunoglobulin k intramuskulárnímu podání. 2. KVALITATIVNÍ
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU ANTITHROMBIN III NF BAXTER, prášek pro přípravu infuzního roztoku s rozpouštědlem 2. SLOŽENÍ KVALITATIVNÍ A KVANTITATIVNÍ 1 ml rozpuštěného přípravku obsahuje
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU ANTITHROMBIN III NF BAXTER, prášek pro přípravu infuzního roztoku s rozpouštědlem 2. SLOŽENÍ KVALITATIVNÍ A KVANTITATIVNÍ 1 ml rozpuštěného přípravku obsahuje
TRANSFUZNÍ PŘÍPRAVKY A KREVNÍ DERIVÁTY. MUDr. Hana Lejdarová TTO FN Brno Katedra laboratorních metod LF MU
 TRANSFUZNÍ PŘÍPRAVKY A KREVNÍ DERIVÁTY MUDr. Hana Lejdarová TTO FN Brno Katedra laboratorních metod LF MU Definice Transfuzní přípravek IVLP Maximálně 10 dárců Není ošetřen metodou inaktivace patogenů
TRANSFUZNÍ PŘÍPRAVKY A KREVNÍ DERIVÁTY MUDr. Hana Lejdarová TTO FN Brno Katedra laboratorních metod LF MU Definice Transfuzní přípravek IVLP Maximálně 10 dárců Není ošetřen metodou inaktivace patogenů
 Ošetřovatelský proces při aplikaci transfuze Transfuze Transfuze krve je převod krve nebo krevních přípravků do krevního oběhu druhého člověka Indikace ke transfuzi - ztráty velkého množství krve (úraz,
Ošetřovatelský proces při aplikaci transfuze Transfuze Transfuze krve je převod krve nebo krevních přípravků do krevního oběhu druhého člověka Indikace ke transfuzi - ztráty velkého množství krve (úraz,
Jedna předplněná injekční stříkačka obsahuje immunoglobulinum humanum anti-d 1500 IU (300 mikrogramů).
 sp. zn. sukls262204/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Igamad 1500 IU, injekční roztok v předplněné injekční stříkačce 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna předplněná injekční stříkačka
sp. zn. sukls262204/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Igamad 1500 IU, injekční roztok v předplněné injekční stříkačce 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna předplněná injekční stříkačka
Komplikace krevního převodu. I. Sulovská
 Komplikace krevního převodu I. Sulovská POTRANSFÚZNÍ REAKCE = všechny nežádoucí účinky související s podáním transfúzního přípravku Dělení: podle časové souvislosti s aplikací transfúze akutní (bezprostředně
Komplikace krevního převodu I. Sulovská POTRANSFÚZNÍ REAKCE = všechny nežádoucí účinky související s podáním transfúzního přípravku Dělení: podle časové souvislosti s aplikací transfúze akutní (bezprostředně
Projekt: Digitální učební materiály ve škole, registrační číslo projektu CZ.1.07/1.5.00/34.0527
 Projekt: Digitální učební materiály ve škole, registrační číslo projektu CZ.1.07/1.5.00/34.0527 Příjemce: Střední zdravotnická škola a Vyšší odborná škola zdravotnická, Husova 3, 371 60 České Budějovice
Projekt: Digitální učební materiály ve škole, registrační číslo projektu CZ.1.07/1.5.00/34.0527 Příjemce: Střední zdravotnická škola a Vyšší odborná škola zdravotnická, Husova 3, 371 60 České Budějovice
Kontrola jakosti transfuzních přípravků BAKALÁŘSKÁ PRÁCE. Studijní program: SPECIALIZACE VE ZDRAVOTNICTVÍ. Autor: Barbora Nováčková
 Kontrola jakosti transfuzních přípravků BAKALÁŘSKÁ PRÁCE Studijní program: SPECIALIZACE VE ZDRAVOTNICTVÍ Autor: Barbora Nováčková Vedoucí práce: PharmDr. Hana Staňková České Budějovice 2017 Prohlášení
Kontrola jakosti transfuzních přípravků BAKALÁŘSKÁ PRÁCE Studijní program: SPECIALIZACE VE ZDRAVOTNICTVÍ Autor: Barbora Nováčková Vedoucí práce: PharmDr. Hana Staňková České Budějovice 2017 Prohlášení
L a b o r a t o r n í p ř í r u č k a. Hematologicko-transfúzní oddělení
 L a b o r a t o r n í p ř í r u č k a Strana 1 z 14 Identifikace, důležité údaje Název zařízení Oblastní nemocnice Kladno, a.s., Nemocnice SČK, Vančurova 1548, Kladno Identifikační údaje IČO 27256537 DIČ
L a b o r a t o r n í p ř í r u č k a Strana 1 z 14 Identifikace, důležité údaje Název zařízení Oblastní nemocnice Kladno, a.s., Nemocnice SČK, Vančurova 1548, Kladno Identifikační údaje IČO 27256537 DIČ
A, B, AB, 0. Interpretace dle návodu k diagnostiku.
 Katalog laboratorních vyšetření změna č. 2, platnost od 01.10.2016 Krevní skupina A, B, AB, 0. Interpretace dle návodu k diagnostiku. Rutina: do 72 hodin Statim: do 2 hodin od doby doručení vzorku na TO
Katalog laboratorních vyšetření změna č. 2, platnost od 01.10.2016 Krevní skupina A, B, AB, 0. Interpretace dle návodu k diagnostiku. Rutina: do 72 hodin Statim: do 2 hodin od doby doručení vzorku na TO
PŘÍLOHA č. 1 TRANSFUZNÍ PŘÍPRAVKY ČÍSLO OOP: Andersová, Sasková DNE: VYPRACOVAL: Obsah
 PŘÍLOHA č. 1 TRANSFUZNÍ PŘÍPRAVKY SPISOVÁ ZNAČKA: SUKLS314042/2018 ČÍSLO OOP: 04-18 VYŘIZUJE: Vysekalová VYPRACOVAL: Andersová, Sasková DNE: 30.8.2018 Obsah 1) Přehled výkonů a přípravků zahrnutých do
PŘÍLOHA č. 1 TRANSFUZNÍ PŘÍPRAVKY SPISOVÁ ZNAČKA: SUKLS314042/2018 ČÍSLO OOP: 04-18 VYŘIZUJE: Vysekalová VYPRACOVAL: Andersová, Sasková DNE: 30.8.2018 Obsah 1) Přehled výkonů a přípravků zahrnutých do
Aplikace transfuzních přípravků je problémem multioborovým a stanované přesné postupy mají zajistit vyšší bezpečnost hemopterapie.
 Název studijního předmětu Téma Název kapitoly Autor - autoři Hemoterapie Transfuze Aplikace transfuzních přípravků MUDr. Dana Galuszková, Ph.D., MBA 1. Motivační úvod ke kapitole Aplikace transfuzních
Název studijního předmětu Téma Název kapitoly Autor - autoři Hemoterapie Transfuze Aplikace transfuzních přípravků MUDr. Dana Galuszková, Ph.D., MBA 1. Motivační úvod ke kapitole Aplikace transfuzních
Příloha č. 3 k rozhodnutí o prodloužení registrace sp.zn. sukls167902/2010 a příloha k sp. zn. sukls16927/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 3 k rozhodnutí o prodloužení registrace sp.zn. sukls167902/2010 a příloha k sp. zn. sukls16927/2011 1. NÁZEV PŘÍPRAVKU SOUHRN ÚDAJŮ O PŘÍPRAVKU Rhophylac 300 mikrogramů/2 ml, injekční roztok
Příloha č. 3 k rozhodnutí o prodloužení registrace sp.zn. sukls167902/2010 a příloha k sp. zn. sukls16927/2011 1. NÁZEV PŘÍPRAVKU SOUHRN ÚDAJŮ O PŘÍPRAVKU Rhophylac 300 mikrogramů/2 ml, injekční roztok
Zajištění hemoterapie u masivního krvácení v KN Liberec. Procházková Renata Transfuzní oddělení, Krajská nemocnice Liberec, a.s.
 Zajištění hemoterapie u masivního krvácení v KN Liberec Procházková Renata Transfuzní oddělení, Krajská nemocnice Liberec, a.s. Masivní krevní ztráta Život ohrožující krvácení 50% ztráta objemu krve během
Zajištění hemoterapie u masivního krvácení v KN Liberec Procházková Renata Transfuzní oddělení, Krajská nemocnice Liberec, a.s. Masivní krevní ztráta Život ohrožující krvácení 50% ztráta objemu krve během
ESA - erytropoézu stimulující agens a jejich použití v klinické praxi
 ESA - erytropoézu stimulující agens a jejich použití v klinické praxi T. Kotulák Klinika anestezie a resuscitace, IKEM, Praha a 1. LF UK a VFN, Praha etiologie ICU anémie anémie kritických stavů je častý
ESA - erytropoézu stimulující agens a jejich použití v klinické praxi T. Kotulák Klinika anestezie a resuscitace, IKEM, Praha a 1. LF UK a VFN, Praha etiologie ICU anémie anémie kritických stavů je častý
Informace ze zdravotnictví Jihomoravského kraje
 Informace ze zdravotnictví Jihomoravského kraje Ústavu zdravotnických informací a statistiky České republiky Brno 1 11.5.2004 Transfúzní služba - činnost v Jihomoravském kraji v roce 2003 Činnost transfúzní
Informace ze zdravotnictví Jihomoravského kraje Ústavu zdravotnických informací a statistiky České republiky Brno 1 11.5.2004 Transfúzní služba - činnost v Jihomoravském kraji v roce 2003 Činnost transfúzní
Léčba anemie. Prim. MUDr. Jan Straub I. Interní klinika VFN Praha
 Léčba anemie Prim. MUDr. Jan Straub I. Interní klinika VFN Praha Anemie Nedostatek červených krvinek - erytrocytů resp. krevního barviva - hemoglobinu Stupně anemie normální KO hgb 120-175 g/l lehká anemie
Léčba anemie Prim. MUDr. Jan Straub I. Interní klinika VFN Praha Anemie Nedostatek červených krvinek - erytrocytů resp. krevního barviva - hemoglobinu Stupně anemie normální KO hgb 120-175 g/l lehká anemie
ČOS vydání ČESKÝ OBRANNÝ STANDARD MINIMÁLNÍ POŽADAVKY NA KREV, DÁRCE KRVE, VYBAVENÍ PRO KREVNÍ TRANSFUZI A OZNAČOVÁNÍ KREVNÍCH SKUPIN
 ČESKÝ OBRANNÝ STANDARD MINIMÁLNÍ POŽADAVKY NA KREV, DÁRCE KRVE, VYBAVENÍ PRO KREVNÍ TRANSFUZI A OZNAČOVÁNÍ KREVNÍCH SKUPIN (VOLNÁ STRANA) 2 ČESKÝ OBRANNÝ STANDARD MINIMÁLNÍ POŽADAVKY NA KREV, DÁRCE KRVE,
ČESKÝ OBRANNÝ STANDARD MINIMÁLNÍ POŽADAVKY NA KREV, DÁRCE KRVE, VYBAVENÍ PRO KREVNÍ TRANSFUZI A OZNAČOVÁNÍ KREVNÍCH SKUPIN (VOLNÁ STRANA) 2 ČESKÝ OBRANNÝ STANDARD MINIMÁLNÍ POŽADAVKY NA KREV, DÁRCE KRVE,
Příloha III. Úpravy příslušných částí Souhrnu údajů o přípravku a Příbalové informace
 Příloha III Úpravy příslušných částí Souhrnu údajů o přípravku a Příbalové informace Poznámka: Tento Souhrn údajů o přípravku, Označení na obalu a Příbalová informace jsou výsledkem posuzovacího řízení.
Příloha III Úpravy příslušných částí Souhrnu údajů o přípravku a Příbalové informace Poznámka: Tento Souhrn údajů o přípravku, Označení na obalu a Příbalová informace jsou výsledkem posuzovacího řízení.
Odběr krvetvorných buněk z periferní krve: příprava, průběh a komplikace
 Odběr krvetvorných buněk z periferní krve: příprava, průběh a komplikace Helena Švábová, Andrea Žmijáková Interní hematologická a onkologická klinika FN Brno Separační středisko je součástí Interní hematologické
Odběr krvetvorných buněk z periferní krve: příprava, průběh a komplikace Helena Švábová, Andrea Žmijáková Interní hematologická a onkologická klinika FN Brno Separační středisko je součástí Interní hematologické
vyrobený z lidské krevní plazmy
 IVIG - léčivý přípravek p pravek vyrobený z lidské krevní plazmy Pacasová R., Tesařov ová E. Transfuzní oddělen lení a krevní banka Fakultní nemocnice Brno IVIG - léčivý přípravekp pravek KIOVIG - BAXTER
IVIG - léčivý přípravek p pravek vyrobený z lidské krevní plazmy Pacasová R., Tesařov ová E. Transfuzní oddělen lení a krevní banka Fakultní nemocnice Brno IVIG - léčivý přípravekp pravek KIOVIG - BAXTER
Vydání: 4 Datum účinnosti: str. 1 z 6 Metodika stanovení úhrady individuálně vyráběných transfuzních přípravků SP-CAU W
 str. 1 z 6 1. CÍL Stanovit metodiku pro postup stanovení úhrady individuálně vyráběných 2. UŽIVATELÉ Postup je závazný pro pracovníky sekce cenové a úhradové regulace. 3. DEFINICE POJMŮ A ZKRATKY SÚKL,
str. 1 z 6 1. CÍL Stanovit metodiku pro postup stanovení úhrady individuálně vyráběných 2. UŽIVATELÉ Postup je závazný pro pracovníky sekce cenové a úhradové regulace. 3. DEFINICE POJMŮ A ZKRATKY SÚKL,
CON plná krev Proč plnou krev nepotřebuji / nechci
 CON plná krev Proč plnou krev nepotřebuji / nechci Pavel Sedlák ARO- Krajská nemocnice Liberec Conflict of interest CSL Behring Fressenius Medista Novo-Nordisk Kde žiju, co dělám Krajská nemocnice Liberec,
CON plná krev Proč plnou krev nepotřebuji / nechci Pavel Sedlák ARO- Krajská nemocnice Liberec Conflict of interest CSL Behring Fressenius Medista Novo-Nordisk Kde žiju, co dělám Krajská nemocnice Liberec,
Guide to the preparation, use and quality assurance of blood components, 18th edition, 2015
 Hana Lejdarová, Rita Pacasová TTO FN Brno Katedra laboratorních metod LF MU XI. Střešovickýý transfuzní den,, 29.11.2017,, Praha Granulocyty z aferézy definice: Guide to the preparation, use and quality
Hana Lejdarová, Rita Pacasová TTO FN Brno Katedra laboratorních metod LF MU XI. Střešovickýý transfuzní den,, 29.11.2017,, Praha Granulocyty z aferézy definice: Guide to the preparation, use and quality
Erytrocyty. Hemoglobin. Krevní skupiny a Rh faktor. Krevní transfúze. Somatologie Mgr. Naděžda Procházková
 Erytrocyty. Hemoglobin. Krevní skupiny a Rh faktor. Krevní transfúze. Somatologie Mgr. Naděžda Procházková Formované krevní elementy: Buněčné erytrocyty, leukocyty Nebuněčné trombocyty Tvorba krevních
Erytrocyty. Hemoglobin. Krevní skupiny a Rh faktor. Krevní transfúze. Somatologie Mgr. Naděžda Procházková Formované krevní elementy: Buněčné erytrocyty, leukocyty Nebuněčné trombocyty Tvorba krevních
Pravidelné roční hodnocení stanovené výše a podmínek úhrad za rok 2014 Podskupina 12 a 15 - individuálně vyráběné transfuzní přípravky
 sp. zn. sukls51964/2015 Pravidelné roční hodnocení stanovené výše a podmínek úhrad za rok 2014 Podskupina 12 a 15 - individuálně vyráběné transfuzní přípravky Státní ústav pro kontrolu léčiv (dále jen
sp. zn. sukls51964/2015 Pravidelné roční hodnocení stanovené výše a podmínek úhrad za rok 2014 Podskupina 12 a 15 - individuálně vyráběné transfuzní přípravky Státní ústav pro kontrolu léčiv (dále jen
Lánská M. 1,Bláha M. 1, Zavřelová A. 1, Řeháček V. 2, Žák P. 1
 Význam výměnné plazmaferézy u AB0 inkompatibilní alogenní transplantace krvetvorných buněk Lánská M. 1,Bláha M. 1, Zavřelová A. 1, Řeháček V. 2, Žák P. 1 1 IV Interní hematologická klinika FN Hradec Králové
Význam výměnné plazmaferézy u AB0 inkompatibilní alogenní transplantace krvetvorných buněk Lánská M. 1,Bláha M. 1, Zavřelová A. 1, Řeháček V. 2, Žák P. 1 1 IV Interní hematologická klinika FN Hradec Králové
Příloha č. 3 k rozhodnutí o prodloužení registrace sp. zn. sukls12350/2006 a příloha k sp zn. sukls41484/2007, sukls49174/2008
 Příloha č. 3 k rozhodnutí o prodloužení registrace sp. zn. sukls12350/2006 a příloha k sp zn. sukls41484/2007, sukls49174/2008 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 NÁZEV PŘÍPRAVKU Rhesonativ 625 IU/ml, injekční
Příloha č. 3 k rozhodnutí o prodloužení registrace sp. zn. sukls12350/2006 a příloha k sp zn. sukls41484/2007, sukls49174/2008 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 NÁZEV PŘÍPRAVKU Rhesonativ 625 IU/ml, injekční
Praxbind doporučení pro podávání (SPC)
 Praxbind doporučení pro podávání (SPC) Idarucizumab je indikován pro použití v případech, kde je zapotřebí rychlá antagonizace antagonizačních účinků dabigatranu Idarucizumab je specifický přípravek pro
Praxbind doporučení pro podávání (SPC) Idarucizumab je indikován pro použití v případech, kde je zapotřebí rychlá antagonizace antagonizačních účinků dabigatranu Idarucizumab je specifický přípravek pro
Transfuzní lékařství. Vít Řeháček, Jiří Masopust a kolektiv. Vít Řeháček, Jiří Masopust a kolektiv
 Grada Publishing, a.s., U Průhonu 22, 170 00 Praha 7 tel.: +420 234 264 401, fax: +420 234 264 400 e-mail: obchod@grada.cz, www.grada.cz Vít Řeháček, Jiří Masopust a kolektiv Transfuzní lékařství Publikace
Grada Publishing, a.s., U Průhonu 22, 170 00 Praha 7 tel.: +420 234 264 401, fax: +420 234 264 400 e-mail: obchod@grada.cz, www.grada.cz Vít Řeháček, Jiří Masopust a kolektiv Transfuzní lékařství Publikace
Trombocytopenie v těhotenství
 Trombocytopenie v těhotenství doc. MUDr. Antonín Pařízek, CSc. Gynekologicko-porodnická klinika 1. LF UK a VFN v Praze Definice normální počet trombocytů u netěhotných žen 150-400 x 10 9 /l v těhotenství
Trombocytopenie v těhotenství doc. MUDr. Antonín Pařízek, CSc. Gynekologicko-porodnická klinika 1. LF UK a VFN v Praze Definice normální počet trombocytů u netěhotných žen 150-400 x 10 9 /l v těhotenství
DVĚ NEJČASTĚJŠÍ SMRTELNÉ POTRANSFUZNÍ PŘÍHODY
 Helena Ondrášková Klinika anesteziologie, resuscitace a intenzivní medicíny Fakultní nemocnice Brno Lékařská fakulta Masarykovy Univerzity Brno Česká společnost bezkrevní medicíny DVĚ NEJČASTĚJŠÍ SMRTELNÉ
Helena Ondrášková Klinika anesteziologie, resuscitace a intenzivní medicíny Fakultní nemocnice Brno Lékařská fakulta Masarykovy Univerzity Brno Česká společnost bezkrevní medicíny DVĚ NEJČASTĚJŠÍ SMRTELNÉ
UNIVERZITA KARLOVA V PRAZE
 UNIVERZITA KARLOVA V PRAZE 2. LÉKAŘSKÁ FAKULTA Oddělení krevní banky Adam Švestka Výskyt potransfuzních reakcí ve Fakultní nemocnici Motol bakalářská práce Praha 2011 Autor práce: Adam Švestka Vedoucí
UNIVERZITA KARLOVA V PRAZE 2. LÉKAŘSKÁ FAKULTA Oddělení krevní banky Adam Švestka Výskyt potransfuzních reakcí ve Fakultní nemocnici Motol bakalářská práce Praha 2011 Autor práce: Adam Švestka Vedoucí
Hematologická vyšetření krve. Tento výukový materiál vznikl za přispění Evropské unie, státního rozpočtu ČR a Středočeského kraje
 Hematologická vyšetření krve Tento výukový materiál vznikl za přispění Evropské unie, státního rozpočtu ČR a Středočeského kraje Bc. Hrušková Jindřiška duben 2009 Hematologická vyšetření Provádí je hematologicko-transfúzní
Hematologická vyšetření krve Tento výukový materiál vznikl za přispění Evropské unie, státního rozpočtu ČR a Středočeského kraje Bc. Hrušková Jindřiška duben 2009 Hematologická vyšetření Provádí je hematologicko-transfúzní
Masarykova univerzita v Brně Lékařská fakulta BAKALÁŘSKÁ PRÁCE Renáta MORAVCOVÁ
 Masarykova univerzita v Brně Lékařská fakulta BAKALÁŘSKÁ PRÁCE 2009 Renáta MORAVCOVÁ Masarykova univerzita v Brně Lékařská fakulta ANALÝZA POTRANSFUZNÍCH REAKCÍ Bakalářská práce v oboru zdravotní laborant
Masarykova univerzita v Brně Lékařská fakulta BAKALÁŘSKÁ PRÁCE 2009 Renáta MORAVCOVÁ Masarykova univerzita v Brně Lékařská fakulta ANALÝZA POTRANSFUZNÍCH REAKCÍ Bakalářská práce v oboru zdravotní laborant
KREV. Autor: Mgr. Anna Kotvrdová 29. 8. 2012
 KREV Autor: Mgr. Anna Kotvrdová 29. 8. 2012 KREV Vzdělávací oblast: Somatologie Tematický okruh: Krev Mezioborové přesahy a vazby: Ošetřovatelství, Klinická propedeutika, První pomoc, Biologie, Vybrané
KREV Autor: Mgr. Anna Kotvrdová 29. 8. 2012 KREV Vzdělávací oblast: Somatologie Tematický okruh: Krev Mezioborové přesahy a vazby: Ošetřovatelství, Klinická propedeutika, První pomoc, Biologie, Vybrané
TRANSFUZNÍ PŘÍPRAVKY A KREVNÍ DERIVÁTY. Hana Lejdarová
 TRANSFUZNÍ PŘÍPRAVKY A KREVNÍ DERIVÁTY Hana Lejdarová Definice Transfuzní přípravek IVLP Maximálně 10 dárců Není ošetřen metodou inaktivace patogenů Vyšší riziko přenosu krví přenosných chorob Zařízení
TRANSFUZNÍ PŘÍPRAVKY A KREVNÍ DERIVÁTY Hana Lejdarová Definice Transfuzní přípravek IVLP Maximálně 10 dárců Není ošetřen metodou inaktivace patogenů Vyšší riziko přenosu krví přenosných chorob Zařízení
SP-CAU-005. Metodika stanovení úhrady individuálně vyráběných transfuzních přípravků
 str. 1 z 5 Datum účinnosti: 20.05.2009 Majitel dokumentu: Jméno PharmDr.Jiří Lamka 33020 odd. datum podpis Interval revizí: 2 roky Přezkoumal MJ: Jméno Ing.Filip Kotal, PhD. datum podpis Schválil: Jméno
str. 1 z 5 Datum účinnosti: 20.05.2009 Majitel dokumentu: Jméno PharmDr.Jiří Lamka 33020 odd. datum podpis Interval revizí: 2 roky Přezkoumal MJ: Jméno Ing.Filip Kotal, PhD. datum podpis Schválil: Jméno
Elecsys anti HCV II ROCHE. 8. střešovický transfuzní den Praha 26. listopadu 2014
 Posouzení IVD: Elecsys anti HCV II ROCHE Tesařová Eva, Křížová Eva, Pacasová Rita 8. střešovický transfuzní den Praha 26. listopadu 2014 Hepatitis C virus obalený RNA virus o průměru 50 nm čeleď Flaviviridae,
Posouzení IVD: Elecsys anti HCV II ROCHE Tesařová Eva, Křížová Eva, Pacasová Rita 8. střešovický transfuzní den Praha 26. listopadu 2014 Hepatitis C virus obalený RNA virus o průměru 50 nm čeleď Flaviviridae,
JAK POMÁHÁ DAROVÁNÍ KRVE A PLAZMY
 JAK POMÁHÁ DAROVÁNÍ KRVE A PLAZMY > Bonusy pro držitele klientských karet > Široký sortiment za výhodné ceny > Osobní přístup k pacientům > Vysoká odbornost personálu > Komplexní péče o pacienta Lékárna
JAK POMÁHÁ DAROVÁNÍ KRVE A PLAZMY > Bonusy pro držitele klientských karet > Široký sortiment za výhodné ceny > Osobní přístup k pacientům > Vysoká odbornost personálu > Komplexní péče o pacienta Lékárna
Laboratorní manuál Transfuzního oddělení FNOL
 Příloha č. 2 LM/TO-01-2 Katalog laboratorních vyšetření Krevní skupina Statim: do 2 hodin od doby doručení vzorku na TO (pouze jako součást předtransfuzní vyšetření - screening protilátek + test slučitelnosti
Příloha č. 2 LM/TO-01-2 Katalog laboratorních vyšetření Krevní skupina Statim: do 2 hodin od doby doručení vzorku na TO (pouze jako součást předtransfuzní vyšetření - screening protilátek + test slučitelnosti
Interpretace dle návodu k diagnostiku.
 Katalog laboratorních vyšetření Krevní skupina Statim: do 2 hodin od doby doručení vzorku na TO (pouze jako součást předtransfuzní vyšetření - screening protilátek + test slučitelnosti v režimu STATIM).
Katalog laboratorních vyšetření Krevní skupina Statim: do 2 hodin od doby doručení vzorku na TO (pouze jako součást předtransfuzní vyšetření - screening protilátek + test slučitelnosti v režimu STATIM).
Okruh otázek k atestační zkoušce pro obor specializačního vzdělávání Klinická hematologie a transfuzní služba
 Okruh otázek k atestační zkoušce pro obor specializačního vzdělávání Klinická hematologie a transfuzní služba Zdravotní laborant pro klinickou hematologii a transfuzní službu I. Hematologie se zaměřením
Okruh otázek k atestační zkoušce pro obor specializačního vzdělávání Klinická hematologie a transfuzní služba Zdravotní laborant pro klinickou hematologii a transfuzní službu I. Hematologie se zaměřením
PŘÍLOHA č. 1 TRANSFUZNÍ PŘÍPRAVKY ČÍSLO OOP: Andersová, Sasková DNE: VYPRACOVAL: Obsah
 PŘÍLOHA č. 1 TRANSFUZNÍ PŘÍPRAVKY SPISOVÁ ZNAČKA: SUKLS338562/2017 ČÍSLO OOP: 04-17 VYŘIZUJE: Vysekalová VYPRACOVAL: Andersová, Sasková DNE: 16.11.2017 Obsah 1) Přehled výkonů a přípravků zahrnutých do
PŘÍLOHA č. 1 TRANSFUZNÍ PŘÍPRAVKY SPISOVÁ ZNAČKA: SUKLS338562/2017 ČÍSLO OOP: 04-17 VYŘIZUJE: Vysekalová VYPRACOVAL: Andersová, Sasková DNE: 16.11.2017 Obsah 1) Přehled výkonů a přípravků zahrnutých do
Zásady účelné hemoterapie a podávání krevních transfuzí. Miloš Bohoněk
 Zásady účelné hemoterapie a podávání krevních transfuzí Miloš Bohoněk Podání krevní transfuze je z mnoha příčin nutné považovat za rizikový výkon. Velikost rizika lze minimalizovat, ale nelze jej nikdy
Zásady účelné hemoterapie a podávání krevních transfuzí Miloš Bohoněk Podání krevní transfuze je z mnoha příčin nutné považovat za rizikový výkon. Velikost rizika lze minimalizovat, ale nelze jej nikdy
Závazné pokyny pro vyplňování statistického formuláře A (MZ) 1-01: Roční výkaz o činnosti poskytovatele zdravotních služeb pro obor
 Program statistických zjišťování Ministerstva zdravotnictví na rok 2016 ÚZIS ČR Závazné pokyny pro vyplňování statistického formuláře A (MZ) 1-01: Roční výkaz o činnosti poskytovatele zdravotních služeb
Program statistických zjišťování Ministerstva zdravotnictví na rok 2016 ÚZIS ČR Závazné pokyny pro vyplňování statistického formuláře A (MZ) 1-01: Roční výkaz o činnosti poskytovatele zdravotních služeb
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. INTRATECT 50 g/l infuzní roztok Immunoglobulinum humanum normale ad usum intravenosum (IVIg)
 Příloha č. 1 k rozhodnutí o registraci sp.zn. sukls228408/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE INTRATECT 50 g/l infuzní roztok Immunoglobulinum humanum normale ad usum intravenosum (IVIg)
Příloha č. 1 k rozhodnutí o registraci sp.zn. sukls228408/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE INTRATECT 50 g/l infuzní roztok Immunoglobulinum humanum normale ad usum intravenosum (IVIg)
Motto: Každá transfuze krve, která není indikovaná, je kontraindikovaná.
 Motto: Každá transfuze krve, která není indikovaná, je kontraindikovaná. NOVÉ PŘÍPADY INFEKCE HIV V ČESKÉ REPUBLICE V JEDNOTLIVÝCH LETECH (jen občané ČR a cizinci s trvalým pobytem) Absolutní údaje ke
Motto: Každá transfuze krve, která není indikovaná, je kontraindikovaná. NOVÉ PŘÍPADY INFEKCE HIV V ČESKÉ REPUBLICE V JEDNOTLIVÝCH LETECH (jen občané ČR a cizinci s trvalým pobytem) Absolutní údaje ke
LABORATORNÍ PŘÍRUČKA. Laboratoř TO
 LABORATORNÍ PŘÍRUČKA Transfuzní oddělení Laboratoř TO Účinnost od 25.01.2016 Verze č. 9 Tímto předpisem se ruší Verze č. 8, platnost od 2. 2. 2015 Odborný garant Zpracoval Přezkoumal Schválil Jméno a příjmení,
LABORATORNÍ PŘÍRUČKA Transfuzní oddělení Laboratoř TO Účinnost od 25.01.2016 Verze č. 9 Tímto předpisem se ruší Verze č. 8, platnost od 2. 2. 2015 Odborný garant Zpracoval Přezkoumal Schválil Jméno a příjmení,
NeuroBloc. botulinový toxin typu B injekční roztok, U/ml
 NeuroBloc botulinový toxin typu B injekční roztok, 5 000 U/ml Důležité bezpečnostní informace určené lékařům Účelem této příručky je poskytnout lékařům, kteří jsou oprávněni předepisovat a aplikovat přípravek
NeuroBloc botulinový toxin typu B injekční roztok, 5 000 U/ml Důležité bezpečnostní informace určené lékařům Účelem této příručky je poskytnout lékařům, kteří jsou oprávněni předepisovat a aplikovat přípravek
Hematologické laboratorní metody. Krevní obraz Koagulace Imunohematologie Podání krevní transfuze
 Hematologické laboratorní metody Krevní obraz Koagulace Imunohematologie Podání krevní transfuze Krevní obraz I leukocyty WBC (white blood cells) norma 4,0 9,0x 10 9 /l leukopenie útlum polékový, toxický,
Hematologické laboratorní metody Krevní obraz Koagulace Imunohematologie Podání krevní transfuze Krevní obraz I leukocyty WBC (white blood cells) norma 4,0 9,0x 10 9 /l leukopenie útlum polékový, toxický,
Výsledky kontroly jakosti transfuzních přípravků ve vztahu k procesu jeho výroby a ve vztahu k pohlaví dárce krve
 Masarykova univerzita v Brně Lékařská fakulta Výsledky kontroly jakosti transfuzních přípravků ve vztahu k procesu jeho výroby a ve vztahu k pohlaví dárce krve Bakalářská práce V oboru zdravotní laborant
Masarykova univerzita v Brně Lékařská fakulta Výsledky kontroly jakosti transfuzních přípravků ve vztahu k procesu jeho výroby a ve vztahu k pohlaví dárce krve Bakalářská práce V oboru zdravotní laborant
Historie Transfuzního oddělení
 Historie Transfuzního oddělení FAKULTNÍ NEMOCNICE OLOMOUC Koukalová A., Válková J., Galuszková D. Historie vzniku Transfuzního oddělení Olomouc Transfuzní stanice v Olomouci zahájila svou činnost v dubnu
Historie Transfuzního oddělení FAKULTNÍ NEMOCNICE OLOMOUC Koukalová A., Válková J., Galuszková D. Historie vzniku Transfuzního oddělení Olomouc Transfuzní stanice v Olomouci zahájila svou činnost v dubnu
PŘÍPRAVA REAGENCIÍ A STABILITA:
 REF 816A 10 lahviček z nichž každá obsahuje 0,5ml LAtrol Abnormální kontroly REF 816N 10 lahviček z nichž každá obsahuje 1,0ml LAtrol Normální kontroly UŽITÍ: LAtrol Abnormální kontrolní plazma (REF 816A)
REF 816A 10 lahviček z nichž každá obsahuje 0,5ml LAtrol Abnormální kontroly REF 816N 10 lahviček z nichž každá obsahuje 1,0ml LAtrol Normální kontroly UŽITÍ: LAtrol Abnormální kontrolní plazma (REF 816A)
??? V odborných časopisech vyhledejte články, které se týkají aplikace autotransfúze a
 Transfúze Mgr. Renata Vytejčková, Ústav ošetřovatelství 3. LF Transfuze - převod lidské krve nebo krevních přípravků od jednoho člověka ( dárce ) do krevního oběhu druhého člověka ( příjemce ) Indikace
Transfúze Mgr. Renata Vytejčková, Ústav ošetřovatelství 3. LF Transfuze - převod lidské krve nebo krevních přípravků od jednoho člověka ( dárce ) do krevního oběhu druhého člověka ( příjemce ) Indikace
Příloha č. 2 k rozhodnutí o změně registrace sp. zn. sukls10679/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 2 k rozhodnutí o změně registrace sp. zn. sukls10679/2012 1. NÁZEV PŘÍPRAVKU THYMOGLOBULINE 5 mg/ml, prášek pro infuzní roztok SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Příloha č. 2 k rozhodnutí o změně registrace sp. zn. sukls10679/2012 1. NÁZEV PŘÍPRAVKU THYMOGLOBULINE 5 mg/ml, prášek pro infuzní roztok SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
SOUHRN ÚDAJŮ O PŘÍPRAVKU. Immunoglobulinum humanum normale Jeden ml injekčního roztoku obsahuje Immunoglobulinum humanum normale 160 mg.
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU IGAMPLIA 160 mg/ml, injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Immunoglobulinum humanum normale Jeden ml injekčního roztoku obsahuje Immunoglobulinum
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU IGAMPLIA 160 mg/ml, injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Immunoglobulinum humanum normale Jeden ml injekčního roztoku obsahuje Immunoglobulinum
Co je to transplantace krvetvorných buněk?
 Co je to transplantace krvetvorných buněk? Transplantace krvetvorných buněk je přenos vlastní (autologní) nebo dárcovské (alogenní) krvetvorné tkáně. Účelem je obnova kostní dřeně po vysoce dávkové chemoterapii
Co je to transplantace krvetvorných buněk? Transplantace krvetvorných buněk je přenos vlastní (autologní) nebo dárcovské (alogenní) krvetvorné tkáně. Účelem je obnova kostní dřeně po vysoce dávkové chemoterapii
Daniela Dušková Fakultní transfuzní oddělení Všeobecné fakultní nemocnice v Praze
 Daniela Dušková Fakultní transfuzní oddělení Všeobecné fakultní nemocnice v Praze Daniela Dušková Fakultní transfuzní oddělení Všeobecné fakultní nemocnice v Praze Není náhrada Potřeba dárcovství Léčba
Daniela Dušková Fakultní transfuzní oddělení Všeobecné fakultní nemocnice v Praze Daniela Dušková Fakultní transfuzní oddělení Všeobecné fakultní nemocnice v Praze Není náhrada Potřeba dárcovství Léčba
Krevní skupiny EU peníze středním školám Didaktický učební materiál
 Krevní skupiny EU peníze středním školám Didaktický učební materiál Anotace Označení DUMU: VY_32_INOVACE_BI1.10 Předmět: Biologie Tematická oblast: Biologie člověka Autor: RNDr. Marta Najbertová Datum
Krevní skupiny EU peníze středním školám Didaktický učební materiál Anotace Označení DUMU: VY_32_INOVACE_BI1.10 Předmět: Biologie Tematická oblast: Biologie člověka Autor: RNDr. Marta Najbertová Datum
VI. KONFERENCE AKUTNĚ.CZ,
 Dárci krve? Eva Tesařová Transfuzní a tkáňové oddělení VI. KONFERENCE AKUTNĚ.CZ, 22.11.2014, Brno Dárci krve? Posouzení způsobilosti Exaktní definice kritérií 67, odst. 4, písm. i) zákona 378/2007 Sb.
Dárci krve? Eva Tesařová Transfuzní a tkáňové oddělení VI. KONFERENCE AKUTNĚ.CZ, 22.11.2014, Brno Dárci krve? Posouzení způsobilosti Exaktní definice kritérií 67, odst. 4, písm. i) zákona 378/2007 Sb.
K čemu slouží záznam provedených výkonů logbook?
 K čemu slouží záznam provedených výkonů logbook? Předkládaný Záznam provedených výkonů ve specializačním vzdělávání neboli logbook je součástí vzdělávacího programu a slouží k evidenci průběhu odborné
K čemu slouží záznam provedených výkonů logbook? Předkládaný Záznam provedených výkonů ve specializačním vzdělávání neboli logbook je součástí vzdělávacího programu a slouží k evidenci průběhu odborné
SKLADOVÁNÍ A PŘEPRAVA KRVE, KREVNÍCH SLOŽEK, SUROVINY PRO DALŠÍ VÝROBU A TRANSFUZNÍCH PŘÍPRAVKŮ
 Doporučení Společnosti pro transfuzní lékařství ČLS JEP č. STL2015_11 ze dne 2. 11. 2015 verze 1 SKLADOVÁNÍ A PŘEPRAVA KRVE, KREVNÍCH SLOŽEK, SUROVINY PRO DALŠÍ VÝROBU A TRANSFUZNÍCH PŘÍPRAVKŮ Toto doporučení
Doporučení Společnosti pro transfuzní lékařství ČLS JEP č. STL2015_11 ze dne 2. 11. 2015 verze 1 SKLADOVÁNÍ A PŘEPRAVA KRVE, KREVNÍCH SLOŽEK, SUROVINY PRO DALŠÍ VÝROBU A TRANSFUZNÍCH PŘÍPRAVKŮ Toto doporučení
Parvovirus B 19. Renata Procházková
 Renata Procházková Parvovirus B 19 - Běžný lidský patogen - Objeven 1975 Yvonne Cossart - Neobalený DNA virus (18-22 nm) - Odolný vůči prostředí - Parvoviridae rod Erythrovirus - 3 genotypy: * klasická
Renata Procházková Parvovirus B 19 - Běžný lidský patogen - Objeven 1975 Yvonne Cossart - Neobalený DNA virus (18-22 nm) - Odolný vůči prostředí - Parvoviridae rod Erythrovirus - 3 genotypy: * klasická
ZÁSADY A RIZIKA HEMOTERAPIE. Hana Lejdarová TTO FN Brno Katedra laboratorních metod LF MU
 ZÁSADY A RIZIKA HEMOTERAPIE Hana Lejdarová TTO FN Brno Katedra laboratorních metod LF MU 1. ZÁSADY HEMOTERAPIE Obecné zásady hemoterapie Hemoterapie představuje léčbu transfuzními přípravky a krevními
ZÁSADY A RIZIKA HEMOTERAPIE Hana Lejdarová TTO FN Brno Katedra laboratorních metod LF MU 1. ZÁSADY HEMOTERAPIE Obecné zásady hemoterapie Hemoterapie představuje léčbu transfuzními přípravky a krevními
Příbalová informace: informace pro uživatele
 sp.zn. sukls55434/2017 Příbalová informace: informace pro uživatele Kybernin P 500 IU prášek a rozpouštědlo pro injekční/infuzní roztok Kybernin P 1000 IU prášek a rozpouštědlo pro injekční/infuzní roztok
sp.zn. sukls55434/2017 Příbalová informace: informace pro uživatele Kybernin P 500 IU prášek a rozpouštědlo pro injekční/infuzní roztok Kybernin P 1000 IU prášek a rozpouštědlo pro injekční/infuzní roztok
APLIKACE KREVNÍCH DERIVÁTŮ V INTENZIVNÍ A RESUSCITAČNÍ PÉČI
 MASARYKOVA UNIVERZITA Lékařská fakulta Katedra ošetřovatelství Bc. Lenka Kozáková APLIKACE KREVNÍCH DERIVÁTŮ V INTENZIVNÍ A RESUSCITAČNÍ PÉČI Diplomová práce Vedoucí práce: Mgr. Zdeňka Knechtová Brno 2015
MASARYKOVA UNIVERZITA Lékařská fakulta Katedra ošetřovatelství Bc. Lenka Kozáková APLIKACE KREVNÍCH DERIVÁTŮ V INTENZIVNÍ A RESUSCITAČNÍ PÉČI Diplomová práce Vedoucí práce: Mgr. Zdeňka Knechtová Brno 2015
CRP. Axis - Shield. SINGLE TESTS CRP kvantitativní stanovení pomocí přístroje NycoCard Reader II
 Lékařská technika a speciální zdravotní materiál Společnost je zapsána v obchodním rejstříku Městského soudu v Praze, odd. C vložka 1299 Obchodní 110, 251 70 Praha Čestlice Tel. +420 296 328 300 Fax. +420
Lékařská technika a speciální zdravotní materiál Společnost je zapsána v obchodním rejstříku Městského soudu v Praze, odd. C vložka 1299 Obchodní 110, 251 70 Praha Čestlice Tel. +420 296 328 300 Fax. +420
Okruh otázek k atestační zkoušce pro obor specializačního vzdělávání Hematologie a transfuzní služba
 Okruh otázek k atestační zkoušce pro obor specializačního vzdělávání Hematologie a transfuzní služba Zdravotní laborant pro hematologii a transfuzní službu I. Imunohematologie a transfúzní služby 1. Skupinový
Okruh otázek k atestační zkoušce pro obor specializačního vzdělávání Hematologie a transfuzní služba Zdravotní laborant pro hematologii a transfuzní službu I. Imunohematologie a transfúzní služby 1. Skupinový
