KVANTITATIVNÍ FTIR SPEKTROMETRIE HUMINOVÝCH LÁTEK
|
|
|
- Radim Mareš
- před 5 lety
- Počet zobrazení:
Transkript
1 KVANTITATIVNÍ FTIR SPEKTROMETRIE HUMINOVÝCH LÁTEK FRANTIŠEK NOVÁK a, VLADIMÍR MACHOVIČ b,c, HANA HRABALOVÁ a a MIROSLAVA NOVOTNÁ c a Technopark Kralupy VŠCHT Praha, Žižkova 7, Kralupy nad Vltavou, b Ústav struktury a mechaniky hornin AV ČR, V Holešovičkách 41, Praha 8, c Laboratoř molekulové spektroskopie VŠCHT Praha, Technická 1905, Praha novaaf@vscht.cz Došlo , přijato Klíčová slova: FTIR, huminové látky, infračervená spektrometrie, struktura Obsah 1. Úvod 2. Metody měření FTIR spekter 3. FTIR spektra huminových látek 3.1. Přiřazení pásů v FTIR spektrech huminových látek 3.2. Významné strukturní parametry z FTIR spekter 3.3. Vliv ph na FTIR spektrum huminových kyselin 4. Klasifikace huminových látek podle FTIR spekter 5. Kvantitativní analýza FTIR spekter huminových látek 6. Závěr 1. Úvod Huminové látky (HL) jsou v tradičním pojetí považovány za relativně vysokomolekulární polyelektrolyty, složené z alifatických, aromatických i heterocyklických strukturních jednotek. Výsledky některých fyzikálněchemických metod naznačují, že na HL můžeme nahlížet rovněž jako na (supra)molekulární asociáty a samovolně seskládané poměrně malé heterogenní molekuly, v neutrálním prostředí vzájemně vázané slabými mezimolekulárními silami ( a CH interakcemi či van der Waalsovými silami). Tato novější hypotéza však není akceptována všeobecně, proto vedle sebe koexistují dva protichůdné názory na strukturu HL: (1) tradiční, považující HL za polymerní látky, v nichž jsou jednotlivé fragmenty vázány silnou kovalentní vazbou, a (2) novější, pokládající zejména půdní 1 HL za asociáty nebo agregáty relativně malých molekul (hovoří se o supramolekulární povaze). Oba modely se zásadně liší důsledkem pro stabilitu HL. Zatímco z tradičního polymerního modelu vyplývá značná rezistence HL vůči rozkladu, model supramolekulárních agregátů neposkytuje pro stabilitu HL vůči rozkladu dostatečný strukturní důvod. Pro některé vědní obory je prvořadá velikost makromolekul nebo agregátů půdních HL, která určuje jejich transport půdním prostředím, a samotná otázka, jedná-li se o látky povahy makro- nebo supramolekulární (případně pseudo-micelární), je pro ně víceméně podružná. Podle schopnosti tvořit vysokodisperzní soustavu s/l v kyselém a zásaditém vodném prostředí se HL dělí na fulvokyseliny (FK), huminové kyseliny (HK) a huminy 2. Navzdory složité struktuře huminových látek pozorujeme v jejich infračervených spektrech řadu absorpčních pásů, charakteristických pro specifické molekulární struktury. I přes nejednoznačné přiřazení některých pásů poskytuje infračervená spektrometrie s Fourierovou transformací (FTIR) důležité informace o povaze huminových látek 3, jejich reaktivitě, prostorovém uspořádání kyslíkatých funkčních skupin, podílu sacharidických a proteinových složek i o obsahu vázaných anorganických příměsí jílových minerálů a iontů kovů. Z těchto důvodů je FTIR spektrometrie důležitou metodou pro strukturní charakterizaci HK různého původu 4,5 a stáří 6, uplatňuje se jako hlavní metoda při charakterizaci dalších přírodních látek izolovaných na základě skupinové separace, např. látek podobných huminovým (HULIK, humic like substances) v aerosolech 7, při analýze produktů mikrobiálního rozkladu biomasy (tzv. humic-like acids) 8, nebo jako doplňková metoda při studiu tepelné konverze lignosulfonanu na lignohumát 9. FTIR spektrometrie je také významným nástrojem při studiu strukturálních změn vodních HK při ozonizaci vod 10, při využití humátů k odstraňování iontů toxických kovů z vod 11,12, při sledování modifikace nanočástic hydroxyapatitu s HK s cílem připravit vysoce účinné sorbenty Cu(II) (cit. 13 ) nebo při monitorování dlouhodobého vlivu anorganických a organických hnojiv na frakce půdní organické hmoty 14. Obecně v infračervené (IR) spektrometrii, podobně jako u jiných optických metod, platí Lambertův-Beerův zákon, a proto při použití speciálních postupů (např. Fourierovy dekonvoluce nebo matematické separace absorpčních pásů) má tato metoda dobré předpoklady pro kvantitativní analýzu funkčních skupin HL. Vedle měření FTIR spekter transmitanční technikou (KBr tablety) se široce uplatňuje také měření difuzně reflektančních IR spekter 15 (DRIFT spektra) huminových látek. Pro kvantitativní účely je však vhodnější metoda transmitanční nebo jednoodrazová reflexe na nástavci ATR (Attenuated Total Reflexion, zeslabený úplný odraz). Ve srovnání s 13 C NMR spektrometrií 16 nebo s titračními metodami 17,18 pro stanovení funkčních skupin HL je předností FTIR spektrometrie 363
2 malé množství spotřebovaného vzorku a podstatně rychlejší měření. Cílem našeho příspěvku je přehledně shrnout metody měření a současný stav interpretace infračervených spekter huminových látek a napomoci tak širšímu uplatnění této metody při studiu jejich struktury a vlastností. 2. Metody měření FTIR spekter FTIR spektrum huminových látek v pevné fázi se obvykle měří v tabletce, připravené mletím mg neabsorbující matrice (nejčastěji KBr) s 1 mg vzorku HL a standardním tlakem slisované do disku. Protože KBr neabsorbuje IR záření, získá se tímto postupem kompletní IR spektrum ve střední spektrální oblasti vlnových délek 2,5 25 m (vlnočty cm 1 ). Jinou méně používanou technikou je měření v olejové suspenzi mezi dvěma okénky z NaCl, KBr aj. Při ní se přibližně 5 mg jemně rozemletého vzorku disperguje v kapce oleje, např. Nujolu (směs vysokomolekulárních parafinických uhlovodíků), který však absorbuje v oblasti valenčních vibrací C H (vlnočty cm 1 ). Použití halogenovaných olejů, např. polychlortrifluorethylenového oleje (Fluorolube), umožňuje studovat také oblast spektra při 3000 cm 1. FTIR spektra huminové kyseliny měřená různými postupy jsou porovnána na obr. 1. Pro studium kyslíkatých funkčních skupin je významná oblast IR spektra mezi vlnočty cm 1. Závažným problémem při měření v KBr tabletách proto bývá adsorbovaná vlhkost, projevující se pásy v oblastech 3600 až 3000 cm 1 a cm 1. Tento problém sice lze minimalizovat použitím D 2 O (cit. 19 ), kompenzací IR spektra vody 20 nebo můžeme adsorbovanou vodu z KBr odstranit zahřátím ve vakuu na teplotu C po 30 min, příp. sušením tablety v exsikátoru po dobu několika hodin; zpravidla tím však nezabráníme částečné deprotonaci huminových látek při ionizaci karboxylových COOH a fenolických skupin OH v průběhu lisování vzorku s KBr za vyššího tlaku. Zvýšená teplota při sušení tablet KBr se vzorkem (u některých autorů 47 až 100 C) však může částečně pozměnit strukturu huminových kyselin. Rozšířené je použití méně hydroskopických tabletovacích matric, např. bromidu thalného 2, jehož nevýhodou je ovšem vysoká toxicita, nebo velmi drahého jodidu cesného. Ve zvláštních případech se používá disk z AgCl (Spectra-Tech, Stamford), na který se opakovaně aplikuje asi 0,5 ml roztoku huminové kyseliny a rozpouštědlo se odpaří v sušárně (15 min při 70 C) až se vytvoří film poskytující vyhovující IR spektra s absorbancí hlavních pásů 0,2 0,7 (cit. 21 ). Tato metoda je úspěšně používána pro semikvantitativní stanovení skupin COOH. Podobný postup využívá místo chloridu stříbrného např. křemíkového okénka 22 nebo selenidu zinečnatého 23. Jiný způsob, jak se vyhnout potížím způsobeným stopami vody, nabízí technika difuzně-reflektančních spekter HL. Při jejich měření není nutné používat matrice, proto nejsou DRIFT spektra huminových látek komplikována absorbancí vody ani ionizací kyselých funkčních skupin. DRIFT spektra mohou být pomocí Kubelkovy- Munkovy funkce převedena na spektra analogická spektrům absorpčním. V limitním případě nízké koncentrace funkčních skupin, tenké vrstvy a velkého povrchu vzorku lze vyjádřit závislost Kubelkovy-Munkovy funkce na koncentraci vztahy: K/ S(v jednotkáchkm) log( K / S) logc logc 2 (1 ). r 2r c S (1) (2) Obr. 1. FTIR spektra huminové kyseliny, izolované z horizontu A h půdního typu podzol (Labský důl, Krkonoše). Spektra byla měřena na IR spektrometru Nicolet 740 technikami KBr tablet, nujolové suspenze a difuzní reflexí (DRIFTS) bez použití matrice. Hvězdičkou * je vyznačeno přerušení spektra v oblasti silné absorpce Nujolu kde K je absorpční koeficient, S je koeficient rozptylu, závislý na velikosti částic a na plnění vzorku, poměr K/S je v jednotkách K-M, r = S/R je relativní reflektance, ε je molární absorpční koeficient, c koncentrace vyjádřená v molech na gram matrice (ředicí látky), C je konstanta. Koeficient rozptylu S je charakteristický pro danou ředicí látku. Na rozdíl od transmitančních FTIR spekter (někdy nepřesně nazývaných pouze FTIR spektra) však při aplikaci Kubelkovy-Munkovy transformace u DRIFT spekter (K-M) 24 dochází k zesílení některých absorpčních pásů, 364
3 zejména vyšších harmonických. K-M transformace tak má sklon zesilovat silné absorpční pásy (malá hodnota r ve vztahu (1)) a potlačovat pásy slabé (velké hodnoty r), což komplikuje přesnější než semikvantitativní vyhodnocení DRIFT spekter. Další technikou měření FTIR spekter bez použití matrice je oblíbené měření na jednoodrazovém ATR nástavci, založené na principu úplného odrazu záření na fázovém rozhraní vzorku a měřícího krystalu z materiálu o vysokém indexu lomu. Běžně se používají krystaly diamantové, křemíkové nebo germaniové. Svazek paprsků je do krystalu přiváděn soustavou zrcadel tak, aby úhel dopadu na fázové rozhraní vyhovoval podmínce úplného odrazu. Měřený vzorek je v dokonalém kontaktu s ATR krystalem, záření částečně proniká do analyzovaného materiálu. Pokud vzorek absorbuje záření o určité frekvenci, je tato složka v totálně odraženém záření zeslabena. Vztah mezi absorbancí při určité vlnové délce i a koncentrací c lze popsat modifikovanou Lambertovou-Beerovou rovnicí A i = a i. l.c, v níž místo délky kyvety l vystupuje hloubka průniku záření d p : d p n 1/2 k sin ( ns / nk) kde a i je molární absorpční koeficient při vlnové délce i, n k a n s jsou indexy lomu krystalu a vzorku (n k > n s ), je vlnová délka záření, je úhel dopadu záření na fázové rozhraní 25. K úplnému vnitřnímu odrazu je třeba, aby byl úhel dopadu větší než kritický úhel C C = sin 1 (n s /n k ) (4) ATR spektra se do značné míry podobají spektrům změřeným transmitanční technikou. Penetrační hloubka záření do povrchu vzorku je řádově v jednotkách µm, takže jde o charakterizaci pouze velmi tenké povrchové vrstvy. Pro zajištění reprodukovatelnosti měření je nezbytné pokrýt vzorkem HL celou plochu krystalu. U pevných vzorků je důležité dodržovat dobrý kontakt s měřicím krystalem. Z rovnice (3) je zřejmé, že s vlnovou délkou záření se zvětšuje hloubka penetrace d p. V důsledku toho se v ATR spektrech s rostoucími vlnočty snižují relativní intenzity pásů. Kompenzace tohoto jevu (ATR korekce) se provádí pomocí vhodného programu. (3) Protože u neasociované skupiny OH bychom očekávali maximum absorpce při vlnočtu ~3600 cm 1, svědčí nižší vlnočty, pozorované u huminových kyselin, o vazbě skupin OH intramolekulárními (příp. intermolekulárními) vodíkovými vazbami. Huminové kyseliny mívají maximum tohoto pásu při 3400 cm 1, u fulvokyselin bývá maximum kvůli výraznějšímu vlivu vodíkových můstků posunuto k nižším vlnočtům (3300 cm 1 ). V této oblasti se na absorpci podílí širokým a výrazným pásem adsorbovaná voda, přispívat mohou také valenční vibrace O H alifatických alkoholů a skupin N H. Není bez zajímavosti, že zbytkový pás v této oblasti bývá zjištěn i u methylovaných nebo acetylovaných HK, což se vysvětluje jednak absorpcí příslušející vibraci N H, jednak rezistencí části OH skupin vůči methylaci nebo acetylaci. Ve spektrech ligninu izolovaného ze dřeva nacházíme maximum tohoto pásu při poněkud vyšších vlnočtech 3412 cm 1 u smrku a 3460 cm 1 u buku 26. Zvýšení intenzity pásu O H při 3420 cm 1, pozorované při tvorbě komplexů HK s kovovými ionty Co 2+, Cu 2+ a Ni 2+, je dáno absorpcí vody v aquakomplexech 27. Absorpční pás při vlnočtech okolo 3030 cm 1 přísluší valenčním vibracím aromatické vazby C H a měl by být zřetelný ve spektrech všech huminových kyselin a fulvokyselin, neboť ani u fulvokyselin nejsou aromatické kruhy zcela substituovány 28. Tento pás je však výraznější jen ve spektrech látek s nízkým počtem (maximálně 2 3) substitucí na benzenovém kruhu, při vyšším počtu substitucí (více než 3 4) je intenzita pásu velmi nízká 29. Absence pásu při vlnočtu 3030 cm 1 ve spektrech HL bývá vysvětlována prakticky úplnou substitucí na aromatickém kruhu 2 nebo překrytím sousedním silným pásem vibrací O H v karboxylových skupinách, který může být v důsledku 3. FTIR spektra huminových látek 3.1. Přiřazení pásů v FTIR spektrech huminových látek Přiřazení hlavních absorpčních pásů v FTIR spektrech huminových látek přehledně shrnuje tab. I. Na obr. 2 jsou srovnána FTIR spektra huminových látek a půdy, z níž byly HL izolovány. V oblasti cm 1 IR spekter huminových látek se nachází výrazný široký absorpční pás, přiřazený valenčním vibracím fenolických OH skupin. Obr. 2. FTIR spektra fulvokyselin (F), huminových kyselin (H), humusojílového komplexu (H5), huminu (HM), půdy (S) a popele huminových kyselin (Ash) 365
4 Tabulka I Přiřazení hlavních pásů v FTIR spektrech huminových kyselin (s přihlédnutím k pracím 28,29,43,44 ) ν/ cm 1 Přiřazení valenční vibrace O H ve fenolických OH skupinách (s příspěvkem alifatických skupin OH a případně N H) 3030 valenční vibrace aromatických vazeb C H valenční vibrace alifatických vazeb C H 2930 antisymetrické valenční vibrace C H ve skupinách CH symetrické valenční vibrace C H ve skupinách CH valenční vibrace O H karboxylových skupin, vázaných vodíkovým můstkem valenční vibrace C=O ve skupině COOH, s malým příspěvkem ketonů ( 1710) 1717 valenční vibrace C=O v karbonylech, aldehydech a alifatických ketonech valenční vibrace C=O v aromatických ketonech valenční vibrace C=O v amidické skupině (amid I); C=O chinonů; valenční vibrace C=O v konjugovaných ketonech, vázané vodíkovou vazbou ke skupině OH aromatické valenční vibrace C=C; C=O v konjugovaných ketonech, vázané vodíkovou vazbou ke skupině OH (silně); příp. antisymetrické valenční vibrace COO (1610 cm 1 ) symetrická vibrace COO, deformační vibrace N H; valenční vibrace C=N amidu II 1580 valenční vibrace aromatických C=C, příp. antisym. valenční vibrace COO ( cm 1 ) 1575 antisymetrická valenční vibrace aniontu COO 1540 valenční vibrace N H v amidické skupině (amid II) 1525 valenční vibrace aromatických C=C 1515 valenční vibrace aromatických C=C a amidu II (deformační N H vibrace polypeptidů) (1460 ) 1440 antisymetrické C H deformační vibrace alifatických skupin CH 3 a CH deformační OH a valenční vibrace C O fenolických skupin OH; deformační vibrace C H skupin CH 2 a CH 3 ; antisymetrické valenční vibrace karboxylového aniontu COO ( cm 1 ) 1350 symetrické valenční vibrace COO, případně symetrické deformační vibrace C CH 3 v alifatických skupinách valenční vibrace C O a deformační vibrace O H ve skupině COOH; valenční vibrace C O aryletherů 1270 valenční vibrace C OH fenolických OH skupin 1225 valenční vibrace C O a deformační vibrace OH ve skupinách COOH 1220 valenční vibrace C N (amid III) 1170 valenční vibrace C OH alifatických OH skupin 1070 ( 950) valenční vibrace C O polysacharidů nebo polysacharidům podobných látek, Si O příměsi 1070 valenční vibrace C C alifatických skupin 830, 775 mimorovinné deformační vibrace aromatické vazby C H vodíkových vazeb rozšířen až ke 2900 cm 1, absence však může být způsobena také interferencí s absorpčním pásem vody, případně chybnou kompenzací pásu vody 36 při zpracování spektra. Absorpční pás při 2900 cm 1, příslušející valenčním vibracím alifatické vazby C H, mívá ve spektrech HK velmi proměnlivou střední nebo malou intenzitu. U methylovaných a acetylovaných preparátů HK je absorpce v této oblasti přiměřeně zvýšena v důsledku zavedení skupin CH 3 nebo CH 2 CH 3 do molekuly. Pásy antisymetrické a symetrické valenční C H vibrace ve skupinách CH 2 mají maxima při 2930 cm 1 a 2840 cm 1. Široký pás valenčních vibrací O H karboxylových skupin, vázaných vodíkovým můstkem v dimeru, mívá maximum při 2600 cm 1. Při srovnání spekter HK měřených technikou DRIFT a KBr tablet bylo zjištěno, že relativní intenzita tohoto pásu je u techniky KBr nižší, zřejmě v důsledku narušení intramolekulárních vodíkových vazeb při přípravě tablet 28 (iontová výměna H + za K + ). 366
5 Pro studium kyslíkatých funkčních skupin je významná oblast spektra mezi cm 1, kde je možno nalézt vibrační pásy karbonylových skupin v následujících sloučeninách: cyklické a smíšené anhydridy (1815, 1780 cm 1 ), karboxylové kyseliny (1720, 1690 cm 1 ), estery (1760, 1740 cm 1 ), aromatické ketony (1660 cm 1 ) a soli karboxylových kyselin (1575 cm 1 ). Absence pásů při vlnočtech 1760 a 1735 cm 1 je považována za důkaz, že jen minimum skupin C=O (popř. žádné) se v HK vyskytuje vázaných v nasycených esterech. Pás s maximem při cm 1, patrný ve spektrech huminových látek získaných oxidací uhlí kyselinou dusičnou nebo za vyšších teplot na vzduchu, zřejmě přísluší vibracím karboxylových skupin 30, bývá však přisuzován též karbonylovým skupinám ovlivněným blízkostí hydroxylových skupin 31 nebo laktonům, jejichž vibracím C=O odpovídají pásy při 1777 až 1781 cm 1 (γ-laktony) a cm 1 (δ-laktony). Méně intenzivní pás při 1843 cm 1 ve spektrech oxidovaných HK nebo uhlí svědčí o tvorbě anhydridů. Ostrý pás s maximem při 1720 cm 1 patří k nejvýraznějším pásům v IR spektrech huminových kyselin a fulvokyselin, je však potlačen ve spektrech jejich solí, což svědčí o tom, že hlavní podíl na absorpci v této oblasti mají valenční vibrace C=O v karboxylových skupinách. Přesná poloha maxima tohoto pásu závisí na konjugacích, substituentech v okolí karboxylu a povaze vodíkové vazby 29. Nižší vlnočet pro valenční vibraci skupiny C=O u HL je způsoben především konjugací skupin C=O. U fulvokyselin, které obsahují více karboxylových skupin, leží maximum tohoto pásu při 1700 cm 1, což svědčí o vazbě na aromatickém kruhu. Huminové kyseliny mají tento pás rozložen okolo 1711 cm 1, často bývá tvořen trojicí překrývajících se pásů karbonylů, které patří karboxylovým skupinám vázaným na alifatické i aromatické struktury. K absorpci v této oblasti přispívají také vibrace aldehydů a ketonů, u některých HK i chinonů. V případě solí nebo komplexů HK se místo tohoto pásu objevují dva nové pásy při 1550 a 1390 cm 1, odpovídající absorpci karboxylátového iontu COO. U methylovaných HK bývá maximum 1720 cm 1 posunuto k vyšším vlnočtům (1725 cm 1 ), což odpovídá tomu, že maximum absorbance skupiny C=O se u esterů nachází u vyšších vlnočtů než u odpovídajících kyselin. Intenzita pásu při 1720 cm 1 je vyšší u fulvokyselin než huminových kyselin, protože FK obsahují více skupin COOH. U jinak velmi podobných spekter FK a HK můžeme též pozorovat posun pásu při 1600 cm 1 k vyšším vlnočtům (~1640 cm 1 ) u fulvokyselin. V IR spektrech řady huminových kyselin, zvláště obsahují-li více dusíku, bývají pozorovány samostatné pásy s maximy při a cm 1, typické pro valenční vibrace amidu (amid I a amid II). Prvý pás, příslušející vibracím C=O amidoskupiny (amid I), zaniká po hydrolýze vzorku v 6 M HCl. Druhý pás, odpovídající deformačním vibracím N H polypeptidů (amid II), může být pozorován až při 1515 cm 1 nebo může koincidovat s valenční vibrací aromatických C=C. Oba pásy dokládají přítomnost polypeptidů v makromolekule HK; absence těchto pásů ve spektru však neznamená, že vzorek HK polypeptidy neobsahuje. V důsledku interakce s intenzivnějšími pásy karbonylů nebo dvojných vazeb C=C se často vibrace amidu (amid I) neprojevuje pásem samostatným, nýbrž kombinovaným pásem s maximem posunutým nad 1650 cm 1. Valenční vibraci C N v amidické skupině (amid III) bývá přiřazován pás při 1220 cm 1. U půdních HK se na absorpci v oblasti 1650 a 1550 cm 1 mohou kromě polypeptidů podílet také vibrace acetamidové skupiny NH(C=O) CH 3 chitinu, produkovaného houbami a v čistém stavu poskytujícího charakteristické pásy při 1665 a 1567 cm 1. Pás při cm 1 patří k nejsilnějším pásům v IR spektru HK. Přísluší vibracím vazby C=C v aromatických strukturách, mohou zde však také přispívat nearomatické dvojné vazby, vibrace amidické a aminové vazby N H, antisymetrická vibrace ionizovaných karboxylových skupin (patrná zejména u humátů) nebo kruhy tvořené vodíkovými vazbami OH skupin ke skupinám chinonů C=O nebo karbonylů. Přítomnost chinonů v molekule huminových kyselin však dosud nebyla spolehlivě prokázána. V této oblasti rovněž absorbuje voda (maximum při 1625 cm 1 ), přítomná ve vzorku a ve vzduchu. Srovnání DRIFT a transmitančních FTIR spekter huminových kyselin prokázalo, že při přípravě KBr tablet dochází k částečné ionizaci karboxylových skupin 28. Vznik komplexů huminových kyselin s ionty Fe 3+ zvyšuje intenzitu pásu u vlnočtu 1620 cm 1 při současném snížení intenzity pásu 29 při 1720 cm 1. Přitom dochází k posunu maxima pásu z 1622 k vlnočtu 1615 cm 1 a současně s poklesem intenzity pásu C=O karboxylů se jeho maximum posouvá z 1723 k 1713 cm 1. Protože již malý obsah anorganických příměsí (Fe 3+ ) může být příčinou ionizace karboxylových skupin huminových látek, je zřejmé, že relativní intenzita pásů a cm 1 je silně ovlivněna obsahem popelovin v preparátu. Schopnost iontů Cu 2+ tvořit pevné komplexy s karboxylovým iontem HK byla prokázána ze snížení vlnočtu maxima pásu symetrické valenční vibrace aniontu COO (1365 cm 1 ) o 22 cm 1 ve srovnání se sodnou solí 28. O neiontovém charakteru vazby v humátu měďnatém svědčí rovněž posun maxima 32 příslušné asymetrické vibrace (1620 cm 1 ) o 4 cm 1 k vyšším vlnočtům. V oblasti 1575 a 1390 cm 1 lze především u solí huminových kyselin pozorovat absorpci vyvolanou antisymetrickou valenční vibrací aniontu COO. Nápadné pásy při 1515 cm 1 ve spektrech huminových kyselin i fulvokyselin dokládají přítomnost para-substituovaného benzenového kruhu. Méně intenzivní pásy bývají pozorovány při 1500 cm 1 (valenční vibrace aromatických C=C), 1460 cm 1 (deformační C H vibrace skupin CH 2 a CH 3 ), 1390 cm 1 (deformační vibrace O H, valenční CH 3 a C O vibrace fenolických OH skupin), při 1270 cm 1 (valenční vibrace C OH fenolů) a 1220 cm 1 (C O valenční vibrace a O H deformační vibrace COOH). U fulvokyselin bývají pozorovány výrazné pásy valenčních vibrací C O sacharidů při 1196 a 1078 cm 1. Pokud byla při přípravě huminových kyselin použita kyselina fluorovodíková, mohou se v této oblasti vyskytnout 29 pásy valenčních vibrací C F (1240 až 1210 a 1150 cm 1 ). Analogické pásy valenčních vibrací C Cl 367
6 Tabulka II Přiřazení pásů vybraných anorganických příměsí v FTIR spektrech huminových kyselin ν/ cm 1 Přiřazení valenční vibrace O H kaolinitu 3640 valenční vibrace O H montmorillonitu vibrace Si O v křemeni 1100, 1030, vibrace Si O v kaolinitu 1010, (1020) Si O v montmorillonitu 1050 vibrace Si O v montmorillonitu 935, 910 H O Al v kaolinitu 830 H O Me 3+ v nontronitu dublet v křemeni SiO amorfní modifikace SiO 2 Obr. 3. FTIR spektra minerálních příměsí, vyskytujících se v huminových kyselinách: kaolinitu, montmorillonitu, křemene, oxidu hlinitého a oxidu železitého mají maximum v oblasti cm 1, zpravidla však nebývají pozorovány. Široký a intenzivní absorpční pás valenčních vibrací C OH alifatických alkoholů má maximum 33 u vlnočtů cm 1. Ve spektrech bezpopelových HK bývají v této oblasti zřetelné dva nebo tři pásy, z nichž nejintenzivnější s maximem při 1050 cm 1 zřejmě přísluší vibracím O H primárních alkoholů. Silná absorpce při cm 1 může být vyvolána valenčními vibracemi C O polysacharidů, často se však jedná spíše o Si O vibrace minerálních nečistot, které snižují význam této oblasti spektra pro studium HL. Huminové kyseliny, při jejichž preparaci byl použit síran sodný nebo kyselina sírová, mívají ve spektru různě intenzivní pás odpovídající vibraci sulfátů ( cm 1 ) a pás valenční vibrace S=O při 1040 cm 1. Použití difosforečnanu při přípravě HK se projevuje různě intenzivním pásem v oblasti cm 1. Oblast vlnočtů pod 1000 cm 1 nemá pro studium struktury huminových kyselin velký význam. Na rozdíl od absorpčních pásů případných minerálních příměsí (tab. II) jsou zde pásy HK málo intenzivní. Slabé pásy s maximy 975, , a cm 1 přísluší mimorovinným deformačním vibracím aromatických C H vazeb 28, často nepozorovaný slabý pás při cm 1 odpovídá vibracím alifatických (CH 2 ) n řetězců (n 4) a nevýrazný pás při 490 cm 1 byl přisouzen polysacharidům 29. Absorpční pásy anorganických látek v IR spektrech mají obecně přibližně dvakrát vyšší intenzitu než pásy organických funkčních skupin. Proto se v IR spektrech huminových látek projevují výraznými absorpčními pásy minerální příměsi, především jílové minerály a oxidy/ hydroxidy hlinitý a železitý (obr. 3). Kaolinit má ostré pásy při cm 1 (valenční vibrace O H), 1020 cm 1 (Si O vibrace) a cm 1 (Al OH vibrace). Montmorillonit lze identifikovat podle pásů při vlnočtech 3640 cm 1 (O H vibrace), 1050 cm 1 (Si O vibrace) a dále při 910, 880 a 850 cm 1. Ve vzorcích HK, připravených extrakcí směsí NaOH a difosforečnanu, jsou patrné pásy difosforečnanu při a cm 1. Přítomnost anorganických fosforečnanů v HK se projevuje pásem s maximem při cm Významné strukturní parametry z FTIR spekter Při analýze vzorků FTIR spektrometrií lze místo kvantitativního stanovení funkčních skupin využít tzv. strukturních parametrů poměrů intenzit (I) nebo integrovaných intenzit (A) dvou vybraných pásů. Tato semikvantitativní metoda, umožňující rychlé srovnání větších sérií analyzovaných vzorků, má široké praktické uplatnění. Například v průběhu zrání kompostu se lineárně s časem zvyšují poměry I 1385 /I 2930 (COO, CH 3 /alifatické C H) a I 1385 /I 1050 (COO, CH 3 / C O polysacharidů) a parametr I 1655 /I 2930 (aromatické C=C, COO /alifatické C H) koreluje lineárně se stupněm humifikace 33 (obsahem HL v kompostu). Poměrně podrobnou informaci o reaktivitě huminových kyselin lze získat z tzv. parametrů O/R (oxygen/ recalcitrant) 28,34, obvykle označovaných R 1 a R 2, které jsou definovány jako poměr intenzit pásů kyslíkatých funkčních skupin a intenzit pásů alifatických a aromatických: R 1 = (I I I I I 1050 )/(I I I I I I I I 779 ) a podobně R 2 = I 1727 /(I I I 779 ). 368
7 K hlavním strukturním parametrům huminových látek patří poměry I 1650 /I 2930 a I 1650 /I 2850 (poměr aromatický C/alif. C) a I 1650 /I 1711 (poměr aromatický C/karboxylový C). Parametr I 2960 /(I I 2929 ) vyjadřuje větvení alifatických řetězců. Pro rozlišení oxidovaných a diageneticky přeměněných vzorků rašelin, uhlí a HK z nich izolovaných se používá poměrů I al = I 2920 /(I I 1610 ) a I C=O = I 1725 /(I I 1610 ), z nichž lze zkonstruovat graf 34 podobný van Krevelenovu diagramu atomových poměrů H/C a O/C. Pro úspěšné použití strukturních parametrů získaných z FTIR spekter je někdy nezbytné provádět separaci (příp. dekonvoluci) pásů, které se ve spektrech huminových látek překrývají (tzv. koincidence) Vliv ph na IR spektrum huminových kyselin Hodnota ph určuje poměr protonizovaných a ionizovaných karboxylových a fenolických OH skupin v huminových látkách, což se projevuje v relativní intenzitě příslušných pásů IR spektra. Na obr. 4 je ukázáno infračervené spektrum HK izolované z půdního typu podzol, měřené ve formě filmu na křemíkovém okénku. Před měřením bylo ph roztoku HK upraveno přídavkem NaOH. Protonizovaná forma HK při ph 3,7 má výrazný široký pás valenčních vibrací vodíkovým můstkem vázaných O H skupin fenolů s vrcholem 3314 cm 1 a O H karboxylových skupin při 2598 cm 1. Pás valenčních vibrací karbonylů karboxylových skupin má vrchol při 1717 cm 1, dva výrazné pásy při 1268 a 1229 cm 1 náleží valenčním C O a deformačním O H vibracím v COOH, fenolech a alkoholech. Se zvýšením ph na hodnotu 4,0 poklesne Obr. 4. FTIR spektrum půdní huminové kyseliny z Trojmezí (Šumava), měřené při různém ph. ph roztoku HK bylo před odpařením na Si okénku upraveno přídavkem 0,01M NaOH na hodnoty 3,70, 4,0 a 11,0. Podmínky měření jsou uvedeny u obr. 6 intenzita pásu COOH skupin při 1717 cm 1 za současného zvýšení intenzity pásu při 1615 cm 1. Z posunu vrcholu tohoto pásu z původních 1624 cm 1 lze soudit na vznik solí COONa. Úprava ph roztoku HK na 11,0 se v FTIR spektru projevuje výraznými změnami. Zcela zmizí pás valenčních vibrací karbonylů karboxylových kyselin při ~1713 cm 1. Ve spektru dominuje pás valenčních antisymetrických a symetrických vibrací karbonylových skupin karboxylových solí COONa při vlnočtech 1588 a 1412 cm 1. Současně jsou významně sníženy intenzity pásů při 1268 a 1229 cm 1 a intenzita pásu valenčních vibrací O H fenolů. Pás valenčních vibrací O H karboxylových skupin při 2598 cm 1 a pás dimeru při 950 cm 1 zcela zaniká. 4. Klasifikace huminových látek pomocí FTIR spekter Infračervená spektra huminových kyselin a fulvokyselin různého původu jsou natolik charakteristická (obr. 5), že umožňují sledovat změny struktury HK v půdním profilu (spektra LH, H1 H4, obr. 5) a rovněž rozlišit několik typů HK, charakteristických pro jednotlivé půdní typy. Například huminové kyseliny izolované z organozemí (rašeliny) mají v FTIR spektrech velmi slabý pás C=C ligninu při 1511 cm 1 a naopak vyšší příspěvek sekundárních amidů (1550 cm 1 ) a zejména polysacharidů (1052 cm 1 ). S klesající molekulovou hmotností vzrůstá v IR spektru HK příspěvek pásů ligninu a současně klesá obsah sekundárních amidů a polysacharidů 35. Na základě studia IR spekter rozdělili Stevenson a Goh 36 HK do tří typů: Typ I zahrnuje HK s více aromatickým a méně alifatickým charakterem, které obsahují více karboxylů a karbonylů, mají výrazné pásy při 1720 a 1600 cm 1, postrádají však zřetelný pás při 1640 cm 1. Další výrazné pásy mají při 3400, 2900 a 1200 cm 1. Do této skupiny patří řada půdních HK. Typ II má více alifatický a méně aromatický charakter, obsahuje více karboxylů a karbonylů a více dvojných vazeb. V IR spektru je velmi výrazný pás při 1720 cm 1, naproti tomu pás při 1600 cm 1 je slabý a posunutý k vlnočtu 1650 cm 1 (tvoří tak rameno pásu karboxylů). Typickým představitelem jsou nízkomolekulární fulvokyseliny a HK některých půd. Typ III má spektra podobná prvému, absorpční pásy aromátů, alifatických řetězců a karboxylových skupin jsou však méně intenzivní. Pravděpodobně se jedná o více kondenzované huminové kyseliny. Jejich IR spektra se liší od spekter ostatních typů HK výraznějšími pásy proteinů, sacharidů i pásem při 1540 cm 1. Vyšší stupeň humifikace se u tohoto typu HK projevuje poklesem intenzity pásu karboxylových skupin a změnami v okolí pásů karbonylů, které nejsou volné nebo slabě vázané k atomům vodíku (intramolekulárním nebo intermolekulárním vodíkovým můstkem), ale zapojené do pevných chelátových vazeb. Intenzivnější je také pás při 2900 cm 1 (valenční vibrace 369
8 Obr. 5. FTIR-ATR spektra fulvokyselin (F) a huminových kyselin (H), izolované metodou IHSS 45,46 z matric různého původu. Spektra byla měřena na FTIR spektrometru Nicolet is50 s ATR nástavcem a Si krystalem, korekce ATR a základní linie byly provedeny pomocí programu Omnic Fulvokyseliny byly izolovány z vody Rašeliníku, Fláje (F0); z horizontů O f (F1) a B h (F2) půdního typu podzol; z rašeliny Branná (F3) a Příbraz (F4); z oxyhumolitu lomu Vršany (F5); z hnědého uhlí lomu Bílina. Huminové kyseliny byly izolovány z průmyslového lignohumátu (LHA); z horizontů O f1 (LH), O f2 (H1), O h (H2), A h (H3) a B h (H4) půdního typu podzol na Trojmezí (Šumava); z horizontu A půdního typu kambizem (H5); z černozemě (H6) u Samary (Rusko); z rašeliny Branná (H7) a Příbraz (H8); z lignitu dolu Mír u Mikulčic (H9); z oxyhumolitů lomu Bílina (H10) a Vršany (H11); z hnědého uhlí (H12), Roth, Karlsruhe alifatické vazby C H). Představitelem této skupiny jsou HK z jezerních sedimentů. Systematičtější klasifikaci půdních HK, založenou na starších pracích 37,38 provedl Kumada 39. Huminové kyseliny rozdělil podle charakteristik jejich VIS spekter do čtyř tříd, označených A, B, P a R p. U huminových kyselin v pořadí R p, P, B a A vzrůstá stupeň humifikace; jednotlivé typy přitom představují stabilní formu HK v půdách silně kyselých (P), kyselých (B) a slabě kyselých až bazických (A, ph < 8). Odlišná struktura uvedených typů HK se projevuje výraznými rozdíly v relativní intenzitě vybraných pásů jejich IR spekter. Označení typu R p pochází z německého Rottenprodukte (produkty rozkladu). Typ R p zahrnuje částečně humifikované produkty rozkladu rostlinného opadu, v jejichž spektrech ve viditelné oblasti bývají někdy pozorovány pásy chlorofylu a pheopigmentů při 660 nm a 400 nm. Huminové kyseliny typu A mají v IR spektrech výrazný pás aromatických vibrací C H při 3075 cm 1, silný pás vibrací O H karboxylů (2630 cm 1 ) a ze všech skupin HK nejmenší pás alifatických vibrací C H při 2940 cm 1. Ostré jsou absorpční pásy poblíž 1710 cm 1 a 1615 cm 1, příslušející valenčním vibracím C=O a C=C. Pásy při 1640 cm 1 a 1515 cm 1, zřetelné ve spektrech typů B a R, se u HK podtypu A 1 nevyskytují, zatímco u podtypu A 2 se pás při 1515 cm 1 projevuje jako rameno sousedního pásu. Dva velmi slabé pásy se vyskytují v oblasti cm 1 a velmi silný a široký pás mezi vlnočty cm 1. IR spektra huminových kyselin typu B mají výrazný a ostrý pás alifatických vibrací C H při 2940 cm 1, zatímco pásy při 3075 cm 1 a 2630 cm 1 jsou slabé, stejně jako pás při 1690 cm 1. Kromě ostrého absorpčního pásu u 1615 cm 1 a výrazného pásu při 1515 cm 1 lze nalézt rameno pásu při 1640 cm 1. Čtyři poměrně ostré pásy mají maxima při vlnočtech 1450, 1480, 1380 a 1330 cm 1, silný pás je rovněž v oblasti cm 1. Spektra HK typu P se podobají spektrům typu A, hlavní rozdíly jsou v poměrně malé intenzitě pásů při 3075, 2940 a 2630 cm 1. Navíc je u typu P intenzita pásu při 1695 cm 1 ve srovnání s pásem při 1615 cm 1 nižší. Označení P bylo zvoleno podle půdního typu podzol, z nějž byly poprvé tyto HK izolovány, později však byly HK tohoto typu zjištěny i v řadě jiných půd. IR spektra HK typu R p se podobají typu B. Kromě menších pozorovaných rozdílů se liší zejména slabou absorbancí při 2630 cm 1 a přítomností malého ramene pásu při 1540 cm Kvantitativní analýza FTIR spekter huminových látek Přestože je metoda FTIR dostupná již delší dobu, bylo publikováno poměrně málo prací zabývajících se kvantitativním studiem funkčních skupin a struktury huminových kyselin pomocí této techniky. Jako referenčního signálu v FTIR spektrech HK se užívá maxim při 3350 a 1070 cm 1 nebo pásu interního 370
9 standardu. Dříve též používaný pás při 1610 cm 1 se nedoporučuje, protože zahrnuje absorpční pásy více funkčních skupin, zejména COO, jejichž absorbance se výrazně mění s ph vzorku. Z podobných důvodů se dnes neužívá ani pásu s maximem u 1515 cm 1. Vhodnými interními standardy jsou azid sodný 21 s dvojitým maximem ve spektru při 2125 a 2037 cm 1 nebo thiokyanatan draselný 22 (obr. 6) s maximem při 2050 cm 1. Metodu použití interního standardu, která umožňuje kvantitativní srovnání vybraných absorpčních pásů v FTIR spektrech různých huminových látek, popsali rovněž Davis a spol. 23, kteří z IR spekter získali výsledky odpovídající hodnotám stanoveným pomocí 13 C NMR. Normalizace spektra pomocí přídavku interního standardu však vnáší do analýzy systémovou (aditivní) chybu a je zdrojem variability dat, protože intenzita pásů standardu (např. NaN 3 ) vykazuje značnou fluktuaci 21. Interakce vnitřního standardu KSCN s huminovými kyselinami může také způsobit rozšíření pásu standardu, posun jeho maxima nebo snížení intenzity např. vlivem interakce s polárními skupinami HK (vodíkový můstek). Zdá se však, že tyto jevy mají pro kvantitativní analýzu HK okrajový význam 23. Spektra měřená pomocí KBr tablet poskytují při opakování měření poměry intenzit absorpčních pásů s menší variabilitou než spektra měřená na AgCl disku 40. Při opakovaném měření FTIR spekter huminových kyselin lze díky tomu dosáhnout variačního koeficientu do 2,5 % (cit. 41 ). Pro kvantitativní vyhodnocení IR spekter se využívá buď výšky pásu (absorpční intenzity) nebo plochy pásu (integrované intenzity) nad základní linií. Oba postupy při normalizaci na vnitřní standard dávají shodné výsledky 23. Při korekci základní linie se zpravidla 33 používá lineární funkce jako spojnice bodů s nulovou absorbancí (např. Obr. 7. Fourierova dekonvoluce pásů v oblasti cm 1 DRIFT spektra: a) diferenční spektrum oxidované a původní HL, b) totéž spektrum po dekonvoluci. Pomocí dekonvoluce lze v původně širokém pásu kyslíkatých skupin rozlišit maxima, odpovídající valenčním vibracím C=O v δ- a γ-laktonech (1774 a 1743 cm 1 ), ve skupině COOH (1729 cm 1 ) a v chinonech (1673 cm 1 ). Srovnej obr. 9 vlnočty 4000, 2000 a 860 cm 1 ). U spekter látek s výrazným pásem minerálního podílu (Si O, okolo 1050 cm 1 ) nebo vody se někdy volí základní linie v menším rozsahu vlnočtů 22, např cm 1. Při analýze látek se složitým FTIR spektrem se často využívá Fourierovy dekonvoluce 42 (obr. 7) a separace pásů (obr. 8) ve zvolené oblasti spektra, obvykle pomocí smíšené Gaussovy a Lorentzovy funkce za využití speciálního software. Pomocí dekonvoluce diferenčního spektra lze sledovat např. změny HL v průběhu jejich oxidace (obr. 9). Pro kvantitativní stanovení je možno po normalizaci separovaných pásů použít jejich výšku nebo plochu. Kvalitních výsledků však lze dosáhnout i jednoduchými postupy. Dobré shody s výsledky NMR analýz dosáhli Celi a spol. 41, kteří pomocí FTIR spektrometrie stanovili obsah karboxylových skupin v HK jako součet absorpčních intenzit pásů a cm 1, přičemž základní linii spektra vedli lineárně mezi vlnočty 1900 a 900 cm Závěr Obr. 6. FTIR spektrum huminové kyseliny s interním standardem. Pro kvantitativní analýzu bylo rozpuštěno 10 mg HK v 1 ml H 2 O, po přidání vnitřního standardu (KSCN, 2,0 mg ml 1 ) a úpravě ph byl roztok odpařen na křemíkovém okénku. FTIR spektrum filmu HK, vzniklého odpařením vody, bylo měřeno na IR spektrometru Nicolet 740 (rozlišení 2 cm 1, 128 akumulací). Výsledné spektrum bylo získáno odečtením spektra Si okénka Moderní FTIR spektrometrie umožňuje provádět kvalitativní i kvantitativní analýzu huminových látek. Její předností ve srovnání s 13 C NMR spektrometrií nebo s titračními metodami stanovení funkčních skupin HL je malé množství spotřebovaného vzorku (několik miligramů oproti mg) a podstatně rychlejší měření (přibližně 10 vzorků za hodinu oproti hodinám při měření jednoho 13 C NMR spektra v roztoku). Další předností 371
10 Obr. 8. Separace pásů DRIFT spektra pro kvantitativní stanovení funkčních skupin. Byla použita metoda Fourierovy dekonvoluce pásů; separace pásů byla provedena programem Galactic Peak Solve (Grams) pomocí smíšené Gaussovy a Lorentzovy funkce v oblasti spektra cm 1 oproti nukleární magnetické rezonanci je cenová dostupnost FTIR spektrometru i pro menší laboratoře. Zejména při analýze větších sérií vzorků HL se může FTIR spektrometrie stát vážným konkurentem 13 C NMR spektrometrie. Vzhledem k tomu, že při 13 C NMR spektrometrii poskytují signály selektivně jádra uhlíku, a proto jsou strukturní závěry jednoznačnější, je při studiu HL vhodné obě metody kombinovat. Nevýhodou FTIR spektrometrie jsou vysoké nároky na čistotu HL, zejména na nízký obsah jílových minerálů, vody a zbytků činidel, použitých při extrakci nebo koagulaci (difosforečnany, sírany, popřípadě kyselina fluorovodíková). Perspektivní je dosud málo rozšířená klasifikace HL podle jejich FTIR spekter. Významně se FTIR spektrometrie uplatní také při sledování reakcí HL, např. při studiu biotransformace odpadů a interakcí HL v životním prostředí. Ramanova spektrometrie, metoda komplementární k FTIR spektrometrii a široce využívaná při studiu struktury a prostorového uspořádání molekul, se při studiu HL 48 využívá zřídka, mj. pro jejich vysokou fluorescenci. Perspektivní se jeví využití povrchově zesílené Ramanovy spektrometrie (SERS, Surface-enhanced Raman scattering), citlivé techniky podstatně zvyšující Ramanův rozptyl vzorku po smísení s koloidem nanočástic stříbra díky jevu povrchové plazmonové rezonance a chemické rezonance. Zkouší se i kombinace SERS s povrchově zesílenou fluorescencí 49 (SEF, surface-enhanced fluorescence), umožňující sledovat strukturální rozdíly HK a jejich reakční vlastnosti, projevující se v důsledku různých podmínek měření (koncentrace, ph). Obr. 9. Využití diferenčního DRIFT spektra při studiu oxidace huminových látek: a) DRIFT spektrum původní huminové látky, b) DRIFT spektrum huminové látky oxidované HNO 3, c) diferenční spektrum (b a). V diferenčním spektru je výrazný kombinovaný absorpční pás kyslíkatých funkčních skupin s maximem při 1743 cm 1 a charakteristické pásy skupiny NO 2 s maximy u vlnočtů 1539 a 1345 cm 1. Pro srovnání je uvedeno spektrum nitrobenzenu LITERATURA 1. Lehmann J., Kleber M.: Nature 528, 60 (2015). 2. Stevenson F. J.: Humus Chemistry. Genesis, Composition, Reactions. J. Willey, New York Li L., Zhao Z. Y., Huang W. L., Peng P., Sheng G. Y., Fu J. M.: Org. Geochem. 35, 1025 (2004). 4. Machovič V., Novák F., Madronová L., Novák J., v knize: Humic Acids from Raw Materials of the Czech Republic (Madronová L., ed.), str. 21. Nova Sci Publisher, New York Heller C., Ellerbrock R. H., Rosskopf N., Klingenfuss C., Zeitz J.: Eur. J. Soil Sci. 66, 847 (2015). 6. Qi Y., Verheyen T. V., Tikkoo T., Vijayaraghavan R., MacFarlane D. R., Chaffee A. L.: Fuel 158, 23 (2015). 7. Kořínková A., Mikuška P., Večeřa Z.: Chem. Listy 108, 667 (2014). 8. Wang S., Dou S., Yu Z., Ma L., Li Y., Yu S.: J. Soil Sci. Plant Nutr. 14, 363 (2014). 9. Novák F., Šestauberová M., Hrabal R.: J. Mol. Struct. 1093, 179 (2015). 10. Rodriguez F. J., Schlenger P., Garcia-Valverde M.: Sci. Total Environ. 541, 623 (2016). 11. Sabirjanovna T. A., Pasa S., Zhumasilovich D. U., Temel H., Oryntayevna N. G.: Desalin. Water Treat. 57, 776 (2016). 372
11 12. Peng Y., Wei W., Zhou H., Yong Z.: J. Dispersion Sci. Technol. 37, 1590 (2016). 13. Yang L., Wei Z., Zhong W., Cuia J., Wei W.: Colloids Surf., A 490, 9 (2016). 14. Ellerbrock R. H., Gerke H. H.: Vadose Zone J. 15, DOI /vzj (2016). 15. Machovič V., Novák F.: Chem Listy 92, 151 (1998). 16. Novák F., Hrabal R.: Chem Listy 101, 752 (2011). 17. Schnitzer M., Gupta U. C.: Soil Sci. Soc. Am. Proc. 29, 274 (1965). 18. Schnitzer M., Khan S. U. (ed.): Humic Substances in The Environment. Marcel Dekker Inc., New York MacCarthy P., Mark H. B. Jr.: Soil Sci. Soc. Am. Proc. 39, 663 (1975). 20. MacCarthy P., Mark H. B. Jr., Griffiths P. R.: J. Agric. Food Chem. 23, 600 (1975). 21. Gressel N., McGrath A. E., McColl J. G., Powers R. F.: Soil. Sci. Soc. Am. J. 59, 1715 (1995). 22. Novák F., Machovič V., Poledna J.: ChemZi 1, 141 (2005). 23. Davis W. M., Erickson C. L., Johnston C. T., Delfino J. J., Porter J. E.: Chemosphere 38, 2913 (1999). 24. Kortum G.: Reflectance Spectroscopy. Springer Verlag, New York Griffiths P. R., de Haseth J. A.: Fourier Transform Infrared Spectrometry. J. Willey, New York Faix O., v knize: Methods in Lignin Chemistry (Lin Y. S., Dence C. W., ed.), str. 83. Springer-Verlag, New York Alvarez-Puebla R. A., Valenzuela-Calahorro C., Garrido J. J.: Langmuir 20, 3657 (2004). 28. Baes A. U., Bloom P. R.: Soil Sci. Soc. Am. J. 53, 695 (1989). 29. Orlov D. S.: Gumusovyje kisloty počv. Izd. Moskovskovo universiteta, Moskva Chingombe P., Saha B., Wakeman R. J.: Carbon 43, 3132 (2005). 31. Lopez F., Medina F., Prodanov M., Guell C.: J. Colloid Interface Sci. 257, 173 (2003). 32. Nakamoto K.: Infrared and Raman Spectra of Inorganic and Coordination Compounds. 5. vyd. Wiley, New York Inbar Y., Chen Y., Hadar Y.: Soil Sci. Soc. Am. J. 53, 1695 (1989). 34. Wander M. M., Traina S. J.: Soil Sci. Soc. Am. J. 60, 1087 (1966). 35. Bedrock C. N., Cheschire M. V., Chudek J. A., Goodman B. A., Shand C. A., v knize: Humic Substances in The Global Environmnent and Implications on Human Health (Senesi N., Miano T. M., ed.), str Elsevier, New York Stevenson F. J., Goh K. M.: Geochim. Cosmochim. Acta 35, 471 (1971). 37. Simon K., Speichermann H.: Bodenk. Pflanzenernähr. 8, 129 (1938). 38. Springer U.: Bodenk. Pflanzenernähr. 6, 312 (1938). 39. Kumada K: Chemistry of Soil Organic Matter. Elsevier, New York Gressel N., McColl J. G., Powers R. F., McGrath A. E.: Soil Sci. Soc. Am. J. 59, 1723 (1995). 41. Celi L., Schnitzer M., Negre M.: Soil Sci. 162, 189 (1997). 42. Pierce J. A., Jackson R. S., Van Every K. W., Griffiths P. R., Hongjin G.: Anal. Chem. 62, 477 (1990). 43. Bellamy L. J.: The Infra-red Spectra of Complex Molecules. Chapman and Hall, London Schnitzer M., Khan S. U. (ed.): Soil Organic Matter. Elsevier, New York Aiken G. R., v knize: Humic Substances and Their Role in the Environment (Frimmel F. H., Christman R. F., ed.), str. 15. J. Wiley, Chichester Swift R. S., v knize: Methods of Soil Analysis (Sparks D. L., ed.), sv. 3, str Soil Science Society of America, Madison Stevenson F. J., Goh K. M.: Soil Sci. 117, 34 (1974). 48. Francioso O., Sanchez-Cortes S., Tugnoli V., Marzadoria C., Ciavatta C.: J. Mol. Struct. 565/566, 481 (2001). 49. Corrado G., Sanchez-Cortes S., Francioso O., Garcia- Ramos J. V.: Anal. Chim. Acta 616, 69 (2008). F. Novák a, V. Machovič,a,b, H. Hrabalová a, and M. Novotná a ( a University of Chemistry and Technology, Prague, b Institute of Rock Structure and Mechanics, Academy of Sciences of the Czech Republic, Prague): Quantitative FTIR Spectrometry of Humic Substances The modern FTIR spectrometry enables both qualitative and quantitative analysis of humic (HS) and humiclike substances. Priority of this method in comparison with 13 C NMR or titration analysis of functional groups consists in small quantity of consumed sample and time. The availability of FTIR spectrometers for smaller laboratories represents an additional advantage. However, the FTIR spectrometry demands high purity of humic substances, in particular low contents of illite minerals, water, and residues of reagents used for extraction or coagulation (diphosphate, sulphate or hydrofluoric acid). Namely, in analysis of large sample series, the FTIR spectrometry can successfully compete with the (in other respects irreplaceable) 13 C NMR spectrometry. Besides the transmission (KBr) technique of FTIR spectra measurement, at which undesirable ion exchange occurs, the DRIFT and namely ATR (Attenuated Total Reflection) techniques are now widely applied for quantitative analysis of HS. The FTIR spectra-based classification of humic substances, which is rarely applied till now, seems to be a prospective tool. The FTIR spectrometry can widely be used also to study the humus biotransformation, interactions with metal ions, etc. 373
SPEKTROMETRIE. aneb co jsem se dozvěděla. autor: Zdeňka Baxová
 SPEKTROMETRIE aneb co jsem se dozvěděla autor: Zdeňka Baxová FTIR spektrometrie analytická metoda identifikace látek (organických i anorganických) všech skupenství měříme pohlcení IČ záření (o různé vlnové
SPEKTROMETRIE aneb co jsem se dozvěděla autor: Zdeňka Baxová FTIR spektrometrie analytická metoda identifikace látek (organických i anorganických) všech skupenství měříme pohlcení IČ záření (o různé vlnové
IDENTIFIKACE NEZNÁMÉ ORGANICKÉ LÁTKY POMOCÍ INFRAČERVENÉ SPEKTROMETRIE
 Úvod Infračervená spektrometrie (IR) je analytická technika určená především k identifikaci a strukturní charakterizaci organických sloučenin a anorganických látek. Tato nedestruktivní analytická technika
Úvod Infračervená spektrometrie (IR) je analytická technika určená především k identifikaci a strukturní charakterizaci organických sloučenin a anorganických látek. Tato nedestruktivní analytická technika
Infračervená spektrometrie
 Podstata infračervené absorpce jednofotonový přechod mezi dvěma vibračními (vibračně-rotačními) rotačními) stavy molekuly, jejichž energie jsou E 1 a E 2, vyvolaný interakcí s fotonem dopadajícího záření
Podstata infračervené absorpce jednofotonový přechod mezi dvěma vibračními (vibračně-rotačními) rotačními) stavy molekuly, jejichž energie jsou E 1 a E 2, vyvolaný interakcí s fotonem dopadajícího záření
Infračervená spektroskopie
 Infračervená spektroskopie 1 Teoretické základy Podstatou infračervené spektroskopie je interakce infračerveného záření se studovanou hmotou, kdy v případě pohlcení fotonu studovanou hmotou mluvíme o absorpční
Infračervená spektroskopie 1 Teoretické základy Podstatou infračervené spektroskopie je interakce infračerveného záření se studovanou hmotou, kdy v případě pohlcení fotonu studovanou hmotou mluvíme o absorpční
INTERPRETACE INFRAČERVENÝCH SPEKTER
 INTERPRETACE INFRAČERVENÝCH SPEKTER Obecné základy nedestruktivní metoda strukturní analýzy měření přechodů mezi vibračními hladinami změna dipólového momentu během vibrace v=3 v=2 v=1 v=0 fundamentální
INTERPRETACE INFRAČERVENÝCH SPEKTER Obecné základy nedestruktivní metoda strukturní analýzy měření přechodů mezi vibračními hladinami změna dipólového momentu během vibrace v=3 v=2 v=1 v=0 fundamentální
Uvod DIFUZNĚ-REFLEXNÍ INFRAČERVENÁ SPEKTROSKOPIE PŮDNÍCH BITUMENŮ Z OBLASTI ŠUMAVY
 Chem. Listy 92, 151-156(1998) DIFUZNĚ-REFLEXNÍ INFRAČERVENÁ SPEKTROSKOPIE PŮDNÍCH BITUMENŮ Z OBLASTI ŠUMAVY VLADIMÍR MACHOVIČ a a FRANTIŠEK NOVÁK b "Centrální laboratoře, Vysoká škola chemicko-technologická,
Chem. Listy 92, 151-156(1998) DIFUZNĚ-REFLEXNÍ INFRAČERVENÁ SPEKTROSKOPIE PŮDNÍCH BITUMENŮ Z OBLASTI ŠUMAVY VLADIMÍR MACHOVIČ a a FRANTIŠEK NOVÁK b "Centrální laboratoře, Vysoká škola chemicko-technologická,
Pokročilé cvičení z fyzikální chemie KFC/POK2 Vibrační spektroskopie
 Pokročilé cvičení z fyzikální chemie KFC/POK2 Vibrační spektroskopie Vibrace molekul mohou být měřeny buď pomocí absorpce infračerveného záření, nebo pomocí neelastického rozptylu záření, tzn. Ramanova
Pokročilé cvičení z fyzikální chemie KFC/POK2 Vibrační spektroskopie Vibrace molekul mohou být měřeny buď pomocí absorpce infračerveného záření, nebo pomocí neelastického rozptylu záření, tzn. Ramanova
INFRAČERVENÁ SPEKTROMETRIE A BIOSLOŽKY PALIV
 VYSOKÁ ŠKOLA CHEMICKO-TECHNOLOGICKÁ V PRAZE Fakulta technologie ochrany prostředí Ústav technologie ropy a alternativních paliv INFRAČERVENÁ SPEKTROMETRIE A BIOSLOŽKY PALIV Laboratorní cvičení ÚVOD V několika
VYSOKÁ ŠKOLA CHEMICKO-TECHNOLOGICKÁ V PRAZE Fakulta technologie ochrany prostředí Ústav technologie ropy a alternativních paliv INFRAČERVENÁ SPEKTROMETRIE A BIOSLOŽKY PALIV Laboratorní cvičení ÚVOD V několika
Využití UV/VIS a IR spektrometrie v analýze potravin
 Využití UV/VIS a IR spektrometrie v analýze potravin Chemické laboratorní metody v analýze potravin MVDr. Zuzana Procházková, Ph.D. MVDr. Michaela Králová, Ph.D. Spektrometrie: základy Interakce záření
Využití UV/VIS a IR spektrometrie v analýze potravin Chemické laboratorní metody v analýze potravin MVDr. Zuzana Procházková, Ph.D. MVDr. Michaela Králová, Ph.D. Spektrometrie: základy Interakce záření
Molekulová spektroskopie 1. Chemická vazba, UV/VIS
 Molekulová spektroskopie 1 Chemická vazba, UV/VIS 1 Chemická vazba Silová interakce mezi dvěma atomy. Chemické vazby jsou soudržné síly působící mezi jednotlivými atomy nebo ionty v molekulách. Chemická
Molekulová spektroskopie 1 Chemická vazba, UV/VIS 1 Chemická vazba Silová interakce mezi dvěma atomy. Chemické vazby jsou soudržné síly působící mezi jednotlivými atomy nebo ionty v molekulách. Chemická
13. Spektroskopie základní pojmy
 základní pojmy Spektroskopicky významné OPTICKÉ JEVY absorpce absorpční spektrometrie emise emisní spektrometrie rozptyl rozptylové metody Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti
základní pojmy Spektroskopicky významné OPTICKÉ JEVY absorpce absorpční spektrometrie emise emisní spektrometrie rozptyl rozptylové metody Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti
SPEKTRÁLNÍ METODY. Ing. David MILDE, Ph.D. Katedra analytické chemie Tel.: ; (c) David MILDE,
 SEKTRÁLNÍ METODY Ing. David MILDE, h.d. Katedra analytické chemie Tel.: 585634443; E-mail: david.milde@upol.cz (c) -2008 oužitá a doporučená literatura Němcová I., Čermáková L., Rychlovský.: Spektrometrické
SEKTRÁLNÍ METODY Ing. David MILDE, h.d. Katedra analytické chemie Tel.: 585634443; E-mail: david.milde@upol.cz (c) -2008 oužitá a doporučená literatura Němcová I., Čermáková L., Rychlovský.: Spektrometrické
INTERPRETACE HMOTNOSTNÍCH SPEKTER
 INTERPRETACE HMOTNOSTNÍCH SPEKTER Hmotnostní spektrometrie hmotnostní spektrometrie = fyzikálně chemická metoda založená na rozdělení hmotnosti iontů v plynné fázi podle jejich poměru hmotnosti a náboje
INTERPRETACE HMOTNOSTNÍCH SPEKTER Hmotnostní spektrometrie hmotnostní spektrometrie = fyzikálně chemická metoda založená na rozdělení hmotnosti iontů v plynné fázi podle jejich poměru hmotnosti a náboje
Úvod do spektrálních metod pro analýzu léčiv
 Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti Úvod do spektrálních metod pro analýzu léčiv Pavel Matějka, Vadym Prokopec pavel.matejka@vscht.cz pavel.matejka@gmail.com Vadym.Prokopec@vscht.cz
Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti Úvod do spektrálních metod pro analýzu léčiv Pavel Matějka, Vadym Prokopec pavel.matejka@vscht.cz pavel.matejka@gmail.com Vadym.Prokopec@vscht.cz
Stanovení kvality humusu spektrofotometricky
 Stanovení kvality humusu spektrofotometricky Definice humusu Synonymum k půdní organické hmotě Odumřelá organická hmota v různém stupni rozkladu a syntézy, jejíž část je vázána na minerální podíl Rozdělení
Stanovení kvality humusu spektrofotometricky Definice humusu Synonymum k půdní organické hmotě Odumřelá organická hmota v různém stupni rozkladu a syntézy, jejíž část je vázána na minerální podíl Rozdělení
Autoři: Pavel Zachař, David Sýkora Ukázky spekter k procvičování na semináři: Tento soubor je pouze prvním ilustrativním seznámením se základními prin
 Autoři: Pavel Zachař, David Sýkora Ukázky spekter k procvičování na semináři: Tento soubor je pouze prvním ilustrativním seznámením se základními principy hmotnostní spektrometrie a v žádném případě nezahrnuje
Autoři: Pavel Zachař, David Sýkora Ukázky spekter k procvičování na semináři: Tento soubor je pouze prvním ilustrativním seznámením se základními principy hmotnostní spektrometrie a v žádném případě nezahrnuje
Opakování
 Slabé vazebné interakce Opakování Co je to atom? Opakování Opakování Co je to atom? Atom je nejmenší částice hmoty, chemicky dále nedělitelná. Skládá se z atomového jádra obsahujícího protony a neutrony
Slabé vazebné interakce Opakování Co je to atom? Opakování Opakování Co je to atom? Atom je nejmenší částice hmoty, chemicky dále nedělitelná. Skládá se z atomového jádra obsahujícího protony a neutrony
Vybrané spektroskopické metody
 Vybrané spektroskopické metody a jejich porovnání s Ramanovou spektroskopií Předmět: Kapitoly o nanostrukturách (2012/2013) Autor: Bc. Michal Martinek Školitel: Ing. Ivan Gregora, CSc. Obsah přednášky
Vybrané spektroskopické metody a jejich porovnání s Ramanovou spektroskopií Předmět: Kapitoly o nanostrukturách (2012/2013) Autor: Bc. Michal Martinek Školitel: Ing. Ivan Gregora, CSc. Obsah přednášky
INFRAČERVENÁ SPEKTROMETRIE KVALITATTIVNÍ A KVANTITATIVNÍ STANOVENÍ
 INFRAČERVENÁ SPEKTROMETRIE KVALITATTIVNÍ A KVANTITATIVNÍ STANOVENÍ Úvod: Infračervená spektrometrie (IR) je analytická technika molekulové vibrační spektrometrie, která se zabývá studiem pohybů atomů v
INFRAČERVENÁ SPEKTROMETRIE KVALITATTIVNÍ A KVANTITATIVNÍ STANOVENÍ Úvod: Infračervená spektrometrie (IR) je analytická technika molekulové vibrační spektrometrie, která se zabývá studiem pohybů atomů v
VIBRAČNÍ SPEKTROMETRIE
 VIBRAČNÍ SPEKTROMETRIE (c) -2012 RAMANOVA SPEKTROMETRIE 1 PRINCIP METODY Měří se rozptýlené záření, které vzniká interakcí monochromatického záření z viditelné oblasti s molekulami vzorku za současné změny
VIBRAČNÍ SPEKTROMETRIE (c) -2012 RAMANOVA SPEKTROMETRIE 1 PRINCIP METODY Měří se rozptýlené záření, které vzniká interakcí monochromatického záření z viditelné oblasti s molekulami vzorku za současné změny
IČ spektroskopie. IR Spectroscopy FTIR moderní technika viz dále
 IR spektroskopie IČ spektroskopie IR Spectroscopy FTIR moderní technika viz dále Použití: identifikace a strukturní charakterizace organických sloučenin a také stanovení anorganických látek k identifikaci
IR spektroskopie IČ spektroskopie IR Spectroscopy FTIR moderní technika viz dále Použití: identifikace a strukturní charakterizace organických sloučenin a také stanovení anorganických látek k identifikaci
Základy NIR spektrometrie a její praktické využití
 Nicolet CZ s.r.o. The world leader in serving science Základy NIR spektrometrie a její praktické využití NIR praktická metoda molekulové spektroskopie, nahrazující pracnější, časově náročnější a dražší
Nicolet CZ s.r.o. The world leader in serving science Základy NIR spektrometrie a její praktické využití NIR praktická metoda molekulové spektroskopie, nahrazující pracnější, časově náročnější a dražší
SPEKTROSKOPICKÉ VLASTNOSTI LÁTEK (ZÁKLADY SPEKTROSKOPIE)
 SPEKTROSKOPICKÉ VLASTNOSTI LÁTEK (ZÁKLADY SPEKTROSKOPIE) Elektromagnetické vlnění SVĚTLO Charakterizace záření Vlnová délka - (λ) : jednotky: m (obvykle nm) λ Souvisí s povahou fotonu Charakterizace záření
SPEKTROSKOPICKÉ VLASTNOSTI LÁTEK (ZÁKLADY SPEKTROSKOPIE) Elektromagnetické vlnění SVĚTLO Charakterizace záření Vlnová délka - (λ) : jednotky: m (obvykle nm) λ Souvisí s povahou fotonu Charakterizace záření
Spektroskopické é techniky a mikroskopie. Spektroskopie. Typy spektroskopických metod. Cirkulární dichroismus. Fluorescence UV-VIS
 Spektroskopické é techniky a mikroskopie Spektroskopie metody zahrnující interakce mezi světlem (fotony) a hmotou (elektrony a protony v atomech a molekulách Typy spektroskopických metod IR NMR Elektron-spinová
Spektroskopické é techniky a mikroskopie Spektroskopie metody zahrnující interakce mezi světlem (fotony) a hmotou (elektrony a protony v atomech a molekulách Typy spektroskopických metod IR NMR Elektron-spinová
Optické spektroskopie 1 LS 2014/15
 Optické spektroskopie 1 LS 2014/15 Martin Kubala 585634179 mkubala@prfnw.upol.cz 1.Úvod Velikosti objektů v přírodě Dítě ~ 1 m (10 0 m) Prst ~ 2 cm (10-2 m) Vlas ~ 0.1 mm (10-4 m) Buňka ~ 20 m (10-5 m)
Optické spektroskopie 1 LS 2014/15 Martin Kubala 585634179 mkubala@prfnw.upol.cz 1.Úvod Velikosti objektů v přírodě Dítě ~ 1 m (10 0 m) Prst ~ 2 cm (10-2 m) Vlas ~ 0.1 mm (10-4 m) Buňka ~ 20 m (10-5 m)
ZŠ ÚnO, Bratří Čapků 1332
 Animovaná chemie Top-Hit Analytická chemie Analýza anorganických látek Důkaz aniontů Důkaz kationtů Důkaz kyslíku Důkaz vody Gravimetrická analýza Hmotnostní spektroskopie Chemická analýza Nukleární magnetická
Animovaná chemie Top-Hit Analytická chemie Analýza anorganických látek Důkaz aniontů Důkaz kationtů Důkaz kyslíku Důkaz vody Gravimetrická analýza Hmotnostní spektroskopie Chemická analýza Nukleární magnetická
INSTRUMENTÁLNÍ METODY
 INSTRUMENTÁLNÍ METODY ACH/IM David MILDE, 2014 Dělení instrumentálních metod Spektrální metody (MILDE) Separační metody (JIROVSKÝ) Elektroanalytické metody (JIROVSKÝ) Ostatní: imunochemické, radioanalytické,
INSTRUMENTÁLNÍ METODY ACH/IM David MILDE, 2014 Dělení instrumentálních metod Spektrální metody (MILDE) Separační metody (JIROVSKÝ) Elektroanalytické metody (JIROVSKÝ) Ostatní: imunochemické, radioanalytické,
Spektrometrické metody. Reflexní a fotoakustická spektroskopie
 Spektrometrické metody Reflexní a fotoakustická spektroskopie odraz elektromagnetického záření - souvislost absorpce a reflexe Kubelka-Munk funkce fotoakustická spektroskopie Měření odrazivosti elmg záření
Spektrometrické metody Reflexní a fotoakustická spektroskopie odraz elektromagnetického záření - souvislost absorpce a reflexe Kubelka-Munk funkce fotoakustická spektroskopie Měření odrazivosti elmg záření
Skupenské stavy látek. Mezimolekulární síly
 Skupenské stavy látek Mezimolekulární síly 1 Interakce iont-dipól Např. hydratační (solvatační) interakce mezi Na + (iont) a molekulou vody (dipól). Jde o nejsilnější mezimolekulární (nevazebnou) interakci.
Skupenské stavy látek Mezimolekulární síly 1 Interakce iont-dipól Např. hydratační (solvatační) interakce mezi Na + (iont) a molekulou vody (dipól). Jde o nejsilnější mezimolekulární (nevazebnou) interakci.
Obsah. 1. Uvod. Chem. Listy 92, 434-440 (1998) VYUŽITÍ INFRAČERVENÉ SPEKTROFOTOMETRIE PRO SLEDOVÁNÍ ZMĚN PŘI OXIDACI ŘEPKOVÉHO OLEJE
 Chem. Listy 92, 434-440 (1998) VYUŽITÍ INFRAČERVENÉ SPEKTROFOTOMETRIE PRO SLEDOVÁNÍ ZMĚN PŘI OXIDACI ŘEPKOVÉHO OLEJE JAROSLAV HÁJEK a, VLADIMÍR MACHOVIČ b *, OLGA KŘÍŽOVÁ a, VLADIMÍRA SEDLÁČKOVÁ 3 a MIROSLAVA
Chem. Listy 92, 434-440 (1998) VYUŽITÍ INFRAČERVENÉ SPEKTROFOTOMETRIE PRO SLEDOVÁNÍ ZMĚN PŘI OXIDACI ŘEPKOVÉHO OLEJE JAROSLAV HÁJEK a, VLADIMÍR MACHOVIČ b *, OLGA KŘÍŽOVÁ a, VLADIMÍRA SEDLÁČKOVÁ 3 a MIROSLAVA
11.Metody molekulové spektrometrie pro kvantitativní analýzu léčiv
 Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti 11.Metody molekulové spektrometrie pro kvantitativní analýzu léčiv Vadym Prokopec Vadym.Prokopec@vscht.cz 11.Metody molekulové spektrometrie
Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti 11.Metody molekulové spektrometrie pro kvantitativní analýzu léčiv Vadym Prokopec Vadym.Prokopec@vscht.cz 11.Metody molekulové spektrometrie
Spektroskopie v UV-VIS oblasti. UV-VIS spektroskopie. Roztok KMnO 4. pracuje nejčastěji v oblasti 200-800 nm
 Spektroskopie v UV-VIS oblasti UV-VIS spektroskopie pracuje nejčastěji v oblasti 2-8 nm lze měřit i < 2 nm či > 8 nm UV VIS IR Ultra Violet VISible Infra Red Roztok KMnO 4 roztok KMnO 4 je červenofialový
Spektroskopie v UV-VIS oblasti UV-VIS spektroskopie pracuje nejčastěji v oblasti 2-8 nm lze měřit i < 2 nm či > 8 nm UV VIS IR Ultra Violet VISible Infra Red Roztok KMnO 4 roztok KMnO 4 je červenofialový
IR a UV VIS spektroskopie
 IR a UV VIS spektroskopie IČ spektroskopie IR Spectroscopy FTIR moderní technika viz dále Použití: identifikace a strukturní charakterizace organických sloučenin a také stanovení anorganických látek k
IR a UV VIS spektroskopie IČ spektroskopie IR Spectroscopy FTIR moderní technika viz dále Použití: identifikace a strukturní charakterizace organických sloučenin a také stanovení anorganických látek k
Sada 7 Název souboru Ročník Předmět Formát Název výukového materiálu Anotace
 Sada 7 Název souboru Ročník Předmět Formát Název výukového materiálu Anotace VY_52_INOVACE_737 8. Chemie notebook Směsi Materiál slouží k vyvození a objasnění pojmů (klíčová slova - chemická látka, směs,
Sada 7 Název souboru Ročník Předmět Formát Název výukového materiálu Anotace VY_52_INOVACE_737 8. Chemie notebook Směsi Materiál slouží k vyvození a objasnění pojmů (klíčová slova - chemická látka, směs,
HPLC - Detektory A.Braithwaite and F.J.Smith; Chromatographic Methods, Fifth edition, Blackie Academic & Professional 1996 Colin F. Poole and Salwa K.
 Vysokoúčinná kapalinová chromatografie - Detektory - I Příprava předmětu byla podpořena projektem OPPA č. CZ.2.17/3.1.00/33253 HPLC - Detektory A.Braithwaite and F.J.Smith; Chromatographic Methods, Fifth
Vysokoúčinná kapalinová chromatografie - Detektory - I Příprava předmětu byla podpořena projektem OPPA č. CZ.2.17/3.1.00/33253 HPLC - Detektory A.Braithwaite and F.J.Smith; Chromatographic Methods, Fifth
Absorpční fotometrie
 Absorpční fotometrie - v ultrafialové (UV) a viditelné (VIS) oblasti přechody mezi elektronovými stavy +... - v infračervené (IČ) oblasti přechody mezi vibračními stavy +... - v mikrovlnné oblasti přechody
Absorpční fotometrie - v ultrafialové (UV) a viditelné (VIS) oblasti přechody mezi elektronovými stavy +... - v infračervené (IČ) oblasti přechody mezi vibračními stavy +... - v mikrovlnné oblasti přechody
ATOMOVÁ SPEKTROMETRIE
 ATOMOVÁ SPEKTROMETRIE doc. Ing. David MILDE, Ph.D. tel.: 585634443 E-mail: david.milde@upol.cz (c) -017 Doporučená literatura Černohorský T., Jandera P.: Atomová spektrometrie. Univerzita Pardubice 1997.
ATOMOVÁ SPEKTROMETRIE doc. Ing. David MILDE, Ph.D. tel.: 585634443 E-mail: david.milde@upol.cz (c) -017 Doporučená literatura Černohorský T., Jandera P.: Atomová spektrometrie. Univerzita Pardubice 1997.
Emise vyvolaná působením fotonů nebo částic
 Emise vyvolaná působením fotonů nebo částic PES (fotoelektronová spektroskopie) XPS (rentgenová fotoelektronová spektroskopie), ESCA (elektronová spektroskopie pro chemickou analýzu) UPS (ultrafialová
Emise vyvolaná působením fotonů nebo částic PES (fotoelektronová spektroskopie) XPS (rentgenová fotoelektronová spektroskopie), ESCA (elektronová spektroskopie pro chemickou analýzu) UPS (ultrafialová
Karboxylové kyseliny a jejich funkční deriváty
 Karboxylové kyseliny a jejich funkční deriváty Úvod Karboxylové kyseliny jsou nejdůležitější organické kyseliny. Jejich funkční skupina je karboxylová skupina a tento název je složen ze slov karbonyl a
Karboxylové kyseliny a jejich funkční deriváty Úvod Karboxylové kyseliny jsou nejdůležitější organické kyseliny. Jejich funkční skupina je karboxylová skupina a tento název je složen ze slov karbonyl a
Organické látky. Organická geochemie a rozpuštěný organický uhlík
 Organická geochemie a rozpuštěný organický uhlík struktura, nomenklatura a funkční skupiny huminové látky a další přírodní OC reaktivita DOC/POC distribuce kyselost (acidita) Přírodní a znečišťující organické
Organická geochemie a rozpuštěný organický uhlík struktura, nomenklatura a funkční skupiny huminové látky a další přírodní OC reaktivita DOC/POC distribuce kyselost (acidita) Přírodní a znečišťující organické
O Minimální počet valencí potřebných ke spojení vícevazných atomů = (24 C + 3 O + 7 N 1) * 2 = 66 valencí
 Jméno a příjmení:_bohumil_dolenský_ Datum:_10.12.2010_ Fakulta:_FCHI_ Kruh:_ÚACh_ 1. Sepište seznam signálů 1 H dle klesajícího chemického posunu (včetně nečistot), uveďte chemický posun, multiplicitu
Jméno a příjmení:_bohumil_dolenský_ Datum:_10.12.2010_ Fakulta:_FCHI_ Kruh:_ÚACh_ 1. Sepište seznam signálů 1 H dle klesajícího chemického posunu (včetně nečistot), uveďte chemický posun, multiplicitu
Diskutujte, jak široký bude pás spojený s fosforescencí versus fluorescencí. Udělejte odhad v cm -1.
 S použitím modelu volného elektronu (=částice v krabici) spočtěte vlnovou délku a vlnočet nejdlouhovlnějšího elektronového přechodu u molekuly dekapentaenu a oktatetraenu. Diskutujte polohu absorpčního
S použitím modelu volného elektronu (=částice v krabici) spočtěte vlnovou délku a vlnočet nejdlouhovlnějšího elektronového přechodu u molekuly dekapentaenu a oktatetraenu. Diskutujte polohu absorpčního
10/21/2013. K. Záruba. Chování a vlastnosti nanočástic ovlivňuje. velikost a tvar (distribuce) povrchové atomy, funkční skupiny porozita stabilita
 Chování a vlastnosti nanočástic ovlivňuje velikost a tvar (distribuce) povrchové atomy, funkční skupiny porozita stabilita K. Záruba Optická mikroskopie Elektronová mikroskopie (SEM, TEM) Fotoelektronová
Chování a vlastnosti nanočástic ovlivňuje velikost a tvar (distribuce) povrchové atomy, funkční skupiny porozita stabilita K. Záruba Optická mikroskopie Elektronová mikroskopie (SEM, TEM) Fotoelektronová
VODA 1. FYZIKÁLNÍ METODY. Charakteristické vlastnosti vody využívané v analytických metodách. chemická reaktivita. těkavost, rozpouštěcí schopnost
 VODA http://www3.interscience interscience.wiley.com/cgi- bin/bookhome bookhome/109880499?cretry=1&sretry=0 Charakteristické vlastnosti vody využívané v analytických metodách chemická reaktivita těkavost,
VODA http://www3.interscience interscience.wiley.com/cgi- bin/bookhome bookhome/109880499?cretry=1&sretry=0 Charakteristické vlastnosti vody využívané v analytických metodách chemická reaktivita těkavost,
SPEKTROSKOPIE NUKLEÁRNÍ MAGNETICKÉ REZONANCE
 SPEKTROSKOPIE NUKLEÁRNÍ MAGNETICKÉ REZONANCE Obecné základy nedestruktivní metoda strukturní analýzy zabývá se rezonancí atomových jader nutná podmínka pro měření spekter: nenulový spin atomového jádra
SPEKTROSKOPIE NUKLEÁRNÍ MAGNETICKÉ REZONANCE Obecné základy nedestruktivní metoda strukturní analýzy zabývá se rezonancí atomových jader nutná podmínka pro měření spekter: nenulový spin atomového jádra
Úvod do strukturní analýzy farmaceutických látek
 Úvod do strukturní analýzy farmaceutických látek Garant předmětu: Vyučující: doc. Ing. Bohumil Dolenský, Ph.D. prof. RNDr. Pavel Matějka, Ph.D., A136, linka 3687, matejkap@vscht.cz doc. Ing. Bohumil Dolenský,
Úvod do strukturní analýzy farmaceutických látek Garant předmětu: Vyučující: doc. Ing. Bohumil Dolenský, Ph.D. prof. RNDr. Pavel Matějka, Ph.D., A136, linka 3687, matejkap@vscht.cz doc. Ing. Bohumil Dolenský,
CHEMICKÉ VÝPOČTY I. ČÁST LÁTKOVÉ MNOŽSTVÍ. HMOTNOSTI ATOMŮ A MOLEKUL.
 CHEMICKÉ VÝPOČTY I. ČÁST LÁTKOVÉ MNOŽSTVÍ. HMOTNOSTI ATOMŮ A MOLEKUL. Látkové množství Značka: n Jednotka: mol Definice: Jeden mol je množina, která má stejný počet prvků, jako je atomů ve 12 g nuklidu
CHEMICKÉ VÝPOČTY I. ČÁST LÁTKOVÉ MNOŽSTVÍ. HMOTNOSTI ATOMŮ A MOLEKUL. Látkové množství Značka: n Jednotka: mol Definice: Jeden mol je množina, která má stejný počet prvků, jako je atomů ve 12 g nuklidu
Fotodegradace rašelinných huminových látek
 Výzkum možností minimalizace obsahů organických škodlivin ve zdrojích pitných vod v Krušných horách Fotodegradace rašelinných huminových látek Krtička M. 1, Novák F. 2, Sýkorová A. 3, Novotná M. 3 Říjen
Výzkum možností minimalizace obsahů organických škodlivin ve zdrojích pitných vod v Krušných horách Fotodegradace rašelinných huminových látek Krtička M. 1, Novák F. 2, Sýkorová A. 3, Novotná M. 3 Říjen
Stanovení koncentrace (kvantifikace) proteinů
 Stanovení koncentrace (kvantifikace) proteinů Bioanalytické metody Prof. RNDr. Pavel Peč, CSc. Úvod Kritéria výběru metod stanovení koncentrace proteinů jsou založena na možnostech pro vlastní analýzu,
Stanovení koncentrace (kvantifikace) proteinů Bioanalytické metody Prof. RNDr. Pavel Peč, CSc. Úvod Kritéria výběru metod stanovení koncentrace proteinů jsou založena na možnostech pro vlastní analýzu,
Diagnostika olejem plněných transformátorů P. Prosr 1, M. Brandt 2 1
 Ročník 2008 Číslo IV Diagnostika olejem plněných transformátorů P. Prosr, M. Brandt 2 Katedra technologií a měření, Fakulta elektrotechnická, ZČU v Plzni, Univerzitní 26, Plzeň 2 Centrum výskumu mechatronických
Ročník 2008 Číslo IV Diagnostika olejem plněných transformátorů P. Prosr, M. Brandt 2 Katedra technologií a měření, Fakulta elektrotechnická, ZČU v Plzni, Univerzitní 26, Plzeň 2 Centrum výskumu mechatronických
Třídění látek. Chemie 1.KŠPA
 Třídění látek Chemie 1.KŠPA Systém (soustava) Vymezím si kus prostoru, látky v něm obsažené nazýváme systém soustava okolí svět Stěny soustavy Soustava může být: Izolovaná = stěny nedovolí výměnu částic
Třídění látek Chemie 1.KŠPA Systém (soustava) Vymezím si kus prostoru, látky v něm obsažené nazýváme systém soustava okolí svět Stěny soustavy Soustava může být: Izolovaná = stěny nedovolí výměnu částic
STANOVENÍ ETHANOLU V ALKOHOLICKÉM NÁPOJI POMOCÍ NIR SPEKTROMETRIE
 STANOVENÍ ETHANOLU V ALKOHOLICKÉM NÁPOJI POMOCÍ NIR SPEKTROMETRIE Úvod Infračervená spektrometrie v blízké oblasti (Near-Infrared Spectrometry NIR spectrometry) je metoda molekulové spektrometrie, která
STANOVENÍ ETHANOLU V ALKOHOLICKÉM NÁPOJI POMOCÍ NIR SPEKTROMETRIE Úvod Infračervená spektrometrie v blízké oblasti (Near-Infrared Spectrometry NIR spectrometry) je metoda molekulové spektrometrie, která
Identifikace barviv pomocí Ramanovy spektrometrie
 Identifikace barviv pomocí Ramanovy spektrometrie V kriminalistických laboratořích se provádí technická expertíza písemností, která se mimo jiné zabývá zkoumáním použitých psacích prostředků: tiskových
Identifikace barviv pomocí Ramanovy spektrometrie V kriminalistických laboratořích se provádí technická expertíza písemností, která se mimo jiné zabývá zkoumáním použitých psacích prostředků: tiskových
Nukleární magnetická rezonance (NMR)
 Nukleární magnetická rezonance (NMR) Mgr. Zdeněk Moravec, Ph.D. Úvod Zkratka NMR znamená Nukleární Magnetická Rezonance. Jde o analytickou metodu, která na základě absorpce radiofrekvenčního záření vzorkem
Nukleární magnetická rezonance (NMR) Mgr. Zdeněk Moravec, Ph.D. Úvod Zkratka NMR znamená Nukleární Magnetická Rezonance. Jde o analytickou metodu, která na základě absorpce radiofrekvenčního záření vzorkem
VIBRAČNÍ SPEKTROMETRIE
 VIBRAČNÍ SPEKTROMETRIE (c) -2012 INFRAČERVENÁ SPEKTROMETRIE 1 INFRAČERVENÉ ZÁŘENÍ Infračervené (IR) záření: vlnočty 13000 10 cm -1, což odpovídá 0,78 1000 µm. DĚLENÍ: blízká IR oblast 13000 5000 cm -1
VIBRAČNÍ SPEKTROMETRIE (c) -2012 INFRAČERVENÁ SPEKTROMETRIE 1 INFRAČERVENÉ ZÁŘENÍ Infračervené (IR) záření: vlnočty 13000 10 cm -1, což odpovídá 0,78 1000 µm. DĚLENÍ: blízká IR oblast 13000 5000 cm -1
HYDROXYDERIVÁTY. Alkoholy Fenoly Bc. Miroslava Wilczková
 HYDROXYDERIVÁTY Alkoholy Fenoly Bc. Miroslava Wilczková HYDROXYDERIVÁTY Alkoholy -OH skupina vázána na uhlíkový atom alifatického řetězce Fenoly -OH skupina vázána na uhlíku, který je součástí aromatického
HYDROXYDERIVÁTY Alkoholy Fenoly Bc. Miroslava Wilczková HYDROXYDERIVÁTY Alkoholy -OH skupina vázána na uhlíkový atom alifatického řetězce Fenoly -OH skupina vázána na uhlíku, který je součástí aromatického
Molekulární krystal vazebné poměry. Bohumil Kratochvíl
 Molekulární krystal vazebné poměry Bohumil Kratochvíl Předmět: Chemie a fyzika pevných léčiv, 2017 Složení farmaceutických substancí - API Z celkového portfolia API tvoří asi 90 % organické sloučeniny,
Molekulární krystal vazebné poměry Bohumil Kratochvíl Předmět: Chemie a fyzika pevných léčiv, 2017 Složení farmaceutických substancí - API Z celkového portfolia API tvoří asi 90 % organické sloučeniny,
Základní parametry 1 H NMR spekter
 LEKCE 1a Základní parametry 1 NMR spekter Počet signálů ve spektru (zjištění počtu skupin chemicky ekvivalentních jader) Integrální intenzita (intenzita pásů závisí na počtu jader) Chemický posun (polohy
LEKCE 1a Základní parametry 1 NMR spekter Počet signálů ve spektru (zjištění počtu skupin chemicky ekvivalentních jader) Integrální intenzita (intenzita pásů závisí na počtu jader) Chemický posun (polohy
Pevné lékové formy. Vlastnosti pevných látek. Charakterizace pevných látek ke zlepšení vlastností je vhodné využít materiálové inženýrství
 Pevné lékové formy Vlastnosti pevných látek stabilita Vlastnosti léčiva rozpustnost krystalinita ke zlepšení vlastností je vhodné využít materiálové inženýrství Charakterizace pevných látek difraktometrie
Pevné lékové formy Vlastnosti pevných látek stabilita Vlastnosti léčiva rozpustnost krystalinita ke zlepšení vlastností je vhodné využít materiálové inženýrství Charakterizace pevných látek difraktometrie
Skupenské stavy. Kapalina Částečně neuspořádané Volný pohyb částic nebo skupin částic Částice blíže u sebe
 Skupenské stavy Plyn Zcela neuspořádané Hodně volného prostoru Zcela volný pohyb částic Částice daleko od sebe Kapalina Částečně neuspořádané Volný pohyb částic nebo skupin částic Částice blíže u sebe
Skupenské stavy Plyn Zcela neuspořádané Hodně volného prostoru Zcela volný pohyb částic Částice daleko od sebe Kapalina Částečně neuspořádané Volný pohyb částic nebo skupin částic Částice blíže u sebe
Infračervená spektrometrie
 Infračervená spektrometrie Obsah kapitoly Teorie Instrumentace Pracovní techniky IR spektrometrie MIR Identifikace látek Kvantitativní analýza Aplikace v analýze potravin NIR Vlastnosti metody Aplikace
Infračervená spektrometrie Obsah kapitoly Teorie Instrumentace Pracovní techniky IR spektrometrie MIR Identifikace látek Kvantitativní analýza Aplikace v analýze potravin NIR Vlastnosti metody Aplikace
Kvantitativní fázová analýza
 Kvantitativní fázová analýza Kvantitativní rentgenová (fázová) analýza Založena na měření intenzity charakteristických linií. Intenzita je ovlivněna: strukturou minerálu a interferencemi uspořádáním aparatury
Kvantitativní fázová analýza Kvantitativní rentgenová (fázová) analýza Založena na měření intenzity charakteristických linií. Intenzita je ovlivněna: strukturou minerálu a interferencemi uspořádáním aparatury
MOLEKULOVÁ ABSORPČNÍ SPEKTROFOTOMETRIE
 OEKUOVÁ BSORPČNÍ SPEKTROFOTOETRIE v UV a viditelné oblasti spektra 4 Studium spektrofotometrických vlastností a komplexů iontů s ligandy 1. bsorpce hydratovaných iontů: Cu(II), Cr(III), Ni(II), Fe(III),
OEKUOVÁ BSORPČNÍ SPEKTROFOTOETRIE v UV a viditelné oblasti spektra 4 Studium spektrofotometrických vlastností a komplexů iontů s ligandy 1. bsorpce hydratovaných iontů: Cu(II), Cr(III), Ni(II), Fe(III),
- Rayleighův rozptyl turbidimetrie, nefelometrie - Ramanův rozptyl. - fluorescence - fosforescence
 ROZPTYLOVÉ a EMISNÍ metody - Rayleighův rozptyl turbidimetrie, nefelometrie - Ramanův rozptyl - fluorescence - fosforescence Ramanova spektroskopie Každá čára Ramanova spektra je svými vlastnostmi závislá
ROZPTYLOVÉ a EMISNÍ metody - Rayleighův rozptyl turbidimetrie, nefelometrie - Ramanův rozptyl - fluorescence - fosforescence Ramanova spektroskopie Každá čára Ramanova spektra je svými vlastnostmi závislá
FTIR absorpční spektrometrie KBr transmisní a ATR metody
 FTIR absorpční spektrometrie KBr transmisní a ATR metody Teorie: Infračervená spektroskopie je nedestruktivní analytická technika určená především pro identifikaci a strukturní charakterizaci organických
FTIR absorpční spektrometrie KBr transmisní a ATR metody Teorie: Infračervená spektroskopie je nedestruktivní analytická technika určená především pro identifikaci a strukturní charakterizaci organických
ABSORPČNÍ A LUMINISCENČNÍ SPEKTROMETRIE V UV/Vis OBLASTI SPEKTRA
 ABSORPČNÍ A LUMINISCENČNÍ SPEKTROMETRIE V UV/Vis OBLASTI SPEKTRA -2014 ABSORPČNÍ SPEKTROMETRIE ACH/IM 1 Absorpce záření ve Vis oblasti Při dopadu bílého světla na vzorek může být záření zcela odraženo
ABSORPČNÍ A LUMINISCENČNÍ SPEKTROMETRIE V UV/Vis OBLASTI SPEKTRA -2014 ABSORPČNÍ SPEKTROMETRIE ACH/IM 1 Absorpce záření ve Vis oblasti Při dopadu bílého světla na vzorek může být záření zcela odraženo
) se ve vodě ihned rozpouští za tvorby amonných solí (iontová, disociovaná forma NH 4+ ). Vzájemný poměr obou forem závisí na ph a teplotě.
 Amoniakální dusík Amoniakální dusík se vyskytuje téměř ve všech typech vod. Je primárním produktem rozkladu organických dusíkatých látek živočišného i rostlinného původu. Organického původu je rovněž ve
Amoniakální dusík Amoniakální dusík se vyskytuje téměř ve všech typech vod. Je primárním produktem rozkladu organických dusíkatých látek živočišného i rostlinného původu. Organického původu je rovněž ve
02 Nevazebné interakce
 02 Nevazebné interakce Nevazebné interakce Druh chemické vazby Určují 3D konfiguraci makromolekul, účastní se mnoha biologických procesů, zodpovědné za uspořádání molekul v krystalu Síla nevazebných interakcí
02 Nevazebné interakce Nevazebné interakce Druh chemické vazby Určují 3D konfiguraci makromolekul, účastní se mnoha biologických procesů, zodpovědné za uspořádání molekul v krystalu Síla nevazebných interakcí
ATOMOVÁ SPEKTROMETRIE
 ATOMOVÁ SPEKTROMETRIE Atomová spektrometrie valenčních e - 1. OES (AES). AAS 3. AFS 1 Atomová spektra čárová spektra Tok záření P - množství zářivé energie (Q E ) přenesené od zdroje za jednotku času.
ATOMOVÁ SPEKTROMETRIE Atomová spektrometrie valenčních e - 1. OES (AES). AAS 3. AFS 1 Atomová spektra čárová spektra Tok záření P - množství zářivé energie (Q E ) přenesené od zdroje za jednotku času.
H H C C C C C C H CH 3 H C C H H H H H H
 Alkany a cykloalkany sexta Martin Dojiva uhlovodíky obsahující pouze jednoduché vazby obecný vzorec alkanů: C n 2n+2 cykloalkanů: C n 2n homologický přírůstek C 2 Dělení alkanů přímé větvené u větvených
Alkany a cykloalkany sexta Martin Dojiva uhlovodíky obsahující pouze jednoduché vazby obecný vzorec alkanů: C n 2n+2 cykloalkanů: C n 2n homologický přírůstek C 2 Dělení alkanů přímé větvené u větvených
Teorie kyselin a zásad poznámky 5.A GVN
 Teorie kyselin a zásad poznámky 5A GVN 13 června 2007 Arrheniova teorie platná pouze pro vodní roztoky kyseliny jsou látky schopné ve vodném roztoku odštěpit vodíkový kation H + HCl H + + Cl - CH 3 COOH
Teorie kyselin a zásad poznámky 5A GVN 13 června 2007 Arrheniova teorie platná pouze pro vodní roztoky kyseliny jsou látky schopné ve vodném roztoku odštěpit vodíkový kation H + HCl H + + Cl - CH 3 COOH
Složení soustav (roztoky, koncentrace látkového množství)
 VZOROVÉ PŘÍKLADY Z CHEMIE A DOPORUČENÁ LITERATURA pro přípravu k přijímací zkoušce studijnímu oboru Nanotechnologie na VŠB TU Ostrava Doporučená literatura z chemie: Prakticky jakákoliv celostátní učebnice
VZOROVÉ PŘÍKLADY Z CHEMIE A DOPORUČENÁ LITERATURA pro přípravu k přijímací zkoušce studijnímu oboru Nanotechnologie na VŠB TU Ostrava Doporučená literatura z chemie: Prakticky jakákoliv celostátní učebnice
Základy Mössbauerovy spektroskopie. Libor Machala
 Základy Mössbauerovy spektroskopie Libor Machala Rudolf L. Mössbauer 1958: jev bezodrazové rezonanční absorpce záření gama atomovým jádrem 1961: Nobelova cena Analogie s rezonanční absorpcí akustických
Základy Mössbauerovy spektroskopie Libor Machala Rudolf L. Mössbauer 1958: jev bezodrazové rezonanční absorpce záření gama atomovým jádrem 1961: Nobelova cena Analogie s rezonanční absorpcí akustických
Základy NIR spektrometrie a její praktické využití
 Nicolet CZ s.r.o. The world leader in serving science Základy NIR spektrometrie a její praktické využití NIR praktická metoda molekulové spektroskopie, nahrazující pracnější, časově náročnější a dražší
Nicolet CZ s.r.o. The world leader in serving science Základy NIR spektrometrie a její praktické využití NIR praktická metoda molekulové spektroskopie, nahrazující pracnější, časově náročnější a dražší
PÍSEMNÁ ČÁST PŘIJÍMACÍ ZKOUŠKY Z CHEMIE bakalářský studijní obor Bioorganická chemie 2011
 Kód uchazeče:... Datum:... PÍSEMNÁ ČÁST PŘIJÍMACÍ ZKUŠKY Z CHEMIE bakalářský studijní obor Bioorganická chemie 2011 30 otázek maximum: 60 bodů čas: 60 minut 1. Napište názvy anorganických sloučenin: (4
Kód uchazeče:... Datum:... PÍSEMNÁ ČÁST PŘIJÍMACÍ ZKUŠKY Z CHEMIE bakalářský studijní obor Bioorganická chemie 2011 30 otázek maximum: 60 bodů čas: 60 minut 1. Napište názvy anorganických sloučenin: (4
INTERAKCE IONTŮ S POVRCHY II.
 Úvod do fyziky tenkých vrstev a povrchů INTERAKCE IONTŮ S POVRCHY II. Metody IBA (Ion Beam Analysis): pružný rozptyl nabitých částic (RBS), detekce odražených atomů (ERDA), metoda PIXE, Spektroskopie rozptýlených
Úvod do fyziky tenkých vrstev a povrchů INTERAKCE IONTŮ S POVRCHY II. Metody IBA (Ion Beam Analysis): pružný rozptyl nabitých částic (RBS), detekce odražených atomů (ERDA), metoda PIXE, Spektroskopie rozptýlených
2.3 CHEMICKÁ VAZBA. Molekula bílého fosforu P 4 a kyseliny sírové H 2 SO 4. Předpona piko p je dílčí jednotkou a udává velikost m.
 2.3 CHEMICKÁ VAZBA Spojováním dvou a více atomů vznikají molekuly. Jestliže dochází ke spojování výhradně atomů téhož chemického prvku, pak se jedná o molekuly daného prvku (vodíku H 2, dusíku N 2, ozonu
2.3 CHEMICKÁ VAZBA Spojováním dvou a více atomů vznikají molekuly. Jestliže dochází ke spojování výhradně atomů téhož chemického prvku, pak se jedná o molekuly daného prvku (vodíku H 2, dusíku N 2, ozonu
STUDIUM POVRCHOVÉ MODIFIKACE STŘÍBRNÝCH NANOČÁSTIC A JEJICH MOŽNÉ VYUŽITÍ V ANALYTICKÉ CHEMII
 STUDIUM POVRCHOVÉ MODIFIKACE STŘÍBRÝCH AOČÁSTIC A JEJICH MOŽÉ VYUŽITÍ V AALYTICKÉ CHEMII Pavel Žvátora, Kamil Záruba, Pavel Řezanka, Vladimír Král Ústav analytické chemie, Fakulta chemicko-inženýrská,
STUDIUM POVRCHOVÉ MODIFIKACE STŘÍBRÝCH AOČÁSTIC A JEJICH MOŽÉ VYUŽITÍ V AALYTICKÉ CHEMII Pavel Žvátora, Kamil Záruba, Pavel Řezanka, Vladimír Král Ústav analytické chemie, Fakulta chemicko-inženýrská,
Chemické veličiny, vztahy mezi nimi a chemické výpočty
 SBÍRKA ŘEŠENÝCH PŘÍKLADŮ PRO PROJEKT PŘÍRODNÍ VĚDY AKTIVNĚ A INTERAKTIVNĚ CZ.1.07/1.1.24/01.0040 Chemické veličiny, vztahy mezi nimi a chemické výpočty Mgr. Jana Žůrková, 2013, 20 stran Obsah 1. Veličiny
SBÍRKA ŘEŠENÝCH PŘÍKLADŮ PRO PROJEKT PŘÍRODNÍ VĚDY AKTIVNĚ A INTERAKTIVNĚ CZ.1.07/1.1.24/01.0040 Chemické veličiny, vztahy mezi nimi a chemické výpočty Mgr. Jana Žůrková, 2013, 20 stran Obsah 1. Veličiny
LEKCE 1b. Základní parametry 1 H NMR spekter. Symetrie v NMR spektrech: homotopické, enantiotopické, diastereotopické protony (skupiny)*
 Základní parametry 1 NMR spekter LEKCE 1b Symetrie v NMR spektrech: homotopické, enantiotopické, diastereotopické protony (skupiny)* 3.5 3.0 2.5 2.0 1.5 Základní parametry 1 NMR spekter Počet signálů ve
Základní parametry 1 NMR spekter LEKCE 1b Symetrie v NMR spektrech: homotopické, enantiotopické, diastereotopické protony (skupiny)* 3.5 3.0 2.5 2.0 1.5 Základní parametry 1 NMR spekter Počet signálů ve
Struktura proteinů. - testík na procvičení. Vladimíra Kvasnicová
 Struktura proteinů - testík na procvičení Vladimíra Kvasnicová Mezi proteinogenní aminokyseliny patří a) kyselina asparagová b) kyselina glutarová c) kyselina acetoctová d) kyselina glutamová Mezi proteinogenní
Struktura proteinů - testík na procvičení Vladimíra Kvasnicová Mezi proteinogenní aminokyseliny patří a) kyselina asparagová b) kyselina glutarová c) kyselina acetoctová d) kyselina glutamová Mezi proteinogenní
CHEMIE - Úvod do organické chemie
 Název školy Číslo projektu Autor Název šablony Název DUMu Stupeň a typ vzdělávání Vzdělávací oblast Vzdělávací obor Vzdělávací okruh Druh učebního materiálu Cílová skupina Anotace SŠHS Kroměříž CZ.1.07/1.5.00/34.0911
Název školy Číslo projektu Autor Název šablony Název DUMu Stupeň a typ vzdělávání Vzdělávací oblast Vzdělávací obor Vzdělávací okruh Druh učebního materiálu Cílová skupina Anotace SŠHS Kroměříž CZ.1.07/1.5.00/34.0911
Nicolet CZ s.r.o. Porovnání infračervené a Ramanovy spektroskopie. Typické aplikace těchto technik. The world leader in serving science
 Nicolet CZ s.r.o. Porovnání infračervené a Ramanovy spektroskopie. The world leader in serving science Typické aplikace těchto technik. Základní princip Infračervená a Ramanova spektroskopie nedestruktivní
Nicolet CZ s.r.o. Porovnání infračervené a Ramanovy spektroskopie. The world leader in serving science Typické aplikace těchto technik. Základní princip Infračervená a Ramanova spektroskopie nedestruktivní
STANOVENÍ CHLORIDŮ. Odměrné argentometrické stanovení chloridů podle Mohra
 STANOVENÍ CHLORIDŮ Odměrné argentometrické stanovení chloridů podle Mohra Cíl práce Stanovte titr odměrného standardního roztoku dusičnanu stříbrného titrací 5 ml standardního srovnávacího roztoku chloridu
STANOVENÍ CHLORIDŮ Odměrné argentometrické stanovení chloridů podle Mohra Cíl práce Stanovte titr odměrného standardního roztoku dusičnanu stříbrného titrací 5 ml standardního srovnávacího roztoku chloridu
APLIKACE POKROČILÝCH METOD IČ SPEKTROSKOPIE
 APLIKACE POKROČILÝCH METOD IČ SPEKTROSKOPIE PŘI ANALÝZE MINERALOGICKÉHO SLOŽENÍ HORNIN Ing. Lenka VACULÍKOVÁ, Ph.D. Ústav geoniky AV ČR, v.v.i. Ostrava Ing. Michal RITZ, Ph.D. Katedra analytické chemie
APLIKACE POKROČILÝCH METOD IČ SPEKTROSKOPIE PŘI ANALÝZE MINERALOGICKÉHO SLOŽENÍ HORNIN Ing. Lenka VACULÍKOVÁ, Ph.D. Ústav geoniky AV ČR, v.v.i. Ostrava Ing. Michal RITZ, Ph.D. Katedra analytické chemie
NMR spektroskopie. Úvod
 NMR spektroskopie Úvod Zkratka NMR znamená Nukleární Magnetická Rezonance. Jde o analytickou metodu, která na základě absorpce radiofrekvenčního záření vzorkem umístěným v silném magnetickém poli poskytuje
NMR spektroskopie Úvod Zkratka NMR znamená Nukleární Magnetická Rezonance. Jde o analytickou metodu, která na základě absorpce radiofrekvenčního záření vzorkem umístěným v silném magnetickém poli poskytuje
Základní chemické pojmy
 MZ CHEMIE 2015 MO 1 Základní chemické pojmy Atom, molekula, prvek, protonové číslo. Sloučenina, chemicky čistá látka, směs, dělení směsí. Relativní atomová hmotnost, molekulová hmotnost, atomová hmotnostní
MZ CHEMIE 2015 MO 1 Základní chemické pojmy Atom, molekula, prvek, protonové číslo. Sloučenina, chemicky čistá látka, směs, dělení směsí. Relativní atomová hmotnost, molekulová hmotnost, atomová hmotnostní
Sorpční charakteristiky půdy stanovení KVK podle Bowera, stanovení hydrolytické acidity, výpočet S,V
 Sorpční charakteristiky půdy stanovení KVK podle Bowera, stanovení hydrolytické acidity, výpočet S,V Sorpční vlastnosti půdy sorpce půdy schopnost půdy zadržovat ve svém sorpčním komplexu prvky a živiny,
Sorpční charakteristiky půdy stanovení KVK podle Bowera, stanovení hydrolytické acidity, výpočet S,V Sorpční vlastnosti půdy sorpce půdy schopnost půdy zadržovat ve svém sorpčním komplexu prvky a živiny,
Základní parametry absorpčního spektra, vliv přístrojové funkce (spektrální šířky štěrbiny), vliv polohy kyvety a vlastní fluorescence vzorku
 Základní parametry absorpčního spektra, vliv přístrojové funkce (spektrální šířky štěrbiny), vliv polohy kyvety a vlastní fluorescence vzorku A. ZADÁNÍ 1. Naučte se ovládat spektrofotometr Unicam UV55
Základní parametry absorpčního spektra, vliv přístrojové funkce (spektrální šířky štěrbiny), vliv polohy kyvety a vlastní fluorescence vzorku A. ZADÁNÍ 1. Naučte se ovládat spektrofotometr Unicam UV55
SEZNAM PŘÍLOH: Popis půdního profilu kambizem litická Popis půdního profilu kambizem modální Popis půdního profilu černozem luvická
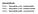 SEZNAM PŘÍLOH: Příloha 1: Popis půdního profilu kambizem litická Příloha 2: Popis půdního profilu kambizem modální Příloha 3: Popis půdního profilu černozem luvická Příloha 1: Popis půdního profilu kambizem
SEZNAM PŘÍLOH: Příloha 1: Popis půdního profilu kambizem litická Příloha 2: Popis půdního profilu kambizem modální Příloha 3: Popis půdního profilu černozem luvická Příloha 1: Popis půdního profilu kambizem
STUDIUM AGREGAČNÍHO CHOVÁNÍ HUMINOVÝCH KYSELIN V PROSTŘEDÍ CIZORODÝCH LÁTEK
 VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ BRNO UNIVERSITY OF TECHNOLOGY FAKULTA CHEMICKÁ ÚSTAV CHEMIE POTRAVIN A BIOTECHNOLOGIÍ FACULTY OF CHEMISTRY INSTITUTE OF FOOD SCIENCE AND BIOTECHNOLOGY STUDIUM AGREGAČNÍHO
VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ BRNO UNIVERSITY OF TECHNOLOGY FAKULTA CHEMICKÁ ÚSTAV CHEMIE POTRAVIN A BIOTECHNOLOGIÍ FACULTY OF CHEMISTRY INSTITUTE OF FOOD SCIENCE AND BIOTECHNOLOGY STUDIUM AGREGAČNÍHO
INFRAČERVENÁ A RAMANOVA SPEKTROMETRIE
 INFRAČERVENÁ A RAMANOVA SPEKTROMETRIE (c) -2008 INFRAČERVENÁ SPEKTROMETRIE 1 INFRAČERVENÉ ZÁŘENÍ Infračervené (IR) záření: vlnočty 13000 10 cm -1, což odpovídá λ 0,78 1000 µm. DĚLENÍ: blízká IR oblast
INFRAČERVENÁ A RAMANOVA SPEKTROMETRIE (c) -2008 INFRAČERVENÁ SPEKTROMETRIE 1 INFRAČERVENÉ ZÁŘENÍ Infračervené (IR) záření: vlnočty 13000 10 cm -1, což odpovídá λ 0,78 1000 µm. DĚLENÍ: blízká IR oblast
Stereochemie 7. Přednáška 7
 Stereochemie 7 Přednáška 7 1 ptická čistota p = [ ]poz [ ]max x 100 = ee = [R] - [S] [R] + [S] x 100 p optická čistota [R], [S] molární frakce R a S enantiomerů ee + 100 %R = ee + %S = ee + 100 - %R =
Stereochemie 7 Přednáška 7 1 ptická čistota p = [ ]poz [ ]max x 100 = ee = [R] - [S] [R] + [S] x 100 p optická čistota [R], [S] molární frakce R a S enantiomerů ee + 100 %R = ee + %S = ee + 100 - %R =
1. ročník Počet hodin
 SOUSTAVY LÁTEK A JEJICH SLOŽENÍ rozdělení přírodních látek a vlastnosti chemických látek soustavy látek a jejich složení STAVBA ATOMU historie pohledu na atom složení a struktura atomu stavba atomu VELIČINY
SOUSTAVY LÁTEK A JEJICH SLOŽENÍ rozdělení přírodních látek a vlastnosti chemických látek soustavy látek a jejich složení STAVBA ATOMU historie pohledu na atom složení a struktura atomu stavba atomu VELIČINY
STŘEDNÍ ODBORNÁ ŠKOLA a STŘEDNÍ ODBORNÉ UČILIŠTĚ, Česká Lípa, 28. října 2707, příspěvková organizace
 Název školy: Číslo a název projektu: Číslo a název šablony klíčové aktivity: Označení materiálu: Typ materiálu: STŘEDNÍ ODBORNÁ ŠKOLA a STŘEDNÍ ODBORNÉ UČILIŠTĚ, Česká Lípa, 28. října 2707, příspěvková
Název školy: Číslo a název projektu: Číslo a název šablony klíčové aktivity: Označení materiálu: Typ materiálu: STŘEDNÍ ODBORNÁ ŠKOLA a STŘEDNÍ ODBORNÉ UČILIŠTĚ, Česká Lípa, 28. října 2707, příspěvková
