Bioenergetika Bioenergetics
|
|
|
- Renáta Hájková
- před 8 lety
- Počet zobrazení:
Transkript
1 Bioenergetika Bioenergetics Tomáš Kučera 2011 Tisková verze Print version Prezentace Presentation
2 Bioenergetika Slide 1a Bioenergetika
3 Bioenergetika Slide 1b Bioenergetika jak organismy získávají, přeměňují, ukládají a využívají energii
4 Bioenergetika Slide 2a Termodynamika
5 Bioenergetika Slide 2b Termodynamika vzájemné přeměny různých druhů energie směřování fyzikálních a chemických pochodů měřítko samovolnosti (uskutečnitelnosti dějů) rovnovážné stavy
6 Bioenergetika Slide 2c Termodynamika vzájemné přeměny různých druhů energie směřování fyzikálních a chemických pochodů měřítko samovolnosti (uskutečnitelnosti dějů) rovnovážné stavy Základní pojmy
7 Bioenergetika Slide 2d Termodynamika vzájemné přeměny různých druhů energie směřování fyzikálních a chemických pochodů měřítko samovolnosti (uskutečnitelnosti dějů) rovnovážné stavy Základní pojmy systém (soustava) libovolná část prostoru uvažovaná odděleně od okolí
8 Bioenergetika Slide 2e Termodynamika vzájemné přeměny různých druhů energie směřování fyzikálních a chemických pochodů měřítko samovolnosti (uskutečnitelnosti dějů) rovnovážné stavy Základní pojmy systém (soustava) libovolná část prostoru uvažovaná odděleně od okolí izolovaný nevyměňuje s okolím hmotu ani energii uzavřený vyměňuje s okolím jen energii, nikoli hmotu otevřený vyměňuje s okolím hmotu i energii
9 Bioenergetika Slide 2f Termodynamika vzájemné přeměny různých druhů energie směřování fyzikálních a chemických pochodů měřítko samovolnosti (uskutečnitelnosti dějů) rovnovážné stavy Základní pojmy systém (soustava) libovolná část prostoru uvažovaná odděleně od okolí izolovaný nevyměňuje s okolím hmotu ani energii uzavřený vyměňuje s okolím jen energii, nikoli hmotu otevřený vyměňuje s okolím hmotu i energii ŽIVÉ SYSTÉMY JSOU VŽDY OTEVŘENÉ!
10 Bioenergetika Slide 2g Termodynamika vzájemné přeměny různých druhů energie směřování fyzikálních a chemických pochodů měřítko samovolnosti (uskutečnitelnosti dějů) rovnovážné stavy Základní pojmy systém (soustava) libovolná část prostoru uvažovaná odděleně od okolí izolovaný nevyměňuje s okolím hmotu ani energii uzavřený vyměňuje s okolím jen energii, nikoli hmotu otevřený vyměňuje s okolím hmotu i energii okolí zbytek vesmíru ŽIVÉ SYSTÉMY JSOU VŽDY OTEVŘENÉ!
11 Bioenergetika Slide 3a První věta termodynamiky
12 Bioenergetika Slide 3b První věta termodynamiky Energii nelze vytvořit ani zničit.
13 Bioenergetika Slide 3c První věta termodynamiky Energii nelze vytvořit ani zničit. U = U konečná U počáteční = Q W U vnitřní energie soustavy Q teplo přijaté soustavou od okolí W práce vykonaná soustavou na okolí
14 Bioenergetika Slide 3d První věta termodynamiky Energii nelze vytvořit ani zničit. U = U konečná U počáteční = Q W U vnitřní energie soustavy Q teplo přijaté soustavou od okolí W práce vykonaná soustavou na okolí izochorický děj (V = konst.)
15 Bioenergetika Slide 3e První věta termodynamiky Energii nelze vytvořit ani zničit. U = U konečná U počáteční = Q W U vnitřní energie soustavy Q teplo přijaté soustavou od okolí W práce vykonaná soustavou na okolí izochorický děj (V = konst.) W = p dv U = Q V
16 Bioenergetika Slide 3f První věta termodynamiky Energii nelze vytvořit ani zničit. U = U konečná U počáteční = Q W U vnitřní energie soustavy Q teplo přijaté soustavou od okolí W práce vykonaná soustavou na okolí izochorický děj (V = konst.) izobarický děj (p = konst.) W = p dv U = Q V
17 Bioenergetika Slide 3g První věta termodynamiky Energii nelze vytvořit ani zničit. U = U konečná U počáteční = Q W U vnitřní energie soustavy Q teplo přijaté soustavou od okolí W práce vykonaná soustavou na okolí izochorický děj (V = konst.) izobarický děj (p = konst.) W = p dv U = Q V U = Q p (pv) U + pv = H H = (U + pv) = Q p p tlak, V objem, H enthalpie
18 Bioenergetika Slide 4a Druhá věta termodynamiky
19 Bioenergetika Slide 4b Druhá věta termodynamiky Nelze sestrojit periodicky pracující tepelný stroj, který by dodával okolí práci na úkor tepla odebíraného jedinému tepelnému rezervoáru.
20 Bioenergetika Slide 4c Druhá věta termodynamiky Nelze sestrojit periodicky pracující tepelný stroj, který by dodával okolí práci na úkor tepla odebíraného jedinému tepelnému rezervoáru. Teplo nemůže při styku dvou těles různých teplot samovolně přecházet z tělesa chladnějšího na těleso teplejší.
21 Bioenergetika Slide 4d Druhá věta termodynamiky Nelze sestrojit periodicky pracující tepelný stroj, který by dodával okolí práci na úkor tepla odebíraného jedinému tepelnému rezervoáru. Teplo nemůže při styku dvou těles různých teplot samovolně přecházet z tělesa chladnějšího na těleso teplejší. dq T 0
22 Bioenergetika Slide 4e Druhá věta termodynamiky Nelze sestrojit periodicky pracující tepelný stroj, který by dodával okolí práci na úkor tepla odebíraného jedinému tepelnému rezervoáru. Teplo nemůže při styku dvou těles různých teplot samovolně přecházet z tělesa chladnějšího na těleso teplejší. dq T 0 entropie S = Q T
23 Bioenergetika Slide 4f Druhá věta termodynamiky Nelze sestrojit periodicky pracující tepelný stroj, který by dodával okolí práci na úkor tepla odebíraného jedinému tepelnému rezervoáru. Teplo nemůže při styku dvou těles různých teplot samovolně přecházet z tělesa chladnějšího na těleso teplejší. dq T 0 entropie S = Q T S = k lnp
24 Bioenergetika Slide 4g Druhá věta termodynamiky Nelze sestrojit periodicky pracující tepelný stroj, který by dodával okolí práci na úkor tepla odebíraného jedinému tepelnému rezervoáru. Teplo nemůže při styku dvou těles různých teplot samovolně přecházet z tělesa chladnějšího na těleso teplejší. dq T 0 entropie S = Q T S = k lnp ukazatel samovolnosti děje v adiabaticky izolovaných soustavách
25 Bioenergetika Slide 4h Druhá věta termodynamiky Nelze sestrojit periodicky pracující tepelný stroj, který by dodával okolí práci na úkor tepla odebíraného jedinému tepelnému rezervoáru. Teplo nemůže při styku dvou těles různých teplot samovolně přecházet z tělesa chladnějšího na těleso teplejší. dq T 0 entropie S = Q T S = k lnp ukazatel samovolnosti děje v adiabaticky izolovaných soustavách S soustava + S okolí = S vesmír > 0
26 Bioenergetika Slide 5a Gibbsova (volná) energie G = H TS G = H T S = Q p T S
27 Bioenergetika Slide 5b Gibbsova (volná) energie G = H TS G = H T S = Q p T S koná-li systém práci, je G = Q p T S + W T S Q p G W
28 Bioenergetika Slide 5c Gibbsova (volná) energie G = H TS G = H T S = Q p T S koná-li systém práci, je G = Q p T S + W T S Q p G W v biol. systému objemová práce zanedbatelná G = max. práce
29 Bioenergetika Slide 5d Gibbsova (volná) energie G = H TS G = H T S = Q p T S koná-li systém práci, je G = Q p T S + W T S Q p G W v biol. systému objemová práce zanedbatelná G = max. práce reálný děj není nikdy reversibilní G < W Práci vloženou do systému nelze celou získat zpět.
30 Bioenergetika Slide 5e Gibbsova (volná) energie G = H TS G = H T S = Q p T S koná-li systém práci, je G = Q p T S + W T S Q p G W v biol. systému objemová práce zanedbatelná G = max. práce reálný děj není nikdy reversibilní G < W Práci vloženou do systému nelze celou získat zpět. Úbytek G je roven maximální práci, kterou může systém odevzdat při izotermicko-izobarickém ději do okolí.
31 Bioenergetika Slide 5f Gibbsova (volná) energie G = H TS G = H T S = Q p T S koná-li systém práci, je G = Q p T S + W T S Q p G W v biol. systému objemová práce zanedbatelná G = max. práce reálný děj není nikdy reversibilní G < W Práci vloženou do systému nelze celou získat zpět. Úbytek G je roven maximální práci, kterou může systém odevzdat při izotermicko-izobarickém ději do okolí. rovnováha: G = 0
32 Bioenergetika Slide 5g Gibbsova (volná) energie G = H TS G = H T S = Q p T S koná-li systém práci, je G = Q p T S + W T S Q p G W v biol. systému objemová práce zanedbatelná G = max. práce reálný děj není nikdy reversibilní G < W Práci vloženou do systému nelze celou získat zpět. Úbytek G je roven maximální práci, kterou může systém odevzdat při izotermicko-izobarickém ději do okolí. rovnováha: G = 0 samovolný (exergonický) děj: G < 0 (může konat práci)
33 Bioenergetika Slide 5h Gibbsova (volná) energie G = H TS G = H T S = Q p T S koná-li systém práci, je G = Q p T S + W T S Q p G W v biol. systému objemová práce zanedbatelná G = max. práce reálný děj není nikdy reversibilní G < W Práci vloženou do systému nelze celou získat zpět. Úbytek G je roven maximální práci, kterou může systém odevzdat při izotermicko-izobarickém ději do okolí. rovnováha: G = 0 samovolný (exergonický) děj: G < 0 (může konat práci) endergonický děj: G > 0
34 Bioenergetika Slide 6a Gibbsova energie jeden z tzv. termodynamických potenciálů
35 Bioenergetika Slide 6b Gibbsova energie jeden z tzv. termodynamických potenciálů žádná informace o rychlosti ta dána mechanismem
36 Bioenergetika Slide 6c Gibbsova energie jeden z tzv. termodynamických potenciálů žádná informace o rychlosti ta dána mechanismem (ne)možnost děje dána jen počátečním a konečným stavem
37 Bioenergetika Slide 6d Gibbsova energie jeden z tzv. termodynamických potenciálů žádná informace o rychlosti ta dána mechanismem (ne)možnost děje dána jen počátečním a konečným stavem katalyzátor (enzym) může urychlit dosažení rovnováhy, ale ne změnit její stav
38 Bioenergetika Slide 6e Gibbsova energie jeden z tzv. termodynamických potenciálů žádná informace o rychlosti ta dána mechanismem (ne)možnost děje dána jen počátečním a konečným stavem katalyzátor (enzym) může urychlit dosažení rovnováhy, ale ne změnit její stav možnost spřažení
39 Bioenergetika Slide 6f Gibbsova energie jeden z tzv. termodynamických potenciálů žádná informace o rychlosti ta dána mechanismem (ne)možnost děje dána jen počátečním a konečným stavem katalyzátor (enzym) může urychlit dosažení rovnováhy, ale ne změnit její stav možnost spřažení závisí na teplotě: rovnováha: T = H S
40 Bioenergetika Slide 6g Gibbsova energie jeden z tzv. termodynamických potenciálů žádná informace o rychlosti ta dána mechanismem (ne)možnost děje dána jen počátečním a konečným stavem katalyzátor (enzym) může urychlit dosažení rovnováhy, ale ne změnit její stav možnost spřažení závisí na teplotě: rovnováha: T = H S
41 Bioenergetika Slide 7a Chemické rovnováhy pro reakci aa + bb cc + dd G = G 0 + RT ln [C]c [D] d [A] a [B] b G 0... standardní změna G dané reakce
42 Bioenergetika Slide 7b Chemické rovnováhy pro reakci aa + bb cc + dd G = G 0 + RT ln [C]c [D] d [A] a [B] b G 0... standardní změna G dané reakce konstantní člen závisí jen na konkrétní reakci
43 Bioenergetika Slide 7c Chemické rovnováhy pro reakci aa + bb cc + dd G = G 0 + RT ln [C]c [D] d G 0... standardní změna G dané reakce [A] a [B] b konstantní člen závisí jen na konkrétní reakci proměnný člen závisí na teplotě a koncentracích reaktantů a produktů
44 Bioenergetika Slide 7d Chemické rovnováhy pro reakci aa + bb cc + dd G = G 0 + RT ln [C]c [D] d G 0... standardní změna G dané reakce [A] a [B] b konstantní člen závisí jen na konkrétní reakci proměnný člen závisí na teplotě a koncentracích reaktantů a produktů rovnováha: G = 0 G 0 = RT ln K eq K eq = [C]c [D] d [A] a [B] b = e G0 RT
45 Bioenergetika Slide 7e Chemické rovnováhy pro reakci aa + bb cc + dd G = G 0 + RT ln [C]c [D] d G 0... standardní změna G dané reakce [A] a [B] b konstantní člen závisí jen na konkrétní reakci proměnný člen závisí na teplotě a koncentracích reaktantů a produktů rovnováha: G = 0 G 0 = RT ln K eq K eq = [C]c [D] d [A] a [B] b = e G0 RT G 0 a K eq v přímém vztahu
46 Bioenergetika Slide 7f Chemické rovnováhy pro reakci aa + bb cc + dd G = G 0 + RT ln [C]c [D] d G 0... standardní změna G dané reakce [A] a [B] b konstantní člen závisí jen na konkrétní reakci proměnný člen závisí na teplotě a koncentracích reaktantů a produktů rovnováha: G = 0 G 0 = RT ln K eq K eq = [C]c [D] d [A] a [B] b = e G0 RT G 0 a K eq v přímém vztahu 10násobná změna K eq změní G 0 o 5.7 kj/mol
47 Bioenergetika Slide 8a Změna Gibbsovy energie G 0 = G 0 f (products) G 0 f (reactants) G 0 f... G0 syntézy z prvků
48 Bioenergetika Slide 8b Změna Gibbsovy energie G 0 = G 0 f (products) G 0 f (reactants) G 0 f... G0 syntézy z prvků
49 Bioenergetika Změna Gibbsovy energie Slide 9a standardní stav
50 Bioenergetika Změna Gibbsovy energie Slide 9b standardní stav aktivita 1 mol/l
51 Bioenergetika Změna Gibbsovy energie Slide 9c standardní stav aktivita 1 mol/l 25 C
52 Bioenergetika Změna Gibbsovy energie Slide 9d standardní stav aktivita 1 mol/l 25 C 1 atm
53 Bioenergetika Slide 9e standardní stav aktivita 1 mol/l 25 C 1 atm Změna Gibbsovy energie biochemický standardní stav
54 Bioenergetika Slide 9f standardní stav aktivita 1 mol/l 25 C 1 atm Změna Gibbsovy energie biochemický standardní stav aktivita vody = 1
55 Bioenergetika Slide 9g standardní stav aktivita 1 mol/l 25 C 1 atm Změna Gibbsovy energie biochemický standardní stav aktivita vody = 1 ph = 7
56 Bioenergetika Slide 9h standardní stav aktivita 1 mol/l 25 C 1 atm Změna Gibbsovy energie biochemický standardní stav aktivita vody = 1 ph = 7 látky podléhající acidobazické disociaci: c = celková c všech forem při ph = 7
57 Bioenergetika Slide 10a Spřažené reakce
58 Bioenergetika Slide 10b Spřažené reakce A + B C + D G 1 D + E F + G G 2
59 Bioenergetika Slide 10c Spřažené reakce A + B C + D G 1 D + E F + G G 2 A + B + E C + F + G G 3 = G 1 + G 2 < 0
60 Bioenergetika Slide 10d Spřažené reakce A + B C + D G 1 D + E F + G G 2 A + B + E C + F + G G 3 = G 1 + G 2 < 0 ΔG 0 (kj.mol -1 ) Endergonická reakce: glukosa + P i glukosa-6-fosfát + H 2 O +13,8 Exergonická reakce: ATP + H 2 O ADP + P i 30,5 Spřažená reakce: glukosa + ATP glukosa-6-fosfát + ADP 16,7
61 Bioenergetika Slide 11a Redoxní potenciál
62 Bioenergetika Slide 11b Redoxní potenciál Aox n+ + B red A red + B n+ ox
63 Bioenergetika Slide 11c Redoxní potenciál Aox n+ + B red A red + B n+ ox
64 Bioenergetika Slide 11d Redoxní potenciál Aox n+ + B red A red + B n+ ox G = G 0 + RT ln [A red][b n+ ox] [A n+ ox ][B red ]
65 Bioenergetika Slide 11e Redoxní potenciál Aox n+ + B red A red + B n+ ox G = G 0 + RT ln [A red][b n+ ox] [A n+ ox ][B red ] G = nf E
66 Bioenergetika Slide 11f Redoxní potenciál Aox n+ + B red A red + B n+ ox Nernst : E = E 0 RT G = G 0 + RT ln [A red][b n+ ox] [A n+ ox ][B red ] nf G = nf E [red] ln [ox] E = E0 RT nf ln [A red][b n+ ox ] [Aox n+ ][B red ]
67 Bioenergetika Slide 12a E jako energetická škála Redoxní potenciál
68 Bioenergetika Redoxní potenciál Slide 12b E jako energetická škála Redukovaná forma Oxidovaná forma E 0 (V) ΔG 0 acetaldehyd acetát -0,60 hodnoty vyšší H 2 2H + -0,42 (reduktans) isocitrát 2-oxoglutarát + CO 2-0,38 glutathion-sh glutathion-ss -0,34 NADH + H + NAD + -0,32 glyceraldehyd-3-fosfát + H 3 P0 4 1,3-bisfosfoglycerát -0,28 FADH 2 FAD -0,20 laktát pyruvát -0,19 malát oxalacetát -0,17 cytochrom b (Fe 2+ ) cytochrom b (Fe 3+ ) 0,00 sukcinát fumarát +0,03 dihydroubichinon ubichinon +0,10 cytochrom c (Fe 2+ ) cytochrom c (Fe 3+ ) +0,26 +ne ne H 2 O 2 O 2 +0,29 + hodnoty H 2 O ½ O 2 +0,82 (oxidans) nižší exergonický děj endergonický děj
69 Bioenergetika Redoxní potenciál Slide 13a E 0 = 0V pro standardní vodíkový poločlánek (elektrodu)
70 Bioenergetika Redoxní potenciál Slide 13b E 0 = 0V pro standardní vodíkový poločlánek (elektrodu) H + při ph 0, 25 C, 1 atm v rovnováze s elektrodou z Pt černi sycenou H 2
71 Bioenergetika Redoxní potenciál Slide 13c E 0 = 0V pro standardní vodíkový poločlánek (elektrodu) H + při ph 0, 25 C, 1 atm v rovnováze s elektrodou z Pt černi sycenou H 2 ph = 7 E 0 = 0.421V
72 Bioenergetika Slide 14a NAD(P) + NikotinamidAdeninDinukleotid(fosfát)
73 Bioenergetika Slide 14b NAD(P) + NikotinamidAdeninDinukleotid(fosfát) Redoxní reakce NAD(P) + NAD(P)H + H +
74 Bioenergetika Slide 15a Makroergické sloučeniny jejich hydrolýza pohání endergonické reakce
75 Bioenergetika Slide 15b Makroergické sloučeniny jejich hydrolýza pohání endergonické reakce obsahují makroergickou vazbu
76 Bioenergetika Slide 15c Makroergické sloučeniny jejich hydrolýza pohání endergonické reakce obsahují makroergickou vazbu ATP centrální role (univerzální energetická měna buňky)
77 Bioenergetika Slide 15d Makroergické sloučeniny jejich hydrolýza pohání endergonické reakce obsahují makroergickou vazbu ATP centrální role (univerzální energetická měna buňky) 3 fosfátové skupiny vázané 1 fosfoesterovou a 2 fosfoanhydridovými vazbami
78 Bioenergetika Slide 15e Makroergické sloučeniny jejich hydrolýza pohání endergonické reakce obsahují makroergickou vazbu ATP centrální role (univerzální energetická měna buňky) 3 fosfátové skupiny vázané 1 fosfoesterovou a 2 fosfoanhydridovými vazbami
79 Bioenergetika Slide 16a ATP R 1 O P + R 2 OH R 1 O H + R 2 OP reakce přenosu fosforylu obrovský metabolický význam
80 Bioenergetika ATP Slide 16b R 1 O P + R 2 OH R 1 O H + R 2 OP reakce přenosu fosforylu obrovský metabolický význam ATP + H 2 O ADP + P i G 0 = 30, 5 kj mol 1 ATP + H 2 O AMP + PP i G 0 = 45, 6 kj mol 1
81 Bioenergetika ATP Slide 16c R 1 O P + R 2 OH R 1 O H + R 2 OP reakce přenosu fosforylu obrovský metabolický význam ATP + H 2 O ADP + P i G 0 = 30, 5 kj mol 1 ATP + H 2 O AMP + PP i G 0 = 45, 6 kj mol 1 ATP se obnovuje za pomoci ještě exergoničtějších reakcí
82 Bioenergetika ATP Slide 16d R 1 O P + R 2 OH R 1 O H + R 2 OP reakce přenosu fosforylu obrovský metabolický význam ATP + H 2 O ADP + P i G 0 = 30, 5 kj mol 1 ATP + H 2 O AMP + PP i G 0 = 45, 6 kj mol 1 ATP se obnovuje za pomoci ještě exergoničtějších reakcí kinetická stabilita, termodynamická nestabilita (vysoké G 0 )
83 Bioenergetika Makroergická vazba Slide 17a
84 Bioenergetika Makroergická vazba Slide 17b fosfoanhydridy
85 Bioenergetika Makroergická vazba Slide 17c fosfoanhydridy rezonanční stabilizace
86 Bioenergetika Makroergická vazba Slide 17d fosfoanhydridy rezonanční stabilizace elektrostatická repulze
87 Bioenergetika Makroergická vazba Slide 17e fosfoanhydridy rezonanční stabilizace elektrostatická repulze
88 Bioenergetika Makroergická vazba Slide 17f fosfoanhydridy rezonanční stabilizace elektrostatická repulze vyšší solvatační energie produktů hydrolýzy
89 Bioenergetika Makroergická vazba Slide 17g fosfoanhydridy rezonanční stabilizace elektrostatická repulze vyšší solvatační energie produktů hydrolýzy ostatní anhydridy
90 Bioenergetika Makroergická vazba Slide 17h fosfoanhydridy rezonanční stabilizace elektrostatická repulze vyšší solvatační energie produktů hydrolýzy ostatní anhydridy fosfosulfáty
91 Bioenergetika Makroergická vazba Slide 17i fosfoanhydridy rezonanční stabilizace elektrostatická repulze vyšší solvatační energie produktů hydrolýzy ostatní anhydridy fosfosulfáty acylfosfáty
92 Bioenergetika Makroergická vazba Slide 17j fosfoanhydridy rezonanční stabilizace elektrostatická repulze vyšší solvatační energie produktů hydrolýzy ostatní anhydridy fosfosulfáty acylfosfáty fosfoguanidiny (fosfageny fosfokreatin, fosfoarginin)
93 Bioenergetika Makroergická vazba Slide 17k fosfoanhydridy rezonanční stabilizace elektrostatická repulze vyšší solvatační energie produktů hydrolýzy ostatní anhydridy fosfosulfáty acylfosfáty fosfoguanidiny (fosfageny fosfokreatin, fosfoarginin) enolfosfáty
94 Bioenergetika Makroergická vazba Slide 17l fosfoanhydridy rezonanční stabilizace elektrostatická repulze vyšší solvatační energie produktů hydrolýzy ostatní anhydridy fosfosulfáty acylfosfáty fosfoguanidiny (fosfageny fosfokreatin, fosfoarginin) enolfosfáty thioestery
95 Bioenergetika Slide 18a
96 Bioenergetika Slide 19a Rozdělení organismů podle způsobu výživy (trofiky) Zdroj energie Světlo CO 2 FOTOLITOTROFNÍ Zdroj uhlíku Organické látky FOTOORGANOTROFNÍ Oxidace substrátů zelené a purpurové sirné bakterie, řasy, sinice, zelené rostliny CHEMOLITOTROFNÍ (anorganické substráty) sirné, železité, nitrifikační bakterie purpurové nesirné bakterie, autotrofní prvoci (krásnoočko) CHEMOORGANOTROFNÍ (organické substráty) bakterie, houby, prvoci, živočichové
97 Bioenergetika Slide 20a Schéma energetického metabolismu aminokyseliny mastné kyseliny β-oxidace cukry glykolýza pyruvát alternativní dráhy NADH NAD + NADH NAD + fermentační regenerace NADH laktát ethanol propionát butyrát butanol formiát H2 CO2 acetát 2,3-butandiol sukcinát oxidační dekarboxylace citrátový cyklus Ac~S CoA Calvinův cyklus CO 2 NADH NAD + NADPH NADP + hν ADP respirační řetězec O 2 fotosyntetický elektrontransportní řetězec ADP ATP oxidační fosforylace H 2 O fotofosforylace ATP
98 Konec
99 Bioenergetika (verze pro tisk na konci souboru) Tomáš Kučera 2011
100 Bioenergetika Slide 1 Bioenergetika jak organismy získávají, přeměňují, ukládají a využívají energii
101 Bioenergetika Slide 2 Termodynamika vzájemné přeměny různých druhů energie směřování fyzikálních a chemických pochodů měřítko samovolnosti (uskutečnitelnosti dějů) rovnovážné stavy Základní pojmy systém (soustava) libovolná část prostoru uvažovaná odděleně od okolí izolovaný nevyměňuje s okolím hmotu ani energii uzavřený vyměňuje s okolím jen energii, nikoli hmotu otevřený vyměňuje s okolím hmotu i energii okolí zbytek vesmíru ŽIVÉ SYSTÉMY JSOU VŽDY OTEVŘENÉ!
102 Bioenergetika Slide 3 První věta termodynamiky Energii nelze vytvořit ani zničit. U = U konečná U počáteční = Q W U vnitřní energie soustavy Q teplo přijaté soustavou od okolí W práce vykonaná soustavou na okolí izochorický děj (V = konst.) izobarický děj (p = konst.) W = p dv U = Q V U = Q p (pv) U + pv = H H = (U + pv) = Q p p tlak, V objem, H enthalpie
103 Bioenergetika Slide 4 Druhá věta termodynamiky Nelze sestrojit periodicky pracující tepelný stroj, který by dodával okolí práci na úkor tepla odebíraného jedinému tepelnému rezervoáru. Teplo nemůže při styku dvou těles různých teplot samovolně přecházet z tělesa chladnějšího na těleso teplejší. dq T 0 entropie S = Q T S = k lnp ukazatel samovolnosti děje v adiabaticky izolovaných soustavách S soustava + S okolí = S vesmír > 0
104 Bioenergetika Slide 5 Gibbsova (volná) energie G = H TS G = H T S = Q p T S koná-li systém práci, je G = Q p T S + W T S Q p G W v biol. systému objemová práce zanedbatelná G = max. práce reálný děj není nikdy reversibilní G < W Práci vloženou do systému nelze celou získat zpět. Úbytek G je roven maximální práci, kterou může systém odevzdat při izotermicko-izobarickém ději do okolí. rovnováha: G = 0 samovolný (exergonický) děj: G < 0 (může konat práci) endergonický děj: G > 0
105 Bioenergetika Slide 6 Gibbsova energie jeden z tzv. termodynamických potenciálů žádná informace o rychlosti ta dána mechanismem (ne)možnost děje dána jen počátečním a konečným stavem katalyzátor (enzym) může urychlit dosažení rovnováhy, ale ne změnit její stav možnost spřažení závisí na teplotě: rovnováha: T = H S
106 Bioenergetika Slide 7 Chemické rovnováhy pro reakci aa + bb cc + dd G = G 0 + RT ln [C]c [D] d G 0... standardní změna G dané reakce [A] a [B] b konstantní člen závisí jen na konkrétní reakci proměnný člen závisí na teplotě a koncentracích reaktantů a produktů rovnováha: G = 0 G 0 = RT ln K eq K eq = [C]c [D] d [A] a [B] b = e G0 RT G 0 a K eq v přímém vztahu 10násobná změna K eq změní G 0 o 5.7 kj/mol
107 Bioenergetika Slide 8 Změna Gibbsovy energie G 0 = G 0 f (products) G 0 f (reactants) G 0 f... G0 syntézy z prvků
108 Bioenergetika Slide 9 standardní stav aktivita 1 mol/l 25 C 1 atm Změna Gibbsovy energie biochemický standardní stav aktivita vody = 1 ph = 7 látky podléhající acidobazické disociaci: c = celková c všech forem při ph = 7
109 Bioenergetika Slide 10 Spřažené reakce A + B C + D G 1 D + E F + G G 2 A + B + E C + F + G G 3 = G 1 + G 2 < 0 ΔG 0 (kj.mol -1 ) Endergonická reakce: glukosa + P i glukosa-6-fosfát + H 2 O +13,8 Exergonická reakce: ATP + H 2 O ADP + P i 30,5 Spřažená reakce: glukosa + ATP glukosa-6-fosfát + ADP 16,7
110 Bioenergetika Slide 11 Redoxní potenciál Aox n+ + B red A red + B n+ ox Nernst : E = E 0 RT G = G 0 + RT ln [A red][b n+ ox] [A n+ ox ][B red ] nf G = nf E [red] ln [ox] E = E0 RT nf ln [A red][b n+ ox ] [Aox n+ ][B red ]
111 Bioenergetika Slide 12 E jako energetická škála Redoxní potenciál Redukovaná forma Oxidovaná forma E 0 (V) ΔG 0 acetaldehyd acetát -0,60 hodnoty vyšší H 2 2H + -0,42 (reduktans) isocitrát 2-oxoglutarát + CO 2-0,38 glutathion-sh glutathion-ss -0,34 NADH + H + NAD + -0,32 glyceraldehyd-3-fosfát + H 3 P0 4 1,3-bisfosfoglycerát -0,28 FADH 2 FAD -0,20 laktát pyruvát -0,19 malát oxalacetát -0,17 cytochrom b (Fe 2+ ) cytochrom b (Fe 3+ ) 0,00 sukcinát fumarát +0,03 dihydroubichinon ubichinon +0,10 cytochrom c (Fe 2+ ) cytochrom c (Fe 3+ ) +0,26 +ne ne H 2 O 2 O 2 +0,29 + hodnoty H 2 O ½ O 2 +0,82 (oxidans) nižší exergonický děj endergonický děj
112 Bioenergetika Slide 13 Redoxní potenciál E 0 = 0V pro standardní vodíkový poločlánek (elektrodu) H + při ph 0, 25 C, 1 atm v rovnováze s elektrodou z Pt černi sycenou H 2 ph = 7 E 0 = 0.421V
113 Bioenergetika Slide 14 NAD(P) + NikotinamidAdeninDinukleotid(fosfát) Redoxní reakce NAD(P) + NAD(P)H + H +
114 Bioenergetika Slide 15 Makroergické sloučeniny jejich hydrolýza pohání endergonické reakce obsahují makroergickou vazbu ATP centrální role (univerzální energetická měna buňky) 3 fosfátové skupiny vázané 1 fosfoesterovou a 2 fosfoanhydridovými vazbami
115 Bioenergetika Slide 16 ATP R 1 O P + R 2 OH R 1 O H + R 2 OP reakce přenosu fosforylu obrovský metabolický význam ATP + H 2 O ADP + P i G 0 = 30, 5 kj mol 1 ATP + H 2 O AMP + PP i G 0 = 45, 6 kj mol 1 ATP se obnovuje za pomoci ještě exergoničtějších reakcí kinetická stabilita, termodynamická nestabilita (vysoké G 0 )
116 Bioenergetika Slide 17 Makroergická vazba fosfoanhydridy rezonanční stabilizace elektrostatická repulze vyšší solvatační energie produktů hydrolýzy ostatní anhydridy fosfosulfáty acylfosfáty fosfoguanidiny (fosfageny fosfokreatin, fosfoarginin) enolfosfáty thioestery
117 Bioenergetika Slide 18
118 Bioenergetika Slide 19 Rozdělení organismů podle způsobu výživy (trofiky) Zdroj energie Světlo CO 2 FOTOLITOTROFNÍ Zdroj uhlíku Organické látky FOTOORGANOTROFNÍ Oxidace substrátů zelené a purpurové sirné bakterie, řasy, sinice, zelené rostliny CHEMOLITOTROFNÍ (anorganické substráty) sirné, železité, nitrifikační bakterie purpurové nesirné bakterie, autotrofní prvoci (krásnoočko) CHEMOORGANOTROFNÍ (organické substráty) bakterie, houby, prvoci, živočichové
119 Bioenergetika Slide 20 Schéma energetického metabolismu aminokyseliny mastné kyseliny β-oxidace cukry glykolýza pyruvát alternativní dráhy NADH NAD + NADH NAD + fermentační regenerace NADH laktát ethanol propionát butyrát butanol formiát H2 CO2 acetát 2,3-butandiol sukcinát oxidační dekarboxylace citrátový cyklus Ac~S CoA Calvinův cyklus CO 2 NADH NAD + NADPH NADP + hν ADP respirační řetězec O 2 fotosyntetický elektrontransportní řetězec ADP ATP oxidační fosforylace H 2 O fotofosforylace ATP
120 Konec
121 Bioenergetics Slide 1a Bioenergetics
122 Bioenergetics Slide 1b Bioenergetics how organisms gain, transform, store and utilize energy
123 Bioenergetics Slide 2a Thermodynamics
124 Bioenergetics Slide 2b Thermodynamics mutual conversions of different energy types directions of physical and chemical processes measure of spontaneity (possibility) of processes equilibrium states
125 Bioenergetics Slide 2c Thermodynamics mutual conversions of different energy types directions of physical and chemical processes measure of spontaneity (possibility) of processes equilibrium states Basic concepts
126 Bioenergetics Slide 2d Thermodynamics mutual conversions of different energy types directions of physical and chemical processes measure of spontaneity (possibility) of processes equilibrium states Basic concepts system an arbitrary part of space considered apart of its surroundings
127 Bioenergetics Slide 2e Thermodynamics mutual conversions of different energy types directions of physical and chemical processes measure of spontaneity (possibility) of processes equilibrium states Basic concepts system an arbitrary part of space considered apart of its surroundings isolated cannot exchange neither matter nor energy with the surroundings closed exchanges only energy, not matter isolated exchanges both energy and matter
128 Bioenergetics Slide 2f Thermodynamics mutual conversions of different energy types directions of physical and chemical processes measure of spontaneity (possibility) of processes equilibrium states Basic concepts system an arbitrary part of space considered apart of its surroundings isolated cannot exchange neither matter nor energy with the surroundings closed exchanges only energy, not matter isolated exchanges both energy and matter LIVING SYSTEMS ARE ALWAYS OPEN!
129 Bioenergetics Slide 2g Thermodynamics mutual conversions of different energy types directions of physical and chemical processes measure of spontaneity (possibility) of processes equilibrium states Basic concepts system an arbitrary part of space considered apart of its surroundings isolated cannot exchange neither matter nor energy with the surroundings closed exchanges only energy, not matter isolated exchanges both energy and matter LIVING SYSTEMS ARE ALWAYS OPEN! surroundings the rest of the universe
130 Bioenergetics Slide 3a First law of thermodynamics
131 Bioenergetics Slide 3b First law of thermodynamics Energy can neither be created nor destroyed.
132 Bioenergetics Slide 3c First law of thermodynamics Energy can neither be created nor destroyed. U = U final U initial = Q W U the system energy Q the heat absorbed by the system from the surroundings W work done by the system on the surroundings
133 Bioenergetics Slide 3d First law of thermodynamics Energy can neither be created nor destroyed. U = U final U initial = Q W U the system energy Q the heat absorbed by the system from the surroundings W work done by the system on the surroundings isochoric process (V = const.)
134 Bioenergetics Slide 3e First law of thermodynamics Energy can neither be created nor destroyed. U = U final U initial = Q W U the system energy Q the heat absorbed by the system from the surroundings W work done by the system on the surroundings isochoric process (V = const.) U = Q V
135 Bioenergetics Slide 3f First law of thermodynamics Energy can neither be created nor destroyed. U = U final U initial = Q W U the system energy Q the heat absorbed by the system from the surroundings W work done by the system on the surroundings isochoric process (V = const.) isobaric process (p = const.) U = Q V
136 Bioenergetics Slide 3g First law of thermodynamics Energy can neither be created nor destroyed. U = U final U initial = Q W U the system energy Q the heat absorbed by the system from the surroundings W work done by the system on the surroundings isochoric process (V = const.) isobaric process (p = const.) U = Q V U = Q p (pv) U + pv = H H = (U + pv) = Q p p pressure, V volume, H enthalpy
137 Bioenergetics Slide 4a Second law of thermodynamics
138 Bioenergetics Slide 4b Second law of thermodynamics No process is possible in which the sole result is the absorption of heat from a reservoir and its complete conversion into work.
139 Bioenergetics Slide 4c Second law of thermodynamics No process is possible in which the sole result is the absorption of heat from a reservoir and its complete conversion into work. No process is possible whose sole result is the transfer of heat from a body of lower temperature to a body of higher temperature.
140 Bioenergetics Slide 4d Second law of thermodynamics No process is possible in which the sole result is the absorption of heat from a reservoir and its complete conversion into work. No process is possible whose sole result is the transfer of heat from a body of lower temperature to a body of higher temperature. dq T 0
141 Bioenergetics Slide 4e Second law of thermodynamics No process is possible in which the sole result is the absorption of heat from a reservoir and its complete conversion into work. No process is possible whose sole result is the transfer of heat from a body of lower temperature to a body of higher temperature. dq T 0 entropy S = Q T
142 Bioenergetics Slide 4f Second law of thermodynamics No process is possible in which the sole result is the absorption of heat from a reservoir and its complete conversion into work. No process is possible whose sole result is the transfer of heat from a body of lower temperature to a body of higher temperature. dq T 0 entropy S = Q T S = k lnp
143 Bioenergetics Slide 4g Second law of thermodynamics No process is possible in which the sole result is the absorption of heat from a reservoir and its complete conversion into work. No process is possible whose sole result is the transfer of heat from a body of lower temperature to a body of higher temperature. dq T 0 entropy S = Q T S = k lnp an indicator of process spontaneity only in adiabatically isolated systems
144 Bioenergetics Slide 4h Second law of thermodynamics No process is possible in which the sole result is the absorption of heat from a reservoir and its complete conversion into work. No process is possible whose sole result is the transfer of heat from a body of lower temperature to a body of higher temperature. dq T 0 entropy S = Q T S = k lnp an indicator of process spontaneity only in adiabatically isolated systems Ssystem + S surroundings = S universe > 0
145 Bioenergetics Slide 5a Gibbs free energy G = H TS G = H T S = Q p T S
146 Bioenergetics Slide 5b Gibbs free energy G = H TS G = H T S = Q p T S the system does a work, then G = Q p T S + W T S Q p G W
147 Bioenergetics Slide 5c Gibbs free energy G = H TS G = H T S = Q p T S the system does a work, then G = Q p T S + W T S Q p G W in a biol. system, pv-work unimportant G = max. work
148 Bioenergetics Slide 5d Gibbs free energy G = H TS G = H T S = Q p T S the system does a work, then G = Q p T S + W T S Q p G W in a biol. system, pv-work unimportant G = max. work a real process is never reversible G < W The work put into any system can never be fully recovered
149 Bioenergetics Slide 5e Gibbs free energy G = H TS G = H T S = Q p T S the system does a work, then G = Q p T S + W T S Q p G W in a biol. system, pv-work unimportant G = max. work a real process is never reversible G < W The work put into any system can never be fully recovered G decrease in a biological process represents its maximum recoverable work.
150 Bioenergetics Slide 5f Gibbs free energy G = H TS G = H T S = Q p T S the system does a work, then G = Q p T S + W T S Q p G W in a biol. system, pv-work unimportant G = max. work a real process is never reversible G < W The work put into any system can never be fully recovered G decrease in a biological process represents its maximum recoverable work. equilibrium: G = 0
151 Bioenergetics Slide 5g Gibbs free energy G = H TS G = H T S = Q p T S the system does a work, then G = Q p T S + W T S Q p G W in a biol. system, pv-work unimportant G = max. work a real process is never reversible G < W The work put into any system can never be fully recovered G decrease in a biological process represents its maximum recoverable work. equilibrium: G = 0 spontaneous (exergonic) process: G < 0 (it can do work)
152 Bioenergetics Slide 5h Gibbs free energy G = H TS G = H T S = Q p T S the system does a work, then G = Q p T S + W T S Q p G W in a biol. system, pv-work unimportant G = max. work a real process is never reversible G < W The work put into any system can never be fully recovered G decrease in a biological process represents its maximum recoverable work. equilibrium: G = 0 spontaneous (exergonic) process: G < 0 (it can do work) endergonic process: G > 0
153 Bioenergetics Slide 6a Free energy one of the thermodynamic potentials
154 Bioenergetics Slide 6b Free energy one of the thermodynamic potentials no information about the rate it is given by the mechanism
155 Bioenergetics Slide 6c Free energy one of the thermodynamic potentials no information about the rate it is given by the mechanism (non-)possibility of a process given only by the initial and final states
156 Bioenergetics Slide 6d Free energy one of the thermodynamic potentials no information about the rate it is given by the mechanism (non-)possibility of a process given only by the initial and final states a catalyst (enzyme) can only accelerate equilibrium attainment, not change its state
157 Bioenergetics Slide 6e Free energy one of the thermodynamic potentials no information about the rate it is given by the mechanism (non-)possibility of a process given only by the initial and final states a catalyst (enzyme) can only accelerate equilibrium attainment, not change its state coupling is possible
158 Bioenergetics Slide 6f Free energy one of the thermodynamic potentials no information about the rate it is given by the mechanism (non-)possibility of a process given only by the initial and final states a catalyst (enzyme) can only accelerate equilibrium attainment, not change its state coupling is possible depends on temperature: equilibrium: T = H S
159 Bioenergetics Slide 6g Free energy one of the thermodynamic potentials no information about the rate it is given by the mechanism (non-)possibility of a process given only by the initial and final states a catalyst (enzyme) can only accelerate equilibrium attainment, not change its state coupling is possible depends on temperature: equilibrium: T = H S
160 Bioenergetics Slide 7a Chemical equilibria for a reaction aa + bb cc + dd G = G 0 + RT ln [C]c [D] d [A] a [B] b G 0... standard G change of the reaction
161 Bioenergetics Slide 7b Chemical equilibria for a reaction aa + bb cc + dd G = G 0 + RT ln [C]c [D] d [A] a [B] b G 0... standard G change of the reaction constant term depends only on the reaction
162 Bioenergetics Slide 7c Chemical equilibria for a reaction aa + bb cc + dd G = G 0 + RT ln [C]c [D] d G 0... standard G change of the reaction [A] a [B] b constant term depends only on the reaction variable term depends on temperature and concentratins of reactants and products
163 Bioenergetics Slide 7d Chemical equilibria for a reaction aa + bb cc + dd G = G 0 + RT ln [C]c [D] d G 0... standard G change of the reaction [A] a [B] b constant term depends only on the reaction variable term depends on temperature and concentratins of reactants and products equilibrium: G = 0 G 0 = RT ln K eq K eq = [C]c [D] d [A] a [B] b = e G0 RT
164 Bioenergetics Slide 7e Chemical equilibria for a reaction aa + bb cc + dd G = G 0 + RT ln [C]c [D] d G 0... standard G change of the reaction [A] a [B] b constant term depends only on the reaction variable term depends on temperature and concentratins of reactants and products equilibrium: G = 0 G 0 = RT ln K eq K eq = [C]c [D] d [A] a [B] b = e G0 RT G 0 and K eq directly related
165 Bioenergetics Slide 7f Chemical equilibria for a reaction aa + bb cc + dd G = G 0 + RT ln [C]c [D] d G 0... standard G change of the reaction [A] a [B] b constant term depends only on the reaction variable term depends on temperature and concentratins of reactants and products equilibrium: G = 0 G 0 = RT ln K eq K eq = [C]c [D] d [A] a [B] b = e G0 RT G 0 and K eq directly related 10-fold change in K eq changes G 0 by 5.7 kj/mol
166 Bioenergetics Slide 8a Free energy changes G 0 = G 0 f (products) G 0 f (reactants) G 0 f... G0 of formation
167 Bioenergetics Slide 8b Free energy changes G 0 = G 0 f (products) G 0 f (reactants) G 0 f... G0 of formation
168 Bioenergetics Free energy changes Slide 9a standard state
169 Bioenergetics Free energy changes Slide 9b standard state activity 1 mol/l
170 Bioenergetics Free energy changes Slide 9c standard state activity 1 mol/l 25 C
171 Bioenergetics Free energy changes Slide 9d standard state activity 1 mol/l 25 C 1 atm
172 Bioenergetics Slide 9e standard state activity 1 mol/l 25 C 1 atm Free energy changes biochemical standard state
173 Bioenergetics Slide 9f standard state activity 1 mol/l 25 C 1 atm Free energy changes biochemical standard state water activity = 1
174 Bioenergetics Slide 9g standard state activity 1 mol/l 25 C 1 atm Free energy changes biochemical standard state water activity = 1 ph = 7
175 Bioenergetics Slide 9h standard state activity 1 mol/l 25 C 1 atm Free energy changes biochemical standard state water activity = 1 ph = 7 substances undergoing acidobasic dissociation: c = total c of all species at ph = 7
176 Bioenergetics Slide 10a Coupled reactions
177 Bioenergetics Slide 10b Coupled reactions A + B C + D G 1 D + E F + G G 2
178 Bioenergetics Slide 10c Coupled reactions A + B C + D G 1 D + E F + G G 2 A + B + E C + F + G G 3 = G 1 + G 2 < 0
179 Bioenergetics Slide 10d Coupled reactions A + B C + D G 1 D + E F + G G 2 A + B + E C + F + G G 3 = G 1 + G 2 < 0 ΔG 0 (kj.mol -1 ) Endergonic reaction: glucose + P i glucose-6-phosphate + H 2 O +13,8 Exergonic reaction: ATP + H 2 O ADP + P i 30,5 Coupled reaction: glucose + ATP glucose-6-phosphate + ADP 16,7
180 Bioenergetics Slide 11a Redox potential
181 Bioenergetics Slide 11b Redox potential Aox n+ + B red A red + B n+ ox
182 Bioenergetics Slide 11c Redox potential Aox n+ + B red A red + B n+ ox
183 Bioenergetics Slide 11d Redox potential Aox n+ + B red A red + B n+ ox G = G 0 + RT ln [A red][b n+ ox] [A n+ ox ][B red ]
184 Bioenergetics Slide 11e Redox potential Aox n+ + B red A red + B n+ ox G = G 0 + RT ln [A red][b n+ ox] [A n+ ox ][B red ] G = W = W el = nf E
185 Bioenergetics Slide 11f Redox potential Aox n+ + B red A red + B n+ ox Nernst : E = E 0 RT G = G 0 + RT ln [A red][b n+ ox] [A n+ ox ][B red ] G = W = W el = nf E nf [red] ln [ox] E = E0 RT nf ln [A red][b n+ ox ] [Aox n+ ][B red ]
186 Bioenergetics Slide 12a E as an energy scale Redox potential
187 Bioenergetics Redox potential Slide 12b E as an energy scale Reduced form Oxidized form E 0 (V) ΔG 0 acetaldehyde acetate -0,60 values higher H 2 2H + -0,42 (reductant) isocitrate 2-oxoglutarate + CO 2-0,38 glutathione-sh glutathione-ss -0,34 NADH + H + NAD + -0,32 glyceraldehyde-3-phosphate + H 3 PO 4 1,3-bisphosphoglycerate -0,28 FADH 2 FAD -0,20 lactate pyruvate -0,19 malate oxalacetate -0,17 cytochrome b (Fe 2+ ) cytochrome b (Fe 3+ ) 0,00 succinate fumarate +0,03 dihydroubiquinone ubiquinone +0,10 cytochrome c (Fe 2+ ) cytochrome c (Fe 3+ ) +0,26 +ne ne H 2 O 2 O 2 +0,29 + values H 2 O ½ O 2 +0,82 (oxidant) lower exergonic reaction endergonic reaction
188 Bioenergetics Slide 13a Redox potential E 0 = 0V for standard hydrogen half-reaction (electrode)
189 Bioenergetics Redox potential Slide 13b E 0 = 0V for standard hydrogen half-reaction (electrode) H + at ph 0, 25 C, 1 atm in equilibrium with Pt-black electrode saturated with H 2
190 Bioenergetics Redox potential Slide 13c E 0 = 0V for standard hydrogen half-reaction (electrode) H + at ph 0, 25 C, 1 atm in equilibrium with Pt-black electrode saturated with H 2 ph = 7 E 0 = 0.421V
191 Bioenergetics Slide 14a NAD(P) + Nicotinamide Adenine Dinucleotide (Phosphate)
192 Bioenergetics Slide 14b NAD(P) + Nicotinamide Adenine Dinucleotide (Phosphate) Redox reaction NAD(P) + NAD(P)H + H +
193 Bioenergetics Slide 15a High-energy compounds hydrolyzed to drive endergonic reactions
194 Bioenergetics Slide 15b High-energy compounds hydrolyzed to drive endergonic reactions contain high-energy bond
195 Bioenergetics Slide 15c High-energy compounds hydrolyzed to drive endergonic reactions contain high-energy bond ATP a central role (universal energy currency of the cell)
196 Bioenergetics Slide 15d High-energy compounds hydrolyzed to drive endergonic reactions contain high-energy bond ATP a central role (universal energy currency of the cell) 3 phosphoryl groups bound by one phosphoester and two phosphoanhydride bonds
197 Bioenergetics Slide 15e High-energy compounds hydrolyzed to drive endergonic reactions contain high-energy bond ATP a central role (universal energy currency of the cell) 3 phosphoryl groups bound by one phosphoester and two phosphoanhydride bonds
198 Bioenergetics Slide 16a ATP R 1 O P + R 2 OH R 1 O H + R 2 OP phosphoryl transfer reaction enormous metabolic significance
199 Bioenergetics ATP Slide 16b R 1 O P + R 2 OH R 1 O H + R 2 OP phosphoryl transfer reaction enormous metabolic significance ATP + H 2 O ADP + P i G 0 = 30.5 kj mol 1 ATP + H 2 O AMP + PP i G 0 = 45.6 kj mol 1
200 Bioenergetics ATP Slide 16c R 1 O P + R 2 OH R 1 O H + R 2 OP phosphoryl transfer reaction enormous metabolic significance ATP + H 2 O ADP + P i G 0 = 30.5 kj mol 1 ATP + H 2 O AMP + PP i G 0 = 45.6 kj mol 1 ATP formed using more highly exergonic reactions
201 Bioenergetics ATP Slide 16d R 1 O P + R 2 OH R 1 O H + R 2 OP phosphoryl transfer reaction enormous metabolic significance ATP + H 2 O ADP + P i G 0 = 30.5 kj mol 1 ATP + H 2 O AMP + PP i G 0 = 45.6 kj mol 1 ATP formed using more highly exergonic reactions kinetic stability, thermodynamic instability (high G 0 )
202 Bioenergetics High-energy bonds Slide 17a
203 Bioenergetics High-energy bonds Slide 17b phosphoanhydrides
204 Bioenergetics High-energy bonds Slide 17c phosphoanhydrides resonance stabilization
205 Bioenergetics High-energy bonds Slide 17d phosphoanhydrides resonance stabilization electrostatic repulsion
206 Bioenergetics High-energy bonds Slide 17e phosphoanhydrides resonance stabilization electrostatic repulsion
207 Bioenergetics High-energy bonds Slide 17f phosphoanhydrides resonance stabilization electrostatic repulsion higher solvation energy of the hydrolysis products
208 Bioenergetics High-energy bonds Slide 17g phosphoanhydrides resonance stabilization electrostatic repulsion higher solvation energy of the hydrolysis products other anhydrides
209 Bioenergetics High-energy bonds Slide 17h phosphoanhydrides resonance stabilization electrostatic repulsion higher solvation energy of the hydrolysis products other anhydrides phosphosulphates
210 Bioenergetics High-energy bonds Slide 17i phosphoanhydrides resonance stabilization electrostatic repulsion higher solvation energy of the hydrolysis products other anhydrides phosphosulphates acylphosphates
211 Bioenergetics High-energy bonds Slide 17j phosphoanhydrides resonance stabilization electrostatic repulsion higher solvation energy of the hydrolysis products other anhydrides phosphosulphates acylphosphates phosphoguanidines (phosphagens phosphocreatine, phosphoarginine)
212 Bioenergetics High-energy bonds Slide 17k phosphoanhydrides resonance stabilization electrostatic repulsion higher solvation energy of the hydrolysis products other anhydrides phosphosulphates acylphosphates phosphoguanidines (phosphagens phosphocreatine, phosphoarginine) enol phosphates
213 Bioenergetics High-energy bonds Slide 17l phosphoanhydrides resonance stabilization electrostatic repulsion higher solvation energy of the hydrolysis products other anhydrides phosphosulphates acylphosphates phosphoguanidines (phosphagens phosphocreatine, phosphoarginine) enol phosphates thioesters
214 Bioenergetics Slide 18a
215 Bioenergetics Slide 19a Organisms according to the metabolism type (trophics) Energy source Light CO 2 PHOTOLITOTROPHIC Carbon source Organic compounds PHOTOORGANOTROPHIC Substrate oxidation green and purple sulphur bacteria, cyanobacteria, algae, green plants CHEMOLITOTROPHIC (inorganic substrates) sulphur, ferric, nitrifying bacteria purple non sulphur bacteria, photototrophic protists (Euglena) CHEMOORGANOTROPHIC (organic substrates) bacteria, fungi, protists, animals
216 Bioenergetics Slide 20a Energy metabolism scheme amino acids fatty acids β-oxidation sugars glycolysis pyruvate alternative pathways NADH NAD + NADH NAD + fermentative NADH regeneration lactate ethanol propionate butyrate butanol formate H2 CO2 acetate 2,3-butandiol succinate oxidative decarboxylation citric acid cycle Ac~S CoA Calvin cycle CO 2 NADH NAD + NADPH NADP + hν ADP respiration chain O 2 photosynthetic electron transport chain ADP ATP oxidative phosphorylation H 2 O photophosphorylation ATP
217 The End
218 Bioenergetics (print version in the end of the file) Tomáš Kučera 2011
219 Bioenergetics Slide 1 Bioenergetics how organisms gain, transform, store and utilize energy
220 Bioenergetics Slide 2 Thermodynamics mutual conversions of different energy types directions of physical and chemical processes measure of spontaneity (possibility) of processes equilibrium states Basic concepts system an arbitrary part of space considered apart of its surroundings isolated cannot exchange neither matter nor energy with the surroundings closed exchanges only energy, not matter isolated exchanges both energy and matter LIVING SYSTEMS ARE ALWAYS OPEN! surroundings the rest of the universe
221 Bioenergetics Slide 3 First law of thermodynamics Energy can neither be created nor destroyed. U = U final U initial = Q W U the system energy Q the heat absorbed by the system from the surroundings W work done by the system on the surroundings isochoric process (V = const.) isobaric process (p = const.) U = Q V U = Q p (pv) U + pv = H H = (U + pv) = Q p p pressure, V volume, H enthalpy
222 Bioenergetics Slide 4 Second law of thermodynamics No process is possible in which the sole result is the absorption of heat from a reservoir and its complete conversion into work. No process is possible whose sole result is the transfer of heat from a body of lower temperature to a body of higher temperature. dq T 0 entropy S = Q T S = k lnp an indicator of process spontaneity only in adiabatically isolated systems Ssystem + S surroundings = S universe > 0
223 Bioenergetics Slide 5 Gibbs free energy G = H TS G = H T S = Q p T S the system does a work, then G = Q p T S + W T S Q p G W in a biol. system, pv-work unimportant G = max. work a real process is never reversible G < W The work put into any system can never be fully recovered G decrease in a biological process represents its maximum recoverable work. equilibrium: G = 0 spontaneous (exergonic) process: G < 0 (it can do work) endergonic process: G > 0
224 Bioenergetics Slide 6 Free energy one of the thermodynamic potentials no information about the rate it is given by the mechanism (non-)possibility of a process given only by the initial and final states a catalyst (enzyme) can only accelerate equilibrium attainment, not change its state coupling is possible depends on temperature: equilibrium: T = H S
225 Bioenergetics Slide 7 Chemical equilibria for a reaction aa + bb cc + dd G = G 0 + RT ln [C]c [D] d G 0... standard G change of the reaction [A] a [B] b constant term depends only on the reaction variable term depends on temperature and concentratins of reactants and products equilibrium: G = 0 G 0 = RT ln K eq K eq = [C]c [D] d [A] a [B] b = e G0 RT G 0 and K eq directly related 10-fold change in K eq changes G 0 by 5.7 kj/mol
226 Bioenergetics Slide 8 Free energy changes G 0 = G 0 f (products) G 0 f (reactants) G 0 f... G0 of formation
227 Bioenergetics Slide 9 standard state activity 1 mol/l 25 C 1 atm Free energy changes biochemical standard state water activity = 1 ph = 7 substances undergoing acidobasic dissociation: c = total c of all species at ph = 7
228 Bioenergetics Slide 10 Coupled reactions A + B C + D G 1 D + E F + G G 2 A + B + E C + F + G G 3 = G 1 + G 2 < 0 ΔG 0 (kj.mol -1 ) Endergonic reaction: glucose + P i glucose-6-phosphate + H 2 O +13,8 Exergonic reaction: ATP + H 2 O ADP + P i 30,5 Coupled reaction: glucose + ATP glucose-6-phosphate + ADP 16,7
229 Bioenergetics Slide 11 Redox potential Aox n+ + B red A red + B n+ ox Nernst : E = E 0 RT G = G 0 + RT ln [A red][b n+ ox] [A n+ ox ][B red ] G = W = W el = nf E nf [red] ln [ox] E = E0 RT nf ln [A red][b n+ ox ] [Aox n+ ][B red ]
230 Bioenergetics Slide 12 E as an energy scale Redox potential Reduced form Oxidized form E 0 (V) ΔG 0 acetaldehyde acetate -0,60 values higher H 2 2H + -0,42 (reductant) isocitrate 2-oxoglutarate + CO 2-0,38 glutathione-sh glutathione-ss -0,34 NADH + H + NAD + -0,32 glyceraldehyde-3-phosphate + H 3 PO 4 1,3-bisphosphoglycerate -0,28 FADH 2 FAD -0,20 lactate pyruvate -0,19 malate oxalacetate -0,17 cytochrome b (Fe 2+ ) cytochrome b (Fe 3+ ) 0,00 succinate fumarate +0,03 dihydroubiquinone ubiquinone +0,10 cytochrome c (Fe 2+ ) cytochrome c (Fe 3+ ) +0,26 +ne ne H 2 O 2 O 2 +0,29 + values H 2 O ½ O 2 +0,82 (oxidant) lower exergonic reaction endergonic reaction
231 Bioenergetics Slide 13 Redox potential E 0 = 0V for standard hydrogen half-reaction (electrode) H + at ph 0, 25 C, 1 atm in equilibrium with Pt-black electrode saturated with H 2 ph = 7 E 0 = 0.421V
232 Bioenergetics Slide 14 NAD(P) + Nicotinamide Adenine Dinucleotide (Phosphate) Redox reaction NAD(P) + NAD(P)H + H +
233 Bioenergetics Slide 15 High-energy compounds hydrolyzed to drive endergonic reactions contain high-energy bond ATP a central role (universal energy currency of the cell) 3 phosphoryl groups bound by one phosphoester and two phosphoanhydride bonds
234 Bioenergetics Slide 16 ATP R 1 O P + R 2 OH R 1 O H + R 2 OP phosphoryl transfer reaction enormous metabolic significance ATP + H 2 O ADP + P i G 0 = 30.5 kj mol 1 ATP + H 2 O AMP + PP i G 0 = 45.6 kj mol 1 ATP formed using more highly exergonic reactions kinetic stability, thermodynamic instability (high G 0 )
235 Bioenergetics Slide 17 phosphoanhydrides resonance stabilization electrostatic repulsion High-energy bonds higher solvation energy of the hydrolysis products other anhydrides phosphosulphates acylphosphates phosphoguanidines (phosphagens phosphocreatine, phosphoarginine) enol phosphates thioesters
236 Bioenergetics Slide 18
Bioenergetika Bioenergetics
 Bioenergetika Bioenergetics Tomáš Kučera 2012 Tisková verze Print version Prezentace Presentation Bioenergetika Slide 1a Bioenergetika Bioenergetika Slide 1b Bioenergetika jak organismy získávají, přeměňují,
Bioenergetika Bioenergetics Tomáš Kučera 2012 Tisková verze Print version Prezentace Presentation Bioenergetika Slide 1a Bioenergetika Bioenergetika Slide 1b Bioenergetika jak organismy získávají, přeměňují,
Bioenergetika a makroergické sloučeniny
 Bioenergetika a makroergické sloučeniny Tomáš Kučera tomas.kucera@lfmotol.cuni.cz Ústav lékařské chemie a klinické biochemie 2. lékařská fakulta, Univerzita Karlova v Praze a Fakultní nemocnice v Motole
Bioenergetika a makroergické sloučeniny Tomáš Kučera tomas.kucera@lfmotol.cuni.cz Ústav lékařské chemie a klinické biochemie 2. lékařská fakulta, Univerzita Karlova v Praze a Fakultní nemocnice v Motole
Biologické redoxní děje Biological redox processes. Tisková verze Print version Prezentace Presentation
 Biologické redoxní děje Biological redox processes Tomáš Kučera 2011 Tisková verze Print version Prezentace Presentation Biologické redoxní děje Slide 1a Biologické redoxní děje Biologické redoxní děje
Biologické redoxní děje Biological redox processes Tomáš Kučera 2011 Tisková verze Print version Prezentace Presentation Biologické redoxní děje Slide 1a Biologické redoxní děje Biologické redoxní děje
METABOLISMUS SLOUČENINY S MAKROERGNÍMI VAZBAMI
 METABOLISMUS SLOUČENINY S MAKROERGNÍMI VAZBAMI Obsah Formy organismů Energetika reakcí Metabolické reakce Makroergické sloučeniny Formy organismů Autotrofní x heterotrofní organismy Práce a energie Energie
METABOLISMUS SLOUČENINY S MAKROERGNÍMI VAZBAMI Obsah Formy organismů Energetika reakcí Metabolické reakce Makroergické sloučeniny Formy organismů Autotrofní x heterotrofní organismy Práce a energie Energie
Metabolismus. Source:
 Source: http://www.roche.com/ http://www.expasy.org/ Metabolismus Source: http://www.roche.com/sustainability/for_communities_and_environment/philanthropy/science_education/pathways.htm Metabolismus -
Source: http://www.roche.com/ http://www.expasy.org/ Metabolismus Source: http://www.roche.com/sustainability/for_communities_and_environment/philanthropy/science_education/pathways.htm Metabolismus -
Citrátový cyklus. Tomáš Kučera.
 itrátový cyklus Tomáš Kučera tomas.kucera@lfmotol.cuni.cz Ústav lékařské chemie a klinické biochemie 2. lékařská fakulta, Univerzita Karlova v Praze a Fakultní nemocnice v Motole 2017 Schéma energetického
itrátový cyklus Tomáš Kučera tomas.kucera@lfmotol.cuni.cz Ústav lékařské chemie a klinické biochemie 2. lékařská fakulta, Univerzita Karlova v Praze a Fakultní nemocnice v Motole 2017 Schéma energetického
16a. Makroergické sloučeniny
 16a. Makroergické sloučeniny Makroergickými sloučeninami v biochemii nazýváme skupinu látek umožňujících uvolnění značného množství energie v jednoduché reakci. Nelze je definovat prostě jako sloučeniny
16a. Makroergické sloučeniny Makroergickými sloučeninami v biochemii nazýváme skupinu látek umožňujících uvolnění značného množství energie v jednoduché reakci. Nelze je definovat prostě jako sloučeniny
Metabolismus. - soubor všech chemických reakcí a příslušných fyzikálních procesů, které souvisejí s aktivními projevy života daného organismu
 Metabolismus Obecné znaky metabolismu Získání a využití energie - bioenergetika Buněčné dýchání (glykolysa + CKC + oxidativní fosforylace) Biosynthesa sacharidů + fotosynthesa Metabolismus lipidů Metabolismus
Metabolismus Obecné znaky metabolismu Získání a využití energie - bioenergetika Buněčné dýchání (glykolysa + CKC + oxidativní fosforylace) Biosynthesa sacharidů + fotosynthesa Metabolismus lipidů Metabolismus
03a-Chemické reakce v živých organizmech FRVŠ 1647/2012
 C3181 Biochemie I 03a-Chemické reakce v živých organizmech FRVŠ 1647/2012 Petr Zbořil 9/23/2014 1 Obsah Obecné rysy metabolismu Chemické reakce a jejich energetika Makroergické sloučeniny Petr Zbořil 9/23/2014
C3181 Biochemie I 03a-Chemické reakce v živých organizmech FRVŠ 1647/2012 Petr Zbořil 9/23/2014 1 Obsah Obecné rysy metabolismu Chemické reakce a jejich energetika Makroergické sloučeniny Petr Zbořil 9/23/2014
Oxidace proteinů, tuků a cukrů jako zdroj energie v živých organismech
 Citrátový cyklus Oxidace proteinů, tuků a cukrů jako zdroj energie v živých organismech 1. stupeň: OXIDACE cukrů, tuků a některých aminokyselin tvorba Acetyl-CoA a akumulace elektronů v NADH a FADH 2 2.
Citrátový cyklus Oxidace proteinů, tuků a cukrů jako zdroj energie v živých organismech 1. stupeň: OXIDACE cukrů, tuků a některých aminokyselin tvorba Acetyl-CoA a akumulace elektronů v NADH a FADH 2 2.
MitoSeminář II: Trochu výpočtů v bioenergetice. Souhrn. MUDr. Jan Pláteník, PhD. Ústav lékařské biochemie 1.LF UK
 MitoSeminář II: Trochu výpočtů v bioenergetice MUDr. Jan Pláteník, PhD. Ústav lékařské biochemie 1.LF UK (se zahrnutím cenných připomínek, kterými přispěl prof. MUDr. Jiří Kraml, DrSc.) 1 Dýchacířet etězec
MitoSeminář II: Trochu výpočtů v bioenergetice MUDr. Jan Pláteník, PhD. Ústav lékařské biochemie 1.LF UK (se zahrnutím cenných připomínek, kterými přispěl prof. MUDr. Jiří Kraml, DrSc.) 1 Dýchacířet etězec
METABOLISMUS SACHARIDŮ
 METABOLISMUS SAHARIDŮ A. Odbourávání sacharidů - nejdůležitější zdroj energie pro heterotrofy - oxidací sacharidů až na. získávají aerobní organismy energii ve formě. - úplná oxidace glukosy: složitý proces
METABOLISMUS SAHARIDŮ A. Odbourávání sacharidů - nejdůležitější zdroj energie pro heterotrofy - oxidací sacharidů až na. získávají aerobní organismy energii ve formě. - úplná oxidace glukosy: složitý proces
Otázka: Metabolismus. Předmět: Biologie. Přidal(a): Furrow. - přeměna látek a energie
 Otázka: Metabolismus Předmět: Biologie Přidal(a): Furrow - přeměna látek a energie Dělení podle typu reakcí: 1.) Katabolismus reakce, při nichž z látek složitějších vznikají látky jednodušší (uvolňuje
Otázka: Metabolismus Předmět: Biologie Přidal(a): Furrow - přeměna látek a energie Dělení podle typu reakcí: 1.) Katabolismus reakce, při nichž z látek složitějších vznikají látky jednodušší (uvolňuje
9. Citrátový cyklus, oxidační dekarboxylace pyruvátu a anaplerotické dráhy
 9. Citrátový cyklus, oxidační dekarboxylace pyruvátu a anaplerotické dráhy Obtížnost A Vyjmenujte kofaktory, které využívá multienzymový komplex pyruvátdehydrogenasy; které z nich řadíme mezi koenzymy
9. Citrátový cyklus, oxidační dekarboxylace pyruvátu a anaplerotické dráhy Obtížnost A Vyjmenujte kofaktory, které využívá multienzymový komplex pyruvátdehydrogenasy; které z nich řadíme mezi koenzymy
- metabolismus soubor chemických reakcí probíhajících v živých organismech a mezi organismy a jejich životním prostředím
 Otázka: Obecné rysy metabolismu Předmět: Chemie Přidal(a): Bára V. ZÁKLADY LÁTKOVÉHO A ENERGETICKÉHO METABOLISMU - metabolismus soubor chemických reakcí probíhajících v živých organismech a mezi organismy
Otázka: Obecné rysy metabolismu Předmět: Chemie Přidal(a): Bára V. ZÁKLADY LÁTKOVÉHO A ENERGETICKÉHO METABOLISMU - metabolismus soubor chemických reakcí probíhajících v živých organismech a mezi organismy
CZ.1.07/2.2.00/ Obecný metabolismus. Energetický metabolismus (obecně) (1).
 mezioborová integrace výuky zaměřená na rostlinnou biochemii a fytopatologii CZ.1.07/2.2.00/28.0171 becný metabolismus Energetický metabolismus (obecně) (1). Prof. RNDr. Pavel Peč, CSc. Katedra biochemie,
mezioborová integrace výuky zaměřená na rostlinnou biochemii a fytopatologii CZ.1.07/2.2.00/28.0171 becný metabolismus Energetický metabolismus (obecně) (1). Prof. RNDr. Pavel Peč, CSc. Katedra biochemie,
Energetika a metabolismus buňky
 Předmět: KBB/BB1P Energetika a metabolismus buňky Cíl přednášky: seznámit posluchače s tím, jak buňky získávají energii k životu a jak s ní hospodaří Klíčová slova: energetika buňky, volná energie, enzymy,
Předmět: KBB/BB1P Energetika a metabolismus buňky Cíl přednášky: seznámit posluchače s tím, jak buňky získávají energii k životu a jak s ní hospodaří Klíčová slova: energetika buňky, volná energie, enzymy,
Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti. Informace Seminář z biochemie II Laboratorní cvičení z biochemie
 Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti Informace Seminář z biochemie II Laboratorní cvičení z biochemie Pravidla pro udělení klasifikovaného zápočtu ze Semináře z Biochemie
Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti Informace Seminář z biochemie II Laboratorní cvičení z biochemie Pravidla pro udělení klasifikovaného zápočtu ze Semináře z Biochemie
Metabolismus krok za krokem - volitelný předmět -
 Metabolismus krok za krokem - volitelný předmět - Vladimíra Kvasnicová pracovna: 411, tel. 267 102 411, vladimira.kvasnicova@lf3.cuni.cz informace, studijní materiály: http://vyuka.lf3.cuni.cz Sylabus
Metabolismus krok za krokem - volitelný předmět - Vladimíra Kvasnicová pracovna: 411, tel. 267 102 411, vladimira.kvasnicova@lf3.cuni.cz informace, studijní materiály: http://vyuka.lf3.cuni.cz Sylabus
ANABOLISMUS SACHARIDŮ
 zdroj sacharidů: autotrofní org. produkty fotosyntézy heterotrofní org. příjem v potravě důležitou roli hraje GLUKÓZA METABOLISMUS SACHARIDŮ ANABOLISMUS SACHARIDŮ 1. FOTOSYNTÉZA autotrofní org. 2. GLUKONEOGENEZE
zdroj sacharidů: autotrofní org. produkty fotosyntézy heterotrofní org. příjem v potravě důležitou roli hraje GLUKÓZA METABOLISMUS SACHARIDŮ ANABOLISMUS SACHARIDŮ 1. FOTOSYNTÉZA autotrofní org. 2. GLUKONEOGENEZE
IDEÁLNÍ PLYN. Stavová rovnice
 IDEÁLNÍ PLYN Stavová rovnice Ideální plyn ) rozměry molekul jsou zanedbatelné vzhledem k jejich vzdálenostem 2) molekuly plynu na sebe působí jen při vzájemných srážkách 3) všechny srážky jsou dokonale
IDEÁLNÍ PLYN Stavová rovnice Ideální plyn ) rozměry molekul jsou zanedbatelné vzhledem k jejich vzdálenostem 2) molekuly plynu na sebe působí jen při vzájemných srážkách 3) všechny srážky jsou dokonale
B4, 2007/2008, I. Literák
 B4, 2007/2008, I. Literák ENERGIE, KATALÝZA, BIOSYNTÉZA Živé organismy vytvářejí a udržují pořádek ve světě, který spěje k čím dál většímu chaosu Druhá věta termodynamiky: Ve vesmíru nebo jakékoliv izolované
B4, 2007/2008, I. Literák ENERGIE, KATALÝZA, BIOSYNTÉZA Živé organismy vytvářejí a udržují pořádek ve světě, který spěje k čím dál většímu chaosu Druhá věta termodynamiky: Ve vesmíru nebo jakékoliv izolované
Energetický metabolismus rostlin
 Energetický metabolismus rostlin Sylabus - témata (Fischer, Duchoslav) 1. Energie v živých systémech Formy energie a základní principy přeměny energií; změny volné energie, rovnovážná konstanta, spřažení
Energetický metabolismus rostlin Sylabus - témata (Fischer, Duchoslav) 1. Energie v živých systémech Formy energie a základní principy přeměny energií; změny volné energie, rovnovážná konstanta, spřažení
Termodynamika a živé systémy. Helena Uhrová
 Termodynamika a živé systémy Helena Uhrová Základní pojmy termodynamiky soustava izolovaná otevřená okolí vlastnosti soustavy znaky popisující soustavu stav rovnováhy tok m či E =0 funkce stavu - soubor
Termodynamika a živé systémy Helena Uhrová Základní pojmy termodynamiky soustava izolovaná otevřená okolí vlastnosti soustavy znaky popisující soustavu stav rovnováhy tok m či E =0 funkce stavu - soubor
Fyzikální chemie. 1.2 Termodynamika
 Fyzikální chemie. ermodynamika Mgr. Sylvie Pavloková Letní semestr 07/08 děj izotermický izobarický izochorický konstantní V ermodynamika rvní termodynamický zákon (zákon zachování energie): U Q + W izotermický
Fyzikální chemie. ermodynamika Mgr. Sylvie Pavloková Letní semestr 07/08 děj izotermický izobarický izochorický konstantní V ermodynamika rvní termodynamický zákon (zákon zachování energie): U Q + W izotermický
Eva Benešová. Dýchací řetězec
 Eva Benešová Dýchací řetězec Dýchací řetězec Během oxidace látek vstupujících do různých metabolických cyklů (glykolýza, CC, beta-oxidace MK) vznikají NADH a FADH 2, které následně vstupují do DŘ. V DŘ
Eva Benešová Dýchací řetězec Dýchací řetězec Během oxidace látek vstupujících do různých metabolických cyklů (glykolýza, CC, beta-oxidace MK) vznikají NADH a FADH 2, které následně vstupují do DŘ. V DŘ
Energetický metabolismus rostlin
 Energetický metabolismus rostlin Sylabus - témata (Fischer, Šantrůček) 1. Základy energetiky v živých systémech Formy energie a základní principy přeměny energií; změny volné energie, rovnovážná konstanta,
Energetický metabolismus rostlin Sylabus - témata (Fischer, Šantrůček) 1. Základy energetiky v živých systémech Formy energie a základní principy přeměny energií; změny volné energie, rovnovážná konstanta,
Buněčný metabolismus. J. Vondráček
 Buněčný metabolismus J. Vondráček Téma přednášky BUNĚČNÝ METABOLISMUS základní dráhy energetického metabolismu buňky a dynamická podstata jejich regulací glykolýza, citrátový cyklus a oxidativní fosforylace,
Buněčný metabolismus J. Vondráček Téma přednášky BUNĚČNÝ METABOLISMUS základní dráhy energetického metabolismu buňky a dynamická podstata jejich regulací glykolýza, citrátový cyklus a oxidativní fosforylace,
Úvod do buněčného metabolismu Citrátový cyklus. Prof. MUDr. Jiří Kraml, DrSc. Ústav lékařské biochemie 1. LF UK
 Úvod do buněčného metabolismu Citrátový cyklus Prof. MUDr. Jiří Kraml, DrSc. Ústav lékařské biochemie 1. LF UK METABOLISMUS = přeměna látek v organismu - má stránku chemickou (látkovou) - reakce anabolické
Úvod do buněčného metabolismu Citrátový cyklus Prof. MUDr. Jiří Kraml, DrSc. Ústav lékařské biochemie 1. LF UK METABOLISMUS = přeměna látek v organismu - má stránku chemickou (látkovou) - reakce anabolické
Energetický metabolizmus buňky
 Energetický metabolizmus buňky Buňky vyžadují neustálý přísun energie pro tvorbu a udržování biologického pořádku (život). Tato energie pochází z energie chemických vazeb v molekulách potravy (energie
Energetický metabolizmus buňky Buňky vyžadují neustálý přísun energie pro tvorbu a udržování biologického pořádku (život). Tato energie pochází z energie chemických vazeb v molekulách potravy (energie
FYZIKÁLNÍ CHEMIE chemická termodynamika
 FYZIKÁLNÍ CHEMIE chemická termodynamika ermodynamika jako vědní disciplína Základní zákony termodynamiky Práce, teplo a energie Vnitřní energie a entalpie Chemická termodynamika Definice termodynamiky
FYZIKÁLNÍ CHEMIE chemická termodynamika ermodynamika jako vědní disciplína Základní zákony termodynamiky Práce, teplo a energie Vnitřní energie a entalpie Chemická termodynamika Definice termodynamiky
2.4 Stavové chování směsí plynů Ideální směs Ideální směs reálných plynů Stavové rovnice pro plynné směsi
 1. ZÁKLADNÍ POJMY 1.1 Systém a okolí 1.2 Vlastnosti systému 1.3 Vybrané základní veličiny 1.3.1 Množství 1.3.2 Délka 1.3.2 Délka 1.4 Vybrané odvozené veličiny 1.4.1 Objem 1.4.2 Hustota 1.4.3 Tlak 1.4.4
1. ZÁKLADNÍ POJMY 1.1 Systém a okolí 1.2 Vlastnosti systému 1.3 Vybrané základní veličiny 1.3.1 Množství 1.3.2 Délka 1.3.2 Délka 1.4 Vybrané odvozené veličiny 1.4.1 Objem 1.4.2 Hustota 1.4.3 Tlak 1.4.4
Oxidace a redukce. Hoření = slučování s kyslíkem = oxidace. 2 Mg + O 2 2 MgO S + O 2 SO 2. Redukce = odebrání kyslíku
 Oxidace a redukce Hoření = slučování s kyslíkem = oxidace 2 Mg + O 2 2 MgO S + O 2 SO 2 Redukce = odebrání kyslíku Fe 2 O 3 + 3 C 2 Fe + 3 CO CuO + H 2 Cu + H 2 O 1 Oxidace a redukce Širší pojem oxidace
Oxidace a redukce Hoření = slučování s kyslíkem = oxidace 2 Mg + O 2 2 MgO S + O 2 SO 2 Redukce = odebrání kyslíku Fe 2 O 3 + 3 C 2 Fe + 3 CO CuO + H 2 Cu + H 2 O 1 Oxidace a redukce Širší pojem oxidace
8. Chemické reakce Energetika - Termochemie
 - Termochemie TERMOCHEMIE oddíl termodynamiky Tepelné zabarvení chemických reakcí Samovolnost chemických reakcí Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti - Termochemie TERMOCHEMIE
- Termochemie TERMOCHEMIE oddíl termodynamiky Tepelné zabarvení chemických reakcí Samovolnost chemických reakcí Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti - Termochemie TERMOCHEMIE
METABOLISMUS SACHARIDŮ
 METABOLISMUS SACHARIDŮ PRINCIP Rozštěpené sacharidy vstřebávání střevní sliznicí do krevního oběhu dopraveny vrátnicovou žílou do jater. V játrech enzymaticky hexózy štěpeny na GLUKÓZU vyplavována do krve
METABOLISMUS SACHARIDŮ PRINCIP Rozštěpené sacharidy vstřebávání střevní sliznicí do krevního oběhu dopraveny vrátnicovou žílou do jater. V játrech enzymaticky hexózy štěpeny na GLUKÓZU vyplavována do krve
Fyzikální chemie. Magda Škvorová KFCH CN463 magda.skvorova@ujep.cz, tel. 3302. 14. února 2013
 Fyzikální chemie Magda Škvorová KFCH CN463 magda.skvorova@ujep.cz, tel. 3302 14. února 2013 Co je fyzikální chemie? Co je fyzikální chemie? makroskopický přístup: (klasická) termodynamika nerovnovážná
Fyzikální chemie Magda Škvorová KFCH CN463 magda.skvorova@ujep.cz, tel. 3302 14. února 2013 Co je fyzikální chemie? Co je fyzikální chemie? makroskopický přístup: (klasická) termodynamika nerovnovážná
Rychlost chemické reakce
 Reakční kinetika Rychlost chemické reakce A B energeticky minimální reakční cesta Rare event vznik/zánik vazeb ~1-10 fs Náhodnost reakce ~ms až roky P R Rychlost chemické reakce A B energeticky minimální
Reakční kinetika Rychlost chemické reakce A B energeticky minimální reakční cesta Rare event vznik/zánik vazeb ~1-10 fs Náhodnost reakce ~ms až roky P R Rychlost chemické reakce A B energeticky minimální
Termomechanika 4. přednáška
 ermomechanika 4. přednáška Miroslav Holeček Upozornění: ato prezentace slouží výhradně pro výukové účely Fakulty strojní Západočeské univerzity v Plzni. Byla sestavena autorem s využitím citovaných zdrojů
ermomechanika 4. přednáška Miroslav Holeček Upozornění: ato prezentace slouží výhradně pro výukové účely Fakulty strojní Západočeské univerzity v Plzni. Byla sestavena autorem s využitím citovaných zdrojů
Didaktické testy z biochemie 2
 Didaktické testy z biochemie 2 Metabolismus Milada Roštejnská Helena Klímová br. 1. Schéma metabolismu Zažívací trubice Sacharidy Bílkoviny Lipidy Ukládány jako glykogen v játrech Ukládány Ukládány jako
Didaktické testy z biochemie 2 Metabolismus Milada Roštejnská Helena Klímová br. 1. Schéma metabolismu Zažívací trubice Sacharidy Bílkoviny Lipidy Ukládány jako glykogen v játrech Ukládány Ukládány jako
Metabolismus mikroorganismů
 Metabolismus mikroorganismů Metabolismus organismů Souvisí s metabolismem polysacharidů, bílkovin, nukleových kyselin a lipidů Cytoplazma, mitochondrie (matrix, membrána) H 3 PO 4 Polysacharidy Pentózový
Metabolismus mikroorganismů Metabolismus organismů Souvisí s metabolismem polysacharidů, bílkovin, nukleových kyselin a lipidů Cytoplazma, mitochondrie (matrix, membrána) H 3 PO 4 Polysacharidy Pentózový
Buněčné dýchání Ch_056_Přírodní látky_buněčné dýchání Autor: Ing. Mariana Mrázková
 Registrační číslo projektu: CZ.1.07/1.1.38/02.0025 Název projektu: Modernizace výuky na ZŠ Slušovice, Fryšták, Kašava a Velehrad Tento projekt je spolufinancován z Evropského sociálního fondu a státního
Registrační číslo projektu: CZ.1.07/1.1.38/02.0025 Název projektu: Modernizace výuky na ZŠ Slušovice, Fryšták, Kašava a Velehrad Tento projekt je spolufinancován z Evropského sociálního fondu a státního
Termodynamické zákony
 Termodynamické zákony Makroskopická práce termodynamické soustavy Již jsme uvedli, že změna vnitřní energie soustavy je obecně vyvolána dvěma ději: tepelnou výměnou mezi soustavou a okolím a konáním práce
Termodynamické zákony Makroskopická práce termodynamické soustavy Již jsme uvedli, že změna vnitřní energie soustavy je obecně vyvolána dvěma ději: tepelnou výměnou mezi soustavou a okolím a konáním práce
Termodynamika materiálů. Vztahy a přeměny různých druhů energie při termodynamických dějích podmínky nutné pro uskutečnění fázových přeměn
 Termodynamika materiálů Vztahy a přeměny různých druhů energie při termodynamických dějích podmínky nutné pro uskutečnění fázových přeměn Důležité konstanty Standartní podmínky Avogadrovo číslo N A = 6,023.10
Termodynamika materiálů Vztahy a přeměny různých druhů energie při termodynamických dějích podmínky nutné pro uskutečnění fázových přeměn Důležité konstanty Standartní podmínky Avogadrovo číslo N A = 6,023.10
Charakteristika složky 3) cytochrom-c NADH-Q-reduktasa cytochrom-c- oxidasa ubichinon cytochromreduktasa
 8. Dýchací řetězec a fotosyntéza Obtížnost A Pomocí následující tabulky charakterizujte jednotlivé složky mitochondriálního dýchacího řetězce. SLOŽKA Pořadí v dýchacím řetězci 1) Molekulový typ 2) Charakteristika
8. Dýchací řetězec a fotosyntéza Obtížnost A Pomocí následující tabulky charakterizujte jednotlivé složky mitochondriálního dýchacího řetězce. SLOŽKA Pořadí v dýchacím řetězci 1) Molekulový typ 2) Charakteristika
Katalýza / inhibice. Katalýza. Katalyzátory. Inhibitory. katalyzátor: Faktory ovlivňující rychlost chemické reakce. Homogenní
 Katalýza Katalýza / inhibice Homogenní acidobazická (katalyzátor: H + nebo OH - ) autokatalýza (katalyzátor: produkt reakce) selektivní (katalyzátor: enzym) Ovlivnění rychlosti chemické reakce pomocí katalyzátoru
Katalýza Katalýza / inhibice Homogenní acidobazická (katalyzátor: H + nebo OH - ) autokatalýza (katalyzátor: produkt reakce) selektivní (katalyzátor: enzym) Ovlivnění rychlosti chemické reakce pomocí katalyzátoru
Ideální plyn. Stavová rovnice Děje v ideálním plynu Práce plynu, Kruhový děj, Tepelné motory
 Struktura a vlastnosti plynů Ideální plyn Vlastnosti ideálního plynu: Ideální plyn Stavová rovnice Děje v ideálním plynu Práce plynu, Kruhový děj, epelné motory rozměry molekul jsou ve srovnání se střední
Struktura a vlastnosti plynů Ideální plyn Vlastnosti ideálního plynu: Ideální plyn Stavová rovnice Děje v ideálním plynu Práce plynu, Kruhový děj, epelné motory rozměry molekul jsou ve srovnání se střední
LOGO. Struktura a vlastnosti plynů Ideální plyn
 Struktura a vlastnosti plynů Ideální plyn Ideální plyn Protože popsat chování plynů je nad naše možnosti, zavádíme zjednodušený model tzv. ideálního plynu, který má tyto vlastnosti: Částice ideálního plynu
Struktura a vlastnosti plynů Ideální plyn Ideální plyn Protože popsat chování plynů je nad naše možnosti, zavádíme zjednodušený model tzv. ideálního plynu, který má tyto vlastnosti: Částice ideálního plynu
SOIL ECOLOGY the general patterns, and the particular
 Soil Biology topic No. 5: SOIL ECOLOGY the general patterns, and the particular patterns SOIL ECOLOGY is an applied scientific discipline dealing with living components of soil, their activities and THEIR
Soil Biology topic No. 5: SOIL ECOLOGY the general patterns, and the particular patterns SOIL ECOLOGY is an applied scientific discipline dealing with living components of soil, their activities and THEIR
Kapitoly z fyzikální chemie KFC/KFCH. II. Termodynamika
 Kapitoly z fyzikální chemie KFC/KFCH II. Termodynamika Karel Berka Univerzita Palackého v Olomouci Katedra Fyzikální chemie karel.berka@upol.cz Termodynamika therme - teplo a dunamis - síla popis jak systémy
Kapitoly z fyzikální chemie KFC/KFCH II. Termodynamika Karel Berka Univerzita Palackého v Olomouci Katedra Fyzikální chemie karel.berka@upol.cz Termodynamika therme - teplo a dunamis - síla popis jak systémy
součástí našeho každodenního života spalování paliv koroze kovů ad.
 Oxidace a redukce Biochemický ústav LF MU (E.T.) 2012 1 Význam oxidačně-redukčních reakcí Oxidačně-redukční (redoxní) reakce jsou součástí našeho každodenního života metabolismus živin fotosyntéza buněčná
Oxidace a redukce Biochemický ústav LF MU (E.T.) 2012 1 Význam oxidačně-redukčních reakcí Oxidačně-redukční (redoxní) reakce jsou součástí našeho každodenního života metabolismus živin fotosyntéza buněčná
Aktivita CLIL Chemie I.
 Škola: Gymnázium Bystřice nad Pernštejnem Jméno vyučujícího: Mgr. Marie Dřínovská Aktivita CLIL Chemie I. Název aktivity: Uhlíkový cyklus v přírodě Carbon cycle Předmět: Chemie Ročník, třída: kvinta Jazyk
Škola: Gymnázium Bystřice nad Pernštejnem Jméno vyučujícího: Mgr. Marie Dřínovská Aktivita CLIL Chemie I. Název aktivity: Uhlíkový cyklus v přírodě Carbon cycle Předmět: Chemie Ročník, třída: kvinta Jazyk
součástí našeho každodenního života spalování paliv koroze kovů ad.
 Oxidace a redukce Srážecí rovnováhy, součin rozpustnosti Biochemický ústav LF MU (E.T.) 2013 1 Význam oxidačně-redukčních reakcí Oxidačně-redukční (redoxní) reakce jsou součástí našeho každodenního života
Oxidace a redukce Srážecí rovnováhy, součin rozpustnosti Biochemický ústav LF MU (E.T.) 2013 1 Význam oxidačně-redukčních reakcí Oxidačně-redukční (redoxní) reakce jsou součástí našeho každodenního života
soustava - část prostoru s látkovou náplní oddělená od okolí skutečnými nebo myšlenými stěnami okolí prostor vně uvažované soustavy
 Soustava soustava - část prostoru s látkovou náplní oddělená od okolí skutečnými nebo myšlenými stěnami okolí prostor vně uvažované soustavy Okolí Hraniční plocha Soustava Soustava Rozdělení podle vztahu
Soustava soustava - část prostoru s látkovou náplní oddělená od okolí skutečnými nebo myšlenými stěnami okolí prostor vně uvažované soustavy Okolí Hraniční plocha Soustava Soustava Rozdělení podle vztahu
Biosyntéza sacharidů 1
 Biosyntéza sacharidů 1 S a c h a r id y p o tr a v y (š k r o b, g ly k o g e n, sa c h a r o sa, a j.) R e z e r v n í p o ly sa c h a r id y J in é m o n o sa c h a r id y Trávení (amylásy - sliny, pankreas)
Biosyntéza sacharidů 1 S a c h a r id y p o tr a v y (š k r o b, g ly k o g e n, sa c h a r o sa, a j.) R e z e r v n í p o ly sa c h a r id y J in é m o n o sa c h a r id y Trávení (amylásy - sliny, pankreas)
Bp1252 Biochemie. #8 Metabolismus živin
 Bp1252 Biochemie #8 Metabolismus živin Chemické reakce probíhající v organismu Katabolické reakce přeměna složitějších látek na jednoduché, jsou většinou exergonické. Anabolické reakce syntéza složitějších
Bp1252 Biochemie #8 Metabolismus živin Chemické reakce probíhající v organismu Katabolické reakce přeměna složitějších látek na jednoduché, jsou většinou exergonické. Anabolické reakce syntéza složitějších
Termodynamika (td.) se obecně zabývá vzájemnými vztahy a přeměnami různých druhů
 Termodynamika (td.) se obecně zabývá vzájemnými vztahy a přeměnami různých druhů energií (mechanické, tepelné, elektrické, magnetické, chemické a jaderné) při td. dějích. Na rozdíl od td. cyklických dějů
Termodynamika (td.) se obecně zabývá vzájemnými vztahy a přeměnami různých druhů energií (mechanické, tepelné, elektrické, magnetické, chemické a jaderné) při td. dějích. Na rozdíl od td. cyklických dějů
Bioenergetika. přeměny energie v živých organismech
 Bioenergetika přeměny energie v živých organismech Chemiosmotická teorie 1978 Mitchell Nobelova cena na semipermeabilní membráně tvorba elektrochemického gradientu na membráně protonové pumpy protonmotivní
Bioenergetika přeměny energie v živých organismech Chemiosmotická teorie 1978 Mitchell Nobelova cena na semipermeabilní membráně tvorba elektrochemického gradientu na membráně protonové pumpy protonmotivní
Oxidace a redukce. Objev kyslíku nový prvek, vyvrácení flogistonové teorie. Hoření = slučování s kyslíkem = oxidace. 2 Mg + O 2 2 MgO S + O 2 SO 2
 Oxidace a redukce Objev kyslíku nový prvek, vyvrácení flogistonové teorie Hoření = slučování s kyslíkem = oxidace 2 Mg + O 2 2 MgO S + O 2 SO 2 Lavoisier Redukce = odebrání kyslíku Fe 2 O 3 + 3 C 2 Fe
Oxidace a redukce Objev kyslíku nový prvek, vyvrácení flogistonové teorie Hoření = slučování s kyslíkem = oxidace 2 Mg + O 2 2 MgO S + O 2 SO 2 Lavoisier Redukce = odebrání kyslíku Fe 2 O 3 + 3 C 2 Fe
Katabolismus - jak budeme postupovat
 Katabolismus - jak budeme postupovat I. fáze aminokyseliny proteiny polysacharidy glukosa lipidy Glycerol + mastné kyseliny II. fáze III. fáze ETS itrátový cyklus yklus trikarboxylových kyselin, Krebsův
Katabolismus - jak budeme postupovat I. fáze aminokyseliny proteiny polysacharidy glukosa lipidy Glycerol + mastné kyseliny II. fáze III. fáze ETS itrátový cyklus yklus trikarboxylových kyselin, Krebsův
Ukázky z pracovních listů z biochemie pro SŠ A ÚVOD
 Ukázky z pracovních listů z biochemie pro SŠ A ÚVD 1) Doplň chybějící údaje. Jak se značí makroergní vazba? Kolik je v ATP makroergních vazeb? Co je to ADP Kolik je v ADP makroergních vazeb 1) Pojmenuj
Ukázky z pracovních listů z biochemie pro SŠ A ÚVD 1) Doplň chybějící údaje. Jak se značí makroergní vazba? Kolik je v ATP makroergních vazeb? Co je to ADP Kolik je v ADP makroergních vazeb 1) Pojmenuj
Fotosyntéza. Ondřej Prášil
 Fotosyntéza 2 Ondřej Prášil prasil@alga.cz 384-340430 Obsah přednášky membrány a organely světlo termodynamika historie Fotosyntetické membrány Electron tomography Cells contain ~100 chlorosomes appressed
Fotosyntéza 2 Ondřej Prášil prasil@alga.cz 384-340430 Obsah přednášky membrány a organely světlo termodynamika historie Fotosyntetické membrány Electron tomography Cells contain ~100 chlorosomes appressed
Inovace profesní přípravy budoucích učitelů chemie
 Inovace profesní přípravy budoucích učitelů chemie I n v e s t i c e d o r o z v o j e v z d ě l á v á n í CZ.1.07/2.2.00/15.0324 Tento projekt je spolufinancován Evropským sociálním fondem a státním rozpočtem
Inovace profesní přípravy budoucích učitelů chemie I n v e s t i c e d o r o z v o j e v z d ě l á v á n í CZ.1.07/2.2.00/15.0324 Tento projekt je spolufinancován Evropským sociálním fondem a státním rozpočtem
Energetika chemických reakcí
 Energetika chemických reakcí Bioenergetika Kinetika Biochemický ústav LF MU (J.D.) 2013 1 Základní pojmy Systém - část prostoru oddělená od svého okolí izolovaný žádná komunikace s okolím uzavřený výměna
Energetika chemických reakcí Bioenergetika Kinetika Biochemický ústav LF MU (J.D.) 2013 1 Základní pojmy Systém - část prostoru oddělená od svého okolí izolovaný žádná komunikace s okolím uzavřený výměna
Electrochemistry of Selected Phosphorus Oxoacids on a Bulk Pt Electrode. Tomas Bystron Martin Prokop Karel Bouzek
 Electrochemistry of Selected Phosphorus Oxoacids on a Bulk Pt Electrode Tomas Bystron Martin Prokop Karel Bouzek High Temperature PEM Fuel Cell (HT PEM FC) Operation temperature 130-200 C Enhanced rate
Electrochemistry of Selected Phosphorus Oxoacids on a Bulk Pt Electrode Tomas Bystron Martin Prokop Karel Bouzek High Temperature PEM Fuel Cell (HT PEM FC) Operation temperature 130-200 C Enhanced rate
33.Krebsův cyklus. AZ Smart Marie Poštová
 33.Krebsův cyklus AZ Smart Marie Poštová m.postova@gmail.com Metabolismus Metabolismus je souhrn chemických reakcí v organismu. Základní metabolické děje jsou: a) katabolické odbourávací (složité látky
33.Krebsův cyklus AZ Smart Marie Poštová m.postova@gmail.com Metabolismus Metabolismus je souhrn chemických reakcí v organismu. Základní metabolické děje jsou: a) katabolické odbourávací (složité látky
Sacharidy a polysacharidy (struktura a metabolismus)
 Sacharidy a polysacharidy (struktura a metabolismus) Sacharidy Živočišné tkáně kolem 2 %, rostlinné 85-90 % V buňkách rozličné fce: Zdroj a zásobárna energie (glukóza, škrob, glykogen) Výztuž a ochrana
Sacharidy a polysacharidy (struktura a metabolismus) Sacharidy Živočišné tkáně kolem 2 %, rostlinné 85-90 % V buňkách rozličné fce: Zdroj a zásobárna energie (glukóza, škrob, glykogen) Výztuž a ochrana
Elektroenergetika 1. Termodynamika
 Elektroenergetika 1 Termodynamika Termodynamika Popisuje procesy, které zahrnují změny teploty, přeměny energie a vzájemný vztah mezi tepelnou energií a mechanickou prací Opakování fyziky Termodynamický
Elektroenergetika 1 Termodynamika Termodynamika Popisuje procesy, které zahrnují změny teploty, přeměny energie a vzájemný vztah mezi tepelnou energií a mechanickou prací Opakování fyziky Termodynamický
Fotosyntéza (2/34) = fotosyntetická asimilace
 Fotosyntéza (2/34) = fotosyntetická asimilace FOTO - protože k fotosyntéze je třeba fotonů Jedná se tedy o zachycování sluneční energie a přeměnu jednoduchých anorganických látek (CO 2 a H 2 O) na složitější
Fotosyntéza (2/34) = fotosyntetická asimilace FOTO - protože k fotosyntéze je třeba fotonů Jedná se tedy o zachycování sluneční energie a přeměnu jednoduchých anorganických látek (CO 2 a H 2 O) na složitější
Respirace. (buněčné dýchání) O 2. Fotosyntéza Dýchání. Energie záření teplo BIOMASA CO 2 (-COO - ) = -COOH -CHO -CH 2 OH -CH 3
 Respirace (buněčné dýchání) Fotosyntéza Dýchání Energie záření teplo chem. energie CO 2 (ATP, NAD(P)H) O 2 Redukce za spotřeby NADPH BIOMASA CO 2 (-COO - ) = -COOH -CHO -CH 2 OH -CH 3 oxidace produkující
Respirace (buněčné dýchání) Fotosyntéza Dýchání Energie záření teplo chem. energie CO 2 (ATP, NAD(P)H) O 2 Redukce za spotřeby NADPH BIOMASA CO 2 (-COO - ) = -COOH -CHO -CH 2 OH -CH 3 oxidace produkující
Termodynamika. T [K ]=t [ 0 C] 273,15 T [ K ]= t [ 0 C] termodynamická teplota: Stavy hmoty. jednotka: 1 K (kelvin) = 1/273,16 část termodynamické
![Termodynamika. T [K ]=t [ 0 C] 273,15 T [ K ]= t [ 0 C] termodynamická teplota: Stavy hmoty. jednotka: 1 K (kelvin) = 1/273,16 část termodynamické Termodynamika. T [K ]=t [ 0 C] 273,15 T [ K ]= t [ 0 C] termodynamická teplota: Stavy hmoty. jednotka: 1 K (kelvin) = 1/273,16 část termodynamické](/thumbs/24/2778201.jpg) Termodynamika termodynamická teplota: Stavy hmoty jednotka: 1 K (kelvin) = 1/273,16 část termodynamické teploty trojného bodu vody (273,16 K = 0,01 o C). 0 o C = 273,15 K T [K ]=t [ 0 C] 273,15 T [ K ]=
Termodynamika termodynamická teplota: Stavy hmoty jednotka: 1 K (kelvin) = 1/273,16 část termodynamické teploty trojného bodu vody (273,16 K = 0,01 o C). 0 o C = 273,15 K T [K ]=t [ 0 C] 273,15 T [ K ]=
Regulace metabolických drah na úrovni buňky
 Regulace metabolických drah na úrovni buňky EB Obsah přednášky Obecné principy regulace metabolických drah na úrovni buňky regulace zajištěná kompartmentací metabolických dějů změna absolutní koncentrace
Regulace metabolických drah na úrovni buňky EB Obsah přednášky Obecné principy regulace metabolických drah na úrovni buňky regulace zajištěná kompartmentací metabolických dějů změna absolutní koncentrace
Mol. fyz. a termodynamika
 Molekulová fyzika pracuje na základě kinetické teorie látek a statistiky Termodynamika zkoumání tepelných jevů a strojů nezajímají nás jednotlivé částice Molekulová fyzika základem jsou: Látka kteréhokoli
Molekulová fyzika pracuje na základě kinetické teorie látek a statistiky Termodynamika zkoumání tepelných jevů a strojů nezajímají nás jednotlivé částice Molekulová fyzika základem jsou: Látka kteréhokoli
Intermediární metabolismus. Vladimíra Kvasnicová
 Intermediární metabolismus Vladimíra Kvasnicová Vztahy v intermediárním metabolismu (sacharidy, lipidy, proteiny) 1. po jídle (přísun energie z vnějšku) oxidace CO 2, H 2 O, urea + ATP tvorba zásob glykogen,
Intermediární metabolismus Vladimíra Kvasnicová Vztahy v intermediárním metabolismu (sacharidy, lipidy, proteiny) 1. po jídle (přísun energie z vnějšku) oxidace CO 2, H 2 O, urea + ATP tvorba zásob glykogen,
1. Napište strukturní vzorce aminokyselin D a Y a vzorce adenosinu a thyminu
 Test pro přijímací řízení magisterské studium Biochemie 2019 1. Napište strukturní vzorce aminokyselin D a Y a vzorce adenosinu a thyminu U dalších otázek zakroužkujte správné tvrzení (pouze jedna správná
Test pro přijímací řízení magisterské studium Biochemie 2019 1. Napište strukturní vzorce aminokyselin D a Y a vzorce adenosinu a thyminu U dalších otázek zakroužkujte správné tvrzení (pouze jedna správná
Termodynamika 1. UJOP Hostivař 2014
 Termodynamika 1 UJOP Hostivař 2014 Termodynamika Zabývá se tepelnými ději obecně. Existují 3 termodynamické zákony: 1. Celkové množství energie (všech druhů) izolované soustavy zůstává zachováno. 2. Teplo
Termodynamika 1 UJOP Hostivař 2014 Termodynamika Zabývá se tepelnými ději obecně. Existují 3 termodynamické zákony: 1. Celkové množství energie (všech druhů) izolované soustavy zůstává zachováno. 2. Teplo
Elektroenergetika 1. Termodynamika a termodynamické oběhy
 Termodynamika a termodynamické oběhy Termodynamika Popisuje procesy, které zahrnují změny teploty, přeměny energie a vzájemný vztah mezi tepelnou energií a mechanickou prací Opakování fyziky Termodynamický
Termodynamika a termodynamické oběhy Termodynamika Popisuje procesy, které zahrnují změny teploty, přeměny energie a vzájemný vztah mezi tepelnou energií a mechanickou prací Opakování fyziky Termodynamický
>>> E A1 + E A2. . aktivační energie potřebná k reakci bez přítomnosti katalyzátoru E A E A1. energie potřebná ke vzniku enzym-substrátového komplexu
 Enzymy Charakteristika enzymů- fermentů katalyzátory biochem. reakcí biokatalyzátory umožňují a urychlují průběh rcí v organismu nachází se ve všech živých systémech z chemického hlediska jednoduché nebo
Enzymy Charakteristika enzymů- fermentů katalyzátory biochem. reakcí biokatalyzátory umožňují a urychlují průběh rcí v organismu nachází se ve všech živých systémech z chemického hlediska jednoduché nebo
CHEMICKÁ ENERGETIKA. Celá termodynamika je logicky odvozena ze tří základních principů, které mají axiomatický charakter.
 CHEMICKÁ ENERGETIKA Energetickou stránkou soustav a změnami v těchto soustavách se zabývá fyzikální disciplína termodynamika. Z široké oblasti obecné termodynamiky se chemická termodynamika zajímá o chemické
CHEMICKÁ ENERGETIKA Energetickou stránkou soustav a změnami v těchto soustavách se zabývá fyzikální disciplína termodynamika. Z široké oblasti obecné termodynamiky se chemická termodynamika zajímá o chemické
Dýchací řetězec, oxidativní fosforylace, mitochondriální transportní systémy
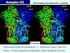 Dýchací řetězec, oxidativní fosforylace, mitochondriální transportní systémy JAN ILLNER Dýchací řetězec & oxidativní fosforylace Tvorba energie v živých systémech ATP zdroj E pro biochemické procesy Tvorba
Dýchací řetězec, oxidativní fosforylace, mitochondriální transportní systémy JAN ILLNER Dýchací řetězec & oxidativní fosforylace Tvorba energie v živých systémech ATP zdroj E pro biochemické procesy Tvorba
BIOCHEMIE. František Vácha.
 BIOCHEMIE František Vácha http://www.prf.jcu.cz/~vacha/ Doporučená literatura: D.L. Nelson, M.M. Cox Lehninger Principles of Biochemistry D.J. Voet, J.G. Voet, C.W. Pratt Principles of Biochemistry L.
BIOCHEMIE František Vácha http://www.prf.jcu.cz/~vacha/ Doporučená literatura: D.L. Nelson, M.M. Cox Lehninger Principles of Biochemistry D.J. Voet, J.G. Voet, C.W. Pratt Principles of Biochemistry L.
Glykolýza Glukoneogeneze Regulace. Alice Skoumalová
 Glykolýza Glukoneogeneze Regulace Alice Skoumalová Metabolismus glukózy - přehled: 1. Glykolýza Glukóza: Univerzální palivo pro buňky Zdroje: potrava (hlavní cukr v dietě) zásoby glykogenu krev (homeostáza
Glykolýza Glukoneogeneze Regulace Alice Skoumalová Metabolismus glukózy - přehled: 1. Glykolýza Glukóza: Univerzální palivo pro buňky Zdroje: potrava (hlavní cukr v dietě) zásoby glykogenu krev (homeostáza
IDEÁLNÍ PLYN 14. TEPELNÉ STROJE, PRVNÍ A DRUHÝ TERMODYNAMICKÝ ZÁKON
 IDEÁLNÍ PLYN 14. TEPELNÉ STROJE, PRVNÍ A DRUHÝ TERMODYNAMICKÝ ZÁKON Autor: Ing. Eva Jančová DESS SOŠ a SOU spol. s r. o. TEPELNÝ STROJ Tepelný stroj je stroj, který pracuje na základě prvního termodynamického
IDEÁLNÍ PLYN 14. TEPELNÉ STROJE, PRVNÍ A DRUHÝ TERMODYNAMICKÝ ZÁKON Autor: Ing. Eva Jančová DESS SOŠ a SOU spol. s r. o. TEPELNÝ STROJ Tepelný stroj je stroj, který pracuje na základě prvního termodynamického
Chemie Ch3 volitelný předmět pro 4. ročník
 Chemie Ch3 volitelný předmět pro 4. ročník Charakteristika vyučovacího předmětu Vyučovací předmět vychází ze vzdělávací oblasti Člověk a příroda, vzdělávacího oboru Chemie. Mezipředmětové přesahy a vazby
Chemie Ch3 volitelný předmět pro 4. ročník Charakteristika vyučovacího předmětu Vyučovací předmět vychází ze vzdělávací oblasti Člověk a příroda, vzdělávacího oboru Chemie. Mezipředmětové přesahy a vazby
Předmět: KBB/BB1P; KBB/BUBIO
 Předmět: KBB/BB1P; KBB/BUBIO Energie z mitochondrií a chloroplastů Cíl přednášky: seznámit posluchače se základními principy získávání energie v mitochondriích a chloroplastech Klíčová slova: mitochondrie,
Předmět: KBB/BB1P; KBB/BUBIO Energie z mitochondrií a chloroplastů Cíl přednášky: seznámit posluchače se základními principy získávání energie v mitochondriích a chloroplastech Klíčová slova: mitochondrie,
DYNAMICKÁ BIOCHEMIE. Daniel Nechvátal :: www.gymzn.cz/nechvatal
 DYNAMICKÁ BIOCHEMIE Daniel Nechvátal :: www.gymzn.cz/nechvatal Energetický metabolismus děje potřebné pro zabezpečení života organismu ANABOLISMUS skladné reakce, spotřeba E KATABOLISMUS rozkladné reakce,
DYNAMICKÁ BIOCHEMIE Daniel Nechvátal :: www.gymzn.cz/nechvatal Energetický metabolismus děje potřebné pro zabezpečení života organismu ANABOLISMUS skladné reakce, spotřeba E KATABOLISMUS rozkladné reakce,
14. Fyziologie rostlin - fotosyntéza, respirace
 14. Fyziologie rostlin - fotosyntéza, respirace Metabolismus -přeměna látek a energií (informací) -procesy: anabolický katabolický autotrofie Anabolismus heterotrofie Autotrofní organismy 1. Chemoautotrofy
14. Fyziologie rostlin - fotosyntéza, respirace Metabolismus -přeměna látek a energií (informací) -procesy: anabolický katabolický autotrofie Anabolismus heterotrofie Autotrofní organismy 1. Chemoautotrofy
je část změny celkové energie schopná konat práci, když systém směřuje k rovnováze (za konstantního P a T). aa + bb cc + dd.
 BIOENERGETIA Základním znakem živých organismů je vysoký stupeň organisovanosti. Ve sání s okolím mají vysoký stupeň strukturní uspořádanosti. To se týká i energetického aparátu. Živý organismus je otevřeným
BIOENERGETIA Základním znakem živých organismů je vysoký stupeň organisovanosti. Ve sání s okolím mají vysoký stupeň strukturní uspořádanosti. To se týká i energetického aparátu. Živý organismus je otevřeným
Melting the ash from biomass
 Ing. Karla Kryštofová Rožnov pod Radhoštěm 2015 Introduction The research was conducted on the ashes of bark mulch, as representatives of biomass. Determining the influence of changes in the chemical composition
Ing. Karla Kryštofová Rožnov pod Radhoštěm 2015 Introduction The research was conducted on the ashes of bark mulch, as representatives of biomass. Determining the influence of changes in the chemical composition
Molekulová fyzika a termika. Přehled základních pojmů
 Molekulová fyzika a termika Přehled základních pojmů Kinetická teorie látek Vychází ze tří experimentálně ověřených poznatků: 1) Látky se skládají z částic - molekul, atomů nebo iontů, mezi nimiž jsou
Molekulová fyzika a termika Přehled základních pojmů Kinetická teorie látek Vychází ze tří experimentálně ověřených poznatků: 1) Látky se skládají z částic - molekul, atomů nebo iontů, mezi nimiž jsou
Thermos teplo Dynamic změna
 Termodynamika Plán přednášky: Předmět studia Základní pojmy Termodynamické zákony předmět studia Co je to termodynamika? Soubor matematických modelů a představ, které nám umožňují popsat jakým způsobem
Termodynamika Plán přednášky: Předmět studia Základní pojmy Termodynamické zákony předmět studia Co je to termodynamika? Soubor matematických modelů a představ, které nám umožňují popsat jakým způsobem
Biologie 30 Metabolismus, fotosyntéza, dýchání, glykolýza, kvašení
 Číslo projektu CZ.1.07/1.5.00/34.0743 Název školy Autor Tematická oblast Moravské gymnázium Brno s.r.o. RNDr. Monika Jörková Biologie 30 Metabolismus, fotosyntéza, dýchání, glykolýza, kvašení Ročník 1.
Číslo projektu CZ.1.07/1.5.00/34.0743 Název školy Autor Tematická oblast Moravské gymnázium Brno s.r.o. RNDr. Monika Jörková Biologie 30 Metabolismus, fotosyntéza, dýchání, glykolýza, kvašení Ročník 1.
1. ročník Počet hodin
 SOUSTAVY LÁTEK A JEJICH SLOŽENÍ rozdělení přírodních látek a vlastnosti chemických látek soustavy látek a jejich složení STAVBA ATOMU historie pohledu na atom složení a struktura atomu stavba atomu VELIČINY
SOUSTAVY LÁTEK A JEJICH SLOŽENÍ rozdělení přírodních látek a vlastnosti chemických látek soustavy látek a jejich složení STAVBA ATOMU historie pohledu na atom složení a struktura atomu stavba atomu VELIČINY
BUŇKA A ENERGIE. kajman brýlový Caiman crocodilus Kostarika, Biologie 8, 2017/2018, Ivan Literák
 BUŇKA A ENERGIE kajman brýlový Caiman crocodilus Kostarika, 2004 Biologie 8, 2017/2018, Ivan Literák ENERGIE, KATALÝZA, BIOSYNTÉZA Živé organismy vytvářejí a udržují POŘÁDEK VE SVĚTĚ, KTERÝ SPĚJE K ČÍM
BUŇKA A ENERGIE kajman brýlový Caiman crocodilus Kostarika, 2004 Biologie 8, 2017/2018, Ivan Literák ENERGIE, KATALÝZA, BIOSYNTÉZA Živé organismy vytvářejí a udržují POŘÁDEK VE SVĚTĚ, KTERÝ SPĚJE K ČÍM
VYBRANÉ STATĚ Z PROCESNÍHO INŢENÝRSTVÍ cvičení 12
 UNIVERZITA TOMÁŠE BATI VE ZLÍNĚ FAKULTA APLIKOVANÉ INFORMATIKY VYBRANÉ STATĚ Z PROCESNÍHO INŢENÝRSTVÍ cvičení 2 Termodynamika reálných plynů část 2 Hana Charvátová, Dagmar Janáčová Zlín 203 Tento studijní
UNIVERZITA TOMÁŠE BATI VE ZLÍNĚ FAKULTA APLIKOVANÉ INFORMATIKY VYBRANÉ STATĚ Z PROCESNÍHO INŢENÝRSTVÍ cvičení 2 Termodynamika reálných plynů část 2 Hana Charvátová, Dagmar Janáčová Zlín 203 Tento studijní
Termodynamika v biochemii
 Termodynamika v biochemii Studium energetických změn Klasická x statistická Rovnovážná x nerovnovážná lineárn rní a nelineárn rní Základní pojmy Makroskopický systém, okolí systému Termodynamický systém
Termodynamika v biochemii Studium energetických změn Klasická x statistická Rovnovážná x nerovnovážná lineárn rní a nelineárn rní Základní pojmy Makroskopický systém, okolí systému Termodynamický systém
13 Oxidačně redukční reakce
 13 Oxidačně redukční reakce Oxidaci a redukci ve smyslu elektronových představ chápeme jako odevzdávání a přibírání elektronů. Kdykoliv se nějaká látka (atom, molekula, ion) oxiduje, odevzdává elektrony
13 Oxidačně redukční reakce Oxidaci a redukci ve smyslu elektronových představ chápeme jako odevzdávání a přibírání elektronů. Kdykoliv se nějaká látka (atom, molekula, ion) oxiduje, odevzdává elektrony
METABOLISMUS MONOSACHARIDŮ
 METABOLISMUS MONOSACHARIDŮ Metabolismus monosacharidů (zejména jejich katabolismus) je prakticky metabolismem glukosy. Ostatní monosacharidy z ní v případě potřeby vznikají, nebo jsou na ni několika reakcemi
METABOLISMUS MONOSACHARIDŮ Metabolismus monosacharidů (zejména jejich katabolismus) je prakticky metabolismem glukosy. Ostatní monosacharidy z ní v případě potřeby vznikají, nebo jsou na ni několika reakcemi
