Úvod do strukturní analýzy farmaceutických látek
|
|
|
- Karel Šimek
- před 6 lety
- Počet zobrazení:
Transkript
1 Úvod do strukturní analýzy farmaceutických látek Garant předmětu: doc. Ing. Bohumil Dolenský, Ph.D. A28, linka 4110, Hmotnostní spektrometrie I. Příprava předmětu byla podpořena projektem OPPA č. CZ.2.17/3.1.00/33253
2 Hmotnostní spektrometrie ( MS, Mass Spectrometry ) Vzorek Hmotnostní spektrometr Elementární a isotopové složení vzorku Hmotnostní spektrum Informace o struktuře organických látek a biomolekul Stanovení fyzikálněchemických vlastností iontů a molekul Kvalitativní a kvantitativní složení vzorku. Knihovny spekter
3 Hmotnostní spektrometrie ( MS, Mass Spectrometry ) Hmotnostní spektrometrie je fyzikálně-chemická metoda analýzy látek spočívající v převedení látek na plynné ionty, jejich rozdělení dle náboje a hmotnosti interakcí s magnetickým a elektrickým polem, a následné detekci odrážející jejich množství. Hmotnostní spektrometrie není spektrální metodou (nedochází k interakci s elektromagnetickým zářením), avšak pro podobnost výstupu se mezi spektrální metody formálně řadí. Termín hmotnostní spektroskopie je zcela nesprávný. Definitions of terms relating to mass spectrometry (IUPAC Recommendations 2013) Pure Appl. Chem., 2013, 85 (7), Mass Spec Terms Project
4 Hmotnostní spektrometrie ( MS, Mass Spectrometry ) Výhody vysoká citlivost rozsáhlé databáze malých molekul informace o velikosti molekuly a jejich fragmentů variabilita MS experimentů; od identifikace malých molekul po sekvenování proteinů a nukleových kyselin; od plynných a kapalných vzorků po skenování povrchů Nevýhody destruktivní metoda (obvyklé množství vzorku jsou ng až µg) vysoké pořizovací a provozní náklady
5 Hmotnostní spektrum Základní pík Molekulový ion M Isotopové píky [M+1] + C 4 H + 7 a/nebo C 2 H 3 O m/z = 98 O + C 5 H 7 O + CH 3 + a/nebo 83 15
6 Hmotnostní spektrometrie v analýze organických látek a biomolekul Sumární vzorec Strukturní fragmenty Fragmentace molekuly Isotopové zastoupení Ekvivalent dvojných vazeb 2D struktura (konstituce) částečně 3D struktura (konformace) (konfigurace) (stereochemie) Funkční skupiny
7 Hmotnostní spektrometr je iontově-optické zařízení, které rozlišuje ionty podle hodnoty poměru m/z m... je relativní hmotnost iontu, z... je množství náboje iontu bez udané polarity m/z... (Od označení Thomson (Th) či mass-to-charge se upouští). Zkratka vyjadřuje bezrozměrné množství vzniklé vydělením hmotnosti iontu atomovou hmotnostní jednotkou a jeho nábojem (bez ohledu na jeho znaménko). Dalton (Da) 1 Da = 1 u = (10) kg = atomové hmotnostní jednotce u (unified atomic mass unit, = 1/12 hmotnosti 12 C) Nejčastěji se používá v biologii pro molekulové hmotnosti proteinů (kda)
8 Hmotnostní spektrometr Hmotnostní spektrometr se skládá z několika základních částí: Vstup vzorku Ionizace a zplynění Separace iontů Přímý vstup nebo spojení s plynovou (GC-MS) či kapalinovou (LC-MS) chromatografií; též TLC-MS Zásadní vliv na získaná data (informace) a využitelnost MS Hmotnostní analyzátor. Separátorů je obvykle řazeno více, buď pro zvýšení rozlišení nebo pro snadné měření MS-MS, MS n, nebo pro reakce iontů Detekce iontů Hmotnostní spektrum
9 Hmotnostní spektrum ( MS spektrum ) Zobrazuje závislost intenzity iontů daného m/z. Intenzita daného iontu odráží jeho množství v ionizovaném vzorku. Spektrum se normalizuje k základnímu píku (base peak, nejintenzivnější pík spektra). Získané profilové (kontinuální) spektrum gaussovský tvar píků kontrola kvality záznamu velké množství dat se obvykle převádí na čárové (centroidální) spektrum. pozice čáry odpovídá středu píku intenzita ploše či výšce píku menší množství dat nelze převézt zpět na profilové spektrum
10 Hmotnostní spektrum ( MS spektrum ) Ion prekurzoru - ion, který reaguje za vzniku konkrétních produktových iontů (od termínu rodičovský ion se upouští). Produktový ion - vzniká jako produkt po reakci z jednotlivých iontů prekurzoru disociací (fragmentový ion), reakcí iontu s molekulou, nebo změnou počtu nábojů. (od termínu "dceřiný ion se upouští). Fragmentový ion - produktový ion vzniklý disociací iontu prekurzoru. Aduktový ion - ion tvořený interakcí iontu s jedním či více atomy nebo molekulami, např.: [M+Na] +, [M+K] +, [M+Cl] -, atd. (tzv. kvazi-či pseudo-molekulové ionty) Molekulový ion - Ion vzniklý odtržením jednoho či více elektronů z molekuly (vznik pozitivního iontu) nebo přidáním jednoho či více elektronů k molekule (vznik negativního iontu). Isotopový ion ( isotopové satelity ) Ionty stejného prvkového složení, lišící se složením isotopovým.
11 Hmotnostní spektrum Exact mass iontů Prvek je definován přirozeným zastoupením isotopů stejného protonového čísla. Isotopy prvku se liší počtem neutronů v jádře (atomovým číslem), tj. hmotností. Např.: uhlík obsahuje 98,90 % isotopu 12 C a 1,10 isotopu 13 C m ( 12 C) = 12, Sumární vzorec iontu m ( 13 C) = 13, Průměrná hmotnost uhlíku = 0,989 * m ( 12 C) + 0,011 * m ( 13 C) = 12,011 Stupeň nenasycenosti V hmotnostní spektrometrii se isotopy prvků rozlišují
12 Molekulový ion [M] Ion s nejvyšším m/z ve spektru muže, ale nemusí být molekulový 2. Molekulový ion je vždy ion-radikál s lichým počtem elektronů 3. Z molekuly se odštěpují smysluplné fragmenty radikály m/z 15, 29, 43 (alkyl), 19 (F), 35 (Cl), 79 (Br), 31 (OCH 3 ), aj. nebo molekuly 18 (H 2 O), 20 (HF), 28 (CO nebo C 2 H 4 nebo N 2 ), 32 (CH 3 OH), 36 (HCl) aj. 4. Zakázané ztráty: m/z = 3 14, neodpovídají žádné reálné fragmentaci molekulového iontu 5. Dusíkové pravidlo: vzhledem k tomu, že dusík je trojvazný, ale jeho majoritní isotop ( 14 N) má sudou nominální hmotnost pak dle počtu dusíků v molekule pozorujeme nominální hmotnosti: a) lichý počet = lichý M + a sudé fragmenty b) sudý počet nebo žádný dusík = sudý M+ a liché fragmenty Molekulová hmotnost Sumární vzorec molekuly
13 Average mass M AV Průměrná hmotnost ~ Molární hmotnost Hmotnost iontu nebo molekuly zohledňující isotopové složení. Exact mass Správná hmotnost Vypočítaná hmotnost iontu nebo molekuly daného isotopového složení. Accurate mass Přesná hmotnost Experimentálně stanovená hmotnost iontu o známém náboji. Nezaměňovat s předchozí. Lze využít pro stanovení elementárního složení iontu. Monoisotopic mass M MONO Monoisotopická hmotnost Exact hmotnost iontu nebo molekuly vypočtená užitím hmotnosti nejvíce zastoupeného isotopu pro každý prvek. Nominal mass Nominální hmotnost Hmotnost iontu nebo molekuly vypočtená užitím hmotnosti nejvíce zastoupeného isotopu pro každý prvek zaokrouhlenou na celé číslo.
14 Spektrometry s nízkým rozlišením umožňují rozlišit ionty lišící se alespoň o m/z 1 m/z (C 2 H 4 ) = 28 m/z (CO) = 28 m/z (N 2 ) = 28 Spektrometry s vysokým rozlišením umožňují rozlišit i ionty o stejné nominální hmotnosti. m/z (C 2 H 4 ) = 28,0313 m/z (CO) = 27,9949 m/z (N 2 ) = 28,0062 Rozlišovací schopnost ( RP ) RP = m/z m/z + m/z dva stejně vysoké píky jednotkového náboje mající překryv s údolím v 10% jejich výšky též používáno RP = m/z m/z m/z je šířka píku m/z v 50% jeho výšky. (též se používá v 5% či v 0,5% jeho výšky)
15 ESI (nanoelectrospray) MS spektrum apomyoglobinu (koňské srdce) voda/acetonitril s 1% HCOOH
16 Hmotnostní spektrum (ESI + ) hemoglobinu je náboj píku rozdíl nábojů mezi píky a hmotnost iontu s nábojem molární hmotnost proteinu molární hmotnost vodíku
17 Hmotnostní spektrum (ESI + ) hemoglobinu
18 Hmotnostní spektrum Exact mass iontů Isotopové složení iontů Sumární vzorec Původ studované látky Stupeň nenasycenosti
19 Přírodní zastoupení isotopů prvků běžných organických sloučenin Prvek M NOM M % M NOM M+1 % M NOM M+2 % Typ H ,015 M C ,1 M+1 N ,37 M+1 O , ,2 M+2 F M Si ,1 30 3,4 M+2 P M S , ,4 M+2 Cl M+2 Br ,3 M+2 I M
20 Nominal mass m/z (C 2 H 4 ) = 28 m/z (CO) = 28 m/z (N 2 ) = 28 Exact mass m/z (C 2 H 4 ) = 28,0313 m/z (CO) = 27,9949 m/z (N 2 ) = 28,0062 Isotopové klastry (%)
21 Isotopový klastr - Skupina píků reprezentující ionty stejného prvkového složení, inzulín C 257 H 383 N 65 O 77 S 6 lišící se však odlišným isotopovým složením. Accurate monoisotopic mass = 5803,64 Exact monoisotopic mass = 5803, Principal ion nejintenzivnější ion isotopového klastru Nominal mass = 5801 Average mass = 5807,59 Exact mass Average mass
22 Hmotnostní spektrum Přesná hmotnost molekulárního iontu s nábojem z = 1 Hmotnost molekulárního iontu s nábojem z > 1 Isotopový klastr Elementární analýza Empirický vzorec Sumární vzorec NMR ( stanovení molární hmotnosti )
23 Sumární vzorec = Molekulový vzorec udává prvky z nichž se látka skládá a skutečný počet jejich atomů v molekule sloučeniny. Stechiometrický vzorec udává pouze poměr atomů v sloučenině, tj. bez ohledu na skutečný počet atomů v molekule. Empirický stechiometrický vzorec = Empirický vzorec stechiometrický vzorec neznáme sloučeniny stanovený kvantitativní prvkovou analýzou (např.: elementární analýzou). Konstituční vzorec V konstitučním vzorci zobrazuje spojení jednotlivých atomů pomocí jednoduchých, zdvojených či ztrojených úseček (v případě potřeby zakřivených čar), znázorňující vazby mezi atomy (jednoduché, dvojnéči trojné vazby). Přitom délka spojovacích úseček a úhly mezi sousedními úsečkami nevyjadřují ani skutečnou délku vazeb v molekuly, ani skutečné úhly mezi vazbami.
24 Ekvivalent dvojných vazeb (DBE) Číslo (stupeň) nenasycenosti ( UN... Unsaturation Number ) Ekvivalent dvojných vazeb ( BDE... Double Bond Ekvivalent ) Ekvivalent dvojných vazeb a ( RDBE... Ring Double Bond Ekvivalent ) kruhů (EDK) ( PBoR... Pi Bonds or Rings ) DBE odráží kolik je v molekule daného sumárního vzorce násobných vazeb a cyklů Informace o počtu cyklů a násobných vazeb Test na funkční skupiny a substruktury Ověření správnosti sumárního vzorce
25 Výpočet DBE ze známé struktury DBE = počet dvojných vazeb + počet cyklů + 2 * počet trojných vazeb C H 3 COOH C H 3 N NO 2 O O HO CF 3 O Cl CH 3 N NH O O NH O H 3 C CH 3 OH O CHO O 2 N N N COOH SO 3 H Řešení: 2, 6, 3, 3, 7, 7, 1, 4, 13, 6, 14
26 Ekvivalent dvojných vazeb (DBE) ze sumárního vzorce Obecné vzorce neobsahují všechny prvky ani jejich možné valence pro C a H b O c N d X e (X = F, Cl, Br, I) DBE = a (b+e)/2 + d/2 + 1 Obsahuje-li sumární vzorec prvky, které mohou nabývat různých vazností, např. síra je dvojvazná v sulfidech, čtyřvazná v sulfoxidech a šestivazná v sulfonových kyselinách, dusík je trojvazný v aminech či pyridinu, ale pětivazný v nitroderivátech, pak je nutné uvažovat všechny možnosti, a zde běžné vzorce selhávají.
27 Ekvivalent dvojných vazeb (DBE) ze sumárního vzorce Výpočet DBE úvahou nad vazností obsažených prvků: 1. Spočítejme valence vícevazných atomů (dvouvazné lze vynechat). např.: C 6 H 11 ClO * 4 = 24 např.: C 12 H 11 F 3 N 2 O * * 3 = Odečtěme valence nezbytné k jejich propojení; pro n atomů je to 2*(n-1) valencí. např.: C 6 H 11 ClO * (6 1) = 14 např.: C 12 H 11 F 3 N 2 O * (14 1) = Odečteme počet valencí jednovazných atomů. např.: C 6 H 11 ClO = 2 např.: C 12 H 11 F 3 N 2 O = Zbylé valence vydělíme dvěmi. např.: C 6 H 11 ClO / 2 = 1 BDE = 1 např.: C 12 H 11 F 3 N 2 O / 2 = 7 BDE = 7
28 Interpretace DBE Hodnota DBE musí být celé kladnéčíslo nebo nula. Pokud ji nemá je sumární vzorec nesprávný. DBE = 0 Molekula neobsahuje žádnou násobnou vazbu ani žádný cyklus. DBE = 1 Molekula obsahuje jednu dvojnou vazbu nebo jeden cyklus. DBE = 2 Molekula obsahuje dvě dvojné vazby nebo dva cykly nebo jednu dvojnou vazbu a jeden cyklus nebo jednu trojnou vazbu. DBE = 3 Molekula obsahuje 0 3 dvojné vazby, 0 3 cykly, 0 1 trojné vazby
29 Accurate mass Molární hmotnost Elementární analýza výpočet Sumární vzorec výpočet Exact mass Elementární složení
30 Elementární analýza ( EA, Elemental analysis ) Elementární analýza poskytuje hmotnostní podíl jednotlivých prvků v analyzovaném vzorku. Obvykle vyjádřen v hmotnostních procentech. Je-li vzorek čistou látkou, pak obsah odpovídá hmotnostnímu podílu jednotlivých prvků v molekule dané látky. Je-li znám sumárníči alespoň empirický vzorec látky lze hmotnostní podíly snadno vypočítat. Výpočet ze sumárního vzorce např.: C 12 H 11 F 3 N 2 O 2 %C = 12 * A r (C) * 100 M r (C 12 H 11 F 3 N 2 O 2 ) = 52,93 %H = 11 * A r (H) * 100 M r (C 12 H 11 F 3 N 2 O 2 ) 3 * A r (F) * 100 = 4,07 %F = = 20,95 M r (C 12 H 11 F 3 N 2 O 2 ) %N = 2 * A r (N) * 100 M r (C 12 H 11 F 3 N 2 O 2 ) 2 * A r (O) * 100 = 10,29 %O = = 11,76 M r (C 12 H 11 F 3 N 2 O 2 )
31 Elementární analýza Empirický vzorec EA 53,15 %C 4,12 %H 10,05 %N 21,74 %F = 10,94 %O Pokud látka obsahuje již jen jeden prvek, který je znám (např. kyslík), lze jeho obsah dopočítat a získat tak úplný empirický vzorec. Pokud látka obsahuje neznámý prvek nebo nečistotu neobsahující stanovované prvky, pak získáme pouze molární poměr stanovovaných prvků v molekule. Pokud látka obsahuje neznámou nečistotu obsahující stanovované prvky, pak je interpretace nemožná. Pokud experimentální EA neodpovídá očekávané, pak je vhodné zvážit existenci solvátů látky pro EA jsou obvykle čištěny krystalizací. EA směsi látek lze vypočíst analogicky jako u čistých látek jen je nutné zahrnout jejich obsah, např.: C 12 H 11 F 3 N 2 O 2.½CHCl 3 budeme uvažovat jako molekulu C 12,5 H 11,5 F 3 N 2 O 2 Cl 1,5 K ověření správnosti vypočteného vzorce lze využít: a) zpětný výpočet obsahu prvků; b) hodnotu DBE, která musí být celočíselná; c) NMR spektra; d) MS data.
32 Elementární analýza Empirický vzorec EA 53,15 %C 4,12 %H 10,05 %N 21,74 %F = 10,94 %O A r 12,011 1,008 14,007 18,998 15,999 EA / A r 4,425 4,087 0,717 1,144 0,684 DBE / min 6,17 5,70 1,00 1,60 0,95 zokrouhlit ,5 EA calc 49,32 % 4,14 % 9,59 % 26,00 % 10,95 % rozdíl EA -3,83 +0,02-0,46 +4,26 +0,01 * 2 12,34 11,40 2,00 3,20 1,90 zokrouhlit ,0 EA calc 52,93 % 4,07 % 10,29 % 20,95 % 11,76 % rozdíl EA -0,22-0,05 +0,24-0,79 +0,82 * 4 24,68 22,80 4,00 6,40 3,80 zokrouhlit ,5 EA calc 53,84 % 4,16 % 10,05 % 20,46 % 11,48 % rozdíl EA +0,69 +0,04 0,00-1,28 +0,54
33 Elementární analýza ( EA, Elemental analysis ) 6 5 Limity elementární analýzy 4 %C (alkenu) %C (alkanu) C 41 H 84 nebo C 41 H
Úvod do strukturní analýzy farmaceutických látek
 Úvod do strukturní analýzy farmaceutických látek Garant předmětu: doc. Ing. Bohumil Dolenský, Ph.D. A28, linka 4110, dolenskb@vscht.cz Hmotnostní spektrometrie I. Příprava předmětu byla podpořena projektem
Úvod do strukturní analýzy farmaceutických látek Garant předmětu: doc. Ing. Bohumil Dolenský, Ph.D. A28, linka 4110, dolenskb@vscht.cz Hmotnostní spektrometrie I. Příprava předmětu byla podpořena projektem
Úvod do strukturní analýzy farmaceutických látek
 Úvod do strukturní analýzy farmaceutických látek Garant předmětu: doc. Ing. Bohumil Dolenský, Ph.D. A28, linka 4110, dolenskb@vscht.cz Hmotnostní spektrometrie II. Příprava předmětu byla podpořena projektem
Úvod do strukturní analýzy farmaceutických látek Garant předmětu: doc. Ing. Bohumil Dolenský, Ph.D. A28, linka 4110, dolenskb@vscht.cz Hmotnostní spektrometrie II. Příprava předmětu byla podpořena projektem
INTERPRETACE HMOTNOSTNÍCH SPEKTER
 INTERPRETACE HMOTNOSTNÍCH SPEKTER Hmotnostní spektrometrie hmotnostní spektrometrie = fyzikálně chemická metoda založená na rozdělení hmotnosti iontů v plynné fázi podle jejich poměru hmotnosti a náboje
INTERPRETACE HMOTNOSTNÍCH SPEKTER Hmotnostní spektrometrie hmotnostní spektrometrie = fyzikálně chemická metoda založená na rozdělení hmotnosti iontů v plynné fázi podle jejich poměru hmotnosti a náboje
Autoři: Pavel Zachař, David Sýkora Ukázky spekter k procvičování na semináři: Tento soubor je pouze prvním ilustrativním seznámením se základními prin
 Autoři: Pavel Zachař, David Sýkora Ukázky spekter k procvičování na semináři: Tento soubor je pouze prvním ilustrativním seznámením se základními principy hmotnostní spektrometrie a v žádném případě nezahrnuje
Autoři: Pavel Zachař, David Sýkora Ukázky spekter k procvičování na semináři: Tento soubor je pouze prvním ilustrativním seznámením se základními principy hmotnostní spektrometrie a v žádném případě nezahrnuje
SPEKTROSKOPIE NUKLEÁRNÍ MAGNETICKÉ REZONANCE
 SPEKTROSKOPIE NUKLEÁRNÍ MAGNETICKÉ REZONANCE Obecné základy nedestruktivní metoda strukturní analýzy zabývá se rezonancí atomových jader nutná podmínka pro měření spekter: nenulový spin atomového jádra
SPEKTROSKOPIE NUKLEÁRNÍ MAGNETICKÉ REZONANCE Obecné základy nedestruktivní metoda strukturní analýzy zabývá se rezonancí atomových jader nutná podmínka pro měření spekter: nenulový spin atomového jádra
HMOTNOSTNÍ SPEKTROMETRIE
 HMOTNOSTNÍ SPEKTROMETRIE MASS SPECTROMETRY (MS) Alternativní názvy (spojení s GC, LC, CZE, ITP): Hmotnostně spektrometrický (selektivní) detektor Mass spectrometric (selective) detector (MSD) Spektrometrie
HMOTNOSTNÍ SPEKTROMETRIE MASS SPECTROMETRY (MS) Alternativní názvy (spojení s GC, LC, CZE, ITP): Hmotnostně spektrometrický (selektivní) detektor Mass spectrometric (selective) detector (MSD) Spektrometrie
HMOTNOSTNÍ SPEKTROMETRIE - kvalitativní i kvantitativní detekce v GC a LC - pyrolýzní hmotnostní spektrometrie - analýza polutantů v životním
 HMOTNOSTNÍ SPEKTROMETRIE - kvalitativní i kvantitativní detekce v GC a LC - pyrolýzní hmotnostní spektrometrie - analýza polutantů v životním prostředí - farmakokinetické studie - kvantifikace proteinů
HMOTNOSTNÍ SPEKTROMETRIE - kvalitativní i kvantitativní detekce v GC a LC - pyrolýzní hmotnostní spektrometrie - analýza polutantů v životním prostředí - farmakokinetické studie - kvantifikace proteinů
LABORATOŘ OBORU I ÚSTAV ORGANICKÉ TECHNOLOGIE (111) Použití GC-MS spektrometrie
 LABORATOŘ OBORU I ÚSTAV ORGANICKÉ TECHNOLOGIE (111) C Použití GC-MS spektrometrie Vedoucí práce: Doc. Ing. Petr Kačer, Ph.D., Ing. Kamila Syslová Umístění práce: laboratoř 79 Použití GC-MS spektrometrie
LABORATOŘ OBORU I ÚSTAV ORGANICKÉ TECHNOLOGIE (111) C Použití GC-MS spektrometrie Vedoucí práce: Doc. Ing. Petr Kačer, Ph.D., Ing. Kamila Syslová Umístění práce: laboratoř 79 Použití GC-MS spektrometrie
Hmotnostní spektrometrie. Historie MS. Schéma MS
 Hmotnostní spektrometrie MS mass spectrometry MS je analytická technika, která se používá k měření poměru hmotnosti ku náboji (m/z) u iontů původně studium izotopového složení dnes dynamicky se vyvíjející
Hmotnostní spektrometrie MS mass spectrometry MS je analytická technika, která se používá k měření poměru hmotnosti ku náboji (m/z) u iontů původně studium izotopového složení dnes dynamicky se vyvíjející
Indentifikace molekul a kvantitativní analýza pomocí MS
 Indentifikace molekul a kvantitativní analýza pomocí MS Identifikace molekul snaha určit molekulovou hmotnost, sumární složení, strukturní části molekuly (funkční skupiny, aromatická jádra, alifatické
Indentifikace molekul a kvantitativní analýza pomocí MS Identifikace molekul snaha určit molekulovou hmotnost, sumární složení, strukturní části molekuly (funkční skupiny, aromatická jádra, alifatické
Úvod do strukturní analýzy farmaceutických látek
 Úvod do strukturní analýzy farmaceutických látek Garant předmětu: doc. Ing. Bohumil Dolenský, Ph.D. A28, linka 40, dolenskb@vscht.cz Nukleární Magnetická Rezonance I. Příprava předmětu byla podpořena projektem
Úvod do strukturní analýzy farmaceutických látek Garant předmětu: doc. Ing. Bohumil Dolenský, Ph.D. A28, linka 40, dolenskb@vscht.cz Nukleární Magnetická Rezonance I. Příprava předmětu byla podpořena projektem
O Minimální počet valencí potřebných ke spojení vícevazných atomů = (24 C + 3 O + 7 N 1) * 2 = 66 valencí
 Jméno a příjmení:_bohumil_dolenský_ Datum:_10.12.2010_ Fakulta:_FCHI_ Kruh:_ÚACh_ 1. Sepište seznam signálů 1 H dle klesajícího chemického posunu (včetně nečistot), uveďte chemický posun, multiplicitu
Jméno a příjmení:_bohumil_dolenský_ Datum:_10.12.2010_ Fakulta:_FCHI_ Kruh:_ÚACh_ 1. Sepište seznam signálů 1 H dle klesajícího chemického posunu (včetně nečistot), uveďte chemický posun, multiplicitu
CHEMIE - Úvod do organické chemie
 Název školy Číslo projektu Autor Název šablony Název DUMu Stupeň a typ vzdělávání Vzdělávací oblast Vzdělávací obor Vzdělávací okruh Druh učebního materiálu Cílová skupina Anotace SŠHS Kroměříž CZ.1.07/1.5.00/34.0911
Název školy Číslo projektu Autor Název šablony Název DUMu Stupeň a typ vzdělávání Vzdělávací oblast Vzdělávací obor Vzdělávací okruh Druh učebního materiálu Cílová skupina Anotace SŠHS Kroměříž CZ.1.07/1.5.00/34.0911
10. Tandemová hmotnostní spektrometrie. Princip tandemové hmotnostní spektrometrie
 10. Tandemová hmotnostní spektrometrie Princip tandemové hmotnostní spektrometrie Informace získávané při tandemové hmotnostní spektrometrii Možné způsoby uspořádání tandemové HS a/ scan fragmentů vzniklých
10. Tandemová hmotnostní spektrometrie Princip tandemové hmotnostní spektrometrie Informace získávané při tandemové hmotnostní spektrometrii Možné způsoby uspořádání tandemové HS a/ scan fragmentů vzniklých
Hmotnostní spektrometrie Mass spectrometry - MS
 Hmotnostní spektrometrie Mass spectrometry - MS Příprava předmětu byla podpořena projektem OPPA č. CZ.2.17/3.1.00/33253 Hmotnostní spektrometrie Mass spectrometry - MS hmotnostní spektroskopie versus hmotnostní
Hmotnostní spektrometrie Mass spectrometry - MS Příprava předmětu byla podpořena projektem OPPA č. CZ.2.17/3.1.00/33253 Hmotnostní spektrometrie Mass spectrometry - MS hmotnostní spektroskopie versus hmotnostní
Hmotnostní spektrometrie
 Hmotnostní spektrometrie Princip: 1. Ze vzorku jsou tvořeny ionty na úrovni molekul, nebo jejich zlomků (fragmentů), nebo až volných atomů dodáváním energie, např. uvolnění atomů ze vzorku nebo přímo rozštěpení
Hmotnostní spektrometrie Princip: 1. Ze vzorku jsou tvořeny ionty na úrovni molekul, nebo jejich zlomků (fragmentů), nebo až volných atomů dodáváním energie, např. uvolnění atomů ze vzorku nebo přímo rozštěpení
Základy interpretace hmotnostních spekter
 Základy interpretace hmotnostních spekter Zpracováno podle: http://www.chem.arizona.edu/massspec/ - doporučený zdroj pro samostudium 1. Měříme četnost iontů pro dané hodnoty m/z 2. Vytvoříme grafickou
Základy interpretace hmotnostních spekter Zpracováno podle: http://www.chem.arizona.edu/massspec/ - doporučený zdroj pro samostudium 1. Měříme četnost iontů pro dané hodnoty m/z 2. Vytvoříme grafickou
No. 1 MW=106. No. 2 MW=156 [C 6 H 5 ] + [M-H] + M CHO [C 4 H 3 ] + 51 M+1
![No. 1 MW=106. No. 2 MW=156 [C 6 H 5 ] + [M-H] + M CHO [C 4 H 3 ] + 51 M+1 No. 1 MW=106. No. 2 MW=156 [C 6 H 5 ] + [M-H] + M CHO [C 4 H 3 ] + 51 M+1](/thumbs/44/23204932.jpg) No. 1 [C 6 H 5 ] + [M-H] + 77 105 106 MW=106 CHO [C 4 H 3 ] + 51 M+1 50 100 150 No. 2 M+1= 4.2 / 64.1*100 = 6.6% : 1.1 = 6*C M+2= 63.7 / 64.1*100 = 99.4% = Br 51 77 [C 6 H 5 ] + [C 4 H 3 ] + MW=156 Br
No. 1 [C 6 H 5 ] + [M-H] + 77 105 106 MW=106 CHO [C 4 H 3 ] + 51 M+1 50 100 150 No. 2 M+1= 4.2 / 64.1*100 = 6.6% : 1.1 = 6*C M+2= 63.7 / 64.1*100 = 99.4% = Br 51 77 [C 6 H 5 ] + [C 4 H 3 ] + MW=156 Br
HMOTNOSTNÍ SPEKTROMETRIE
 HMOTNOSTNÍ SPEKTROMETRIE A MOŽNOSTI JEJÍHO SPOJENÍ SE SEPARAČNÍMI METODAMI SEPARACE chromatografie CGC, GC x GC HPLC, UPLC, UHPLC, CHIP-LC elektromigrační m. CZE, CITP INTERFACE SPOJENÍ x ROZHRANÍ GC vyhřívaná
HMOTNOSTNÍ SPEKTROMETRIE A MOŽNOSTI JEJÍHO SPOJENÍ SE SEPARAČNÍMI METODAMI SEPARACE chromatografie CGC, GC x GC HPLC, UPLC, UHPLC, CHIP-LC elektromigrační m. CZE, CITP INTERFACE SPOJENÍ x ROZHRANÍ GC vyhřívaná
Dusíkové pravidlo. Počet dusíků m/z lichá m/z sudá 0, 2, 4,... (sudý) EE + OE +.
 Dusíkové pravidlo Základní formulace (platí pro M R a OE +. ): lichá M R = lichý počet dusíků v molekule sudá M R = sudý počet dusíků v molekule nebo nula Pro ionty EE + přesně naopak: lichá hodnota m/z
Dusíkové pravidlo Základní formulace (platí pro M R a OE +. ): lichá M R = lichý počet dusíků v molekule sudá M R = sudý počet dusíků v molekule nebo nula Pro ionty EE + přesně naopak: lichá hodnota m/z
Náboj a hmotnost elektronu
 1911 určení náboje elektronu q pomocí mlžné komory q = 1.602 177 10 19 C Náboj a hmotnost elektronu Elektrický náboj je kvantován Každý náboj je celistvým násobkem elementárního náboje (elektronu) z hodnoty
1911 určení náboje elektronu q pomocí mlžné komory q = 1.602 177 10 19 C Náboj a hmotnost elektronu Elektrický náboj je kvantován Každý náboj je celistvým násobkem elementárního náboje (elektronu) z hodnoty
Základy interpretace MS spekter získaných měkkými ionizačními technikami. Příprava předmětu byla podpořena projektem OPPA č. CZ.2.17/3.1.
 Základy interpretace MS spekter získaných měkkými ionizačními technikami Příprava předmětu byla podpořena projektem OPPA č. CZ.2.17/3.1.00/33253 Pravidlo sudého počtu elektronů v (kvazi)molekulárním iontu
Základy interpretace MS spekter získaných měkkými ionizačními technikami Příprava předmětu byla podpořena projektem OPPA č. CZ.2.17/3.1.00/33253 Pravidlo sudého počtu elektronů v (kvazi)molekulárním iontu
Výpočet stechiometrického a sumárního vzorce
 Výpočet stechiometrického a sumárního vzorce Stechiometrický (empirický) vzorec vyjadřuje základní složení sloučeniny udává, z kterých prvků se sloučenina skládá a v jakém poměru jsou atomy těchto prvků
Výpočet stechiometrického a sumárního vzorce Stechiometrický (empirický) vzorec vyjadřuje základní složení sloučeniny udává, z kterých prvků se sloučenina skládá a v jakém poměru jsou atomy těchto prvků
Moderní nástroje v analýze biomolekul
 Moderní nástroje v analýze biomolekul Definice Hmotnostní spektrometrie (zkratka MS z anglického Mass spectrometry) je fyzikálně chemická metoda. Metoda umožňující určit molekulovou hmotnost chemických
Moderní nástroje v analýze biomolekul Definice Hmotnostní spektrometrie (zkratka MS z anglického Mass spectrometry) je fyzikálně chemická metoda. Metoda umožňující určit molekulovou hmotnost chemických
Třídění látek. Chemie 1.KŠPA
 Třídění látek Chemie 1.KŠPA Systém (soustava) Vymezím si kus prostoru, látky v něm obsažené nazýváme systém soustava okolí svět Stěny soustavy Soustava může být: Izolovaná = stěny nedovolí výměnu částic
Třídění látek Chemie 1.KŠPA Systém (soustava) Vymezím si kus prostoru, látky v něm obsažené nazýváme systém soustava okolí svět Stěny soustavy Soustava může být: Izolovaná = stěny nedovolí výměnu částic
Laboratoř ze speciální analýzy potravin II. Úloha 3 - Plynová chromatografie (GC-MS)
 1 Úvod... 1 2 Cíle úlohy... 2 3 Předpokládané znalosti... 2 4 Autotest základních znalostí... 2 5 Základy práce se systémem GC-MS (EI)... 3 5.1 Parametry plynového chromatografu... 3 5.2 Základní charakteristiky
1 Úvod... 1 2 Cíle úlohy... 2 3 Předpokládané znalosti... 2 4 Autotest základních znalostí... 2 5 Základy práce se systémem GC-MS (EI)... 3 5.1 Parametry plynového chromatografu... 3 5.2 Základní charakteristiky
Hmotnostní spektrometrie
 Hmotnostní spektrometrie Vznik a detekce iontů EI spektra, interpretace Příprava předmětu byla podpořena projektem OPPA č. CZ.2.17/3.1.00/33253 Charakter hmotnostního spektra Způsob detekce (pokud jde
Hmotnostní spektrometrie Vznik a detekce iontů EI spektra, interpretace Příprava předmětu byla podpořena projektem OPPA č. CZ.2.17/3.1.00/33253 Charakter hmotnostního spektra Způsob detekce (pokud jde
Hmotnostní spektrometrie v organické analýze
 Hmotnostní spektrometrie v organické analýze Miroslav Lísa, Michal Holčapek každé úterý 16-18 hod, učebna HB-S23 plný text přednášek: http://holcapek.upce.cz/ zkouška: a/ písemný test (60 min) 40% známky
Hmotnostní spektrometrie v organické analýze Miroslav Lísa, Michal Holčapek každé úterý 16-18 hod, učebna HB-S23 plný text přednášek: http://holcapek.upce.cz/ zkouška: a/ písemný test (60 min) 40% známky
Dusíkové pravidlo. Počet dusíků m/z lichá m/z sudá 0, 2, 4,... (sudý) EE + OE +. 1, 3, 5,... (lichý) OE +. EE +
 Dusíkové pravidlo Základní formulace (platí pro M R a OE +. ): lichá M R = lichý počet dusíků v molekule sudá M R = sudý počet dusíků v molekule nebo nula Pro ionty EE + přesně naopak: lichá hodnota m/z
Dusíkové pravidlo Základní formulace (platí pro M R a OE +. ): lichá M R = lichý počet dusíků v molekule sudá M R = sudý počet dusíků v molekule nebo nula Pro ionty EE + přesně naopak: lichá hodnota m/z
Typy vzorců v organické chemii
 Typy vzorců v organické chemii Tento výukový materiál vznikl za přispění Evropské unie, státního rozpočtu ČR a Středočeského kraje Březen 2010 Mgr. Alena Jirčáková Typy vzorců v organické chemii Zápis
Typy vzorců v organické chemii Tento výukový materiál vznikl za přispění Evropské unie, státního rozpočtu ČR a Středočeského kraje Březen 2010 Mgr. Alena Jirčáková Typy vzorců v organické chemii Zápis
CHEMICKÉ VÝPOČTY I. ČÁST LÁTKOVÉ MNOŽSTVÍ. HMOTNOSTI ATOMŮ A MOLEKUL.
 CHEMICKÉ VÝPOČTY I. ČÁST LÁTKOVÉ MNOŽSTVÍ. HMOTNOSTI ATOMŮ A MOLEKUL. Látkové množství Značka: n Jednotka: mol Definice: Jeden mol je množina, která má stejný počet prvků, jako je atomů ve 12 g nuklidu
CHEMICKÉ VÝPOČTY I. ČÁST LÁTKOVÉ MNOŽSTVÍ. HMOTNOSTI ATOMŮ A MOLEKUL. Látkové množství Značka: n Jednotka: mol Definice: Jeden mol je množina, která má stejný počet prvků, jako je atomů ve 12 g nuklidu
Náboj a hmotnost elektronu
 1911 změřil náboj elektronu Pomocí mlžné komory q = 1.602 177 10 19 C Náboj a hmotnost elektronu Elektrický náboj je kvantován, Každý náboj je celistvým násobkem elementárního náboje (elektronu) z hodnoty
1911 změřil náboj elektronu Pomocí mlžné komory q = 1.602 177 10 19 C Náboj a hmotnost elektronu Elektrický náboj je kvantován, Každý náboj je celistvým násobkem elementárního náboje (elektronu) z hodnoty
ATOM. atom prvku : jádro protony (p + ) a neutrony (n) obal elektrony (e - ) protonové číslo 8 nukleonové číslo 16 (8 protonů + 8 neutronů v jádře)
 ATOM atom prvku : jádro protony (p + ) a neutrony (n) obal elektrony (e - ) protonové číslo 8 nukleonové číslo 16 (8 protonů + 8 neutronů v jádře) Atom lze rozložit na menší složky, označované jako subatomární
ATOM atom prvku : jádro protony (p + ) a neutrony (n) obal elektrony (e - ) protonové číslo 8 nukleonové číslo 16 (8 protonů + 8 neutronů v jádře) Atom lze rozložit na menší složky, označované jako subatomární
Úvod do studia organické chemie
 Úvod do studia organické chemie 1828... Wöhler... uměle připravil močovinu Organická chemie - chemie sloučenin uhlíku a vodíku, případně dalších prvků (O, N, X, P, S) Příčiny stability uhlíkových řetězců:
Úvod do studia organické chemie 1828... Wöhler... uměle připravil močovinu Organická chemie - chemie sloučenin uhlíku a vodíku, případně dalších prvků (O, N, X, P, S) Příčiny stability uhlíkových řetězců:
stechiometrický vzorec, platné číslice 1 / 10
 Základní chemické zákony Chemické zákony, látkové množství, atomová a molekulová hmotnost, stechiometrický vzorec, platné číslice http://z-moravec.net 1 / 10 Zákony zachování Zákon zachování hmoty Lavoisier,
Základní chemické zákony Chemické zákony, látkové množství, atomová a molekulová hmotnost, stechiometrický vzorec, platné číslice http://z-moravec.net 1 / 10 Zákony zachování Zákon zachování hmoty Lavoisier,
MENÍ A INTERPRETACE SPEKTER BIOMOLEKUL. Miloslav Šanda
 MENÍ A INTERPRETACE SPEKTER BIOMOLEKUL Miloslav Šanda Ionizaní techniky využívané k analýze biomolekul (biopolymer) MALDI : proteiny, peptidy, oligonukleotidy, sacharidy ESI : proteiny, peptidy, oligonukleotidy,
MENÍ A INTERPRETACE SPEKTER BIOMOLEKUL Miloslav Šanda Ionizaní techniky využívané k analýze biomolekul (biopolymer) MALDI : proteiny, peptidy, oligonukleotidy, sacharidy ESI : proteiny, peptidy, oligonukleotidy,
MO 1 - Základní chemické pojmy
 MO 1 - Základní chemické pojmy Hmota, látka, atom, prvek, molekula, makromolekula, sloučenina, chemicky čistá látka, směs. Hmota Filozofická kategorie, která se používá k označení objektivní reality v
MO 1 - Základní chemické pojmy Hmota, látka, atom, prvek, molekula, makromolekula, sloučenina, chemicky čistá látka, směs. Hmota Filozofická kategorie, která se používá k označení objektivní reality v
Hmotnostní spektrometrie - Mass Spectrometry (MS)
 Hmotnostní spektrometrie - Mass Spectrometry (MS) Další pojem: Hmotnostně spektrometrický (selektivní) detektor - Mass spectrometric (selective) detector (MSD) Spektrometrie - metoda založená na interakci
Hmotnostní spektrometrie - Mass Spectrometry (MS) Další pojem: Hmotnostně spektrometrický (selektivní) detektor - Mass spectrometric (selective) detector (MSD) Spektrometrie - metoda založená na interakci
No. 1- určete MW, vysvětlení izotopů
 No. 1- určete MW, vysvětlení izotopů ESI/APCI + 325 () 102 (35) 327 (33) 326 (15) 328 (5) 150 200 250 300 350 400 450 500 ESI/APCI - 323 () 97 (51) 325 (32) 324 (13) 326 (6) 150 200 250 300 350 400 450
No. 1- určete MW, vysvětlení izotopů ESI/APCI + 325 () 102 (35) 327 (33) 326 (15) 328 (5) 150 200 250 300 350 400 450 500 ESI/APCI - 323 () 97 (51) 325 (32) 324 (13) 326 (6) 150 200 250 300 350 400 450
Hmotnostní spektrometrie
 Hmotnostní spektrometrie Podstatou hmotnostní spektrometrie je studium iontů v plynném stavu. Tato metoda v sobě zahrnuje tři hlavní části:! generování iontů sledovaných atomů nebo molekul! separace iontů
Hmotnostní spektrometrie Podstatou hmotnostní spektrometrie je studium iontů v plynném stavu. Tato metoda v sobě zahrnuje tři hlavní části:! generování iontů sledovaných atomů nebo molekul! separace iontů
Klinická a farmaceutická analýza. Petr Kozlík Katedra analytické chemie
 Klinická a farmaceutická analýza Petr Kozlík Katedra analytické chemie e-mail: kozlik@natur.cuni.cz http://web.natur.cuni.cz/~kozlik/ 1 Spojení separačních technik s hmotnostní spektrometrem Separační
Klinická a farmaceutická analýza Petr Kozlík Katedra analytické chemie e-mail: kozlik@natur.cuni.cz http://web.natur.cuni.cz/~kozlik/ 1 Spojení separačních technik s hmotnostní spektrometrem Separační
Úvod do spektrálních metod pro analýzu léčiv
 Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti Úvod do spektrálních metod pro analýzu léčiv Pavel Matějka, Vadym Prokopec pavel.matejka@vscht.cz pavel.matejka@gmail.com Vadym.Prokopec@vscht.cz
Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti Úvod do spektrálních metod pro analýzu léčiv Pavel Matějka, Vadym Prokopec pavel.matejka@vscht.cz pavel.matejka@gmail.com Vadym.Prokopec@vscht.cz
Hmotnostní spektrometrie (1)
 Hmotnostní spektrometrie (1) 12_Chudoba_HCVDGrigsby_1ACC 12 (0.677) 57 % 27 43 55 41 28 29 32 54 69 67 67 71 83 81 79 85 95 93 97 99 105 111 113 125 127 137 153155 165 183 197 211 225 20 40 60 80 100 120
Hmotnostní spektrometrie (1) 12_Chudoba_HCVDGrigsby_1ACC 12 (0.677) 57 % 27 43 55 41 28 29 32 54 69 67 67 71 83 81 79 85 95 93 97 99 105 111 113 125 127 137 153155 165 183 197 211 225 20 40 60 80 100 120
OBECNÁ CHEMIE. Kurz chemie pro fyziky MFF-UK přednášející: Jaroslav Burda, KChFO.
 OBECNÁ CHEMIE Kurz chemie pro fyziky MFF-UK přednášející: Jaroslav Burda, KChFO burda@karlov.mff.cuni.cz HMOTA, JEJÍ VLASTNOSTI A FORMY Definice: Každý hmotný objekt je charakterizován dvěmi vlastnostmi
OBECNÁ CHEMIE Kurz chemie pro fyziky MFF-UK přednášející: Jaroslav Burda, KChFO burda@karlov.mff.cuni.cz HMOTA, JEJÍ VLASTNOSTI A FORMY Definice: Každý hmotný objekt je charakterizován dvěmi vlastnostmi
Gymnázium Vysoké Mýto nám. Vaňorného 163, 566 01 Vysoké Mýto
 Gymnázium Vysoké Mýto nám. Vaňorného 163, 566 01 Vysoké Mýto Chemický vzorec je zápis chemické látky. Izolovaný atom se zapíše značkou prvku. Fe atom železa Molekula je svazek atomů. Počet atomů v molekule
Gymnázium Vysoké Mýto nám. Vaňorného 163, 566 01 Vysoké Mýto Chemický vzorec je zápis chemické látky. Izolovaný atom se zapíše značkou prvku. Fe atom železa Molekula je svazek atomů. Počet atomů v molekule
Stereochemie 7. Přednáška 7
 Stereochemie 7 Přednáška 7 1 ptická čistota p = [ ]poz [ ]max x 100 = ee = [R] - [S] [R] + [S] x 100 p optická čistota [R], [S] molární frakce R a S enantiomerů ee + 100 %R = ee + %S = ee + 100 - %R =
Stereochemie 7 Přednáška 7 1 ptická čistota p = [ ]poz [ ]max x 100 = ee = [R] - [S] [R] + [S] x 100 p optická čistota [R], [S] molární frakce R a S enantiomerů ee + 100 %R = ee + %S = ee + 100 - %R =
DUSÍK NITROGENIUM 14,0067 3,1. Doplňte:
 Doplňte: Protonové číslo: Relativní atomová hmotnost: Elektronegativita: Značka prvku: Latinský název prvku: Český název prvku: Nukleonové číslo: Prvek je chemická látka tvořena z atomů o stejném... čísle.
Doplňte: Protonové číslo: Relativní atomová hmotnost: Elektronegativita: Značka prvku: Latinský název prvku: Český název prvku: Nukleonové číslo: Prvek je chemická látka tvořena z atomů o stejném... čísle.
Hmotnostní detekce v separačních metodách
 Hmotnostní detekce v separačních metodách MC230P83 2/1 Z+Zk 4 kredity doc. RNDr. Josef Cvačka, Ph.D. Mgr. Martin Hubálek, Ph.D. Ústav organické chemie a biochemie AVČR, v.v.i. Flemingovo nám. 2, 166 10
Hmotnostní detekce v separačních metodách MC230P83 2/1 Z+Zk 4 kredity doc. RNDr. Josef Cvačka, Ph.D. Mgr. Martin Hubálek, Ph.D. Ústav organické chemie a biochemie AVČR, v.v.i. Flemingovo nám. 2, 166 10
Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti LC-NMR 1. Jan Sýkora
 Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti LC-NMR 1 Jan Sýkora LC/NMR Jan Sýkora (ÚCHP AV ČR) LC - NMR 1 H NMR (500 MHz) mez detekce ~ 1 mg/ml (5 µmol látky) NMR parametry doba
Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti LC-NMR 1 Jan Sýkora LC/NMR Jan Sýkora (ÚCHP AV ČR) LC - NMR 1 H NMR (500 MHz) mez detekce ~ 1 mg/ml (5 µmol látky) NMR parametry doba
Základní principy interpretace spekter
 Základní principy interpretace spekter Vyloučení iontů, které nesouvisí s analytem Určení molekulové hmotnosti Určení prvků přítomných v molekule Určení elementárního složení z přesné hmotnosti Hledání
Základní principy interpretace spekter Vyloučení iontů, které nesouvisí s analytem Určení molekulové hmotnosti Určení prvků přítomných v molekule Určení elementárního složení z přesné hmotnosti Hledání
I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í
 ORGANIKÁ EMIE = chemie sloučenin látek obsahujících vazby Organické látky = všechny uhlíkaté sloučeniny kromě..., metal... and metal... Zdroje organických sloučenin = živé organismy nebo jejich fosílie:
ORGANIKÁ EMIE = chemie sloučenin látek obsahujících vazby Organické látky = všechny uhlíkaté sloučeniny kromě..., metal... and metal... Zdroje organických sloučenin = živé organismy nebo jejich fosílie:
Opakování
 Slabé vazebné interakce Opakování Co je to atom? Opakování Opakování Co je to atom? Atom je nejmenší částice hmoty, chemicky dále nedělitelná. Skládá se z atomového jádra obsahujícího protony a neutrony
Slabé vazebné interakce Opakování Co je to atom? Opakování Opakování Co je to atom? Atom je nejmenší částice hmoty, chemicky dále nedělitelná. Skládá se z atomového jádra obsahujícího protony a neutrony
Úvod do strukturní analýzy farmaceutických látek
 Úvod do strukturní analýzy farmaceutických látek Garant předmětu: doc. Ing. Bohumil Dolenský, Ph.D. A28, linka 40, dolenskb@vscht.cz Nukleární Magnetická Rezonance II. Příprava předmětu byla podpořena
Úvod do strukturní analýzy farmaceutických látek Garant předmětu: doc. Ing. Bohumil Dolenský, Ph.D. A28, linka 40, dolenskb@vscht.cz Nukleární Magnetická Rezonance II. Příprava předmětu byla podpořena
Názvosloví anorganických sloučenin
 Chemické názvosloví Chemické prvky jsou látky složené z atomů o stejném protonovém čísle (počet protonů v jádře atomu. Každému prvku přísluší určitý mezinárodní název a od něho odvozený symbol (značka).
Chemické názvosloví Chemické prvky jsou látky složené z atomů o stejném protonovém čísle (počet protonů v jádře atomu. Každému prvku přísluší určitý mezinárodní název a od něho odvozený symbol (značka).
Zdroje iont používané v hmotnostní spektrometrii. Miloslav Šanda
 Zdroje iont používané v hmotnostní spektrometrii Miloslav Šanda Ionizace v MS Hmotnostní spektrometrie je fyzikáln chemická metoda, pi které se provádí separace iont podle jejich hmotnosti a náboje m/z
Zdroje iont používané v hmotnostní spektrometrii Miloslav Šanda Ionizace v MS Hmotnostní spektrometrie je fyzikáln chemická metoda, pi které se provádí separace iont podle jejich hmotnosti a náboje m/z
ZŠ ÚnO, Bratří Čapků 1332
 Animovaná chemie Top-Hit Analytická chemie Analýza anorganických látek Důkaz aniontů Důkaz kationtů Důkaz kyslíku Důkaz vody Gravimetrická analýza Hmotnostní spektroskopie Chemická analýza Nukleární magnetická
Animovaná chemie Top-Hit Analytická chemie Analýza anorganických látek Důkaz aniontů Důkaz kationtů Důkaz kyslíku Důkaz vody Gravimetrická analýza Hmotnostní spektroskopie Chemická analýza Nukleární magnetická
Výukový materiál zpracován v rámci operačního projektu. EU peníze školám. Registrační číslo projektu: CZ.1.07/1.5.00/34.0512
 Výukový materiál zpracován v rámci operačního projektu EU peníze školám Registrační číslo projektu: Z.1.07/1.5.00/34.0512 Střední škola ekonomiky, obchodu a služeb SČMSD Benešov, s.r.o. HEMIE Organická
Výukový materiál zpracován v rámci operačního projektu EU peníze školám Registrační číslo projektu: Z.1.07/1.5.00/34.0512 Střední škola ekonomiky, obchodu a služeb SČMSD Benešov, s.r.o. HEMIE Organická
Emise vyvolaná působením fotonů nebo částic
 Emise vyvolaná působením fotonů nebo částic PES (fotoelektronová spektroskopie) XPS (rentgenová fotoelektronová spektroskopie), ESCA (elektronová spektroskopie pro chemickou analýzu) UPS (ultrafialová
Emise vyvolaná působením fotonů nebo částic PES (fotoelektronová spektroskopie) XPS (rentgenová fotoelektronová spektroskopie), ESCA (elektronová spektroskopie pro chemickou analýzu) UPS (ultrafialová
2. Atomové jádro a jeho stabilita
 2. Atomové jádro a jeho stabilita Atom je nejmenší hmotnou a chemicky nedělitelnou částicí. Je tvořen jádrem, které obsahuje protony a neutrony, a elektronovým obalem. Elementární částice proton neutron
2. Atomové jádro a jeho stabilita Atom je nejmenší hmotnou a chemicky nedělitelnou částicí. Je tvořen jádrem, které obsahuje protony a neutrony, a elektronovým obalem. Elementární částice proton neutron
Stručná historie hmotnostní spektrometrie. Analytická chemie II: Úvod do hmotnostní spektrometrie. Stručná historie hmotnostní spektrometrie.
 ACh II - MS Analytická chemie II: Úvod do hmotnostní spektrometrie Jan Preisler 3A14, Ústav chemie PřF MU, UKB, tel.: 54949 6629 preisler@chemi.muni.cz Specializovaný kurz: C7895 Hmotnostní spektrometrie
ACh II - MS Analytická chemie II: Úvod do hmotnostní spektrometrie Jan Preisler 3A14, Ústav chemie PřF MU, UKB, tel.: 54949 6629 preisler@chemi.muni.cz Specializovaný kurz: C7895 Hmotnostní spektrometrie
ORGANICKÉ SLOUČENINY
 ORGANICKÉ SLOUČENINY Autor: Mgr. Stanislava Bubíková Datum (období) tvorby: 12. 7. 2012 Ročník: devátý Vzdělávací oblast: Člověk a příroda / Chemie / Organické sloučeniny 1 Anotace: Žáci se seznámí se
ORGANICKÉ SLOUČENINY Autor: Mgr. Stanislava Bubíková Datum (období) tvorby: 12. 7. 2012 Ročník: devátý Vzdělávací oblast: Člověk a příroda / Chemie / Organické sloučeniny 1 Anotace: Žáci se seznámí se
Metody analýzy povrchu
 Metody analýzy povrchu Metody charakterizace nanomateriálů I RNDr. Věra Vodičková, PhD. Povrch pevné látky: Poslední monoatomární vrstva + absorbovaná monovrstva Ovlivňuje fyzikální vlastnosti (ukončení
Metody analýzy povrchu Metody charakterizace nanomateriálů I RNDr. Věra Vodičková, PhD. Povrch pevné látky: Poslední monoatomární vrstva + absorbovaná monovrstva Ovlivňuje fyzikální vlastnosti (ukončení
Měření a interpretace NMR spekter
 Měření a interpretace NMR spekter Bohumil Dolenský E-mail : Telefon : Místnost : www : dolenskb@vscht.cz (+420) 220 44 4110 budova A, místnost 28 http://www.vscht.cz/anl/dolensky/technmr/index.html Řešení
Měření a interpretace NMR spekter Bohumil Dolenský E-mail : Telefon : Místnost : www : dolenskb@vscht.cz (+420) 220 44 4110 budova A, místnost 28 http://www.vscht.cz/anl/dolensky/technmr/index.html Řešení
LEKCE 2b. NMR a chiralita, posunová činidla. Interpretace 13 C NMR spekter
 LEKCE 2b NMR a chiralita, posunová činidla Interpretace 13 C NMR spekter Stanovení optické čistoty Enantiomery jsou nerozlišitelné v NMR spektroskopii není možné rozlišit enantiomer od racemátu!!! Enantiotopické
LEKCE 2b NMR a chiralita, posunová činidla Interpretace 13 C NMR spekter Stanovení optické čistoty Enantiomery jsou nerozlišitelné v NMR spektroskopii není možné rozlišit enantiomer od racemátu!!! Enantiotopické
Postup při interpretaci NMR spekter neznámého vzorku
 Postup při interpretaci NMR spekter neznámého vzorku VŠCT 2017, Bohumil Dolenský, dolenskb@vscht.cz Tento text byl vypracován pro projekt Inovace předmětu Semestrální práce oboru analytická chemie I. Slouží
Postup při interpretaci NMR spekter neznámého vzorku VŠCT 2017, Bohumil Dolenský, dolenskb@vscht.cz Tento text byl vypracován pro projekt Inovace předmětu Semestrální práce oboru analytická chemie I. Slouží
Spektra 1 H NMR. Velmi zjednodušeně! Bohumil Dolenský
 Spektra 1 MR Velmi zjednodušeně! Bohumil Dolenský Spektra 1 MR... Počet signálů C 17 18 2 O 2 MeO Počet signálů = počet neekvivalentních skupin OMe = informace o symetrii molekuly Spektrum 1 MR... Počet
Spektra 1 MR Velmi zjednodušeně! Bohumil Dolenský Spektra 1 MR... Počet signálů C 17 18 2 O 2 MeO Počet signálů = počet neekvivalentních skupin OMe = informace o symetrii molekuly Spektrum 1 MR... Počet
13. Spektroskopie základní pojmy
 základní pojmy Spektroskopicky významné OPTICKÉ JEVY absorpce absorpční spektrometrie emise emisní spektrometrie rozptyl rozptylové metody Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti
základní pojmy Spektroskopicky významné OPTICKÉ JEVY absorpce absorpční spektrometrie emise emisní spektrometrie rozptyl rozptylové metody Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti
Analytická technika HPLC-MS/MS a možnosti jejího využití v hygieně
 Analytická technika HPLC-MS/MS a možnosti jejího využití v hygieně Šárka Dušková 24. září 2015-61. konzultační den Hodnocení expozice chemickým látkám na pracovištích 1 HPLC-MS/MS HPLC high-performance
Analytická technika HPLC-MS/MS a možnosti jejího využití v hygieně Šárka Dušková 24. září 2015-61. konzultační den Hodnocení expozice chemickým látkám na pracovištích 1 HPLC-MS/MS HPLC high-performance
Teorie chemické vazby a molekulární geometrie Molekulární geometrie VSEPR
 Geometrie molekul Lewisovy vzorce poskytují informaci o tom které atomy jsou spojeny vazbou a o jakou vazbu se jedná (topologie molekuly). Geometrické uspořádání molekuly je charakterizováno: Délkou vazeb
Geometrie molekul Lewisovy vzorce poskytují informaci o tom které atomy jsou spojeny vazbou a o jakou vazbu se jedná (topologie molekuly). Geometrické uspořádání molekuly je charakterizováno: Délkou vazeb
Základní principy interpretace spekter
 Základní principy interpretace spekter Obecný postup interpretace spekter Určení molekulové hmotnosti Fragmentace iontů se sudým počtem elektronů Fragmentace iontů s lichým počtem elektronů Interpretace
Základní principy interpretace spekter Obecný postup interpretace spekter Určení molekulové hmotnosti Fragmentace iontů se sudým počtem elektronů Fragmentace iontů s lichým počtem elektronů Interpretace
Biochemický ústav LF MU (V.P.) 2010
 1 * Biochemický ústav LF MU (V.P.) 2010 2 1. seminář LC Biochemický ústav LF MU (V.P.) 2010 3 Mol : jednotka látkového množství (látkové množství je veličina úměrná počtu látkových částic) 4 Mol : jednotka
1 * Biochemický ústav LF MU (V.P.) 2010 2 1. seminář LC Biochemický ústav LF MU (V.P.) 2010 3 Mol : jednotka látkového množství (látkové množství je veličina úměrná počtu látkových částic) 4 Mol : jednotka
Základy Mössbauerovy spektroskopie. Libor Machala
 Základy Mössbauerovy spektroskopie Libor Machala Rudolf L. Mössbauer 1958: jev bezodrazové rezonanční absorpce záření gama atomovým jádrem 1961: Nobelova cena Analogie s rezonanční absorpcí akustických
Základy Mössbauerovy spektroskopie Libor Machala Rudolf L. Mössbauer 1958: jev bezodrazové rezonanční absorpce záření gama atomovým jádrem 1961: Nobelova cena Analogie s rezonanční absorpcí akustických
Látkové množství. 6,022 10 23 atomů C. Přípravný kurz Chemie 07. n = N. Doporučená literatura. Látkové množství n. Avogadrova konstanta N A
 Doporučená literatura Přípravný kurz Chemie 2006/07 07 RNDr. Josef Tomandl, Ph.D. Mailto: tomandl@med.muni.cz Předmět: Přípravný kurz chemie J. Vacík a kol.: Přehled středoškolské chemie. SPN, Praha 1990,
Doporučená literatura Přípravný kurz Chemie 2006/07 07 RNDr. Josef Tomandl, Ph.D. Mailto: tomandl@med.muni.cz Předmět: Přípravný kurz chemie J. Vacík a kol.: Přehled středoškolské chemie. SPN, Praha 1990,
N A = 6,023 10 23 mol -1
 Pro vyjadřování množství látky se v chemii zavádí veličina látkové množství. Značí se n, jednotkou je 1 mol. Látkové množství je jednou ze základních veličin soustavy SI. Jeden mol je takové množství látky,
Pro vyjadřování množství látky se v chemii zavádí veličina látkové množství. Značí se n, jednotkou je 1 mol. Látkové množství je jednou ze základních veličin soustavy SI. Jeden mol je takové množství látky,
Značí se A r Určí se z periodické tabulky. Jednotkou je 1/12 hmotnosti atomu uhlíku. A r (H) = 1 A r (O) = 16
 CHEMICKÉ VÝPOČTY Značí se A r Určí se z periodické tabulky. Jednotkou je 1/12 hmotnosti atomu uhlíku. A r (H) = 1 A r (O) = 16 12 6 C Značí se M r Vypočítá se jako součet relativních atomových hmotností
CHEMICKÉ VÝPOČTY Značí se A r Určí se z periodické tabulky. Jednotkou je 1/12 hmotnosti atomu uhlíku. A r (H) = 1 A r (O) = 16 12 6 C Značí se M r Vypočítá se jako součet relativních atomových hmotností
jádro a elektronový obal jádro nukleony obal elektrony, pro chemii významné valenční elektrony
 atom jádro a elektronový obal jádro nukleony obal elektrony, pro chemii významné valenční elektrony molekula Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti seskupení alespoň dvou atomů
atom jádro a elektronový obal jádro nukleony obal elektrony, pro chemii významné valenční elektrony molekula Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti seskupení alespoň dvou atomů
A. Výpočty z chemických vzorců B. Určení vzorce sloučeniny. Čas potřebný k prostudování učiva kapitoly: 0,5 + 2 hodiny (teorie + řešení úloh)
 III. Chemické vzorce 1 1.CHEMICKÉ VZORCE A. Výpočty z chemických vzorců B. Určení vzorce sloučeniny Klíčová slova této kapitoly: Chemický vzorec, hmotnostní zlomek w, hmotnostní procento p m, stechiometrické
III. Chemické vzorce 1 1.CHEMICKÉ VZORCE A. Výpočty z chemických vzorců B. Určení vzorce sloučeniny Klíčová slova této kapitoly: Chemický vzorec, hmotnostní zlomek w, hmotnostní procento p m, stechiometrické
SADA VY_32_INOVACE_CH2
 SADA VY_32_INOVACE_CH2 Přehled anotačních tabulek k dvaceti výukovým materiálům vytvořených Ing. Zbyňkem Pyšem. Kontakt na tvůrce těchto DUM: pys@szesro.cz Výpočet empirického vzorce Název vzdělávacího
SADA VY_32_INOVACE_CH2 Přehled anotačních tabulek k dvaceti výukovým materiálům vytvořených Ing. Zbyňkem Pyšem. Kontakt na tvůrce těchto DUM: pys@szesro.cz Výpočet empirického vzorce Název vzdělávacího
FYZIKA MIKROSVĚTA. Mgr. Jan Ptáčník - GJVJ - Fyzika - Fyzika mikrosvěta - 3. ročník
 FYZIKA MIKROSVĚTA Mgr. Jan Ptáčník - GJVJ - Fyzika - Fyzika mikrosvěta - 3. ročník Mikrosvět Svět o rozměrech 10-9 až 10-18 m. Mikrosvět není zmenšeným makrosvětem! Chování v mikrosvětě popisuje kvantová
FYZIKA MIKROSVĚTA Mgr. Jan Ptáčník - GJVJ - Fyzika - Fyzika mikrosvěta - 3. ročník Mikrosvět Svět o rozměrech 10-9 až 10-18 m. Mikrosvět není zmenšeným makrosvětem! Chování v mikrosvětě popisuje kvantová
Jádro se skládá z kladně nabitých protonů a neutrálních neutronů -> nukleony
 Otázka: Atom a molekula Předmět: Chemie Přidal(a): Dituse Atom = základní stavební částice všech látek Skládá se ze 2 částí: o Kladně nabité jádro o Záporně nabitý elektronový obal Jádro se skládá z kladně
Otázka: Atom a molekula Předmět: Chemie Přidal(a): Dituse Atom = základní stavební částice všech látek Skládá se ze 2 částí: o Kladně nabité jádro o Záporně nabitý elektronový obal Jádro se skládá z kladně
4. Chemická ionizace. (E el = ev, p CH4 = Pa, p M = 0,05 0,1 Pa) => 0,1 % analytu)
 4. Chemická ionizace Munson, Field - 1966 Princip: reakce ion - molekula jako zdroj iontů => zprostředkování ionizace analytu jiným médiem Výsledek: iontové adukty (často protonované molekuly) Iont. zdroj:
4. Chemická ionizace Munson, Field - 1966 Princip: reakce ion - molekula jako zdroj iontů => zprostředkování ionizace analytu jiným médiem Výsledek: iontové adukty (často protonované molekuly) Iont. zdroj:
COSY + - podmínky měření a zpracování dat ztráta rozlišení ve spektru. inphase dublet, disperzní. antiphase dublet, absorpční
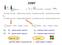 y x COSY 90 y chem. posuv J vazba 90 x : : inphase dublet, disperzní inphase dublet, disperzní antiphase dublet, absorpční antiphase dublet, absorpční diagonální pík krospík + - - + podmínky měření a zpracování
y x COSY 90 y chem. posuv J vazba 90 x : : inphase dublet, disperzní inphase dublet, disperzní antiphase dublet, absorpční antiphase dublet, absorpční diagonální pík krospík + - - + podmínky měření a zpracování
4.4.6 Jádro atomu. Předpoklady: Pomůcky:
 4.4.6 Jádro atomu Předpoklady: 040404 Pomůcky: Jádro je stotisíckrát menší než vlastní atom (víme z Rutherfordova experimentu), soustřeďuje téměř celou hmotnost atomu). Skládá se z: protonů: kladné částice,
4.4.6 Jádro atomu Předpoklady: 040404 Pomůcky: Jádro je stotisíckrát menší než vlastní atom (víme z Rutherfordova experimentu), soustřeďuje téměř celou hmotnost atomu). Skládá se z: protonů: kladné částice,
Agrochemie - cvičení 05
 Agrochemie - cvičení 05 Hmotnostní zlomky a procenta Relativní atomová hmotnost (Ar) bezrozměrná veličina veličina Relativní atomová hmotnost (též poměrná atomová hmotnost) je podíl klidové hmotnosti Relativní
Agrochemie - cvičení 05 Hmotnostní zlomky a procenta Relativní atomová hmotnost (Ar) bezrozměrná veličina veličina Relativní atomová hmotnost (též poměrná atomová hmotnost) je podíl klidové hmotnosti Relativní
Přírodní vědy - Chemie vymezení zájmu
 Přírodní vědy - Chemie vymezení zájmu Hmota Hmota má dualistický, korpuskulárně (částicově) vlnový charakter. Převládající charakter: korpuskulární (částicový) - látku vlnový - pole. Látka se skládá z
Přírodní vědy - Chemie vymezení zájmu Hmota Hmota má dualistický, korpuskulárně (částicově) vlnový charakter. Převládající charakter: korpuskulární (částicový) - látku vlnový - pole. Látka se skládá z
GC-MS aplikace v toxikologii
 Plynová chromatografie a hmotnostní spektrometrie (GC-MS) GC-MS aplikace v toxikologii M. Balíková GC-MS aplikace v toxikologii MS (mass spectrometry) hmotnostní spektrometrie: fyzikálně chemická metoda
Plynová chromatografie a hmotnostní spektrometrie (GC-MS) GC-MS aplikace v toxikologii M. Balíková GC-MS aplikace v toxikologii MS (mass spectrometry) hmotnostní spektrometrie: fyzikálně chemická metoda
Základní principy interpretace hmotnostních spekter malých molekul
 Hmotnostní detekce v separačních metodách V. Základní principy interpretace hmotnostních spekter malých molekul Proč je dobré porozumět hmotnostním spektrům? 1. Správné nastavení detektoru pro citlivou
Hmotnostní detekce v separačních metodách V. Základní principy interpretace hmotnostních spekter malých molekul Proč je dobré porozumět hmotnostním spektrům? 1. Správné nastavení detektoru pro citlivou
Sada 7 Název souboru Ročník Předmět Formát Název výukového materiálu Anotace
 Sada 7 Název souboru Ročník Předmět Formát Název výukového materiálu Anotace VY_52_INOVACE_737 8. Chemie notebook Směsi Materiál slouží k vyvození a objasnění pojmů (klíčová slova - chemická látka, směs,
Sada 7 Název souboru Ročník Předmět Formát Název výukového materiálu Anotace VY_52_INOVACE_737 8. Chemie notebook Směsi Materiál slouží k vyvození a objasnění pojmů (klíčová slova - chemická látka, směs,
Měření a interpretace NMR spekter
 Měření a interpretace NMR spekter Bohumil Dolenský E-mail : Telefon : Místnost : www : dolenskb@vscht.cz (+420) 220 44 4110 budova A, místnost 28 http://www.vscht.cz/anl/dolensky/technmr/index.html Struktura
Měření a interpretace NMR spekter Bohumil Dolenský E-mail : Telefon : Místnost : www : dolenskb@vscht.cz (+420) 220 44 4110 budova A, místnost 28 http://www.vscht.cz/anl/dolensky/technmr/index.html Struktura
Nukleární Overhauserův efekt (NOE)
 Nukleární Overhauserův efekt (NOE) NOE je důsledek dipolární interakce mezi dvěma jádry. Vzniká přímou interakcí volně přes prostor, tudíž není ovlivněn chemickými vazbami jako nepřímá spin-spinová interakce.
Nukleární Overhauserův efekt (NOE) NOE je důsledek dipolární interakce mezi dvěma jádry. Vzniká přímou interakcí volně přes prostor, tudíž není ovlivněn chemickými vazbami jako nepřímá spin-spinová interakce.
INTERAKCE IONTŮ S POVRCHY II.
 Úvod do fyziky tenkých vrstev a povrchů INTERAKCE IONTŮ S POVRCHY II. Metody IBA (Ion Beam Analysis): pružný rozptyl nabitých částic (RBS), detekce odražených atomů (ERDA), metoda PIXE, Spektroskopie rozptýlených
Úvod do fyziky tenkých vrstev a povrchů INTERAKCE IONTŮ S POVRCHY II. Metody IBA (Ion Beam Analysis): pružný rozptyl nabitých částic (RBS), detekce odražených atomů (ERDA), metoda PIXE, Spektroskopie rozptýlených
Nukleární Overhauserův efekt (NOE)
 LEKCE 8 Nukleární verhauserův efekt (NE) určení prostorové struktury molekul využití REY spektroskopie projevy NE a chemické výměny v jednom systému Nukleární verhauserův efekt (NE) důsledek dipolární
LEKCE 8 Nukleární verhauserův efekt (NE) určení prostorové struktury molekul využití REY spektroskopie projevy NE a chemické výměny v jednom systému Nukleární verhauserův efekt (NE) důsledek dipolární
Atomistická teorie (Dalton, 1803)
 Atomistická teorie (Dalton, 1803) Zákon stálých poměrů slučovacích: hmotnosti prvků tvořících čistou látku jsou k sobě vždy ve stejném poměru, bez ohledu na to jakým způsobem látka vznikla. Některé prvky
Atomistická teorie (Dalton, 1803) Zákon stálých poměrů slučovacích: hmotnosti prvků tvořících čistou látku jsou k sobě vždy ve stejném poměru, bez ohledu na to jakým způsobem látka vznikla. Některé prvky
Organická chemie - úvod
 rganická chemie - úvod Trocha historie Původní dělení hmoty: Neživá anorganická Živá organická Rozdělení chemie na organickou a anorganickou objevy a isolace látek z přírodních materiálů.w.scheele(1742-1786):
rganická chemie - úvod Trocha historie Původní dělení hmoty: Neživá anorganická Živá organická Rozdělení chemie na organickou a anorganickou objevy a isolace látek z přírodních materiálů.w.scheele(1742-1786):
Ch - Chemické reakce a jejich zápis
 Ch - Chemické reakce a jejich zápis Autor: Mgr. Jaromír Juřek Kopírování a jakékoliv další využití výukového materiálu je povoleno pouze s uvedením odkazu na www.jarjurek.cz. VARIACE Tento dokument byl
Ch - Chemické reakce a jejich zápis Autor: Mgr. Jaromír Juřek Kopírování a jakékoliv další využití výukového materiálu je povoleno pouze s uvedením odkazu na www.jarjurek.cz. VARIACE Tento dokument byl
