NUKLEÁRNÍ MAGNETICKÁ REZONANČNÍ SPEKTROMETRIE
|
|
|
- Štefan Novotný
- před 7 lety
- Počet zobrazení:
Transkript
1 NUKLEÁRNÍ MAGNETIKÁ REZNANČNÍ SPEKTRMETRIE Teoretický úvod Pracovní technika NMR 1 -NMR organických sloučenin 13 -NMR Aplikace NMR Nukleární (jaderná) magnetická rezonanční spektrometrie je založena na absorpci radiofrekvenčního elektromagnetického záření (desítky-stovky Mz) jádry některých atomů v molekulách analyzovaných látek (vzorků) umístěných v magnetickém poli kvalitativní analýza: identifikace a řešení struktury organických sloučenin (nejčastěji využití 1 -, 13 -, 19 F-, 31 P-NMR) určování způsobu vazby méně běžných prvků (Al, Se, Sn ) kvantitativní analýza směsí analýza izotopového zastoupení prvků ve složkách vzorků (SNIF-NMR) 1
2 Fyzikální podstata NMR Základní podmínka: nenulový jaderný magnetický moment µ; splněno u jader s jaderným spinovým kvantovým číslem I 0. Spin jádra je dán kombinací spinů jednotlivých protonů a neutronů, které nabývají hodnot +1/2 nebo -1/2. Typy jader: sudý počet protonů i neutronů ( 4 e, 12, 16 ) I = 0 lichý počet protonů i neutronů ( 2, 6 Li, 10 B, 14 N) I = 1, 2, 3 lichý počet nukleonů, tj. lichý počet protonů a sudý počet neutronů ( 1, 11 B, 15 N, 19 F, 23 Na, 27 Al, 31 P, 35 l, 79 Br, 133 s) nebo sudý počet protonů a lichý počet neutronů ( 13, 17, 29 Si, 33 S, 77 Se, 125 Te) I = 1/2, 3/2, 5/2 Účinek magnetického pole na jádro vnější magnetické pole (indukce B 0 ) vyvolává rozštěpení základního energetického stavu jádra na diskrétní hladiny počet hladin = 2 I +1, tj. počet možných orientací vektoru magnetického momentu jádra v magnetickém poli Jádro lehkého vodíku 1 proton I = 1/2 2 I +1 = 2 dojde k rozštěpení na dvě hladiny vzdálenost energetických hladin E = γ B 0 h / 2π E -1/2 E γ gyromagnetický poměr jádra B 0 indukce vnějšího magnetického pole [T] h Planckova konstanta, h = 6, Js B 0 = 0 B 0 > 0 +1/2 B 0 2
3 Magnetická rezonance jádra je energetický přechod mezi hladinami, který nastává při absorpci elektromagnetického záření o frekvenci odpovídající rozdílu energetických hladin ν = E/h = γ B 0 / 2π rezonanční podmínka Tato frekvence je rovna frekvenci precesního pohybu, který koná vektor magnetického momentu jádra kolem osy vnějšího magnetického pole. ω = 100 Mz hν ν = 100 Mz absorpce h ν= h ω +1/2-1/2 Rezonance lze dosáhnout: změnou ν při konstantní B 0 změnou B 0 při konstantní ν B 0 Vlastnosti některých jader Nuklid 1 Výskyt nuklidu [atom %] 99,98 Spin 1/2 Frekvence [Mz] (pro B=2,35T) 100 Relativní citlivost 1 2 0, ,35 1, ,11 1/2 25,14 1, N 99,63 1 7,22 1, N 0,37 1/2 10,13 3, ,037 5/2 13,56 1, F 100 1/2 94,1 0,83 31 P 100 1/2 40,48 6,
4 NMR spektrum Skutečná hodnota magnetické indukce B, která působí na atomové jádro atomu v molekule je nižší, než vnější indukce B 0. Je to dáno stínícím účinkem elektronového obalu atomu a sousedních atomů. B = B 0 (1 σ) σ je stínící konstanta; nabývá hodnot cca 10-4 až 10-2 Rezonanční podmínka je tedy splněna při jiné hodnotě frekvence ν = γ B 0 (1 σ) / 2π a dochází k posunu rezonanční frekvence různých aktivních jader v molekule podle míry stínícího účinku okolí jádra. Posun signálů na frekvenční ose se vyjadřuje jako relativní veličina tzv. chemický posun δ. hemický posun vzdálenost signálu vzorku na frekvenční ose od signálu referenční látky (nejčastěji tetramethylsilan TMS) vztažená vůči pracovní frekvenci přístroje 3 3 Si 3 3 δ = (ν v ν TMS ) / ν 0 [ppm] ν v frekvence rezonančního signálu určitého jádra ve vzorku ν TMS frekvence rezonančního signálu TMS přidaného ke vzorku ν 0 nominální frekvence přístroje 4
5 První pohled na 1 -NMR spektrum počet signálů chemické posuny signálů multiplicita signálů singlet dublet: dvěčáry, poměr 1:1 triplet: tři čáry, poměr 1:2:1 kvartet: čtyři čáry, poměr 1:3:3:1 kvintet: pět čar, poměr 1:4:6:4:1 sextet: šest čar, poměr 1:5:10:10:5:1 septet: sedm čar, poměr 1:6:15:20:15:6:1 oktet: 8 čar, poměr 1:7:21:35:35:21:7:1 nonet:9čar, poměr1:8:28:56:70:56:28:8:1 velikost signálů (plocha pod křivkou) je úměrná počtu vodíků interakční konstanta štěpení signálů do multipletu je způsobeno spinovou interakcí protonu, kterému signál přísluší, s protony na sousedním uhlíku; u jednoduchých spekter se multiplicita řídí pravidlem n+1 5
6 Příklad 1 -NMR spektra se spinovými interakcemi Ethylacetát: tři signály = tři různé typy vodíků v molekule Poměr intenzit A:B: = 3:3:2 Signál A triplet odpovídá 3 vodíkům, které spinově interagují se 2 vodíky v okolí (skupina 3 vedle skupiny 2 ) Signál B singlet odpovídá 3 vodíkům, v jejichž okolí není další vodík (izolovaná skupina 3 ) Signál kvartet odpovídá 2 vodíkům, které spinově interagují se 3 vodíky v okolí (skupina 2 vedle skupiny 3 ) Pracovní technika NMR Schéma NMR spektrometru 6
7 Měření NMR spekter kontinuální metoda: plynule se mění frekvence nebo magnetická indukce pulsní metoda: všechna jádra se uvedou do resonance pulsním vstupním radiofrekvenčním signálem odezvu (free induction decay FID) je třeba převést na spektrum Fourierovou transformací Rozpouštědla pro 1 -NMR l 4, S 2 neposkytují rezonanční signál normální rozpouštědla: aceton, chloroform, benzen, cyklohexan, dimethylsulfoxid, trifluoroctová kyselina, dioxan, voda poskytují jeden rezonanční signál nejběžnější jsou deuterovaná rozpouštědla: deuteriumoxid (D 2 ), chloroform-d (Dl 3 ), aceton-d 6 ((D 3 ) 2 ), dimethylformamid-d 7 (DN(D 3 ) 2 ), dimethylsulfoxid-d 6 ((D 3 ) 2 S), benzen-d 6, octová kyselina-d 4, ethanol-d 6, methanol-d 3 poskytují jen malý signál nečistot nedeuterovaných molekul 7
8 Referenční (standardní) látky pro 1 -NMR tetramethylsilan (TMS) poskytuje jediný rezonanční signál, je nepolární, nerozpustný v D 2, nereaktivní a velmi těkavý (t.v. 27 ) hexamethyldisiloxan poskytuje jediný signál (chem. posun proti TMS je 0,05), má obdobné vlastnosti, je méně těkavý (t.v. 100 ) hodí se pro měření při vyšších teplotách 3-(trimethylsilyl)-propansulfonan sodný je rozpustný v polárních rozpouštědlech, signál methylových skupin má vzhledem k TMS chem. posun 0,02 (methylenové skupiny dávají jen slabý signál, který neruší spektrum vzorku). další látky: chloroform, cyklohexan, voda, trichloroctová kys. 1 -NMR spektra organických sloučenin hemické posuny l 3 - -N R- R-= R 2 F 2 l 2 Br 2 I 2 2 N 2 2 Ar 2 NR 2 2 S 2 -()
9 oblast slabého pole (downfield) vyšší frekvence menší stínění (deshielding) diamagnetický posun increased shielding paramagnetický posun deshielding oblast silného pole (upfield) nižší frekvence větší stínění (shielding) δ Vliv substituce na chemický posun Substituce v alifatickém řetězci 9
10 Interakční konstanta J vzdálenost jednotlivých čar (jednoduchého) multipletu udává se v z interakční konstanta pro určitý typ spinové interakce je nezávislá na podmínkách měření (tj. na pracovní frekvenci spektrometru) Spektra ethyljodidu triplet: δ=110/60 = 1,83 ppm kvartet: δ=183/60 = 3,05 ppm triplet: δ=183/100 = 1,83 ppm kvartet: δ=305/100 = 3,05 ppm Vliv pracovní frekvence přístroje na spektrum 60 Mz nižší rozlišení 300 Mz vyšší rozlišení δ 10
11 Některé skupiny organických látek Alkany, cykloalkany a jejich (halogen- a nitro-)deriváty R- 3 δ = 0,7 1,3 ppm 0,22 ppm R- 2 -R R 3 δ = 1,2 1,4 ppm δ = 1,4 1,7 ppm ( 2 ) n 1,96 ppm 1,51 ppm Spinové interakce a e 1,1 ppm (a) 1,6 ppm (e) 3 J = 7 8 z Lineární vs. rozvětvený řetězec 3 2 X X triplet intenzita 3 kvartet intenzita 2 triplet intenzita 3 sextet intenzita 2 triplet intenzita 2 dublet intenzita X dublet intenzita X 3 septet intenzita 1 nonet intenzita 1 dublet intenzita 2 11
12 alogenalkany hemický posun eteronukleární spinové interakce I δ = 2,0 4,0 ppm pouze u fluorderivátů Br δ = 2,7 4,1 ppm F 2 J = 50 z F l δ = 3,1 4,1 ppm 3 J = 20 z F δ = 4,2 4,8 ppm alogenalkany 1-chlorbutan 12
13 Alkyny hemický posun δ = 1,7 2,7 ppm δ = 1,6 2,6 ppm Spinová interakce 4 J = 2 3 z Alkyny: 1-pentyn 4 J dc = 2,6 z 3 J db = 7 z 4 J cd = 2,6 z a b d c ,0 1,0 δ 13
14 Aromatické uhlovodíky a jejich deriváty δ = 6,5 8,0 ppm (benzen 7,27) δ = 2,3 2,7 ppm Spinové interakce 3 J ortho = 7 10 z 4 J meta = 2 3 z 5 J para = 0 1 z 6 4 BrI Br I 2 dublety 2 triplety v oblasti chem. posunu vodíků aromatického jádra velikosti signálů jsou stejné přítomnosti aromatického jádra odpovídá index nenasycenosti 4 jde o disubstituovaný benzen ortho? meta? para? 14
15 X Y X X Y Y 2 dublety 2 triplety singlet triplet 2 dublety dublet dublet ortho- meta- paraα-chlor-p-xylen 15
16 Alkoholy, fenoly a karboxylové kyseliny hemický posun Spinová interakce δ = 0,5 5 ppm δ = 3,2 3,8 ppm obvykle nenastává v důsledku výměny protonů (vliv rozpouštědla), pokud nastává, 3 J = 5 z δ = 4,24 ppm R δ = ppm zpravidla nenastává δ = 2,1 2,5 ppm Alkoholy, fenoly, karboxylové kyseliny Výměna protonu R + A R + A A nejčastěji voda rychlost výměny roste za přítomnosti stop minerálních kyselin a zásad a zvýšením teploty Důsledky výměny: velmi variabilní pozice signálu skupiny δ = 3,5 5,5 ppm (roztoky 0,1 0,9 M), cca 0,8 ppm (velké zředění) při rychlé výměně nedochází ke spinové interakci (signál skupiny je singlet) po přídavku D 2 ke vzorku signál skupiny mizí: R + D 2 RD + D při velmi pomalé výměně (roztoky v DMS-d 6 nebo čistý alkohol) skupina spinově interaguje signál je multiplet Vodíkové můstky tvorba oligomerů a dimerů R R R R R 16
17 Vliv rozpouštědla na spektrum ethanolu 3 J 2-3 = 7 z 3 J 2- = 5 z kvartet dubletů Diagram spinové interakce složitého multipletu skupiny 2 Spektrum ethanolu v DMS-d 6 17
18 Signál septet singlet dublet ppm 3,82 3,64 1,03 intenzita *3 Index nenasycenosti = = 1 + (2. 3 8)/2 = l l Signál singlet triplet triplet kvintet ppm 3,78 3,67 3,57 1,90 intenzita
19 Karboxylové kyseliny: ethylmalonová kyselina a triplet δ = 0,92 ppm intenzita 3 b kvintet δ = 1,8 ppm intenzita 2 c triplet δ = 3,1 ppm intenzita 1 d singlet δ = 12,3 ppm intenzita 2 Aldehydy a ketony hemický posun Spinová interakce R δ = 9 10 ppm 3 J = 1 3 z δ = 2,1 2,4 ppm R R δ = 2,1 2,4 ppm R singlet, δ = 2,1 ppm 19
20 Aldehydy: 2-methylpropanal (isobutyraldehyd) a dublet δ = 1,1 ppm intenzita 6 J ab = 7 z b septet dubletů δ = 2,4 ppm intenzita 1 J ba = 7 z J bc = 1,5 z c dublet δ = 9,6 ppm intenzita 1 J cb = 1,5 z Estery hemický posun 2 2 δ = 2,1 2,5 ppm δ = 3,5 4,8 ppm 20
21 Estery: isobutylacetát a dublet δ = 0,94 ppm intenzita 6 b nonet δ = 1,9 ppm intenzita 1 c singlet δ = 2,05 ppm intenzita 3 d dublet δ = 3,8 ppm Signál kvartet singlet triplet ppm 4,04 1,96 1,18 intenzita 1 2 1,5 3 1,5 3 Index nenasycenosti = = 1 + (2. 4 8)/2 = 1 1 dvojná vazba nebo 1 kruh 4 uhlíky, jen 3 z nich jsou vázány s vodíkem 21
22 Klasifikace 1 spekter podle složitosti spektra nultého řádu obsahují jen singlety spektra prvního řádu obsahují jednoduché multiplety odpovídající skupinám se spinovou interakcí jednotlivé signály mají značně rozdílné chemické posuny: ν/j 10 např. spektra se spinovými systémy AX, A 2 X, A 2 X 2, A 3 X 2, spektra druhého řádu obsahují multiplety multipletů jednotlivé signály jsou blízké hodnotou chemického posunu: ν/j 3 např. spektra se spinovými systémy AB, A 2 B, ABX, AB J AX J AX ν/j 10 ν A ν X AX ν/j = 5 3 ν A ν B AB 2 ν A ν B 1 J AB J AB ν A ν B ν/j 0 ν A = ν B A 2 22
23 Příklad spektra se spinovým systémem AB trans-skořicová kyselina v Dl 3, 60 Mz J AB = 16 z ν A = 469 z ν B = 388 z ν/j = 5,06 Alkeny hemický posun δ = 4,5 8,0 ppm Spinové interakce 3 J trans = z (obvykle 15 18) δ = 1,6 2,6 ppm 3 J cis = 6 15 z (obvykle 9 12) 2 J = 0 5 z (obvykle 1 3) nebo 4 J = 0 3 z 23
24 Příklad spektra se spinovým systémem AMX styren v Dl 3, 600 Mz δ A = 5,25 ppm δ M =5,75 ppm δ X = 6,73 ppm J MX = 17 z J AX = 11 z J AM = 1 z Pravidla pro značení spinových systémů chemicky ekvivalentní protony značíme stejným písmenem, např. A 3 pro tři protony methylové skupiny neekvivalentní jádra, kterým odpovídají chemické posuny, mezi nimiž je malý rozdíl, značíme sousedními písmeny abecedy, např. A, B, neekvivalentní jádra, kterým odpovídají více rozdílné nebo značně rozdílné chemické posuny, značíme písmeny, které jsou v abecedě od sebe vzdáleny, např. A, M, X chemicky ekvivalentní ale magneticky neekvivalentní jádra značíme stejnými písmeny a rozlišujeme je čárkou, např. AA' B,B' pro vícespinové systémy se používají kombinace těchto zápisů, např. AX, A 2 X, AMX, AB, ABX, A 3 X 2 24
25 Některé možnosti zjednodušování NMR spekter zvýšení operační frekvence přístroje (velmi nákladné) dekapling (decoupling): zrušení spinové interakce mezi stejnými jádry (např. 1-1 ): homonukleární dekapling mezi různými jádry (např ): heteronukleární dekapling pro konkrétní skupinu nebo atom: selektivní dekapling pro více skupin (signálů ve spektru): širokopásmový dekapling změna teploty vzorku deuterace D 2 jako rozpouštědlo: mizí signály vyměnitelných protonů (skupiny, -S, -N 2, -) použití chemických posunových činidel Selektivní homonukleární dekapling: 3-butyn-1-ol 300 Mz rozpouštědlo: Dl 3 a bez dekaplingu b zrušena spinová interakce vodíků na 1 c zrušena spinová interakce vodíků na 2 d zrušena spinová interakce vodíků na 4 25
26 13 -NMR spektrometrie rezonance jader 13 nastává ve srovnání s 1 při cca čtvrtinové frekvenci, tj. pracovní frekvenci 100 Mz (v 1 ) odpovídá 25,15 Mz ( 13 ) a frekvenci 600 Mz (v 1 ) odpovídá 150,9 Mz ( 13 ) obvyklý rozsah chemického posunu: ppm (vs. TMS) nejběžnější rozpouštědlo Dl 3 (signál: triplet, δ = 77 ppm) zastoupení 13 v normální izotopové směsi uhlíku: 1,1 % spinové interakce se ve spektru neobjevují dochází ke spinovým interakcím 13-1, případně F, P hemický posun v uhlíkových NMR spektrech sp 3 uhlík sp 3 uhlík vázaný s elektronegativním atomem R 2 R R 3 R 4 l R 3 δ (ppm) Br alkyny alkeny areny karbonylové sloučeniny aldehydy, ketony kyseliny, estery, amidy, anhydridy
27 Spinová interakce 13-1 a její projev ve spektru jádro 13 interaguje s přímo připojenými protony multiplet multiplicita: n methylový uhlík methylenový uhlík methinový uhlík kvarterní uhlík kvartet triplet dublet singlet Rušení spinové interakce 13-1 (protonový širokopásmový dekapling) současné ozáření vzorku rezonančními frekvencemi protonů označení spektra: 13 { 1 }-NMR důsledky dekaplingu: zjednodušení spektra (multiplet singlet) každému signálu ve spektru odpovídá jeden uhlík nebo skupina chemicky ekvivalentních uhlíků všechny signály (singlety) jsou dostatečně separovány zvýšení některých signálů potlačení šumu spektra 27
28 Vliv protonového dekaplingu na uhlíkové spektrum (a) Spektra diethylftalátu v Dl 3 150,9 Mz a) 13 -NMR b) 13 { 1 }-NMR (b) Vliv protonového dekaplingu na uhlíkové spektrum Spektra cholesterolu v Dl 3 150,9 Mz a) 13 -NMR b) 13 { 1 }-NMR 28
29 Některé vlastnosti uhlíkových spekter ( 13 i 13 { 1 }) odlišné od protonových spekter záznam spektra je třeba vícekrát (mnohokrát) opakovat (akumulace spekter) velikost jednotlivých signálů není zcela úměrná počtu chemicky ekvivalentních atomů uhlíku kvantitativní analýza je problematičtější atomy uhlíku, které nemají vázaný žádný atom vodíku (kvarterní uhlíky, uhlíky karbonylové skupiny s výjimkou formylové skupiny), poskytují menší signál ve spektru 13 { 1 }-NMR zpravidla velikost signálů klesá v řadě 3 > 2 > >> Aplikace NMR spektrometrie becný přehled aplikací identifikace organických (i anorganických) sloučenin (např. léčiva, drogy ) kvantitativní analýza (farmacie, potraviny) stanovení enantiomerní čistoty stanovení absolutní konfigurace chirálních sloučenin stanovení rovnovážných konstant (např. disociační konstanty) stanovení tautomerního zastoupení studium struktury polymerů stanovení izotopového zastoupení 29
30 Kvantitativní analýza metodou NMR integrální intenzita signálu je přímo úměrná obsahu složky, které tento signál přísluší v 1 -NMR je velikost signálu rovněž přímo úměrná počtu atomů vodíku v příslušné skupině molekuly detegované látky možnost použití metody vnitřního standardu (IS) pro kvantifikaci analytu: m analyt NIS Manalyt A = mis Nanalyt MIS A analyt IS A integrální intenzity signálů analytu a vnitřního standardu M molární hmotnosti analytu a vnitřního standardu N počty atomů ve skupinách molekul analytu a vnitřního standardu, které příslušejí signálům analytu a vnitřního standardu Příklad kvantitativní NMR analýzy: dvousložková směs ethanol-voda A = 2 y 2 + y Et A 2 = 2 y Et NMR spektrum vzorku vodky 1152 = 2 y 2 + y Et 203 = 2 y Et y Et =101,5 y 2 = 525,25 m Et /m 2 = (y Et /y 2 ). (M Et /M 2 ) = = (101,5/525,25). (46,07/18,015) = = 0,49394 w Et = m Et / (m Et + m 2 ) = = 0, m 2 / (0,49394.m 2 + m 2 ) = = 0,49394/1,49394 = 0,3306 p Et = 33,06 % (m/m) φ Et = 39,75 % (V/V) 30
31 Analýza izotopového složení: SNIF-NMR = Site-specific Natural Isotope Fractionation izotopové poměry (např. D/ 1 ), 13 / 12 ) v přírodních produktech nejsou zcela konstantní závisejí na původu vzorku (druh rostliny, biochemické, geografické a klimatické faktory) např. 4 rostliny (cukrová třtina, kukuřice) mají vyšší poměr 13 / 12 než 3 rostliny (cukrová řepa, hrozny) možnost určování původu potraviny, druhu použité suroviny SNIF-NMR: určování původu alkoholických nápojů ze vzorku se oddestiluje ethanol ( 96 % Et) provede se měření 2 -NMR určí se poměry signálů odpovídající výskytu deuteria v jednotlivých skupinách molekuly Monodeuterované molekuly ethanolu: typ I: 2 D 2 (mol. zlomek 1/2) typii: 3 D (mol. zlomek 1/3) typ III: 3 2 D (mol. zlomek 1/6) Kritérium R = 3. (S II /S I ) = 2. [(D/) II /(D/) I ] S I je signál D v methylové skupině, S II je signál D v methylenové skupině Při náhodné distribuci izotopů v molekule Et bude R=2; skutečné hodnoty R pro kvasný ethanol jsou 2,2 až 2,7 podle druhu suroviny: R 2,25 cukrová třtina, kukuřice R 2,5 pšenice, ječmen, jablka, hrozny R 2,7 cukrová řepa, brambory 31
Nukleární magnetická rezonanční spektrometrie
 Nukleární magnetická rezonanční spektrometrie bsah kapitoly Teoretický úvod Pracovní technika NMR 1 -NMR organických sloučenin 13 -NMR 31 P-NMR Aplikace NMR v analýze potravin Nukleární (jaderná) magnetická
Nukleární magnetická rezonanční spektrometrie bsah kapitoly Teoretický úvod Pracovní technika NMR 1 -NMR organických sloučenin 13 -NMR 31 P-NMR Aplikace NMR v analýze potravin Nukleární (jaderná) magnetická
Chemický posun v uhlíkových NMR spektrech
 13 -NMR spektrometrie rezonance jader 13 nastává ve srovnání s 1 při cca čtvrtinové frekvenci, tj. pracovní frekvenci 100 Mz (v 1 ) odpovídá 25,15 Mz ( 13 ) a frekvenci 600 Mz (v 1 ) odpovídá 150,9 Mz
13 -NMR spektrometrie rezonance jader 13 nastává ve srovnání s 1 při cca čtvrtinové frekvenci, tj. pracovní frekvenci 100 Mz (v 1 ) odpovídá 25,15 Mz ( 13 ) a frekvenci 600 Mz (v 1 ) odpovídá 150,9 Mz
SPEKTROSKOPIE NUKLEÁRNÍ MAGNETICKÉ REZONANCE
 SPEKTROSKOPIE NUKLEÁRNÍ MAGNETICKÉ REZONANCE Obecné základy nedestruktivní metoda strukturní analýzy zabývá se rezonancí atomových jader nutná podmínka pro měření spekter: nenulový spin atomového jádra
SPEKTROSKOPIE NUKLEÁRNÍ MAGNETICKÉ REZONANCE Obecné základy nedestruktivní metoda strukturní analýzy zabývá se rezonancí atomových jader nutná podmínka pro měření spekter: nenulový spin atomového jádra
OPVK CZ.1.07/2.2.00/
 18.2.2013 OPVK CZ.1.07/2.2.00/28.0184 Cvičení z NMR OCH/NMR Mgr. Tomáš Pospíšil, Ph.D. LS 2012/2013 18.2.2013 NMR základní principy NMR Nukleární Magnetická Resonance N - nukleární (studujeme vlastnosti
18.2.2013 OPVK CZ.1.07/2.2.00/28.0184 Cvičení z NMR OCH/NMR Mgr. Tomáš Pospíšil, Ph.D. LS 2012/2013 18.2.2013 NMR základní principy NMR Nukleární Magnetická Resonance N - nukleární (studujeme vlastnosti
Spektra 1 H NMR. Velmi zjednodušeně! Bohumil Dolenský
 Spektra 1 MR Velmi zjednodušeně! Bohumil Dolenský Spektra 1 MR... Počet signálů C 17 18 2 O 2 MeO Počet signálů = počet neekvivalentních skupin OMe = informace o symetrii molekuly Spektrum 1 MR... Počet
Spektra 1 MR Velmi zjednodušeně! Bohumil Dolenský Spektra 1 MR... Počet signálů C 17 18 2 O 2 MeO Počet signálů = počet neekvivalentních skupin OMe = informace o symetrii molekuly Spektrum 1 MR... Počet
Úvod do strukturní analýzy farmaceutických látek
 Úvod do strukturní analýzy farmaceutických látek Garant předmětu: doc. Ing. Bohumil Dolenský, Ph.D. A28, linka 40, dolenskb@vscht.cz Nukleární Magnetická Rezonance II. Příprava předmětu byla podpořena
Úvod do strukturní analýzy farmaceutických látek Garant předmětu: doc. Ing. Bohumil Dolenský, Ph.D. A28, linka 40, dolenskb@vscht.cz Nukleární Magnetická Rezonance II. Příprava předmětu byla podpořena
LEKCE 1b. Základní parametry 1 H NMR spekter. Symetrie v NMR spektrech: homotopické, enantiotopické, diastereotopické protony (skupiny)*
 Základní parametry 1 NMR spekter LEKCE 1b Symetrie v NMR spektrech: homotopické, enantiotopické, diastereotopické protony (skupiny)* 3.5 3.0 2.5 2.0 1.5 Základní parametry 1 NMR spekter Počet signálů ve
Základní parametry 1 NMR spekter LEKCE 1b Symetrie v NMR spektrech: homotopické, enantiotopické, diastereotopické protony (skupiny)* 3.5 3.0 2.5 2.0 1.5 Základní parametry 1 NMR spekter Počet signálů ve
Základní parametry 1 H NMR spekter
 LEKCE 1a Základní parametry 1 NMR spekter Počet signálů ve spektru (zjištění počtu skupin chemicky ekvivalentních jader) Integrální intenzita (intenzita pásů závisí na počtu jader) Chemický posun (polohy
LEKCE 1a Základní parametry 1 NMR spekter Počet signálů ve spektru (zjištění počtu skupin chemicky ekvivalentních jader) Integrální intenzita (intenzita pásů závisí na počtu jader) Chemický posun (polohy
NMR spektroskopie rádiové frekvence jádra spinovou rezonancí jader spinový moment lichý počet
 NMR spektroskopie NMR spektroskopie Nukleární Magnetická Resonance - spektroskopická metoda založená na měření absorpce elektromagnetického záření (rádiové frekvence asi od 4 do 900 MHz). Na rozdíl od
NMR spektroskopie NMR spektroskopie Nukleární Magnetická Resonance - spektroskopická metoda založená na měření absorpce elektromagnetického záření (rádiové frekvence asi od 4 do 900 MHz). Na rozdíl od
Nukleární magnetická rezonance (NMR)
 Nukleární magnetická rezonance (NMR) Nukleární magnetické rezonance (NMR) princip ZDROJ E = h. elektro-magnetické záření E energie záření h Plankova konstanta frekvence záření VZOREK E E 1 E 0 DETEKTOR
Nukleární magnetická rezonance (NMR) Nukleární magnetické rezonance (NMR) princip ZDROJ E = h. elektro-magnetické záření E energie záření h Plankova konstanta frekvence záření VZOREK E E 1 E 0 DETEKTOR
NMR spektroskopie Instrumentální a strukturní analýza
 NMR spektroskopie Instrumentální a strukturní analýza prof. RNDr. Zdeněk Friedl, CSc. Použitá a doporučená literatura Solomons T.W.G., Fryhle C.B.: Organic Chemistry, 8th Ed., Wiley 2004. Günther H.: NMR
NMR spektroskopie Instrumentální a strukturní analýza prof. RNDr. Zdeněk Friedl, CSc. Použitá a doporučená literatura Solomons T.W.G., Fryhle C.B.: Organic Chemistry, 8th Ed., Wiley 2004. Günther H.: NMR
ZÁKLADY SPEKTROMETRIE NUKLEÁRNÍ MAGNETICKÉ REZONANCE
 ZÁKLADY SPEKTROMETRIE NUKLEÁRNÍ MAGNETICKÉ REZONANCE Co to je NMR? nedestruktivní spektroskopická metoda využívající magnetických vlastností atomových jader ke studiu struktury molekul metoda č.1 pro určování
ZÁKLADY SPEKTROMETRIE NUKLEÁRNÍ MAGNETICKÉ REZONANCE Co to je NMR? nedestruktivní spektroskopická metoda využívající magnetických vlastností atomových jader ke studiu struktury molekul metoda č.1 pro určování
Úvod do strukturní analýzy farmaceutických látek
 Úvod do strukturní analýzy farmaceutických látek Garant předmětu: doc. Ing. Bohumil Dolenský, Ph.D. A28, linka 40, dolenskb@vscht.cz Nukleární Magnetická Rezonance I. Příprava předmětu byla podpořena projektem
Úvod do strukturní analýzy farmaceutických látek Garant předmětu: doc. Ing. Bohumil Dolenský, Ph.D. A28, linka 40, dolenskb@vscht.cz Nukleární Magnetická Rezonance I. Příprava předmětu byla podpořena projektem
Nukleární magnetická rezonance (NMR)
 Nukleární magnetická rezonance (NMR) Mgr. Zdeněk Moravec, Ph.D. Úvod Zkratka NMR znamená Nukleární Magnetická Rezonance. Jde o analytickou metodu, která na základě absorpce radiofrekvenčního záření vzorkem
Nukleární magnetická rezonance (NMR) Mgr. Zdeněk Moravec, Ph.D. Úvod Zkratka NMR znamená Nukleární Magnetická Rezonance. Jde o analytickou metodu, která na základě absorpce radiofrekvenčního záření vzorkem
NMR spektroskopie. Úvod
 NMR spektroskopie Úvod Zkratka NMR znamená Nukleární Magnetická Rezonance. Jde o analytickou metodu, která na základě absorpce radiofrekvenčního záření vzorkem umístěným v silném magnetickém poli poskytuje
NMR spektroskopie Úvod Zkratka NMR znamená Nukleární Magnetická Rezonance. Jde o analytickou metodu, která na základě absorpce radiofrekvenčního záření vzorkem umístěným v silném magnetickém poli poskytuje
spinový rotační moment (moment hybnosti) kvantové číslo jaderného spinu I pro NMR - jádra s I 0
 Spektroskopie NMR - teoretické základy spin nukleonů, spin jádra, kvantová čísla energetické stavy jádra v magnetickém poli rezonanční podmínka - instrumentace pulsní metody, pulsní sekvence relaxační
Spektroskopie NMR - teoretické základy spin nukleonů, spin jádra, kvantová čísla energetické stavy jádra v magnetickém poli rezonanční podmínka - instrumentace pulsní metody, pulsní sekvence relaxační
NUKLEÁRNÍ MAGNETICKÁ REZONANCE
 NUKLEÁRNÍ MAGNETICKÁ REZONANCE NMR spektrometrie PRINCIP NMR Jsou-li atomová jádra některých prvků v externím magnetickém poli vystavena vysokofrekvenčnímu elmag. záření, mohou absorbovat záření určitých.
NUKLEÁRNÍ MAGNETICKÁ REZONANCE NMR spektrometrie PRINCIP NMR Jsou-li atomová jádra některých prvků v externím magnetickém poli vystavena vysokofrekvenčnímu elmag. záření, mohou absorbovat záření určitých.
Strukturní analýza. NMR spektroskopie
 Strukturní analýza NMR spektroskopie RNDr. Zdeněk Tošner, Ph.D. lavova 8, místnost 020 tel. 22195 1323 tosner@natur.cuni.cz www.natur.cuni.cz/nmr/vyuka.html Literatura Böhm, Smrčková-Voltrová: Strukturní
Strukturní analýza NMR spektroskopie RNDr. Zdeněk Tošner, Ph.D. lavova 8, místnost 020 tel. 22195 1323 tosner@natur.cuni.cz www.natur.cuni.cz/nmr/vyuka.html Literatura Böhm, Smrčková-Voltrová: Strukturní
Symetrie v NMR spektrech: homotopické, enantiotopické, diastereotopické protony (skupiny)*
 Základní parametry 1 NMR spekter NMR a chiralita, posunová činidla Symetrie v NMR spektrech: homotopické, enantiotopické, diastereotopické protony (skupiny)* 3.5 3.0 2.5 2.0 1.5 Základní parametry 1 NMR
Základní parametry 1 NMR spekter NMR a chiralita, posunová činidla Symetrie v NMR spektrech: homotopické, enantiotopické, diastereotopické protony (skupiny)* 3.5 3.0 2.5 2.0 1.5 Základní parametry 1 NMR
Měření a interpretace NMR spekter
 Měření a interpretace NMR spekter Bohumil Dolenský E-mail : Telefon : Místnost : www : dolenskb@vscht.cz (+420) 220 44 4110 budova A, místnost 28 http://www.vscht.cz/anl/dolensky/technmr/index.html Řešení
Měření a interpretace NMR spekter Bohumil Dolenský E-mail : Telefon : Místnost : www : dolenskb@vscht.cz (+420) 220 44 4110 budova A, místnost 28 http://www.vscht.cz/anl/dolensky/technmr/index.html Řešení
Základní parametry 1 H NMR spekter
 LEKCE 6 Základní parametry 1 NMR spekter Počet signálů ve spektru (zjištění počtu skupin chemicky ekvivalentních jader) Integrální intenzita (intenzita pásů závisí na počtu jader) Chemický posun (polohy
LEKCE 6 Základní parametry 1 NMR spekter Počet signálů ve spektru (zjištění počtu skupin chemicky ekvivalentních jader) Integrální intenzita (intenzita pásů závisí na počtu jader) Chemický posun (polohy
Postup při interpretaci NMR spekter neznámého vzorku
 Postup při interpretaci NMR spekter neznámého vzorku VŠCT 2017, Bohumil Dolenský, dolenskb@vscht.cz Tento text byl vypracován pro projekt Inovace předmětu Semestrální práce oboru analytická chemie I. Slouží
Postup při interpretaci NMR spekter neznámého vzorku VŠCT 2017, Bohumil Dolenský, dolenskb@vscht.cz Tento text byl vypracován pro projekt Inovace předmětu Semestrální práce oboru analytická chemie I. Slouží
Program. Materiály ke studiu NMR. Data, Soubory. Seminář z Analytické chemie B. \\PYR\SCRATCH\
 Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti Seminář z Analytické chemie B Tento materiál vznikl za podpory projektu CHEMnote PPA CZ..7/../48 Inovace bakalářského studijního programu
Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti Seminář z Analytické chemie B Tento materiál vznikl za podpory projektu CHEMnote PPA CZ..7/../48 Inovace bakalářského studijního programu
Spektrální metody NMR I. opakování
 Spektrální metody NMR I opakování Využití NMR určování chemické struktury přírodní látky, organická syntéza konstituce, konformace, konfigurace ověření čistoty studium dynamických procesů reakční kinetika
Spektrální metody NMR I opakování Využití NMR určování chemické struktury přírodní látky, organická syntéza konstituce, konformace, konfigurace ověření čistoty studium dynamických procesů reakční kinetika
Metody spektrální. Metody molekulové spektroskopie NMR. Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti
 Metody spektrální Metody molekulové spektroskopie NMR Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti Spektroskopie NMR - teoretické základy spin nukleonů, spin jádra, kvantová čísla
Metody spektrální Metody molekulové spektroskopie NMR Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti Spektroskopie NMR - teoretické základy spin nukleonů, spin jádra, kvantová čísla
12.NMR spektrometrie při analýze roztoků
 Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti 12.NMR spektrometrie při analýze roztoků Pavel Matějka pavel.matejka@vscht.cz pavel.matejka@gmail.com 12.NMR spektrometrie při analýze
Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti 12.NMR spektrometrie při analýze roztoků Pavel Matějka pavel.matejka@vscht.cz pavel.matejka@gmail.com 12.NMR spektrometrie při analýze
O Minimální počet valencí potřebných ke spojení vícevazných atomů = (24 C + 3 O + 7 N 1) * 2 = 66 valencí
 Jméno a příjmení:_bohumil_dolenský_ Datum:_10.12.2010_ Fakulta:_FCHI_ Kruh:_ÚACh_ 1. Sepište seznam signálů 1 H dle klesajícího chemického posunu (včetně nečistot), uveďte chemický posun, multiplicitu
Jméno a příjmení:_bohumil_dolenský_ Datum:_10.12.2010_ Fakulta:_FCHI_ Kruh:_ÚACh_ 1. Sepište seznam signálů 1 H dle klesajícího chemického posunu (včetně nečistot), uveďte chemický posun, multiplicitu
LEKCE 2b. NMR a chiralita, posunová činidla. Interpretace 13 C NMR spekter
 LEKCE 2b NMR a chiralita, posunová činidla Interpretace 13 C NMR spekter Stanovení optické čistoty Enantiomery jsou nerozlišitelné v NMR spektroskopii není možné rozlišit enantiomer od racemátu!!! Enantiotopické
LEKCE 2b NMR a chiralita, posunová činidla Interpretace 13 C NMR spekter Stanovení optické čistoty Enantiomery jsou nerozlišitelné v NMR spektroskopii není možné rozlišit enantiomer od racemátu!!! Enantiotopické
Autoři: Pavel Zachař, David Sýkora Ukázky spekter k procvičování na semináři: Tento soubor je pouze prvním ilustrativním seznámením se základními prin
 Autoři: Pavel Zachař, David Sýkora Ukázky spekter k procvičování na semináři: Tento soubor je pouze prvním ilustrativním seznámením se základními principy hmotnostní spektrometrie a v žádném případě nezahrnuje
Autoři: Pavel Zachař, David Sýkora Ukázky spekter k procvičování na semináři: Tento soubor je pouze prvním ilustrativním seznámením se základními principy hmotnostní spektrometrie a v žádném případě nezahrnuje
Techniky měření a interpretace NMR spekter. Bohumil Dolenský VŠCHT Praha místnost A28 linka 4110
 Techniky měření a interpretace NMR spekter Bohumil Dolenský VŠCT Praha místnost A28 linka 4110 NMR je nejsilnějším analytickým nástrojem k řešení struktury organický látek královna strukturních metod.
Techniky měření a interpretace NMR spekter Bohumil Dolenský VŠCT Praha místnost A28 linka 4110 NMR je nejsilnějším analytickým nástrojem k řešení struktury organický látek královna strukturních metod.
doc. Ing. Richard Hrabal, CSc. Ing. Hana Dvořáková, CSc. RNDr. Jan Lang, PhD. Číslo dveří A 42, telefon 3805,
 Vyučující: doc. Ing. Richard rabal, CSc. Ing. ana Dvořáková, CSc. RNDr. Jan Lang, PhD. Číslo dveří A 42, telefon 3805, e-mail hrabalr@vscht.cz Termín: každé pondělí od 8.30 do 11.30 Místo: posluchárna
Vyučující: doc. Ing. Richard rabal, CSc. Ing. ana Dvořáková, CSc. RNDr. Jan Lang, PhD. Číslo dveří A 42, telefon 3805, e-mail hrabalr@vscht.cz Termín: každé pondělí od 8.30 do 11.30 Místo: posluchárna
CHEMIE - Úvod do organické chemie
 Název školy Číslo projektu Autor Název šablony Název DUMu Stupeň a typ vzdělávání Vzdělávací oblast Vzdělávací obor Vzdělávací okruh Druh učebního materiálu Cílová skupina Anotace SŠHS Kroměříž CZ.1.07/1.5.00/34.0911
Název školy Číslo projektu Autor Název šablony Název DUMu Stupeň a typ vzdělávání Vzdělávací oblast Vzdělávací obor Vzdělávací okruh Druh učebního materiálu Cílová skupina Anotace SŠHS Kroměříž CZ.1.07/1.5.00/34.0911
Nukleární Overhauserův efekt (NOE)
 LEKCE 8 Nukleární verhauserův efekt (NE) určení prostorové struktury molekul využití REY spektroskopie projevy NE a chemické výměny v jednom systému Nukleární verhauserův efekt (NE) důsledek dipolární
LEKCE 8 Nukleární verhauserův efekt (NE) určení prostorové struktury molekul využití REY spektroskopie projevy NE a chemické výměny v jednom systému Nukleární verhauserův efekt (NE) důsledek dipolární
Nukleární Overhauserův efekt (NOE)
 Nukleární Overhauserův efekt (NOE) NOE je důsledek dipolární interakce mezi dvěma jádry. Vzniká přímou interakcí volně přes prostor, tudíž není ovlivněn chemickými vazbami jako nepřímá spin-spinová interakce.
Nukleární Overhauserův efekt (NOE) NOE je důsledek dipolární interakce mezi dvěma jádry. Vzniká přímou interakcí volně přes prostor, tudíž není ovlivněn chemickými vazbami jako nepřímá spin-spinová interakce.
HYDROXYDERIVÁTY. Alkoholy Fenoly Bc. Miroslava Wilczková
 HYDROXYDERIVÁTY Alkoholy Fenoly Bc. Miroslava Wilczková HYDROXYDERIVÁTY Alkoholy -OH skupina vázána na uhlíkový atom alifatického řetězce Fenoly -OH skupina vázána na uhlíku, který je součástí aromatického
HYDROXYDERIVÁTY Alkoholy Fenoly Bc. Miroslava Wilczková HYDROXYDERIVÁTY Alkoholy -OH skupina vázána na uhlíkový atom alifatického řetězce Fenoly -OH skupina vázána na uhlíku, který je součástí aromatického
2. Atomové jádro a jeho stabilita
 2. Atomové jádro a jeho stabilita Atom je nejmenší hmotnou a chemicky nedělitelnou částicí. Je tvořen jádrem, které obsahuje protony a neutrony, a elektronovým obalem. Elementární částice proton neutron
2. Atomové jádro a jeho stabilita Atom je nejmenší hmotnou a chemicky nedělitelnou částicí. Je tvořen jádrem, které obsahuje protony a neutrony, a elektronovým obalem. Elementární částice proton neutron
INTERPRETACE INFRAČERVENÝCH SPEKTER
 INTERPRETACE INFRAČERVENÝCH SPEKTER Obecné základy nedestruktivní metoda strukturní analýzy měření přechodů mezi vibračními hladinami změna dipólového momentu během vibrace v=3 v=2 v=1 v=0 fundamentální
INTERPRETACE INFRAČERVENÝCH SPEKTER Obecné základy nedestruktivní metoda strukturní analýzy měření přechodů mezi vibračními hladinami změna dipólového momentu během vibrace v=3 v=2 v=1 v=0 fundamentální
Základy Mössbauerovy spektroskopie. Libor Machala
 Základy Mössbauerovy spektroskopie Libor Machala Rudolf L. Mössbauer 1958: jev bezodrazové rezonanční absorpce záření gama atomovým jádrem 1961: Nobelova cena Analogie s rezonanční absorpcí akustických
Základy Mössbauerovy spektroskopie Libor Machala Rudolf L. Mössbauer 1958: jev bezodrazové rezonanční absorpce záření gama atomovým jádrem 1961: Nobelova cena Analogie s rezonanční absorpcí akustických
ZÁKLADNÍ EXPERIMENTÁLNÍ
 Kurz praktické NMR spektroskopie 10. - 12. říjen 2011, Praha ZÁKLADNÍ EXPERIMENTÁLNÍ POSTUPY NMR ROZTOKŮ A KAPALIN Jana Svobodová Ústav Makromolekulární chemie AV ČR, v.v.i. Bruker 600 Avance III PŘÍSTROJOVÉ
Kurz praktické NMR spektroskopie 10. - 12. říjen 2011, Praha ZÁKLADNÍ EXPERIMENTÁLNÍ POSTUPY NMR ROZTOKŮ A KAPALIN Jana Svobodová Ústav Makromolekulární chemie AV ČR, v.v.i. Bruker 600 Avance III PŘÍSTROJOVÉ
Fyzika IV. 1) orbitální magnetický moment (... moment proudové smyčky) gyromagnetický poměr: kvantování: Bohrův magneton: 2) spinový magnetický moment
 λ=21 cm 1) orbitální magnetický moment (... moment proudové smyčky) μ I S gyromagnetický poměr: kvantování: Bohrův magneton: 2) spinový magnetický moment 2 Zeemanův jev - rozštěpení spektrálních čar v
λ=21 cm 1) orbitální magnetický moment (... moment proudové smyčky) μ I S gyromagnetický poměr: kvantování: Bohrův magneton: 2) spinový magnetický moment 2 Zeemanův jev - rozštěpení spektrálních čar v
Techniky měření a interpretace NMR spekter
 Techniky měření a interpretace MR spekter Bohumil Dolenský VŠT Praha místnost A28 linka 4110 MR EZ 500R JEL Supravodičový magnet ( 4,2 K ) 11,74736 Tesla 261052-krát pole Země 1 500,1599 Mz 125,7653 Mz
Techniky měření a interpretace MR spekter Bohumil Dolenský VŠT Praha místnost A28 linka 4110 MR EZ 500R JEL Supravodičový magnet ( 4,2 K ) 11,74736 Tesla 261052-krát pole Země 1 500,1599 Mz 125,7653 Mz
Opakování
 Slabé vazebné interakce Opakování Co je to atom? Opakování Opakování Co je to atom? Atom je nejmenší částice hmoty, chemicky dále nedělitelná. Skládá se z atomového jádra obsahujícího protony a neutrony
Slabé vazebné interakce Opakování Co je to atom? Opakování Opakování Co je to atom? Atom je nejmenší částice hmoty, chemicky dále nedělitelná. Skládá se z atomového jádra obsahujícího protony a neutrony
NMR SPEKTROSKOPIE PRO CHEMIKY
 NMR SPEKTROSKOPIE PRO CHEMIKY 1. Úvod 1.1 Historický úvod 1.2 Jazykové okénko 2. Principy NMR spektroskopie 2.1 Jaderný spin 2.2 Chemický posun 2.3 Snímání NMR signálu 2.4 Fourierova transformace 2.5 Magnetické
NMR SPEKTROSKOPIE PRO CHEMIKY 1. Úvod 1.1 Historický úvod 1.2 Jazykové okénko 2. Principy NMR spektroskopie 2.1 Jaderný spin 2.2 Chemický posun 2.3 Snímání NMR signálu 2.4 Fourierova transformace 2.5 Magnetické
Sekunda (2 hodiny týdně) Chemické látky a jejich vlastnosti Směsi a jejich dělení Voda, vzduch
 Sekunda (2 hodiny týdně) Chemické látky a jejich vlastnosti Směsi a jejich dělení Voda, vzduch Atom, složení a struktura Chemické prvky-názvosloví, slučivost Chemické sloučeniny, molekuly Chemická vazba
Sekunda (2 hodiny týdně) Chemické látky a jejich vlastnosti Směsi a jejich dělení Voda, vzduch Atom, složení a struktura Chemické prvky-názvosloví, slučivost Chemické sloučeniny, molekuly Chemická vazba
Kyslíkaté deriváty. 1) Hydroxyderiváty: a) Alkoholy b) Fenoly. řešení. Dle OH = hydroxylová skupina
 Kyslíkaté deriváty řešení 1) Hydroxyderiváty: a) Alkoholy b) Fenoly Dle = hydroxylová skupina 1 Hydroxyderiváty Alifatické alkoholy: náhrada 1 nebo více atomů H. hydroxylovou skupinou (na 1 atom C vázaná
Kyslíkaté deriváty řešení 1) Hydroxyderiváty: a) Alkoholy b) Fenoly Dle = hydroxylová skupina 1 Hydroxyderiváty Alifatické alkoholy: náhrada 1 nebo více atomů H. hydroxylovou skupinou (na 1 atom C vázaná
Základy NMR 2D spektroskopie
 Základy NMR 2D spektroskopie Jaroslav Kříž Ústav makromolekulární chemie AV ČR v.v.i. puls 1D : d 1 Fourierova transformace časového rozvoje odezvy dá 1D spektrum 2D: d 1 d 1 d 1 d 0 d 0 + in 0 d 0 + 2in
Základy NMR 2D spektroskopie Jaroslav Kříž Ústav makromolekulární chemie AV ČR v.v.i. puls 1D : d 1 Fourierova transformace časového rozvoje odezvy dá 1D spektrum 2D: d 1 d 1 d 1 d 0 d 0 + in 0 d 0 + 2in
INTERPRETACE HMOTNOSTNÍCH SPEKTER
 INTERPRETACE HMOTNOSTNÍCH SPEKTER Hmotnostní spektrometrie hmotnostní spektrometrie = fyzikálně chemická metoda založená na rozdělení hmotnosti iontů v plynné fázi podle jejich poměru hmotnosti a náboje
INTERPRETACE HMOTNOSTNÍCH SPEKTER Hmotnostní spektrometrie hmotnostní spektrometrie = fyzikálně chemická metoda založená na rozdělení hmotnosti iontů v plynné fázi podle jejich poměru hmotnosti a náboje
Stereochemie. Přednáška 6
 Stereochemie Přednáška 6 Stereoheterotopické ligandy a NMR spektroskopie Stereoheterotopické ligandy a NMR spektroskopie NMR může rozlišit atomy v odlišném okolí stíněny jinou měrou rozdíl v chemických
Stereochemie Přednáška 6 Stereoheterotopické ligandy a NMR spektroskopie Stereoheterotopické ligandy a NMR spektroskopie NMR může rozlišit atomy v odlišném okolí stíněny jinou měrou rozdíl v chemických
Třídění látek. Chemie 1.KŠPA
 Třídění látek Chemie 1.KŠPA Systém (soustava) Vymezím si kus prostoru, látky v něm obsažené nazýváme systém soustava okolí svět Stěny soustavy Soustava může být: Izolovaná = stěny nedovolí výměnu částic
Třídění látek Chemie 1.KŠPA Systém (soustava) Vymezím si kus prostoru, látky v něm obsažené nazýváme systém soustava okolí svět Stěny soustavy Soustava může být: Izolovaná = stěny nedovolí výměnu částic
ZŠ ÚnO, Bratří Čapků 1332
 Animovaná chemie Top-Hit Analytická chemie Analýza anorganických látek Důkaz aniontů Důkaz kationtů Důkaz kyslíku Důkaz vody Gravimetrická analýza Hmotnostní spektroskopie Chemická analýza Nukleární magnetická
Animovaná chemie Top-Hit Analytická chemie Analýza anorganických látek Důkaz aniontů Důkaz kationtů Důkaz kyslíku Důkaz vody Gravimetrická analýza Hmotnostní spektroskopie Chemická analýza Nukleární magnetická
Středoškolská odborná činnost 2005/2006
 Středoškolská odborná činnost 2005/2006 Obor 3 - chemie Autor: Martin Hejda MSŠCH, Křemencova 12 116 28 Praha 1, 3. ročník Zadavatel a vedoucí práce: Mgr. Miroslav Kašpar CSc. Fyzikální ústav AVČR Na Slovance
Středoškolská odborná činnost 2005/2006 Obor 3 - chemie Autor: Martin Hejda MSŠCH, Křemencova 12 116 28 Praha 1, 3. ročník Zadavatel a vedoucí práce: Mgr. Miroslav Kašpar CSc. Fyzikální ústav AVČR Na Slovance
ATOMOVÁ SPEKTROMETRIE
 ATOMOVÁ SPEKTROMETRIE Atomová spektrometrie valenčních e - 1. OES (AES). AAS 3. AFS 1 Atomová spektra čárová spektra Tok záření P - množství zářivé energie (Q E ) přenesené od zdroje za jednotku času.
ATOMOVÁ SPEKTROMETRIE Atomová spektrometrie valenčních e - 1. OES (AES). AAS 3. AFS 1 Atomová spektra čárová spektra Tok záření P - množství zářivé energie (Q E ) přenesené od zdroje za jednotku času.
Optické spektroskopie 1 LS 2014/15
 Optické spektroskopie 1 LS 2014/15 Martin Kubala 585634179 mkubala@prfnw.upol.cz 1.Úvod Velikosti objektů v přírodě Dítě ~ 1 m (10 0 m) Prst ~ 2 cm (10-2 m) Vlas ~ 0.1 mm (10-4 m) Buňka ~ 20 m (10-5 m)
Optické spektroskopie 1 LS 2014/15 Martin Kubala 585634179 mkubala@prfnw.upol.cz 1.Úvod Velikosti objektů v přírodě Dítě ~ 1 m (10 0 m) Prst ~ 2 cm (10-2 m) Vlas ~ 0.1 mm (10-4 m) Buňka ~ 20 m (10-5 m)
doc. Ing. Richard Hrabal, CSc. Ing. Hana Dvořáková, CSc. doc. RNDr. Jan Lang, PhD. Ing. Jan Prchal, Ph.D.
 Vyučující: doc. Ing. Richard rabal, CSc. Ing. ana Dvořáková, CSc. doc. RNDr. Jan Lang, PhD. Ing. Jan Prchal, Ph.D. Číslo dveří A 42, telefon 3805, e-mail hrabalr@vscht.cz Termín: každý čtvrtek od 10,00
Vyučující: doc. Ing. Richard rabal, CSc. Ing. ana Dvořáková, CSc. doc. RNDr. Jan Lang, PhD. Ing. Jan Prchal, Ph.D. Číslo dveří A 42, telefon 3805, e-mail hrabalr@vscht.cz Termín: každý čtvrtek od 10,00
LEKCE 7. Interpretace 13 C NMR spekter. Využití 2D experimentů. Zpracování, výpočet a databáze NMR spekter (ACD/Labs, Topspin, Mnova) ppm
 LEKCE 7 Interpretace 13 C MR spekter Využití 2D experimentů ppm 1.0 1.5 2.0 2.5 3.0 3.5 4.0 4.5 5.0 5.5 6.0 6.5 6.5 6.0 5.5 5.0 4.5 4.0 3.5 3.0 2.5 2.0 1.5 1.0 ppm Zpracování, výpočet a databáze MR spekter
LEKCE 7 Interpretace 13 C MR spekter Využití 2D experimentů ppm 1.0 1.5 2.0 2.5 3.0 3.5 4.0 4.5 5.0 5.5 6.0 6.5 6.5 6.0 5.5 5.0 4.5 4.0 3.5 3.0 2.5 2.0 1.5 1.0 ppm Zpracování, výpočet a databáze MR spekter
Gymnázium Jiřího Ortena, Kutná Hora
 Předmět: Náplň: Třída: Počet hodin: Pomůcky: Chemie (CHE) Obecná chemie 1. ročník a kvinta 2 hodiny týdně Školní tabule, interaktivní tabule, tyčinkové a kalotové modely molekul, zpětný projektor, transparenty,
Předmět: Náplň: Třída: Počet hodin: Pomůcky: Chemie (CHE) Obecná chemie 1. ročník a kvinta 2 hodiny týdně Školní tabule, interaktivní tabule, tyčinkové a kalotové modely molekul, zpětný projektor, transparenty,
Dekapling, koherentní transfer polarizace, nukleární Overhauserův jev
 Dekapling Dekapling, koherentní transfer polarizace, nukleární Overhauserův jev Dekaplingem rozumíme odstranění vlivu J-vazby XA na na spektra jader A působením dalšího radiofrekvenčního pole ( ω X )na
Dekapling Dekapling, koherentní transfer polarizace, nukleární Overhauserův jev Dekaplingem rozumíme odstranění vlivu J-vazby XA na na spektra jader A působením dalšího radiofrekvenčního pole ( ω X )na
Tabulace učebního plánu. Obecná chemie. Vzdělávací obsah pro vyučovací předmět : Ročník: 1.ročník a kvinta
 Tabulace učebního plánu Vzdělávací obsah pro vyučovací předmět : CHEMIE Ročník: 1.ročník a kvinta Obecná Bezpečnost práce Názvosloví anorganických sloučenin Zná pravidla bezpečnosti práce a dodržuje je.
Tabulace učebního plánu Vzdělávací obsah pro vyučovací předmět : CHEMIE Ročník: 1.ročník a kvinta Obecná Bezpečnost práce Názvosloví anorganických sloučenin Zná pravidla bezpečnosti práce a dodržuje je.
INFRAČERVENÁ SPEKTROMETRIE A BIOSLOŽKY PALIV
 VYSOKÁ ŠKOLA CHEMICKO-TECHNOLOGICKÁ V PRAZE Fakulta technologie ochrany prostředí Ústav technologie ropy a alternativních paliv INFRAČERVENÁ SPEKTROMETRIE A BIOSLOŽKY PALIV Laboratorní cvičení ÚVOD V několika
VYSOKÁ ŠKOLA CHEMICKO-TECHNOLOGICKÁ V PRAZE Fakulta technologie ochrany prostředí Ústav technologie ropy a alternativních paliv INFRAČERVENÁ SPEKTROMETRIE A BIOSLOŽKY PALIV Laboratorní cvičení ÚVOD V několika
Skoro každý prvek má nějaký stabilní isotop s nenulovým spinem. (Výjimky: Ar, Tc, Ce, Pm)
 Gyromagnetická částice, jev magnetické rezonance Pojmy s kterýma se můžete setkat: u elektronů lze Bohrův magneton Zkoumat NMR lze jen ty jádra, které mají nenulový jaderný spin: Několik systematických
Gyromagnetická částice, jev magnetické rezonance Pojmy s kterýma se můžete setkat: u elektronů lze Bohrův magneton Zkoumat NMR lze jen ty jádra, které mají nenulový jaderný spin: Několik systematických
LEKCE 2a. Interpretace 13 C NMR spekter. NMR a chiralita, posunová činidla. Zpracování, výpočet a databáze NMR spekter (ACD/Labs, Topspin, Mnova)
 LEKCE 2a NMR a chiralita, posunová činidla Interpretace 13 C NMR spekter Zpracování, výpočet a databáze NMR spekter (ACD/Labs, Topspin, Mnova) Symetrie v NMR spektrech - homotopické, enantiotopické, diastereotopické
LEKCE 2a NMR a chiralita, posunová činidla Interpretace 13 C NMR spekter Zpracování, výpočet a databáze NMR spekter (ACD/Labs, Topspin, Mnova) Symetrie v NMR spektrech - homotopické, enantiotopické, diastereotopické
SPEKTRÁLNÍ METODY. Ing. David MILDE, Ph.D. Katedra analytické chemie Tel.: ; (c) David MILDE,
 SEKTRÁLNÍ METODY Ing. David MILDE, h.d. Katedra analytické chemie Tel.: 585634443; E-mail: david.milde@upol.cz (c) -2008 oužitá a doporučená literatura Němcová I., Čermáková L., Rychlovský.: Spektrometrické
SEKTRÁLNÍ METODY Ing. David MILDE, h.d. Katedra analytické chemie Tel.: 585634443; E-mail: david.milde@upol.cz (c) -2008 oužitá a doporučená literatura Němcová I., Čermáková L., Rychlovský.: Spektrometrické
Měření a interpretace NMR spekter
 Měření a interpretace NMR spekter Bohumil Dolenský E-mail : Telefon : Místnost : www : dolenskb@vscht.cz (+420) 220 44 40 budova A, místnost 28 http://www.vscht.cz/anl/dolensky/technmr/index.html Struktura
Měření a interpretace NMR spekter Bohumil Dolenský E-mail : Telefon : Místnost : www : dolenskb@vscht.cz (+420) 220 44 40 budova A, místnost 28 http://www.vscht.cz/anl/dolensky/technmr/index.html Struktura
Analýza směsí, kvantitativní NMR spektroskopie a využití NMR spektroskopie ve forenzní analýze
 Analýza směsí, kvantitativní NMR spektroskopie a využití NMR spektroskopie ve forenzní analýze Analýza směsí a kvantitativní NMR NMR spektrum čisté látky je lineární kombinací spekter jejích jednotlivých
Analýza směsí, kvantitativní NMR spektroskopie a využití NMR spektroskopie ve forenzní analýze Analýza směsí a kvantitativní NMR NMR spektrum čisté látky je lineární kombinací spekter jejích jednotlivých
Měření a interpretace NMR spekter
 Měření a interpretace NMR spekter Bohumil Dolenský E-mail : Telefon : Místnost : www : dolenskb@vscht.cz (+420) 220 44 4110 budova A, místnost 28 http://www.vscht.cz/anl/dolensky/technmr/index.html Struktura
Měření a interpretace NMR spekter Bohumil Dolenský E-mail : Telefon : Místnost : www : dolenskb@vscht.cz (+420) 220 44 4110 budova A, místnost 28 http://www.vscht.cz/anl/dolensky/technmr/index.html Struktura
Látkové množství. 6,022 10 23 atomů C. Přípravný kurz Chemie 07. n = N. Doporučená literatura. Látkové množství n. Avogadrova konstanta N A
 Doporučená literatura Přípravný kurz Chemie 2006/07 07 RNDr. Josef Tomandl, Ph.D. Mailto: tomandl@med.muni.cz Předmět: Přípravný kurz chemie J. Vacík a kol.: Přehled středoškolské chemie. SPN, Praha 1990,
Doporučená literatura Přípravný kurz Chemie 2006/07 07 RNDr. Josef Tomandl, Ph.D. Mailto: tomandl@med.muni.cz Předmět: Přípravný kurz chemie J. Vacík a kol.: Přehled středoškolské chemie. SPN, Praha 1990,
COSY + - podmínky měření a zpracování dat ztráta rozlišení ve spektru. inphase dublet, disperzní. antiphase dublet, absorpční
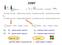 y x COSY 90 y chem. posuv J vazba 90 x : : inphase dublet, disperzní inphase dublet, disperzní antiphase dublet, absorpční antiphase dublet, absorpční diagonální pík krospík + - - + podmínky měření a zpracování
y x COSY 90 y chem. posuv J vazba 90 x : : inphase dublet, disperzní inphase dublet, disperzní antiphase dublet, absorpční antiphase dublet, absorpční diagonální pík krospík + - - + podmínky měření a zpracování
Diskutujte, jak široký bude pás spojený s fosforescencí versus fluorescencí. Udělejte odhad v cm -1.
 S použitím modelu volného elektronu (=částice v krabici) spočtěte vlnovou délku a vlnočet nejdlouhovlnějšího elektronového přechodu u molekuly dekapentaenu a oktatetraenu. Diskutujte polohu absorpčního
S použitím modelu volného elektronu (=částice v krabici) spočtěte vlnovou délku a vlnočet nejdlouhovlnějšího elektronového přechodu u molekuly dekapentaenu a oktatetraenu. Diskutujte polohu absorpčního
MATURITNÍ OTÁZKY Z CHEMIE
 MATURITNÍ OTÁZKY Z CHEMIE 1 Složení a struktura atomu Vývoj představ o složení a struktuře atomu, elektronový obal atomu, modely atomu, pojem orbital, typy orbitalů, jejich znázorňování a pravidla pro
MATURITNÍ OTÁZKY Z CHEMIE 1 Složení a struktura atomu Vývoj představ o složení a struktuře atomu, elektronový obal atomu, modely atomu, pojem orbital, typy orbitalů, jejich znázorňování a pravidla pro
Sada 7 Název souboru Ročník Předmět Formát Název výukového materiálu Anotace
 Sada 7 Název souboru Ročník Předmět Formát Název výukového materiálu Anotace VY_52_INOVACE_737 8. Chemie notebook Směsi Materiál slouží k vyvození a objasnění pojmů (klíčová slova - chemická látka, směs,
Sada 7 Název souboru Ročník Předmět Formát Název výukového materiálu Anotace VY_52_INOVACE_737 8. Chemie notebook Směsi Materiál slouží k vyvození a objasnění pojmů (klíčová slova - chemická látka, směs,
Karboxylové kyseliny a jejich funkční deriváty
 Karboxylové kyseliny a jejich funkční deriváty Úvod Karboxylové kyseliny jsou nejdůležitější organické kyseliny. Jejich funkční skupina je karboxylová skupina a tento název je složen ze slov karbonyl a
Karboxylové kyseliny a jejich funkční deriváty Úvod Karboxylové kyseliny jsou nejdůležitější organické kyseliny. Jejich funkční skupina je karboxylová skupina a tento název je složen ze slov karbonyl a
Dynamické procesy & Pokročilé aplikace NMR. chemická výměna, translační difuze, gradientní pulsy, potlačení rozpouštědla, NMR proteinů
 Dynamické procesy & Pokročilé aplikace NMR chemická výměna, translační difuze, gradientní pulsy, potlačení rozpouštědla, NMR proteinů Chemická výměna jakýkoli proces při kterém dané jádro mění svůj stav
Dynamické procesy & Pokročilé aplikace NMR chemická výměna, translační difuze, gradientní pulsy, potlačení rozpouštědla, NMR proteinů Chemická výměna jakýkoli proces při kterém dané jádro mění svůj stav
Přednášky z lékařské biofyziky Biofyzikální ústav Lékařské fakulty Masarykovy univerzity, Brno
 Přednášky z lékařské biofyziky Biofyzikální ústav Lékařské fakulty Masarykovy univerzity, Brno 1 Přednášky z lékařské biofyziky Biofyzikální ústav Lékařské fakulty Masarykovy univerzity, Brno Struktura
Přednášky z lékařské biofyziky Biofyzikální ústav Lékařské fakulty Masarykovy univerzity, Brno 1 Přednášky z lékařské biofyziky Biofyzikální ústav Lékařské fakulty Masarykovy univerzity, Brno Struktura
3. ročník Vzdělávací obor - Člověk a příroda
 Gymnázium, Milevsko, Masarykova 183 Školní vzdělávací program (ŠVP) pro vyšší stupeň osmiletého studia a čtyřleté studium Vyučovací předmět - Chemie 3. ročník Vzdělávací obor - Člověk a příroda Očekávané
Gymnázium, Milevsko, Masarykova 183 Školní vzdělávací program (ŠVP) pro vyšší stupeň osmiletého studia a čtyřleté studium Vyučovací předmět - Chemie 3. ročník Vzdělávací obor - Člověk a příroda Očekávané
Jádro se skládá z kladně nabitých protonů a neutrálních neutronů -> nukleony
 Otázka: Atom a molekula Předmět: Chemie Přidal(a): Dituse Atom = základní stavební částice všech látek Skládá se ze 2 částí: o Kladně nabité jádro o Záporně nabitý elektronový obal Jádro se skládá z kladně
Otázka: Atom a molekula Předmět: Chemie Přidal(a): Dituse Atom = základní stavební částice všech látek Skládá se ze 2 částí: o Kladně nabité jádro o Záporně nabitý elektronový obal Jádro se skládá z kladně
NMR spektrometr. Interpretace NMR spektra
 N (R)--propylpiperidin C N (S)--propylpiperidin C ( bod) Pon vadž se jedná o chirální organickou bázi, bylo by možné ji rozšt pit na izomery krystalizací vínan, pop ípad kafr-0-sulfonát. C C (7,7-dimethylbicyklo[..]hept--yl)methansulfonová
N (R)--propylpiperidin C N (S)--propylpiperidin C ( bod) Pon vadž se jedná o chirální organickou bázi, bylo by možné ji rozšt pit na izomery krystalizací vínan, pop ípad kafr-0-sulfonát. C C (7,7-dimethylbicyklo[..]hept--yl)methansulfonová
Naše NMR spektrometry
 Naše NMR spektrometry Varian NMR System 300 MHz Varian INOVA 400 MHz Bruker Avance III 600 MHz NMR spektrometr magnet průřez supravodičem NMR spektrometr sonda Tvar spektra reálná část imaginární část
Naše NMR spektrometry Varian NMR System 300 MHz Varian INOVA 400 MHz Bruker Avance III 600 MHz NMR spektrometr magnet průřez supravodičem NMR spektrometr sonda Tvar spektra reálná část imaginární část
H H C C C C C C H CH 3 H C C H H H H H H
 Alkany a cykloalkany sexta Martin Dojiva uhlovodíky obsahující pouze jednoduché vazby obecný vzorec alkanů: C n 2n+2 cykloalkanů: C n 2n homologický přírůstek C 2 Dělení alkanů přímé větvené u větvených
Alkany a cykloalkany sexta Martin Dojiva uhlovodíky obsahující pouze jednoduché vazby obecný vzorec alkanů: C n 2n+2 cykloalkanů: C n 2n homologický přírůstek C 2 Dělení alkanů přímé větvené u větvených
Halogenderiváty. Halogenderiváty
 Názvosloví Halogeny jsou v názvu vždy v předponě. Trichlormethan mátriviálnínázev CHLOROFORM Podle připojení halogenu je dělíme na primární sekundární a terciární Br Vazba mezi uhlíkem a halogenem je polarizovaná
Názvosloví Halogeny jsou v názvu vždy v předponě. Trichlormethan mátriviálnínázev CHLOROFORM Podle připojení halogenu je dělíme na primární sekundární a terciární Br Vazba mezi uhlíkem a halogenem je polarizovaná
CH 2 = CH 2 ethen systematický název propen CH 2 = CH CH 3 but-1-en CH 2 = CH CH 2 CH 3 but-2-en CH 3 CH = CH CH 3 buta-1,3-dien CH 2 = CH CH = CH 2
 Základní názvy organických látek alifatické nasycené alkany (příklady s nerozvětvenými řetězci) methan CH 4 ethan CH 3 CH 3 propan CH 3 CH 2 CH 3 butan CH 3 CH 2 CH 2 CH 3 pentan CH 3 CH 2 CH 2 CH 2 CH
Základní názvy organických látek alifatické nasycené alkany (příklady s nerozvětvenými řetězci) methan CH 4 ethan CH 3 CH 3 propan CH 3 CH 2 CH 3 butan CH 3 CH 2 CH 2 CH 3 pentan CH 3 CH 2 CH 2 CH 2 CH
Emise vyvolaná působením fotonů nebo částic
 Emise vyvolaná působením fotonů nebo částic PES (fotoelektronová spektroskopie) XPS (rentgenová fotoelektronová spektroskopie), ESCA (elektronová spektroskopie pro chemickou analýzu) UPS (ultrafialová
Emise vyvolaná působením fotonů nebo částic PES (fotoelektronová spektroskopie) XPS (rentgenová fotoelektronová spektroskopie), ESCA (elektronová spektroskopie pro chemickou analýzu) UPS (ultrafialová
Protonové číslo Z - udává počet protonů v jádře atomu, píše se jako index vlevo dole ke značce prvku
 Stavba jádra atomu Protonové Z - udává protonů v jádře atomu, píše se jako index vlevo dole ke značce prvku Neutronové N - udává neutronů v jádře atomu Nukleonové A = Z + N, udává nukleonů (protony + neutrony)
Stavba jádra atomu Protonové Z - udává protonů v jádře atomu, píše se jako index vlevo dole ke značce prvku Neutronové N - udává neutronů v jádře atomu Nukleonové A = Z + N, udává nukleonů (protony + neutrony)
Hamiltonián popisující atom vodíku ve vnějším magnetickém poli:
 Orbitální a spinový magnetický moment a jejich interakce s vnějším polem Vše na příkladu atomu H: Elektron (e - ) a jádro (u atomu H pouze p + ) mají vlastní magnetický moment (= spin). Tyto dva dipóly
Orbitální a spinový magnetický moment a jejich interakce s vnějším polem Vše na příkladu atomu H: Elektron (e - ) a jádro (u atomu H pouze p + ) mají vlastní magnetický moment (= spin). Tyto dva dipóly
ABSORPČNÍ A EMISNÍ SPEKTRÁLNÍ METODY
 ABSORPČNÍ A EMISNÍ SPEKTRÁLNÍ METODY 1 Fyzikální základy spektrálních metod Monochromatický zářivý tok 0 (W, rozměr m 2.kg.s -3 ): Absorbován ABS Propuštěn Odražen zpět r Rozptýlen s Bilance toků 0 = +
ABSORPČNÍ A EMISNÍ SPEKTRÁLNÍ METODY 1 Fyzikální základy spektrálních metod Monochromatický zářivý tok 0 (W, rozměr m 2.kg.s -3 ): Absorbován ABS Propuštěn Odražen zpět r Rozptýlen s Bilance toků 0 = +
Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti LC-NMR 1. Jan Sýkora
 Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti LC-NMR 1 Jan Sýkora LC/NMR Jan Sýkora (ÚCHP AV ČR) LC - NMR 1 H NMR (500 MHz) mez detekce ~ 1 mg/ml (5 µmol látky) NMR parametry doba
Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti LC-NMR 1 Jan Sýkora LC/NMR Jan Sýkora (ÚCHP AV ČR) LC - NMR 1 H NMR (500 MHz) mez detekce ~ 1 mg/ml (5 µmol látky) NMR parametry doba
Elektromagnetické záření. lineárně polarizované záření. Cirkulárně polarizované záření
 Elektromagnetické záření lineárně polarizované záření Cirkulárně polarizované záření Levotočivé Pravotočivé 1 Foton Jakékoli elektromagnetické vlnění je kvantováno na fotony, charakterizované: Vlnovou
Elektromagnetické záření lineárně polarizované záření Cirkulárně polarizované záření Levotočivé Pravotočivé 1 Foton Jakékoli elektromagnetické vlnění je kvantováno na fotony, charakterizované: Vlnovou
Charakteristika Teorie kyselin a zásad. Příprava kyselin Vlastnosti + typické reakce. Významné kyseliny. Arrheniova teorie Teorie Brönsted-Lowryho
 Petra Ustohalová 1 harakteristika Teorie kyselin a zásad Arrheniova teorie Teorie Brönsted-Lowryho Příprava kyselin Vlastnosti + typické reakce Fyzikální a chemické Významné kyseliny 2 Látky, které ve
Petra Ustohalová 1 harakteristika Teorie kyselin a zásad Arrheniova teorie Teorie Brönsted-Lowryho Příprava kyselin Vlastnosti + typické reakce Fyzikální a chemické Významné kyseliny 2 Látky, které ve
Organické látky. Organická geochemie a rozpuštěný organický uhlík
 Organická geochemie a rozpuštěný organický uhlík struktura, nomenklatura a funkční skupiny huminové látky a další přírodní OC reaktivita DOC/POC distribuce kyselost (acidita) Přírodní a znečišťující organické
Organická geochemie a rozpuštěný organický uhlík struktura, nomenklatura a funkční skupiny huminové látky a další přírodní OC reaktivita DOC/POC distribuce kyselost (acidita) Přírodní a znečišťující organické
6. Vyberte látku, která má nepolární charakter: 1b. a) voda b) diethylether c) kyselina bromovodíková d) ethanol e) sulfan
 1. Ionizace je: 1b. a) vysrážení iontů z roztoku b) vznik iontových vazeb c) solvatace iontů d) vznik iontů z elektroneutrálních sloučenin e) elektrolýza sloučenin 2. Počet elektronů v orbitalech s,p,d,f
1. Ionizace je: 1b. a) vysrážení iontů z roztoku b) vznik iontových vazeb c) solvatace iontů d) vznik iontů z elektroneutrálních sloučenin e) elektrolýza sloučenin 2. Počet elektronů v orbitalech s,p,d,f
ALKOHOLY, FENOLY A ETHERY. b. Jaké zdroje cukru znáte a jak se nazývají produkty jejich kvašení?
 ALKOLY, FENOLY A ETHERY Kvašení 1. S použitím literatury nebo internetu odpovězte na následující otázky: a. Jakým způsobem v přírodě vzniká etanol? Napište rovnici. b. Jaké zdroje cukru znáte a jak se
ALKOLY, FENOLY A ETHERY Kvašení 1. S použitím literatury nebo internetu odpovězte na následující otázky: a. Jakým způsobem v přírodě vzniká etanol? Napište rovnici. b. Jaké zdroje cukru znáte a jak se
NMR spektroskopie vysokého rozlišení v kapalné a pevné fázi spinový hamiltonián, typy interakcí, projevy ve spektrech
 NMR spektroskopie vysokého rozlišení v kapalné a pevné fázi spinový hamiltonián, typy interakcí, projevy ve spektrech Spinový hamiltonián Hamiltonián soustavy jader a elektronů v magnetickém poli lze zapsat
NMR spektroskopie vysokého rozlišení v kapalné a pevné fázi spinový hamiltonián, typy interakcí, projevy ve spektrech Spinový hamiltonián Hamiltonián soustavy jader a elektronů v magnetickém poli lze zapsat
Seminář NMR. Mgr. Zdeněk Moravec, Ph.D.; hugo@chemi.muni.cz Ústav chemie, PřF MU, 22.-25. 7. 2013 http://nmrlab.chemi.muni.cz/
 Seminář NMR Mgr. Zdeněk Moravec, Ph.D.; hugo@chemi.muni.cz Ústav chemie, PřF MU, 22.-25. 7. 2013 http://nmrlab.chemi.muni.cz/ Osnova Úvod, základní princip Instrumentace magnety, měřící sondy, elektronika
Seminář NMR Mgr. Zdeněk Moravec, Ph.D.; hugo@chemi.muni.cz Ústav chemie, PřF MU, 22.-25. 7. 2013 http://nmrlab.chemi.muni.cz/ Osnova Úvod, základní princip Instrumentace magnety, měřící sondy, elektronika
Reálné gymnázium a základní škola města Prostějova Školní vzdělávací program pro ZV Ruku v ruce
 6 ČLOVĚK A PŘÍRODA UČEBNÍ OSNOVY 6. 2 Chemie Časová dotace 8. ročník 2 hodiny 9. ročník 2 hodiny Celková dotace na 2. stupni je 4 hodiny. Charakteristika: Vyučovací předmět chemie vede k poznávání chemických
6 ČLOVĚK A PŘÍRODA UČEBNÍ OSNOVY 6. 2 Chemie Časová dotace 8. ročník 2 hodiny 9. ročník 2 hodiny Celková dotace na 2. stupni je 4 hodiny. Charakteristika: Vyučovací předmět chemie vede k poznávání chemických
Gymnázium Jiřího Ortena, Kutná Hora
 Předmět: Náplň: Třída: Počet hodin: Pomůcky: Chemie (CHE) Obecná chemie, anorganická chemie Tercie 2 hodiny týdně Školní tabule, interaktivní tabule, Apple TV, tablety, tyčinkové a kalotové modely molekul,
Předmět: Náplň: Třída: Počet hodin: Pomůcky: Chemie (CHE) Obecná chemie, anorganická chemie Tercie 2 hodiny týdně Školní tabule, interaktivní tabule, Apple TV, tablety, tyčinkové a kalotové modely molekul,
Atom vodíku. Nejjednodušší soustava: p + e Řešitelná exaktně. Kulová symetrie. Potenciální energie mezi p + e. e =
 Atom vodíku Nejjednodušší soustava: p + e Řešitelná exaktně Kulová symetrie Potenciální energie mezi p + e V 2 e = 4πε r 0 1 Polární souřadnice využití kulové symetrie atomu Ψ(x,y,z) Ψ(r,θ, φ) x =? y=?
Atom vodíku Nejjednodušší soustava: p + e Řešitelná exaktně Kulová symetrie Potenciální energie mezi p + e V 2 e = 4πε r 0 1 Polární souřadnice využití kulové symetrie atomu Ψ(x,y,z) Ψ(r,θ, φ) x =? y=?
Organická chemie 3.ročník studijního oboru - kosmetické služby.
 Organická chemie 3.ročník studijního oboru - kosmetické služby. T-7 Funkční a substituční deriváty karboxylových kyselin Zpracováno v rámci projektu Zlepšení podmínek ke vzdělávání Registrační číslo projektu:
Organická chemie 3.ročník studijního oboru - kosmetické služby. T-7 Funkční a substituční deriváty karboxylových kyselin Zpracováno v rámci projektu Zlepšení podmínek ke vzdělávání Registrační číslo projektu:
