Stavové rovnice. v = (zobecnìný) vylouèený objem. plyn + kapalina
|
|
|
- Štěpán Jaroš
- před 6 lety
- Počet zobrazení:
Transkript
1 Stavové rovnice Stavová rovnice je vztah mezi p, T, V a n (u smìsí slo¾ením n i ), alternativnì p, T, Vm = V/n (u smìsí je¹tì x i ) èi jinými ekvivalentními velièinami. plyn ideální plyn: pvm/rt = 1 viriálová EOS: pvm/rt = 1 + B/Vm + C/V 2 m... B (= druhý viriálový koecient) je dán párovými interakcemi: plyn + kapalina B = N [e A u(r)/k T B 1 ] d r = vn A 2 2 1/18 v = (zobecnìný) vylouèený objem kubické dvoukonstantové: van der Waals, Redlich{Kwong, Peng{Robinson aj. (nastavení na Tc, pc) tøíkonstantové lep¹í reference: augmented van der Waals, SAFT vícekonstantové empirické: Benedict{Webb{Rubin empirické (pro VLE): (l) pomocí aktivitních koecientù, (g) ideální plyn
2 Stavové rovnice 2/18 kapaliny, pøíp. kapalina+pevná látka kapaliny: Hildebrand polymery: Flory{Huggins Základní teoretické postupy odhad entropické èásti: ideální plyn/smìs odhad energetické èásti: støední pole (mean eld) okolních (= náhodnì se vyskytujících) molekul oblast kritického bodu: renormalizace poruchové teorie (vhodná snadno popsatelná reference jako tuhé koule + pøita¾livé síly jako porucha)
3 van der Waalsova stavová rovnice: p [show/vdw.sh] 3/18 Mezimolekulové síly: odpudivé (repulze): Vm Vm b kriticky bod (g) Molekulám je dostupný objem men¹í o vlastní objem molekul b. pøita¾livé (atrakce), p nasycena kapalina kapalina + para v rovnovaze nasycena para p p + a/v 2 m Molekul u stìny je 1/Vm a zároveò ka¾dá je vtahována do objemové fáze silou 1/Vm, úèinek nárazù klesne 1/V 2 m. 0 0 (l) (l)+(g) pvm = RT V ( p + a ) Vm 2 (Vm b) = RT
4 van der Waalsova stavová rovnice: F [show/vdwf.sh] 4/18 Rozvoj kolem ideálního plynu jako reference: entropie id. plyn: Sm = R ln Vm + const (dostupný prostor = Vm) van der Waals: Sm = R ln(vm b) + const (dostupný prostor = Vm b) energie id. plyn: Um = 0 (molekuly neinteragují) van der Waals: Um = a/vm (square-well pro λ ) Poznámky k ukázce F vdw (V): Fm = Um TSm = a Vm RT ln(v m b) ( ) F p = = a V T Vm 2 + RT Vm b = to samé termodynamické potenciály F, G jsou v¾dy konvexní jako funkce svých pøirozených promìnných pokud (v modelu) nejsou konvexní, existuje bod s ni¾¹í hodnotou termodynamického potenciálu (na konvexním obalu), který odpovídá dvìma fázím v rovnováze spoleèná teèna Maxwellovo pravidlo
5 Rovnováha a stabilita Maxwellovo jsou stejné: pravidlo: oran¾ové plochy Za konst. T integrujeme plochy se znaménkem: V2 V 1 ( peos p equil ) dv p stejne kriticky bod nestabilni izoterma binodala = (V 2 V 1 )p equil + V2 V 1 p EOS dv metastabilni izoterma 5/18 (g) stabilni izoterma spinodala = (V 2 V 1 )p equil F = G = 0 (l) (l)+(g) ( p V ( p V ) ) T T 0 0 V 1 V 2 V < 0: lokálnì mechanicky stabilní; uvnitø binodály metastabilní > 0: mechanicky nestabilní { okam¾itì se rozpadne na fáze
6 Møí¾kový model smìsi 6/18 Uva¾ujme model slo¾ený z þmonomerùÿ (nikoliv nutnì chemických èi Kuhnových) nebo þèlánkùÿ na møí¾ce. Zároveò platí Amagatùv zákon (objem se smícháním nezmìní). Molekula A nech» zaujímá N A møí¾kových bodù (èlánkù). Molekula B nech» zaujímá N B møí¾kových bodù. Poèet stavù molekuly A na møí¾ce o poètu vrcholù n A je NA = 2 NA = 2 W A = n A W i,a W i,a = poèet konformací (bez ohledu na translace) n A = poèet translací Poèet stavù molekuly A na møí¾ce o poètu vrcholù n = n A + n B je NA 1 NB = 1 W = nw i,a (pøedpokládáme, ¾e poèet konformací molekuly A ve smìsi s B je stejný jako v èisté látce, toti¾ W i,a )
7 Møí¾kový model smìsi II: entropie v akci Zmìna entropie látky A je 7/18 mix S A = k B ln W k B ln W A = k B ln(n A /n) k B ln φ A kde φ A je objemový zlomek. Poèet molekul typu A je n A /N A. Pro obì molekuly: ( na mix S = k B ln φ N A + n B ln φ A N B B Smì¹ovací entropie na jeden vrchol møí¾ky je mix S = mixs n ) = k B ( φa N A ln φ A + φ B N B ln φ B Pro monomery (N A = N B = 1) o stejném objemu (φ A = x A ), na mol: mix Sm = R(x A ln x A + x B ln x B ) co¾ je ideální smì¹ovací entropie. Pro roztok 1 makromolekuly A v rozpou¹tìdle B co¾ je ménì. mix S = k B ( φa N A ln φ A + φ B ln φ B ) )
8 Møí¾kový model smìsi III Roztok s ideální smì¹ovací entropií, tj. náhodným rozmístìním molekul na møí¾ce, ale obecnì neideální energií (entalpií), se nazývá regulární roztok. Název obv. rezervován pro malé molekuly, ne polymery. Bývá dobrou aproximací, jsou-li zmìny energie malé (efekt 2. øádu). Støední energie smìsi monomerù (N A = N B = 1) na møí¾ce s koordinaèním èíslem (poètem sousedù) z (tzv. smì¹ovací pravidlo): U = zn 2 kde φ = φ A, φ B = 1 φ A = 1 φ [u AA φ 2 + 2u AB φ(1 φ) + u BB (1 φ) 2] mix U = U U A U B = U zn 2 u AAφ zn 2 u BB(1 φ) 8/18 u ij < 0 Na 1 vrchol møí¾ky: kde Floryho interakèní parametr je = zn 2 φ(1 φ)(2u AB u AA u BB ) mix U = χφ(1 φ)k B T χ = z 22u AB u AA u BB k B T u u 0 +C vrchol T A + B T
9 Helmholtzova energie smìsi [plot/oryhuggins.sh] 9/18 Helmholtzova energie smìsi (na 1 vrchol møí¾ky) [ φ mix F = mix U T mix S = k B T ln φ + 1 φ ln(1 φ) + χφ(1 φ) N A N B regulární roztok (N A = N B = 1) (Hildebrand): mix F = k B T [ φ ln φ + (1 φ) ln(1 φ) + χφ(1 φ) ] roztok polymeru A v rozpou¹tìdle B (Flory{Huggins): [ φ mix F = k B T ln φ + (1 φ) ln(1 φ) + χφ(1 φ) N A Poznámky k ukázce: ideální smì¹ovací èlen je v¾dy konvexní, derivace v φ = 0, φ = 1 je nekoneèno interakèní èlen je obvykle kladný (pak je konkávní) je-li interakèní èlen dost velký [χ velké u AB (u AA + u BB )/2], rozpadne se systém na dvì fáze ] ]
10 Hustota kohezní energie 10/18 = energie potøebná pro rozebrání jednotkového objemu látky a pøenesení molekul do : vapu V = vapum Vm Hildebrandùv parametr rozpustnosti: δ = vapu V = vaphm RT Vm Jednotka: MPa 1/2 (pøíp. (cal cm 3 ) 1/2 = MPa 1/2 ) Látky s podobným δ se v sobì rozpou¹tí, polymer bobtná. patnì funguje pro silnì polární a vodíkové vazby. Pøíklady: látka δ/mpa 1/2 n-hexan 15 chloroform 19 ethanol 26 voda 48 látka δ/mpa 1/2 poly(ethylen) 16 PVC 19 nylon 6,6 28 (hydroxyethyl)methakrylát 52
11 Kombinaèní pravidla 11/18 Oznaème objem pøipadající na møí¾kový bod = v 0 Energie na 1 vrchol v èisté látce A: zu AA 2 = v 0 vapu V = v 0 δ 2 A Energie na 1 vrchol v èisté látce B: zu BB 2 = v 0 vapu V = v 0 δ 2 B Odhad energie A{B geometrickým prùmìrem: zu AB 2 = v 0 δ A δ B χ = z 22u AB u AA u BB k B T = v 0 k B T (δ A δ B ) 2 > 0 vyhovující pro Londonovy interakce hor¹í pro polární molekuly èi vodíkové vazby
12 Vsuvka: Kombinaèní a smì¹ovací pravidla 12/18 Vztahu pro u AB apod. na základì èistých látek se øíká kombinaèní pravidlo (combining rule). Modikace kombinaèního pravidla: zu AB = v 2 0 (1 k AB )δ A δ B Rovnì¾ pro parametry potenciálu máme kombinaèní pravidla, napø. [ (σ ) 12 ( σ ) ] 6 u(r) = 4ɛ r r : ɛ ij = (1 k ij ) ɛ i ɛ j, σ ij = { (σ i + σ j )/2, σ ij = σ i σ j Vztahu pro energii (potenciál èi jinou velièinu) smìsi, jako napø. u = u AA φ 2 + 2u AB φ(1 φ) + u BB (1 φ) 2 se øíká smì¹ovací pravidlo (mixing rule) Pøíklad smì¹ovacích a kombinaèních pravidel pro van der Waalsovu rovnici: a = a 11 x a 12x 1 x 2 + a 22 x 2 2, a 12 = (1 k 12 ) a 11 a 22 aditivní objem: b = b 1 x 1 + b 2 x 2 aditivní polomìr: b 1/3 = b 1/3 1 x 1 + b 1/3 2 x 2
13 Stabilita fází Helmholtzova energie F(V) nebo Gibbsova energie G(p) systému v rovnováze jsou v¾dy konvexní funkce. Pokud ne, rozpadne se systém na dvì fáze Mno¾ství fází: pákové pravidlo [uvodsim/showisi.sh] 13/18 Lokálnì stabilní: 2 F φ 2 > 0 Stabilní: lokálnì stabilní + le¾í na konvexním obalu Lokálnì nestabilní: 2 F φ 2 < 0 vznik stabilní fáze spinodální dekompozicí Spinodála (inexní bod): 2 F φ 2 = 0 Spinodála je pojem teorií støedního pole, v experimentu nedosa¾itelná Kritický bod: 2 F φ 2 = 3 F φ 3 = 0, 4 F φ 4 > 0 Metastabilní: lokálnì stabilní + nele¾í na konvexním obalu vznik stabilní fáze nukleací f(x) je konvexní v intervalu I kdy¾ x, y I a t [0, 1] : f(tx + (1 t)y) tf(x) + (1 t)f(y) striktnì konvexní: < konkávní: striktnì konkávní: >
14 Pøíklad: symetrická tavenina polymerù 14/18 Symetrická tavenina: N A = N B = N [ φ mix F = k B T N ln φ + 1 φ N Binodála: mixf φ Spinodála: χ = 1 2N ] ln(1 φ) + χφ(1 φ) ln[φ/(1 φ)] = 0 χ = (2φ 1)N ( 1 φ φ Kritický bod (symetrická smìs): χ = 2 N, φ = 1 2 Kritický bod (obecná smìs): χ = 1 2 ) ( 1/ NA + 1/ N B ) 2, φ = NB NA + N B Pro χ = A + B/T, B > 0 (obvyklej¹í pøípad): T crit = horní kritická rozpou¹tìcí teplota (UCST) Pro χ = A + B/T, B < 0 (ménì èasté): T crit = dolní kritická rozpou¹tìcí teplota (LCST) β mix F χ χ=3 χ=2 χ= metastabilni 2 kriticky bod 1 binodala F-H binodala 2D spinodala F-H binodala 3D φ nestabilni φ metastabilni
15 Møí¾kové modely: Isingùv model 15/ Jako model feromagnetu: U = J <i,j> s i s j + h i s i { 1, +1} = {, } s i, J = interakèní konstanta: J > 0: feromagnet, J < 0: antiferomagnet h = intenzita magn. pole Kritický (Curieùv) bod: h c = 0; 2D: T c /J = 2/ ln(1 + 2) Jako møí¾kový plyn: U = ɛ <i,j> n i n j + µ i n i {0, 1} = {, } n i, ɛ = velikost pøita¾livých sil µ = chemický potenciál Ekvivalence: n i = (1 + s i )/2 Jako model binární slitiny: U = <i,j> ɛ ki k j + i k i {, } µ ki, ɛ,, ɛ,, ɛ, = interakce sousedních atomù µ, µ = chem. pot. atomù Ekviv.: n i = 0 k i = n i = 1 k i =.
16 [showvid -d9 pic/harddisks.vid] Vsuvka: klasikace fázových pøechodù + 16/18 1. druhu: zlom na G, skok v entalpii, hustotì aj. (krystalizace, var) 2. druhu: Ehrenfest: zlom v entalpii, hustotì, vy¹¹í derivace skok; nyní i: vy¹¹í derivace divergují (kritický bod [CP], Curieùv bod, lambda-pøechod He, perkolace) { e spojité: v¹echny derivace spojité; napø.: 1/x pro x > 0 f(x) = 0 pro x 0 (nìkteré 2D systémy) Zeskelnìní (glass transition) = viskozita > Pa s { není fázový pøechod Vznik micel (v CMC) není fázový pøechod Krystalizace micel (do laminární/brilární fáze) je fázový pøechod 1. druhu 1. druh 2. druh (CP) 1. druh (?) spojitý
17 Bonus: Kritický bod jako náhodný fraktál Isingùv model jako møí¾kový plyn èi binární smìs. Transformace: ètvereèek barva dle pøevládající barvy 9 ètvereèkù [tchem/showisi.sh] 17/18 Kongurace po renormalizaci þvypadá stejnìÿ jako kongurace pùvodního systému pøi jiné teplotì Renormalizace pro h = 0: pro T > T c je T > T, tj. renormalizovaná kongurace je þnáhodnìj¹íÿ pro T < T c je T < T, tj. renormalizovaná kongurace obsahuje ménì spinù opaèného znaménka pro T = T c je T = T, tj. renormalizovaná kongurace vypadá stejnì, tj. je to fraktál Renormalizací se vzdalujeme od kritického bodu
18 Kritické exponenty 18/18 Flory{Huggins, van der Waals a jiné klasické teorie dávají pro T Tc, T < Tc: Správnì je ale ρ (l) ρ (g) const(t T c ) 1/2 ρ (l) ρ (g) const(t T c ) β kde β = (3) je kritický exponent Hodnota pochází z renormalizaèních studií Isingova modelu a vìøí se, ¾e je univerzální Kritická fáze má nekoneènou kompresibilitu a obsahuje uktuace hustoty, které ubývají se vzdáleností jako r η a projevují se kritickou opalescencí kritická opalescence SF 6 credit:
Viriálová stavová rovnice 1 + s.1
 Viriálová stavová rovnice 1 + s.1 (Mírnì nestandardní odvození Prùmìrná energie molekul okolo vybrané molekuly (β = 1/(k B T : 0 u(r e βu(r 4πr 2 dr Energie souboru N molekul: U = f 2 k B T + N 2 2V Tlak
Viriálová stavová rovnice 1 + s.1 (Mírnì nestandardní odvození Prùmìrná energie molekul okolo vybrané molekuly (β = 1/(k B T : 0 u(r e βu(r 4πr 2 dr Energie souboru N molekul: U = f 2 k B T + N 2 2V Tlak
Rovnováha kapalina{pára u binárních systémù
 Rovnováha kapalina{pára u binárních systémù 1 Pøedpoklad: 1 kapalná fáze Oznaèení: molární zlomky v kapalné fázi: x i molární zlomky v plynné fázi: y i Poèet stupòù volnosti: v = k f + 2 = 2 stav smìsi
Rovnováha kapalina{pára u binárních systémù 1 Pøedpoklad: 1 kapalná fáze Oznaèení: molární zlomky v kapalné fázi: x i molární zlomky v plynné fázi: y i Poèet stupòù volnosti: v = k f + 2 = 2 stav smìsi
Potenciální energie atom{atom
 Potenciální energie atom{atom 1/16 Londonovy (disperzní) síly: na del¹ích vzdálenostech, v¾dy pøita¾livé Model uktuující dipól { uktuující dipól elst. pole E 1/r 3 indukovaný dipól µ ind E energie u(r)
Potenciální energie atom{atom 1/16 Londonovy (disperzní) síly: na del¹ích vzdálenostech, v¾dy pøita¾livé Model uktuující dipól { uktuující dipól elst. pole E 1/r 3 indukovaný dipól µ ind E energie u(r)
Klasická termodynamika (aneb pøehled FCH I)
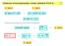 Klasická termodynamika (aneb pøehled FCH I) 1/16 0. zákon 1. zákon id. plyn: pv = nrt pv κ = konst (id., ad.) id. plyn: U = U(T) }{{} Carnotùv cyklus dq T = 0 2. zákon rg, K,... lim S = 0 T 0 S, ds = dq
Klasická termodynamika (aneb pøehled FCH I) 1/16 0. zákon 1. zákon id. plyn: pv = nrt pv κ = konst (id., ad.) id. plyn: U = U(T) }{{} Carnotùv cyklus dq T = 0 2. zákon rg, K,... lim S = 0 T 0 S, ds = dq
Opakování: Standardní stav þ ÿ
 Opakování: Standardní stav þ ÿ s.1 12. øíjna 215 Standardní stav þ ÿ = èistá slo¾ka ve stavu ideálního plynu za teploty soustavy T a standardního tlaku = 1 kpa, døíve 11,325 kpa. Èistá látka: Pøibli¾nì:
Opakování: Standardní stav þ ÿ s.1 12. øíjna 215 Standardní stav þ ÿ = èistá slo¾ka ve stavu ideálního plynu za teploty soustavy T a standardního tlaku = 1 kpa, døíve 11,325 kpa. Èistá látka: Pøibli¾nì:
Stanislav Labík. Ústav fyzikální chemie V CHT Praha budova A, 3. patro u zadního vchodu, místnost
 Stanislav Labík Ústav fyzikální chemie V CHT Praha budova A, 3. patro u zadního vchodu, místnost 325 labik@vscht.cz 220 444 257 http://www.vscht.cz/fch/ Výuka Letní semestr N403032 Základy fyzikální chemie
Stanislav Labík Ústav fyzikální chemie V CHT Praha budova A, 3. patro u zadního vchodu, místnost 325 labik@vscht.cz 220 444 257 http://www.vscht.cz/fch/ Výuka Letní semestr N403032 Základy fyzikální chemie
Fázová rozhraní a mezifázová energie
 Fázová rozhraní a mezifázová energie druhy: l/g l/l }{{} mobilní s/g s/l s/s 1/14 Pøíklad. Kolik % molekul vody je na povrchu kapièky mlhy o prùmìru a) 0.1 mm (hranice viditelnosti okem) b) 200 nm (hranice
Fázová rozhraní a mezifázová energie druhy: l/g l/l }{{} mobilní s/g s/l s/s 1/14 Pøíklad. Kolik % molekul vody je na povrchu kapièky mlhy o prùmìru a) 0.1 mm (hranice viditelnosti okem) b) 200 nm (hranice
Do známky zkoušky rovnocenným podílem započítávají získané body ze zápočtového testu.
 Podmínky pro získání zápočtu a zkoušky z předmětu Chemicko-inženýrská termodynamika pro zpracování ropy Zápočet je udělen, pokud student splní zápočtový test alespoň na 50 %. Zápočtový test obsahuje 3
Podmínky pro získání zápočtu a zkoušky z předmětu Chemicko-inženýrská termodynamika pro zpracování ropy Zápočet je udělen, pokud student splní zápočtový test alespoň na 50 %. Zápočtový test obsahuje 3
Termochemie { práce. Práce: W = s F nebo W = F ds. Objemová práce (p vn = vnìj¹í tlak): W = p vn dv. Vratný dìj: p = p vn (ze stavové rovnice) W =
 Termochemie { práce Práce: W = s F nebo W = Objemová práce (p vn = vnìj¹í tlak): W = V2 V 1 p vn dv s2 Vratný dìj: p = p vn (ze stavové rovnice) W = V2 V 1 p dv s 1 F ds s.1 Diferenciální tvar: dw = pdv
Termochemie { práce Práce: W = s F nebo W = Objemová práce (p vn = vnìj¹í tlak): W = V2 V 1 p vn dv s2 Vratný dìj: p = p vn (ze stavové rovnice) W = V2 V 1 p dv s 1 F ds s.1 Diferenciální tvar: dw = pdv
Fázová rozhraní a mezifázová energie
 Fázová rozhraní a mezifázová energie druhy: l/g l/l }{{} mobilní 1/15 s/g s/l s/s povrch koule = 4πr 2 Pøíklad. Kolik % molekul vody je na povrchu kapièky mlhy o prùmìru a) 0.1 mm (hranice viditelnosti
Fázová rozhraní a mezifázová energie druhy: l/g l/l }{{} mobilní 1/15 s/g s/l s/s povrch koule = 4πr 2 Pøíklad. Kolik % molekul vody je na povrchu kapièky mlhy o prùmìru a) 0.1 mm (hranice viditelnosti
Tepelná vodivost. střední rychlost. T 1 > T 2 z. teplo přenesené za čas dt: T 1 T 2. tepelný tok střední volná dráha. součinitel tepelné vodivosti
 Tepelná vodivost teplo přenesené za čas dt: T 1 > T z T 1 S tepelný tok střední volná dráha T součinitel tepelné vodivosti střední rychlost Tepelná vodivost součinitel tepelné vodivosti při T = 300 K součinitel
Tepelná vodivost teplo přenesené za čas dt: T 1 > T z T 1 S tepelný tok střední volná dráha T součinitel tepelné vodivosti střední rychlost Tepelná vodivost součinitel tepelné vodivosti při T = 300 K součinitel
Nultá věta termodynamická
 TERMODYNAMIKA Nultá věta termodynamická 2 Práce 3 Práce - příklady 4 1. věta termodynamická 5 Entalpie 6 Tepelné kapacity 7 Vnitřní energie a entalpie ideálního plynu 8 Výpočet tepla a práce 9 Adiabatický
TERMODYNAMIKA Nultá věta termodynamická 2 Práce 3 Práce - příklady 4 1. věta termodynamická 5 Entalpie 6 Tepelné kapacity 7 Vnitřní energie a entalpie ideálního plynu 8 Výpočet tepla a práce 9 Adiabatický
Fyzikální chemie. Magda Škvorová KFCH CN463 magda.skvorova@ujep.cz, tel. 3302. 14. února 2013
 Fyzikální chemie Magda Škvorová KFCH CN463 magda.skvorova@ujep.cz, tel. 3302 14. února 2013 Co je fyzikální chemie? Co je fyzikální chemie? makroskopický přístup: (klasická) termodynamika nerovnovážná
Fyzikální chemie Magda Škvorová KFCH CN463 magda.skvorova@ujep.cz, tel. 3302 14. února 2013 Co je fyzikální chemie? Co je fyzikální chemie? makroskopický přístup: (klasická) termodynamika nerovnovážná
Nekovalentní interakce
 Nekovalentní interakce Jan Řezáč UOCHB AV ČR 31. října 2017 Jan Řezáč (UOCHB AV ČR) Nekovalentní interakce 31. října 2017 1 / 28 Osnova 1 Teorie 2 Typy nekovalentních interakcí 3 Projevy v chemii 4 Výpočty
Nekovalentní interakce Jan Řezáč UOCHB AV ČR 31. října 2017 Jan Řezáč (UOCHB AV ČR) Nekovalentní interakce 31. října 2017 1 / 28 Osnova 1 Teorie 2 Typy nekovalentních interakcí 3 Projevy v chemii 4 Výpočty
5.7 Vlhkost vzduchu 5.7.5 Absolutní vlhkost 5.7.6 Poměrná vlhkost 5.7.7 Rosný bod 5.7.8 Složení vzduchu 5.7.9 Měření vlhkosti vzduchu
 Fázové přechody 5.6.5 Fáze Fázové rozhraní 5.6.6 Gibbsovo pravidlo fází 5.6.7 Fázový přechod Fázový přechod prvního druhu Fázový přechod druhého druhu 5.6.7.1 Clausiova-Clapeyronova rovnice 5.6.8 Skupenství
Fázové přechody 5.6.5 Fáze Fázové rozhraní 5.6.6 Gibbsovo pravidlo fází 5.6.7 Fázový přechod Fázový přechod prvního druhu Fázový přechod druhého druhu 5.6.7.1 Clausiova-Clapeyronova rovnice 5.6.8 Skupenství
Statistická termodynamika (mechanika)
 Statistická termodynamika (mechanika) 1/16 Makroskopické velièiny jsou výsledkem zprùmìrovaného chování mnoha èástic Tlak ideálního plynu z kinetické teorie 1 [tchem/simplyn.sh] 2/16 Molekula = hmotný
Statistická termodynamika (mechanika) 1/16 Makroskopické velièiny jsou výsledkem zprùmìrovaného chování mnoha èástic Tlak ideálního plynu z kinetické teorie 1 [tchem/simplyn.sh] 2/16 Molekula = hmotný
Nekovalentní interakce
 Nekovalentní interakce Jan Řezáč UOCHB AV ČR 3. listopadu 2016 Jan Řezáč (UOCHB AV ČR) Nekovalentní interakce 3. listopadu 2016 1 / 28 Osnova 1 Teorie 2 Typy nekovalentních interakcí 3 Projevy v chemii
Nekovalentní interakce Jan Řezáč UOCHB AV ČR 3. listopadu 2016 Jan Řezáč (UOCHB AV ČR) Nekovalentní interakce 3. listopadu 2016 1 / 28 Osnova 1 Teorie 2 Typy nekovalentních interakcí 3 Projevy v chemii
Fázová rozhraní a mezifázová energie
 Fázová rozhraní a mezifázová energie druhy: l/g l/l }{{} mobilní s/g s/l s/s 1/21 povrch koule = 4πr 2 Pøíklad. Kolik % molekul vody je na povrchu kapièky mlhy o prùmìru a) 0.1 mm (hranice viditelnosti
Fázová rozhraní a mezifázová energie druhy: l/g l/l }{{} mobilní s/g s/l s/s 1/21 povrch koule = 4πr 2 Pøíklad. Kolik % molekul vody je na povrchu kapièky mlhy o prùmìru a) 0.1 mm (hranice viditelnosti
Plyn. 11 plynných prvků. Vzácné plyny. He, Ne, Ar, Kr, Xe, Rn Diatomické plynné prvky H 2, N 2, O 2, F 2, Cl 2
 Plyny Plyn T v, K Vzácné plyny 11 plynných prvků He, Ne, Ar, Kr, Xe, Rn 165 Rn 211 N 2 O 2 77 F 2 90 85 Diatomické plynné prvky Cl 2 238 H 2, N 2, O 2, F 2, Cl 2 H 2 He Ne Ar Kr Xe 20 4.4 27 87 120 1 Plyn
Plyny Plyn T v, K Vzácné plyny 11 plynných prvků He, Ne, Ar, Kr, Xe, Rn 165 Rn 211 N 2 O 2 77 F 2 90 85 Diatomické plynné prvky Cl 2 238 H 2, N 2, O 2, F 2, Cl 2 H 2 He Ne Ar Kr Xe 20 4.4 27 87 120 1 Plyn
Fázová rozhraní a mezifázová energie
 Fázová rozhraní a mezifázová energie druhy: l/g l/l }{{} mobilní 1/23 s/g s/l s/s povrch koule = 4πr 2 Pøíklad. Kolik % molekul vody je na povrchu kapièky mlhy o prùmìru 200 nm (hranice viditelnosti optickým
Fázová rozhraní a mezifázová energie druhy: l/g l/l }{{} mobilní 1/23 s/g s/l s/s povrch koule = 4πr 2 Pøíklad. Kolik % molekul vody je na povrchu kapièky mlhy o prùmìru 200 nm (hranice viditelnosti optickým
Mezimolekulové interakce
 Mezimolekulové interakce Interakce molekul reaktivně vzniká či zaniká kovalentní vazba překryv elektronových oblaků, mění se vlastnosti nereaktivně vznikají molekulové komplexy slabá, nekovalentní, nechemická,
Mezimolekulové interakce Interakce molekul reaktivně vzniká či zaniká kovalentní vazba překryv elektronových oblaků, mění se vlastnosti nereaktivně vznikají molekulové komplexy slabá, nekovalentní, nechemická,
Plyn. 11 plynných prvků. Vzácné plyny. He, Ne, Ar, Kr, Xe, Rn Diatomické plynné prvky H 2, N 2, O 2, F 2, Cl 2
 Plyny Plyn T v, K Vzácné plyny 11 plynných prvků He, Ne, Ar, Kr, Xe, Rn 165 Rn 211 N 2 O 2 77 F 2 90 85 Diatomické plynné prvky Cl 2 238 H 2, N 2, O 2, F 2, Cl 2 H 2 He Ne Ar Kr Xe 20 4.4 27 87 120 1 Plyn
Plyny Plyn T v, K Vzácné plyny 11 plynných prvků He, Ne, Ar, Kr, Xe, Rn 165 Rn 211 N 2 O 2 77 F 2 90 85 Diatomické plynné prvky Cl 2 238 H 2, N 2, O 2, F 2, Cl 2 H 2 He Ne Ar Kr Xe 20 4.4 27 87 120 1 Plyn
Stavové chování kapalin a plynů II. 12. března 2010
 Stavové chování kapalin a plynů II. 12. března 2010 Stavové rovnice - obecně Van der Waalsova rovnice V čem je ukryta síla van der Waalse... A b=4n A V mol. Van der Waalsova rovnice (r. 1873) - první úspěšná
Stavové chování kapalin a plynů II. 12. března 2010 Stavové rovnice - obecně Van der Waalsova rovnice V čem je ukryta síla van der Waalse... A b=4n A V mol. Van der Waalsova rovnice (r. 1873) - první úspěšná
Aproximace funkcí. Chceme þvzoreèekÿ. Známe: celý prùbìh funkce
 Aproximace funkcí 1/13 Známe: celý prùbìh funkce Chceme þvzoreèekÿ hodnoty ve vybraných bodech, pøíp. i derivace Kvalita údajù: známe pøesnì (máme algoritmus) známe pøibli¾nì (experiment èi simulace) {
Aproximace funkcí 1/13 Známe: celý prùbìh funkce Chceme þvzoreèekÿ hodnoty ve vybraných bodech, pøíp. i derivace Kvalita údajù: známe pøesnì (máme algoritmus) známe pøibli¾nì (experiment èi simulace) {
Rovnováha Tepelná - T všude stejná
 Fázové heterogenní rovnováhy Fáze = homogenní část soustavy, oddělná fyzickým rozhraním, na rozhraní se vlastnosti mění skokem Rovnováha Tepelná - T všude stejná Mechanická - p všude stejný Chemická -
Fázové heterogenní rovnováhy Fáze = homogenní část soustavy, oddělná fyzickým rozhraním, na rozhraní se vlastnosti mění skokem Rovnováha Tepelná - T všude stejná Mechanická - p všude stejný Chemická -
Statistická termodynamika (mechanika)
 Statistická termodynamika (mechanika) 1/18 Makroskopické velièiny jsou výsledkem zprùmìrovaného chování mnoha èástic Tlak ideálního plynu z kinetické teorie 1 [simolant -I0] 2/18 Molekula = hmotný bod
Statistická termodynamika (mechanika) 1/18 Makroskopické velièiny jsou výsledkem zprùmìrovaného chování mnoha èástic Tlak ideálního plynu z kinetické teorie 1 [simolant -I0] 2/18 Molekula = hmotný bod
2.4 Stavové chování směsí plynů Ideální směs Ideální směs reálných plynů Stavové rovnice pro plynné směsi
 1. ZÁKLADNÍ POJMY 1.1 Systém a okolí 1.2 Vlastnosti systému 1.3 Vybrané základní veličiny 1.3.1 Množství 1.3.2 Délka 1.3.2 Délka 1.4 Vybrané odvozené veličiny 1.4.1 Objem 1.4.2 Hustota 1.4.3 Tlak 1.4.4
1. ZÁKLADNÍ POJMY 1.1 Systém a okolí 1.2 Vlastnosti systému 1.3 Vybrané základní veličiny 1.3.1 Množství 1.3.2 Délka 1.3.2 Délka 1.4 Vybrané odvozené veličiny 1.4.1 Objem 1.4.2 Hustota 1.4.3 Tlak 1.4.4
Neideální plyny. Z e dr dr dr. Integrace přes hybnosti. Neideální chování
 eideální plyny b H Q(, V, T )... e dp 3... dpdr... dr! h Integrace přes hybnosti QVT (,, ) pmkt! h 3 / e dr dr dr /... U kt... eideální chování p kt r B ( T) r B ( T) r 3 3 Vyšší koeficinety velice složité
eideální plyny b H Q(, V, T )... e dp 3... dpdr... dr! h Integrace přes hybnosti QVT (,, ) pmkt! h 3 / e dr dr dr /... U kt... eideální chování p kt r B ( T) r B ( T) r 3 3 Vyšší koeficinety velice složité
Fázové heterogenní rovnováhy Fáze = homogenní část soustavy, oddělná fyzickým rozhraním, na rozhraní se vlastnosti mění skokem
 Fázové heterogenní rovnováhy Fáze = homogenní část soustavy, oddělná fyzickým rozhraním, na rozhraní se vlastnosti mění skokem Rovnováha Tepelná - T všude stejná Mechanická - p všude stejný Chemická -
Fázové heterogenní rovnováhy Fáze = homogenní část soustavy, oddělná fyzickým rozhraním, na rozhraní se vlastnosti mění skokem Rovnováha Tepelná - T všude stejná Mechanická - p všude stejný Chemická -
FYZIKÁLNÍ CHEMIE I: 1. ČÁST KCH/P401
 Univerzita J. E. Purkyně v Ústí nad Labem Přírodovědecká fakulta FYZIKÁLNÍ CHEMIE I: 1. ČÁST KCH/P401 Magda Škvorová Ústí nad Labem 2013 Obor: Toxikologie a analýza škodlivin, Chemie (dvouoborová) Klíčová
Univerzita J. E. Purkyně v Ústí nad Labem Přírodovědecká fakulta FYZIKÁLNÍ CHEMIE I: 1. ČÁST KCH/P401 Magda Škvorová Ústí nad Labem 2013 Obor: Toxikologie a analýza škodlivin, Chemie (dvouoborová) Klíčová
6. Stavy hmoty - Plyny
 skupenství plynné plyn x pára (pod kritickou teplotou) stavové chování Ideální plyn Reálné plyny Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti skupenství plynné reálný plyn ve stavu
skupenství plynné plyn x pára (pod kritickou teplotou) stavové chování Ideální plyn Reálné plyny Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti skupenství plynné reálný plyn ve stavu
Plyn. 11 plynných prvků. Vzácné plyny He, Ne, Ar, Kr, Xe, Rn Diatomické plynné prvky H 2, N 2, O 2, F 2, Cl 2
 Plyny Plyn T v, K 11 plynných prvků Vzácné plyny He, Ne, Ar, Kr, Xe, Rn Diatomické plynné prvky H 2, N 2, O 2, F 2, Cl 2 H 2 20 He 4.4 Ne 27 Ar 87 Kr 120 Xe 165 Rn 211 N 2 77 O 2 90 F 2 85 Cl 2 238 1 Plyn
Plyny Plyn T v, K 11 plynných prvků Vzácné plyny He, Ne, Ar, Kr, Xe, Rn Diatomické plynné prvky H 2, N 2, O 2, F 2, Cl 2 H 2 20 He 4.4 Ne 27 Ar 87 Kr 120 Xe 165 Rn 211 N 2 77 O 2 90 F 2 85 Cl 2 238 1 Plyn
Základem molekulové fyziky je kinetická teorie látek. Vychází ze tří pouček:
 Molekulová fyzika zkoumá vlastnosti látek na základě jejich vnitřní struktury, pohybu a vzájemného působení částic, ze kterých se látky skládají. Termodynamika se zabývá zákony přeměny různých forem energie
Molekulová fyzika zkoumá vlastnosti látek na základě jejich vnitřní struktury, pohybu a vzájemného působení částic, ze kterých se látky skládají. Termodynamika se zabývá zákony přeměny různých forem energie
Termomechanika 8. přednáška Doc. Dr. RNDr. Miroslav Holeček
 Termomechanika 8. přednáška Doc. Dr. RNDr. Miroslav Holeček Upozornění: Tato prezentace slouží výhradně pro výukové účely Fakulty strojní Západočeské univerzity v Plzni. Byla sestavena autorem s využitím
Termomechanika 8. přednáška Doc. Dr. RNDr. Miroslav Holeček Upozornění: Tato prezentace slouží výhradně pro výukové účely Fakulty strojní Západočeské univerzity v Plzni. Byla sestavena autorem s využitím
Fluktuace termodynamických veličin
 Kvantová a statistická fyzika (Termodynamika a statistická fyzika Fluktuace termodynamických veličin Fluktuace jsou odchylky hodnot fyzikálních veličin od svých středních (rovnovážných hodnot. Mají původ
Kvantová a statistická fyzika (Termodynamika a statistická fyzika Fluktuace termodynamických veličin Fluktuace jsou odchylky hodnot fyzikálních veličin od svých středních (rovnovážných hodnot. Mají původ
Cvičení z termodynamiky a statistické fyziky
 Cvičení termodynamiky a statistické fyiky 1Nechť F(x, y=xe y Spočtěte F/ x, F/, 2 F/ x 2, 2 F/ x, 2 F/ x, 2 F/ x 2 2 Bud dω = A(x, ydx+b(x, ydy libovolná diferenciální forma(pfaffián Ukažte, ževpřípadě,žedωjeúplnýdiferenciál(existujefunkce
Cvičení termodynamiky a statistické fyiky 1Nechť F(x, y=xe y Spočtěte F/ x, F/, 2 F/ x 2, 2 F/ x, 2 F/ x, 2 F/ x 2 2 Bud dω = A(x, ydx+b(x, ydy libovolná diferenciální forma(pfaffián Ukažte, ževpřípadě,žedωjeúplnýdiferenciál(existujefunkce
Statistická termodynamika (mechanika) Makroskopické velièiny jsou výsledkem zprùmìrovaného chování mnoha èástic
 Statistická termodynamika (mechanika) 1/23 Makroskopické velièiny jsou výsledkem zprùmìrovaného chování mnoha èástic Tlak ideálního plynu z kinetické teorie 1 [simolant -I0] 2/23 Molekula = hmotný bod
Statistická termodynamika (mechanika) 1/23 Makroskopické velièiny jsou výsledkem zprùmìrovaného chování mnoha èástic Tlak ideálního plynu z kinetické teorie 1 [simolant -I0] 2/23 Molekula = hmotný bod
PROCESY V TECHNICE BUDOV 8
 UNIVERZITA TOMÁŠE BATI VE ZLÍNĚ FAKULTA APLIKOVANÉ INFORMATIKY PROCESY V TECHNICE BUDOV 8 Dagmar Janáčová, Hana Charvátová Zlín 2013 Tento studijní materiál vznikl za finanční podpory Evropského sociálního
UNIVERZITA TOMÁŠE BATI VE ZLÍNĚ FAKULTA APLIKOVANÉ INFORMATIKY PROCESY V TECHNICE BUDOV 8 Dagmar Janáčová, Hana Charvátová Zlín 2013 Tento studijní materiál vznikl za finanční podpory Evropského sociálního
Cvièení { 2D Clausiova-Clapeyronova rovnice
 Cvièení { 2D Clausiova-Clapeyronova rovnice 1/12 Evropský sociální fond þpraha & EU: Investujeme do va¹í budoucnostiÿ Inovace pøedmìtu Poèítaèová chemie je podporována projektem CHEMnote (Inovace bakaláøského
Cvièení { 2D Clausiova-Clapeyronova rovnice 1/12 Evropský sociální fond þpraha & EU: Investujeme do va¹í budoucnostiÿ Inovace pøedmìtu Poèítaèová chemie je podporována projektem CHEMnote (Inovace bakaláøského
Polymery. Pøírodní (polysacharidy, polypeptidy, polynukleotidy... ) Syntéza ji¾ 19. stol., osmotický tlak koloidní hypotéza
 Polymery [show -IG pic/ala30; show -Iggg -b2 pic/ala30] 1/31 Pøírodní (polysacharidy, polypeptidy, polynukleotidy... ) Syntéza ji¾ 19. stol., osmotický tlak koloidní hypotéza 1920 Hermann Staudinger (Nobel
Polymery [show -IG pic/ala30; show -Iggg -b2 pic/ala30] 1/31 Pøírodní (polysacharidy, polypeptidy, polynukleotidy... ) Syntéza ji¾ 19. stol., osmotický tlak koloidní hypotéza 1920 Hermann Staudinger (Nobel
Matematika II Extrémy funkcí více promìnných
 Matematika II Extrémy funkcí více promìnných RNDr. Renata Klufová, Ph. D. Jihoèeská univerzita v Èeských Budìjovicích EF Katedra aplikované matematiky a informatiky Parciální derivace vy¹¹ích øádù Def.
Matematika II Extrémy funkcí více promìnných RNDr. Renata Klufová, Ph. D. Jihoèeská univerzita v Èeských Budìjovicích EF Katedra aplikované matematiky a informatiky Parciální derivace vy¹¹ích øádù Def.
Nauka o materiálu. Přednáška č.10 Difuze v tuhých látkách, fáze a fázové přeměny
 Nauka o materiálu Přednáška č.10 Difuze v tuhých látkách, fáze a fázové přeměny Difuze v tuhých látkách Difuzí nazýváme přesun atomů nebo iontů na vzdálenost větší než je meziatomová vzdálenost. Hnací
Nauka o materiálu Přednáška č.10 Difuze v tuhých látkách, fáze a fázové přeměny Difuze v tuhých látkách Difuzí nazýváme přesun atomů nebo iontů na vzdálenost větší než je meziatomová vzdálenost. Hnací
Chemická kinetika. Reakce 1. řádu rychlost přímo úměrná koncentraci složky
 Chemická kinetika Chemická kinetika Reakce 0. řádu reakční rychlost nezávisí na čase a probíhá konstantní rychlostí v = k (rychlost se rovná rychlostní konstantě) velmi pomalé reakce (prakticky se nemění
Chemická kinetika Chemická kinetika Reakce 0. řádu reakční rychlost nezávisí na čase a probíhá konstantní rychlostí v = k (rychlost se rovná rychlostní konstantě) velmi pomalé reakce (prakticky se nemění
Matematika II Lineární diferenciální rovnice
 Matematika II Lineární diferenciální rovnice RNDr. Renata Klufová, Ph. D. Jihoèeská univerzita v Èeských Budìjovicích EF Katedra aplikované matematiky a informatiky Lineární diferenciální rovnice Denice
Matematika II Lineární diferenciální rovnice RNDr. Renata Klufová, Ph. D. Jihoèeská univerzita v Èeských Budìjovicích EF Katedra aplikované matematiky a informatiky Lineární diferenciální rovnice Denice
Matematika II Limita a spojitost funkce, derivace
 Matematika II Limita a spojitost funkce, derivace RNDr. Renata Klufová, Ph. D. Jihoèeská univerzita v Èeských Budìjovicích EF Katedra aplikované matematiky a informatiky Prstencové a kruhové okolí bodu
Matematika II Limita a spojitost funkce, derivace RNDr. Renata Klufová, Ph. D. Jihoèeská univerzita v Èeských Budìjovicích EF Katedra aplikované matematiky a informatiky Prstencové a kruhové okolí bodu
Matematika II Funkce více promìnných
 Matematika II Funkce více promìnných RNDr. Renata Klufová, Ph. D. Jihoèeská univerzita v Èeských Budìjovicích EF Katedra aplikované matematiky a informatiky Euklidovský n-rozmìrný prostor Def. Euklidovským
Matematika II Funkce více promìnných RNDr. Renata Klufová, Ph. D. Jihoèeská univerzita v Èeských Budìjovicích EF Katedra aplikované matematiky a informatiky Euklidovský n-rozmìrný prostor Def. Euklidovským
Skupenské stavy. Kapalina Částečně neuspořádané Volný pohyb částic nebo skupin částic Částice blíže u sebe
 Skupenské stavy Plyn Zcela neuspořádané Hodně volného prostoru Zcela volný pohyb částic Částice daleko od sebe Kapalina Částečně neuspořádané Volný pohyb částic nebo skupin částic Částice blíže u sebe
Skupenské stavy Plyn Zcela neuspořádané Hodně volného prostoru Zcela volný pohyb částic Částice daleko od sebe Kapalina Částečně neuspořádané Volný pohyb částic nebo skupin částic Částice blíže u sebe
Matematika II Urèitý integrál
 Matematika II Urèitý integrál RNDr. Renata Klufová, Ph. D. Jihoèeská univerzita v Èeských Budìjovicích EF Katedra aplikované matematiky a informatiky Motivace Je dána funkce f(x) = 2 + x2 x 4. Urèete co
Matematika II Urèitý integrál RNDr. Renata Klufová, Ph. D. Jihoèeská univerzita v Èeských Budìjovicích EF Katedra aplikované matematiky a informatiky Motivace Je dána funkce f(x) = 2 + x2 x 4. Urèete co
Termodynamika (td.) se obecně zabývá vzájemnými vztahy a přeměnami různých druhů
 Termodynamika (td.) se obecně zabývá vzájemnými vztahy a přeměnami různých druhů energií (mechanické, tepelné, elektrické, magnetické, chemické a jaderné) při td. dějích. Na rozdíl od td. cyklických dějů
Termodynamika (td.) se obecně zabývá vzájemnými vztahy a přeměnami různých druhů energií (mechanické, tepelné, elektrické, magnetické, chemické a jaderné) při td. dějích. Na rozdíl od td. cyklických dějů
Skupenské stavy látek. Mezimolekulární síly
 Skupenské stavy látek Mezimolekulární síly 1 Interakce iont-dipól Např. hydratační (solvatační) interakce mezi Na + (iont) a molekulou vody (dipól). Jde o nejsilnější mezimolekulární (nevazebnou) interakci.
Skupenské stavy látek Mezimolekulární síly 1 Interakce iont-dipól Např. hydratační (solvatační) interakce mezi Na + (iont) a molekulou vody (dipól). Jde o nejsilnější mezimolekulární (nevazebnou) interakci.
Fázové rozhraní - plocha,na které se vlastnosti systému mění skokem ; fáze o určité tloušťce
 Fázové rozhraní Fázové rozhraní - plocha,na které se vlastnosti systému mění skokem ; fáze o určité tloušťce Homogenní - kapalina/plyn - povrch;kapalina/kapalina Nehomogenní - tuhá látka/plyn - povrch;
Fázové rozhraní Fázové rozhraní - plocha,na které se vlastnosti systému mění skokem ; fáze o určité tloušťce Homogenní - kapalina/plyn - povrch;kapalina/kapalina Nehomogenní - tuhá látka/plyn - povrch;
Fyzikální chemie. ochrana životního prostředí analytická chemie chemická technologie denní. Platnost: od 1. 9. 2009 do 31. 8. 2013
 Učební osnova předmětu Fyzikální chemie Studijní obor: Aplikovaná chemie Zaměření: Forma vzdělávání: Celkový počet vyučovacích hodin za studium: Analytická chemie Chemická technologie Ochrana životního
Učební osnova předmětu Fyzikální chemie Studijní obor: Aplikovaná chemie Zaměření: Forma vzdělávání: Celkový počet vyučovacích hodin za studium: Analytická chemie Chemická technologie Ochrana životního
Roztok. Homogenní směs molekul, které mohou být v pevném, kapalném nebo plynném stavu
 Roztok Homogenní směs molekul, které mohou být v pevném, kapalném nebo plynném stavu Pravé roztoky Micelární a koloidní roztoky (suspenze): částice 1 nm 10 μm Micela Tyndallův jev rozptyl světla 1 Druhy
Roztok Homogenní směs molekul, které mohou být v pevném, kapalném nebo plynném stavu Pravé roztoky Micelární a koloidní roztoky (suspenze): částice 1 nm 10 μm Micela Tyndallův jev rozptyl světla 1 Druhy
Gymnázium Jiřího Ortena, Kutná Hora
 Předmět: Seminář chemie (SCH) Náplň: Obecná chemie, anorganická chemie, chemické výpočty, základy analytické chemie Třída: 3. ročník a septima Počet hodin: 2 hodiny týdně Pomůcky: Vybavení odborné učebny,
Předmět: Seminář chemie (SCH) Náplň: Obecná chemie, anorganická chemie, chemické výpočty, základy analytické chemie Třída: 3. ročník a septima Počet hodin: 2 hodiny týdně Pomůcky: Vybavení odborné učebny,
Stavové chování kapalin a plynů. 4. března 2010
 Stavové chování kapalin a plynů 4. března 2010 Studium plynů Plyn JE tekutina Studium plynů Studium plynů Létání v balónu aneb... Jak se vzepřít gravitaci? Studium plynů Studium plynů Létání v balónu aneb...
Stavové chování kapalin a plynů 4. března 2010 Studium plynů Plyn JE tekutina Studium plynů Studium plynů Létání v balónu aneb... Jak se vzepřít gravitaci? Studium plynů Studium plynů Létání v balónu aneb...
Termodynamika materiálů. Vztahy a přeměny různých druhů energie při termodynamických dějích podmínky nutné pro uskutečnění fázových přeměn
 Termodynamika materiálů Vztahy a přeměny různých druhů energie při termodynamických dějích podmínky nutné pro uskutečnění fázových přeměn Důležité konstanty Standartní podmínky Avogadrovo číslo N A = 6,023.10
Termodynamika materiálů Vztahy a přeměny různých druhů energie při termodynamických dějích podmínky nutné pro uskutečnění fázových přeměn Důležité konstanty Standartní podmínky Avogadrovo číslo N A = 6,023.10
a) Jaká je hodnota polytropického exponentu? ( 1,5257 )
 Ponorka se potopí do 50 m. Na dně ponorky je výstupní tunel o průměru 70 cm a délce, m. Tunel je napojen na uzavřenou komoru o objemu 4 m. Po otevření vnějšího poklopu vnikne z části voda tunelem do komory.
Ponorka se potopí do 50 m. Na dně ponorky je výstupní tunel o průměru 70 cm a délce, m. Tunel je napojen na uzavřenou komoru o objemu 4 m. Po otevření vnějšího poklopu vnikne z části voda tunelem do komory.
Aplikovaná fyzikální chemie. Magda Škvorová KFCH CN463 tel. 3302
 Aplikovaná fyzikální chemie Aplikovaná fyzikální chemie Magda Škvorová KFCH CN463 magda.skvorova@ujep.cz, tel. 3302 1. září 2014 Aplikovaná fyzikální chemie Bylo nebylo... Bylo nebylo... Nejvzácnějšímu
Aplikovaná fyzikální chemie Aplikovaná fyzikální chemie Magda Škvorová KFCH CN463 magda.skvorova@ujep.cz, tel. 3302 1. září 2014 Aplikovaná fyzikální chemie Bylo nebylo... Bylo nebylo... Nejvzácnějšímu
Stanovení křivky rozpustnosti fenol-voda. 3. laboratorní cvičení
 Stanovení křivky rozpustnosti fenol-voda 3. laboratorní cvičení Mgr. Sylvie Pavloková Letní semestr 2016/2017 Cíl pochopení základních principů fázové rovnováhy heterogenních soustav základní principy
Stanovení křivky rozpustnosti fenol-voda 3. laboratorní cvičení Mgr. Sylvie Pavloková Letní semestr 2016/2017 Cíl pochopení základních principů fázové rovnováhy heterogenních soustav základní principy
Pravdìpodobnostní popis
 Pravdìpodobnostní popis 1/19 klasická mechanika { stav = { r 1,..., r N, p 1,..., p N } stavù je { hustota pravdìpodobnosti stavù ρ( r 1,..., r N, p 1,..., p N ) kvantové mechaniky { stav = stavù je koneènì
Pravdìpodobnostní popis 1/19 klasická mechanika { stav = { r 1,..., r N, p 1,..., p N } stavù je { hustota pravdìpodobnosti stavù ρ( r 1,..., r N, p 1,..., p N ) kvantové mechaniky { stav = stavù je koneènì
LWS při heteroskedasticitě
 Stochastické modelování v ekonomii a financích Petr Jonáš 7. prosince 2009 Obsah 1 2 3 4 5 47 1 Předpoklad 1: Y i = X i β 0 + e i i = 1,..., n. (X i, e i) je posloupnost nezávislých nestejně rozdělených
Stochastické modelování v ekonomii a financích Petr Jonáš 7. prosince 2009 Obsah 1 2 3 4 5 47 1 Předpoklad 1: Y i = X i β 0 + e i i = 1,..., n. (X i, e i) je posloupnost nezávislých nestejně rozdělených
Adsorpce. molekulární adsorpce: (g) (s), (l) (s)/(l),... iontová adsorpce Paneth{Fajans výmìnná iontová adsorpce, protionty v aluminosilikátech
 Adsorpce molekulární adsorpce: (g) (s), (l) (s)/(l),... iontová adsorpce Paneth{Fajans výmìnná iontová adsorpce, protionty v aluminosilikátech 1/16 Ar na gratu adsorpce: na povrch/rozhraní absorpce: dovnitø
Adsorpce molekulární adsorpce: (g) (s), (l) (s)/(l),... iontová adsorpce Paneth{Fajans výmìnná iontová adsorpce, protionty v aluminosilikátech 1/16 Ar na gratu adsorpce: na povrch/rozhraní absorpce: dovnitø
Typy molekul, látek a jejich vazeb v organismech
 Typy molekul, látek a jejich vazeb v organismech Typy molekul, látek a jejich vazeb v organismech Organismy se skládají z molekul rozličných látek Jednotlivé látky si organismus vytváří sám z jiných látek,
Typy molekul, látek a jejich vazeb v organismech Typy molekul, látek a jejich vazeb v organismech Organismy se skládají z molekul rozličných látek Jednotlivé látky si organismus vytváří sám z jiných látek,
èlánky øetìzce spojeny ohebnì (vazby, úhly, torze)
 Roztoky polymerù Model ideálního øetìzce: èlánky øetìzce spojeny ohebnì (vazby, úhly, torze) èlánky dostateènì daleko od sebe ji¾ neinteragují (rozumí se efektivní interakce zprostøedkovaná prostøedím)
Roztoky polymerù Model ideálního øetìzce: èlánky øetìzce spojeny ohebnì (vazby, úhly, torze) èlánky dostateènì daleko od sebe ji¾ neinteragují (rozumí se efektivní interakce zprostøedkovaná prostøedím)
Brownovská (stochastická) dynamika, disipativní èásticová dynamika = MD + náhodné síly. i = 1,..., N. r i. U = i<j. u(r ij ) du(r ji ) r ji
 Molekulová dynamika Síly: tuhé koule ap. { nárazy þklasickáÿ MD { integrace pohybových rovnic 1/20 Brownovská (stochastická) dynamika, disipativní èásticová dynamika = MD + náhodné síly Pøíklad: f i =
Molekulová dynamika Síly: tuhé koule ap. { nárazy þklasickáÿ MD { integrace pohybových rovnic 1/20 Brownovská (stochastická) dynamika, disipativní èásticová dynamika = MD + náhodné síly Pøíklad: f i =
Roztok. Homogenní směs molekul, které mohou být v pevném, kapalném nebo plynném stavu. Pravé roztoky
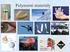 Roztok Homogenní směs molekul, které mohou být v pevném, kapalném nebo plynném stavu Pravé roztoky Micelární a koloidní roztoky (suspenze): částice velké 1 nm 10 µm Tyndallův jev 1 Druhy roztoků Složka
Roztok Homogenní směs molekul, které mohou být v pevném, kapalném nebo plynném stavu Pravé roztoky Micelární a koloidní roztoky (suspenze): částice velké 1 nm 10 µm Tyndallův jev 1 Druhy roztoků Složka
Roztok. Homogenní směs molekul, které mohou být v pevném, kapalném nebo plynném stavu. Pravé roztoky
 Roztok Homogenní směs molekul, které mohou být v pevném, kapalném nebo plynném stavu Pravé roztoky Micelární a koloidní roztoky (suspenze): částice velké 1 nm 10 µm Tyndallův jev rozptyl světla 1 Druhy
Roztok Homogenní směs molekul, které mohou být v pevném, kapalném nebo plynném stavu Pravé roztoky Micelární a koloidní roztoky (suspenze): částice velké 1 nm 10 µm Tyndallův jev rozptyl světla 1 Druhy
Speciální analytické metody pro léčiva
 Speciální analytické metody pro léčiva doc. RNDr. Ing. Pavel Řezanka, Ph.D. E-mail: pavel.rezanka@vscht.cz Místnost: A234 Příprava předmětu byla podpořena projektem OPPA č. CZ.2.17/3.1.00/33253 1 Harmonogram
Speciální analytické metody pro léčiva doc. RNDr. Ing. Pavel Řezanka, Ph.D. E-mail: pavel.rezanka@vscht.cz Místnost: A234 Příprava předmětu byla podpořena projektem OPPA č. CZ.2.17/3.1.00/33253 1 Harmonogram
Roztoky - druhy roztoků
 Roztoky - druhy roztoků Roztok = homogenní směs molekul, které mohou být v pevném (s), kapalném (l) nebo plynném (g) stavu Složka 1 Složka 2 Stav směsi Příklad G G G Vzduch G L L Sodová voda (CO 2 ) G
Roztoky - druhy roztoků Roztok = homogenní směs molekul, které mohou být v pevném (s), kapalném (l) nebo plynném (g) stavu Složka 1 Složka 2 Stav směsi Příklad G G G Vzduch G L L Sodová voda (CO 2 ) G
Matematika I Ètvercové matice - determinanty
 Matematika I Ètvercové matice - determinanty RNDr. Renata Klufová, Ph. D. Jihoèeská univerzita v Èeských Budìjovicích EF Katedra aplikované matematiky a informatiky Co u¾ známe? vektory - základní operace
Matematika I Ètvercové matice - determinanty RNDr. Renata Klufová, Ph. D. Jihoèeská univerzita v Èeských Budìjovicích EF Katedra aplikované matematiky a informatiky Co u¾ známe? vektory - základní operace
Fyzika IV Dynamika jader v molekulách
 Dynamika jader v molekulách vibrace rotace Dynamika jader v molekulách rotační energetické hladiny (dvouatomová molekula) moment setrvačnosti kolem osy procházející těžištěm osa těžiště m2 m1 r2 r1 R moment
Dynamika jader v molekulách vibrace rotace Dynamika jader v molekulách rotační energetické hladiny (dvouatomová molekula) moment setrvačnosti kolem osy procházející těžištěm osa těžiště m2 m1 r2 r1 R moment
Elektrochemie. Pøedmìt elektrochemie: disociace (roztoky elektrolytù, taveniny solí) vodivost jevy na rozhraní s/l (elektrolýza, èlánky)
 Elektrochemie 1 Pøedmìt elektrochemie: disociace (roztoky elektrolytù, taveniny solí) vodivost jevy na rozhraní s/l (elektrolýza, èlánky) Vodièe: I. tøídy { vodivost zpùsobena pohybem elektronù uvnitø
Elektrochemie 1 Pøedmìt elektrochemie: disociace (roztoky elektrolytù, taveniny solí) vodivost jevy na rozhraní s/l (elektrolýza, èlánky) Vodièe: I. tøídy { vodivost zpùsobena pohybem elektronù uvnitø
Matematika I Posloupnosti
 Matematika I Posloupnosti RNDr. Renata Klufová, Ph. D. Jihoèeská univerzita v Èeských Budìjovicích EF Katedra aplikované matematiky a informatiky Posloupnost Def. Nekoneènou posloupností reálných èísel
Matematika I Posloupnosti RNDr. Renata Klufová, Ph. D. Jihoèeská univerzita v Èeských Budìjovicích EF Katedra aplikované matematiky a informatiky Posloupnost Def. Nekoneènou posloupností reálných èísel
Osnova pro předmět Fyzikální chemie II magisterský kurz
 Osnova pro předmět Fyzikální chemie II magisterský kurz Časový a obsahový program přednášek Týden Obsahová náplň přednášky Pozn. Stavové chování tekutin 1,2a 1, 2a Molekulární přístup kinetická teorie
Osnova pro předmět Fyzikální chemie II magisterský kurz Časový a obsahový program přednášek Týden Obsahová náplň přednášky Pozn. Stavové chování tekutin 1,2a 1, 2a Molekulární přístup kinetická teorie
Krystalizace, transformace, kongruence, frustrace a jak se to všechno spolu rýmuje
 Krystalizace, transformace, kongruence, frustrace a jak se to všechno spolu rýmuje Pavel Svoboda, Silvie Mašková Univerzita Karlova v Praze, Matematicko-fyzikální fakulta, Katedra fyziky kondenzovaných
Krystalizace, transformace, kongruence, frustrace a jak se to všechno spolu rýmuje Pavel Svoboda, Silvie Mašková Univerzita Karlova v Praze, Matematicko-fyzikální fakulta, Katedra fyziky kondenzovaných
III. STRUKTURA A VLASTNOSTI PLYNŮ
 III. STRUKTURA A VLASTNOSTI PLYNŮ 3.1 Ideální plyn a) ideální plyn model, předpoklady: 1. rozměry molekul malé (ve srovnání se střední vzdáleností molekul). molekuly na sebe navzálem silově nepůsobí (mimo
III. STRUKTURA A VLASTNOSTI PLYNŮ 3.1 Ideální plyn a) ideální plyn model, předpoklady: 1. rozměry molekul malé (ve srovnání se střední vzdáleností molekul). molekuly na sebe navzálem silově nepůsobí (mimo
TERMOMECHANIKA 15. Základy přenosu tepla
 FSI VUT v Brně, Energetický ústav Odbor termomechaniky a techniky prostředí Prof. Ing. Milan Pavelek, CSc. TERMOMECHANIKA 15. Základy přenosu tepla OSNOVA 15. KAPITOLY Tři mechanizmy přenosu tepla Tepelný
FSI VUT v Brně, Energetický ústav Odbor termomechaniky a techniky prostředí Prof. Ing. Milan Pavelek, CSc. TERMOMECHANIKA 15. Základy přenosu tepla OSNOVA 15. KAPITOLY Tři mechanizmy přenosu tepla Tepelný
Cvièení { 2D Clausiova{Clapeyronova rovnice
 Cvièení { 2D Clausiova{Clapeyronova rovnice 1/15 Evropský sociální fond þpraha & EU: Investujeme do va¹í budoucnostiÿ Inovace pøedmìtu Poèítaèová chemie je podporována projektem CHEMnote (Inovace bakaláøského
Cvièení { 2D Clausiova{Clapeyronova rovnice 1/15 Evropský sociální fond þpraha & EU: Investujeme do va¹í budoucnostiÿ Inovace pøedmìtu Poèítaèová chemie je podporována projektem CHEMnote (Inovace bakaláøského
Fázová rozhraní a mezifázová energie
 Fázová ozhaní a mezifázová enegie 1/15 duhy: } l/ g {{ l/ } l mobilní s/g s/l s/s povch koule = 4π 2 Příklad. Kolik % molekul vody je na povchu kapičky mlhy o půměu 200 nm (hanice viditelnosti optickým
Fázová ozhaní a mezifázová enegie 1/15 duhy: } l/ g {{ l/ } l mobilní s/g s/l s/s povch koule = 4π 2 Příklad. Kolik % molekul vody je na povchu kapičky mlhy o půměu 200 nm (hanice viditelnosti optickým
Trocha termodynamiky ještě nikdy nikoho nezabila (s pravděpodobností
 Trocha termodynamiky ještě nikdy nikoho nezabila (s pravděpodobností 95 %) Studium tohoto podpůrného textu není k vyřešení úlohy B3 potřeba, slouží spíše k obohacení vašich znalostí o rovnovážných dějích,
Trocha termodynamiky ještě nikdy nikoho nezabila (s pravděpodobností 95 %) Studium tohoto podpůrného textu není k vyřešení úlohy B3 potřeba, slouží spíše k obohacení vašich znalostí o rovnovážných dějích,
Kontrolní otázky k 1. přednášce z TM
 Kontrolní otázky k 1. přednášce z TM 1. Jak závisí hodnota izobarického součinitele objemové roztažnosti ideálního plynu na teplotě a jak na tlaku? Odvoďte. 2. Jak závisí hodnota izochorického součinitele
Kontrolní otázky k 1. přednášce z TM 1. Jak závisí hodnota izobarického součinitele objemové roztažnosti ideálního plynu na teplotě a jak na tlaku? Odvoďte. 2. Jak závisí hodnota izochorického součinitele
Fáze a fázové přechody
 Kvantová a statistická fyzika 2 (Termodynamika a statistická fyzika) Fáze a fázové přechody Pojem fáze je zobecněním pojmu skupenství, označuje homogenní část makroskopického tělesa. Jednotlivé fáze v
Kvantová a statistická fyzika 2 (Termodynamika a statistická fyzika) Fáze a fázové přechody Pojem fáze je zobecněním pojmu skupenství, označuje homogenní část makroskopického tělesa. Jednotlivé fáze v
15,45 17,90 19,80 21,28. 24,38 28,18 27,92 28,48 dichlormethan trichlormethan tetrachlormethan kys. mravenčí kys. octová kys. propionová kys.
 zkapalněné plyny - velmi nízké; např. helium 0354 mn m při teplotě 270C vodík 2 mn m při teplotě 253C roztavené kovy - velmi vysoké; např. měď při teplotě tání = 00 mn m rtuť při 0 o C = 470 mn m organické
zkapalněné plyny - velmi nízké; např. helium 0354 mn m při teplotě 270C vodík 2 mn m při teplotě 253C roztavené kovy - velmi vysoké; např. měď při teplotě tání = 00 mn m rtuť při 0 o C = 470 mn m organické
ČESKÉ VYSOKÉ UČENÍ TECHNICKÉ V PRAZE Fakulta biomedicínského inženýrství. Teplotní vlastnosti
 ČESKÉ VYSOKÉ UČENÍ TECHNICKÉ V PRAZE Fakulta biomedicínského inženýrství Teplotní vlastnosti Student: Ondřej Rozinek květen 2009 1 Teplotní vlastnosti Vlastnosti materiálu závisí na skupenství. Skupenství
ČESKÉ VYSOKÉ UČENÍ TECHNICKÉ V PRAZE Fakulta biomedicínského inženýrství Teplotní vlastnosti Student: Ondřej Rozinek květen 2009 1 Teplotní vlastnosti Vlastnosti materiálu závisí na skupenství. Skupenství
Disperzní systémy. jsou slo¾ené ze dvou (i více) fází. Zpravidla dispergovaná fáze ve spojité fázi Obvykle s/l, l/l,...
 Disperzní systémy 1/21 jsou slo¾ené ze dvou (i více) fází. Zpravidla dispergovaná fáze ve spojité fázi Obvykle s/l, l/l,... Rozdìlení podle velikosti èástic: hrubì disperzní (heterogenní), > 1 µm koloidní
Disperzní systémy 1/21 jsou slo¾ené ze dvou (i více) fází. Zpravidla dispergovaná fáze ve spojité fázi Obvykle s/l, l/l,... Rozdìlení podle velikosti èástic: hrubì disperzní (heterogenní), > 1 µm koloidní
ZAKLADY FYZIKALNI CHEMIE HORENí, VÝBUCHU A HAŠENí
 r SDRUŽENí POŽÁRNíHO A BEZPEČNOSTNíHO INžENÝRSTVí. JAROSLAV K,\LOUSEK,.,.,. ZAKLADY FYZIKALNI CHEMIE HORENí, VÝBUCHU A HAŠENí EDICESPBI SPEKTRUM OBSAH. strana 1. FyzikálnÍ chemie v požární ochranč a bezpečnosti
r SDRUŽENí POŽÁRNíHO A BEZPEČNOSTNíHO INžENÝRSTVí. JAROSLAV K,\LOUSEK,.,.,. ZAKLADY FYZIKALNI CHEMIE HORENí, VÝBUCHU A HAŠENí EDICESPBI SPEKTRUM OBSAH. strana 1. FyzikálnÍ chemie v požární ochranč a bezpečnosti
Termomechanika 9. přednáška Doc. Dr. RNDr. Miroslav Holeček
 Termomechanika 9. přednáška Doc. Dr. RNDr. Miroslav Holeček Upozornění: Tato prezentace slouží výhradně pro výukové účely Fakulty strojní Západočeské univerzity v Plzni. Byla sestavena autorem s využitím
Termomechanika 9. přednáška Doc. Dr. RNDr. Miroslav Holeček Upozornění: Tato prezentace slouží výhradně pro výukové účely Fakulty strojní Západočeské univerzity v Plzni. Byla sestavena autorem s využitím
Definice 1.1. Nechť je M množina. Funkci ρ : M M R nazveme metrikou, jestliže má následující vlastnosti:
 Přednáška 1. Definice 1.1. Nechť je množina. Funkci ρ : R nazveme metrikou, jestliže má následující vlastnosti: (1 pro každé x je ρ(x, x = 0; (2 pro každé x, y, x y, je ρ(x, y = ρ(y, x > 0; (3 pro každé
Přednáška 1. Definice 1.1. Nechť je množina. Funkci ρ : R nazveme metrikou, jestliže má následující vlastnosti: (1 pro každé x je ρ(x, x = 0; (2 pro každé x, y, x y, je ρ(x, y = ρ(y, x > 0; (3 pro každé
8. Normální rozdělení
 8. Normální rozdělení 8.. Definice: Normální (Gaussovo) rozdělení N(µ, 2 ) s parametry µ a > 0 je rozdělení určené hustotou ( ) f(x) = (x µ) 2 e 2 2, x (, ). Rozdělení N(0; ) s parametry µ = 0 a = se nazývá
8. Normální rozdělení 8.. Definice: Normální (Gaussovo) rozdělení N(µ, 2 ) s parametry µ a > 0 je rozdělení určené hustotou ( ) f(x) = (x µ) 2 e 2 2, x (, ). Rozdělení N(0; ) s parametry µ = 0 a = se nazývá
v trojúhelníku P QC sestrojíme vý¹ky na základnu a jedno rameno, patu vý¹ky na rameno oznaèíme R a patu na základnu S
 Øe¹ení 5. série IV. roèníku kategorie JUNIOR RS-IV-5-1 Pro na¹e úvahy bude vhodné upravit si na¹í rovnici do tvaru 3 jx 1 4 j+2 = 5 + 4 sin 2x: Budeme uva¾ovat o funkci na pravé stranì na¹í rovnice, tj.
Øe¹ení 5. série IV. roèníku kategorie JUNIOR RS-IV-5-1 Pro na¹e úvahy bude vhodné upravit si na¹í rovnici do tvaru 3 jx 1 4 j+2 = 5 + 4 sin 2x: Budeme uva¾ovat o funkci na pravé stranì na¹í rovnice, tj.
bak-06=1/1 http://www.vscht.cz/fch/cz/pomucky/kolafa/n403011p.html
 bak-06=1/1 pst=101325 = 1.013e+05 Pa R=8.314 = 8.314JK 1 mol 1 Gibbsovo fázové pravidlo v = k f + 2 C počet stupnů volnosti počet složek počet fází počet vazných podmínek 1. Gibbsovo fázové pravidlo Určete
bak-06=1/1 pst=101325 = 1.013e+05 Pa R=8.314 = 8.314JK 1 mol 1 Gibbsovo fázové pravidlo v = k f + 2 C počet stupnů volnosti počet složek počet fází počet vazných podmínek 1. Gibbsovo fázové pravidlo Určete
Teorie transportu plynů a par polymerními membránami. Doc. Ing. Milan Šípek, CSc. Ústav fyzikální chemie VŠCHT Praha
 Teorie transportu plynů a par polymerními membránami Doc. Ing. Milan Šípek, CSc. Ústav fyzikální chemie VŠCHT Praha Úvod Teorie transportu Difuze v polymerních membránách Propustnost polymerních membrán
Teorie transportu plynů a par polymerními membránami Doc. Ing. Milan Šípek, CSc. Ústav fyzikální chemie VŠCHT Praha Úvod Teorie transportu Difuze v polymerních membránách Propustnost polymerních membrán
Transportní jevy. J = konst F
 Transportní jevy 1/23 Transportní (kinetické) jevy: difuze, elektrická vodivost, viskozita (vnitøní tøení), vedení tepla... Tok (ux) (té¾ zobecnìný tok) hmoty, náboje, hybnosti, tepla... : J = mno¾ství
Transportní jevy 1/23 Transportní (kinetické) jevy: difuze, elektrická vodivost, viskozita (vnitøní tøení), vedení tepla... Tok (ux) (té¾ zobecnìný tok) hmoty, náboje, hybnosti, tepla... : J = mno¾ství
John Dalton Amadeo Avogadro
 Spojením atomů vznikají molekuly... John Dalton 1766 1844 Amadeo Avogadro 1776 1856 Výpočet molekuly 2, metoda valenční vazby Walter eitler 1904 1981 Fritz W. London 1900 1954 Teorie molekulových orbitalů
Spojením atomů vznikají molekuly... John Dalton 1766 1844 Amadeo Avogadro 1776 1856 Výpočet molekuly 2, metoda valenční vazby Walter eitler 1904 1981 Fritz W. London 1900 1954 Teorie molekulových orbitalů
8.1. Definice: Normální (Gaussovo) rozdělení N(µ, σ 2 ) s parametry µ a. ( ) ϕ(x) = 1. označovat písmenem U. Její hustota je pak.
 8. Normální rozdělení 8.. Definice: Normální (Gaussovo) rozdělení N(µ, ) s parametry µ a > 0 je rozdělení určené hustotou ( ) f(x) = (x µ) e, x (, ). Rozdělení N(0; ) s parametry µ = 0 a = se nazývá normované
8. Normální rozdělení 8.. Definice: Normální (Gaussovo) rozdělení N(µ, ) s parametry µ a > 0 je rozdělení určené hustotou ( ) f(x) = (x µ) e, x (, ). Rozdělení N(0; ) s parametry µ = 0 a = se nazývá normované
J., HÁJEK B., VOTINSKÝ J.
 Kontakty a materiály J. Šedlbauer e-mail: josef.sedlbauer@tul.cz tel.: 48-535-3375 informace a materiály k Obecné chemii: www.fp.tul.cz/kch/sedlbauer (odkaz na předmět) konzultace: úterý odpoledne nebo
Kontakty a materiály J. Šedlbauer e-mail: josef.sedlbauer@tul.cz tel.: 48-535-3375 informace a materiály k Obecné chemii: www.fp.tul.cz/kch/sedlbauer (odkaz na předmět) konzultace: úterý odpoledne nebo
Kapaliny Molekulové vdw síly, vodíkové můstky
 Kapaliny Molekulové vdw síly, vodíkové můstky Metalické roztavené kovy, ionty + elektrony, elektrostatické síly Iontové roztavené soli, FLINAK (LiF + NaF + KF), volně pohyblivé anionty a kationty, iontová
Kapaliny Molekulové vdw síly, vodíkové můstky Metalické roztavené kovy, ionty + elektrony, elektrostatické síly Iontové roztavené soli, FLINAK (LiF + NaF + KF), volně pohyblivé anionty a kationty, iontová
Úvodní info. Studium
 [mozilla le:/home/jiri/www/fch/cz/pomucky/kolafa/n4316.html] 1/16 Úvodní info Jiøí Kolafa Ústav fyzikální chemie V CHT Praha budova A, místnost 325 (zadním vchodem) jiri.kolafa@vscht.cz 2244 4257 Web pøedmìtu:
[mozilla le:/home/jiri/www/fch/cz/pomucky/kolafa/n4316.html] 1/16 Úvodní info Jiøí Kolafa Ústav fyzikální chemie V CHT Praha budova A, místnost 325 (zadním vchodem) jiri.kolafa@vscht.cz 2244 4257 Web pøedmìtu:
VLASTNOSTI PLOŠNÝCH SPOJÙ
 Vážení zákazníci, dovolujeme si Vás upozornit, že na tuto ukázku knihy se vztahují autorská práva, tzv. copyright. To znamená, že ukázka má sloužit výhradnì pro osobní potøebu potenciálního kupujícího
Vážení zákazníci, dovolujeme si Vás upozornit, že na tuto ukázku knihy se vztahují autorská práva, tzv. copyright. To znamená, že ukázka má sloužit výhradnì pro osobní potøebu potenciálního kupujícího
Základní prvky modelování ve fyzice a chemii
 Základní prvky modelování ve fyzice a chemii 1/40? elementární èástice + gravitace: þteorie v¹ehoÿ { temná hmota... (známé) elementární èástice: standardní model { atomová jádra... jádra + elektrony +
Základní prvky modelování ve fyzice a chemii 1/40? elementární èástice + gravitace: þteorie v¹ehoÿ { temná hmota... (známé) elementární èástice: standardní model { atomová jádra... jádra + elektrony +
