Ac - +H 2 O HAc + OH -, naopak roztok soli silné kyseliny a slabé zásady (např. chlorid amonný NH 4 Cl) vykazuje kyselou reakci K A
|
|
|
- Ludmila Mašková
- před 8 lety
- Počet zobrazení:
Transkript
1 YDROLÝZ SOLÍ ydrolýze podléhjí soli, jejihž ktion přísluší slbé bázi /nebo nion slbé kyselině. ydrolýz soli je reke soli s vodou z vzniku neutrálníh molekul příslušného slbého elektrolytu. Důsledkem hydrolýzy soli slbé kyseliny silné zásdy (npř. otn sodný N) je lkliký roztok O O, nopk roztok soli silné kyseliny slbé zásdy (npř. hlorid monný N 4 Cl) vykzuje kyselou reki N 4 O N 3 3 O. Sůl slbé kyseliny silné zásdy Sůl silné kyseliny slbé zásdy O O O 3 O O v ( ) O 3 ( ) [ ] [ ] [ ] [ ] γ [ ] γ. předpokld: i : γ. předpokld: i : γ i [ ] [ O ] [ ] [ ] 3O [ ] [ ]. předpokld: [ ] [ O ]. předpokld: [ ] [ O ] i 3 [ ] γ γ γ γ 3. předpokld: γ << 3. předpokld: γ << p γ [ O ] γ [ O ] [ p p ( ) log ] p p ( ) v 3 [ log ] 3
2 Sůl slbé kyseliny slbé zásdy p O O O 3 O [ p ( ) p ( )] rovnovážná konstnt hydrolýzy, γ stupeň hydrolýzy, nlytiká konentre soli Splnění.. zjednodušujíího předpokldu nelze obeně očekávt výsledné vzthy pro výpočet p je nutno brát pouze jko přibližné. ydrolýzu solí musíme vzít v úvhu při idobzikýh titríh, indikujemeli bod ekvivlene idobzikým indikátorem. 4
3 PUFRY neboli tlumivé roztoky, jsou roztoky, které jsou shopny tlumit výkyvy p při přídvku oxoniovýh či hydroxidovýh iontů. Tuto vlstnost vykzuje roztok slbé kyseliny její soli se silnou zásdou tzv. kyselý pufr, slbé báze její soli se silnou kyselinou tzv. bziký pufr. Pufrční mehnismus je zložen n ovlivňování rovnovážného složení příslušného slbého elektrolytu přídvkem či odčerpáním oxoniovýh iontů. Př. pro kyselý pufr O 3 O přídvek 3 O iontů poruší rovnováhu vyvolá reki 3 O O přídvek O iontů odčerpá oxoniové ktionty O 3 O O vyvolá reki O 3 O } O O Přidné oxoniové resp. hydroxidové ionty nezůstnou v roztoku v původním množství, le z větší části se spotřebují uvedenými rekemi p roztoku se změní jen málo. V roztoku ovšem musí být dosttečná zásob jk neutrálníh molekul, tk niontů. 5
4 Výpočet p pufru: yselý pufr ziký pufr O 3 O O 3 O 3O 3O 3 O 3O. předpokld: [ ], [ ]. předpokld: [ ], [ ] p [ ] [ p ] log p p log [ ]. předpokld: α <<, γ <<. předpokld: α <<, γ << [ ] Příprv pufru: ze slbé kyseliny její soli nlytiká konentre slbé kyseliny S nlytiká konentre soli p p log S Příprv pufru: ze slbé báze její soli nlytiká konentre slbé báze S nlytiká konentre soli p p log S ze slbé kyseliny silné báze nlytiká konentre slbé kyseliny nlytiká konentre silné báze ze slbé báze silné kyseliny nlytiká konentre slbé báze nlytiká konentre silné kyseliny p p log p p log endersonovysselblhovy rovnie 6
5 Míru shopnosti pufru tlumit výkyvy p vyjdřuje pufrční kpit β definovná pro kyselý pufr β d d p pro bziký pufr d β. dp Závislost β n složení pufru Př.: pro kyselý pufr p p β dp d log ln0 β ln0 Pufrční kpit závisí nejen n poměru konentrí dy má pufr mximální pufrční kpitu? d β 0 d, le i n hodnotě konentre. kyselin je právě z poloviny ztitrován silnou bází (v pufru je kyselin její sůl v poměru :) p p log p p kritérium pro výběr vhodného pufru (použitelnost pufru: p p ± ½) 7
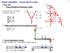
6 Grfiké znázornění závislosti pufrční kpity n složení pufru / /mol dm 3 0,00 0,04 0,08 0, 0,6 0,0 0, β mx 0,0 0, mol dm 3 β /mol dm 3 0,08 0,06 β mx 0, mol dm 3 0,04 0,0 0,00 0,00 0,0 0,04 0,06 0,08 0,0 / /mol dm 3 Grfiké znázornění závislosti pufrční kpity n p pufru 0,06 β mx 0,0 β /mol dm 3 0,05 0,04 0,03 p 4 0, mol dm 3 0,08 0,06 /mol dm 3 0,0 0,04 0,0 0,0 0, p 0,00 8
[ ][ ] Kyseliny a zásady. Acidobazické rovnováhy. Výpočet ph silných jednosytných kyselin (zásad) Autoprotolýza vody
![[ ][ ] Kyseliny a zásady. Acidobazické rovnováhy. Výpočet ph silných jednosytných kyselin (zásad) Autoprotolýza vody [ ][ ] Kyseliny a zásady. Acidobazické rovnováhy. Výpočet ph silných jednosytných kyselin (zásad) Autoprotolýza vody](/thumbs/33/16164414.jpg) Aidoziké rovnováhy při idozikýh rovnováháh (proteolytikýh) přeno vodíkového ktiontu mezi ionty (molekulmi) zúčtněnými v rovnováze kyelin donor protonů zád keptor protonů KYELINA 1 zád ZÁADA 1 kyelin vod
Aidoziké rovnováhy při idozikýh rovnováháh (proteolytikýh) přeno vodíkového ktiontu mezi ionty (molekulmi) zúčtněnými v rovnováze kyelin donor protonů zád keptor protonů KYELINA 1 zád ZÁADA 1 kyelin vod
E ŘEŠENÍ KONTROLNÍHO TESTU ŠKOLNÍHO KOLA
 Ústřední komise Chemické olympiády 49. ročník 2012/201 ŠKLNÍ KL ktegorie A ŘŠNÍ KNTRLNÍH TSTU ŠKLNÍH KLA Řešení kontrolního testu školního kol Ch kt. A 2012/201 KNTRLNÍ TST ŠKLNÍH KLA (60 BDŮ) ANRGANICKÁ
Ústřední komise Chemické olympiády 49. ročník 2012/201 ŠKLNÍ KL ktegorie A ŘŠNÍ KNTRLNÍH TSTU ŠKLNÍH KLA Řešení kontrolního testu školního kol Ch kt. A 2012/201 KNTRLNÍ TST ŠKLNÍH KLA (60 BDŮ) ANRGANICKÁ
Stanovení disociační konstanty slabé jednosytné kyseliny ve vodě z měření koncentrační závislosti měrné elektrické vodivosti roztoku
 Stnovení disoiční konstnty slbé jednosytné kyseliny ve vodě z měření konentrční závislosti měrné elektriké vodivosti roztoku Teorie Elektriká vodivost V elektriky vodivé homogenní láte, která obshuje nositele
Stnovení disoiční konstnty slbé jednosytné kyseliny ve vodě z měření konentrční závislosti měrné elektriké vodivosti roztoku Teorie Elektriká vodivost V elektriky vodivé homogenní láte, která obshuje nositele
2. PROTOLYTICKÉ REAKCE
 2. PROTOLYTICKÉ REAKCE Protolytické reakce představují všechny reakce spojené s výměnou protonů a jsou označovány jako reakce acidobazické. Teorie Arrheniova (1884): kyseliny disociují ve vodě na vodíkový
2. PROTOLYTICKÉ REAKCE Protolytické reakce představují všechny reakce spojené s výměnou protonů a jsou označovány jako reakce acidobazické. Teorie Arrheniova (1884): kyseliny disociují ve vodě na vodíkový
Chemické výpočty II. Vladimíra Kvasnicová
 Chemické výpočty II Vladimíra Kvasnicová Převod jednotek pmol/l nmol/l µmol/l mmol/l mol/l 10-12 10-9 10-6 10-3 mol/l µg mg g 10-6 10-3 g µl ml dl L 10-6 10-3 10-1 L Cvičení 12) cholesterol (MW=386,7g/mol):
Chemické výpočty II Vladimíra Kvasnicová Převod jednotek pmol/l nmol/l µmol/l mmol/l mol/l 10-12 10-9 10-6 10-3 mol/l µg mg g 10-6 10-3 g µl ml dl L 10-6 10-3 10-1 L Cvičení 12) cholesterol (MW=386,7g/mol):
PROTOLYTICKÉ ROVNOVÁHY
 PROTOLYTICKÉ ROVNOVÁHY Protolytické rovnováhy - úvod Obecná chemická reakce a A + b B c C + d D Veličina Symbol, jednotka Definice rovnovážná konstanta reakce K K = ac C a d D a a A a b B aktivita a a
PROTOLYTICKÉ ROVNOVÁHY Protolytické rovnováhy - úvod Obecná chemická reakce a A + b B c C + d D Veličina Symbol, jednotka Definice rovnovážná konstanta reakce K K = ac C a d D a a A a b B aktivita a a
Roztoky - elektrolyty
 Roztoky - elektrolyty Roztoky - vodné roztoky prakticky vždy vedou elektrický proud Elektrolyty látky, které se štěpí disociují na elektricky nabité částice ionty Původně se předpokládalo, že k disociaci
Roztoky - elektrolyty Roztoky - vodné roztoky prakticky vždy vedou elektrický proud Elektrolyty látky, které se štěpí disociují na elektricky nabité částice ionty Původně se předpokládalo, že k disociaci
CZ.1.07/1.5.00/34.0802 Zkvalitnění výuky prostřednictvím ICT. Protolytické děje VY_32_INOVACE_18_15. Mgr. Věra Grimmerová. grimmerova@gymjev.
 Průvodka Číslo projektu Název projektu Číslo a název šablony klíčové aktivity CZ.1.07/1.5.00/34.0802 Zkvalitnění výuky prostřednictvím ICT III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Příjemce
Průvodka Číslo projektu Název projektu Číslo a název šablony klíčové aktivity CZ.1.07/1.5.00/34.0802 Zkvalitnění výuky prostřednictvím ICT III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Příjemce
Nejprve je nutno převést hmotnostní koncentrace na molární (správný výsledek je 1,345M).
 11. vičení ph II. 1. Jaké je ph 8% ota, = 1,0097 g/m, = 60,05 g.mol -1, = 1,75. -5? Nejprve je nutno převést hmotnostní konentrae na molární (správný výsledek je 1,5). Poté použijeme jednu z následujííh
11. vičení ph II. 1. Jaké je ph 8% ota, = 1,0097 g/m, = 60,05 g.mol -1, = 1,75. -5? Nejprve je nutno převést hmotnostní konentrae na molární (správný výsledek je 1,5). Poté použijeme jednu z následujííh
Acidobazické rovnováhy
 Aidobaziké rovnováhy při aidobazikýh rovnováháh (proteolytikýh) - přenos vodíkového kationtu mezi ionty (molekulami) zúčastněnými v rovnováze kyselina donor protonů zásada akeptor protonů YSELINA + zásada
Aidobaziké rovnováhy při aidobazikýh rovnováháh (proteolytikýh) - přenos vodíkového kationtu mezi ionty (molekulami) zúčastněnými v rovnováze kyselina donor protonů zásada akeptor protonů YSELINA + zásada
Redoxní rovnováhy. OX 1 + n 1 e RED 1 ox 2 + n 2 e red 2. aox + bb + ne cred + dd (účast i jiných látek) K = RED. redox. red
 Rední rovnováhy Rední rovnováhy rovnováhy srážecí, komplexotvorné, cidobzické zloženy n kombinci (výměně) iontů ní rovnováhy - zloženy n přenosu elektronů ukční činidl (donory elektronů) idční činidl (kceptory
Rední rovnováhy Rední rovnováhy rovnováhy srážecí, komplexotvorné, cidobzické zloženy n kombinci (výměně) iontů ní rovnováhy - zloženy n přenosu elektronů ukční činidl (donory elektronů) idční činidl (kceptory
3 Acidobazické reakce
 3 Acidobazické reakce Brønstedova teorie 1. Uveďte explicitní definice podle Brønstedovy teorie. Kyselina je... Báze je... Konjugovaný pár je... 2. Doplňte tabulku a pojmenujte všechny sloučeniny. Kyselina
3 Acidobazické reakce Brønstedova teorie 1. Uveďte explicitní definice podle Brønstedovy teorie. Kyselina je... Báze je... Konjugovaný pár je... 2. Doplňte tabulku a pojmenujte všechny sloučeniny. Kyselina
Biochemický ústav LF MU (E.T.) 2013
 Roztoky elektrolytů: ph, hydrolýza solí, pufry Biochemický ústav LF MU (E.T.) 2013 1 Pojmy, jejichž znalost ze střední školy je nezbytná pro porozumění přednášené látce : elektrolyty, jejich chování, typy
Roztoky elektrolytů: ph, hydrolýza solí, pufry Biochemický ústav LF MU (E.T.) 2013 1 Pojmy, jejichž znalost ze střední školy je nezbytná pro porozumění přednášené látce : elektrolyty, jejich chování, typy
REAKCE: 1) ACIDOBAZICKÉ Acidum = kyselina Baze = zásada. Využití: V analytické kvantitativní chemii v odměrné analýze
 KYSELINY A ZÁSADY 1 REAKCE: 1) ACIDOBAZICKÉ Acidum = kyselina Baze = zásada Využití: V analytické kvantitativní chemii v odměrné analýze A) ALKALIMETRIE = odměrný roztok je zásada B) ACIDIMETRIE = odměrný
KYSELINY A ZÁSADY 1 REAKCE: 1) ACIDOBAZICKÉ Acidum = kyselina Baze = zásada Využití: V analytické kvantitativní chemii v odměrné analýze A) ALKALIMETRIE = odměrný roztok je zásada B) ACIDIMETRIE = odměrný
Odměrná analýza, volumetrie ODMĚRNÁ ANALÝZA, VOLUMETRIE. Základní kroky při odměrné analýze. 1. Odvážení/odměření vzorku
 Odměrná nlýz, volumetrie metod zložená n měření ojemu metod solutní: stnovení nlytu ze změřeného ojemu roztoku činidl o přesně známé koncentrci, který je zpotřeí k úplné stechiometricky definovné rekci
Odměrná nlýz, volumetrie metod zložená n měření ojemu metod solutní: stnovení nlytu ze změřeného ojemu roztoku činidl o přesně známé koncentrci, který je zpotřeí k úplné stechiometricky definovné rekci
Gymnázium Vysoké Mýto nám. Vaňorného 163, 566 01 Vysoké Mýto
 Gymnázium Vysoké Mýto nám. Vaňorného 163, 566 01 Vysoké Mýto Výpočty ph roztoků kyselin a zásad ph silných jednosytných kyselin a zásad. Pro výpočty se uvažuje, že silné kyseliny a zásady jsou úplně disociovány.
Gymnázium Vysoké Mýto nám. Vaňorného 163, 566 01 Vysoké Mýto Výpočty ph roztoků kyselin a zásad ph silných jednosytných kyselin a zásad. Pro výpočty se uvažuje, že silné kyseliny a zásady jsou úplně disociovány.
[ ] d[ Y] rychlost REAKČNÍ KINETIKA X Y
![[ ] d[ Y] rychlost REAKČNÍ KINETIKA X Y [ ] d[ Y] rychlost REAKČNÍ KINETIKA X Y](/thumbs/78/77051926.jpg) REAKČNÍ KINETIKA Faktory ovlivňující rychlost chemických reakcí Chemická povaha reaktantů - reaktivita Fyzikální stav reaktantů homogenní vs. heterogenní reakce Teplota 10 C zvýšení rychlosti 2x 3x zýšení
REAKČNÍ KINETIKA Faktory ovlivňující rychlost chemických reakcí Chemická povaha reaktantů - reaktivita Fyzikální stav reaktantů homogenní vs. heterogenní reakce Teplota 10 C zvýšení rychlosti 2x 3x zýšení
4. přednáška 22. října Úplné metrické prostory. Metrický prostor (M, d) je úplný, když každá cauchyovská posloupnost bodů v M konverguje.
 4. přednášk 22. říjn 2007 Úplné metrické prostory. Metrický prostor (M, d) je úplný, když kždá cuchyovská posloupnost bodů v M konverguje. Příkldy. 1. Euklidovský prostor R je úplný, kždá cuchyovská posloupnost
4. přednášk 22. říjn 2007 Úplné metrické prostory. Metrický prostor (M, d) je úplný, když kždá cuchyovská posloupnost bodů v M konverguje. Příkldy. 1. Euklidovský prostor R je úplný, kždá cuchyovská posloupnost
Teorie kyselin a zásad poznámky 5.A GVN
 Teorie kyselin a zásad poznámky 5A GVN 13 června 2007 Arrheniova teorie platná pouze pro vodní roztoky kyseliny jsou látky schopné ve vodném roztoku odštěpit vodíkový kation H + HCl H + + Cl - CH 3 COOH
Teorie kyselin a zásad poznámky 5A GVN 13 června 2007 Arrheniova teorie platná pouze pro vodní roztoky kyseliny jsou látky schopné ve vodném roztoku odštěpit vodíkový kation H + HCl H + + Cl - CH 3 COOH
10 Acidobazické reakce
 10 cidobazické reakce cidobazické reakce probíhají v roztocích mezi kyselinami a zásadami a dochází při nich k výměně protonu. Pojem kyseliny a zásady Podle teorie Brønsteda a Lowryho jsou kyseliny látky,
10 cidobazické reakce cidobazické reakce probíhají v roztocích mezi kyselinami a zásadami a dochází při nich k výměně protonu. Pojem kyseliny a zásady Podle teorie Brønsteda a Lowryho jsou kyseliny látky,
Stanovení disociační konstanty acidobazického indikátoru
 Stnovení disociční konstnty cidobzického indikátoru Teorie: cidobzické indikátory se chovjí buď jko slbé kyseliny nebo slbé báze disociují ve vodných roztocích omezeně. Kvntittivní mírou disocice je hodnot
Stnovení disociční konstnty cidobzického indikátoru Teorie: cidobzické indikátory se chovjí buď jko slbé kyseliny nebo slbé báze disociují ve vodných roztocích omezeně. Kvntittivní mírou disocice je hodnot
Inovace bakalářského studijního oboru Aplikovaná chemie CZ.1.07/2.2.00/ Výpočty z chemických vzorců
 Výpočty z chemických vzorců 1. Hmotnost kyslíku je 80 g. Vypočítejte : a) počet atomů kyslíku ( 3,011 10 atomů) b) počet molů kyslíku (2,5 mol) c) počet molekul kyslíku (1,505 10 24 molekul) d) objem (dm
Výpočty z chemických vzorců 1. Hmotnost kyslíku je 80 g. Vypočítejte : a) počet atomů kyslíku ( 3,011 10 atomů) b) počet molů kyslíku (2,5 mol) c) počet molekul kyslíku (1,505 10 24 molekul) d) objem (dm
Stanovení disociační konstanty acidobazického indikátoru. = a
 Stnovení disociční konstnty cidobzického indikátoru Teorie: Slbé kyseliny nebo báze disociují ve vodných roztocích jen omezeně; kvntittivní mírou je hodnot disociční konstnty. Disociční rekci příslušející
Stnovení disociční konstnty cidobzického indikátoru Teorie: Slbé kyseliny nebo báze disociují ve vodných roztocích jen omezeně; kvntittivní mírou je hodnot disociční konstnty. Disociční rekci příslušející
10 Acidobazické reakce
 10 idobaziké reake idobaziké reake probíhají v roztoíh mezi kyselinami a zásadami a dohází při nih k výměně protonu. Pojem kyseliny a zásady Podle teorie rønsteda a Lowryho jsou kyseliny látky, které mají
10 idobaziké reake idobaziké reake probíhají v roztoíh mezi kyselinami a zásadami a dohází při nih k výměně protonu. Pojem kyseliny a zásady Podle teorie rønsteda a Lowryho jsou kyseliny látky, které mají
CHEMIE. Pracovní list č. 7 - žákovská verze Téma: ph. Mgr. Lenka Horutová. Projekt: Student a konkurenceschopnost Reg. číslo: CZ.1.07/1.1.07/03.
 www.projektsako.cz CHEMIE Pracovní list č. 7 - žákovská verze Téma: ph Lektor: Mgr. Lenka Horutová Projekt: Student a konkurenceschopnost Reg. číslo: CZ.1.07/1.1.07/03.0075 Teorie: Pro snadnější výpočet
www.projektsako.cz CHEMIE Pracovní list č. 7 - žákovská verze Téma: ph Lektor: Mgr. Lenka Horutová Projekt: Student a konkurenceschopnost Reg. číslo: CZ.1.07/1.1.07/03.0075 Teorie: Pro snadnější výpočet
E = 1,1872 V ( = E Cu. (γ ± = 0, ,001 < I < 0,1 rozšířený D-H vztah)
 GALVANICKÉ ČLÁNKY E = E red,rvý E red,levý E D = E red,rvý E ox,levý E D G = z E E E S = z = z T E T T Q= T S [] G = z E rg E E rs = = z, r rg T rs z = = T E T T T E E T T ν i E = E ln i z i mimo rovnováhu
GALVANICKÉ ČLÁNKY E = E red,rvý E red,levý E D = E red,rvý E ox,levý E D G = z E E E S = z = z T E T T Q= T S [] G = z E rg E E rs = = z, r rg T rs z = = T E T T T E E T T ν i E = E ln i z i mimo rovnováhu
Elektrochemie. Předmět elektrochemie: disociace (roztoky elektrolytů, taveniny solí) vodivost. jevy na rozhraní s/l (elektrolýza, články)
 Elektrochemie 1/30 Předmět elektrochemie: disociace (roztoky elektrolytů, taveniny solí) vodivost jevy na rozhraní s/l (elektrolýza, články) Vodiče: vodivost způsobena pohybem elektronů uvnitř mřížky:
Elektrochemie 1/30 Předmět elektrochemie: disociace (roztoky elektrolytů, taveniny solí) vodivost jevy na rozhraní s/l (elektrolýza, články) Vodiče: vodivost způsobena pohybem elektronů uvnitř mřížky:
ELEKTROCHEMIE. - studuje soustavy, které obsahují elektricky nabité částice.
 ELEKTROCHEMIE - studuje soustavy, které obsahují elektricky nabité částice. ZÁKLADNÍ POJMY Vodiče látky, které vedou elektrický proud. Vodiče I. třídy přenos elektrického náboje je zprostředkován volně
ELEKTROCHEMIE - studuje soustavy, které obsahují elektricky nabité částice. ZÁKLADNÍ POJMY Vodiče látky, které vedou elektrický proud. Vodiče I. třídy přenos elektrického náboje je zprostředkován volně
Vnit ní síly ve 2D - p íklad 2
 Vnit ní síly ve D - p íkld Orázek 1: Zt ºoví shém. Úkol: Ur ete nlytiké pr hy vnit níh sil n konstruki vykreslete je. e²ení: Pro výpo et rekí je vhodné si spojité ztíºení nhrdit odpovídjíím náhrdním emenem.
Vnit ní síly ve D - p íkld Orázek 1: Zt ºoví shém. Úkol: Ur ete nlytiké pr hy vnit níh sil n konstruki vykreslete je. e²ení: Pro výpo et rekí je vhodné si spojité ztíºení nhrdit odpovídjíím náhrdním emenem.
8. cvičení z Matematiky 2
 8. cvičení z Mtemtiky 2 11.-1. dubn 2016 8.1 Njděte tři pozitivní čísl jejichž součin je mximální, jejichž součet je roven 100. Zdání příkldu lze interpretovt tké tk, že hledáme mximální objem kvádru,
8. cvičení z Mtemtiky 2 11.-1. dubn 2016 8.1 Njděte tři pozitivní čísl jejichž součin je mximální, jejichž součet je roven 100. Zdání příkldu lze interpretovt tké tk, že hledáme mximální objem kvádru,
3 Acidobazické reakce
 3 Acidobazické reakce Brønstedova teorie 1. Uveďte explicitní definice podle Brønstedovy teorie. Kyselina je... Báze je... Konjugovaný pár je... 2. Doplňte tabulku a pojmenujte všechny sloučeniny. Kyselina
3 Acidobazické reakce Brønstedova teorie 1. Uveďte explicitní definice podle Brønstedovy teorie. Kyselina je... Báze je... Konjugovaný pár je... 2. Doplňte tabulku a pojmenujte všechny sloučeniny. Kyselina
Výpočty koncentrací. objemová % (objemový zlomek) krvi m. Vsložky. celku. Objemy nejsou aditivní!!!
 Výpočty koncentrací objemová % (objemový zlomek) Vsložky % obj. = 100 V celku Objemy nejsou aditivní!!! Příklad: Kolik ethanolu je v 700 ml vodky (40 % obj.)? Kolik promile ethanolu v krvi bude mít muž
Výpočty koncentrací objemová % (objemový zlomek) Vsložky % obj. = 100 V celku Objemy nejsou aditivní!!! Příklad: Kolik ethanolu je v 700 ml vodky (40 % obj.)? Kolik promile ethanolu v krvi bude mít muž
Elektrotechnika a informatika
 Vrint A Část I.: Elektrotehnik Strn: 1/4 Osobní číslo uhzeče: Test k přijímímu řízení ke studiu n Fkultě elektrotehniké Zápdočeské univerzity v Plzni Elektrotehnik informtik 1. Jká je jednotk proudové
Vrint A Část I.: Elektrotehnik Strn: 1/4 Osobní číslo uhzeče: Test k přijímímu řízení ke studiu n Fkultě elektrotehniké Zápdočeské univerzity v Plzni Elektrotehnik informtik 1. Jká je jednotk proudové
ZÁKLADNÍ CHEMICKÉ POJMY A ZÁKONY
 ZÁKLADNÍ CHEMICKÉ POJMY A ZÁKONY Klíčová slova: relativní atomová hmotnost (A r ), relativní molekulová hmotnost (M r ), Avogadrova konstanta (N A ), látkové množství (n, mol), molární hmotnost (M, g/mol),
ZÁKLADNÍ CHEMICKÉ POJMY A ZÁKONY Klíčová slova: relativní atomová hmotnost (A r ), relativní molekulová hmotnost (M r ), Avogadrova konstanta (N A ), látkové množství (n, mol), molární hmotnost (M, g/mol),
 OBECNÁ CHEMIE František Zachoval CHEMICKÉ ROVNOVÁHY 1. Rovnovážný stav, rovnovážná konstanta a její odvození Dlouhou dobu se chemici domnívali, že jakákoliv chem.
OBECNÁ CHEMIE František Zachoval CHEMICKÉ ROVNOVÁHY 1. Rovnovážný stav, rovnovážná konstanta a její odvození Dlouhou dobu se chemici domnívali, že jakákoliv chem.
TVRDOST, VODIVOST A ph MINERÁLNÍ VODY
 TRDOST, ODIOST A ph MINERÁLNÍ ODY A) STANOENÍ TRDOSTI MINERÁLNÍCH OD Prinip: Tvrdost, resp. elková tvrdost vody, je způsobena obsahem solí alkalikýh zemin vápník, hořčík, stronium a barium. Stronium a
TRDOST, ODIOST A ph MINERÁLNÍ ODY A) STANOENÍ TRDOSTI MINERÁLNÍCH OD Prinip: Tvrdost, resp. elková tvrdost vody, je způsobena obsahem solí alkalikýh zemin vápník, hořčík, stronium a barium. Stronium a
Hydrochemie Oxid uhličitý a jeho iontové formy, ph, NK
 1 Oxid uhličitý - CO 2 původ: atmosférický - neznečištěný vzduch 0,03 obj. % CO 2 biogenní aerobní a anaerobní rozklad OL hlubinný magma, termický rozklad uhličitanových minerálů, rozklad uhličitanových
1 Oxid uhličitý - CO 2 původ: atmosférický - neznečištěný vzduch 0,03 obj. % CO 2 biogenní aerobní a anaerobní rozklad OL hlubinný magma, termický rozklad uhličitanových minerálů, rozklad uhličitanových
Potenciometrické stanovení disociační konstanty
 Potenciometrické stanovení disociační konstanty TEORIE Elektrolytická disociace kyseliny HA ve vodě vede k ustavení disociační rovnováhy: HA + H 2O A - + H 3O +, kterou lze charakterizovat disociační konstantou
Potenciometrické stanovení disociační konstanty TEORIE Elektrolytická disociace kyseliny HA ve vodě vede k ustavení disociační rovnováhy: HA + H 2O A - + H 3O +, kterou lze charakterizovat disociační konstantou
Kyseliny. Gerber (~1300) příprava H 2 SO 4, HNO 3. Libavius příprava HCl a aqua regia (rozpouští Au)
 Kyseliny Gerber (~1300) příprava H 2 SO 4, HNO 3 Libavius příprava HCl a aqua regia (rozpouští Au) Chemická látka produkovaná na světě v největším množství za rok: H 2 SO 4 Andreas Libau (Libavius) (1540-1616)
Kyseliny Gerber (~1300) příprava H 2 SO 4, HNO 3 Libavius příprava HCl a aqua regia (rozpouští Au) Chemická látka produkovaná na světě v největším množství za rok: H 2 SO 4 Andreas Libau (Libavius) (1540-1616)
Výpočty ph silných a slabých protolytů a barevné acidobazické indikátory
 Výpočty ph silných a slabých protolytů a barevné acidobazické indikátory Kamil Záruba Text vznikl jako doplňující zdroj pro soutěžící kategorie B (2012/13). Použitá literatura: Volka a kol., Analytická
Výpočty ph silných a slabých protolytů a barevné acidobazické indikátory Kamil Záruba Text vznikl jako doplňující zdroj pro soutěžící kategorie B (2012/13). Použitá literatura: Volka a kol., Analytická
Laboratorní práce č. 6 Úloha č. 5. Měření odporu, indukčnosti a vzájemné indukčnosti můstkovými metodami:
 Truhlář Michl 3 005 Lbortorní práce č 6 Úloh č 5 p 99,8kP Měření odporu, indukčnosti vzájemné indukčnosti můstkovými metodmi: Úkol: Whetstoneovým mostem změřte hodnoty odporů dvou rezistorů, jejich sériového
Truhlář Michl 3 005 Lbortorní práce č 6 Úloh č 5 p 99,8kP Měření odporu, indukčnosti vzájemné indukčnosti můstkovými metodmi: Úkol: Whetstoneovým mostem změřte hodnoty odporů dvou rezistorů, jejich sériového
Rovinná napjatost tenzometrická růžice Obsah:
 5. leke Rovinná npjtost tenzometriká růžie Osh: 5. Úvod 5. Rovinná npjtost 5. Tenzometriká růžie 4 5.4 Posouzení přípustnosti nměřenýh hodnot deforme resp. vyhodnoenýh npět 7 strn z 8 5. Úvod Při měření
5. leke Rovinná npjtost tenzometriká růžie Osh: 5. Úvod 5. Rovinná npjtost 5. Tenzometriká růžie 4 5.4 Posouzení přípustnosti nměřenýh hodnot deforme resp. vyhodnoenýh npět 7 strn z 8 5. Úvod Při měření
Sbírka příkladů z teoretických základů analytické chemie Tomáš Křížek Karel Nesměrák
 UNIVERZITA KARLOVA Přírodovědecká fakulta Katedra analytické chemie Sbírka příkladů z teoretických základů analytické chemie Tomáš Křížek Karel Nesměrák Praha 2016 1 Protolytické rovnováhy 1.1 Vypočítejte
UNIVERZITA KARLOVA Přírodovědecká fakulta Katedra analytické chemie Sbírka příkladů z teoretických základů analytické chemie Tomáš Křížek Karel Nesměrák Praha 2016 1 Protolytické rovnováhy 1.1 Vypočítejte
INTEGRACE KOMPLEXNÍ FUNKCE KŘIVKOVÝ INTEGRÁL
 INTEGRAE KOMPLEXNÍ FUNKE KŘIVKOVÝ INTEGRÁL N konci kpitoly o derivci je uveden souvislost existence derivce s potenciálním polem. Existuje dlší chrkterizce potenciálného pole, která nebyl v kpitole o derivci
INTEGRAE KOMPLEXNÍ FUNKE KŘIVKOVÝ INTEGRÁL N konci kpitoly o derivci je uveden souvislost existence derivce s potenciálním polem. Existuje dlší chrkterizce potenciálného pole, která nebyl v kpitole o derivci
Matematika 1A. PetrSalačaJiříHozman Fakulta přírodovědně-humanitní a pedagogická Technická univerzita v Liberci
 Mtemtik 1A. PetrSlčJiříHozmn Fkult přírodovědně-humnitní pedgogická Technická univerzit v Liberci petr.slc@tul.cz jiri.hozmn@tul.cz 21.11.2016 Fkult přírodovědně-humnitní pedgogická TUL ZS 2016-2017 1/
Mtemtik 1A. PetrSlčJiříHozmn Fkult přírodovědně-humnitní pedgogická Technická univerzit v Liberci petr.slc@tul.cz jiri.hozmn@tul.cz 21.11.2016 Fkult přírodovědně-humnitní pedgogická TUL ZS 2016-2017 1/
 !!! #!! # % & ()!+ %& #( ) +,,!,!!./0./01 2 34 % 00 (1!#! #! #23 + )!!,,5,!+ 4)!005!! 6 )! %,76!,8, )! 44 %!! #! #236!!1 1 5 6 5+!!1 ( 9 9!5 6 + /+ # % 7 8 % : 4; 2,/! = %
!!! #!! # % & ()!+ %& #( ) +,,!,!!./0./01 2 34 % 00 (1!#! #! #23 + )!!,,5,!+ 4)!005!! 6 )! %,76!,8, )! 44 %!! #! #236!!1 1 5 6 5+!!1 ( 9 9!5 6 + /+ # % 7 8 % : 4; 2,/! = %
NEWTONŮV INTEGRÁL. V předchozích kapitolách byla popsána inverzní operace k derivování. Zatím nebylo jasné, k čemu tento nástroj slouží.
 NEWTONŮV INTEGRÁL V předchozích kpitolách byl popsán inverzní operce k derivování. Ztím nebylo jsné, k čemu tento nástroj slouží. Uvžujme trmvj, která je poháněn elektřinou při brždění vyrábí dynmem elektřinu:
NEWTONŮV INTEGRÁL V předchozích kpitolách byl popsán inverzní operce k derivování. Ztím nebylo jsné, k čemu tento nástroj slouží. Uvžujme trmvj, která je poháněn elektřinou při brždění vyrábí dynmem elektřinu:
2002 Katedra obecné elektrotechniky FEI VŠB-TU Ostrava Ing.Stanislav Kocman
 STEJNOSĚRNÉ STROJE 1. Princip činnosti stejnosměrného stroje 2. Rekce kotvy komutce stejnosměrných strojů 3. Rozdělení stejnosměrných strojů 4. Stejnosměrné generátory 5. Stejnosměrné motory 2002 Ktedr
STEJNOSĚRNÉ STROJE 1. Princip činnosti stejnosměrného stroje 2. Rekce kotvy komutce stejnosměrných strojů 3. Rozdělení stejnosměrných strojů 4. Stejnosměrné generátory 5. Stejnosměrné motory 2002 Ktedr
V předchozích kapitolách byla popsána inverzní operace k derivování. Zatím nebylo jasné, k čemu tento nástroj slouží.
 NEWTONŮV INTEGRÁL V předchozích kpitolách byl popsán inverzní operce k derivování Ztím nebylo jsné, k čemu tento nástroj slouží Uvžujme trmvj, která je poháněn elektřinou při brždění vyrábí dynmem elektřinu:
NEWTONŮV INTEGRÁL V předchozích kpitolách byl popsán inverzní operce k derivování Ztím nebylo jsné, k čemu tento nástroj slouží Uvžujme trmvj, která je poháněn elektřinou při brždění vyrábí dynmem elektřinu:
Sešit pro laboratorní práci z chemie
 Sešit pro laboratorní práci z chemie téma: Hydrolýza solí autor: MVDr. Alexandra Gajová vytvořeno při realizaci projektu: Inovace školního vzdělávacího programu biologie a chemie registrační číslo projektu:
Sešit pro laboratorní práci z chemie téma: Hydrolýza solí autor: MVDr. Alexandra Gajová vytvořeno při realizaci projektu: Inovace školního vzdělávacího programu biologie a chemie registrační číslo projektu:
III/2 - Inovace a zkvalitnění výuky prostřednictvím ICT Inovace výuky na GSN prostřednictvím ICT
 Škola: Gymnázium, Brno, Slovanské náměstí 7 Šablona: Název projektu: Číslo projektu: Autor: Tematická oblast: Název DUMu: Kód: Datum: 10. 9. 2013 Cílová skupina: Klíčová slova: Anotace: III/2 - Inovace
Škola: Gymnázium, Brno, Slovanské náměstí 7 Šablona: Název projektu: Číslo projektu: Autor: Tematická oblast: Název DUMu: Kód: Datum: 10. 9. 2013 Cílová skupina: Klíčová slova: Anotace: III/2 - Inovace
2 Roztoky elektrolytů. Osmotický tlak
 Roztoky elektrolytů. Osmotický tlak 1. Doplněním uvedených schémat vyjádřete rozdílné chování různých typů látek po jejich rozpuštění ve vodě. Použijte symboly AB(aq), A + (aq), B - (aq). [s pevná fáze,
Roztoky elektrolytů. Osmotický tlak 1. Doplněním uvedených schémat vyjádřete rozdílné chování různých typů látek po jejich rozpuštění ve vodě. Použijte symboly AB(aq), A + (aq), B - (aq). [s pevná fáze,
Vzdělávací materiál. vytvořený v projektu OP VK. Název školy: Gymnázium, Zábřeh, náměstí Osvobození 20. Číslo projektu: CZ.1.07/1.5.00/34.
 Vzdělávcí mteriál vytvořený v projektu OP VK Název školy: Gymnázium, Zářeh, náměstí Osvoození 20 Číslo projektu: Název projektu: Číslo název klíčové ktivity: CZ.1.07/1.5.00/34.0211 Zlepšení podmínek pro
Vzdělávcí mteriál vytvořený v projektu OP VK Název školy: Gymnázium, Zářeh, náměstí Osvoození 20 Číslo projektu: Název projektu: Číslo název klíčové ktivity: CZ.1.07/1.5.00/34.0211 Zlepšení podmínek pro
OBECNÝ URČITÝ INTEGRÁL
 OBECNÝ URČITÝ INTEGRÁL Zobecnění Newtonov nebo Riemnnov integrálu se definují různým způsobem dostnou se někdy různé, někdy stejné pojmy. V tomto textu bude postup volen jko zobecnění Newtonov integrálu,
OBECNÝ URČITÝ INTEGRÁL Zobecnění Newtonov nebo Riemnnov integrálu se definují různým způsobem dostnou se někdy různé, někdy stejné pojmy. V tomto textu bude postup volen jko zobecnění Newtonov integrálu,
Osové namáhání osová síla N v prutu
 Osové nmáhání osová síl v prutu 3 typy úloh:. Pruty příhrdové konstrukce, táhl Dvě podmínky rovnováhy v kždém styčníku: F ix 0 F iz 0. Táhl podporující pevnou ztíženou desku R z M ib 0 P R R b P 6 6 P
Osové nmáhání osová síl v prutu 3 typy úloh:. Pruty příhrdové konstrukce, táhl Dvě podmínky rovnováhy v kždém styčníku: F ix 0 F iz 0. Táhl podporující pevnou ztíženou desku R z M ib 0 P R R b P 6 6 P
Oxidačně-redukční reakce (Redoxní reakce)
 Seminář z nlytické chemie idčně-redukční rekce (Redoxní rekce) RNDr. R. Čbl, Dr. Univerzit Krlov v Prze Přírodovědecká fkult Ktedr nlytické chemie Definice pojmů idce částice (tom, molekul, ion) ztrácí
Seminář z nlytické chemie idčně-redukční rekce (Redoxní rekce) RNDr. R. Čbl, Dr. Univerzit Krlov v Prze Přírodovědecká fkult Ktedr nlytické chemie Definice pojmů idce částice (tom, molekul, ion) ztrácí
Jana Fauknerová Matějčková
 Jana Fauknerová Matějčková převody jednotek výpočet ph ph vodných roztoků ph silných kyselin a zásad ph slabých kyselin a zásad, disociační konstanta, pk ph pufrů koncentace 1000mg př. g/dl mg/l = = *10000
Jana Fauknerová Matějčková převody jednotek výpočet ph ph vodných roztoků ph silných kyselin a zásad ph slabých kyselin a zásad, disociační konstanta, pk ph pufrů koncentace 1000mg př. g/dl mg/l = = *10000
Gymnázium, Milevsko, Masarykova 183 Školní vzdělávací program (ŠVP) pro vyšší stupeň osmiletého studia a čtyřleté studium 4.
 Vyučovací předmět - Chemie Vzdělávací obor - Člověk a příroda Gymnázium, Milevsko, Masarykova 183 Školní vzdělávací program (ŠVP) pro vyšší stupeň osmiletého studia a čtyřleté studium 4. ročník - seminář
Vyučovací předmět - Chemie Vzdělávací obor - Člověk a příroda Gymnázium, Milevsko, Masarykova 183 Školní vzdělávací program (ŠVP) pro vyšší stupeň osmiletého studia a čtyřleté studium 4. ročník - seminář
Acidobazické děje - maturitní otázka z chemie
 Otázka: Acidobazické děje Předmět: Chemie Přidal(a): Žaneta Teorie kyselin a zásad: Arrhemiova teorie (1887) Kyseliny jsou látky, které odštěpují ve vodném roztoku proton vodíku H+ HA -> H+ + A- Zásady
Otázka: Acidobazické děje Předmět: Chemie Přidal(a): Žaneta Teorie kyselin a zásad: Arrhemiova teorie (1887) Kyseliny jsou látky, které odštěpují ve vodném roztoku proton vodíku H+ HA -> H+ + A- Zásady
4. cvičení z Matematiky 2
 4. cvičení z Mtemtiky 2 14.-18. březn 2016 4.1 Njděte ity (i (ii (iii (iv 2 +(y 1 2 +1 1 2 +(y 1 2 z 2 y 2 z yz 1 2 y 2 (,y (0,0 2 +y 2 2 y 2 (,y (0,0 2 +y 3 (i Pro funkci f(, y = 2 +(y 1 2 +1 1 2 +(y
4. cvičení z Mtemtiky 2 14.-18. březn 2016 4.1 Njděte ity (i (ii (iii (iv 2 +(y 1 2 +1 1 2 +(y 1 2 z 2 y 2 z yz 1 2 y 2 (,y (0,0 2 +y 2 2 y 2 (,y (0,0 2 +y 3 (i Pro funkci f(, y = 2 +(y 1 2 +1 1 2 +(y
Autor: Mgr. Stanislava Bubíková. Datum (období) tvorby: 12. 4. 2013. Ročník: osmý
 ph Autor: Mgr. Stanislava Bubíková Datum (období) tvorby: 12. 4. 2013 Ročník: osmý Vzdělávací oblast: Člověk a příroda / Chemie / Anorganické sloučeniny 1 Anotace: Žáci se seznámí se základní vlastností
ph Autor: Mgr. Stanislava Bubíková Datum (období) tvorby: 12. 4. 2013 Ročník: osmý Vzdělávací oblast: Člověk a příroda / Chemie / Anorganické sloučeniny 1 Anotace: Žáci se seznámí se základní vlastností
Moravské gymnázium Brno s.r.o. RNDr. Miroslav Štefan. Chemie obecná síla kyselin a zásad. Datum tvorby 11.12.2013
 Číslo projektu CZ.1.07/1.5.00/34.0743 Název školy Autor Tematická oblast Ročník Moravské gymnázium Brno s.r.o. RNDr. Miroslav Štefan Chemie obecná síla kyselin a zásad 1. ročník Datum tvorby 11.12.2013
Číslo projektu CZ.1.07/1.5.00/34.0743 Název školy Autor Tematická oblast Ročník Moravské gymnázium Brno s.r.o. RNDr. Miroslav Štefan Chemie obecná síla kyselin a zásad 1. ročník Datum tvorby 11.12.2013
Repetitorium chemie XI.
 Repetitorium chemie XI. Užitečné rovnováhy v roztocích elektrolytů: znovu o ph, co jsou pufry, rozpustnost, omezeně rozpustné soli, a tklivá historie o rozpůlení dcery hostinské (2014) Dissociace ve vodných
Repetitorium chemie XI. Užitečné rovnováhy v roztocích elektrolytů: znovu o ph, co jsou pufry, rozpustnost, omezeně rozpustné soli, a tklivá historie o rozpůlení dcery hostinské (2014) Dissociace ve vodných
1 i= VLIV ZMĚN FYZIKÁLNÍCH PARAMETRŮ FLUIDNÍCH VRSTEV NA CHARAKTERISTIKY TLAKOVÝCH FLUKTUACÍ. OTAKAR TRNKA a MILOSLAV HARTMAN. i M
 Chem. Listy, 55 53 (7) VLIV ZMĚN FYZIKÁLNÍCH PARAMETRŮ FLUIDNÍCH VRSTEV NA CHARAKTERISTIKY TLAKOVÝCH FLUKTUACÍ OTAKAR TRNKA MILOSLAV HARTMAN Ústv chemických procesů, AV ČR, Rozvojová 35, 65 Prh 6 trnk@icpf.cs.cz
Chem. Listy, 55 53 (7) VLIV ZMĚN FYZIKÁLNÍCH PARAMETRŮ FLUIDNÍCH VRSTEV NA CHARAKTERISTIKY TLAKOVÝCH FLUKTUACÍ OTAKAR TRNKA MILOSLAV HARTMAN Ústv chemických procesů, AV ČR, Rozvojová 35, 65 Prh 6 trnk@icpf.cs.cz
Elektrolyty. Disociace termická disociace (pomocí zvýšené teploty) elektrolytická disociace (pomocí polárního rozpouštědla)
 Elektrolyty Elektrolyty látky, které při rozpouštění nebo tavení disociují (štěpí se) na elektricky nabité částice (ionty) jejich roztoky a taveniny jsou elektricky vodivé kyseliny, hydroxidy, soli Ionty
Elektrolyty Elektrolyty látky, které při rozpouštění nebo tavení disociují (štěpí se) na elektricky nabité částice (ionty) jejich roztoky a taveniny jsou elektricky vodivé kyseliny, hydroxidy, soli Ionty
ZEMNÍ TLAKY. Princip určování: teorie mezní rovnováhy, rovinná úloha, předpoklad rovinných kluzných ploch
 Druhy!"tlk v klidu S r!"ktivní zemní tlk S!"psivní odpor S p ZEMNÍ TLAKY Obr.. Druhy zemních tlků ) tlk zeminy v klidu, b) ktivní zemní tlk, c) psivní zemní odpor, d) závislost velikosti zemního tlku od
Druhy!"tlk v klidu S r!"ktivní zemní tlk S!"psivní odpor S p ZEMNÍ TLAKY Obr.. Druhy zemních tlků ) tlk zeminy v klidu, b) ktivní zemní tlk, c) psivní zemní odpor, d) závislost velikosti zemního tlku od
Fyzikální chemie. ochrana životního prostředí analytická chemie chemická technologie denní. Platnost: od 1. 9. 2009 do 31. 8. 2013
 Učební osnova předmětu Fyzikální chemie Studijní obor: Aplikovaná chemie Zaměření: Forma vzdělávání: Celkový počet vyučovacích hodin za studium: Analytická chemie Chemická technologie Ochrana životního
Učební osnova předmětu Fyzikální chemie Studijní obor: Aplikovaná chemie Zaměření: Forma vzdělávání: Celkový počet vyučovacích hodin za studium: Analytická chemie Chemická technologie Ochrana životního
CVIČENÍ Z ENVIRONMENTÁLNÍ CHEMIE I
 ČESKÁ ZEMĚDĚLSKÁ UNIVEZITA V PRAZE Fakulta životního prostředí Katedra vodního hospodářství a environmentálního modelování CVIČENÍ Z ENVIRONMENTÁLNÍ CHEMIE I doc. Mgr. Marek VACH, Ph.D. Ing. Martin HEŘMANOVSKÝ
ČESKÁ ZEMĚDĚLSKÁ UNIVEZITA V PRAZE Fakulta životního prostředí Katedra vodního hospodářství a environmentálního modelování CVIČENÍ Z ENVIRONMENTÁLNÍ CHEMIE I doc. Mgr. Marek VACH, Ph.D. Ing. Martin HEŘMANOVSKÝ
Chelatometrie. Stanovení tvrdosti vody
 Chelatometrie Stanovení tvrdosti vody CHELATOMETRIE Cheláty (vnitřně komplexní sloučeniny; řecky chelé = klepeto) jsou komplexní sloučeniny, kde centrální ion je členem jednoho nebo více vznikajících kruhů.
Chelatometrie Stanovení tvrdosti vody CHELATOMETRIE Cheláty (vnitřně komplexní sloučeniny; řecky chelé = klepeto) jsou komplexní sloučeniny, kde centrální ion je členem jednoho nebo více vznikajících kruhů.
STANOVENÍ CHLORIDŮ. Odměrné argentometrické stanovení chloridů podle Mohra
 STANOVENÍ CHLORIDŮ Odměrné argentometrické stanovení chloridů podle Mohra Cíl práce Stanovte titr odměrného standardního roztoku dusičnanu stříbrného titrací 5 ml standardního srovnávacího roztoku chloridu
STANOVENÍ CHLORIDŮ Odměrné argentometrické stanovení chloridů podle Mohra Cíl práce Stanovte titr odměrného standardního roztoku dusičnanu stříbrného titrací 5 ml standardního srovnávacího roztoku chloridu
Základní příklady. 18) Určete velikost úhlu δ, jestliže velikost úhlu α je 27.
 Zákldní příkld 1) Stín věže je dlouhý 55 m stín tče vsoké 1,5 m má v tutéž dou délku 150 cm. Vpočtěte výšku věže. ) Určete měřítko mp, jestliže odélníkové pole o rozměrech 600 m 450 m je n mpě zkresleno
Zákldní příkld 1) Stín věže je dlouhý 55 m stín tče vsoké 1,5 m má v tutéž dou délku 150 cm. Vpočtěte výšku věže. ) Určete měřítko mp, jestliže odélníkové pole o rozměrech 600 m 450 m je n mpě zkresleno
Složení soustav (roztoky, koncentrace látkového množství)
 VZOROVÉ PŘÍKLADY Z CHEMIE A DOPORUČENÁ LITERATURA pro přípravu k přijímací zkoušce studijnímu oboru Nanotechnologie na VŠB TU Ostrava Doporučená literatura z chemie: Prakticky jakákoliv celostátní učebnice
VZOROVÉ PŘÍKLADY Z CHEMIE A DOPORUČENÁ LITERATURA pro přípravu k přijímací zkoušce studijnímu oboru Nanotechnologie na VŠB TU Ostrava Doporučená literatura z chemie: Prakticky jakákoliv celostátní učebnice
x + F F x F (x, f(x)).
 I. Funkce dvou více reálných proměnných 8. Implicitně dné funkce. Budeme se zbývt úlohou, kdy funkce není zdná přímo předpisem, který vyjdřuje závislost její hodnoty n hodnotách proměnných. Jeden z možných
I. Funkce dvou více reálných proměnných 8. Implicitně dné funkce. Budeme se zbývt úlohou, kdy funkce není zdná přímo předpisem, který vyjdřuje závislost její hodnoty n hodnotách proměnných. Jeden z možných
PŘIJÍMACÍ ZKOUŠKY 2017 Učitelství chemie čas na vypracování: 60 minut Zakroužkujte zvolenou odpověď. Pouze 1 možnost je správná.
 AUTORSKÉ ŘEŠENÍ (mx. 60 oů) PŘIJÍMACÍ ZKOUŠKY 2017 oor: Učitelství hemie čs n vyprování: 60 minut Zkroužkujte zvolenou opověď. Pouze 1 možnost je správná. Vyerte skupinu prvků, které jsou seřzeny le rostouí
AUTORSKÉ ŘEŠENÍ (mx. 60 oů) PŘIJÍMACÍ ZKOUŠKY 2017 oor: Učitelství hemie čs n vyprování: 60 minut Zkroužkujte zvolenou opověď. Pouze 1 možnost je správná. Vyerte skupinu prvků, které jsou seřzeny le rostouí
Repetitorium chemie X
 Repetitorium chemie X Užitečné rovnováhy v roztocích elektrolytů: znovu o ph, co jsou pufry, rozpustnost, omezeně rozpustné soli a směšné pravidlo, a tklivá historie o rozpůlení dcery hostinské (2016)
Repetitorium chemie X Užitečné rovnováhy v roztocích elektrolytů: znovu o ph, co jsou pufry, rozpustnost, omezeně rozpustné soli a směšné pravidlo, a tklivá historie o rozpůlení dcery hostinské (2016)
3 Acidobazické reakce
 3 Acidobazické reakce Brønstedova teorie 1. Uveďte explicitní definice podle Brønstedovy teorie. Kyselina je... Báze je... Konjugovaný pár je... 2. Doplňte tabulku a pojmenujte všechny sloučeniny. Kyselina
3 Acidobazické reakce Brønstedova teorie 1. Uveďte explicitní definice podle Brønstedovy teorie. Kyselina je... Báze je... Konjugovaný pár je... 2. Doplňte tabulku a pojmenujte všechny sloučeniny. Kyselina
M A = M k1 + M k2 = 3M k1 = 2400 Nm. (2)
 5.3 Řešené příkldy Příkld 1: U prutu kruhového průřezu o průměrech d d b, který je ztížen kroutícími momenty M k1 M k2 (M k2 = 2M k1 ), viz obr. 1, vypočítejte rekční účinek v uložení prutu, vyšetřete
5.3 Řešené příkldy Příkld 1: U prutu kruhového průřezu o průměrech d d b, který je ztížen kroutícími momenty M k1 M k2 (M k2 = 2M k1 ), viz obr. 1, vypočítejte rekční účinek v uložení prutu, vyšetřete
6. a 7. března Úloha 1.1. Vypočtěte obsah obrazce ohraničeného parabolou y = 1 x 2 a osou x.
 KMA/MAT Přednášk cvičení č. 4, Určitý integrál 6. 7. březn 17 1 Aplikce určitého integrálu 1.1 Počáteční úvhy o výpočtu obshu geometrických útvrů v rovině Úloh 1.1. Vypočtěte obsh obrzce ohrničeného prbolou
KMA/MAT Přednášk cvičení č. 4, Určitý integrál 6. 7. březn 17 1 Aplikce určitého integrálu 1.1 Počáteční úvhy o výpočtu obshu geometrických útvrů v rovině Úloh 1.1. Vypočtěte obsh obrzce ohrničeného prbolou
REAKČNÍ KINETIKA 1. ZÁKLADNÍ POJMY. α, ß jsou dílčí reakční řády, α je dílčí reakční řád vzhledem ke složce A, ß vzhledem ke složce
 REKČNÍ KINETIK - zabývá se ryhlosí hemikýh reakí ZÁKLDNÍ POJMY Definie reakční ryhlosi v - pro reake probíhajíí za konsanního objemu v dξ di v V d ν d i [] moldm 3 s Ryhlosní rovnie obeně vyjadřuje vzah
REKČNÍ KINETIK - zabývá se ryhlosí hemikýh reakí ZÁKLDNÍ POJMY Definie reakční ryhlosi v - pro reake probíhajíí za konsanního objemu v dξ di v V d ν d i [] moldm 3 s Ryhlosní rovnie obeně vyjadřuje vzah
Acidobazické reakce. 1. Arrheniova teorie. 2. Neutralizace
 Acidobazické reakce 1. Arrheniova teorie Kyseliny látky schopné ve vodných roztocích odštěpit H + např: HCl H + + Cl -, obecně HB H + + B - Zásady látky schopné ve vodných roztocích poskytovat OH - např.
Acidobazické reakce 1. Arrheniova teorie Kyseliny látky schopné ve vodných roztocích odštěpit H + např: HCl H + + Cl -, obecně HB H + + B - Zásady látky schopné ve vodných roztocích poskytovat OH - např.
SLOŽENÁ NAMÁHÁNÍ SLOŽENÁ NAMÁHÁNÍ
 h Předmět: Ročník: Vytvořil: Dtum: MECHANIKA DRUHÝ ŠČERBOVÁ M. PAVELKA V. 11. SRPNA 2013 Název zprcovného celku: SLOŽENÁ NAMÁHÁNÍ SLOŽENÁ NAMÁHÁNÍ Ke sloţenému nmáhání dojde tehdy, vyskytnou-li se součsně
h Předmět: Ročník: Vytvořil: Dtum: MECHANIKA DRUHÝ ŠČERBOVÁ M. PAVELKA V. 11. SRPNA 2013 Název zprcovného celku: SLOŽENÁ NAMÁHÁNÍ SLOŽENÁ NAMÁHÁNÍ Ke sloţenému nmáhání dojde tehdy, vyskytnou-li se součsně
Vzorová řešení čtvrté série úloh
 FYZIKÁLNÍ SEKCE Přírodovědecká fkult Msrykovy univerzity v Brně KORESPONDENČNÍ SEMINÁŘ Z FYZIKY 8. ročník 001/00 Vzorová řešení čtvrté série úloh (5 bodů) Vzorové řešení úlohy č. 1 (8 bodů) Volný pád Měsíce
FYZIKÁLNÍ SEKCE Přírodovědecká fkult Msrykovy univerzity v Brně KORESPONDENČNÍ SEMINÁŘ Z FYZIKY 8. ročník 001/00 Vzorová řešení čtvrté série úloh (5 bodů) Vzorové řešení úlohy č. 1 (8 bodů) Volný pád Měsíce
třecí síla (tečná vazba podložky) F normálová reakce podložky výsledná reakce podložky Podmínky rovnováhy:
 SPŠ VOŠ KLADO SAIKA - PASIVÍ ODPORY PASIVÍ ODPORY Při vzájemném pohybu těles vznikjí v reálných vzbách psivní odpory, jejichž práce se mění v teplo. Psivní odpory předstvují ztráty, které snižují účinnost
SPŠ VOŠ KLADO SAIKA - PASIVÍ ODPORY PASIVÍ ODPORY Při vzájemném pohybu těles vznikjí v reálných vzbách psivní odpory, jejichž práce se mění v teplo. Psivní odpory předstvují ztráty, které snižují účinnost
ŘEŠENÍ. PÍSEMNÁ ČÁST PŘIJÍMACÍ ZKOUŠKY Z CHEMIE Bakalářský studijní obor Bioorganická chemie a chemická biologie 2016
 ŘEŠENÍ Kód uchazeče.. Datum.. PÍSEMNÁ ČÁST PŘIJÍMACÍ ZKOUŠKY Z CHEMIE Bakalářský studijní obor Bioorganická chemie a chemická biologie 016 1 otázek Maximum 60 bodů Při výběru z několika možností je jen
ŘEŠENÍ Kód uchazeče.. Datum.. PÍSEMNÁ ČÁST PŘIJÍMACÍ ZKOUŠKY Z CHEMIE Bakalářský studijní obor Bioorganická chemie a chemická biologie 016 1 otázek Maximum 60 bodů Při výběru z několika možností je jen
Otázky ke zkoušce z obecné chemie (Prof. RNDr. Karel Procházka, DrSc.)
 Otázky ke zkoušce z obecné chemie (Prof. RNDr. Karel Procházka, DrSc.) Na ústní zkoušku se může přihlásit student, který má zápočet ze cvičení a úspěšně složenou zkouškovou písemku. Na ústní zkoušku se
Otázky ke zkoušce z obecné chemie (Prof. RNDr. Karel Procházka, DrSc.) Na ústní zkoušku se může přihlásit student, který má zápočet ze cvičení a úspěšně složenou zkouškovou písemku. Na ústní zkoušku se
Kurz 1 Úvod k biochemickému praktiku
 Kurz 1 Úvod k biochemickému praktiku Pavla Balínová http://vyuka.lf3.cuni.cz/ Důležité informace Kroužkový asistent: RNDr. Pavla Balínová e-mailová adresa: pavla.balinova@lf3.cuni.cz místnost: 410 studijní
Kurz 1 Úvod k biochemickému praktiku Pavla Balínová http://vyuka.lf3.cuni.cz/ Důležité informace Kroužkový asistent: RNDr. Pavla Balínová e-mailová adresa: pavla.balinova@lf3.cuni.cz místnost: 410 studijní
Ústřední komise Chemické olympiády. 55. ročník 2018/2019 TEST ŠKOLNÍHO KOLA. Kategorie E ŘEŠENÍ
 Ústřední komise Chemické olympiády 55. ročník 2018/2019 TEST ŠKOLNÍHO KOLA Kategorie E ŘEŠENÍ ANORGANICKÁ CHEMIE 16 BODŮ Úloha 1 Vlastnosti sloučenin manganu a chromu 8 bodů 1) Elektronová konfigurace:
Ústřední komise Chemické olympiády 55. ročník 2018/2019 TEST ŠKOLNÍHO KOLA Kategorie E ŘEŠENÍ ANORGANICKÁ CHEMIE 16 BODŮ Úloha 1 Vlastnosti sloučenin manganu a chromu 8 bodů 1) Elektronová konfigurace:
Vypočtěte, kolikaprocentní roztok hydroxidu sodného vznikne přidáním 700 g vody do 2,2 kg 80%ního roztoku hydroxidu.
 Kolik g bromidu sodného potřebujeme na přípravu pěti litrů roztoku této látky o molární koncentraci 0,20 mol/l? Ar: Na 23; Br 80 NaBr; V = 5 l; c = 0,20 mol/l c = n/v n = m/m c = m / (M. V).m = c M V MNaBr
Kolik g bromidu sodného potřebujeme na přípravu pěti litrů roztoku této látky o molární koncentraci 0,20 mol/l? Ar: Na 23; Br 80 NaBr; V = 5 l; c = 0,20 mol/l c = n/v n = m/m c = m / (M. V).m = c M V MNaBr
Název: Chemická rovnováha II
 Název: Chemicá rovnováha II Autor: Mgr. Štěpán Miča Název šoly: Gymnázium Jana Nerudy, šola hl. města Prahy Předmět, mezipředmětové vztahy: chemie, fyzia Roční: 6. Tématicý cele: Chemicá rovnováha (fyziální
Název: Chemicá rovnováha II Autor: Mgr. Štěpán Miča Název šoly: Gymnázium Jana Nerudy, šola hl. města Prahy Předmět, mezipředmětové vztahy: chemie, fyzia Roční: 6. Tématicý cele: Chemicá rovnováha (fyziální
PÍSEMNÁ ČÁST PŘIJÍMACÍ ZKOUŠKY Z CHEMIE Bakalářský studijní obor Bioorganická chemie a chemická biologie 2016
 Kód uchazeče.. Datum.. PÍSEMNÁ ČÁST PŘIJÍMACÍ ZKOUŠKY Z CHEMIE Bakalářský studijní obor Bioorganická chemie a chemická biologie 016 1 otázek Maximum 60 bodů Při výběru z několika možností je jen jedna
Kód uchazeče.. Datum.. PÍSEMNÁ ČÁST PŘIJÍMACÍ ZKOUŠKY Z CHEMIE Bakalářský studijní obor Bioorganická chemie a chemická biologie 016 1 otázek Maximum 60 bodů Při výběru z několika možností je jen jedna
Matematické metody v kartografii
 Mtemtické metody v krtogrfii. Přednášk Referenční elipsoid zákldní vzthy. Poloměry křivosti. Délky poledníkového rovnoběžkového oblouku. 1. Zákldní vzthy n rotčním elipoidu Rotční elipsoid dán následujícími
Mtemtické metody v krtogrfii. Přednášk Referenční elipsoid zákldní vzthy. Poloměry křivosti. Délky poledníkového rovnoběžkového oblouku. 1. Zákldní vzthy n rotčním elipoidu Rotční elipsoid dán následujícími
DOPLŇKOVÝ STUDIJNÍ MATERIÁL CHEMICKÉ VÝPOČTY. Zuzana Špalková. Věra Vyskočilová
 DOPLŇKOVÝ STUDIJNÍ MATERIÁL CHEMICKÉ VÝPOČTY Zuzana Špalková Věra Vyskočilová BRNO 2014 Doplňkový studijní materiál zaměřený na Chemické výpočty byl vytvořen v rámci projektu Interní vzdělávací agentury
DOPLŇKOVÝ STUDIJNÍ MATERIÁL CHEMICKÉ VÝPOČTY Zuzana Špalková Věra Vyskočilová BRNO 2014 Doplňkový studijní materiál zaměřený na Chemické výpočty byl vytvořen v rámci projektu Interní vzdělávací agentury
 ý ů č č Í ď ř č ý ř ý č č ď č ř ý ř ó Í ř č ď ď ř ů ý ý Š ř ďý ř Ž č č ý ř ý ř ř ý ý čř ď É Ř Ě ý č ů ř ď č č ř ý ř ý č č ý č ř ď ř ů ý ř ř č ř ď ď ď ý ý č ď ů ů ů ř ď ď ř č č ý č ď ř ď ý ý ý ď ů ř ř ď
ý ů č č Í ď ř č ý ř ý č č ď č ř ý ř ó Í ř č ď ď ř ů ý ý Š ř ďý ř Ž č č ý ř ý ř ř ý ý čř ď É Ř Ě ý č ů ř ď č č ř ý ř ý č č ý č ř ď ř ů ý ř ř č ř ď ď ď ý ý č ď ů ů ů ř ď ď ř č č ý č ď ř ď ý ý ý ď ů ř ř ď
Kyseliny. Gerber - Jabir ibn Hayyan ( ) Chemická látka produkovaná na světě v největším množství za rok: H 2 SO 4
 Kyseliny Gerber - Jabir ibn Hayyan (721-815) Andreas Libau (Libavius) (1540-1616) Gerber - příprava z H 2 SO 4 a solí: HNO 3, HCl a aqua regia, izolace kyseliny citronové, octové a vinné Libavius - příprava
Kyseliny Gerber - Jabir ibn Hayyan (721-815) Andreas Libau (Libavius) (1540-1616) Gerber - příprava z H 2 SO 4 a solí: HNO 3, HCl a aqua regia, izolace kyseliny citronové, octové a vinné Libavius - příprava
KONTROLNÍ TEST ŠKOLNÍHO KOLA (70 BODŮ)
 KONTROLNÍ TEST ŠKOLNÍHO KOLA (70 BODŮ) Úloha 1 Ic), IIa), IIId), IVb) za každé správné přiřazení po 1 bodu; celkem Úloha 2 8 bodů 1. Sodík reaguje s vodou za vzniku hydroxidu sodného a dalšího produktu.
KONTROLNÍ TEST ŠKOLNÍHO KOLA (70 BODŮ) Úloha 1 Ic), IIa), IIId), IVb) za každé správné přiřazení po 1 bodu; celkem Úloha 2 8 bodů 1. Sodík reaguje s vodou za vzniku hydroxidu sodného a dalšího produktu.
3. ROVNICE A NEROVNICE 85. 3.1. Lineární rovnice 85. 3.2. Kvadratické rovnice 86. 3.3. Rovnice s absolutní hodnotou 88. 3.4. Iracionální rovnice 90
 ROVNICE A NEROVNICE 8 Lineární rovnice 8 Kvdrtické rovnice 8 Rovnice s bsolutní hodnotou 88 Ircionální rovnice 90 Eponenciální rovnice 9 Logritmické rovnice 9 7 Goniometrické rovnice 98 8 Nerovnice 0 Úlohy
ROVNICE A NEROVNICE 8 Lineární rovnice 8 Kvdrtické rovnice 8 Rovnice s bsolutní hodnotou 88 Ircionální rovnice 90 Eponenciální rovnice 9 Logritmické rovnice 9 7 Goniometrické rovnice 98 8 Nerovnice 0 Úlohy

