Kvantová mechanika - model téměř volných elektronů. model těsné vazby
|
|
|
- Jana Marešová
- před 6 lety
- Počet zobrazení:
Transkript
1 Kvantová mechanika - model téměř volných elektronů model těsné vazby
2 Částice (elektron) v periodickém potenciálu- Blochův teorém Dále už nebudeme považovat elektron za zcela volný (Sommerfeld), ale připustíme vliv atomů tvořících strukturu krystalu na stav elektronu. Translační symetrie krystalu T = n a + n 2 a 2 +n 3 a 3 n i a j celá čísla nekomplanární vektory vede k tomu, že i potenciál libovolné částice v tomto krystalu je periodický V T + r = V r tato periodicita (ať už má jakýkoliv průběh) dovoluje vyjádřit potenciál ve formě Fourierovy řady G jsou vektory rozměrově i významově identické s vlnovým vektorem!!! V r = G V G e i G r V G jsou Fourierovy koeficienty = 2π λ i x u t = Ae
3 Z předchozích dvou rovnic (vlnový charakter +peridicita) vyplývá (srovnej s řešením elastických vln v pevné látce) e i G T = G T = 2π(z) i x u t = Ae Ae i r i T+ r = Ae 2π nebo jeho z-násobky G = m A + m 2 A 2 +m 3 A 3 musí existovat takové, že G je vektor tzv. reciproké mřížky (srovnej s ) a j A k = 2πδ jk δ jk je Kroneckerovo delta = pro j=k Složky reálného. reciprokého vektoru =0 pro j k xistence periodické reálné mřížky rovněž znamená existenci reciproké mřížky. V 3 = A A 2 A 3 m 3 Porovnej s axiomem kvantové mechaniky u Sommerfeldova modelu. Brillouinova zóna Vektory A k jsou primitivní translační vektory reciproké mřížky. Vektory G jsou vlastně povolené vlnové vektory částic (elektronů) v krystalu, můžeme chápat jako jejich kvantová čísla.
4 Ukázka aproximace pilovitého průběhu součtem pěti harmonických funkcí Periodic_identity_function.gif Z vln z ranku G se tvoří periodický potenciál. V r = V G e i G r G
5 .Brilouinova zóna obsahuje veškeré informace o povolených stavech částice v krystalu! xistence periodické reciproké mříže si však vynucuje existenci N disperzních závislostí () místo jedné. Vždy, když přičteme další G, vznikne nová - stejná. N je počet elementárních buněk (cel) Vlnové funkce φ r popisující pohyb částic v krystalu musí reflektovat periodicitu mříže Pro vlnu φ r = ei r ωt -G 0 G 2G + aplikace cyklických podmínek (Born von Karman) Porovnej s řešením elastických vln φ r + N j a j = φ r T = n a + n 2 a 2 +n 3 a 3 SLOVY: Ve zvoleném místě elementární buňky musí být vlna stejná (co velikosti i fáze) v kterékoli elementární buňce N krystalu ve kterémkoli směru j. N N 2 N 3 = N = počet primitivních cel j = 3 j = j =,2,3 j = 2
6 φ r + N j a j = φ r e in j a j = Pro j =,2,3 Máme tedy povolené hodnoty : = 3 mj j= N j A j j =,2,3 jsou složky vektoru Vždy, když změníme m j o jednotku, generujeme nový stav pro částici, nové kvantové číslo. Velkost N j a A j jsou jednoznačně určeny velikostí krystalu, stejně jako e i G T = ( G = m A + m 2 A 2 +m 3 A 3 ) m j jsou celá čísla Každá Brilouinova zóna obsahuje tolik stavů, kolik je elementárních buněk v krystalu. Objem -prostoru připadající na jeden stav je A N A 2 N 2 A 3 N 3 = N A A 2 A 3 = V 3 N
7 Schrödigerova rovnice částice v periodickém potenciálu Hψ = ħ2 2 2m + V r ψ = ψ V r = V G e i G r Vlnová funkce ψ musí splňovat cyklické podmínky (Born von Karman) G ψ r = i r C e kde = j m j N j A j k ħ 2 2 2m C e i r + G V G e i G r i r C e = i r C e Bloch ukázal, že řešením Hamiltonianu jsou takové vlnové funkce, jejichž koeficienty jsou C, kde = G a je vlnový vektor spadající pouze do. Brilouinovy zóny. Tyto koeficienty C určují tvar vlnové funkce. algebraická manipulace Musí to být vlny spadající do spektra krystalové mříže
8 ψ r = C e i r ψ r = G C G ei G r ψ r = e i r G C G ei G r (Blochova funkce) ψ r = Rovinná vlna v rámci.b.z. funkce s periodicitou reciproké mříže To lze vyjádřit rovněž ve formě ψ r + T = e i T ψ r Vyjadřuje periodicitu Blochův teorém Schrödigerova rovnice se řeší typicky pro dva krajní případy ) model téměř volných elektronů 2) model těsné vazby
9 Hψ = ħ2 2 ) Model téměř volných elektronů Valenční elektrony se téměř neváží na ionty atomové mříže jejich potenciál v poli iontů je malý. Vhodný pro popis pásů s velkým překryvem původních atomových orbitalů mělčí pásy. disperzní závislost Pro 2m + V r ψ = ψ V r 0 G = ħ2 G 2 ψ = Ce i G r Hψ = ψ 2m se vracíme k modelu volných elektronů. Až na to, že na hranici. BZ, tam kde se kříží jednotlivé disperzní závislosti () dochází k deformaci a vzniku energetických gapů. Dochází zde k superpozici / interferenci vlnových funkcí elektronů. -G 0 G 2G Degenerace stavů
10 Superpozice vln (vede k největšímu štěpení pro = 2 G) ψ = C G e i G r ψ 2 = C G 2 e i G 2 r -G 0 G 2G Hustota pravděpodobnosti superponovaných vln ψ ± 2 = ψ ± ψ 2 2 C G x = C Stojaté vlny s periodicitou mříže ψ 2 + = ψ + ψ 2 2 = 2 C 2 + cos G G 2 r ψ 2 = ψ ψ 2 2 = 2 C 2 cos G G 2 r vzniku energetických gapů = zakázané pásy energie vazebný π protivazebný
11 Závěry plynoucí z modelu téměř volných elektronů ) Pro elektrony s vlnovými vektory vzdálenými od hranic.bz máme disperzi podobnou disperzi téměř volného elektronu. 2) Zejména poblíž hranic. BZ vznikají zakázané pásy energií v důsledku superpozice vln. 3) lektron, který by měl příliš velké přechází na vyšší energetickou hladinu
12 2) Model pevně vázaných elektronů Valenční elektrony se váží na ionty atomové mříže, takže jejich pohyb je silně omezen-jsou lokalizovány. Vhodný pro popis pásů s malým překryvem původních atomových orbitalů hlubší pásy. Blochův teorém ψ r + T = e it ψ r ψ r = T e it φ j r T Blochovu funkci volíme jako lineární kombinaci vlnových funkcí φ j atomových orbitalů (pouze valenčních), tato funkce je lokalizována na atomu má krátký dosah ψ r splňuje Blochovu podmínku a zároveň si zachovává atomový charakter energetických hladin
13 Hamiltonian Model pevně vázaných elektronů H = H atom + V r V 0 r Hψ = ψ V r je průměrný potenciál v krystalu v důsledku všech atomů V 0 r je potenciál spojený s izolovaným atomem ψ r = T e it φ j r T H atom T e it φ j r T + V r V 0 r T e it φ j r T = = T e it φ j r T To nám dovolí nalézt disperzní závislost
14 H atom e it φ j r T + V r V 0 r e it φ j r T = e it φ j r T T T T disperzní závislost Vynásobíme φ j a integrujeme přes všechna r. Při integraci přispívají jen nejbližší sousedé = φ B 2t x cos x a 2t y cos y b 2t z cos z c t x, t y, t z jsou transferové integrály (TI), které charakterizují (jsou úměrné) velikost překryvu atomových orbitalů a zároveň, jak snadno může elektron přecházet z atomu na atom. φ je energie lokalizace elektronu na atomovém orbitalu c a b T = a, b, c B je energie spojená s průměrným potenciálem v krystalu v důsledku přítomnosti všech atomů
15 V r r Pásy, každý s N hodnotami k atom N atomů, elementárních buněk ) TI jsou mírou energetické šířky pásu čím menší, tím užší 2) fektivní hmotnost volného nositele je nepřímo úměrná TI 3) Tvar pásů je určen a) reálnou strukturou, která určuje překryvy v daných směrech grafit diamant b) druhem atomu (druh orbitalů a jejich energetické uspořádání) C Si Ge
16 Brilouinova zóna - konstrukce Krystalová struktura je invariantní vůči translaci v reálném prostoru o T = n a + n 2 a 2 +n 3 a 3 r = r, + T Bazální vektory v reálné (přímé) mřížce a = a a 2 = a a 3 = a Bazální vektory reciproké mřížky G = m A + m 2 A 2 + m 3 A 3 obdržíme inverzí matice reprezentace příslušné přímé mřížky 00 A x A 2x A 3x A y A 2y A 3y A z A 2z A 3z T = 2π a x a 2x a 3x a y a 2y a 3y a z a 2z a 3z A 3 A A = 2π a 0 A 2 = 2π a 0 A 3 = 2π a 0 00 A 2 00
17 Brilouinova zóna = Wiegner-Seitzova buňka reciproké mřížky Pásová struktura Význačné body Oblast která rozhoduje o vlastnostech
18 Disperzní závislost můžeme rozvést do Taylorovy řady = 0 + =0 2 k + 2 =0 První derivace pro minimum u =0 je rovna 0 Parabolické přiblížení 2 + Malá koncentrace elektronů v pásu Díry kde = 0 + ħ2 2 2m m = 2 ħ 2 2 elektrony Velká koncentrace elektronů v pásu Neparabolicita - složité struktury (d a f prvky) -vysoké koncentrace -vysoká pole,
19 Charakteristiky pásové struktury společné ) i 2) První derivace =0 pro minimum/maximum (=0) je rovna 0 V okolí minim/maxim) jsou pásy parabolické ( cos a a 2 2 ) Pravda leží mezi ) i 2)
20 Obecné pojmy popisující elektron v pásu Vlnový vektor elektronu lze chápat jako kvantové číslo popisující stav elektronu v krystalu / ħ je hybnost systému elektronů jako celku, ne jednotlivého elektronu. Jelikož popisujeme elektron jako vlnu, lze užít pojmu grupové rychlosti. Ta vyjadřuje rychlost pohybu elektronu v daném stavu. = 0 + ħ2 2 Síla F působící na elektron: 2m v = ħ v = dω d d d = ħ F = ħ d dt d = Fvdt
21 hmotnost elektronu m v pásu se může odlišovat od hmotnosti elektronu volného a muže být i záporná (díra). F = ħ d dt = m dv dt dv dt = ħ d 2 d d 2 dt v = ħ d d m = d 2 ħ 2 d 2 elektrony + Díry - Pro parabolický pás bude konstantní Nemluvíme o kladné a záporné hmotnosti, ale o elektronu a díře
22 fektivní hmotnost parametrizace pásu g d = 2π 2 (4/3) 2m ħ d Hustota stavů úzce souvisí s efektivní hmotností VNP. fektivní hmotnost tedy vyjadřuje zároveň hustotu stavů: velká hmotnost = velká hustota Rozptyl elektronů Blochův přístup Jelikož se elektron chová v krystalu jako vlna, v přísně periodickém prostředí se jeho stav nebude měnit. Nebude existovat žádný rozptyl díky konstruktivní interferenci. Destruktivní interference nebude existovat. Rozptyl přinese až ne-periodicita způsobená teplotou, příměsemi, atd.
23 Rozptyl elektronů = konečná vodivost Jelikož se elektron chová v krystalu jako vlna, jeho rychlostí je grupová rychlost. Při působení vnější síly se může měnit pohybový stav elektronu tak, že jeho zrychlení mění během působení síly svoje znaménko. Bez přítomnosti rozptylu by se tak elektrická vodivost blížila nule. = 0 2tcos a F = ħ d dt = e v = ħ m = d d = 2ta sin a ħ ħ2 2 2 = x = 2t e = cos ħ 2 2ta 2 cos a aet ħ t = e ħ t t
Fyzika IV. -ezv -e(z-zv) kov: valenční elektrony vodivostní elektrony. Elektronová struktura pevných látek model volných elektronů
 Elektronová struktura pevných látek model volných elektronů 1897: J.J. Thomson - elektron jako částice 1900: P. Drude: kinetická teorie plynů - kov jako plyn elektronů Drudeho model elektrony se mezi srážkami
Elektronová struktura pevných látek model volných elektronů 1897: J.J. Thomson - elektron jako částice 1900: P. Drude: kinetická teorie plynů - kov jako plyn elektronů Drudeho model elektrony se mezi srážkami
Fyzika IV. g( ) Vibrace jader atomů v krystalové mříži
 Vibrace jader atomů v krystalové mříži v krystalu máme N základních buněk, v každé buňce s atomů, které kmitají kolem rovnovážných poloh výchylky kmitů jsou malé (Taylorův rozvoj): harmonická aproximace
Vibrace jader atomů v krystalové mříži v krystalu máme N základních buněk, v každé buňce s atomů, které kmitají kolem rovnovážných poloh výchylky kmitů jsou malé (Taylorův rozvoj): harmonická aproximace
Vibrace atomů v mřížce, tepelná kapacita pevných látek
 Vibrace atomů v mřížce, tepelná kapacita pevných látek Atomy vázané v mřížce nejsou v klidu. Míru jejich pohybu vyjadřuje podobně jako u plynů a kapalin teplota. - Elastické vlny v kontinuu neatomární
Vibrace atomů v mřížce, tepelná kapacita pevných látek Atomy vázané v mřížce nejsou v klidu. Míru jejich pohybu vyjadřuje podobně jako u plynů a kapalin teplota. - Elastické vlny v kontinuu neatomární
Kovy - model volných elektronů
 Kovy - model volných elektronů Kovová vazba 1. Preferuje ji většina prvků vyskytujících se v přírodě. Kov je tvořen kladně nabitými ionty (s konfigurací vzácného plynu) a relativně velmi volnými elektrony.
Kovy - model volných elektronů Kovová vazba 1. Preferuje ji většina prvků vyskytujících se v přírodě. Kov je tvořen kladně nabitými ionty (s konfigurací vzácného plynu) a relativně velmi volnými elektrony.
Kvantová fyzika pevných látek
 Kvantová fyzika pevných látek Přednáška 2: Základy krystalografie Pavel Márton 30. října 2013 Pavel Márton () Kvantová fyzika pevných látek Přednáška 2: Základy krystalografie 30. října 2013 1 / 10 Pavel
Kvantová fyzika pevných látek Přednáška 2: Základy krystalografie Pavel Márton 30. října 2013 Pavel Márton () Kvantová fyzika pevných látek Přednáška 2: Základy krystalografie 30. října 2013 1 / 10 Pavel
elektrony v pevné látce verze 1. prosince 2016
 F6122 Základy fyziky pevných látek seminář elektrony v pevné látce verze 1. prosince 2016 1 Drudeho model volných elektronů 1 1.1 Mathiessenovo pravidlo............................................... 1
F6122 Základy fyziky pevných látek seminář elektrony v pevné látce verze 1. prosince 2016 1 Drudeho model volných elektronů 1 1.1 Mathiessenovo pravidlo............................................... 1
1. Kvantové jámy. Tabulka 1: Efektivní hmotnosti nosičů v krystalech GaAs, AlAs, v jednotkách hmotnosti volného elektronu m o.
 . Kvantové jámy Pokročilé metody růstu krystalů po jednotlivých vrstvách (jako MBE) dovolují vytvořit si v krystalu libovolný potenciál. Jeden z hojně používaných materiálů je: GaAs, AlAs a jejich ternární
. Kvantové jámy Pokročilé metody růstu krystalů po jednotlivých vrstvách (jako MBE) dovolují vytvořit si v krystalu libovolný potenciál. Jeden z hojně používaných materiálů je: GaAs, AlAs a jejich ternární
Fourierovské metody v teorii difrakce a ve strukturní analýze
 Osnova přednášky na 31 kolokviu Krystalografické společnosti Výpočetní metody v rtg a neutronové strukturní analýze Nové Hrady, 16 20 6 2003 Fourierovské metody v teorii difrakce a ve strukturní analýze
Osnova přednášky na 31 kolokviu Krystalografické společnosti Výpočetní metody v rtg a neutronové strukturní analýze Nové Hrady, 16 20 6 2003 Fourierovské metody v teorii difrakce a ve strukturní analýze
nano.tul.cz Inovace a rozvoj studia nanomateriálů na TUL
 Inovace a rozvoj studia nanomateriálů na TUL nano.tul.cz Tyto materiály byly vytvořeny v rámci projektu ESF OP VK: Inovace a rozvoj studia nanomateriálů na Technické univerzitě v Liberci Optické vlastnosti
Inovace a rozvoj studia nanomateriálů na TUL nano.tul.cz Tyto materiály byly vytvořeny v rámci projektu ESF OP VK: Inovace a rozvoj studia nanomateriálů na Technické univerzitě v Liberci Optické vlastnosti
Od kvantové mechaniky k chemii
 Od kvantové mechaniky k chemii Jan Řezáč UOCHB AV ČR 19. září 2017 Jan Řezáč (UOCHB AV ČR) Od kvantové mechaniky k chemii 19. září 2017 1 / 33 Úvod Vztah mezi molekulovou strukturou a makroskopickými vlastnostmi
Od kvantové mechaniky k chemii Jan Řezáč UOCHB AV ČR 19. září 2017 Jan Řezáč (UOCHB AV ČR) Od kvantové mechaniky k chemii 19. září 2017 1 / 33 Úvod Vztah mezi molekulovou strukturou a makroskopickými vlastnostmi
6 Potenciály s δ funkcemi II
 6 Potenciály s δ funkcemi II 6.1 Periodická δ funkce (Diracův hřeben) Částice o hmotnosti M se pohybuje v jednorozměrné mřížce popsané periodickým potenciálem V(x) = c δ(x na), (6.1.1) n= kde a je vzdálenost
6 Potenciály s δ funkcemi II 6.1 Periodická δ funkce (Diracův hřeben) Částice o hmotnosti M se pohybuje v jednorozměrné mřížce popsané periodickým potenciálem V(x) = c δ(x na), (6.1.1) n= kde a je vzdálenost
Vlastnosti pevných látek
 Vlastnosti pevných látek fyzikální vlastnost: odezva na určitý podnět, fyzikální rovnice definuje vztah mezi nimi (fyzikální veličiny skaláry, vektory, tenzory) Příklad: elastická deformace izotropního
Vlastnosti pevných látek fyzikální vlastnost: odezva na určitý podnět, fyzikální rovnice definuje vztah mezi nimi (fyzikální veličiny skaláry, vektory, tenzory) Příklad: elastická deformace izotropního
E g IZOLANT POLOVODIČ KOV. Zakázaný pás energií
 Polovodiče To jestli nazýváme danou látku polovodičem, závisí především na jejích vlastnostech ve zvoleném teplotním oboru. Obecně jsou to látky s 0 ev < Eg < ev. KOV POLOVODIČ E g IZOLANT Zakázaný pás
Polovodiče To jestli nazýváme danou látku polovodičem, závisí především na jejích vlastnostech ve zvoleném teplotním oboru. Obecně jsou to látky s 0 ev < Eg < ev. KOV POLOVODIČ E g IZOLANT Zakázaný pás
Laserová technika prosince Katedra fyzikální elektroniky.
 Laserová technika 1 Aktivní prostředí Šíření rezonančního záření dvouhladinovým prostředím Jan Šulc Katedra fyzikální elektroniky České vysoké učení technické jan.sulc@fjfi.cvut.cz 22. prosince 2016 Program
Laserová technika 1 Aktivní prostředí Šíření rezonančního záření dvouhladinovým prostředím Jan Šulc Katedra fyzikální elektroniky České vysoké učení technické jan.sulc@fjfi.cvut.cz 22. prosince 2016 Program
Ideální krystalová mřížka periodický potenciál v krystalu. pásová struktura polovodiče
 Cvičení 3 Ideální krystalová mřížka periodický potenciál v krystalu Aplikace kvantové mechaniky pásová struktura polovodiče Nosiče náboje v polovodiči hustota stavů obsazovací funkce, Fermiho hladina koncentrace
Cvičení 3 Ideální krystalová mřížka periodický potenciál v krystalu Aplikace kvantové mechaniky pásová struktura polovodiče Nosiče náboje v polovodiči hustota stavů obsazovací funkce, Fermiho hladina koncentrace
Tepelná vodivost pevných látek
 Tepelná vodivost pevných látek Přenos tepla vedení mřížková část tepelné vodivosti Dvouatomový lineární řetězec přiblížení např. NaCl (1) u -1 (A) u s-1 (B) u (A) u s (B) u s+1 (B) u +1 (A) Např. = příčné
Tepelná vodivost pevných látek Přenos tepla vedení mřížková část tepelné vodivosti Dvouatomový lineární řetězec přiblížení např. NaCl (1) u -1 (A) u s-1 (B) u (A) u s (B) u s+1 (B) u +1 (A) Např. = příčné
Atom vodíku. Nejjednodušší soustava: p + e Řešitelná exaktně. Kulová symetrie. Potenciální energie mezi p + e. e =
 Atom vodíku Nejjednodušší soustava: p + e Řešitelná exaktně Kulová symetrie Potenciální energie mezi p + e V 2 e = 4πε r 0 1 Polární souřadnice využití kulové symetrie atomu Ψ(x,y,z) Ψ(r,θ, φ) x =? y=?
Atom vodíku Nejjednodušší soustava: p + e Řešitelná exaktně Kulová symetrie Potenciální energie mezi p + e V 2 e = 4πε r 0 1 Polární souřadnice využití kulové symetrie atomu Ψ(x,y,z) Ψ(r,θ, φ) x =? y=?
Hamiltonián popisující atom vodíku ve vnějším magnetickém poli:
 Orbitální a spinový magnetický moment a jejich interakce s vnějším polem Vše na příkladu atomu H: Elektron (e - ) a jádro (u atomu H pouze p + ) mají vlastní magnetický moment (= spin). Tyto dva dipóly
Orbitální a spinový magnetický moment a jejich interakce s vnějším polem Vše na příkladu atomu H: Elektron (e - ) a jádro (u atomu H pouze p + ) mají vlastní magnetický moment (= spin). Tyto dva dipóly
Opakování: shrnutí základních poznatků o struktuře atomu
 11. Polovodiče Polovodiče jsou krystalické nebo amorfní látky, jejichž elektrická vodivost leží mezi elektrickou vodivostí kovů a izolantů a závisí na teplotě nebo dopadajícím optickém záření. Elektrické
11. Polovodiče Polovodiče jsou krystalické nebo amorfní látky, jejichž elektrická vodivost leží mezi elektrickou vodivostí kovů a izolantů a závisí na teplotě nebo dopadajícím optickém záření. Elektrické
2. Elektrotechnické materiály
 . Elektrotechnické materiály Předpokladem vhodného využití elektrotechnických materiálů v konstrukci elektrotechnických součástek a zařízení je znalost jejich vlastností. Elektrické vlastnosti materiálů
. Elektrotechnické materiály Předpokladem vhodného využití elektrotechnických materiálů v konstrukci elektrotechnických součástek a zařízení je znalost jejich vlastností. Elektrické vlastnosti materiálů
Vazby v pevných látkách
 Vazby v pevných látkách Hlavní body 1. Tvorba pevných látek 2. Van der Waalsova vazba elektrostatická interakce indukovaných dipólů 3. Iontová vazba elektrostatická interakce iontů 4. Kovalentní vazba
Vazby v pevných látkách Hlavní body 1. Tvorba pevných látek 2. Van der Waalsova vazba elektrostatická interakce indukovaných dipólů 3. Iontová vazba elektrostatická interakce iontů 4. Kovalentní vazba
V nejnižším energetickém stavu valenční elektrony úplně obsazují všechny hladiny ve valenčním pásu, nemohou zprostředkovat vedení proudu.
 POLOVODIČE Vlastní polovodiče Podle typu nosiče náboje dělíme polovodiče na vlastní (intrinsické) a příměsové. Příměsové polovodiče mohou být dopované typu N (majoritními nosiči volného náboje jsou elektrony)
POLOVODIČE Vlastní polovodiče Podle typu nosiče náboje dělíme polovodiče na vlastní (intrinsické) a příměsové. Příměsové polovodiče mohou být dopované typu N (majoritními nosiči volného náboje jsou elektrony)
Úloha 1: Vypočtěte hustotu uhlíku (diamant), křemíku, germania a α-sn (šedý cín) z mřížkové konstanty a hmotnosti jednoho atomu.
 Úloha : Vypočtěte hustotu uhlíku (diamant), křemíku, germania a α-sn (šedý cín) z mřížkové konstanty a hmotnosti jednoho atomu. Všechny zadané prvky mají krystalovou strukturu kub. diamantu. (http://en.wikipedia.org/wiki/diamond_cubic),
Úloha : Vypočtěte hustotu uhlíku (diamant), křemíku, germania a α-sn (šedý cín) z mřížkové konstanty a hmotnosti jednoho atomu. Všechny zadané prvky mají krystalovou strukturu kub. diamantu. (http://en.wikipedia.org/wiki/diamond_cubic),
ω=2π/t, ω=2πf (rad/s) y=y m sin ωt okamžitá výchylka vliv má počáteční fáze ϕ 0
 Kmity základní popis kmitání je periodický pohyb, při kterém těleso pravidelně prochází rovnovážnou polohou mechanický oscilátor zařízení vykonávající kmity Základní veličiny Perioda T [s], frekvence f=1/t
Kmity základní popis kmitání je periodický pohyb, při kterém těleso pravidelně prochází rovnovážnou polohou mechanický oscilátor zařízení vykonávající kmity Základní veličiny Perioda T [s], frekvence f=1/t
Molekuly. Všeobecně známý fakt: atomy se slučujou do molekul, pokud to zrovna nejsou atomy inertních plynů v posledním sloupci periodické tabulky
 Molekuly Všeobecně známý fakt: atomy se slučujou do molekul, pokud to zrovna nejsou atomy inertních plynů v posledním sloupci periodické tabulky Nejjednodušší případ: molekulární iont H +, tj. dva protony
Molekuly Všeobecně známý fakt: atomy se slučujou do molekul, pokud to zrovna nejsou atomy inertních plynů v posledním sloupci periodické tabulky Nejjednodušší případ: molekulární iont H +, tj. dva protony
Elektronová struktura
 Elektronová struktura Přiblížení pohybu elektronů v periodickém potenciálu dokonalého krystalu. Blochůvteorémpak říká, že řešení Schrödingerovy rovnice pro elektron v periodickém potenciálu je ve tvaru
Elektronová struktura Přiblížení pohybu elektronů v periodickém potenciálu dokonalého krystalu. Blochůvteorémpak říká, že řešení Schrödingerovy rovnice pro elektron v periodickém potenciálu je ve tvaru
ATOM VODÍKU MODEL : STOJÍCÍ BODOVÉ JÁDRO A ELEKTRON VZÁJEMNĚ ELEKTROSTATICKY INTERAGUJÍCÍ SCHRÖDINGEROVA ROVNICE PRO PŘÍPAD POTENCIÁLNÍ ENERGIE.
 ATOMY + MOLEKULY ATOM VODÍKU MODEL : STOJÍCÍ BODOVÉ JÁDRO A ELEKTRON VZÁJEMNĚ ELEKTROSTATICKY INTERAGUJÍCÍ SCHRÖDINGEROVA ROVNICE H ˆψ = Eψ PRO PŘÍPAD POTENCIÁLNÍ ENERGIE Vˆ = Ze 2 4πε o r ŘEŠENÍ HLEDÁME
ATOMY + MOLEKULY ATOM VODÍKU MODEL : STOJÍCÍ BODOVÉ JÁDRO A ELEKTRON VZÁJEMNĚ ELEKTROSTATICKY INTERAGUJÍCÍ SCHRÖDINGEROVA ROVNICE H ˆψ = Eψ PRO PŘÍPAD POTENCIÁLNÍ ENERGIE Vˆ = Ze 2 4πε o r ŘEŠENÍ HLEDÁME
Jiří Oswald. Fyzikální ústav AV ČR v.v.i.
 Jiří Oswald Fyzikální ústav AV ČR v.v.i. I. Úvod Polovodiče Zákládní pojmy Kvantově-rozměrový jev II. Luminiscence Si nanokrystalů III. Luminiscence polovodičových nanostruktur A III B V IV. Aplikace Pásová
Jiří Oswald Fyzikální ústav AV ČR v.v.i. I. Úvod Polovodiče Zákládní pojmy Kvantově-rozměrový jev II. Luminiscence Si nanokrystalů III. Luminiscence polovodičových nanostruktur A III B V IV. Aplikace Pásová
České vysoké učení technické v Praze Fakulta jaderná a fyzikálně inženýrská. Příloha formuláře C OKRUHY
 Příloha formuláře C OKRUHY ke státním závěrečným zkouškám BAKALÁŘSKÉ STUDIUM Obor: Studijní program: Aplikace přírodních věd Základy fyziky kondenzovaných látek 1. Vazebné síly v kondenzovaných látkách
Příloha formuláře C OKRUHY ke státním závěrečným zkouškám BAKALÁŘSKÉ STUDIUM Obor: Studijní program: Aplikace přírodních věd Základy fyziky kondenzovaných látek 1. Vazebné síly v kondenzovaných látkách
Krystalografie a strukturní analýza
 Krystalografie a strukturní analýza O čem to dneska bude (a nebo také nebude): trocha historie aneb jak to všechno začalo... jak a čím pozorovat strukturu látek difrakce - tak trochu jiný mikroskop rozptyl
Krystalografie a strukturní analýza O čem to dneska bude (a nebo také nebude): trocha historie aneb jak to všechno začalo... jak a čím pozorovat strukturu látek difrakce - tak trochu jiný mikroskop rozptyl
Elementární částice. 1. Leptony 2. Baryony 3. Bosony. 4. Kvarkový model 5. Slabé interakce 6. Partonový model
 Elementární částice 1. Leptony 2. Baryony 3. Bosony 4. Kvarkový model 5. Slabé interakce 6. Partonový model I.S. Hughes: Elementary Particles M. Leon: Particle Physics W.S.C. Williams Nuclear and Particle
Elementární částice 1. Leptony 2. Baryony 3. Bosony 4. Kvarkový model 5. Slabé interakce 6. Partonový model I.S. Hughes: Elementary Particles M. Leon: Particle Physics W.S.C. Williams Nuclear and Particle
Příklad 1: Komutační relace [d/dx, x] Příklad 2: Operátor B = i d/dx
![Příklad 1: Komutační relace [d/dx, x] Příklad 2: Operátor B = i d/dx Příklad 1: Komutační relace [d/dx, x] Příklad 2: Operátor B = i d/dx](/thumbs/91/106542832.jpg) 1 Příklad 1: Komutační relace [d/, x] Mějme na dva operátory: ˆ d/ a ˆ 5 D X x, například na prvek x působí takto Určeme jejich komutátor ˆ 5 d 5 4 ˆ 5 5 6 D x x 5 x, X x xx x ˆ ˆ ˆ ˆ ˆ ˆ d d [ DX, ] f
1 Příklad 1: Komutační relace [d/, x] Mějme na dva operátory: ˆ d/ a ˆ 5 D X x, například na prvek x působí takto Určeme jejich komutátor ˆ 5 d 5 4 ˆ 5 5 6 D x x 5 x, X x xx x ˆ ˆ ˆ ˆ ˆ ˆ d d [ DX, ] f
Elektronový obal atomu
 Elektronový obal atomu Vlnění o frekvenci v se může chovat jako proud částic (kvant - fotonů) o energii E = h.v Částice pohybující se s hybností p se může chovat jako vlna o vlnové délce λ = h/p Kde h
Elektronový obal atomu Vlnění o frekvenci v se může chovat jako proud částic (kvant - fotonů) o energii E = h.v Částice pohybující se s hybností p se může chovat jako vlna o vlnové délce λ = h/p Kde h
2. Difrakce elektronů na krystalu
 2. Difrakce elektronů na krystalu Interpretace pozorování v TEM faktory ovlivňující interakci e - v krystalu 2 způsoby náhledu na interakci e - s krystalem Rozptyl x difrakce částice x vlna Difrakce odchýlení
2. Difrakce elektronů na krystalu Interpretace pozorování v TEM faktory ovlivňující interakci e - v krystalu 2 způsoby náhledu na interakci e - s krystalem Rozptyl x difrakce částice x vlna Difrakce odchýlení
17 Vlastnosti molekul
 17 Vlastnosti molekul Experimentálně molekuly charakterizujeme pomocí nejrůznějších vlastností: můžeme změřit třeba NMR posuny, elektrické či magnetické parametry či třeba jejich optickou otáčivost. Tyto
17 Vlastnosti molekul Experimentálně molekuly charakterizujeme pomocí nejrůznějších vlastností: můžeme změřit třeba NMR posuny, elektrické či magnetické parametry či třeba jejich optickou otáčivost. Tyto
r W. Shockley, J. Bardeen a W. Brattain, zahájil epochu polovodičové elektroniky, která se rozvíjí dodnes.
 r. 1947 W. Shockley, J. Bardeen a W. Brattain, zahájil epochu polovodičové elektroniky, která se rozvíjí dodnes. 2.2. Polovodiče Lze je definovat jako látku, která má elektronovou bipolární vodivost, tj.
r. 1947 W. Shockley, J. Bardeen a W. Brattain, zahájil epochu polovodičové elektroniky, která se rozvíjí dodnes. 2.2. Polovodiče Lze je definovat jako látku, která má elektronovou bipolární vodivost, tj.
5. Vedení elektrického proudu v polovodičích
 5. Vedení elektrického proudu v polovodičích - zápis výkladu - 26. až 27. hodina - A) Stavba látky a nosiče náboje Atom: základní stavební částice; skládá se z atomového jádra (protony a neutrony) a atomového
5. Vedení elektrického proudu v polovodičích - zápis výkladu - 26. až 27. hodina - A) Stavba látky a nosiče náboje Atom: základní stavební částice; skládá se z atomového jádra (protony a neutrony) a atomového
Matematika I A ukázkový test 1 pro 2011/2012. x + y + 3z = 1 (2a 1)x + (a + 1)y + z = 1 a
 Matematika I A ukázkový test 1 pro 2011/2012 1. Je dána soustava rovnic s parametrem a R x y + z = 1 a) Napište Frobeniovu větu. x + y + 3z = 1 (2a 1)x + (a + 1)y + z = 1 a b) Vyšetřete počet řešení soustavy
Matematika I A ukázkový test 1 pro 2011/2012 1. Je dána soustava rovnic s parametrem a R x y + z = 1 a) Napište Frobeniovu větu. x + y + 3z = 1 (2a 1)x + (a + 1)y + z = 1 a b) Vyšetřete počet řešení soustavy
Molekuly 1 12/4/2011. Molekula definice IUPAC. Molekuly. Proč existují molekuly? Kosselův model. Představy o molekulách
 1/4/011 Molekuly 1 Molekula definice IUPC elektricky neutrální entita sestávající z více nežli jednoho atomu. Přesně, molekula, v níž je počet atomů větší nežli jedna, musí odpovídat snížení na ploše potenciální
1/4/011 Molekuly 1 Molekula definice IUPC elektricky neutrální entita sestávající z více nežli jednoho atomu. Přesně, molekula, v níž je počet atomů větší nežli jedna, musí odpovídat snížení na ploše potenciální
Singulární charakter klasické limity
 Singulární charakter klasické limity obecná speciální Teorie O Teorie S Parametr δ : δ ) O S) O S Pieter Bruegel starší +569) Velké ryby jedí malé ryby 556) obecná speciální Teorie O Teorie S Parametr
Singulární charakter klasické limity obecná speciální Teorie O Teorie S Parametr δ : δ ) O S) O S Pieter Bruegel starší +569) Velké ryby jedí malé ryby 556) obecná speciální Teorie O Teorie S Parametr
ATOMOVÁ SPEKTROMETRIE
 ATOMOVÁ SPEKTROMETRIE Atomová spektrometrie valenčních e - 1. OES (AES). AAS 3. AFS 1 Atomová spektra čárová spektra Tok záření P - množství zářivé energie (Q E ) přenesené od zdroje za jednotku času.
ATOMOVÁ SPEKTROMETRIE Atomová spektrometrie valenčních e - 1. OES (AES). AAS 3. AFS 1 Atomová spektra čárová spektra Tok záření P - množství zářivé energie (Q E ) přenesené od zdroje za jednotku času.
Elektrické vlastnosti pevných látek
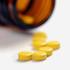 Elektrické vlastnosti pevných látek elektrická vodivost gradient vnějšího elektrického pole vyvolá přenos náboje volnými nositeli (elektrony, díry, ionty) měrná vodivost = e n n e p p [ -1 m -1 ] Kovy
Elektrické vlastnosti pevných látek elektrická vodivost gradient vnějšího elektrického pole vyvolá přenos náboje volnými nositeli (elektrony, díry, ionty) měrná vodivost = e n n e p p [ -1 m -1 ] Kovy
Základní pojmy teorie struktury ideálního krystalu
 Základní pojmy teorie struktury ideálního krystalu Ideální krystal nekonečná velikost a zcela pravidelná struktura 3D skupina elementů = motiv pravidelným opakováním motivu v prostoru (3D translační periodicita)
Základní pojmy teorie struktury ideálního krystalu Ideální krystal nekonečná velikost a zcela pravidelná struktura 3D skupina elementů = motiv pravidelným opakováním motivu v prostoru (3D translační periodicita)
STEJNOSMĚRNÝ PROUD Polovodiče TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY.
 STEJNOSMĚRNÝ PROUD Polovodiče TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY. Polovodiče Mezi polovodiče patří velké množství pevných látek. Často se využívá
STEJNOSMĚRNÝ PROUD Polovodiče TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY. Polovodiče Mezi polovodiče patří velké množství pevných látek. Často se využívá
2.6. Koncentrace elektronů a děr
 Obr. 2-11 Rozložení nosičů při poloze Fermiho hladiny: a) v horní polovině zakázaného pásu (p. typu N), b) uprostřed zakázaného pásu (vlastní p.), c) v dolní polovině zakázaného pásu (p. typu P) 2.6. Koncentrace
Obr. 2-11 Rozložení nosičů při poloze Fermiho hladiny: a) v horní polovině zakázaného pásu (p. typu N), b) uprostřed zakázaného pásu (vlastní p.), c) v dolní polovině zakázaného pásu (p. typu P) 2.6. Koncentrace
12 DYNAMIKA SOUSTAVY HMOTNÝCH BODŮ
 56 12 DYNAMIKA SOUSTAVY HMOTNÝCH BODŮ Těžiště I. impulsová věta - věta o pohybu těžiště II. impulsová věta Zákony zachování v izolované soustavě hmotných bodů Náhrada pohybu skutečných objektů pohybem
56 12 DYNAMIKA SOUSTAVY HMOTNÝCH BODŮ Těžiště I. impulsová věta - věta o pohybu těžiště II. impulsová věta Zákony zachování v izolované soustavě hmotných bodů Náhrada pohybu skutečných objektů pohybem
Úvod do moderní fyziky. lekce 3 stavba a struktura atomu
 Úvod do moderní fyziky lekce 3 stavba a struktura atomu Vývoj představ o stavbě atomu 1904 J. J. Thomson pudinkový model atomu 1909 H. Geiger, E. Marsden experiment s ozařováním zlaté fólie alfa částicemi
Úvod do moderní fyziky lekce 3 stavba a struktura atomu Vývoj představ o stavbě atomu 1904 J. J. Thomson pudinkový model atomu 1909 H. Geiger, E. Marsden experiment s ozařováním zlaté fólie alfa částicemi
Orbitaly, VSEPR 1 / 18
 rbitaly, VSEPR Rezonanční struktury, atomové a molekulové orbitaly, hybridizace, určování tvaru molekuly pomocí teorie VSEPR, úvod do symetrie molekul, dipólový moment 1 / 18 Formální náboj Rozdíl mezi
rbitaly, VSEPR Rezonanční struktury, atomové a molekulové orbitaly, hybridizace, určování tvaru molekuly pomocí teorie VSEPR, úvod do symetrie molekul, dipólový moment 1 / 18 Formální náboj Rozdíl mezi
Teorie chemické vazby a molekulární geometrie Molekulární geometrie VSEPR
 Geometrie molekul Lewisovy vzorce poskytují informaci o tom které atomy jsou spojeny vazbou a o jakou vazbu se jedná (topologie molekuly). Geometrické uspořádání molekuly je charakterizováno: Délkou vazeb
Geometrie molekul Lewisovy vzorce poskytují informaci o tom které atomy jsou spojeny vazbou a o jakou vazbu se jedná (topologie molekuly). Geometrické uspořádání molekuly je charakterizováno: Délkou vazeb
Orbitaly, VSEPR. Zdeněk Moravec, 16. listopadu / 21
 rbitaly, VSEPR Rezonanční struktury, atomové a molekulové orbitaly, hybridizace, určování tvaru molekuly pomocí teorie VSEPR, úvod do symetrie molekul, dipólový moment Zdeněk Moravec, http://z-moravec.net
rbitaly, VSEPR Rezonanční struktury, atomové a molekulové orbitaly, hybridizace, určování tvaru molekuly pomocí teorie VSEPR, úvod do symetrie molekul, dipólový moment Zdeněk Moravec, http://z-moravec.net
SIGNÁLY A SOUSTAVY, SIGNÁLY A SYSTÉMY
 SIGNÁLY A SOUSTAVY, SIGNÁLY A SYSTÉMY TEMATICKÉ OKRUHY Signály se spojitým časem Základní signály se spojitým časem (základní spojité signály) Jednotkový skok σ (t), jednotkový impuls (Diracův impuls)
SIGNÁLY A SOUSTAVY, SIGNÁLY A SYSTÉMY TEMATICKÉ OKRUHY Signály se spojitým časem Základní signály se spojitým časem (základní spojité signály) Jednotkový skok σ (t), jednotkový impuls (Diracův impuls)
Elektromagnetické pole je generováno elektrickými náboji a jejich pohybem. Je-li zdroj charakterizován nábojovou hustotou ( r r
 Záření Hertzova dipólu, kulové vlny, Rovnice elektromagnetického pole jsou vektorové diferenciální rovnice a podle symetrie bývá vhodné je řešit v křivočarých souřadnicích. Základní diferenciální operátory
Záření Hertzova dipólu, kulové vlny, Rovnice elektromagnetického pole jsou vektorové diferenciální rovnice a podle symetrie bývá vhodné je řešit v křivočarých souřadnicích. Základní diferenciální operátory
Fyzika IV Dynamika jader v molekulách
 Dynamika jader v molekulách vibrace rotace Dynamika jader v molekulách rotační energetické hladiny (dvouatomová molekula) moment setrvačnosti kolem osy procházející těžištěm osa těžiště m2 m1 r2 r1 R moment
Dynamika jader v molekulách vibrace rotace Dynamika jader v molekulách rotační energetické hladiny (dvouatomová molekula) moment setrvačnosti kolem osy procházející těžištěm osa těžiště m2 m1 r2 r1 R moment
Elektronový obal atomu
 Elektronový obal atomu Ondřej Havlíček.ročník F-Vt/SŠ Jsoucno je vždy něco, co jsme si sami zkonstruovali ve své mysli. Podstata takovýchto konstrukcí nespočívá v tom, že by byly odvozeny ze smyslových
Elektronový obal atomu Ondřej Havlíček.ročník F-Vt/SŠ Jsoucno je vždy něco, co jsme si sami zkonstruovali ve své mysli. Podstata takovýchto konstrukcí nespočívá v tom, že by byly odvozeny ze smyslových
Příklad 6: Bariéra a tunelový jev
 1 Příklad 6: Bariéra a tunelový jev Předpokládejme, že částice o hmotnosti m a energii E dopadá zleva na potenciálovou bariéru (viz obrázek) o výšce V 0. Energie částice je menší než výška potenciálové
1 Příklad 6: Bariéra a tunelový jev Předpokládejme, že částice o hmotnosti m a energii E dopadá zleva na potenciálovou bariéru (viz obrázek) o výšce V 0. Energie částice je menší než výška potenciálové
Matematika I A ukázkový test 1 pro 2014/2015
 Matematika I A ukázkový test 1 pro 2014/2015 1. Je dána soustava rovnic s parametrem a R x y + z = 1 x + y + 3z = 1 (2a 1)x + (a + 1)y + z = 1 a a) Napište Frobeniovu větu (existence i počet řešení). b)
Matematika I A ukázkový test 1 pro 2014/2015 1. Je dána soustava rovnic s parametrem a R x y + z = 1 x + y + 3z = 1 (2a 1)x + (a + 1)y + z = 1 a a) Napište Frobeniovu větu (existence i počet řešení). b)
Počátky: už jsme potkali
 KVANTOVÁ MECHANIKA Počátky: už jsme potkali Záření černého tělesa Kvantování energie Fotoefekt PLANCK 1858-1947 EINSTEIN 1879-1955 Model atomu Vlnové vlastnosti částic BOHR 1885-1962 de BROGLIE 1892-1987
KVANTOVÁ MECHANIKA Počátky: už jsme potkali Záření černého tělesa Kvantování energie Fotoefekt PLANCK 1858-1947 EINSTEIN 1879-1955 Model atomu Vlnové vlastnosti částic BOHR 1885-1962 de BROGLIE 1892-1987
Měření šířky zakázaného pásu polovodičů
 Měření šířky zakázaného pásu polovodičů Úkol : 1. Určete šířku zakázaného pásu ze spektrální citlivosti fotorezistoru pro šterbinu 1,5 mm. Na monochromátoru nastavujte vlnovou délku od 200 nm po 50 nm
Měření šířky zakázaného pásu polovodičů Úkol : 1. Určete šířku zakázaného pásu ze spektrální citlivosti fotorezistoru pro šterbinu 1,5 mm. Na monochromátoru nastavujte vlnovou délku od 200 nm po 50 nm
John Dalton Amadeo Avogadro
 Spojením atomů vznikají molekuly... John Dalton 1766 1844 Amadeo Avogadro 1776 1856 Výpočet molekuly 2, metoda valenční vazby Walter eitler 1904 1981 Fritz W. London 1900 1954 Teorie molekulových orbitalů
Spojením atomů vznikají molekuly... John Dalton 1766 1844 Amadeo Avogadro 1776 1856 Výpočet molekuly 2, metoda valenční vazby Walter eitler 1904 1981 Fritz W. London 1900 1954 Teorie molekulových orbitalů
SPEKTRÁLNÍ METODY. Ing. David MILDE, Ph.D. Katedra analytické chemie Tel.: ; (c) David MILDE,
 SEKTRÁLNÍ METODY Ing. David MILDE, h.d. Katedra analytické chemie Tel.: 585634443; E-mail: david.milde@upol.cz (c) -2008 oužitá a doporučená literatura Němcová I., Čermáková L., Rychlovský.: Spektrometrické
SEKTRÁLNÍ METODY Ing. David MILDE, h.d. Katedra analytické chemie Tel.: 585634443; E-mail: david.milde@upol.cz (c) -2008 oužitá a doporučená literatura Němcová I., Čermáková L., Rychlovský.: Spektrometrické
Teorie Molekulových Orbitalů (MO)
 Teorie Molekulových Orbitalů (MO) Kombinace atomových orbitalů na všech atomech v molekule Vhodná symetrie Vhodná (podobná) energie Z n AO vytvoříme n MO Pro začátek dvouatomové molekuly: H 2, F 2, CO,...
Teorie Molekulových Orbitalů (MO) Kombinace atomových orbitalů na všech atomech v molekule Vhodná symetrie Vhodná (podobná) energie Z n AO vytvoříme n MO Pro začátek dvouatomové molekuly: H 2, F 2, CO,...
Nekovalentní interakce
 Nekovalentní interakce Jan Řezáč UOCHB AV ČR 3. listopadu 2016 Jan Řezáč (UOCHB AV ČR) Nekovalentní interakce 3. listopadu 2016 1 / 28 Osnova 1 Teorie 2 Typy nekovalentních interakcí 3 Projevy v chemii
Nekovalentní interakce Jan Řezáč UOCHB AV ČR 3. listopadu 2016 Jan Řezáč (UOCHB AV ČR) Nekovalentní interakce 3. listopadu 2016 1 / 28 Osnova 1 Teorie 2 Typy nekovalentních interakcí 3 Projevy v chemii
U01 = 30 V, U 02 = 15 V R 1 = R 4 = 5 Ω, R 2 = R 3 = 10 Ω
 B 9:00 hod. Elektrotechnika a) Definujte stručně princip superpozice a uveďte, pro které obvody platí. b) Vypočítejte proudy větvemi uvedeného obvodu metodou superpozice. 0 = 30 V, 0 = 5 V R = R 4 = 5
B 9:00 hod. Elektrotechnika a) Definujte stručně princip superpozice a uveďte, pro které obvody platí. b) Vypočítejte proudy větvemi uvedeného obvodu metodou superpozice. 0 = 30 V, 0 = 5 V R = R 4 = 5
frekvence f (Hz) perioda T = 1/f (s)
 1.) Periodický pohyb - každý pohyb, který se opakuje v pravidelných intervalech Poet Poet cykl cykl za za sekundu sekundu frekvence f (Hz) perioda T 1/f (s) Doba Doba trvání trvání jednoho jednoho cyklu
1.) Periodický pohyb - každý pohyb, který se opakuje v pravidelných intervalech Poet Poet cykl cykl za za sekundu sekundu frekvence f (Hz) perioda T 1/f (s) Doba Doba trvání trvání jednoho jednoho cyklu
Nekovalentní interakce
 Nekovalentní interakce Jan Řezáč UOCHB AV ČR 31. října 2017 Jan Řezáč (UOCHB AV ČR) Nekovalentní interakce 31. října 2017 1 / 28 Osnova 1 Teorie 2 Typy nekovalentních interakcí 3 Projevy v chemii 4 Výpočty
Nekovalentní interakce Jan Řezáč UOCHB AV ČR 31. října 2017 Jan Řezáč (UOCHB AV ČR) Nekovalentní interakce 31. října 2017 1 / 28 Osnova 1 Teorie 2 Typy nekovalentních interakcí 3 Projevy v chemii 4 Výpočty
Úvod do strukturní analýzy farmaceutických látek
 Úvod do strukturní analýzy farmaceutických látek Garant předmětu: Vyučující: doc. Ing. Bohumil Dolenský, Ph.D. prof. RNDr. Pavel Matějka, Ph.D., A136, linka 3687, matejkap@vscht.cz doc. Ing. Bohumil Dolenský,
Úvod do strukturní analýzy farmaceutických látek Garant předmětu: Vyučující: doc. Ing. Bohumil Dolenský, Ph.D. prof. RNDr. Pavel Matějka, Ph.D., A136, linka 3687, matejkap@vscht.cz doc. Ing. Bohumil Dolenský,
5 Potenciály s δ funkcemi I
 5 Potenciály s δ funkcemi 5. Jednoduchá δ jáma nebo bariéra Mějme potenciál ve tvaru jednoduché δ funkce V cδ, kde c je konstanta, jejíž velikost udává sílu potenciálu. Pokud je c
5 Potenciály s δ funkcemi 5. Jednoduchá δ jáma nebo bariéra Mějme potenciál ve tvaru jednoduché δ funkce V cδ, kde c je konstanta, jejíž velikost udává sílu potenciálu. Pokud je c
Struktura elektronového obalu
 Projekt: Inovace oboru Mechatronik pro Zlínský kraj Registrační číslo: CZ.1.07/1.1.08/03.0009 Struktura elektronového obalu Představy o modelu atomu se vyvíjely tak, jak se zdokonalovaly možnosti vědy
Projekt: Inovace oboru Mechatronik pro Zlínský kraj Registrační číslo: CZ.1.07/1.1.08/03.0009 Struktura elektronového obalu Představy o modelu atomu se vyvíjely tak, jak se zdokonalovaly možnosti vědy
Projekt: Inovace oboru Mechatronik pro Zlínský kraj Registrační číslo: CZ.1.07/1.1.08/ Vlnění
 Projekt: Inovace oboru Mechatronik pro Zlínský kraj Registrační číslo: CZ.1.07/1.1.08/03.0009 Vlnění Vhodíme-li na klidnou vodní hladinu kámen, hladina se jeho dopadem rozkmitá a z místa rozruchu se začnou
Projekt: Inovace oboru Mechatronik pro Zlínský kraj Registrační číslo: CZ.1.07/1.1.08/03.0009 Vlnění Vhodíme-li na klidnou vodní hladinu kámen, hladina se jeho dopadem rozkmitá a z místa rozruchu se začnou
Hodnocení parametrů signálu AE při únavovém zatěžování tří typů konstrukčních materiálů. Vypracoval: Kolář Lukáš
 Hodnocení parametrů signálu AE při únavovém zatěžování tří typů konstrukčních materiálů Vypracoval: Kolář Lukáš Cíl práce: Analýza současného stavu testování metodou AE Návrh experimentálního zajištění
Hodnocení parametrů signálu AE při únavovém zatěžování tří typů konstrukčních materiálů Vypracoval: Kolář Lukáš Cíl práce: Analýza současného stavu testování metodou AE Návrh experimentálního zajištění
Obr Teplotní závislost intrinzické koncentrace nosičů n i [cm -3 ] pro GaAs, Si, Ge Fermiho hladina Výpočet polohy Fermiho hladiny
![Obr Teplotní závislost intrinzické koncentrace nosičů n i [cm -3 ] pro GaAs, Si, Ge Fermiho hladina Výpočet polohy Fermiho hladiny Obr Teplotní závislost intrinzické koncentrace nosičů n i [cm -3 ] pro GaAs, Si, Ge Fermiho hladina Výpočet polohy Fermiho hladiny](/thumbs/54/33760815.jpg) Obr. 2-12 Teplotní závislost intrinzické koncentrace nosičů n i [cm -3 ] pro GaAs, Si, Ge 2.7. Fermiho hladina 2.7.1. Výpočet polohy Fermiho hladiny Z Obr. 2-11. a ze vztahů ( 2-9) nebo ( 2-14) je zřejmá
Obr. 2-12 Teplotní závislost intrinzické koncentrace nosičů n i [cm -3 ] pro GaAs, Si, Ge 2.7. Fermiho hladina 2.7.1. Výpočet polohy Fermiho hladiny Z Obr. 2-11. a ze vztahů ( 2-9) nebo ( 2-14) je zřejmá
Born-Oppenheimerova aproximace
 Born-Oppenheimerova aproximace Oddělení elektronického a jaderného pohybu Jádra 2000 x těžší než elektrony elektrony kvantová chemie, popis systému (do 100 atomů) na základě vlastností elektronů (jádra
Born-Oppenheimerova aproximace Oddělení elektronického a jaderného pohybu Jádra 2000 x těžší než elektrony elektrony kvantová chemie, popis systému (do 100 atomů) na základě vlastností elektronů (jádra
1 Rozdělení mechaniky a její náplň
 1 Rozdělení mechaniky a její náplň Mechanika je nauka o rovnováze a pohybu hmotných útvarů pohybujících se rychlostí podstatně menší, než je rychlost světla (v c). Vlastnosti skutečných hmotných útvarů
1 Rozdělení mechaniky a její náplň Mechanika je nauka o rovnováze a pohybu hmotných útvarů pohybujících se rychlostí podstatně menší, než je rychlost světla (v c). Vlastnosti skutečných hmotných útvarů
Řešit atom vodíku znamená nalézt řešení Schrödingerovy rovnice s příslušným hamiltoniánem. 1 4πǫ 0. 2m e
 8 Atom vodíku Správné řešení atomu vodíku je jedním z velkých vítězství kvantové mechaniky. Podle klasické fyziky náboj, který se pohybuje se zrychlením (elektron obíhající vodíkové jádro proton), by měl
8 Atom vodíku Správné řešení atomu vodíku je jedním z velkých vítězství kvantové mechaniky. Podle klasické fyziky náboj, který se pohybuje se zrychlením (elektron obíhající vodíkové jádro proton), by měl
Úvod do laserové techniky
 Úvod do laserové techniky Látka jako soubor kvantových soustav Jan Šulc Katedra fyzikální elektroniky České vysoké učení technické v Praze petr.koranda@gmail.com 18. září 2018 Světlo jako elektromagnetické
Úvod do laserové techniky Látka jako soubor kvantových soustav Jan Šulc Katedra fyzikální elektroniky České vysoké učení technické v Praze petr.koranda@gmail.com 18. září 2018 Světlo jako elektromagnetické
nano.tul.cz Inovace a rozvoj studia nanomateriálů na TUL
 Inovace a rozvoj studia nanomateriálů na TUL nano.tul.cz Tyto materiály byly vytvořeny v rámci projektu ESF OP VK: Inovace a rozvoj studia nanomateriálů na Technické univerzitě v Liberci Optické vlastnosti
Inovace a rozvoj studia nanomateriálů na TUL nano.tul.cz Tyto materiály byly vytvořeny v rámci projektu ESF OP VK: Inovace a rozvoj studia nanomateriálů na Technické univerzitě v Liberci Optické vlastnosti
Elektrický proud v polovodičích
 Elektrický proud v polovodičích Polovodič Látka, jejíž měrný elektrický odpor je při obvyklých teplotách mnohem menší než u izolantů, ale zase mnohem větší než u kovů. Polovodič Látka, jejíž měrný elektrický
Elektrický proud v polovodičích Polovodič Látka, jejíž měrný elektrický odpor je při obvyklých teplotách mnohem menší než u izolantů, ale zase mnohem větší než u kovů. Polovodič Látka, jejíž měrný elektrický
Úvod do kvantového počítání
 2. přednáška Katedra počítačů, Fakulta elektrotechnická České vysoké učení technické v Praze 17. března 2005 Opakování Část I Přehled z minulé hodiny Opakování Alternativní výpočetní modely Kvantové počítače
2. přednáška Katedra počítačů, Fakulta elektrotechnická České vysoké učení technické v Praze 17. března 2005 Opakování Část I Přehled z minulé hodiny Opakování Alternativní výpočetní modely Kvantové počítače
Překryv orbitalů. Vznik vazby překryvem orbitalů na dvou různých atomech A, B Obsazeno dvojicí elektronů Ψ = Ψ A Ψ Β
 Překryv orbitalů Vznik vazby překryvem orbitalů na dvou různých atomech A, B Obsazeno dvojicí elektronů Ψ = Ψ A Ψ Β Podmínky překryvu: Vhodná symetrie, znaménko vlnové funkce Vhodná energie, srovnatelná,
Překryv orbitalů Vznik vazby překryvem orbitalů na dvou různých atomech A, B Obsazeno dvojicí elektronů Ψ = Ψ A Ψ Β Podmínky překryvu: Vhodná symetrie, znaménko vlnové funkce Vhodná energie, srovnatelná,
Charakteristiky optického záření
 Fyzika III - Optika Charakteristiky optického záření / 1 Charakteristiky optického záření 1. Spektrální charakteristika vychází se z rovinné harmonické vlny jako elementu elektromagnetického pole : primární
Fyzika III - Optika Charakteristiky optického záření / 1 Charakteristiky optického záření 1. Spektrální charakteristika vychází se z rovinné harmonické vlny jako elementu elektromagnetického pole : primární
1.8. Mechanické vlnění
 1.8. Mechanické vlnění 1. Umět vysvětlit princip vlnivého pohybu.. Umět srovnat a zároveň vysvětlit rozdíl mezi periodickým kmitavým pohybem jednoho bodu s periodickým vlnivým pohybem bodové řady. 3. Znát
1.8. Mechanické vlnění 1. Umět vysvětlit princip vlnivého pohybu.. Umět srovnat a zároveň vysvětlit rozdíl mezi periodickým kmitavým pohybem jednoho bodu s periodickým vlnivým pohybem bodové řady. 3. Znát
Opakování
 Slabé vazebné interakce Opakování Co je to atom? Opakování Opakování Co je to atom? Atom je nejmenší částice hmoty, chemicky dále nedělitelná. Skládá se z atomového jádra obsahujícího protony a neutrony
Slabé vazebné interakce Opakování Co je to atom? Opakování Opakování Co je to atom? Atom je nejmenší částice hmoty, chemicky dále nedělitelná. Skládá se z atomového jádra obsahujícího protony a neutrony
SIGNÁLY A LINEÁRNÍ SYSTÉMY
 SIGNÁLY A LINEÁRNÍ SYSTÉMY prof. Ing. Jiří Holčík, CSc. holcik@iba.muni.cz, Kamenice 3, 4. patro, dv.č.424 INVESTICE Institut DO biostatistiky ROZVOJE VZDĚLÁVÁNÍ a analýz IV. FREKVENČNÍ TRASFORMACE SPOJITÉ
SIGNÁLY A LINEÁRNÍ SYSTÉMY prof. Ing. Jiří Holčík, CSc. holcik@iba.muni.cz, Kamenice 3, 4. patro, dv.č.424 INVESTICE Institut DO biostatistiky ROZVOJE VZDĚLÁVÁNÍ a analýz IV. FREKVENČNÍ TRASFORMACE SPOJITÉ
F6121 Základy fyziky pevných látek příklady do cvičení
 F6121 Základy fyziky pevných látek příklady do cvičení 1 Drudeho model volných elektronů 1 1.1 Poissonovo rozdělení............................................ 1 1.2 Jouleho teplo................................................
F6121 Základy fyziky pevných látek příklady do cvičení 1 Drudeho model volných elektronů 1 1.1 Poissonovo rozdělení............................................ 1 1.2 Jouleho teplo................................................
8. Úvod do fyziky pevných látek
 8. Úvod do fyziky pevných látek V předchozích kapitolách jsme se seznámili s kvantově mechanickým popisem jednotlivých atomů. V této kapitole si ukážeme, že kvantová teorie umí stejně dobře popsat i seskupení
8. Úvod do fyziky pevných látek V předchozích kapitolách jsme se seznámili s kvantově mechanickým popisem jednotlivých atomů. V této kapitole si ukážeme, že kvantová teorie umí stejně dobře popsat i seskupení
Úvod do nano a mikrotechnologií
 Úvod do nano a mikrotechnologií 5. přednáška: Kvantová mechanika - Schrödingerova rovnice Tunelový jev a kvantové uvěznění Pásový diagram pevné látky a jeho závislost na struktuře materiálu Elektrofyzikální
Úvod do nano a mikrotechnologií 5. přednáška: Kvantová mechanika - Schrödingerova rovnice Tunelový jev a kvantové uvěznění Pásový diagram pevné látky a jeho závislost na struktuře materiálu Elektrofyzikální
4. Stanovení teplotního součinitele odporu kovů
 4. Stanovení teplotního součinitele odporu kovů 4.. Zadání úlohy. Změřte teplotní součinitel odporu mědi v rozmezí 20 80 C. 2. Změřte teplotní součinitel odporu platiny v rozmezí 20 80 C. 3. Vyneste graf
4. Stanovení teplotního součinitele odporu kovů 4.. Zadání úlohy. Změřte teplotní součinitel odporu mědi v rozmezí 20 80 C. 2. Změřte teplotní součinitel odporu platiny v rozmezí 20 80 C. 3. Vyneste graf
Státní závěrečná zkouška z oboru Matematika a její použití v přírodních vědách
 Státní závěrečná zkouška z oboru Matematika a její použití v přírodních vědách Ústní zkouška z oboru Náročnost zkoušky je podtržena její ústní formou a komisionálním charakterem. Předmětem bakalářské zkoušky
Státní závěrečná zkouška z oboru Matematika a její použití v přírodních vědách Ústní zkouška z oboru Náročnost zkoušky je podtržena její ústní formou a komisionálním charakterem. Předmětem bakalářské zkoušky
Symetrie Platonovská tělesa
 Symetrie Platonovská tělesa 1 Symetrie Virus rýmy Virus obrny Virus slintavky a kulhavky 2 Symetrie molekul Jak jsou atomy v molekule uspořádány = ekvivalentní atomy 3 Prvky a operace symetrie Značk a
Symetrie Platonovská tělesa 1 Symetrie Virus rýmy Virus obrny Virus slintavky a kulhavky 2 Symetrie molekul Jak jsou atomy v molekule uspořádány = ekvivalentní atomy 3 Prvky a operace symetrie Značk a
Oddělení pohybu elektronů a jader
 Oddělení pohybu elektronů a ader Adiabatická aproximace Born-Oppenheimerova aproximace Důležité vztahy sou 4, 5, 7, 0,,, udělal sem to zbytečně podrobně, e to samostatný okruh Separace translačního pohybu:
Oddělení pohybu elektronů a ader Adiabatická aproximace Born-Oppenheimerova aproximace Důležité vztahy sou 4, 5, 7, 0,,, udělal sem to zbytečně podrobně, e to samostatný okruh Separace translačního pohybu:
ATOMOVÁ SPEKTROMETRIE
 ATOMOVÁ SPEKTROMETRIE doc. Ing. David MILDE, Ph.D. tel.: 585634443 E-mail: david.milde@upol.cz (c) -017 Doporučená literatura Černohorský T., Jandera P.: Atomová spektrometrie. Univerzita Pardubice 1997.
ATOMOVÁ SPEKTROMETRIE doc. Ing. David MILDE, Ph.D. tel.: 585634443 E-mail: david.milde@upol.cz (c) -017 Doporučená literatura Černohorský T., Jandera P.: Atomová spektrometrie. Univerzita Pardubice 1997.
Kvantová fyzika atomárních soustav letní semestr VIII. KOTLÁŘSKÁ 23. DUBNA 2014
 F40 Kvantová fyzika atomárních soustav letní semestr 03-04 VIII. Vibrace víceatomových molekul cvičení KOTLÁŘSKÁ 3. DUBNA 04 Úvodem capsule o maticích a jejich diagonalisaci definice "vibračních módů"
F40 Kvantová fyzika atomárních soustav letní semestr 03-04 VIII. Vibrace víceatomových molekul cvičení KOTLÁŘSKÁ 3. DUBNA 04 Úvodem capsule o maticích a jejich diagonalisaci definice "vibračních módů"
Úvod do elektrokinetiky
 Úvod do elektrokinetiky Hlavní body - elektrokinetika Elektrické proudy pohyb nábojů Ohmův zákon, mikroskopický pohled Měrná vodivost σ izolanty, vodiče, polovodiče Elektrické zdroje napětí (a proudu)
Úvod do elektrokinetiky Hlavní body - elektrokinetika Elektrické proudy pohyb nábojů Ohmův zákon, mikroskopický pohled Měrná vodivost σ izolanty, vodiče, polovodiče Elektrické zdroje napětí (a proudu)
1. Náhodný vektor (X, Y ) má diskrétní rozdělení s pravděpodobnostní funkcí p, kde. p(x, y) = a(x + y + 1), x, y {0, 1, 2}.
 VIII. Náhodný vektor. Náhodný vektor (X, Y má diskrétní rozdělení s pravděpodobnostní funkcí p, kde p(x, y a(x + y +, x, y {,, }. a Určete číslo a a napište tabulku pravděpodobnostní funkce p. Řešení:
VIII. Náhodný vektor. Náhodný vektor (X, Y má diskrétní rozdělení s pravděpodobnostní funkcí p, kde p(x, y a(x + y +, x, y {,, }. a Určete číslo a a napište tabulku pravděpodobnostní funkce p. Řešení:
Matematika II, úroveň A ukázkový test č. 1 (2016) 1. a) Napište postačující podmínku pro diferencovatelnost funkce n-proměnných v otevřené
 22. 2. 2016 Matematika II, úroveň A ukázkový test č. 1 (2016) 1. a) Napište postačující podmínku pro diferencovatelnost funkce n-proměnných v otevřené mn. M E n. Zapište a načrtněte množinu D, ve které
22. 2. 2016 Matematika II, úroveň A ukázkový test č. 1 (2016) 1. a) Napište postačující podmínku pro diferencovatelnost funkce n-proměnných v otevřené mn. M E n. Zapište a načrtněte množinu D, ve které
Kmity a mechanické vlnění. neperiodický periodický
 rozdělení časově proměnných pohybů (dějů): Mechanické kmitání neperiodický periodický ne(an)harmonický harmonický vlastní kmity nucené kmity - je pohyb HB (tělesa), při němž HB nepřekročí konečnou vzdálenost
rozdělení časově proměnných pohybů (dějů): Mechanické kmitání neperiodický periodický ne(an)harmonický harmonický vlastní kmity nucené kmity - je pohyb HB (tělesa), při němž HB nepřekročí konečnou vzdálenost
Atomové a molekulové orbitaly Ion molekuly vodíku. Molekula vodíku Heitler-Londonovou metodou. Metoda LCAO. Báze atomových orbitalů.
 Atomové a molekulové orbitaly Ion molekuly vodíku. Molekula vodíku Heitler-Londonovou metodou. Metoda LCAO. Báze atomových orbitalů. Ion molekuly vodíku H + 2 První použití metody je demonstrováno při
Atomové a molekulové orbitaly Ion molekuly vodíku. Molekula vodíku Heitler-Londonovou metodou. Metoda LCAO. Báze atomových orbitalů. Ion molekuly vodíku H + 2 První použití metody je demonstrováno při
Základy vakuové techniky
 Základy vakuové techniky Střední rychlost plynů Rychlost molekuly v p = (2 k N A ) * (T/M 0 ), N A = 6. 10 23 molekul na mol (Avogadrova konstanta), k = 1,38. 10-23 J/K.. Boltzmannova konstanta, T.. absolutní
Základy vakuové techniky Střední rychlost plynů Rychlost molekuly v p = (2 k N A ) * (T/M 0 ), N A = 6. 10 23 molekul na mol (Avogadrova konstanta), k = 1,38. 10-23 J/K.. Boltzmannova konstanta, T.. absolutní
