Řešení struktury proteinů pomocí NMR spektroskopie
|
|
|
- Dagmar Müllerová
- před 9 lety
- Počet zobrazení:
Transkript
1 Řešení struktury proteinů pomocí NMR spektroskopie
2 Využití NMR spektroskopie v jednotlivých oborech podle nositele Nobelovy ceny za chemii Prof. Richarda Ernsta: Medicine Biochemistry Chemistry Physics J.W. Emsley: NMR started as the plaything of the physicists, became the favourite toy of the chemists and finally went on to seduce biochemists.
3 Důvody pro využití NMR spektroskopie ke studiu biomolekul fyziologické prostředí jednoduchá příprava vzorku vysoce selektivní odezva široký rozsah fyzikálně-chemických vlastností protože se zabýváme NMR spektroskopií
4 1. Jaké typy biologicky aktivních molekul? peptidy a proteiny nukleové kyseliny oligosacharidy 2. Jaký typ informace může být pomocí NMR získán? identifikace substrátu prostorová struktura molekuly studium dynamického chování systému prostorová struktura komplexu zkoumání vazby ligandu a substrátu
5
6 Strategie pro určování struktur biomolekul NMR vzorek NMR experimenty NMR spektra Přiřazení signálů Přiřazení experimentálních NMR parametrů (NOE ) Obecné informace o molekule (primární struktura, kovalentní vazby ) Odhad přibližné struktury Zhodnocení kvality struktur Oprava přiřazení NMR parametrů, signálů Výpočet souboru struktur Výpočet statistických údajů pro soubor konečných struktur Porovnání s databázemi (Procheck, Whatif.) Výpočet NOESY spekter
7 Požadavky na vzorek pro NMR experimenty Úspěšné řešení proteinových struktur bezpodmínečně vyžaduje kvalitní spolupráci mezi NMR specialisty a biochemiky! Vzorek musí zůstat aktivní a nedenaturovaný během NMR experimentů!!! rozpouštědlo H 2 O % D 2 O (časová stabilizace magnetického pole) pufr teplota aditiva nejběžnější je fosfátový pufr, neobsahuje žádné protony acetátový pufr (lze pořídit deuterovaný) podle požadavků studovaného materiálu (15 40C) nutná aditiva je možné někdy zaměnit za deuterovaná analoga koncentrace pro NMR experimenty musí být v rozsahu alespoň mm, vzorek nesmí podléhat agregaci, koagulaci, sebezničení v tomto konc. rozmezí stabilita nutná dlouhodobá stabilita v rozsahu minimálně několika týdnů
8 Příprava vzorku proteinu pro NMR měření 1. Získání DNA proteinu 2. Příprava plasmidové DNA 3. Exprese rekombinantního proteinu, např. v E.Coli 4. Izolace a čištění 5. Zakoncentrování vzorku 6. Zopakování procesu se značeným médiem
9 Příprava vzorků se zvýšeným obsahem 13 C/ 15 N C C H C H C CO N CO C H H H Exprese proteinů: - v minimálním médiu ( 15 NH 4 Cl, 15 NH 4 SO 4 - jediný zdroj 15 N ) ( 13 C-glukosa, 13 C-glycerol - jediný zdroj 13 C) - izotopově obohacené růstové médium
10 Segmentové izotopové obohacení Capsidový protein HIV-1 N-terminální doména C-terminální doména
11 Segmentové izotopové obohacení 1. Obě domény se exprimují zvlášť N-term Intein N-term Tag Cys C-term 2. Intein se odštěpí thiolem a Tag proteasou N-term Intein N-term Tag Cys C-term 3. Domény se spojí vytvořením peptidové vazby N-term Cys C-term
12 Segmentové izotopové obohacení 15 N 1 doména obohacena ( 15 N) celý protein obohacen ( 15 N) 1 H
13 Cell-free expresní systém Zdroj: propagační materiál firmy Promega
14 Přehled metod pro izotopové obohacení proteinů
15 Postup přípravy izotopově obohaceného vzorku Příprava neznačeného vzorku proteinu o příslušné koncentraci kontrola správného sbalení proteinu kontrola dostatečně vysoké koncentrace sledování dlouhodobé stability Příprava 15 N obohaceného vzorku proteinu kontrola čistoty proteinu kontrola správného sbalení proteinu kontrola dostatečně vysoké koncentrace Příprava 13 C/ 15 N ( 13 C/ 15 N/ 2 H) obohaceného vzorku proteinu vlastní strukturní studie
16 Zakoncentrování vzorku Koncentrace měřeného vzorku v případě využití chlazené sondy Objem roztoku ~ 0,5 1,0 mm ~ 0,1 0,5 mm l
17 Srovnání NMR spekter sbalené a nesbalené struktury proteinu správně sbalená forma proteinu WVQPI 107 AA (12 kda) IMMCS 83 AA (9 kda) WVQPI 107 AA (12 kda) IMMCS nesbalená forma téhož proteinu ( 1 H) ppm 1 H- 15 N korelace v oblasti amidických vodíků (vzorek nespecificky obohacen 15 N) čerstvě připravený vzorek ( 15 N) vzorek po 5 dnech ( 1 H) ppm ppm
18 Strategie pro určování struktur biomolekul NMR vzorek NMR experimenty NMR spektra Přiřazení signálů Přiřazení experimentálních NMR parametrů (NOE ) Obecné informace o molekule (primární struktura, kovalentní vazby ) Odhad přibližné struktury Zhodnocení kvality struktur Oprava přiřazení NMR parametrů, signálů Výpočet souboru struktur Výpočet statistických údajů pro soubor konečných struktur Porovnání s databázemi (Procheck, Whatif.) Výpočet NOESY spekter
19 Biomolekulární NMR spektroskopie: měřená jádra 1 H 13 C 15 N 2 H vysoké přirozené zastoupení (99.98%) vysoká citlivost (1.00) malá disperze chemických posunů NMR signálů (~15.0 ppm) velká disperze chemických posunů NMR signálů (~200.0 ppm) nízké přirozené zastoupení (1.108%), možné uměle navýšit až na 100% nízká citlivost (1.76x10-4 ), po 100%ním izotopovém obohacení (1.59x10-2 ) střední disperze chemických posunů NMR signálů (~30.0 ppm) (oproti 13 C nezávislost na typu aminokyseliny) nízké přirozené zastoupení (0.37%), možné uměle navýšit až na 100% velmi nízká citlivost (3.85x10-6 ), po 100%ním izotopovém obohacení (1.04x10-3 ) používá se pro speciální účely
20 Proč H 2 O? Potlačení signálu vody 1. Voda je fyziologické prostředí 2. Nelze použít D 2 O z důvodů chemické výměny s amidickými protony. Signál H 2 O je násobně intenzivnější než odezva měřené molekuly.
21 Potlačení signálu vody: metoda presaturace CW-ozařování 90 Během relaxační doby ozařujeme signál vody slabým RF polem. 1 H spektrum proteinu po presaturaci H 2 O zbytkový signál H 2 O
22 Potlačení signálu vody: metoda WATERGATE Selektivní manipulace se signály vody a rozpuštěné látky doplněná o čistící gradientní echo H G t 180 t G G Selektivní 180 puls
23 Potlačení signálu vody: metoda WATERGATE
24 Multidimensionální NMR spektroskopie F 2 ( 13 C) F 3 ( 1 H) F 1 ( 15 N)
25 1 H - spektrum H H H H H H N H ppm
26 1D 1 H spektrum proteinu kuřecí lysozym 129 AA, M w = 14.6 kda methyl H NH-backbone aromatic H NH-SC aliphatic H CH
27 Odezva více jader v jednom spektru p N (0 p N 1) 13 C 35Hz 13 C Hz H C H 35Hz 35Hz p C (0 p C 1) 13 55Hz 13 15Hz C C 15 N 11Hz 13 55Hz C 13 C H 7Hz 90Hz H N 140Hz H <1Hz p H (0 p H 1) pravděpodobnost překryvu při zobrazení jednoho jádra p H (H),p N (N) a p C (C) při zobrazení dvou jader (H-N) najednou P = p H. p N při zobrazení tří jader (H-N-C) najednou P = p H. p N. p C
28 Korelační spektroskopie jako nástroj pro zjednodušení NMR spekter 1D 3D 2D F 1 ( 1 H) F 2 (X) F 2 ( 1 H) 4D F 1 ( 1 H/X) F 3 (X) F 3 ( 1 H) F 1 ( 1 H/X) Lepší rozlišení je ve vícedimenzionálních spektrech zajištěno využitím izotopového obohacení 15 N a 13 C. F 2 (X) F 4 ( 1 H) F 1 ( 1 H)
29 Přiřazování rezonancí NMR experimenty pro přiřazení signálů pracují se dvěma nebo třemi různými jádry najednou (experimenty s trojnásobnou rezonancí), chemické posuny těchto jáder jsou navzájem zkorelovány. Názvy takovýchto experimentů se tvoří podle typu jader, která korelují: HNCA koreluje amidický vodík s příslušným dusíkem a uhlíkem v pozici. HN(CO)CA koreluje stejné typy atomů (jader) jako HNCA, ale přes CO. To naznačuje směr korelace, tj. H a N i-té aminokyseliny a C aminokyseliny v pozici i-1. Směr přenosu magnetizace je v případě těchto experimentů H N C a zpět. Experimenty se nazývají out and back Naproti tomu přenos magnetizace u experimentů např. CBCA(CO)NH začíná na atomu C B (i-1) aminokyseliny a končí na amidickém H aminokyseliny následující, tj. experimenty out and stay.
30 Strategie pro určování struktur biomolekul NMR vzorek NMR experimenty NMR spektra Přiřazení signálů Přiřazení experimentálních NMR parametrů (NOE ) Obecné informace o molekule (primární struktura, kovalentní vazby ) Odhad přibližné struktury Zhodnocení kvality struktur Oprava přiřazení NMR parametrů, signálů Výpočet souboru struktur Výpočet statistických údajů pro soubor konečných struktur Porovnání s databázemi (Procheck, Whatif.) Výpočet NOESY spekter
31 Přiřazování rezonancí 13 C HNCA experiment 35Hz 13 C 13 H C 130Hz H aminokyselinový zbytek I 35Hz aminokyselinový zbytek I-1 35Hz 13 C 55Hz 13 C 15Hz 15 N 11Hz 13 C 55Hz 13 C H 7Hz 90Hz H N 140Hz H <1Hz
32 Konstrukce multidimensionálních NMR spekter 3D HNCA F 2 ( 15 N ) I F 1 ( 13 C ) F 2 ( 15 N ) I-1 F 3 ( 1 H N ) F 1 ( 13 C ) F 3 ( 1 H N )
33 Přiřazování rezonancí 13 C HN(CO)CA experiment 35Hz 13 C 13 H C 130Hz H 35Hz 35Hz 13 C 55Hz 13 C 15Hz 15 N 11Hz 13 C 55Hz 13 C H 7Hz 90Hz H N 140Hz H <1Hz
34 Konstrukce multidimensionálních NMR spekter 3D HNCA/HN(CO)CA F 2 ( 15 N ) F 2 ( 15 N ) I F 1 ( 13 C) F 2 ( 15 N ) I-1 I-1 F 3 ( 1 H N ) F 1 ( 13 C) F 3 ( 1 H N )
35 Sekvenční přiřazení hlavního řetězce HN(CO)CA HNCA missing crosspík
36 HNCACB experiment Přiřazování rezonancí Využití atomů uhlíku C 13 C Výhoda: chemický posun C je charakteristický pro typ aminokyselinového zbytku 35Hz 13 C 13 H C 130Hz H 35Hz aminokyselinový zbytek I-1 35Hz aminokyselinový zbytek I 13 C 55Hz 13 C 15Hz 15 N 11Hz 13 C 55Hz 13 C H 7Hz 90Hz H N 140Hz H <1Hz
37 Přiřazování rezonancí Využití atomů uhlíku C HN(CO)CACB experiment 13 C 35Hz 13 C 13 H C 130Hz H 35Hz 35Hz 13 C 55Hz 13 C 15Hz 15 N 11Hz 13 C 55Hz 13 C H 7Hz 90Hz H N 140Hz H <1Hz
38 ( 13 C) Přiřazování rezonancí Využití atomů uhlíku C HNCACB/HN(CO)CACB experiment Ser11 Leu12 Thr13 Leu14 Trp ( 15 N) ppm ( 15 N) ppm ( 15 N) ppm ( 15 N) ppm ( 15 N) ppm ( 1 H) ( 1 H) ( 1 H) ( 1 H) ( 1 H)
39 Přiřazování rezonancí postranních řetězců H C H H C H H C H H C H C C N C C H H N H
40 ( 13 C) Přiřazování rezonancí postranních řetězců ppm Kompletní přiřazení Prolinu 4 proteázy M-PMV pomocí hcch-cosy spektra H : ppm H : ppm Pro4CG-CB-HB2 H : ppm Pro4CG-CB-HB3 H : ppm Pro4CG-CG-HG H : ppm Pro4CG-CD-HD2 H : ppm Pro4CG-CD-HD3 H H H H N H H H O 30 Pro4CB-CA-HA Pro4CB-CB-HB2 Pro4CB-CB-HB3 Pro4CB-CG-HG 30 H 3 C O D 50 Pro4CD-CG-HG Pro4CD-CD-HD2 Pro4CD-CD-HD3 50 F 2 ( 1 H) 60 Pro4CA-CA-HA Pro4CA-CB-HB2 Pro4CA-CB-HB3 60 F 1 ( 13 C) ( 13 C) ppm F 3 ( 13 C)
41 Práce s extra velkými molekulami M w > 25 kda Práce s velkými molekulami způsobuje dvojí komplikaci velmi komplikovaná spektra rychlá spin-spinová relaxace R H ( D) C 8r 6 CH [ J ' s... f t ( )] c H / D ~ 6.6 Řešení: výměna atomů vodíku za deuterium
42 Práce s extra velkými molekulami M w > 25 kda Exprese proteinu v růstovém médiu obohaceném o 13 C/ 15 N/ 2 H 13 C 35Hz CD 3 CD Hz C HD C HD C D 35Hz 13 55Hz 13 15Hz C C H D 7Hz 15 11Hz N 90Hz H N 35Hz 13 55Hz C 140Hz H D 13 C <1Hz N H C D CO Teoreticky může být R 2 snížen až 44 násobně, prakticky většinou maximálně 15x.
43 Fully protonated versus perdeuterated EIN protein
44 Fully protonated versus perdeuterated EIN protein Missing crosspeaks are marked
45
46 Praktické návody-jak na to?
47 Strategie pro určování struktur biomolekul NMR vzorek NMR experimenty NMR spektra Přiřazení signálů Přiřazení experimentálních NMR parametrů (NOE ) Obecné informace o molekule (primární struktura, kovalentní vazby ) Odhad přibližné struktury Zhodnocení kvality struktur Oprava přiřazení NMR parametrů, signálů Výpočet souboru struktur Výpočet statistických údajů pro soubor konečných struktur Porovnání s databázemi (Procheck, Whatif.) Výpočet NOESY spekter
48 Získání experimentálních parametrů z NMR spekter. chemický posun (chemické okolí jádra) NOE interakce (meziatomová vzdálenost) interakční konstanta (dihedrální úhel) zbytková dipolární interakce (orientace) vodíková vazba (vzdálenost, vazebný úhel)
49 Chemický posun Výpočet indexu chemického posunu Změna chemického posunu indukovaná sekundární strukturou (H ) Chemické posuny některých jader jsou ovlivněny typem pravidelné sekundární struktury, do které jsou zahrnuty!!! -sheet random coil -helix Histogram indexu chemického posunu jader H, C a C. Přiřazení rezonancí hlavního řetězce: H,C, C +1 0 Výpočet indexů chemického posunu, tzv. CSI -1 Odhad sekundární struktury na základě lokální hustoty těchto indexů N helix I helix II helix III helix IV C Sekvence aminokyselin
50 CSI Secondary structure of M-PMV PR from CSI
51 Nukleární Overhauserův efekt NOE Experimentální omezení vzdáleností přímá spin-spinová interakce mezi jádry r IS < 5-6 Ǻ interakce mezi dipóly interagujících jader relaxační jev H H výměna energie mezi oběma jádry charakterizuje vzdálenost mezi oběma jádry IS h t c 1 4 t 2 c t c r 6 IS IS - rychlost nárustu NOE t c - korelační čas r IS - meziatomová vzdálenost - pracovní frekvence IS f r 6
52 Převod intenzity NOE krospíků na vzdálenost mezi atomy. 1.8 Ǻ r 2.5 Ǻ 1.8 Ǻ r 3.5 Ǻ 1.8 Ǻ r 5.0 Ǻ Dolní mez :1.8 Ǻ Jedná se o součet vzdáleností van der Waalsovských poloměrů dvou interagujících atomů vodíku Horní mez : Nastavuje se podle intenzity příslušného krospíku. Pro větší molekuly se používá max. vzdálenost až 6 Å.
53 Editovaná NOESY spektra 4D 13 C/ 15 N-editované NOESY 15 N NOE 1 H 1 H 13 C J HN 15 N 13 C J HC 1 H 1 H 3D 15 N-editované NOESY 4D 13 C/ 15 N-editované NOESY 15 N= ppm 15 N= ppm 13 C= 45.8 ppm 15 N= ppm 13 C= 56.1 ppm G78 HN -G78 H G78 HN -S77 H
54 Nepřímá spin-spinová interakční konstanta Experimentální omezení dihedrálních úhlů H O N f C C C y H H C c 1 O H c 2 C 3 J 10 8 Karplusova rovnice 3 J = A cos 2 Q B cosq C Vztah mezi interakční konstantou a dihedrálními úhly peptidu H-NC -H H-NC -CO H-NC -C 6 CO-NC -H [Hz] Q deg
55 Typické hodnoty interakčních konstant 3 J HH pro dihedrální úhel f -helix f ~ 60 deg J 6 Hz typické nastavení pro úhel f: 110 f 10 deg -struktura skládaného listu f ~ 10 6 J 9 Hz typické nastavení pro úhel f: 170 f 70 deg
56 Residual dipolar couplings RDC Long-range constraint NMR experiments: - experiments for measurement J constants - IPAP experiments (better resolution) 15 N Principal axis system B o A zz H N H D Jiso Janiso 15 N D resid J aniso J iso A xx f q A yy H
57 Stretched polyacrylamide gel ~ 6% polyacrylamide gel (crosslinked with bisacrylamide) protein diffuses into dried gel axial stretching (radial compression) of the gel NMR tube squeeze alignment of protein in oblate pores
58 -helix Vodíkové vazby v pravidelných strukturách Další omezení vzdáleností C Měření: - výměnné experimenty s D 2 O - teplotní závislost labilních protonů (NH, OH ) Z NMR experimentů je možné získat pouze informaci o donoru! -sheet-antiparalelní N Informaci o příslušném akceptoru lze získat až z vypočtených struktur N C
59 Strategie pro určování struktur biomolekul NMR vzorek NMR experimenty NMR spektra Přiřazení signálů Přiřazení experimentálních NMR parametrů (NOE ) Obecné informace o molekule (primární struktura, kovalentní vazby ) Odhad přibližné struktury Zhodnocení kvality struktur Oprava přiřazení NMR parametrů, signálů Výpočet souboru struktur Výpočet statistických údajů pro soubor konečných struktur Porovnání s databázemi (Procheck, Whatif.) Výpočet NOESY spekter
60 Jak vše poskládat dohromady???? Omezení vzdáleností (NOEs) Omezení dihedrálních úhlů (interakční konst.) Info o kovalentní struktuře Cray T3E E tot E kin E pot Výpočetní algoritmus: Molekulární mechanika simulované žíhání s experimentálními omezeními (vzdálenosti, dihedrální úhly ) - molekula se ohřeje na vysokou teplotu ( K) - pomalu se ochladí na teplotu blízkou nule simulované žíhání v Kartézském prostoru (Newtonovy pohybové rovnice) simulované žíhání v prostoru torsních úhlů (Lagrangeovy rovnice)
61 Simulované žíhání (simulated annealing) typický průběh teplota [K] vysokoteplotní perioda perioda postupného ochlazování minimalizace potenciálové energie časová osa [ns]
62 Jak vše poskládat dohromady???? E D 2 pot E tot E kin E E kin je kinetická energie vypočítávaná v každém kroku z teploty molekuly E pot je součet energií produkovaných penalizačními funkcemi Molekulární parametry (hmotnost atomů, délka vazby, vazebné úhly vstupují do výpočtu ve formě tzv force fields pot kvdw D kkovd knoed vdw kov NOE DIH ( d d exp 0 ) 2 k DIH D 2... d exp je experimentální nebo aktuální hodnota d 0 je ideální hodnota Př: penalizační fukce pro NOE: E NOE dolní mez (1,8 Å) horní mez (< 6 Å) Cílem je minimalizovat E pot 0 d Soubor struktur vyhovující nejlépe získaným experimentálním omezením
63 Prezentace vypočtených struktur helix III helix IV helix II helix I C N N C C N C N
64 Strategie pro určování struktur biomolekul NMR vzorek NMR experimenty NMR spektra Přiřazení signálů Přiřazení experimentálních NMR parametrů (NOE ) Obecné informace o molekule (primární struktura, kovalentní vazby ) Odhad přibližné struktury Zhodnocení kvality struktur Oprava přiřazení NMR parametrů, signálů Výpočet souboru struktur Výpočet statistických údajů pro soubor konečných struktur Porovnání s databázemi (Procheck, Whatif.) Výpočet NOESY spekter
65 Charakterizace vypočtených struktur 1. Shoda vypočtených struktur s experimentálními daty - velikost potenciálová energie - počet a velikost neshod s experimentálními parametry (NOE, dihedrální úhly. - počet a velikost špatných kontaktů mezi atomy (van der Waalsovský příspěvek) - počet a velikost neshod s ideálními hodnotami kovalentních parametrů (délky vazeb, vazebné úhly, planarita aromatických kruhů ) 2. Rozptyl struktur v souboru RMSD n i1 x i n x 2 - mezi jednotlivými strukturami a průměrnou strukturou (mean) - mezi jednotlivými strukturami navzájem - počítá se buď pro celou molekulu, jednotlivé části nebo jednotlivé aminokyseliny
66 Charakterizace vypočtených struktur 3. Porovnání strukturních parametrů vypočtených struktur s parametry v databázích software Procheck, Whatif Ramachandranův diagram f/y diagram je charakteristický pro konformaci páteře proteinu - takto lze porovnávat i ostatní dihedrální úhly, vazebné úhly, délky vazeb - lze vytypovat problémové oblasti
67 Malate synthase, 723 AA, 82 kda Tugarinov V., Choy W.Y., Orekhov, V.Y., Kay L.E.(2005) PNAS, 102,
68
COSY + - podmínky měření a zpracování dat ztráta rozlišení ve spektru. inphase dublet, disperzní. antiphase dublet, absorpční
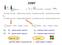 y x COSY 90 y chem. posuv J vazba 90 x : : inphase dublet, disperzní inphase dublet, disperzní antiphase dublet, absorpční antiphase dublet, absorpční diagonální pík krospík + - - + podmínky měření a zpracování
y x COSY 90 y chem. posuv J vazba 90 x : : inphase dublet, disperzní inphase dublet, disperzní antiphase dublet, absorpční antiphase dublet, absorpční diagonální pík krospík + - - + podmínky měření a zpracování
NMR spektroskopie biologicky aktivních molekul
 NMR spektroskopie biologicky aktivních molekul Jak vidí současné a budoucí uplatnění NMR spektroskopie profesor Richard Ernst. Medicine Biochemistry Nobel prize in chemistry 1991 Chemistry Physics J.W.
NMR spektroskopie biologicky aktivních molekul Jak vidí současné a budoucí uplatnění NMR spektroskopie profesor Richard Ernst. Medicine Biochemistry Nobel prize in chemistry 1991 Chemistry Physics J.W.
Dynamické procesy & Pokročilé aplikace NMR. chemická výměna, translační difuze, gradientní pulsy, potlačení rozpouštědla, NMR proteinů
 Dynamické procesy & Pokročilé aplikace NMR chemická výměna, translační difuze, gradientní pulsy, potlačení rozpouštědla, NMR proteinů Chemická výměna jakýkoli proces při kterém dané jádro mění svůj stav
Dynamické procesy & Pokročilé aplikace NMR chemická výměna, translační difuze, gradientní pulsy, potlačení rozpouštědla, NMR proteinů Chemická výměna jakýkoli proces při kterém dané jádro mění svůj stav
Využití NMR spektroskopie pro studium biomakromolekul RCSB PDB
 Využití NMR spektroskopie pro studium biomakromolekul RCSB PDB Uplatnění NMR spektroskopie chemická struktura kovalentní struktura konformace, geometrie molekul dynamické procesy chemické a konformační
Využití NMR spektroskopie pro studium biomakromolekul RCSB PDB Uplatnění NMR spektroskopie chemická struktura kovalentní struktura konformace, geometrie molekul dynamické procesy chemické a konformační
NMR biomakromolekul RCSB PDB. Progr. NMR
 NMR biomakromolekul Typy biomakromolekul a možnosti studia pomocí NMR proteiny a peptidy rozmanité složení, omezení jen velikostí molekul nukleové kyseliny (RNA, DNA) a oligonukleotidy omezení malou rozmanitostí
NMR biomakromolekul Typy biomakromolekul a možnosti studia pomocí NMR proteiny a peptidy rozmanité složení, omezení jen velikostí molekul nukleové kyseliny (RNA, DNA) a oligonukleotidy omezení malou rozmanitostí
Nukleární Overhauserův efekt (NOE)
 Nukleární Overhauserův efekt (NOE) NOE je důsledek dipolární interakce mezi dvěma jádry. Vzniká přímou interakcí volně přes prostor, tudíž není ovlivněn chemickými vazbami jako nepřímá spin-spinová interakce.
Nukleární Overhauserův efekt (NOE) NOE je důsledek dipolární interakce mezi dvěma jádry. Vzniká přímou interakcí volně přes prostor, tudíž není ovlivněn chemickými vazbami jako nepřímá spin-spinová interakce.
Experimentální data pro určení struktury proteinu
 Experimentální data pro určení struktury proteinu přiřazení co největšího počtu rezonancí intenzita NOESY krospíků chemické posuvy J-vazby vodíkové můstky zbytková dipolární interakce... omezení vzdáleností
Experimentální data pro určení struktury proteinu přiřazení co největšího počtu rezonancí intenzita NOESY krospíků chemické posuvy J-vazby vodíkové můstky zbytková dipolární interakce... omezení vzdáleností
spinový rotační moment (moment hybnosti) kvantové číslo jaderného spinu I pro NMR - jádra s I 0
 Spektroskopie NMR - teoretické základy spin nukleonů, spin jádra, kvantová čísla energetické stavy jádra v magnetickém poli rezonanční podmínka - instrumentace pulsní metody, pulsní sekvence relaxační
Spektroskopie NMR - teoretické základy spin nukleonů, spin jádra, kvantová čísla energetické stavy jádra v magnetickém poli rezonanční podmínka - instrumentace pulsní metody, pulsní sekvence relaxační
ZÁKLADNÍ EXPERIMENTÁLNÍ
 Kurz praktické NMR spektroskopie 10. - 12. říjen 2011, Praha ZÁKLADNÍ EXPERIMENTÁLNÍ POSTUPY NMR ROZTOKŮ A KAPALIN Jana Svobodová Ústav Makromolekulární chemie AV ČR, v.v.i. Bruker 600 Avance III PŘÍSTROJOVÉ
Kurz praktické NMR spektroskopie 10. - 12. říjen 2011, Praha ZÁKLADNÍ EXPERIMENTÁLNÍ POSTUPY NMR ROZTOKŮ A KAPALIN Jana Svobodová Ústav Makromolekulární chemie AV ČR, v.v.i. Bruker 600 Avance III PŘÍSTROJOVÉ
Základní parametry 1 H NMR spekter
 LEKCE 1a Základní parametry 1 NMR spekter Počet signálů ve spektru (zjištění počtu skupin chemicky ekvivalentních jader) Integrální intenzita (intenzita pásů závisí na počtu jader) Chemický posun (polohy
LEKCE 1a Základní parametry 1 NMR spekter Počet signálů ve spektru (zjištění počtu skupin chemicky ekvivalentních jader) Integrální intenzita (intenzita pásů závisí na počtu jader) Chemický posun (polohy
Metody spektrální. Metody molekulové spektroskopie NMR. Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti
 Metody spektrální Metody molekulové spektroskopie NMR Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti Spektroskopie NMR - teoretické základy spin nukleonů, spin jádra, kvantová čísla
Metody spektrální Metody molekulové spektroskopie NMR Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti Spektroskopie NMR - teoretické základy spin nukleonů, spin jádra, kvantová čísla
Nukleární Overhauserův efekt (NOE)
 LEKCE 8 Nukleární verhauserův efekt (NE) určení prostorové struktury molekul využití REY spektroskopie projevy NE a chemické výměny v jednom systému Nukleární verhauserův efekt (NE) důsledek dipolární
LEKCE 8 Nukleární verhauserův efekt (NE) určení prostorové struktury molekul využití REY spektroskopie projevy NE a chemické výměny v jednom systému Nukleární verhauserův efekt (NE) důsledek dipolární
Základy NMR 2D spektroskopie
 Základy NMR 2D spektroskopie Jaroslav Kříž Ústav makromolekulární chemie AV ČR v.v.i. puls 1D : d 1 Fourierova transformace časového rozvoje odezvy dá 1D spektrum 2D: d 1 d 1 d 1 d 0 d 0 + in 0 d 0 + 2in
Základy NMR 2D spektroskopie Jaroslav Kříž Ústav makromolekulární chemie AV ČR v.v.i. puls 1D : d 1 Fourierova transformace časového rozvoje odezvy dá 1D spektrum 2D: d 1 d 1 d 1 d 0 d 0 + in 0 d 0 + 2in
Měření a interpretace NMR spekter
 Měření a interpretace NMR spekter Bohumil Dolenský E-mail : Telefon : Místnost : www : dolenskb@vscht.cz (+420) 220 44 4110 budova A, místnost 28 http://www.vscht.cz/anl/dolensky/technmr/index.html Řešení
Měření a interpretace NMR spekter Bohumil Dolenský E-mail : Telefon : Místnost : www : dolenskb@vscht.cz (+420) 220 44 4110 budova A, místnost 28 http://www.vscht.cz/anl/dolensky/technmr/index.html Řešení
LEKCE 1b. Základní parametry 1 H NMR spekter. Symetrie v NMR spektrech: homotopické, enantiotopické, diastereotopické protony (skupiny)*
 Základní parametry 1 NMR spekter LEKCE 1b Symetrie v NMR spektrech: homotopické, enantiotopické, diastereotopické protony (skupiny)* 3.5 3.0 2.5 2.0 1.5 Základní parametry 1 NMR spekter Počet signálů ve
Základní parametry 1 NMR spekter LEKCE 1b Symetrie v NMR spektrech: homotopické, enantiotopické, diastereotopické protony (skupiny)* 3.5 3.0 2.5 2.0 1.5 Základní parametry 1 NMR spekter Počet signálů ve
NMR spektroskopie. Úvod
 NMR spektroskopie Úvod Zkratka NMR znamená Nukleární Magnetická Rezonance. Jde o analytickou metodu, která na základě absorpce radiofrekvenčního záření vzorkem umístěným v silném magnetickém poli poskytuje
NMR spektroskopie Úvod Zkratka NMR znamená Nukleární Magnetická Rezonance. Jde o analytickou metodu, která na základě absorpce radiofrekvenčního záření vzorkem umístěným v silném magnetickém poli poskytuje
LEKCE 3b. Využití 2D experimentů k přiřazení složitější molekuly. Zpracování, výpočet a databáze NMR spekter (ACD/Labs, Topspin, Mnova) ppm
 LEKCE 3b Využití D experimentů k přiřazení složitější molekuly ppm ppm 10 1.0 1.5 15.0 130.5 3.0 135 3.5 140 4.0 4.5 145 5.0 150 5.5 155 6.0 6.5 6.5 6.0 5.5 5.0 4.5 4.0 3.5 3.0.5.0 1.5 1.0 ppm 160.6.4..0
LEKCE 3b Využití D experimentů k přiřazení složitější molekuly ppm ppm 10 1.0 1.5 15.0 130.5 3.0 135 3.5 140 4.0 4.5 145 5.0 150 5.5 155 6.0 6.5 6.5 6.0 5.5 5.0 4.5 4.0 3.5 3.0.5.0 1.5 1.0 ppm 160.6.4..0
Studium komplexace -cyklodextrinu s diclofenacem s využitím NMR spektroskopie
 Jména: Datum: Studium komplexace -cyklodextrinu s diclofenacem s využitím NMR spektroskopie Cílem laboratorního cvičení je prozkoumat interakce léčiva diclofenac s -cyklodextrinem v D 2 O při tvorbě komplexu
Jména: Datum: Studium komplexace -cyklodextrinu s diclofenacem s využitím NMR spektroskopie Cílem laboratorního cvičení je prozkoumat interakce léčiva diclofenac s -cyklodextrinem v D 2 O při tvorbě komplexu
12.NMR spektrometrie při analýze roztoků
 Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti 12.NMR spektrometrie při analýze roztoků Pavel Matějka pavel.matejka@vscht.cz pavel.matejka@gmail.com 12.NMR spektrometrie při analýze
Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti 12.NMR spektrometrie při analýze roztoků Pavel Matějka pavel.matejka@vscht.cz pavel.matejka@gmail.com 12.NMR spektrometrie při analýze
LEKCE 7. Interpretace 13 C NMR spekter. Využití 2D experimentů. Zpracování, výpočet a databáze NMR spekter (ACD/Labs, Topspin, Mnova) ppm
 LEKCE 7 Interpretace 13 C MR spekter Využití 2D experimentů ppm 1.0 1.5 2.0 2.5 3.0 3.5 4.0 4.5 5.0 5.5 6.0 6.5 6.5 6.0 5.5 5.0 4.5 4.0 3.5 3.0 2.5 2.0 1.5 1.0 ppm Zpracování, výpočet a databáze MR spekter
LEKCE 7 Interpretace 13 C MR spekter Využití 2D experimentů ppm 1.0 1.5 2.0 2.5 3.0 3.5 4.0 4.5 5.0 5.5 6.0 6.5 6.5 6.0 5.5 5.0 4.5 4.0 3.5 3.0 2.5 2.0 1.5 1.0 ppm Zpracování, výpočet a databáze MR spekter
Naše NMR spektrometry
 Naše NMR spektrometry Varian NMR System 300 MHz Varian INOVA 400 MHz Bruker Avance III 600 MHz NMR spektrometr magnet průřez supravodičem NMR spektrometr sonda Tvar spektra reálná část imaginární část
Naše NMR spektrometry Varian NMR System 300 MHz Varian INOVA 400 MHz Bruker Avance III 600 MHz NMR spektrometr magnet průřez supravodičem NMR spektrometr sonda Tvar spektra reálná část imaginární část
SPEKTROSKOPIE NUKLEÁRNÍ MAGNETICKÉ REZONANCE
 SPEKTROSKOPIE NUKLEÁRNÍ MAGNETICKÉ REZONANCE Obecné základy nedestruktivní metoda strukturní analýzy zabývá se rezonancí atomových jader nutná podmínka pro měření spekter: nenulový spin atomového jádra
SPEKTROSKOPIE NUKLEÁRNÍ MAGNETICKÉ REZONANCE Obecné základy nedestruktivní metoda strukturní analýzy zabývá se rezonancí atomových jader nutná podmínka pro měření spekter: nenulový spin atomového jádra
O Minimální počet valencí potřebných ke spojení vícevazných atomů = (24 C + 3 O + 7 N 1) * 2 = 66 valencí
 Jméno a příjmení:_bohumil_dolenský_ Datum:_10.12.2010_ Fakulta:_FCHI_ Kruh:_ÚACh_ 1. Sepište seznam signálů 1 H dle klesajícího chemického posunu (včetně nečistot), uveďte chemický posun, multiplicitu
Jméno a příjmení:_bohumil_dolenský_ Datum:_10.12.2010_ Fakulta:_FCHI_ Kruh:_ÚACh_ 1. Sepište seznam signálů 1 H dle klesajícího chemického posunu (včetně nečistot), uveďte chemický posun, multiplicitu
Význam interakční konstanty, Karplusova rovnice. konfigurace na dvojné vazbě a na šestičlenných kruzích konformace furanosového kruhu TOCSY
 Význam interakční konstanty, Karplusova rovnice konfigurace na dvojné vazbě a na šestičlenných kruzích konformace furanosového kruhu TOCSY Karplusova rovnice ve strukturní analýze J(H,H) = A + B cos f
Význam interakční konstanty, Karplusova rovnice konfigurace na dvojné vazbě a na šestičlenných kruzích konformace furanosového kruhu TOCSY Karplusova rovnice ve strukturní analýze J(H,H) = A + B cos f
Základy Mössbauerovy spektroskopie. Libor Machala
 Základy Mössbauerovy spektroskopie Libor Machala Rudolf L. Mössbauer 1958: jev bezodrazové rezonanční absorpce záření gama atomovým jádrem 1961: Nobelova cena Analogie s rezonanční absorpcí akustických
Základy Mössbauerovy spektroskopie Libor Machala Rudolf L. Mössbauer 1958: jev bezodrazové rezonanční absorpce záření gama atomovým jádrem 1961: Nobelova cena Analogie s rezonanční absorpcí akustických
Spektra 1 H NMR. Velmi zjednodušeně! Bohumil Dolenský
 Spektra 1 MR Velmi zjednodušeně! Bohumil Dolenský Spektra 1 MR... Počet signálů C 17 18 2 O 2 MeO Počet signálů = počet neekvivalentních skupin OMe = informace o symetrii molekuly Spektrum 1 MR... Počet
Spektra 1 MR Velmi zjednodušeně! Bohumil Dolenský Spektra 1 MR... Počet signálů C 17 18 2 O 2 MeO Počet signálů = počet neekvivalentních skupin OMe = informace o symetrii molekuly Spektrum 1 MR... Počet
Dvourozměrná NMR spektroskopie metody
 Dvourozměrná NMR spektroskopie metody Marcela Strnadová 1D-NMR: experimentální FID je funkcí jediné časové proměnné - detekčního času t 2, spektrum získané Fourierovou transformací je funkcí frekvence
Dvourozměrná NMR spektroskopie metody Marcela Strnadová 1D-NMR: experimentální FID je funkcí jediné časové proměnné - detekčního času t 2, spektrum získané Fourierovou transformací je funkcí frekvence
Postup při interpretaci NMR spekter neznámého vzorku
 Postup při interpretaci NMR spekter neznámého vzorku VŠCT 2017, Bohumil Dolenský, dolenskb@vscht.cz Tento text byl vypracován pro projekt Inovace předmětu Semestrální práce oboru analytická chemie I. Slouží
Postup při interpretaci NMR spekter neznámého vzorku VŠCT 2017, Bohumil Dolenský, dolenskb@vscht.cz Tento text byl vypracován pro projekt Inovace předmětu Semestrální práce oboru analytická chemie I. Slouží
Korelační spektroskopie jako základ multidimensionální NMR spektroskopie
 Korelační spektroskopie jako základ multidimensionální NMR spektroskopie Richard Hrabal Laboratoř NMR spektroskopie, Vysoká škola chemicko-technologická v Praze, Technická 5, 166 28 Praha 6, tel. 220 443
Korelační spektroskopie jako základ multidimensionální NMR spektroskopie Richard Hrabal Laboratoř NMR spektroskopie, Vysoká škola chemicko-technologická v Praze, Technická 5, 166 28 Praha 6, tel. 220 443
02 Nevazebné interakce
 02 Nevazebné interakce Nevazebné interakce Druh chemické vazby Určují 3D konfiguraci makromolekul, účastní se mnoha biologických procesů, zodpovědné za uspořádání molekul v krystalu Síla nevazebných interakcí
02 Nevazebné interakce Nevazebné interakce Druh chemické vazby Určují 3D konfiguraci makromolekul, účastní se mnoha biologických procesů, zodpovědné za uspořádání molekul v krystalu Síla nevazebných interakcí
Analýza směsí, kvantitativní NMR spektroskopie a využití NMR spektroskopie ve forenzní analýze
 Analýza směsí, kvantitativní NMR spektroskopie a využití NMR spektroskopie ve forenzní analýze Analýza směsí a kvantitativní NMR NMR spektrum čisté látky je lineární kombinací spekter jejích jednotlivých
Analýza směsí, kvantitativní NMR spektroskopie a využití NMR spektroskopie ve forenzní analýze Analýza směsí a kvantitativní NMR NMR spektrum čisté látky je lineární kombinací spekter jejích jednotlivých
Dekapling, koherentní transfer polarizace, nukleární Overhauserův jev
 Dekapling Dekapling, koherentní transfer polarizace, nukleární Overhauserův jev Dekaplingem rozumíme odstranění vlivu J-vazby XA na na spektra jader A působením dalšího radiofrekvenčního pole ( ω X )na
Dekapling Dekapling, koherentní transfer polarizace, nukleární Overhauserův jev Dekaplingem rozumíme odstranění vlivu J-vazby XA na na spektra jader A působením dalšího radiofrekvenčního pole ( ω X )na
Počítačová chemie. výpočetně náročné simulace chemických a biomolekulárních systémů. Zora Střelcová
 Počítačová chemie výpočetně náročné simulace chemických a biomolekulárních systémů Zora Střelcová Národní centrum pro výzkum biomolekul, Masarykova univerzita, Kotlářská 2, 611 37 Brno, Česká Republika
Počítačová chemie výpočetně náročné simulace chemických a biomolekulárních systémů Zora Střelcová Národní centrum pro výzkum biomolekul, Masarykova univerzita, Kotlářská 2, 611 37 Brno, Česká Republika
Úvod do strukturní analýzy farmaceutických látek
 Úvod do strukturní analýzy farmaceutických látek Garant předmětu: doc. Ing. Bohumil Dolenský, Ph.D. A28, linka 40, dolenskb@vscht.cz Nukleární Magnetická Rezonance II. Příprava předmětu byla podpořena
Úvod do strukturní analýzy farmaceutických látek Garant předmětu: doc. Ing. Bohumil Dolenský, Ph.D. A28, linka 40, dolenskb@vscht.cz Nukleární Magnetická Rezonance II. Příprava předmětu byla podpořena
Mezimolekulové interakce
 Mezimolekulové interakce Interakce molekul reaktivně vzniká či zaniká kovalentní vazba překryv elektronových oblaků, mění se vlastnosti nereaktivně vznikají molekulové komplexy slabá, nekovalentní, nechemická,
Mezimolekulové interakce Interakce molekul reaktivně vzniká či zaniká kovalentní vazba překryv elektronových oblaků, mění se vlastnosti nereaktivně vznikají molekulové komplexy slabá, nekovalentní, nechemická,
Nukleární magnetická rezonance (NMR)
 Nukleární magnetická rezonance (NMR) Mgr. Zdeněk Moravec, Ph.D. Úvod Zkratka NMR znamená Nukleární Magnetická Rezonance. Jde o analytickou metodu, která na základě absorpce radiofrekvenčního záření vzorkem
Nukleární magnetická rezonance (NMR) Mgr. Zdeněk Moravec, Ph.D. Úvod Zkratka NMR znamená Nukleární Magnetická Rezonance. Jde o analytickou metodu, která na základě absorpce radiofrekvenčního záření vzorkem
Nekovalentní interakce
 Nekovalentní interakce Jan Řezáč UOCHB AV ČR 3. listopadu 2016 Jan Řezáč (UOCHB AV ČR) Nekovalentní interakce 3. listopadu 2016 1 / 28 Osnova 1 Teorie 2 Typy nekovalentních interakcí 3 Projevy v chemii
Nekovalentní interakce Jan Řezáč UOCHB AV ČR 3. listopadu 2016 Jan Řezáč (UOCHB AV ČR) Nekovalentní interakce 3. listopadu 2016 1 / 28 Osnova 1 Teorie 2 Typy nekovalentních interakcí 3 Projevy v chemii
Význam interakční konstanty, Karplusova rovnice
 LEKCE 9 Význam interakční konstanty, Karplusova rovnice konfigurace na dvojné vazbě a na šestičlenných kruzích konformace furanosového kruhu TCSY T E E 1 E 1 T 0 6 T E 1 T 0 88 7 0 T E 0 0 E T 0 5 108
LEKCE 9 Význam interakční konstanty, Karplusova rovnice konfigurace na dvojné vazbě a na šestičlenných kruzích konformace furanosového kruhu TCSY T E E 1 E 1 T 0 6 T E 1 T 0 88 7 0 T E 0 0 E T 0 5 108
Autoři: Pavel Zachař, David Sýkora Ukázky spekter k procvičování na semináři: Tento soubor je pouze prvním ilustrativním seznámením se základními prin
 Autoři: Pavel Zachař, David Sýkora Ukázky spekter k procvičování na semináři: Tento soubor je pouze prvním ilustrativním seznámením se základními principy hmotnostní spektrometrie a v žádném případě nezahrnuje
Autoři: Pavel Zachař, David Sýkora Ukázky spekter k procvičování na semináři: Tento soubor je pouze prvním ilustrativním seznámením se základními principy hmotnostní spektrometrie a v žádném případě nezahrnuje
Nekovalentní interakce
 Nekovalentní interakce Jan Řezáč UOCHB AV ČR 31. října 2017 Jan Řezáč (UOCHB AV ČR) Nekovalentní interakce 31. října 2017 1 / 28 Osnova 1 Teorie 2 Typy nekovalentních interakcí 3 Projevy v chemii 4 Výpočty
Nekovalentní interakce Jan Řezáč UOCHB AV ČR 31. října 2017 Jan Řezáč (UOCHB AV ČR) Nekovalentní interakce 31. října 2017 1 / 28 Osnova 1 Teorie 2 Typy nekovalentních interakcí 3 Projevy v chemii 4 Výpočty
Molekulární krystal vazebné poměry. Bohumil Kratochvíl
 Molekulární krystal vazebné poměry Bohumil Kratochvíl Předmět: Chemie a fyzika pevných léčiv, 2017 Složení farmaceutických substancí - API Z celkového portfolia API tvoří asi 90 % organické sloučeniny,
Molekulární krystal vazebné poměry Bohumil Kratochvíl Předmět: Chemie a fyzika pevných léčiv, 2017 Složení farmaceutických substancí - API Z celkového portfolia API tvoří asi 90 % organické sloučeniny,
LEKCE 2b. NMR a chiralita, posunová činidla. Interpretace 13 C NMR spekter
 LEKCE 2b NMR a chiralita, posunová činidla Interpretace 13 C NMR spekter Stanovení optické čistoty Enantiomery jsou nerozlišitelné v NMR spektroskopii není možné rozlišit enantiomer od racemátu!!! Enantiotopické
LEKCE 2b NMR a chiralita, posunová činidla Interpretace 13 C NMR spekter Stanovení optické čistoty Enantiomery jsou nerozlišitelné v NMR spektroskopii není možné rozlišit enantiomer od racemátu!!! Enantiotopické
NMR spektroskopie Instrumentální a strukturní analýza
 NMR spektroskopie Instrumentální a strukturní analýza prof. RNDr. Zdeněk Friedl, CSc. Použitá a doporučená literatura Solomons T.W.G., Fryhle C.B.: Organic Chemistry, 8th Ed., Wiley 2004. Günther H.: NMR
NMR spektroskopie Instrumentální a strukturní analýza prof. RNDr. Zdeněk Friedl, CSc. Použitá a doporučená literatura Solomons T.W.G., Fryhle C.B.: Organic Chemistry, 8th Ed., Wiley 2004. Günther H.: NMR
OPVK CZ.1.07/2.2.00/
 18.2.2013 OPVK CZ.1.07/2.2.00/28.0184 Cvičení z NMR OCH/NMR Mgr. Tomáš Pospíšil, Ph.D. LS 2012/2013 18.2.2013 NMR základní principy NMR Nukleární Magnetická Resonance N - nukleární (studujeme vlastnosti
18.2.2013 OPVK CZ.1.07/2.2.00/28.0184 Cvičení z NMR OCH/NMR Mgr. Tomáš Pospíšil, Ph.D. LS 2012/2013 18.2.2013 NMR základní principy NMR Nukleární Magnetická Resonance N - nukleární (studujeme vlastnosti
Autor: martina urbanová, jiří brus. Základní experimentální postupy NMR spektroskopie pevného stavu
 Autor: martina urbanová, jiří brus Základní experimentální postupy NMR spektroskopie pevného stavu Obsah přednášky anizotropní interakce v pevných látkách techniky rušení anizotropie jaderných interakcí
Autor: martina urbanová, jiří brus Základní experimentální postupy NMR spektroskopie pevného stavu Obsah přednášky anizotropní interakce v pevných látkách techniky rušení anizotropie jaderných interakcí
Opakování
 Slabé vazebné interakce Opakování Co je to atom? Opakování Opakování Co je to atom? Atom je nejmenší částice hmoty, chemicky dále nedělitelná. Skládá se z atomového jádra obsahujícího protony a neutrony
Slabé vazebné interakce Opakování Co je to atom? Opakování Opakování Co je to atom? Atom je nejmenší částice hmoty, chemicky dále nedělitelná. Skládá se z atomového jádra obsahujícího protony a neutrony
Aplikovaná bioinformatika
 Aplikovaná bioinformatika Číslo aktivity: 2.V Název klíčové aktivity: Na realizaci se podílí: Implementace nových předmětů do daného studijního programu doc. RNDr. Michaela Wimmerová, Ph.D., Mgr. Josef
Aplikovaná bioinformatika Číslo aktivity: 2.V Název klíčové aktivity: Na realizaci se podílí: Implementace nových předmětů do daného studijního programu doc. RNDr. Michaela Wimmerová, Ph.D., Mgr. Josef
Typy molekul, látek a jejich vazeb v organismech
 Typy molekul, látek a jejich vazeb v organismech Typy molekul, látek a jejich vazeb v organismech Organismy se skládají z molekul rozličných látek Jednotlivé látky si organismus vytváří sám z jiných látek,
Typy molekul, látek a jejich vazeb v organismech Typy molekul, látek a jejich vazeb v organismech Organismy se skládají z molekul rozličných látek Jednotlivé látky si organismus vytváří sám z jiných látek,
Skupenské stavy. Kapalina Částečně neuspořádané Volný pohyb částic nebo skupin částic Částice blíže u sebe
 Skupenské stavy Plyn Zcela neuspořádané Hodně volného prostoru Zcela volný pohyb částic Částice daleko od sebe Kapalina Částečně neuspořádané Volný pohyb částic nebo skupin částic Částice blíže u sebe
Skupenské stavy Plyn Zcela neuspořádané Hodně volného prostoru Zcela volný pohyb částic Částice daleko od sebe Kapalina Částečně neuspořádané Volný pohyb částic nebo skupin částic Částice blíže u sebe
Nukleární magnetická rezonance (NMR)
 Nukleární magnetická rezonance (NMR) Nukleární magnetické rezonance (NMR) princip ZDROJ E = h. elektro-magnetické záření E energie záření h Plankova konstanta frekvence záření VZOREK E E 1 E 0 DETEKTOR
Nukleární magnetická rezonance (NMR) Nukleární magnetické rezonance (NMR) princip ZDROJ E = h. elektro-magnetické záření E energie záření h Plankova konstanta frekvence záření VZOREK E E 1 E 0 DETEKTOR
STANOVENÍ STRUKTURY LÁTEK
 STANOVENÍ STRUKTURY LÁTEK 1nm 10 10 2 10 3 10 4 10 5 10 6 10 7 (the wave) X-ray UV/VIS Infrared Microwave Radio Frequency (the transition) electronic Vibration Rotation Nuclear (spectrometer) X-ray UV/VIS
STANOVENÍ STRUKTURY LÁTEK 1nm 10 10 2 10 3 10 4 10 5 10 6 10 7 (the wave) X-ray UV/VIS Infrared Microwave Radio Frequency (the transition) electronic Vibration Rotation Nuclear (spectrometer) X-ray UV/VIS
Základní parametry 1 H NMR spekter
 LEKCE 6 Základní parametry 1 NMR spekter Počet signálů ve spektru (zjištění počtu skupin chemicky ekvivalentních jader) Integrální intenzita (intenzita pásů závisí na počtu jader) Chemický posun (polohy
LEKCE 6 Základní parametry 1 NMR spekter Počet signálů ve spektru (zjištění počtu skupin chemicky ekvivalentních jader) Integrální intenzita (intenzita pásů závisí na počtu jader) Chemický posun (polohy
Hemoglobin a jemu podobní... Studijní materiál. Jan Komárek
 Hemoglobin a jemu podobní... Studijní materiál Jan Komárek Bioinformatika Bioinformatika je vědní disciplína, která se zabývá metodami pro shromážďování, analýzu a vizualizaci rozsáhlých souborů biologických
Hemoglobin a jemu podobní... Studijní materiál Jan Komárek Bioinformatika Bioinformatika je vědní disciplína, která se zabývá metodami pro shromážďování, analýzu a vizualizaci rozsáhlých souborů biologických
Symetrie v NMR spektrech: homotopické, enantiotopické, diastereotopické protony (skupiny)*
 Základní parametry 1 NMR spekter NMR a chiralita, posunová činidla Symetrie v NMR spektrech: homotopické, enantiotopické, diastereotopické protony (skupiny)* 3.5 3.0 2.5 2.0 1.5 Základní parametry 1 NMR
Základní parametry 1 NMR spekter NMR a chiralita, posunová činidla Symetrie v NMR spektrech: homotopické, enantiotopické, diastereotopické protony (skupiny)* 3.5 3.0 2.5 2.0 1.5 Základní parametry 1 NMR
Optické spektroskopie 1 LS 2014/15
 Optické spektroskopie 1 LS 2014/15 Martin Kubala 585634179 mkubala@prfnw.upol.cz 1.Úvod Velikosti objektů v přírodě Dítě ~ 1 m (10 0 m) Prst ~ 2 cm (10-2 m) Vlas ~ 0.1 mm (10-4 m) Buňka ~ 20 m (10-5 m)
Optické spektroskopie 1 LS 2014/15 Martin Kubala 585634179 mkubala@prfnw.upol.cz 1.Úvod Velikosti objektů v přírodě Dítě ~ 1 m (10 0 m) Prst ~ 2 cm (10-2 m) Vlas ~ 0.1 mm (10-4 m) Buňka ~ 20 m (10-5 m)
Seminář NMR. Mgr. Zdeněk Moravec, Ph.D.; hugo@chemi.muni.cz Ústav chemie, PřF MU, 22.-25. 7. 2013 http://nmrlab.chemi.muni.cz/
 Seminář NMR Mgr. Zdeněk Moravec, Ph.D.; hugo@chemi.muni.cz Ústav chemie, PřF MU, 22.-25. 7. 2013 http://nmrlab.chemi.muni.cz/ Osnova Úvod, základní princip Instrumentace magnety, měřící sondy, elektronika
Seminář NMR Mgr. Zdeněk Moravec, Ph.D.; hugo@chemi.muni.cz Ústav chemie, PřF MU, 22.-25. 7. 2013 http://nmrlab.chemi.muni.cz/ Osnova Úvod, základní princip Instrumentace magnety, měřící sondy, elektronika
Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti LC-NMR 1. Jan Sýkora
 Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti LC-NMR 1 Jan Sýkora LC/NMR Jan Sýkora (ÚCHP AV ČR) LC - NMR 1 H NMR (500 MHz) mez detekce ~ 1 mg/ml (5 µmol látky) NMR parametry doba
Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti LC-NMR 1 Jan Sýkora LC/NMR Jan Sýkora (ÚCHP AV ČR) LC - NMR 1 H NMR (500 MHz) mez detekce ~ 1 mg/ml (5 µmol látky) NMR parametry doba
Diskutujte, jak široký bude pás spojený s fosforescencí versus fluorescencí. Udělejte odhad v cm -1.
 S použitím modelu volného elektronu (=částice v krabici) spočtěte vlnovou délku a vlnočet nejdlouhovlnějšího elektronového přechodu u molekuly dekapentaenu a oktatetraenu. Diskutujte polohu absorpčního
S použitím modelu volného elektronu (=částice v krabici) spočtěte vlnovou délku a vlnočet nejdlouhovlnějšího elektronového přechodu u molekuly dekapentaenu a oktatetraenu. Diskutujte polohu absorpčního
Genomické databáze. Shlukování proteinových sekvencí. Ivana Rudolfová. školitel: doc. Ing. Jaroslav Zendulka, CSc.
 Genomické databáze Shlukování proteinových sekvencí Ivana Rudolfová školitel: doc. Ing. Jaroslav Zendulka, CSc. Obsah Proteiny Zdroje dat Predikce struktury proteinů Cíle disertační práce Vstupní data
Genomické databáze Shlukování proteinových sekvencí Ivana Rudolfová školitel: doc. Ing. Jaroslav Zendulka, CSc. Obsah Proteiny Zdroje dat Predikce struktury proteinů Cíle disertační práce Vstupní data
jako modelové látky pro studium elektronických vlivů při katalytických hydrogenacích
 Pt(0) komplexy jako modelové látky pro studium elektronických vlivů při katalytických hydrogenacích David Karhánek Školitelé: Ing. Petr Kačer, PhD.; Ing. Marek Kuzma Katalytické hydrogenace eterogenní
Pt(0) komplexy jako modelové látky pro studium elektronických vlivů při katalytických hydrogenacích David Karhánek Školitelé: Ing. Petr Kačer, PhD.; Ing. Marek Kuzma Katalytické hydrogenace eterogenní
Struktura proteinů. - testík na procvičení. Vladimíra Kvasnicová
 Struktura proteinů - testík na procvičení Vladimíra Kvasnicová Mezi proteinogenní aminokyseliny patří a) kyselina asparagová b) kyselina glutarová c) kyselina acetoctová d) kyselina glutamová Mezi proteinogenní
Struktura proteinů - testík na procvičení Vladimíra Kvasnicová Mezi proteinogenní aminokyseliny patří a) kyselina asparagová b) kyselina glutarová c) kyselina acetoctová d) kyselina glutamová Mezi proteinogenní
Program. Materiály ke studiu NMR. Data, Soubory. Seminář z Analytické chemie B. \\PYR\SCRATCH\
 Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti Seminář z Analytické chemie B Tento materiál vznikl za podpory projektu CHEMnote PPA CZ..7/../48 Inovace bakalářského studijního programu
Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti Seminář z Analytické chemie B Tento materiál vznikl za podpory projektu CHEMnote PPA CZ..7/../48 Inovace bakalářského studijního programu
10A1_IR spektroskopie
 C6200-Biochemické metody 10A1_IR spektroskopie Petr Zbořil IR spektroskopie Excitace vibračních a rotačních přechodů Valenční vibrace n Deformační vibrace d IR spektroskopie N atomů = 3N stupňů volnosti
C6200-Biochemické metody 10A1_IR spektroskopie Petr Zbořil IR spektroskopie Excitace vibračních a rotačních přechodů Valenční vibrace n Deformační vibrace d IR spektroskopie N atomů = 3N stupňů volnosti
(9) X-X a X-Y korelace zvýšení spektrálního rozlišení
 (9) X-X a X-Y korelace zvýšení spektrálního rozlišení 90 ±y 1 H: CP Decoupling (TPPM) 13 C: 180 t t t 1 180 t t Acquisition t 2 ppm 6 1 11 15 17 9 5 3 4 13 2 19 7 140 6/ 7 7/ 6 160 180 200 220 240 260
(9) X-X a X-Y korelace zvýšení spektrálního rozlišení 90 ±y 1 H: CP Decoupling (TPPM) 13 C: 180 t t t 1 180 t t Acquisition t 2 ppm 6 1 11 15 17 9 5 3 4 13 2 19 7 140 6/ 7 7/ 6 160 180 200 220 240 260
Strukturní analýza. NMR spektroskopie
 Strukturní analýza NMR spektroskopie RNDr. Zdeněk Tošner, Ph.D. lavova 8, místnost 020 tel. 22195 1323 tosner@natur.cuni.cz www.natur.cuni.cz/nmr/vyuka.html Literatura Böhm, Smrčková-Voltrová: Strukturní
Strukturní analýza NMR spektroskopie RNDr. Zdeněk Tošner, Ph.D. lavova 8, místnost 020 tel. 22195 1323 tosner@natur.cuni.cz www.natur.cuni.cz/nmr/vyuka.html Literatura Böhm, Smrčková-Voltrová: Strukturní
Magnetická rezonance (3)
 Magnetická rezonance (3) J. Kybic, J. Hornak 1, M. Bock, J. Hozman 2008 2018 1 http://www.cis.rit.edu/htbooks/mri/ MRI zobrazovací techniky Multislice imaging Šikmé zobrazování Spinové echo Inversion recovery
Magnetická rezonance (3) J. Kybic, J. Hornak 1, M. Bock, J. Hozman 2008 2018 1 http://www.cis.rit.edu/htbooks/mri/ MRI zobrazovací techniky Multislice imaging Šikmé zobrazování Spinové echo Inversion recovery
Využití magneticko-rezonanční tomografie v měřicí technice. Ing. Jan Mikulka, Ph.D. Ing. Petr Marcoň
 Využití magneticko-rezonanční tomografie v měřicí technice Ing. Jan Mikulka, Ph.D. Ing. Petr Marcoň Osnova Podstata nukleární magnetické rezonance (MR) Historie vývoje MR Spektroskopie MRS Tomografie MRI
Využití magneticko-rezonanční tomografie v měřicí technice Ing. Jan Mikulka, Ph.D. Ing. Petr Marcoň Osnova Podstata nukleární magnetické rezonance (MR) Historie vývoje MR Spektroskopie MRS Tomografie MRI
Vybrané kapitoly z praktické NMR spektroskopie
 Vybrané kapitoly z praktické NMR spektroskopie DRX 500 Avance SPECTROSPIN 500 Způsob snímání dat, CW versus FT CW frekvence RF záření postupně se mění B eff 2 efektivní magnetické pole zůstává konstantní
Vybrané kapitoly z praktické NMR spektroskopie DRX 500 Avance SPECTROSPIN 500 Způsob snímání dat, CW versus FT CW frekvence RF záření postupně se mění B eff 2 efektivní magnetické pole zůstává konstantní
Magnetická rezonance (3)
 Magnetická rezonance (3) J. Kybic, J. Hornak 1, M. Bock, J. Hozman April 28, 2008 1 http://www.cis.rit.edu/htbooks/mri/ MRI zobrazovací techniky Multislice imaging Šikmé zobrazování Spinové echo Inversion
Magnetická rezonance (3) J. Kybic, J. Hornak 1, M. Bock, J. Hozman April 28, 2008 1 http://www.cis.rit.edu/htbooks/mri/ MRI zobrazovací techniky Multislice imaging Šikmé zobrazování Spinové echo Inversion
Skupenské stavy látek. Mezimolekulární síly
 Skupenské stavy látek Mezimolekulární síly 1 Interakce iont-dipól Např. hydratační (solvatační) interakce mezi Na + (iont) a molekulou vody (dipól). Jde o nejsilnější mezimolekulární (nevazebnou) interakci.
Skupenské stavy látek Mezimolekulární síly 1 Interakce iont-dipól Např. hydratační (solvatační) interakce mezi Na + (iont) a molekulou vody (dipól). Jde o nejsilnější mezimolekulární (nevazebnou) interakci.
Vazebné interakce protein s DNA
 Vazebné interakce protein s DNA Vazebné možnosti vn jší vazba atmosféra + iont kolem nabité DNA vazba ve žlábku van der Waalsovský kontakt s lé ivem ve žlábku interkalace vmeze ení planárního aromat.
Vazebné interakce protein s DNA Vazebné možnosti vn jší vazba atmosféra + iont kolem nabité DNA vazba ve žlábku van der Waalsovský kontakt s lé ivem ve žlábku interkalace vmeze ení planárního aromat.
Přednáška IX: Elektronová spektroskopie II.
 Přednáška IX: Elektronová spektroskopie II. 1 Försterův resonanční přenos energie Pravděpodobnost (rychlost) přenosu je určená jako: k ret 1 = τ 0 D R r 0 6 0 τ D R 0 r Doba života donoru v excitovaném
Přednáška IX: Elektronová spektroskopie II. 1 Försterův resonanční přenos energie Pravděpodobnost (rychlost) přenosu je určená jako: k ret 1 = τ 0 D R r 0 6 0 τ D R 0 r Doba života donoru v excitovaném
Techniky přenosu polarizace cross -polarizace a spinová difuse
 (3) jiri brus Techniky přenosu polarizace cross -polarizace a spinová difuse laboratory frame, spin rotating frame laboratory frame, spin Ω H B H ω, ω, ω 0, B H ω 0, Ω C B C ω B 0,, 0 ω B, B C B B,, Zvýšení
(3) jiri brus Techniky přenosu polarizace cross -polarizace a spinová difuse laboratory frame, spin rotating frame laboratory frame, spin Ω H B H ω, ω, ω 0, B H ω 0, Ω C B C ω B 0,, 0 ω B, B C B B,, Zvýšení
Úvod do strukturní analýzy farmaceutických látek
 Úvod do strukturní analýzy farmaceutických látek Garant předmětu: doc. Ing. Bohumil Dolenský, Ph.D. A28, linka 4110, dolenskb@vscht.cz Hmotnostní spektrometrie II. Příprava předmětu byla podpořena projektem
Úvod do strukturní analýzy farmaceutických látek Garant předmětu: doc. Ing. Bohumil Dolenský, Ph.D. A28, linka 4110, dolenskb@vscht.cz Hmotnostní spektrometrie II. Příprava předmětu byla podpořena projektem
Kapitoly z fyzikální chemie KFC/KFCH. VII. Spektroskopie a fotochemie
 Kapitoly z fyzikální chemie KFC/KFCH VII. Spektroskopie a fotochemie Karel Berka Univerzita Palackého v Olomouci Katedra Fyzikální chemie karel.berka@upol.cz Spektroskopie Analýza světla Excitované Absorbované
Kapitoly z fyzikální chemie KFC/KFCH VII. Spektroskopie a fotochemie Karel Berka Univerzita Palackého v Olomouci Katedra Fyzikální chemie karel.berka@upol.cz Spektroskopie Analýza světla Excitované Absorbované
Heteronukleární korelační experimenty
 () jiri brus eteronukleární korelační eperimenty = ±lg ±lg +lg -lg +lg -lg +lg +lg -lg +lg -lg +lg -lg kz AM 9 ±±±y LGPI ±±±y ±±±y : - - - - - - - - - - t t C: ±±± ±±± t f t f - - - r ττ ττ r rotor period
() jiri brus eteronukleární korelační eperimenty = ±lg ±lg +lg -lg +lg -lg +lg +lg -lg +lg -lg +lg -lg kz AM 9 ±±±y LGPI ±±±y ±±±y : - - - - - - - - - - t t C: ±±± ±±± t f t f - - - r ττ ττ r rotor period
Přednášky z lékařské biofyziky Biofyzikální ústav Lékařské fakulty Masarykovy univerzity, Brno
 Přednášky z lékařské biofyziky Biofyzikální ústav Lékařské fakulty Masarykovy univerzity, Brno 1 Přednášky z lékařské biofyziky Biofyzikální ústav Lékařské fakulty Masarykovy univerzity, Brno Struktura
Přednášky z lékařské biofyziky Biofyzikální ústav Lékařské fakulty Masarykovy univerzity, Brno 1 Přednášky z lékařské biofyziky Biofyzikální ústav Lékařské fakulty Masarykovy univerzity, Brno Struktura
INTERPRETACE HMOTNOSTNÍCH SPEKTER
 INTERPRETACE HMOTNOSTNÍCH SPEKTER Hmotnostní spektrometrie hmotnostní spektrometrie = fyzikálně chemická metoda založená na rozdělení hmotnosti iontů v plynné fázi podle jejich poměru hmotnosti a náboje
INTERPRETACE HMOTNOSTNÍCH SPEKTER Hmotnostní spektrometrie hmotnostní spektrometrie = fyzikálně chemická metoda založená na rozdělení hmotnosti iontů v plynné fázi podle jejich poměru hmotnosti a náboje
Jiří Brus. (Verze 1.0.1-2005) (neupravená a neúplná)
 Jiří Brus (Verze 1.0.1-2005) (neupravená a neúplná) Ústav makromolekulární chemie AV ČR, Heyrovského nám. 2, Praha 6 - Petřiny 162 06 e-mail: brus@imc.cas.cz Transverzální magnetizace, která vykonává precesi
Jiří Brus (Verze 1.0.1-2005) (neupravená a neúplná) Ústav makromolekulární chemie AV ČR, Heyrovského nám. 2, Praha 6 - Petřiny 162 06 e-mail: brus@imc.cas.cz Transverzální magnetizace, která vykonává precesi
ZÁKLADY SPEKTROMETRIE NUKLEÁRNÍ MAGNETICKÉ REZONANCE
 ZÁKLADY SPEKTROMETRIE NUKLEÁRNÍ MAGNETICKÉ REZONANCE Co to je NMR? nedestruktivní spektroskopická metoda využívající magnetických vlastností atomových jader ke studiu struktury molekul metoda č.1 pro určování
ZÁKLADY SPEKTROMETRIE NUKLEÁRNÍ MAGNETICKÉ REZONANCE Co to je NMR? nedestruktivní spektroskopická metoda využívající magnetických vlastností atomových jader ke studiu struktury molekul metoda č.1 pro určování
Struktura atomů a molekul
 Struktura atomů a molekul Obrazová příloha Michal Otyepka tento text byl vysázen systémem L A TEX2 ε ii Úvod Dokument obsahuje všechny obrázky tak, jak jsou uvedeny ve druhém vydání skript Struktura atomů
Struktura atomů a molekul Obrazová příloha Michal Otyepka tento text byl vysázen systémem L A TEX2 ε ii Úvod Dokument obsahuje všechny obrázky tak, jak jsou uvedeny ve druhém vydání skript Struktura atomů
Tabulace učebního plánu. Obecná chemie. Vzdělávací obsah pro vyučovací předmět : Ročník: 1.ročník a kvinta
 Tabulace učebního plánu Vzdělávací obsah pro vyučovací předmět : CHEMIE Ročník: 1.ročník a kvinta Obecná Bezpečnost práce Názvosloví anorganických sloučenin Zná pravidla bezpečnosti práce a dodržuje je.
Tabulace učebního plánu Vzdělávací obsah pro vyučovací předmět : CHEMIE Ročník: 1.ročník a kvinta Obecná Bezpečnost práce Názvosloví anorganických sloučenin Zná pravidla bezpečnosti práce a dodržuje je.
Úvod do strukturní analýzy farmaceutických látek
 Úvod do strukturní analýzy farmaceutických látek Garant předmětu: doc. Ing. Bohumil Dolenský, Ph.D. A28, linka 40, dolenskb@vscht.cz Nukleární Magnetická Rezonance I. Příprava předmětu byla podpořena projektem
Úvod do strukturní analýzy farmaceutických látek Garant předmětu: doc. Ing. Bohumil Dolenský, Ph.D. A28, linka 40, dolenskb@vscht.cz Nukleární Magnetická Rezonance I. Příprava předmětu byla podpořena projektem
doc. Ing. Richard Hrabal, CSc. Ing. Hana Dvořáková, CSc. doc. RNDr. Jan Lang, PhD. Ing. Jan Prchal, Ph.D.
 Vyučující: doc. Ing. Richard rabal, CSc. Ing. ana Dvořáková, CSc. doc. RNDr. Jan Lang, PhD. Ing. Jan Prchal, Ph.D. Číslo dveří A 42, telefon 3805, e-mail hrabalr@vscht.cz Termín: každý čtvrtek od 10,00
Vyučující: doc. Ing. Richard rabal, CSc. Ing. ana Dvořáková, CSc. doc. RNDr. Jan Lang, PhD. Ing. Jan Prchal, Ph.D. Číslo dveří A 42, telefon 3805, e-mail hrabalr@vscht.cz Termín: každý čtvrtek od 10,00
Určení molekulové hmotnosti: ESI a nanoesi
 Cvičení Určení molekulové hmotnosti: ESI a nanoesi ) 1)( ( ) ( H m z H m z M k j j j m z z zh M Molekula o hmotnosti M se nabije z-krát protonem, pík iontu ve spektru je na m z : ) ( H m z M z Pro dva
Cvičení Určení molekulové hmotnosti: ESI a nanoesi ) 1)( ( ) ( H m z H m z M k j j j m z z zh M Molekula o hmotnosti M se nabije z-krát protonem, pík iontu ve spektru je na m z : ) ( H m z M z Pro dva
Spektrální metody NMR I
 Spektrální metody NMR I RNDr. Zdeněk Tošner, Ph.D. Hlavova 8, místnost 020 tel. 22195 1323 tosner@natur.cuni.cz www.natur.cuni.cz/nmr/vyuka.html Literatura Böhm, Smrčková-Voltrová: Strukturní analýza organických
Spektrální metody NMR I RNDr. Zdeněk Tošner, Ph.D. Hlavova 8, místnost 020 tel. 22195 1323 tosner@natur.cuni.cz www.natur.cuni.cz/nmr/vyuka.html Literatura Böhm, Smrčková-Voltrová: Strukturní analýza organických
Bioinformatika pro PrfUK 2003
 Bioinformatika pro PrfUK 2003 Jiří Vondrášek Ústav organické chemie a biochemie vondrasek@uochb.cas.cz Jan Pačes Ústav molekulární genetiky hpaces@img.cas.cz http://bio.img.cas.cz/prfuk2003 What is Bioinformatics?---The
Bioinformatika pro PrfUK 2003 Jiří Vondrášek Ústav organické chemie a biochemie vondrasek@uochb.cas.cz Jan Pačes Ústav molekulární genetiky hpaces@img.cas.cz http://bio.img.cas.cz/prfuk2003 What is Bioinformatics?---The
P ro te i n o vé d a ta b á ze
 Proteinové databáze Osnova Základní stavební jednotky proteinů Hierarchie proteinové struktury Stanovení proteinové struktury Důležitost proteinové struktury Proteinové strukturní databáze Proteinové klasifikační
Proteinové databáze Osnova Základní stavební jednotky proteinů Hierarchie proteinové struktury Stanovení proteinové struktury Důležitost proteinové struktury Proteinové strukturní databáze Proteinové klasifikační
jádro a elektronový obal jádro nukleony obal elektrony, pro chemii významné valenční elektrony
 atom jádro a elektronový obal jádro nukleony obal elektrony, pro chemii významné valenční elektrony molekula Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti seskupení alespoň dvou atomů
atom jádro a elektronový obal jádro nukleony obal elektrony, pro chemii významné valenční elektrony molekula Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti seskupení alespoň dvou atomů
Chromatofokusace. separace proteinů na základě jejich pi vysoké rozlišení. není potřeba připravovat ph gradient zaostřovací efekt jednoduchost
 Chromatofokusace separace proteinů na základě jejich pi vysoké rozlišení není potřeba připravovat ph gradient zaostřovací efekt jednoduchost Polypufry - amfolyty Stacionární fáze Polybuffer 96 - ph 9-6
Chromatofokusace separace proteinů na základě jejich pi vysoké rozlišení není potřeba připravovat ph gradient zaostřovací efekt jednoduchost Polypufry - amfolyty Stacionární fáze Polybuffer 96 - ph 9-6
Jiří Brus. (Verze ) (neupravená a neúplná)
 Jiří Brus (Verze 1.0.1-2005) (neupravená a neúplná) Vodík-vodíkový korelační dvou-dimenzionální experiment byl prvně navržen Jeanem Jeenerem na letní škole v Basko Polje už v roce 1971. Po pěti letech
Jiří Brus (Verze 1.0.1-2005) (neupravená a neúplná) Vodík-vodíkový korelační dvou-dimenzionální experiment byl prvně navržen Jeanem Jeenerem na letní škole v Basko Polje už v roce 1971. Po pěti letech
Laboratoř NMR Strukturní analýza a 2D NMR spektra
 Laboratoř NMR Strukturní analýza a 2D NMR spektra Místo: Laboratoř NMR, místnost A28, Kontakt: doc. Ing. Bohumil DOLENSKÝ, Ph.D., Ústav analytické chemie, Vysoká škola chemicko-technologická, Technická
Laboratoř NMR Strukturní analýza a 2D NMR spektra Místo: Laboratoř NMR, místnost A28, Kontakt: doc. Ing. Bohumil DOLENSKÝ, Ph.D., Ústav analytické chemie, Vysoká škola chemicko-technologická, Technická
Chemická reaktivita NK.
 Chemické vlastnosti, struktura a interakce nukleových kyselin Bi7015 Chemická reaktivita NK. Hydrolýza NK, redukce, oxidace, nukleofily, elektrofily, alkylační činidla. Mutageny, karcinogeny, protinádorově
Chemické vlastnosti, struktura a interakce nukleových kyselin Bi7015 Chemická reaktivita NK. Hydrolýza NK, redukce, oxidace, nukleofily, elektrofily, alkylační činidla. Mutageny, karcinogeny, protinádorově
CHEMIE - Úvod do organické chemie
 Název školy Číslo projektu Autor Název šablony Název DUMu Stupeň a typ vzdělávání Vzdělávací oblast Vzdělávací obor Vzdělávací okruh Druh učebního materiálu Cílová skupina Anotace SŠHS Kroměříž CZ.1.07/1.5.00/34.0911
Název školy Číslo projektu Autor Název šablony Název DUMu Stupeň a typ vzdělávání Vzdělávací oblast Vzdělávací obor Vzdělávací okruh Druh učebního materiálu Cílová skupina Anotace SŠHS Kroměříž CZ.1.07/1.5.00/34.0911
OPVK CZ.1.07/2.2.00/
 OPVK CZ.1.07/2.2.00/28.0184 Základní principy vývoje nových léčiv OCH/ZPVNL Mgr. Radim Nencka, Ph.D. ZS 2012/2013 Molekulární interakce SAR Možné interakce jednotlivých funkčních skupin 1. Interakce alkoholů
OPVK CZ.1.07/2.2.00/28.0184 Základní principy vývoje nových léčiv OCH/ZPVNL Mgr. Radim Nencka, Ph.D. ZS 2012/2013 Molekulární interakce SAR Možné interakce jednotlivých funkčních skupin 1. Interakce alkoholů
IZOLACE, SEPARACE A DETEKCE PROTEINŮ I. Vlasta Němcová, Michael Jelínek, Jan Šrámek
 IZOLACE, SEPARACE A DETEKCE PROTEINŮ I Vlasta Němcová, Michael Jelínek, Jan Šrámek Studium aktinu, mikrofilamentární složky cytoskeletu pomocí dvou metod: detekce přímo v buňkách - fluorescenční barvení
IZOLACE, SEPARACE A DETEKCE PROTEINŮ I Vlasta Němcová, Michael Jelínek, Jan Šrámek Studium aktinu, mikrofilamentární složky cytoskeletu pomocí dvou metod: detekce přímo v buňkách - fluorescenční barvení
Bioinformatika a výpočetní biologie KFC/BIN. I. Přehled
 Bioinformatika a výpočetní biologie KFC/BIN I. Přehled RNDr. Karel Berka, Ph.D. Univerzita Palackého v Olomouci Definice bioinformatiky (Molecular) bio informatics: bioinformatics is conceptualising biology
Bioinformatika a výpočetní biologie KFC/BIN I. Přehled RNDr. Karel Berka, Ph.D. Univerzita Palackého v Olomouci Definice bioinformatiky (Molecular) bio informatics: bioinformatics is conceptualising biology
Jiří Brus. (Verze ) (neupravená a neúplná)
 Jiří Brus (Verze 1.0.1-2005) (neupravená a neúplná) Ústav makromolekulární chemie AV ČR, Heyrovského nám. 2, Praha 6 - Petřiny 162 06 e-mail: brus@imc.cas.cz I v roztoku probíhá řada experimentů tak že,
Jiří Brus (Verze 1.0.1-2005) (neupravená a neúplná) Ústav makromolekulární chemie AV ČR, Heyrovského nám. 2, Praha 6 - Petřiny 162 06 e-mail: brus@imc.cas.cz I v roztoku probíhá řada experimentů tak že,
Úvod do studia organické chemie
 Úvod do studia organické chemie 1828... Wöhler... uměle připravil močovinu Organická chemie - chemie sloučenin uhlíku a vodíku, případně dalších prvků (O, N, X, P, S) Příčiny stability uhlíkových řetězců:
Úvod do studia organické chemie 1828... Wöhler... uměle připravil močovinu Organická chemie - chemie sloučenin uhlíku a vodíku, případně dalších prvků (O, N, X, P, S) Příčiny stability uhlíkových řetězců:
