ÚVOD DO KVANTOVÉ CHEMIE
|
|
|
- Vítězslav Bařtipán
- před 7 lety
- Počet zobrazení:
Transkript
1 ÚVOD DO KVANTOVÉ CHEME. Navození kvantové mechanky Postuláty kvantové mechanky, základy operátorové algebry, navození kvantové mechanky, jednoduché modely.. Vodíkový atom 3. Základní aproxmace používané př řešení staconární Schrödngerovy rovnce pro více-elektronové systémy Aproxmace v Hamltonánu, aproxmace ve vlnové funkc. Bornova-Oppenhemerova aproxmace, poruchová teore, varační prncp, MO LCAO aproxmace, model nezávslých elektronů 4. Atom hela - příklady výpočtů pomocí různých aproxmací 5. Herarche metod kvantové cheme Ab nto metody, sememprcké metody, emprcké metody. 6. Spn elektronu, Paulho prncp 7. Hartree-Fockova metoda Navození HF rovnc pro dvou-elektronový systém, kulombcký a výměnný ntegrál, SCF rovnce. Systémy s uzavřeným a otevřeným elektronovým slupkam, Hartree-Fock-Roothanovy rovnce. 8. Báze pro MO LCAO rozvoj LTERATURA: R. Polák a R. Zahradník: Kvantová cheme, SNTL, Praha 985. P. Čársky, J. Pancíř, R. Zahradník: Molekulové orbtaly v chem, Academa, Praha 974. J. Fšer: Úvod do molekulové symetre, SNTL, Praha Levn: Quantum Chemstry, Prentce Hall, New Jersey 99. A. Szabo a N. S. Ostlund: Modern Quantum Chemsty, McGraw-Hll, New York 98.
2 KORELAČNÍ ENERGE. Korelační energe Hartree-Fockova lmta, defnce korelační energe, Koopmansův teorém a Brllounův teorém. Metody pro výpočet korelační energe Metoda konfgurační nterakce, Møller-Plessetova formulace poruchové teore, Metoda vázaných klastrů 3. Metody založené na funkconálu hustoty Teorémy vedoucí k formulac metod DFT, výměnné a korelační funkconály hustoty LTERATURA: R. Polák a R. Zahradník: Kvantová cheme, SNTL, Praha 985. P. Čársky a M. Urban: Ab nto výpočty v chem, SNTL, Praha 985. J. Fšer: Úvod do kvantové cheme, Academa, Praha Levn: Quantum Chemstry, Prentce Hall, New Jersey 99. A. Szabo a N. S. Ostlund: Modern Quantum Chemsty, McGraw-Hll, New York 98.
3 Kvantová cheme aplkace kvantové mechanky na chemké problémy Kvantová mechanka popsuje chování mkročástc, podává určtou syntézu pojmů částce a pole POUŽTÍ KVANTOVÉ CHEME. nterpretace molekulových spekter elektronová - hladny elektronových stavů! onzační potencály, elektronové afnty, exctační energe vbrační rotační- struktura molekul! vazebné délky a úhly, dpólové momenty. Teoretcká předpověď vlastností molekul 3. Vlastnost transtních stavů chemckých reakcí! odhad reakčních rychlostí 4. Klasfkace mezmolekulových sl 5. Určování relatvní stablty molekul 6. Analýza NMR spekter 7. Mechansmy chemckých reakcí 8. Termodynamcké vlastnost (např. Entrope, tepelné kapacty) - ve spojení se statstckou termodynamkou.
4 Proč potřebujeme kvantovou mechanku? Proč nevystačíme s klasckou mechankou? klascká mechanka byla formulována pro pops chování makroskopckých těles na přelomu 9., 0. století se byly popsány jevy, které nebylo možno nterpretovat na základě klascké mechanky potřeba formulovat zákontost pro pops chování částc mkrosvěta
5 HSTORCKÉ POZADÍ KVANTOVÉ MECHANKY 80 Thomas Young podal přesvědčvý důkaz o tom, že světlo má vlnový charakter (dfrakce světla) 860 James Clerk Maxwell formuloval Maxwellovy rovnce elektromagrensmu urychlovaný elektrcký náboj vyzařuje energ ve formě elektromagnetckých vln rychlost tohoto vlnění se ukázala být stejná, jako rychlost světla expermentálně změřená SVĚTLO JE ELEKTROMAGNETCKÉ ZÁŘENÍ 888 Henrch Hertz expermentálně potvrdl Maxwellovy závěry změřl radové vlny vznklé urychlením nabtých částc ve výboj 900 Max Planck nterpretace záření černého tělesa Černé těleso: objekt, který absorbuje veškeré světlo, které na něj dopadá závslost ntenzty na energ záření černého tělesa: experment v rozporu s predkcí založenou na Maxwellových rovncích Planck předpokládal, že atomy mohou emtovat světlo jen v určtých energetckých dávkách hν (h je konstanta úměrnost, dnes nazývaná Planckova konstanta h6,6x0-34 J.s, a ν je frekvence záření) KVANTOVÁNÍ SVĚTLA - je v přímém rozporu s tehdejším chápáním světla (energe vlnění je přímo úměrná jeho ampltudě a ta se může měnt spojtě)
6 905 Alber Ensten Vysvětll podstatu fotoelektrckého efektu: Fotoelektrcký jev: z kovu ozařovaného světlem jsou emtovány eletkrony podle klascké trore by knetcká energe emtovaných elektronů měla závset na ntenztě dopadajícího světla experment: knetcká energe emtovaných elektronů nezávsí na ntenztě dopadajícího světla, ale na jeho vlnové délce Ensten ukázal, že toto může být vysvětleno, díváme-l se na světlo jako na částce, fotony, jejchž energe je dána vztahem E foton hν částe energe fotonu se v kovu použje na vytržení elektronu z kovu a zbytek je ve formě knetcké energe emtovaného elektronu hν Φ /mv Φ je výstupní práce 909 RutherfordGeger Expermentálně pozoroval rozptyl α-částc na kovové fol α částce mají též vlnový charakter kladný náboj je soustředěn na atomovém jádře (většna částc prolétla fól anž by změnla směr) MODELY ATOMU 904 Thomsonův 9 Rutherfordův 93 Bohrův
7 93 L. De Brogle Pohyb elektronu může mít vlnový charakter Částc o hmotnost m, pohybující se rychlostí v přísluší vlnová délka λ h/mv h/p 96 E. Schrödnger Pohyb částc mkrosvěta se řídí rovncí HΨ h(δψ/δt) 97 W. Hesenberg Prncp neurčtost 97 DavssonGermer Expermentální potvrzení de Brogleho hypotézy pro elektrony 93 Stern Expermentální pozorování dfrakce H a He atomů
8 Srovnání klascké a kvantové mechanky KLASCKÁ MECHANKA Pohyb částc se řídí. Newtonovým zákonen: Známe-l pozc a rychlost částce v čase t a sílu F - můžeme vypočítat souřadnce a hybnost v lbovolném okamžku KVANTOVÁ MECHANKA V důsledku prncpu neurčtost nemůžeme určt přesně stav systému. Pravděpodobnostní charakter vlnové funkce Úplný determnsmus Φ(x,t)
9 Operátorová algebra OPERÁTOR - předps, kterým se jedné funkc f(x,y) přřazuje funkce jná, g(x,y) O f ( x, y) g( x, y) Lneární operátor: O( f f ) O f O f Komutátor: O cf co f [ P, Q] PQ Q P Vlastní funkce a vlastní hodnota operátoru: O f k o k f k Vlastní hodnota Vlastní funkce Hermtovský operátor: vlastní funkce hermtovského operátoru jsou reálná čísla Tvoří úplný ortonormální soubor funkcí.
10 Dracova notace: ( braket ) Φ Φ * * ( x) Φ( x) dx ( x) H Φ( x) dx Φ( x) Φ( x) Φ Φ Φ( x) H Φ( x) Φ H Φ bra -vektor ket -vektor * ϕ Ortonormální funkce: ( x) ( x) dx j 0... j j ϕ * ϕ j δ j ( x) ( x) dx ϕ ϕ ϕ ϕ ϕ ϕ ϕ j Kroneckerova delta Úplný ortonormální soubor vlastních funkcí hermtovského operátoru: Lbovolnou funkc Φ můžeme vyjádřt jako lneární kombnac vlastních funkcí f k Φ k f c k k ck f Φ k
11 . Postulát Postuláty kvantové mechanky Ke každé pozorovatelné fyzkální velčně A exstuje lneární hermtovský operátor A^, který lze získat nasledujícím postupem:. vyjdeme z klasckého výrazu pro příslušnou velčnu vyjádřenou v kartézských souřadncích a hybnostech. souřadnce a čas ponecháme beze změny 3. za hybnost p x dosadíme operátor hybnost p h x x. Postulát Stav systému je popsán vlnovou funkcí Φ, která musí splňovat následující podmínky:. exstuje v celém defnčním oboru proměnných. je spojtá a konečná v defnčním oboru (vyjma sngulárních bodů) 3. je jednoznačná Fyzkální nterpretace vlnové funkce Φ : [Φ(x,,x n, t)] výraz Φ*Φ dτ udává pravděpodobnost, že v čase t jsou proměnné x x n v ntervalech (x,x dx ) až (x n,x n dx n ) Celková pravděpodobnost musí být rovna jedné: Φ * Φdτ
12 3. Postulát Vlnová funkce Φ vyhovuje časově závslé Schrödngerově rovnc Φ HˆΦ h t kde H je Hamltonův operátor daného systému. 4. Postulát Jedné možné hodnoty, které lze získat měřením pozorovatelné velčny A, jsou její charakterstcké (vlastní) hodnoty a k rovnce ÂΨ k ak Ψ k kde A je operátor pozorovatelné velčny A a Ψ k je vlastní funkcí operátoru A. 5. Postulát Pro systém, který je ve stavu popsaném vlnovou funkcí Φ, střední hodnota a pozorovatelné velčny A Φ AΦdτ a * Φ Φdτ * )
13 6. Spnový postulát Každá elementární částce má svůj vlastní spnový moment hybnost a magnetcký spnový moment. 7. Symetrzační postulát Pro systémy s více stejným (nerozlštelným) částcem platí: Stav systému N dentckých částc může být popsán a) SYMETRCKOU vlnovou funkcí - celočíselný spn (bosony) b) ANTSYMETRCKOU vlnovou funcí - poločíselný spn (fermony) Př záměně souřadnc dvou částc změní antsymetrcká vlnová funkce znaménko
14 Časově závslá vs. staconární Schrödngerova rovnce Φ HˆΦ h t Omezíme se na systémy, kde potencál V nezávsí na čase - V(x) > Φ ( x, t) φ( x) f ( t ) [ h ( x)] x V Separace proměnných: H φ ( x) Eφ( x) f ( t) A exp( Et / h) Φ( x, t) exp( Et / h) φ( x) Staconární stavy: Φ( x, t) Φ( x, t) exp( Et / h) exp( Et / h) * Φ( x, t) * φ ( x) φ( x) φ( x)
15 Staconární Schrödngerova rovnce H Ψ EΨ Vlnová funkce popsující stav systému Hamltonán H T V Odvozen z klasckého výrazu pro kn. a pot. energe Příklad - harmoncký osclátor Molekulový Hamltonán: T h n m H T J T e V JJ V Je V ee Cvčení - Hamltonán pro molekulu vody
16 Staconární Schrödngerova rovnce - není problém rovnc sestavt ale vyřešt. Jednoelektronové systémy: exaktní (analytcké řešení) atomy vodíkového typu - atomové orbtaly Víceelektronové systémy: Problémové členy - závsejí na souřadncích dvou částc (V ee, V Je, V JJ ) nelze separovat proměnné v Hamltonánu - aproxmatvní řešení Příklad # - atom He se zanedbáním elektronové repulse Příklad # - zahrnutí elektronové repulse pomocí poruchové teore Hledáme takové aproxmace, jejchž přesnost můžeme kontrolovat!. Bornova-Oppenhemerova aproxmace. Model nezávslých elektronů 3. MO LCAO
17 Bornova-Oppenhemerova aproxmace Atomová jádra považujeme za staconární - E J kn 0 H T J T e V JJ 0 konst. V Je V ee H T e V Je V ee konst. Jednoelektronová část Dvouelektronová část Elektrony se pohybují v potencálu jader o souřadncích R: H Ψ ( r, R) E ( R) Ψ ( r, R) Hyperplocha potencální energe Úplná separace jaderného a elektronového pohybu Pohyb jader řešíme na získané PES - kvantová nebo klascká dynamka pohybu jader
18 Hamltonán pro molekulu vody > > H J J J j j e R R Z Z r r r R Z e e e m m πε πε πε h h Coulombcká atrakce elektron-jádro Knetcká energe jader Knetcká energe elektronů Coulombcká repulze elektron-elektron Coulombcká repulze jádro-jádro. 4 4 H konst r r r R Z j j e e e m > πε πε h Problémový člen!!
19 Model nezávslých elektronů Formálně můžeme Hamltonán psát ve tvaru: H () (, ) h vj j> V ee n n n vj(,) V j> () T V J Závsí na souřadncích dvou elektronů - obecně nelze řešt analytcky. Efektvní potencál - elektron se pohybuje ve zprůměrovaném pol ostatních elektronů H n [ h( ) V ( )] n H '( ) Každý člen Hamltonánu působí pouze na jeden z elektronů Celkovou vlnovou funkc systému můžeme hledat ve tvaru produktu jednoelektronových funkcí
20 n H '( ) Ψ(,,..., n) EΨ(,,..., n) Ψ(,,..., n) ϕ ( ) n Původní staconární Schrödngerova rovnce se rozpadá na n jednoelektronovýh rovnc. Abychom vyhověl antsymetrzačnímu postulátu musíme celkovou vlnovou funkc hledat ve tvaru Slaterova determnantu (př záměně souřadnc dvou elektronů vlnová funkce změní znaménko). Ψ(,,..., n) det( ϕ ) n! ϕ () ϕ () n!... ϕ ( n) ϕ () ϕ ()... ϕ ( n) ϕ () n ϕ () n... ϕ ( n) n
21 Celková vlnová funkce - ve tvaru produktové funkce (Slaterova determnantu) sestávající z jednoelektronových vlnových funkc ϕ V jakém tvaru jsou jednoelektronové funkce ϕ? Jednoelektronové vlnové funkce molekul - MOLEKULOVÉ ORBTALY - hledáme ve tvaru lneární kombnace vlnových funkcí atomů: MO LCAO MO, jednoelektronová vlnová funkce ndex MO ϕ b c χ µ µ µ ndex AO AO, jednoelektronová vlnová funkce BÁZOVÉ FUNKCE, báze {χ } n MO z n AO přesnost aproxmace kontrolujeme pomocí změny velkost báze mnmalzace energe v závslost na c µ
22 Varační teorém Φ H Φ E Přesná energe 0 Zkusmá vlnová funkce Aproxmatvní vlnová funkce dává energ, která je vždy větší (nebo rovna) E 0 Příklad #3 - atom He varačně Lneární varační funkce: Φ k ck f Podmínka pro nalezení nejvhodnější varační funkce (mnmální energe): k W c 0 > vede na systém sekulárních rovnc: H f H f S k f f k k k b k [ H k WS Systém N lneárních rovnc o N neznámých - netrvální řešení pouze je-l determnant soustavy roven 0 k ] c k 0
23 Hartree-Fockova metoda H () (, ) h vj j> Ψ(,,..., n) det( ϕ ) n! ϕ () ϕ () n!... ϕ ( n) ϕ () ϕ ()... ϕ ( n) ϕ () n ϕ () n... ϕ ( n) n E[ Ψ ] Ψ H 0 Ψ δe[ Ψ] Genalta metody spočívá v technckém řešení - - postupně se řeší problém pro jednotlvé elektrony - jednotlvé elektrony se pohybují v zprůměrovaném potencálu ostatních elektronů
24 n n n E [ Ψ] Ψ H Ψ h ( J K ) j j j Jednoelektronový ntegrál h ( ϕ ) h ϕ () Coulombcký ntegrál J j ( j j j ϕ ) ϕ () v (,) ϕ () ϕ () Výměnný ntegrál K j ( j j j ϕ ) ϕ () v (,) ϕ () ϕ () δe[ψ]0 > systém Fockových rovnc F ϕ ' ε ϕ ' n F() h() ϕ j () v'(,) ϕ j () j Řešení Fockových rovnc probíhá teračně - metoda označována jako SCF
25 Systémy s uzavřenou elektronovou strukturou Systémy s otevřenou elektronovou strukturou. UHF - Unrestrcted HF. RHF (ROHF) - Restrcted Open-Shell HF Hartree-Fockovy rovnce původně odvozeny pro atomy Roothaan - zavedení MO LCAO do HF rovnc > Hartree-Fock-Roothaan Koncept BÁZE atomových orbtalů HF lmta
26 Závslost HF energe na kvaltě a velkost použté báze - molekula vody Báze Energe (a.u.) µ[d] θ R(OH) [Å] Experment HF lmta -76, STO-3G Mnmal STO G G G* G* 0 GTO -76,067.98
27 Koopmansůvteorém: onzační potencál pro elektron v orbtalu je dán zápornou hodnotou energe tohoto orbtalu: P ε Spolehlvost Koopmansova theorému [ev] KT SCF C Experment H O b a a t a
28 Staconární Schrödngerova rovnce H Ψ EΨ Metoda konfgurační nterakce Metoda vázaných klastrů Poruchová teore Zahrnutí el. korelace Bornova-Oppenhemerova aproxmace Model nezávslých elektronů Vlnová funkce ve tvaru Slaterova determnantu MO LCAO varační prncp Hartreeho-Fockova metoda (HF) Separace σ-π Neemprcké π-elektronové metody Zanedbání některých ntegrálů Emprcké parametry Sememprcké π-elektronové metody Zanedbání elektronové repulse Hückelova metoda MO Zanedbání některých ntegrálů Emprcké parametry Sememprcké metody (NDO, AM, PM3) Metoda EHT Zanedbání elektronové repulse Separace σ-π
29 Korelační energe HF energe s různou bází HF lmta E cor Nerelatvstcká energe systému Přesná expermentální energe
30 Příklad: Model harmonckého osclátoru - hmotný bod na pužně Celková energe systému: T V p m h x T mv p x V kx T h d m dx V kx Hamltonán pro harmoncký osclátor: H h m d dx kx
31 Hamltonán pro molekulu vody Knetcká energe jader Knetcká energe elektronů Coulombcká atrakce elektron-jádro H e 4πε 0 h 0 0 j> 3 m r r j h m e 0 e 4πε J > e 4πε Z Z J R R J Z R r Coulombcká repulze elektron-elektron Coulombcká repulze jádro-jádro
Korelační energie. Celkovou elektronovou energii molekuly lze experimentálně určit ze vztahu. E vib. = E at. = 39,856, E d
 Korelační energe Referenční stavy Energ molekul a atomů lze vyjádřt vzhledem k různým referenčním stavům. V kvantové mechance za referenční stav s nulovou energí bereme stav odpovídající nenteragujícím
Korelační energe Referenční stavy Energ molekul a atomů lze vyjádřt vzhledem k různým referenčním stavům. V kvantové mechance za referenční stav s nulovou energí bereme stav odpovídající nenteragujícím
Hartreeho-Fockova metoda (HF)
 Staonární Shrödngerova rovne H Ψ = EΨ Metoda konfgurační nterake Metoda vázanýh klastrů Poruhová teore Zahrnutí el. korelae Bornova-Oppenhemerova aproxmae Model nezávslýh elektronů Vlnová funke ve tvaru
Staonární Shrödngerova rovne H Ψ = EΨ Metoda konfgurační nterake Metoda vázanýh klastrů Poruhová teore Zahrnutí el. korelae Bornova-Oppenhemerova aproxmae Model nezávslýh elektronů Vlnová funke ve tvaru
Lambertův-Beerův zákon
 Lambertův-Beerův zákon Intenzta záření po průchodu kavtou se vzorkem: Integrovaný absorpční koecent: I nal = I ntal e ε c L A = ε ( ~ ν ) d~ ν Bezjednotková včna síla osclátoru: v cm -1 = 4.3 10 9 A Síla
Lambertův-Beerův zákon Intenzta záření po průchodu kavtou se vzorkem: Integrovaný absorpční koecent: I nal = I ntal e ε c L A = ε ( ~ ν ) d~ ν Bezjednotková včna síla osclátoru: v cm -1 = 4.3 10 9 A Síla
11 Kvantová teorie molekul
 11 Kvantová teore molekul Pops molekul v rámc kvantové teore je ústředním tématem kvantové cheme. Na rozdíl od atomů nejsou molekuly centrálně symetrcké, což výpočty jejch vlastností komplkuje. V důsledku
11 Kvantová teore molekul Pops molekul v rámc kvantové teore je ústředním tématem kvantové cheme. Na rozdíl od atomů nejsou molekuly centrálně symetrcké, což výpočty jejch vlastností komplkuje. V důsledku
Molekulová vibrace dvojatomové molekuly. Disociační křivka dvojatomové molekuly
 Molekulová vbrace dvojatomové molekuly Dsocační křvka dvojatomové molekuly x Potencální energe, E Repulsvní síly x Přtažlvé síly síly x Pro malé odchylky [(x-x ) ] možno aproxmovat parabolou, jak plyne
Molekulová vbrace dvojatomové molekuly Dsocační křvka dvojatomové molekuly x Potencální energe, E Repulsvní síly x Přtažlvé síly síly x Pro malé odchylky [(x-x ) ] možno aproxmovat parabolou, jak plyne
9 PŘEDNÁŠKA 9: Heisenbergovy relace neurčitosti, důsledky. Tunelový jev. Shrnutí probrané látky, příprava na zkoušku.
 9 PŘEDNÁŠKA 9: Hesenbergovy relace neurčtost, důsledky. Tunelový jev. Shrnutí probrané látky, příprava na zkoušku. Hesenbergovy relace neurčtost(tnqu.5., SKM) Jednoduchý pohled na věc: Vždy exstuje určtá
9 PŘEDNÁŠKA 9: Hesenbergovy relace neurčtost, důsledky. Tunelový jev. Shrnutí probrané látky, příprava na zkoušku. Hesenbergovy relace neurčtost(tnqu.5., SKM) Jednoduchý pohled na věc: Vždy exstuje určtá
Ab initio výpočty v chemii a biochemii
 Ab initio výpočty v chemii a biochemii Doc. RNDr. Ing. Jaroslav Burda, CSc., jaroslav.burda@mff.cuni.cz Dr. Vladimír Sychrovský vladimir.sychrovsky@uochb.cas.cz Studijní literatura Szabo A., Ostlund N.S.
Ab initio výpočty v chemii a biochemii Doc. RNDr. Ing. Jaroslav Burda, CSc., jaroslav.burda@mff.cuni.cz Dr. Vladimír Sychrovský vladimir.sychrovsky@uochb.cas.cz Studijní literatura Szabo A., Ostlund N.S.
Energie elektrického pole
 Energe elektrckého pole Jž v úvodní kaptole jsme poznal, že nehybný (centrální elektrcký náboj vytváří v celém nekonečném prostoru slové elektrcké pole, které je konzervatvní, to znamená, že jakýkolv jný
Energe elektrckého pole Jž v úvodní kaptole jsme poznal, že nehybný (centrální elektrcký náboj vytváří v celém nekonečném prostoru slové elektrcké pole, které je konzervatvní, to znamená, že jakýkolv jný
Od kvantové mechaniky k chemii
 Od kvantové mechaniky k chemii Jan Řezáč UOCHB AV ČR 19. září 2017 Jan Řezáč (UOCHB AV ČR) Od kvantové mechaniky k chemii 19. září 2017 1 / 33 Úvod Vztah mezi molekulovou strukturou a makroskopickými vlastnostmi
Od kvantové mechaniky k chemii Jan Řezáč UOCHB AV ČR 19. září 2017 Jan Řezáč (UOCHB AV ČR) Od kvantové mechaniky k chemii 19. září 2017 1 / 33 Úvod Vztah mezi molekulovou strukturou a makroskopickými vlastnostmi
Hartre-Fock method (HF)
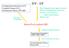 Cofgurato Iteracto (CI) Coupled Clusters (CC) Perturbato Theory (PT, MP) Electro correlato H Ψ = EΨ Bor-Oppehemer approxmato Model of depedet electros Product wave fucto (Slater determat) MO LCAO Hartre-Fock
Cofgurato Iteracto (CI) Coupled Clusters (CC) Perturbato Theory (PT, MP) Electro correlato H Ψ = EΨ Bor-Oppehemer approxmato Model of depedet electros Product wave fucto (Slater determat) MO LCAO Hartre-Fock
Operátory a maticové elementy
 Operátory a matice Operátory a maticové elementy operátory je výhodné reprezentovat maticemi maticové elementy operátorů jsou dány vztahy mezi Slaterovými determinanty obsahujícími ortonormální orbitaly
Operátory a matice Operátory a maticové elementy operátory je výhodné reprezentovat maticemi maticové elementy operátorů jsou dány vztahy mezi Slaterovými determinanty obsahujícími ortonormální orbitaly
MODELOVÁNÍ A SIMULACE
 MODELOVÁNÍ A SIMULACE základní pojmy a postupy vytváření matematckých modelů na základě blancí prncp numerckého řešení dferencálních rovnc základy práce se smulačním jazykem PSI Základní pojmy matematcký
MODELOVÁNÍ A SIMULACE základní pojmy a postupy vytváření matematckých modelů na základě blancí prncp numerckého řešení dferencálních rovnc základy práce se smulačním jazykem PSI Základní pojmy matematcký
Atom vodíku. Nejjednodušší soustava: p + e Řešitelná exaktně. Kulová symetrie. Potenciální energie mezi p + e. e =
 Atom vodíku Nejjednodušší soustava: p + e Řešitelná exaktně Kulová symetrie Potenciální energie mezi p + e V 2 e = 4πε r 0 1 Polární souřadnice využití kulové symetrie atomu Ψ(x,y,z) Ψ(r,θ, φ) x =? y=?
Atom vodíku Nejjednodušší soustava: p + e Řešitelná exaktně Kulová symetrie Potenciální energie mezi p + e V 2 e = 4πε r 0 1 Polární souřadnice využití kulové symetrie atomu Ψ(x,y,z) Ψ(r,θ, φ) x =? y=?
Nerovnovážná termodynamika
 erovnovážná termodynamka Fázový prostor Dmenze 6 Bod ve ázovém prostoru ( phase pont ) ednoznačně určue dynamku systému pohybue se Soubor podmnožna ázového prostoru Hustota bodů ve ázovém prostoru: rakce
erovnovážná termodynamka Fázový prostor Dmenze 6 Bod ve ázovém prostoru ( phase pont ) ednoznačně určue dynamku systému pohybue se Soubor podmnožna ázového prostoru Hustota bodů ve ázovém prostoru: rakce
Tepelná kapacita = T. Ē = 1 2 hν + hν. 1 = 1 e x. ln dx. Einsteinův výpočet (1907): Soustava N nezávislých oscilátorů se stejnou vlastní frekvencí má
 Tepelná kapacta C x = C V = ( ) dq ( ) du Dulong-Pettovo pravdlo: U = 3kT N C V = 3kN x V = T ( ) ds x Tepelná kapacta mřížky Osclátor s kvantovanou energí E n = ( n + 2) hν má střední hodnotu energe (po
Tepelná kapacta C x = C V = ( ) dq ( ) du Dulong-Pettovo pravdlo: U = 3kT N C V = 3kN x V = T ( ) ds x Tepelná kapacta mřížky Osclátor s kvantovanou energí E n = ( n + 2) hν má střední hodnotu energe (po
Sdílení tepla. Úvod - Přehled. Sdílení tepla mezi termodynamickou soustavou a okolím je podmíněno rozdílností teplot soustavy T.
 7.4.0 Úvod - Přehled Sdílení tepla Sdílení tepla mez termodynamckou soustavou a okolím je podmíněno rozdílností teplot soustavy T s a okolí T o. Teplo mez soustavou a okolím se sdílí třem základním způsoby:
7.4.0 Úvod - Přehled Sdílení tepla Sdílení tepla mez termodynamckou soustavou a okolím je podmíněno rozdílností teplot soustavy T s a okolí T o. Teplo mez soustavou a okolím se sdílí třem základním způsoby:
Fyzika biopolymerů. Elektrostatické interakce makromolekul ve vodných roztocích. Vodné roztoky. Elektrostatická Poissonova rovnice.
 Fyzka bopolymerů Elektrostatcké nterakce makromolekul ve vodných roztocích Robert Vácha Kamence 5, A4 2.13 robert.vacha@mal.mun.cz Vodné roztoky ldské tělo se skládá z 55-75 % z vody (roztoků) většna roztoků
Fyzka bopolymerů Elektrostatcké nterakce makromolekul ve vodných roztocích Robert Vácha Kamence 5, A4 2.13 robert.vacha@mal.mun.cz Vodné roztoky ldské tělo se skládá z 55-75 % z vody (roztoků) většna roztoků
Chemická struktura B
 Chemcká struktura B Elektronová struktura molekul Lubomír Rulíšek, Martn Srnec rulsek@uochb.cas.cz; srnec@h-nst.cas.cz (2016/17: pondělí CH3 8:10 9:40, CH3 9:50 10:35) 1 Přednáška 6: Od vodíku k protenům
Chemcká struktura B Elektronová struktura molekul Lubomír Rulíšek, Martn Srnec rulsek@uochb.cas.cz; srnec@h-nst.cas.cz (2016/17: pondělí CH3 8:10 9:40, CH3 9:50 10:35) 1 Přednáška 6: Od vodíku k protenům
REGRESNÍ ANALÝZA. 13. cvičení
 REGRESNÍ ANALÝZA 13. cvčení Závslost náhodných velčn Závslost mez kvanttatvním proměnným X a Y: Funkční závslost hodnotam nezávsle proměnných je jednoznačně dána hodnota závslé proměnné. Y=f(X) Stochastcká
REGRESNÍ ANALÝZA 13. cvčení Závslost náhodných velčn Závslost mez kvanttatvním proměnným X a Y: Funkční závslost hodnotam nezávsle proměnných je jednoznačně dána hodnota závslé proměnné. Y=f(X) Stochastcká
Relativistická kvantová mechanika
 Relatvstcká kvantová mechanka Mchal Lenc Poznámky k přednášce v jarním semestru Obrazy Postulát o kvantové kausaltě Evoluční operátor 3 Schrödngerův a Hesenbergův obraz 3 4 Interakční obraz4 Relatvta a
Relatvstcká kvantová mechanka Mchal Lenc Poznámky k přednášce v jarním semestru Obrazy Postulát o kvantové kausaltě Evoluční operátor 3 Schrödngerův a Hesenbergův obraz 3 4 Interakční obraz4 Relatvta a
Elektronový obal atomu
 Elektronový obal atomu Chemické vlastnosti atomů (a molekul) jsou určeny vlastnostmi elektronového obalu. Chceme znát energii a prostorové rozložení elektronů Znalosti o elektronovém obalu byly získány
Elektronový obal atomu Chemické vlastnosti atomů (a molekul) jsou určeny vlastnostmi elektronového obalu. Chceme znát energii a prostorové rozložení elektronů Znalosti o elektronovém obalu byly získány
Úvod do magnetizmu pevných látek
 Úvod do magnetzmu pevných látek. Úvod. Izolované magnetcké momenty 3. Prostředí 4. Interakce 5. agnetcké struktury 6. Doménová struktura a magnetzace .agnetzmus pevných látek -úvod. Zdroje magnetsmu -
Úvod do magnetzmu pevných látek. Úvod. Izolované magnetcké momenty 3. Prostředí 4. Interakce 5. agnetcké struktury 6. Doménová struktura a magnetzace .agnetzmus pevných látek -úvod. Zdroje magnetsmu -
Kinetika spalovacích reakcí
 Knetka spalovacích reakcí Základy knetky spalování - nauka o průběhu spalovacích reakcí a závslost rychlost reakcí na různých faktorech Hlavní faktory: - koncentrace reagujících látek - teplota - tlak
Knetka spalovacích reakcí Základy knetky spalování - nauka o průběhu spalovacích reakcí a závslost rychlost reakcí na různých faktorech Hlavní faktory: - koncentrace reagujících látek - teplota - tlak
3 VYBRANÉ MODELY NÁHODNÝCH VELIČIN. 3.1 Náhodná veličina
 3 VBRANÉ MODEL NÁHODNÝCH VELIČIN 3. Náhodná velčna Tato kaptola uvádí stručný pops vybraných pravděpodobnostních modelů spojtých náhodných velčn s důrazem na jejch uplatnění př rozboru spolehlvost stavebních
3 VBRANÉ MODEL NÁHODNÝCH VELIČIN 3. Náhodná velčna Tato kaptola uvádí stručný pops vybraných pravděpodobnostních modelů spojtých náhodných velčn s důrazem na jejch uplatnění př rozboru spolehlvost stavebních
Matematika I A ukázkový test 1 pro 2018/2019
 Matematka I A ukázkový test 1 pro 2018/2019 1. Je dána soustava rovnc s parametrem a R x y + z = 1 x + y + 3z = 1 (2a 1)x + (a + 1)y + z = 1 a a) Napšte Frobenovu větu (předpoklady + tvrzení). b) Vyšetřete
Matematka I A ukázkový test 1 pro 2018/2019 1. Je dána soustava rovnc s parametrem a R x y + z = 1 x + y + 3z = 1 (2a 1)x + (a + 1)y + z = 1 a a) Napšte Frobenovu větu (předpoklady + tvrzení). b) Vyšetřete
METODY VÝPOČETNÍ CHEMIE
 METODY VÝPOČETNÍ CHEMIE Metody výpočetní chemie Ab initio metody Semiempirické metody Molekulová mechanika Molekulová simulace Ab initio metody Ab initio - od počátku Metody kvantově-mechanické vycházejí
METODY VÝPOČETNÍ CHEMIE Metody výpočetní chemie Ab initio metody Semiempirické metody Molekulová mechanika Molekulová simulace Ab initio metody Ab initio - od počátku Metody kvantově-mechanické vycházejí
Elektronový obal atomu
 Elektronový obal atomu Chemické vlastnosti atomů (a molekul) jsou určeny vlastnostmi elektronového obalu. Chceme znát energii a prostorové rozložení elektronů Znalosti o elektronovém obalu byly získány
Elektronový obal atomu Chemické vlastnosti atomů (a molekul) jsou určeny vlastnostmi elektronového obalu. Chceme znát energii a prostorové rozložení elektronů Znalosti o elektronovém obalu byly získány
17 Vlastnosti molekul
 17 Vlastnosti molekul Experimentálně molekuly charakterizujeme pomocí nejrůznějších vlastností: můžeme změřit třeba NMR posuny, elektrické či magnetické parametry či třeba jejich optickou otáčivost. Tyto
17 Vlastnosti molekul Experimentálně molekuly charakterizujeme pomocí nejrůznějších vlastností: můžeme změřit třeba NMR posuny, elektrické či magnetické parametry či třeba jejich optickou otáčivost. Tyto
Neurčitost a provázanost kvantový svět
 Pavel Cejnar Ústav částcové a jaderné fyzky MFF UK Přednáška 6 Neurčtost a provázanost kvantový svět Fyzka jako dobrodružství poznání MFF UK v Praze, letní semestr 5 Q-svět Nanofyzka Fyzka kondenzované
Pavel Cejnar Ústav částcové a jaderné fyzky MFF UK Přednáška 6 Neurčtost a provázanost kvantový svět Fyzka jako dobrodružství poznání MFF UK v Praze, letní semestr 5 Q-svět Nanofyzka Fyzka kondenzované
Modelové výpočty na H 2 a HeH +
 Modelové výpočty na H 2 a HeH + Minimální báze Všechny teoretické poznatky je užitečné ilustrovat modelovým výpočtem. Budeme aplikovat Hartree-Fockovy výpočty na uzavřených slupkách systémů H 2 a HeH +.
Modelové výpočty na H 2 a HeH + Minimální báze Všechny teoretické poznatky je užitečné ilustrovat modelovým výpočtem. Budeme aplikovat Hartree-Fockovy výpočty na uzavřených slupkách systémů H 2 a HeH +.
Fyzika na malých rozměrech
 Fyzka na malých rozměrech Mění se klascká fyzka př zmenšování? Mění! mění se poměr mez povrchem a objemem vlv povrchového napětí vody pevnost materálů Budeme zmenšovat ještě víc! ZS 6/7 Fyzkální obraz
Fyzka na malých rozměrech Mění se klascká fyzka př zmenšování? Mění! mění se poměr mez povrchem a objemem vlv povrchového napětí vody pevnost materálů Budeme zmenšovat ještě víc! ZS 6/7 Fyzkální obraz
ANALÝZA VZTAHU DVOU SPOJITÝCH VELIČIN
 ANALÝZA VZTAHU DVOU SPOJITÝCH VELIČIN V dokumentu 7a_korelacn_a_regresn_analyza jsme řešl rozdíl mez korelační a regresní analýzou. Budeme se teď věnovat pouze lneárnímu vztahu dvou velčn, protože je nejjednodušší
ANALÝZA VZTAHU DVOU SPOJITÝCH VELIČIN V dokumentu 7a_korelacn_a_regresn_analyza jsme řešl rozdíl mez korelační a regresní analýzou. Budeme se teď věnovat pouze lneárnímu vztahu dvou velčn, protože je nejjednodušší
VÝPOČETNÍ CHEMIE V ANALÝZE STRUKTURY
 VÝPOČETNÍ CHEMIE V ANALÝZE STRUKTURY A VLASTNOSTÍ MOLEKUL Michal Čajan Katedra anorganické chemie PřF UP v Olomouci MOLEKULOVÉ MODELOVÁNÍ V CHEMII MOLEKULOVÉ MODELOVÁNÍ aplikace zobrazení a analýza strukturních
VÝPOČETNÍ CHEMIE V ANALÝZE STRUKTURY A VLASTNOSTÍ MOLEKUL Michal Čajan Katedra anorganické chemie PřF UP v Olomouci MOLEKULOVÉ MODELOVÁNÍ V CHEMII MOLEKULOVÉ MODELOVÁNÍ aplikace zobrazení a analýza strukturních
Numerická matematika 1. t = D u. x 2 (1) tato rovnice určuje chování funkce u(t, x), která závisí na dvou proměnných. První
 Numercká matematka 1 Parabolcké rovnce Budeme se zabývat rovncí t = D u x (1) tato rovnce určuje chování funkce u(t, x), která závsí na dvou proměnných. První proměnná t mívá význam času, druhá x bývá
Numercká matematka 1 Parabolcké rovnce Budeme se zabývat rovncí t = D u x (1) tato rovnce určuje chování funkce u(t, x), která závsí na dvou proměnných. První proměnná t mívá význam času, druhá x bývá
ESR, spinový hamiltonián a spektra
 ER, spnový hamltonán a spektra NMR k k získávání důležtých nformací o struktuře látky využívá gyromagnetckých vlastností atomových jader. Podobně ER (EPR) využívá k obdobným účelům gyromagnetckých vlastností
ER, spnový hamltonán a spektra NMR k k získávání důležtých nformací o struktuře látky využívá gyromagnetckých vlastností atomových jader. Podobně ER (EPR) využívá k obdobným účelům gyromagnetckých vlastností
Univerzita Karlova v Praze Matematicko-fyzikální fakulta
 Unverzta Karlova v Praze Matematcko-fyzkální fakulta Martn Golan Katedra chemcké fyzky a optky Vedoucí bakalářské práce: Doc. RNDr. Ing. Jaroslav Burda, CSc. Studjní obor: Bofyzka a chemcká fyzka 2010
Unverzta Karlova v Praze Matematcko-fyzkální fakulta Martn Golan Katedra chemcké fyzky a optky Vedoucí bakalářské práce: Doc. RNDr. Ing. Jaroslav Burda, CSc. Studjní obor: Bofyzka a chemcká fyzka 2010
2. Elektrotechnické materiály
 . Elektrotechnické materiály Předpokladem vhodného využití elektrotechnických materiálů v konstrukci elektrotechnických součástek a zařízení je znalost jejich vlastností. Elektrické vlastnosti materiálů
. Elektrotechnické materiály Předpokladem vhodného využití elektrotechnických materiálů v konstrukci elektrotechnických součástek a zařízení je znalost jejich vlastností. Elektrické vlastnosti materiálů
Zkouškový test z fyzikální a koloidní chemie
 Zkouškový test z fyzkální a kolodní cheme VZOR/1 jméno test zápočet průměr známka Čas 9 mnut. Povoleny jsou kalkulačky. Nejsou povoleny žádné písemné pomůcky. Uotázeksvýběrema,b,c...odpověd b kroužkujte.platí:
Zkouškový test z fyzkální a kolodní cheme VZOR/1 jméno test zápočet průměr známka Čas 9 mnut. Povoleny jsou kalkulačky. Nejsou povoleny žádné písemné pomůcky. Uotázeksvýběrema,b,c...odpověd b kroužkujte.platí:
FYZIKA I. Pohybová rovnice. Prof. RNDr. Vilém Mádr, CSc. Prof. Ing. Libor Hlaváč, Ph.D. Doc. Ing. Irena Hlaváčová, Ph.D. Mgr. Art.
 VYSOKÁ ŠKOLA BÁŇSKÁ TECHNICKÁ UNIVERZITA OSTRAVA FAKULTA STROJNÍ FYZIKA I Pohybová rovnce Prof. RNDr. Vlém Mádr, CSc. Prof. Ing. Lbor Hlaváč, Ph.D. Doc. Ing. Irena Hlaváčová, Ph.D. Mgr. Art. Dagmar Mádrová
VYSOKÁ ŠKOLA BÁŇSKÁ TECHNICKÁ UNIVERZITA OSTRAVA FAKULTA STROJNÍ FYZIKA I Pohybová rovnce Prof. RNDr. Vlém Mádr, CSc. Prof. Ing. Lbor Hlaváč, Ph.D. Doc. Ing. Irena Hlaváčová, Ph.D. Mgr. Art. Dagmar Mádrová
1.3. Transport iontů v elektrickém poli
 .3. Transport ontů v elektrckém pol Ionty se v roztoku vystaveném působení elektrckého pole pohybují katonty směrem ke katodě, anonty k anodě. Tento pohyb ontů se označuje jako mgrace. VODIVOST Vodvost
.3. Transport ontů v elektrckém pol Ionty se v roztoku vystaveném působení elektrckého pole pohybují katonty směrem ke katodě, anonty k anodě. Tento pohyb ontů se označuje jako mgrace. VODIVOST Vodvost
Odraz a lom rovinné monochromatické vlny na rovinném rozhraní dvou izotropních prostředí
 Odraz a lom rovnné monochromatcké vlny na rovnném rozhraní dvou zotropních prostředí Doplňující předpoklady: prostředí č.1, ze kterého vlna dopadá na rozhraní neabsorbuje (má r r reálný ndex lomu), obě
Odraz a lom rovnné monochromatcké vlny na rovnném rozhraní dvou zotropních prostředí Doplňující předpoklady: prostředí č.1, ze kterého vlna dopadá na rozhraní neabsorbuje (má r r reálný ndex lomu), obě
John Dalton Amadeo Avogadro
 Spojením atomů vznikají molekuly... John Dalton 1766 1844 Amadeo Avogadro 1776 1856 Výpočet molekuly 2, metoda valenční vazby Walter eitler 1904 1981 Fritz W. London 1900 1954 Teorie molekulových orbitalů
Spojením atomů vznikají molekuly... John Dalton 1766 1844 Amadeo Avogadro 1776 1856 Výpočet molekuly 2, metoda valenční vazby Walter eitler 1904 1981 Fritz W. London 1900 1954 Teorie molekulových orbitalů
Mechatronické systémy s elektronicky komutovanými motory
 Mechatroncké systémy s elektroncky komutovaným motory 1. EC motor Uvedený motor je zvláštním typem synchronního motoru nazývaný též bezkartáčovým stejnosměrným motorem (anglcky Brushless Drect Current
Mechatroncké systémy s elektroncky komutovaným motory 1. EC motor Uvedený motor je zvláštním typem synchronního motoru nazývaný též bezkartáčovým stejnosměrným motorem (anglcky Brushless Drect Current
Atomové a molekulové orbitaly Ion molekuly vodíku. Molekula vodíku Heitler-Londonovou metodou. Metoda LCAO. Báze atomových orbitalů.
 Atomové a molekulové orbitaly Ion molekuly vodíku. Molekula vodíku Heitler-Londonovou metodou. Metoda LCAO. Báze atomových orbitalů. Ion molekuly vodíku H + 2 První použití metody je demonstrováno při
Atomové a molekulové orbitaly Ion molekuly vodíku. Molekula vodíku Heitler-Londonovou metodou. Metoda LCAO. Báze atomových orbitalů. Ion molekuly vodíku H + 2 První použití metody je demonstrováno při
VÍTEJTE V MIKROSVĚTĚ
 VÍTEJTE V MIKROSVĚTĚ Klasická vs. Moderní fyzika Klasická fyzika fyzika obyčejných věcí viditelných pouhým okem Moderní fyzika Relativita zabývá se tím co se pohybuje rychle nebo v silovém gravitačním
VÍTEJTE V MIKROSVĚTĚ Klasická vs. Moderní fyzika Klasická fyzika fyzika obyčejných věcí viditelných pouhým okem Moderní fyzika Relativita zabývá se tím co se pohybuje rychle nebo v silovém gravitačním
Počátky kvantové mechaniky. Petr Beneš ÚTEF
 Počátky kvantové mechaniky Petr Beneš ÚTEF Úvod Stav fyziky k 1. 1. 1900 Hypotéza atomu velmi rozšířená, ne vždy však přijatá. Atomy bodové, není jasné, jak se liší atomy jednotlivých prvků. Elektron byl
Počátky kvantové mechaniky Petr Beneš ÚTEF Úvod Stav fyziky k 1. 1. 1900 Hypotéza atomu velmi rozšířená, ne vždy však přijatá. Atomy bodové, není jasné, jak se liší atomy jednotlivých prvků. Elektron byl
Elektronový obal atomu
 Elektronový obal atomu Vlnění o frekvenci v se může chovat jako proud částic (kvant - fotonů) o energii E = h.v Částice pohybující se s hybností p se může chovat jako vlna o vlnové délce λ = h/p Kde h
Elektronový obal atomu Vlnění o frekvenci v se může chovat jako proud částic (kvant - fotonů) o energii E = h.v Částice pohybující se s hybností p se může chovat jako vlna o vlnové délce λ = h/p Kde h
Neparametrické metody
 Neparametrcké metody Přestože parametrcké metody zaujímají klíčovou úlohu ve statstcké analýze dat, je možné některé problémy řešt př neparametrckém přístupu. V této přednášce uvedeme neparametrcké odhady
Neparametrcké metody Přestože parametrcké metody zaujímají klíčovou úlohu ve statstcké analýze dat, je možné některé problémy řešt př neparametrckém přístupu. V této přednášce uvedeme neparametrcké odhady
Přednáška 9 Reverzibilita fyzikálních procesů a šipka času
 Pavel Cejnar Ústav částcové a jaderné fyzky MFF UK Přednáška 9 Reverzblta fyzkálních procesů a špka času Fyzka jako dobrodružství poznání MFF UK v Praze, letní semestr 05 Reverzblta fyzkálních zákonů I
Pavel Cejnar Ústav částcové a jaderné fyzky MFF UK Přednáška 9 Reverzblta fyzkálních procesů a špka času Fyzka jako dobrodružství poznání MFF UK v Praze, letní semestr 05 Reverzblta fyzkálních zákonů I
PLANCK EINSTEIN BOHR de BROGLIE
 KVANTOVÁ MECHANIKA PLANCK 1858-1947 EINSTEIN 1879-1955 BOHR 1885-1962 de BROGLIE 1892-1987 HEISENBERG 1901-1976 SCHRÖDINGER 1887-1961 BORN 1882-1970 JORDAN 1902-1980 PAULI 1900-1958 DIRAC 1902-1984 VŠECHNO
KVANTOVÁ MECHANIKA PLANCK 1858-1947 EINSTEIN 1879-1955 BOHR 1885-1962 de BROGLIE 1892-1987 HEISENBERG 1901-1976 SCHRÖDINGER 1887-1961 BORN 1882-1970 JORDAN 1902-1980 PAULI 1900-1958 DIRAC 1902-1984 VŠECHNO
3. Absorpční spektroskopie
 3. Absorpční spetrosope Lambert-Beerův záon Nechť olmovaný svaze ntenzty (λ) dopadá na homogenní planparalelní vrstvu tloušťy l. (λ) (x) Př průchodu vrstvou (x, x+dx) se ntenzta dx sníží o d = -α(λ) (λ,x)
3. Absorpční spetrosope Lambert-Beerův záon Nechť olmovaný svaze ntenzty (λ) dopadá na homogenní planparalelní vrstvu tloušťy l. (λ) (x) Př průchodu vrstvou (x, x+dx) se ntenzta dx sníží o d = -α(λ) (λ,x)
5 Potenciály s δ funkcemi I
 5 Potenciály s δ funkcemi 5. Jednoduchá δ jáma nebo bariéra Mějme potenciál ve tvaru jednoduché δ funkce V cδ, kde c je konstanta, jejíž velikost udává sílu potenciálu. Pokud je c
5 Potenciály s δ funkcemi 5. Jednoduchá δ jáma nebo bariéra Mějme potenciál ve tvaru jednoduché δ funkce V cδ, kde c je konstanta, jejíž velikost udává sílu potenciálu. Pokud je c
Q N v místě r. Zobecnění Coulombova zákona Q 3 Q 4 Q 1 Q 2
 Zobecnění Coulombova zákona Uvažme nyní, jaké elektostatcké pole vytvoří ne jeden centální) bodový náboj, ale více nábojů, tzv. soustava bodových) nábojů : echť je náboj v místě v místě.... v místě Pak
Zobecnění Coulombova zákona Uvažme nyní, jaké elektostatcké pole vytvoří ne jeden centální) bodový náboj, ale více nábojů, tzv. soustava bodových) nábojů : echť je náboj v místě v místě.... v místě Pak
Fyzika IV. Pojem prvku. alchymie. Paracelsus (16.st) Elektronová struktura atomů
 Elektronová struktura atomů Pojem prvku alchymie Paracelsus (16.st) Elektronová struktura atomů alchymie 17.-18.století - při hoření látky ztrácí těkavou součást - flogiston. látka = flogiston + popel
Elektronová struktura atomů Pojem prvku alchymie Paracelsus (16.st) Elektronová struktura atomů alchymie 17.-18.století - při hoření látky ztrácí těkavou součást - flogiston. látka = flogiston + popel
Úvod do moderní fyziky. lekce 3 stavba a struktura atomu
 Úvod do moderní fyziky lekce 3 stavba a struktura atomu Vývoj představ o stavbě atomu 1904 J. J. Thomson pudinkový model atomu 1909 H. Geiger, E. Marsden experiment s ozařováním zlaté fólie alfa částicemi
Úvod do moderní fyziky lekce 3 stavba a struktura atomu Vývoj představ o stavbě atomu 1904 J. J. Thomson pudinkový model atomu 1909 H. Geiger, E. Marsden experiment s ozařováním zlaté fólie alfa částicemi
Inovace studia molekulární a buněčné biologie reg. č. CZ.1.07/2.2.00/
 Inovace studia molekulární a buněčné biologie reg. č. CZ.1.07/2.2.00/07.0354 Předmět: LRR/CHPB1/Chemie pro biology 1 Elektronový obal Mgr. Karel Doležal Dr. Cíl přednášky: seznámit posluchače se stavbou
Inovace studia molekulární a buněčné biologie reg. č. CZ.1.07/2.2.00/07.0354 Předmět: LRR/CHPB1/Chemie pro biology 1 Elektronový obal Mgr. Karel Doležal Dr. Cíl přednášky: seznámit posluchače se stavbou
Vibrace atomů v mřížce, tepelná kapacita pevných látek
 Vibrace atomů v mřížce, tepelná kapacita pevných látek Atomy vázané v mřížce nejsou v klidu. Míru jejich pohybu vyjadřuje podobně jako u plynů a kapalin teplota. - Elastické vlny v kontinuu neatomární
Vibrace atomů v mřížce, tepelná kapacita pevných látek Atomy vázané v mřížce nejsou v klidu. Míru jejich pohybu vyjadřuje podobně jako u plynů a kapalin teplota. - Elastické vlny v kontinuu neatomární
Interpretační dokumenty ID1 až ID6
 Prof. Ing. Mlan Holcký, DrSc. ČVUT, Šolínova 7, 66 08 Praha 6 Tel.: 224 353 842, Fax: 224 355 232 E-mal: holcky@klok.cvut.cz, k http://web.cvut.cz/k/70/prednaskyfa.html Metody navrhování Základní pojmy
Prof. Ing. Mlan Holcký, DrSc. ČVUT, Šolínova 7, 66 08 Praha 6 Tel.: 224 353 842, Fax: 224 355 232 E-mal: holcky@klok.cvut.cz, k http://web.cvut.cz/k/70/prednaskyfa.html Metody navrhování Základní pojmy
Elektromagnetické záření. lineárně polarizované záření. Cirkulárně polarizované záření
 Elektromagnetické záření lineárně polarizované záření Cirkulárně polarizované záření Levotočivé Pravotočivé 1 Foton Jakékoli elektromagnetické vlnění je kvantováno na fotony, charakterizované: Vlnovou
Elektromagnetické záření lineárně polarizované záření Cirkulárně polarizované záření Levotočivé Pravotočivé 1 Foton Jakékoli elektromagnetické vlnění je kvantováno na fotony, charakterizované: Vlnovou
Interakce. Přednáška 3, ve které se pokusíme přiblížit elementárním kvantovým procesům. Pavel Cejnar. Principy kvantové fyziky
 Pavel Cejnar Ústav částcové a jaderné fyzky MFF UK Přednáška 3, ve které se pokusíme přblížt elementárním kvantovým procesům Interakce Prncpy kvantové fyzky Fyzka jako dobrodružství poznání MFF UK v Praze,
Pavel Cejnar Ústav částcové a jaderné fyzky MFF UK Přednáška 3, ve které se pokusíme přblížt elementárním kvantovým procesům Interakce Prncpy kvantové fyzky Fyzka jako dobrodružství poznání MFF UK v Praze,
Hamiltonián popisující atom vodíku ve vnějším magnetickém poli:
 Orbitální a spinový magnetický moment a jejich interakce s vnějším polem Vše na příkladu atomu H: Elektron (e - ) a jádro (u atomu H pouze p + ) mají vlastní magnetický moment (= spin). Tyto dva dipóly
Orbitální a spinový magnetický moment a jejich interakce s vnějším polem Vše na příkladu atomu H: Elektron (e - ) a jádro (u atomu H pouze p + ) mají vlastní magnetický moment (= spin). Tyto dva dipóly
Kovy - model volných elektronů
 Kovy - model volných elektronů Kovová vazba 1. Preferuje ji většina prvků vyskytujících se v přírodě. Kov je tvořen kladně nabitými ionty (s konfigurací vzácného plynu) a relativně velmi volnými elektrony.
Kovy - model volných elektronů Kovová vazba 1. Preferuje ji většina prvků vyskytujících se v přírodě. Kov je tvořen kladně nabitými ionty (s konfigurací vzácného plynu) a relativně velmi volnými elektrony.
Na základě toho vysvětlil Eisnstein vnější fotoefekt, kterým byla platnost tohoto vztahu povrzena.
 Vlnově-korpuskulární dualismus, fotony, fotoelektrický jev vnější a vnitřní. Elmg. teorie záření vysvětluje dobře mnohé jevy v optice interference, difrakci, polarizaci. Nelze jí ale vysvětlit např. fotoelektrický
Vlnově-korpuskulární dualismus, fotony, fotoelektrický jev vnější a vnitřní. Elmg. teorie záření vysvětluje dobře mnohé jevy v optice interference, difrakci, polarizaci. Nelze jí ale vysvětlit např. fotoelektrický
Jednosložkové soustavy
 Jednosložkové soustavy Fázové rovnováhy Prezentace je určena pro výuku. roč. studjního oboru Nanotechnologí a není dovoleno její šíření bez vědomí garanta předmětu. K jejímu vytvoření bylo použto materálů
Jednosložkové soustavy Fázové rovnováhy Prezentace je určena pro výuku. roč. studjního oboru Nanotechnologí a není dovoleno její šíření bez vědomí garanta předmětu. K jejímu vytvoření bylo použto materálů
Modelování rizikových stavů v rodinných domech
 26. 28. června 2012, Mkulov Modelování rzkových stavů v rodnných domech Mlada Kozubková 1, Marán Bojko 2, Jaroslav Krutl 3 1 2 3 Vysoká škola báňská techncká unverzta Ostrava, Fakulta strojní, Katedra
26. 28. června 2012, Mkulov Modelování rzkových stavů v rodnných domech Mlada Kozubková 1, Marán Bojko 2, Jaroslav Krutl 3 1 2 3 Vysoká škola báňská techncká unverzta Ostrava, Fakulta strojní, Katedra
Stavba hmoty. Atomová teorie Korpuskulární model látky - chemické
 Stavba hmoty Atomová teorie Korpuskulární model látky - chemické látky jsou složeny z mikroskopických, chemicky dále neděčástic atomů. Později byl model rozšířen na molekuly a ionty (chemický druh - specie).
Stavba hmoty Atomová teorie Korpuskulární model látky - chemické látky jsou složeny z mikroskopických, chemicky dále neděčástic atomů. Později byl model rozšířen na molekuly a ionty (chemický druh - specie).
Praktikum III - Optika
 Oddělení fyzikálních praktik při Kabinetu výuky obecné fyziky MFF UK Praktikum III - Optika Úloha č. 13 Název: Vlastnosti rentgenového záření Pracoval: Matyáš Řehák stud.sk.: 13 dne: 3. 4. 2008 Odevzdal
Oddělení fyzikálních praktik při Kabinetu výuky obecné fyziky MFF UK Praktikum III - Optika Úloha č. 13 Název: Vlastnosti rentgenového záření Pracoval: Matyáš Řehák stud.sk.: 13 dne: 3. 4. 2008 Odevzdal
Regresní a korelační analýza
 Regresní a korelační analýza Závslost příčnná (kauzální). Závslostí pevnou se označuje případ, kdy výskytu jednoho jevu nutně odpovídá výskyt druhé jevu (a často naopak). Z pravděpodobnostního hledska
Regresní a korelační analýza Závslost příčnná (kauzální). Závslostí pevnou se označuje případ, kdy výskytu jednoho jevu nutně odpovídá výskyt druhé jevu (a často naopak). Z pravděpodobnostního hledska
Přednášky část 4 Analýza provozních zatížení a hypotézy kumulace poškození, příklady. Milan Růžička
 Přednášky část 4 Analýza provozních zatížení a hypotézy kumulace poškození, příklady Mlan Růžčka mechanka.fs.cvut.cz mlan.ruzcka@fs.cvut.cz Analýza dynamckých zatížení Harmoncké zatížení x(t) přes soubor
Přednášky část 4 Analýza provozních zatížení a hypotézy kumulace poškození, příklady Mlan Růžčka mechanka.fs.cvut.cz mlan.ruzcka@fs.cvut.cz Analýza dynamckých zatížení Harmoncké zatížení x(t) přes soubor
ATOM VODÍKU MODEL : STOJÍCÍ BODOVÉ JÁDRO A ELEKTRON VZÁJEMNĚ ELEKTROSTATICKY INTERAGUJÍCÍ SCHRÖDINGEROVA ROVNICE PRO PŘÍPAD POTENCIÁLNÍ ENERGIE.
 ATOMY + MOLEKULY ATOM VODÍKU MODEL : STOJÍCÍ BODOVÉ JÁDRO A ELEKTRON VZÁJEMNĚ ELEKTROSTATICKY INTERAGUJÍCÍ SCHRÖDINGEROVA ROVNICE H ˆψ = Eψ PRO PŘÍPAD POTENCIÁLNÍ ENERGIE Vˆ = Ze 2 4πε o r ŘEŠENÍ HLEDÁME
ATOMY + MOLEKULY ATOM VODÍKU MODEL : STOJÍCÍ BODOVÉ JÁDRO A ELEKTRON VZÁJEMNĚ ELEKTROSTATICKY INTERAGUJÍCÍ SCHRÖDINGEROVA ROVNICE H ˆψ = Eψ PRO PŘÍPAD POTENCIÁLNÍ ENERGIE Vˆ = Ze 2 4πε o r ŘEŠENÍ HLEDÁME
Mul$determinantální metody: CASSCF
 Mul$determinantální metody: CASSCF Mul%konfiguračni (mnohadeterninantálni MC SCF) metody použivají narozdíl od metody Hartreeho- Focka pro popis N- elektronového systému větší počet Slaterových determinantů.
Mul$determinantální metody: CASSCF Mul%konfiguračni (mnohadeterninantálni MC SCF) metody použivají narozdíl od metody Hartreeho- Focka pro popis N- elektronového systému větší počet Slaterových determinantů.
6 PŘEDNÁŠKA 6: Stav kvantového systému, úplná množina pozorovatelných. Operátor momentu hybnosti a kvadrátu momentu hybnosti.
 6 PŘEDNÁŠKA 6: Stav kvantového systému, úplná množina pozorovatelných Operátor momentu hybnosti a kvadrátu momentu hybnosti Víme už tedy téměř vše o operátorech Jsou to vlastně měřící přístroje v kvantové
6 PŘEDNÁŠKA 6: Stav kvantového systému, úplná množina pozorovatelných Operátor momentu hybnosti a kvadrátu momentu hybnosti Víme už tedy téměř vše o operátorech Jsou to vlastně měřící přístroje v kvantové
3 Základní modely reaktorů
 3 Základní modely reaktorů Rovnce popsující chování reakční směs v reaktoru (v čase a prostoru) vycházejí z blančních rovnc pro hmotu, energ a hybnost. Blanc lze formulovat pro extenzvní velčnu B v obecném
3 Základní modely reaktorů Rovnce popsující chování reakční směs v reaktoru (v čase a prostoru) vycházejí z blančních rovnc pro hmotu, energ a hybnost. Blanc lze formulovat pro extenzvní velčnu B v obecném
Inovace studia molekulární a buněčné biologie
 Investice do rozvoje vzdělávání Inovace studia molekulární a buněčné biologie Tento projekt je spolufinancován Evropským sociálním fondem a státním rozpočtem České republiky. Investice do rozvoje vzdělávání
Investice do rozvoje vzdělávání Inovace studia molekulární a buněčné biologie Tento projekt je spolufinancován Evropským sociálním fondem a státním rozpočtem České republiky. Investice do rozvoje vzdělávání
13 Elektronová struktura molekul
 13 Elektronová struktura molekul Ústředním úkolem kvantové chemie po zavedení Bornovy-Oppenheimerovy aproximace je výpočet elektronové energie molekul Ĥ e ψ e ( r, R) = E e ( R)ψ e ( r, R), (13.1) kde
13 Elektronová struktura molekul Ústředním úkolem kvantové chemie po zavedení Bornovy-Oppenheimerovy aproximace je výpočet elektronové energie molekul Ĥ e ψ e ( r, R) = E e ( R)ψ e ( r, R), (13.1) kde
Řešit atom vodíku znamená nalézt řešení Schrödingerovy rovnice s příslušným hamiltoniánem. 1 4πǫ 0. 2m e
 8 Atom vodíku Správné řešení atomu vodíku je jedním z velkých vítězství kvantové mechaniky. Podle klasické fyziky náboj, který se pohybuje se zrychlením (elektron obíhající vodíkové jádro proton), by měl
8 Atom vodíku Správné řešení atomu vodíku je jedním z velkých vítězství kvantové mechaniky. Podle klasické fyziky náboj, který se pohybuje se zrychlením (elektron obíhající vodíkové jádro proton), by měl
Analýza závislosti veličin sledovaných v rámci TBD
 Analýza závslost velčn sledovaných v rámc BD Helena Koutková Vysoké učení techncké v Brně, Fakulta stavební, Ústav matematky a deskrptvní geometre e-mal: koutkovah@fcevutbrcz Abstrakt Příspěvek se zabývá
Analýza závslost velčn sledovaných v rámc BD Helena Koutková Vysoké učení techncké v Brně, Fakulta stavební, Ústav matematky a deskrptvní geometre e-mal: koutkovah@fcevutbrcz Abstrakt Příspěvek se zabývá
2.5. MATICOVÉ ŘEŠENÍ SOUSTAV LINEÁRNÍCH ROVNIC
 25 MATICOVÉ ŘEŠENÍ SOUSTAV LINEÁRNÍCH ROVNIC V této kaptole se dozvíte: jak lze obecnou soustavu lneárních rovnc zapsat pomocí matcového počtu; přesnou formulac podmínek řeštelnost soustavy lneárních rovnc
25 MATICOVÉ ŘEŠENÍ SOUSTAV LINEÁRNÍCH ROVNIC V této kaptole se dozvíte: jak lze obecnou soustavu lneárních rovnc zapsat pomocí matcového počtu; přesnou formulac podmínek řeštelnost soustavy lneárních rovnc
Druhé kvantování. Slaterův determinant = χ χ
 Druhé kvntování Druhé kvntování žádná nová fyzk! jný formlsmus upltnění prncpu ntsymetre bez použtí Slterových determnntů. Antsymetrcké vlstnost vlnových funkcí jsou přeneseny n lgebrcké vlstnost dných
Druhé kvntování Druhé kvntování žádná nová fyzk! jný formlsmus upltnění prncpu ntsymetre bez použtí Slterových determnntů. Antsymetrcké vlstnost vlnových funkcí jsou přeneseny n lgebrcké vlstnost dných
Spinový moment hybnosti /magnetický moment, interakce s magnetickým polem
 Spnový oent hybnost /anetcký oent, nterakce s anetcký pole Velkost jednoho elektronového spnu: Velkost jednoho jaderného spnu: s s( s ) 3 ( ) Sudé Sudé Z 0 Sudé Lché Z... apř: He, C, 6 O celočíselné apř:
Spnový oent hybnost /anetcký oent, nterakce s anetcký pole Velkost jednoho elektronového spnu: Velkost jednoho jaderného spnu: s s( s ) 3 ( ) Sudé Sudé Z 0 Sudé Lché Z... apř: He, C, 6 O celočíselné apř:
CHYBY MĚŘENÍ. uvádíme ve tvaru x = x ± δ.
 CHYBY MĚŘENÍ Úvod Představte s, že máte změřt délku válečku. Použjete posuvné měřítko a získáte určtou hodnotu. Pamětlv přísloví provedete ještě jedno měření. Ale ouha! Výsledek je jný. Co dělat? Měřt
CHYBY MĚŘENÍ Úvod Představte s, že máte změřt délku válečku. Použjete posuvné měřítko a získáte určtou hodnotu. Pamětlv přísloví provedete ještě jedno měření. Ale ouha! Výsledek je jný. Co dělat? Měřt
Molekuly. Všeobecně známý fakt: atomy se slučujou do molekul, pokud to zrovna nejsou atomy inertních plynů v posledním sloupci periodické tabulky
 Molekuly Všeobecně známý fakt: atomy se slučujou do molekul, pokud to zrovna nejsou atomy inertních plynů v posledním sloupci periodické tabulky Nejjednodušší případ: molekulární iont H +, tj. dva protony
Molekuly Všeobecně známý fakt: atomy se slučujou do molekul, pokud to zrovna nejsou atomy inertních plynů v posledním sloupci periodické tabulky Nejjednodušší případ: molekulární iont H +, tj. dva protony
Určení tlouštky folie metodou konvergentního elektronového svazku (TEM)-studijní text.
 Určení tlouštky fole metodou konverentního elektronového svazku (TEM)-studjní text. Pracovní úkol: 1) Nastavte a vyfotorafujte snímek dfrakce elektronů v konverentním svazku, který je vhodný pro určení
Určení tlouštky fole metodou konverentního elektronového svazku (TEM)-studjní text. Pracovní úkol: 1) Nastavte a vyfotorafujte snímek dfrakce elektronů v konverentním svazku, který je vhodný pro určení
ATOMOVÁ SPEKTROMETRIE
 ATOMOVÁ SPEKTROMETRIE Atomová spektrometrie valenčních e - 1. OES (AES). AAS 3. AFS 1 Atomová spektra čárová spektra Tok záření P - množství zářivé energie (Q E ) přenesené od zdroje za jednotku času.
ATOMOVÁ SPEKTROMETRIE Atomová spektrometrie valenčních e - 1. OES (AES). AAS 3. AFS 1 Atomová spektra čárová spektra Tok záření P - množství zářivé energie (Q E ) přenesené od zdroje za jednotku času.
Elektromagnetické vlnění, vlny a částice
 Elektromagnetické vlnění, vlny a částice Vznik elektromagnetického záření Elektromagnetické vlnění vzniká, když částice s elektrickým nábojem se pohybuje se zrychlením. Příklady: - Střídavé napětí v anténě:
Elektromagnetické vlnění, vlny a částice Vznik elektromagnetického záření Elektromagnetické vlnění vzniká, když částice s elektrickým nábojem se pohybuje se zrychlením. Příklady: - Střídavé napětí v anténě:
Fyzika atomového jádra
 Fyzika atomového jádra (NJSF064) František Knapp http://www-ucjf.troja.mff.cuni.cz/~knapp/jf/ frantisek.knapp@mff.cuni.cz Slupkový model jádra evidence magických čísel: hmoty, separační energie, vazbové
Fyzika atomového jádra (NJSF064) František Knapp http://www-ucjf.troja.mff.cuni.cz/~knapp/jf/ frantisek.knapp@mff.cuni.cz Slupkový model jádra evidence magických čísel: hmoty, separační energie, vazbové
Ideální krystalová mřížka periodický potenciál v krystalu. pásová struktura polovodiče
 Cvičení 3 Ideální krystalová mřížka periodický potenciál v krystalu Aplikace kvantové mechaniky pásová struktura polovodiče Nosiče náboje v polovodiči hustota stavů obsazovací funkce, Fermiho hladina koncentrace
Cvičení 3 Ideální krystalová mřížka periodický potenciál v krystalu Aplikace kvantové mechaniky pásová struktura polovodiče Nosiče náboje v polovodiči hustota stavů obsazovací funkce, Fermiho hladina koncentrace
POKUSY VEDOUCÍ KE KVANTOVÉ MECHANICE III
 POKUSY VEDOUCÍ KE KVANTOVÉ MECHANICE III FOTOELEKTRICKÝ JEV OBJEV ATOMOVÉHO JÁDRA 1911 Rutherford některé radioaktivní prvky vyzařují částice α, jde o kladné částice s nábojem 2e a hmotností 4 vodíkových
POKUSY VEDOUCÍ KE KVANTOVÉ MECHANICE III FOTOELEKTRICKÝ JEV OBJEV ATOMOVÉHO JÁDRA 1911 Rutherford některé radioaktivní prvky vyzařují částice α, jde o kladné částice s nábojem 2e a hmotností 4 vodíkových
Transport hmoty a tepla v mikrofluidních systémech
 Transport hmoty a tepla v mkrofludních systémech Konvektvní transport v zařízeních s malým charakterstckým rozměrem Konvektvní tok vznká působením plošných, objemových, nercálních a třecích sl v objemu
Transport hmoty a tepla v mkrofludních systémech Konvektvní transport v zařízeních s malým charakterstckým rozměrem Konvektvní tok vznká působením plošných, objemových, nercálních a třecích sl v objemu
Dr. Petr Jizba. I. Relativistická QM a dráhové integrály. Ia. Bezspinová částice a bosonová struna
 Příklady k předmětu Metody Funkconálního Integrálu Dr Petr Jzba I Relatvstcká QM a dráhové ntegrály Ia Bezspnová částce a bosonová struna Příklad 1: Dokažte, že na úrovn pohybových rovnc jsou následující
Příklady k předmětu Metody Funkconálního Integrálu Dr Petr Jzba I Relatvstcká QM a dráhové ntegrály Ia Bezspnová částce a bosonová struna Příklad 1: Dokažte, že na úrovn pohybových rovnc jsou následující
OPVK CZ.1.07/2.2.00/
 18.2.2013 OPVK CZ.1.07/2.2.00/28.0184 Cvičení z NMR OCH/NMR Mgr. Tomáš Pospíšil, Ph.D. LS 2012/2013 18.2.2013 NMR základní principy NMR Nukleární Magnetická Resonance N - nukleární (studujeme vlastnosti
18.2.2013 OPVK CZ.1.07/2.2.00/28.0184 Cvičení z NMR OCH/NMR Mgr. Tomáš Pospíšil, Ph.D. LS 2012/2013 18.2.2013 NMR základní principy NMR Nukleární Magnetická Resonance N - nukleární (studujeme vlastnosti
Diskutujte, jak široký bude pás spojený s fosforescencí versus fluorescencí. Udělejte odhad v cm -1.
 S použitím modelu volného elektronu (=částice v krabici) spočtěte vlnovou délku a vlnočet nejdlouhovlnějšího elektronového přechodu u molekuly dekapentaenu a oktatetraenu. Diskutujte polohu absorpčního
S použitím modelu volného elektronu (=částice v krabici) spočtěte vlnovou délku a vlnočet nejdlouhovlnějšího elektronového přechodu u molekuly dekapentaenu a oktatetraenu. Diskutujte polohu absorpčního
elektrony v pevné látce verze 1. prosince 2016
 F6122 Základy fyziky pevných látek seminář elektrony v pevné látce verze 1. prosince 2016 1 Drudeho model volných elektronů 1 1.1 Mathiessenovo pravidlo............................................... 1
F6122 Základy fyziky pevných látek seminář elektrony v pevné látce verze 1. prosince 2016 1 Drudeho model volných elektronů 1 1.1 Mathiessenovo pravidlo............................................... 1
6 LINEÁRNÍ REGRESNÍ MODELY
 1 6 LINEÁRNÍ REGRESNÍ MODELY Př budování regresních modelů se běžně užívá metody nejmenších čtverců. Metoda nejmenších čtverců poskytuje postačující odhady parametrů jenom př současném splnění všech předpokladů
1 6 LINEÁRNÍ REGRESNÍ MODELY Př budování regresních modelů se běžně užívá metody nejmenších čtverců. Metoda nejmenších čtverců poskytuje postačující odhady parametrů jenom př současném splnění všech předpokladů
í I - 13 - Průchod a rozptyl záření gama ve vrstvách materiálu Prof. Ing. J. Šeda, DrSc. KDAIZ - PJPI
 - 13 - í Průchod a rozptyl záření gama ve vrstvách materálu Prof. ng. J. Šeda, DrSc. KDAZ - PJP Na našem pracovšt byl vypracován program umožňující modelovat průchod záření gama metodou Monte Carlo, homogenním
- 13 - í Průchod a rozptyl záření gama ve vrstvách materálu Prof. ng. J. Šeda, DrSc. KDAZ - PJP Na našem pracovšt byl vypracován program umožňující modelovat průchod záření gama metodou Monte Carlo, homogenním
Nerovnovážné systémy Onsagerova hypotéza, fluktuačně disipační teorém
 Nerovnovážné systémy Onsagerova hypotéza, fluktuačně disipační teorém Omezení se na nerovnážné systémy v blízkosti rovnováhy Chování systému lze popsat v rámci linear response theory (teorie lineární odezvy)
Nerovnovážné systémy Onsagerova hypotéza, fluktuačně disipační teorém Omezení se na nerovnážné systémy v blízkosti rovnováhy Chování systému lze popsat v rámci linear response theory (teorie lineární odezvy)
FYZIKA MIKROSVĚTA. Mgr. Jan Ptáčník - GJVJ - Fyzika - Fyzika mikrosvěta - 3. ročník
 FYZIKA MIKROSVĚTA Mgr. Jan Ptáčník - GJVJ - Fyzika - Fyzika mikrosvěta - 3. ročník Mikrosvět Svět o rozměrech 10-9 až 10-18 m. Mikrosvět není zmenšeným makrosvětem! Chování v mikrosvětě popisuje kvantová
FYZIKA MIKROSVĚTA Mgr. Jan Ptáčník - GJVJ - Fyzika - Fyzika mikrosvěta - 3. ročník Mikrosvět Svět o rozměrech 10-9 až 10-18 m. Mikrosvět není zmenšeným makrosvětem! Chování v mikrosvětě popisuje kvantová
Ing. Pavel Hrzina, Ph.D. - Laboratoř diagnostiky fotovoltaických systémů Katedra elektrotechnologie K13113
 Sluneční energie, fotovoltaický jev Ing. Pavel Hrzina, Ph.D. - Laboratoř diagnostiky fotovoltaických systémů Katedra elektrotechnologie K13113 1 Osnova přednášky Slunce jako zdroj energie Vlastnosti slunečního
Sluneční energie, fotovoltaický jev Ing. Pavel Hrzina, Ph.D. - Laboratoř diagnostiky fotovoltaických systémů Katedra elektrotechnologie K13113 1 Osnova přednášky Slunce jako zdroj energie Vlastnosti slunečního
2. Atomové jádro a jeho stabilita
 2. Atomové jádro a jeho stabilita Atom je nejmenší hmotnou a chemicky nedělitelnou částicí. Je tvořen jádrem, které obsahuje protony a neutrony, a elektronovým obalem. Elementární částice proton neutron
2. Atomové jádro a jeho stabilita Atom je nejmenší hmotnou a chemicky nedělitelnou částicí. Je tvořen jádrem, které obsahuje protony a neutrony, a elektronovým obalem. Elementární částice proton neutron
Optické spektroskopie 1 LS 2014/15
 Optické spektroskopie 1 LS 2014/15 Martin Kubala 585634179 mkubala@prfnw.upol.cz 1.Úvod Velikosti objektů v přírodě Dítě ~ 1 m (10 0 m) Prst ~ 2 cm (10-2 m) Vlas ~ 0.1 mm (10-4 m) Buňka ~ 20 m (10-5 m)
Optické spektroskopie 1 LS 2014/15 Martin Kubala 585634179 mkubala@prfnw.upol.cz 1.Úvod Velikosti objektů v přírodě Dítě ~ 1 m (10 0 m) Prst ~ 2 cm (10-2 m) Vlas ~ 0.1 mm (10-4 m) Buňka ~ 20 m (10-5 m)
