Lehký úvod do elektrostatiky { vakuum ( ε = ε 0 )
|
|
|
- Božena Vaňková
- před 5 lety
- Počet zobrazení:
Transkript
1 Lehký úvod do elektrostatiky { vakuum ( ε = ε 0 ) 1/16 Síla na náboj q zpùsobená nábojem Q: F = 1 qq r 4πε 0 r 2 r Intenzita pole: E = F q = 1 Q r 4πε 0 r 2 r Potenciál: φ = 1 Q 4πε 0 r, platí φ ( r φ grad φ x, y, ) φ = E z Celkový tok el. pole kulovou plochou (sférou) o polomìrur: E d s = Q sféra ε 0 Zachování poètu siloèar ( nezávisí na r ani smìru plochy) pro náboj uvnitø plochy S platí: Q = E d s ε 0 S Intenzita pole tìsnì u rovinné desky: E = Q 2ε 0 A Intenzita pole mezi deskami kondenzátoru: E = (A = plocha desky, S = 2A) Q ε 0 A
2 Lehký úvod do elektrostatiky { dielektrikum 2/16 Dielektrikum = þkladný náboj (hustota +ρ) + záporný náboj ( ρ)ÿ V el. poli v kondenzátoru Q Q se náboje posunou o d Stínící náboj vlevo je Q s, vpravo +Q s, Q s = daρ Efektivní náboj klesne v pomìru 1 : ε r (= denice ε r ): Q Q s = Q/ε r (stínící náboj = Q s, Q s > 0) Ve stejném pomìru klesne intenzita pole ( síla): E = Q Aε r ε 0 = Q Aε (def. ε = ε r ε 0 ) Objemová hustota dipólového momentu (= polarizace) v ka¾dém objemu V je (Vρd)/V = ρd = P. Dohromady: Q s = Aρd = AP = Q Q ε r, tj. Q = Q ε r + Q s = Q ε r + AP vydìlíme A a denujeme elektrickou indukci: D Q A = Q Aε r +P = ε 0 E+P = εe Kapacita kondenzátoru: C = Q φ = AD φ = AεE φ = Aε vzdálenost desek
3 Poissonova rovnice Zachovává se poèet el. indukèních èar: Q = D d s, S D = ε E Integrál spoèítáme pøes povrch krychlièky dx dy dz: dq = dvρ = D d s = dydz[d x (x + dx) D x (x)] = dxdydz S ( Dx x + D y y + D z z + dxdz[d y (y + dy) D y (y)] + dxdy[d z (z + dz) D z (z)] ) = dvε ( 2 φ x φ y φ z 2 kde ρ = dq/dv je hustota náboje a permitivita je konstantní. ) 3/16 Laplaceùv operátor: symbol nebudeme ( ) 2 pou¾ívat, aby se nepletl x y z 2 2 s φ = φ vpravo φ vlevo Poissonova rovnice: 2 φ = ρ ε nebo v jedné dimenzi d 2 φ dx 2 = ρ ε
4 Elektrická dvojvrstva { vznik 4/16 Na rozhraní (pevné látky, bublina) a iontového roztoku vzniká povrchový náboj v dùsledku rùzné anity iontù rùzného znaménka, napø.: ionizace (disociace/protonizace) skupin (-COOH se nabije zápornì, -NH 2 kladnì) pøednostní rozpou¹tìní èi adsorpce iontù (AgCl v NaCl se nabije zápornì) Panethovo{Fajansovo[{Hahnovo] pravidlo: Ionty se adsorbují z na povrchu krystalu, jestli¾e tvoøí s iontem opaèného znaménka málo rozpustnou slouèeninu pøednostní adsorpce povrchovì aktivní látky (povrch mýdlové vody je záporný) izomorfní substituce (Al 3+ /Si 4+ na povrchu jílu) roz¹típnutí krystalu Otázka: co tento náboj udìlá v?
5 Elektrická dvojvrstva: Tak ne! [show/doublelayer.sh] 5/16 Mìjme NaCl mezi elektrodami. Intenzita elektrostatického pole = E. Ionty s elektrodou neinteragují (o interakci a¾ pozdìji... ) Jak se bude mìnit koncentrace Na + a Cl mezi elektrodami? Naivní øe¹ení: elst. potenciál = φ(x) = Ex pot. energie kationtu = eφ(x) pravdìpodobnost: exp[ eφ(x)/k B T] = exp(eex/k B T) pot. energie aniontu = eφ(x) pravdìpodobnost: exp[ eφ(x)/k B T] = exp( eex/k B T) c ion /mol.dm Na + dobre Cl - dobre x/nm Na + spatne Cl - spatne Pø. NaCl 0.1 mol dm 3, vzdálenost elektrod = 50 nm, napìtí = 50 mv Neutralita (nulový potenciál) uprostøed 1 ev = J/mol : správnì : naivní øe¹ení odporuje po¾adavku elektroneutrality objemové fáze
6 Difuzní vrstva: Gouy{Chapman elektrický potenciál v objemové fázi je φ( ) = 0 6/16 elektrický potenciál na elektrodì je φ(0) = φ 0 (o pùvod φ 0 se zatím nebudeme starat) ionty jsou nabité body, elektroda je tuhá zeï elektroda neinteraguje (¾ádná adsorpce) koncentraci iontù nahradíme prùmìrnou hodnotou (zanedbáváme korelace iontù) x rozpou¹tìdlo je dielektrické kontinuum (permitivita = ε = ε r ε 0 ) omezíme se na roztok soli 1:1 o koncentraci c (lze snadno zobecnit) Poissonova rovnice: d2 φ dx 2 = ρ ε Objemová hustota náboje: ρ = z i ρ i = ρ ρ, kde i [ ρ = cf exp φ(x)e ] [ ] φ(x)e ρ = cf exp k B T k B T Rovnice pro potenciál: d2 φ dx 2 = cf [e ] φe/kbt e φe/k BT ε
7 Difuzní vrstva: Gouy{Chapman Rovnice pro potenciál (Poisson{Boltzmann): d 2 φ dx 2 = cf ε [ e φe/k BT e φe/k BT ], φ(0) = φ 0, φ( ) = 0 Linearizace aneb pøibli¾né øe¹ení pro malé potenciály (φe/k B T 1, tj. φ 26 mv pro 298 K): 7/16 exp(x) = x0 0! + x1 1! + x2 2! + x3 3! + 1+x d2 φ dx 2 = 2cF φe φ = φ ε k B T 0 e x/λ εkb T εrt λ = 2cFe = εrt = Debyeova stínící délka, smìs: λ = 2cF2 2I c F 2 Pøíklad. NaCl ve vodì c = 0.1 mol dm 3, 25 C λ = 0.96 nm (ε = ε r ε 0, ε r = 78.4, ε 0 = F m 1 ) Pro srovnání: O{O vzdálenost ve vodì 0.28 nm, 120 molekul v λ-kouli Bjerrumova délka (energie páru elementárních nábojù = k B T) λ B = e 2 4πɛk B T voda 0.7 nm
8 Difuzní vrstva: Gouy{Chapman 8/16 φ(x)/v φ 0 = 50 mv φ 0 = 0.05 V linearizovane presne x/nm 1:1 elektrolyt, c = 0.1 mol dm 3 φ(x)/v φ 0 = 100 mv φ 0 = 0.1 V linearizovane presne x/nm Potenciál (v závislosti na vzdálenosti od povrchu) ubývá exponenciálnì v dùsledku stínìní náboje ionty opaèného znaménka Nazývá se difuzní vrstva, proto¾e lze ekvivalentnì vysvìtlit jako rovnováhu mezi difuzí a pøitahováním k elektrodì
9 Elektrická dvojvrstva II 9/16 Nabitý povrch pøitahuje protiionty (counterions). Gouy-Chapman nabitý povrch difuzní vrstva postupnì odstíní náboj neutrální roztok Helmholtz nabitý povrch adsorbované protionty stíní celý náboj neutrální roztok Stern nabitý povrch adsorbované protiionty stíní èást náboje difuzní vrstva stíní zbylý náboj neutrální roztok
10 Povrchový náboj (povrchový náboj) = (náboj Gouyovy{Chapmanovy vrstvy) { [ σ = (ρ + ρ )dx = cf exp φ(x)e ] [ ]} φ(x)e exp dx 0 0 k B T k B T Pou¾ijeme linearizovanou teorii, exp(x) 1 + x, proto¾e φ(x)e/k B T 1 10/16 σ 2cF φ(x)e 0 k B T dx = 2λcFφ e 0 k B T = ε λ φ 0 (1) Kapacita Gouyovy{Chapmanovy dvojvrstvy jako kondenzátoru: C A = σ φ 0 = ε λ Zpravidla se mìøí diferenciální kapacita, dσ/dφ, proto¾e obecnì σ / φ Pøíklad. Molekula mýdla zaujímá na povrchu plochu asi a = 0.2 nm 2. Protionty jsou v o koncentraci 0.1 mol dm 3 v prùmìru λ = 1 nm daleko. a) Jaký je povrchový náboj? b) Jaké kapacitì kondenzátoru (na m 2 ) to odpovídá? (ε r = 78.) c) Jaký je potenciál povrchu mýdlové vody? a) 0.8 C m 2, b) 0.7 F m 2, c) 1.1 V (ve skut. ménì)
11 Ionty [traj/traj.sh] 11/16 Plazma, roztoky elektrolytù: interakce náboj-náboj ubývá pomalu velké odchylky od ideálního chování neexistuje B 2 helium T=300 K helium T= K
12 Debyeova{Hückelova teorie pro roztoky elektrolytù 12/16 Zjednodu¹ující pøedpoklady: rozpou¹tìdlo je homogenní dielektrické kontinuum ionty (mù¾e být nìkolik druhù) aproximujeme tuhou nabitou kulièkou o prùmìru σ; jiné ne¾ elektrostatické interakce zanedbáváme rozlo¾ení iontù v okolí vybraného iontu popisujeme pravdìpodobnostnì jako spojité rozlo¾ení náboje (iontová atmosféra); korelace iontù v atmosféøe zanedbáváme platí zeφ k B T { alespoò þpro vìt¹inu iontùÿ { pro 1:1 nastane pro dostateènì zøedìný roztok (< 0.1 mol dm 3 ) { pro z > 1 nutné mnohem zøedìnìj¹í roztoky Iontová síla: I c = 1 z 2 2 i c i èasto pomocí molalit: I = 1 2 i sèítá se pøes v¹echny ionty v roztoku z 2 i m i i
13 Debyeova{Hückelova teorie pro roztoky elektrolytù 13/16 Výsledky (stínìný Coulombùv nebo Yukawùv potenciál) stínìní φ(r) = 1 ze φ(r) = 1 ze 4πε r 4πε r exp( r/λ) Debyeova délka (velikost iontové atmosféry): εrt λ = 0.96 nm pro 1:1, c = 0.1 mol dm λ = 3 2I c F 2 v kouli o polomìru λ je 120 H 2 O Aktivitní koecient iontu: ln γ i = Az 2 Ic i 1 + a σ=0 Az 2 I i c Ic bodové ionty (limitní zákon) A = e3 N 2 A 2 8π(εRT) 3/2 (= dm 3/2 mol 1/2 pro vodu 25 C) a = 2F 2 εrt σ (. = 1 dm 3/2 mol 1/2 pro σ = 0.3 nm) Pou¾itelnost max. do I c = 0.1 mol dm 3 (jednomocné), jinak je¹tì míò
14 Roztok silného elektrolytu 14/16 Obecnì: Al 2 (SO 4 ) 3 Kν Aν 2 Al SO 2 4 ν K z + + ν A z Elektroneutralita (zde denuji: z > 0, z > 0): ν z = ν z γ a γ nejsou samostatnì mìøitelné bì¾nými metodami Støední chemický potenciál (1 = rozpou¹tìdlo, 2 = sùl) Støední aktivita (ν = ν + ν ) µ 2 ± = ν µ + ν µ ν + ν a 2 ± = ν a ν aν Iontová síla pro sùl o molaritì c (pou¾ije se elektroneutralita): I c = 1 2 z z (ν + ν )c
15 Roztok silného elektrolytu 15/16 Støední aktivitní koecient γ 2± = ln γ 2± Debye{Hückel ν γ ν γν Ic = z z A 1 + a I c kde A = dm 3/2 mol 1/2, a = 1 dm 3/2 mol 1/2 Test pro NaCl: 0 experiment Debye-Huckel limiting Debye-Huckel ln γ (I / mol kg 1 ) 1/2
16 Aktivitní koecienty iontù Vypoètìte støední aktivitní koecient iontù v CaCl 2, c = 0.01 mol dm 3 16/ støední aktivitní koecient iontù v CH 3 COOH, c = 0.1 mol dm 3, je-li stupeò disociace α = aktivitní koecient protonù v H 2 SO 4, c = 0.01 mol dm 3, je-li disociace do 1. stupnì úplná a do 2. stupnì 60 % Rozpustnost málo rozpustné soli (napø. BaSO 4 ): klesne v obsahujícím jeden z iontù (napø. Ba(NO 3 ) 2 nebo Na 2 SO 4 ) ponìkud stoupne v pøítomnosti jiných iontù, proto¾e klesnou aktivitní koecienty Ba 2+ a SO 4 2 Pøíklad. Souèin rozpustnosti síranu barnatého je Vypoètìte rozpustnost BaSO 4 a) v èisté vodì a b) v 0.01 M roztoku NaCl. 10 µmol dm 3, 15 µmol dm 3 mù¾e se také zmìnit v dùsledku zmìny ph, dochází-li k hydrolýze (¹»avelan vápenatý v kys. ¹»avelové, vápenec a oxid uhlièitý) aj.
Elektrické jevy na membránách
 Elektrické jevy na membránách Polopropustná (semipermeabilní) membrána; frita, diafragma propou¹tí ionty, vzniká el. napìtí rùzné koncentrace iontù na obou stranách rùzná propustnost/difuzivita pro rùzné
Elektrické jevy na membránách Polopropustná (semipermeabilní) membrána; frita, diafragma propou¹tí ionty, vzniká el. napìtí rùzné koncentrace iontù na obou stranách rùzná propustnost/difuzivita pro rùzné
Opakování: Standardní stav þ ÿ
 Opakování: Standardní stav þ ÿ s.1 12. øíjna 215 Standardní stav þ ÿ = èistá slo¾ka ve stavu ideálního plynu za teploty soustavy T a standardního tlaku = 1 kpa, døíve 11,325 kpa. Èistá látka: Pøibli¾nì:
Opakování: Standardní stav þ ÿ s.1 12. øíjna 215 Standardní stav þ ÿ = èistá slo¾ka ve stavu ideálního plynu za teploty soustavy T a standardního tlaku = 1 kpa, døíve 11,325 kpa. Èistá látka: Pøibli¾nì:
Motivace: Poissonova rovnice
 Motivace: Poissonova rovnice Zachovává se poèet el. indukèních èar: Q = D d s, S D = ε E Integrál spoèítáme pøes povrch krychlièky dx dy dz: dq = dvρ = D d s = dydz[d x (x + dx) D x (x)] = dxdydz S ( Dx
Motivace: Poissonova rovnice Zachovává se poèet el. indukèních èar: Q = D d s, S D = ε E Integrál spoèítáme pøes povrch krychlièky dx dy dz: dq = dvρ = D d s = dydz[d x (x + dx) D x (x)] = dxdydz S ( Dx
Rovnováha kapalina{pára u binárních systémù
 Rovnováha kapalina{pára u binárních systémù 1 Pøedpoklad: 1 kapalná fáze Oznaèení: molární zlomky v kapalné fázi: x i molární zlomky v plynné fázi: y i Poèet stupòù volnosti: v = k f + 2 = 2 stav smìsi
Rovnováha kapalina{pára u binárních systémù 1 Pøedpoklad: 1 kapalná fáze Oznaèení: molární zlomky v kapalné fázi: x i molární zlomky v plynné fázi: y i Poèet stupòù volnosti: v = k f + 2 = 2 stav smìsi
Klasická termodynamika (aneb pøehled FCH I)
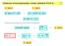 Klasická termodynamika (aneb pøehled FCH I) 1/16 0. zákon 1. zákon id. plyn: pv = nrt pv κ = konst (id., ad.) id. plyn: U = U(T) }{{} Carnotùv cyklus dq T = 0 2. zákon rg, K,... lim S = 0 T 0 S, ds = dq
Klasická termodynamika (aneb pøehled FCH I) 1/16 0. zákon 1. zákon id. plyn: pv = nrt pv κ = konst (id., ad.) id. plyn: U = U(T) }{{} Carnotùv cyklus dq T = 0 2. zákon rg, K,... lim S = 0 T 0 S, ds = dq
Viriálová stavová rovnice 1 + s.1
 Viriálová stavová rovnice 1 + s.1 (Mírnì nestandardní odvození Prùmìrná energie molekul okolo vybrané molekuly (β = 1/(k B T : 0 u(r e βu(r 4πr 2 dr Energie souboru N molekul: U = f 2 k B T + N 2 2V Tlak
Viriálová stavová rovnice 1 + s.1 (Mírnì nestandardní odvození Prùmìrná energie molekul okolo vybrané molekuly (β = 1/(k B T : 0 u(r e βu(r 4πr 2 dr Energie souboru N molekul: U = f 2 k B T + N 2 2V Tlak
Elektrochemie. Pøedmìt elektrochemie: disociace (roztoky elektrolytù, taveniny solí) vodivost jevy na rozhraní s/l (elektrolýza, èlánky)
 Elektrochemie 1 Pøedmìt elektrochemie: disociace (roztoky elektrolytù, taveniny solí) vodivost jevy na rozhraní s/l (elektrolýza, èlánky) Vodièe: I. tøídy { vodivost zpùsobena pohybem elektronù uvnitø
Elektrochemie 1 Pøedmìt elektrochemie: disociace (roztoky elektrolytù, taveniny solí) vodivost jevy na rozhraní s/l (elektrolýza, èlánky) Vodièe: I. tøídy { vodivost zpùsobena pohybem elektronù uvnitø
GAUSSŮV ZÁKON ELEKTROSTATIKY
 GAUSSŮV ZÁKON ELEKTROSTATIKY PLOCHA JAKO VEKTOR Matematický doplněk n n Elementární plocha ΔS ds Ploše přiřadíme vektor, který 1) je k této ploše kolmý 2) má velikost rovnou velikosti (obsahu) plochy Δ
GAUSSŮV ZÁKON ELEKTROSTATIKY PLOCHA JAKO VEKTOR Matematický doplněk n n Elementární plocha ΔS ds Ploše přiřadíme vektor, který 1) je k této ploše kolmý 2) má velikost rovnou velikosti (obsahu) plochy Δ
12. Elektrochemie základní pojmy
 Důležité veličiny Elektroda, článek Potenciometrie Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti Důležité veličiny proud I (ampér - A) náboj Q (coulomb - C) Q t 0 I dt napětí, potenciál
Důležité veličiny Elektroda, článek Potenciometrie Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti Důležité veličiny proud I (ampér - A) náboj Q (coulomb - C) Q t 0 I dt napětí, potenciál
Fázová rozhraní a mezifázová energie
 Fázová rozhraní a mezifázová energie druhy: l/g l/l }{{} mobilní s/g s/l s/s 1/14 Pøíklad. Kolik % molekul vody je na povrchu kapièky mlhy o prùmìru a) 0.1 mm (hranice viditelnosti okem) b) 200 nm (hranice
Fázová rozhraní a mezifázová energie druhy: l/g l/l }{{} mobilní s/g s/l s/s 1/14 Pøíklad. Kolik % molekul vody je na povrchu kapièky mlhy o prùmìru a) 0.1 mm (hranice viditelnosti okem) b) 200 nm (hranice
Plazma. magnetosféra komety. zbytky po výbuchu supernovy. formování hvězdy. slunce
 magnetosféra komety zbytky po výbuchu supernovy formování hvězdy slunce blesk polární záře sluneční vítr - plazma je označována jako čtvrté skupenství hmoty - plazma je plyn s významným množstvím iontů
magnetosféra komety zbytky po výbuchu supernovy formování hvězdy slunce blesk polární záře sluneční vítr - plazma je označována jako čtvrté skupenství hmoty - plazma je plyn s významným množstvím iontů
Fyzika biopolymerů. Elektrostatické interakce makromolekul ve vodných roztocích. Vodné roztoky. Elektrostatická Poissonova rovnice.
 Fyzka bopolymerů Elektrostatcké nterakce makromolekul ve vodných roztocích Robert Vácha Kamence 5, A4 2.13 robert.vacha@mal.mun.cz Vodné roztoky ldské tělo se skládá z 55-75 % z vody (roztoků) většna roztoků
Fyzka bopolymerů Elektrostatcké nterakce makromolekul ve vodných roztocích Robert Vácha Kamence 5, A4 2.13 robert.vacha@mal.mun.cz Vodné roztoky ldské tělo se skládá z 55-75 % z vody (roztoků) většna roztoků
Elektromagnetické pole je generováno elektrickými náboji a jejich pohybem. Je-li zdroj charakterizován nábojovou hustotou ( r r
 Záření Hertzova dipólu, kulové vlny, Rovnice elektromagnetického pole jsou vektorové diferenciální rovnice a podle symetrie bývá vhodné je řešit v křivočarých souřadnicích. Základní diferenciální operátory
Záření Hertzova dipólu, kulové vlny, Rovnice elektromagnetického pole jsou vektorové diferenciální rovnice a podle symetrie bývá vhodné je řešit v křivočarých souřadnicích. Základní diferenciální operátory
Chemie povrchů verze 2013
 Chemie povrchů verze 2013 Definice povrchu složitá, protože v nanoměřítku (na úrovni velikosti atomů) je elektronový obal atomů difúzní většinou definován fyzikální adsorpcí nereaktivních plynů Vlastnosti
Chemie povrchů verze 2013 Definice povrchu složitá, protože v nanoměřítku (na úrovni velikosti atomů) je elektronový obal atomů difúzní většinou definován fyzikální adsorpcí nereaktivních plynů Vlastnosti
Elektrochemie. Předmět elektrochemie: disociace (roztoky elektrolytů, taveniny solí) vodivost. jevy na rozhraní s/l (elektrolýza, články)
 Elektrochemie 1/30 Předmět elektrochemie: disociace (roztoky elektrolytů, taveniny solí) vodivost jevy na rozhraní s/l (elektrolýza, články) Vodiče: vodivost způsobena pohybem elektronů uvnitř mřížky:
Elektrochemie 1/30 Předmět elektrochemie: disociace (roztoky elektrolytů, taveniny solí) vodivost jevy na rozhraní s/l (elektrolýza, články) Vodiče: vodivost způsobena pohybem elektronů uvnitř mřížky:
 OBECNÁ CHEMIE František Zachoval CHEMICKÉ ROVNOVÁHY 1. Rovnovážný stav, rovnovážná konstanta a její odvození Dlouhou dobu se chemici domnívali, že jakákoliv chem.
OBECNÁ CHEMIE František Zachoval CHEMICKÉ ROVNOVÁHY 1. Rovnovážný stav, rovnovážná konstanta a její odvození Dlouhou dobu se chemici domnívali, že jakákoliv chem.
VI. Disociace a iontové rovnováhy
 VI. Disociace a iontové 1 VI. Disociace a iontové 6.1 Základní pojmy 6.2 Disociace 6.3 Elektrolyty 6.3.1 Iontová rovnováha elektrolytů 6.3.2 Roztoky ideální a reálné 6.4 Teorie kyselin a zásad 6.4.1 Arrhenius
VI. Disociace a iontové 1 VI. Disociace a iontové 6.1 Základní pojmy 6.2 Disociace 6.3 Elektrolyty 6.3.1 Iontová rovnováha elektrolytů 6.3.2 Roztoky ideální a reálné 6.4 Teorie kyselin a zásad 6.4.1 Arrhenius
Pro zředěné roztoky za konstantní teploty T je osmotický tlak úměrný molární koncentraci
 TRANSPORTNÍ MECHANISMY Transport látek z vnějšího prostředí do buňky a naopak se může uskutečňovat dvěma cestami - aktivním a pasivním transportem. Pasivním transportem rozumíme přenos látek ve směru energetického
TRANSPORTNÍ MECHANISMY Transport látek z vnějšího prostředí do buňky a naopak se může uskutečňovat dvěma cestami - aktivním a pasivním transportem. Pasivním transportem rozumíme přenos látek ve směru energetického
Exponenciální rozdìlení
 Exponenciální rozdìlení Ing. Michael Rost, Ph. D. Jihoèeská univerzita v Èeských Budìjovicích Katedra aplikované matematiky a informatiky Exponenciální rozdìlení Exp(A, λ) "Rozdìlení bez pamìti" Exponenciální
Exponenciální rozdìlení Ing. Michael Rost, Ph. D. Jihoèeská univerzita v Èeských Budìjovicích Katedra aplikované matematiky a informatiky Exponenciální rozdìlení Exp(A, λ) "Rozdìlení bez pamìti" Exponenciální
Transportní jevy. J = konst F
 Transportní jevy 1/23 Transportní (kinetické) jevy: difuze, elektrická vodivost, viskozita (vnitøní tøení), vedení tepla... Tok (ux) (té¾ zobecnìný tok) hmoty, náboje, hybnosti, tepla... : J = mno¾ství
Transportní jevy 1/23 Transportní (kinetické) jevy: difuze, elektrická vodivost, viskozita (vnitøní tøení), vedení tepla... Tok (ux) (té¾ zobecnìný tok) hmoty, náboje, hybnosti, tepla... : J = mno¾ství
3. NEROVNOVÁŽNÉ ELEKTRODOVÉ DĚJE
 3. NEROVNOVÁŽNÉ ELEKTRODOVÉ DĚJE (Elektrochemické články kinetické aspekty) Nerovnovážné elektrodové děje = děje probíhající na elektrodách při průchodu proudu. 3.1. Polarizace Pojem polarizace se používá
3. NEROVNOVÁŽNÉ ELEKTRODOVÉ DĚJE (Elektrochemické články kinetické aspekty) Nerovnovážné elektrodové děje = děje probíhající na elektrodách při průchodu proudu. 3.1. Polarizace Pojem polarizace se používá
Termochemie { práce. Práce: W = s F nebo W = F ds. Objemová práce (p vn = vnìj¹í tlak): W = p vn dv. Vratný dìj: p = p vn (ze stavové rovnice) W =
 Termochemie { práce Práce: W = s F nebo W = Objemová práce (p vn = vnìj¹í tlak): W = V2 V 1 p vn dv s2 Vratný dìj: p = p vn (ze stavové rovnice) W = V2 V 1 p dv s 1 F ds s.1 Diferenciální tvar: dw = pdv
Termochemie { práce Práce: W = s F nebo W = Objemová práce (p vn = vnìj¹í tlak): W = V2 V 1 p vn dv s2 Vratný dìj: p = p vn (ze stavové rovnice) W = V2 V 1 p dv s 1 F ds s.1 Diferenciální tvar: dw = pdv
Úvodní info. Studium
 [mozilla le:/home/jiri/www/fch/cz/pomucky/kolafa/n4316.html] 1/16 Úvodní info Jiøí Kolafa Ústav fyzikální chemie V CHT Praha budova A, místnost 325 (zadním vchodem) jiri.kolafa@vscht.cz 2244 4257 Web pøedmìtu:
[mozilla le:/home/jiri/www/fch/cz/pomucky/kolafa/n4316.html] 1/16 Úvodní info Jiøí Kolafa Ústav fyzikální chemie V CHT Praha budova A, místnost 325 (zadním vchodem) jiri.kolafa@vscht.cz 2244 4257 Web pøedmìtu:
a) [0,4 b] r < R, b) [0,4 b] r R c) [0,2 b] Zakreslete obě závislosti do jednoho grafu a vyznačte na osách důležité hodnoty.
![a) [0,4 b] r < R, b) [0,4 b] r R c) [0,2 b] Zakreslete obě závislosti do jednoho grafu a vyznačte na osách důležité hodnoty. a) [0,4 b] r < R, b) [0,4 b] r R c) [0,2 b] Zakreslete obě závislosti do jednoho grafu a vyznačte na osách důležité hodnoty.](/thumbs/88/115052329.jpg) Příklady: 24. Gaussův zákon elektrostatiky 1. Na obrázku je řez dlouhou tenkostěnnou kovovou trubkou o poloměru R, která nese na povrchu náboj s plošnou hustotou σ. Vyjádřete velikost intenzity E jako
Příklady: 24. Gaussův zákon elektrostatiky 1. Na obrázku je řez dlouhou tenkostěnnou kovovou trubkou o poloměru R, která nese na povrchu náboj s plošnou hustotou σ. Vyjádřete velikost intenzity E jako
Adsorpce. molekulární adsorpce: (g) (s), (l) (s)/(l),... iontová adsorpce Paneth{Fajans výmìnná iontová adsorpce, protionty v aluminosilikátech
 Adsorpce molekulární adsorpce: (g) (s), (l) (s)/(l),... iontová adsorpce Paneth{Fajans výmìnná iontová adsorpce, protionty v aluminosilikátech 1/16 Ar na gratu adsorpce: na povrch/rozhraní absorpce: dovnitø
Adsorpce molekulární adsorpce: (g) (s), (l) (s)/(l),... iontová adsorpce Paneth{Fajans výmìnná iontová adsorpce, protionty v aluminosilikátech 1/16 Ar na gratu adsorpce: na povrch/rozhraní absorpce: dovnitø
test zápočet průměr známka
 Zkouškový test z FCH mikrosvěta 6. ledna 2015 VZOR/1 jméno test zápočet průměr známka Čas 90 minut. Povoleny jsou kalkulačky. Nejsou povoleny žádné písemné pomůcky. U otázek označených symbolem? uvádějte
Zkouškový test z FCH mikrosvěta 6. ledna 2015 VZOR/1 jméno test zápočet průměr známka Čas 90 minut. Povoleny jsou kalkulačky. Nejsou povoleny žádné písemné pomůcky. U otázek označených symbolem? uvádějte
Podle skupenského stavu stýkajících se objemových fází: kapalina / plyn (l/g) - povrch kapalina / kapalina (l/l) tuhá látka / plyn (s/g) - povrch
 Fáze I Fáze II FÁZOVÁ ROZHRANÍ a koloidy kolem nás z mikroskopického, molekulárního hlediska Fáze I Fáze II z makroskopického hlediska Podle skupenského stavu stýkajících se objemových fází: kapalina /
Fáze I Fáze II FÁZOVÁ ROZHRANÍ a koloidy kolem nás z mikroskopického, molekulárního hlediska Fáze I Fáze II z makroskopického hlediska Podle skupenského stavu stýkajících se objemových fází: kapalina /
Matematika II Funkce více promìnných
 Matematika II Funkce více promìnných RNDr. Renata Klufová, Ph. D. Jihoèeská univerzita v Èeských Budìjovicích EF Katedra aplikované matematiky a informatiky Euklidovský n-rozmìrný prostor Def. Euklidovským
Matematika II Funkce více promìnných RNDr. Renata Klufová, Ph. D. Jihoèeská univerzita v Èeských Budìjovicích EF Katedra aplikované matematiky a informatiky Euklidovský n-rozmìrný prostor Def. Euklidovským
Zkouškový test z fyzikální a koloidní chemie
 Zkouškový test z fyzkální a kolodní cheme VZOR/1 jméno test zápočet průměr známka Čas 9 mnut. Povoleny jsou kalkulačky. Nejsou povoleny žádné písemné pomůcky. Uotázeksvýběrema,b,c...odpověd b kroužkujte.platí:
Zkouškový test z fyzkální a kolodní cheme VZOR/1 jméno test zápočet průměr známka Čas 9 mnut. Povoleny jsou kalkulačky. Nejsou povoleny žádné písemné pomůcky. Uotázeksvýběrema,b,c...odpověd b kroužkujte.platí:
Optické vlastnosti koloidních soustav
 Optické vlastnosti koloidních soustav (fyzikální princip metody měření velikosti částic a zeta potenciálu) Optické vlastnosti koloidních soustav jsou silně závislé zejména na fyzikálních vlastnostech koloidních
Optické vlastnosti koloidních soustav (fyzikální princip metody měření velikosti částic a zeta potenciálu) Optické vlastnosti koloidních soustav jsou silně závislé zejména na fyzikálních vlastnostech koloidních
Disperzní systémy. jsou slo¾ené ze dvou (i více) fází. Zpravidla dispergovaná fáze ve spojité fázi Obvykle s/l, l/l,...
 Disperzní systémy 1/21 jsou slo¾ené ze dvou (i více) fází. Zpravidla dispergovaná fáze ve spojité fázi Obvykle s/l, l/l,... Rozdìlení podle velikosti èástic: hrubì disperzní (heterogenní), > 1 µm koloidní
Disperzní systémy 1/21 jsou slo¾ené ze dvou (i více) fází. Zpravidla dispergovaná fáze ve spojité fázi Obvykle s/l, l/l,... Rozdìlení podle velikosti èástic: hrubì disperzní (heterogenní), > 1 µm koloidní
Petr Zikán. Studentský seminář, Březen 2011
 Sondová měření v plazmatu Petr Zikán Studentský seminář, Březen 2011 Přehled prezentace 1 Child-Langmuirův zákon Přehled prezentace 1 Child-Langmuirův zákon 2 Sheath a pre-sheath Přehled prezentace 1 Child-Langmuirův
Sondová měření v plazmatu Petr Zikán Studentský seminář, Březen 2011 Přehled prezentace 1 Child-Langmuirův zákon Přehled prezentace 1 Child-Langmuirův zákon 2 Sheath a pre-sheath Přehled prezentace 1 Child-Langmuirův
Úvod do vln v plazmatu
 Úvod do vln v plazmatu Co je to vlna? (fázová a grupová rychlost) Přehled vln v plazmatu Plazmové oscilace Iontové akustické vlny Horní hybridní frekvence Elektrostatické iontové cyklotronové vlny Dolní
Úvod do vln v plazmatu Co je to vlna? (fázová a grupová rychlost) Přehled vln v plazmatu Plazmové oscilace Iontové akustické vlny Horní hybridní frekvence Elektrostatické iontové cyklotronové vlny Dolní
Roztoky - elektrolyty
 Roztoky - elektrolyty Roztoky - vodné roztoky prakticky vždy vedou elektrický proud Elektrolyty látky, které se štěpí disociují na elektricky nabité částice ionty Původně se předpokládalo, že k disociaci
Roztoky - elektrolyty Roztoky - vodné roztoky prakticky vždy vedou elektrický proud Elektrolyty látky, které se štěpí disociují na elektricky nabité částice ionty Původně se předpokládalo, že k disociaci
Matematika II Urèitý integrál
 Matematika II Urèitý integrál RNDr. Renata Klufová, Ph. D. Jihoèeská univerzita v Èeských Budìjovicích EF Katedra aplikované matematiky a informatiky Motivace Je dána funkce f(x) = 2 + x2 x 4. Urèete co
Matematika II Urèitý integrál RNDr. Renata Klufová, Ph. D. Jihoèeská univerzita v Èeských Budìjovicích EF Katedra aplikované matematiky a informatiky Motivace Je dána funkce f(x) = 2 + x2 x 4. Urèete co
Galvanický článek. Li Rb K Na Be Sr Ca Mg Al Be Mn Zn Cr Fe Cd Co Ni Sn Pb H Sb Bi As CU Hg Ag Pt Au
 Řada elektrochemických potenciálů (Beketova řada) v níž je napětí mezi dvojicí kovů tím větší, čím větší je jejich vzdálenost v této řadě. Prvek více vlevo vytěsní z roztoku kov nacházející se vpravo od
Řada elektrochemických potenciálů (Beketova řada) v níž je napětí mezi dvojicí kovů tím větší, čím větší je jejich vzdálenost v této řadě. Prvek více vlevo vytěsní z roztoku kov nacházející se vpravo od
II. Statické elektrické pole v dielektriku. 2. Dielektrikum 3. Polarizace dielektrika 4. Jevy v dielektriku
 II. Statické elektické pole v dielektiku Osnova: 1. Dipól 2. Dielektikum 3. Polaizace dielektika 4. Jevy v dielektiku 1. Dipól Konečný dipól 2 bodové náboje stejné velikosti a opačného znaménka ve vzdálenosti
II. Statické elektické pole v dielektiku Osnova: 1. Dipól 2. Dielektikum 3. Polaizace dielektika 4. Jevy v dielektiku 1. Dipól Konečný dipól 2 bodové náboje stejné velikosti a opačného znaménka ve vzdálenosti
Elektrická dvojvrstva
 1 Elektrická dvojvrstva o povrchový náboj (především hydrofobních) částic vyrovnáván ekvivalentním množstvím opačně nabitých iontů (protiiontů) o náboj koloidní částice + obal protiiontů = tzv. elektrická
1 Elektrická dvojvrstva o povrchový náboj (především hydrofobních) částic vyrovnáván ekvivalentním množstvím opačně nabitých iontů (protiiontů) o náboj koloidní částice + obal protiiontů = tzv. elektrická
GE - Vyšší kvalita výuky CZ.1.07/1.5.00/
 Gymnázium, Brno, Elgartova 3 GE - Vyšší kvalita výuky CZ.1.07/1.5.00/34.0925 III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Téma: Elektřina a magnetismus Autor: Název: Alena Škárová Vodič a izolant
Gymnázium, Brno, Elgartova 3 GE - Vyšší kvalita výuky CZ.1.07/1.5.00/34.0925 III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Téma: Elektřina a magnetismus Autor: Název: Alena Škárová Vodič a izolant
ELEKTRICKÝ NÁBOJ A ELEKTRICKÉ POLE POJMY K ZOPAKOVÁNÍ. Testové úlohy varianta A
 Škola: Autor: DUM: Vzdělávací obor: Tematický okruh: Téma: Masarykovo gymnázium Vsetín Mgr. Jitka Novosadová MGV_F_SS_3S3_D12_Z_OPAK_E_Elektricky_naboj_a_elektricke_ pole_t Člověk a příroda Fyzika Elektrický
Škola: Autor: DUM: Vzdělávací obor: Tematický okruh: Téma: Masarykovo gymnázium Vsetín Mgr. Jitka Novosadová MGV_F_SS_3S3_D12_Z_OPAK_E_Elektricky_naboj_a_elektricke_ pole_t Člověk a příroda Fyzika Elektrický
ELEKTROSTATIKA. Mgr. Jan Ptáčník - GJVJ - Fyzika - Elektřina a magnetismus - 2. ročník
 ELEKTROSTATIKA Mgr. Jan Ptáčník - GJVJ - Fyzika - Elektřina a magnetismus - 2. ročník Elektrický náboj Dva druhy: kladný a záporný. Elektricky nabitá tělesa. Elektroskop a elektrometr. Vodiče a nevodiče
ELEKTROSTATIKA Mgr. Jan Ptáčník - GJVJ - Fyzika - Elektřina a magnetismus - 2. ročník Elektrický náboj Dva druhy: kladný a záporný. Elektricky nabitá tělesa. Elektroskop a elektrometr. Vodiče a nevodiče
Elektrické pole vybuzené nábojem Q2 působí na náboj Q1 silou, která je stejně veliká a opačná: F 12 F 21
 Příklad : Síla působící mezi dvěma bodovými náboji Dva bodové náboje na sebe působí ve vakuu silou, která je dána Coulombovým zákonem. Síla je přímo úměrná velikosti nábojů, nepřímo úměrná kvadrátu vzdálenosti,
Příklad : Síla působící mezi dvěma bodovými náboji Dva bodové náboje na sebe působí ve vakuu silou, která je dána Coulombovým zákonem. Síla je přímo úměrná velikosti nábojů, nepřímo úměrná kvadrátu vzdálenosti,
Zápo tová písemná práce. 1 z p edm tu 01RMF varianta A
 Zápo tová písemná práce. 1 z p edm tu 1MF varianta A tvrtek 19. listopadu 215, 13:215:2 ➊ (5 bod ) Nech f (x), g(x) L 1 () a f (x) dx = A, x f (x) dx = µ, Vypo ítejte, emu se rovná z( f g)(z) dz. g(x)
Zápo tová písemná práce. 1 z p edm tu 1MF varianta A tvrtek 19. listopadu 215, 13:215:2 ➊ (5 bod ) Nech f (x), g(x) L 1 () a f (x) dx = A, x f (x) dx = µ, Vypo ítejte, emu se rovná z( f g)(z) dz. g(x)
Atom vodíku. Nejjednodušší soustava: p + e Řešitelná exaktně. Kulová symetrie. Potenciální energie mezi p + e. e =
 Atom vodíku Nejjednodušší soustava: p + e Řešitelná exaktně Kulová symetrie Potenciální energie mezi p + e V 2 e = 4πε r 0 1 Polární souřadnice využití kulové symetrie atomu Ψ(x,y,z) Ψ(r,θ, φ) x =? y=?
Atom vodíku Nejjednodušší soustava: p + e Řešitelná exaktně Kulová symetrie Potenciální energie mezi p + e V 2 e = 4πε r 0 1 Polární souřadnice využití kulové symetrie atomu Ψ(x,y,z) Ψ(r,θ, φ) x =? y=?
m05 G id.směs m (p,t)= x i H mi i=1 x i S mi R k x i ln x i k x i G mi + RT k G mi = H mi TS mi k x i V mi V id.směs m (T,p)=
 Ø ÐÓú Ú ÙÔ Ò ØÚ Ñ Þ Ø ÔÐÓØÝ ËØ Ò Ö Ò Ø Ú ÓÙ Ø ÚÝ ØÐ Ù ËØ Ò Ö Ò Ø Ú ÐÒ ÓÒ ÒÞÓÚ Ò Ñ s.1 ½ º ÞÒ ¾¼¼ Ó Ø ØÒ Ú Ð ÒÝ Ñ ÐÓ Þ Ú Ò ØÐ Ùµ Ò ÐÒ Ñ H d.směs m (p,t)= S d.směs m (p,t)= k k x H m x S m R k x ln x G d.směs
Ø ÐÓú Ú ÙÔ Ò ØÚ Ñ Þ Ø ÔÐÓØÝ ËØ Ò Ö Ò Ø Ú ÓÙ Ø ÚÝ ØÐ Ù ËØ Ò Ö Ò Ø Ú ÐÒ ÓÒ ÒÞÓÚ Ò Ñ s.1 ½ º ÞÒ ¾¼¼ Ó Ø ØÒ Ú Ð ÒÝ Ñ ÐÓ Þ Ú Ò ØÐ Ùµ Ò ÐÒ Ñ H d.směs m (p,t)= S d.směs m (p,t)= k k x H m x S m R k x ln x G d.směs
Detekce nabitých částic Jak se ztrácí energie průchodem částice hmotou?
 Detekce nabitých částic Jak se ztrácí energie průchodem částice hmotou? 10/20/2004 1 Bethe Blochova formule (1) je maximální možná předaná energie elektronu N r e - vogadrovo čislo - klasický poloměr elektronu
Detekce nabitých částic Jak se ztrácí energie průchodem částice hmotou? 10/20/2004 1 Bethe Blochova formule (1) je maximální možná předaná energie elektronu N r e - vogadrovo čislo - klasický poloměr elektronu
Cvičení F2070 Elektřina a magnetismus
 Cvičení F2070 Elektřina a magnetismus 20.3.2009 Elektrický potenciál, elektrická potenciální energie, ekvipotenciální plochy, potenciál bodového náboje, soustavy bodových nábojů, elektrického pole dipólu,
Cvičení F2070 Elektřina a magnetismus 20.3.2009 Elektrický potenciál, elektrická potenciální energie, ekvipotenciální plochy, potenciál bodového náboje, soustavy bodových nábojů, elektrického pole dipólu,
Výpočty koncentrací. objemová % (objemový zlomek) krvi m. Vsložky. celku. Objemy nejsou aditivní!!!
 Výpočty koncentrací objemová % (objemový zlomek) Vsložky % obj. = 100 V celku Objemy nejsou aditivní!!! Příklad: Kolik ethanolu je v 700 ml vodky (40 % obj.)? Kolik promile ethanolu v krvi bude mít muž
Výpočty koncentrací objemová % (objemový zlomek) Vsložky % obj. = 100 V celku Objemy nejsou aditivní!!! Příklad: Kolik ethanolu je v 700 ml vodky (40 % obj.)? Kolik promile ethanolu v krvi bude mít muž
Elektrochemický potenciál Standardní vodíková elektroda Oxidačně-redukční potenciály
 Elektrochemický potenciál Standardní vodíková elektroda Oxidačně-redukční potenciály Elektrochemie rovnováhy a děje v soustavách nesoucích elektrický náboj Krystal kovu ponořený do destilované vody + +
Elektrochemický potenciál Standardní vodíková elektroda Oxidačně-redukční potenciály Elektrochemie rovnováhy a děje v soustavách nesoucích elektrický náboj Krystal kovu ponořený do destilované vody + +
7 Gaussova věta 7 GAUSSOVA VĚTA. Použitím Gaussovy věty odvod te velikost vektorů elektrické indukce a elektrické intenzity pro
 7 Gaussova věta Zadání Použitím Gaussovy věty odvod te velikost vektorů elektrické indukce a elektrické intenzity pro následující nabitá tělesa:. rovnoměrně nabitou kouli s objemovou hustotou nábojeρ,
7 Gaussova věta Zadání Použitím Gaussovy věty odvod te velikost vektorů elektrické indukce a elektrické intenzity pro následující nabitá tělesa:. rovnoměrně nabitou kouli s objemovou hustotou nábojeρ,
Počet atomů a molekul v monomolekulární vrstvě
 Počet atomů a molekul v monomolekulární vrstvě ϑ je stupeň pokrytí ϑ = N 1 N 1p N 1 = ϑn 1p ν 1 = 1 4 nv a ν 1ef = γν 1 = γ 1 4 nv a γ je koeficient ulpění () F6450 1 / 23 8kT v a = πm = 8kNa T π M 0 ν
Počet atomů a molekul v monomolekulární vrstvě ϑ je stupeň pokrytí ϑ = N 1 N 1p N 1 = ϑn 1p ν 1 = 1 4 nv a ν 1ef = γν 1 = γ 1 4 nv a γ je koeficient ulpění () F6450 1 / 23 8kT v a = πm = 8kNa T π M 0 ν
Stanislav Labík. Ústav fyzikální chemie V CHT Praha budova A, 3. patro u zadního vchodu, místnost
 Stanislav Labík Ústav fyzikální chemie V CHT Praha budova A, 3. patro u zadního vchodu, místnost 325 labik@vscht.cz 220 444 257 http://www.vscht.cz/fch/ Výuka Letní semestr N403032 Základy fyzikální chemie
Stanislav Labík Ústav fyzikální chemie V CHT Praha budova A, 3. patro u zadního vchodu, místnost 325 labik@vscht.cz 220 444 257 http://www.vscht.cz/fch/ Výuka Letní semestr N403032 Základy fyzikální chemie
ANODA KATODA elektrolyt:
 Ukázky z pracovních listů 1) Naznač pomocí šipek, které částice putují k anodě a které ke katodě. Co je elektrolytem? ANODA KATODA elektrolyt: Zn 2+ Cl - Zn 2+ Zn 2+ Cl - Cl - Cl - Cl - Cl - Zn 2+ Cl -
Ukázky z pracovních listů 1) Naznač pomocí šipek, které částice putují k anodě a které ke katodě. Co je elektrolytem? ANODA KATODA elektrolyt: Zn 2+ Cl - Zn 2+ Zn 2+ Cl - Cl - Cl - Cl - Cl - Zn 2+ Cl -
Složení soustav (roztoky, koncentrace látkového množství)
 VZOROVÉ PŘÍKLADY Z CHEMIE A DOPORUČENÁ LITERATURA pro přípravu k přijímací zkoušce studijnímu oboru Nanotechnologie na VŠB TU Ostrava Doporučená literatura z chemie: Prakticky jakákoliv celostátní učebnice
VZOROVÉ PŘÍKLADY Z CHEMIE A DOPORUČENÁ LITERATURA pro přípravu k přijímací zkoušce studijnímu oboru Nanotechnologie na VŠB TU Ostrava Doporučená literatura z chemie: Prakticky jakákoliv celostátní učebnice
DOPLŇKOVÝ STUDIJNÍ MATERIÁL CHEMICKÉ VÝPOČTY. Zuzana Špalková. Věra Vyskočilová
 DOPLŇKOVÝ STUDIJNÍ MATERIÁL CHEMICKÉ VÝPOČTY Zuzana Špalková Věra Vyskočilová BRNO 2014 Doplňkový studijní materiál zaměřený na Chemické výpočty byl vytvořen v rámci projektu Interní vzdělávací agentury
DOPLŇKOVÝ STUDIJNÍ MATERIÁL CHEMICKÉ VÝPOČTY Zuzana Špalková Věra Vyskočilová BRNO 2014 Doplňkový studijní materiál zaměřený na Chemické výpočty byl vytvořen v rámci projektu Interní vzdělávací agentury
Základní chemické výpočty I
 Základní chemické výpočty I Tomáš Kučera tomas.kucera@lfmotol.cuni.cz Ústav lékařské chemie a klinické biochemie 2. lékařská fakulta, Univerzita Karlova v Praze a Fakultní nemocnice v Motole 2017 Relativní
Základní chemické výpočty I Tomáš Kučera tomas.kucera@lfmotol.cuni.cz Ústav lékařské chemie a klinické biochemie 2. lékařská fakulta, Univerzita Karlova v Praze a Fakultní nemocnice v Motole 2017 Relativní
ELEKTRICKÝ NÁBOJ A ELEKTRICKÉ POLE
 ELEKTRICKÝ NÁBOJ ELEKTRICKÉ POLE 1. Elektrický náboj, elektrická síla Elektrické pole je prostor v okolí nabitých těles nebo částic. Jako jiné druhy polí je to způsob existence hmoty. Elektrický náboj
ELEKTRICKÝ NÁBOJ ELEKTRICKÉ POLE 1. Elektrický náboj, elektrická síla Elektrické pole je prostor v okolí nabitých těles nebo částic. Jako jiné druhy polí je to způsob existence hmoty. Elektrický náboj
[ ] d[ Y] rychlost REAKČNÍ KINETIKA X Y
![[ ] d[ Y] rychlost REAKČNÍ KINETIKA X Y [ ] d[ Y] rychlost REAKČNÍ KINETIKA X Y](/thumbs/78/77051926.jpg) REAKČNÍ KINETIKA Faktory ovlivňující rychlost chemických reakcí Chemická povaha reaktantů - reaktivita Fyzikální stav reaktantů homogenní vs. heterogenní reakce Teplota 10 C zvýšení rychlosti 2x 3x zýšení
REAKČNÍ KINETIKA Faktory ovlivňující rychlost chemických reakcí Chemická povaha reaktantů - reaktivita Fyzikální stav reaktantů homogenní vs. heterogenní reakce Teplota 10 C zvýšení rychlosti 2x 3x zýšení
Historie. - elektrizace tením (elektron = jantar) - Magnetismus magnetovec pitahuje železo. procházející proud vytváí magnetické pole
 Historie Staréecko: elektrizace tením (elektron = jantar) Magnetismus magnetovec pitahuje železo Hans Christian Oersted objevil souvislost mezi elektinou a magnetismem procházející proud vytváí magnetické
Historie Staréecko: elektrizace tením (elektron = jantar) Magnetismus magnetovec pitahuje železo Hans Christian Oersted objevil souvislost mezi elektinou a magnetismem procházející proud vytváí magnetické
Roztok. Homogenní směs molekul, které mohou být v pevném, kapalném nebo plynném stavu. Pravé roztoky
 Roztok Homogenní směs molekul, které mohou být v pevném, kapalném nebo plynném stavu Pravé roztoky Micelární a koloidní roztoky (suspenze): částice velké 1 nm 10 µm Tyndallův jev 1 Druhy roztoků Složka
Roztok Homogenní směs molekul, které mohou být v pevném, kapalném nebo plynném stavu Pravé roztoky Micelární a koloidní roztoky (suspenze): částice velké 1 nm 10 µm Tyndallův jev 1 Druhy roztoků Složka
Elektrické jevy na membránách
 Elektrcké jevy na membránách Polopropustná (sempermeablní) membrána; frta, dafragma propou¹tí onty, vznká el. napìtí rùzné koncentrace ontù na obou stranách rùzná propustnost/dfuzvta pro rùzné onty rùzný
Elektrcké jevy na membránách Polopropustná (sempermeablní) membrána; frta, dafragma propou¹tí onty, vznká el. napìtí rùzné koncentrace ontù na obou stranách rùzná propustnost/dfuzvta pro rùzné onty rùzný
Ústřední komise Chemické olympiády. 42. ročník. KRAJSKÉ KOLO Kategorie D. SOUTĚŽNÍ ÚLOHY TEORETICKÉ ČÁSTI Časová náročnost: 60 minut
 Ústřední komise Chemické olympiády 42. ročník 2005 2006 KRAJSKÉ KOLO Kategorie D SOUTĚŽNÍ ÚLOHY TEORETICKÉ ČÁSTI Časová náročnost: 60 minut Institut dětí a mládeže Ministerstva školství, mládeže a tělovýchovy
Ústřední komise Chemické olympiády 42. ročník 2005 2006 KRAJSKÉ KOLO Kategorie D SOUTĚŽNÍ ÚLOHY TEORETICKÉ ČÁSTI Časová náročnost: 60 minut Institut dětí a mládeže Ministerstva školství, mládeže a tělovýchovy
Vibrace atomů v mřížce, tepelná kapacita pevných látek
 Vibrace atomů v mřížce, tepelná kapacita pevných látek Atomy vázané v mřížce nejsou v klidu. Míru jejich pohybu vyjadřuje podobně jako u plynů a kapalin teplota. - Elastické vlny v kontinuu neatomární
Vibrace atomů v mřížce, tepelná kapacita pevných látek Atomy vázané v mřížce nejsou v klidu. Míru jejich pohybu vyjadřuje podobně jako u plynů a kapalin teplota. - Elastické vlny v kontinuu neatomární
Skupenské stavy. Kapalina Částečně neuspořádané Volný pohyb částic nebo skupin částic Částice blíže u sebe
 Skupenské stavy Plyn Zcela neuspořádané Hodně volného prostoru Zcela volný pohyb částic Částice daleko od sebe Kapalina Částečně neuspořádané Volný pohyb částic nebo skupin částic Částice blíže u sebe
Skupenské stavy Plyn Zcela neuspořádané Hodně volného prostoru Zcela volný pohyb částic Částice daleko od sebe Kapalina Částečně neuspořádané Volný pohyb částic nebo skupin částic Částice blíže u sebe
VÝPO C TY. Tomáš Kuc era & Karel Kotaška
 ZÁKLADNÍ CHEMICKÉ VÝPO C TY I Tomáš Kuc era & Karel Kotaška tomas.kucera@lfmotol.cuni.cz Ústav lékar ské chemie a klinické biochemie 2. lékar ská fakulta, Univerzita Karlova v Praze a Fakultní nemocnice
ZÁKLADNÍ CHEMICKÉ VÝPO C TY I Tomáš Kuc era & Karel Kotaška tomas.kucera@lfmotol.cuni.cz Ústav lékar ské chemie a klinické biochemie 2. lékar ská fakulta, Univerzita Karlova v Praze a Fakultní nemocnice
Ú L O H Y
 Ú L O H Y 1. Vylučování kovů - Faradayův zákon; Př. 8.1 Stejný náboj, 5789 C, projde při elektrolýze každým z roztoků těchto solí: (a) AgNO 3, (b) CuSO 4, (c) Na 2 SO 4, (d) Al(NO 3 ) 3, (e) Al 2 (SO 4
Ú L O H Y 1. Vylučování kovů - Faradayův zákon; Př. 8.1 Stejný náboj, 5789 C, projde při elektrolýze každým z roztoků těchto solí: (a) AgNO 3, (b) CuSO 4, (c) Na 2 SO 4, (d) Al(NO 3 ) 3, (e) Al 2 (SO 4
Nekovalentní interakce
 Nekovalentní interakce Jan Řezáč UOCHB AV ČR 31. října 2017 Jan Řezáč (UOCHB AV ČR) Nekovalentní interakce 31. října 2017 1 / 28 Osnova 1 Teorie 2 Typy nekovalentních interakcí 3 Projevy v chemii 4 Výpočty
Nekovalentní interakce Jan Řezáč UOCHB AV ČR 31. října 2017 Jan Řezáč (UOCHB AV ČR) Nekovalentní interakce 31. října 2017 1 / 28 Osnova 1 Teorie 2 Typy nekovalentních interakcí 3 Projevy v chemii 4 Výpočty
John Dalton Amadeo Avogadro
 Spojením atomů vznikají molekuly... John Dalton 1766 1844 Amadeo Avogadro 1776 1856 Výpočet molekuly 2, metoda valenční vazby Walter eitler 1904 1981 Fritz W. London 1900 1954 Teorie molekulových orbitalů
Spojením atomů vznikají molekuly... John Dalton 1766 1844 Amadeo Avogadro 1776 1856 Výpočet molekuly 2, metoda valenční vazby Walter eitler 1904 1981 Fritz W. London 1900 1954 Teorie molekulových orbitalů
Membránové potenciály
 Membránové potenciály Vznik a podstata membránového potenciálu vzniká v důsledku nerovnoměrného rozdělení fyziologických iontů po obou stranách membrány nestejná propustnost membrány pro různé ionty různá
Membránové potenciály Vznik a podstata membránového potenciálu vzniká v důsledku nerovnoměrného rozdělení fyziologických iontů po obou stranách membrány nestejná propustnost membrány pro různé ionty různá
Základní zákony a terminologie v elektrotechnice
 Základní zákony a terminologie v elektrotechnice (opakování učiva SŠ, Fyziky) Určeno pro studenty komb. formy FMMI předmětu 452702 / 04 Elektrotechnika Zpracoval: Jan Dudek Prosinec 2006 Elektrický náboj
Základní zákony a terminologie v elektrotechnice (opakování učiva SŠ, Fyziky) Určeno pro studenty komb. formy FMMI předmětu 452702 / 04 Elektrotechnika Zpracoval: Jan Dudek Prosinec 2006 Elektrický náboj
ELEKTŘINA A MAGNETIZMUS Řešené úlohy a postupy: Gaussův zákon
 ELEKTŘINA A MAGNETIZMUS Řešené úlohy a postupy: Gaussův zákon Peter Dourmashkin MIT 006, překlad: Jan Pacák (007) Obsah 3. GAUSSŮV ZÁKON 3.1 ALGORITMUS PRO ŘEŠENÍ PROBLÉMŮ POMOCÍ GAUSSOVA ZÁKONA ÚLOHA
ELEKTŘINA A MAGNETIZMUS Řešené úlohy a postupy: Gaussův zákon Peter Dourmashkin MIT 006, překlad: Jan Pacák (007) Obsah 3. GAUSSŮV ZÁKON 3.1 ALGORITMUS PRO ŘEŠENÍ PROBLÉMŮ POMOCÍ GAUSSOVA ZÁKONA ÚLOHA
III. Stacionární elektrické pole, vedení el. proudu v látkách
 III. Stacionární elektrické pole, vedení el. proudu v látkách Osnova: 1. Elektrický proud a jeho vlastnosti 2. Ohmův zákon 3. Kirhoffovy zákony 4. Vedení el. proudu ve vodičích 5. Vedení el. proudu v polovodičích
III. Stacionární elektrické pole, vedení el. proudu v látkách Osnova: 1. Elektrický proud a jeho vlastnosti 2. Ohmův zákon 3. Kirhoffovy zákony 4. Vedení el. proudu ve vodičích 5. Vedení el. proudu v polovodičích
Matematika II Limita a spojitost funkce, derivace
 Matematika II Limita a spojitost funkce, derivace RNDr. Renata Klufová, Ph. D. Jihoèeská univerzita v Èeských Budìjovicích EF Katedra aplikované matematiky a informatiky Prstencové a kruhové okolí bodu
Matematika II Limita a spojitost funkce, derivace RNDr. Renata Klufová, Ph. D. Jihoèeská univerzita v Èeských Budìjovicích EF Katedra aplikované matematiky a informatiky Prstencové a kruhové okolí bodu
Fázová rozhraní a mezifázová energie
 Fázová rozhraní a mezifázová energie druhy: l/g l/l }{{} mobilní 1/15 s/g s/l s/s povrch koule = 4πr 2 Pøíklad. Kolik % molekul vody je na povrchu kapièky mlhy o prùmìru a) 0.1 mm (hranice viditelnosti
Fázová rozhraní a mezifázová energie druhy: l/g l/l }{{} mobilní 1/15 s/g s/l s/s povrch koule = 4πr 2 Pøíklad. Kolik % molekul vody je na povrchu kapièky mlhy o prùmìru a) 0.1 mm (hranice viditelnosti
Kapaliny Molekulové vdw síly, vodíkové můstky
 Kapaliny Molekulové vdw síly, vodíkové můstky Metalické roztavené kovy, ionty + elektrony, elektrostatické síly Iontové roztavené soli, FLINAK (LiF + NaF + KF), volně pohyblivé anionty a kationty, iontová
Kapaliny Molekulové vdw síly, vodíkové můstky Metalické roztavené kovy, ionty + elektrony, elektrostatické síly Iontové roztavené soli, FLINAK (LiF + NaF + KF), volně pohyblivé anionty a kationty, iontová
Kapaliny Molekulové vdw síly, vodíkové můstky
 Kapaliny Molekulové vdw síly, vodíkové můstky Metalické roztavené kovy, ionty + elektrony, elektrostatické síly Iontové roztavené soli, FLINAK (LiF + NaF + KF), volně pohyblivé anionty a kationty, iontová
Kapaliny Molekulové vdw síly, vodíkové můstky Metalické roztavené kovy, ionty + elektrony, elektrostatické síly Iontové roztavené soli, FLINAK (LiF + NaF + KF), volně pohyblivé anionty a kationty, iontová
Laserová technika prosince Katedra fyzikální elektroniky.
 Laserová technika 1 Aktivní prostředí Šíření rezonančního záření dvouhladinovým prostředím Jan Šulc Katedra fyzikální elektroniky České vysoké učení technické jan.sulc@fjfi.cvut.cz 22. prosince 2016 Program
Laserová technika 1 Aktivní prostředí Šíření rezonančního záření dvouhladinovým prostředím Jan Šulc Katedra fyzikální elektroniky České vysoké učení technické jan.sulc@fjfi.cvut.cz 22. prosince 2016 Program
Mgr. Jakub Janíček VY_32_INOVACE_Ch1r0118
 Chemická vazba Mgr. Jakub Janíček VY_32_INOVACE_Ch1r0118 Chemická vazba Většina atomů má tendenci se spojovat do větších celků (molekul), v nichž jsou vzájemně vázané chemickou vazbou. Chemická vazba je
Chemická vazba Mgr. Jakub Janíček VY_32_INOVACE_Ch1r0118 Chemická vazba Většina atomů má tendenci se spojovat do větších celků (molekul), v nichž jsou vzájemně vázané chemickou vazbou. Chemická vazba je
Nekovalentní interakce
 Nekovalentní interakce Jan Řezáč UOCHB AV ČR 3. listopadu 2016 Jan Řezáč (UOCHB AV ČR) Nekovalentní interakce 3. listopadu 2016 1 / 28 Osnova 1 Teorie 2 Typy nekovalentních interakcí 3 Projevy v chemii
Nekovalentní interakce Jan Řezáč UOCHB AV ČR 3. listopadu 2016 Jan Řezáč (UOCHB AV ČR) Nekovalentní interakce 3. listopadu 2016 1 / 28 Osnova 1 Teorie 2 Typy nekovalentních interakcí 3 Projevy v chemii
1.3. Transport iontů v elektrickém poli
 .3. Transport ontů v elektrckém pol Ionty se v roztoku vystaveném působení elektrckého pole pohybují katonty směrem ke katodě, anonty k anodě. Tento pohyb ontů se označuje jako mgrace. VODIVOST Vodvost
.3. Transport ontů v elektrckém pol Ionty se v roztoku vystaveném působení elektrckého pole pohybují katonty směrem ke katodě, anonty k anodě. Tento pohyb ontů se označuje jako mgrace. VODIVOST Vodvost
Potenciální energie atom{atom
 Potenciální energie atom{atom 1/16 Londonovy (disperzní) síly: na del¹ích vzdálenostech, v¾dy pøita¾livé Model uktuující dipól { uktuující dipól elst. pole E 1/r 3 indukovaný dipól µ ind E energie u(r)
Potenciální energie atom{atom 1/16 Londonovy (disperzní) síly: na del¹ích vzdálenostech, v¾dy pøita¾livé Model uktuující dipól { uktuující dipól elst. pole E 1/r 3 indukovaný dipól µ ind E energie u(r)
ELT1 - Přednáška č. 6
 ELT1 - Přednáška č. 6 Elektrotechnická terminologie a odborné výrazy, měřicí jednotky a činitelé, které je ovlivňují. Rozdíl potenciálů, elektromotorická síla, napětí, el. napětí, proud, odpor, vodivost,
ELT1 - Přednáška č. 6 Elektrotechnická terminologie a odborné výrazy, měřicí jednotky a činitelé, které je ovlivňují. Rozdíl potenciálů, elektromotorická síla, napětí, el. napětí, proud, odpor, vodivost,
CHEMICKÉ VÝPOČTY I. ČÁST LÁTKOVÉ MNOŽSTVÍ. HMOTNOSTI ATOMŮ A MOLEKUL.
 CHEMICKÉ VÝPOČTY I. ČÁST LÁTKOVÉ MNOŽSTVÍ. HMOTNOSTI ATOMŮ A MOLEKUL. Látkové množství Značka: n Jednotka: mol Definice: Jeden mol je množina, která má stejný počet prvků, jako je atomů ve 12 g nuklidu
CHEMICKÉ VÝPOČTY I. ČÁST LÁTKOVÉ MNOŽSTVÍ. HMOTNOSTI ATOMŮ A MOLEKUL. Látkové množství Značka: n Jednotka: mol Definice: Jeden mol je množina, která má stejný počet prvků, jako je atomů ve 12 g nuklidu
N A = 6,023 10 23 mol -1
 Pro vyjadřování množství látky se v chemii zavádí veličina látkové množství. Značí se n, jednotkou je 1 mol. Látkové množství je jednou ze základních veličin soustavy SI. Jeden mol je takové množství látky,
Pro vyjadřování množství látky se v chemii zavádí veličina látkové množství. Značí se n, jednotkou je 1 mol. Látkové množství je jednou ze základních veličin soustavy SI. Jeden mol je takové množství látky,
Roztok. Homogenní směs molekul, které mohou být v pevném, kapalném nebo plynném stavu. Pravé roztoky
 Roztok Homogenní směs molekul, které mohou být v pevném, kapalném nebo plynném stavu Pravé roztoky Micelární a koloidní roztoky (suspenze): částice velké 1 nm 10 µm Tyndallův jev rozptyl světla 1 Druhy
Roztok Homogenní směs molekul, které mohou být v pevném, kapalném nebo plynném stavu Pravé roztoky Micelární a koloidní roztoky (suspenze): částice velké 1 nm 10 µm Tyndallův jev rozptyl světla 1 Druhy
Plazmové metody. Základní vlastnosti a parametry plazmatu
 Plazmové metody Základní vlastnosti a parametry plazmatu Atom je základní částice běžné hmoty. Částice, kterou již chemickými prostředky dále nelze dělit a která definuje vlastnosti daného chemického prvku.
Plazmové metody Základní vlastnosti a parametry plazmatu Atom je základní částice běžné hmoty. Částice, kterou již chemickými prostředky dále nelze dělit a která definuje vlastnosti daného chemického prvku.
Úvod do biologie rostlin Transport látek TRANSPORT. Krátké, střední, dlouhé vzdálenosti
 Slide 1a TRANSPORT Krátké, střední, dlouhé vzdálenosti Slide 1b TRANSPORT Krátké, střední, dlouhé vzdálenosti Aktivní, pasivní Slide 1c TRANSPORT Krátké, střední, dlouhé vzdálenosti Aktivní, pasivní Kapalin,
Slide 1a TRANSPORT Krátké, střední, dlouhé vzdálenosti Slide 1b TRANSPORT Krátké, střední, dlouhé vzdálenosti Aktivní, pasivní Slide 1c TRANSPORT Krátké, střední, dlouhé vzdálenosti Aktivní, pasivní Kapalin,
Aproximace funkcí. Chceme þvzoreèekÿ. Známe: celý prùbìh funkce
 Aproximace funkcí 1/13 Známe: celý prùbìh funkce Chceme þvzoreèekÿ hodnoty ve vybraných bodech, pøíp. i derivace Kvalita údajù: známe pøesnì (máme algoritmus) známe pøibli¾nì (experiment èi simulace) {
Aproximace funkcí 1/13 Známe: celý prùbìh funkce Chceme þvzoreèekÿ hodnoty ve vybraných bodech, pøíp. i derivace Kvalita údajù: známe pøesnì (máme algoritmus) známe pøibli¾nì (experiment èi simulace) {
VLASTNOSTI KAPALIN. Část 2. Literatura : Otakar Maštovský; HYDROMECHANIKA Jaromír Noskijevič; MECHANIKA TEKUTIN František Šob; HYDROMECHANIKA
 HYDROMECHANIKA LASTNOSTI KAPALIN Část 2 Literatura : Otakar Maštovský; HYDROMECHANIKA Jaromír Noskijevič; MECHANIKA TEKUTIN František Šob; HYDROMECHANIKA lastnosti kapalin: Molekulární stavba hmoty Příklad
HYDROMECHANIKA LASTNOSTI KAPALIN Část 2 Literatura : Otakar Maštovský; HYDROMECHANIKA Jaromír Noskijevič; MECHANIKA TEKUTIN František Šob; HYDROMECHANIKA lastnosti kapalin: Molekulární stavba hmoty Příklad
TERMIKA II. Stacionární vedení s dokonalou i nedokonalou izolací; Obecná rovnice vedení tepla; Přestup a prostup tepla;
 TERMIKA II Šíření tepla vedením, prouděním a zářením; Stacionární vedení s dokonalou i nedokonalou izolací; Nestacionární vedení tepla; Obecná rovnice vedení tepla; Přestup a prostup tepla; 1 Šíření tepla
TERMIKA II Šíření tepla vedením, prouděním a zářením; Stacionární vedení s dokonalou i nedokonalou izolací; Nestacionární vedení tepla; Obecná rovnice vedení tepla; Přestup a prostup tepla; 1 Šíření tepla
Vnitřní magnetosféra
 Vnitřní magnetosféra Plazmasféra Elektrické pole díky konvenkci (1) (Convection Electric Field) Vodivost σ, tj. ve vztažné soustavě pohybující se s plazmatem rychlostí v je elektrické pole rovno nule (
Vnitřní magnetosféra Plazmasféra Elektrické pole díky konvenkci (1) (Convection Electric Field) Vodivost σ, tj. ve vztažné soustavě pohybující se s plazmatem rychlostí v je elektrické pole rovno nule (
Registrační číslo projektu: CZ.1.07/1.4.00/21.2939. Název projektu: Investice do vzdělání - příslib do budoucnosti
 Registrační číslo projektu: CZ.1.07/1.4.00/21.2939 Název projektu: Investice do vzdělání - příslib do budoucnosti Číslo přílohy: VY_číslo šablony_inovace_číslo přílohy Autor Datum vytvoření vzdělávacího
Registrační číslo projektu: CZ.1.07/1.4.00/21.2939 Název projektu: Investice do vzdělání - příslib do budoucnosti Číslo přílohy: VY_číslo šablony_inovace_číslo přílohy Autor Datum vytvoření vzdělávacího
V mnoha běžných případech v optickém oboru je zanedbáváno silové působení magnetické složky elektromagnetického pole na náboje v látce str. 3 6.
 Nekvantový popis interakce světla s pasivní látkou Zcela nekvantová fyzika nemůže interakci elektromagnetického záření s látkou popsat, např. atom jako soustava kladných a záporných nábojů by vůbec nebyl
Nekvantový popis interakce světla s pasivní látkou Zcela nekvantová fyzika nemůže interakci elektromagnetického záření s látkou popsat, např. atom jako soustava kladných a záporných nábojů by vůbec nebyl
Matematika I Ètvercové matice - determinanty
 Matematika I Ètvercové matice - determinanty RNDr. Renata Klufová, Ph. D. Jihoèeská univerzita v Èeských Budìjovicích EF Katedra aplikované matematiky a informatiky Co u¾ známe? vektory - základní operace
Matematika I Ètvercové matice - determinanty RNDr. Renata Klufová, Ph. D. Jihoèeská univerzita v Èeských Budìjovicích EF Katedra aplikované matematiky a informatiky Co u¾ známe? vektory - základní operace
Definice spojité náhodné veličiny zjednodušená verze
 Definice spojité náhodné veličiny zjednodušená verze Náhodná veličina X se nazývá spojitá, jestliže existuje nezáporná funkce f : R R taková, že pro každé a, b R { }, a < b, platí P(a < X < b) = b a f
Definice spojité náhodné veličiny zjednodušená verze Náhodná veličina X se nazývá spojitá, jestliže existuje nezáporná funkce f : R R taková, že pro každé a, b R { }, a < b, platí P(a < X < b) = b a f
