Termomechanika 8. přednáška Doc. Dr. RNDr. Miroslav Holeček
|
|
|
- Oldřich Bartoš
- před 8 lety
- Počet zobrazení:
Transkript
1 Termomechanika 8. přednáška Doc. Dr. RNDr. Miroslav Holeček Upozornění: Tato prezentace slouží výhradně pro výukové účely Fakulty strojní Západočeské univerzity v Plzni. Byla sestavena autorem s využitím citovaných zdrojů a veřejně dostupných internetových zdrojů. Využití této prezentace nebo jejich částí pro jiné účely, stejně jako její veřejné šíření je nepřípustné.
2 Tekutina = kapalina, plyn
3 Van der Waalsova rovnice stavu F F Přitažlivá síla mezi částicemi je úměrná ρ 2 tlak, který cítí částice p = p a v 2 Objem nelze zmenšit pod jistou mez: v = v b tlak, který měříme Částice splňují rovnici ideálního plynu, ale s tlakem a objemem, který cítí : p v = r T objem, který mají částice k pohybu objem, který měříme p + a v 2 v b = r T
4 Van der Waalsova rov. stavu p + a v 2 v b = r T p + a v 2 v b = r T / v 2 p p v 2 + a v b = r T v 2 p v 3 p v 2 b + a v ab = r T v 2 v 3 v 2 b + r T p + v a p a b p = 0 Pro každý konkrétní tlak p má rovnice maximálně tři různá řešení v.
5 Van der Waalsova rov. stavu v 3 v 2 r T b + p + v a p a b p = 0 Pro každý konkrétní tlak p má rovnice maximálně tři různé řešení v. V kritickém bodě: v v K 3 = 0 v 3 3 v 2 v K + 3 v v K 2 v K 3 = 0
6 v 3 v 2 b + r T p + v a p a b p = 0 v 3 3 v 2 v K + 3 v v K 2 v K 3 = 0 3 v K = b + r T K p K 3 v K 2 = a p K a = 3 p K v K 2 v K 3 = r = p K T K a b b = p K v K p K a 3 v K = v K 3 + r T K p K 3 v K v K 3 = = v K 3 p K v K T K
7 a = 3 p K v K 2 b = v K 3 r = 8 3 p K v K T K Dosazení do van der Waalsovy rovnice: p + 3 p K v K 2 v 2 v v K 3 = 8 3 p K v K T K T p + 3 v K p K v 2 2 v v K 1 3 = 8 3 T T K
8 Zavedeme označení π p p k, φ v v k, τ T T k A dostaneme van der Waalsovu rovnici ve tvaru π + 3 φ 2 φ 1 3 = 8 3 τ Z toho vyplývá, že pokud dvě tekutiny splňují van der Waalsovu rovnici a platí např. π 1 = π 2 a φ 1 = φ 2, pak platí i τ 1 = τ 2
9 Izotermy van der Waalsovy rov. stavu CDE: nereálné, protože by došlo ke zvyšování tlaku při zvětšování objemu, tj. bylo by.. p v T > 0 AC, EB metastabilní stavy metastabilní přehřátá kapalina metastabilní podchlazená pára Maxwellovo pravidlo: plocha ADCA = plocha DBED
10 Termodynamická plocha látek, u nichž dochází při tuhnutí ke zmenšování objemu (ne H 2 O) trojný bod (vůči p, T)
11 Termodynamická plocha látek, které při tuhnutí zvětšují objem (H 2 O) v
12 Průměty termodynamické plochy obcházíme oblast mokré páry trojný bod
13 Voda a vodní pára závislost c p (T, p) dq p = mc p dt c p nadkritické tlaky dt = 0, dq p 0 c p přehřátá pára
14 Voda a vodní pára závislost κ(t, p) Pro tříatomový ideální plyn: κ = 1. 3
15 Diagram T-s T K dodávání tepla A B izoterma s
16 Voda a vodní pára hmotnost syté páry Suchost: x = m m +m hmotnost syté kapaliny
17 Voda a vodní pára
18 Mokrá pára Suchost: x = m m + m m = m V = V + V m v = m v + m v v = m m v + m m v v = v + x v v H = H + H m h = m h + m h h = m m h + m m h h = h + x h h /: m
19 S = S + S m s = m s + m s s = m m s + m m s = s + x s s s konstantní suchost
20 Diagram T-s Diagram h-s (Molliérův) konstantní suchost konstantní suchost
21 Skupenství: Skupenské teplo: Výparné teplo: 1 tuhá fáze (led) 2 kapalná fáze (voda) 3 plynná fáze (pára) l 12 tání l 23 vypařování l 13 sublimace l 23 = T s s = h h kapalinné teplo q k výrobní teplo q v = q k + l 23 T = T 0
22 Clapeyronova-Clausiova rovnice dp v v = dt s s VYKONANÁ PRÁCE ROZDÍL TEPEL dp = s s dt EV v v = l 23 = T s s l 23 T v v vypařování dp dt MELT = l 12 T v v tání dp dt SUBL = l 13 T v v sublimace
23 Pro H 2 O: v < v < v v v < 0 dp dt < 0 tání dp dt MELT = l 12 T v v Fázový diagram
24 Škrcení reálných tekutin h 1 + w = h 2 + w h 1 h 2 Joule-Thomsonův součinitel k JT = T V porézní látce dp < 0 p h T 2 > T 1 dt > 0 a k JT < 0 T 2 < T 1 dt < 0 a k JT > 0 T 2 = T 1 dt = 0 a k JT = 0
25 dq = dh v dp; dq = T ds Matematická vsuvka: ds = 1 T dh v T dp f x, y df = f x dx + f y dy y f x = x f y ds = 1 dh + v dp T T p 1 T = h v T 1 T 2 T p h = v T v T T p T p T 2 T h p
26 1 T 2 T p h = v T v T T p T p T 2 T h p T p h = v T p T v T h p h T p = c p T = 1 h p c p k JT = T = 1 p h c p v T p T v
27 Ideální plyn k JT = 1 c p p v = r T r T v = p v = r T p p r p T v = 1 c p v v = 0 h 1 h 2 dh = c p dt c p = konst h 2 h 1 = c p T 2 T 1 Reálná tekutina k JT = 1 c p v T p T v tan α = T v p, A tan β = T A v A tan α > tan β k JT < 0 b
28 Reálná tekutina k JT < 0 k JT = T p h < 0 T 2 > T 1 T inv1 : T inv2 : α = β k JT = 0 T 2 = T 1 α = β T 2 = T 1 Pro T inv1 < T < T inv2 k JT > 0 T 2 < T 1 b
29 Škrcení mokré páry Škrticí kalorimetr přehřátá pára mokrá pára
30 Směšování a) Stálý součet objemů m s = m 1 + m 2 V s = V 1 + V 2 da = p dv = 0 dq = 0 dq = du + da du = 0 U = konst m 1 u 1 + m 2 u 2 = m s u s u s = m 1u 1 + m 2 u 2 m s v s = V s m s
31 b) Směšování proudů m 1 h 1 + w m 2 h 2 + w 2 2 = m s h s + w s = h s = m 1 h 1 + m 2 h 2 m 1 + m 2
32 Termodynamika proudících reálných plynů w 2 = 2 h 1 h 2 + w 1 2 w 2 = 2 h 1 + w h 2 totální entalpie Hmotnostní průtok Dále platí m = ρ w S = S = m v w w S v dw w 1 Ma2 + ds S = 0
33 Rychlost zvuku pokud platí pv κ konst a κ konst pak a p k p 1 κ p v 2 κ + 1 κ κ 1
34 Parní oběhy (s kondenzací) Pracovní oběh Clausiův-Rankinův a T = h 1 h 2 (s = konst) a č = h 4 h 3 (s = konst) q kot = h 1 h 4 (p = konst) q kond = h 2 h 3 (p = konst) η = a T q kot
35 Zvyšování termické účinnosti Clausiova - Rankinova oběhu Regenerace v oběhu s mokrou párou Regenerace v oběhu s přehřátou párou přihřívání páry
36 Chladicí oběh ε = q p a = q o q p q p > 1 ε t = q o a = q o q o q p Chladicí oběh s expandérem ε t = q o q o q p = q o q p + q p q o q p = 1 + q o q o q p = 1 + ε a = q o q p
37 Chladicí oběh se škrtícím ventilem Chladnička Tepelné čerpadlo
38 Konec Děkuji za pozornost
Termomechanika 6. přednáška Doc. Dr. RNDr. Miroslav Holeček
 Termomechanika 6. přednáška Doc. Dr. RNDr. Miroslav Holeček Upozornění: Tato prezentace slouží výhradně pro výukové účely Fakulty strojní Západočeské univerzity v Plzni. Byla sestavena autorem s využitím
Termomechanika 6. přednáška Doc. Dr. RNDr. Miroslav Holeček Upozornění: Tato prezentace slouží výhradně pro výukové účely Fakulty strojní Západočeské univerzity v Plzni. Byla sestavena autorem s využitím
Termomechanika 9. přednáška Doc. Dr. RNDr. Miroslav Holeček
 Termomechanika 9. přednáška Doc. Dr. RNDr. Miroslav Holeček Upozornění: Tato prezentace slouží výhradně pro výukové účely Fakulty strojní Západočeské univerzity v Plzni. Byla sestavena autorem s využitím
Termomechanika 9. přednáška Doc. Dr. RNDr. Miroslav Holeček Upozornění: Tato prezentace slouží výhradně pro výukové účely Fakulty strojní Západočeské univerzity v Plzni. Byla sestavena autorem s využitím
Termomechanika 4. přednáška
 ermomechanika 4. přednáška Miroslav Holeček Upozornění: ato prezentace slouží výhradně pro výukové účely Fakulty strojní Západočeské univerzity v Plzni. Byla sestavena autorem s využitím citovaných zdrojů
ermomechanika 4. přednáška Miroslav Holeček Upozornění: ato prezentace slouží výhradně pro výukové účely Fakulty strojní Západočeské univerzity v Plzni. Byla sestavena autorem s využitím citovaných zdrojů
Tepelná vodivost. střední rychlost. T 1 > T 2 z. teplo přenesené za čas dt: T 1 T 2. tepelný tok střední volná dráha. součinitel tepelné vodivosti
 Tepelná vodivost teplo přenesené za čas dt: T 1 > T z T 1 S tepelný tok střední volná dráha T součinitel tepelné vodivosti střední rychlost Tepelná vodivost součinitel tepelné vodivosti při T = 300 K součinitel
Tepelná vodivost teplo přenesené za čas dt: T 1 > T z T 1 S tepelný tok střední volná dráha T součinitel tepelné vodivosti střední rychlost Tepelná vodivost součinitel tepelné vodivosti při T = 300 K součinitel
PROCESY V TECHNICE BUDOV 8
 UNIVERZITA TOMÁŠE BATI VE ZLÍNĚ FAKULTA APLIKOVANÉ INFORMATIKY PROCESY V TECHNICE BUDOV 8 Dagmar Janáčová, Hana Charvátová Zlín 2013 Tento studijní materiál vznikl za finanční podpory Evropského sociálního
UNIVERZITA TOMÁŠE BATI VE ZLÍNĚ FAKULTA APLIKOVANÉ INFORMATIKY PROCESY V TECHNICE BUDOV 8 Dagmar Janáčová, Hana Charvátová Zlín 2013 Tento studijní materiál vznikl za finanční podpory Evropského sociálního
Termomechanika 11. přednáška Doc. Dr. RNDr. Miroslav Holeček
 Termomechanika 11. přednáška Doc. Dr. RNDr. Miroslav Holeček Upozornění: Tato prezentace slouží výhradně pro výukové účely Fakulty strojní Západočeské univerzity v Plzni. Byla sestavena autorem s využitím
Termomechanika 11. přednáška Doc. Dr. RNDr. Miroslav Holeček Upozornění: Tato prezentace slouží výhradně pro výukové účely Fakulty strojní Západočeské univerzity v Plzni. Byla sestavena autorem s využitím
Termomechanika 10. přednáška Doc. Dr. RNDr. Miroslav Holeček
 Termomechanika 10. přednáška Doc. Dr. RNDr. Miroslav Holeček Upozornění: Tato prezentace slouží výhradně pro výukové účely Fakulty strojní Západočeské univerzity v Plzni. Byla sestavena autorem s využitím
Termomechanika 10. přednáška Doc. Dr. RNDr. Miroslav Holeček Upozornění: Tato prezentace slouží výhradně pro výukové účely Fakulty strojní Západočeské univerzity v Plzni. Byla sestavena autorem s využitím
Termodynamika par. Rovnovážný diagram látky 1 pevná fáze, 2 kapalná fáze, 3 plynná fáze
 ermodynamika par Fázové změny látky: Přivádíme-li pevné fázi látky teplo, dochází při jisté teplotě a tlaku ke změně pevné fáze na fázi kapalnou (tání) Jestliže spojíme body tání při různých tlacích, získáme
ermodynamika par Fázové změny látky: Přivádíme-li pevné fázi látky teplo, dochází při jisté teplotě a tlaku ke změně pevné fáze na fázi kapalnou (tání) Jestliže spojíme body tání při různých tlacích, získáme
Otázky Termomechanika (2014)
 Otázky Termomechanika (2014) 1. Základní pojmy a veličiny termomechaniky a. Makroskopický a mikroskopický popis systému, makroskopické veličiny b. Tlak: definice makroskopická a mikroskopické objasnění
Otázky Termomechanika (2014) 1. Základní pojmy a veličiny termomechaniky a. Makroskopický a mikroskopický popis systému, makroskopické veličiny b. Tlak: definice makroskopická a mikroskopické objasnění
VYBRANÉ STATĚ Z PROCESNÍHO INŢENÝRSTVÍ cvičení 12
 UNIVERZITA TOMÁŠE BATI VE ZLÍNĚ FAKULTA APLIKOVANÉ INFORMATIKY VYBRANÉ STATĚ Z PROCESNÍHO INŢENÝRSTVÍ cvičení 2 Termodynamika reálných plynů část 2 Hana Charvátová, Dagmar Janáčová Zlín 203 Tento studijní
UNIVERZITA TOMÁŠE BATI VE ZLÍNĚ FAKULTA APLIKOVANÉ INFORMATIKY VYBRANÉ STATĚ Z PROCESNÍHO INŢENÝRSTVÍ cvičení 2 Termodynamika reálných plynů část 2 Hana Charvátová, Dagmar Janáčová Zlín 203 Tento studijní
Termomechanika 12. přednáška Doc. Dr. RNDr. Miroslav Holeček
 Termomechanika 2. přednáška Doc. Dr. RNDr. Miroslav Holeček Upozornění: Tato prezentace slouží výhradně pro výukové účely Fakulty strojní Západočeské univerzity v Plzni. Byla sestavena autorem s využitím
Termomechanika 2. přednáška Doc. Dr. RNDr. Miroslav Holeček Upozornění: Tato prezentace slouží výhradně pro výukové účely Fakulty strojní Západočeské univerzity v Plzni. Byla sestavena autorem s využitím
přednáška č. 6 Elektrárny B1M15ENY Tepelné oběhy: Stavové změny Typy oběhů Možnosti zvýšení účinnosti Ing. Jan Špetlík, Ph.D.
 Elektrárny B1M15ENY přednáška č. 6 Tepelné oběhy: Stavové změny Typy oběhů Možnosti zvýšení účinnosti Ing. Jan Špetlík, Ph.D. ČVUT FEL Katedra elektroenergetiky E-mail: spetlij@fel.cvut.cz Termodynamika:
Elektrárny B1M15ENY přednáška č. 6 Tepelné oběhy: Stavové změny Typy oběhů Možnosti zvýšení účinnosti Ing. Jan Špetlík, Ph.D. ČVUT FEL Katedra elektroenergetiky E-mail: spetlij@fel.cvut.cz Termodynamika:
Elektroenergetika 1. Termodynamika a termodynamické oběhy
 Termodynamika a termodynamické oběhy Termodynamika Popisuje procesy, které zahrnují změny teploty, přeměny energie a vzájemný vztah mezi tepelnou energií a mechanickou prací Opakování fyziky Termodynamický
Termodynamika a termodynamické oběhy Termodynamika Popisuje procesy, které zahrnují změny teploty, přeměny energie a vzájemný vztah mezi tepelnou energií a mechanickou prací Opakování fyziky Termodynamický
Poznámky k cvičením z termomechaniky Cvičení 3.
 Vnitřní energie U Vnitřní energie U je stavová veličina U = U (p, V, T), ale závisí pouze na teplotě (experiment Gay-Lussac / Joule) U = f(t) Pro měrnou vnitřní energii (tedy pro vnitřní energii jednoho
Vnitřní energie U Vnitřní energie U je stavová veličina U = U (p, V, T), ale závisí pouze na teplotě (experiment Gay-Lussac / Joule) U = f(t) Pro měrnou vnitřní energii (tedy pro vnitřní energii jednoho
Mol. fyz. a termodynamika
 Molekulová fyzika pracuje na základě kinetické teorie látek a statistiky Termodynamika zkoumání tepelných jevů a strojů nezajímají nás jednotlivé částice Molekulová fyzika základem jsou: Látka kteréhokoli
Molekulová fyzika pracuje na základě kinetické teorie látek a statistiky Termodynamika zkoumání tepelných jevů a strojů nezajímají nás jednotlivé částice Molekulová fyzika základem jsou: Látka kteréhokoli
Fyzikální učebna vybavená audiovizuální technikou, interaktivní tabule, fyzikální pomůcky
 Předmět: Náplň: Třída: Počet hodin: Pomůcky: Fyzika (FYZ) Molekulová fyzika, termika 2. ročník, sexta 2 hodiny týdně Fyzikální učebna vybavená audiovizuální technikou, interaktivní tabule, fyzikální pomůcky
Předmět: Náplň: Třída: Počet hodin: Pomůcky: Fyzika (FYZ) Molekulová fyzika, termika 2. ročník, sexta 2 hodiny týdně Fyzikální učebna vybavená audiovizuální technikou, interaktivní tabule, fyzikální pomůcky
Kontrolní otázky k 1. přednášce z TM
 Kontrolní otázky k 1. přednášce z TM 1. Jak závisí hodnota izobarického součinitele objemové roztažnosti ideálního plynu na teplotě a jak na tlaku? Odvoďte. 2. Jak závisí hodnota izochorického součinitele
Kontrolní otázky k 1. přednášce z TM 1. Jak závisí hodnota izobarického součinitele objemové roztažnosti ideálního plynu na teplotě a jak na tlaku? Odvoďte. 2. Jak závisí hodnota izochorického součinitele
Transportní jevy v plynech Reálné plyny Fázové přechody Kapaliny
 Transportní jevy v plynech Reálné plyny Fázové přechody Kapaliny Hustota toku Zatím jsme studovali pouze soustavy, které byly v rovnovážném stavu není-li soustava v silovém poli, je hustota částic stejná
Transportní jevy v plynech Reálné plyny Fázové přechody Kapaliny Hustota toku Zatím jsme studovali pouze soustavy, které byly v rovnovážném stavu není-li soustava v silovém poli, je hustota částic stejná
12. Termomechanika par, Clausiova-Clapeyronova rovnice, parní tabulky, základni termodynamické děje v oblasti par
 1/18 12. Termomechanika par, Clausiova-Clapeyronova rovnice, parní tabulky, základni termodynamické děje v oblasti par Příklad: 12.1, 12.2, 12.3, 12.4, 12.5, 12.6, 12.7, 12.8, 12.9, 12.10, 12.11, 12.12,
1/18 12. Termomechanika par, Clausiova-Clapeyronova rovnice, parní tabulky, základni termodynamické děje v oblasti par Příklad: 12.1, 12.2, 12.3, 12.4, 12.5, 12.6, 12.7, 12.8, 12.9, 12.10, 12.11, 12.12,
Základem molekulové fyziky je kinetická teorie látek. Vychází ze tří pouček:
 Molekulová fyzika zkoumá vlastnosti látek na základě jejich vnitřní struktury, pohybu a vzájemného působení částic, ze kterých se látky skládají. Termodynamika se zabývá zákony přeměny různých forem energie
Molekulová fyzika zkoumá vlastnosti látek na základě jejich vnitřní struktury, pohybu a vzájemného působení částic, ze kterých se látky skládají. Termodynamika se zabývá zákony přeměny různých forem energie
VYBRANÉ STATĚ Z PROCESNÍHO INŽENÝRSTVÍ cvičení 11
 UNIVERZITA TOMÁŠE BATI VE ZLÍNĚ FAKULTA APLIKOVANÉ INFORMATIKY VYBRANÉ STATĚ Z PROCESNÍHO INŽENÝRSTVÍ cvičení 11 Termodynamika reálných plynů část 1 Hana Charvátová, Dagmar Janáčová Zlín 2013 Tento studijní
UNIVERZITA TOMÁŠE BATI VE ZLÍNĚ FAKULTA APLIKOVANÉ INFORMATIKY VYBRANÉ STATĚ Z PROCESNÍHO INŽENÝRSTVÍ cvičení 11 Termodynamika reálných plynů část 1 Hana Charvátová, Dagmar Janáčová Zlín 2013 Tento studijní
Termomechanika 5. přednáška
 Termomechanika 5. přednáška Miroslav Holeček, Jan Vychytil Upozornění: Tato prezentace slouží výhradně pro výukové účely Fakulty strojní Západočeské univerzity v Plzni. Byla sestavena autory s využitím
Termomechanika 5. přednáška Miroslav Holeček, Jan Vychytil Upozornění: Tato prezentace slouží výhradně pro výukové účely Fakulty strojní Západočeské univerzity v Plzni. Byla sestavena autory s využitím
Termodynamika. T [K ]=t [ 0 C] 273,15 T [ K ]= t [ 0 C] termodynamická teplota: Stavy hmoty. jednotka: 1 K (kelvin) = 1/273,16 část termodynamické
![Termodynamika. T [K ]=t [ 0 C] 273,15 T [ K ]= t [ 0 C] termodynamická teplota: Stavy hmoty. jednotka: 1 K (kelvin) = 1/273,16 část termodynamické Termodynamika. T [K ]=t [ 0 C] 273,15 T [ K ]= t [ 0 C] termodynamická teplota: Stavy hmoty. jednotka: 1 K (kelvin) = 1/273,16 část termodynamické](/thumbs/24/2778201.jpg) Termodynamika termodynamická teplota: Stavy hmoty jednotka: 1 K (kelvin) = 1/273,16 část termodynamické teploty trojného bodu vody (273,16 K = 0,01 o C). 0 o C = 273,15 K T [K ]=t [ 0 C] 273,15 T [ K ]=
Termodynamika termodynamická teplota: Stavy hmoty jednotka: 1 K (kelvin) = 1/273,16 část termodynamické teploty trojného bodu vody (273,16 K = 0,01 o C). 0 o C = 273,15 K T [K ]=t [ 0 C] 273,15 T [ K ]=
IV. Fázové rovnováhy. 4. Fázové rovnováhy Ústav procesní a zpracovatelské techniky FS ČVUT v Praze
 IV. Fázové rovnováhy 1 4. Fázové rovnováhy 4.1 Základní pojmy 4.2 Fázové rovnováhy jednosložkové soustavy 4.3 Fázové rovnováhy dvousložkových soustav 4.3.1 Soustava tuhá složka tuhá složka 4.3.2 Soustava
IV. Fázové rovnováhy 1 4. Fázové rovnováhy 4.1 Základní pojmy 4.2 Fázové rovnováhy jednosložkové soustavy 4.3 Fázové rovnováhy dvousložkových soustav 4.3.1 Soustava tuhá složka tuhá složka 4.3.2 Soustava
FYZIKÁLNÍ CHEMIE I: 1. ČÁST KCH/P401
 Univerzita J. E. Purkyně v Ústí nad Labem Přírodovědecká fakulta FYZIKÁLNÍ CHEMIE I: 1. ČÁST KCH/P401 Magda Škvorová Ústí nad Labem 2013 Obor: Toxikologie a analýza škodlivin, Chemie (dvouoborová) Klíčová
Univerzita J. E. Purkyně v Ústí nad Labem Přírodovědecká fakulta FYZIKÁLNÍ CHEMIE I: 1. ČÁST KCH/P401 Magda Škvorová Ústí nad Labem 2013 Obor: Toxikologie a analýza škodlivin, Chemie (dvouoborová) Klíčová
Jméno: _ podpis: ročník: č. studenta. Otázky typu A (0.25 bodů za otázku, správně je pouze jedna odpověď)
 Jméno: _ podpis: ročník: č. studenta Otázky typu A (0.25 bodů za otázku, správně je pouze jedna odpověď) 1. JEDNOTKA PASCAL JE DEFINOVÁNÁ JAKO a. N.m.s b. kg.m-1.s-2 c. kg.m-2 d. kg.m.s 2. KALORIMETRICKÁ
Jméno: _ podpis: ročník: č. studenta Otázky typu A (0.25 bodů za otázku, správně je pouze jedna odpověď) 1. JEDNOTKA PASCAL JE DEFINOVÁNÁ JAKO a. N.m.s b. kg.m-1.s-2 c. kg.m-2 d. kg.m.s 2. KALORIMETRICKÁ
Nultá věta termodynamická
 TERMODYNAMIKA Nultá věta termodynamická 2 Práce 3 Práce - příklady 4 1. věta termodynamická 5 Entalpie 6 Tepelné kapacity 7 Vnitřní energie a entalpie ideálního plynu 8 Výpočet tepla a práce 9 Adiabatický
TERMODYNAMIKA Nultá věta termodynamická 2 Práce 3 Práce - příklady 4 1. věta termodynamická 5 Entalpie 6 Tepelné kapacity 7 Vnitřní energie a entalpie ideálního plynu 8 Výpočet tepla a práce 9 Adiabatický
1/1 PŘEHLED TEORIE A VÝPOČTOVÝCH VZTAHŮ. Základní stavové veličiny látky. Vztahy mezi stavovými veličinami ideálních plynů
 1/1 PŘEHLED TEORIE A VÝPOČTOVÝCH VZTAHŮ Základní stavové veličiny látky Vztahy mezi stavovými veličinami ideálních plynů Stavová rovnice ideálního plynu f(p, v, T)=0 Měrné tepelné kapacity, c = f (p,t)
1/1 PŘEHLED TEORIE A VÝPOČTOVÝCH VZTAHŮ Základní stavové veličiny látky Vztahy mezi stavovými veličinami ideálních plynů Stavová rovnice ideálního plynu f(p, v, T)=0 Měrné tepelné kapacity, c = f (p,t)
Fyzikální chemie. Magda Škvorová KFCH CN463 magda.skvorova@ujep.cz, tel. 3302. 14. února 2013
 Fyzikální chemie Magda Škvorová KFCH CN463 magda.skvorova@ujep.cz, tel. 3302 14. února 2013 Co je fyzikální chemie? Co je fyzikální chemie? makroskopický přístup: (klasická) termodynamika nerovnovážná
Fyzikální chemie Magda Škvorová KFCH CN463 magda.skvorova@ujep.cz, tel. 3302 14. února 2013 Co je fyzikální chemie? Co je fyzikální chemie? makroskopický přístup: (klasická) termodynamika nerovnovážná
MOLEKULOVÁ FYZIKA A TERMODYNAMIKA
 MOLEKULOVÁ FYZIKA A TERMODYNAMIKA 2 metody zkoumání látek na základě vnějších projevů: I. KINETICKÁ TEORIE LÁTEK -studium vlastností látek na základě vnitřní struktury, pohybu a vzájemného působení jednotlivých
MOLEKULOVÁ FYZIKA A TERMODYNAMIKA 2 metody zkoumání látek na základě vnějších projevů: I. KINETICKÁ TEORIE LÁTEK -studium vlastností látek na základě vnitřní struktury, pohybu a vzájemného působení jednotlivých
=, V = T * konst. =, p = T * konst. Termodynamika ideálních plynů
 Termodynamika ideálních plynů 1. Definice uzavřené termodynamické soustav : Hmotnost procházející kontrolní plochou je nulová 2. Definice otevřené termodynamické soustav: Hmotnost procházející kontrolní
Termodynamika ideálních plynů 1. Definice uzavřené termodynamické soustav : Hmotnost procházející kontrolní plochou je nulová 2. Definice otevřené termodynamické soustav: Hmotnost procházející kontrolní
PROCESY V TECHNICE BUDOV 9
 UNIVERZIA OMÁŠE BAI VE ZLÍNĚ FAKULA APLIKOVANÉ INFORMAIKY PROCESY V ECHNICE BUDOV 9 ermodynamika reálných plynů (2. část) Dagmar Janáčová, Hana Charvátová Zlín 2013 ento studijní materiál vznikl za finanční
UNIVERZIA OMÁŠE BAI VE ZLÍNĚ FAKULA APLIKOVANÉ INFORMAIKY PROCESY V ECHNICE BUDOV 9 ermodynamika reálných plynů (2. část) Dagmar Janáčová, Hana Charvátová Zlín 2013 ento studijní materiál vznikl za finanční
5.4 Adiabatický děj Polytropický děj Porovnání dějů Základy tepelných cyklů První zákon termodynamiky pro cykly 42 6.
 OBSAH Předmluva 9 I. ZÁKLADY TERMODYNAMIKY 10 1. Základní pojmy 10 1.1 Termodynamická soustava 10 1.2 Energie, teplo, práce 10 1.3 Stavy látek 11 1.4 Veličiny popisující stavy látek 12 1.5 Úlohy technické
OBSAH Předmluva 9 I. ZÁKLADY TERMODYNAMIKY 10 1. Základní pojmy 10 1.1 Termodynamická soustava 10 1.2 Energie, teplo, práce 10 1.3 Stavy látek 11 1.4 Veličiny popisující stavy látek 12 1.5 Úlohy technické
Zpracování teorie 2010/11 2011/12
 Zpracování teorie 2010/11 2011/12 Cykly Děje Proudění (turbíny) počet v: roce 2010/11 a roce 2011/12 Chladící zařízení (nakreslete cyklus a nakreslete schéma)... zde 13 + 2 (15) Izochorický děj páry (nakreslit
Zpracování teorie 2010/11 2011/12 Cykly Děje Proudění (turbíny) počet v: roce 2010/11 a roce 2011/12 Chladící zařízení (nakreslete cyklus a nakreslete schéma)... zde 13 + 2 (15) Izochorický děj páry (nakreslit
Fáze a fázové přechody
 Kvantová a statistická fyzika 2 (Termodynamika a statistická fyzika) Fáze a fázové přechody Pojem fáze je zobecněním pojmu skupenství, označuje homogenní část makroskopického tělesa. Jednotlivé fáze v
Kvantová a statistická fyzika 2 (Termodynamika a statistická fyzika) Fáze a fázové přechody Pojem fáze je zobecněním pojmu skupenství, označuje homogenní část makroskopického tělesa. Jednotlivé fáze v
TERMOMECHANIKA 1. Základní pojmy
 1 FSI VUT v Brně, Energetický ústav Odbor termomechaniky a techniky prostředí prof. Ing. Milan Pavelek, CSc. TERMOMECHANIKA 1. Základní pojmy OSNOVA 1. KAPITOLY Termodynamická soustava Energie, teplo,
1 FSI VUT v Brně, Energetický ústav Odbor termomechaniky a techniky prostředí prof. Ing. Milan Pavelek, CSc. TERMOMECHANIKA 1. Základní pojmy OSNOVA 1. KAPITOLY Termodynamická soustava Energie, teplo,
5.7 Vlhkost vzduchu 5.7.5 Absolutní vlhkost 5.7.6 Poměrná vlhkost 5.7.7 Rosný bod 5.7.8 Složení vzduchu 5.7.9 Měření vlhkosti vzduchu
 Fázové přechody 5.6.5 Fáze Fázové rozhraní 5.6.6 Gibbsovo pravidlo fází 5.6.7 Fázový přechod Fázový přechod prvního druhu Fázový přechod druhého druhu 5.6.7.1 Clausiova-Clapeyronova rovnice 5.6.8 Skupenství
Fázové přechody 5.6.5 Fáze Fázové rozhraní 5.6.6 Gibbsovo pravidlo fází 5.6.7 Fázový přechod Fázový přechod prvního druhu Fázový přechod druhého druhu 5.6.7.1 Clausiova-Clapeyronova rovnice 5.6.8 Skupenství
Přehled základních fyzikálních veličin užívaných ve výpočtech v termomechanice. Autor Ing. Jan BRANDA Jazyk Čeština
 Identifikátor materiálu: ICT 2 41 Registrační číslo projektu CZ.1.07/1.5.00/34.0796 Název projektu Vzděláváme pro život Název příjemce podpory SOU plynárenské Pardubice název materiálu (DUM) Mechanika
Identifikátor materiálu: ICT 2 41 Registrační číslo projektu CZ.1.07/1.5.00/34.0796 Název projektu Vzděláváme pro život Název příjemce podpory SOU plynárenské Pardubice název materiálu (DUM) Mechanika
TEPELNÉ JEVY. Mgr. Jan Ptáčník - GJVJ - Fyzika - Tercie
 TEPELNÉ JEVY Mgr. Jan Ptáčník - GJVJ - Fyzika - Tercie Vnitřní energie tělesa Každé těleso se skládá z látek. Látky se skládají z částic. neustálý neuspořádaný pohyb kinetická energie vzájemné působení
TEPELNÉ JEVY Mgr. Jan Ptáčník - GJVJ - Fyzika - Tercie Vnitřní energie tělesa Každé těleso se skládá z látek. Látky se skládají z částic. neustálý neuspořádaný pohyb kinetická energie vzájemné působení
2.4 Stavové chování směsí plynů Ideální směs Ideální směs reálných plynů Stavové rovnice pro plynné směsi
 1. ZÁKLADNÍ POJMY 1.1 Systém a okolí 1.2 Vlastnosti systému 1.3 Vybrané základní veličiny 1.3.1 Množství 1.3.2 Délka 1.3.2 Délka 1.4 Vybrané odvozené veličiny 1.4.1 Objem 1.4.2 Hustota 1.4.3 Tlak 1.4.4
1. ZÁKLADNÍ POJMY 1.1 Systém a okolí 1.2 Vlastnosti systému 1.3 Vybrané základní veličiny 1.3.1 Množství 1.3.2 Délka 1.3.2 Délka 1.4 Vybrané odvozené veličiny 1.4.1 Objem 1.4.2 Hustota 1.4.3 Tlak 1.4.4
STRUKTURA PEVNÝCH LÁTEK A KAPALIN
 STRUKTURA PEVNÝCH LÁTEK A KAPALIN 19. ZMĚNY SKUPENSTVÍ, FÁZOVÝ DIAGRAM Autor: Ing. Eva Jančová DESS SOŠ a SOU spol. s r. o. SKUPENSTVÍ - Skupenství neboli stav je konkrétní forma látky, charakterizovaná
STRUKTURA PEVNÝCH LÁTEK A KAPALIN 19. ZMĚNY SKUPENSTVÍ, FÁZOVÝ DIAGRAM Autor: Ing. Eva Jančová DESS SOŠ a SOU spol. s r. o. SKUPENSTVÍ - Skupenství neboli stav je konkrétní forma látky, charakterizovaná
Fyzika - Sexta, 2. ročník
 - Sexta, 2. ročník Fyzika Výchovné a vzdělávací strategie Kompetence komunikativní Kompetence k řešení problémů Kompetence sociální a personální Kompetence občanská Kompetence k podnikavosti Kompetence
- Sexta, 2. ročník Fyzika Výchovné a vzdělávací strategie Kompetence komunikativní Kompetence k řešení problémů Kompetence sociální a personální Kompetence občanská Kompetence k podnikavosti Kompetence
h nadmořská výška [m]
![h nadmořská výška [m] h nadmořská výška [m]](/thumbs/92/109475205.jpg) Katedra prostředí staveb a TZB KLIMATIZACE, VĚTRÁNÍ Cvičení pro navazující magisterské studium studijního oboru Prostředí staveb Cvičení č. 1 Zpracoval: Ing. Zdeněk GALDA Nové výukové moduly vznikly za
Katedra prostředí staveb a TZB KLIMATIZACE, VĚTRÁNÍ Cvičení pro navazující magisterské studium studijního oboru Prostředí staveb Cvičení č. 1 Zpracoval: Ing. Zdeněk GALDA Nové výukové moduly vznikly za
Elektroenergetika 1. Termodynamika
 Elektroenergetika 1 Termodynamika Termodynamika Popisuje procesy, které zahrnují změny teploty, přeměny energie a vzájemný vztah mezi tepelnou energií a mechanickou prací Opakování fyziky Termodynamický
Elektroenergetika 1 Termodynamika Termodynamika Popisuje procesy, které zahrnují změny teploty, přeměny energie a vzájemný vztah mezi tepelnou energií a mechanickou prací Opakování fyziky Termodynamický
Do známky zkoušky rovnocenným podílem započítávají získané body ze zápočtového testu.
 Podmínky pro získání zápočtu a zkoušky z předmětu Chemicko-inženýrská termodynamika pro zpracování ropy Zápočet je udělen, pokud student splní zápočtový test alespoň na 50 %. Zápočtový test obsahuje 3
Podmínky pro získání zápočtu a zkoušky z předmětu Chemicko-inženýrská termodynamika pro zpracování ropy Zápočet je udělen, pokud student splní zápočtový test alespoň na 50 %. Zápočtový test obsahuje 3
ZMĚNY SKUPENSTVÍ LÁTEK
 ZMĚNY SKUPENSTVÍ LÁTEK TÁNÍ A TUHNUTÍ - OSNOVA Kapilární jevy příklad Skupenské přeměny látek Tání a tuhnutí Teorie s video experimentem Příklad KAPILÁRNÍ JEVY - OPAKOVÁNÍ KAPILÁRNÍ JEVY - PŘÍKLAD Jak
ZMĚNY SKUPENSTVÍ LÁTEK TÁNÍ A TUHNUTÍ - OSNOVA Kapilární jevy příklad Skupenské přeměny látek Tání a tuhnutí Teorie s video experimentem Příklad KAPILÁRNÍ JEVY - OPAKOVÁNÍ KAPILÁRNÍ JEVY - PŘÍKLAD Jak
Fázové rozhraní - plocha,na které se vlastnosti systému mění skokem ; fáze o určité tloušťce
 Fázové rozhraní Fázové rozhraní - plocha,na které se vlastnosti systému mění skokem ; fáze o určité tloušťce Homogenní - kapalina/plyn - povrch;kapalina/kapalina Nehomogenní - tuhá látka/plyn - povrch;
Fázové rozhraní Fázové rozhraní - plocha,na které se vlastnosti systému mění skokem ; fáze o určité tloušťce Homogenní - kapalina/plyn - povrch;kapalina/kapalina Nehomogenní - tuhá látka/plyn - povrch;
Poznámky k cvičením z termomechaniky Cvičení 10.
 Příklad 1 Topné těleso o objemu 0,5 [m 3 ], naplněné sytou párou o tlaku 0,15 [MPa], bylo odstaveno. Po nějaké době vychladlo na teplotu 30 C. Určete množství uvolněného tepla a konečný stav páry v tělese.
Příklad 1 Topné těleso o objemu 0,5 [m 3 ], naplněné sytou párou o tlaku 0,15 [MPa], bylo odstaveno. Po nějaké době vychladlo na teplotu 30 C. Určete množství uvolněného tepla a konečný stav páry v tělese.
Řešení: Fázový diagram vody
 Řešení: 1) Menší hustota ledu v souladu s Archimédovým zákonem zapříčiňuje plování jedu ve vodě. Vodní nádrže a toky tudíž zamrzají shora (od hladiny). Kdyby hustota ledu byla větší než hustota vody, docházelo
Řešení: 1) Menší hustota ledu v souladu s Archimédovým zákonem zapříčiňuje plování jedu ve vodě. Vodní nádrže a toky tudíž zamrzají shora (od hladiny). Kdyby hustota ledu byla větší než hustota vody, docházelo
Fázové heterogenní rovnováhy Fáze = homogenní část soustavy, oddělná fyzickým rozhraním, na rozhraní se vlastnosti mění skokem
 Fázové heterogenní rovnováhy Fáze = homogenní část soustavy, oddělná fyzickým rozhraním, na rozhraní se vlastnosti mění skokem Rovnováha Tepelná - T všude stejná Mechanická - p všude stejný Chemická -
Fázové heterogenní rovnováhy Fáze = homogenní část soustavy, oddělná fyzickým rozhraním, na rozhraní se vlastnosti mění skokem Rovnováha Tepelná - T všude stejná Mechanická - p všude stejný Chemická -
Termomechanika 5. přednáška Michal Hoznedl
 Termomechanika 5. přednáška Michal Hoznedl Upozornění: Tato prezentace slouží výhradně pro výukové účely Fakulty strojní Západočeské univerzity v Plzni. Byla sestavena autory s využitím citovaných zdrojů
Termomechanika 5. přednáška Michal Hoznedl Upozornění: Tato prezentace slouží výhradně pro výukové účely Fakulty strojní Západočeské univerzity v Plzni. Byla sestavena autory s využitím citovaných zdrojů
5 Základy termodynamiky
 5 Základy termodynamiky Teplo, teplota, tepelná kapacita, metody jejich měření. Termodynamická soustava a její rovnováha. Hlavní věty termodynamiky. Ideální plyn. Stavová rovnice, Carnotův cyklus. Reálné
5 Základy termodynamiky Teplo, teplota, tepelná kapacita, metody jejich měření. Termodynamická soustava a její rovnováha. Hlavní věty termodynamiky. Ideální plyn. Stavová rovnice, Carnotův cyklus. Reálné
Parní turbíny Rovnotlaký stupe
 Parní turbíny Dominanci parních turbín v energetickém průmyslu vyvolaly provozní a ekonomické výhody,zejména: Menší investiční náklady, hmotnost a obestavěný prostor, vztažený na jednotku výkonu. Možnost
Parní turbíny Dominanci parních turbín v energetickém průmyslu vyvolaly provozní a ekonomické výhody,zejména: Menší investiční náklady, hmotnost a obestavěný prostor, vztažený na jednotku výkonu. Možnost
Chemická kinetika. Reakce 1. řádu rychlost přímo úměrná koncentraci složky
 Chemická kinetika Chemická kinetika Reakce 0. řádu reakční rychlost nezávisí na čase a probíhá konstantní rychlostí v = k (rychlost se rovná rychlostní konstantě) velmi pomalé reakce (prakticky se nemění
Chemická kinetika Chemická kinetika Reakce 0. řádu reakční rychlost nezávisí na čase a probíhá konstantní rychlostí v = k (rychlost se rovná rychlostní konstantě) velmi pomalé reakce (prakticky se nemění
Dynamika proudících plynů
 Dynamika proudících plynů Při výpočtech se budeme zabývat prouděním ideálních plynů. Jejich vlastnosti již byly popsány na předchozích přednáškách/cvičeních. Při proudění ideálního plynu si zavedeme ještě
Dynamika proudících plynů Při výpočtech se budeme zabývat prouděním ideálních plynů. Jejich vlastnosti již byly popsány na předchozích přednáškách/cvičeních. Při proudění ideálního plynu si zavedeme ještě
6. Stavy hmoty - Plyny
 skupenství plynné plyn x pára (pod kritickou teplotou) stavové chování Ideální plyn Reálné plyny Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti skupenství plynné reálný plyn ve stavu
skupenství plynné plyn x pára (pod kritickou teplotou) stavové chování Ideální plyn Reálné plyny Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti skupenství plynné reálný plyn ve stavu
Termodynamika. Děj, který není kvazistatický, se nazývá nestatický.
 Termodynamika Zabývá se ději, při nichž se mění tepelná energie v jiné druhy energie (zejména mechanické). Studuje vlastnosti látek bez přihlédnutí k jejich mikrostruktuře. Je vystavěna na axiomech (0.,
Termodynamika Zabývá se ději, při nichž se mění tepelná energie v jiné druhy energie (zejména mechanické). Studuje vlastnosti látek bez přihlédnutí k jejich mikrostruktuře. Je vystavěna na axiomech (0.,
ČVUT v Praze, Fakulta strojní, Ústav mechaniky tekutin a energetiky. Tomáš Hyhĺık,
 Vyhodnocení kritického tlakového poměru v nadkritické oblasti ve vodní páře Tomáš Hyhĺık ČVUT v Praze, Fakulta strojní, Ústav mechaniky tekutin a energetiky PTSE září 2006 Úvod Uvedená problematika spadá
Vyhodnocení kritického tlakového poměru v nadkritické oblasti ve vodní páře Tomáš Hyhĺık ČVUT v Praze, Fakulta strojní, Ústav mechaniky tekutin a energetiky PTSE září 2006 Úvod Uvedená problematika spadá
Cvičení z termodynamiky a statistické fyziky
 Cvičení termodynamiky a statistické fyiky 1Nechť F(x, y=xe y Spočtěte F/ x, F/, 2 F/ x 2, 2 F/ x, 2 F/ x, 2 F/ x 2 2 Bud dω = A(x, ydx+b(x, ydy libovolná diferenciální forma(pfaffián Ukažte, ževpřípadě,žedωjeúplnýdiferenciál(existujefunkce
Cvičení termodynamiky a statistické fyiky 1Nechť F(x, y=xe y Spočtěte F/ x, F/, 2 F/ x 2, 2 F/ x, 2 F/ x, 2 F/ x 2 2 Bud dω = A(x, ydx+b(x, ydy libovolná diferenciální forma(pfaffián Ukažte, ževpřípadě,žedωjeúplnýdiferenciál(existujefunkce
Termodynamika 2. UJOP Hostivař 2014
 Termodynamika 2 UJOP Hostivař 2014 Skupenské teplo tání/tuhnutí je (celkové) teplo, které přijme pevná látka při přechodu na kapalinu během tání nebo naopak Značka Veličina Lt J Nedochází při něm ke změně
Termodynamika 2 UJOP Hostivař 2014 Skupenské teplo tání/tuhnutí je (celkové) teplo, které přijme pevná látka při přechodu na kapalinu během tání nebo naopak Značka Veličina Lt J Nedochází při něm ke změně
CVIČENÍ 3: VLHKÝ VZDUCH A MOLLIÉRŮV DIAGRAM
 CVIČENÍ 3: VLHKÝ VZDUCH A MOLLIÉRŮV DIAGRAM Co to je vlhký vzduch? - vlhký vzduch je směsí suchého vzduchu a vodní páry okupující společný objem - vodní pára ve směsi může měnit formu z plynné na kapalnou
CVIČENÍ 3: VLHKÝ VZDUCH A MOLLIÉRŮV DIAGRAM Co to je vlhký vzduch? - vlhký vzduch je směsí suchého vzduchu a vodní páry okupující společný objem - vodní pára ve směsi může měnit formu z plynné na kapalnou
TERMOMECHANIKA PRO STUDENTY STROJNÍCH FAKULT prof. Ing. Milan Pavelek, CSc. Brno 2013
 Vysoké učení technické v Brně Fakulta strojního inženýrství, Energetický ústav Odbor termomechaniky a techniky prostředí TERMOMECHANIKA PRO STUDENTY STROJNÍCH FAKULT prof. Ing. Milan Pavelek, CSc. Brno
Vysoké učení technické v Brně Fakulta strojního inženýrství, Energetický ústav Odbor termomechaniky a techniky prostředí TERMOMECHANIKA PRO STUDENTY STROJNÍCH FAKULT prof. Ing. Milan Pavelek, CSc. Brno
Jednotlivým bodům (n,2,a,e,k) z blokového schématu odpovídají body na T-s a h-s diagramu:
 Elektroenergetika 1 (A1B15EN1) 3. cvičení Příklad 1: Rankin-Clausiův cyklus Vypočtěte tepelnou účinnost teoretického Clausius-Rankinova parního oběhu, jsou-li admisní parametry páry tlak p a = 80.10 5
Elektroenergetika 1 (A1B15EN1) 3. cvičení Příklad 1: Rankin-Clausiův cyklus Vypočtěte tepelnou účinnost teoretického Clausius-Rankinova parního oběhu, jsou-li admisní parametry páry tlak p a = 80.10 5
SKUPENSKÉ PŘEMĚNY POJMY K ZOPAKOVÁNÍ. Testové úlohy varianta A
 Škola: Autor: DUM: Vzdělávací obor: Tematický okruh: Téma: Masarykovo gymnázium Vsetín Mgr. Jitka Novosadová MGV_F_SS_3S3_D11_Z_OPAK_T_Skupenske_premeny_T Člověk a příroda Fyzika Skupenské přeměny Opakování
Škola: Autor: DUM: Vzdělávací obor: Tematický okruh: Téma: Masarykovo gymnázium Vsetín Mgr. Jitka Novosadová MGV_F_SS_3S3_D11_Z_OPAK_T_Skupenske_premeny_T Člověk a příroda Fyzika Skupenské přeměny Opakování
1141 HYA (Hydraulika)
 ČVUT v Praze, fakulta stavební katedra hydrauliky a hydrologie (K4) Přednáškové slidy předmětu 4 HYA (Hydraulika) verze: 09/008 K4 Fv ČVUT Tato webová stránka nabízí k nahlédnutí/stažení řadu pdf souborů
ČVUT v Praze, fakulta stavební katedra hydrauliky a hydrologie (K4) Přednáškové slidy předmětu 4 HYA (Hydraulika) verze: 09/008 K4 Fv ČVUT Tato webová stránka nabízí k nahlédnutí/stažení řadu pdf souborů
Rovnováha Tepelná - T všude stejná
 Fázové heterogenní rovnováhy Fáze = homogenní část soustavy, oddělná fyzickým rozhraním, na rozhraní se vlastnosti mění skokem Rovnováha Tepelná - T všude stejná Mechanická - p všude stejný Chemická -
Fázové heterogenní rovnováhy Fáze = homogenní část soustavy, oddělná fyzickým rozhraním, na rozhraní se vlastnosti mění skokem Rovnováha Tepelná - T všude stejná Mechanická - p všude stejný Chemická -
Termomechanika. Doc. Dr. RNDr. Miroslav HOLEČEK
 ermomechanika. přednáška Doc. Dr. RNDr. Miroslav HOLEČEK Upozornění: ato prezentace slouží výhradně pro výukové účely Fakulty strojní Západočeské univerzity v Plzni. Byla sestavena autorem s využitím citovaných
ermomechanika. přednáška Doc. Dr. RNDr. Miroslav HOLEČEK Upozornění: ato prezentace slouží výhradně pro výukové účely Fakulty strojní Západočeské univerzity v Plzni. Byla sestavena autorem s využitím citovaných
Cvičení z NOFY / Termodynamika. 1 Cvičení Totální diferenciál. 1.1 Totální diferenciál Teplota a tlak pro ideální plyn
 Cvičení z NOFY031 2009/2010 1 Termodynamika 1 Cvičení 1.10.2008 Totální diferenciál 1.1 Totální diferenciál 1. Jsou zadány dva výrazy: df 1 (x, y) = 6xy 3 dx + 9x 2 y 2 dy, df 2 (x, y) = 6xy 2 dx + 9x
Cvičení z NOFY031 2009/2010 1 Termodynamika 1 Cvičení 1.10.2008 Totální diferenciál 1.1 Totální diferenciál 1. Jsou zadány dva výrazy: df 1 (x, y) = 6xy 3 dx + 9x 2 y 2 dy, df 2 (x, y) = 6xy 2 dx + 9x
d T FP = fázový přechod (tání, tuhnutí, vypařování, kapalnění, sublimace)
 Fázové rovnováhy jednoložkový ytém Gibbův fázový zákon k f C Popi záviloti tlaku naycených par na teploě Clapeyronova rovnice: d p F P m n e b o F P d l np F P m F P z FP fázový přechod (tání, tuhnutí,
Fázové rovnováhy jednoložkový ytém Gibbův fázový zákon k f C Popi záviloti tlaku naycených par na teploě Clapeyronova rovnice: d p F P m n e b o F P d l np F P m F P z FP fázový přechod (tání, tuhnutí,
Poznámky k semináři z termomechaniky Grafy vody a vodní páry
 Příklad 1 Sytá pára o tlaku 1 [MPa] expanduje izotermicky na tlak 0,1 [MPa]. Znázorněte v diagramech vody a vodní páry. Jelikož se jedná o izotermický děj, je výhodné použít diagram T-s. Dále máme v zadání,
Příklad 1 Sytá pára o tlaku 1 [MPa] expanduje izotermicky na tlak 0,1 [MPa]. Znázorněte v diagramech vody a vodní páry. Jelikož se jedná o izotermický děj, je výhodné použít diagram T-s. Dále máme v zadání,
Jednosložkové soustavy
 Jednosložkové soustavy Fázové rovnováhy Prezentace je určena pro výuku. roč. studjního oboru Nanotechnologí a není dovoleno její šíření bez vědomí garanta předmětu. K jejímu vytvoření bylo použto materálů
Jednosložkové soustavy Fázové rovnováhy Prezentace je určena pro výuku. roč. studjního oboru Nanotechnologí a není dovoleno její šíření bez vědomí garanta předmětu. K jejímu vytvoření bylo použto materálů
F8 - Změny skupenství Číslo variace: 1
 F8 - Změny skupenství Číslo variace: 1 1. K vypařování kapaliny dochází: při každé teplotě v celém jejím objemu pouze při teplotě 100 C v celém objemu kapaliny pouze při normální teplotě a normálním tlaku
F8 - Změny skupenství Číslo variace: 1 1. K vypařování kapaliny dochází: při každé teplotě v celém jejím objemu pouze při teplotě 100 C v celém objemu kapaliny pouze při normální teplotě a normálním tlaku
POZNÁMKA: V USA se používá ještě Fahrenheitova teplotní stupnice. Převodní vztahy jsou vzhledem k volbě základních bodů složitější: 9 5
 TEPLO, TEPLOTA Tepelný stav látek je charakterizován veličinou termodynamická teplota T Jednotkou je kelvin T K Mezi Celsiovou a Kelvinovou teplotní stupnicí existuje převodní vztah T 73,5C t POZNÁMKA:
TEPLO, TEPLOTA Tepelný stav látek je charakterizován veličinou termodynamická teplota T Jednotkou je kelvin T K Mezi Celsiovou a Kelvinovou teplotní stupnicí existuje převodní vztah T 73,5C t POZNÁMKA:
Termodynamika ideálních plynů
 Za správnost neručím, cokoli s jinou než černou barvou je asi špatně Informace jsou primárně z přednášek Termodynamika ideálních plynů 1. Definice uzavřené termodynamické soustavy - neprochází přes ni
Za správnost neručím, cokoli s jinou než černou barvou je asi špatně Informace jsou primárně z přednášek Termodynamika ideálních plynů 1. Definice uzavřené termodynamické soustavy - neprochází přes ni
CVIČENÍ 1 - část 2: MOLLIÉRŮV DIAGRAM A ZMĚNY STAVU VLHKÉHO VZDUCHU
 CVIČENÍ 1 - část 2: MOLLIÉRŮV DIAGRAM A ZMĚNY STAVU VLHKÉHO VZDUCHU Co to je Molliérův diagram? - grafický nástroj pro zpracování izobarických změn stavů vlhkého vzduchu - diagram je sestaven pro konstantní
CVIČENÍ 1 - část 2: MOLLIÉRŮV DIAGRAM A ZMĚNY STAVU VLHKÉHO VZDUCHU Co to je Molliérův diagram? - grafický nástroj pro zpracování izobarických změn stavů vlhkého vzduchu - diagram je sestaven pro konstantní
Parní turbíny Rovnotlaký stupeň
 Parní turbíny Dominanci parních turbín v energetickém průmyslu vyvolaly provozní a ekonomické výhody,zejména: Menší investiční náklady, hmotnost a obestavěný prostor, vztažený na jednotku výkonu. Možnost
Parní turbíny Dominanci parních turbín v energetickém průmyslu vyvolaly provozní a ekonomické výhody,zejména: Menší investiční náklady, hmotnost a obestavěný prostor, vztažený na jednotku výkonu. Možnost
UČIVO. Termodynamická teplota. První termodynamický zákon Přenos vnitřní energie
 PŘEDMĚT: FYZIKA ROČNÍK: SEXTA VÝSTUP UČIVO MEZIPŘEDM. VZTAHY, PRŮŘEZOVÁ TÉMATA, PROJEKTY, KURZY POZNÁMKY Zná 3 základní poznatky kinetické teorie látek a vysvětlí jejich praktický význam Vysvětlí pojmy
PŘEDMĚT: FYZIKA ROČNÍK: SEXTA VÝSTUP UČIVO MEZIPŘEDM. VZTAHY, PRŮŘEZOVÁ TÉMATA, PROJEKTY, KURZY POZNÁMKY Zná 3 základní poznatky kinetické teorie látek a vysvětlí jejich praktický význam Vysvětlí pojmy
Termomechanika 3. přednáška Doc. Dr. RNDr. Miroslav HOLEČEK
 ermomechanika 3. přednáška Doc. Dr. RNDr. Miroslav HOLEČEK Upozornění: ato prezentace slouží výhradně pro výukové účely Fakulty strojní Západočeské univerzity v Plzni. Byla sestavena autorem s využitím
ermomechanika 3. přednáška Doc. Dr. RNDr. Miroslav HOLEČEK Upozornění: ato prezentace slouží výhradně pro výukové účely Fakulty strojní Západočeské univerzity v Plzni. Byla sestavena autorem s využitím
9. Struktura a vlastnosti plynů
 9. Struktura a vlastnosti plynů Osnova: 1. Základní pojmy 2. Střední kvadratická rychlost 3. Střední kinetická energie molekuly plynu 4. Stavová rovnice ideálního plynu 5. Jednoduché děje v plynech a)
9. Struktura a vlastnosti plynů Osnova: 1. Základní pojmy 2. Střední kvadratická rychlost 3. Střední kinetická energie molekuly plynu 4. Stavová rovnice ideálního plynu 5. Jednoduché děje v plynech a)
Termodynamika pro +EE1 a PEE
 ermodynamika ro +EE a PEE Literatura: htt://home.zcu.cz/~nohac/vyuka.htm#ee [0] Zakladni omocny text rednasek Doc. Schejbala [] Pomocne texty ke cviceni [] Prednaska cislo 7 - Zaklady termodynamiky [3]
ermodynamika ro +EE a PEE Literatura: htt://home.zcu.cz/~nohac/vyuka.htm#ee [0] Zakladni omocny text rednasek Doc. Schejbala [] Pomocne texty ke cviceni [] Prednaska cislo 7 - Zaklady termodynamiky [3]
TERMOMECHANIKA 15. Základy přenosu tepla
 FSI VUT v Brně, Energetický ústav Odbor termomechaniky a techniky prostředí Prof. Ing. Milan Pavelek, CSc. TERMOMECHANIKA 15. Základy přenosu tepla OSNOVA 15. KAPITOLY Tři mechanizmy přenosu tepla Tepelný
FSI VUT v Brně, Energetický ústav Odbor termomechaniky a techniky prostředí Prof. Ing. Milan Pavelek, CSc. TERMOMECHANIKA 15. Základy přenosu tepla OSNOVA 15. KAPITOLY Tři mechanizmy přenosu tepla Tepelný
Plyn. 11 plynných prvků. Vzácné plyny. He, Ne, Ar, Kr, Xe, Rn Diatomické plynné prvky H 2, N 2, O 2, F 2, Cl 2
 Plyny Plyn T v, K Vzácné plyny 11 plynných prvků He, Ne, Ar, Kr, Xe, Rn 165 Rn 211 N 2 O 2 77 F 2 90 85 Diatomické plynné prvky Cl 2 238 H 2, N 2, O 2, F 2, Cl 2 H 2 He Ne Ar Kr Xe 20 4.4 27 87 120 1 Plyn
Plyny Plyn T v, K Vzácné plyny 11 plynných prvků He, Ne, Ar, Kr, Xe, Rn 165 Rn 211 N 2 O 2 77 F 2 90 85 Diatomické plynné prvky Cl 2 238 H 2, N 2, O 2, F 2, Cl 2 H 2 He Ne Ar Kr Xe 20 4.4 27 87 120 1 Plyn
Energetika Osnova předmětu 1) Úvod
 Osnova předmětu 1) Úvod 2) Energetika 3) Technologie přeměny 4) Tepelná elektrárna a její hlavní výrobní zařízení 5) Jaderná elektrárna 6) Ostatní tepelné elektrárny 7) Kombinovaná výroba elektřiny a tepla
Osnova předmětu 1) Úvod 2) Energetika 3) Technologie přeměny 4) Tepelná elektrárna a její hlavní výrobní zařízení 5) Jaderná elektrárna 6) Ostatní tepelné elektrárny 7) Kombinovaná výroba elektřiny a tepla
Blokové schéma Clausius-Rankinova (C-R) cyklu s přihříváním páry je na obrázku.
 Příklad 1: Přihřívání páry Teoretický parní oběh s přihříváním páry pracuje s následujícími parametry: Admisní tlak páry p a = 10 MPa a teplota t a = 530 C. Tlak páry po expanzi ve vysokotlaké části turbíny
Příklad 1: Přihřívání páry Teoretický parní oběh s přihříváním páry pracuje s následujícími parametry: Admisní tlak páry p a = 10 MPa a teplota t a = 530 C. Tlak páry po expanzi ve vysokotlaké části turbíny
Parní turbíny a kondenzátory
 Parní turbíny a kondenzátory. přednáška Autor: Jiří Kučera Datum: 3..8 OBSAH Informace o předmětu Parní turbína v tepelném cyklu I. - tepelná a termodynamická účinnost, spotřeby tepla a páry - změny hlavních
Parní turbíny a kondenzátory. přednáška Autor: Jiří Kučera Datum: 3..8 OBSAH Informace o předmětu Parní turbína v tepelném cyklu I. - tepelná a termodynamická účinnost, spotřeby tepla a páry - změny hlavních
Cvičení z termomechaniky Cvičení 7.
 Příklad 1 Vypočítejte účinnost a výkon Humpreyoho spalovacího cyklu bez regenerace, když látkou porovnávacího oběhu je vzduch. Cyklus nakreslete v p-v a T-s diagramu. Dáno: T 1 = 300 [K]; τ = T 1 = 4;
Příklad 1 Vypočítejte účinnost a výkon Humpreyoho spalovacího cyklu bez regenerace, když látkou porovnávacího oběhu je vzduch. Cyklus nakreslete v p-v a T-s diagramu. Dáno: T 1 = 300 [K]; τ = T 1 = 4;
Termodynamika. Martin Keppert. Katedra materiálového inženýrství a chemie
 Termodynamika Martin Keppert Katedra materiálového inženýrství a chemie keppert@fsv.cvut.cz http://tpm.fsv.cvut.cz/ Co to je termodynamika Nauka o energii, jejích formách a přenosu Energie schopnost systému
Termodynamika Martin Keppert Katedra materiálového inženýrství a chemie keppert@fsv.cvut.cz http://tpm.fsv.cvut.cz/ Co to je termodynamika Nauka o energii, jejích formách a přenosu Energie schopnost systému
3.2 Látka a její skupenství
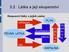 3.2 Látka a její skupenství Skupenství látky a jejich změny sublimace PEVNÁ LÁTKA tání desublimace tuhnutí PLYN vy pa řo vá ní KAPALINA zka pal ňo vá ní Látka a změna vnitřní energie Změna vnitřní energie
3.2 Látka a její skupenství Skupenství látky a jejich změny sublimace PEVNÁ LÁTKA tání desublimace tuhnutí PLYN vy pa řo vá ní KAPALINA zka pal ňo vá ní Látka a změna vnitřní energie Změna vnitřní energie
Termochemie { práce. Práce: W = s F nebo W = F ds. Objemová práce (p vn = vnìj¹í tlak): W = p vn dv. Vratný dìj: p = p vn (ze stavové rovnice) W =
 Termochemie { práce Práce: W = s F nebo W = Objemová práce (p vn = vnìj¹í tlak): W = V2 V 1 p vn dv s2 Vratný dìj: p = p vn (ze stavové rovnice) W = V2 V 1 p dv s 1 F ds s.1 Diferenciální tvar: dw = pdv
Termochemie { práce Práce: W = s F nebo W = Objemová práce (p vn = vnìj¹í tlak): W = V2 V 1 p vn dv s2 Vratný dìj: p = p vn (ze stavové rovnice) W = V2 V 1 p dv s 1 F ds s.1 Diferenciální tvar: dw = pdv
Tepelně vlhkostní mikroklima. Vlhkost v budovách
 Tepelně vlhkostní mikroklima Vlhkost v budovách Zdroje vodní páry stavební vlhkost - vodní pára vázaná v materiálech v důsledku mokrých technologických procesů (chemicky nebo fyzikálně vázaná) zemní vlhkost
Tepelně vlhkostní mikroklima Vlhkost v budovách Zdroje vodní páry stavební vlhkost - vodní pára vázaná v materiálech v důsledku mokrých technologických procesů (chemicky nebo fyzikálně vázaná) zemní vlhkost
Kapaliny Molekulové vdw síly, vodíkové můstky
 Kapaliny Molekulové vdw síly, vodíkové můstky Metalické roztavené kovy, ionty + elektrony, elektrostatické síly Iontové roztavené soli, FLINAK (LiF + NaF + KF), volně pohyblivé anionty a kationty, iontová
Kapaliny Molekulové vdw síly, vodíkové můstky Metalické roztavené kovy, ionty + elektrony, elektrostatické síly Iontové roztavené soli, FLINAK (LiF + NaF + KF), volně pohyblivé anionty a kationty, iontová
Vnitřní energie, teplo a práce
 Přednáška 3 Vnitřní energie, teplo a práce 3.1 Vnitřní energie Pro popis stavu termodynamických soustav je výhodné zavést stavovou funkci, tzv. vnitřní energii soustavy U, která vyjadřuje charakter pohybu
Přednáška 3 Vnitřní energie, teplo a práce 3.1 Vnitřní energie Pro popis stavu termodynamických soustav je výhodné zavést stavovou funkci, tzv. vnitřní energii soustavy U, která vyjadřuje charakter pohybu
Kapaliny Molekulové vdw síly, vodíkové můstky
 Kapaliny Molekulové vdw síly, vodíkové můstky Metalické roztavené kovy, ionty + elektrony, elektrostatické síly Iontové roztavené soli, FLINAK (LiF + NaF + KF), volně pohyblivé anionty a kationty, iontová
Kapaliny Molekulové vdw síly, vodíkové můstky Metalické roztavené kovy, ionty + elektrony, elektrostatické síly Iontové roztavené soli, FLINAK (LiF + NaF + KF), volně pohyblivé anionty a kationty, iontová
IDEÁLNÍ PLYN. Stavová rovnice
 IDEÁLNÍ PLYN Stavová rovnice Ideální plyn ) rozměry molekul jsou zanedbatelné vzhledem k jejich vzdálenostem 2) molekuly plynu na sebe působí jen při vzájemných srážkách 3) všechny srážky jsou dokonale
IDEÁLNÍ PLYN Stavová rovnice Ideální plyn ) rozměry molekul jsou zanedbatelné vzhledem k jejich vzdálenostem 2) molekuly plynu na sebe působí jen při vzájemných srážkách 3) všechny srážky jsou dokonale
Aplikovaná fyzikální chemie. Magda Škvorová KFCH CN463 tel. 3302
 Aplikovaná fyzikální chemie Aplikovaná fyzikální chemie Magda Škvorová KFCH CN463 magda.skvorova@ujep.cz, tel. 3302 1. září 2014 Aplikovaná fyzikální chemie Bylo nebylo... Bylo nebylo... Nejvzácnějšímu
Aplikovaná fyzikální chemie Aplikovaná fyzikální chemie Magda Škvorová KFCH CN463 magda.skvorova@ujep.cz, tel. 3302 1. září 2014 Aplikovaná fyzikální chemie Bylo nebylo... Bylo nebylo... Nejvzácnějšímu
SBÍRKA ŘEŠENÝCH FYZIKÁLNÍCH ÚLOH
 SBÍRKA ŘEŠENÝCH FYZIKÁLNÍCH ÚLOH MECHANIKA MOLEKULOVÁ FYZIKA A TERMIKA ELEKTŘINA A MAGNETISMUS KMITÁNÍ A VLNĚNÍ OPTIKA FYZIKA MIKROSVĚTA TERMODYNAMICKÁ TEPLOTNÍ STUPNICE, TEPLOTA 1) Převeďte hodnoty v
SBÍRKA ŘEŠENÝCH FYZIKÁLNÍCH ÚLOH MECHANIKA MOLEKULOVÁ FYZIKA A TERMIKA ELEKTŘINA A MAGNETISMUS KMITÁNÍ A VLNĚNÍ OPTIKA FYZIKA MIKROSVĚTA TERMODYNAMICKÁ TEPLOTNÍ STUPNICE, TEPLOTA 1) Převeďte hodnoty v
Jiří ŠVEC 1, Pavel ŠVEC 2 OBJEMOVÉ ZMĚNY LÁTEK
 Jiří ŠC, Pavel ŠC 2 OBJMOÉ ZMĚNY LÁTK Abstrakt Předložený článek se zabývá objemovými změnami látek. Jsou diskutovány objemové změny vyvolané vnějšími silami a teplotní délkovou nebo objemovou roztažností,
Jiří ŠC, Pavel ŠC 2 OBJMOÉ ZMĚNY LÁTK Abstrakt Předložený článek se zabývá objemovými změnami látek. Jsou diskutovány objemové změny vyvolané vnějšími silami a teplotní délkovou nebo objemovou roztažností,
Svaz chladící a klimatizační techniky ve spolupráci s firmou Schiessl, s.r.o. Pro certifikaci dle Nařízení 303/2008/EK. 2010-01 Ing.
 Svaz chladící a klimatizační techniky ve spolupráci s firmou Schiessl, s.r.o Diagram chladícího okruhu Pro certifikaci dle Nařízení 303/2008/EK 2010-01 Ing. Jiří Brož Úvod k prezentaci Tato jednoduchá
Svaz chladící a klimatizační techniky ve spolupráci s firmou Schiessl, s.r.o Diagram chladícího okruhu Pro certifikaci dle Nařízení 303/2008/EK 2010-01 Ing. Jiří Brož Úvod k prezentaci Tato jednoduchá
F - Změny skupenství látek
 F - Změny skupenství látek Určeno jako učební text pro studenty dálkového studia a jako shrnující text pro studenty denního studia. VARIACE 1 Tento dokument byl kompletně vytvořen, sestaven a vytištěn
F - Změny skupenství látek Určeno jako učební text pro studenty dálkového studia a jako shrnující text pro studenty denního studia. VARIACE 1 Tento dokument byl kompletně vytvořen, sestaven a vytištěn
LOGO. Změny skupenství
 Změny skupenství Látka existuje ve třech skupenstvích Pevném Kapalném Plynném Látka může přecházet z jednoho skupenství do druhého. Existují tedy tyto změny skupenství: Změny skupenství plyn sublimace
Změny skupenství Látka existuje ve třech skupenstvích Pevném Kapalném Plynném Látka může přecházet z jednoho skupenství do druhého. Existují tedy tyto změny skupenství: Změny skupenství plyn sublimace
