Molekulová mechanika { statický pohled. Základní prvky modelování. (Hyper)plocha potenciální energie. Co je to pohyb? Modelování v chemii: dìlba práce
|
|
|
- Julie Adéla Bláhová
- před 6 lety
- Počet zobrazení:
Transkript
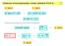
1 Základní prvky modelování? elementární èástice + gravitace: þteorie v¹ehoÿ { temná hmota... (známé) elementární èástice: standardní model { atomová jádra... jádra + elektrony + fotony: QED { pøesná spektroskopie... jádra + elektrony: Schrödingerova rovnice { (praktická) chemie vlastnosti malých molekul, spektra, kinetika, fotochemie... Atomy { klasické molekulové modelování ; kvantová jádra: PI Hrubozrnné (coarse-grained) modely: mezo/nanoskopická ¹kála více atomù = 1 objekt (surfaktant = hlavièka + ocásek, èlánek polymerního øetìzce... ) Mikroskopická ¹kála: disperzní systémy, sypké materiály Materiál jako kontinuum: parciální diferenciální rovnice gravitace: prostoroèas multiscale modeling: QM/MM,... pøíp. pomocná centra / vìt¹í skupiny (-CH3) 1/40 Molekulová { statický pohled 5/40 Energie jako funkce souøadnic (hyperplocha potenciální energie, PES). Aproximujeme funkcí zvanou silové pole (FF). Minimalizace energie (T = 0), þoptimalizace strukturyÿ Renement { zpøesnìní struktury (z rozptylových experimentù) Biochemie: tvar molekul (klíè + zámek), síly (hydrolní/hydrofobní...) Deskriptory pro QSAR (Quantitative Structure{Activity Relationship)... ale co pohyb? (Hyper)plocha potenciální energie [plot/rcoord.sh] 2/40 Jádra jsou mnohem tì¾¹í ne¾ elektrony elektronové pohyby jsou mnohem rychlej¹í (tzv. Bornova{Oppenheimerova aproximace) potential energy surface (PES) energie jako funkce souøadnic poloh v¹ech atomových jader Co je to pohyb? þskuteènýÿ pohyb molekul (tekutiny,... ) v èase Soubor v¹ech mo¾ných kongurací (molekul) zprùmìrovaný v èase: 6/40 E pot ( r 1, r 2,..., r N ) Reakce probíhá cestou nejmen¹ího odporu = pøes sedlový bod (pøesnìji: v jeho blízkosti) = tranzitní stav credits: ucecmst/publications.html, Statistická termodynamika se systematicky zabývá výpoètem velièin (bod varu, anita ligandu k receptoru... ) na základì pøedstavy (makro)stavu systému jako þprùmìruÿ v¹ech mo¾ných kongurací Modelování v chemii: dìlba práce jádra elektrony kvantová kvantová (kvantové simulace) molekulový model makroskopické vlastnosti statistická kinetická teorie simulace 3/40 Molekulové simulace molekulová dynamika (MD) èasový vývoj systému slo¾eného z mnoha molekul pohyb ka¾dého atomu je urèen silami, které na nìj v ka¾dém okam¾iku pùsobí 7/40 metoda Monte Carlo (MC); pøesnìji Metropolisova metoda a varianty posloupnost kongurací systému se generuje pomocí náhodných èísel provedeme náhodný pohyb molekuly a rozhodneme se, zda jej pøijmeme { tak, aby pravdìpodobnosti výskytu kongurací molekul byly stejné jako v realitì kinetické Monte Carlo simulovaný dìj je rozdìlen na elementární události (napø. adsorpce atomu na rostoucím krystalu, reakce na katalyzátoru) událost, ke které dojde, vybíráme podle známé pravdìpodobnosti kvantové simulace { MD, MC Pøed r /40 Co simulujeme 8/40 Kapaliny: vliv struktury na vlastnosti (anomálie vody), roztoky fázové rovnováhy, rozpustnost molekulový model makroskopické vlastnosti statistická kinetická teorie povrchy a rozhraní, surfaktanty Pevné látky: struktura krystalù, materiály (poruchy) adsorpce (zeolity) Biochemie: proteiny, nukleové kyseliny, iontové kanály, lipidické membrány Nanoobjekty: micely, polymery, samoskladba (coarse-grained modely, møí¾ky) Podobnými metodami lze studovat: atd. sypké materiály, rùzné minimalizace (MC), ¹íøení epidemií
2 [uvodsim/blend.sh] Optimalizace struktury (molekulová ) 9/40 [show/janus.sh] Self-assembly (samoskladba) 13/40 skládání molekul pomocí (zpravidla) nekovalentních sil (van der Waals, vodíkové vazby) do strukturovaných celkù Ukázka: dvoufunkèní èástice v roztoku Janus particles Supramolekulární chemie: chair ¾idlièka experiment: 28 kj/mol model: 26 kj/mol Janus Janus Iapetus credit: wikipedie, pages/cassini Ukázka: + ètyøfunkèní èástice twist (skew) boat zkøí¾ená vanièka experiment: 45 kj/mol model: 53 kj/mol credit: Atwood et al., Science 309, 2037 (2005) Pøíklad { elektrosprej Cytochromu C [uvodsim/cytox.sh] 10/40 Yi Mao, J. Woenckhaus, J. Kolafa, M.A. Ratner, M.F. Jarrold Elektrosprej: rozpra¹ování nabitých èástic Mìøí se úèinný prùøez [cd /home/jiri/tex/talks/letniskola; showvid.sh] 14/40 Na10Cl10 rychlé chlazení pomalé chlazení Pøíklad { voda [uvodsim/min.sh] Jak dostat minimum energie 11/40 [uvodsim/salesman.sh 64] Simulované ¾íhání (simulated annealing) 15/40 Hledáme globální minimum funkce (þenergieÿ) s mnoha lokálními minimy Zaèneme nìjakou ¹patnou kon gurací (napø. náhodnou) Navrhneme vhodné zmìny kon gurace Ai Aj Aplikujeme Metropolisovu metodu za sni¾ující se þteplotyÿ T molekul 300 K periodické ve smìrech x,y adhezivní podlo¾ka neadhezivní poklièka Problém obchodního cestujícího (traveling salesman) uvodsim/salesman.sh: 50 mìst náhodnì ve ètverci 1 1 random start Kon gurace = poøadí mìst numerical results in þenergieÿ = délka cesty the console Zmìna kon gurace = zámìna 2 náhodnì zvolených mìst Pøíklad: T = l = 5.37 SIMOLANT [cd uvodsim; simolant -g T.1] Vlastnosti: 2D þatomyÿ (potenciál Lennard-Jonesova typu) odpudivé/pøita¾livé stìny, gravitace MC i MD konstantní energie i termostat Jevy: kondenzace plynu zmrznutí kapky poruchy krystalu kapilární deprese a elevace plyn v gravitaèním poli nukleace Chcete si sami nainstalovat? Staèí Google SIMOLANT... 12/40 T =0 l = 7.93 [../simul/rayleigh/show.sh] (Plateauova-)Rayleighova nestabilita Èúrek vody se rozpadá na kapky. Nestabilita pro kr < 1 (pro poruchu sin(kz)), max. nestabilita pro kr = ln 2. 16/40
3 Nukleace pøi supersonické expanzi [show/supexp.sh] 17/40 Vodní pára o tlaku cca 5 bar se pou¹tí velmi úzkým otvorem pøes trysku do vakua a adiabaticky se ochlazuje pod bod mrazu. Lze tak studovat napø. chem. reakce ve stratosféøe. Otázka: Jaký je tvar, velikost a struktura klastrù ledu? credit: M. Fárník Silové pole 21/40 Molekulový model èi silové pole (force eld) je matematický zápis energie molekuly nebo souboru molekul jako funkce souøadnic atomù, r i, i = 1,..., N. malé: tuhá tìlesa { rotace (voda 25 C: vibruje 0.05 % molekul) velké: mnoho èlenù vazebné síly: vibrace vazeb (1{2): U = K(r r 0 ) 2 lze nahradit pevnou vazbou vibrace úhlù torze (1{4) a torzní potenciál: n K n cos(nφ) \improper torsion" (dr¾í >C=O v rovinì) nevazebné síly (èást. 1{4, 1{dále): Lennard-Jones, náboje A v¹echny pøíspìvky seèteme = aproximace párové aditivity Noo, ideálnì pøesná není, øeknìme na 90 % φ Tání nanoèástic [show/kroupa.sh] 18/40 Molekulová dynamika 22/40 kroupa z 600 molekul vody (led Ih) tuhé koule ap. { nárazy ohøívání þklasickáÿ MD { integrace pohybových rovnic èas simulace = 5 ns Brownovská (stochastická) dynamika { MD + náhodné síly tento model vody taje pøi 250 K nanoèástice taje pøi ni¾¹í teplotì nanokrystal s 489 atomy zlata ohøívání èas simulace 77 ps Teorie, kterou teprve usly¹íte: Síla = gradient (rychlost zmìny) potenciální energie: f i = U( rn ) r i Newtonovy pohybové rovnice: i = 1,..., N d 2 r i dt 2 = f i m i, i = 1,..., N... nepropadejte panice, zkusíme to je¹tì jednodu¹eji Síly mezi molekulami 19/40 Londonovy (disperzní) síly pro vìt¹í vzdálenosti: model uktuující dipól{ {indukovaný dipól elst. pole E 1/r 3 indukovaný dipól µ ind E energie u(r) µe 1/r 6 (v¾dy záporná) Odpuzování na krat¹ích vzdálenostech: u(r) e const r Celkem: u(r) = Ae Br C/r 6 Aproximace odpudivých sil: 2 0 Ar...Ar Ae Br A /r 12 Lennard-Jonesùv potenciál: [ (σ ) 12 ( σ ) ] u(r) = 4ɛ r r r / nm Tyto síly jsou souèástí interakcí mezi v¹emi atomy a molekulami E / (kj mol -1 ) Metoda leap-frog rychlost = dráha (zmìna polohy) za jednotku èasu (h) r(t + h) r(t) v(t + h/2) = h zrychlení = zmìna rychlosti za jednotku èasu a(t) = v(t + h/2) r(t + h) v(t + h/2) v(t h/2) = f h m = v(t h/2) + a(t)h = r(t) + v(t + h/2)h Tahle metoda se skuteènì pou¾ívá! opakujeme s t := t + h 23/40 credit: Elektrické síly 20/40 Pøíklad: dráha planety [uvodsim/verlet.sh] 24/40 náboj{náboj (ionty) U = 1 4πɛ 0 q i q j r ij parciální náboje: takové náboje na atomových jádrech, aby se to chovalo stejnì jako skuteèné nábojové rozlo¾ení dipólový moment polarizovatelnost (el. pole indukuje dipól) WWW verze:
4 Teplota V mechanickém systému se zachovává U + E kin. Ale kde je teplota? 25/40 Teorie, kterou teprve usly¹íte: Ekvipartièní princip Ka¾dý stupeò volnosti odpovídající kvadratické funkci ve výrazu pro celkovou energii (pot.+kin.) pøispívá 1 2 k BT k prùmìrné hodnotì. (k B = R/N A = J K 1 = Boltzmannova konstanta.) Napø. plynný argon má U m = N 3 A2 k B T = 3 2RT, proto¾e ka¾dá slo¾ka rychlosti je kvadratická funkce a celkem jich je v molu 3N A Ve MD simulaci proto teplotu mìøíme: E T = kin 1 2 k = T kin Bf f = 3N f zachování 3N Ale u¾iteènìj¹í je mít konstantní teplotu: pøe¹kálování rychlostí: _ ri,new = _ ri (T/T kin ) 1/2 o nìco lep¹í (Berendsen): _ ri,new = _ ri (T/T kin ) q, q < 1/2 Jsou i lep¹í metody... Okrajové podmínky vakuové, volné (kapka, protein ve vakuu aj.) pevné stìny velké povrchové jevy periodické (to je ale divná baòka!) B D A E C póry, vrstva (slab),... [simolant -N5] 29/40 Monte Carlo integrace (naivní Monte Carlo) [xpi] 26/40 Struktura tekutin { korelaèní funkce 30/40 Pøíklad: Výpoèet èísla π metodou MC INTEGER n celkový poèet bodù INTEGER i INTEGER nu poèet bodù v kruhu REAL x,y souøadnice bodu ve ètverci REAL rnd(-1,1) funkce vracející náhodné èíslo v intervalu ( 1, 1) nu := 0 FOR i := 1 TO n DO x := rnd(-1,1) y := rnd(-1,1) IF x*x+y*y < 1 THEN nu := nu + 1 PRINT "pi=", 4*nu/n plocha ètverce = 4 PRINT "chyba=", 4*sqrt((1-nu/n)*(nu/n)/(n-1)) náhodnì rozmístìné molekuly (ideální plyn) kapalina g(r) = párová korelaèní funkce = radiální distribuèní funkce Boltzmannova pravdìpodobnost 27/40 Struktura tekutin { korelaèní funkce 31/40 Teorie, kterou teprve usly¹íte: Boltzmannova pravdìpodobnost Pravdìpodobnost stavu s energií E je úmìrná Pøíklady: e E/k BT Barometrická rovnice pro tlak ve vý¹ce h: Potenciální energie molekuly je E = hmg, a proto pro tlak (který je úmìrný hustotì) proto¾e R = N A k B a M = N A m. p = p 0 e hmg/k BT = p 0 e hmg/rt Rychlost reakce r (èasto) závisí na teplotì podle vztahu r = r 0 e E A/RT kde E A je molární aktivaèní energie { potøebná pro to, aby reakce mohla zaèít probíhat. Monte Carlo { Metropolisova metoda 28/40 Jak získám strukturu { experiment 32/40 naivní MC importance sampling Zvolíme èástici i, kterou se bude hýbat r zkus i = náhodná poloha vybrané èástice U = U( r zkus i ) U( r i ) { je-li U 0, pohyb pøijmeme v¾dy { je-li U > 0, pohyb pøijmeme s pravdìpodobostí e U/kT odmítneme s pravdìpodobostí 1 e U/kT Mìøím (neutrony, elektrony, rtg.) þstrukturní faktorÿ Opakujeme...
5 Jak získám strukturu? 33/40 Realizace pseudoexperimentu Start: krystal, náhodná kongurace, známá kongurace Zrovnová¾nìní [sleep 3; simul/spce.sh] 37/40 Mìøení vè. odhadu chyb: prùmìrná hodnota velièiny v èase Korelaèní funkce ze strukturního faktoru inverzní Fourierova transformace Teorie, kterou teprve usly¹íte: Fourierova transformace V podstatì to dìlá va¹e ucho, kdy¾ rozeznává tóny 34/40 [start /home/jiri/www/fch/cz/pomucky/kolafa/nacl.avi] Ukázka: þzonální tavbaÿ krystalu NaCl 38/40 pøíprava krystalku Na 108 Cl 108 simulace krystalku za dané teploty a tlaku pøíprava trojnásobného krystalku (hranol) roztavení poloviny krystalku del¹í rozmìr se mù¾e mìnit = konst. tlak simulace v rovnováze: krystal roste: T < T tání krystal taje: T > T tání Argon a voda 35/40 Møí¾kové modely: Isingùv model 39/40 Struktura jednoduché tekutiny (kapalný argon) je organizovaná po slupkách Struktura vody je dána tetraedrickou geometrií vodíkových vazeb Ve vzdálenosti nìkolika molekulových prùmìrù jsou ji¾ molekuly nekorelované { pohybují se nezávisle Jako model feromagnetu: U = J s i s j + h s i, s i { 1, +1} = {, } Jako møí¾kový plyn: U = ɛ n i n j + µ n i, n i {0, 1} = {, } J = interakèní konstanta: ɛ = velikost pøita¾livých sil J > 0: feromagnet, µ = chemický potenciál J < 0: antiferomagnet Ekvivalence: h = intenzita magn. pole n Kritický (Curieùv) bod: h c = i = (1 + s i )/2 0; 2D: T c/j = 2/ ln(1 + 2) Jako model binární slitiny: U = ɛ ki k j + µ ki, k i {, } ɛ,, ɛ,, ɛ, = interakce sousedních atomù µ, µ = chem. pot. atomù Ekviv.: n i = 0 k i = n i = 1 k i =. Molekulový poèítaèový experiment té¾ þpseudoexperimentÿ 36/40 REÁLNÝ EXPERIMENT POÈÍTAÈOVÝ EXPERIMENT Vedení laboratorního deníku Vedení laboratorního deníku Stavba aparatury (z èástí) Stáhni/kup/napi¹ poèítaèový program, slo¾ bloky kódu Nakup chemikálie, syntetizuj, co není ke koupi Pøiprav experiment Proveï experiment, pozornì sleduj, co se dìje Analyzuj a poèítej Ukliï laboratoø Stáhni silové pole, natuj parametry, které nejsou dostupné Pøiprav poèáteèní konguraci ap. Spus» program, sleduj èasovou závislost velièin vè. kontrolních Stanov støední hodnoty (s odhady chyb) Zapi¹ zálohy, vyma¾ nepotøebné soubory Isingùv model rychle ochlazená slitina: kritický (Curieùv) bod: [tchem/showisi.sh] 40/40
Základní prvky modelování ve fyzice a chemii
 Základní prvky modelování ve fyzice a chemii 1/40? elementární èástice + gravitace: þteorie v¹ehoÿ { temná hmota... (známé) elementární èástice: standardní model { atomová jádra... jádra + elektrony +
Základní prvky modelování ve fyzice a chemii 1/40? elementární èástice + gravitace: þteorie v¹ehoÿ { temná hmota... (známé) elementární èástice: standardní model { atomová jádra... jádra + elektrony +
Základní prvky modelování
 Základní prvky modelování? elementární èástice + gravitace: þteorie v¹ehoÿ { temná hmota... (známé) elementární èástice: standardní model { atomová jádra... jádra + elektrony + fotony: QED { pøesná spektroskopie...
Základní prvky modelování? elementární èástice + gravitace: þteorie v¹ehoÿ { temná hmota... (známé) elementární èástice: standardní model { atomová jádra... jádra + elektrony + fotony: QED { pøesná spektroskopie...
Molekulární modelování a simulace
 Molekulární modelování a simulace 1/23 Evropský sociální fond þpraha & EU: Investujeme do va¹í budoucnostiÿ Inovace pøedmìtu Poèítaèová chemie je podporována projektem CHEMnote (Inovace bakaláøského studijního
Molekulární modelování a simulace 1/23 Evropský sociální fond þpraha & EU: Investujeme do va¹í budoucnostiÿ Inovace pøedmìtu Poèítaèová chemie je podporována projektem CHEMnote (Inovace bakaláøského studijního
Základní prvky modelování
 Základní prvky modelování? elementární èástice + gravitace: þteorie v¹ehoÿ { temná hmota... (známé) elementární èástice: standardní model { atomová jádra... jádra + elektrony + fotony: QED { pøesná spektroskopie...
Základní prvky modelování? elementární èástice + gravitace: þteorie v¹ehoÿ { temná hmota... (známé) elementární èástice: standardní model { atomová jádra... jádra + elektrony + fotony: QED { pøesná spektroskopie...
Základní prvky modelování. Pøed r (Hyper)plocha potenciální energie. Molekulová mechanika { statický pohled. Co je to pohyb? Jak získám PES?
 Základní prvky modelování 1/44 Pøed r. 1930 5/44? elementární èástice + gravitace: þteorie v¹ehoÿ { temná hmota... (známé) elementární èástice: standardní model { atomová jádra... jádra + elektrony + fotony:
Základní prvky modelování 1/44 Pøed r. 1930 5/44? elementární èástice + gravitace: þteorie v¹ehoÿ { temná hmota... (známé) elementární èástice: standardní model { atomová jádra... jádra + elektrony + fotony:
Molekulární modelování a simulace
 Molekulární modelování a simulace 1/35 Evropský sociální fond þpraha & EU: Investujeme do va¹í budoucnostiÿ Inovace pøedmìtu Poèítaèová chemie je podporována projektem CHEMnote (Inovace bakaláøského studijního
Molekulární modelování a simulace 1/35 Evropský sociální fond þpraha & EU: Investujeme do va¹í budoucnostiÿ Inovace pøedmìtu Poèítaèová chemie je podporována projektem CHEMnote (Inovace bakaláøského studijního
Úvodní info. Ústav fyzikální chemie VŠCHT Praha, budova A, místnost 325 (zadním vchodem)
 Úvodní info [mozilla file:/home/jiri/www/fch/cz/talks/mgr.html] 1/20 Jiří Kolafa Ústav fyzikální chemie VŠCHT Praha, budova A, místnost 325 (zadním vchodem) http://www.mapy.cz/s/98vc jiri.kolafa@vscht.cz
Úvodní info [mozilla file:/home/jiri/www/fch/cz/talks/mgr.html] 1/20 Jiří Kolafa Ústav fyzikální chemie VŠCHT Praha, budova A, místnost 325 (zadním vchodem) http://www.mapy.cz/s/98vc jiri.kolafa@vscht.cz
Co je to pohyb? Molekulové simulace. Pøíklad { elektrosprej Cytochromu C. Co simulujeme. Pøíklad { voda SIMOLANT
 Molekulární modelování a simulace Evropský sociální fond þpraha & EU: Investujeme do va¹í budoucnostiÿ /35 Inovace pøedmìtu Poèítaèová chemie je podporována projektem CHEMnote (Inovace bakaláøského studijního
Molekulární modelování a simulace Evropský sociální fond þpraha & EU: Investujeme do va¹í budoucnostiÿ /35 Inovace pøedmìtu Poèítaèová chemie je podporována projektem CHEMnote (Inovace bakaláøského studijního
Potenciální energie atom{atom
 Potenciální energie atom{atom 1/16 Londonovy (disperzní) síly: na del¹ích vzdálenostech, v¾dy pøita¾livé Model uktuující dipól { uktuující dipól elst. pole E 1/r 3 indukovaný dipól µ ind E energie u(r)
Potenciální energie atom{atom 1/16 Londonovy (disperzní) síly: na del¹ích vzdálenostech, v¾dy pøita¾livé Model uktuující dipól { uktuující dipól elst. pole E 1/r 3 indukovaný dipól µ ind E energie u(r)
Monte Carlo, analýza výsledkù simulací
 Monte Carlo, analýza výsledkù simulací 1/26 Evropský sociální fond þpraha & EU: Investujeme do va¹í budoucnostiÿ Inovace pøedmìtu Poèítaèová chemie je podporována projektem CHEMnote (Inovace bakaláøského
Monte Carlo, analýza výsledkù simulací 1/26 Evropský sociální fond þpraha & EU: Investujeme do va¹í budoucnostiÿ Inovace pøedmìtu Poèítaèová chemie je podporována projektem CHEMnote (Inovace bakaláøského
Stanislav Labík. Ústav fyzikální chemie V CHT Praha budova A, 3. patro u zadního vchodu, místnost
 Stanislav Labík Ústav fyzikální chemie V CHT Praha budova A, 3. patro u zadního vchodu, místnost 325 labik@vscht.cz 220 444 257 http://www.vscht.cz/fch/ Výuka Letní semestr N403032 Základy fyzikální chemie
Stanislav Labík Ústav fyzikální chemie V CHT Praha budova A, 3. patro u zadního vchodu, místnost 325 labik@vscht.cz 220 444 257 http://www.vscht.cz/fch/ Výuka Letní semestr N403032 Základy fyzikální chemie
Nekovalentní interakce
 Nekovalentní interakce Jan Řezáč UOCHB AV ČR 31. října 2017 Jan Řezáč (UOCHB AV ČR) Nekovalentní interakce 31. října 2017 1 / 28 Osnova 1 Teorie 2 Typy nekovalentních interakcí 3 Projevy v chemii 4 Výpočty
Nekovalentní interakce Jan Řezáč UOCHB AV ČR 31. října 2017 Jan Řezáč (UOCHB AV ČR) Nekovalentní interakce 31. října 2017 1 / 28 Osnova 1 Teorie 2 Typy nekovalentních interakcí 3 Projevy v chemii 4 Výpočty
Skupenské stavy. Kapalina Částečně neuspořádané Volný pohyb částic nebo skupin částic Částice blíže u sebe
 Skupenské stavy Plyn Zcela neuspořádané Hodně volného prostoru Zcela volný pohyb částic Částice daleko od sebe Kapalina Částečně neuspořádané Volný pohyb částic nebo skupin částic Částice blíže u sebe
Skupenské stavy Plyn Zcela neuspořádané Hodně volného prostoru Zcela volný pohyb částic Částice daleko od sebe Kapalina Částečně neuspořádané Volný pohyb částic nebo skupin částic Částice blíže u sebe
Nekovalentní interakce
 Nekovalentní interakce Jan Řezáč UOCHB AV ČR 3. listopadu 2016 Jan Řezáč (UOCHB AV ČR) Nekovalentní interakce 3. listopadu 2016 1 / 28 Osnova 1 Teorie 2 Typy nekovalentních interakcí 3 Projevy v chemii
Nekovalentní interakce Jan Řezáč UOCHB AV ČR 3. listopadu 2016 Jan Řezáč (UOCHB AV ČR) Nekovalentní interakce 3. listopadu 2016 1 / 28 Osnova 1 Teorie 2 Typy nekovalentních interakcí 3 Projevy v chemii
Skupenské stavy látek. Mezimolekulární síly
 Skupenské stavy látek Mezimolekulární síly 1 Interakce iont-dipól Např. hydratační (solvatační) interakce mezi Na + (iont) a molekulou vody (dipól). Jde o nejsilnější mezimolekulární (nevazebnou) interakci.
Skupenské stavy látek Mezimolekulární síly 1 Interakce iont-dipól Např. hydratační (solvatační) interakce mezi Na + (iont) a molekulou vody (dipól). Jde o nejsilnější mezimolekulární (nevazebnou) interakci.
Viriálová stavová rovnice 1 + s.1
 Viriálová stavová rovnice 1 + s.1 (Mírnì nestandardní odvození Prùmìrná energie molekul okolo vybrané molekuly (β = 1/(k B T : 0 u(r e βu(r 4πr 2 dr Energie souboru N molekul: U = f 2 k B T + N 2 2V Tlak
Viriálová stavová rovnice 1 + s.1 (Mírnì nestandardní odvození Prùmìrná energie molekul okolo vybrané molekuly (β = 1/(k B T : 0 u(r e βu(r 4πr 2 dr Energie souboru N molekul: U = f 2 k B T + N 2 2V Tlak
Klasická termodynamika (aneb pøehled FCH I)
 Klasická termodynamika (aneb pøehled FCH I) 1/16 0. zákon 1. zákon id. plyn: pv = nrt pv κ = konst (id., ad.) id. plyn: U = U(T) }{{} Carnotùv cyklus dq T = 0 2. zákon rg, K,... lim S = 0 T 0 S, ds = dq
Klasická termodynamika (aneb pøehled FCH I) 1/16 0. zákon 1. zákon id. plyn: pv = nrt pv κ = konst (id., ad.) id. plyn: U = U(T) }{{} Carnotùv cyklus dq T = 0 2. zákon rg, K,... lim S = 0 T 0 S, ds = dq
Fyzika IV Dynamika jader v molekulách
 Dynamika jader v molekulách vibrace rotace Dynamika jader v molekulách rotační energetické hladiny (dvouatomová molekula) moment setrvačnosti kolem osy procházející těžištěm osa těžiště m2 m1 r2 r1 R moment
Dynamika jader v molekulách vibrace rotace Dynamika jader v molekulách rotační energetické hladiny (dvouatomová molekula) moment setrvačnosti kolem osy procházející těžištěm osa těžiště m2 m1 r2 r1 R moment
Molekulový počítačový experiment
 Molekulový počítačový experiment 1/16 též pseudoexperiment REÁLNÝ EXPERIMENT Vedení laboratorního deníku POČÍTAČOVÝ EXPERIMENT Vedení laboratorního deníku Zvol metodu (přístroj, protokol) Zvol metody (MD,
Molekulový počítačový experiment 1/16 též pseudoexperiment REÁLNÝ EXPERIMENT Vedení laboratorního deníku POČÍTAČOVÝ EXPERIMENT Vedení laboratorního deníku Zvol metodu (přístroj, protokol) Zvol metody (MD,
Opakování
 Slabé vazebné interakce Opakování Co je to atom? Opakování Opakování Co je to atom? Atom je nejmenší částice hmoty, chemicky dále nedělitelná. Skládá se z atomového jádra obsahujícího protony a neutrony
Slabé vazebné interakce Opakování Co je to atom? Opakování Opakování Co je to atom? Atom je nejmenší částice hmoty, chemicky dále nedělitelná. Skládá se z atomového jádra obsahujícího protony a neutrony
Elementární reakce. stechiometrický zápis vystihuje mechanismus (Cl. + H 2 HCl + H. ) 2 NO 2 ; radioak-
 Elementární reakce 1/15 stechiometrický zápis vystihuje mechanismus (Cl. + H 2 HCl + H. ) 2 NO 2 ; radioak- reakce monomolekulární (rozpad molekuly: N 2 O 4 tivní rozpad; izomerizace) reakce bimolekulární
Elementární reakce 1/15 stechiometrický zápis vystihuje mechanismus (Cl. + H 2 HCl + H. ) 2 NO 2 ; radioak- reakce monomolekulární (rozpad molekuly: N 2 O 4 tivní rozpad; izomerizace) reakce bimolekulární
Fázová rozhraní a mezifázová energie
 Fázová rozhraní a mezifázová energie druhy: l/g l/l }{{} mobilní s/g s/l s/s 1/14 Pøíklad. Kolik % molekul vody je na povrchu kapièky mlhy o prùmìru a) 0.1 mm (hranice viditelnosti okem) b) 200 nm (hranice
Fázová rozhraní a mezifázová energie druhy: l/g l/l }{{} mobilní s/g s/l s/s 1/14 Pøíklad. Kolik % molekul vody je na povrchu kapièky mlhy o prùmìru a) 0.1 mm (hranice viditelnosti okem) b) 200 nm (hranice
Vazby v pevných látkách
 Vazby v pevných látkách Hlavní body 1. Tvorba pevných látek 2. Van der Waalsova vazba elektrostatická interakce indukovaných dipólů 3. Iontová vazba elektrostatická interakce iontů 4. Kovalentní vazba
Vazby v pevných látkách Hlavní body 1. Tvorba pevných látek 2. Van der Waalsova vazba elektrostatická interakce indukovaných dipólů 3. Iontová vazba elektrostatická interakce iontů 4. Kovalentní vazba
Rovnováha kapalina{pára u binárních systémù
 Rovnováha kapalina{pára u binárních systémù 1 Pøedpoklad: 1 kapalná fáze Oznaèení: molární zlomky v kapalné fázi: x i molární zlomky v plynné fázi: y i Poèet stupòù volnosti: v = k f + 2 = 2 stav smìsi
Rovnováha kapalina{pára u binárních systémù 1 Pøedpoklad: 1 kapalná fáze Oznaèení: molární zlomky v kapalné fázi: x i molární zlomky v plynné fázi: y i Poèet stupòù volnosti: v = k f + 2 = 2 stav smìsi
Kapitoly z fyzikální chemie KFC/KFCH. I. Základní pojmy FCH a kinetická teorie plynů
 Kapitoly z fyzikální chemie KFC/KFCH I. Základní pojmy FCH a kinetická teorie plynů RNDr. Karel Berka, Ph.D. Univerzita Palackého v Olomouci Zkouška a doporučená literatura Ústní kolokvium Doporučená literatura
Kapitoly z fyzikální chemie KFC/KFCH I. Základní pojmy FCH a kinetická teorie plynů RNDr. Karel Berka, Ph.D. Univerzita Palackého v Olomouci Zkouška a doporučená literatura Ústní kolokvium Doporučená literatura
Od kvantové mechaniky k chemii
 Od kvantové mechaniky k chemii Jan Řezáč UOCHB AV ČR 19. září 2017 Jan Řezáč (UOCHB AV ČR) Od kvantové mechaniky k chemii 19. září 2017 1 / 33 Úvod Vztah mezi molekulovou strukturou a makroskopickými vlastnostmi
Od kvantové mechaniky k chemii Jan Řezáč UOCHB AV ČR 19. září 2017 Jan Řezáč (UOCHB AV ČR) Od kvantové mechaniky k chemii 19. září 2017 1 / 33 Úvod Vztah mezi molekulovou strukturou a makroskopickými vlastnostmi
Termochemie { práce. Práce: W = s F nebo W = F ds. Objemová práce (p vn = vnìj¹í tlak): W = p vn dv. Vratný dìj: p = p vn (ze stavové rovnice) W =
 Termochemie { práce Práce: W = s F nebo W = Objemová práce (p vn = vnìj¹í tlak): W = V2 V 1 p vn dv s2 Vratný dìj: p = p vn (ze stavové rovnice) W = V2 V 1 p dv s 1 F ds s.1 Diferenciální tvar: dw = pdv
Termochemie { práce Práce: W = s F nebo W = Objemová práce (p vn = vnìj¹í tlak): W = V2 V 1 p vn dv s2 Vratný dìj: p = p vn (ze stavové rovnice) W = V2 V 1 p dv s 1 F ds s.1 Diferenciální tvar: dw = pdv
Mezimolekulové interakce
 Mezimolekulové interakce Interakce molekul reaktivně vzniká či zaniká kovalentní vazba překryv elektronových oblaků, mění se vlastnosti nereaktivně vznikají molekulové komplexy slabá, nekovalentní, nechemická,
Mezimolekulové interakce Interakce molekul reaktivně vzniká či zaniká kovalentní vazba překryv elektronových oblaků, mění se vlastnosti nereaktivně vznikají molekulové komplexy slabá, nekovalentní, nechemická,
Chemická vazba. John Dalton Amadeo Avogadro
 Chemická vazba John Dalton 1766-1844 Amadeo Avogadro 1776-1856 Výpočet molekuly 2, metoda valenční vazby Walter eitler 1904-1981 Fritz W. London 1900-1954 Teorie molekulových orbitalů Friedrich und 1896-1997
Chemická vazba John Dalton 1766-1844 Amadeo Avogadro 1776-1856 Výpočet molekuly 2, metoda valenční vazby Walter eitler 1904-1981 Fritz W. London 1900-1954 Teorie molekulových orbitalů Friedrich und 1896-1997
Neideální plyny. Z e dr dr dr. Integrace přes hybnosti. Neideální chování
 eideální plyny b H Q(, V, T )... e dp 3... dpdr... dr! h Integrace přes hybnosti QVT (,, ) pmkt! h 3 / e dr dr dr /... U kt... eideální chování p kt r B ( T) r B ( T) r 3 3 Vyšší koeficinety velice složité
eideální plyny b H Q(, V, T )... e dp 3... dpdr... dr! h Integrace přes hybnosti QVT (,, ) pmkt! h 3 / e dr dr dr /... U kt... eideální chování p kt r B ( T) r B ( T) r 3 3 Vyšší koeficinety velice složité
Fyzikální chemie. Magda Škvorová KFCH CN463 magda.skvorova@ujep.cz, tel. 3302. 14. února 2013
 Fyzikální chemie Magda Škvorová KFCH CN463 magda.skvorova@ujep.cz, tel. 3302 14. února 2013 Co je fyzikální chemie? Co je fyzikální chemie? makroskopický přístup: (klasická) termodynamika nerovnovážná
Fyzikální chemie Magda Škvorová KFCH CN463 magda.skvorova@ujep.cz, tel. 3302 14. února 2013 Co je fyzikální chemie? Co je fyzikální chemie? makroskopický přístup: (klasická) termodynamika nerovnovážná
Opakování: Standardní stav þ ÿ
 Opakování: Standardní stav þ ÿ s.1 12. øíjna 215 Standardní stav þ ÿ = èistá slo¾ka ve stavu ideálního plynu za teploty soustavy T a standardního tlaku = 1 kpa, døíve 11,325 kpa. Èistá látka: Pøibli¾nì:
Opakování: Standardní stav þ ÿ s.1 12. øíjna 215 Standardní stav þ ÿ = èistá slo¾ka ve stavu ideálního plynu za teploty soustavy T a standardního tlaku = 1 kpa, døíve 11,325 kpa. Èistá látka: Pøibli¾nì:
John Dalton Amadeo Avogadro
 Spojením atomů vznikají molekuly... John Dalton 1766 1844 Amadeo Avogadro 1776 1856 Výpočet molekuly 2, metoda valenční vazby Walter eitler 1904 1981 Fritz W. London 1900 1954 Teorie molekulových orbitalů
Spojením atomů vznikají molekuly... John Dalton 1766 1844 Amadeo Avogadro 1776 1856 Výpočet molekuly 2, metoda valenční vazby Walter eitler 1904 1981 Fritz W. London 1900 1954 Teorie molekulových orbitalů
Plyn. 11 plynných prvků. Vzácné plyny. He, Ne, Ar, Kr, Xe, Rn Diatomické plynné prvky H 2, N 2, O 2, F 2, Cl 2
 Plyny Plyn T v, K Vzácné plyny 11 plynných prvků He, Ne, Ar, Kr, Xe, Rn 165 Rn 211 N 2 O 2 77 F 2 90 85 Diatomické plynné prvky Cl 2 238 H 2, N 2, O 2, F 2, Cl 2 H 2 He Ne Ar Kr Xe 20 4.4 27 87 120 1 Plyn
Plyny Plyn T v, K Vzácné plyny 11 plynných prvků He, Ne, Ar, Kr, Xe, Rn 165 Rn 211 N 2 O 2 77 F 2 90 85 Diatomické plynné prvky Cl 2 238 H 2, N 2, O 2, F 2, Cl 2 H 2 He Ne Ar Kr Xe 20 4.4 27 87 120 1 Plyn
Brownovská (stochastická) dynamika, disipativní èásticová dynamika = MD + náhodné síly. i = 1,..., N. r i. U = i<j. u(r ij ) du(r ji ) r ji
 Molekulová dynamika Síly: tuhé koule ap. { nárazy þklasickáÿ MD { integrace pohybových rovnic 1/20 Brownovská (stochastická) dynamika, disipativní èásticová dynamika = MD + náhodné síly Pøíklad: f i =
Molekulová dynamika Síly: tuhé koule ap. { nárazy þklasickáÿ MD { integrace pohybových rovnic 1/20 Brownovská (stochastická) dynamika, disipativní èásticová dynamika = MD + náhodné síly Pøíklad: f i =
Statistická termodynamika (mechanika)
 Statistická termodynamika (mechanika) 1/18 Makroskopické velièiny jsou výsledkem zprùmìrovaného chování mnoha èástic Tlak ideálního plynu z kinetické teorie 1 [simolant -I0] 2/18 Molekula = hmotný bod
Statistická termodynamika (mechanika) 1/18 Makroskopické velièiny jsou výsledkem zprùmìrovaného chování mnoha èástic Tlak ideálního plynu z kinetické teorie 1 [simolant -I0] 2/18 Molekula = hmotný bod
02 Nevazebné interakce
 02 Nevazebné interakce Nevazebné interakce Druh chemické vazby Určují 3D konfiguraci makromolekul, účastní se mnoha biologických procesů, zodpovědné za uspořádání molekul v krystalu Síla nevazebných interakcí
02 Nevazebné interakce Nevazebné interakce Druh chemické vazby Určují 3D konfiguraci makromolekul, účastní se mnoha biologických procesů, zodpovědné za uspořádání molekul v krystalu Síla nevazebných interakcí
Statistická termodynamika (mechanika)
 Statistická termodynamika (mechanika) 1/16 Makroskopické velièiny jsou výsledkem zprùmìrovaného chování mnoha èástic Tlak ideálního plynu z kinetické teorie 1 [tchem/simplyn.sh] 2/16 Molekula = hmotný
Statistická termodynamika (mechanika) 1/16 Makroskopické velièiny jsou výsledkem zprùmìrovaného chování mnoha èástic Tlak ideálního plynu z kinetické teorie 1 [tchem/simplyn.sh] 2/16 Molekula = hmotný
Molekulární dynamika vody a alkoholů
 Molekulární dynamika vody a alkoholů Pavel Petrus Katedra fyziky, Univerzita J. E. Purkyně, Ústí nad Labem 10. týden 22.4.2010 Modely vody SPC SPC/E TIP4P TIP5P Modely alkoholů OPLS TraPPE Radiální distribuční
Molekulární dynamika vody a alkoholů Pavel Petrus Katedra fyziky, Univerzita J. E. Purkyně, Ústí nad Labem 10. týden 22.4.2010 Modely vody SPC SPC/E TIP4P TIP5P Modely alkoholů OPLS TraPPE Radiální distribuční
Studium enzymatické reakce metodami výpočetní chemie
 Studium enzymatické reakce metodami výpočetní chemie 2. kolo Petr Kulhánek, Zora Střelcová kulhanek@chemi.muni.cz CEITEC - Středoevropský technologický institut Masarykova univerzita, Kamenice 5, 625 00
Studium enzymatické reakce metodami výpočetní chemie 2. kolo Petr Kulhánek, Zora Střelcová kulhanek@chemi.muni.cz CEITEC - Středoevropský technologický institut Masarykova univerzita, Kamenice 5, 625 00
Úvod do molekulové dynamiky simulace proteinů. Eva Fadrná evaf@chemi.muni.cz
 Úvod do molekulové dynamiky simulace proteinů Eva Fadrná evaf@chemi.muni.cz Molekulová mechanika = metoda silového pole = force field Energie vypočtená řešením Schrodingerovy rovnice Energie vypočtená
Úvod do molekulové dynamiky simulace proteinů Eva Fadrná evaf@chemi.muni.cz Molekulová mechanika = metoda silového pole = force field Energie vypočtená řešením Schrodingerovy rovnice Energie vypočtená
Plyn. 11 plynných prvků. Vzácné plyny. He, Ne, Ar, Kr, Xe, Rn Diatomické plynné prvky H 2, N 2, O 2, F 2, Cl 2
 Plyny Plyn T v, K Vzácné plyny 11 plynných prvků He, Ne, Ar, Kr, Xe, Rn 165 Rn 211 N 2 O 2 77 F 2 90 85 Diatomické plynné prvky Cl 2 238 H 2, N 2, O 2, F 2, Cl 2 H 2 He Ne Ar Kr Xe 20 4.4 27 87 120 1 Plyn
Plyny Plyn T v, K Vzácné plyny 11 plynných prvků He, Ne, Ar, Kr, Xe, Rn 165 Rn 211 N 2 O 2 77 F 2 90 85 Diatomické plynné prvky Cl 2 238 H 2, N 2, O 2, F 2, Cl 2 H 2 He Ne Ar Kr Xe 20 4.4 27 87 120 1 Plyn
Mgr. Jakub Janíček VY_32_INOVACE_Ch1r0118
 Chemická vazba Mgr. Jakub Janíček VY_32_INOVACE_Ch1r0118 Chemická vazba Většina atomů má tendenci se spojovat do větších celků (molekul), v nichž jsou vzájemně vázané chemickou vazbou. Chemická vazba je
Chemická vazba Mgr. Jakub Janíček VY_32_INOVACE_Ch1r0118 Chemická vazba Většina atomů má tendenci se spojovat do větších celků (molekul), v nichž jsou vzájemně vázané chemickou vazbou. Chemická vazba je
Počítačová chemie. výpočetně náročné simulace chemických a biomolekulárních systémů. Zora Střelcová
 Počítačová chemie výpočetně náročné simulace chemických a biomolekulárních systémů Zora Střelcová Národní centrum pro výzkum biomolekul, Masarykova univerzita, Kotlářská 2, 611 37 Brno, Česká Republika
Počítačová chemie výpočetně náročné simulace chemických a biomolekulárních systémů Zora Střelcová Národní centrum pro výzkum biomolekul, Masarykova univerzita, Kotlářská 2, 611 37 Brno, Česká Republika
Plyn. 11 plynných prvků. Vzácné plyny He, Ne, Ar, Kr, Xe, Rn Diatomické plynné prvky H 2, N 2, O 2, F 2, Cl 2
 Plyny Plyn T v, K 11 plynných prvků Vzácné plyny He, Ne, Ar, Kr, Xe, Rn Diatomické plynné prvky H 2, N 2, O 2, F 2, Cl 2 H 2 20 He 4.4 Ne 27 Ar 87 Kr 120 Xe 165 Rn 211 N 2 77 O 2 90 F 2 85 Cl 2 238 1 Plyn
Plyny Plyn T v, K 11 plynných prvků Vzácné plyny He, Ne, Ar, Kr, Xe, Rn Diatomické plynné prvky H 2, N 2, O 2, F 2, Cl 2 H 2 20 He 4.4 Ne 27 Ar 87 Kr 120 Xe 165 Rn 211 N 2 77 O 2 90 F 2 85 Cl 2 238 1 Plyn
Exponenciální rozdìlení
 Exponenciální rozdìlení Ing. Michael Rost, Ph. D. Jihoèeská univerzita v Èeských Budìjovicích Katedra aplikované matematiky a informatiky Exponenciální rozdìlení Exp(A, λ) "Rozdìlení bez pamìti" Exponenciální
Exponenciální rozdìlení Ing. Michael Rost, Ph. D. Jihoèeská univerzita v Èeských Budìjovicích Katedra aplikované matematiky a informatiky Exponenciální rozdìlení Exp(A, λ) "Rozdìlení bez pamìti" Exponenciální
Struktura atomů a molekul
 Struktura atomů a molekul Obrazová příloha Michal Otyepka tento text byl vysázen systémem L A TEX2 ε ii Úvod Dokument obsahuje všechny obrázky tak, jak jsou uvedeny ve druhém vydání skript Struktura atomů
Struktura atomů a molekul Obrazová příloha Michal Otyepka tento text byl vysázen systémem L A TEX2 ε ii Úvod Dokument obsahuje všechny obrázky tak, jak jsou uvedeny ve druhém vydání skript Struktura atomů
Kapaliny Molekulové vdw síly, vodíkové můstky
 Kapaliny Molekulové vdw síly, vodíkové můstky Metalické roztavené kovy, ionty + elektrony, elektrostatické síly Iontové roztavené soli, FLINAK (LiF + NaF + KF), volně pohyblivé anionty a kationty, iontová
Kapaliny Molekulové vdw síly, vodíkové můstky Metalické roztavené kovy, ionty + elektrony, elektrostatické síly Iontové roztavené soli, FLINAK (LiF + NaF + KF), volně pohyblivé anionty a kationty, iontová
Chemie povrchů verze 2013
 Chemie povrchů verze 2013 Definice povrchu složitá, protože v nanoměřítku (na úrovni velikosti atomů) je elektronový obal atomů difúzní většinou definován fyzikální adsorpcí nereaktivních plynů Vlastnosti
Chemie povrchů verze 2013 Definice povrchu složitá, protože v nanoměřítku (na úrovni velikosti atomů) je elektronový obal atomů difúzní většinou definován fyzikální adsorpcí nereaktivních plynů Vlastnosti
Statistická termodynamika (mechanika) Makroskopické velièiny jsou výsledkem zprùmìrovaného chování mnoha èástic
 Statistická termodynamika (mechanika) 1/23 Makroskopické velièiny jsou výsledkem zprùmìrovaného chování mnoha èástic Tlak ideálního plynu z kinetické teorie 1 [simolant -I0] 2/23 Molekula = hmotný bod
Statistická termodynamika (mechanika) 1/23 Makroskopické velièiny jsou výsledkem zprùmìrovaného chování mnoha èástic Tlak ideálního plynu z kinetické teorie 1 [simolant -I0] 2/23 Molekula = hmotný bod
Tepelná vodivost. střední rychlost. T 1 > T 2 z. teplo přenesené za čas dt: T 1 T 2. tepelný tok střední volná dráha. součinitel tepelné vodivosti
 Tepelná vodivost teplo přenesené za čas dt: T 1 > T z T 1 S tepelný tok střední volná dráha T součinitel tepelné vodivosti střední rychlost Tepelná vodivost součinitel tepelné vodivosti při T = 300 K součinitel
Tepelná vodivost teplo přenesené za čas dt: T 1 > T z T 1 S tepelný tok střední volná dráha T součinitel tepelné vodivosti střední rychlost Tepelná vodivost součinitel tepelné vodivosti při T = 300 K součinitel
6. Stavy hmoty - Plyny
 skupenství plynné plyn x pára (pod kritickou teplotou) stavové chování Ideální plyn Reálné plyny Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti skupenství plynné reálný plyn ve stavu
skupenství plynné plyn x pára (pod kritickou teplotou) stavové chování Ideální plyn Reálné plyny Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti skupenství plynné reálný plyn ve stavu
Kapaliny Molekulové vdw síly, vodíkové můstky
 Kapaliny Molekulové vdw síly, vodíkové můstky Metalické roztavené kovy, ionty + elektrony, elektrostatické síly Iontové roztavené soli, FLINAK (LiF + NaF + KF), volně pohyblivé anionty a kationty, iontová
Kapaliny Molekulové vdw síly, vodíkové můstky Metalické roztavené kovy, ionty + elektrony, elektrostatické síly Iontové roztavené soli, FLINAK (LiF + NaF + KF), volně pohyblivé anionty a kationty, iontová
Matematika II Lineární diferenciální rovnice
 Matematika II Lineární diferenciální rovnice RNDr. Renata Klufová, Ph. D. Jihoèeská univerzita v Èeských Budìjovicích EF Katedra aplikované matematiky a informatiky Lineární diferenciální rovnice Denice
Matematika II Lineární diferenciální rovnice RNDr. Renata Klufová, Ph. D. Jihoèeská univerzita v Èeských Budìjovicích EF Katedra aplikované matematiky a informatiky Lineární diferenciální rovnice Denice
Atom vodíku. Nejjednodušší soustava: p + e Řešitelná exaktně. Kulová symetrie. Potenciální energie mezi p + e. e =
 Atom vodíku Nejjednodušší soustava: p + e Řešitelná exaktně Kulová symetrie Potenciální energie mezi p + e V 2 e = 4πε r 0 1 Polární souřadnice využití kulové symetrie atomu Ψ(x,y,z) Ψ(r,θ, φ) x =? y=?
Atom vodíku Nejjednodušší soustava: p + e Řešitelná exaktně Kulová symetrie Potenciální energie mezi p + e V 2 e = 4πε r 0 1 Polární souřadnice využití kulové symetrie atomu Ψ(x,y,z) Ψ(r,θ, φ) x =? y=?
Maturitní témata fyzika
 Maturitní témata fyzika 1. Kinematika pohybů hmotného bodu - mechanický pohyb a jeho sledování, trajektorie, dráha - rychlost hmotného bodu - rovnoměrný pohyb - zrychlení hmotného bodu - rovnoměrně zrychlený
Maturitní témata fyzika 1. Kinematika pohybů hmotného bodu - mechanický pohyb a jeho sledování, trajektorie, dráha - rychlost hmotného bodu - rovnoměrný pohyb - zrychlení hmotného bodu - rovnoměrně zrychlený
Chemická kinetika. Reakce 1. řádu rychlost přímo úměrná koncentraci složky
 Chemická kinetika Chemická kinetika Reakce 0. řádu reakční rychlost nezávisí na čase a probíhá konstantní rychlostí v = k (rychlost se rovná rychlostní konstantě) velmi pomalé reakce (prakticky se nemění
Chemická kinetika Chemická kinetika Reakce 0. řádu reakční rychlost nezávisí na čase a probíhá konstantní rychlostí v = k (rychlost se rovná rychlostní konstantě) velmi pomalé reakce (prakticky se nemění
Cvièení { 2D Clausiova-Clapeyronova rovnice
 Cvièení { 2D Clausiova-Clapeyronova rovnice 1/12 Evropský sociální fond þpraha & EU: Investujeme do va¹í budoucnostiÿ Inovace pøedmìtu Poèítaèová chemie je podporována projektem CHEMnote (Inovace bakaláøského
Cvièení { 2D Clausiova-Clapeyronova rovnice 1/12 Evropský sociální fond þpraha & EU: Investujeme do va¹í budoucnostiÿ Inovace pøedmìtu Poèítaèová chemie je podporována projektem CHEMnote (Inovace bakaláøského
Mol. fyz. a termodynamika
 Molekulová fyzika pracuje na základě kinetické teorie látek a statistiky Termodynamika zkoumání tepelných jevů a strojů nezajímají nás jednotlivé částice Molekulová fyzika základem jsou: Látka kteréhokoli
Molekulová fyzika pracuje na základě kinetické teorie látek a statistiky Termodynamika zkoumání tepelných jevů a strojů nezajímají nás jednotlivé částice Molekulová fyzika základem jsou: Látka kteréhokoli
Kapaliny Molekulové vdw síly, vodíkové můstky
 Kapaliny Molekulové vdw síly, vodíkové můstky Metalické roztavené kovy, ionty + elektrony, elektrostatické síly Iontové roztavené soli, FLINAK (LiF + NaF + KF), volně pohyblivé anionty a kationty, iontová
Kapaliny Molekulové vdw síly, vodíkové můstky Metalické roztavené kovy, ionty + elektrony, elektrostatické síly Iontové roztavené soli, FLINAK (LiF + NaF + KF), volně pohyblivé anionty a kationty, iontová
Základem molekulové fyziky je kinetická teorie látek. Vychází ze tří pouček:
 Molekulová fyzika zkoumá vlastnosti látek na základě jejich vnitřní struktury, pohybu a vzájemného působení částic, ze kterých se látky skládají. Termodynamika se zabývá zákony přeměny různých forem energie
Molekulová fyzika zkoumá vlastnosti látek na základě jejich vnitřní struktury, pohybu a vzájemného působení částic, ze kterých se látky skládají. Termodynamika se zabývá zákony přeměny různých forem energie
Mezimolekulové interakce
 Mezimolekulové interakce, od teorie po interakce biomolekul s grafenem Pavel Banáš Mezimolekulové interakce slabé mezimolekulové interakce fyzikální původ mezimolekulárních interakcí poruchová teorie mezimolekulárních
Mezimolekulové interakce, od teorie po interakce biomolekul s grafenem Pavel Banáš Mezimolekulové interakce slabé mezimolekulové interakce fyzikální původ mezimolekulárních interakcí poruchová teorie mezimolekulárních
POŽADAVKY KE STÁTNÍ ZÁVĚREČNÉ ZKOUŠCE MAGISTERSKÉ STUDIUM POČÍTAČOVÉ MODELOVÁNÍ VE VĚDĚ A TECHNICE (NAVAZUJÍCÍ STUDIUM I DOBÍHAJÍCÍ 5-LETÉ STUDIUM)
 POŽADAVKY KE STÁTNÍ ZÁVĚREČNÉ ZKOUŠCE MAGISTERSKÉ STUDIUM POČÍTAČOVÉ MODELOVÁNÍ VE VĚDĚ A TECHNICE (NAVAZUJÍCÍ STUDIUM I DOBÍHAJÍCÍ 5-LETÉ STUDIUM) Organizace zkoušky Zkouška je ústní a má čtyři části:
POŽADAVKY KE STÁTNÍ ZÁVĚREČNÉ ZKOUŠCE MAGISTERSKÉ STUDIUM POČÍTAČOVÉ MODELOVÁNÍ VE VĚDĚ A TECHNICE (NAVAZUJÍCÍ STUDIUM I DOBÍHAJÍCÍ 5-LETÉ STUDIUM) Organizace zkoušky Zkouška je ústní a má čtyři části:
Fyzikální chemie Úvod do studia, základní pojmy
 Fyzikální chemie Úvod do studia, základní pojmy HMOTA A JEJÍ VLASTNOSTI POSTAVENÍ FYZIKÁLNÍ CHEMIE V PŘÍRODNÍCH VĚDÁCH HISTORIE FYZIKÁLNÍ CHEMIE ZÁKLADNÍ POJMY DEFINICE FORMY HMOTY Formy a nositelé hmoty
Fyzikální chemie Úvod do studia, základní pojmy HMOTA A JEJÍ VLASTNOSTI POSTAVENÍ FYZIKÁLNÍ CHEMIE V PŘÍRODNÍCH VĚDÁCH HISTORIE FYZIKÁLNÍ CHEMIE ZÁKLADNÍ POJMY DEFINICE FORMY HMOTY Formy a nositelé hmoty
Chemická vazba. Příčinou nestability atomů a jejich ochoty tvořit vazbu je jejich elektronový obal.
 Chemická vazba Volné atomy v přírodě jen zcela výjimečně (vzácné plyny). Atomy prvků mají snahu se navzájem slučovat a vytvářet molekuly prvků nebo sloučenin. Atomy jsou v molekulách k sobě poutány chemickou
Chemická vazba Volné atomy v přírodě jen zcela výjimečně (vzácné plyny). Atomy prvků mají snahu se navzájem slučovat a vytvářet molekuly prvků nebo sloučenin. Atomy jsou v molekulách k sobě poutány chemickou
Fázová rozhraní a mezifázová energie
 Fázová rozhraní a mezifázová energie druhy: l/g l/l }{{} mobilní 1/15 s/g s/l s/s povrch koule = 4πr 2 Pøíklad. Kolik % molekul vody je na povrchu kapièky mlhy o prùmìru a) 0.1 mm (hranice viditelnosti
Fázová rozhraní a mezifázová energie druhy: l/g l/l }{{} mobilní 1/15 s/g s/l s/s povrch koule = 4πr 2 Pøíklad. Kolik % molekul vody je na povrchu kapièky mlhy o prùmìru a) 0.1 mm (hranice viditelnosti
Fyzikální chemie. ochrana životního prostředí analytická chemie chemická technologie denní. Platnost: od 1. 9. 2009 do 31. 8. 2013
 Učební osnova předmětu Fyzikální chemie Studijní obor: Aplikovaná chemie Zaměření: Forma vzdělávání: Celkový počet vyučovacích hodin za studium: Analytická chemie Chemická technologie Ochrana životního
Učební osnova předmětu Fyzikální chemie Studijní obor: Aplikovaná chemie Zaměření: Forma vzdělávání: Celkový počet vyučovacích hodin za studium: Analytická chemie Chemická technologie Ochrana životního
Matematika II Urèitý integrál
 Matematika II Urèitý integrál RNDr. Renata Klufová, Ph. D. Jihoèeská univerzita v Èeských Budìjovicích EF Katedra aplikované matematiky a informatiky Motivace Je dána funkce f(x) = 2 + x2 x 4. Urèete co
Matematika II Urèitý integrál RNDr. Renata Klufová, Ph. D. Jihoèeská univerzita v Èeských Budìjovicích EF Katedra aplikované matematiky a informatiky Motivace Je dána funkce f(x) = 2 + x2 x 4. Urèete co
Autor by chtìl podìkovat všem svým spolupracovníkùm a kolegùm, kteøí mu pomohli s pøípravou textu. K vydání knihy pøispìla firma Newport Electronics s
 Pavel Nevøiva ANALÝZA SIGNÁLÙ A SOUSTAV Praha 2000 Autor by chtìl podìkovat všem svým spolupracovníkùm a kolegùm, kteøí mu pomohli s pøípravou textu. K vydání knihy pøispìla firma Newport Electronics spol.
Pavel Nevøiva ANALÝZA SIGNÁLÙ A SOUSTAV Praha 2000 Autor by chtìl podìkovat všem svým spolupracovníkùm a kolegùm, kteøí mu pomohli s pøípravou textu. K vydání knihy pøispìla firma Newport Electronics spol.
Molekulární krystal vazebné poměry. Bohumil Kratochvíl
 Molekulární krystal vazebné poměry Bohumil Kratochvíl Předmět: Chemie a fyzika pevných léčiv, 2017 Složení farmaceutických substancí - API Z celkového portfolia API tvoří asi 90 % organické sloučeniny,
Molekulární krystal vazebné poměry Bohumil Kratochvíl Předmět: Chemie a fyzika pevných léčiv, 2017 Složení farmaceutických substancí - API Z celkového portfolia API tvoří asi 90 % organické sloučeniny,
Test vlastnosti látek a periodická tabulka
 DUM Základy přírodních věd DUM III/2-T3-2-08 Téma: Test vlastnosti látek a periodická tabulka Střední škola Rok: 2012 2013 Varianta: A Zpracoval: Mgr. Pavel Hrubý Mgr. Josef Kormaník TEST Test vlastnosti
DUM Základy přírodních věd DUM III/2-T3-2-08 Téma: Test vlastnosti látek a periodická tabulka Střední škola Rok: 2012 2013 Varianta: A Zpracoval: Mgr. Pavel Hrubý Mgr. Josef Kormaník TEST Test vlastnosti
Stavové rovnice. v = (zobecnìný) vylouèený objem. plyn + kapalina
 Stavové rovnice Stavová rovnice je vztah mezi p, T, V a n (u smìsí slo¾ením n i ), alternativnì p, T, Vm = V/n (u smìsí je¹tì x i ) èi jinými ekvivalentními velièinami. plyn ideální plyn: pvm/rt = 1 viriálová
Stavové rovnice Stavová rovnice je vztah mezi p, T, V a n (u smìsí slo¾ením n i ), alternativnì p, T, Vm = V/n (u smìsí je¹tì x i ) èi jinými ekvivalentními velièinami. plyn ideální plyn: pvm/rt = 1 viriálová
Otázky ke zkoušce z obecné chemie (Prof. RNDr. Karel Procházka, DrSc.)
 Otázky ke zkoušce z obecné chemie (Prof. RNDr. Karel Procházka, DrSc.) Na ústní zkoušku se může přihlásit student, který má zápočet ze cvičení a úspěšně složenou zkouškovou písemku. Na ústní zkoušku se
Otázky ke zkoušce z obecné chemie (Prof. RNDr. Karel Procházka, DrSc.) Na ústní zkoušku se může přihlásit student, který má zápočet ze cvičení a úspěšně složenou zkouškovou písemku. Na ústní zkoušku se
Aproximace funkcí. Chceme þvzoreèekÿ. Známe: celý prùbìh funkce
 Aproximace funkcí 1/13 Známe: celý prùbìh funkce Chceme þvzoreèekÿ hodnoty ve vybraných bodech, pøíp. i derivace Kvalita údajù: známe pøesnì (máme algoritmus) známe pøibli¾nì (experiment èi simulace) {
Aproximace funkcí 1/13 Známe: celý prùbìh funkce Chceme þvzoreèekÿ hodnoty ve vybraných bodech, pøíp. i derivace Kvalita údajù: známe pøesnì (máme algoritmus) známe pøibli¾nì (experiment èi simulace) {
Typy molekul, látek a jejich vazeb v organismech
 Typy molekul, látek a jejich vazeb v organismech Typy molekul, látek a jejich vazeb v organismech Organismy se skládají z molekul rozličných látek Jednotlivé látky si organismus vytváří sám z jiných látek,
Typy molekul, látek a jejich vazeb v organismech Typy molekul, látek a jejich vazeb v organismech Organismy se skládají z molekul rozličných látek Jednotlivé látky si organismus vytváří sám z jiných látek,
Gymnázium Jiřího Ortena, Kutná Hora
 Předmět: Seminář chemie (SCH) Náplň: Obecná chemie, anorganická chemie, chemické výpočty, základy analytické chemie Třída: 3. ročník a septima Počet hodin: 2 hodiny týdně Pomůcky: Vybavení odborné učebny,
Předmět: Seminář chemie (SCH) Náplň: Obecná chemie, anorganická chemie, chemické výpočty, základy analytické chemie Třída: 3. ročník a septima Počet hodin: 2 hodiny týdně Pomůcky: Vybavení odborné učebny,
Úvodní info. Studium
 [mozilla le:/home/jiri/www/fch/cz/pomucky/kolafa/n4316.html] 1/16 Úvodní info Jiøí Kolafa Ústav fyzikální chemie V CHT Praha budova A, místnost 325 (zadním vchodem) jiri.kolafa@vscht.cz 2244 4257 Web pøedmìtu:
[mozilla le:/home/jiri/www/fch/cz/pomucky/kolafa/n4316.html] 1/16 Úvodní info Jiøí Kolafa Ústav fyzikální chemie V CHT Praha budova A, místnost 325 (zadním vchodem) jiri.kolafa@vscht.cz 2244 4257 Web pøedmìtu:
Vibrace atomů v mřížce, tepelná kapacita pevných látek
 Vibrace atomů v mřížce, tepelná kapacita pevných látek Atomy vázané v mřížce nejsou v klidu. Míru jejich pohybu vyjadřuje podobně jako u plynů a kapalin teplota. - Elastické vlny v kontinuu neatomární
Vibrace atomů v mřížce, tepelná kapacita pevných látek Atomy vázané v mřížce nejsou v klidu. Míru jejich pohybu vyjadřuje podobně jako u plynů a kapalin teplota. - Elastické vlny v kontinuu neatomární
Matematika II Limita a spojitost funkce, derivace
 Matematika II Limita a spojitost funkce, derivace RNDr. Renata Klufová, Ph. D. Jihoèeská univerzita v Èeských Budìjovicích EF Katedra aplikované matematiky a informatiky Prstencové a kruhové okolí bodu
Matematika II Limita a spojitost funkce, derivace RNDr. Renata Klufová, Ph. D. Jihoèeská univerzita v Èeských Budìjovicích EF Katedra aplikované matematiky a informatiky Prstencové a kruhové okolí bodu
Cvièení { 2D Clausiova{Clapeyronova rovnice
 Cvièení { 2D Clausiova{Clapeyronova rovnice 1/15 Evropský sociální fond þpraha & EU: Investujeme do va¹í budoucnostiÿ Inovace pøedmìtu Poèítaèová chemie je podporována projektem CHEMnote (Inovace bakaláøského
Cvièení { 2D Clausiova{Clapeyronova rovnice 1/15 Evropský sociální fond þpraha & EU: Investujeme do va¹í budoucnostiÿ Inovace pøedmìtu Poèítaèová chemie je podporována projektem CHEMnote (Inovace bakaláøského
Transportní jevy v plynech Reálné plyny Fázové přechody Kapaliny
 Transportní jevy v plynech Reálné plyny Fázové přechody Kapaliny Hustota toku Zatím jsme studovali pouze soustavy, které byly v rovnovážném stavu není-li soustava v silovém poli, je hustota částic stejná
Transportní jevy v plynech Reálné plyny Fázové přechody Kapaliny Hustota toku Zatím jsme studovali pouze soustavy, které byly v rovnovážném stavu není-li soustava v silovém poli, je hustota částic stejná
Fyzika, maturitní okruhy (profilová část), školní rok 2014/2015 Gymnázium INTEGRA BRNO
 1. Jednotky a veličiny soustava SI odvozené jednotky násobky a díly jednotek skalární a vektorové fyzikální veličiny rozměrová analýza 2. Kinematika hmotného bodu základní pojmy kinematiky hmotného bodu
1. Jednotky a veličiny soustava SI odvozené jednotky násobky a díly jednotek skalární a vektorové fyzikální veličiny rozměrová analýza 2. Kinematika hmotného bodu základní pojmy kinematiky hmotného bodu
Vojtěch Hrubý: Esej pro předmět Seminář EVF
 Vojtěch Hrubý: Esej pro předmět Seminář EVF Plazma Pod pojmem plazma většinou myslíme plynné prostředí, které se skládá z neutrálních částic, iontů a elektronů. Poměr množství neutrálních a nabitých částic
Vojtěch Hrubý: Esej pro předmět Seminář EVF Plazma Pod pojmem plazma většinou myslíme plynné prostředí, které se skládá z neutrálních částic, iontů a elektronů. Poměr množství neutrálních a nabitých částic
ANODA KATODA elektrolyt:
 Ukázky z pracovních listů 1) Naznač pomocí šipek, které částice putují k anodě a které ke katodě. Co je elektrolytem? ANODA KATODA elektrolyt: Zn 2+ Cl - Zn 2+ Zn 2+ Cl - Cl - Cl - Cl - Cl - Zn 2+ Cl -
Ukázky z pracovních listů 1) Naznač pomocí šipek, které částice putují k anodě a které ke katodě. Co je elektrolytem? ANODA KATODA elektrolyt: Zn 2+ Cl - Zn 2+ Zn 2+ Cl - Cl - Cl - Cl - Cl - Zn 2+ Cl -
Nultá věta termodynamická
 TERMODYNAMIKA Nultá věta termodynamická 2 Práce 3 Práce - příklady 4 1. věta termodynamická 5 Entalpie 6 Tepelné kapacity 7 Vnitřní energie a entalpie ideálního plynu 8 Výpočet tepla a práce 9 Adiabatický
TERMODYNAMIKA Nultá věta termodynamická 2 Práce 3 Práce - příklady 4 1. věta termodynamická 5 Entalpie 6 Tepelné kapacity 7 Vnitřní energie a entalpie ideálního plynu 8 Výpočet tepla a práce 9 Adiabatický
Základní charakteristika výzkumné činnosti Ústavu fyzikální chemie
 Základní charakteristika výzkumné činnosti Ústavu fyzikální chemie Základním předmětem výzkumu prováděného ústavem je chemická termodynamika a její aplikace pro popis vybraných vlastností chemických systémů
Základní charakteristika výzkumné činnosti Ústavu fyzikální chemie Základním předmětem výzkumu prováděného ústavem je chemická termodynamika a její aplikace pro popis vybraných vlastností chemických systémů
Chemie. Mgr. Petra Drápelová Mgr. Jaroslava Vrbková. Gymnázium, SOŠ a VOŠ Ledeč nad Sázavou
 Chemie Mgr. Petra Drápelová Mgr. Jaroslava Vrbková Gymnázium, SOŠ a VOŠ Ledeč nad Sázavou CHEMICKÁ VAZBA VY_32_INOVACE_03_3_07_CH Gymnázium, SOŠ a VOŠ Ledeč nad Sázavou CHEMICKÁ VAZBA Volné atomy v přírodě
Chemie Mgr. Petra Drápelová Mgr. Jaroslava Vrbková Gymnázium, SOŠ a VOŠ Ledeč nad Sázavou CHEMICKÁ VAZBA VY_32_INOVACE_03_3_07_CH Gymnázium, SOŠ a VOŠ Ledeč nad Sázavou CHEMICKÁ VAZBA Volné atomy v přírodě
Chemická vazba. Molekula vodíku. Elektronová teorie. Oktetové pravidlo (Kossel, Lewis, 1916) Pevnost vazby vazebná energie.
 Elektronová teorie ktetové pravidlo (Kossel, Lewis, 1916) Chemická vazba sdílení 2 valenčních e - opačného spinu 2 atomy za vzniku stabilní elektronové konfigurace vzácného plynu Spojení atomů prvků v
Elektronová teorie ktetové pravidlo (Kossel, Lewis, 1916) Chemická vazba sdílení 2 valenčních e - opačného spinu 2 atomy za vzniku stabilní elektronové konfigurace vzácného plynu Spojení atomů prvků v
Rovnováha Tepelná - T všude stejná
 Fázové heterogenní rovnováhy Fáze = homogenní část soustavy, oddělná fyzickým rozhraním, na rozhraní se vlastnosti mění skokem Rovnováha Tepelná - T všude stejná Mechanická - p všude stejný Chemická -
Fázové heterogenní rovnováhy Fáze = homogenní část soustavy, oddělná fyzickým rozhraním, na rozhraní se vlastnosti mění skokem Rovnováha Tepelná - T všude stejná Mechanická - p všude stejný Chemická -
ANALÝZA FRAGMENTAČNÍCH KANÁLŮ IONIZOVANÝCH KLASTRŮ Rg N ; N>4, rozvoj programu Mdisreader
 ANALÝZA FRAGMENTAČNÍCH KANÁLŮ IONIZOVANÝCH KLASTRŮ Rg N ; N>4, rozvoj programu Mdisreader Autor: Pavel Naar Vedoucí práce: Doc. Ing. Ivan Janeček, CSc. Práce vznikla v rámci projektu SGS17/PřF/2012 Obsah
ANALÝZA FRAGMENTAČNÍCH KANÁLŮ IONIZOVANÝCH KLASTRŮ Rg N ; N>4, rozvoj programu Mdisreader Autor: Pavel Naar Vedoucí práce: Doc. Ing. Ivan Janeček, CSc. Práce vznikla v rámci projektu SGS17/PřF/2012 Obsah
Molekulová fyzika a termodynamika
 Molekulová fyzika a termodynamika Molekulová fyzika a termodynamika Úvod, vnitřní energie soustavy, teplo, teplota, stavová rovnice ideálního plynu Termodynamické zákony, termodynamické děje Teplotní a
Molekulová fyzika a termodynamika Molekulová fyzika a termodynamika Úvod, vnitřní energie soustavy, teplo, teplota, stavová rovnice ideálního plynu Termodynamické zákony, termodynamické děje Teplotní a
Látkové množství n poznámky 6.A GVN
 Látkové množství n poznámky 6.A GVN 10. září 2007 charakterizuje látky z hlediska počtu částic (molekul, atomů, iontů), které tato látka obsahuje je-li v tělese z homogenní látky N částic, pak látkové
Látkové množství n poznámky 6.A GVN 10. září 2007 charakterizuje látky z hlediska počtu částic (molekul, atomů, iontů), které tato látka obsahuje je-li v tělese z homogenní látky N částic, pak látkové
Kvantová fyzika atomárních soustav letní semestr VIII. KOTLÁŘSKÁ 23. DUBNA 2014
 F40 Kvantová fyzika atomárních soustav letní semestr 03-04 VIII. Vibrace víceatomových molekul cvičení KOTLÁŘSKÁ 3. DUBNA 04 Úvodem capsule o maticích a jejich diagonalisaci definice "vibračních módů"
F40 Kvantová fyzika atomárních soustav letní semestr 03-04 VIII. Vibrace víceatomových molekul cvičení KOTLÁŘSKÁ 3. DUBNA 04 Úvodem capsule o maticích a jejich diagonalisaci definice "vibračních módů"
Pravdìpodobnostní popis
 Pravdìpodobnostní popis 1/19 klasická mechanika { stav = { r 1,..., r N, p 1,..., p N } stavù je { hustota pravdìpodobnosti stavù ρ( r 1,..., r N, p 1,..., p N ) kvantové mechaniky { stav = stavù je koneènì
Pravdìpodobnostní popis 1/19 klasická mechanika { stav = { r 1,..., r N, p 1,..., p N } stavù je { hustota pravdìpodobnosti stavù ρ( r 1,..., r N, p 1,..., p N ) kvantové mechaniky { stav = stavù je koneènì
PDWHULiO FS>-NJ ±. FS>NFDONJ ± ƒ& VW teur åhoh]r FtQ KOLQtN N HPtN. OHG DONRKRO ROHM FFD FFD SHWUROHM UWX YRGD Y]GXFK YRGQtSiUD KHOLXP
![PDWHULiO FS>-NJ ±. FS>NFDONJ ± ƒ& VW teur åhoh]r FtQ KOLQtN N HPtN. OHG DONRKRO ROHM FFD FFD SHWUROHM UWX YRGD Y]GXFK YRGQtSiUD KHOLXP PDWHULiO FS>-NJ ±. FS>NFDONJ ± ƒ& VW teur åhoh]r FtQ KOLQtN N HPtN. OHG DONRKRO ROHM FFD FFD SHWUROHM UWX YRGD Y]GXFK YRGQtSiUD KHOLXP](/thumbs/50/25995224.jpg) Vážení zákazníci, dovolujeme si Vás upozornit, že na tuto ukázku knihy se vztahují autorská práva, tzv. copyright. To znamená, že ukázka má sloužit výhradnì pro osobní potøebu potenciálního kupujícího
Vážení zákazníci, dovolujeme si Vás upozornit, že na tuto ukázku knihy se vztahují autorská práva, tzv. copyright. To znamená, že ukázka má sloužit výhradnì pro osobní potøebu potenciálního kupujícího
Termodynamika. T [K ]=t [ 0 C] 273,15 T [ K ]= t [ 0 C] termodynamická teplota: Stavy hmoty. jednotka: 1 K (kelvin) = 1/273,16 část termodynamické
![Termodynamika. T [K ]=t [ 0 C] 273,15 T [ K ]= t [ 0 C] termodynamická teplota: Stavy hmoty. jednotka: 1 K (kelvin) = 1/273,16 část termodynamické Termodynamika. T [K ]=t [ 0 C] 273,15 T [ K ]= t [ 0 C] termodynamická teplota: Stavy hmoty. jednotka: 1 K (kelvin) = 1/273,16 část termodynamické](/thumbs/24/2778201.jpg) Termodynamika termodynamická teplota: Stavy hmoty jednotka: 1 K (kelvin) = 1/273,16 část termodynamické teploty trojného bodu vody (273,16 K = 0,01 o C). 0 o C = 273,15 K T [K ]=t [ 0 C] 273,15 T [ K ]=
Termodynamika termodynamická teplota: Stavy hmoty jednotka: 1 K (kelvin) = 1/273,16 část termodynamické teploty trojného bodu vody (273,16 K = 0,01 o C). 0 o C = 273,15 K T [K ]=t [ 0 C] 273,15 T [ K ]=
České vysoké učení technické v Praze Fakulta jaderná a fyzikálně inženýrská. Příloha formuláře C OKRUHY
 Příloha formuláře C OKRUHY ke státním závěrečným zkouškám BAKALÁŘSKÉ STUDIUM Obor: Studijní program: Aplikace přírodních věd Základy fyziky kondenzovaných látek 1. Vazebné síly v kondenzovaných látkách
Příloha formuláře C OKRUHY ke státním závěrečným zkouškám BAKALÁŘSKÉ STUDIUM Obor: Studijní program: Aplikace přírodních věd Základy fyziky kondenzovaných látek 1. Vazebné síly v kondenzovaných látkách
Okruhy k maturitní zkoušce z fyziky
 Okruhy k maturitní zkoušce z fyziky 1. Fyzikální obraz světa - metody zkoumaní fyzikální reality, pojem vztažné soustavy ve fyzice, soustava jednotek SI, skalární a vektorové fyzikální veličiny, fyzikální
Okruhy k maturitní zkoušce z fyziky 1. Fyzikální obraz světa - metody zkoumaní fyzikální reality, pojem vztažné soustavy ve fyzice, soustava jednotek SI, skalární a vektorové fyzikální veličiny, fyzikální
