Léčba pokročilého gastrointestinálního
|
|
|
- Břetislav Král
- před 6 lety
- Počet zobrazení:
Transkript
1 207 Léčba pokročilého gastrointestinálního stromálního nádoru Zdeněk Linke, Jana Prausová Radioterapeuticko-onkologické oddělení FN Motol, Praha Článek se zabývá možnostmi terapie gastrointestinálního stromálního nádoru jednoho z prvních solidních nádorů, u kterého byla chemická a radiační léčba zcela vytlačena cílenou biologickou léčbou. Primární target léčbou u pokročilého inoperabilního gastrointestinálního stromálního nádoru představuje imatinib mesylát. Kromě přehledu klinických studií a léčebných výsledků odpovídá i na kontroverzní otázky iniciální dávka imatinibu, prediktivní faktory, které možná povedou ke standardní primární eskalaci dávky, dále otázka pokračování v léčbě i po dosažení kompletní remise. Článek také poukazuje na další možnosti pokračování v biologické cílené terapii i po selhání imatinibu užití sunitinibu, nilotinibu, mtor. Klíčová slova: gastrointestinální stromální nádor, imatinib, nilotinib, mtor inhibitor. Treatment of gastrointestinal stromal tumours The article deals with possibilities of gastrointestinal stromal tumour therapy one of the first solid tumour, whose chemical and radiation treatment was completely displaced by biologic treatment. Imatinib mesylát represents primary target treatment of progressed inoperable gastrointestinal stromal tumour. Except overview of clinical studies and treatment results the article responses to controversial questions initial imatinib dosage, predictive factors, which cal lead to standards primary dosage escalation, question of treatment continuation after complete remission. The article also refers to others possibilities continuation in biological target therapy even after imatinib failure use of sunitinib, nilotinib, mtor perspective IPI-504. Key words: gastrointestinal stromal tumour, imatinib, nilotinib, mtor inhibitor. Onkológia (Bratisl.), 2010; roč. 5 (4): Úvod Incidence gastrointestinálního stromálního tumoru se v poslední době zvyšuje, a to nejen díky lepšící se imunohistochemické patologické diagnostice. Tvoří cca odhadem % nádorů zažívacího traktu, na druhou stranu představuje až 80 % mezenchymálních primárních nádorů GIT. Gastrointestinální stromální nádor patří mezi zvláště refrakterní nádory vůči chemoterapii i radioterapii historicky býval uváděn počet léčebných odpovědí (RR) na chemoterapii na bázi antracyklinů v monoterapii nebo spolu s ifosfamidem pod 10 %, trvání léčebných odpovědí bylo velice krátké a pohybovalo se jen mezi 2 5 měsíci; data o účinnosti radioterapie nejsou k dispozici aktuálně žádná. Gastrointestinální stromální nádor je charakterizován častou přítomností tyrozinkinázových receptorů receptoru CD34 poukazující na jeho pravděpodobnou mateřskou buňku buňku hladké svaloviny, prakticky u všech nádorů dále přítomností receptoru tyrozinkinázy C-KIT (CD117) a receptoru pro destičkový růstový faktor (PDGFR). Nádor je nejčastěji primárně diagnostikován v oblasti žaludku (cca 50 %), dále v oblasti tenkého střeva (cca 25 %), méně častou primární lokalizací je rektum a tlusté střevo (10 %), vzácnou primární lokalizací je jícen, omentum, peritoneum (celkem 15 %). Prognóza radikálně chirurgicky odstraněných tumorů je odvozena dle prognostických faktorů. Paliativní desobstrukční výkony či paliativní resekce chronicky krvácejících tumorů se běžně s paliativním záměrem provádí, ale jasně cytoredukční výkony s cílem od počátku zmenšit, ale neodstranit tumor se u pokročilé nemoci v současné době nedoporučují. Takové výkony v éře biologické terapie neprodlužují celkové přežití, jen zvyšují morbiditu nebo jen oddalují nasazení biologické léčby. V současné době je u lokálně pokročilé nemoci zkoumána možnost léčby neoadjuvantní. Obrázek 1. C-KIT receptor Extracelulární a juxtamembranózní část Intracelulární a juxtamembranózní část TK1 Kinase insert TK2 C-KIT genové mutace u GIST Ligand (SCF)-binding Léčba gastrointestinálního stromálního nádoru Léčba adjuvantní imatinib mesylát Primární léčbou by měla být radikální chirurgická resekce. Výhodou předchozího předoperačního vyšetření je případný chirurgický přístup k ošetření resekabilní metastatické nemoci. Standardem pro pacienty s radikální chirurgickou resekcí byla observace a dispenzarizace bez ohledu na stupeň rizika recidivy. U metastatické choroby se však dal předpoklá- EXON 9 (~5 10 % mutací) EXON 11 (~70 % mutací) EXON 13 (~5 % mutací) EXON 17 (~5 % mutací) Genová mapa mezi 4q11 a 4q exonů ; 5 (4) Onkológia
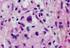
2 208 dat benefit z adjuvantní léčby u skupiny nádorů s vysokým rizikem recidivy. Proto byla započata celá řada adjuvantních studií, které mají odpovědět na otázku, zda adjuvantní aplikace imatinibu snižuje riziko recidivy. Významnou je studie ACOSOG Z9000, kde bylo mezi 9/2001 až 9/2003 zařazeno celkem 110 pacientů po radikálním chirurgickém odstranění nádoru a studie ACOSOG Z9001 (1), u nichž je jasný benefit stran progression free survival (PFS) u pacientů s imatinibem. Zejména pokračovací studie ACOSOG Z9001, kde bylo celkem 708 pacientů po radikální resekci rizikového GIST nad 3 cm v největším rozměru randomizováno do 2 ramen v prvém rameni roční aplikace imatinibu 400 mg/den, v druhém rameni denně placebo. Při analýze 644 hodnotitelných pacientů byl vyhodnocen jednoroční relapse free survival tj. porovnání obou ramen s ohledem na trvající remisi bez detekce progrese. Tento jednoroční RFS vyzněl jednoznačně pro pacienty v rameni s aktivní adjuvantní léčbou imatinibem RFS v rameni s imatinibem činil 97 %, v rameni s placebem 83 % (hazard ratio = 0.325). Data o celkovém přežití jsou dosud dostatečně zralá, nicméně i zde lze vypozorovat trend zlepšení v rameni s imatinibem; rozdíly zatím nejsou signifikantní a je potřeba dlouhý follow-up (ve studii se počítá s 10letým followup). Klinická studie Z9001 se stala základním důvodem pro dnes standardně doporučovanou roční adjuvanci imatinibem 400 mg/den u pacientů vysokého a středního rizika. Podobná data prezentovala i menší klinická studie čínských autorů (22), kteří prokázali 1letý RFS (přežití bez progrese) u 96.1 % subjektů. Protože vyvstala pochopitelná otázka, zda je jednoletá adjuvance dostatečně časově dlouhá, byla koncipována a v současnosti probíhá otevřená prospektivní klinická studie SSG XVIII (23), která bude porovnávat dnes standardní Tabulka 1. Stupně rizika GIST Identifikace rizika po radikální resekci tumoru GIST: Maligní potenciál a doporučovanou roční adjuvanci imatinibem v dávce 400 mg oproti prodloužené 36měsíční adjuvantní léčbě imatinibem 400 mg/den. Starší skandinávská studie byla postavena na podobném předpokladu a adjuvantně byl imatinib v dávce 400 mg/den aplikován po dobu 24 měsíců. Na výsledky těchto klinických studií čekáme; mohou poukázat na případný benefit z prodloužení adjuvance imatinibem na dobu 2 3 let! Klinická studie fáze II (Phase II Study of Neoadjuvant and Adjuvant Imatinib Mesylate in Patient With Primary or Recurrent Potentially Resectable Malignant GIST (RTOG-S0132)) je koncipována jako primární neoadjuvantní studie a zařazuje pacienty s lokálně inoperabilním nemetastatickým GISTem. Pacienti podstoupí osmitýdenní léčbu imatinibem 600 mg/ den, následuje resekce regredujícího tumoru a pooperačně adjuvantně je imatinib aplikován opět v dávce 600 mg/den po dobu 2 let, primárními cíly jsou počty léčebných odpovědí (RR), přežití bez progrese (PFS) a bezpečnost. Léčba paliativní imatinib mesylát O účinnosti imatinibu (STI 571; Glivec ) u metastatické choroby nebylo pochyb již z dat iniciálních studií fáze I a II z roku 2001 studie Blankeho (2) a van Oosteroma (3). Poprvé byly prezentovány i obvyklé nežádoucí účinky imatinibu jako periorbitální otoky (40 %), periferní otoky (30 %), výskyt únavy (30 %), kožní rash (15 %), nauzea, vomitus (10 25 %). Ve studii fáze II Blankeho a Demetriho (4) klinická studie B2222 byly poprvé použity záměrně různé dávky imatinibu u metastatického GISTu celkem 147 pacientů bylo randomizováno do 2 ramen v prvním rameni byli pacienti léčeni iniciální dávkou 400 mg imatinibu denně a v případě progrese byla následně možná eskalace na 600 mg/den, v druhém rameni byli pacienti léčeni od počátku dávkou 600 mg/den. Bylo Velikost (cm) Počet mitóz (HPF) Velmi nízké riziko very low risk < 2 < 5/50 Nízké riziko low risk 2 5 < 5/50 Středně vysoké riziko intermediate risk Vysoké riziko high risk HPF, high-power fields. 1. Fletcher CD, et al. Hum Pathol. 2002; 33: Miettinen M, et al. Hum Pathol. 2002; 33: < > 5 > 10 Jakákoliv velikost 6 10/50 < 5/50 > 5/50 Jakýkoliv počet mitóz > 10/50 dosaženo parciálních odpovědí u 53.7 %, stabilizace nemoci u 27.9 % pacientů (léčebný benefit 81 %) a iniciální progrese přitom jen u 13.6 % pacientů. Poprvé byla zmíněna efektivita eskalace imatinibu při progresi na iniciální dávce 400 mg, ale poprvé byla reportována také asi nejnebezpečnější komplikace při léčbě imatinibem, a to intratumorózní krvácení stupně s cca 5% rizikem. Při dalším sledování byl uveden čas do progrese (TTP) 72 týdnů. Nebyl signifikantně zhoršen toxický profil při eskalaci z iniciálních 400 mg na 600 mg/den; 80 % pacientů dosáhlo tzv. PET kompletní remise. Medián do dosažení léčebných odpovědí (CR; PR) byl 13 týdnů, medián celkového přežití nebyl v době follow-up periody 34 měsíců dosažen! Velice zajímavá data poskytla tato studie po 5letém sledování; medián celkového přežití se prakticky nelišil u pacientů, kteří dosáhli parciální léčebné odpovědi proti pacientům s pouhou stabilizací metastatické choroby medián přežití 248 týdnů oproti výrazně horšímu přežití u pacientů s primární progresí medián 36 týdnů (graf 1). Pravděpodobnost 5letého přežití u pacientů Obrázek 2. Příklady změny celularity tumoru po neoadjuvantní léčbě imatinibem; A Biopsie GIST před léčbou. Vysoká mitotická aktivita, vysoká buněčnost; B Histologie GIST z definitivního resekátu po 12 měsících léčby imatinibem. Minimální buněčnost, hyalinní degenerace A) B) Obrázek 3. Příklady změny celularity tumoru po neoadjuvantní léčbě imatinibem. Biopsie GIST před resekcí: Vysoká buněčnost, vysoká mitotická aktivita, buněčné atypie; B Histologie z resekátu GIST po 11 měsících léčby imatinibem. Nádor z řídce uložených vřetenitých buněk bez výraznějších atypií v hutném hyalinizovaném kolagenním vazivu A) B)
3 210 s léčebnou odpovědí či stabilizací na iniciální dávce imatinibu byla 55 %, kdežto u pacientů s primární progresí na inicální dávce imatinibu jen 9 %! Protože byl zřejmý benefit z eskalace imatinibu na 600, resp. dnes primárně 800 mg/den při předchozí progresi na imatinibu 400 mg/den, vyvstala otázka, zda by bylo výhodně paušálně začít léčit iniciálně eskalační dávkou tj. 800 mg/den imatinibem. V klinické studii EORTC ISG AGITG (7) bylo celkem 946 pacientů randomizováno do dvou ramen v prvním rameni s iniciální dávkou 400 mg/den a při progresi choroby s eskalací na 800 mg/den, v 2. rameni od počátku léčby s dávkou imatinibu 800 mg/den. Počet léčebných odpovědí (RR) se signifikantně v obou ramenech nelišil v rameni s dávkou 400 mg byl RR 50 % (kompletních remisí z toho 5 %) a v rameni s primární dávkou 800 mg/den byl RR 54 % (z toho kompletních remisí 6 %). Při 2letém follow-up bylo dosaženo signifikantně lepšího počtu pacientů bez progrese po 2 letech (PFS progression free survival); a to ve skupině s iniciální dávkou 400 mg/ den imatinibu 44 %, ve skupině se vstupně vysokou dávkou u 52 % (P = 0.026). Výhoda celkového přežití po 2 letech má trend ve prospěch pro skupinu s iniciálně vysokou dávkou 69 % versus 74 %, ale není klinicky signifikantní. V další klinické studii fáze III S0033 (6) bylo celkem 746 pacientů s metastatickým GIST randomizováno do dvou ramen v prvém rameni nízká dávka iniciálně 400 mg/den imatinibu a při následné progresi eskalace na 800 mg/den, ve druhém rameni léčba iniciálně vysokou dávkou 800 mg/den imatinibem. Celkově bylo dosaženo 3 % kompletních, 45 % parciálních léčebných odpovědí a 27 % stabilizací nemoci. Rozdíly nebyly signifikatní po 2 letech sledování bylo PFS (čas přežití bez progrese) s trendem zlepšení ve skupině se zvýšenou dávkou 50 % ve skupině s nízkou dávkou a 54 % ve skupině s vysokou dávkou, na druhou stranu paradoxně celkové přežití po 2 letech vyšlo nesignifikantně, ale mírně zlepšené v rameni s nižší dávkou 400 mg oproti iniciální vysoké dávce 78 % versus 73 %! Při progresi pokročilé nemoci bylo u pacientů s iniciálně nízkou dávkou imatinibu po jejich eskalaci na vysokou dávku dosaženo u 7 % pacientů parciálních léčebných odpovědí a v dalších 29 % stabilizace choroby. Na podkladě této i předchozí studie je jasně doporučeno iniciálně léčit pokročilou chorobu imatinibem s dávkou 400 mg/den a až při progresi nemoci teprve eskalaci na 800 mg/den. Další otázkou bylo, zda léčit pacienty i nadále po dosažení výrazné léčebné odpovědi, případně kompletní remisi nebo raději terapii Graf 1. 5leté celkové přežití pacientů, kteří dosáhli léčebné odpovědi nebo stabilizace (PR, SD) proti primární progresi B2222 Probability 1,0 0,9 0,8 0,7 0,6 0,5 0,4 0,3 0,2 0,1 0,0 0 PD (n=17): Median 36 wks Number at Risk Median 95 % Cl Best Response Wks: Duration LL UL PR Wks 226 N/A SD N/A 149 N/A PD Wks přerušit a znovu nasadit až při další progresi choroby. Blayova studie fáze III (8) se na tuto otázku snažila odpovědět zařadila 182 pacientů s pokročilým ckit pozitivním GIST. Po dosažení léčebné odpovědi u 98 z nich (42 % parciálních a 10 % kompletních odpovědí; tj. RR = 52 %) bylo do studie nakonec z etických důvodů a se souhlasem zařazeno 58 pacientů a randomizováno buď do ramene s kontinuálním pokračováním aplikace imatinibu, nebo do ramene s přerušením a opětným nasazením při případné progresi. Po roce vyhodnocení došlo k progresi u 8 pacientů ve skupině s pokračující léčbou (26 pacientů) a u 26 pacientů ve skupině s přerušením (32 pacientů), což je signifikantní rozdíl (P < ). Je ale pravdou, že u většiny z nich u 22 pacientů z 26 progredujících pacientů po přerušení došlo po znovunasazení imatinibu k opětné rychlé regresi. Pro tyto 2 skupiny bylo 2leté celkové přežití 92 % ve skupině s pokračováním léčby a 87 % s přerušením léčby (P = 0.87). Z této studie tedy jednoznačně vyplývá, že dojde-li k výrazné léčebné odpovědi (výrazná parciální nebo kompletní léčebná odpověď) u pokročilé metastatické choroby a imatinib je snášen prakticky bez potíží, pak pacient nemá žádný benefit z přerušení léčby a doporučuje se s léčbou pokračovat do progrese pokročilé choroby nebo do limitujících nežádoucích účinků. V roce 2006 však byla opětně nastolena otázka optimální iniciální dávky imatinibu; dosud uváděná a doporučovaná iniciální dávka byla 400 mg imatinibu denně, ale při subanalýzách se objevoval fakt, že kromě nejobvyklejší mutace exonu 11 kit receptoru je u ostatních mutací exonů 9, 4 i ostatních raritních mutací včetně PR (n=98): Median 248 wks SD (n=23): Median n/a Weeks Post First Dose KIT receptoru bez mutace ( wild typ) trend benefitu z hlediska PFS (progression free survival) u dávek iniciálně vyšších! Proto se v současné době hovoří o možnosti prediktivního faktoru mutace exonu 9 s ohledem na vyšší účinnosti imatinibu v primárně eskalovaných dávkách imatinibu. Toto podporuje práce Cioffiho (12), který prezentuje skupinu dlouhodobě přežívajících pacientů s pokročilými metastatickými gastrointestinálními stromálními tumory. Z 200 pacientů trvala významná remise u 31 z nich, a to více než 5 let. Tyto případy byly podrobněji zkoumány a jako potencionální příznivé prognostické faktory se jeví mužské pohlaví (61 %), původ v tenkém střevě (60 % toto je proti původní představě o lepší prognóze GIST žaludku), izolované jaterní metastatické postižení (80 %), iniciálně normální hemoglobin > 10 g/dl (92 %) a prakticky u všech případů byla prokázána mutace exonu 11 (většinou v oblasti kodonu ). Léčba sunitinibem Pro imatinib rezistentní pacienty je v současnosti k dispozici 2. linie biologické léčby SU11248 sunitinib (Sutent ). Ve studiích fáze I/II byl demonstrován benefit sunitinibu proti placebu u imatinib rezistentních případů. Ve studii Heindricha (14) bylo sice dosaženo jen 8 % léčebných odpovědí, na druhou stranu většina ostatních pacientů docílila na delší stabilizaci pokročilé nemoci; dále ze závěrů studie vyplývá, že k sunitinibu jsou senzitivnější gastrointestinální stromální tumory s mutacemi exonu 9 či wild typy bez mutací oproti mutaci exonu 11 kit receptoru! Ve dvojitě slepé studii 3. fáze Demetriho a van Oosteroma (15) bylo 312 pa-
4 211 Tabulka 2. Přehled základních klinických studií s imatinibem mesylátem a jeho užitím u pokročilého gastrointestinálního stromálního nádoru Studie Fáze, design Glivec dávkování trvání N Počet pacientů Věk medián (roky) Léčebná odpověď (RR) Odhad PFS Celkové přežití (OS) Novartis study CSTI571-B2222 (USA, Finsko) Fáze II R, O, M 400 mg versus 600 mg 1 denně 34 měsíců medián FU (18 83) Po 34 měsících 1 % CR 67 % PR 16 % SD 84 týdnů čas do selhání léčby Medián přežití v 34 měsících EORTC, ISG & AGITG (Italie, Holandsko, Auastralie, Francie, Německo, Belgie, UK) Fáze III R, M 400 mg 1 denně 17 měsíců FU crossover 800 mg při progresi (18 91) 6 % CR 45 % PR 33 % SD 2.5 % PR 30 % SD Medián PFS 19 měsíců medián PFS 4 měsíce Medián přežití v 17 měsících 57 intergroup S0033 (USA, Kanada) Fáze III R, M 400 mg 2 roky FU crossover 800 mg při progresi (17 94) 3 % CR 45 % PR 27 % SD 6 % PR 32 % SD Ve 2 letech FU PFS 47 % Medián PFS 4 měsíce Medián ve 2 letech R = randomizovaná studie; O = otevřená studie; M = multicentrická studie cientů s imatinib rezistentním GIST randomizováno do 2 ramen do ramene s aktivní látkou, sunitinibem a do druhého ramene s placebem, kde až při případné progresi byli subjekti studie převedeni již do otevřeného ramene se sunitinibem. Sunitinib výrazně prodloužil čas do progrese (TTP), a to již při první interim analýze v rameni se sunitinibem byl TTP 6.3 měsíců (27.3 týdnů), kdežto v rameni s placebem pouhých TTP 1.5 měsíce (6.4 týdne). Sunitinib dále snížil riziko úmrtí v prvém roce follow-up o 51 %, jeho medián nebyl v reportované době follow-up dosažen. Po 6 měsících léčby přežívalo 79 % pacientů léčených sunitinibem a v rameni s placebem 6 měsíců přežívalo jen 57 % zařazených pacientů. V rameni se sunitinibem došlo k parciální léčebné odpovědi u 2 % pacientů, ke stabilizaci nemoci u dalších 17 % pacientů, kdežto v rameni s placebem došlo ke stabilizaci u 7 % pacientů, k léčebné odpovědi pochopitelně nedošlo u žádného subjektu. Léčba metastatického gastrointestinálního stromálního tumoru ostatními preparáty nilotinib, mtor, IPI-504 Pro třetí linii se jeví jako nejnadějnější nilotinib (AMN107), který byl aplikován ve studii fáze I u imatinib rezistentních nebo intolerantních, a to ve studii spolu s imatinibem v dávce 400 mg/den, nebo samotný v dávce 2 denně 400 mg (tj. 800 mg/den) (18). Z 18 pacientů léčených samotným nilotinibem byla u 1 pacienta dosažena parciální léčebná odpověď, dále u 13 pacientů stabilizace choroby. Celkem tedy u 14 pacientů z 18 bylo dosaženo léčebného benefitu (78 %), medián trvání léčebné odpovědi či stabilizace choroby byl 5.3 měsíců. V update této klinické studii fáze I (21) byl nilotinib aplikován pacientům s pokročilým GIST a s předchozím selháním imatinibu, sunitinibu, případně AMG 706 a to nilotinib buď v monoterapii 800 mg/den (2 denně 400 mg), nebo v různých dávkách (1 denně 200 mg, 1 denně 400 mg, 2 denně 200 mg nebo 2 denně 800 mg) spolu opět s imatinibem 400 mg/ den. Kombinace nilotinibu a imatinibu nevykázaly lepší léčebnou odpověď oproti plné dávce nilotinibu 2 denně 400 mg (800 mg/den). Monoterapie nilotinibem vykázala léčebný benefit 78 % (1 parciální léčebná odpověď a 13 stabilizace nemoci z 18 léčených) Klinická studie CAMN107A2201 (24) byla otevřená multicentrická studie a randomizovala do 2 otevřených ramen pacienty rezistentní na imatinib a sunitinib. Byla provedena randomizace v poměru 2:1 nilotinib 800 mg/den proti nejlepší podpůrné terapii (+ event. s imatinibem nebo sunitinibem dle uvážení zkoušejícího). Bylo randomizováno celkem 237 pacientů a primárním cílem bylo stanovení přežití bez progrese (PFS), sekundárními cíly počet léčebných odpovědí, trvání léčebné odpovědi, čas do dosažení léčebné odpovědi, čas do progrese (TTP), celkové přežití, bezpečnost a farmakokinetika nilotinibu. Klinická studie CAMN 107G2301 (25) zařazovala primárně metastatické případy GIST do primoléčby nilotinibem 800 mg/den nebo imatinibem 400 mg/den, byla přípustná předchozí adjuvance imatinibem 400 mg/den v odstupu delším než 6 měsíců od jejího skončení. V případě progrese v jednom rameni je umožněn switch do 2. ramene; u GIST s mutací exonu 9 C-kit receptoru byl imatinib aplikován v iniciální dávce 800 mg/den. Na velkém počtu pacientů (N = 736) je snaha zodpovědět hypotézu, zda multitarget nilotinib není výhodnější než imatinib již v 1. paliativní linii. Otevřená jednoramenná studie CAMN 107DDE06 zařadila do primoléčby nilotinibem zcela nepředléčené pacienty s pokročilým GIST (26). Klinická studie LANGIST (CAMN107DBR01) plánuje zařadit nepředléčené pacienty s pokročilým GIST do primoléčby nilotinibem 800 mg (randomizace léčba imatinibem v dávce 400 mg/den nebo imatinibem 800 mg/den s tím, že při progresi v jednom rameni možný cross-over do druhého ramene (27). Tato klinická studie již bude porovnávat účinnost léčby s intracelulární koncentrací obou preparátů (na preklinických modelech dosahuje nilotinib intracelulární koncentrace v buňkách GIST 7 10 vyšších než imatinib). V klinických studiích, které startovaly před započetím léčby 2. linie sunitibem, byla snaha překonat rezistenci na imatinib přidáním k pokračujícímu imatinibu inhibitor serin-threo ninové kinázy m-tor (mammalian target of rapamycine). V aplikaci imatinibu se pokračovalo většinou v nižší dávce (redukce z 800 mg na 600 mg) a byl nejčastěji zkoušen everolimus (RAD001) (16). Léčebný benefit ve většině malých studií fáze nedosahoval 30 % (u 7 pacientů z 18 pacientů léčených byl dosažen léčebný benefit 1 PR a 6 SD), ale toxicita, zejména hematologická, dále vomitus, kožní a jaterní toxicita nebyly v následné éře sunitinibu únosné k pokračování těchto studií prospektivně dále. Zajímavé se zprvu zdálo užití blokátoru heat shock proteinu (Hsp90) IPI-504. Jeho předchůdce AAG-17 byl znevýhodněn nízkou solubilitou, kdežto tento preparát je dobře rozpustný a byl v klinické studii fáze I aplikován 18 pacientům vesměs refrakterních na imatinib, sunitinib, nilotinib i gefinitib. Byl podáván bolusově v dávce ; 5 (4) Onkológia
5 mg/m 2 (nejčastěji však mg/m 2 ). U 12 pacientů z 18 léčených došlo k významné devitalizaci nádoru, dokumentované rychlým poklesem akumulace radioaktivně značené glukózy na PET vyšetření, dle RECIST hodnoceno jako stabilizace choroby (17). Již započatá pokračovací studie pro pacienty s pokročilým GIST refrakterním na imatinib však skončila zklamáním již během prvé interim analýzy a to pro vyšší morbiditu, ale i mortalitu v rameni s IPI-504 oproti ramenu s placebem; tato studie byla definitivně předčasně ukončena. Existují minimální data rovněž o užití sorafenibu a to u 21 pacientů v klinické studii Nimeriho bylo u 14 hodnotitelných dosaženo léčebného benefitu u 11 z nich (2 PR, 9 SD) a byl uveden čas přežití bez progrese (PFS) 13.3 měsíců. Další data o účinnosti sorafenibu již prezentována nebyla. Klinické studie stran účinnosti masatinibu a dasatinibu tyrozinkinázových blokátorů jsou na svém počátku; jsou koncipovány jako non-inferior studie s porovnáním proti imatinibu. Závěr Díky pokrokům cílené léčby se prognóza pacientů s pokročilým gastrointestinálním stromálním nádorem výrazně zlepšila. Počet léčebných odpovědí, který se pohybuje v prvé paliativní linii okolo 85 %, je v onkologické léčbě metastatických solidních nádorů celkem neobvyklý a přežití bez progrese na 1. linie léčby mnohdy i 5 7 let je zcela unikátní. I po progresi na iniciálním imatinibu lze provést eskalaci imatinibu, při další progresi lze aplikovat sunitinib. Rýsuje se možnost třetí linie nilotinibem. Je jasné, že v léčbě pokročilých GIST nemá již chemoterapie nebo radioterapie větší uplatnění. Adjuvantní roční terapie imatinibem u radikálně resekovaných GIST středního a vysokého rizika je podepřena natolik silnými klinickými daty, že o ní již nelze pochybovat. Je pravděpodobně jen otázkou času, kdy vážně vyvstane polemika o její délce zda neprodloužit adjuvanci na 2 3 roky. Neoadjuvantní indikaci biologické léčby u lokálně pokročilého nemetastatického GIST lze očekávat v nejbližší době. Tlačová správa Literatura 1. De Matteo R, Owzar K, et al. Adjuvant imatinib mesylate increases recurrence free survival (RFS) in patients with completely resected localized primary gastrointestinal stromal tumor (GIST): North American Intergroup Phase III trial ACOSOG Z9001; ASCO Blanke C. Evaluation of the Safety and Efficacy of an Oral Molecularly-Targeted Therapy, STI571, in Patients (Pts) with Unresectable or Metastatic Gastrointestinal Stromal Tumors (GISTS) Expressing C-KIT (CD117). ASCO Annual Meeting, abstract Van Oosterom, et al. Update of the Imatinib (STI571, Glivec) phase I study in gastro intestinal stromal tumours (GISTs). ASCO 2001, abstract Blanke C, Demetri G, et al. Efficacy and Safety of Imatinib Mesylate in Advanced Gastrointestinal Stromal Tumors. NEJM, 2002; 347: Verweij J, Casali PG, Zalcberg J, Le Cesne A, Reichardt P, Blay JY. Progression free survival in gastrointestinal stromal tumor with high a low dose imatinib: randomised trial. Lancet 2004; 364: Rankin C, Von Mehren M, Blanke C, Benjamin R, Fletcher ClD, Bramwell V. Dose effect of imatinib in patients with metastatic GIST: Phase III Sarcoma Group Study S0033 (abstract 9005), Proc ASCO 2004; 23: Van Glabbeke M, Verweij J, et al. Initial and late resistance to imatinib in advanced gastro-intestinal stromal tumor are predicted by different prognostic factors, an eortc-isg-agitg study. J Clin Oncol 2005; 23: Blay JY, Le Cesne A, et al. Prospective Multicenter Randomized Phase III Study of Imatinib in Patients With Advanced Gastrointestinal Stromal Tumors Comparing Interruption Versus Continuation of Treatment Beyond 1 Year: The French Sarmoma Group. J Clin Oncol 25: ios M, La Cesne A, et al. Interruption of imatinib in GIST patients with advanced diasease after one year of treatment: Updated results of the prospective French Sarcoma Group randomized phase III trial on long term survival. ASCO Ann Meet 2007, abstract Rutkowski P, et al. The outcomes of imatinib therapy gastrointestinal stromal tumors (GISTs) originating from the small bowel. ASCO Ann Meet 2007, abstract Van Glabbeke MM, Owzar K, Rankin C, et al. Comparison of two doses of imatinib for the treatment of unresectable or metastatic gastrointestinal stromal tumors (GIST): A meta metaanalysis based on patients. ASCO Ann Meet 2007, abstract Cioffi A, Emile JF, Domont J, et al. Long term progression-free-survival correlates with KIT/PDGFR mutational status in advanced GIST patients treated with imatinib (IM). ASCO Ann Meet 2007, abstract Bulusu VR, Jephcott CR, Fawcett S, Cook N, et al. RECIST and Choi criteria for response assessment (RA) in patients with inoperable and metastatic gastrointestinal stromal tumors on imatinib mesylate. Cambridge GIST study group experience. J Clin Oncol, 2007 ASCO Meet Proceed Part I, Vol 25, No 18S (June 20 Suppl), 2007: HeindrichMC, Maki RG, Corless CL, et al. Sunitinib response in imatinib resistant GIST correlates with KIT and PDGFR mutation status. J Clin Oncol 2006; 24: Demetri GD, van Oosterom AT, et al. Efficacy and safety of sunitinib in patients with advanced gastointestinal stromal tumour after failure of imatinib: a randomised controlled trial. Lancet 2006: Van Oosterom AT, Dumez H, Desai J, et al. Combination signal transduction inhibition: A phase I/II trial of the oral m- TOR-inhibitor everolimus (E, RAD001) and imatinib mesylate in patients with gastrointestinal stromal tumors refractory to imatinib mesylate. J Clin Oncol 2004, 22: Demetri GD. Inhibition of the Heat Shock Protein 90 (Hsp90) chaperone with the novel agent IPI-504 to overcome resistance to tyrosine kinase inhibitors (TKIs) in metastatic GIST: Updated results of a phase I trial ASCO Annual Meeting, Sarcoma. 18. Reichardt P, Casali PG, Blay J, Von Mehren M. A phase I study of AMN107 alone and in combination with imatinib in patients (pts) with imatinib-resistant gastrointestinal stromal tumors (GIST) ASCO Annual Meeting. 19. El-Rifai, Sarlomo-Rikala M, Andersson LC, et al. DNA sequence copy number changes in gastrointestinal stromal tumor: tumor progression and prognostic significance. Cancer Res 2000; 60: Data on file, Novartis UK Ltd. Study No STI571B2222. Open, randomized, phase II study of Glivec in patients with unresectable or metastatic malignant gastrointestinal stromal tumors expressing c-kit. Report 15 th December Von Mehren M, Reichardt P, Casali PG, Blay J. A phase I study of AMN107 alone and in combination with imatinib in patients (pts) with imatinib-resistant gastrointestinal stromal tumors (GIST) Study Update ASCO Meeting. 22. Zhan A, et al. Presented at: ASCO 2007, June 1 5, Chigaco; III; Abstract Clinical trial SSG XVIII; Available at: ct/show/nct CAMN107A2201; NCT Accessed October 26, CAMN107G2301; NCT Accessed October 26, CAMN107DDE06; NCT Accessed December 4, CAMN107DBR01; NCT Accessed October 26, Článok je prevzatý z Onkologie 2010; 4(1): MUDr. Zdeněk Linke Radioterapeuticko-onkologické oddělení, FN Motol V Úvalu 84, Praha 5 zdenek.linke@lfmotol.cuni.cz Nádejné liečivo novej generácie v onkológii Nemecká spoločnosť Boehringer Ingelheim predstavila na tohtoročnom stretnutí Americkej spoločnosti klinickej onkológie (ASCO) v dňoch júna sľubné výsledky ďalšej zo štúdií prebiehajúceho klinického skúšania účinnej látky BIBW Výsledky štúdie s novým orálne podávaným liečivom preukázali jeho účinnosť minimálne na úrovni cetuximabu pri liečbe rakoviny v oblasti hlavy a krku a potvrdili jeho účinnosť v terapii nemalobunkových pľúcnych karcinómov s mutáciou EGFR. BIBW 2992 je ďalšou generáciou inhibítorov tyrozín-kinázy, ktorá je cielená na receptor epidermálneho rastového faktora (EGFR/HER1) a na receptor ľudského epidermálneho faktora 2 (HER2). Mechanizmus účinku spočíva v ireverzibilnom naviazaní sa na receptor a je odlišný od všetkých ostatných dostupných foriem liečby v tejto triede.
Léčba pokročilého gastrointestinálního stromálního tumoru
 Léčba pokročilého gastrointestinálního stromálního tumoru Zdeněk Linke Onkologická klinika UK a 2. LF a FN Motol, Praha Gastrointestinální stromální tumor je nejčastějším neepiteliálním tumorem zažívacího
Léčba pokročilého gastrointestinálního stromálního tumoru Zdeněk Linke Onkologická klinika UK a 2. LF a FN Motol, Praha Gastrointestinální stromální tumor je nejčastějším neepiteliálním tumorem zažívacího
Gastrointestinální stromální nádor
 Gastrointestinální stromální nádor Endoskopický Seminář Jablonec nad Nisou 4.12.2012 Zdeněk Linke, KOC Motol, Praha 1 2 GIST: Primární lokalizace GIST může být primárně lokalizován kdekoli v GIT, peritoneu
Gastrointestinální stromální nádor Endoskopický Seminář Jablonec nad Nisou 4.12.2012 Zdeněk Linke, KOC Motol, Praha 1 2 GIST: Primární lokalizace GIST může být primárně lokalizován kdekoli v GIT, peritoneu
(Glivec)) u pacient s. nebo metastazujícím gastrointestináln tumorem na KOC Motol
 Zkušenosti s užitu itím imatinib mesylátu (Glivec)) u pacient s lokáln ln pokro ilým inoperabilním nebo metastazujícím gastrointestináln lním stromáln lním tumorem na KOC Motol Zden k Linke Komplexní onkologické
Zkušenosti s užitu itím imatinib mesylátu (Glivec)) u pacient s lokáln ln pokro ilým inoperabilním nebo metastazujícím gastrointestináln lním stromáln lním tumorem na KOC Motol Zden k Linke Komplexní onkologické
Gastrointestinální stromální tumor
 Gastrointestinální stromální tumor léčebné aspekty z pohledu chirurga Neoral Č.,Aujeský R.,Stašek M.,Vrba,R.,Janíková M.,Škarda J. I. chirurgická klinika LF UP a FN Olomouc Ústav patologické anatomie LF
Gastrointestinální stromální tumor léčebné aspekty z pohledu chirurga Neoral Č.,Aujeský R.,Stašek M.,Vrba,R.,Janíková M.,Škarda J. I. chirurgická klinika LF UP a FN Olomouc Ústav patologické anatomie LF
VÝZNAM DETEKCE MUTACÍ C-KIT ONKOGENU U ADENOIDNĚ CYSTICKÝCH KARCINOMŮ SLINNÝCH ŽLÁZ. M.Brož, I.Stárek, T.Bakaj
 VÝZNAM DETEKCE MUTACÍ C-KIT ONKOGENU U ADENOIDNĚ CYSTICKÝCH KARCINOMŮ SLINNÝCH ŽLÁZ M.Brož, I.Stárek, T.Bakaj Adenoidně cystický karcinom slinných žláz je druhým nejčastějším maligním tumorem slinných
VÝZNAM DETEKCE MUTACÍ C-KIT ONKOGENU U ADENOIDNĚ CYSTICKÝCH KARCINOMŮ SLINNÝCH ŽLÁZ M.Brož, I.Stárek, T.Bakaj Adenoidně cystický karcinom slinných žláz je druhým nejčastějším maligním tumorem slinných
M. Babjuk Urologická klinika 2.LF UK a FN Motol
 Operační léčba jako součást multimodálního přístupu k léčbě vysocerizikového karcinomu prostaty M. Babjuk Urologická klinika 2.LF UK a FN Motol Synopse Definice Výsledky a místo operační léčby Kombinace
Operační léčba jako součást multimodálního přístupu k léčbě vysocerizikového karcinomu prostaty M. Babjuk Urologická klinika 2.LF UK a FN Motol Synopse Definice Výsledky a místo operační léčby Kombinace
GastroIntestinální Stromální Tumory. Klinické zkušenosti s imatinibem, data z registru (register) MUDr. Kocáková Ilona, Ph.
 GastroIntestinální Stromální Tumory Klinické zkušenosti s imatinibem, data z registru (register) MUDr. Kocáková Ilona, Ph.D, KKOP, MOÚ Brno GIST: možnosti léčby Chirurgická léčba 1,2 základní léčba primárního
GastroIntestinální Stromální Tumory Klinické zkušenosti s imatinibem, data z registru (register) MUDr. Kocáková Ilona, Ph.D, KKOP, MOÚ Brno GIST: možnosti léčby Chirurgická léčba 1,2 základní léčba primárního
9. ZHOUBNÝ NOVOTVAR MĚKKÝCH TKÁNÍ (C38, 47-49)
 9. ZHOUBNÝ NOVOTVAR MĚKKÝCH TKÁNÍ (C38, 47-49) Léčba sarkomů měkkých tkání by měla být vedena na základě rozhodnutí multioborového týmu (ortoped, hrudní chirurg, příp. cévní, plastický chirurg, radiodiagnostik,
9. ZHOUBNÝ NOVOTVAR MĚKKÝCH TKÁNÍ (C38, 47-49) Léčba sarkomů měkkých tkání by měla být vedena na základě rozhodnutí multioborového týmu (ortoped, hrudní chirurg, příp. cévní, plastický chirurg, radiodiagnostik,
SYSTÉMOVÁ LÉČBA NÁDORŮ MOČOVÉHO MĚCHÝŘE
 SYSTÉMOVÁ LÉČBA NÁDORŮ MOČOVÉHO MĚCHÝŘE Jana Katolická FN u svaté Anny, Brno CZ/ONCO/617/0088 1 UROTELIÁLNÍ KARCINOM MOČOVÉHO MĚCHÝŘE CHEMOSENZITIVNÍ ONEMOCNĚNÍ. V době stanovení diagnózy je 15 % lokálně
SYSTÉMOVÁ LÉČBA NÁDORŮ MOČOVÉHO MĚCHÝŘE Jana Katolická FN u svaté Anny, Brno CZ/ONCO/617/0088 1 UROTELIÁLNÍ KARCINOM MOČOVÉHO MĚCHÝŘE CHEMOSENZITIVNÍ ONEMOCNĚNÍ. V době stanovení diagnózy je 15 % lokálně
Radioterapie po radikální prostatektomii
 Radioterapie po radikální prostatektomii Štěpán Veselý Urologická klinika UK 2. LF a FN Motol, Praha ART po RRP - ART (aplikace u high-risk do 90 dnů po operaci) high-risk: - pozitivní chirurgické okraje
Radioterapie po radikální prostatektomii Štěpán Veselý Urologická klinika UK 2. LF a FN Motol, Praha ART po RRP - ART (aplikace u high-risk do 90 dnů po operaci) high-risk: - pozitivní chirurgické okraje
Nové chemoterapeutické režimy u karcinomu prsu. Miloš Holánek, Ji í Vysko il KKOP, MOÚ Brno
 Nové chemoterapeutické režimy u karcinomu prsu Miloš Holánek, Jií Vyskoil KKOP, MOÚ Brno Úvod Terapeutické modality u karcinomu prsu: - chirurgická léba -hormonoterapie -radioterapie - chemoterapie - cílená
Nové chemoterapeutické režimy u karcinomu prsu Miloš Holánek, Jií Vyskoil KKOP, MOÚ Brno Úvod Terapeutické modality u karcinomu prsu: - chirurgická léba -hormonoterapie -radioterapie - chemoterapie - cílená
22. ZHOUBNÝ NOVOTVAR MĚKKÝCH TKÁNÍ (C48-49)
 22. ZHOUBNÝ NOVOTVAR MĚKKÝCH TKÁNÍ (C48-49) Léčba sarkomů měkkých tkání by měla být vedena na základě rozhodnutí multioborového týmu (ortoped, hrudní chirurg, příp. cévní, plastický chirurg, radiodiagnostik,
22. ZHOUBNÝ NOVOTVAR MĚKKÝCH TKÁNÍ (C48-49) Léčba sarkomů měkkých tkání by měla být vedena na základě rozhodnutí multioborového týmu (ortoped, hrudní chirurg, příp. cévní, plastický chirurg, radiodiagnostik,
Systémová léčba gastrointestinálních stromálních nádorů. Bohuslav Melichar Onkologická klinika LF UP a FN Olomouc
 Systémová léčba gastrointestinálních stromálních nádorů Bohuslav Melichar Onkologická klinika LF UP a FN Olomouc Sarkomy měkkých tkání Skupina nádorových onemocnění heterogenní z pohledu histologie, biologického
Systémová léčba gastrointestinálních stromálních nádorů Bohuslav Melichar Onkologická klinika LF UP a FN Olomouc Sarkomy měkkých tkání Skupina nádorových onemocnění heterogenní z pohledu histologie, biologického
Biologická léčba karcinomu prsu. Prof. MUDr. Jitka Abrahámová, DrSc. Onkologická klinika 1.LF UK a TN KOC (NNB+VFN+TN)
 Biologická léčba karcinomu prsu Prof. MUDr. Jitka Abrahámová, DrSc. Onkologická klinika 1.LF UK a TN KOC (NNB+VFN+TN) Cílená léčba Ca prsu Trastuzumab (HercepNn) AnN HER2 neu pronlátka LapaNnib (Tyverb)
Biologická léčba karcinomu prsu Prof. MUDr. Jitka Abrahámová, DrSc. Onkologická klinika 1.LF UK a TN KOC (NNB+VFN+TN) Cílená léčba Ca prsu Trastuzumab (HercepNn) AnN HER2 neu pronlátka LapaNnib (Tyverb)
9. ZHOUBNÝ NOVOTVAR MĚKKÝCH TKÁNÍ (C36, C38, 47-49)
 9. ZHOUBNÝ NOVOTVAR MĚKKÝCH TKÁNÍ (C36, C38, 47-49) Léčba sarkomů měkkých tkání by měla být vedena na základě rozhodnutí multioborového týmu (ortoped, hrudní chirurg, příp. cévní, plastický chirurg, radiodiagnostik,
9. ZHOUBNÝ NOVOTVAR MĚKKÝCH TKÁNÍ (C36, C38, 47-49) Léčba sarkomů měkkých tkání by měla být vedena na základě rozhodnutí multioborového týmu (ortoped, hrudní chirurg, příp. cévní, plastický chirurg, radiodiagnostik,
Přínos molekulární genetiky pro diagnostiku a terapii malignit GIT v posledních 10 letech
 Přínos molekulární genetiky pro diagnostiku a terapii malignit GIT v posledních 10 letech Minárik M. Centrum aplikované genomiky solidních nádorů (CEGES), Genomac výzkumný ústav, Praha XXIV. JARNÍ SETKÁNÍ
Přínos molekulární genetiky pro diagnostiku a terapii malignit GIT v posledních 10 letech Minárik M. Centrum aplikované genomiky solidních nádorů (CEGES), Genomac výzkumný ústav, Praha XXIV. JARNÍ SETKÁNÍ
22. ZHOUBNÝ NOVOTVAR MĚKKÝCH TKÁNÍ (C38, C47-49)
 22. ZHOUBNÝ NOVOTVAR MĚKKÝCH TKÁNÍ (C38, C47-49) Léčba sarkomů měkkých tkání by měla být vedena na základě rozhodnutí multioborového týmu (ortoped, hrudní chirurg, příp. cévní, plastický chirurg, radiodiagnostik,
22. ZHOUBNÝ NOVOTVAR MĚKKÝCH TKÁNÍ (C38, C47-49) Léčba sarkomů měkkých tkání by měla být vedena na základě rozhodnutí multioborového týmu (ortoped, hrudní chirurg, příp. cévní, plastický chirurg, radiodiagnostik,
22. ZHOUBNÝ NOVOTVAR MĚKKÝCH TKÁNÍ (C48-49)
 22. ZHOUBNÝ NOVOTVAR MĚKKÝCH TKÁNÍ (C48-49) Léčba sarkomů měkkých tkání by měla být vedena na základě rozhodnutí multioborového týmu (ortoped, hrudní chirurg, příp. cévní, plastický chirurg, radiodiagnostik,
22. ZHOUBNÝ NOVOTVAR MĚKKÝCH TKÁNÍ (C48-49) Léčba sarkomů měkkých tkání by měla být vedena na základě rozhodnutí multioborového týmu (ortoped, hrudní chirurg, příp. cévní, plastický chirurg, radiodiagnostik,
Chemoterapie pokročil kolorektáln. karcinomu
 Chemoterapie pokročil ilého kolorektáln lního karcinomu Jindřich ich FínekF Chemoterapie pokročil ilého kolorektáln lního karcinomu v prvé linii Incidence ve světě Incidence a mortalita v ČR Stádia onemocnění
Chemoterapie pokročil ilého kolorektáln lního karcinomu Jindřich ich FínekF Chemoterapie pokročil ilého kolorektáln lního karcinomu v prvé linii Incidence ve světě Incidence a mortalita v ČR Stádia onemocnění
CORECT - VECTIBIX. Klinický registr pacientů s metastatickým kolorektálním karcinomem. Stav registru k datu
 CORECT - VECTIBIX Klinický registr pacientů s metastatickým kolorektálním karcinomem Stav registru k datu 26. 3. 2012 Management projektu: Analýza dat: Technické zajištění: Mgr. Karel Hejduk, Ing. Petr
CORECT - VECTIBIX Klinický registr pacientů s metastatickým kolorektálním karcinomem Stav registru k datu 26. 3. 2012 Management projektu: Analýza dat: Technické zajištění: Mgr. Karel Hejduk, Ing. Petr
9. ZHOUBNÝ NOVOTVAR MĚKKÝCH TKÁNÍ (C36, C38, 47-49)
 9. ZHOUBNÝ NOVOTVAR MĚKKÝCH TKÁNÍ (C36, C38, 47-49) Léčba sarkomů měkkých tkání by měla být vedena na základě rozhodnutí multioborového týmu (ortoped, chirurg se sarkomovou erudicí, hrudní chirurg, příp.
9. ZHOUBNÝ NOVOTVAR MĚKKÝCH TKÁNÍ (C36, C38, 47-49) Léčba sarkomů měkkých tkání by měla být vedena na základě rozhodnutí multioborového týmu (ortoped, chirurg se sarkomovou erudicí, hrudní chirurg, příp.
STUDIE 2014 KLINIKA ONKOLOGIE A RADIOTERAPIE AKTIVNÍ NÁBOR PACIENTŮ
 STUDIE 2014 KLINIKA ONKOLOGIE A RADIOTERAPIE AKTIVNÍ NÁBOR PACIENTŮ KARCINOM PRSU Spoluzkoušející: MUDr.Iva Slánská, MUDr.Peter Priester,MUDr.Adam Paulík Název studie : PH3-01 Studie Present Prevence recidivy
STUDIE 2014 KLINIKA ONKOLOGIE A RADIOTERAPIE AKTIVNÍ NÁBOR PACIENTŮ KARCINOM PRSU Spoluzkoušející: MUDr.Iva Slánská, MUDr.Peter Priester,MUDr.Adam Paulík Název studie : PH3-01 Studie Present Prevence recidivy
3.3 KARCINOM SLINIVKY BŘIŠNÍ
 3.3 KARCINOM SLINIVKY BŘIŠNÍ Epidemiologie Zhoubné nádory pankreatu se vyskytují převážně ve vyšším věku po 60. roce života, převážně u mužů. Zhoubné nádory pankreatu Incidence a mortalita v České republice
3.3 KARCINOM SLINIVKY BŘIŠNÍ Epidemiologie Zhoubné nádory pankreatu se vyskytují převážně ve vyšším věku po 60. roce života, převážně u mužů. Zhoubné nádory pankreatu Incidence a mortalita v České republice
Analýza dat z klinického registru RenIS České onkologické společnosti ČLS JEP shrnutí výsledků pro elektronický report
 Účinnost a bezpečnost přípravku Afinitor (everolimus) v léčbě pacientů s pokročilým karcinomem ledviny v podmínkách reálné klinické praxe v České republice Analýza dat z klinického registru RenIS České
Účinnost a bezpečnost přípravku Afinitor (everolimus) v léčbě pacientů s pokročilým karcinomem ledviny v podmínkách reálné klinické praxe v České republice Analýza dat z klinického registru RenIS České
RADIOTERAPIE. karcinom prostaty s vysokým rizikem
 RADIOTERAPIE karcinom prostaty s vysokým rizikem K. Odrážka Oddělení klinické a radiační onkologie Multiscan s.r.o., Pardubická krajská nemocnice a.s. 1. a 3. LF UK v Praze IPVZ Praha POOPERAČNÍ RT Indikace
RADIOTERAPIE karcinom prostaty s vysokým rizikem K. Odrážka Oddělení klinické a radiační onkologie Multiscan s.r.o., Pardubická krajská nemocnice a.s. 1. a 3. LF UK v Praze IPVZ Praha POOPERAČNÍ RT Indikace
Léčba endokrinních nádorů-máme co nabídnout?
 Léčba endokrinních nádorů-máme co nabídnout? MUDr. Eugen Kubala Klinika Radioterapie a Onkologie Fakultní nemocnice Hradec Králové Sokolská 581, 500 05 Hradec Králové Co jsou neuroendokrinní tumory? Heterogenní
Léčba endokrinních nádorů-máme co nabídnout? MUDr. Eugen Kubala Klinika Radioterapie a Onkologie Fakultní nemocnice Hradec Králové Sokolská 581, 500 05 Hradec Králové Co jsou neuroendokrinní tumory? Heterogenní
LÉ BA PACIENT S GIST PREPARÁTEM GLIVEC ZKUŠENOSTI A LÉ EBNÉ VÝSLEDKY Z MOÚ. Kocáková Ilona
 LÉ BA PACIENT S GIST PREPARÁTEM GLIVEC ZKUŠENOSTI A LÉ EBNÉ VÝSLEDKY Z MOÚ Kocáková Ilona Definice GIST V etenobun né i i epiteloidní, výjime n pleiomofní mezenchymální nádory trávicího ústrojí, exprimující
LÉ BA PACIENT S GIST PREPARÁTEM GLIVEC ZKUŠENOSTI A LÉ EBNÉ VÝSLEDKY Z MOÚ Kocáková Ilona Definice GIST V etenobun né i i epiteloidní, výjime n pleiomofní mezenchymální nádory trávicího ústrojí, exprimující
Registr Herceptin Karcinom prsu
 I. Primární diagnostika Registr Herceptin Karcinom prsu Vstupní parametry Rok narození Věk Kód zdravotní pojišťovny (výběr) o 111 o 201 o 205 o 207 o 209 o 211 o 213 o 217 o 222 Datum stanovení diagnózy
I. Primární diagnostika Registr Herceptin Karcinom prsu Vstupní parametry Rok narození Věk Kód zdravotní pojišťovny (výběr) o 111 o 201 o 205 o 207 o 209 o 211 o 213 o 217 o 222 Datum stanovení diagnózy
Léčebné predikce u karcinomu prsu pro rok 2013 chystané novinky
 Léčebné predikce u karcinomu prsu pro rok 2013 chystané novinky Prof. MUDr. Jitka Abrahámová, DrSc Onkologická klinika TN a 1. LF UK KOC (NNB + VFN + TN) St Gallén 2011 Rozsah onemocnění T, N, M ER, PgR
Léčebné predikce u karcinomu prsu pro rok 2013 chystané novinky Prof. MUDr. Jitka Abrahámová, DrSc Onkologická klinika TN a 1. LF UK KOC (NNB + VFN + TN) St Gallén 2011 Rozsah onemocnění T, N, M ER, PgR
Léčba DLBCL s nízkým rizikem
 Léčba DLBCL s nízkým rizikem Jan Hudeček Klinika hematológie a transfuziológie JLF UK a UNM, Martin Lymfómové fórum 2014 Bratislava, 21. 23. 3. 2014 Difuzní velkobuněčný B-lymfom (DLBCL) heterogenní skupina
Léčba DLBCL s nízkým rizikem Jan Hudeček Klinika hematológie a transfuziológie JLF UK a UNM, Martin Lymfómové fórum 2014 Bratislava, 21. 23. 3. 2014 Difuzní velkobuněčný B-lymfom (DLBCL) heterogenní skupina
Několik poznámek k diagnostice a léčbě diferencovaných karcinomů štítné žlázy (DTC) Otakar Kraft, Martin Havel Klinika nukleární medicíny FN Ostrava
 Několik poznámek k diagnostice a léčbě diferencovaných karcinomů štítné žlázy (DTC) Otakar Kraft, Martin Havel Klinika nukleární medicíny FN Ostrava 51. Dny nukleární medicíny Seč 12.-14.11.2014 Úvod Cíle
Několik poznámek k diagnostice a léčbě diferencovaných karcinomů štítné žlázy (DTC) Otakar Kraft, Martin Havel Klinika nukleární medicíny FN Ostrava 51. Dny nukleární medicíny Seč 12.-14.11.2014 Úvod Cíle
Jak dlouho podávat adjuvantní LHRH analoga? Stanislav Batko Radioterap.-onkol. Odd FNM
 Jak dlouho podávat adjuvantní LHRH analoga? Stanislav Batko Radioterap.-onkol. Odd FNM Krátce na úvod hypothalamus hypofýza ovarium X X X Pokles tvorby estradiolu Goserelin Blokáda tvorby LH mamma LHRH
Jak dlouho podávat adjuvantní LHRH analoga? Stanislav Batko Radioterap.-onkol. Odd FNM Krátce na úvod hypothalamus hypofýza ovarium X X X Pokles tvorby estradiolu Goserelin Blokáda tvorby LH mamma LHRH
Metastatický renální karcinom Andrašina Tomáš
 Metastatický renální karcinom Andrašina Tomáš Department of Radiology and Nuclear Medicine, University Hospital Brno and Medical Faculty, Masaryk University, Brno, Czech Republic Renální karcinom 25-30
Metastatický renální karcinom Andrašina Tomáš Department of Radiology and Nuclear Medicine, University Hospital Brno and Medical Faculty, Masaryk University, Brno, Czech Republic Renální karcinom 25-30
Význam endosonografie v diagnostice GIST. R.Repák
 GIST NET 2013 Litomyšl 29.-30.112013 Význam endosonografie v diagnostice GIST. R.Repák II.interní gastroenterologická klinika FN a LF UK Hradec Králové GIST - definice se vyvíjí - kontroverze, progenitorové
GIST NET 2013 Litomyšl 29.-30.112013 Význam endosonografie v diagnostice GIST. R.Repák II.interní gastroenterologická klinika FN a LF UK Hradec Králové GIST - definice se vyvíjí - kontroverze, progenitorové
Novinky v léčbě. Úvod: Srdeční selhání epidemie 21. století. Prof. MUDr. Jindřich Špinar, CSc., FESC Interní kardiologická klinika FN Brno
 Novinky v léčbě Úvod: Srdeční selhání epidemie 21. století Prof. MUDr. Jindřich Špinar, CSc., FESC Interní kardiologická klinika FN Brno PARADIGM-HF: Design studie Randomizace n=8442 Dvojitě slepá Léčebná
Novinky v léčbě Úvod: Srdeční selhání epidemie 21. století Prof. MUDr. Jindřich Špinar, CSc., FESC Interní kardiologická klinika FN Brno PARADIGM-HF: Design studie Randomizace n=8442 Dvojitě slepá Léčebná
Velcade První výsledky z IHOK FN Brno. Luděk Pour. Roman Hájek, Marta Krejčí,Andrea Křivanová, Lenka Zahradová, Zdeněk Adam CMG
 Velcade První výsledky z IHOK FN Brno Luděk Pour Roman Hájek, Marta Krejčí,Andrea Křivanová, Lenka Zahradová, Zdeněk Adam CZECH CMG M Y E L O M A GROUP Č ESKÁ MYELOMOVÁ SKUPINA Velcade = bortezomib Nobelova
Velcade První výsledky z IHOK FN Brno Luděk Pour Roman Hájek, Marta Krejčí,Andrea Křivanová, Lenka Zahradová, Zdeněk Adam CZECH CMG M Y E L O M A GROUP Č ESKÁ MYELOMOVÁ SKUPINA Velcade = bortezomib Nobelova
= lokálně pokročilý CaP + lokalizovaný (ct1, ct2) se špatnými prognostickými faktory ct3a PSA > 20 ng/ml GS > 7
 Léčba vysocerizikového karcinomu prostaty pohled urologa M. Babjuk Urologická klinika 2.LF UK a FN Motol High-risk CaP = lokálně pokročilý CaP + lokalizovaný (ct1, ct2) se špatnými prognostickými faktory
Léčba vysocerizikového karcinomu prostaty pohled urologa M. Babjuk Urologická klinika 2.LF UK a FN Motol High-risk CaP = lokálně pokročilý CaP + lokalizovaný (ct1, ct2) se špatnými prognostickými faktory
ŽIVOTNÍ CYKLUS LÉKŮ KLINICKÉ HODNOCENÍ STUDIE. Kateřina Kopečková FN Motol, Praha
 ŽIVOTNÍ CYKLUS LÉKŮ KLINICKÉ HODNOCENÍ STUDIE Kateřina Kopečková FN Motol, Praha Klinická hodnocení LP Nedílnou součásti vývoje léčiva Navazují na preklinický výzkum Pacienti jsou subjekty hodnocení V
ŽIVOTNÍ CYKLUS LÉKŮ KLINICKÉ HODNOCENÍ STUDIE Kateřina Kopečková FN Motol, Praha Klinická hodnocení LP Nedílnou součásti vývoje léčiva Navazují na preklinický výzkum Pacienti jsou subjekty hodnocení V
9. ZHOUBNÝ NOVOTVAR MĚKKÝCH TKÁNÍ (C36, C38, 47-49)
 9. ZHOUBNÝ NOVOTVAR MĚKKÝCH TKÁNÍ (C36, C38, 47-49) Léčba sarkomů měkkých tkání by měla být vedena na základě rozhodnutí multioborového týmu (ortoped, chirurg se sarkomovou erudicí, hrudní chirurg, příp.
9. ZHOUBNÝ NOVOTVAR MĚKKÝCH TKÁNÍ (C36, C38, 47-49) Léčba sarkomů měkkých tkání by měla být vedena na základě rozhodnutí multioborového týmu (ortoped, chirurg se sarkomovou erudicí, hrudní chirurg, příp.
Hodnocení segmentu centrové léčby z dat plátců zdravotní péče. Společné pracoviště ÚZIS ČR a IBA MU
 Hodnocení segmentu centrové léčby z dat plátců zdravotní péče Společné pracoviště ÚZIS ČR a IBA MU Realita současné české medicíny: úspěšné výsledky léčby = podstatné prodlužování doby života pacienta
Hodnocení segmentu centrové léčby z dat plátců zdravotní péče Společné pracoviště ÚZIS ČR a IBA MU Realita současné české medicíny: úspěšné výsledky léčby = podstatné prodlužování doby života pacienta
Nádory podjaterní krajiny Onkologická terapie. Doc. MUDr. Martina Kubecová, Ph.D. Radioterapeutická a onkologická klinika 3. LF UK a FNKV, Praha
 Nádory podjaterní krajiny Onkologická terapie Doc. MUDr. Martina Kubecová, Ph.D. Radioterapeutická a onkologická klinika 3. LF UK a FNKV, Praha Český a slovenský gastroenterologický kongres 13.11.2015
Nádory podjaterní krajiny Onkologická terapie Doc. MUDr. Martina Kubecová, Ph.D. Radioterapeutická a onkologická klinika 3. LF UK a FNKV, Praha Český a slovenský gastroenterologický kongres 13.11.2015
RENIS - Votrient. Klinický registr pacientů s renálním karcinomem. Stav registru k datu 26. 3. 2012
 RENIS - Votrient Klinický registr pacientů s renálním karcinomem Stav registru k datu 26. 3. 2012 Management projektu: Analýza dat: Technické zajištění: Mgr. Karel Hejduk, Ing. Petr Brabec Mgr. Zbyněk
RENIS - Votrient Klinický registr pacientů s renálním karcinomem Stav registru k datu 26. 3. 2012 Management projektu: Analýza dat: Technické zajištění: Mgr. Karel Hejduk, Ing. Petr Brabec Mgr. Zbyněk
STIVARGA (REGORAFENIB)
 NÁDORY TLUSTÉHO STŘEVA A REKTA 31 STIVARGA (REGORAFENIB) Kolektiv autorů Úvod Regorafenib (Stivarga ) je nový perorální multikinázový inhibitor, který byl v roce 2013 registrován pro léčbu dospělých pacientů
NÁDORY TLUSTÉHO STŘEVA A REKTA 31 STIVARGA (REGORAFENIB) Kolektiv autorů Úvod Regorafenib (Stivarga ) je nový perorální multikinázový inhibitor, který byl v roce 2013 registrován pro léčbu dospělých pacientů
Možnosti léčby CRPC s časem přibývají
 Možnosti léčby CRPC s časem přibývají Jana Katolická Onkologicko-chirurgické oddělení Fakultní nemocnice u Sv. Anny Mnoho studií - jen čtyři nové léky Enzalutamid Abirateron + prednison Cabazitaxel Radium-223
Možnosti léčby CRPC s časem přibývají Jana Katolická Onkologicko-chirurgické oddělení Fakultní nemocnice u Sv. Anny Mnoho studií - jen čtyři nové léky Enzalutamid Abirateron + prednison Cabazitaxel Radium-223
AKTUÁLNÍ VÝSLEDKY KLINICKÝCH STUDIÍ
 SEKCE NÁDORY PRSU PŮVODNÍ SDĚLENÍ AKTUÁLNÍ VÝSLEDKY KLINICKÝCH STUDIÍ Letošní konference ASCO 2017 přinesla řadu zajímavých výsledků a naději na opětovné zlepšení přežití pacientů so solidními nádory,
SEKCE NÁDORY PRSU PŮVODNÍ SDĚLENÍ AKTUÁLNÍ VÝSLEDKY KLINICKÝCH STUDIÍ Letošní konference ASCO 2017 přinesla řadu zajímavých výsledků a naději na opětovné zlepšení přežití pacientů so solidními nádory,
Vliv způsobu podání bortezomibu na účinnost a bezpečnost léčby pacientů s mnohočetným myelomem. MUDr. P. Pavlíček FN KV a 3.
 Vliv způsobu podání bortezomibu na účinnost a bezpečnost léčby pacientů s mnohočetným myelomem MUDr. P. Pavlíček FN KV a 3. LF UK Praha Tato prezentace vznikla s finanční podporou společnosti Johnson &
Vliv způsobu podání bortezomibu na účinnost a bezpečnost léčby pacientů s mnohočetným myelomem MUDr. P. Pavlíček FN KV a 3. LF UK Praha Tato prezentace vznikla s finanční podporou společnosti Johnson &
STRUKTURA REGISTRU MPM
 STRUKTURA REGISTRU MPM 1. Vstupní parametry 1. Kouření (výběr) 1. Kuřák 2. Bývalý kuřák (rok před stanovením DG - dle WHO) 3. Nekuřák 4. Neuvedeno 2. Výška [cm] (reálné číslo) 3. Hmotnost pacienta v době
STRUKTURA REGISTRU MPM 1. Vstupní parametry 1. Kouření (výběr) 1. Kuřák 2. Bývalý kuřák (rok před stanovením DG - dle WHO) 3. Nekuřák 4. Neuvedeno 2. Výška [cm] (reálné číslo) 3. Hmotnost pacienta v době
R.A. Burger, 1 M.F. Brady, 2 J. Rhee, 3 M.A. Sovak, 3 H. Nguyen, 3 M.A. Bookman 4
 NEZÁVISLÉ RADIOLOOGICKÉ HODNOCENÍ STUDIE FÁZE III GOG218 S BEVACIZUMABEM (BEV) V PRIMÁRNÍ LÉČBĚ POKROČILÉHO EPITELOVÉHO NÁDORU VAJEČNÍKŮ, PRIMÁRNÍHO NÁDORU PERITONEA NEBO VEJCOVODŮ. R.A. Burger, 1 M.F.
NEZÁVISLÉ RADIOLOOGICKÉ HODNOCENÍ STUDIE FÁZE III GOG218 S BEVACIZUMABEM (BEV) V PRIMÁRNÍ LÉČBĚ POKROČILÉHO EPITELOVÉHO NÁDORU VAJEČNÍKŮ, PRIMÁRNÍHO NÁDORU PERITONEA NEBO VEJCOVODŮ. R.A. Burger, 1 M.F.
Skalický Tomáš,Třeška V.,Liška V., Fichtl J., Brůha J. CHK LFUK a FN Plzeň Loket 2015
 Skalický Tomáš,Třeška V.,Liška V., Fichtl J., Brůha J. CHK LFUK a FN Plzeň Loket 2015 Kdy můžeme resekovat jaterní metastázy KRCa? 1. synchronně s primárním karcinomem 2. po resekci primárního karcinomu
Skalický Tomáš,Třeška V.,Liška V., Fichtl J., Brůha J. CHK LFUK a FN Plzeň Loket 2015 Kdy můžeme resekovat jaterní metastázy KRCa? 1. synchronně s primárním karcinomem 2. po resekci primárního karcinomu
2. pražské mezioborové onkologické kolokvium Prague ONCO 2011
 Záštitu nad kolokviem převzaly: Evropská onkologická společnost Ministerstvo školství, mládeže a tělovýchovy ČR Ministerstvo zdravotnictví ČR Česká onkologická společnost Česká urologická společnost Česká
Záštitu nad kolokviem převzaly: Evropská onkologická společnost Ministerstvo školství, mládeže a tělovýchovy ČR Ministerstvo zdravotnictví ČR Česká onkologická společnost Česká urologická společnost Česká
VYŠETŘOVÁNÍ MUTACÍ c-kit a pdgfrα U GASTROINTESTINÁLNÍCH STROMÁLNÍCH NÁDORŮ K DOPLNĚNÍ INDIKACE TERAPIE IMATINIB MESYLÁTEM
 VYŠETŘOVÁNÍ MUTACÍ c-kit a pdgfrα U GASTROINTESTINÁLNÍCH STROMÁLNÍCH NÁDORŮ K DOLNĚNÍ INDIKACE TERAIE IMATINIB MESYLÁTEM Augustiňáková Alena, Hilská Irena, Kalinová Markéta, Břízová Helena Kodet Roman
VYŠETŘOVÁNÍ MUTACÍ c-kit a pdgfrα U GASTROINTESTINÁLNÍCH STROMÁLNÍCH NÁDORŮ K DOLNĚNÍ INDIKACE TERAIE IMATINIB MESYLÁTEM Augustiňáková Alena, Hilská Irena, Kalinová Markéta, Břízová Helena Kodet Roman
Protonová radioterapie
 Protonová radioterapie Vítek P. Proton Therapy Center Czech Prague, Czech republic Protonová radioterapie (PRT) Benefit? (translace fyzikální výhody do výhody klinické) Léčená onemocnění Ekonomický aspekt
Protonová radioterapie Vítek P. Proton Therapy Center Czech Prague, Czech republic Protonová radioterapie (PRT) Benefit? (translace fyzikální výhody do výhody klinické) Léčená onemocnění Ekonomický aspekt
Pomalidomid první rok léčby v ČR
 C Z E C H G R O U P CZECH GROUP 1 Pomalidomid první rok léčby v ČR Luděk Pour IHOK FN Brno XIII. Výroční setkání CMG 10. 4. 2015 Mikulov C M G M Y E L O M A Č E S K Á M YE LO M O VÁ S K U P IN A CMG ČESKÁ
C Z E C H G R O U P CZECH GROUP 1 Pomalidomid první rok léčby v ČR Luděk Pour IHOK FN Brno XIII. Výroční setkání CMG 10. 4. 2015 Mikulov C M G M Y E L O M A Č E S K Á M YE LO M O VÁ S K U P IN A CMG ČESKÁ
Revlimid v léčbě myelomu u nemocných s renální insuficiencí MUDr. Jan Straub
 Revlimid v léčbě myelomu u nemocných s renální insuficiencí MUDr. Jan Straub Updated December 2009. 1 Závěry s ASH 2009 Len-Dex u rr MM s úpravou dávkování v závislosti na stupni renální insuficience Soubor
Revlimid v léčbě myelomu u nemocných s renální insuficiencí MUDr. Jan Straub Updated December 2009. 1 Závěry s ASH 2009 Len-Dex u rr MM s úpravou dávkování v závislosti na stupni renální insuficience Soubor
Nové možnosti. terapeutického ovlivnění pokročilého karcinomu prostaty. Mám nádor prostaty a co dál? Jana Katolická
 MEZINÁRODNÍ CENTRUM KLINICKÉHO VÝZKUMU Nové možnosti TVOŘÍME BUDOUCNOST MEDICÍNY terapeutického ovlivnění pokročilého karcinomu prostaty Jana Katolická Primář onkologicko-chirurgické oddělení Mám nádor
MEZINÁRODNÍ CENTRUM KLINICKÉHO VÝZKUMU Nové možnosti TVOŘÍME BUDOUCNOST MEDICÍNY terapeutického ovlivnění pokročilého karcinomu prostaty Jana Katolická Primář onkologicko-chirurgické oddělení Mám nádor
CEBO: (Center for Evidence Based Oncology) Incidence Kostních příhod u nádorů prsu PROJEKT IKARUS. Neintervenční epidemiologická studie
 CEBO: (Center for Evidence Based Oncology) Incidence Kostních příhod u nádorů prsu PROJEKT Neintervenční epidemiologická studie PROTOKOL PROJEKTU Verze: 4.0 Datum: 26.09.2006 Strana 2 PROTOKOL PROJEKTU
CEBO: (Center for Evidence Based Oncology) Incidence Kostních příhod u nádorů prsu PROJEKT Neintervenční epidemiologická studie PROTOKOL PROJEKTU Verze: 4.0 Datum: 26.09.2006 Strana 2 PROTOKOL PROJEKTU
Léčba MM LP Revlimid v ČR - aktuální analýza dat RMG
 Léčba MM LP Revlimid v ČR - aktuální analýza dat RMG Statistická analýza 262 pacientů Vladimír Maisnar za II. interní klinika OKH FN a LF UK Hradec Králové Léčba MM LP Revlimid v ČR Látka patřící do skupiny
Léčba MM LP Revlimid v ČR - aktuální analýza dat RMG Statistická analýza 262 pacientů Vladimír Maisnar za II. interní klinika OKH FN a LF UK Hradec Králové Léčba MM LP Revlimid v ČR Látka patřící do skupiny
Lze předvídat výsledek léčby bevacizumabem u metastatického kolorektálního karcinomu na základě stavu onkogenu K-ras? Komentář
 Lze předvídat výsledek léčby bevacizumabem u metastatického kolorektálního karcinomu na základě stavu onkogenu K-ras? MUDr. Jiří Tomášek Komentář MUDr. Pavel Vítek, Ph.D. Lze předvídat výsledek léčby
Lze předvídat výsledek léčby bevacizumabem u metastatického kolorektálního karcinomu na základě stavu onkogenu K-ras? MUDr. Jiří Tomášek Komentář MUDr. Pavel Vítek, Ph.D. Lze předvídat výsledek léčby
1. EPIDEMIOLOGIE ZHOUBNÉHO NOVOTVARU MOČOVÉHO MĚCHÝŘE (C67) V ČESKÉ REPUBLICE - AKTUÁLNÍ STAV 12
 OBSAH KARCINOM MOČOVĚHO MĚCHÝŘE I 1. EPIDEMIOLOGIE ZHOUBNÉHO NOVOTVARU MOČOVÉHO MĚCHÝŘE (C67) V ČESKÉ REPUBLICE - AKTUÁLNÍ STAV 12 2. DIAGNOSTIKA A SLEDOVÁNI PACIENTŮ S TUMORY MĚCHÝŘE SYSTÉMEM EVIS EXERA
OBSAH KARCINOM MOČOVĚHO MĚCHÝŘE I 1. EPIDEMIOLOGIE ZHOUBNÉHO NOVOTVARU MOČOVÉHO MĚCHÝŘE (C67) V ČESKÉ REPUBLICE - AKTUÁLNÍ STAV 12 2. DIAGNOSTIKA A SLEDOVÁNI PACIENTŮ S TUMORY MĚCHÝŘE SYSTÉMEM EVIS EXERA
Chirurgické možnosti řešení rhabdomyosarkomu pánve u mladé pacientky v rámci multimodálního přístupu
 Chirurgické možnosti řešení rhabdomyosarkomu pánve u mladé pacientky v rámci multimodálního přístupu Macík D. 1, Doležel J. 1, Múdry P. 2, Zerhau P. 3, Staník M. 1, Čapák I. 1 1 ODDĚLENÍ UROLOGICKÉ ONKOLOGIE,
Chirurgické možnosti řešení rhabdomyosarkomu pánve u mladé pacientky v rámci multimodálního přístupu Macík D. 1, Doležel J. 1, Múdry P. 2, Zerhau P. 3, Staník M. 1, Čapák I. 1 1 ODDĚLENÍ UROLOGICKÉ ONKOLOGIE,
OPERAČNÍ LÉČBA KARCINOMU PROSTATY
 MEZINÁRODNÍ CENTRUM KLINICKÉHO VÝZKUMU TVOŘÍME BUDOUCNOST MEDICÍNY OPERAČNÍ LÉČBA KARCINOMU PROSTATY Petr Filipenský Primář Urologického oddělení Seminář pro pacienty Mám rakovinu prostaty, co dál? 08.11.2018
MEZINÁRODNÍ CENTRUM KLINICKÉHO VÝZKUMU TVOŘÍME BUDOUCNOST MEDICÍNY OPERAČNÍ LÉČBA KARCINOMU PROSTATY Petr Filipenský Primář Urologického oddělení Seminář pro pacienty Mám rakovinu prostaty, co dál? 08.11.2018
Léčba mrcc. Jindřich Fínek Alena Dvořáková FN a LF UK v Plzni
 Léčba mrcc Jindřich Fínek Alena Dvořáková FN a LF UK v Plzni Možnosti systémové léčby Látka Název Registrace EU Účinek Indikace sunitinib Sutent 01/2007 VEGFR-TKI 1.Linie (dobrá a středně d.p.) sorafenib
Léčba mrcc Jindřich Fínek Alena Dvořáková FN a LF UK v Plzni Možnosti systémové léčby Látka Název Registrace EU Účinek Indikace sunitinib Sutent 01/2007 VEGFR-TKI 1.Linie (dobrá a středně d.p.) sorafenib
Presidio Ospedaliero di Livorno
 Aprile Jasná perspektiva role inhibitorů tyrozinkinázy (TKI) EGFR Piano Generale Istituto Toscano di Tumori Emergenza Presidio Ospedaliero di Livorno Livorno-Italy Viale Alfieri 36 Federico Cappuzzo Ospedale
Aprile Jasná perspektiva role inhibitorů tyrozinkinázy (TKI) EGFR Piano Generale Istituto Toscano di Tumori Emergenza Presidio Ospedaliero di Livorno Livorno-Italy Viale Alfieri 36 Federico Cappuzzo Ospedale
Opakované resekce jater pro metastázy kolorektálního karcinomu
 Opakované resekce jater pro metastázy kolorektálního karcinomu Visokai V., Lipská L., Mráček M., Levý M. Chirurgická klinika 1. LF UK a Fakultní Thomayerovy nemocnice v Praze přednosta Doc. MUDr. V. Visokai,
Opakované resekce jater pro metastázy kolorektálního karcinomu Visokai V., Lipská L., Mráček M., Levý M. Chirurgická klinika 1. LF UK a Fakultní Thomayerovy nemocnice v Praze přednosta Doc. MUDr. V. Visokai,
20. ZHOUBNÉ NOVOTVARY HLAVY A KRKU (C00-14, C30-32)
 20. ZHOUBNÉ NOVOTVARY HLAVY A KRKU (C00-14, C30-32) Léčba nádorů hlavy a krku je velmi komplexní. Volba léčebné strategie závisí na lokalizaci primárního nádoru a jeho histologickém typu, přítomnosti regionálních
20. ZHOUBNÉ NOVOTVARY HLAVY A KRKU (C00-14, C30-32) Léčba nádorů hlavy a krku je velmi komplexní. Volba léčebné strategie závisí na lokalizaci primárního nádoru a jeho histologickém typu, přítomnosti regionálních
TORISEL. Kocák I. NÁDORY LEDVIN A MOČOVÉHO MĚCHÝŘE 43 O O
 NÁDRY LEDVIN A MČVÉH MĚCHÝŘE 43 TRISEL Kocák I. Úvod Torisel (temsirolimus, CCI- 779) patří do skupiny látek, tzv. m- TR inhibitorů. Temsirolimus má dva základní mechanizmy účinku: kontroluje buněčné dělení
NÁDRY LEDVIN A MČVÉH MĚCHÝŘE 43 TRISEL Kocák I. Úvod Torisel (temsirolimus, CCI- 779) patří do skupiny látek, tzv. m- TR inhibitorů. Temsirolimus má dva základní mechanizmy účinku: kontroluje buněčné dělení
Udržovací léčba: zamířeno na anti-vegf léčbu Alan Sandler
 Udržovací léčba: zamířeno na anti-vegf léčbu Alan Sandler Department of Hematology/Oncology Oregon Health and Science University Knight Cancer Institute Portland, OR, USA Medián OS (měsíce) Studie v 1.linii
Udržovací léčba: zamířeno na anti-vegf léčbu Alan Sandler Department of Hematology/Oncology Oregon Health and Science University Knight Cancer Institute Portland, OR, USA Medián OS (měsíce) Studie v 1.linii
24. ZHOUBNÝ NOVOTVAR ŠTÍTNÉ ŽLÁZY (C73)
 24. ZHOUBNÝ NOVOTVAR ŠTÍTNÉ ŽLÁZY (C73) 24.1 Diferencovaný karcinom štítné žlázy Papilární karcinom představuje 40 80% a folikulární karcinom 15 % tyreoidálních malignit. Léčba diferencovaných karcinomů
24. ZHOUBNÝ NOVOTVAR ŠTÍTNÉ ŽLÁZY (C73) 24.1 Diferencovaný karcinom štítné žlázy Papilární karcinom představuje 40 80% a folikulární karcinom 15 % tyreoidálních malignit. Léčba diferencovaných karcinomů
Nové léčebné možnosti v terapii metastazujícího karcinomu žaludku
 Nové léčebné možnosti v terapii metastazujícího karcinomu žaludku Prof. MUDr. Jitka Abrahámová, DrSc. Onkologická klinika 1. LF UK a TN KOC (NNB+VFN+TN) Žaludek pravidla klasifikace Klasifikace se používá
Nové léčebné možnosti v terapii metastazujícího karcinomu žaludku Prof. MUDr. Jitka Abrahámová, DrSc. Onkologická klinika 1. LF UK a TN KOC (NNB+VFN+TN) Žaludek pravidla klasifikace Klasifikace se používá
GIST je nejčastější sarkom
 GIST je nejčastější sarkom GIST: Definice Vřetenobuněčné Mesenchymové nádory Lokalizované primárně v GIT, omentu a mesenteriu Obvykle pozitivní barvení pro KIT (CD 117) Kulatobuněčné 8% Jiné (mesenterium,
GIST je nejčastější sarkom GIST: Definice Vřetenobuněčné Mesenchymové nádory Lokalizované primárně v GIT, omentu a mesenteriu Obvykle pozitivní barvení pro KIT (CD 117) Kulatobuněčné 8% Jiné (mesenterium,
Možnosti využití technologie DNA microarrays v predikci odpovědi na neoadjuvantní terapii u pacientů s karcinomem jícnu
 Možnosti využití technologie DNA microarrays v predikci odpovědi na neoadjuvantní terapii u pacientů s karcinomem jícnu Srovnal J. 1, Cincibuch J. 2, Cwierkta K. 2, Melichar B. 2, Aujeský R. 3, Vrba R.
Možnosti využití technologie DNA microarrays v predikci odpovědi na neoadjuvantní terapii u pacientů s karcinomem jícnu Srovnal J. 1, Cincibuch J. 2, Cwierkta K. 2, Melichar B. 2, Aujeský R. 3, Vrba R.
Režimy s nízkým rizikem FN riziko do 10 % Režimy se středním rizikem FN riziko 10 19% Režimy s vysokým rizikem FN riziko 20 a více procent
 Portál DIOS verze II Druhá verze portálu DIOS a jeho elektronické knihovny chemorežimů přináší nové informace a nové nástroje týkající se problematiky toxicity chemoterapie. Jde především o problematiku
Portál DIOS verze II Druhá verze portálu DIOS a jeho elektronické knihovny chemorežimů přináší nové informace a nové nástroje týkající se problematiky toxicity chemoterapie. Jde především o problematiku
IMUNOTERAPIE NÁDORŮ MOČOVÉHO MĚCHÝŘE. Michaela Matoušková
 IMUNOTERAPIE NÁDORŮ MOČOVÉHO MĚCHÝŘE Michaela Matoušková IMUNOTERAPIE ZN Z UROTELU lokalizovaná onemocnění - BCG VAKCÍNA pokročilá onemocnění BCG VAKCÍNA po instilaci vazba BCG k fibronektinu produkovanému
IMUNOTERAPIE NÁDORŮ MOČOVÉHO MĚCHÝŘE Michaela Matoušková IMUNOTERAPIE ZN Z UROTELU lokalizovaná onemocnění - BCG VAKCÍNA pokročilá onemocnění BCG VAKCÍNA po instilaci vazba BCG k fibronektinu produkovanému
: Medikamentózní léčba kastračně rezistentního karcinomu. Prof. MUDr. Jitka Abrahámová, DrSc. Onkologická klinika 1. LF UK a TN KOC ( NNB+VFN+TN )
 : Medikamentózní léčba kastračně rezistentního karcinomu Prof. MUDr. Jitka Abrahámová, DrSc. Onkologická klinika 1. LF UK a TN KOC ( NNB+VFN+TN ) Vývoj standardizované incidence a úmrtnosv ( na 100 000
: Medikamentózní léčba kastračně rezistentního karcinomu Prof. MUDr. Jitka Abrahámová, DrSc. Onkologická klinika 1. LF UK a TN KOC ( NNB+VFN+TN ) Vývoj standardizované incidence a úmrtnosv ( na 100 000
Cílená léčba metastatického renálního karcinomu, možnosti sekvenční léčby: současný pohled
 115 Cílená léčba metastatického renálního karcinomu, možnosti sekvenční léčby: současný pohled MUDr. Alexandr Poprach, Ph.D. 1, doc. MUDr. Tomáš Büchler, Ph.D. 2, MUDr. Radek Lakomý, Ph.D. 1, MUDr. Jiří
115 Cílená léčba metastatického renálního karcinomu, možnosti sekvenční léčby: současný pohled MUDr. Alexandr Poprach, Ph.D. 1, doc. MUDr. Tomáš Büchler, Ph.D. 2, MUDr. Radek Lakomý, Ph.D. 1, MUDr. Jiří
Czech Society for Oncology / Česká onkologická společnost ČLS JEP
 www.linkos.cz Czech Society for Oncology / Česká onkologická společnost ČLS JEP Best of ASCO Meeting Licensed by the American Society of Clinical Oncology, www.asco.org September 8 th, 2012 / 8. září 2012
www.linkos.cz Czech Society for Oncology / Česká onkologická společnost ČLS JEP Best of ASCO Meeting Licensed by the American Society of Clinical Oncology, www.asco.org September 8 th, 2012 / 8. září 2012
Thalidomid analýza 292 pacientů s MM léčených na IHOK FN Brno
 Thalidomid analýza 292 pacientů s MM léčených na IHOK FN Brno Marta Krejčí, Petra Kaisarová Základní charakteristika souboru (zahájení léčby thalidomidem) Základní charakteristika Pohlaví muži 146 (5.%)
Thalidomid analýza 292 pacientů s MM léčených na IHOK FN Brno Marta Krejčí, Petra Kaisarová Základní charakteristika souboru (zahájení léčby thalidomidem) Základní charakteristika Pohlaví muži 146 (5.%)
Přehled klinických studií u CLL v ČR v roce 2014
 Přehled klinických studií u CLL v ČR v roce 2014 Datum aktualizace: 28. 3. 2014 Zpracoval: dr. Špaček,VFN Praha, martin.spacek2@vfn.cz http://www.cll.cz Klinické studie v ČR 2014 Lenalidomid imunomodulace
Přehled klinických studií u CLL v ČR v roce 2014 Datum aktualizace: 28. 3. 2014 Zpracoval: dr. Špaček,VFN Praha, martin.spacek2@vfn.cz http://www.cll.cz Klinické studie v ČR 2014 Lenalidomid imunomodulace
Nové možnos* v nechirugické léčbě gynekologických nádorů. Jiří Petera Klinika onkologie a radioterapie FN a LF Hradec Králové
 Nové možnos* v nechirugické léčbě gynekologických nádorů Jiří Petera Klinika onkologie a radioterapie FN a LF Hradec Králové Nové techniky radioterapie a jejich využih u nádorů cervixu a endometria IMRT,
Nové možnos* v nechirugické léčbě gynekologických nádorů Jiří Petera Klinika onkologie a radioterapie FN a LF Hradec Králové Nové techniky radioterapie a jejich využih u nádorů cervixu a endometria IMRT,
Postavení taxanů a anthracyklinů v terapii karcinomu prsu. MUDr. Tomáš Svoboda KMO, Medlov
 Postavení taxanů a anthracyklinů v terapii karcinomu prsu MUDr. Tomáš Svoboda KMO, Medlov 14.6.2008 EBCTCG Meta-analýza 2005-06 Mortalita na karcinom prsu Taxany > Anthra > CMF > Bez Chemo 50 10-y přínos
Postavení taxanů a anthracyklinů v terapii karcinomu prsu MUDr. Tomáš Svoboda KMO, Medlov 14.6.2008 EBCTCG Meta-analýza 2005-06 Mortalita na karcinom prsu Taxany > Anthra > CMF > Bez Chemo 50 10-y přínos
Jak dlouho léčit tromboembolickou nemoc? MUDr. Petr Kessler Odd. hematologie a transfuziologie Nemocnice Pelhřimov
 Jak dlouho léčit tromboembolickou nemoc? MUDr. Petr Kessler Odd. hematologie a transfuziologie Nemocnice Pelhřimov 1995 Six weeks versus six months. 40% provokovaných trombóz Schulman Six weeks versus.
Jak dlouho léčit tromboembolickou nemoc? MUDr. Petr Kessler Odd. hematologie a transfuziologie Nemocnice Pelhřimov 1995 Six weeks versus six months. 40% provokovaných trombóz Schulman Six weeks versus.
Klinická studie CMG stav příprav. Roman Hájek. Velké Bílovice CMG CZECH GROUP M Y E L O M A Č ESKÁ MYELOMOVÁ SKUPINA
 Klinická studie 2006 - stav příprav Roman Hájek Velké Bílovice 8.4.2006 Č ESKÁ MYELOMOVÁ SKUPINA Klinické studie s cílem dosáhnout dlouhodobého přežití 20% v období 1995-2006 ROK 1996 ROK 2002 ROK 2006
Klinická studie 2006 - stav příprav Roman Hájek Velké Bílovice 8.4.2006 Č ESKÁ MYELOMOVÁ SKUPINA Klinické studie s cílem dosáhnout dlouhodobého přežití 20% v období 1995-2006 ROK 1996 ROK 2002 ROK 2006
TARCEVA klinický registr
 TARCEVA klinický registr Karcinom pankreatu Stav k datu 10. 4. 2011 Registr Tarceva je podporován výzkumným ý grantem firmy Roche. Česká onkologická společnost Institut biostatistiky a analýz Stav registru
TARCEVA klinický registr Karcinom pankreatu Stav k datu 10. 4. 2011 Registr Tarceva je podporován výzkumným ý grantem firmy Roche. Česká onkologická společnost Institut biostatistiky a analýz Stav registru
24. ZHOUBNÝ NOVOTVAR ŠTÍTNÉ ŽLÁZY (C73)
 24. ZHOUBNÝ NOVOTVAR ŠTÍTNÉ ŽLÁZY (C73) 24.1 Diferencovaný karcinom štítné žlázy Papilární karcinom představuje 40 80% a folikulární karcinom 15 % tyreoidálních malignit. Léčba diferencovaných karcinomů
24. ZHOUBNÝ NOVOTVAR ŠTÍTNÉ ŽLÁZY (C73) 24.1 Diferencovaný karcinom štítné žlázy Papilární karcinom představuje 40 80% a folikulární karcinom 15 % tyreoidálních malignit. Léčba diferencovaných karcinomů
Modul obecné onkochirurgie
 Modul obecné onkochirurgie 1. Principy kancerogeneze, genetické a epigenetické faktory 2. Onkogeny, antionkogeny, reparační geny, instabilita nádorového genomu 3. Nádorová proliferace a apoptóza, důsledky
Modul obecné onkochirurgie 1. Principy kancerogeneze, genetické a epigenetické faktory 2. Onkogeny, antionkogeny, reparační geny, instabilita nádorového genomu 3. Nádorová proliferace a apoptóza, důsledky
Terapie mnohočetného myelomu poznatky z ASH 2004
 Terapie mnohočetného myelomu poznatky z ASH 2004 December 3-7, 2004, San Diego, USA Marta Krejčí Prezentace ASH meeting 2004 Celkem 3669 abstrakt, z toho 846 formou přednášek, 2823 formou posterů Mnohočetný
Terapie mnohočetného myelomu poznatky z ASH 2004 December 3-7, 2004, San Diego, USA Marta Krejčí Prezentace ASH meeting 2004 Celkem 3669 abstrakt, z toho 846 formou přednášek, 2823 formou posterů Mnohočetný
NOVINKY V DIAGNOSTICE A LÉČBĚ NEHODKINOVÝCH LYMFOMŮ
 NOVINKY V DIAGNOSTICE A LÉČBĚ NEHODKINOVÝCH LYMFOMŮ Martin Šimkovič IV. interní hematologická klinika Fakultní nemocnice Lékařská fakulta Univerzity Karlovy Hradec Králové Seminář - Novinky v léčbě lymfoproliferací,
NOVINKY V DIAGNOSTICE A LÉČBĚ NEHODKINOVÝCH LYMFOMŮ Martin Šimkovič IV. interní hematologická klinika Fakultní nemocnice Lékařská fakulta Univerzity Karlovy Hradec Králové Seminář - Novinky v léčbě lymfoproliferací,
POOPERAČNÍ ANALGEZIE MORPHINEM NEGATIVNĚ OVLIVŇUJE MINIMÁLNÍ REZIDUÁLNÍ CHOROBU A PŘEŽÍVÁNÍ PACIENTŮ PO RADIKÁLNÍ RESEKCI KOLOREKTÁLNÍHO KARCINOMU
 POOPERAČNÍ ANALGEZIE MORPHINEM NEGATIVNĚ OVLIVŇUJE MINIMÁLNÍ REZIDUÁLNÍ CHOROBU A PŘEŽÍVÁNÍ PACIENTŮ PO RADIKÁLNÍ RESEKCI KOLOREKTÁLNÍHO KARCINOMU RETROSPEKTIVNÍ STUDIE Petr Prášil 1, Emil Berta 2,3 1
POOPERAČNÍ ANALGEZIE MORPHINEM NEGATIVNĚ OVLIVŇUJE MINIMÁLNÍ REZIDUÁLNÍ CHOROBU A PŘEŽÍVÁNÍ PACIENTŮ PO RADIKÁLNÍ RESEKCI KOLOREKTÁLNÍHO KARCINOMU RETROSPEKTIVNÍ STUDIE Petr Prášil 1, Emil Berta 2,3 1
Dostupnost kvalitní léčby, informovanost pacienta. Jana Prausová Komplexní onkologické centrum FN v Motole Seminář Standardy léčby rakoviny prsu
 Dostupnost kvalitní léčby, informovanost pacienta Jana Prausová Komplexní onkologické centrum FN v Motole Seminář Standardy léčby rakoviny prsu Epidemiologie Epidemiologie Epidemiologie Epidemiologie Epidemiologie
Dostupnost kvalitní léčby, informovanost pacienta Jana Prausová Komplexní onkologické centrum FN v Motole Seminář Standardy léčby rakoviny prsu Epidemiologie Epidemiologie Epidemiologie Epidemiologie Epidemiologie
PŘEHLED KLINICKÝCH AKTIVIT
 PŘEHLED KLINICKÝCH AKTIVIT CLINICAL TRIAL 4W 7 th Annual Report Multicentrická randomizovaná studie 4W Datum zahájení studie : 15. 4. 1996 Datum ukončení náběru: 3. 2002 Datum zjištění mediánu přežití:
PŘEHLED KLINICKÝCH AKTIVIT CLINICAL TRIAL 4W 7 th Annual Report Multicentrická randomizovaná studie 4W Datum zahájení studie : 15. 4. 1996 Datum ukončení náběru: 3. 2002 Datum zjištění mediánu přežití:
Systémová léčba lokálně pokročilých a metastatických GEP-NET
 Systémová léčba lokálně pokročilých a metastatických GEP-NET Jiří Tomášek Masarykův onkologický ústav, Brno Vzácné nádory a raritní stavy v oblasti GITu Seminář pro onkology, gastroenterology,radiology
Systémová léčba lokálně pokročilých a metastatických GEP-NET Jiří Tomášek Masarykův onkologický ústav, Brno Vzácné nádory a raritní stavy v oblasti GITu Seminář pro onkology, gastroenterology,radiology
Možnosti léčby CRPC. Michaela Matoušková
 Možnosti léčby CRPC Michaela Matoušková Pokročilý karcinom prostaty prevalence CaP 65215 pokročilý CaP st. III 8492 st. IV 5884 14376 CRPC cca 900-1000 Zdroj dat www.uroweb.cz CRPC Kastrační hladina testosteronu
Možnosti léčby CRPC Michaela Matoušková Pokročilý karcinom prostaty prevalence CaP 65215 pokročilý CaP st. III 8492 st. IV 5884 14376 CRPC cca 900-1000 Zdroj dat www.uroweb.cz CRPC Kastrační hladina testosteronu
XOFIGO (RADIUM-223 DICHLORID) V LÉČBĚ METASTATICKÉHO KASTRAČNĚ REZISTENTNÍHO KARCINOMU PROSTATY
 NÁDORY PROSTATY 63 XOFIGO (RADIUM-223 DICHLORID) V LÉČBĚ METASTATICKÉHO KASTRAČNĚ REZISTENTNÍHO KARCINOMU PROSTATY Kolektiv autorů Úvod Léčivý přípravek (radium-223 dichlorid) byl 13. listopadu 2013 schválen
NÁDORY PROSTATY 63 XOFIGO (RADIUM-223 DICHLORID) V LÉČBĚ METASTATICKÉHO KASTRAČNĚ REZISTENTNÍHO KARCINOMU PROSTATY Kolektiv autorů Úvod Léčivý přípravek (radium-223 dichlorid) byl 13. listopadu 2013 schválen
Obsah. Autoři. Předmluva. Introduction. Úvod. 1. Patogeneze a biologie metastatického procesu (Aleš Rejthar) 1.1. Typy nádorového růstu
 Obsah Autoři Předmluva Introduction Úvod 1. Patogeneze a biologie metastatického procesu (Aleš Rejthar) 1.1. Typy nádorového růstu 1.2. Šíření maligních nádorů 1.3. Souhrn 1.4. Summary 2. Obecné klinické
Obsah Autoři Předmluva Introduction Úvod 1. Patogeneze a biologie metastatického procesu (Aleš Rejthar) 1.1. Typy nádorového růstu 1.2. Šíření maligních nádorů 1.3. Souhrn 1.4. Summary 2. Obecné klinické
Studie probíhající v Onkologickém centru FNKV Praha Karcinom prsu:
 Studie probíhající v Onkologickém centru FNKV Praha Karcinom prsu: ALTTO EGF 106708 Adjuvantní biologická terapie po skončení adjuvantní chemoterapie nebo v kombinaci s ní. Studie má 4 ramena: trastuzumab
Studie probíhající v Onkologickém centru FNKV Praha Karcinom prsu: ALTTO EGF 106708 Adjuvantní biologická terapie po skončení adjuvantní chemoterapie nebo v kombinaci s ní. Studie má 4 ramena: trastuzumab
Východiska. Čtvrtá nejčastější příčina úmrtí na nádorová onemocní u žen, v celém světě je ročně nových onemocnění a úmrtí
 ICON7: studie fáze III Gynaecologic Cancer InterGroup (GCIG) s přidáním bevacizumabu ke standardní chemoterapii u žen s nově diagnostikovaným epitelovým nádorem vaječníků, primárním nádorem pobřišnice
ICON7: studie fáze III Gynaecologic Cancer InterGroup (GCIG) s přidáním bevacizumabu ke standardní chemoterapii u žen s nově diagnostikovaným epitelovým nádorem vaječníků, primárním nádorem pobřišnice
PREDIKTORY ČÁSTEČNÉ VS. KOMPLETNÍ SYMPTOMATICKÉ ODPOVĚDI U PACIENTŮ S ACHALÁZIÍ JÍCNU PO PERORÁLNÍ ENDOSKOPICKÉ MYOTOMII (POEM)
 PREDIKTORY ČÁSTEČNÉ VS. KOMPLETNÍ SYMPTOMATICKÉ ODPOVĚDI U PACIENTŮ S ACHALÁZIÍ JÍCNU PO PERORÁLNÍ ENDOSKOPICKÉ MYOTOMII (POEM) Vacková Z, Švecová H, Štirand P, Špičák J, Krajčíová J, Fremundová L, Loudová
PREDIKTORY ČÁSTEČNÉ VS. KOMPLETNÍ SYMPTOMATICKÉ ODPOVĚDI U PACIENTŮ S ACHALÁZIÍ JÍCNU PO PERORÁLNÍ ENDOSKOPICKÉ MYOTOMII (POEM) Vacková Z, Švecová H, Štirand P, Špičák J, Krajčíová J, Fremundová L, Loudová
Co mě může potkat při návratu onemocnění. Nové přístupy biologická léčba karcinomu prostaty. MUDr. Hana Študentová, Ph.D.
 Co mě může potkat při návratu onemocnění. Nové přístupy biologická léčba karcinomu prostaty MUDr. Hana Študentová, Ph.D. Obsah Obecný úvod Androgenní signalizace Možnosti systémové léčby Závěr Koho se
Co mě může potkat při návratu onemocnění. Nové přístupy biologická léčba karcinomu prostaty MUDr. Hana Študentová, Ph.D. Obsah Obecný úvod Androgenní signalizace Možnosti systémové léčby Závěr Koho se
Přínos snížení srdeční frekvence u srdečního selhání
 Přínos snížení srdeční frekvence u srdečního selhání Jaromír Hradec 3. interní klinika 1. LF UK a VFN Praha Things we knew, things we did Things we have learnt, things we should do O ČEM BUDU MLUVIT: 1.
Přínos snížení srdeční frekvence u srdečního selhání Jaromír Hradec 3. interní klinika 1. LF UK a VFN Praha Things we knew, things we did Things we have learnt, things we should do O ČEM BUDU MLUVIT: 1.
Standard. Zhoubné nádory pankreatu Incidence a mortalita v České republice (2014) ZN slinivky břišní MUŽI ŽENY CELKEM
 /7. Epidemiologie: Karcinom slinivky břišní je celosvětově čtvrtou nejčastější příčinou úmrtí na nádorové onemocnění a Česká republika je druhou zemí s nejvyšší incidencí tohoto onemocnění. Incidence karcinomu
/7. Epidemiologie: Karcinom slinivky břišní je celosvětově čtvrtou nejčastější příčinou úmrtí na nádorové onemocnění a Česká republika je druhou zemí s nejvyšší incidencí tohoto onemocnění. Incidence karcinomu
