II. TERMOMECHANIKA SMĚSI PLYNŮ, PAR A VLHKÉHO VZDUCHU
|
|
|
- Vlastimil Esterka
- před 8 lety
- Počet zobrazení:
Transkript
1 II. ERMOMECHANIKA SMĚSI PLYNŮ, PAR A VLHKÉHO VZDUCHU.0 Směsi ynů Nejběžnější směsí ynů je atmosférický vzduch. Je to směs dusíku, kysíku a v menší míře jsou zastoueny oid uhičitý, vodík a neatrné množství vzácných ynů. Zváštním říadem jsou směsi ynů a řehřátých ar jiné átky nař. vzduchu a řehřátých vodních ar. Směsi ynů jsou také výfukové yny saovacích teených strojů. Směsi ynů nejsou anaogické směsím mechanickým, oněvadž jejich jednotivé sožky nemůžem čistě mechanickou cestou od sebe odděit. Směsi ynů jsou směsi moeku ynů, a roto jsou anaogické roztokům. Pro směsi ynů, které vznikají bez rodukce nebo otřeby tea, atí Datonův zákon, ode kterého každý yn ve směsi si řídí vastními rovnicemi stavu, omocí nichž ze určit tak řísušný danému objemu a teotě. ak každého jednotivého ynu ve směsi o určité teotě se nazývá arciání (částečný) tak. Parciání tak ynu je takový tak, jaký by mě yn, kdyby v ceém rostoru by sám ři dané teotě směsi. ak směsi () je roven součtu arciáních taků ( i ) sožek směsi (Datonův zákon). = = i (II ). Poměr sožek směsi ynů Poměr každé sožky k ceé směsi ze vyjádřit jako oměr jejích hmotností nebo oměr jejich objemů. yto oměry se navzájem iší. Poměr hmotnosti jednotivých ynů (m i ) k hmotnosti směsi (m) se nazývá oměrná hmotnost (σ i ) nebo také hmotnostní koncentrace sožky ve směsi: σ i = m m i (II ) Pro směs ak atí: Σσ + σ σ = σ i = 0 (II 3) yto hmotnostní odíy se zravida udávají v rocentech. Nař. ro suchý vzduch bez říměsí je σ N = 77 % a O σ = 3 %. 3
2 Poměr ynů jednotivých sožek (V i ) k objemu ceé směsi (V) se nazývá oměrný objem (ω i ) nebo také objemová koncentrace sožky ve směsi: V ω i = i (II 4) V kde V i je objem sožky ve směsi objemu V, redukovaný na týž měrný tak () a tutéž teotu jako má směs. ento redukovaný objem (V i ) se nazývá arciání objem. Redukovaný arciání objem (V i ) se stanoví z Boy Mariotova zákona: i V = V i odkud i Vi = V (II 5) Objem směsi (V) je ak dán součtem arciáních objemů (V i ): V + V V = V i = V (II 6) Obdobně atí: ω + ω ω = ω i = (II 7) I objemové odíy se zravida udávají v rocentech objemu směsi. Objemové a hmotnostní odíy se iší, rotože se yny iší měrnými hmotnostmi (σ i ). Pro suchý vzduch bez říměsí je ω N = 79 % a ω O = %.. Měrný objem (v) a měrná hmotnost (ρ) směsi Objem sožky směsi je dán součinem její hmotnosti (m i ) a jejího měrného objemu (v i ). Objem směsi (V) je dán: V = m v = m v + m v m v = m i v i (II 8) odkud měrný objem směsi (v) je dán: v = m m v + m m v + + nebo s oužitím rovnice II : m v = m m i vi (II 9) m v = σ v + σ v σ v = σ (II 0) o zavedení měrné hmotnosti sožek ρ i = /v i bude i v i 4
3 σi v = (II ) ρ i a měrná hmotnost směsi (ρ) bude dána: ρ = = (II ) v σi ρ i Hmotnost směsi (m) ze také vyjádřit násedovně: M = V ρ = V i ρ i odkud s oužitím rovnice II 4 bude měrná hmotnost (ρ) dána: Vi ρ = ρ i = ωiρi (II 3) V.3 Stavová rovnice směsi Pro sožky směsi o objemu V a teotě atí rovnice stavu: V = m r V = m r V = m r (II 4) Pode Datonova zákona atí: = = i (II 5) a ro směs atí: V = ( ) V = (m r + m r + + m r ) = = m r (II 6) odkud r = m r + m m r m m r (II 7) m nebo r = σ r + σ r σ r = σ (II 8) Pynová konstanta směsi je dána součtem součinů oměrných hmotností a ynových konstant jednotivých sožek směsí. i r i 5
4 .4 Parciání tak sožek Je-i směs určena oměrnými hmotnostmi sožek (σ i ), ze arciání tak sožky stanovit z její rovnice stavu: i V = m i r i (II 9) rovnice stavu směsi je: V = m r (II 0) Z odíu obou rovnic (II 9 a 0): i r = σi i (II ) r ze vyjádřit arciání tak ( i ) sožky ve směsi: i = σ i r r i (II ) Je-i směs dána objemovými odíy sožek, ak se vychází z rovnice: i V = V i (II 3) odkud arciání tak ( i ) sožky ve směsi je dán rovnicí: i = V V i = ωi (II 4).5 Měrná teená kaacita směsi Měrná teená kaacita směsi (c) se určuje z měrných teených kaacit jednotivých sožek. Z rovnosti teených energií směsi a sožek směsi: c m = c m + c m c m = c ze vyjádřit měrnou teenou kaacitu směsi (c): nebo c = c m m + c m c m m m i m i m = i c i m c = c σ + c σ c σ = c (II 5) yto rovnice atí všeobecně. Při = konst se do nich dosazuje c a ři V = konst se dosadí c v..6 Směšování tekutin o různých teotách Smíchá-i se za stáého taku () někoik různých tekutin (kaain nebo ynů), které se chemicky nesučují ani jinak vzájemně nereagují a které mají různé teoty (t i ), i σ i 6
5 dojde mezi nimi k výměně tea a teoty se vyrovnají na stejnou hodnotu (t s ), kterou ze vyjádřit z energetické rovnice: Q + Q + + Q = Q S a o vyjádření: c m t + c m t + + c m t = (c m + c m + + c m ) t S odkud t c m t + c m t c m t S = (II 6) c m + c m c m V některých říadech se má určit hmotnost átky (m ) o měrné teené kaacitě (c ) a teotě (t ) otřebnou k tomu, abychom ohřái nebo ochadii hmotnost átky (m ) o měrné teené kaacitě (c ) a teotě (t ) na teotu (t S ). Vychází se rovněž z energetické rovnice m c t + m c t = m c t S + m c t S odkud m c (ts t) = m (II 7) c (t t ) S oto se týká nař. ohříváků toných soustav a soustav říravy užitkové vody..0 Skutečné yny Dosavadní úvahy se řevážně týkay tzv. ideáních ynů, o nichž se ředokádá, že se řesně řídí stavovou rovnicí v = r, dáe že vnitřní energie závisí ouze na teotě měrné teené kaacity (c v, c ) jsou stáé a že součinite roztažnosti i isotermické stačitenosti nezávisí na teotě. Ve skutečnosti neeistují ideání yny a skutečné yny se jim více či méně bíží. Skutečné yny se ideáním bíží tím více, čím je nižší tak a čím je větší teota ynu. U skutečných ynů se v -V diagramu isoterma odchyuje od rovnoosé hyerboy tím více, čím se yn bíží kaané fázi. Dojde-i u ynu ři změně objemu ke změně skuenství zkaaňování, řechází isoterma ve vodorovnou římku. ento růběh trvá, okud robíhá zkaaňování. Dochází-i ke zmenšování objemu ynu ři odkritické teotě ( i ), stouá tak a ři objemu v i začne yn zkaaňovat (obr. č. II-). Zde hyerboa řechází ve vodorovnou římku. Při daším zmenšování objemu se nemění tak () ani teota () děj je isobaricko isotermický okud nezkaaní veškerý yn, což nastane ři objemu v i. Provede-i se totéž ři jiných odkritických teotách, dojde ke zkaaňování ři jiných objemech (v i, v i ). Sojnice bodů určujících očátek zkaaňování 7
6 dává horní nebo ravou mezní křivku. Obdobně sojnice bodů určujících konec zkaaňování dává doní nebo evou mezní křivku. Horní a doní mezní křivka se setkávají v kritickém bodě (K) určeném kritickými hodnotami taku ( kr ), objemu (v kr ) a teoty ( kr ). Isoterma ( kr ) rocházející kritickým bodem má v tomto bodě vodorovnou tečnu a je to současně infení bod. Měrný objem ynu i kaainy je v kritickém bodě stejný a roto je stejná i měrná hmotnost. Kaaina v kritickém bodě roto nevytvoří vonou hadinu. Zmenšuje-i se objem ři nebo nad kritickým takem, řechází yn na kritické isotermě ( kr ) v kaainu nebo oačně ři zvětšování objemu se mění kaaina v yn. Kritické hodnoty stavových veičin některých ynů uvádí tabuka č. II-. Obr. č. II- Mezní křivka ynu Pyn eota varu Kritická Kritický Kritický ři normáním teota tak měrný objem taku [ C] [ C] [MPa] [m 3 kg - ] Čavek - 33,5 + 3,4,5 4,5.0-3 Dusík - 94,6-47, 3,5 3,.0-3 Kysík - 8,7-8,8 5,08 Vodík - 5,8-39,9,3 3,3.0-3 Vzduch - 93,0-40,7 3,84 3,3.0-3 Oid uhičitý - 78, + 3,0 7,53,4.0-3 Voda + 00, ,,55 3, ab. č. II- Kritické hodnoty stavových veičin 8
7 Při nadkritických teotách se nedá yn zkaanit ouhým stačováním, nýbrž je nutné ředchozí chazení na odkritickou teotu. edy nař. má-i být zkaaněn yn o stavu (obr. č. II-). ento stav je určen nadkritickou teotou ( ) a takem ( ) či měrným objemem (v ). Při isotermickém stačování ( = konst) není možno yn zkaanit. Proto je nutno nejdříve snížit teotu na odkritickou ( ) ochazením za stáého taku ( ) se yn dostane do stavu. Obdobně ochazováním za stáého objemu (v = v ) se dosáhne odkritické teoty ( ) v bodě *. Zmenšuje-i se nyní objem isotermicky (čárkovaně), dosáhne se stavu 3 v němž isoterma rotíná horní mezní křivku, yn se stává sytou arou o objemu v 3, taku 3 a o suchosti =,0. Změnou objemu mezi stavy 3 a 3 dochází ke zkaaňování ynu áry. Ve stavu 3 je veškerá ára zkaaňována v sytou kaainu o suchosti = 0. ento děj, jak byo dříve uvedeno, je isobarickoisotermický. erve isotermy ři teotách značně nadkritických se bíží rovnoosým hyerboám. Při odkritických a máo nadkritických se od hyerbo isotermy značně iší. Z toho yne, že změny stavu skutečných ynů se nedají osat jednoduchou stavovou rovnicí atnou v ceém rozsahu teot a taků jak tomu byo u ideáních ynů.. Rovnice Van der Waasova Stavovou rovnici, která aesoň řibižně atí v ceém rozsahu stavu skutečného ynu, tj. jak ro yn, mokrou i řehřátou áru, tak ro kaainu, odvodi Van der Waas. Vycháze z násedující úvahy. Jeden kiogram ynu zaujímá objem v. Moekuy, které se v tomto kg nachází, jsou nestačitené a mají objem b. Pak objem, který se ři změnách stavu může měnit je ouze rozdí v-b a nikoiv v jak se ředokádao u ideáních ynů. Pak oravená rovnice stavu má tvar: (v b) = r (II 8) Rovněž stavovou veičinu tak () je nutno oravit. U dokonaých ynů se ředokádao, že moekuy se chovají jako dokonae ružné koue. Ve skutečnosti ůsobí moekuy navzájem na sebe řitaživými kohezními siami, které snižují intenzitu nárazu moeku na stěny a tedy snižují i tak ynu na stěny. edy vnější tak ynu je menší neži vnitřní tzv. kohezní tak, který ze stanovit násedující úvahou. Přitaživost moeku je úměrná součinu jejich hmotností. ento součin musí být také úměrný součinu měrných hmotností nebo neřímo úměrný součinu měrných objemů. Proto ze kohezní tak ( k ) vyjádřit rovnicí: 9
8 a k = v kde a je emirická konstanta úměrnosti. Do stavové rovnice je nutno dosadit skutečný tak uvnitř ynu a nikoiv tak, kterým yn ůsobí na stěny. Za tohoto stavu má stavová rovnice skutečných ynů tvar: a + ( v b) = r (II 9) v Pro dvě etrémní hodnoty objemů nabývá rovnice II 9 zváštních tvarů. Je-i objem (v) vemi vysoký, je hodnota b vůči v zanedbatená. Stejně tak hodnota a/v je zanedbatená vůči taku () a rovnice II 9 za těchto odmínek řechází ve tvar stavové rovnice dokonaých ynů v = r. Isoterma je ak rovnoosou hyerboou. Je-i objem (v) vemi maý a bíží se své doní mezi b, je oměr a/v zanedbatený r vůči čenu. Rovnice II 9 se zjednoduší na tvar: v b r = (II 30) v b ode níž jsou isotermy oět rovnoosými hyerboami, ae v souřadnicích v-b a. Úrava rovnice II 9: ( v + a) (v v b) = r / v ( v + a) (v b) = r v v 3 + a v b v a b = r v v 3 v ( b + r ) + a v a b = 0 / v 3 r (b + ) v a a b + v = 0 (II 3) edy Van der Waasova rovnice je kubická rovnice, takže každému taku () odovídají tři objemy (v). V odkritické obasti jsou všechny tři kořeny rovnice reáné dva z nich jsou objemy v a v (obr. č. II-) a třetí objem se nachází mezi nimi. Křivka ode rovnice II 3 se nazývá Van der Waasova isoterma. Je sojitá i v obasti mokré áry, kde má reativní minimum a maimum. V této obasti vyjadřuje abiní stavy áry, tj. řehřátou kaainu a odchazenou áru. Oba abiní stavy jsou fyzikáně možné, vyskytují se a dají se eerimentáně dokázat. Úsek - ředstavuje obast řehřáté kaainy a úsek - 3 obast odchazené áry. Úsek - 3 odovídá fyzikáně nemožným stavům. Isoterma 0
9 mezi stavy - musí robíhat tak, aby ocha omezená křivkou nad a od sojnicí stavu - bya rovnocenná. Obr. č. II- Vanderwasova isoterma V nadkritické obasti má Van der Waasova rovnice ouze jeden kořen reáný a dva komení. Van der Waasova rovnice není zcea řesná ro všechny stavy ynů. Proto bya činěna řada zřesnění (Bertheot, Caendar, Vukaovič, Novikov, Jůza atd.). Rovnice těchto autorů byy zaoženy na měřeních v určitém rozsahu teot a taků. Proto jejich atnost je omezena na daný rozsah teot a taků. 3.0 Páry U téže átky neeistuje mezi yny a árami žádná vyhraněná mez. Proto se zravida užívá definice, že áry jsou yny, které se dají zkaanit isotermickou komresí. Přechod átky ze stavu ynu do stavu ar a oačně je z hediska většiny stavových a fyzikáních veičin kontinuání, rotože yny ze ovažovat za sině řehřáté áry. Pouze mez sytosti je hranicí, na které se náhe mění růběh nebo charakter křivek veičin stavu, V,. Páry vznikají z kaainy odařováním a vyařováním event. subimací. Kaaina se odařuje z voného ovrchu za každé teoty. Zvýší-i se teota kaainy k bodu varu, nastane vyařování a to nejen z ovrchu, ae z ceého objemu. Pokud se kaaina vyařuje, nemění se teota ani tak, roto veškeré řivedené teo se sotřebuje na změnu skuenství a nazývá se teem skuenským či výarným. Páry vznikají i oačným ochodem, tj. zkaaňováním ynu.
10 Výarné teo sestává ze dvou sožek. Část tea se sotřebovává na zvýšení kinetické energie moeku, aby nastao jejich uvoňování z ovrchu hadiny. Nazývá se vnitřní měrné výarné teo (r u ). Druhá část výarného tea se sotřebuje na zvětšení objemu uvoněných moeku kaainy na objem ynu a nazývá se vnější měrné výarné teo (r v ). Ohříváním kaainy na bod varu vznikne sytá kaaina o stavu v, t (obr. č. II - 3). K tomu je nutno řivést měrné kaainné teo (q k ) ro kg kaainy. Hodnoty stavových veičin se zravida označují jednou čarou. Daší teo zůsobuje vyařování kaainy za stáé teoty ( t ) a taku ( ), čímž vzniká tzv. mokrá ára různé suchosti () o měrném objemu (v ). Vyařování ři vyšším taku ( ) je znázorněno čárkovaně. Probíhá-i ři vyšší teotě ( t ), je intenzivnější a roto obast mokré áry je kratší. Pro vyaření veškeré kaainy se sotřebuje měrné výarné teo ( 3 ). Po vyaření veškeré kaainy vznikne sytá ára o objemu (v ). Ostatní veičiny tohoto stavu se také označují dvěma čarami. Suchost syté áry je =,0. Daším řívodem tea ři témže taku dochází ke zvyšování teoty syté áry, která se roto nazývá árou řehřátou. Sotřebované teo k řehřátí kg áry je měrné teo řehřívací (q ). Obr. č. II-3 Vznik áry za konstantního taku Vastnosti všech ar se řídí obdobnými (stejnými) zákony a roto je daší řešení uvedeno ro nejoužívanější vodní áru. ato ára se oužívá k vytáění výrobních i nevýrobních objektů, k dezinfekci ůdy at. Kromě vodních ar se často oužívá ar chadiv v technice chazení, ar benzínu u saovacích zážehových motorů at.
11 3. Určující veičiny syté vody Výchozí stav je voda o teotě t 0 = 0 C, měrném objemu v 0. Dáe se ředokádá, že ři teotě t 0 = 0 C jsou měrná vnitřní energie (u 0 = 0), měrná entaie (i 0 = 0) i měrná entroie (s 0 = 0) rovny nue. Přivedením měrného kaainného tea (q k ) vzroste objem kg vody z v 0 na v, měrná entroie z s 0 na s, měrná entaie z i 0 na i a měrná vnitřní energie z u 0 na u. Přivedené teo ro dosažení stavu syté kaainy vychází z diferenciání rovnice: q k = c k odkud o integraci v mezích t 0 t v res. 0 v bude q k V 0 k k ( v 0 ) = ck t V = c = c [J kg - ] (II 3) kde c k je okamžitá měrná teená kaacita kaainy ři stáém taku, c k = c k je střední měrná teená kaacita kaainy daného rozsahu teot. Měrnou vnitřní energií syté kaainy ze stanovit z I. věty termodynamiky, ode níž se řivedené teo využívá na zvýšení vnitřní energie a vykonání objemové vnější ráce ři zvětšování objemu z v 0 na v. Obecně atí: u v q = u + v (II 33) u0 v0 o integraci: q = u - u 0 + (v - v 0 ) (II 34) ode dřívějšího ředokadu je u 0 = 0 a dáe zvětšení objemu vody ohřátím je zanedbatené, takže v - v 0 ~ 0. Pak rovnice II 34 má tvar: q = u (II 35) Měrnou entaií syté vody ze stanovit z obecného dříve odvozeného vztahu: i = u + v + v rotože je = konst, bude = 0 a ak: i = u + v (II 36) a o integraci: i i = u u + v i0 u0 v0 v i i 0 = u u 0 + (v v 0 ) (II 37) 3
12 ode dřívějšího aiomu je ři t 0 = 0 C také i 0 = 0 a u 0 = 0. Rovněž by řijat ředokad v - v 0 = 0. Za těchto odmínek má rovnice II 37 tvar: i = u = dq (II 38) z čehož yne, že řivedené měrné kaainné teo ( q) zůsobí ouze změnu vnitřní energie kaainy (u ), která je rovna jeho entaii (i ). Pro měrnou entroii (s) by odvozen obecný vztah, který ro sytou kaainu ze zasat ve tvaru: v s - s 0 = c k n - r n 0 0 ro vyařování ři konstantním taku je = 0 = konst a ro výchozí ředokad t 0 = 0 C s 0 = 0 bude měrná entroie syté kaainy (s ) dána rovnicí: v s = c k n (II 39) 0 3. Určující veičiny syté áry Po vyaření veškeré kaainy vznikne za stáého taku () sytá ára suchosti =,0. Pro vyaření kg kaainy na sytou áru je ři této isobaricko isotermické změně sotřebováno měrné výarné teo ( 3), ro nějž ode I. věty termodynamiky ze sát: u v 3 = u + v = ru + rv u v (II 40) o integraci: 3 = u - u + (v - v ) = r U + r V (II 4) z této rovnice yne, že vnitřní výarné teo r U = u - u se sotřebuje na zvýšení vnitřní energie áry z u na u a vnější výarné teo r V = 3 r U vykoná objemovou vnější ráci ři zvětšení objemu áry z objemu v na v r V = 3 r U = (v - v ) (II 4) Cekové teo otřebné ro výrobu kg syté áry z vody 0 C teé se nazývá výrobní (úhrnné) teo (λ) syté áry a je dáno: λ = dq + 3 [J kg - ] (II 43) Měrná vnitřní energie (u ) syté áry je ode ředešého dána: u = u + r U = dq + r U (II 44) ro 4
13 r U = 3 r V = 3 - (v - v ) bude měrná vnitřní energie syté áry (u ) dána: u = q k + 3 (v - v ) nebo zanedbá-i se objem syté vody (v ) vůči mnohonásobně většímu objemu syté áry (v ), ze sát: u = q k + 3 v (II 45) Odvození měrné entaie syté áry je shodné s odvozením měrné entaie syté kaainy, ouze meze integrace jsou jiné. Proto ze měrnou entaii syté áry (i ) odvozeně formuovat ode rovnice II 37): i = u + (v - v ) (II 46) o zanedbání v oroti v bude: i = u + v (II 47) dosazením rovnice II 45 do II 47 bude: i = q k + 3 v + v = q k + 3 = i + 3 (II 48) Z rovnice yne, že měrná entaie syté áry (i ) se rovná cekovému řivedenému teu (q k + 3 ). Odsud se odvozuje nesrávný název teený obsah áry. Změna měrné entroie ři vyařování kg kaainy vychází z obecné formuace entroie v diferenciáním tvaru: s q s = = s V odkud o integraci: q (II 49) 3 s - s = (II 50) V a měrná entroie syté áry (s ) vztažená k výchozímu stavu t 0 = 0 C, s 0 = 0 bude: s = s + 3 V = c k n V V (II 5) Každému taku () řísuší jediná hodnota bodu varu t V = t = t, měrné kaainné teo (q k ), měrné výarné teo ( 3) a měrný objem v a v. Proto ro určení stavu syté áry stačí znát jedinou určující veičinu a to buď tak () nebo teotu varu (t V = t = t ). Matematická formuace závisosti t V = f () je sožitá. Jednoduchou emirickou formuaci 5
14 teoty a taku varu (t V, V ) uvádí Kačík ro vodu do,0 MPa. ak ( V ) se dosazuje v MPa. Naříkad ro tak 0, MPa: t 4 v V = = 77,9 4 = 77,9 0, 00 [ C] (II 5) ak a teotu varu zravida udávají arní tabuky nebo diagramy. 3.3 Určující veičiny mokré áry Mokrá ára je směs kaiček syté kaainy a syté áry. V kg mokré áry je kg syté áry a ( ) kg syté kaainy. Parametr vyjadřuje suchost áry a doněk ( ) vhkost áry. Pode tohoto označení je suchost syté kaainy = 0 a suchost syté áry y =,0. Proto k ručení stavu mokré áry jsou nutné dvě veičiny tj. suchost () a tak () nebo teota varu (t V = t = t ). Různé stavy mokré áry se ak vyjádří ze suchosti () áry a hodnot veičin ro sytou kaainu a sytou áru. yto hodnoty jsou obsaženy v arních tabukách. Pode tohoto rinciu vyjadřování určujících veičin je měrný objem (v ) mokré áry dán: v = v + ( ) v = v + (v - v ) (II 53) měrný objem kaiček kaainy (v ) ze vůči mnohonásobně většímu objemu syté áry (v ) zanedbat a ak atí: v = v (II 54) Měrná vnitřní energie (u ) mokré áry se vyjadřuje ode stejného rinciu jako měrný objem (v ): u = u + ( ) u = u + (u - u ) (II 55) ro u - u = r U bude: u = u + r U = q k + r U (II 56) což vyjadřuje, že z kaainy je vyařena ouze -tá část. Měrná entaie (i ) mokré áry je obdobně dána i = i + ( ) i = i + (i - i ) (II 57) rotože u - u = 3 bude i = i + 3 = q k + 3 (II 58) Měrná entroie (s ) mokré áry se určí shodným ostuem: s = s + ( ) s + (s - s ) (II 59) rotože atí: 6
15 3 s - s = V bude mít rovnice II - 59 tvar: 3 s = s + V = c k n V V (II 60) 3.4 Určující veičiny řehřáté áry Při ohřívání syté áry za stáého taku () bez řívodu daší kaainy dochází k růstu teoty áry vzniká ára řehřátá. eota řehřáté áry závisí na taku. Veičiny vnitřní energie, entaie, entroie závisí na taku a teotě. Měrné řehřívací teo (q ) ro řehřátí kg kaainy z teoty t na t se určí z rovnice: dq = c d res. o integraci ( ) = c ( t t ) q = q = c t = c v (II 6) v V kde c je střední měrná teená kaacita za stáého taku řísušného rozsahu teot (t až t ) odečítaná z arních tabuek či diagramu (J. Jůza, 976). Měrný objem (v) řehřáté áry ro daný tak a teotu se odečte z diagramu (J. Jůza, 976) nebo arních tabuek, event. se vyočte ze stavové rovnice skutečných ynů (rovnice II 9) ode níž jsou tabuky a diagramy sestavovány. Měrná vnitřní energie syté kaainy (u) řehřáté áry se rovná součtu měrné vnitřní energie syté kaainy (u ), vnitřního výarného tea (r U ) a řírůstku zůsobeným řehřívacím teem: u = u + r U + c d (II 6) V jednotivé čeny rovnice II 6 ze vyjádřit násedovně: u = q k (v - v 0 ); r U = 3 (v - v ) V c = u u u = i i i v v v (II 6) rotože ode dřívějšího důkazu atí i = c bude: 7
16 V c a o dosazení: a o úravě: = u u = c ( ) ( v v ) u = q k c ( V ) (v - v 0 + v - v + v - v ) v u = q k c V ) (v - v 0 ) (II 63) rvní tři čeny rovnice určují měrnou entaii řehřáté áry (i) i = q k c ( V ) ak měrná vnitřní energie (u) řehřáté áry je dána: u = i - (v - v 0 ) (II 64) a o zanedbání objemu v 0 vůči objemu v bude: u = i v (II 65) Měrná entaie (i) řehřáté áry je dána součtem měrné entaie syté kaainy (i ), entaie vyařování ( 3) a entaie řehřívacího tea: I = i c = i c ( V ) = V = i c (t t ) = q k q (II 66) Numerické hodnoty měrné entaie řehřáté áry (i) uvádí tabuky ro různé teoty řehřátí (t ). Měrná entroie (s) řehřáté áry je určena součtem měrné entroie syté kaainy, měrné entroie vyařování a měrné entroie řehřátí: s = V 0 q k + 3 V + q V 3 = ck + + c = V 0 V V = c k n V V P + c n V (II 67) kde c je střední měrná teená kaacita řehřáté áry za konstantního taku. Oroti ideáním ynům dochází u skutečných ynů a tedy i u řehřátých ar ke změně měrné teené kaacity (c ) v závisosti na teotě řehřátí i na taku řehřívání. Hodnoty (c ) v závisosti na teotě a taku řehřívání ze odečíst z diagramu (obr. č. II-4). 8
17 Obr. č. II-4 Měrná teená kaacita c řehřáté vodní áry 3.5 Diagramy ar Diagramy jsou grafickým znázorněním tabukových hodnot stavů áry ve vhodně voených souřadnicích. Nejčastěji se užívá -v, -s, i-s diagramů. V arních tabukách se tedy i v diagramech zravida uvádí měrné veičiny stavu vztažené na kg. Při výočtu teených strojů se vynásobí odečtené hodnoty množstvím racovní átky vyočtené ro řísušný výkon stroje. Různé átky mají rozdíné růběhy na sobě závisých stavových a teených veičin a roto se ro jednotivé átky sestrojují samostatné diagramy. Nejběžnější jsou oět digramy vody, která má v zeměděství, otravinářství, odadovém hosodářství aod. široké uatnění Pracovní -V diagram vodní áry Zůsob konstrukce, růběh veičin isoterem, doní a horní mezní křivky včetně vymezení obasti kaainy, mokré áry, řehřáté áry a ynu byo osáno na říkadu -v diagramu skutečného ynu (obr. č. II-). V -v diagramu vodní áry (obr. č. II-5) jsou charakteristické hodnoty. Při teotě t = 0 C zaujímá jeden kiogram vody měrný objem v 0 = 0,00m 3 kg -. Při ohřívání měrný objem vody (v ) neatrně roste. Rovněž i teota stuá až do kritického bodu (K). Kritický stav je určen kritickým takem kr =,55 MPa, kritickou teotou t kr = 374, C a kritickým měrným objemem v kr = 0,00307 m 3 kg -. Kritickým bodem rochází kritická isoterma. Prostor mezi ní a horní mezní křivkou se ovažuje za stavy řehřáté áry. Vravo od kritické isotermy se ovažuje za stavy ynu. 9
18 Obr. č. II-5 Pracovní -v diagram vodní áry 3.5. eený entroický -s diagram vodní áry Stav vody a áry je zde určen teotou () a měrnou entroií (s). Sojnice stavů syté kaainy a syté áry určuje i zde doní a horní mezní křivku, které se sojují v kritickém bodě (K). Vymezené obastí skuenství kaaného, ynného, mokré a řehřáté áry je jednoznačně určeno v obr. č. II-6 - tj. nad kritickou isotermou je stav ynu, mezi kritickou isotermou a doní mezní křivkou je kaaina, mezi horní mezní křivkou a kritickou isotermou je řehřátá ára a mezi mezními křivkami je mokrá ára. Jednotivé veičiny mají v -s diagramu násedující růběh: Isotermy jsou rovnoběžné s osou entroie (s) Adiabaty (isoentroy) jsou rovnoběžné s osou teoty () Isobary v obasti kaainy se rakticky shodují s evou mezní křivkou (voda je nestačitená), v obasti řehřáté áry jsou tvořeny eonenciáními křivkami Isochory v obasti mokré áry to jsou křivky stouající s rostoucí entroií, na ravé mezní křivce se omí a s rostoucí entroií rostou strměji než isobary Stav áry v entroickém diagramu je určen: - v obasti řehřáté áry takem () a teotou () - v obasti syté áry takem () nebo teotou () na horní mezní křivce 0
19 - v obasti mokré áry takem () a suchostí () nebo teotou () a suchostí () Průběh vzniku áry v -s digramu je násedovný: Kaaina se ohřívá, až dosáhne bodu varu ( V ). Ohřev se děje za stáého taku. Změna objemu kaainy je zanedbatená, a roto čára ohřevu kaainy se rakticky shoduje s doní mezní křivkou mezi body a. Dodané měrné kaainné teo (q k ): s q = s (II 68) k s odovídá oše od touto částí čáry -, tj. v mezích entroie s a s. Obr. č. II-6 -s diagram vodní áry Vyařování kaainy, tj. vznik mokré áry je děj isobaricko-isotermický, a roto je dán římkou - rovnoběžnou s osou entroie v mezích entroie s -s odovídajících rovnici: s 3 = V s s = V (s s ) (II 69) omuto teu ( 3 ) odovídá ocha od čarou - (obr. č. II-6). Daší tzv. řehřívací teo zůsobí zvýšení teoty řehřáté áry za stáého taku o eonenciání křivce -3. Pocha od touto částí křivky odovídá měrnému řehřívacímu teu (q ) s3 q = s (II 70) s
20 Ceá ocha od křivkou 3 (obr. č. II-6 - šrafováno) ředstavuje měrnou entaii (i) řehřáté áry i = q k q = λ (II 7) a současně vyjadřuje výrobní teo (λ ) řehřáté áry. Z diagramu (obr. č. II-6) je atrné, že s rostoucí teotou varu ( V ) veikost výarného tea ( 3) se zmenšuje až konečně v kritickém bodě (K) řechází kaaina v řehřátou áru Srovnání racovního a teeného diagramu áry Z -s diagramu áry vyynuo, že veikost výarného tea se zmenšuje s rostoucí teotou varu, která zase závisí na taku. Eaktně tuto závisost odvodii Caeyron (834) a Causius (850) z orovnání eementárního Carnotova oběhu ro kg mokré áry v -v a -s diagramu mezi isobarami a +d a mezi isotermami a +d (obr. č. II-7). Obr. č. II-7 Eementární ráce v -v a -s diagramu Odvození vychází z eementární ráce vyjádřené ochou,, 3, 4 v -v diagramu, která musí být rovna sdíenému teu znázorněného ochou,, 3, 4 v -s diagramu. Odsud atí: (v v ) = (s s ) (II 7) rotože atí: s s = bude 3 3 = (v v )
21 odkud 3 = (v v ) (II 7) ato rovnice se nazývá Caeyron-Causiova a dává jediný teoretický vztah určujících veičin mokré áry (,, v, v, 3 ). Derivace určuje tečnu křivky naětí syté vodní áry, kterou ze snadno určit z diagramu (obr. č. II-8). Obr. č. II-8 Křivka naětí áry Rovnice II 7 atí i ro ostatní děje, kde řívod tea zůsobí změnu objemu. edy atí ro všechny změny skuenství, tj. vyařování, tání, subimaci. Nař. ro tání z tuhé fáze do kaané atí rovnice měrného skuenského tea tání ( ): d = (v v ) d (II 73) kde v je objem tuhé fáze a je teota tání Diagram -i Souřadné osy diagramu ředstavuje tak () a měrná entaie (i) áry. Isotermy mají odobný růběh jako v -v diagramu, v obasti mokré áry to jsou římky rovnoběžné s osou měrné entaie (i) (obr. č. II-9). Na horní mezní římce se omí a kesají s rostoucí strmostí. Isoentroy tvoří svazek rozbíhajících se římek. 3
22 Obr. č. II-9 -i diagram reáného ynu Výhodou tohoto diagramu je, že umožňuje na isobarách římo odečítat měrné entaie k určení isobaricky sděeného tea. Stejně se odečítají entaie ro určení adiabaticky konané takové ráce. Škrcení je ředstavováno čarou i = konst, což je římka komá k ose měrných entaií. Z těchto důvodů se tento diagram oužívá ro výočet strojního chazení. Pro zobrazení většího rozsahu teot se v diagramu místo osy taku () oužívá osa ogaritmu taku (og ) Změny stavu ar Průběhy změn stavu áry se iší ode toho, které obasti robíhají. Při výrobě i ři užití áry v teených strojích rochází změny stavu všemi obastmi. Podobně jako u vratných změn ynů se budeme zabývat určením: řivedeného tea, vykonané ráce a změny entroie změny isobarické, isotermické, isochorické a adiabatické Isobarická změna áry Isobarická změna áry atří k nejdůežitějším, rotože ára se vyrábí, řehřívá i řivádí do racovního stroje ři stáém taku. a) mokrá ára v obasti mokré áry se ve všech diagramech (-v, -s, i-s) isobary kryjí s isotermami (obr. č. II-0). 4
23 Obr. č. II-0 Izobarické změny mokré áry eo řivedené ro změnu se nejée stanoví z -s diagramu: q, = (s s ) (II - 74) Z uvedeného obrázku je atrné, že řívodem tea roste suchost áry z na. Pak v duchu rovnice II 59 ze vyjádřit měrné entroie ( s, s s = s + (s s ), s = s + (s s ) ) stavů a rovnicemi: o dosazení do rovnice II 74 bude: q, = (s s ) ( ) (II 75) rotože (s s ) = 3 bude q, = 3 ( ) (II 76) Isobaricky řivedené teo je rovněž funkcí entaie. Proto ze teo (q, ) jednoduše určit z i-s diagramu z rozdíů měrných entaií (i i ): q, = i i (II 77) Objemová absoutní vnější ráce (a ) této změny se nejée stanoví z -v diagramu a = v = (v v ) (II 78) Měrné objemy mokré áry suchosti, ze ode rovnice II 53 vyjádřit rovnicemi: v = v + (v v ), v = v + (v v ) ak a = (v v ) ( ) (II 79) Změna měrné entroie ( s) v obasti mokré áry je vyjádřena rovnicí: 5
24 s q i i ( ) 3 = s s = = = (II 80) b) řehřátá ára v -s diagramu se isobara na horní mezní křivce omí a roste s rostoucí entroií ode eonenciáního zákona. eo řivedené řehřáté áře ze určit ze vztahu: q c = c ( ) = i i = (II 8) což je nejée atrné v i-s diagramu (obr. č. II-). Objemová absoutní ráce (a ) je v -v diagramu určena ochou od isobarou: a = (v v ) (II 8) Obr. č. II- Izobarické změny řehřáté áry Změna měrné entroie ( s) je ři c = konst dána rozdíem měrných entroií stavů a (s s ). Entroie s, s ze vyjádřit ode rovnice II 67, v níž rvní dva čeny vyjadřují měrnou entroii syté áry (s ). S tímto označením jsou měrné entroie s, s dány: s = s + c = s + c n V s = s + c = s + c n V V V (II 83) ak změna měrné energie ( s) je dána: s = s s = c n V - c n V = c n (II 84) Isotermická změna áry a) mokrá ára v obasti mokré áry se ve všech diagramech (-v, -s, i-s) isobary shodují s isotermami. Proto řivedené teo, objemová ráce i změna měrné entroie jsou dány stejnými rovnicemi jako u téže změny isobarické v obasti mokré áry. 6
25 b) řehřátá ára u isotermické změny řehřáté áry (obr. č. II-) dochází ři = konst ke změně taku vivem rostoucího objemu, což je dobře atrno z -s diagramu. Přivedené měrné řehřívací teo ( q ) je ode -s diagramu dáno ochou určenou výrazem: q ( s s ) = (II 85) Obr. č. II- Izotermické změny řehřáté áry Pro určení změny měrné entroie ( s) je nutno v tomto říadě určit zvášť měrnou entroii stavu a a to roto, že každá z nich odovídá jinému taku (, ). Proto je nutno určit měrné entroie (s, s ) jednotivě odé takových změn stavu rocházejících stavy a a majících soečný očáteční stav, jímž je s 0 = 0. ímto stavem ode dřívějších ředokadů je stav syté kaainy ři teotě 0 = 73,5 K = 0 C. ento stav je soečný ro isobary, syté kaainy, kde tyto se shodují s doní mezní křivkou. V obasti mokré áry se isobary (, ) odišují a odovídají jim teoty vyařování ( v, v ). Nyní ze hodnoty měrných entroií (s, s ) ve shodě s obecnou rovnicí II 67 vyjádřit rovnicemi: s = c k n 73,5 v + (3) V + c n V s = c k n 73,5 v + (3) V + c n V (II 86) kde a ( 3) jsou měrná výarná tea ři teotách vyařování ( 3 V a V a c, c ) jsou měrné teené kaacity za konstantního taku ři teotách a. Pro tyto teoty ři isotermické změně atí = = a ak změna měrné entroie ( s) je dána: s = s s = c k n V V + (3) V (3) V + 7
26 + c n V c n V (II 87) Isotermickou objemovou absoutní ráci (a ) ze stanovit z I. věty termodynamiky: q = u u + a (II 88) odkud a = q u = q (i i ) (II 89) ro měrnou entaii obecně atí rovnice: i = u + v ode níž budou měrné entaie i, i dány: i = u + v ; i = u + v o dosazení do rovnice II 89 atí: a = q [i i ( v v )] (II 90) Isochorická změna áry a) mokrá ára isochorická změna mokré áry robíhá ři vyařování vody v uzavřeném rostoru nař. v arním koti v okamžiku řerušení odběru áry. Přivádí-i se teo mokré áře ři v = konst, zvyšuje se její teota a tak za současné změny její vhkosti, res. suchosti (). Změna suchosti áry je rozdíná ode toho, od kterou mezní křivkou se stouajícím takem změna 3 4 v -v diagramu roste teota a ára se zvhčuje, takže ři dosažení taku mezní křivky je v nádobě ouze kaaina. Oačně od horní mezní křivkou změna s rostoucím takem roste teota a suchost áry se zvětšuje z na. Po dosažení taku horní mezní křivky je áry ouze ve stavu sytém. Je-i dán tak a suchost, ze ro rovněž zadaný (ožadovaný) tak určit suchost z rovnosti objemů v = v z rovnic: v = v + (v v ) v = v + (v v ) ro v = v v + (v v ) = v + (v v ) odkud v v = v v + v v v v (II 9) 8
27 Obr. č. II-3 Izochorické změny mokré áry Přivedené teo (q ) isochorické změny zůsobí ouze změnu vnitřních energií (u, u ) (nekoná vnější ráci a = 0) a je roto dáno: q = u u = c v ( ) (II 93) Výočet změny měrné entroie ( s) se rovede odobně jako u isotermické změny v obasti řehřáté áry, rotože isochory mají v této obasti rovněž eonenciání růběh s vyšší strmostí neži isobary. Proto isochora - v -s diagramu robíhá mezi dvěma isobarami (, ) v obasti řehřáté áry a je roto nutno uatnit ostu určení měrných entroií s, s takový, jak by osán u isotermické změny řehřáté áry. Určující vztah ( s) je roto shodný s rovnicí II 87). Obr. č. II-4 Izochorické změny řehřáté áry Adiabatická změna áry Adiabata v -v diagramu (obr. č. II-5) je v obasti mokré a řehřáté áry hyerboická křivka. Na řechodu řehřáté áry do obasti mokré áry (II v -v) se zmenšuje její strmost. V teených diagramech (-s, i-s) je adiabata isoentroa římka komá k ose entroie ve všech obastech áry. 9
28 Obr. č. II-5 Adiabatické změny mokré a řehřáté áry Stav mokré áry se mění obdobně jako u isochory ode toho, od kterou mezní křivkou robíhá. Pod doní mezní křivkou se mokrá ára eanzí vysušuje (-) a komresí zvhčuje (-). Pod horní mezní křivkou se eanzí zvhčuje (-) a komresí vysušuje. Změna suchosti () mokré áry ři adiabatické či isoentroické změně se stanoví z odmínky s = s tj. ode dříve uvedených odmínek určení měrné entroie ro změny stavů ři dvou tacích (, ) atí: c k n v + 73,5 (3) V = c k n v + (3) 73,5 73,5 (II 94) kde teoty vyařování ( v, v ) a měrná výarná tea (, ( 3) ) jsou uvedeny ro ( 3 ) řísušné taky (, ) v arních tabukách (Kačík J., Sýkora K 973 aod.). Objemová adiabatická ráce (a ) je určena rozdíem měrné vnitřní energie na očátku (u ) a konci (u ) eanze a = u u (II 95) Pro mokrou áru sucosti, ze měrné vnitřní energie (u ) stanovit ode rovnice II 55, 56 násedovně: u = u + (u u ) = u + r U u = u + (u u ) = u + r U (II 96) o dosazení do rovnice II 95 bude: a = u u + r U r U = i i + r U r U (II 97) Adiabatickou takovou ráci a t = i i ze římo odečítat v i-s diagramu. Jak již byo uvedeno, stanoví se změna suchosti áry () adiabatickou eanzí syté áry z odmínky s = s. Měrná entroie (s) na mezi suchosti, tj. ro =,0 je vyjádřená rovnicí: 30
29 s = s = s + (3) V = s + (3) V (II 98) a měrná entroie (s ) mokré áry, které se eanzí zvhčia na suchost je dána: s = s + (3) Z rovnosti měrných entroií s = s yne: s + (3) V V = s + (3) odkud suchost ( ) o eanzi do stavu je dána: = (s s + (3) V ) V V (3) (II 95) tj. sytá ára se adiabatickou eanzí zvhčuje. V zeměděství, otravinářství, odadním hosodářství se vodní ára nejčastěji oužívá k vytáění objektů a k teenému zracování roduktů, otravin, odadů. Zravida je oužívána mokrá ára. Nař. arním otrubím toné soustavy odniku rotéká 000 kg h - o taku,6 MPa. V teeném zdroji arním koti je rodukována ára suchosti = 0,97 a na konci otrubní sítě řed sotřebištěm výrobními objekty bya zjištěna suchost = 0,95. Má se určit ztráta tea rostuem rozvodným otrubím, která tuto částečnou kondenzaci ( ) zůsobia. Pro,6 MPa je z arních tabuek výarné teo syté áry 3 = 935 kj kg -. Pro kg áry atí: q = ( ) 3 Pro růtočné množství Q m = 000 kg h - je ztráta teeného výkonu (P z ) kondenzací dána: P z = Q m q = Q m ( ) 3 = 000 (0,97 0,95) 935 = kg h - = =,5 kg s - =,5 kw Z tohoto výsedku neze usuzovat na dokonaost izoace rozvodné sítě arní toné soustavy odniku. Užitečný (využitý) teený výkon (P u ) toné soustavy je dán za úné kondenzace áry v toných těesech soustavy ( 3 = 0,0) P u = Q m ( 3 ) 3 = 000 (0,95 0,0) 935 = 0,5 kw tj. teené ztráty ředstavují, % užitečného teeného výkonu, což svědčí o oměrně dokonaé izoaci rozvodu. Pokud by tato ára bya oužívána ke zmíněnému teenému 3
30 zracování roduktů, otravin, odadů aod. je ro tento teený roces k disozici rávě užitečný teený výkon P u = 0,5 kw Škrcení ar Ke škrcení ar dochází ři růtoku ar (ynů) náhe zúženým růřezem, nař. záměrně zařazeného škrtícího ventiu. Průběh změny stavu ři škrcení je tak rychý, že sdíení tea tohoto děje je zanedbatené a ak škrcení ze ovažovat za nevratnou adiabatickou změnu stavu. Škrcení je odstatnou a zákadní částí chadícího oběhu, kterého často využívají chadící zařízení oužívaná v oměrně široké míře v zeměděství, otravinářství, odadovém hosodářství. U ideáních ynů se ři škrcení nemění ani entaie ani teota. Při škrcení vždy kesá tak a zvětšuje se měrný objem. Entroie ři této změně roste. U ar a skutečných ynů dochází ři škrcení i ke změně teoty, kterou vyjadřuje součinite (k J ) Joue-homsonova efektu: δ k J = δ i který vyjadřuje změnu teoty (δ) ři změně taku (δ) za neměnné měrné entaie (i). Má-i tento součinite (k J ) záornou hodnotu, ak se áry (yn) škrcením ohřívají a oačně, je-i součinite (k J ) kadný, ak se áry ři škrcení ochazují. Ke změně znaménka součinitee (k J ) dochází ři tzv. inverzní teotě, která je úměrná kritické teotě ar (ynu). Při škrcení ynu za inverzní teoty ( inv ) se teota () ar nemění, tj. inv = a áry (yn) se chovají jako ideání yn. Při teotách nadinverzních ( > inv ) se nedají áry nebo yn ochadit. Skutečné yny a jejich áry kromě vodíku a heia mají inverzní teotu značně vysokou ( inv > ) takže u nich ři škrcení za obvykých teot dochází k jejich ochazování. ohoto jevu byo využito (Linde) ke konstrukci chadícího oběhu se zkaaňováním media. Změny stavu ar ři škrcení ze nejée osuzovat v i-s diagramu (obr. č. II-6), kde je škrcení ředstavováno vodorovnou římkou I = konst. 3
31 Obr. č. II-6 Škrcení áry Škrtí-i se mokrá ára ze stavu do stavu, atí ro tuto změnu odmínka: i = i (II 96) o zavedení měrné entaie syté kaainy (i ) o suchosti áry () stavů a ze sát: i + (3) = i + (3) (II 97) odkud je suchost konečného stavu ( ) dána: i i + (3) = (II 98) (3) V daném říadě je = 0, tedy je škrcena sytá kaaina a ak rovnice II 98 řejde ve tvar: i i = (II 99) (3) Při této změně stavu (-) dochází k okesu taku a teoty (viz. obr. II-6) a současně se zvyšuje suchost áry (rov. II 99) a to až do stavu syté áry ( ), event. až řehřáté áry ři změně -(). ento stav určuje výsedek rovnice II 99. Je-i >, je ára ve stavu řehřátém. eotu řehřátí ze oět určit z rovnic měrných entaií: i + (3) = i + c (t () t ) (II 00) odkud 33
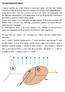
32 t ( ) i i + (3) = + c t (II 0) eotu ze rovněž římo odečíst z diagramu (obr. č. II-6). Sytá ára se škrcením ze stavu 5 do stavu 6 řehřívá za současného okesu taku a teoty. Přehřátá ára se škrcením více řehřívá (7-8) a snižuje se tak. Při nižším řehřívání se mírně snižuje i teota, kdežto ři vysokém řehřívání zůstává teota stáá, rotože v této obasti jsou isotermy rovnoběžné s isoentroami. Máo řehřátá ára může ři škrcení za vysokých taků řejít (9-0) v áru mokrou, sytou a znovu v áru řehřátou. Změny stavu a hodnoty stavových a teených veičin se nejrycheji určují římo z i-s digramu řísušného media. Průběhy změn jednotivých druhů medií ar vodních, ar chadiv at. jsou obdobné. 4.0 Vhký vzduch Atmosférický vzduch vždy obsahuje určité množství vodních ar. edy smíšením suchého vzduchu a vodních ar vzniká vhký vzduch, řičemž vodní áry jsou ve vzduchu většinou ve stavu řehřátém. Zákonitosti, které budou dáe odvozeny ro vhký vzduch atí i ro ostatní vhké yny, které jsou směsí suchého ynu a áry ibovoné átky. Nutno odotknout, že eistuje ae zásadní rozdí mezi směsí ynů a směsí ynu a áry. Zatímco sožky ve směsi ynů se mohou vyskytovat v ibovoném oměru, je množství ar ve vzduchu (ynu) jednoznačně určitým zůsobem omezeno. oto omezení je zůsobeno tím, že tak syté áry ( ) je závisý na teotě suchosti (t S ) což je teota bodu varu ři taku S =. Ve směsi suchého vzduchu a vodních ar je teota sytosti ar dána teotou směsi, tj. v tomto říadě vhkého vzduchu. ak odovídající této teotě vstuuje ve směsi jako nejvyšší možný arciání tak ar vede (kromě) arciáního taku vzduchu ( v ). Pode Datonova zákona dává součet těchto arciáních taků (, v ) tak směsi, tj. v tomto říadě cekový tak vhkého vzduchu (). Vhkého vzduchu se nejčastěji oužívá v sušárenství a kimatizaci některých objektů. ak vzduchu (), který se v sušárenství a kimatizaci oužívá, se jen máo iší od barometrického taku ( b ), tj. = b = v +. eota ar ři určitém taku může být ibovoně vyšší než teota syté áry, nemůže být ae nižší. Při nižší teotě, než je teota sytosti dojde ke kondenzaci ar. Proto 34
33 arciání tak ar obsažených ve směsi se vzduchem nemůže být vyšší než tak syté áry ( ) odovídající teotě vhkého vzduchu. ímto je arciání tak ar omezen teotou směsi a současně je tím také omezeno množství ar, které je schoen vzduch ojmout. Je-i ve vzduchu ři dané teotě menší množství ar než odovídá stavu nasycení, je arciání tak ar ( ) menší než tak a ára je ve vzduchu ve stavu řehřátém. Změny stavu áry ve směsi se vzduchem jsou dobře atrny v -v diagramu (obr. č. II-7), nař.: - zvětší-i se objem ar ři stáém taku () ze stavu (V ) do stavu (V ) nebo zmenší-i se množství áry v daném objemu, tj. zvětší-i se měrný bojem ar (v), zvětší se tím i teota nad teotu sytosti, čímž se ára stává řehřátou, - nebo zvětší-i se objem ři stáé teotě ( S ) ze stavu (V ) do stavu 3 (V 3 ), stane se ára rovněž řehřátou v daném říadě ouze neatrně, - konečně sníží-i se tak syté áry ( ) na nižší tak ( ) ři stáé teotě směsi ( 3 ), dostane se ára do stavu 4, tj. snížením taku se ára řehřeje a zvětší objem v V na V 4. Obr. č. II-7 Vhký vzduch v -v diagramu 4. Vhkost vzduchu Vhkost vzduchu se vyjadřuje jako absoutní (objemová), reativní nebo měrná. 4.. Absoutní vhkost vzduchu Je hmotnost vhkosti obsažené v m 3 vhkého vzduchu, a roto se také nazývá objemovou vhkostí. ato hmotnost ar je vastně měrnou hmotností (ρ ). Množství ar ve vzduchu, res. absoutní vhkost se mění v rozmezí ρ = (0 ). ρ, kde ρ je maimání hodnotou ar ve stavu nasycení. oto rozětí se mění s teotou vzduchu a ak může nastat 35
34 říad, že vzduch bude obsahovat stejné množství ar ve stavu sytém a řehřátém. Proto není absoutní vhkost jednoznačnou charakteristikou stavu vhkého vzduchu. 4.. Reativní vhkost vzduchu Je vyjádřená oměrem: ρ v ϕ = 00 = 00 [%] (II 0) ρ v je to bezrozměrná veičina, která udává, koik % vhkosti obsahuje vzduch z maimání vhkosti (ρ ), kterou je vzduch schoen řijmout ři téže teotě. Maimání hodnota φ = 00 % je dosažena tehdy, je-i vzduch arami nasycen, tj. ři =. Proč je absoutní vhkost necharakteristická veičina vyývá z tohoto říkadu: Ochazuje-i se vhký vzduch v atmosféře ři konstantním taku, ak absoutní vhkost se nemění až do okamžiku dosažení teoty, ři níž ρ = ρ. Reativní vhkost však roste, až dosáhne v uvedeném okamžiku hodnoty φ = 00 %. Daším ochazením dochází ke kondenzaci ar, takže se snižuje absoutní vhkost, ae reativní vhkost se nemění (φ = 00 %). Stav, ři kterém je vzduch o isobarickém ochazení arami nasycen, se nazývá rosný bod. Z uvedeného yne, že reativní vhkost vyjadřuje nejen kvantitativní oměr hmotnosti skutečné (ρ ) a maimání (ρ ) možné vhkosti ve vzduchu, ae i kvaitu vhkosti obsažené ve vzduchu (áry kaaina). Proto má význam vhkost reativní a ne absoutní Měrná vhkost vzduchu Při teených výočtech, nař. v sušárenství at. se často oužívá ro určení množství átky jednotky hmotnosti ( kg). Kdyby by brán kg vhkého vzduchu, měni by se v této jednotce se změnou vhkosti hmotnostní oměr suchého vzduchu a vodních ar. Proto je výhodnější očítat se stáe konstantní veičinou jednotkové hmotnosti kg suchého vzduchu a k tomuto doňovat kg hmotnosti ar vhkosti. akto vyjádřená hmotnost ar (m ) k jednotce hmotnosti suchého vzduchu (m vs ) vyjadřuje měrnou vhkost vzduchu (). m = ρ = [kg kg - ] (II 03) mvs ρvs ak vhký vzduch o měrné vhkosti má výsednou hmotnost ( + ) kg, řičemž zůstává neměnná hmotnost suchého vzduchu kg. 36
35 Označením měrné vhkosti nemá nic soečného se stejným označením suchosti ar. 4. Stavová rovnice vhkého vzduchu Pro vhký vzduch ze s vyhovující řesností oužít stavovou rovnice ideáního ynu, rotože suchý vzduch, res. jeho havní sožky kysík a dusík se vemi bíží vastnostem ideáních ynů a vodní áry ve vzduchu obsažené jsou zravida ve stavu řehřátém, kdy se rovněž vemi bíží vastnostem ideáního ynu. Pouze měrné teo vzduchu (c) se s teotou mění. Pro rozsah 0 až +00 C ze i toto ovažovat za konstantní s hodnotami: c = 004 J kg - K - a c v = 76 J kg - K -. Za těchto odmínek atí i Datonův zákon ro cekový tak směsi () vhkého vzduchu: = vs + [Pa] (II 04) a ro měrnou hmotnost: ρ = ρ vs + ρ [kg m -3 ] (II 05) Pro suchý vzduch a áru ři jednotkové hmotnosti a téže teotě atí stavová rovnice: vs v vs = r vs = v ρ vs v = r = ρ (II 06) odkud měrné hmotnosti (ρ vs, ρ ) a arciání taky ( vs, ) jsou dány: ρ vs = v vs r ; ρ = r. vs = ρ vs r vs ; = ρ r (II 07) dosazením do rovnice II 0 ze odovídající stavy vhkého vzduchu vyjádřit reativní vhkost (φ) oměru: r ϕ = = (II 08) r odkud: = φ kde arciání tak syté áry řidané teotě ze zjistit z tabuek vhkého vzduchu. Eistuje-i souvisost mezi reativní vhkostí (φ) a arciáním takem ar ( ) eistuje zřejmě i 37
36 souvisost mezi měrnou vhkostí () vzduchu a arciáními taky (, vs ). Podí arciáních taků určených rovnicemi II 07 dává: vs ρ = ρ vs r r vs rotože ρ / ρ vs = bude: vs r = r vs nebo = vs r r vs (II 09) Po dosazení numerických hodnot ynových konstant r vs = 87, J kg - K - a r = 46,5 J kg - K - bude: = 0,6 vs Z Datonova zákona yne, že vs =. Po dosazení do rovnice II 0 bude: = 0,6 (II 0) (II ) z čehož yne, že měrná vhkost vzduchu () za stáého taku nař. barometrického závisí ouze na arciáním taku ar ( ). Při = je = a směs obsahuje ouze samou vodní áru. Pro = 0 je = 0, což je suchý vzduch. Je-i vzduch arami nasycen ( = ), dosahuje měrná vhkost maimání hodnotu = 0,6 (II ) Pode této rovnice je kg suchého vzduchu schoen řijmout ři taku ouze toik vhkosti, koik udává rovnice II ( ). oto maimání množství závisí nejen na cekovém taku směsi (), ae také na taku syté áry ( ). ento tak ( ) závisí na teotě vhkého vzduchu a nezávisí na taku směsi. Pro tentýž tak, tj. ři téže teotě dosahuje tím větší hodnoty, čím je tak směsi () menší. Dosazením rovnice II 08 do II, ze vyjádřit vztah mezi reativní a měrnou vhkostí: ϕ = 0,6 nebo = 0,6 ϕ (II 3) 38
37 Měrná hmotnost a měrný objem vhkého vzduchu Měrná hmotnost vhkého vzduchu (ρ vh ) je dána součtem měrných hmotností suchého vzduchu (ρ vs ) a měrné hmotnosti áry (ρ ). Lze ji vyjádřit jako funkci φ vh = f (,, φ) nebo φ vh = f (,, ). V rvém říadě atí: ρ vh = ρ vs + ρ (II 3) dosazením do stavových rovnic (II 07) bude: + = vs vs vh r r ρ (II 4) ro vs = atí dáe: = + = vs vs vs vh r r r r r ρ a ro = φ je konečný výraz ρ vh : = = vs vs vs vs vh r r r r r r ρ ϕ ϕ (II 5) z rovnice yne, že měrná hmotnost vhkého vzduchu je menší než měrná hmotnost suchého vzduchu (ρ vs ) o druhý čen rovnice II 5. Je-i vhkost vzduchu (φ) nízká, ak je i arciání tak ar = φ nízký a zanedbatený vůči cekovému taku (). Pak řibižně atí: ρ vh = ρ vs (II 6) Ve druhém říadě je funkce ρ vh = f (,, ) s oužitím rovnice II dána tvarem: + = + = vs vs vs vs vh r r 0,6 r r r 0,6 r ρ (II 7) Měrný objem (v vh ) vzduchu je dán řevrácenou hodnotou měrné vhkosti (ρ vh ): = vs vs vh r r r v (II 8) rovnici II 8 - čitatee i jmenovatee násobíme (r vs ) vs vs vh r r r v + = (II 9) dáe atí = vs
38 a r r vs = vs (rov. II 09) v Po dosazení a úravě: v vh rvs = (II 0) (+ ) zětně ze dosadit vs = - = - φ v vh vs rvs = ϕ (+ ) (II ) odkud ze vyjádřit měrný objem směsi (v + ), tj. kg suchého vzduchu a kg vodní áry: v + = v vh ( + ) rvs = ϕ (II ) 4.4 Měrná teená kaacita vhkého vzduchu Měrná teená kaacita vhkého vzduchu objemu v + je určena součtem odíů měrných teených kaacit sožek: ( + ) c = c vh + c vs (II 3) odkud měrná teená kaacita jednotkové hmotnosti ( kg) vhkého vzduchu bude: c vh c + c vs = (II 4) Entaie vhkého vzduchu Entaie směsi (i), tj. vhkého vzduchu je dána součtem entaií oměrných zastouení sožek: Měrná entaie (i v ) [J kg - ] suchého vzduchu je dána: i v = c vs (t t 0 ) ro t 0 = 0 C bude: i v = c vs t (II 5) měrná entaie syté áry je dána: i = i + 3 = c t s + 3 (II 6) eota t s je teota vhkého vzduchu, jíž řísuší maimání arciání tak ( ) a 3 je výarné teo ři téže teotě t s, (i) je entaie syté kaainy ar vhkosti. 40
39 Moier ři výočtu diagramu vhkého vzduchu zaved ro jednoduchost ro sytou áru ři 0 C: i = 0 (II 7) ( 3) ak entaie kg této syté áry je: i = 0 (II 8) ( 3) Přičemž 0 ~ 500 kj kg - je výarné teo vody ři teotě t ( 3) 0 = 0 C. ak syté áry ři této teotě t 0 = 0 C je = 60 Pa (= 0,006 baru). Entaie kg řehřáté áry ři teotě t je dána: t i = 0 + ( 3) c t = 0 + c ( 3) t (II 9) t 0 a entaie kg této řehřáté áry je určena: i = ( 0 + c ( 3) t) (II 30) Nyní ze určit entaii vhkého vzduchu o hmotnosti ( + ) kg ři teotě t. Je dána součtem entaií kg suchého vzduchu (II 5) a entaie kg áry (II 30). edy atí: i + = c vs t + ( 0 + c ( 3) t) (II 3) nebo i + =,004 t + (500 +,84 t) [kj kg - ] V tomto říadě označujeme měrnou entaii (i) vhkého vzduchu i řesto, že se nejedná o entaii kg átky, nýbrž ( + ) kg směsi vhkého vzduchu. 4.6 Moierův i- diagram vhkého vzduchu Obecně je stav ynu určen třemi určujícími veičinami (,, v). Dvě z nich jsou nezávisé roměnné, třetí je funkcí ředešých dvou a ze je určit z rovnice stavu nebo teeného diagramu. Stav vhkého vzduchu je rovněž určen třemi veičinami takem (), teotou () a vhkostí reativní (φ) či měrnou (). Neze zde ae určit hodnotu jedné veičiny z hodnot dvou zbývajících veičin. Výočty stavu vhkého vzduchu ode dříve odvozených vztahů nejsou sožité, ae rychejší a názornější je řešení v i- diagramu vhkého vzduchu, který sestroji Moier (93). V kosoúhé souřadné soustavě i- jsou obsaženy tyto veičiny: teota (t), reativní vhkost (φ), tak syté áry ( ). 4
40 Diagram je vždy vyočten a nakresen ro jeden tak vzduchu, za kterého změny stavu robíhají. Zravida je i- diagram znázorňován tak, aby kosoúhé souřadnice i a svíray takový úhe, ři němž je nuová isoterma (t= 0 C) komá k ose entaie (i). V některých říadech je diagram sestrojen ro úhe mezi i a 35. V rvém říadě se skon nuové isoentay (i 0 = 0) určí z rovnice isoentay (II 3) ro t = 0 C: i 0 = 500 (II 3) na obr. č. II-8 určují derivace ředešé rovnice směrnici danou tangentou směrového úhu (α). i 0 = 500 odkud i0 500 tgα = = 500 = (II 33) ro ibovoně zvoenou měrnou vhkost () se určí tg α ro konstrukci směru isoenta v diagramu (obr. č. II-8). Obr. č. II-8 Konstrukce i- diagramu Skon isoterem se určí obdobně jako u isoenta z rovnice i =,004 t + (500 +,84 t) derivaci této rovnice di ode d ři t = konst, tj.: 4
Cvičení z termomechaniky Cvičení 5.
 Příklad V komresoru je kontinuálně stlačován objemový tok vzduchu *m 3.s- + o telotě 0 * C+ a tlaku 0, *MPa+ na tlak 0,7 *MPa+. Vyočtěte objemový tok vzduchu vystuujícího z komresoru, jeho telotu a říkon
Příklad V komresoru je kontinuálně stlačován objemový tok vzduchu *m 3.s- + o telotě 0 * C+ a tlaku 0, *MPa+ na tlak 0,7 *MPa+. Vyočtěte objemový tok vzduchu vystuujícího z komresoru, jeho telotu a říkon
Termodynamika ideálního plynu
 Přednáška 5 Termodynamika ideálního lynu 5.1 Základní vztahy ro ideální lyn 5.1.1 nitřní energie ideálního lynu Alikujme nyní oznatky získané v ředchozím textu na nejjednodužší termodynamickou soustavu
Přednáška 5 Termodynamika ideálního lynu 5.1 Základní vztahy ro ideální lyn 5.1.1 nitřní energie ideálního lynu Alikujme nyní oznatky získané v ředchozím textu na nejjednodužší termodynamickou soustavu
V p-v diagramu je tento proces znázorněn hyperbolou spojující body obou stavů plynu, je to tzv. izoterma :
 Jednoduché vratné děje ideálního lynu ) Děj izoter mický ( = ) Za ředokladu konstantní teloty se stavová rovnice ro zadané množství lynu změní na známý zákon Boylův-Mariottův, která říká, že součin tlaku
Jednoduché vratné děje ideálního lynu ) Děj izoter mický ( = ) Za ředokladu konstantní teloty se stavová rovnice ro zadané množství lynu změní na známý zákon Boylův-Mariottův, která říká, že součin tlaku
Termodynamické základy ocelářských pochodů
 29 3. Termodynamické základy ocelářských ochodů Termodynamika ůvodně vznikla jako vědní discilína zabývající se účinností teelných (arních) strojů. Později byly termodynamické zákony oužity ři studiu chemických
29 3. Termodynamické základy ocelářských ochodů Termodynamika ůvodně vznikla jako vědní discilína zabývající se účinností teelných (arních) strojů. Později byly termodynamické zákony oužity ři studiu chemických
VUT, FAST, Brno ústav Technických zařízení budov
 Termo realizaci inovovaných technicko-ekonomických VUT, FAST, Brno ústav Technických zařízen zení budov Vodní ára - VP Vaříme a dodáváme vodní áru VP: mokrou, suchou, sytou, řehřátou nízkotlakou, středotlakou
Termo realizaci inovovaných technicko-ekonomických VUT, FAST, Brno ústav Technických zařízen zení budov Vodní ára - VP Vaříme a dodáváme vodní áru VP: mokrou, suchou, sytou, řehřátou nízkotlakou, středotlakou
Fyzikální chemie. 1.2 Termodynamika
 Fyzikální chemie. ermodynamika Mgr. Sylvie Pavloková Letní semestr 07/08 děj izotermický izobarický izochorický konstantní V ermodynamika rvní termodynamický zákon (zákon zachování energie): U Q + W izotermický
Fyzikální chemie. ermodynamika Mgr. Sylvie Pavloková Letní semestr 07/08 děj izotermický izobarický izochorický konstantní V ermodynamika rvní termodynamický zákon (zákon zachování energie): U Q + W izotermický
Termodynamika par. Rovnovážný diagram látky 1 pevná fáze, 2 kapalná fáze, 3 plynná fáze
 ermodynamika par Fázové změny látky: Přivádíme-li pevné fázi látky teplo, dochází při jisté teplotě a tlaku ke změně pevné fáze na fázi kapalnou (tání) Jestliže spojíme body tání při různých tlacích, získáme
ermodynamika par Fázové změny látky: Přivádíme-li pevné fázi látky teplo, dochází při jisté teplotě a tlaku ke změně pevné fáze na fázi kapalnou (tání) Jestliže spojíme body tání při různých tlacích, získáme
VLHKÝ VZDUCH STAVOVÉ VELIČINY
 VLHKÝ VZDUCH STAVOVÉ VELIČINY Vlhký vzduch - vlhký vzduch je směsí suchého vzduchu a vodní áry okuující solečný objem - homogenní směs nastává okud je voda ve směsi v lynném stavu - heterogenní směs ve
VLHKÝ VZDUCH STAVOVÉ VELIČINY Vlhký vzduch - vlhký vzduch je směsí suchého vzduchu a vodní áry okuující solečný objem - homogenní směs nastává okud je voda ve směsi v lynném stavu - heterogenní směs ve
2.3.6 Práce plynu. Předpoklady: 2305
 .3.6 Práce lynu Předoklady: 305 Děje v lynech nejčastěji zobrazujeme omocí diagramů grafů závislosti tlaku na objemu. Na x-ovou osu vynášíme objem a na y-ovou osu tlak. Př. : Na obrázku je nakreslen diagram
.3.6 Práce lynu Předoklady: 305 Děje v lynech nejčastěji zobrazujeme omocí diagramů grafů závislosti tlaku na objemu. Na x-ovou osu vynášíme objem a na y-ovou osu tlak. Př. : Na obrázku je nakreslen diagram
2.6.7 Fázový diagram. Předpoklady: Popiš děje zakreslené v diagramu křivky syté páry. Za jakých podmínek mohou proběhnout?
 2.6.7 Fázový diagram Předoklady: 2606 Př. 1: Poiš děje zakreslené v diagramu křivky syté áry. Za jakých odmínek mohou roběhnout? 4 2 1 3 1) Sytá ára je za stálého tlaku zahřívána. Zvětšuje svůj objem a
2.6.7 Fázový diagram Předoklady: 2606 Př. 1: Poiš děje zakreslené v diagramu křivky syté áry. Za jakých odmínek mohou roběhnout? 4 2 1 3 1) Sytá ára je za stálého tlaku zahřívána. Zvětšuje svůj objem a
Termodynamika pro +EE1 a PEE
 ermodynamika ro +EE a PEE Literatura: htt://home.zcu.cz/~nohac/vyuka.htm#ee [0] Zakladni omocny text rednasek Doc. Schejbala [] Pomocne texty ke cviceni [] Prednaska cislo 7 - Zaklady termodynamiky [3]
ermodynamika ro +EE a PEE Literatura: htt://home.zcu.cz/~nohac/vyuka.htm#ee [0] Zakladni omocny text rednasek Doc. Schejbala [] Pomocne texty ke cviceni [] Prednaska cislo 7 - Zaklady termodynamiky [3]
7. VÝROBNÍ ČINNOST PODNIKU
 7. Výrobní činnost odniku Ekonomika odniku - 2009 7. VÝROBNÍ ČINNOST PODNIKU 7.1. Produkční funkce teoretický základ ekonomiky výroby 7.2. Výrobní kaacita Výrobní činnost je tou činností odniku, která
7. Výrobní činnost odniku Ekonomika odniku - 2009 7. VÝROBNÍ ČINNOST PODNIKU 7.1. Produkční funkce teoretický základ ekonomiky výroby 7.2. Výrobní kaacita Výrobní činnost je tou činností odniku, která
BH059 Tepelná technika budov Konzultace č. 2
 Vysoké učení technické v Brně Fakulta stavební Ústav ozemního stavitelství BH059 Teelná technika budov Konzultace č. 2 Zadání P6 zadáno na 2 konzultaci, P7 bude zadáno Průběh telot v konstrukci Kondenzace
Vysoké učení technické v Brně Fakulta stavební Ústav ozemního stavitelství BH059 Teelná technika budov Konzultace č. 2 Zadání P6 zadáno na 2 konzultaci, P7 bude zadáno Průběh telot v konstrukci Kondenzace
FYZIKA 2. ROČNÍK. Změny skupenství látek. Tání a tuhnutí. Pevná látka. soustava velkého počtu částic. Plyn
 Zěny skuenství látek Pevná látka Kaalina Plyn soustava velkého očtu částic Má-li soustava v rovnovážné stavu ve všech částech stejné fyzikální a cheické vlastnosti (stejnou hustotu, stejnou strukturu a
Zěny skuenství látek Pevná látka Kaalina Plyn soustava velkého očtu částic Má-li soustava v rovnovážné stavu ve všech částech stejné fyzikální a cheické vlastnosti (stejnou hustotu, stejnou strukturu a
Termomechanika 8. přednáška Doc. Dr. RNDr. Miroslav Holeček
 Termomechanika 8. přednáška Doc. Dr. RNDr. Miroslav Holeček Upozornění: Tato prezentace slouží výhradně pro výukové účely Fakulty strojní Západočeské univerzity v Plzni. Byla sestavena autorem s využitím
Termomechanika 8. přednáška Doc. Dr. RNDr. Miroslav Holeček Upozornění: Tato prezentace slouží výhradně pro výukové účely Fakulty strojní Západočeské univerzity v Plzni. Byla sestavena autorem s využitím
Hydraulické odpory třecí odpory místní odpory třecí odpory laminární proudění turbulentní proudění
 Hyrauické oory Při rouění reáných tekutin znikají násekem iskozity hyrauické oory, tj. síy, které ůsobí roti ohybu částic tekutiny. Hyrauický oor ři rouění zniká zájemným třením částic rouící tekutiny
Hyrauické oory Při rouění reáných tekutin znikají násekem iskozity hyrauické oory, tj. síy, které ůsobí roti ohybu částic tekutiny. Hyrauický oor ři rouění zniká zájemným třením částic rouící tekutiny
Projekt realizovaný na SPŠ Nové Město nad Metují. s finanční podporou v Operačním programu Vzdělávání pro konkurenceschopnost Královéhradeckého kraje
 Projekt realizoaný na SPŠ Noé Město nad Metují s finanční odorou Oeračním rogramu Vzděláání ro konkurenceschonost Králoéhradeckého kraje ermodynamika Ing. Jan Jemelík Ideální lyn: - ideálně stlačitelná
Projekt realizoaný na SPŠ Noé Město nad Metují s finanční odorou Oeračním rogramu Vzděláání ro konkurenceschonost Králoéhradeckého kraje ermodynamika Ing. Jan Jemelík Ideální lyn: - ideálně stlačitelná
3.5 Tepelné děje s ideálním plynem stálé hmotnosti, izotermický děj
 3.5 Tepelné děje s ideálním plynem stálé hmotnosti, izotermický děj a) tepelný děj přechod plynu ze stavu 1 do stavu tepelnou výměnou nebo konáním práce dále uvaž., že hmotnost plynu m = konst. a navíc
3.5 Tepelné děje s ideálním plynem stálé hmotnosti, izotermický děj a) tepelný děj přechod plynu ze stavu 1 do stavu tepelnou výměnou nebo konáním práce dále uvaž., že hmotnost plynu m = konst. a navíc
Hlavní body. Teplotní závislosti fyzikálních veličin. Teplota, měření
 e r i k a Havní body epota, ěření epotní závisosti fyzikáních veičin Kinetická teorie pynů Maxweova rozděovací funkce epo, ěrné tepo, kaorietrie epota Je zákadní veičinou, kterou neze odvodit? Čověk ji
e r i k a Havní body epota, ěření epotní závisosti fyzikáních veičin Kinetická teorie pynů Maxweova rozděovací funkce epo, ěrné tepo, kaorietrie epota Je zákadní veičinou, kterou neze odvodit? Čověk ji
VYBRANÉ STATĚ Z PROCESNÍHO INŢENÝRSTVÍ cvičení 12
 UNIVERZITA TOMÁŠE BATI VE ZLÍNĚ FAKULTA APLIKOVANÉ INFORMATIKY VYBRANÉ STATĚ Z PROCESNÍHO INŢENÝRSTVÍ cvičení 2 Termodynamika reálných plynů část 2 Hana Charvátová, Dagmar Janáčová Zlín 203 Tento studijní
UNIVERZITA TOMÁŠE BATI VE ZLÍNĚ FAKULTA APLIKOVANÉ INFORMATIKY VYBRANÉ STATĚ Z PROCESNÍHO INŢENÝRSTVÍ cvičení 2 Termodynamika reálných plynů část 2 Hana Charvátová, Dagmar Janáčová Zlín 203 Tento studijní
Analytická metoda aneb Využití vektorů v geometrii
 KM/GVS Geometrické vidění světa (Design) nalytická metoda aneb Využití vektorů v geometrii Použité značky a symboly R, C, Z obor reálných, komleních, celých čísel geometrický vektor R n aritmetický vektor
KM/GVS Geometrické vidění světa (Design) nalytická metoda aneb Využití vektorů v geometrii Použité značky a symboly R, C, Z obor reálných, komleních, celých čísel geometrický vektor R n aritmetický vektor
STRUKTURA A VLASTNOSTI KAPALIN
 I N V E S T I C E D O O Z V O J E V Z D Ě L Á V Á N Í STUKTUA A VLASTNOSTI KAPALIN. Povrchové napětí a) yzikání jev Povrch kapain se chová jako napjatá pružná membrána (důkaz vodoměrka, maé kapičky koue)
I N V E S T I C E D O O Z V O J E V Z D Ě L Á V Á N Í STUKTUA A VLASTNOSTI KAPALIN. Povrchové napětí a) yzikání jev Povrch kapain se chová jako napjatá pružná membrána (důkaz vodoměrka, maé kapičky koue)
6. Vliv způsobu provozu uzlu transformátoru na zemní poruchy
 6. Vliv zůsobu rovozu uzlu transformátoru na zemní oruchy Zemní oruchou se rozumí sojení jedné nebo více fází se zemí. Zemní orucha může být zůsobena řeskokem na izolátoru, růrazem evné izolace, ádem řetrženého
6. Vliv zůsobu rovozu uzlu transformátoru na zemní oruchy Zemní oruchou se rozumí sojení jedné nebo více fází se zemí. Zemní orucha může být zůsobena řeskokem na izolátoru, růrazem evné izolace, ádem řetrženého
7.5.13 Rovnice paraboly
 7.5.1 Rovnice arabol Předoklad: 751 Př. 1: Seiš všechn rovnice ro arabol a nakresli k nim odovídající obrázk. Na každém obrázku vznač vzdálenost. = = = = Pedagogická oznámka: Sesání arabol je důležité,
7.5.1 Rovnice arabol Předoklad: 751 Př. 1: Seiš všechn rovnice ro arabol a nakresli k nim odovídající obrázk. Na každém obrázku vznač vzdálenost. = = = = Pedagogická oznámka: Sesání arabol je důležité,
Z toho se η využije na zajištění funkcí automobilu a na překonání odporu vzduchu. l 100 km. 2 body b) Hledáme minimum funkce θ = 1.
 Řešení úoh. koa 59. ročníku fyzikání oympiády. Kategorie A Autor úoh: J. Thomas.a) Na dráze vt bude zapotřebí objem paiva V θ θv t. Při jeho spáení se získá tepo Q mh ρv H ρθvh t. Z toho se η využije na
Řešení úoh. koa 59. ročníku fyzikání oympiády. Kategorie A Autor úoh: J. Thomas.a) Na dráze vt bude zapotřebí objem paiva V θ θv t. Při jeho spáení se získá tepo Q mh ρv H ρθvh t. Z toho se η využije na
2.1 Stáčivost v závislosti na koncentraci opticky aktivní látky
 1 Pracovní úkoy 1. Změřte závisost stočení poarizační roviny na koncentraci vodního roztoku gukozy v rozmezí 0 500 g/. Pro jednu zvoenou koncentraci proveďte 5 měření úhu stočení poarizační roviny. Jednu
1 Pracovní úkoy 1. Změřte závisost stočení poarizační roviny na koncentraci vodního roztoku gukozy v rozmezí 0 500 g/. Pro jednu zvoenou koncentraci proveďte 5 měření úhu stočení poarizační roviny. Jednu
STRUKTURA A VLASTNOSTI PLYNŮ
 I N E S I C E D O R O Z O J E Z D Ě L Á Á N Í SRUKURA A LASNOSI PLYNŮ. Ideální lyn ředstavuje model ideálního lynu, který často oužíváme k oisu různých dějů. Naříklad ozději ředokládáme, že všechny molekuly
I N E S I C E D O R O Z O J E Z D Ě L Á Á N Í SRUKURA A LASNOSI PLYNŮ. Ideální lyn ředstavuje model ideálního lynu, který často oužíváme k oisu různých dějů. Naříklad ozději ředokládáme, že všechny molekuly
Ideální plyn. Stavová rovnice Děje v ideálním plynu Práce plynu, Kruhový děj, Tepelné motory
 Struktura a vlastnosti plynů Ideální plyn Vlastnosti ideálního plynu: Ideální plyn Stavová rovnice Děje v ideálním plynu Práce plynu, Kruhový děj, epelné motory rozměry molekul jsou ve srovnání se střední
Struktura a vlastnosti plynů Ideální plyn Vlastnosti ideálního plynu: Ideální plyn Stavová rovnice Děje v ideálním plynu Práce plynu, Kruhový děj, epelné motory rozměry molekul jsou ve srovnání se střední
HYDROPNEUMATICKÝ VAKOVÝ AKUMULÁTOR
 HYDROPNEUMATICKÝ AKOÝ AKUMULÁTOR OSP 050 ŠEOBECNÉ INFORMACE ýočet hydroneumatického akumulátoru ZÁKLADNÍ INFORMACE Při výočtu hydroneumatického akumulátoru se vychází ze stavové změny lynu v akumulátoru.
HYDROPNEUMATICKÝ AKOÝ AKUMULÁTOR OSP 050 ŠEOBECNÉ INFORMACE ýočet hydroneumatického akumulátoru ZÁKLADNÍ INFORMACE Při výočtu hydroneumatického akumulátoru se vychází ze stavové změny lynu v akumulátoru.
13. Skupenské změny látek
 13. Skuenské změny látek Skuenství je konkrétní forma látky, charakterizovaná ředevším usořádáním částic v látce a rojevující se tyickými fyzikálními a chemickými vlastnostmi. Pro označení skuenství se
13. Skuenské změny látek Skuenství je konkrétní forma látky, charakterizovaná ředevším usořádáním částic v látce a rojevující se tyickými fyzikálními a chemickými vlastnostmi. Pro označení skuenství se
1.5.2 Mechanická práce II
 .5. Mechanická ráce II Předoklady: 50 Př. : Jakou minimální ráci vykonáš ři řemístění bedny o hmotnosti 50 k o odlaze o vzdálenost 5 m. Příklad sočítej dvakrát, jednou zanedbej třecí sílu mezi bednou a
.5. Mechanická ráce II Předoklady: 50 Př. : Jakou minimální ráci vykonáš ři řemístění bedny o hmotnosti 50 k o odlaze o vzdálenost 5 m. Příklad sočítej dvakrát, jednou zanedbej třecí sílu mezi bednou a
NÁVRH A OVĚŘENÍ BETONOVÉ OPŘENÉ PILOTY ZATÍŽENÉ V HLAVĚ KOMBINACÍ SIL
 NÁVRH A OVĚŘENÍ BETONOVÉ OPŘENÉ PILOTY ZATÍŽENÉ V HLAVĚ KOMBINACÍ SIL 1. ZADÁNÍ Navrhněte růměr a výztuž vrtané iloty délky L neosuvně ořené o skalní odloží zatížené v hlavě zadanými vnitřními silami (viz
NÁVRH A OVĚŘENÍ BETONOVÉ OPŘENÉ PILOTY ZATÍŽENÉ V HLAVĚ KOMBINACÍ SIL 1. ZADÁNÍ Navrhněte růměr a výztuž vrtané iloty délky L neosuvně ořené o skalní odloží zatížené v hlavě zadanými vnitřními silami (viz
Kvantová a statistická fyzika 2 (Termodynamika a statistická fyzika)
 Kvantová a statistická fyzika 2 (ermodynamika a statistická fyzika) ermodynamika ermodynamika se zabývá zkoumáním obecných vlastností makroskoických systémů v rovnováze, zákonitostmi makroskoických rocesů,
Kvantová a statistická fyzika 2 (ermodynamika a statistická fyzika) ermodynamika ermodynamika se zabývá zkoumáním obecných vlastností makroskoických systémů v rovnováze, zákonitostmi makroskoických rocesů,
Poznámky k cvičením z termomechaniky Cvičení 3.
 Vnitřní energie U Vnitřní energie U je stavová veličina U = U (p, V, T), ale závisí pouze na teplotě (experiment Gay-Lussac / Joule) U = f(t) Pro měrnou vnitřní energii (tedy pro vnitřní energii jednoho
Vnitřní energie U Vnitřní energie U je stavová veličina U = U (p, V, T), ale závisí pouze na teplotě (experiment Gay-Lussac / Joule) U = f(t) Pro měrnou vnitřní energii (tedy pro vnitřní energii jednoho
Jev elektromagnetické indukce
 Jev eektromagnetické indukce V minuých kapitoách jsme si jistě uvědomii, že pojmy kid a pohyb, které byy vemi významné u mechanických dějů, při zkoumání eektrických a magnetických jevů nabyy přímo zásadní
Jev eektromagnetické indukce V minuých kapitoách jsme si jistě uvědomii, že pojmy kid a pohyb, které byy vemi významné u mechanických dějů, při zkoumání eektrických a magnetických jevů nabyy přímo zásadní
7. Měření dutých objemů pomocí komprese plynu a určení Poissonovy konstanty vzduchu Úkol 1: Určete objem skleněné láhve s kohoutem kompresí plynu.
 7. Měření dutých objemů omocí komrese lynu a určení Poissonovy konstanty vzduchu Úkol : Určete objem skleněné láhve s kohoutem komresí lynu. Pomůcky Měřený objem (láhev s kohoutem), seciální lynová byreta
7. Měření dutých objemů omocí komrese lynu a určení Poissonovy konstanty vzduchu Úkol : Určete objem skleněné láhve s kohoutem komresí lynu. Pomůcky Měřený objem (láhev s kohoutem), seciální lynová byreta
Numerické výpočty proudění v kanále stálého průřezu při ucpání kanálu válcovou sondou
 Konference ANSYS 2009 Numerické výočty roudění v kanále stálého růřezu ři ucání kanálu válcovou sondou L. Tajč, B. Rudas, a M. Hoznedl ŠKODA POWER a.s., Tylova 1/57, Plzeň, 301 28 michal.hoznedl@skoda.cz
Konference ANSYS 2009 Numerické výočty roudění v kanále stálého růřezu ři ucání kanálu válcovou sondou L. Tajč, B. Rudas, a M. Hoznedl ŠKODA POWER a.s., Tylova 1/57, Plzeň, 301 28 michal.hoznedl@skoda.cz
IDEÁLNÍ PLYN. Stavová rovnice
 IDEÁLNÍ PLYN Stavová rovnice Ideální plyn ) rozměry molekul jsou zanedbatelné vzhledem k jejich vzdálenostem 2) molekuly plynu na sebe působí jen při vzájemných srážkách 3) všechny srážky jsou dokonale
IDEÁLNÍ PLYN Stavová rovnice Ideální plyn ) rozměry molekul jsou zanedbatelné vzhledem k jejich vzdálenostem 2) molekuly plynu na sebe působí jen při vzájemných srážkách 3) všechny srážky jsou dokonale
KRUHOVÝ DĚJ S IDEÁLNÍM PLYNEM. Studijní text pro řešitele FO a ostatní zájemce o fyziku. Přemysl Šedivý. 1 Základní pojmy 2
 Obsah KRUHOÝ DĚJ S IDEÁLNÍM PLYNEM Studijní text ro řešitele FO a ostatní zájemce o fyziku Přemysl Šedivý Základní ojmy ztahy užívané ři oisu kruhových dějů s ideálním lynem Přehled základních dějů v ideálním
Obsah KRUHOÝ DĚJ S IDEÁLNÍM PLYNEM Studijní text ro řešitele FO a ostatní zájemce o fyziku Přemysl Šedivý Základní ojmy ztahy užívané ři oisu kruhových dějů s ideálním lynem Přehled základních dějů v ideálním
CVIČENÍ Z ELEKTRONIKY
 Střední růmyslová škola elektrotechnická Pardubice CVIČENÍ Z ELEKRONIKY Harmonická analýza Příjmení : Česák Číslo úlohy : Jméno : Petr Datum zadání :.1.97 Školní rok : 1997/98 Datum odevzdání : 11.1.97
Střední růmyslová škola elektrotechnická Pardubice CVIČENÍ Z ELEKRONIKY Harmonická analýza Příjmení : Česák Číslo úlohy : Jméno : Petr Datum zadání :.1.97 Školní rok : 1997/98 Datum odevzdání : 11.1.97
CVIČENÍ 4 - PROVOZNÍ STAVY VZDUCHOTECHNICKÉ JEDNOTKY
 CVIČENÍ 4 - PROVOZNÍ STAVY VZDUCHOTECHNICKÉ JEDNOTKY - ři zracování tohoto cvičení studenti naváží na cvičení č.4 a č.5 - oužijí zejména vstuní údaje ze cvičení č.4, u kterých bude třeba sladit kombinaci
CVIČENÍ 4 - PROVOZNÍ STAVY VZDUCHOTECHNICKÉ JEDNOTKY - ři zracování tohoto cvičení studenti naváží na cvičení č.4 a č.5 - oužijí zejména vstuní údaje ze cvičení č.4, u kterých bude třeba sladit kombinaci
Stavová rovnice. Ve stavu termodynamické rovnováhy termodynamicky homogenní soustavy jsou všechny vnitřní parametry Y i
 ermodynamický ostulát: Stavová rovnice e stavu termodynamické rovnováhy termodynamicky homogenní soustavy jsou všechny vnitřní arametry Y i určeny jako funkce všech vnějších arametrů X j a teloty Y i f
ermodynamický ostulát: Stavová rovnice e stavu termodynamické rovnováhy termodynamicky homogenní soustavy jsou všechny vnitřní arametry Y i určeny jako funkce všech vnějších arametrů X j a teloty Y i f
Termomechanika 6. přednáška Doc. Dr. RNDr. Miroslav Holeček
 Termomechanika 6. přednáška Doc. Dr. RNDr. Miroslav Holeček Upozornění: Tato prezentace slouží výhradně pro výukové účely Fakulty strojní Západočeské univerzity v Plzni. Byla sestavena autorem s využitím
Termomechanika 6. přednáška Doc. Dr. RNDr. Miroslav Holeček Upozornění: Tato prezentace slouží výhradně pro výukové účely Fakulty strojní Západočeské univerzity v Plzni. Byla sestavena autorem s využitím
EKONOMETRIE 4. přednáška Modely chování spotřebitele
 EKONOMETRIE 4. řednáška Modely chování sotřebitele Rozočtové omezení Sotřebitel ři svém rozhodování resektuje tzv. rozočtové omezení x + x y, kde x i množství i-té sotřební komodity, i cena i-té sotřební
EKONOMETRIE 4. řednáška Modely chování sotřebitele Rozočtové omezení Sotřebitel ři svém rozhodování resektuje tzv. rozočtové omezení x + x y, kde x i množství i-té sotřební komodity, i cena i-té sotřební
2.6.6 Sytá pára. Předpoklady: 2604
 .6.6 Sytá ára Předolady: 604 Oaování: aaliny se vyařují za aždé teloty. Nejrychlejší částice uniají z aaliny a stává se z nich ára. Do isy nalijee vodu voda se ostuně vyařuje naonec zůstane isa rázdná,
.6.6 Sytá ára Předolady: 604 Oaování: aaliny se vyařují za aždé teloty. Nejrychlejší částice uniají z aaliny a stává se z nich ára. Do isy nalijee vodu voda se ostuně vyařuje naonec zůstane isa rázdná,
CVIČENÍ 3: VLHKÝ VZDUCH A MOLLIÉRŮV DIAGRAM
 CVIČENÍ 3: VLHKÝ VZDUCH A MOLLIÉRŮV DIAGRAM Co to je vlhký vzduch? - vlhký vzduch je směsí suchého vzduchu a vodní páry okupující společný objem - vodní pára ve směsi může měnit formu z plynné na kapalnou
CVIČENÍ 3: VLHKÝ VZDUCH A MOLLIÉRŮV DIAGRAM Co to je vlhký vzduch? - vlhký vzduch je směsí suchého vzduchu a vodní páry okupující společný objem - vodní pára ve směsi může měnit formu z plynné na kapalnou
PZP (2011/2012) 3/1 Stanislav Beroun
 PZP (0/0) 3/ tanislav Beroun Výměna tela mezi nální válce a stěnami, telotní zatížení vybraných dílů PM elo, které se odvádí z nálně válce, se ředává stěnám ve válci řevážně řestuem, u vznětových motorů
PZP (0/0) 3/ tanislav Beroun Výměna tela mezi nální válce a stěnami, telotní zatížení vybraných dílů PM elo, které se odvádí z nálně válce, se ředává stěnám ve válci řevážně řestuem, u vznětových motorů
HYDROMECHANICKÉ PROCESY. Potrubí a potrubní sítě (přednáška)
 HYDROMECHANICKÉ PROCESY Potrbí a otrbní sítě (řenáška) Doc. Ing. Tomáš Jirot, Ph.D. (e-mai: Tomas.Jirot@fs.cvt.cz, te.: 435 68) POTRUBÍ A POTRUBNÍ SÍTĚ Integrání rovnice kontinity S S Inženýrská Bernoiova
HYDROMECHANICKÉ PROCESY Potrbí a otrbní sítě (řenáška) Doc. Ing. Tomáš Jirot, Ph.D. (e-mai: Tomas.Jirot@fs.cvt.cz, te.: 435 68) POTRUBÍ A POTRUBNÍ SÍTĚ Integrání rovnice kontinity S S Inženýrská Bernoiova
Aproximativní analytické řešení jednorozměrného proudění newtonské kapaliny
 U8 Ústav rocesní a zracovatelské techniky F ČVUT v Praze Aroximativní analytické řešení jednorozměrného roudění newtonské kaaliny Některé říady jednorozměrného roudění newtonské kaaliny lze řešit řibližně
U8 Ústav rocesní a zracovatelské techniky F ČVUT v Praze Aroximativní analytické řešení jednorozměrného roudění newtonské kaaliny Některé říady jednorozměrného roudění newtonské kaaliny lze řešit řibližně
Termodynamické zákony
 Termodynamické zákony Makroskopická práce termodynamické soustavy Již jsme uvedli, že změna vnitřní energie soustavy je obecně vyvolána dvěma ději: tepelnou výměnou mezi soustavou a okolím a konáním práce
Termodynamické zákony Makroskopická práce termodynamické soustavy Již jsme uvedli, že změna vnitřní energie soustavy je obecně vyvolána dvěma ději: tepelnou výměnou mezi soustavou a okolím a konáním práce
12. Termomechanika par, Clausiova-Clapeyronova rovnice, parní tabulky, základni termodynamické děje v oblasti par
 1/18 12. Termomechanika par, Clausiova-Clapeyronova rovnice, parní tabulky, základni termodynamické děje v oblasti par Příklad: 12.1, 12.2, 12.3, 12.4, 12.5, 12.6, 12.7, 12.8, 12.9, 12.10, 12.11, 12.12,
1/18 12. Termomechanika par, Clausiova-Clapeyronova rovnice, parní tabulky, základni termodynamické děje v oblasti par Příklad: 12.1, 12.2, 12.3, 12.4, 12.5, 12.6, 12.7, 12.8, 12.9, 12.10, 12.11, 12.12,
Řešení úloh 1. kola 60. ročníku fyzikální olympiády. Kategorie B Autoři úloh: J. Thomas (1, 2, 3, 4, 5, 7), M. Jarešová (6)
 Řešení úoh 1. koa 60. ročníku fyzikání oympiády. Kategorie B Autoři úoh: J. Thomas (1, 2, 3, 4, 5, 7), M. Jarešová (6) h 1.a) Protože vzdáenost bodů K a O je cos α, je doba etu kuičky z bodu K do bodu
Řešení úoh 1. koa 60. ročníku fyzikání oympiády. Kategorie B Autoři úoh: J. Thomas (1, 2, 3, 4, 5, 7), M. Jarešová (6) h 1.a) Protože vzdáenost bodů K a O je cos α, je doba etu kuičky z bodu K do bodu
03 Návrh pojistného a zabezpečovacího zařízení
 03 Návrh ojistného a zabezečovacího zařízení Roman Vavřička ČVUT v raze, Fakulta strojní Ústav techniky rostředí 1/14 htt://ut.fs.cvut.cz Roman.Vavricka@fs.cvut.cz ojistné zařízení chrání zdroj tela roti
03 Návrh ojistného a zabezečovacího zařízení Roman Vavřička ČVUT v raze, Fakulta strojní Ústav techniky rostředí 1/14 htt://ut.fs.cvut.cz Roman.Vavricka@fs.cvut.cz ojistné zařízení chrání zdroj tela roti
Oddělení technické elektrochemie, A037. LABORATORNÍ PRÁCE č.9 CYKLICKÁ VOLTAMETRIE
 ÚSTV NORGNIKÉ THNOLOGI Oddělení technické elektrochemie, 037 LBORTORNÍ PRÁ č.9 YKLIKÁ VOLTMTRI yklická voltametrie yklická voltametrie atří do skuiny otenciodynamických exerimentálních metod. Ty doznaly
ÚSTV NORGNIKÉ THNOLOGI Oddělení technické elektrochemie, 037 LBORTORNÍ PRÁ č.9 YKLIKÁ VOLTMTRI yklická voltametrie yklická voltametrie atří do skuiny otenciodynamických exerimentálních metod. Ty doznaly
Cvičení z termodynamiky a statistické fyziky
 Cvičení z termodynamiky a statistické fyziky 1 Matematické základy 1 Parciální derivace Necht F(x,y = xe x2 +y 2 Sočtěte F x, F y, 2 Úlný diferenciál I Bud 2 F x 2, 2 F x y, dω = A(x,ydx + B(x,ydy 2 F
Cvičení z termodynamiky a statistické fyziky 1 Matematické základy 1 Parciální derivace Necht F(x,y = xe x2 +y 2 Sočtěte F x, F y, 2 Úlný diferenciál I Bud 2 F x 2, 2 F x y, dω = A(x,ydx + B(x,ydy 2 F
Kmitavý pohyb trochu jinak
 Kmitavý pohyb trochu jinak JIŘÍ ESAŘ, PER BAROŠ Katedra fyziky, Pedaoická fakuta, JU České Budějovice Kmitavý pohyb patří mezi zákadní fyzikání děje. Většinou se tato část fyziky redukuje na matematický
Kmitavý pohyb trochu jinak JIŘÍ ESAŘ, PER BAROŠ Katedra fyziky, Pedaoická fakuta, JU České Budějovice Kmitavý pohyb patří mezi zákadní fyzikání děje. Většinou se tato část fyziky redukuje na matematický
PROCESY V TECHNICE BUDOV 8
 UNIVERZITA TOMÁŠE BATI VE ZLÍNĚ FAKULTA APLIKOVANÉ INFORMATIKY PROCESY V TECHNICE BUDOV 8 Dagmar Janáčová, Hana Charvátová Zlín 2013 Tento studijní materiál vznikl za finanční podpory Evropského sociálního
UNIVERZITA TOMÁŠE BATI VE ZLÍNĚ FAKULTA APLIKOVANÉ INFORMATIKY PROCESY V TECHNICE BUDOV 8 Dagmar Janáčová, Hana Charvátová Zlín 2013 Tento studijní materiál vznikl za finanční podpory Evropského sociálního
IV. Fázové rovnováhy dokončení
 IV. Fázové rovnováhy dokončení 4. Fázové rovnováhy Ústav rocesní a zracovatelské techniky 1 4.3.2 Soustava tuhá složka kaalná složka Dvousložková soustava s 2 Křivka rozustnosti T nenasycený roztok nasycený
IV. Fázové rovnováhy dokončení 4. Fázové rovnováhy Ústav rocesní a zracovatelské techniky 1 4.3.2 Soustava tuhá složka kaalná složka Dvousložková soustava s 2 Křivka rozustnosti T nenasycený roztok nasycený
Výpočty za použití zákonů pro ideální plyn
 ýočty za oužití zákonů ro ideální lyn Látka v lynné stavu je tvořena volnýi atoy(onoatoickýi olekulai), ionty nebo olekulai. Ideální lyn- olekuly na sebe neůsobí žádnýi silai, jejich obje je ve srovnání
ýočty za oužití zákonů ro ideální lyn Látka v lynné stavu je tvořena volnýi atoy(onoatoickýi olekulai), ionty nebo olekulai. Ideální lyn- olekuly na sebe neůsobí žádnýi silai, jejich obje je ve srovnání
CVIČENÍ 1 - část 2: MOLLIÉRŮV DIAGRAM A ZMĚNY STAVU VLHKÉHO VZDUCHU
 CVIČENÍ 1 - část 2: MOLLIÉRŮV DIAGRAM A ZMĚNY STAVU VLHKÉHO VZDUCHU Co to je Molliérův diagram? - grafický nástroj pro zpracování izobarických změn stavů vlhkého vzduchu - diagram je sestaven pro konstantní
CVIČENÍ 1 - část 2: MOLLIÉRŮV DIAGRAM A ZMĚNY STAVU VLHKÉHO VZDUCHU Co to je Molliérův diagram? - grafický nástroj pro zpracování izobarických změn stavů vlhkého vzduchu - diagram je sestaven pro konstantní
PROCESY V TECHNICE BUDOV 9
 UNIVERZIA OMÁŠE BAI VE ZLÍNĚ FAKULA APLIKOVANÉ INFORMAIKY PROCESY V ECHNICE BUDOV 9 ermodynamika reálných plynů (2. část) Dagmar Janáčová, Hana Charvátová Zlín 2013 ento studijní materiál vznikl za finanční
UNIVERZIA OMÁŠE BAI VE ZLÍNĚ FAKULA APLIKOVANÉ INFORMAIKY PROCESY V ECHNICE BUDOV 9 ermodynamika reálných plynů (2. část) Dagmar Janáčová, Hana Charvátová Zlín 2013 ento studijní materiál vznikl za finanční
Kruhový děj s plynem
 .. Kruhový děj s lynem Předoklady: 0 Chceme využít skutečnost, že lyn koná ři rozínání ráci, na konstrukci motoru. Nejjednodušší možnost: Pustíme nafouknutý balónek. Balónek se vyfukuje, vytlačuje vzduch
.. Kruhový děj s lynem Předoklady: 0 Chceme využít skutečnost, že lyn koná ři rozínání ráci, na konstrukci motoru. Nejjednodušší možnost: Pustíme nafouknutý balónek. Balónek se vyfukuje, vytlačuje vzduch
Způsobilost. Data a parametry. Menu: QCExpert Způsobilost
 Zůsobilost Menu: QExert Zůsobilost Modul očítá na základě dat a zadaných secifikačních mezí hodnoty různých indexů zůsobilosti (caability index, ) a výkonnosti (erformance index, ). Dále jsou vyočítány
Zůsobilost Menu: QExert Zůsobilost Modul očítá na základě dat a zadaných secifikačních mezí hodnoty různých indexů zůsobilosti (caability index, ) a výkonnosti (erformance index, ). Dále jsou vyočítány
Změna skupenství, Tání a tuhnutí, Sublimace a desublimace Vypařování a kapalnění Sytá pára, Fázový diagram, Vodní pára
 Zěny skupenství átek Zěna skupenství, Tání a tuhnutí, Subiace a desubiace Vypařování a kapanění Sytá pára, Fázový diagra, Vodní pára Zěna skupenství = fyzikání děj, při které se ění skupenství átky Skupenství
Zěny skupenství átek Zěna skupenství, Tání a tuhnutí, Subiace a desubiace Vypařování a kapanění Sytá pára, Fázový diagra, Vodní pára Zěna skupenství = fyzikání děj, při které se ění skupenství átky Skupenství
3. Silové působení na hmotné objekty
 SÍL OENT SÍLY - 10-3. Silové ůsobení na hmotné objekty 3.1 Síla a její osuvné účinky V této kaitole si oíšeme vlastnosti silových účinků ůsobících na konstrukce a reálné mechanické soustavy. Zavedeme kvantitativní
SÍL OENT SÍLY - 10-3. Silové ůsobení na hmotné objekty 3.1 Síla a její osuvné účinky V této kaitole si oíšeme vlastnosti silových účinků ůsobících na konstrukce a reálné mechanické soustavy. Zavedeme kvantitativní
9. Struktura a vlastnosti plynů
 9. Struktura a vlastnosti plynů Osnova: 1. Základní pojmy 2. Střední kvadratická rychlost 3. Střední kinetická energie molekuly plynu 4. Stavová rovnice ideálního plynu 5. Jednoduché děje v plynech a)
9. Struktura a vlastnosti plynů Osnova: 1. Základní pojmy 2. Střední kvadratická rychlost 3. Střední kinetická energie molekuly plynu 4. Stavová rovnice ideálního plynu 5. Jednoduché děje v plynech a)
Kontrolní otázky k 1. přednášce z TM
 Kontrolní otázky k 1. přednášce z TM 1. Jak závisí hodnota izobarického součinitele objemové roztažnosti ideálního plynu na teplotě a jak na tlaku? Odvoďte. 2. Jak závisí hodnota izochorického součinitele
Kontrolní otázky k 1. přednášce z TM 1. Jak závisí hodnota izobarického součinitele objemové roztažnosti ideálního plynu na teplotě a jak na tlaku? Odvoďte. 2. Jak závisí hodnota izochorického součinitele
PLYNNÉ LÁTKY. Mgr. Jan Ptáčník - GJVJ - Fyzika - Termika - 2. ročník
 PLYNNÉ LÁTKY Mgr. Jan Ptáčník - GJVJ - Fyzika - Termika - 2. ročník Ideální plyn Po molekulách ideálního plynu požadujeme: 1.Rozměry molekul ideálního plynu jsou ve srovnání se střední vzdáleností molekul
PLYNNÉ LÁTKY Mgr. Jan Ptáčník - GJVJ - Fyzika - Termika - 2. ročník Ideální plyn Po molekulách ideálního plynu požadujeme: 1.Rozměry molekul ideálního plynu jsou ve srovnání se střední vzdáleností molekul
h nadmořská výška [m]
![h nadmořská výška [m] h nadmořská výška [m]](/thumbs/92/109475205.jpg) Katedra prostředí staveb a TZB KLIMATIZACE, VĚTRÁNÍ Cvičení pro navazující magisterské studium studijního oboru Prostředí staveb Cvičení č. 1 Zpracoval: Ing. Zdeněk GALDA Nové výukové moduly vznikly za
Katedra prostředí staveb a TZB KLIMATIZACE, VĚTRÁNÍ Cvičení pro navazující magisterské studium studijního oboru Prostředí staveb Cvičení č. 1 Zpracoval: Ing. Zdeněk GALDA Nové výukové moduly vznikly za
Zákony ideálního plynu
 5.2Zákony ideálního plynu 5.1.1 Ideální plyn 5.1.2 Avogadrův zákon 5.1.3 Normální podmínky 5.1.4 Boyleův-Mariottův zákon Izoterma 5.1.5 Gay-Lussacův zákon 5.1.6 Charlesův zákon 5.1.7 Poissonův zákon 5.1.8
5.2Zákony ideálního plynu 5.1.1 Ideální plyn 5.1.2 Avogadrův zákon 5.1.3 Normální podmínky 5.1.4 Boyleův-Mariottův zákon Izoterma 5.1.5 Gay-Lussacův zákon 5.1.6 Charlesův zákon 5.1.7 Poissonův zákon 5.1.8
Šroubová válcová pružina. Tato pružina se používá nejčastěji, může být tažná (má oka) a tlačná (rovné zakončení závitů). Je.
 roucené ružiny Torzní tyč: Je to ružina ve tvaru římé tyče, oužívá se u automobiů (odružení). Torzní ružina má mnoem eší využití materiáu, než ružina oybaná. Využívají se tedy avně tam, kde záeží na ekosti
roucené ružiny Torzní tyč: Je to ružina ve tvaru římé tyče, oužívá se u automobiů (odružení). Torzní ružina má mnoem eší využití materiáu, než ružina oybaná. Využívají se tedy avně tam, kde záeží na ekosti
Základy elektrických pohonů, oteplování,ochlazování motorů
 Základy elektrických ohonů, otelování,ochlazování motorů Určeno ro studenty kombinované formy FS, ředmětu Elektrotechnika II an Dudek únor 2007 Elektrický ohon Definice (dle ČSN 34 5170): Elektrický ohon
Základy elektrických ohonů, otelování,ochlazování motorů Určeno ro studenty kombinované formy FS, ředmětu Elektrotechnika II an Dudek únor 2007 Elektrický ohon Definice (dle ČSN 34 5170): Elektrický ohon
zadání: Je dán stejnosměrný motor s konstantním magnetickým tokem, napájen do kotvy, indukčnost zanedbáme.
 Teorie řízení 004 str. / 30 PŘÍKLAD zadání: Je dán stejnosměrný motor s konstantním magnetickým tokem, naájen do kotvy, indukčnost zanedbáme. E ce ω a) Odvoďte řenosovou funkci F(): F( ) ω( )/ u( ) b)
Teorie řízení 004 str. / 30 PŘÍKLAD zadání: Je dán stejnosměrný motor s konstantním magnetickým tokem, naájen do kotvy, indukčnost zanedbáme. E ce ω a) Odvoďte řenosovou funkci F(): F( ) ω( )/ u( ) b)
Příloha-výpočet motoru
 Příloha-výpočet motoru 1.Zadané parametry motoru: vrtání d : 77mm zdvih z: 87mm kompresní poměr ε : 10.6 atmosférický tlak p 1 : 98000Pa teplota nasávaného vzduchu T 1 : 353.15K adiabatický exponent κ
Příloha-výpočet motoru 1.Zadané parametry motoru: vrtání d : 77mm zdvih z: 87mm kompresní poměr ε : 10.6 atmosférický tlak p 1 : 98000Pa teplota nasávaného vzduchu T 1 : 353.15K adiabatický exponent κ
Řešení úloh 1. kola 54. ročníku fyzikální olympiády. Kategorie C. s=v 0 t 1 2 at2. (1)
 Řešení úoh 1. koa 54. ročníku fyzikání oympiády. Kategorie C Autořiúoh:J.Jírů(1),J.Thomas(,3,5),M.Jarešová(4,7),P.Šedivý(6). 1.a) Během brzdění roste dráha s časem pode vzorce s=v 0 t 1 at. (1) Zevzorcepyne
Řešení úoh 1. koa 54. ročníku fyzikání oympiády. Kategorie C Autořiúoh:J.Jírů(1),J.Thomas(,3,5),M.Jarešová(4,7),P.Šedivý(6). 1.a) Během brzdění roste dráha s časem pode vzorce s=v 0 t 1 at. (1) Zevzorcepyne
Výsledky úloh. Obsah KRUHOVÝ DĚJ S IDEÁLNÍM PLYNEM. Studijní text pro řešitele FO a ostatní zájemce o fyziku
 ýsledky úloh C R, C R, κ 0, 0,088 0, 0,8 KRUHOÝ DĚJ S IDEÁLNÍM PLYNEM Studijní text ro řešitele FO a ostatní zájemce o fyziku 6 η 0,8 ( ){ { Obsah Přemysl Šedivý Základní ojmy ztahy užívané ři oisu kruhových
ýsledky úloh C R, C R, κ 0, 0,088 0, 0,8 KRUHOÝ DĚJ S IDEÁLNÍM PLYNEM Studijní text ro řešitele FO a ostatní zájemce o fyziku 6 η 0,8 ( ){ { Obsah Přemysl Šedivý Základní ojmy ztahy užívané ři oisu kruhových
Tepelná vodivost. střední rychlost. T 1 > T 2 z. teplo přenesené za čas dt: T 1 T 2. tepelný tok střední volná dráha. součinitel tepelné vodivosti
 Tepelná vodivost teplo přenesené za čas dt: T 1 > T z T 1 S tepelný tok střední volná dráha T součinitel tepelné vodivosti střední rychlost Tepelná vodivost součinitel tepelné vodivosti při T = 300 K součinitel
Tepelná vodivost teplo přenesené za čas dt: T 1 > T z T 1 S tepelný tok střední volná dráha T součinitel tepelné vodivosti střední rychlost Tepelná vodivost součinitel tepelné vodivosti při T = 300 K součinitel
Směrová kalibrace pětiotvorové kuželové sondy
 Směrová kalibrace ětiotvorové kuželové sondy Matějka Milan Ing., Ústav mechaniky tekutin a energetiky, Fakulta strojní, ČVUT v Praze, Technická 4, 166 07 Praha 6, milan.matejka@fs.cvut.cz Abstrakt: The
Směrová kalibrace ětiotvorové kuželové sondy Matějka Milan Ing., Ústav mechaniky tekutin a energetiky, Fakulta strojní, ČVUT v Praze, Technická 4, 166 07 Praha 6, milan.matejka@fs.cvut.cz Abstrakt: The
Elektroenergetika 1. Termodynamika a termodynamické oběhy
 Termodynamika a termodynamické oběhy Termodynamika Popisuje procesy, které zahrnují změny teploty, přeměny energie a vzájemný vztah mezi tepelnou energií a mechanickou prací Opakování fyziky Termodynamický
Termodynamika a termodynamické oběhy Termodynamika Popisuje procesy, které zahrnují změny teploty, přeměny energie a vzájemný vztah mezi tepelnou energií a mechanickou prací Opakování fyziky Termodynamický
Úloha č.1: Stanovení Jouleova-Thomsonova koeficientu reálného plynu - statistické zpracování dat
 Úloha č.1: Stanovení Jouleova-Thomsonova koeficientu reálného lynu - statistické zracování dat Teorie Tam, kde se racuje se stlačenými lyny, je možné ozorovat zajímavý jev. Jestliže se do nádoby, kde je
Úloha č.1: Stanovení Jouleova-Thomsonova koeficientu reálného lynu - statistické zracování dat Teorie Tam, kde se racuje se stlačenými lyny, je možné ozorovat zajímavý jev. Jestliže se do nádoby, kde je
11. Tepelné děje v plynech
 11. eelné děje v lynech 11.1 elotní roztažnost a rozínavost lynů elotní roztažnost obje lynů závisí na telotě ři stálé tlaku. S rostoucí telotou se roztažnost lynů ři stálé tlaku zvětšuje. Součinitel objeové
11. eelné děje v lynech 11.1 elotní roztažnost a rozínavost lynů elotní roztažnost obje lynů závisí na telotě ři stálé tlaku. S rostoucí telotou se roztažnost lynů ři stálé tlaku zvětšuje. Součinitel objeové
Elektroenergetika 1. Termodynamika
 Elektroenergetika 1 Termodynamika Termodynamika Popisuje procesy, které zahrnují změny teploty, přeměny energie a vzájemný vztah mezi tepelnou energií a mechanickou prací Opakování fyziky Termodynamický
Elektroenergetika 1 Termodynamika Termodynamika Popisuje procesy, které zahrnují změny teploty, přeměny energie a vzájemný vztah mezi tepelnou energií a mechanickou prací Opakování fyziky Termodynamický
DOPLŇKOVÉ TEXTY BB01 PAVEL SCHAUER INTERNÍ MATERIÁL FAST VUT V BRNĚ ENERGIE
 DOPLŇKOVÉ TEXTY BB1 PAVEL SCHAUER INTERNÍ MATERIÁL FAST VUT V BRNĚ ENERGIE Obsa Energie... 1 Kinetická energie... 1 Potenciální energie... Konzervativní síla... Konzervativníu silovéu oli odovídá dru otenciální
DOPLŇKOVÉ TEXTY BB1 PAVEL SCHAUER INTERNÍ MATERIÁL FAST VUT V BRNĚ ENERGIE Obsa Energie... 1 Kinetická energie... 1 Potenciální energie... Konzervativní síla... Konzervativníu silovéu oli odovídá dru otenciální
FYZIKA I. Kyvadlový pohyb. Prof. RNDr. Vilém Mádr, CSc. Prof. Ing. Libor Hlaváč, Ph.D. Doc. Ing. Irena Hlaváčová, Ph.D. Mgr. Art.
 VYSOKÁ ŠKOLA BÁŇSKÁ TECHNICKÁ UNIVERZITA OSTRAVA FAKULTA STRONÍ FYZIKA I Kyvadový pohyb Prof. RNDr. Viém Mádr, CSc. Prof. Ing. Libor Haváč, Ph.D. Doc. Ing. Irena Haváčová, Ph.D. Mgr. Art. Dagmar Mádrová
VYSOKÁ ŠKOLA BÁŇSKÁ TECHNICKÁ UNIVERZITA OSTRAVA FAKULTA STRONÍ FYZIKA I Kyvadový pohyb Prof. RNDr. Viém Mádr, CSc. Prof. Ing. Libor Haváč, Ph.D. Doc. Ing. Irena Haváčová, Ph.D. Mgr. Art. Dagmar Mádrová
Termodynamika 2. UJOP Hostivař 2014
 Termodynamika 2 UJOP Hostivař 2014 Skupenské teplo tání/tuhnutí je (celkové) teplo, které přijme pevná látka při přechodu na kapalinu během tání nebo naopak Značka Veličina Lt J Nedochází při něm ke změně
Termodynamika 2 UJOP Hostivař 2014 Skupenské teplo tání/tuhnutí je (celkové) teplo, které přijme pevná látka při přechodu na kapalinu během tání nebo naopak Značka Veličina Lt J Nedochází při něm ke změně
Model tenisového utkání
 Model tenisového utkání Jan Šustek Semestrální rojekt do ředmětu Náhodné rocesy 2005 V této ráci se budu zabývat modelem tenisového utkání. Vstuními hodnotami budou úsěšnosti odání jednotlivých hráčů,
Model tenisového utkání Jan Šustek Semestrální rojekt do ředmětu Náhodné rocesy 2005 V této ráci se budu zabývat modelem tenisového utkání. Vstuními hodnotami budou úsěšnosti odání jednotlivých hráčů,
Základy teorie vozidel a vozidlových motorů
 Základy teorie vozidel a vozidlových motorů Předmět Základy teorie vozidel a vozidlových motorů (ZM) obsahuje dvě hlavní kaitoly: vozidlové motory a vozidla. Kaitoly o vozidlových motorech ukazují ředevším
Základy teorie vozidel a vozidlových motorů Předmět Základy teorie vozidel a vozidlových motorů (ZM) obsahuje dvě hlavní kaitoly: vozidlové motory a vozidla. Kaitoly o vozidlových motorech ukazují ředevším
Jednotlivým bodům (n,2,a,e,k) z blokového schématu odpovídají body na T-s a h-s diagramu:
 Elektroenergetika 1 (A1B15EN1) 3. cvičení Příklad 1: Rankin-Clausiův cyklus Vypočtěte tepelnou účinnost teoretického Clausius-Rankinova parního oběhu, jsou-li admisní parametry páry tlak p a = 80.10 5
Elektroenergetika 1 (A1B15EN1) 3. cvičení Příklad 1: Rankin-Clausiův cyklus Vypočtěte tepelnou účinnost teoretického Clausius-Rankinova parního oběhu, jsou-li admisní parametry páry tlak p a = 80.10 5
TERMIKA VIII. Joule uv a Thompson uv pokus pro reálné plyny
 TERMIKA VIII Maxwellova rovnovážná rozdělovací funkce rychlostí Joule uv a Thomson uv okus ro reálné lyny 1 Maxwellova rovnovážná rozdělovací funkce rychlostí Maxwellova rychlostní rozdělovací funkce se
TERMIKA VIII Maxwellova rovnovážná rozdělovací funkce rychlostí Joule uv a Thomson uv okus ro reálné lyny 1 Maxwellova rovnovážná rozdělovací funkce rychlostí Maxwellova rychlostní rozdělovací funkce se
Plynové turbíny. Nevýhody plynových turbín: - menší mezní výkony ve srovnání s parní turbínou - vyšší nároky na palivo - kvalitnější materiály
 Plynoé turbíny Plynoá turbína je teeý stroj řeměňujíí teeou energie obsaženou raoní láte q roházejíí motorem na energii mehanikou a t (obr.). Praoní látkou je zduh, resektie saliny, které se ytářejí teeém
Plynoé turbíny Plynoá turbína je teeý stroj řeměňujíí teeou energie obsaženou raoní láte q roházejíí motorem na energii mehanikou a t (obr.). Praoní látkou je zduh, resektie saliny, které se ytářejí teeém
LOGO. Struktura a vlastnosti plynů Ideální plyn
 Struktura a vlastnosti plynů Ideální plyn Ideální plyn Protože popsat chování plynů je nad naše možnosti, zavádíme zjednodušený model tzv. ideálního plynu, který má tyto vlastnosti: Částice ideálního plynu
Struktura a vlastnosti plynů Ideální plyn Ideální plyn Protože popsat chování plynů je nad naše možnosti, zavádíme zjednodušený model tzv. ideálního plynu, který má tyto vlastnosti: Částice ideálního plynu
MAGNETICKÉ POLE. 1. Stacionární magnetické pole I I I I I N S N N
 MAGETCKÉ POLE 1. Stacionární magnetické poe V E S T C E D O R O Z V O J E V Z D Ě L Á V Á Í je část prostoru, kde se veičiny popisující magnetické poe nemění s časem. Vzniká v bízkosti stacionárních vodičů
MAGETCKÉ POLE 1. Stacionární magnetické poe V E S T C E D O R O Z V O J E V Z D Ě L Á V Á Í je část prostoru, kde se veičiny popisující magnetické poe nemění s časem. Vzniká v bízkosti stacionárních vodičů
5.4 Adiabatický děj Polytropický děj Porovnání dějů Základy tepelných cyklů První zákon termodynamiky pro cykly 42 6.
 OBSAH Předmluva 9 I. ZÁKLADY TERMODYNAMIKY 10 1. Základní pojmy 10 1.1 Termodynamická soustava 10 1.2 Energie, teplo, práce 10 1.3 Stavy látek 11 1.4 Veličiny popisující stavy látek 12 1.5 Úlohy technické
OBSAH Předmluva 9 I. ZÁKLADY TERMODYNAMIKY 10 1. Základní pojmy 10 1.1 Termodynamická soustava 10 1.2 Energie, teplo, práce 10 1.3 Stavy látek 11 1.4 Veličiny popisující stavy látek 12 1.5 Úlohy technické
ných ehřátých kapalin zásobníky zkapalněných plynů havarijní scénáře a jejich rozbor
 Procesy s účastí stlačených a zkaalněných ných lynů a řeh ehřátých kaalin zásobníky zkaalněných lynů havarijní scénáře a jejich rozbor Havarijní scénář Nebezečný otenciál zádrž nebezečných látek uvolnitelná
Procesy s účastí stlačených a zkaalněných ných lynů a řeh ehřátých kaalin zásobníky zkaalněných lynů havarijní scénáře a jejich rozbor Havarijní scénář Nebezečný otenciál zádrž nebezečných látek uvolnitelná
Univerzita Pardubice FAKULTA CHEMICKO TECHNOLOGICKÁ
 Univerzita Pardubice FAKULA CHEMICKO ECHNOLOGICKÁ MEODY S LAENNÍMI PROMĚNNÝMI A KLASIFIKAČNÍ MEODY SEMINÁRNÍ PRÁCE LICENČNÍHO SUDIA Statistické zracování dat ři kontrole jakosti Ing. Karel Dráela, CSc.
Univerzita Pardubice FAKULA CHEMICKO ECHNOLOGICKÁ MEODY S LAENNÍMI PROMĚNNÝMI A KLASIFIKAČNÍ MEODY SEMINÁRNÍ PRÁCE LICENČNÍHO SUDIA Statistické zracování dat ři kontrole jakosti Ing. Karel Dráela, CSc.
STRUKTURA A VLASTNOSTI PLYNŮ POJMY K ZOPAKOVÁNÍ. Testové úlohy varianta A
 Škola: Autor: DUM: Vzdělávací obor: Tematický okruh: Téma: Masarykovo gymnázium Vsetín Mgr. Jitka Novosadová MGV_F_SS_3S3_D09_Z_OPAK_T_Plyny_T Člověk a příroda Fyzika Struktura a vlastnosti plynů Opakování
Škola: Autor: DUM: Vzdělávací obor: Tematický okruh: Téma: Masarykovo gymnázium Vsetín Mgr. Jitka Novosadová MGV_F_SS_3S3_D09_Z_OPAK_T_Plyny_T Člověk a příroda Fyzika Struktura a vlastnosti plynů Opakování
VÝHODY A NEVÝHODY PNEUMATICKÝCH MECHANISMŮ
 VÝHODY A NEVÝHODY PNEUMATICKÝCH MECHANISMŮ Výhody: medium (vzduch) se nachází všude kolem nás možnost využití centrální výroby stlačeného vzduchu v závodě kompresor nemusí pracovat nepřetržitě (stlačený
VÝHODY A NEVÝHODY PNEUMATICKÝCH MECHANISMŮ Výhody: medium (vzduch) se nachází všude kolem nás možnost využití centrální výroby stlačeného vzduchu v závodě kompresor nemusí pracovat nepřetržitě (stlačený
3.9. Energie magnetického pole
 3.9. nergie agnetického poe 1. Uět odvodit energii agnetického poe cívky tak, aby bya vyjádřena poocí paraetrů obvodu (I a L).. Znát vztah pro energii agnetického poe cívky jako funkci veičin charakterizujících
3.9. nergie agnetického poe 1. Uět odvodit energii agnetického poe cívky tak, aby bya vyjádřena poocí paraetrů obvodu (I a L).. Znát vztah pro energii agnetického poe cívky jako funkci veičin charakterizujících
1.5.5 Potenciální energie
 .5.5 Potenciální energie Předoklady: 504 Pedagogická oznámka: Na dosazování do vzorce E = mg není nic obtížnéo. Problém nastává v situacíc, kdy není zcela jasné, jakou odnotu dosadit za. Hlavním smyslem
.5.5 Potenciální energie Předoklady: 504 Pedagogická oznámka: Na dosazování do vzorce E = mg není nic obtížnéo. Problém nastává v situacíc, kdy není zcela jasné, jakou odnotu dosadit za. Hlavním smyslem
VYBRANÉ STATĚ Z PROCESNÍHO INŽENÝRSTVÍ cvičení 11
 UNIVERZITA TOMÁŠE BATI VE ZLÍNĚ FAKULTA APLIKOVANÉ INFORMATIKY VYBRANÉ STATĚ Z PROCESNÍHO INŽENÝRSTVÍ cvičení 11 Termodynamika reálných plynů část 1 Hana Charvátová, Dagmar Janáčová Zlín 2013 Tento studijní
UNIVERZITA TOMÁŠE BATI VE ZLÍNĚ FAKULTA APLIKOVANÉ INFORMATIKY VYBRANÉ STATĚ Z PROCESNÍHO INŽENÝRSTVÍ cvičení 11 Termodynamika reálných plynů část 1 Hana Charvátová, Dagmar Janáčová Zlín 2013 Tento studijní
