Definice termodynamiky
|
|
|
- Dagmar Pokorná
- před 6 lety
- Počet zobrazení:
Transkript
1 erodynaika
2 Definice terodynaiky erodynaika (θερμη telo, δυναμις síla) je obor fyziky zabývající se vzájenýi řeěnai různých fore energie, zejéna ráce a tela, a s nii související robleatikou sontánnosti dějů robíhajících v řírodě. Sontánní (nevratné) děje sěřují k rovnovážnéu stavu. Příklady terodynaických dějů: exanze lynu ve válci s íste: robíhá dokud se tlaky uvnitř a vně válce nevyrovnají ohřívání chladnějšího tělesa od okolí: robíhá, dokud se telota tělesa nevyrovná s telotou okolí vyařování kaaliny: robíhá, dokud tlak ar nad kaalinou nedosáhne tlaku nasycených ar rozouštění evné látky v kaalině: robíhá, dokud nevznikne nasycený roztok cheická reakce: robíhá, dokud se nevyrovná rychlost říé a zětné reakce Probleatikou energetické bilance cheických reakcí a cheických rovnováh se zabývá cheická terodynaika.
3 Rozdělení terodynaiky Rovnovážná terodynaika se zabývá studie odínek rovnováhy v terodynaických soustavách, nerovnovážná oisuje látkové a energetické toky rovázející nevratné terodynaické děje e vztazích rovnovážné terodynaiky nevystuuje čas: Poisuje odínky rovnováhy, ale nezabývá se otázkou, za jak dlouho (a zda vůbec) se rovnováha ustaví. Klasická terodynaika: vrzení o chování terodynaických soustav odvozuje z terodynaických rinciů (ostulátů). Statistická terodynaika (statistická echanika): hování terodynaických soustav studuje na základě oisu ohybu částic tvořících soustavu. Protože nelze stanovit trajektorii (říadně vlnovou funkci) každé jednotlivé částice v soustavě, oisuje se jejich ohybový stav statistickýi etodai: Střední hodnota veličiny F závislé na olohách a hybnostech N částic tvořících soustavu, FF(r 1, r,..., r N, 1,,... N ): F... F( r ρ , r,..., rn, 1,,..., N ) ( r1, r,..., rn, 1,,..., N )d r1d r...d rnd 1d... d ρ(r 1, r,..., r N, 1,,... N ): rozdělovací funkce, oisující ravděodobnost, že částice soustavy ají olohy a hybnosti r 1, r,..., r N, 1,,... N. N
4 erodynaická soustava erodynaická soustava (systé): Část světa oddělená od jeho zbytku (okolí) stěnai (skutečnýi nebo yšlenýi) látkový tok okolí soustava tok energie Látkové a energetické bilance vždy oisujee z hlediska soustavy, tok z okolí do soustavy á kladné znaénko, tok ze soustavy do okolí záorné
5 Rozdělení terodynaických soustav Podle roustnosti stěn dělíe soustavy na otevřené: dovolují výěnu látek i energie s okolí uzavřené: uožňují ouze výěnu energie izolované: neuožňují výěnu ani látek, ani energie Podle struktury a složení dělíe soustavy na hoogenní: ají ve všech ístech stejné složení i vlastnosti heterogenní: jsou složeny ze dvou či více hoogenních oblastí, které se nazývají fáze jednosložkové: jsou tvořené čistou látkou vícesložkové: jsou tvořené sěsí látek Fáze jsou od sebe odděleny fázový rozhraní (ezifází), které á jiné vlastnosti než vnitřní části stýkajících se fází (nař. ovrchové naětí) Příklady hoogenních/heterogenních a jednosložkových/vícesložkových soustav: hoogenní heterogenní jednosložková voda, krystal Nal voda s lede vícesložková vodný roztok Nal nasycený roztok Nal s evný Nal
6 Stavové veličiny a terodynaické děje Stavové veličiny (stavové araetry): Poisují rovnovážný stav soustavy, jejich zěna ři terodynaické ději je dána rozdíle hodnot očátečního a koncového stavu, a nezávisí tedy na růběhu děje. Při cyklické ději je zěna každé stavové veličiny nulová. Stavové veličiny jsou nař. telota, tlak, obje a látková nožství (říadně hotnosti) složek soustavy. Dělí se na extenzivní, jejichž hodnota závisí na velikosti soustavy (obje, hotnost, látkové nožství) a intenzivní, jejichž hodnota je na velikosti soustavy nezávislá (telota, tlak). Podíle dvou extenzivních veličin získáe intenzivní veličinu, nař. olární obje, hustota, aod. ratný (reverzibilní) terodynaický děj: Stavové araetry se ři jeho růběhu ění nekonečně oalu, takže se neustále ustavuje rovnovážný stav: Při vratné ději je systé neustále v rovnováze, takže libovolně alé vychýlení ěnících se araetrů oačný sěre zůsobí obrácení děje (odtud oje vratný děj). Pois stavu soustavy io rovnováhu je nohe složitější. Zatíco za rovnováhy jsou tlak a telota stejné v celé soustavě a složení je stejné v každé fázi, v nerovnovážné stavu se všechny tyto veličiny ohou libovolně ěnit s olohou, t.j. k oisu je třeba nohe víc araetrů.
7 erodynaické děje Příklady vratných dějů Exanze lynu: tlak uvnitř a vně nádoby je stejný, tlak vně je oalu snižován. I ři jeho alé zvýšení by se děj obrátil a došlo ke koresi. Ohřev tělesa od okolí. elota tělesa je stejná jako telota okolí, telota okolí je oalu zvyšována. I ři její alé snížení by se děj obrátil a těleso by se ochlazovalo. heická reakce. Za rovnováhy řidáe do reakční sěsi reaktant, takže reakce začne robíhat sěre k roduktů, aby se znovu ustavila rovnováha. Kdybycho řidali rodukt, reakce by k ustavení rovnováhy robíhala oačný sěre. zlede k tou, že zěny stavových veličin nezávisí na růběhu děje, lze vždy uvažovat, že roběhl jako vratný a k oisu užít rovnovážnou terodynaiku. Rozdělení terodynaických dějů odle veličiny, která běhe děje zůstává konstantní: d 0 d 0 d 0 dq 0 izobarický izochorický izoterický adiabatický
8 elota Nultý rinci terodynaiky. Existuje stavová funkce zvaná telota, která ve všech soustavách, které jsou navzáje v teelné rovnováze, nabývá stejné hodnoty. eloěr: Zařízení, jehož telotu lze určit oocí ěření jiné, telotně závislé veličiny (objeu, elektrického odoru aod.). Znáe-li ak telotu teloěru, znáe také telotu tělesa, které je s teloěre v teelné rovnováze. elotní stunice elsiova: Fahrenheitova: 0 : bod tání vody za norálního tlaku 100 : bod varu vody za norálního tlaku 0 : eutektická telota sěsi chlorid aonný voda (ca. 18 ) 100 : ův. norální telota lidského těla (ca. 37 ), dnes osunuto na 38 [ F] [ ] Absolutní: 1 kelvin je 73,16-tá část trojného bodu vody (0,01 ) 0 K odovídá nejnižší ožné telotě [K] [ ] + 73,15
9 Práce a telo Práce a telo ředstavují různé fory výěny energie ezi soustavou a okolí. Práci (W) soustava řijíá res. odevzdává ůsobení akroskoických sil z okolí na soustavu res. ze soustavy na okolí, jde o zobecnění oju ráce zavedeného v echanice: dw Fds, F ůsobící síla, ds dráha, odél níž síla ůsobí. Na ikroskoické úrovni síla souvisí s usořádaný ohybe částic. elo (Q) se vyěňuje řenose energie ikroskoického, chaotického ohybu částic, souvisí tedy se neusořádaný ohybe částic. ráce Při exanzi ístu o loše A roti dx telo vnějšíu tlaku na vzdálenost dx A vykoná soustava ráci Adx; obje soustavy se ři osunutí zvětší o d Adx Příklady ráce v terodynaických soustavách: objeová exanze: d vnější tlak, d zěna objeu soustavy ovrchové interakce: γda γ ovrchové naětí, da zěna ovrchu soustavy řenos náboje ϕdq ϕ elektrický otenciál, dq zěna elektrického náboje elektrická olarizace Ed Eintenzita elektrického ole, d zěna el. diól. oentu agnetizace Bd B agnetická indukce, d zěna ag. diól. oentu
10 První rinci terodynaiky: vnitřní energie a enthalie Existuje terodynaická stavová funkce vnitřní energie, jejíž zěna ři každé ději je dána součte ráce a tela vyěněného soustavou s okolí v růběhu děje : Δ W + Q d dw + dq; koná-li se jen objeová ráce: d d + dq První rinci terodynaiky ředstavuje zobecněný zákon zachování energie. Její význa sočívá v to, že ačkoli ani ráce, ani telo nejsou stavové veličiny (kolik ráce a tela se vyění ezi soustavou a okolí, závisí na růběhu děje), jejich součet stavovou veličinou je. Molární vnitřní energie n Nekoná-li se neobjeová ráce, je zěna vnitřní energie soustavy ři izochorické ději rovna telu vyěněnéu soustavou s okolí: d 0 d d + dq dq Enthalie: + Nekoná-li se neobjeová ráce, je zěna enthalie soustavy ři izobarické ději rovna telu vyěněnéu soustavou s okolí: d 0 d d + d( ) d + dq + d + d dq
11 Molární teelné kaacity, Molární teelná kaacita látky je veličina udávající, kolik tela usí řijout 1 ol látky za konstantního objeu (izochorická t.k.) nebo za konstantního tlaku (izobarická t.k.), aby se její telota zvýšila z dané teloty o 1 K. Jednotkou olární t.k. je J K -1 ol -1. izobarická olární t.k., izochorická olární t.k. Molární teelné kaacity jsou telotně závislé (t. j., k ohřevu 1 olu látky z 0 na 1 je otřeba jiné nožství tela než z 0 na 1 ), ro výočty v alých telotních intervalech lze telotní závislost zanedbat a ředokládat, že t.k. je konstantní. ) ( d ), ( d 1,, 1,, 1 1 n n n n Δ Δ ztah ezi, a, : ,, ro s, l:,, 0 ro ideální g: R R,, 0 Mayerův vztah
12 ztah ezi teelnou kaacitou a strukturou látek Energie olekul (zředěného) lynu a atoů v krystalové řížce: jednoatoová olekula E Etr ( ux + u y + uz ) I dvouatoová olekula E Etr + Erot + Evib + vib x y z x ω 0 E vib uv, x + uv, y + uv, z + rv, x + rv, y + r ( u + u + u ) + ( ω + ω ) + u + 0 x ato v krystalové řížce ( ) ( ) Ekviartiční rinci (ekviartiční teoré) vztah ezi telotou a střední hodnotou energie lynu: rovnovážné stavu ři telotě řiadá na každý kvadratický člen ve výrazu ro celkovou energii olekuly (atou) střední hodnota k/, jíž odovídá řísěvek R/ k olární vnitřní energie lynu (krystalu) a R/ k izochorické olární teelné kaacitě. lyn, jednoatoová olekula: , R 1,5 J ol K lyn, dvouatoová olekula: , R 9,1 J ol K atoární krystal: -1-1, 3 R 4,9 J ol K (Dulongovo-Petitovo ravidlo) 1 at, 98 K: e: 1,5 J ol -1 K -1 Ar: 1,5 J ol -1 K -1 l : 4,1 J ol -1 K -1 O: 0, J ol -1 K -1 u: 4,5 J ol -1 K -1 Ag: 4,9 J ol -1 K -1 Pb: 6,4 J ol -1 K -1 v, z y v ω Odchylky jsou zůsobené kvantování rotační a vibrační energie v
13 erocheie erocheie: Zabývá se uvolňování/ohlcování tela ři cheických reakcích aa +bb c + dd rozsah reakce (reakční obrat): ξ reakční enthalie: d Δr dξ Δn a Δn b Δn c Δn d A B D Δn i ν Δ r < 0, ři reakci se telo uvolňuje (exoterická reakce) Δ r > 0 ři reakci se telo sotřebovává (endoterická reakce) i stechioetrické koeficienty u reaktantů záorné, u roduktů kladné Slučovací enthalie (f foring): Zěna enthalie odovídající vzniku 1 olu dané látky z rvků Salná enthalie (c cobustion): Zěna enthalie odovídající sloučení jednoho olu dané látky na oxidy s nejvyšší oxidační čísle Δ f 98K, kj ol -1 Nal(s) 407 NO (g) +33 SO 4 (l) 814 O(l) 85.8 O(g) 41.8 Δ c 98K, kj ol
14 ýočty reakčních enthalií erocheické zákony: Jsou říý důsledke skutečnosti, že enthalie je stavová veličina Δ Δ r r A B A B Δ Δ r r B A A + Δ n Δr A B ν iδf i i 1 r B (1) Lalaceův Lavoisierův zákon: Enthalie říé a zětné reakce jsou až na znaénko stejné () essův zákon: elková reakční enthalie je součte enthalií dílčích kroků reakce. o latí i tehdy, jde-li o kroky ouze hyotetické a reakce ve skutečnosti robíhá jiný echanise ýočet reakční enthalie ze standardních slučovacích enthalií: Příklad: Jsou dána následující slučovací tela: Úkol: yočítat salné telo. Reakce: + 5/ O O + O Δ f 98 /kjol -1 (g) 6,73 Δ r 6,73 + ( 393,5) + ( 85,83) O(l) 85,83 199,6 kj ol -1 O (g) 393,5 ýočet reakční enthalie ze standardních salných enthalií: Δr ν iδci A B n i 1
15 Závislost reakční enthalie na telotě Je-li třeba sočítat reakční enthalii ři jiné telotě než standardní: (1) Sočítá se telo uvolněné (ohlcené) ři ochlazení (zahřátí) reaktantů z ožadované teloty na telotu standardní () Sočítá se reakční enthalie ři standardní telotě (3) Sočítá se telo ohlcené (uvolněné) ři zahřátí (ochlazení) roduktů ze standardní teloty na ožadovanou telotu (4) ýsledná reakční enthalie je součte těchto tří řísěvků Kirchhoffova rovnice: ν i (, ) d Δ + i ( ) i r ( 1 1, i Δr Δr + ) 1 1 i ν i
Fyzikální chemie. 1.2 Termodynamika
 Fyzikální chemie. ermodynamika Mgr. Sylvie Pavloková Letní semestr 07/08 děj izotermický izobarický izochorický konstantní V ermodynamika rvní termodynamický zákon (zákon zachování energie): U Q + W izotermický
Fyzikální chemie. ermodynamika Mgr. Sylvie Pavloková Letní semestr 07/08 děj izotermický izobarický izochorický konstantní V ermodynamika rvní termodynamický zákon (zákon zachování energie): U Q + W izotermický
11. Tepelné děje v plynech
 11. eelné děje v lynech 11.1 elotní roztažnost a rozínavost lynů elotní roztažnost obje lynů závisí na telotě ři stálé tlaku. S rostoucí telotou se roztažnost lynů ři stálé tlaku zvětšuje. Součinitel objeové
11. eelné děje v lynech 11.1 elotní roztažnost a rozínavost lynů elotní roztažnost obje lynů závisí na telotě ři stálé tlaku. S rostoucí telotou se roztažnost lynů ři stálé tlaku zvětšuje. Součinitel objeové
FYZIKA 2. ROČNÍK. Změny skupenství látek. Tání a tuhnutí. Pevná látka. soustava velkého počtu částic. Plyn
 Zěny skuenství látek Pevná látka Kaalina Plyn soustava velkého očtu částic Má-li soustava v rovnovážné stavu ve všech částech stejné fyzikální a cheické vlastnosti (stejnou hustotu, stejnou strukturu a
Zěny skuenství látek Pevná látka Kaalina Plyn soustava velkého očtu částic Má-li soustava v rovnovážné stavu ve všech částech stejné fyzikální a cheické vlastnosti (stejnou hustotu, stejnou strukturu a
Výpočty za použití zákonů pro ideální plyn
 ýočty za oužití zákonů ro ideální lyn Látka v lynné stavu je tvořena volnýi atoy(onoatoickýi olekulai), ionty nebo olekulai. Ideální lyn- olekuly na sebe neůsobí žádnýi silai, jejich obje je ve srovnání
ýočty za oužití zákonů ro ideální lyn Látka v lynné stavu je tvořena volnýi atoy(onoatoickýi olekulai), ionty nebo olekulai. Ideální lyn- olekuly na sebe neůsobí žádnýi silai, jejich obje je ve srovnání
Popis fyzikálního chování látek
 Popis fyzikálního chování látek pro vysvětlení noha fyzikálních jevů již nevystačíe s pouhý echanický popise Terodynaika oblast fyziky, která kroě echaniky zkouá vlastnosti akroskopických systéů, zejéna
Popis fyzikálního chování látek pro vysvětlení noha fyzikálních jevů již nevystačíe s pouhý echanický popise Terodynaika oblast fyziky, která kroě echaniky zkouá vlastnosti akroskopických systéů, zejéna
Termodynamické základy ocelářských pochodů
 29 3. Termodynamické základy ocelářských ochodů Termodynamika ůvodně vznikla jako vědní discilína zabývající se účinností teelných (arních) strojů. Později byly termodynamické zákony oužity ři studiu chemických
29 3. Termodynamické základy ocelářských ochodů Termodynamika ůvodně vznikla jako vědní discilína zabývající se účinností teelných (arních) strojů. Později byly termodynamické zákony oužity ři studiu chemických
V p-v diagramu je tento proces znázorněn hyperbolou spojující body obou stavů plynu, je to tzv. izoterma :
 Jednoduché vratné děje ideálního lynu ) Děj izoter mický ( = ) Za ředokladu konstantní teloty se stavová rovnice ro zadané množství lynu změní na známý zákon Boylův-Mariottův, která říká, že součin tlaku
Jednoduché vratné děje ideálního lynu ) Děj izoter mický ( = ) Za ředokladu konstantní teloty se stavová rovnice ro zadané množství lynu změní na známý zákon Boylův-Mariottův, která říká, že součin tlaku
1 Poznámka k termodynamice: Jednoatomový či dvouatomový plyn?
 Kvantová a statistická fyzika (erodynaika a statistická fyzika) 1 Poznáka k terodynaice: Jednoatoový či dvouatoový plyn? Jeden ol jednoatoového plynu o teplotě zaujíá obje V. Plyn však ůže projít cheickou
Kvantová a statistická fyzika (erodynaika a statistická fyzika) 1 Poznáka k terodynaice: Jednoatoový či dvouatoový plyn? Jeden ol jednoatoového plynu o teplotě zaujíá obje V. Plyn však ůže projít cheickou
2.6.7 Fázový diagram. Předpoklady: Popiš děje zakreslené v diagramu křivky syté páry. Za jakých podmínek mohou proběhnout?
 2.6.7 Fázový diagram Předoklady: 2606 Př. 1: Poiš děje zakreslené v diagramu křivky syté áry. Za jakých odmínek mohou roběhnout? 4 2 1 3 1) Sytá ára je za stálého tlaku zahřívána. Zvětšuje svůj objem a
2.6.7 Fázový diagram Předoklady: 2606 Př. 1: Poiš děje zakreslené v diagramu křivky syté áry. Za jakých odmínek mohou roběhnout? 4 2 1 3 1) Sytá ára je za stálého tlaku zahřívána. Zvětšuje svůj objem a
Výpo ty Výpo et hmotnostní koncentrace zne ující látky ,
 "Zracováno odle Skácel F. - Tekáč.: Podklady ro Ministerstvo životního rostředí k rovádění Protokolu o PRTR - řehled etod ěření a identifikace látek sledovaných odle Protokolu o registrech úniků a řenosů
"Zracováno odle Skácel F. - Tekáč.: Podklady ro Ministerstvo životního rostředí k rovádění Protokolu o PRTR - řehled etod ěření a identifikace látek sledovaných odle Protokolu o registrech úniků a řenosů
TERMODYNAMIKA 1. AXIOMATICKÁ VÝSTAVBA KLASICKÉ TD Základní pojmy
 ERMODYNAMIKA. AXIOMAICKÁ ÝSABA KLASICKÉ D.. Základní ojmy Soustava (systém) je část rostoru od okolí oddělený stěnou uzavřená - stěna brání výměně hmoty mezi soustavou a okolím vers. otevřená (uzavřená
ERMODYNAMIKA. AXIOMAICKÁ ÝSABA KLASICKÉ D.. Základní ojmy Soustava (systém) je část rostoru od okolí oddělený stěnou uzavřená - stěna brání výměně hmoty mezi soustavou a okolím vers. otevřená (uzavřená
TERMODYNAMIKA 1. AXIOMATICKÁ VÝSTAVBA KLASICKÉ TD Základní pojmy
 ERMODYNAMIKA. AXIOMAICKÁ ÝSABA KLASICKÉ D.. Základní ojmy Soustava (systém) je část rostoru od okolí oddělený stěnou uzavřená - stěna brání výměně hmoty mezi soustavou a okolím vers. otevřená (uzavřená
ERMODYNAMIKA. AXIOMAICKÁ ÝSABA KLASICKÉ D.. Základní ojmy Soustava (systém) je část rostoru od okolí oddělený stěnou uzavřená - stěna brání výměně hmoty mezi soustavou a okolím vers. otevřená (uzavřená
7. Fázové přeměny Separace
 7. Fázové řeměny Searace Fáze Fázové rovnováhy Searace látek Evroský sociální fond Praha & EU: Investujeme do vaší budoucnosti 7. Fázové řeměny Searace fáze - odlišitelný stav látky v systému; v určité
7. Fázové řeměny Searace Fáze Fázové rovnováhy Searace látek Evroský sociální fond Praha & EU: Investujeme do vaší budoucnosti 7. Fázové řeměny Searace fáze - odlišitelný stav látky v systému; v určité
Druhá věta termodynamiky
 Druhá věta termoynamiky cience owes more to the steam engine than the steam engine owes to cience. Lawrence J. Henerson (97) Nicolas R. ai arnot 796 83 William homson, lor Kelvin 84 907 Ruolf J.E. lausius
Druhá věta termoynamiky cience owes more to the steam engine than the steam engine owes to cience. Lawrence J. Henerson (97) Nicolas R. ai arnot 796 83 William homson, lor Kelvin 84 907 Ruolf J.E. lausius
DOPLŇKOVÉ TEXTY BB01 PAVEL SCHAUER INTERNÍ MATERIÁL FAST VUT V BRNĚ ENERGIE
 DOPLŇKOVÉ TEXTY BB1 PAVEL SCHAUER INTERNÍ MATERIÁL FAST VUT V BRNĚ ENERGIE Obsa Energie... 1 Kinetická energie... 1 Potenciální energie... Konzervativní síla... Konzervativníu silovéu oli odovídá dru otenciální
DOPLŇKOVÉ TEXTY BB1 PAVEL SCHAUER INTERNÍ MATERIÁL FAST VUT V BRNĚ ENERGIE Obsa Energie... 1 Kinetická energie... 1 Potenciální energie... Konzervativní síla... Konzervativníu silovéu oli odovídá dru otenciální
Hustota plynů - jak ji změřit?
 eletrh náadů učitelů fyziky 9 Hustota lynů - jak ji zěřit? ER SÁDEK, UKÁŠ AWERA edagogická fakulta U, Brno Abstrakt ěření hustoty evných látek a kaalin je běžná laboratorní úloha na řadě škol, nicéně ěření
eletrh náadů učitelů fyziky 9 Hustota lynů - jak ji zěřit? ER SÁDEK, UKÁŠ AWERA edagogická fakulta U, Brno Abstrakt ěření hustoty evných látek a kaalin je běžná laboratorní úloha na řadě škol, nicéně ěření
Úloha č.1: Stanovení Jouleova-Thomsonova koeficientu reálného plynu - statistické zpracování dat
 Úloha č.1: Stanovení Jouleova-Thomsonova koeficientu reálného lynu - statistické zracování dat Teorie Tam, kde se racuje se stlačenými lyny, je možné ozorovat zajímavý jev. Jestliže se do nádoby, kde je
Úloha č.1: Stanovení Jouleova-Thomsonova koeficientu reálného lynu - statistické zracování dat Teorie Tam, kde se racuje se stlačenými lyny, je možné ozorovat zajímavý jev. Jestliže se do nádoby, kde je
KINETICKÁ TEORIE PLYNŮ
 KINEICKÁ EORIE PLYNŮ IDEÁLNÍ PLYN plyn skládající se z velkého počtu veli alých částic stejné hotnosti částice jsou stejně velké a ají tvar koule všechny polohy a všechny sěry pohybu částice jsou stejně
KINEICKÁ EORIE PLYNŮ IDEÁLNÍ PLYN plyn skládající se z velkého počtu veli alých částic stejné hotnosti částice jsou stejně velké a ají tvar koule všechny polohy a všechny sěry pohybu částice jsou stejně
IDEÁLNÍ PLYN II. Prof. RNDr. Emanuel Svoboda, CSc.
 IDEÁLNÍ PLYN II Prof. RNDr. Eanuel Svoboa, Sc. ZÁKLADNÍ RONIE PRO LAK IP F ýchoisko efinice tlaku vztahe S Náoba tvaru krychle, stejná rychlost olekul všei sěry (olekulární chaos, všechny sěry stejně ravěoobné)
IDEÁLNÍ PLYN II Prof. RNDr. Eanuel Svoboa, Sc. ZÁKLADNÍ RONIE PRO LAK IP F ýchoisko efinice tlaku vztahe S Náoba tvaru krychle, stejná rychlost olekul všei sěry (olekulární chaos, všechny sěry stejně ravěoobné)
Termodynamika ideálního plynu
 Přednáška 5 Termodynamika ideálního lynu 5.1 Základní vztahy ro ideální lyn 5.1.1 nitřní energie ideálního lynu Alikujme nyní oznatky získané v ředchozím textu na nejjednodužší termodynamickou soustavu
Přednáška 5 Termodynamika ideálního lynu 5.1 Základní vztahy ro ideální lyn 5.1.1 nitřní energie ideálního lynu Alikujme nyní oznatky získané v ředchozím textu na nejjednodužší termodynamickou soustavu
HYDROPNEUMATICKÝ VAKOVÝ AKUMULÁTOR
 HYDROPNEUMATICKÝ AKOÝ AKUMULÁTOR OSP 050 ŠEOBECNÉ INFORMACE ýočet hydroneumatického akumulátoru ZÁKLADNÍ INFORMACE Při výočtu hydroneumatického akumulátoru se vychází ze stavové změny lynu v akumulátoru.
HYDROPNEUMATICKÝ AKOÝ AKUMULÁTOR OSP 050 ŠEOBECNÉ INFORMACE ýočet hydroneumatického akumulátoru ZÁKLADNÍ INFORMACE Při výočtu hydroneumatického akumulátoru se vychází ze stavové změny lynu v akumulátoru.
III. Základy termodynamiky
 III. Základy termodynamiky 3. ermodynamika FS ČU v Praze 3. Základy termodynamiky 3. Úvod 3. Základní ojmy 3.3 Základní ostuláty 3.4 Další termodynamické funkce volná energie a volná entalie 3.5 Kritérium
III. Základy termodynamiky 3. ermodynamika FS ČU v Praze 3. Základy termodynamiky 3. Úvod 3. Základní ojmy 3.3 Základní ostuláty 3.4 Další termodynamické funkce volná energie a volná entalie 3.5 Kritérium
2.6.6 Sytá pára. Předpoklady: 2604
 .6.6 Sytá ára Předolady: 604 Oaování: aaliny se vyařují za aždé teloty. Nejrychlejší částice uniají z aaliny a stává se z nich ára. Do isy nalijee vodu voda se ostuně vyařuje naonec zůstane isa rázdná,
.6.6 Sytá ára Předolady: 604 Oaování: aaliny se vyařují za aždé teloty. Nejrychlejší částice uniají z aaliny a stává se z nich ára. Do isy nalijee vodu voda se ostuně vyařuje naonec zůstane isa rázdná,
DOPLŇKOVÉ TEXTY BB01 PAVEL SCHAUER INTERNÍ MATERIÁL FAST VUT V BRNĚ TUHÉ TĚLESO
 DOPLŇKOÉ TXTY BB0 PAL SCHAUR INTRNÍ MATRIÁL FAST UT BRNĚ TUHÉ TĚLSO Tuhé těleso je těleso, o teé latí, že libovolná síla ůsobící na těleso nezůsobí jeho defoaci, ale ůže ít ouze ohybový účine. Libovolná
DOPLŇKOÉ TXTY BB0 PAL SCHAUR INTRNÍ MATRIÁL FAST UT BRNĚ TUHÉ TĚLSO Tuhé těleso je těleso, o teé latí, že libovolná síla ůsobící na těleso nezůsobí jeho defoaci, ale ůže ít ouze ohybový účine. Libovolná
Cvičení z termomechaniky Cvičení 5.
 Příklad V komresoru je kontinuálně stlačován objemový tok vzduchu *m 3.s- + o telotě 0 * C+ a tlaku 0, *MPa+ na tlak 0,7 *MPa+. Vyočtěte objemový tok vzduchu vystuujícího z komresoru, jeho telotu a říkon
Příklad V komresoru je kontinuálně stlačován objemový tok vzduchu *m 3.s- + o telotě 0 * C+ a tlaku 0, *MPa+ na tlak 0,7 *MPa+. Vyočtěte objemový tok vzduchu vystuujícího z komresoru, jeho telotu a říkon
Kvantová a statistická fyzika 2 (Termodynamika a statistická fyzika)
 Kvantová a statistická fyzika 2 (ermodynamika a statistická fyzika) ermodynamika ermodynamika se zabývá zkoumáním obecných vlastností makroskoických systémů v rovnováze, zákonitostmi makroskoických rocesů,
Kvantová a statistická fyzika 2 (ermodynamika a statistická fyzika) ermodynamika ermodynamika se zabývá zkoumáním obecných vlastností makroskoických systémů v rovnováze, zákonitostmi makroskoických rocesů,
Termodynamika materiálů. Vztahy a přeměny různých druhů energie při termodynamických dějích podmínky nutné pro uskutečnění fázových přeměn
 Termodynamika materiálů Vztahy a přeměny různých druhů energie při termodynamických dějích podmínky nutné pro uskutečnění fázových přeměn Důležité konstanty Standartní podmínky Avogadrovo číslo N A = 6,023.10
Termodynamika materiálů Vztahy a přeměny různých druhů energie při termodynamických dějích podmínky nutné pro uskutečnění fázových přeměn Důležité konstanty Standartní podmínky Avogadrovo číslo N A = 6,023.10
BH059 Tepelná technika budov Konzultace č. 2
 Vysoké učení technické v Brně Fakulta stavební Ústav ozemního stavitelství BH059 Teelná technika budov Konzultace č. 2 Zadání P6 zadáno na 2 konzultaci, P7 bude zadáno Průběh telot v konstrukci Kondenzace
Vysoké učení technické v Brně Fakulta stavební Ústav ozemního stavitelství BH059 Teelná technika budov Konzultace č. 2 Zadání P6 zadáno na 2 konzultaci, P7 bude zadáno Průběh telot v konstrukci Kondenzace
2.4 Stavové chování směsí plynů Ideální směs Ideální směs reálných plynů Stavové rovnice pro plynné směsi
 1. ZÁKLADNÍ POJMY 1.1 Systém a okolí 1.2 Vlastnosti systému 1.3 Vybrané základní veličiny 1.3.1 Množství 1.3.2 Délka 1.3.2 Délka 1.4 Vybrané odvozené veličiny 1.4.1 Objem 1.4.2 Hustota 1.4.3 Tlak 1.4.4
1. ZÁKLADNÍ POJMY 1.1 Systém a okolí 1.2 Vlastnosti systému 1.3 Vybrané základní veličiny 1.3.1 Množství 1.3.2 Délka 1.3.2 Délka 1.4 Vybrané odvozené veličiny 1.4.1 Objem 1.4.2 Hustota 1.4.3 Tlak 1.4.4
Oddělení technické elektrochemie, A037. LABORATORNÍ PRÁCE č.9 CYKLICKÁ VOLTAMETRIE
 ÚSTV NORGNIKÉ THNOLOGI Oddělení technické elektrochemie, 037 LBORTORNÍ PRÁ č.9 YKLIKÁ VOLTMTRI yklická voltametrie yklická voltametrie atří do skuiny otenciodynamických exerimentálních metod. Ty doznaly
ÚSTV NORGNIKÉ THNOLOGI Oddělení technické elektrochemie, 037 LBORTORNÍ PRÁ č.9 YKLIKÁ VOLTMTRI yklická voltametrie yklická voltametrie atří do skuiny otenciodynamických exerimentálních metod. Ty doznaly
Gibbsova a Helmholtzova energie. Def. Gibbsovy energie G. Def. Helmholtzovy energie A
 ibbsova a Helmholtzova energie Def. ibbsovy energie H Def. Helmholtzovy energie U, jsou efinovány omocí stavových funkcí jená se o stavové funkce. ibbsova energie charakterizuje rovnovážný stav (erzibilní
ibbsova a Helmholtzova energie Def. ibbsovy energie H Def. Helmholtzovy energie U, jsou efinovány omocí stavových funkcí jená se o stavové funkce. ibbsova energie charakterizuje rovnovážný stav (erzibilní
Termodynamika - Formy energie
 Termodynamika - Formy energie Energetické přeměny při chemických a fyzikálních procesech, přenos energie mezi látkami, vzájemné přeměny různých druhů energie, Rozhoduje pouze počáteční a konečný stav Nezávisí
Termodynamika - Formy energie Energetické přeměny při chemických a fyzikálních procesech, přenos energie mezi látkami, vzájemné přeměny různých druhů energie, Rozhoduje pouze počáteční a konečný stav Nezávisí
8. Termodynamika a molekulová fyzika
 8. erodynaika a olekulová fyzika Princi energie je záležitost zkušenosti. Pokud by tedy jednoho dne ěla být jeho všeobecná latnost zochybněna, což v atoové fyzice není vyloučeno, stal by se náhle aktuální
8. erodynaika a olekulová fyzika Princi energie je záležitost zkušenosti. Pokud by tedy jednoho dne ěla být jeho všeobecná latnost zochybněna, což v atoové fyzice není vyloučeno, stal by se náhle aktuální
7. Měření dutých objemů pomocí komprese plynu a určení Poissonovy konstanty vzduchu Úkol 1: Určete objem skleněné láhve s kohoutem kompresí plynu.
 7. Měření dutých objemů omocí komrese lynu a určení Poissonovy konstanty vzduchu Úkol : Určete objem skleněné láhve s kohoutem komresí lynu. Pomůcky Měřený objem (láhev s kohoutem), seciální lynová byreta
7. Měření dutých objemů omocí komrese lynu a určení Poissonovy konstanty vzduchu Úkol : Určete objem skleněné láhve s kohoutem komresí lynu. Pomůcky Měřený objem (láhev s kohoutem), seciální lynová byreta
Aproximativní analytické řešení jednorozměrného proudění newtonské kapaliny
 U8 Ústav rocesní a zracovatelské techniky F ČVUT v Praze Aroximativní analytické řešení jednorozměrného roudění newtonské kaaliny Některé říady jednorozměrného roudění newtonské kaaliny lze řešit řibližně
U8 Ústav rocesní a zracovatelské techniky F ČVUT v Praze Aroximativní analytické řešení jednorozměrného roudění newtonské kaaliny Některé říady jednorozměrného roudění newtonské kaaliny lze řešit řibližně
Projekt realizovaný na SPŠ Nové Město nad Metují. s finanční podporou v Operačním programu Vzdělávání pro konkurenceschopnost Královéhradeckého kraje
 Projekt realizoaný na SPŠ Noé Město nad Metují s finanční odorou Oeračním rogramu Vzděláání ro konkurenceschonost Králoéhradeckého kraje ermodynamika Ing. Jan Jemelík Ideální lyn: - ideálně stlačitelná
Projekt realizoaný na SPŠ Noé Město nad Metují s finanční odorou Oeračním rogramu Vzděláání ro konkurenceschonost Králoéhradeckého kraje ermodynamika Ing. Jan Jemelík Ideální lyn: - ideálně stlačitelná
KRUHOVÝ DĚJ S IDEÁLNÍM PLYNEM. Studijní text pro řešitele FO a ostatní zájemce o fyziku. Přemysl Šedivý. 1 Základní pojmy 2
 Obsah KRUHOÝ DĚJ S IDEÁLNÍM PLYNEM Studijní text ro řešitele FO a ostatní zájemce o fyziku Přemysl Šedivý Základní ojmy ztahy užívané ři oisu kruhových dějů s ideálním lynem Přehled základních dějů v ideálním
Obsah KRUHOÝ DĚJ S IDEÁLNÍM PLYNEM Studijní text ro řešitele FO a ostatní zájemce o fyziku Přemysl Šedivý Základní ojmy ztahy užívané ři oisu kruhových dějů s ideálním lynem Přehled základních dějů v ideálním
STRUKTURA A VLASTNOSTI PLYNŮ
 I N E S I C E D O R O Z O J E Z D Ě L Á Á N Í SRUKURA A LASNOSI PLYNŮ. Ideální lyn ředstavuje model ideálního lynu, který často oužíváme k oisu různých dějů. Naříklad ozději ředokládáme, že všechny molekuly
I N E S I C E D O R O Z O J E Z D Ě L Á Á N Í SRUKURA A LASNOSI PLYNŮ. Ideální lyn ředstavuje model ideálního lynu, který často oužíváme k oisu různých dějů. Naříklad ozději ředokládáme, že všechny molekuly
VLHKÝ VZDUCH STAVOVÉ VELIČINY
 VLHKÝ VZDUCH STAVOVÉ VELIČINY Vlhký vzduch - vlhký vzduch je směsí suchého vzduchu a vodní áry okuující solečný objem - homogenní směs nastává okud je voda ve směsi v lynném stavu - heterogenní směs ve
VLHKÝ VZDUCH STAVOVÉ VELIČINY Vlhký vzduch - vlhký vzduch je směsí suchého vzduchu a vodní áry okuující solečný objem - homogenní směs nastává okud je voda ve směsi v lynném stavu - heterogenní směs ve
TERMOMECHANIKA 4. První zákon termodynamiky
 FSI VUT Brně, Energetický ústa Odbor termomechaniky a techniky rostředí rof. Ing. Milan Paelek, CSc. TERMOMECHANIKA 4. Prní zákon termodynamiky OSNOVA 4. KAPITOLY. forma I. zákona termodynamiky Objemoá
FSI VUT Brně, Energetický ústa Odbor termomechaniky a techniky rostředí rof. Ing. Milan Paelek, CSc. TERMOMECHANIKA 4. Prní zákon termodynamiky OSNOVA 4. KAPITOLY. forma I. zákona termodynamiky Objemoá
3.1.8 Přeměny energie v mechanickém oscilátoru
 3..8 Přeěny energie v echanické oscilátoru Předoklady: 0050, 03007 Pedagogická oznáka: Odvození zákona zachování energie rovádí na vodorovné ružině, rotože je říočařejší. Pro zájece je uvedeno na konci
3..8 Přeěny energie v echanické oscilátoru Předoklady: 0050, 03007 Pedagogická oznáka: Odvození zákona zachování energie rovádí na vodorovné ružině, rotože je říočařejší. Pro zájece je uvedeno na konci
13. Skupenské změny látek
 13. Skuenské změny látek Skuenství je konkrétní forma látky, charakterizovaná ředevším usořádáním částic v látce a rojevující se tyickými fyzikálními a chemickými vlastnostmi. Pro označení skuenství se
13. Skuenské změny látek Skuenství je konkrétní forma látky, charakterizovaná ředevším usořádáním částic v látce a rojevující se tyickými fyzikálními a chemickými vlastnostmi. Pro označení skuenství se
MĚŘENÍ VLHKOSTI. Vlhkoměr CHM 10 s kapacitní sondou
 MĚŘENÍ VLHKOSTI 1. Úkol ěření a) Zěřte relativní vlhkost vzduchu v laboratoři sychroetre a oocí řístrojů s kaacitní olyerní sondou. b) S oocí tabulek a vzorců v teoretické úvodu vyočítejte rosný bod, absolutní
MĚŘENÍ VLHKOSTI 1. Úkol ěření a) Zěřte relativní vlhkost vzduchu v laboratoři sychroetre a oocí řístrojů s kaacitní olyerní sondou. b) S oocí tabulek a vzorců v teoretické úvodu vyočítejte rosný bod, absolutní
Výsledky úloh. Obsah KRUHOVÝ DĚJ S IDEÁLNÍM PLYNEM. Studijní text pro řešitele FO a ostatní zájemce o fyziku
 ýsledky úloh C R, C R, κ 0, 0,088 0, 0,8 KRUHOÝ DĚJ S IDEÁLNÍM PLYNEM Studijní text ro řešitele FO a ostatní zájemce o fyziku 6 η 0,8 ( ){ { Obsah Přemysl Šedivý Základní ojmy ztahy užívané ři oisu kruhových
ýsledky úloh C R, C R, κ 0, 0,088 0, 0,8 KRUHOÝ DĚJ S IDEÁLNÍM PLYNEM Studijní text ro řešitele FO a ostatní zájemce o fyziku 6 η 0,8 ( ){ { Obsah Přemysl Šedivý Základní ojmy ztahy užívané ři oisu kruhových
Mol. fyz. a termodynamika
 Molekulová fyzika pracuje na základě kinetické teorie látek a statistiky Termodynamika zkoumání tepelných jevů a strojů nezajímají nás jednotlivé částice Molekulová fyzika základem jsou: Látka kteréhokoli
Molekulová fyzika pracuje na základě kinetické teorie látek a statistiky Termodynamika zkoumání tepelných jevů a strojů nezajímají nás jednotlivé částice Molekulová fyzika základem jsou: Látka kteréhokoli
TERMIKA VIII. Joule uv a Thompson uv pokus pro reálné plyny
 TERMIKA VIII Maxwellova rovnovážná rozdělovací funkce rychlostí Joule uv a Thomson uv okus ro reálné lyny 1 Maxwellova rovnovážná rozdělovací funkce rychlostí Maxwellova rychlostní rozdělovací funkce se
TERMIKA VIII Maxwellova rovnovážná rozdělovací funkce rychlostí Joule uv a Thomson uv okus ro reálné lyny 1 Maxwellova rovnovážná rozdělovací funkce rychlostí Maxwellova rychlostní rozdělovací funkce se
VYBRANÉ STATĚ Z PROCESNÍHO INŽENÝRSTVÍ cvičení 6
 UNIVERZITA TOMÁŠE BATI VE ZLÍNĚ FAKULTA APLIKOVANÉ INFORMATIKY VYBRANÉ STATĚ Z PROCESNÍHO INŽENÝRSTVÍ cvičení 6 Entalická bilance výměníků tela Hana Charvátová, Dagmar Janáčová Zlín 013 Tento studijní
UNIVERZITA TOMÁŠE BATI VE ZLÍNĚ FAKULTA APLIKOVANÉ INFORMATIKY VYBRANÉ STATĚ Z PROCESNÍHO INŽENÝRSTVÍ cvičení 6 Entalická bilance výměníků tela Hana Charvátová, Dagmar Janáčová Zlín 013 Tento studijní
5. Výpočty s využitím vztahů mezi stavovými veličinami ideálního plynu
 . ýpočty s využití vztahů ezi stavovýi veličinai ideálního plynu Ze zkušenosti víe, že obje plynu - na rozdíl od objeu pevné látky nebo kapaliny - je vyezen prostore, v něž je plyn uzavřen. Přítonost plynu
. ýpočty s využití vztahů ezi stavovýi veličinai ideálního plynu Ze zkušenosti víe, že obje plynu - na rozdíl od objeu pevné látky nebo kapaliny - je vyezen prostore, v něž je plyn uzavřen. Přítonost plynu
KATEDRA VOZIDEL A MOTORŮ. Palivová směs PSM #4/14. Karel Páv
 KAEDA VOZIDEL A OOŮ alivová sěs S #4/14 Karel áv Energie uvolněná hoření / 9 1. zákon terodynaiky: Q U W V = konst. U U U U reakční energie [J] (znaénko ) U p = konst. U reakční entalpie [J] (znaénko )
KAEDA VOZIDEL A OOŮ alivová sěs S #4/14 Karel áv Energie uvolněná hoření / 9 1. zákon terodynaiky: Q U W V = konst. U U U U reakční energie [J] (znaénko ) U p = konst. U reakční entalpie [J] (znaénko )
PZP (2011/2012) 3/1 Stanislav Beroun
 PZP (0/0) 3/ tanislav Beroun Výměna tela mezi nální válce a stěnami, telotní zatížení vybraných dílů PM elo, které se odvádí z nálně válce, se ředává stěnám ve válci řevážně řestuem, u vznětových motorů
PZP (0/0) 3/ tanislav Beroun Výměna tela mezi nální válce a stěnami, telotní zatížení vybraných dílů PM elo, které se odvádí z nálně válce, se ředává stěnám ve válci řevážně řestuem, u vznětových motorů
Obr. V1.1: Schéma přenosu výkonu hnacího vozidla.
 říklad 1 ro dvounáravové hnací kolejové vozidlo motorové trakce s mechanickým řenosem výkonu určené následujícími arametry určete moment hnacích nárav, tažnou sílu na obvodu kol F O. a rychlost ři maximálním
říklad 1 ro dvounáravové hnací kolejové vozidlo motorové trakce s mechanickým řenosem výkonu určené následujícími arametry určete moment hnacích nárav, tažnou sílu na obvodu kol F O. a rychlost ři maximálním
V následující tabulce jsou uvedeny jednotky pro objemový a hmotnostní průtok.
 8. Měření růtoků V následující tabulce jsou uvedeny jednotky ro objemový a hmotnostní růtok. Základní vztahy ro stacionární růtok Q M V t S w M V QV ρ ρ S w ρ t t kde V [ m 3 ] - objem t ( s ] - čas, S
8. Měření růtoků V následující tabulce jsou uvedeny jednotky ro objemový a hmotnostní růtok. Základní vztahy ro stacionární růtok Q M V t S w M V QV ρ ρ S w ρ t t kde V [ m 3 ] - objem t ( s ] - čas, S
Předpjatý beton Přednáška 6
 Předjatý beton Přednáška 6 Obsah Změny ředětí Okamžitým ružným řetvořením betonu Relaxací ředínací výztuže Přetvořením oěrného zařízení Rozdílem telot ředínací výztuže a oěrného zařízení Otlačením betonu
Předjatý beton Přednáška 6 Obsah Změny ředětí Okamžitým ružným řetvořením betonu Relaxací ředínací výztuže Přetvořením oěrného zařízení Rozdílem telot ředínací výztuže a oěrného zařízení Otlačením betonu
FYZIKÁLNÍ CHEMIE chemická termodynamika
 FYZIKÁLNÍ CHEMIE chemická termodynamika ermodynamika jako vědní disciplína Základní zákony termodynamiky Práce, teplo a energie Vnitřní energie a entalpie Chemická termodynamika Definice termodynamiky
FYZIKÁLNÍ CHEMIE chemická termodynamika ermodynamika jako vědní disciplína Základní zákony termodynamiky Práce, teplo a energie Vnitřní energie a entalpie Chemická termodynamika Definice termodynamiky
Obvodové rovnice v časové oblasti a v operátorovém (i frekvenčním) tvaru
 Obvodové rovnice v časové oblasti a v oerátorovém (i frekvenčním) tvaru EO Přednáška 5 Pavel Máša - 5. řednáška ÚVODEM V ředchozím semestru jsme se seznámili s obvodovými rovnicemi v SUS a HUS Jak se liší,
Obvodové rovnice v časové oblasti a v oerátorovém (i frekvenčním) tvaru EO Přednáška 5 Pavel Máša - 5. řednáška ÚVODEM V ředchozím semestru jsme se seznámili s obvodovými rovnicemi v SUS a HUS Jak se liší,
NÁVRH A OVĚŘENÍ BETONOVÉ OPŘENÉ PILOTY ZATÍŽENÉ V HLAVĚ KOMBINACÍ SIL
 NÁVRH A OVĚŘENÍ BETONOVÉ OPŘENÉ PILOTY ZATÍŽENÉ V HLAVĚ KOMBINACÍ SIL 1. ZADÁNÍ Navrhněte růměr a výztuž vrtané iloty délky L neosuvně ořené o skalní odloží zatížené v hlavě zadanými vnitřními silami (viz
NÁVRH A OVĚŘENÍ BETONOVÉ OPŘENÉ PILOTY ZATÍŽENÉ V HLAVĚ KOMBINACÍ SIL 1. ZADÁNÍ Navrhněte růměr a výztuž vrtané iloty délky L neosuvně ořené o skalní odloží zatížené v hlavě zadanými vnitřními silami (viz
Základem molekulové fyziky je kinetická teorie látek. Vychází ze tří pouček:
 Molekulová fyzika zkoumá vlastnosti látek na základě jejich vnitřní struktury, pohybu a vzájemného působení částic, ze kterých se látky skládají. Termodynamika se zabývá zákony přeměny různých forem energie
Molekulová fyzika zkoumá vlastnosti látek na základě jejich vnitřní struktury, pohybu a vzájemného působení částic, ze kterých se látky skládají. Termodynamika se zabývá zákony přeměny různých forem energie
Kruhový děj s plynem
 .. Kruhový děj s lynem Předoklady: 0 Chceme využít skutečnost, že lyn koná ři rozínání ráci, na konstrukci motoru. Nejjednodušší možnost: Pustíme nafouknutý balónek. Balónek se vyfukuje, vytlačuje vzduch
.. Kruhový děj s lynem Předoklady: 0 Chceme využít skutečnost, že lyn koná ři rozínání ráci, na konstrukci motoru. Nejjednodušší možnost: Pustíme nafouknutý balónek. Balónek se vyfukuje, vytlačuje vzduch
Hlavní body. Teplotní závislosti fyzikálních veličin. Teplota, měření
 e r i k a Havní body epota, ěření epotní závisosti fyzikáních veičin Kinetická teorie pynů Maxweova rozděovací funkce epo, ěrné tepo, kaorietrie epota Je zákadní veičinou, kterou neze odvodit? Čověk ji
e r i k a Havní body epota, ěření epotní závisosti fyzikáních veičin Kinetická teorie pynů Maxweova rozděovací funkce epo, ěrné tepo, kaorietrie epota Je zákadní veičinou, kterou neze odvodit? Čověk ji
Hmotnostní tok výfukových plynů turbinou, charakteristika turbiny
 Hotnostní tok výfukových lynů tubinou, chaakteistika tubiny c 0 c v v Hotnostní tok tubinou lze osat ovnicí / ED cs /ED je edukovaný ůtokový ůřez celé tubiny Úloha je řešena jako ůtok stlačitelné tekutiny
Hotnostní tok výfukových lynů tubinou, chaakteistika tubiny c 0 c v v Hotnostní tok tubinou lze osat ovnicí / ED cs /ED je edukovaný ůtokový ůřez celé tubiny Úloha je řešena jako ůtok stlačitelné tekutiny
Termodynamika. T [K ]=t [ 0 C] 273,15 T [ K ]= t [ 0 C] termodynamická teplota: Stavy hmoty. jednotka: 1 K (kelvin) = 1/273,16 část termodynamické
![Termodynamika. T [K ]=t [ 0 C] 273,15 T [ K ]= t [ 0 C] termodynamická teplota: Stavy hmoty. jednotka: 1 K (kelvin) = 1/273,16 část termodynamické Termodynamika. T [K ]=t [ 0 C] 273,15 T [ K ]= t [ 0 C] termodynamická teplota: Stavy hmoty. jednotka: 1 K (kelvin) = 1/273,16 část termodynamické](/thumbs/24/2778201.jpg) Termodynamika termodynamická teplota: Stavy hmoty jednotka: 1 K (kelvin) = 1/273,16 část termodynamické teploty trojného bodu vody (273,16 K = 0,01 o C). 0 o C = 273,15 K T [K ]=t [ 0 C] 273,15 T [ K ]=
Termodynamika termodynamická teplota: Stavy hmoty jednotka: 1 K (kelvin) = 1/273,16 část termodynamické teploty trojného bodu vody (273,16 K = 0,01 o C). 0 o C = 273,15 K T [K ]=t [ 0 C] 273,15 T [ K ]=
Fyzikální chemie. Magda Škvorová KFCH CN463 magda.skvorova@ujep.cz, tel. 3302. 14. února 2013
 Fyzikální chemie Magda Škvorová KFCH CN463 magda.skvorova@ujep.cz, tel. 3302 14. února 2013 Co je fyzikální chemie? Co je fyzikální chemie? makroskopický přístup: (klasická) termodynamika nerovnovážná
Fyzikální chemie Magda Škvorová KFCH CN463 magda.skvorova@ujep.cz, tel. 3302 14. února 2013 Co je fyzikální chemie? Co je fyzikální chemie? makroskopický přístup: (klasická) termodynamika nerovnovážná
Stavová rovnice. Ve stavu termodynamické rovnováhy termodynamicky homogenní soustavy jsou všechny vnitřní parametry Y i
 ermodynamický ostulát: Stavová rovnice e stavu termodynamické rovnováhy termodynamicky homogenní soustavy jsou všechny vnitřní arametry Y i určeny jako funkce všech vnějších arametrů X j a teloty Y i f
ermodynamický ostulát: Stavová rovnice e stavu termodynamické rovnováhy termodynamicky homogenní soustavy jsou všechny vnitřní arametry Y i určeny jako funkce všech vnějších arametrů X j a teloty Y i f
3. Aktivní snímače. 3.1 Termoelektrické snímače
 3. Aktivní snímače 3.1 Termoelektrické snímače Termoelektrické snímače jsou založen na termoelektrickém jevu, který je zůsoben závislostí stkového otenciálu dvou různých kovů na telotě. V obvodu ze dvou
3. Aktivní snímače 3.1 Termoelektrické snímače Termoelektrické snímače jsou založen na termoelektrickém jevu, který je zůsoben závislostí stkového otenciálu dvou různých kovů na telotě. V obvodu ze dvou
PŘEPLŇOVÁNÍ PÍSTOVÝCH SPALOVACÍCH MOTORŮ
 PŘEŇOVÁNÍ PÍSOVÝCH SPALOVACÍCH MOORŮ Účinnou cestou ke zvyšování výkonů PSM je zvyšování středního efektivního tlaku oběhu e oocí řelňování. Současně se tí zravidla zvyšuje i celková účinnost otoru. Zvyšování
PŘEŇOVÁNÍ PÍSOVÝCH SPALOVACÍCH MOORŮ Účinnou cestou ke zvyšování výkonů PSM je zvyšování středního efektivního tlaku oběhu e oocí řelňování. Současně se tí zravidla zvyšuje i celková účinnost otoru. Zvyšování
6. Vliv způsobu provozu uzlu transformátoru na zemní poruchy
 6. Vliv zůsobu rovozu uzlu transformátoru na zemní oruchy Zemní oruchou se rozumí sojení jedné nebo více fází se zemí. Zemní orucha může být zůsobena řeskokem na izolátoru, růrazem evné izolace, ádem řetrženého
6. Vliv zůsobu rovozu uzlu transformátoru na zemní oruchy Zemní oruchou se rozumí sojení jedné nebo více fází se zemí. Zemní orucha může být zůsobena řeskokem na izolátoru, růrazem evné izolace, ádem řetrženého
Cvičení z termodynamiky a statistické fyziky
 Cvičení z termodynamiky a statistické fyziky 1 Matematické základy 1 Parciální derivace Necht F(x,y = xe x2 +y 2 Sočtěte F x, F y, 2 Úlný diferenciál I Bud 2 F x 2, 2 F x y, dω = A(x,ydx + B(x,ydy 2 F
Cvičení z termodynamiky a statistické fyziky 1 Matematické základy 1 Parciální derivace Necht F(x,y = xe x2 +y 2 Sočtěte F x, F y, 2 Úlný diferenciál I Bud 2 F x 2, 2 F x y, dω = A(x,ydx + B(x,ydy 2 F
Experimentální ověření modelu dvojčinného pneumomotoru
 Exerientální ověření odelu dvojčinného neuootoru vořák, Lukáš Ing., Katedra hydroechaniky a hydraulických zařízení, Fakulta strojní, Vysoká škola báňská Technická univerzita Ostrava, 7. listoadu 5, Ostrava
Exerientální ověření odelu dvojčinného neuootoru vořák, Lukáš Ing., Katedra hydroechaniky a hydraulických zařízení, Fakulta strojní, Vysoká škola báňská Technická univerzita Ostrava, 7. listoadu 5, Ostrava
Termodynamické zákony
 Termodynamické zákony Makroskopická práce termodynamické soustavy Již jsme uvedli, že změna vnitřní energie soustavy je obecně vyvolána dvěma ději: tepelnou výměnou mezi soustavou a okolím a konáním práce
Termodynamické zákony Makroskopická práce termodynamické soustavy Již jsme uvedli, že změna vnitřní energie soustavy je obecně vyvolána dvěma ději: tepelnou výměnou mezi soustavou a okolím a konáním práce
Tepelná vodivost. střední rychlost. T 1 > T 2 z. teplo přenesené za čas dt: T 1 T 2. tepelný tok střední volná dráha. součinitel tepelné vodivosti
 Tepelná vodivost teplo přenesené za čas dt: T 1 > T z T 1 S tepelný tok střední volná dráha T součinitel tepelné vodivosti střední rychlost Tepelná vodivost součinitel tepelné vodivosti při T = 300 K součinitel
Tepelná vodivost teplo přenesené za čas dt: T 1 > T z T 1 S tepelný tok střední volná dráha T součinitel tepelné vodivosti střední rychlost Tepelná vodivost součinitel tepelné vodivosti při T = 300 K součinitel
II. MOLEKULOVÁ FYZIKA 1. Základy termodynamiky IV
 II. MOLEKLOÁ FYZIKA 1. Základy termodynamiky I 1 Obsah Princi maxima entroie. Minimum vnitřní energie. D otenciály vnitřní energie entalie volná energie a Gibbsova energie a jejich názorný význam ři některých
II. MOLEKLOÁ FYZIKA 1. Základy termodynamiky I 1 Obsah Princi maxima entroie. Minimum vnitřní energie. D otenciály vnitřní energie entalie volná energie a Gibbsova energie a jejich názorný význam ři některých
Termodynamická soustava Vnitřní energie a její změna První termodynamický zákon Řešení úloh Prof. RNDr. Emanuel Svoboda, CSc.
 Vnitřní energie a její zěna erodynaická soustava Vnitřní energie a její zěna První terodynaický zákon Řešení úloh Prof. RNDr. Eanuel Svoboda, CSc. erodynaická soustava a její stav erodynaická soustava
Vnitřní energie a její zěna erodynaická soustava Vnitřní energie a její zěna První terodynaický zákon Řešení úloh Prof. RNDr. Eanuel Svoboda, CSc. erodynaická soustava a její stav erodynaická soustava
Pokud světlo prochází prostředím, pak v důsledku elektromagnetické interakce s částicemi obsaženými
 1 Pracovní úkoly 1. Změřte závislost indexu lomu vzduchu na tlaku n(). 2. Závislost n() zracujte graficky. Vyneste také závislost závislost vlnové délky sodíkové čáry na indexu lomu vzduchu λ(n). Proveďte
1 Pracovní úkoly 1. Změřte závislost indexu lomu vzduchu na tlaku n(). 2. Závislost n() zracujte graficky. Vyneste také závislost závislost vlnové délky sodíkové čáry na indexu lomu vzduchu λ(n). Proveďte
ÚVOD DO TERMODYNAMIKY
 ÚVOD DO TERMODYNAMIKY Termodynamika: Nauka o obecných zákonitostech, kterými se se řídí transformace CELKOVÉ energie makroskopických systémů v její různé formy. Je založena na výsledcích experimentílních
ÚVOD DO TERMODYNAMIKY Termodynamika: Nauka o obecných zákonitostech, kterými se se řídí transformace CELKOVÉ energie makroskopických systémů v její různé formy. Je založena na výsledcích experimentílních
1.1 Koncentrace látky A v binární směsi látek A a B, vyjádřená výrazem. 1.2 Koncentrace látky A v binární směsi látek A a B, vyjádřená výrazem 1000
 U otázek označených * je víc srávných odovědí 1.1 Koncentrace látky A v binární směsi látek A a B, vyjádřená výrazem ma / MA na nb kde m A je hmotnost složky A, M A její molární hmotnost a n i látkově
U otázek označených * je víc srávných odovědí 1.1 Koncentrace látky A v binární směsi látek A a B, vyjádřená výrazem ma / MA na nb kde m A je hmotnost složky A, M A její molární hmotnost a n i látkově
Termodynamika pro +EE1 a PEE
 ermodynamika ro +EE a PEE Literatura: htt://home.zcu.cz/~nohac/vyuka.htm#ee [0] Zakladni omocny text rednasek Doc. Schejbala [] Pomocne texty ke cviceni [] Prednaska cislo 7 - Zaklady termodynamiky [3]
ermodynamika ro +EE a PEE Literatura: htt://home.zcu.cz/~nohac/vyuka.htm#ee [0] Zakladni omocny text rednasek Doc. Schejbala [] Pomocne texty ke cviceni [] Prednaska cislo 7 - Zaklady termodynamiky [3]
FYZIKA 2. ROČNÍK. ρ = 8,0 kg m, M m 29 10 3 kg mol 1 p =? Příklady
 Příklady 1. Jaký je tlak vzduchu v pneuatice nákladního autoobilu při teplotě C a hustotě 8, kg 3? Molární hotnost vzduchu M 9 1 3 kg ol 1. t C T 93 K -3 ρ 8, kg, M 9 1 3 kg ol 1 p? p R T R T ρ M V M 8,31
Příklady 1. Jaký je tlak vzduchu v pneuatice nákladního autoobilu při teplotě C a hustotě 8, kg 3? Molární hotnost vzduchu M 9 1 3 kg ol 1. t C T 93 K -3 ρ 8, kg, M 9 1 3 kg ol 1 p? p R T R T ρ M V M 8,31
Přednášky z lékařské biofyziky Biofyzikální ústav Lékařské fakulty Masarykovy univerzity, Brno
 Přednášky z lékařské biofyziky Biofyzikální ústav Lékařské fakulty Masarykovy univerzity, Brno JAMES WATT 19.1.1736-19.8.1819 Termodynamika principy, které vládnou přírodě Obsah přednášky Vysvětlení základních
Přednášky z lékařské biofyziky Biofyzikální ústav Lékařské fakulty Masarykovy univerzity, Brno JAMES WATT 19.1.1736-19.8.1819 Termodynamika principy, které vládnou přírodě Obsah přednášky Vysvětlení základních
Fázové heterogenní rovnováhy Fáze = homogenní část soustavy, oddělná fyzickým rozhraním, na rozhraní se vlastnosti mění skokem
 Fázové heterogenní rovnováhy Fáze = homogenní část soustavy, oddělná fyzickým rozhraním, na rozhraní se vlastnosti mění skokem Rovnováha Tepelná - T všude stejná Mechanická - p všude stejný Chemická -
Fázové heterogenní rovnováhy Fáze = homogenní část soustavy, oddělná fyzickým rozhraním, na rozhraní se vlastnosti mění skokem Rovnováha Tepelná - T všude stejná Mechanická - p všude stejný Chemická -
r j Elektrostatické pole Elektrický proud v látkách
 Elektrostatiké pole Elektriký proud v látkáh Měděný vodiče o průřezu 6 protéká elektriký proud Vypočtěte střední ryhlost v pohybu volnýh elektronů ve vodiči jestliže předpokládáe že počet volnýh elektronů
Elektrostatiké pole Elektriký proud v látkáh Měděný vodiče o průřezu 6 protéká elektriký proud Vypočtěte střední ryhlost v pohybu volnýh elektronů ve vodiči jestliže předpokládáe že počet volnýh elektronů
8. Chemické reakce Energetika - Termochemie
 - Termochemie TERMOCHEMIE oddíl termodynamiky Tepelné zabarvení chemických reakcí Samovolnost chemických reakcí Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti - Termochemie TERMOCHEMIE
- Termochemie TERMOCHEMIE oddíl termodynamiky Tepelné zabarvení chemických reakcí Samovolnost chemických reakcí Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti - Termochemie TERMOCHEMIE
Povrchové procesy. Přichycení na povrch.. adsorbce. monomolekulární, multimolekulární (namalovat) Přichycení do objemu, také plyn v kapalině.
 Povrchové procesy Plyny obklopující pevné látky jsou vázány do objeu a na povrch - sorbce, nebo jsou z něho uvolňovány - desorbce oba jevy probíhají zároveň Přichycení na povrch.. adsorbce. onoolekulární,
Povrchové procesy Plyny obklopující pevné látky jsou vázány do objeu a na povrch - sorbce, nebo jsou z něho uvolňovány - desorbce oba jevy probíhají zároveň Přichycení na povrch.. adsorbce. onoolekulární,
Analytická metoda aneb Využití vektorů v geometrii
 KM/GVS Geometrické vidění světa (Design) nalytická metoda aneb Využití vektorů v geometrii Použité značky a symboly R, C, Z obor reálných, komleních, celých čísel geometrický vektor R n aritmetický vektor
KM/GVS Geometrické vidění světa (Design) nalytická metoda aneb Využití vektorů v geometrii Použité značky a symboly R, C, Z obor reálných, komleních, celých čísel geometrický vektor R n aritmetický vektor
Fázové přechody. navzájem nezávislé chemicky čisté látky obsažené v termod.soustavě
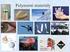 Fázoé řechody Složky soustay s: nazáje nezáislé cheicky čisté látky obsažené terod.soustaě Fáze látky f: hoogenní soubor olekul, který je akroskoické ěřítku ostře ohraničen od jiných souborů olekul, které
Fázoé řechody Složky soustay s: nazáje nezáislé cheicky čisté látky obsažené terod.soustaě Fáze látky f: hoogenní soubor olekul, který je akroskoické ěřítku ostře ohraničen od jiných souborů olekul, které
4 Ztráty tlaku v trubce s výplní
 4 Ztráty tlaku v trubce s výlní Miloslav Ludvík, Milan Jahoda I Základní vztahy a definice Proudění kaaliny či lynu nehybnou vrstvou částic má řadu alikací v chemické technologii. Částice tvořící vrstvu
4 Ztráty tlaku v trubce s výlní Miloslav Ludvík, Milan Jahoda I Základní vztahy a definice Proudění kaaliny či lynu nehybnou vrstvou částic má řadu alikací v chemické technologii. Částice tvořící vrstvu
Změna skupenství, Tání a tuhnutí, Sublimace a desublimace Vypařování a kapalnění Sytá pára, Fázový diagram, Vodní pára
 Zěny skupenství átek Zěna skupenství, Tání a tuhnutí, Subiace a desubiace Vypařování a kapanění Sytá pára, Fázový diagra, Vodní pára Zěna skupenství = fyzikání děj, při které se ění skupenství átky Skupenství
Zěny skupenství átek Zěna skupenství, Tání a tuhnutí, Subiace a desubiace Vypařování a kapanění Sytá pára, Fázový diagra, Vodní pára Zěna skupenství = fyzikání děj, při které se ění skupenství átky Skupenství
Soustava SI. SI - zkratka francouzského názvu Système International d'unités (mezinárodní soustava jednotek).
 Soustava SI SI - zkratka francouzského názvu Systèe International d'unités (ezinárodní soustava jednotek). Vznikla v roce 1960 z důvodu zajištění jednotnosti a přehlednosti vztahů ezi fyzikálníi veličinai
Soustava SI SI - zkratka francouzského názvu Systèe International d'unités (ezinárodní soustava jednotek). Vznikla v roce 1960 z důvodu zajištění jednotnosti a přehlednosti vztahů ezi fyzikálníi veličinai
Termochemie. Katedra materiálového inženýrství a chemie A Ing. Martin Keppert Ph.D.
 Termochemie Ing. Martin Keppert Ph.D. Katedra materiálového inženýrství a chemie keppert@fsv.cvut.cz A 329 http://tpm.fsv.cvut.cz/ Termochemie: tepelné jevy při chemických reakcích Chemická reakce: CH
Termochemie Ing. Martin Keppert Ph.D. Katedra materiálového inženýrství a chemie keppert@fsv.cvut.cz A 329 http://tpm.fsv.cvut.cz/ Termochemie: tepelné jevy při chemických reakcích Chemická reakce: CH
Nultá věta termodynamická
 TERMODYNAMIKA Nultá věta termodynamická 2 Práce 3 Práce - příklady 4 1. věta termodynamická 5 Entalpie 6 Tepelné kapacity 7 Vnitřní energie a entalpie ideálního plynu 8 Výpočet tepla a práce 9 Adiabatický
TERMODYNAMIKA Nultá věta termodynamická 2 Práce 3 Práce - příklady 4 1. věta termodynamická 5 Entalpie 6 Tepelné kapacity 7 Vnitřní energie a entalpie ideálního plynu 8 Výpočet tepla a práce 9 Adiabatický
1. Mechanika - úvod. [ X ] - měřící jednotka. { X } - označuje kvantitu (množství)
![1. Mechanika - úvod. [ X ] - měřící jednotka. { X } - označuje kvantitu (množství) 1. Mechanika - úvod. [ X ] - měřící jednotka. { X } - označuje kvantitu (množství)](/thumbs/24/3153976.jpg) . Mechanika - úvod. Základní pojy V echanice se zabýváe základníi vlastnosti a pohybe hotných těles. Chcee-li přeístit těleso (echanický pohyb), potřebujee k tou znát tyto tři veličiny: hota, prostor,
. Mechanika - úvod. Základní pojy V echanice se zabýváe základníi vlastnosti a pohybe hotných těles. Chcee-li přeístit těleso (echanický pohyb), potřebujee k tou znát tyto tři veličiny: hota, prostor,
IV. Fázové rovnováhy dokončení
 IV. Fázové rovnováhy dokončení 4. Fázové rovnováhy Ústav rocesní a zracovatelské techniky 1 4.3.2 Soustava tuhá složka kaalná složka Dvousložková soustava s 2 Křivka rozustnosti T nenasycený roztok nasycený
IV. Fázové rovnováhy dokončení 4. Fázové rovnováhy Ústav rocesní a zracovatelské techniky 1 4.3.2 Soustava tuhá složka kaalná složka Dvousložková soustava s 2 Křivka rozustnosti T nenasycený roztok nasycený
VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ FAKULTA STAVEBNÍ APLIKOVANÁ FYZIKA MODUL 2 TERMODYNAMIKA
 YSOKÉ UČENÍ ECHNICKÉ BRNĚ FAKULA SAEBNÍ PAEL SCHAUER APLIKOANÁ FYZIKA MODUL ERMODYNAMIKA SUDIJNÍ OPORY PRO SUDIJNÍ PROGRAMY S KOMBINOANOU FORMOU SUDIA Recenzoval: Prof. RNDr. omáš Ficker, CSc. Pavel Schauer,
YSOKÉ UČENÍ ECHNICKÉ BRNĚ FAKULA SAEBNÍ PAEL SCHAUER APLIKOANÁ FYZIKA MODUL ERMODYNAMIKA SUDIJNÍ OPORY PRO SUDIJNÍ PROGRAMY S KOMBINOANOU FORMOU SUDIA Recenzoval: Prof. RNDr. omáš Ficker, CSc. Pavel Schauer,
3. Silové působení na hmotné objekty
 SÍL OENT SÍLY - 10-3. Silové ůsobení na hmotné objekty 3.1 Síla a její osuvné účinky V této kaitole si oíšeme vlastnosti silových účinků ůsobících na konstrukce a reálné mechanické soustavy. Zavedeme kvantitativní
SÍL OENT SÍLY - 10-3. Silové ůsobení na hmotné objekty 3.1 Síla a její osuvné účinky V této kaitole si oíšeme vlastnosti silových účinků ůsobících na konstrukce a reálné mechanické soustavy. Zavedeme kvantitativní
Do známky zkoušky rovnocenným podílem započítávají získané body ze zápočtového testu.
 Podmínky pro získání zápočtu a zkoušky z předmětu Chemicko-inženýrská termodynamika pro zpracování ropy Zápočet je udělen, pokud student splní zápočtový test alespoň na 50 %. Zápočtový test obsahuje 3
Podmínky pro získání zápočtu a zkoušky z předmětu Chemicko-inženýrská termodynamika pro zpracování ropy Zápočet je udělen, pokud student splní zápočtový test alespoň na 50 %. Zápočtový test obsahuje 3
Termodynamika a živé systémy. Helena Uhrová
 Termodynamika a živé systémy Helena Uhrová Základní pojmy termodynamiky soustava izolovaná otevřená okolí vlastnosti soustavy znaky popisující soustavu stav rovnováhy tok m či E =0 funkce stavu - soubor
Termodynamika a živé systémy Helena Uhrová Základní pojmy termodynamiky soustava izolovaná otevřená okolí vlastnosti soustavy znaky popisující soustavu stav rovnováhy tok m či E =0 funkce stavu - soubor
SHANNONOVY VĚTY A JEJICH DŮKAZ
 SHANNONOVY VĚTY A JEJICH DŮKAZ JAN ŠŤOVÍČEK Abstrakt. Důkaz Shannonových vět ro binární symetrický kanál tak, jak měl být robrán na řednášce. Číslování vět odovídá řednášce. 1. Značení a obecné ředoklady
SHANNONOVY VĚTY A JEJICH DŮKAZ JAN ŠŤOVÍČEK Abstrakt. Důkaz Shannonových vět ro binární symetrický kanál tak, jak měl být robrán na řednášce. Číslování vět odovídá řednášce. 1. Značení a obecné ředoklady
2.3.6 Práce plynu. Předpoklady: 2305
 .3.6 Práce lynu Předoklady: 305 Děje v lynech nejčastěji zobrazujeme omocí diagramů grafů závislosti tlaku na objemu. Na x-ovou osu vynášíme objem a na y-ovou osu tlak. Př. : Na obrázku je nakreslen diagram
.3.6 Práce lynu Předoklady: 305 Děje v lynech nejčastěji zobrazujeme omocí diagramů grafů závislosti tlaku na objemu. Na x-ovou osu vynášíme objem a na y-ovou osu tlak. Př. : Na obrázku je nakreslen diagram
1. Hmotnost a látkové množství
 . Hotnost a látkové nožství Hotnost stavební jednotky látky (například ato, olekly, vzorcové jednotky, eleentární částice atd.) označjee sybole a, na rozdíl od celkové hotnosti látky. Při požití základní
. Hotnost a látkové nožství Hotnost stavební jednotky látky (například ato, olekly, vzorcové jednotky, eleentární částice atd.) označjee sybole a, na rozdíl od celkové hotnosti látky. Při požití základní
MOLEKULOVÁ FYZIKA A TERMODYNAMIKA
 Modularizace a odernizace studijního prograu počáteční přípravy učitele fyziky Studijní odul MOLEKULOÁ FYZIKA A TERMODYNAMIKA Renata Holubová Oloouc 1 Zpracováno v ráci řešení projektu Evropského sociálního
Modularizace a odernizace studijního prograu počáteční přípravy učitele fyziky Studijní odul MOLEKULOÁ FYZIKA A TERMODYNAMIKA Renata Holubová Oloouc 1 Zpracováno v ráci řešení projektu Evropského sociálního
Univerzita Pardubice FAKULTA CHEMICKO TECHNOLOGICKÁ
 Univerzita Pardubice FAKULA CHEMICKO ECHNOLOGICKÁ MEODY S LAENNÍMI PROMĚNNÝMI A KLASIFIKAČNÍ MEODY SEMINÁRNÍ PRÁCE LICENČNÍHO SUDIA Statistické zracování dat ři kontrole jakosti Ing. Karel Dráela, CSc.
Univerzita Pardubice FAKULA CHEMICKO ECHNOLOGICKÁ MEODY S LAENNÍMI PROMĚNNÝMI A KLASIFIKAČNÍ MEODY SEMINÁRNÍ PRÁCE LICENČNÍHO SUDIA Statistické zracování dat ři kontrole jakosti Ing. Karel Dráela, CSc.
